ZAENAL ABIDIN
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
ZAENAL ABIDIN
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Perairan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
NIM : C 151 040 141
Disetujui
Komisi Pembimbing
Prof. Dr. Ing Mokoginta, M.Si. Ketua
Dr. M. Agus Suprayudi, M.Si. Anggota
Diketahui
Ketua Program Studi Ilmu Perairan
Prof. Dr. Enang Harris, M.Si.
Dekan Sekolah Pascasarjana
Dr. Ir. Khairil Anwar Notodiputro, MS.
Dengan ini saya menyatakan bahwa tesis yang berjudul Pengaruh Kadar Tepung Bungkil Kelapa Sawit dalam Pakan Ikan Lele (Clarias sp) adalah karya saya sendiri dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan ma upun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, 2 Oktober 2006
Pakan Ikan Lele (Clarias sp). Dibimbing oleh ING MOKOGINTA DAN MUHAMMAD AGUS SUPRAYUDI.
© Hak cipta milik Zaenal Abidin, tahun 2006 Hak cipta dilindungi
Puji dan syukur penulis panjatkan kepada Allah SWT, karena hanya atas rahmat dan karunia serta ridho-Nyalah tesis yang berjudul “Pengaruh Kadar Tepung Bungkil Kelapa Sawit dalam Pakan Ikan Lele (Clarias sp)”dapat terselesaikan.
Pelaksanaan penelitian dan penulisan tesis ini tidak terlepas dari bantuan dan bimbingan berbagai pihak. Pada kesempatan ini, penulis menyampaikan terima kas ih yang sebesar-besarnya kepada :
1. Ibu Prof. Dr. Ing Mokoginta, M.Si. dan Bapak Dr. M. Agus Suprayudi, M.Si. selaku komisi pembimbing atas pengarahan dan bimbingan yang telah diberikan selama penelitian dan penulisan tesis ini sehingga penulis dapat menyelesaikannya dengan baik.
2. Ketua Program Studi Ilmu Perairan, Ketua dan Staf Laboratorium Nutrisi Ikan, Laboratorium Kesehatan Ikan Departemen Budidaya Perairan Institut Pertanian Bogor yang telah membantu dalam penyediaan fasilitas hingga terlaksananya penelitian ini.
3. Ayahanda Syamsuddin Arief dan Ibunda Sitti Amirah Amin yang telah memberikan dukungan, pengorbanan dan doa tiada henti selama penulis menjalani pendidikan.
4. Rekan-rekan mahasiswa Pascasarjana Program Studi Ilmu Perairan atas persahabatan dan kerjasamanya selama ini.
Akhirnya semoga tesis ini dapat bermanfaat bagi semuanya. Amin..
Bogor, 1 Oktober 2006
Syamsuddin Arief dan Sitti Amirah Amin. Penulis merupakan anak ke tiga dari lima bersaudara.
i
DAFTAR TABEL………. iii
DAFTAR GAMBAR ………. iv
DAFTAR LAMPIRAN ………. v
PENDAHULUAN Latar Belakang ..………..……… 1
Perumusan Masalah ………..……… 2
Perumusan Hipotesis ….…..……….. 4
Tujuan dan Manfaat ………..……… 4
TINJAUAN PUSTAKA Kebutuhan Nutrien Ikan lele ……….. 5
Bahan Pakan Sumber Nutrien/Protein ……… 7
Tepung Bungkil Kedelai (Soybean Meal/SBM) …………..…. 7
Tepung Bungkil Sawit (Palm Kernel Meal/PKM) ………..….. 9
Tepung Tulang dan Daging (Meat and Bone Meal/MBM) ……. 11
BAHAN DAN METODE Pakan Uji ………. 14
Pemeliharaan Ikan dan Pengumpulan Data ……… 15
Analisis Kimia ……….….. 16
Histolo gi Hati ………..….. 16
Uji Kecernaan Pakan ……….….. 17
Pengukuran Eskresi Total Amonia Nitrogen (TAN) ……… 17
Analisis Data ………..………. 17
HASIL DAN PEMBAHASAN Hasil ……….………. 20
Pembahasan ………. 26
KESIMPULAN Kesimpulan ……… 31
iii
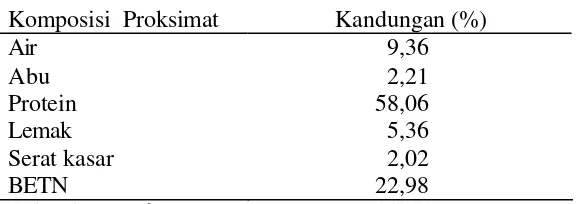
1. Komposisi proksimat SBM ……….……… 7
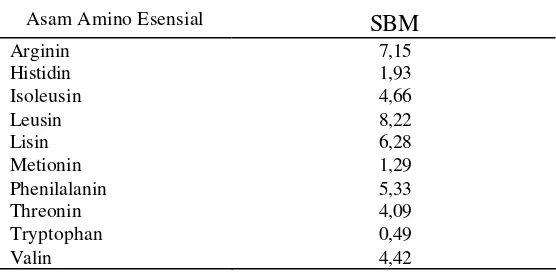
2. Komposisi asam amino esensial SBM (% protein) ………. 7
3. Komposisi proksimat PKM ……….……… 9
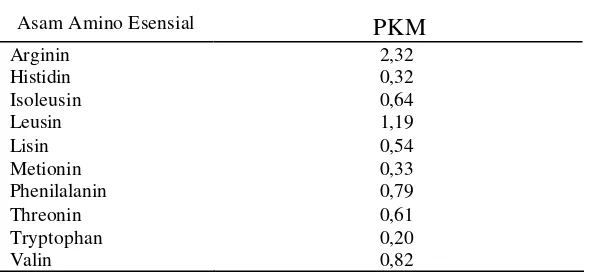
4. Komposisi asam amino esensial PKM (% protein) ………. 9
5. Komposisi proksimat MBM ………..……….. 11
6. Komposisi asam amino esensial MBM (% protein) ………. 11
7. Komposisi pakan uji (g/100 g pakan) ………. 14
8. Komposisi proksimat pakan (% bobot kering) ……… 15
9. Rata-rata Konsumsi Pakan (KP), Laju Pertumbuhan Harian (LPH), Efisiensi Pakan (EF), Retensi Protein (RP) dan Retensi Lemak (RL) ……… 21
10. Komposisi proksimat tubuh (% bobot kering) dan hati (% bobot basah) ikan lele (Clarias sp) ……..……… 22
11. Kecernaan Pakan (KP), Kecernaan Protein Pakan (KPP) dan eskresi Total Amonia Nitrogen (TAN) ……….. 22
iv 1. Bobot rata-rata ikan lele (Clarias sp) pada awal dan akhir
penelitian ……….. 20
2. Histologi hati ikan lele (Clarias sp ) yang diberi perlakuan
A(0) (pembesaran 1000x) ………..……….. 23
3. Histologi hati ikan lele (Clarias sp ) yang diberi perlakuan
B(8) (pembesaran 1000x) ………..……….. 24
4. Histologi hati ikan lele (Clarias sp ) yang diberi perlakuan
C(12) (pembesaran 1000x) ……….……….. 24
5. Histologi hati ikan lele (Clarias sp ) yang diberi perlakuan
D(16) (pembesaran 1000x) ……….……….. 25
6. Histologi hati ikan lele (Clarias sp ) yang diberi perlakuan
E(18) (pembesaran 1000x) ……….……….. 25
7. Perbandingan (%) asam amino esensial pakan
v
1. Prosedur analisa proksimat ……… 38
2. Proses pembuatan preparat histologi ……….. 41
3. Perhitungan rata-rata laju pertumbuhan harian dan efisiensi pakan .. 43
4. Perhitungan retensi protein ………. 44
5. Perhitungan retensi lemak ……… 45
6. Komposisi proksimat tubuh dan hati ikan lele (Clarias sp) ………. 46
7. Kecernaan protein dan kecernaan pakan ………. 47
8. Eskresi Total Amonia Nitrogen (TAN) ……….. 48
9. Analisa statistik konsumsi pakan ……….. 49
10. Analisa statistik laju pertumbuhan harian ……… 49
11. Analisa statistik efisiensi pakan ……….. 49
12. Analisa statistik retensi protein ……… 50
13. Analisa statistik retensi lemak ………. 50
14. Analisa statistik kandungan protein tubuh (bobot basah) ……… 50
15. Analisa statistik kandungan lemak tubuh (bobot basah) ………. 50
16. Analisa statistik kandungan abu tubuh (bobot basah) ……….. 51
17. Analisa statistik kandungan air tubuh ……… 51
18. Analisa statistik kandungan protein hati (bobot basah) ……… 52
19. Analisa statistik kandungan lemak hati (bobot basah) ………. 52
20. Analisa statistik kandungan air hati ……….. 52
21. Analisa statistik kecernaan pakan ……….. 53
22. Analisa statistik kecernaan protein pakan ……… 53
PENDAHULUAN
Latar Belakang
Ikan lele (Clarias sp) adalah ikan yang hidup di perairan umum dan
merupakan ikan yang bernilai ekonomis serta disukai oleh masyarakat. Budidaya
ikan ini banyak dilakukan dengan sistem tradisional maupun dengan sistem
intensif. Semakin meningkatnya kegiatan budidaya ikan pada umumnya dan ikan
lele pada khususnya telah meningkatkan permintaan akan penyediaan pakan
buatan.
Pakan buatan umumnya menggunakan tepung ikan (fish meal/FM) sebagai
sumber protein dalam pakan yang berkisar 30 sampai 80% dari total bahan
(Utomo et al. 1999). Penggantian tepung ikan dengan bahan lain sebagai sumber
protein sudah berhasil dilakukan dengan menggunakan tepung bungkil kedelai
(SBM/soybean meal) (Suprayudi et al. 1999; Pebriyadi 2004; Elangovan dan
Shim 2000; Cheng et al. 2003; Catacutan dan Pagador 2004).
Walaupun SBM mampu mengganti sebagian tepung ikan, namun
ketersediaan SBM masih bergantung dari impor. Tingginya komponen impor
yakni tepung ikan dan SBM dalam pakan akan berdampak terhadap harga pakan.
Indonesia harus mengimpor SBM lebih dari 1 juta ton per tahun sejak tahun 2000
(Siagian dan Danang 2003; Suara Pembaharuan 2004; Ritonga 2002) dan pada
tahun 2005 sudah mencapai 1,8 juta ton (Riady 2006), sedangkan volume impor
tepung ikan rata-rata 32.000 ton perbulan dan 40% diantaranya diolah menjadi
pakan ikan (Kompas 2005). Produksi tepung ikan yang dipergunakan sebagai
bahan pakan ikan meningkat sekitar 35% pada tahun 2000 dan diperkirakan akan
mencapai 44% pada tahun 2010 (Baruah et al. 2004). Semakin tingginya
permintaan akan tepung ikan dan SBM menyebabkan semakin tingginya harga
pakan ikan.
Salah satu upaya untuk mengurangi ketergantungan terhadap bahan baku
impor dalam hal ini SBM, dapat dilakukan dengan penggunaan bahan baku
alternatif lokal yang harganya murah serta dapat disediakan dalam jumlah yang
Sumber protein nabati selain tepung bungkil kedelai yang dapat digunakan
dalam pakan ikan adalah tepung bungkil sawit (palm kernel meal/PKM) yang
merupakan produk sampingan dari pembuatan minyak kelapa sawit. Ketersediaan
PKM dalam negeri sangat melimpah bahkan 94% PKM yang diproduksi di
ekspor. Indonesia adalah negara penghasil PKM nomor dua setelah Malaysia
(Gelder et al. 2005). Penggunaan PKM dalam pakan ikan diharapkan dapat
mengurangi penggunaan bahan baku impor sehingga dapat menurunkan harga
pakan.
Penggunaan PKM dalam pakan dibatasi oleh tiga faktor yaitu: (1)
Rendahnya kandungan protein (4 sampai 18%), (2) kekurangan asam amino
esensial khususnya asam amino sulphur dan kemungkinan juga lisin, (3) adanya
antinutrien (Ng 2003). PKM mengandung 74,3 % non-starch polysaccharides
(NSP) yang sulit dicerna (Choct 2001). Walaupun demikian, penggunaan PKM
dalam pakan ikan sudah dilakukan oleh beberapa peneliti. Penelitian yang
dilakukan oleh Ng et al. (2002) menunjukkan bahwa penggunaan PKM 20% pada
pakan ikan tilapia (Oreochromis sp) dapat memberikan pertumbuhan dan efisiensi
pakan yang tidak berbeda nyata dengan pakan yang menggunakan FM 21% dan
SBM 23,83%. Penelitian lainnya menunjukkan bahwa penggunaan PKM yang
optimal dalam pakan ikan nila tilapia (Oreochromis mosambicus) dapat mencapai
30% (Lim et al. 2001), juvenile Labeo senegalensis 10% (Omoregie 2000) dan
pada juvenil patin jambal (Pangasius djambal) dapat mencapai 27% (Afifah,
2006). Hertrampf dan Felicitas (2000) merekomendasikan penggunaan PKM
dalam pakan sebesar 3 sampai 8% untuk ikan karnivora sedangkan untuk ikan
herbivora 5 sampai 10%. Penggunaan PKM dengan komposisi yang tepat dalam
pakan diharapkan dapat memberikan pakan yang harganya relatif lebih murah
namun tetap menghasilkan efisiensi pakan dan pertumbuhan yang tinggi bagi ikan
lele (Clarias sp).
Perumusan Masalah
Penggunaan bahan baku alternatif (selain tepung ikan) dalam pakan sering
menyebabkan terjadinya pertumbuhan yang rendah. Pertumbuhan sangat
dapat dimanfaatkan oleh ikan untuk pertumbuhan dan pemeliharaan. Pemanfaatan
protein ini sangat dipengaruhi oleh kualitas protein. Suatu protein dikatakan
berkualitas apabila mengandung asam amino esensial yang komposisinya serta
jumlahnya sesuai dengan kebutuhan tubuh, serta asam amino tersebut dapat
digunakan oleh tubuh (tersedia bagi tubuh). Dengan demikian, kualitas suatu
protein ditentukan juga oleh daya cerna atau nilai cernanya yang pada akhirnya
menentukan ketersediaan asam aminonya secara biologis. Keseimbangan jumlah
asam amino esensial dalam pakan akan mempengaruhi tingkat sintesis protein
yang akan diretens i.
Selain dari protein itu sendiri, jumlah energi total yang terkandung dalam
pakan juga akan mempengaruhi tingkat retensi protein. Keseimbangan antara
energi total pakan yang dapat dicerna dan kadar protein pakan sangat penting
untuk pertumbuhan ikan, karena apabila energi kurang, maka protein akan
dipecah dan digunakan sebagai sumber energi. Pemakaian sebagian protein
sebagai sumber energi ini akan menyebabkan pertumbuhan ikan terhambat,
karena protein sangat berperan dalam pembentukan sel baru. Ketersediaan energi
non protein harus didukung oleh kecernaan total pakan yang tinggi.
Kualitas protein pakan yang meliputi keseimbangan komposisi asam
amino esensial serta kecernaannya sangat dipengaruhi oleh bahan baku
penyumbang protein dalam pakan. Bahan baku pakan yang terbaik saat ini adalah
tepung ikan karena memiliki komposisi dan jumlah asam amino yang seimbang,
namun hal ini tidak berarti bahwa semua sumber protein selain tepung ikan tidak
dapat dipergunakan sebagai bahan baku pakan, paling tidak dapat menggantikan
sebagian dari tepung ikan.
Penggunaan PKM sebagai bahan baku alternatif harus menjamin bahwa
pakan yang dibentuk mempunyai kecernaan total dan kecernaan protein yang
yang tinggi dan mempunyai komposisi asam amino yang seimbang agar dapat
dimanfaatkan dalam proses metabolisme. Jumlah PKM yang tepat dalam pakan
diharapkan dapat membentuk pakan yang dapat dimanfaatkan secara optimal
Perumusan Hipotesis
Jumlah PKM yang tepat dalam pakan dapat menghasilkan pakan yang
memberikan tingkat pertumbuhan dan efisiensi pakan yang tinggi pada ikan lele
(Clarias sp.).
Tujuan dan Manfaat
Percobaan ini bertujuan untuk menentukan jumlah PKM yang dapat
memberikan pertumbuhan serta efisiensi pakan yang optimal pada ikan lele
(Clarias sp).
Manfaat penelitian adalah untuk memberikan informasi tentang
penggunaan PKM sebagai bahan baku alternatif dalam pakan ikan lele
TINJAUAN PUSTAKA
Kebutuhan Nutrien Ikan Lele
Protein adalah merupakan komponen utama jaringan dan organ dari tubuh
hewan dan juga senyawa nitrogen lainnya seperti asam nukleat, enzim, hormon
dan vitamin, sehingga keberadaannya harus secara terus menerus disuplai dari
makanan untuk pertumbuhan dan perbaikan jaringan tubuh (Furuichi 1988).
Jumlah protein yang diperlukan dalam pakan secara langsung dipengaruhi oleh
komposisi asam amino pakan. Ikan membutuhkan 10 jenis asam amino esensial
untuk menghasilkan pertumbuhan yang maksimal yaitu arginin, histidin,
metionin, lisin, fenilalanin, isoleusin, treonin, triptofan dan valin. Asam amino
esensial adalah asam amino yang tidak dapat disintesis oleh tubuh sehingga harus
tersedia dalam pakan (NRC 1983).
Kualitas suatu protein sangat ditentukan oleh kualitas dan kuantitas dari
asam amino khususnya bioavailabilitas dari asam amino tersebut. Asam amino
yang terserap dalam usus akan digunakan untuk: 1) Mengganti dan memelihara
jaringan protein dan senyawa nitrogen; 2) pertumbuhan (peningkatan protein
tubuh); dan 3) sebagai sumber energi. Peranan paling penting adalah untuk
memelihara jaringan tubuh dan untuk pertumbuhan sedangkan sebagai sumber
energi dapat diganti oleh karbohidrat dan lemak (Furuichi 1988).
Jumlah asam amino yang digunakan untuk pertumbuhan akan semakin
menurun seiring dengan penurunan tingkat pertumbuhan. Jumlah asam amino
yang dapat digunakan untuk pertumbuhan dan maintenance sangat tergantung dari
kualitas protein, tingkat asupan protein dan kandungan energi yang dapat dicerna
dari pakan serta keadaan fisiologi ikan itu sendiri. Asam amino yang digunakan
sebagai sumber energi akan dideaminasi dan dilepaskan sebagai amonia yang
akan dikeluarkan melalui insang. Pakan yang mempunyai kualitas protein yang
baik akan menghasilkan eskresi nitrogen yang lebih sedikit dari pada pakan yang
mempunyai kualitas protein yang buruk (Furuichi 1988).
Protein atau asam amino dibutuhkan secara terus menerus oleh ikan untuk
membentuk jaringan baru (pertumbuhan dan reproduksi) atau untuk mengganti
menurunkan pertumbuhan atau hilangnya bobot badan karena diambilnya protein
dari jaringan yang kurang penting untuk memelihara jaringan yang lebih penting.
Disisi lain jika protein terlalu banyak disuplai dari makanan, maka hanya sebagian
kecil yang akan digunakan untuk membuat protein baru dan sisanya akan
dikonversi menjadi energi (Halver dan Hardy 2002). Hal ini berarti bahwa
pemanfaatan protein untuk pertumbuhan menjadi tidak efisien.
Respon biologi yang penting dari organisme akuatik yang diberi pakan
yang mengandung bahan pengganti tepung ikan antara lain adalah feed intake,
perolehan bobot tubuh, rasio konversi pakan, komposisi tubuh, karakteristik
sensory, tingkat kelulusan hidup dan respon imun (Yu 2005).
Ikan, seperti juga dengan hewan lainnya, tidak mempunyai kebutuhan
protein yang pasti, tapi membutuhkan komposisi asam amino esensial dan non
esensial yang seimbang. Tingkat protein yang optimal dalam pakan untuk ikan
dipengaruhi oleh keseimbangan protein dengan energi total pakan, komposisi
asam amino dan kecernaan protein. Kebutuhan akan protein dipengaruhi oleh
spesies, ukuran dan umur serta suhu air. Kebutuhan akan protein akan menurun
seiring dengan peningkatan ukuran dan pertambahan umur dan meningkat seiring
dengan peningkatan suhu (Halver dan Hardy 2002).
Kebutuhan protein ikan salah satunya dipengaruhi oleh ukuran dan umur
ikan. Kebutuhan protein kasar Clarias batrachus adalah 30% sedangkan untuk
Clarias gariepinus adalah 40%, dengan energi total 18,6 kJ/g dan rasio energi
protein 21,5 (mg/Kj) (Hasan 2000). Nursyam (1991) yang melakukan penelitian
dengan menggunakan Clarias batrachus yang berukuran 1 g mengatakan bahwa
bahwa secara umum kadar protein yang paling baik untuk Clarias batrachus
adalah 40% dengan menggunakan kasein dan gelatin sebagai sumber protein
dengan kandungan energi pakan adalah 3000 kkal/kg pakan. Penelitian yang
dilakukan oleh Suhenda (1988) mendapatkan bahwa pakan dengan kadar protein
40% dan energi 3000 kkal/kg dapat digunakan untuk budidaya Clarias batrachus
dengan bobot 1,5 g.
Kebutuhan asam amino esensial ikan dapat diperkirakan berdasarkan
komposisi asam amino otot ikan (Cho 1983). Pada beberapa penelitian diperoleh
bahwa komposisi asam amino ikan tidak jauh berbeda dengan ik an lainnya,
flounder) (Kim dan Santosh 2000). Lemak berfungsi sebagai sumber energi dan
sumber asam lemak esensial yang diperlukan untuk pertumbuhan. Lemak juga
dapat membantu penyerapan vitamin yang larut dalam lemak. Ikan lele (Clarias
batrachus Linn) memerlukan asam linoleat dan asam linolenat sebesar 1,53 – 1,56
% dan 0,60 – 0,73 % dalam pakannya (bobot kering) (Mokoginta 1986).
Bahan Pakan Sumber Nutrien/Protein
Tepung Bungkil Kedelai (Soybean Meal/SBM)
Komposisi proksimat SBM dapat dilihat pada Tabel 1.
Tabel 1. Komposisi proksimat SBM
Komposisi proksimat Kandungan (%) Air
SBM mempunyai profil asam amino yang terbaik dibanding semua
sumber protein nabati. Asam amino pembatas pada SBM adalah metionin dan
lisin sedangkan arginin dan phenilalanin mempunyai jumlah yang cukup
(Tabel 2). SBM memiliki makromineral dan mikromineral yang rendah termasuk
fosfor jika dibandingkan dengan tepung ikan (NRC 1983). SBM adalah
merupakan sumber vitamin B (Hertrampf dan Felicitas 2000; Bureau 2005: Cheng
et al. 2003).
Tabel 2. Komposisi asam amino esensial SBM (% protein)
Selain itu SBM memiliki kandungan anti nutrien yaitu protease inhibitors,
lektin, phytic acid, saponin, phytoestrogen, antivitamin dan allergens. Anti nutrien
ini dapat mempengaruhi penggunaan dan pencernaan protein, penggunaan
mineral, antivitamin dan bersifat racun (Francis 2001).
Tingkat kecernaan energi SBM oleh ikan pada umumnya berkisar antara
2,572 sampai 3,340 kkal/kg (10,8 sampai 14,0 MJ/kg). Pada ikan channel catfish
tingkat kecernaan protein kasar SBM adalah sebesar 81,8%, dan tingkat kecernaan
energinya adalah 51,4%. Namun demikian kecernaan protein tidak selalu
menunjukkan kecernaan asam amino esensial. Berdasarkan data yang tersedia,
kecernaan asam amino dari SBM oleh ikan channel catfish lebih baik dari pada
kecernaan proteinnya (Hertrampf dan Felicitas 2000). Tingkat kecernaan nutrien
SBM pada ikan- ikan salmon air tawar lebih tinggi dibandingkan ikan salmon yang
ada di air laut (Usher et al. 1990).
Penggantian tepung ikan sebanyak 50% dengan menggunakan SBM pada
pakan rainbow trout menghasilkan pertumbuhan yang tidak berbeda nya ta dengan
pakan kontrol (fish meal/FM 32,8%). Penggantian tepung ikan sampai 75% akan
menghambat pertumbuhan namun tingkat FCR tidak berbeda secara signifikan
dengan pakan yang mengandung FM 32,8%. Penggantian total FM akan
menurunkan pertumbuhan dan mempertinggi nilai FCR sedangkan penambahan
asam amino metionin hidroxy analog pada pakan ikan rainbow trout yang
menggunakan SBM sebagai pengganti FM tidak mempengaruhi pertumbuhan dan
FCR (Cheng et al. 2003). Pada ikan red snapper (Lutjanus argentimaculatus)
penggunaan SBM untuk mengganti FM juga dapat mencapai 50% (Catacutan dan
Pagador 2004). Suprayudi et al. (1999) menyatakan bahwa penggantian tepung
ikan dengan defatted soybean meal pada ikan gurami (Osphronemus gouramy)
sebesar 50% memberikan palatabilitas yang baik. Peningkatan SBM sebesar
Tepung Bungkil Sawit (Palm Kernel Meal/PKM)
Tepung bungkil sawit adalah merupakan produk sampingan dari minyak
sawit. PKM lebih tepat disebut sebagai sumber karbohidrat dibanding sebagai
sumber protein karena kandungan proteinnya yang rendah sedangkan kandungan
karbohidratnya tinggi.
Komposisi proksimat PKM dapat dilihat pada Tabel 3.
Tabel 3. Komposisi proksimat PKM
Komposisi proksimat Kandungan (%) Air
PKM mempunyai kandungan protein yang berkisar antara 15 sampai 18%
dan mengalami kekurangan lisine dan metionin (Tabel 4). Kandungan serat kasar
dari PKM sangat tinggi dan rasio Ca:P adalah 1:2,4. PKM merupakan sumber
mangan yang baik (Hertrampf dan Felicitas 2000).
Tabel 4. Komposisi asam amino esensial PKM (% protein)
Asam Amino Esensial PKM
Sumber : PKM (Hertrampf dan Felicitas 2000).
PKM mengandung sedikitnya 60% NSP (non-starch polysaccharides)
yang merupakan faktor pembatas utama dalam penggunaannya pada pakan hewan
monogastric karena tidak dapat dicerna (Choct 2001; Choi et al. 2004 ). Pada
juvenil turbot (Psetta maxima) keberadaan NSP dan faktor anti nutrien lainnya
dalam pakan yang menggunakan tepung Lubinus albus sebagai pengganti tepung
tingkat pengambilan pakan (Fournier 2004). NSP dapat mengganggu
pertumbuhan karena NSP akan terikat dalam air dan membentuk semacam gum di
dalam intestine, meningkatkan viskositas baha n-bahan yang ada dalam usus dan
menghalangi aktifitas enzim pencernaan sehingga berpotensi menjadi antinutrisi
jika berada dalam pakan ikan (Francis et al. 2001)
Penggunaan PKM 20% (bobot kering) dalam pakan ikan nila tilapia
(Oreocromis sp) tidak menunj ukkan pengaruh negatif terhadap pertumbuhan dan
efisiensi pakan bila dibandingkan dengan pakan kontrol yang menggunakan FM
21,19 dan SBM 30,73% sebagai sumber protein, namun jika PKM diberi
perlakuan dengan menggunakan enzim maka penggunaan PKM 40 % akan
memberikan pertumbuhan yang lebih baik dari penggunaan PKM tanpa ada
perlakuan. Semakin tinggi penggunaan PKM dalam pakan ikan nila tilapia
(Oreochromis sp) akan semakin menurunkan tingkat kecernaan protein, lemak
dan energi (Ng 2002).
Penelitian yang dilakukan oleh Lim (2001) pada ikan tilapia (Oreocromis
mossambicus) menunjukkan bahwa penggunaan PKM 30% dalam pakan
memberikan pertumbuhan yang tidak berbeda nyata dengan ikan yang diberi
pakan kontrol yang menggunakan tepung ikan 43% dan SBM 20,75% sebagai
sumber protein walaupun tingkat kecernaan proteinnya lebih rendah dari pakan
kontrol. Semakin tinggi penggunaan PKM dalam pakan akan menurunkan
kecernaan bahan kering pakan dan kecernaan proteinnya.
Pada juvenil Labeo senegalensis pemberian pakan yang menga ndung
PKM 10% dalam pakan menunjukkan pertumbuhan dan tingkat konversi pakan
yang sama dengan pakan kontrol yang hanya menggunakan tepung ikan sebagai
sumber protein meskipun tingkat kecernaan pakannya lebih rendah. Penggunaan
PKM lebih dari 10% akan menekan pertumbuhan juvenil Labeo senegalensis
(Omoregie 2001). Juvenil patin jambal siam (Pangasius djambal) dapat
menggunakan PKM sebanyak 27% dalam pakan dengan sumbangan protein dari
PKM dapat mencapai 11% (Afifah 2006).
Hertrampf dan Felicitas (2000) menyarankan penggunaan PKM dalam
pakan sebanyak 5 sampai 10 % untuk ikan herbivora dan 3 sampai 8 % untuk ikan
Tepung Tulang dan Daging (Meat and Bone Meal/MBM)
MBM adalah merupakan suatu sumber protein hewani yang mempunyai
komposisi kimia yang sangat bervariasi yang bergantung pada kualitas dari bahan
bakunya. Tingginya bagian tulang dan/atau lemak dalam bahan dasar MBM akan
menyebabkan tingginya kadar abu dan/atau kandungan lemak yang dapat
mereduksi kandungan protein yang dihasilkan (Hertrampf dan Felicitas 2000).
Komposisi proksimat MBM dapat dilihat pada Tabel 5.
Tabel 5. Komposisi proksimat MBM
Komposisi Proksimat Kandungan (%) Air
Kisaran komposisi nutrien MBM sangat tinggi, sehingga dalam
penggunaannya sebaiknya MBM terlebih dahulu dianalisa pada setiap kali akan
menggunakan tepung tersebut. Hal ini disebabkan karena terjadinya perbedaan
bahan baku (daging) dan pengolahan yang dilakukan terhadap bahan baku
(Hertrampf dan Felicitas 2000; Yu 2005).
Pakan dengan sumber protein hewani yang berasal dari produk sampingan
hewan seperti, tepung darah, tepung bulu, dan MBM kemungkinan kekurangan
beberapa asam amino karena bahan-bahan ini cenderung mempunyai profile asam
amino (Tabel 6) yang tidak sempurna dan pola kecernaan asam amino yang
bervariasi (Bureau 2005).
Tabel 6. Komposisi asam amino esensial MBM (% protein)
Asam Amino Esensial MBM
Isoleusin dan metionin+sistein adalah merupakan asam amino pembatas
jika dibandingkan dengan komposisi asam amino pada protein telur. Semakin
tinggi kandungan abu maka kandungan makromineral juga akan meningkat
sedangkan kandungan mikromineral (trace) lebih sedikit karena umumnya
mikromineral disimpan dalam daging. Kandungan vitamin MBM sangat rendah
(Hertrampf dan Felicitas 2000).
Tingkat kecernaan energi MBM secara umum pada ikan lebih rendah 8
sampai 10% dari pada tepung ikan sedangkan kecernaan fosfornya adalah 63
sampai 70%. Kecernaan semu protein MBM pada ikan trout, salmon, Japanese
seabass dan striped bass adalah sebesar 83% sedangkan kecernaan energinya
sebesar 73% (Yu 2005). Pada ikan silver perch (Bidyanus bidyanus) tingkat
kecernaan semu proteinnya adalah 71,5%, energi 75,2% dan bahan kering 50,1%
(Allan et al. 2000). Kecernaan protein MBM pada berbagai pene litian relatif
tinggi namun demikian kecernaan bahan kering MBM relatif rendah (40 sampai
50%) yang disebabkan karena tingginya kadar abu (25 sampai 30% dan fosfor 4
sampai 5 %) (Bureau 2005).
Pada pakan benih ikan nila (Oreochromis niloticus), MBM dapat
menggantikan 25% tepung ikan tanpa menimbulkan efek negatif terhadap
pertumbuhannya (Tacon et al. 1984). Pada benih tilapia (Oreochromis
mossambicus) penggantian sebagian tepung ikan dengan menggunakan MBM
memperlihatkan pertumbuhan yang sama dengan ikan yang diberi pakan dengan
menggunakan 100% tepung ikan, akan tetapi apabila dilakukan penggantian total
tepung ikan dengan menggunakan MBM akan memberikan pertumbuhan yang
buruk. Pertumbuhan yang tidak baik akan ditunjukkan oleh juvenil ikan common
carp jika dalam pakannya digunakan MBM dengan tingkat substitusi FM lebih
dari 70% (Hertrampf dan Felicitas 2000). Tepung ikan pada pakan catfish dapat
diganti dengan MBM sebanyak 80%, tilapia 70%, eel 30%, juvenil common carp
20%; dan yearling common carp 70% (Yu 2005).
Beberapa literatur menunjukkan bahwa penggunanan MBM dibawah 50%
sebagai substitusi protein FM tidak memberikan pengaruh yang signifikan
terhadap konsumsi pakan, survival rate, komposisi tubuh dan sensor ikan namun
kemungkinan disebabkan oleh menurunnya kecernaan pakan, profile asam amino,
kandungan energi dan kandungan lemak (Yu 2005).
Kandungan asam amino ensensial pada MBM lebih rendah daripada FM,
namun demikian perbedaan kandungan tersebut dapat diperbaiki dengan
penggunaan asam amino kristallin atau dengan mencampurnya dengan bahan
protein lainnya. MBM tidak mengandung faktor anti nutrien, phytate fosforus,
karbohidrat kompleks, non-palatabel dan tidak berbahaya (Yu 2005).
Penggunaan MBM di dalam pakan dibatasi oleh kandungan abunya yang
tinggi. Jumlah MBM yang direkomendasikan untuk digunakan dalam pakan
BAHAN DAN METODE
Penelitian ini dilakukan di Laboratorium Basah Nutrisi Ikan Departemen
Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian
Bogor. Penelitian dilaksanakan pada bulan Maret sampai Juli 2006.
Pakan Uji
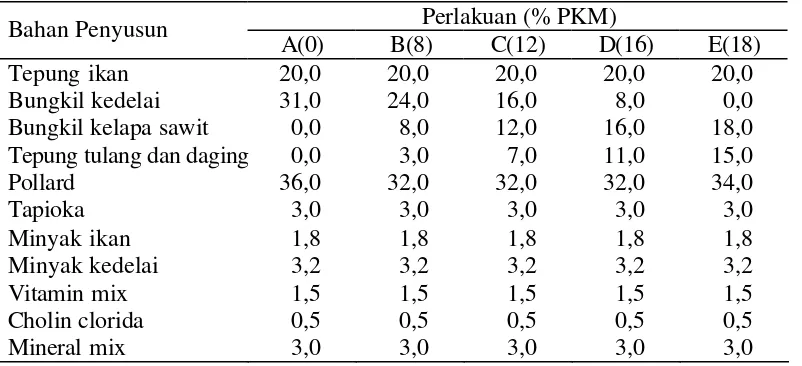
Pakan uji berbentuk pelet dan terdiri dari lima jenis pakan dengan
komposisi jumlah bahan baku yang berbeda. Kandungan protein pakan berkisar
30% dengan CP ratio yang berkisar 14,28 kkal GE/g protein. Semua pakan
menggunakan 20% tepung ikan dalam pakan. Pakan A sebagai kontrol
menggunakan 31% SBM dalam pakan tanpa menggunakan PKM. Pakan B, C, D
dan E menggunakan PKM sebagai berikut :
Perlakuan A : 0% PKM
Perlakuan B : 8 % PKM
Perlakuan C : 12% PKM
Perlakuan D : 16% PKM
Perlakuan E : 18% PKM
Minyak ikan dan minyak kedelai digunakan sebagai sumber lemak dengan
perbandingan 0,8:1,4. Komposisi pakan uji dan hasil analisa proksimat pakan uji
disajikan pada Tabel 7 dan 8.
Tabel 7. Komposisi pakan uji (g/100 g pakan)
Perlakuan (% PKM) Bahan Penyusun
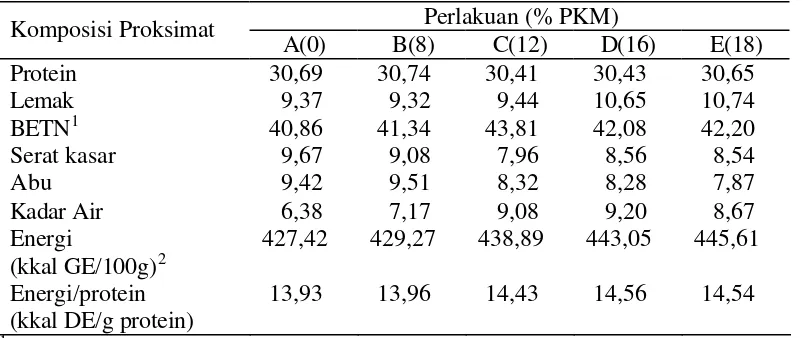
Tabel 8. Komposisi proksimat pakan (% bobot kering)
Total energi tercerna (GE/Gross Energy) dihitung berdasarkan nilai ekuivalen untuk protein 5,6 kkal g-1, lemak 9,4 kkal g-1, dan BETN 4,1 kkal g-1.
Pemeliharaan Ikan dan Pengumpulan Data
Ikan uji yang digunakan adalah ikan lele (Clarias sp) dengan bobot
18,4+0,3 g dengan kepadatan 10 ekor per akuarium. Wadah pemeliharaan
menggunakan 15 akuarium yang berukuran 50×40×35 cm dengan volume 60 liter
yang dilengkapi dengan sistem aerasi dan sirkulasi air. Ikan yang akan dijadikan
sampel diadaptasikan selama 20 hari sebelum diberi pakan uji.
Air yang digunakan untuk pemeliharaan terlebih dahulu diendapkan dan
diaerasi minimal selama 24 jam dalam bak penampungan. Pengukuran kualitas air
dilakukan tiga kali yaitu pada awal, pertengahan dan akhir penelitian. Hasil
pengukuran kualitas air : Suhu 30 sampai 32oC, pH 6,15 sampai 7,2, amonia 0,5
sampai 1,05 mg/l. Kisaran hasil pengukuran kualitas air yang diperoleh masih
dalam batas toleransi yang dapat mendukung pertumbuhan ikan lele (Clarias sp).
Pemeliharaan ikan dilakukan selama 60 hari. Selama masa pemeliharaan
ikan diberi pakan sesuai perlakuan sampai kenyang (at satiation) sebanyak tiga
kali sehari yaitu pada jam 06.00, 12.00 dan 18.00 WIB.
Pengukuran bobot dilakukan pada awal dan akhir penelitian. Bobot yang
diukur adalah bobot biomassa yang kemudian dirata-ratakan untuk setiap ekor
ikan. Pada saat penimbangan, ikan terlebih dahulu dibius dengan menggunakan
2-phenoxy ethanol 0,5 mg/liter untuk mengurangi stress pada ikan. Sebelum
Pengukuran bobot dilakukan untuk mengetahui tingkat pertumbuhan. Jumlah
pakan yang diberikan selama penelitian dihitung untuk mengetahui tingkat
konsumsi pakan dan perhitungan efisiensi pakan.
Analisis Kimia
Analisis kimia dilakukan untuk mengetahui komposisi proksimat bahan
baku pakan, pakan, tubuh ikan, hati dan feses. Bahan baku pakan diproksimat
sebagai dasar penyusunan pakan sedangkan pakan yang telah dibentuk juga
diproksimat untuk mengecek komposisi proksimatnya. Analisa proksimat tubuh
dan hati dilakukan pada awal dan akhir penelitian yang bertujuan untuk
menghitung tingkat retensi protein dan retensi lemak tubuh sedangkan proksimat
hati dilakukan untuk mengetahui terjadinya penumpukan lemak pada hati. Analisa
proksimat feses dilakukan untuk menghitung kecernaan total pakan dan kecernaan
protein pakan. Analisa proksimat yang dilakukan terdiri atas : protein, lemak,
sarat kasar, abu, bahan ekstrak tanpa nitrogen (BETN) dan kadar air. Khusus
untuk hati, analisa proksimatnya hanya menghitung kandungan lemak, protein dan
air sedangkan analisa proksimat feses hanya mengukur kandungan protein.
Analisa proksimat untuk protein kasar dilakukan dengan metode Kjeldhal
lemak dengan metode ekstraksi menggunakan alat Soxhlet; abu dengan
menggunakan pemanasan dalam tanur pada suhu 400 sampai 600 oC, serat kasar
menggunakan metode pelarutan sampel dengan asam dan basa kuat serta
pemanasan, dan; kadar air dengan menggunakan metode pemanasan dalam oven
pada suhu 105 sampai 110oC. Lemak hati diproksimat dengan menggunakan
metode Folch et al. (Takeuchi 1988). Prosedur analisa dapat dilihat pada
Lampiran 1.
Histologi Hati
Histologi hati dilakukan untuk melihat terjadinya penumpukan lemak dan
perbedaan keadaan hepatosit pada setiap perlakuan. Pengambilan sampel hati
dilakukan pada akhir penelitian. Hati langsung diambil sesaat setelah ikan mati
dilakukan dengan metode pewarnaan hematoksilin-eosin. Prosedur histologis hati
dapat dilihat pada Lampiran 2. Hasil histologi selanjutnya diamati dengan
mikroskop pada pembesaran 1000x.
Uji Kecernaan Pakan
Uji kecernaan pakan dilakukan setelah masa perlakuan untuk respon
pertumbuhan selesai (setelah 60 hari). Pakan yang diberikan adalah pakan
perlakuan yang telah diberi Cr2O3 0,7%. Sebelum pengambilan feses, ikan
diadaptasikan selama 10 hari dengan pakan uji. Pemberian pakan uji dilakukan
sampai kenyang dan pengambilan feses dilakukan 2 jam setelah pemberian pakan.
Pengambilan feses dilakukan dengan metode penyiponan. Pengumpulan feses
dilakukan selama 10 hari.
Pengukuran Eskresi Total Amonia Nitrogen (TAN)
Pengukuran total amonia nitrogen (TAN) dilakukan untuk mengetahui
besarnya total amonia nitrogen (NH3-N) yang dieskresikan oleh ikan. Pengukuran
TAN dalam air menggunakan metode Phenate. Ikan uji ditimbang kemudian
dipuasakan selama 24 jam. Koreksi konsentrasi amonia di air selama pengukuran
TAN dilakukan dengan menyediakan akuarium yang diisi air tanpa ikan sebagai
kontrol. Pengambilan sampel air dilakukan setelah ikan diberi pakan sampai
kenyang (jam ke 0). Pengukuran TAN berikutnya dilakukan setiap jam sampai
jam kelima. Selama pengukuran berlangsung, aerasi dan sistem sirkulasi
dihentikan. Untuk menghindari terjadinya pengaruh dari luar (difusi oksigen atau
lepasnya amonia) maka akuarium ditutup dengan stirofoam.
Analisis Data
Penelitian ini menggunakan rancangan acak lengkap yang terdiri atas 5
perlakuan dan 3 ulangan dengan jumlah satuan percobaan 15 yang berupa
akuarium. Uji kecernaan dan total eskresi amonia hanya menggunakan 2 ulangan.
Parameter yang akan diuji secara statistik adalah tingkat konsumsi pakan, retensi
protein, retensi lemak, laju pertumbuhan harian, efisiensi pakan, tingkat kecernaan
terhadap setiap peubah yang diukur digunakan analisis ragam (uji F). Jika terdapat
perbedaan antara perlakuan dilanjutkan dengan uji BNT (Duncan test). Histologi
hati dianalisa secara deskriptif.
Variabel yang diuji secara statistik adalah sebagai berikut :
1. Retensi protein dan lemak (Takeuchi 1988)
RP = bobot protein tubuh akhir (g) – bobot protein tubuh awal (g) x 100 %
2. Laju pertumbuhan (Huisman 1976)
Wt = Wo (1 + 0,01 a )t
Keterangan :
a = Laju pertumbuhan harian
Wo = Bobot rata-rata ikan pada awal percobaan (g)
Wt = Bobot rata-rata ikan pada akhir percobaan (g)
t = Waktu pemeliharaan (hari)
3. Efisiensi pakan (Takeuchi 1988)
(
)
Bt = Bobot ikan pada akhir percobaan (g)
Bo = Bobot ikan pada awal percobaan (g)
Bd = Jumlah bobot ikan yang mati selama percobaan (g)
F = Jumlah pakan yang dikonsumsi selama percobaan (g)
4. Kecernaan pakan (Apparent Digestibility Coeficient/ADC) (Takeuchi 1988)
5. Eskresi amonia nitrogen/NH3-N
Ekskresi NH3-N (mg/g tubuh/jam) =
[
] [
]
t
x
g
xV
N
NH
N
NH
t ti 3 0
3
−
−
−
Keterangan :
[NH3-N]ti = Konsentrasi amonia pada akhir pengamatan (mg/l)
[NH3-N]to = Konsentrasi amonia pada awal pengamatan (mg/l)
HASIL DAN PEMBAHASAN
Hasil
Hasil percobaan penggunaan tepung bungkil kelapa sawit (PKM) dalam
pakan dapat mempengaruhi pertumbuhan ikan lele (Clarias sp). Data perubahan
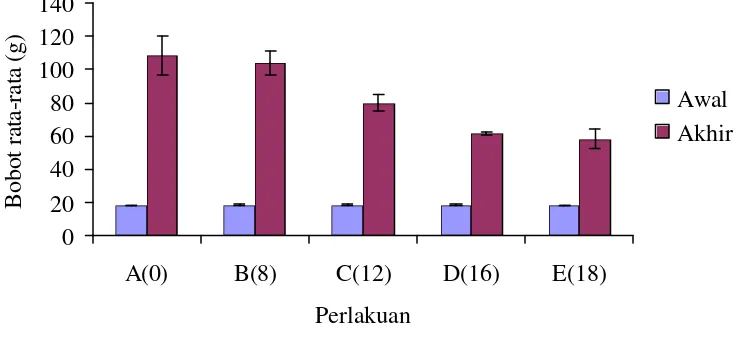
bobot rata-rata ikan per ekor dapat dilihat pada Gambar 1. Data selengkapnya
dapat dilihat pada Lampiran 3.
0 20 40 60 80 100 120 140
A(0) B(8) C(12) D(16) E(18)
Perlakuan
Bobot rata-rata (g)
Awal Akhir
Gambar 1. Bobot rata-rata ikan lele (Clarias sp) pada awal dan akhir percobaan
Penggunaan PKM dalam pakan dapat mempengaruhi (p<0,05) tingkat
konsumsi pakan, laju pertumbuhan harian, efisiensi pakan dan retensi protein,
sedangkan untuk retensi lemak tidak dipengaruhi (p>0,05) oleh perlakuan
(Lampiran 9,10,11,12 dan 13). Data mengenai tingkat konsumsi pakan, laju
pertumbuhan harian, efisiensi pakan, retensi protein dan retensi lemak untuk
setiap perlakuan disajikan pada Tabel 9 dan data selengkapnya dapat dilihat pada
Tabel 9. Rata-rata Konsumsi Pakan (KP), Laju Pertumbuhan Harian (LPH), Efisiensi Pakan (EP), Retensi Protein (RP) dan Retensi Lemak (RL).
Perlakuan (% PKM) Para-
meter A(0) B(8) C(12) D(16) E(18)
KP (g) 113,71 + 11,54a 1 05,40 + 7,09a 85,00 + 6,63b 62,66 + 2,00c 62,39 + 5,38c LPH (%) 3,11 + 0,22a 3,01 + 0,13a 2,56 + 0,13b 2,09 + 0,06c 2,00 + 0,19c EP (%) 79,01 + 4,19ab 82,05 + 2,83a 73,38 + 2,47b 68,39 + 1,50bc 63,34 + 6,81c RP (%) 34,22 + 2,26a 36,13 + 2,29a 30,59 + 2,23b 31,23 + 1,51b 27,52 + 1,57c RL (%) 55,42 + 9,49a 58,72 + 6,50a 55,32 + 4,03a 53,42 + 1,01a 50,77 + 16,22a Keterangan: Huruf superskrip dibelakang nilai standar deviasi yang berbeda pada setiap baris
menunjukkan adanya perbedaan nyata antara perlakuan (p<0,05)
Tingkat konsumsi pakan paling tinggi terjadi pada perlakuan A(0) dan
B(8) (p>0,05). Kemudian menurun seiring dengan semakin meningkatnya
penggunaan PKM yaitu pada perlakuan C(12) kemudian D(16)=E(18) (p>0,05)
(Lampiran 9).
Laju pertumbuhan harian tertinggi diperoleh pada perlakuan A(0) dan B(8)
(p>0,05). Laju pertumbuhan semakin menurun seiring dengan semakin tingginya
penggunaan PKM. Laju pertumbuhan ikan yang terendah terjadi pada perlakuan
D(16) dan E(18) (p>0,05) (Lampiran 10). Perlakuan A(0) dan B(8) memiliki
tingkat efisiensi paling tinggi (p>0,05) dan semakin menurun pada perlakuan
C(12), D(16) dan E(18) (p<0,05) (Lampiran 11).
Retensi protein tertinggi terjadi pada perlakuan A(0) dan B(8) (p>0,05).
Retensi protein selanjutnya akan semakin menurun pada perlakuan C(12) dan
D(16) (p>0,05) dan paling rendah pada perlakuan E(18) (Lampiran 12),
sedangkan retensi lemak tidak dipengaruhi (p>0,05) oleh penggunaan PKM
dalam pakan (Lampiran 13).
Hasil analisa proksimat tubuh ikan pada awal dan akhir penelitian
menunjukkan bahwa secara umum terjadi peningkatan kandungan protein dan
lemak tubuh selama pemberian pakan perlakuan. Pengaruh pakan percobaan
terhadap komposisi proksimat tubuh ikan pada setiap perlakuan disajikan pada
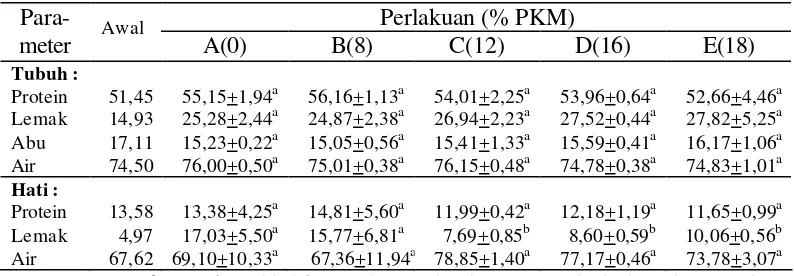
Tabel 10. Komposisi proksimat tubuh (% bobot kering) dan hati (% bobot basah) Keterangan: Huruf superskrip dibelakang nilai standar deviasi yang berbeda pada setiap baris
menunjukkan adanya perbedaan nyata antara perlakuan (p<0,05)
Secara umum penggunaan PKM tidak mempengaruhi kandungan protein,
lemak, abu dan air tubuh ikan lele (p>0,05) (Lampiran 14, 15, 16 dan 17).
Kandungan lemak tubuh mengalami peningkatan yang cukup tinggi dibandingkan
dengan peningkatan kandungan protein. Hasil proksimat hati ikan lele
menunjukkan adanya pengaruh (p<0,05) perlakuan terhadap kandungan lemak
hati namun tidak berpengaruh terhadap kandungan protein dan air hati ikan lele
(p<0,05). Kandungan lemak hati tertinggi terjadi pada perlakuan A(0) kemudian
diikuti oleh perlakuan B(8) (p>0,05) sedangkan perlakuan C(12), D(16) dan E(18)
memiliki kandungan lemak yang lebih rendah (p>0,05) (Lampiran 18, 19 dan 20).
Hasil pengukuran eskresi total amonia nitrogen (NH3-N), kecernaan
protein serta kecernaan pakan disajikan pada Tabel 11. Data untuk setiap ulangan
dapat dilihat pada Lampiran 7 dan 8.
Tabel 11.Kecernaan Pakan (KP), Kecernaan Protein Pakan (KPP) dan eskresi Total Amonia Nitrogen (TAN)
% Protein SBM:% Protein PKM: % Protein MBM
Para-
Penggunaan PKM dalam pakan dapat mempengaruhi (p<0,05) tingkat
kecernaan total pakan dan protein pakan. Semakin tinggi tingkat penggunaan
PKM dalam pakan maka tingkat kecernaan pakan dan kecernaan protein pakan
akan semakin menurun. Kecernaan pakan tertinggi terjadi pada perlakuan
A(0),B(8) dan C(12) (p>0,05) kemudian menur un pada perlakuan D(16) dan
E(18) (p>0,05). Perlakuan A(0) dan B(8) (p>0,05) memiliki kecernaan protein
paling tinggi dan kemudian menurun pada perlakuan C(12) dan paling rendah
pada perlakuan D(16) dan E(18) (p>0,05) (Lampiran 21 dan 22).
Total ekskresi NH3-N yang diukur selama lima jam menunjukkan tidak
adanya pengaruh (p>0,05) perlakuan terhadap total eskresi amonia (Lampiran
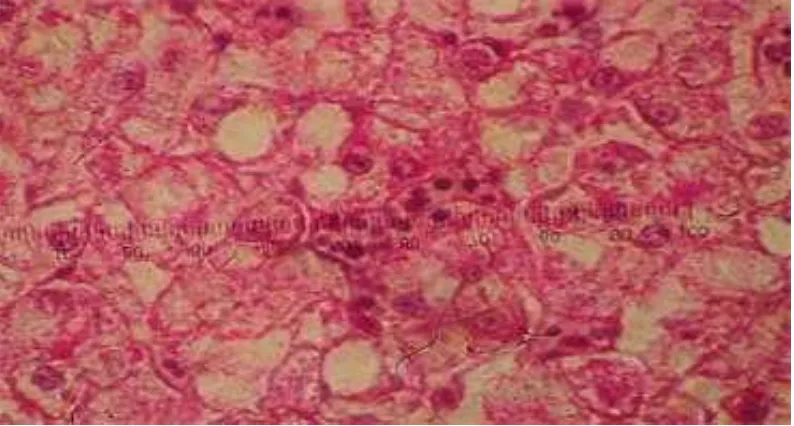
23). Pengaruh penggunaan PKM dalam pakan terhadap hati ikan lele dilakukan
dengan mengamati preparat histologi hati ikan pada pembesaran 1000 kali seperti
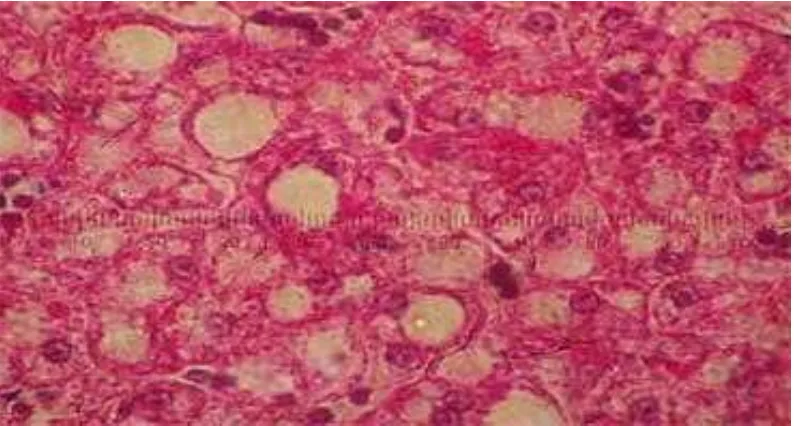
yang ditampilkan pada Gambar 2 sampai Gambar 6. Preparat hati ikan lele yang
diberi perlakuan menunjukkan bahwa terdapat perbedaan dalam hal jumlah sel
persatuan luas dan ukuran vakuola yang berbeda.
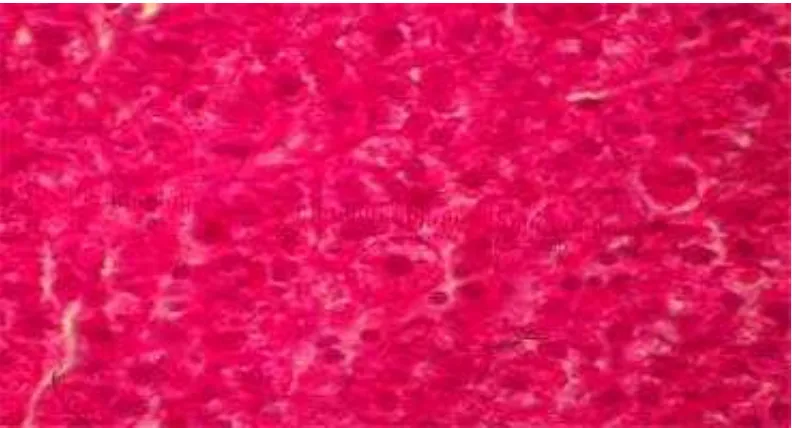
Gambar 3. Histologi hati ikan lele (Clarias sp) yang diberi perlakuan B(8) (pembesaran 1000 x).
Gambar 5. Histologi hati ikan lele (Clarias sp) yang diberi perlakuan D(16) (pembesaran 1000 x).
Gambar 6. Histologi hati ikan lele (Clarias sp) yang diberi perlakuan E(18) (pembesaran 1000 x).
Berdasarkan ga mbar histologi hati di atas dapat diketahui bahwa, hepatosit
ikan pada perlakuan A(0) dan B(8) memiliki vakuola dengan ukuran yang lebih
besar jika dibandingkan dengan perlakuan lainnya. Perlakuan C(12), D(16) dan
E(18) hampir tidak memiliki vakuola dan memiliki kerapatan yang lebih tinggi
Pembahasan
Parameter uji yang digunakan untuk mengevaluasi pengaruh penggunaan
tepung bungkil kelapa sawit (PKM) menunjukkan bahwa tingkat penggunaan
PKM yang optimal dalam pakan adalah sebesar 8%. Terjadinya pertumbuhan
pada semua perlakuan merupakan indikator bahwa energi yang dikonsumsi sudah
melebihi energi yang dibutuhkan untuk maintenance dan voluntary (NRC 1983;
Steffens 1989).
Laju pertumbuhan harian menunjukkan tingkat pertumbuhan ikan setiap
harinya. Tingkat pertumbuhan tertinggi terjadi pada pakan A(0) dan B(8).
Penggunaan PKM pada pakan B(8) memberikan efisiensi pakan yang setara
dengan perlakuan A(0). Yamamoto et al. (1995) mengatakan bahwa
penggabungan beberapa sumber protein dapat meningkatkan tingkat penggantian
tepung ikan.
Semakin tinggi penggunaan PKM dalam pakan dapat menekan
pertumbuhan ikan. Hal ini kemungkinan disebabkan oleh komposisi asam amino
pakan yang tidak seimbang, penurunan tingkat kecernaan nutrisi pakan dan
palatabilitas. Selain itu PKM banyak mengandung non-starch polysaccharida
(NSP) yang berpotensi untuk menjadi anti nutrisi jika berada dalam pakan ikan
karena NSP akan terikat dalam air dan membentuk semacam gum di dalam
intestine, meningkatkan viskositas bahan-bahan yang ada dalam usus dan
menghalangi aktifitas enzim pencernaan sehingga akan menekan pertumbuhan
(Francis et al. 2001). Di daerah tropis yang mempunyai kelembaban dan suhu
yang tinggi serta penyimpanan yang kurang baik dapat menyebabkan tumbuhnya
jamur khususnya dari genus Aspergillus yang menghasilkan senyawa kimia yang
sangat toksik yakni aflatoksin. Aflatoksin akan menyebabkan pertumbuhan yang
lambat, mengurangi tingkat konsumsi pakan, pathologis pada hati serta
mempengaruhi pankreas dan ginjal (Lim et al. 2001). Kandungan aflatoksin
dalam PKM bisa diminimalisir bahkan tidak teridentifikasi jika PKM ditangani
Indeks asam amino esensial pakan dan asam amino esensial tubuh dapat
digunakan untuk menentukan kebutuhan asam amino esensial ikan. Pola asam
amino esensial pakan dapat dihitung berdasarkan kandungan asam amino esensial
bahan baku penyumbang protein (Tabel 12).
Tabel 12. Komposisi asam amino esensial pakan percobaan dan tubuh ikan
Berdasarkan data dari Tabel 12, kebutuhan asam amino esensial ikan lele
(Clarias sp) dan ketersediaan asam amino esensial dalam pakan dapat
digambarkan dengan menghitung rasio asam amino esensial pakan/tubuh ikan
(Gambar 7).
Arginin Histidin Isoleusin Leusin Lisin Metionin
Phenilalanin Threonin Tryptophan
Gambar 7 menunjukkan bahwa dari keseluruhan asam amino esensial,
hanya asam amino triptopan yang mengalami peningkatan jumlah sedangkan yang
lainnya mengalami penurunan seiring dengan semakin meningkatnya tingkat
penggunaan PKM dan MBM. Gambar 7 juga menunjukkan bahwa semua pakan
uji mengalami kekurangan asam amino histidin dan metionin.
Penggunaan PKM 8% memberikan komposisi asam amino pakan yang
lebih rendah dari pakan kontrol namun belum mempengaruhi tingkat
pertumbuhan pada perlakuan B(8). Penggunaan PKM yang melebihi 8% akan
menyebabkan terjadinya penurunan nilai nutrien pakan yang ditandai dengan
semakin menurunnya tingkat pertumbuhan seperti pada perlakuan C(12), D(16)
dan E(18) yang disebabkan oleh semakin rendahnya ketersediaan asam amino
esensial dalam pakan yang menekan potensi pertumbuhan harian ikan.
Tingkat penggunaan PKM dalam pakan ikan lele yang dapat memberikan
pertumbuhan yang optimal pada penelitian ini menunjukkan hasil yang lebih
rendah dibandingkan dengan penggunaan PKM dalam pakan ikan tilapia
(Oreocromis sp) yang dapat mencapai 20% (Ng et al. 2002), pada juvenile Labeo
senegalensis sebesar 10% (Omoregie 2000), ikan nila tilapia Oreochromis
mosambicus dapat mencapai 30% (Lim et al. 2001) dan pada juvenil patin jambal
siam (Pangasius djambal) dapat menggunakan PKM sebanyak 27% dalam pakan
(Afifah 2006).
Faktor lain yang mempengaruhi tingkat pertumbuhan adalah tingkat
kecernaan total pakan dan kecernaan protein. Penggunaan PKM dapat
mempengaruhi tingkat kecernaan total dan protein pakan. Tingkat kecernaan
menunjukkan perbedaan jumlah antara nutrien yang diambil dan nutrien yang
diekskresikan dalam feses yang diekspresikan dalam persentase dari jumlah pakan
yang dimakan (Steffens 1989). Semakin tinggi penggunaan PKM dalam pakan
maka tingkat kecernaan pakan cenderung semakin menurun. Gejala yang sama
ditemukan pada Oreochromis mossambicus (Lim et al. 2001 ), Oreochromis sp
(Ng WK et al. 2002) dan Labeo senegalensis (Omoregie 2001) yang diberi pakan
dengan kandungan PKM yang berbeda. Penggunaan MBM yang semakin tinggi
juga menunjukkan tingkat kecernaan pakan yang semakin rendah seperti pada
beberapa spesies ikan, kecernaan protein PKM dan MBM lebih rendah dari
kecernaan SBM (Hertramft dan Felicitas 2000) sehingga semakin tinggi
penggunaan PKM dan MBM dalam pakan yang menekan jumlah SBM
menyebabkan tingkat kecernaan protein akan semakin menurun.
Tingkat kecernaan pakan yang semakin rendah pada perlakuan C(12),
D(16) dan E(18) menyebabkan rendahnya asupan energi yang dapat diambil ole h
ikan. Perbedaaan asupan energi ini dapat dilihat dari histologis hati yang memiliki
ukuran vakuola yang berbeda. Vakuola pada sel hati menggambarkan bekas
simpanan lemak yang terlarut oleh alkohol pada saat proses preparasi histologi
sehingga menyebabkan terbentuknya vakuola pada hepatosit. Semakin banyak
energi yang dapat dicerna maka simpanan energi dalam bentuk lemak di hati
semakin tinggi seperti pada perlakuan A(0) dan B(8) yang memilki vakuola yang
paling besar. Perlakuan C(12), D(16) dan E(18) memiliki vakuola yang lebih kecil
bahkan pada perlakuan tersebut banyak sel yang tidak memiliki vakuola. Data
yang diperoleh dari kandungan lemak hati juga menunjukkan bahwa ikan yang
memiliki asupan energi yang rendah karena kecernaan pakan yang rendah pada
perlakuan C(12), D(16) dan E(18) memiliki kandungan lemak hati yang lebih
rendah dari perlakuan A(0) dan B(8) yang memiliki kecernaan pakan yang lebih
tinggi.
Perbedaan tingkat konsumsi dapat disebabkan oleh perbedaan tingkat
pertumbuhan ikan. Ukuran ikan yang lebih besar pada perlakuan A(0) dan B(8)
memiliki konsumsi pakan yang tinggi sedangkan untuk ikan yang berukuran lebih
kecil memiliki tingkat konsumsi pakan yang rendah seperti pada perlakuan C(12),
D(16) dan E(18). Faktor lain yang menyebabkan perbedaan konsumsi pakan
adalah palatabilitas pakan. Rendahnya tingkat konsumsi pakan pada perlakuan
C(12), D(16) dan E(18) kemungkinan juga disebabkan karena semakin tingginya
kandungan MBM dalam pakan sehingga menurunkan palatabilitas pakan.
Penelitian yang dilakukan oleh Xue dan Cui (2000) menunjukkan bahwa semakin
tinggi tingkat penggunaan MBM dalam pakan akan menurunkan tingkat
palatabilitas pakan yang dibuktikan dengan rendahnya tingkat
pemilihan/preferensi pakan oleh ikan gibel carp pada pakan yang mengandung
pakan tersebut. Penurunan tingkat konsumsi pakan kemungkinan juga dapat
disebabkan oleh keberadaan NSP yang banyak terkandung dalam PKM. NSP pada
juvenil turbot (Psetta maxima) bersama dengan faktor anti nutrisi lainnya diduga
memperlambat retensi pakan dalam lambung sehingga mempengaruhi tingkat
pengambilan pakan (Fournier 2004).
Palatabilitas pakan juga berhubungan erat dengan atraktabilitas yang
diberikan oleh asam amino yang selanjutnya akan mempengaruhi searching
respon, pengambilan serta penelanan pakan dari ikan sehingga asam amino dapat
berperan sebagai feeding stimulant dalam pakan. Rangsangan sensor kimia oleh
asam amino tertentu akan menyebabkan repleks cephalic untuk meningkatkan
sekresi cairan gastrik dan meningkatkan kecernaan protein dan karbohidrat.
Adanya feeding stimulant yang berasal dari asam amino glicogenic seperti L-
alanin, L-proline dan glycine juga mempengaruhi preferensi penggunaan energi
dalam tubuh ikan sehingga akan meningkatkan penggunaan karbohidrat sebagai
sumber energi (Hara 1993), yang akhirnya akan meningkatkan efisiensi protein
pakan. Kecenderungan semakin rendahnya asam amino esensial pakan (Tabel 12)
dengan semakin meningkatnya penggunaan PKM kemungkinan juga
menunjukkan semakin rendahnya asamamino non esensial (L- alanin, L-proline
dan glycine) pakan yang dapat menjadi feeding stimulant dalam pakan yang
mengakibatkan tingkat konsumsi pakan menjadi lebih rendah.
Retensi nutrisi tertentu pada tubuh ikan selama periode tertentu biasanya
digunakan untuk mengevaluasi ketersediaan dan keseimbangan asam amino dan
ketersediaan beberapa elemen esensial nutrient lainnya. Retensi protein/lemak
merupakan persentase protein/lemak yang dimakan oleh ikan selama masa
percobaan yang dapat disimpan dalam tubuh ikan (Halver dan Hardy 2002).
Tingkat retensi protein yang semakin turun seiring dengan meningkatnya
penggunaan PKM dan MBM dalam pakan menunjukkan bahwa nilai nutrisi
protein pakan semakin menurun, hal ini dapat dilihat dari semakin rendahnya
tingkat kecernaan protein pakan dan komposisi asam amino esensial pakan yang
secara umum semakin menurun seiring dengan semakin tingginya tingkat
penggantian SBM. Retensi lemak yang berada di bawah 100% menunjukkan
diretensi sebagian besar merupakan lemak yang berasal dari lemak pakan.
Semakin tinggi tingkat penggunaan PKM dan MBM dalam pakan tidak
mempengaruhi retensi lemak.
Hasil ana lisa proksimat tubuh menunjukkan bahwa penggunaan PKM dan
MBM tidak menyebabkan perbedaan kandungan lemak dan protein tubuh. Pada
penelitian yang dilakukan oleh Lim et al. (2001) dan Ng et al. (2002) penggunaan
PKM dalam pakan ikan tilapia yang isoenergi dan isolipid tidak mempengaruhi
kandungan protein tubuh tetapi mempengaruhi kandungan lemak tubuh,
sedangkan pada penelitian yang dilakukan oleh Omoregie (2001) mendapatkan
tidak adanya perbedaan kandungan protein otot daging pada juvenile Labeo
senegalensis yang diberi pakan yang mengandung PKM.
Total eskresi amoniak (TAN) ikan yang mengkonsumsi pakan perlakuan
menunjukkan tidak adanya pengaruh perlakuan terhadap eskresi nitrogen ikan.
Eskresi amoniak sangat berhubungan dengan katabolisme asam amino yang
digunakan sebagai energi. Ikan akan mengeluarkan nitrogen yang dihasilkan dari
katabolisme asam amino dan metabolisme senyawa nitrogen lainnya ke dalam air
sebagai amonia dari insang (Halver dan Hardy 2002). Semakin tinggi nilai TAN
menunjukkan semakin banyaknya protein yang dideaminasi karena komposisi
asam amino yang tidak seimbang sehingga cenderung menurunkan retensi protein.
Menurut Lovell (1987) jika protein mempunyai komposisi asam amino yang tidak
seimbang maka hanya sebagian kecil asam amino yang akan disintesis dan asam
amino yang tidak digunakan akan dideaminasi dan diekskresikan sebagai
nitrogen. Pada penelitian ini, nilai TAN yang tidak berbeda menunjukkan bahwa
tingkat deaminasi asam amino esensial pakan sebagai akibat dari
Kesimpulan
Berdasarkan hasil penelitian ini dapat disimpulkan bahwa tingkat
penggunaan PKM sebanyak 8% dalam pakan dapat menghasilkan kinerja
pertumbuhan yang optimal pada ikan lele (Clarias sp).
Saran
PKM sebanyak 8% dapat digunakan sebagai bahan baku dalam pembuatan
DAFTAR PUSTAKA
Affandi R dan Tang UM 2002. Fisiologi Hewan Air. Pekanbaru-Riau: Unri Press. 217 hal.
Allan GL, Parkinson S. Booth MA, Stone DAJ, Rowland SJ, Frances J, Smith RW. 2000. Replacement of Fish Meal in Diets for Australian Silver Perch, Bidyanus bidyanus: I. Digestibility of Alternative Ingredients. Aquaculture 186: 293-310.
Afifah R. 2006. Pemanfaatan Bungkil Kelapa Sawit dalam Pakan Juvenil Ikan Patin Jambal (Pangasius djambal) [Skripsi]. Bogor: Fakultas Perikanan dan Ilmu Kelautan, Institut Perikanan Bogor. 29 hal.
Baruah K, Sahu NP, Pal AK, Debnath D. 2004. Dietary Phytase: An Ideal Approach for A Cost Effective and Low-Polluting Aquafeed. NAGA : Worldfish Center. Quarterly Vol 27 (3) July-Desember. p15–19.
Bureau DP et al.. 2000. Feather Meals and Meat and Bone Meals From Different Origin as Protein Sources in Rainbow Trout (Onchorhyncus mykiss) Diets. Aquaculture: 181. 281-291.
Bureau DP. 2005. Formulating More Cost-Effective Aquaculture Feeds. Canada, Ontario: University of Guelph. 12 pp.
Catacutan MR dan Gregoria EP. 2004. Partial Replacement of Fishmeal by Defatted Soybean Meal in Formulated Diets for The Mangrove Red Snapper, Lutjanus argentimaculatus (Forsskal 1775). Aquaculture Research 35: 299-306.
Cheng ZJ, Hardy RW, Blair M. 2003. Effects of Supplementing Methionine Hydroxy Analogue in Soybean Meal and Distiller’s Dried Grain- Based Diets on The Performance and Nutrient Retention of Rainbow Trout [Oncorhynchus Mykiss (Walbaum)]. Aquaculture Research 34: 1303-1310.
Chien YH dan Chiu YH. 2003. Replacement of Soybean (Glycine max (L.) Merrill) Meal by Lupin (Lupinus angustifolius) Seed Meal in Diet for Juvenil Tilapia (Oreochromis niloticus x O. aureus) Reared Indoors. Aquaculture Research: 34. 1261-1268.
Choct M. 2001. Nutritional Constraints to Alternative Ingredients. ASA Technical Bulletin Vol. AN31. p 1-3.
Chou SM, Wang X, Park GJ, Lim SR, Kim KW, Bai SC, Shim IS. 2004. Dietary Dehulled Soybean Meal as a Replacement for Fish Meal in Fingerling and Growing Olive Flounder, Paralichthys olivaceus (Temminck et Schlegel). Aquaculture Research 35: 410-418.
Elangovan A dan K.F Shim. 2000. The Influence of Replacing Fish Meal Partially in The Diet with Soybean Meal on Growth and Body Composition of Juvenile Tin Foil Barb (Barbodesw altus). Aquaculture 189: 133-144.
Fournier V, Huelvan C, Desbruyeres E. 2004. Incorpor ation of A Micture of Plant Feedstuffs as Subtitute for Fish Meal in Diets of Juvenile Turbot (Psetta maxima). Aquaculture: 236. 451-465.
Francis G, Makkar HPS, Becker K. 2001. Antinutritional Factors Present in Plant-Derived Alternate Fish Feed Ingredients and Their Effects in Fish: Review article. Aquaculture 199: 197-227.
Furuichi M. 1988. Dietary Requirements: Carbohydrates. di dalam: Watanabe T. Fish Nutrition and Mariculture. Departement of Aquatic Biosciences Tokyo University of Fishes. Tokyo: p 1-77.
Gelder Jan Willer van, Waklw Eriz, Schung Matthjs, H Myrthi 2005. Kutukan Komoditas: Panduan bagi ORNOP Indoneia. 82 Hal. http://www.profunfo.nl/downloads/kutukan.pdf?search=%22.indonesia%2 0palm%20kernel%20produser%27. [07 September 2006].
Halver JE dan Hardy RW, editor. 2002. Fish Nutrition. Third Edition. California USA: Academic Press. 822 pp.
Hasan MR. 2000. Nutrition and Feeding for Sustainable Aquaculture Development in the Third Millenium. [Article]. Technical Proceedings of The Conference on Aquaculture in the Third Millenium, Bangkok, Thailand. Bangkok. 36 pp.
Hara TJ. 1993. Chemoreception. di dalam: Evans HD. The Physiology of Fishes. CRC Press. London. 192-218 pp.
Kim JD dan Santosh PL. 2000. Amino Acid Composition of Whole Body Tissue of Atlantic Halibut (Hippoglossus hippoglossus), Yellowtail Flounder (Pleuronectes ferruginea) and Japanese Flounder (Paralichthys olivaceus). Aquaculture187: 367-373.
Kompas. 05 Agustus 2005. Limbah Sawit Bernilai Ekonomis. http://www. kompas.com/kompas_cetak/0608/05/ekonomi/2860110.htm.[07 September 2006].
Lim HA, Ng WK, Lim SL, Ibrahim CO. 2001. Contamination of Falm Kernel Meal with Aspergillus Flavus Affects its Nutritive Value in Pelleted Feed for Tilapia Oreochromis mossambicus. Aquaculture Researches 32:895-905.
Lovell T. 1987. Nutrition and Feeding of Fish. Department of Fisheries and Allied Aquaculture Auburn University. Auburn, Alabama. 330 pp.
Mokoginta I. 1986. Kebutuhan Ikan Lele (Clarias batrachus Linn) akan Asam-asam Lemak Linoleat dan Linolenat [Tesis]. Bogor: Fakultas Pasca Sarjana, Institut Perikanan Bogor. 66 hal.
Ng WK, Lim HA, Lim SL, Ibrahim CO. 2002. Nutritive Value of Palm Kernel Meal Pretreated with Enzyme or Fermented with Trichoderma koningii (Oudemans) as a Dietary Ingredient for Red Hybrid Tilapia (Oreochromis sp.). Aquaculture Research 33: 1199-1207.
Ng WK. Januari-Maret 2003. The Potential Use of Palm Kernel Meal in Aquaculture Feeds. Aquculture Asia Vol. VIII No.1. J. p 38-39.
[NRC] National Research Council. 1983. Nutrient Requirements of Domestic Animal: Nutrient Requirements of Warmwater Fishes and Shellfishes. Washington: National Academy Press. 102 pp.
Nursyam H. 1991. Ransum Ikan Lele (Clarias batrachus Linn) dari Limbah Ikan Tuna. [Tesis]. Bogor: Fakultas Pascasarjana, Institut Perikanan Bogor. 74 hal.
Omoregie E. (2001). Utilizatio n and Nutrient Digestibility of Mango Seeds and
Palm Kernel Meal by Juvenile Labeo senegalensis
(Antheriniformes:Cyprinidae). Aquaculture Research 32: 681-687.
Refstie S, Svihus B, Shearer, KD, Storebakken T. 1999. Nutrient Digestibility in Atlantic Salmon and Broiler Chickens Related to Viscosity and non-Starch Polysaccharide Content in Different Soybean Products. Animal Feed Science Technology : 79. 331-345.
Riady M.2006. Kebijakan Pemerintah di Bidang Pakan. Disampaikan pada Seminar Pakan Nasional; Fakultas Peternakan IPB, 9 September 2006.
Ritonga U. 18 Februari 2002. Produksi Pakan Ternak Naik 15 Persen pada Tahun 2002. Tempo Interaktif. http://www.tempointeractive.com/hg/ekbis/ 2002/ 02/18/brk,20020218-35,id.html [07 September 2006].
Robaina L et al. 1997. Corn Gluten and Meat and Bone Meals as Protein Sources in Diets for Gilthead Seabream (Sparus aurata) : Nutritional and Histological Implication. Aquaculture:157. 347-359.
Siagian N dan JM Danang. 2003. Derita Peternak Ayam Tak Pernah Berhenti. Sinar Harapan. http://www.sinarharapan.co.id/ekonomi/industri/2004/0505/ind1. html.[07 September 2006].
Steffens W. 1989. Principles of Fish Nutrition. Ellis Horwood Limited. England. 384 pp.
Suara Pembaharuan. 28 Agustus 2004. Kebutuhan Pakan Ternak pada 2010. Capai 13 Juta Ton. Suara Pembaharuan Daily. http://www. com/news/ 2004/08/26ekonom/eko04.htm. [07 September 2006].
Sue TT. 2001. Quality and Characteristics of Malaysian Palm Kernel Cakes/Expellers. Palm Oil Developments 34. Malaysia: p. 1-3.
Suhenda N. 1988. Pertumbuhan Ikan Lele (Clarias batrachus Linn) ya ng Mendapat Ransum dengan Kadar Protein dan Energi yang Berbeda [Tesis]. Bogor: Fakultas Pasca Sarjana, Institut Pertanian Bogor. 64 hal.
Suprayudi MA, Bintang M, Takeuchi T, Mokoginta I, Toha S. 1999. Defatted Soybean Meal as An Alternative Source to Substitute Fish Meal in The Feed of Giant Gouramy Osphronemus gouramy Lac. Suisanzoshoku 47(4): 551-557.
Takeuchi T. 1988. Laboratory Work –Chemical Evaluation of Dietary Nutrients. di dalam: Watanabe T .Fish Nutrition and Mariculture. Departement of Aquatic Biosciences Tokyo University of Fishes. Tokyo: 179-233.
Usher. 1990. Effects of Transfer to Seawater on Digestion and Gut Function in Atlantic Salmon Smolts Salmo salar L. Aquaculture: 90. 85–96.
Utomo NBP et al.. 1999. Pengkajian Pemanfaatan Bahan Lokal untuk Pengganti Komponen Impor pada Pakan Ikan. Bogor: Lembaga Penelitian Institut Pertanian Bogor. 31 hal.
Webster CD, Thompson KR, Morgan AM, Grisby EJ, Gannan AL. 2000. Use of Hempseed Meal, Poultry by-Product Meal and Canola Meal in Practical Diets without Fish Meal for Sunshines Bass (Morone chrysops X M. saxatilis). Aquaculture: 188(299-309).
Xue M dan Cui Y. 2000. Effect of Several Feeding Stimulant on Diet Preference by Juvenil Gibel Carp (Carassius auratus gibelio), Fed Diets with or Without Partial Replacement of Fish Meal by Meat and Bone Meal. Aquaculture: 198. 281–292.
Yamamoto T, Unuma T, Akiyama T. 1995. The Effect of Combined Use of Several Alternative Protein Sources in Fingerling Rainbow Trout Diets. Fisheries Science 61(6): 915-920.
Lampiran 1. Prosedur analisa proksimat
A. Prosedur analisa kadar air
1. Cawan porselen dioven pada suhu 110oC selama satu jam dan kemudian ditimbang (X1).
2. Bahan diambil sebanyak 1 g (A) dan dimasukkan pada cawan tadi dan kemudian dipanaskan /dioven pada suhu 110oC selama 2 jam.
3. Setelah dioven, cawan tersebut dipindahkan ke deksikator selama 30 menit.
4. Setelah dingin, cawan tersebut ditimbang dan beratnya dicatat (X2). 5. Kadar air dihitung dengan menggunakan rumus berikut ini :
%
B. Prosedur analisa kadar abu
1. Cawan porselen dioven pada suhu 110oC selama 1 jam lalu didinginkan dalam eksikator selama 15 sampai 30 menit dan kemudian ditimbang (X1). 2. Bahan diambil 1 g (A) dan dimasukkan dalam cawan porselen tersebut. 3. Cawan yang berisi bahan tadi dipanaskan dalam tanur pada suhu 600oC
sampai bahan menjadi putih semua atau menjadi abu, kemudian dimasukkan ke oven (suhu 100oC sampai 110oC) selama 15 menit untuk menurunkan suhunya.
4. Cawan dipindahkan ke eksikator selama 15 sampai 30 menit dan kemudia n ditimbang (X2).
5. Kadar abu dihitung dengan menggunaan rumus berikut ini :
%
C. Prosedur analisa protein (Metode Kjeldahl) Tahap Oksidasi
1. Bahan ditimbang 1 g (A) dengan menggunakan alumunium foil. Bahan yang telah ditimbang dimasukkan ke dalam labu Kjeldahl.
2. Tiga g katalis dimasukkan dalam labu Kjeldahl bersama dengan 10 ml H2SO4 pekat untuk mempercepat penguraian.
3. Labu Kjeldahl dipanaskan dalam rak oksidasi/digestion selama 3 hingga 4 jam sampai terjadi perubahan warna menjadi hijau bening.
4. Labu Kjeldahl selanjutnya didinginkan dan kemudian diencerkan dalam erlenmeyer hingga 100 ml.
Tahap destilasi
1. Larutan hasil oksidasi diambil sebanyak 5 ml dan dimasukkan ke dalam labu destilasi dan kemudian ditambah dengan beberapa tetes H2SO4.
2. Erlenmeyer diisi dengan 10 ml H2SO4 0,05N dan 2 tetes larutan indikator
yang disimpan di bawah pipa pembuangan kondensor dengan cara dimiringkan sehingga ujung pipa tenggelam dalam cairan.
Lanjutan lampiran 1…..
4. Campuran alkalin dalam labu destilasi disulin menjadi uap air selama 10 menit setelah tejadi pengembungan pada kondensor.
Tahap titrasi
1. Hasil destruksi dititrasi dengan larutan NaOH 0,05 N hingga berubah warna.
2. Hasil volume titran dicatat.
3. Prosedur yang sama juga dilakukan pada blanko.
4. Persentase protein dicari dengan menggunakan rumus sebagai berikut :
%
D. Prosedur analisa lemak
Metode estraksi dengan Soxhlet
1. Labu ekstraksi dipanaskan dalam oven pada suhu110oC selama 1 jam kemudian didinginkan dalam deksikator selama 30 menit dan ditimbang (X1).
2. Bahan ditimbang sebanyak 3 g (A) dan dimasukkan dalam selongsong, setelah itu dimasukkan ke soxhlet yang ditekan dengan pemberat pada bagian atasnya.
3. N-hexan sebanyak 100 sampai 150 ml dimasukkan ke dalam soxhlet sampai selongsong terendam dan sisa hexan dimasukkan ke dalam labu. 4. Labu yang sudah dihubungkan dengan soxhlet dipanaskan di atas water
bath sampai cairan dalam Soxhlet berwarna bening.
6. Labu dilepaskan dari soxhlet dan tetap dipanaskan hingga N-hexan menguap semua.
7. Labu dan lemak yang tersisa dipanaskan dalam oven selama 15 sampai 60 menit, kemudian didinginkan dalam eksikator selama 15 hingga 30 menit dan ditimbang (X2).
8. Persentase lemak dihitung dengan menggunakan rumus :
%
Metode Folch et al. (analisis lemak untuk hati)
1. Labu silinder dioven pada suhu 110oC selama 1 jam kemudian didinginkan dalam desikator selama 30 menit kemudian ditimbang (X1).
2. Bahan ditimbang 2 g (A) dan kemudian dimasukkan dalam gelas
homogenizer, kemudian ditambahkan dengan larutan kloroform/methanol C(20xA) dan disisakan sebagian untuk membilas pada saat penyaringan. 3. Sampel yang telah diberi larutan kemudian dihomogenizer selama 5 menit,