PENETAPAN KADAR SULFAMETOKSAZOL DAN TRIMETOPRIM DALAM SEDIAAN SUSPENSI DENGAN NAMA DAGANG DAN GENERIK DENGAN METODE KROMATOGRAFI CAIR KINERJA
TINGGI (KCKT)
SKRIPSI
Oleh:
DEVIANTI NIM 071524014
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENETAPAN KADAR SULFAMETOKSAZOL DAN TRIMETOPRIM DALAM SEDIAAN SUSPENSI DENGAN NAMA DAGANG DAN GENERIK DENGAN METODE KROMATOGRAFI CAIR KINERJA
TINGGI (KCKT)
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh:
DEVIANTI NIM 071524014FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang telah
memberikan rahmat dan hidayah-Nya, serta shalawat beriring salam kepada Nabi
Muhammad SAW sehingga penulis dapat menyelesaikan skripsi ini.
Penulis menyampaikan rasa hormat dan terima kasih yang
sebesar-besarnya kepada ayahanda Tusar dan ibunda Nursiah, serta Bunda Sumarni, SH.,
abangku Hari Syahrian, SE., adikku Ira Jayanti dan suamiku Robby Ismail P, SE.,
atas doa yang tulus dan dukungan moril maupun materil serta cinta dan kasih
yang telah diberikan kepada penulis dalam menghantarkan penulis untuk meraih
cita-cita.
Pada kesempatan ini, penulis juga menyampaikan terima kasih yang
sebesar-besarnya kepada:
1. Bapak Prof. Dr. rer.nat. Effendy De Lux Putra, SU., Apt, dan Bapak Drs.
Muchlisyam, M.Si., Apt., yang telah membimbing penulis dengan sabar
hingga selesainya penulisan skripsi ini.
2. Bapak Dekan Fakultas Farmasi Prof. Dr. Sumadio Hadisahputra., Apt.,
yang telah memberikan fasilitas kepada penulis sehingga dapat
menyelesaikan pendidikan.
3. Bapak Prof. Dr. M Timbul Simanjuntak, Msc., Apt., Dra. Salbiah, M.Si., Apt.,
Drs. Syafruddin, MS., Apt., sebagai tim penguji yang sangat banyak
memberikan masukan dan saran atas skripsi ini.
4. Ibu, Dra., Erly Sitompul, MS., Apt., selaku penasehat akademik yang
telah memberikan nasehat dan arahan kepada penulis serta seluruh staf
perkuliahan dan juga staf tata usaha yang telah memberikan bantuan
administrasinya.
5. Teman- teman penulis Ika, Winda, Febby, Icut, Ike, kak Nova, Alfan,
Lissa, Limiyanto dan seluruh mahasiswa Farmasi Ekstensi stambuk 2007
serta kakak-kakak maupun adik-adik mahasiswa Farmasi yang tidak dapat
penulis sebutkan satu persatu atas segala bantuan dan motivasinya.
Akhirnya penulis mengucapkan terima kasih yang sebesar-besarnya kepada
semua pihak yang telah turut membantu penulis dalam menyelesaikan skripsi ini
yang tidak bisa penulis sebutkan satu-persatu.
Medan, Maret 2010
Penulis
PENETAPAN KADAR SULFAMETOKSAZOL DAN TRIMETOPRIM DALAM SEDIAAN SUSPENSI DENGAN NAMA DAGANG DAN GENERIK DENGAN METODE KROMATOGRAFI CAIR KINERJA
TINGGI (KCKT)
Abstrak
Menurut Farmakope Indonesia edisi IV (1995) bahwa campuran Sulfametoksazol dan Trimetoprim ditentukan kadarnya menggunakan Kromatografi Cair Kinerja Tinggi dengan fase gerak campuran air : asetonitril : trietylamin (1400 : 400 : 2) v/v, menggunakan detektor 254 nm dengan kolom ODS (3,9 mm x 30 cm), laju alir 2 ml/menit dalam sediaan tablet, sedangkan dalam sediaan suspensi tidak tercantum.
Penelitian ini bertujuan menetapkan kadar sulfametoksazol dan trimetoprim dalam sediaan suspensi dengan nama dagang dan nama generik dengan menggunakan kromatografi cair kinerja tinggi (KCKT) kolom VP-ODS (4,6 mm x 25 cm) dan fase gerak, laju alir dan detektor yang sama seperti yang tertera pada Farmakope Indonesia edisi IV (1995).
Uji kualitatif masing-masing zat dilakukan dengan menginjeksikan larutan sulfametoksazol dan trimetoprim secara terpisah ke sistem KCKT, diperoleh waktu retensi sulfametoksazol 2,2 menit dan waktu retensi trimetoprim 6,5 menit.
Penentuan linieritas kurva kalibrasi menunjukkan hubungan yang linier antara luas puncak dengan konsentrasi untuk sulfametoksazol pada konsentrasi 50 sampai 250 µg/ml dengan koefisien korelasi, r = 0,9997 dari hasil perhitungan diperoleh persamaan regresi Y = 46709,25327X +46088,31281, untuk trimetoprim pada konsentrasi 10 sampai 50 µg/ml dengan koefisien korelasi, r = 0,9997 dari hasil perhitungan diperoleh persamaan regresi Y = 5800,13118X + 5576,943053.
Hasil uji validasi metode memenuhi persyaratan dengan persen perolehan kembali Sulfametoksazol 103,28% ; Trimetoprim 98,67%. Uji presisi parameter standar deviasi (SD) Sulfametoksazol sebesar 1,79% ; Trimetoprim 1,44% dan relative standar deviasi (RSD) Sulfametoksazol 1,74% ; Trimetoprim 1,46%. Hasil perhitungan Batas deteksi (LOD) dan batas kuantitasi (LOQ) diperoleh; Sulfametoksazol sebesar 13,46 mcg/ml dan 44,88 mcg/ml ; Trimetoprim sebesar 4,51 mcg/ml dan 15,03 mcg/ml.
Persyaratan suspensi oral menurut USP XXXI tahun 2008 baik untuk sulfametoksazol maupun trimetoprim mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket Sulfametoksazol dan Trimetoprim. Hasil penetapan kadar sampel Trimoxul, Sanprima dan Primadex, semua sampel memenuhi persyaratan, kecuali sampel cotrimoxazole yang tidak memenuhi persyaratan.
DETERMINATION OF SULFAMETOXAZOLE AND TRIMETOPRIM IN ORAL SUSPENSION WITH TRADE NAME AND GENERIC NAME BY
HIGH PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC) Abstract
According to Farmakope Indonesia (1995), combination of Sulfametoxazole and Trimetoprim can be determined by High Performance Liquid Chromatography with mobile phase, mixture of water : acetonitril : triethylamine (1400 : 400 : 2) v/v, using 254 nm detector and ODS coloum (3,9 mm x 30 cm), with flow rate 2 ml/minute in tablet, but in suspension did’nt included.
The purpose of this research to determine mixture of Sulfametoxazole and Trimetoprim in suspension with trade and generic name using of High Performance Liquid Chromatography , VP-ODS coloum (4,6 mm x 25 cm), with mobile phase, flow rate and detector same as included in Farmakope Indonesia (1995).
The qualitatif test of each drug was done to injection sulfametoksazol and trimetoprim solution to system HPLC, from the result was obtained retention time of sulfametoksazol 2,2 minute and retention time of trimetoprim 6,5 minute.
The determination of calibration curve linearity gave a linear correlation betwen the peak area versus concentration, for sulfametoksazo from 50 to 250 µg/ml with the correlation coefficient, r = 0,9997 and the calculated had got the regression Y = 46709,25327X +46088,31281, for trimetoprim 10 to 50 µg/ml with the correlation coefficient, r = 0,9997 and the calculated had got the regression Y = 5800,13118X + 5576,943053.
The validation test methode, concluded that this methode fulfilled clauses of validation test methode with percentage recovery 103,28% for Sulfametoxazole ; Trimetoprim 98,67%. Standart deviation (SD) Sulfametoxazole 1,79% ; Trimetoprim 1,44% dan relative standard deviation (RSD) Sulfametoxazole 1,74% ; Trimetoprim 1,46%. Limit of Detection (LOD) Sulfametokxazol 13,46 mcg/ml ; Trimetoprim 4,51 mcg/ml ; Limit of Quantitation (LOQ) Sulfametokxazol 44,88 mcg/ml ; Trimetoprim 15,03 mcg/ml
The requirement oral suspension of the therty one edition USP (2008) namely containing sulfametoxazole and trimetoprim not less than 90.0 % and not more than 110.0 % from the label declared.The result test of sample Trimoxul, Sanprima, Primadex, Cotrimoxazole, all samples fulfilled the requirement, except of cotrimoxazole sample that did not meet the requirement.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRAK ... v
ABSTRACT ... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... ... x
DAFTAR LAMPIRAN ... xi
BAB I PENDAHULUAN ... ...1
1.1. Latar Belakang...1
1.2. Perumusan Masalah ... .2
1.3. Hipotesis ... .3
1.4. Tujuan Penelitian...3
BAB II TINJAUAN PUSTAKA...4
2.1. Suspensi Kotrimoksazol...4
2.2.1. Sifat Fisikokimia...4
2.2.1.1. Sulfametoksazol...4
2.2.1.2. Trimetoprim...5
2.2.2. Mekanisme Kerja...5
2.2.3. Farmakokinetika...6
2.2.4. Efek Samping...6
2.2.5. Kegunaan...7
2.2.6. Bentuk Sediaan...7
2.2.7. Dosis...7
2.3. Kromatografi...7
2.3.1. Pembagian Kromatografi...8
2.3.2. Migrasi dan Retensi Solut...9
2.3.3. Pemisahan Pada Kolom...9
2.3.4. Profil Puncak dan Pelebaran Puncak...10
2.3.5. Jenis Kromatografi...10
2.4. Kromatografi Cair Kinerja Tinggi...13
2.4.1. Komponen Kromatografi Cair Kinerja Tinggi...13
2.4.2. Wadah fase Gerak...14
2.4.3. Pompa...14
2.4.4. Injektor...14
2.4.5. Kolom...15
2.4.7. Fase Gerak...16
2.5. Parameter Kromatografi Cair Kinerja Tinggi...17
2.6. Uji Validasi...18
BAB III METODOLOGI PENELITIAN...20
3.1. Waktu dan Tempat Penelitian...20
3.2. Alat-alat...20
3.3. Bahan-bahan...20
3.4. Prosedur Penelitian... 21
3.4.1. Pengambilan Sampel... 21
3.4.2. Pembuatan Fase Gerak ... 21
3.4.3. Pembuatan larutan induk baku BPFI...22
3.4.4. Penyiapan alat KCKT...22
3.4.5. Identifikasi...22
3.4.6. Penentuan kuantitatif...22
3.4.6.1 Pembuatan linieritas kurva kalibrasi...22
3.4.6.1.1 Kurva kalibrasi sulfametoksazol BPFI...22
3.4.6.1.2 Kurva kalibrasi trimetoprim BPFI...23
3.4.7. Perlakuan Sampel...23
3.4.7.1 Penetapan Kadar sampel...24
3.4.8. Penentuan Spektra Infra Red...24
3.4.8.1 Penentuan Spektra Infra Red Sulfametoksazol...24
3.4.8.2 Penentuan Spektra Infra Red Trimetoprim...24
3.4.9. Prosedur Validasi...24
3.4.10.Penentuan Penentuan Limit of Detection (LOD) dan Limit of Quantitation (LOQ)...25
3.4.11.Analisis Statistik...25
BAB IV HASIL DAN PEMBAHASAN...27
BAB V KESIMPULAN DAN SARAN 5.1. Kesimpulan...43
5.2. Saran ... 44
DAFTAR PUSTAKA...45
DAFTAR TABEL
Halaman
Tabel 3.1. Nilai Q kritis pada taraf kepercayaan 99%...26
Tabel 4.1. Data hasil penetapan kadar sulfametoksazol dan trimetoprim dalam
sediaan suspensi...40
Tabel 4.2. Data hasil pengujian perolehan kembali sulfametoksazol dan trimetoprim
dengan metode penambahan bahan baku (Standard Addition
DAFTAR GAMBAR
Halaman
Gambar 4.1. Spektrum hasil dari identifikasi baku sulfametoksazol...29
Gambar 4.2. Spektrum hasil dari identifikasi baku trimetoprim...30
Gambar 4.3. Hasil kromatogram dengan metode Kromatografi Cair Kinerja tinggi dengan fase gerak asetonitril : air (25 : 75) mengandung ammonium acetat laju alir 1 ml/menit dan UV detektor 254 nm...31
Gambar 4.4. Kromatogram hasil penyuntikan larutan baku Sulfametoksazol BPFI...34
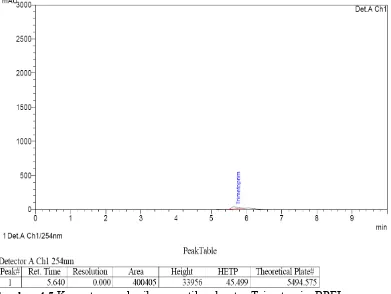
Gambar 4.5 Kromatogram hasil penyuntikan larutan baku Trimetoprim BPFI...34
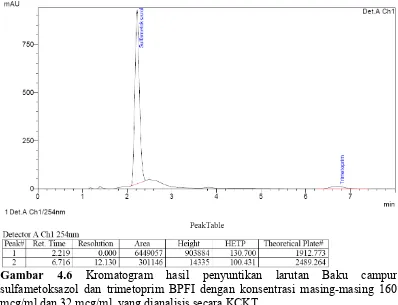
Gambar 4.6. Kromatogram hasil penyuntikan larutan baku campur Sulfametoksazol dan Trimetoprim BPFI dengan konsentrasi masing-masing 160 mcg/ml dan 32 mcg/ml, yang dianalisis secara KCKT...35
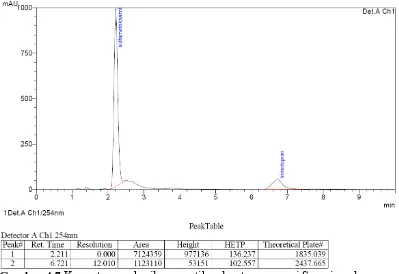
Gambar 4.7 Kromatogram hasil penyuntikan larutan suspensi Sanprima dengan penambahan spike baku trimetoprim ...36
Gambar 4.8. Kromatogram hasil penyuntikan larutan suspensi Trimoxul...36
Gambar 4.9. Kromatogram hasil penyuntikan larutan suspensi Sanprima...37
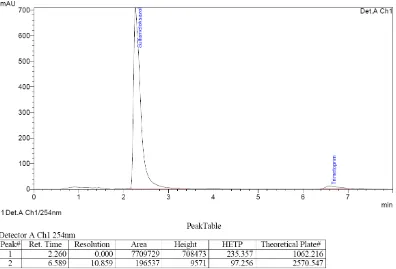
Gambar 4.10. Kromatogram hasil penyuntikan larutan suspensi Primadex ...37
Gambar 4.11. Kromatogram hasil penyuntikan larutan suspensi Cotrimoksazol ...38
Gambar 4.12. Kurva kalibrasi sulfametoksazol BPFI………...38
DAFTAR LAMPIRAN
Halaman Lampiran 1. Gambar alat KCKT dan Syringe ...46
Lampiran 2. Gambar alat ultrasonic cleaner dan penyaring ...47
Lampiran 3. Gambar alat sentrifuge...48
Lampiran 4. Spektrum Inframerah Sulfametoksazol pada literatur
Pharmaceutical Sub stance (UV/IR)...49
Lampiran 5. Spektrum inframerah Trimetoprim pada literatur
Pharmaceutical Sub stance (UV/IR)...50
Lampiran 6. Kromatogram dari larutan Sulfametoksazol dan Trimetoprim BPFI
...51
Lampiran 7. Perhitungan persamaan regresi dari kurva kalibrasi baku campur
sulfametoksazol dan trimetoprim BPFI...54
Lampiran 8. Contoh perhitungan persen perolehan kembali...58
Lampiran 9. Kromatogram hasil persen perolehan kembali dari sampel
Trimoxul (PT. Interbat)...61
Lampiran 10. Data hasil perolehan kembali Sulfametoksazol dan Trimetoprim
Pada Metode Penambahan Baku (Standard addition Methode)...64
Lampiran 11. Analisa data statistik persen perolehan kembali pada suspensi
Trimoxul (PT. Interbat)...65
Lampiran 12. Contoh perhitungan limit deteksi (LOD) dan limit kuantitasi (LOQ)
...68
Lampiran 13. Kromatogram dari laruran suspensi Trimoxul (PT. Interbat)...70
Lampiran 14. Analisa data statistik untuk mencari kadar sebenarnya dari
penyuntikan larutan suspensi Trimoxul (PT. Interbat) secara KCKT
...73
Lampiran 15. Kromatogram dari larutan suspensi Sanprima (PT. Sanbe Farma).75
Lampiran 16. Analisa data statistik untuk mencari kadar sebenarnya dari
penyuntikan larutan suspensi Sanprima (PT. Sanbe Farma)
secara KCKT... 78
Lampiran 17. Kromatogram dari larutan suspensi Primadex (PT Dexa
Lampiran 18. Analisa data statistik untuk mencari kadar sebenarnya dari
penyuntikan larutan suspensi Primadex (PT. Dexa Medica)
secara KCKT... 83
Lampiran 19. Kromatogram dari larutan suspensi Cotrimoksazole (PT. Phyto Kemo Agung Farma)... 85
Lampiran 20. Analisa data statistik untuk mencari kadar sebenarnya dari penyuntikan larutan suspensi Cotrimoksazole (PT. Phyto Kemo Agung Farma) secara KCKT... 88
Lampiran 21. Perhitungan pemipetan sampel... 90
Lampiran 22. Contoh perhitungan untuk mencari kadar sulfametoksazol dan trimetoprim... 91
Lampiran 23. Data hasil perhitungan kadar rata-rata Sulfametoksazol dan Trimetoprim suspensi Trimoxul (PT. Interbat)... 92
Lampiran 24. Daftar Spesifikasi sampel... 93
Lampiran 25. Sertifikat pengujian Sulfametoksazol BPFI... 94
Lampiran 26. Sertifikat pengujian Trimetoprim BPFI... 95
Lampiran 27. Sertifikat bahan baku Sulfametoksazol pabrik PT. Mutifa... 96
PENETAPAN KADAR SULFAMETOKSAZOL DAN TRIMETOPRIM DALAM SEDIAAN SUSPENSI DENGAN NAMA DAGANG DAN GENERIK DENGAN METODE KROMATOGRAFI CAIR KINERJA
TINGGI (KCKT)
Abstrak
Menurut Farmakope Indonesia edisi IV (1995) bahwa campuran Sulfametoksazol dan Trimetoprim ditentukan kadarnya menggunakan Kromatografi Cair Kinerja Tinggi dengan fase gerak campuran air : asetonitril : trietylamin (1400 : 400 : 2) v/v, menggunakan detektor 254 nm dengan kolom ODS (3,9 mm x 30 cm), laju alir 2 ml/menit dalam sediaan tablet, sedangkan dalam sediaan suspensi tidak tercantum.
Penelitian ini bertujuan menetapkan kadar sulfametoksazol dan trimetoprim dalam sediaan suspensi dengan nama dagang dan nama generik dengan menggunakan kromatografi cair kinerja tinggi (KCKT) kolom VP-ODS (4,6 mm x 25 cm) dan fase gerak, laju alir dan detektor yang sama seperti yang tertera pada Farmakope Indonesia edisi IV (1995).
Uji kualitatif masing-masing zat dilakukan dengan menginjeksikan larutan sulfametoksazol dan trimetoprim secara terpisah ke sistem KCKT, diperoleh waktu retensi sulfametoksazol 2,2 menit dan waktu retensi trimetoprim 6,5 menit.
Penentuan linieritas kurva kalibrasi menunjukkan hubungan yang linier antara luas puncak dengan konsentrasi untuk sulfametoksazol pada konsentrasi 50 sampai 250 µg/ml dengan koefisien korelasi, r = 0,9997 dari hasil perhitungan diperoleh persamaan regresi Y = 46709,25327X +46088,31281, untuk trimetoprim pada konsentrasi 10 sampai 50 µg/ml dengan koefisien korelasi, r = 0,9997 dari hasil perhitungan diperoleh persamaan regresi Y = 5800,13118X + 5576,943053.
Hasil uji validasi metode memenuhi persyaratan dengan persen perolehan kembali Sulfametoksazol 103,28% ; Trimetoprim 98,67%. Uji presisi parameter standar deviasi (SD) Sulfametoksazol sebesar 1,79% ; Trimetoprim 1,44% dan relative standar deviasi (RSD) Sulfametoksazol 1,74% ; Trimetoprim 1,46%. Hasil perhitungan Batas deteksi (LOD) dan batas kuantitasi (LOQ) diperoleh; Sulfametoksazol sebesar 13,46 mcg/ml dan 44,88 mcg/ml ; Trimetoprim sebesar 4,51 mcg/ml dan 15,03 mcg/ml.
Persyaratan suspensi oral menurut USP XXXI tahun 2008 baik untuk sulfametoksazol maupun trimetoprim mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket Sulfametoksazol dan Trimetoprim. Hasil penetapan kadar sampel Trimoxul, Sanprima dan Primadex, semua sampel memenuhi persyaratan, kecuali sampel cotrimoxazole yang tidak memenuhi persyaratan.
DETERMINATION OF SULFAMETOXAZOLE AND TRIMETOPRIM IN ORAL SUSPENSION WITH TRADE NAME AND GENERIC NAME BY
HIGH PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC) Abstract
According to Farmakope Indonesia (1995), combination of Sulfametoxazole and Trimetoprim can be determined by High Performance Liquid Chromatography with mobile phase, mixture of water : acetonitril : triethylamine (1400 : 400 : 2) v/v, using 254 nm detector and ODS coloum (3,9 mm x 30 cm), with flow rate 2 ml/minute in tablet, but in suspension did’nt included.
The purpose of this research to determine mixture of Sulfametoxazole and Trimetoprim in suspension with trade and generic name using of High Performance Liquid Chromatography , VP-ODS coloum (4,6 mm x 25 cm), with mobile phase, flow rate and detector same as included in Farmakope Indonesia (1995).
The qualitatif test of each drug was done to injection sulfametoksazol and trimetoprim solution to system HPLC, from the result was obtained retention time of sulfametoksazol 2,2 minute and retention time of trimetoprim 6,5 minute.
The determination of calibration curve linearity gave a linear correlation betwen the peak area versus concentration, for sulfametoksazo from 50 to 250 µg/ml with the correlation coefficient, r = 0,9997 and the calculated had got the regression Y = 46709,25327X +46088,31281, for trimetoprim 10 to 50 µg/ml with the correlation coefficient, r = 0,9997 and the calculated had got the regression Y = 5800,13118X + 5576,943053.
The validation test methode, concluded that this methode fulfilled clauses of validation test methode with percentage recovery 103,28% for Sulfametoxazole ; Trimetoprim 98,67%. Standart deviation (SD) Sulfametoxazole 1,79% ; Trimetoprim 1,44% dan relative standard deviation (RSD) Sulfametoxazole 1,74% ; Trimetoprim 1,46%. Limit of Detection (LOD) Sulfametokxazol 13,46 mcg/ml ; Trimetoprim 4,51 mcg/ml ; Limit of Quantitation (LOQ) Sulfametokxazol 44,88 mcg/ml ; Trimetoprim 15,03 mcg/ml
The requirement oral suspension of the therty one edition USP (2008) namely containing sulfametoxazole and trimetoprim not less than 90.0 % and not more than 110.0 % from the label declared.The result test of sample Trimoxul, Sanprima, Primadex, Cotrimoxazole, all samples fulfilled the requirement, except of cotrimoxazole sample that did not meet the requirement.
BAB I PENDAHULUAN 1.1Latar Belakang
Kotrimoksazol merupakan kombinasi dari Sulfametoksazol dan
Trimetoprim dengan perbandingan 5:1, bersifat bakterisid dengan spektrum kerja
lebih lebar dibandingkan dengan sulfonamida. Trimetoprim dan sulfametoksazol
menghambat reaksi enzimatik obligat pada dua tahap yang berurutan pada bakteri
sehingga kombinasi kedua obat memberikan efek sinergistik. Spektrum
antibakteri Trimetoprim sama dengan sulfametoksazol, meskipun daya
antibakterinya 20-100 kali lebih kuat dari Sulfametoksazol (Mariana, 1995).
Menurut Farmakope Indonesia edisi IV (1995), campuran Sulfametoksazol
dan Trimetoprim ditentukan kadarnya menggunakan Kromatografi Cair Kinerja
Tinggi dengan fase gerak campuran air : asetonitril : triethylamina (1400 : 400 : 2)
v/v, menggunakan detektor 254 nm dengan kolom ODS (3,9 mm x 30 cm), laju
alir 2 ml/menit, untuk sediaan tablet.
Menurut beberapa literatur penetapan kadar suspensi Sulfametoksazol dan
Trimetoprim dapat dilakukan dengan KCKT menggunakan fase gerak, laju alir
yang berbeda antara lain dalam USP XXXI (2008) suspensi Sulfametoksazol dan
Trimetoprim ditentukan kadarnya secara Kromatografi Cair Kinerja Tinggi
menggunakan fase gerak, laju alir, kolom dan detektor yang sama seperti yang
tertera pada Farmakope Indonesia edisi IV (1995). Menurut Bergh,J.J dan
Breytenbach (1987) dilakukan dengan fase gerak acetonitril : air (25 : 75) v/v
mengandung ammonium acetat 1% pH 6.90 ± 0.1 dengan laju alir 1 ml/menit dan
dengan fase gerak metanol : asam asetat : triethylamin : air (20 :1.5 : 0.5 : 78) v/v
dengan laju alir 1.5, UV detektor pada 254 nm, kolom 300 x 3.9 10 µm
µBondapak C 18.
Metode kromatografi cair kinerja tinggi memiliki banyak keuntungan
antara lain cepat, daya pisahnya baik, ideal untuk molekul besar dan ion, mudah
untuk memperoleh kembali cuplikan, kolom dapat dipakai berulang kali dan
perangkatnya dapat digunakan secara otomatis dan kuantitatif (Johnson and
Stevenson, 1991; Rohman, 2007).
Persyaratan kadar untuk sediaan suspensi kotrimoksazol Menurut USP
XXXI (2008) yaitu mengandung Sulfametoksazol, C10H11N3O3S dan
Trimetoprim, C14H18N4O3, tidak kurang dari 90,0% dan tidak lebih dari 110,0%
dari jumlah yang tertera pada etiket.
Dalam penelitian ini, peneliti mencoba menggunakan kondisi kromatografi
yang sedikit berbeda dari prosedur yang terdapat pada USP XXXI (2008) yaitu
kolom VP-ODS (4.6 mm x 25 cm) sehingga perlu dilakukan uji validasi terhadap
sediaan suspensi dengan penambahan bahan baku yang umumnya digunakan
dalam pembuatan suspensi kotimoksazol. Adapun parameter uji validasi yang
dilakukan yaitu akurasi (kecermatan) dengan parameter kesalahan relatif, presisi
(keseksamaan) dengan parameter koefisien variasi, sensitivitas dengan parameter
limit deteksi dan limit kuantitasi
1.2 Perumusan masalah
- Apakah kadar sulfametoksazol dan trimetoprim dalam sediaan suspensi dapat ditentukan dengan menggunakan metode Kromatografi Cair Kinerja Tinggi
- Apakah kadar sulfametoksazol dan trimetoprim dalam sediaan suspensi dengan
nama dagang dan nama generik yang ditetapkan secara KCKT memenuhi
persyaratan yang yang ditetapkan Oleh USP edisi XXXI (2008)
- Apakah metode KCKT yang digunakan memenuhi persyaratan uji validasi?
1.3 Hipotesis
- Diduga kadar Sulfametoksazol dan Trimetoprim dalam sediaan suspensi dapat ditentukan dengan menggunakan metode Kromatografi Cair Kinerja Tinggi
(KCKT).
- Diduga kadar Sulfametoksazol dan Trimetoprim dalam sediaan suspensi dengan
nama dagang dan nama generik yang ditetapkan secara KCKT memenuhi
persyaratan yang ditetapkan oleh Oleh USP edisi XXXI (2008)
- Diduga metode KCKT yang digunakan memenuhi persyaratan uji validasi yang
ditetapkan.
1.4 Tujuan penelitian
- Menentukan kadar Sulfametoksazol dan Trimetoprim dalam sediaan suspensi
secara Kromatografi Cair Kinerja Tinggi.
- Mengetahui kadar Sulfametoksazol dan Trimetoprim dalam sediaan suspensi
yang beredar di pasaran memenuhi persyaratan yang ditetapkan oleh USP
edisi XXXI (2008)
BAB II
TINJAUAN PUSTAKA 2.1 Suspensi Kotrimoksazol
Suspensi adalah sediaan cair yang mengandung partikel padat tidak larut
yang terdispersi dalam fase cair.
Suspensi Kotrimoksazol mengandung Sulfametoksazol C10H11N3O3S dan
Trimetoprim, C14H18N4O3, tidak kurang dari 90,0% dan tidak lebih dari 110,0%
dari jumlah yang tertera pada etiket (USP, 2008).
2.2.1 Sifat Fisikokimia 2.2.1.1 Sulfametoksazol
Rumus struktur : H2N SO2NH
N
O CH3 Nama kimia : N1 – (5-metil-3-isoksazolil)sulfanilamida
Rumus molekul : C10H11N3O3S
Berat molekul : 253,28
Pemerian : Serbuk hablur, putih sampai hampir putih, praktis
tidak berbau
Kelarutan : Praktis tidak larut dalam air, dalam eter dan dalam
kloroform, mudah larut dalam aseton dan dalam
larutan natrium hidroksida encer, agak sukar larut
2.2.1.2 Trimetoprim
Rumus struktur :
NH2 OCH3 N
H2N CH2 OCH3 N
OCH3
Nama kimia : 2,4-Diamino-5-(3,4,5-trimetoksibenzil)pirimidina
Rumus molekul : C14H18N4O3
Berat molekul : 290,36
Pemerian : Hablur atau serbuk hablur,putih sampai krem,
tidak berbau
Kelarutan : Sangat sukar larut dalam air, larut dalam
benzilalkohol, agak sukar larut dalam kloroform dan
dalam methanol, sangat sukar larut dalam etanol dan
dalam aseton, praktis tidak larut dalam eter dan
dalam karbon tetraklorida.
2.2.2 Mekanisme kerja
Aktivitas antibakteri kombinasi antara sulfametoksazol dan trimetoprim (
kotrimoksazol) berdasarkan kerjanya pada dua tahap yang berurutan pada reaksi
enzimatik untuk pembentukan asam tetrahidrofolat. Sulfonamida manghambat
masuknya para-aminobenzoic acid (PABA) ke dalam molekul asam folat dan
trimetoprim menghambat terjadinya reaksi reduksi dari dihidrofolat menjadi
tetrahidrofolat. Tetrahidrofolat penting untuk reaksi-reaksi pemindahan satu atom
C, seperti pembentukan basa purin (adenine, guanine dan timidin) dan beberapa
asam amino (metinin, glisin). Sel-sel mamalia menggunakan folat jadi yang
menghambat enzim dihidrofolat reduktase mikroba secara sangat selektif. Hal ini
penting, karena enzim tersebut juga terdapat pada sel mamalia.
Efek sinergis dapat dicapai dengan perbandingan kadar yang optimal dari
kedua obat. Untuk kebanyakan kuman, rasio kadar Sulfametoksazol : Trimetoprim
yang optimal ialah 20:1, sifat farmakokinetik sulfonamid untuk kombinasi dengan
Trimetoprim sangat penting untuk kadar yang relatif tetap dari kedua obat tersebut
dalam tubuh. Trimetoprim pada umumnya 20 – 100 kali lebih poten daripada
sulfametoksazol, sehingga sediaan kombinasi diformulasikan untuk mendapatkan
kadar Sulfametoksazol 20 kali lebih besar daripada Trimetoprim.
2.2.3 Farmakokinetika
Trimetoprim biasanya diberikan secara oral, baik tunggal maupun
dikombinasikan dengan sulfametoksazol, kombinasi ini merupakan bentuk
terakhir yang dipilih karena trimetoprim dan sulfametoksazol memiliki waktu
paruh yang hampir sama. Trimetoprim diabsorbsi dengan baik dari usus dan
didistribusikan secara luas dalam cairan- cairan dan jaringan-jaringan tubuh,
termasuk cairan serebrospinal. Karena trimetoprim lebih larut dalam lemak
dibandingkan sulfametoksazol, maka volume distribusi trimetoprim lebih banyak
dibandingkan sulfametoksazol. Jika 1 bagian trimetoprim diberikan dengan 5
bagian sulfametoksazol, maka konsentrasi plasma puncaknya adalah pada rasio 1 :
20 yang merupakan konsentrasi optimal. Sulfametoksazol lebih banyak terikat
pada protein plasma dibandingkan trimetoprim (Katzung, 2004).
2.2.4 Efek samping
Biasanya berupa gangguan kulit dan gangguan lambung-usus, stomatitis.
dan efek-efek darah (neutropenia, trombositopenia). Oleh karena itu, penggunaan
lebih dari dua minggu hendaknya disertai dengan pengawasan darah. Resiko
kristaluria dapat dihindari dengan meminum lebih dari 1,5 liter air sehari. (Tjay
dan Rahardja, 2002).
2.2.5 Kegunaan
Kombinasi Sulfametoksazol dan Trimetoprim merupakan pengobatan
yang efektif untuk infeksi-infeksi saluran kemih dengan komplikasi, prostatitis
dan infeksi saluran cerna (Katzung, 2004).
2.2.6 Bentuk sediaan
Kotrimoksazol tersedia dalam bentuk tablet oral yang mengandung 400
mg Sulfametoksazol dan 80 mg Trimetoprim atau 800 mg Sulfametoksazol dan
160 mg Trimetoprim. Untuk anak- anak tersedia dalam bentuk suspensi oral yang
mengandung 200 mg Sulfametoksazol dan 40 mg Trimetoprim / 5 ml, serta tablet
pediatrik yang mengandung 100 mg Sulfametoksazol dan 20 mg Trimetoprim.
Untuk pemberian intravena tersedia sediaan infus yang mengandung 400 mg
Sulfametoksazol dan 80 mg Trimetoprim / 5 ml.
2.2.7 Dosis
Dosis dewasa 800 mg Sulfametoksazol dan 160 mg Trimetoprim setiap 12
jam. Pada infeksi yang berat diberikan dosis lebih besar. Dosis yang dianjurkan
untuk anak-anak ialah Sulfametoksazol 40 mg/kg/BB/hari dan 8 mg/kg/BB/hari
Trimetoprim (Mariana, 1995).
2.3 Kromatografi
Kromatografi pertama kali dikembangkan oleh seorang ahli botani Rusia
tanaman dengan cara perkolasi ekstrak petroleum eter dalam kolom gelas yang
berisi kalsium karbonat (CaCO3). Saat ini kromatografi merupakan teknik
pemisahan yang paling umum dan paling sering digunakan dalam bidang kimia
untuk melakukan analisis, baik analisis kualitatif, kuantitatif atau preparatif
dalam bidang farmasi (Gandjar dan Rohman, 2007).
Kromatografi merupakan suatu teknik pemisahan zat yang menggunakan fase diam (stationary phase) dan fase gerak (mobile phase).
Teknik kromatografi telah berkembang dan telah digunakan untuk
memisahkan berbagai macam komponen yang kompleks,baik komponen organik maupun komponen anorganik (Gandjar dan Rohman, 2007).
2.3.1 Pembagian Kromatografi
Kromatografi dapat dibedakan atas berbagai macam, tergantung pada
pengelompokannya. Berdasarkan pada mekanisme pemisahannya, kromatografi
dibedakan menjadi : (a) kromatografi adsorbsi; (b) kromatografi partisi; (c)
kromatografi pasangan ion; (d) kromatografi penukar ion (e) kromatografi
eksklusi ukuran dan (f) kromatografi afinitas (Gandjar dan Rohman, 2007).
Berdasarkan alat yang digunakan, kromatografi dapat dibagi atas : (a) kromatografi kertas ; (b) kromatografi lapis tipis, yang keduanya sering disebut kromatografi planar, (c) kromatografi cair kinerja tinggi (KCKT) dan (d) kromatografi gas (KG). Bentuk kromatografi yang paling awal adalah
kromatografi kolom yang digunakan untuk pemisahan sampel dalam jumlah yang besar (Gandjar dan Rohman, 2007).
2.3.2 Migrasi dan Retensi Solut
Kecepatan migrasi solut melalui fase diam ditentukan oleh perbandingan
distribusinya (D) dan besarnya D ditentukan oleh afinitas relatif solut pada kedua
didefinisikan sebagai perbandingan konsentrasi solut dalam fase diam (Cs) dan
dalam fase gerak (Cm).
D =
Cm Cs
Jadi semakin besar nilai D maka migrasi solut semakin lambat; dan semakin kecil nilai D migrasi solut semakin cepat. Solut akan terelusi menurut perbandingan distribusinya. Jika perbedaan perbandingan distribusi solut cukup besar maka campuran-campuran solut akan mudah dan cepat dipisahkan (Gandjar dan Rohman, 2007).
2.3.3 Pemisahan pada kolom
Kolom merupakan bagian terpenting dari keseluruhan peralatan kromatografi karena proses pemisahan campuran komponen. Pada pemisahan campuran-campuran dalam kolom, solut-solut dicirikan dengan waktu retensi (tR) dan faktor retensi (k’) yang berbanding lurus dengan nilai D.
tR = tM (1+ k’)
Kondisi kromatografi umumnya diatur sedemikian rupa sehingga nilai k’ lebih kecil daripada 20 untuk menghindari waktu retensi yang terlalu panjang. Nlai k’ dapat dihitung dengan persamaan :
k’ = tR- tM
tM
2.3.4 Profil Puncak dan Pelebaran Puncak
Selama pemisahan kromatografi, solut individual akan membentuk profil
konsentrasi yang simetris atau dikenal juga dengan profil Gaussian dalam arah
aliran fase gerak. Profil, dikenal juga dengan puncak atau pita, secara
perlahan-lahan akan melebar dan sering juga membentuk profil yang asimetrik karena
Gambar 2. Profil-profil puncak
Adanya puncak, yang asimetris dapat disebabkan oleh hal –hal berikut:
Ukuran sampel yang dianalisis terlalu besar. Jika sampel terlalu besar maka
fase gerak tidak mampu membawa solut dengan sempurna karenanya terjadi
pengekoran atau tailing.
Interaksi yang kuat antara solut dengan fase diam dapat menyebabkan solut
sukar terelusi sehingga dapat menyebabkan terbentuknya puncak yang
mengekor.
Adanya kontaminan dalam sampel yang dapat muncul terlebih dahulu
sehingga menimbulkan puncak mendahului (fronting) (Gandjar dan Rohman,
2007).
2.3.5 Jenis kromatografi
Menurut Johnson dan Stevenson (1991) jenis-jenis kromatografi yaitu:
1. Kromatografi Cair-Padat (LSC)
Tehnik ini biasanya menggunakan fase diam silika gel atau alumina, meskipun
demikian sekitar 90% kromatografi ini memakai silika gel sebagai fase diamnya.
Fase geraknya berupa pelarut non polar yang ditambah dengan pelarut polar
seperti air atau alkohol rantai pendek untuk meningkatkan kemampuan elusinya
sehingga tidak timbul pengekoran puncak, seperti n-heksana ditambah metanol.
Jenis KCKT ini sesuai untuk pemisahan-pemisahan campuran isomer struktur dan
untuk pemisahan solut dengan gugus fungsional yang berbeda.
2. Kromatografi Partisi (LLC)
Kromatografi jenis ini disebut juga dengan kromatografi fase terikat.
fase terikat. Sejauh ini yang digunakan untuk memodifikasi silika adalah
hidrokarbon-hidrokarbon non polar seperti oktadesilsilana, oktilsilana, atau
dengan fenil.
Fase diam yang paling populer digunakan adalah oktadesilsilana (ODS atau
C18) dan kebanyakan pemisahannya adalah dengan fase terbalik. Sedangkan fase
geraknya adalah campuran asetonitril atau metanol dengan air atau dengan larutan
buffer.
Kromatografi partisi (LLC), disebut “fase normal” bila fase diam lebih polar
dari fase gerak dan “fase terbalik” bila fase gerak lebih polar dari fase diam.
a. Kromatografi fase normal
Kromatografi fase normal (fase diam lebih polar daripada fase gerak),
kemampuan elusi meningkat dengan meningkatnya polaritas pelarut. Fase
gerak ini biasanya tidak polar. Dietil eter, benzen, hidrokarbon lurus seperti
pentana, heksana, heptana maupun iso-oktana sering digunakan. Halida
alifatis seperti diklorometana, dikloroetana, butilklorida dan kloroform juga
digunakan. Umumnya gas terlarut tidak menimbulkan masalah pada fase
normal. (Gandjar dan Rohman, 2007)
b. Kromatografi fase terbalik
Kromatografi fase terbalik (fase diam kurang polar daripada fase gerak),
kemampuan elusi menurun dengan meningkatnya polaritas pelarut.
Kandungan utama fase gerak fase terbalik adalah air. Pelarut yang dapat
campur dengan air seperti metanol, etanol, asetonitril, dioksan, tetrahidrofuran
Dapat ditambahkan pula asam, basa, dapar dan/atau surfaktan. Mutu air harus
tinggi baik air destilasi maupun air mineral.
3. Kromatografi penukar ion
Tehnik ini tergantung pada penukaran (adsorpsi) ion-ion diantara fase gerak
dan tempat-tempat berion dari kemasan. Kebanyakan resin-resin berasal dari
polimer stiren divinilbenzen dimana gugus-gugus fungsinya telah ditambah.
Resin-resin tipe asam sulfonat dan amin kuarterner merupakan jenis resin
pilihan paling baik dan banyak digunakan. Keduanya, fase terikat dan resin
telah digunakan. Tehnik ini dipakai secara luas dalam life sciences dan dikenal
secara khas untuk pemisahan asam-asam amino. Tehnik ini dapat dipakai
untuk keduanya, kation-kation dan anion-anion.
4. Kromatografi eksklusi (EC)
Tehnik ini unik karena dalam pemisahan didasarkan pada ukuran molekul dari
solut. Kemasan adalah suatu gel dengan suatu permukaan berlubang-lubang
sangat kecil yang inert. Molekul-molekul kecil dapat masuk ke dalam jaringan
dan ditahan dalam fase gerak yang menggenang. Molekul-molekul yang lebih
besar tidak dapat masuk ke dalam jaringan dan lewat melalui kolom tanpa
ditahan.
5. Kromatografi Pasangan Ion (IPC)
Kromatografi ini merupakan bentuk khusus dari kromatografi cair-cair yang
digunakan untuk pemisahan senyawa atau cuplikan yang mengandung
komponen ion dan non ion, seperti garam ammonium kuarterner, sulfonat,
sistem pelarut campuran air dengan metanol atau asetonitril dan kolom seperti
oktadesilsilana yang terikat pada silika.
2.4 Kromatografi Cair Kinerja Tinggi
Kromatogarfi cair kinerja tinggi (KCKT) merupakan sistem pemisahan
dengan kecepatan dan efisiensi yang tinggi karena didukung oleh kemajuan dalam
teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sangat sensitif
dan beragam sehingga mampu menganalisa berbagai cuplikan secara kualitatif
maupun kuantitatif, baik dalam komponen tunggal maupun campuran (Depkes RI,
1995).
2.4.1 Komponen Kromatografi cair kinerja tinggi
Gambar 2.1. Bagan alat KCKT
2.4.2 Wadah Fase gerak
Wadah fase gerak terbuat dari bahan yang inert terhadap fase gerak. Bahan
yang umum digunakan adalah gelas dan baja anti karat. Daya tampung tandon
harus lebih besar dari 500 ml, yang dapat digunakan selama 4 jam untuk
kecepatan alir yang umumnya 1-2 ml/menit.
2.4.3 Pompa
Untuk menggerakkan fase gerak melalui kolom diperlukan pompa. Pompa
harus mampu menghasilkan tekanan 6000 Psi pada kecepatan alir 0,1–10
pompa
injektor
kolom
oven
detektor
ml/menit. Pompa ada 2 jenis yaitu pompa volume konstan dan pompa tekanan
konstan. Pompa terbuat dari bahan yang inert terhadap semua pelarut. Bahan yang
umum digunakan adalah gelas baja antikarat dan teflon. Aliran pelarut dari pompa
harus tanpa denyut untuk menghindari hasil yang menyimpang pada detektor.
2.4.4 Injektor
Cuplikan harus dimasukkan ke dalam pangkal kolom (kepala kolom),
diusahakan agar sesedikit mungkin terjadi gangguan pada kemasan kolom.
Ada tiga jenis dasar injektor, yaitu:
a. Hentikan aliran/stop flow: Aliran dihentikan, injeksi dilakukan pada
kinerja atmosfir, sistem tertutup, dan aliran dilanjutkan lagi. Tehnik ini
bisa digunakan karena difusi di dalam aliran kecil dan resolusi tidak
dipengaruhi.
b. Septum: Injektor-injektor langsung ke aliran fase gerak umumnya sama
dengan yang digunakan pada kromatografi gas. Injektor ini dapat
digunakan pada kinerja sampai 60-70 atmosfir. Tetapi septum ini tidak
tahan dengan semua pelarut-pelarut kromatografi cair. Disamping itu,
partikel kecil dari septum yang terkoyak (akibat jarum injektor) dapat
menyebabkan penyumbatan.
c. Katup putaran (loop valve): ditunjukkan secara skematik dalam Gambar 6,
tipe injektor ini umumnya digunakan untuk menginjeksi volume lebih
besar dari pada 10 µl dan sekarang digunakan dengan cara automatis
(dengan adaptor khusus, volume-volume lebih kecil dapat diinjeksikan
diisi pada tekanan atmosfir. Bila katup difungsikan, maka cuplikan di
dalam putaran akan bergerak ke dalam kolom.
Gambar 2.2 Tipe injektor katup putaran
2.4.5 Kolom
Kolom adalah jantung kromatografi. Berhasil atau gagalnya suatu analisis
tergantung pada pemilihan kolom dan kondisi percobaan yang sesuai. Kolom
dapat dibagi menjadi dua kelompok:
Kolom analitik: diameter khas adalah 2-6 mm. Panjang kolom tergantung
pada jenis kemasan. Untuk kemasan pelikular, panjang yang lumrah
adalah 50-100 cm. Untuk kemasan poros mikropartikilat, umumnya 10-30
cm. Dewasa ini ada yang 5 cm
Kolom preparatif: umumnya memiliki diameter 6 mm atau lebih besar dan
panjang kolom 25 -100 cm.
Kolom umumnya dibuat dari stainless steel dan biasanya dioperasikan
pada temperatur kamar, tetapi bisa juga digunakan temperatur lebih tinggi,
terutama untuk kromatografi penukar ion dan kromatografi eksklusi. Kemasan
kolom tergantung pada mode kromatografi cair kinerja tinggi yang digunakan.
2.4.6 Detektor
Detektor universal: Mampu mendeteksi zat secara umum, tidak bersifat
spesifik, dan tidak bersifat selektif, seperti detektor indeks bias dan
detektor spektrometri massa.
Detektor spesifik: Hanya mendeteksi analit secara spesifik dan selektif,
seperti detektor UV-Vis, detektor fluoresensi dan elektrokimia
(Rohman,2007).
2.4.7 Fase Gerak
Fase gerak atau eluen biasanya terdiri atas campuran pelarut yang dapat
bercampur yang secara keseluruhan berperan dalam daya elusi dan resolusi. Daya
elusi dan resolusi ini ditentukan oleh polaritas keseluruhan pelarut, polaritas fase
diam, dan sifat komponen-komponen sampel (Johnson dan Stevenson, 1991 dan
Rohman, 2007).
Terdapat keragaman yang luas dari solvent yang digunakan dalam semua
mode Kromatografi Cair Kinerja Tinggi, tetapi ada beberapa sifat yang diinginkan
yang mana umumnya harus dipenuhi oleh semua solven.
Menurut De Lux Putra (2007), fase gerak dalam Kromatografi Cair
Kinerja Tinggi (KCKT) harus memenuhi persyaratan sebagai berikut :
Murni; tidak ada pencemar/kontaminan
Tidak bereaksi dengan pengemas Sesuai dengan detektor
Melarutkan cuplikan
Mempunyai viskositas rendah
Mudah rekoveri cuplikan, bila diinginkan
2.5 Parameter Kromatografi Cair Kinerja Tinggi
Ada beberapa parameter yang perlu diperhatikan dalam memperoleh
kondisi yang diinginkan dalam kromatografi antara lain :
a. Waktu Retensi
Waktu yang dibutuhkan suatu komponen untuk melewati suatu kolom
disebut waktu retensi yang dapat didefinisikan sebagai waktu yang diperlukan
untuk membawa keluar suatu komponen dari dalam kolom, dihitung mulai
diinjeksikan hingga keluar kolom tepat pada saat konsentrasi maksimum.
2. Faktor Selektifitas
Suatu kolom dinyatakan baik apabila kolom tersebut cukup selektif, dan
dikatakan selektif apabila kolom tadi mampu menahan berbagai komponen
dengan kekuatan yang berbeda-beda.
3. Efisiensi Kolom
Jumlah plat teoritik dalam suatu kolom sebanding dengan panjang kolom.
Karena itu jumlah plat teoritik suatu kolom dapat ditingkatkan dengan
memperpanjang kolom. Makin panjang kolom makin banyak jumlah plat
teoritiknya maka makin sempurna pemisahan.
4. Resolusi
Derajat pemisahan atau resolusi dari dua pita yang berdekatan
didefinisikan sebagai jarak antara puncak-puncak pita (atau pusat-pusat) dibagi
dengan luas pita rata-rata. Semakin tinggi harga N selalu memberikan resolusi
yang membaik. Oleh karena itu resolusi dapat diperbaiki dengan menambah
5. Faktor Ikutan
Keasimetrisan puncak dinyatakan dengan faktor ikutan atau faktor
asimetris. Pembentukan puncak yang curam bagian depan tetapi landai bagian
belakang disebut tailing, sebaliknya puncak yang landai bagian depan dan curam
bagian belakang disebut fronting.
2.6 Uji Validasi
Validasi metode menurut United States Pharmacopeia (USP) dilakukan
untuk menjamin bahwa metode analisis akurat, spesifik, reprodusibel dan tahan
pada kisaran analit yang akan dianalisis. Suatu metode analisis harus divalidasi untuk melakukan verifikasi bahwa parameter-parameter kinerjanya cukup mampu
untuk mengatasi problem analisis.
Parameter-parameter uji validasi antara lain :
a. Ketepatan (Akurasi)
Merupakan ketelitian metode analisis atau kedekatan antara nilai terukur
dengan nilai yang diterima baik nilai konvensi, nilai sebenarnya, atau nilai
rujukan. Akurasi diukur sebagai banyaknya analit yang diperoleh kembali
pada suatu pengukuran dengan melakukan spiking pada suatu sampel.
Untuk pengujian senyawa obat, akurasi diperoleh dengan membandingkan
hasil pengukuran dengan bahan rujukan standar.
b. Presisi (keseksamaan)
Merupakan ukuran keterulangan metode analisis dan biasanya dinyatakan
sebagai simpangan baku relatif dari sejumlah sampel yang berbeda
signifikan secara statistik.
Merupakan konsentrasi analit terkecil dalam sampel yang masih dapat
dideteksi, meskipun tidak selalu dapat dikuantifikasi.
d. Batas kuantitasi (Limit of Quantitation, LOQ)
Merupakan konsentrasi analit terendah dalam sampel yang dapat
ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi
BAB III
METODOLOGI PENELITIAN 3.1 Waktu dan tempat penelitian
Penelitian dilakukan di laboratorium Kimia Farmasi Kuantitatif dan
laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan
September sampai November 2009.
3.2 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah satu unit alat
kromatografi cair kinerja tinggi (Shimadzu) yang terdiri dari pompa (LC 20 AD),
detektor UV/Vis (SPD 20 A), kolom Sim-Pack VP ODS (4,6 x 250 mm), degasser
(DGU 20 A5), injector (Rheodyne 7225 i), pompa vakum (Gast DO A-PG04-BN),
Sonifikator (Branson 1510), syringe 100 μl (SGE), alat penyaring fase gerak dan
sampel dilengkapi membran Whatman PTFE 0,45 μm, membran selulosa nitrat
0,45 μm, dan membran Whatman PTFE 0,2 μm, alat spektofotometer infra red
(Shimadzu), DRS 8000, neraca analitik (Mettler Tolledo), sentrifuge, pH meter
(Hanna), dan alat gelas lainnya.
3.3 Bahan-bahan
Bahan-bahan yang digunakan jika tidak dinyatakan lain adalah kualitas p.a
produksi E.Merck yaitu asetonitril, metanol, trietilamina, asam asetat glasial,
natrium hidroksida, aquabidestilata (PT. Ikapharmindo Putramas),
Sulfametoksazol BPFI (PPOM Jakarta), Trimetoprim BPFI (PPOM Jakarta),
Sulfametoksazol baku (PT. Mutifa), Trimetoprim baku (PT. Mutifa), KBr,
Primadex (PT. Dexa Medica), suspensi Cotrimoksazole (PT. Phyto Kemo Agung
Farma).
3.4 Prosedur Penelitian 3.4.1 Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif yaitu tanpa
membandingkan satu tempat dengan tempat yang lain karena tempat pengambilan
sampel dianggap homogen. Dari hasil sampling diperoleh suspensi Trimoxul (PT.
Interbat), Sanprima (PT. Sanbe Farma), Primadex (PT. Dexa Medica) dan
Cotrimoxazole (PT. Phyto Kemo Agung Farma).
3.4.2 Pembuatan Fase Gerak
Dicampurkan 1400 ml air, 400 ml asetonitril, dan 2,0 ml trietilamina
dalam labu tentukur 2000 ml, biarkan hingga suhu kamar dan atur pH hingga 5,9
± 0,1 dengan larutan asam asetat glasial dalam air (1 dalam 100). Encerkan
dengan air sampai garis tanda, saring melalui membran 0,45 μm. Sebelum
digunakan, fase gerak diawaudarakan selama lebih kurang 15 menit.
3.4.3 Pembuatan larutan induk baku BPFI
Ditimbang seksama sejumlah 50,0 mg sulfametoksazol BPFI dan
trimetoprim BPFI, masing-masing dimasukkan ke dalam labu tentukur 50 ml,
dilarutkan dan diencerkan dengan metanol hingga garis tanda sehingga diperoleh
larutan dengan konsentrasi 1000 mcg/ml, disaring, filtratnya digunakan sebagai
3.4.4 Penyiapan alat KCKT
Kolom yang digunakan Shimpac VP-ODS (4.6 mm x 25 cm), detektor
UV-Vis pada panjang gelombang 254 nm. Pompa yang digunakan metode aliran
tetap dengan laju aliran (flow rate) 2 ml/menit, sensitivitas 1,000 AUFS.
Setelah alat KCKT dihidupkan, maka pompa dijalankan dan fase gerak
dibiarkan mengalir beberapa lama sampai diperoleh garis alas yang datar yang
menandakan sistem tersebut telah stabil.
3.4.5 Uji kualitatif Sulfametoksazol dan Trimetoprim menggunakan KCKT 3.4.5.1 Menentukan waktu tambat Sulfametoksazol dan Trimetoprim BPFI
Larutan Sulfametoksazol BPFI disuntikkan ke sistem KCKT dengan
volume penyuntikan 20 µl pada kondisi KCKT yang sama. Larutan trimetoprim
BPFI disonikasi selama 10 menit dan disuntikkan ke sistem KCKT dengan
volume penyuntikan 20 µl pada kondisi KCKT yang sama, diperoleh
kromatogram dan dicatat waktu tambat masing-masing (Hasil dapat dilihat pada
gambar 4.4 dan 4.5 di halaman 34)
3.4.6 Penentuan kuantitatif
3.4.6.1 Pembuatan linieritas kurva kalibrasi 3.4.6.1.1 Kurva kalibrasi sulfametoksazol BPFI
Dipipet larutan induk baku sulfametoksazol sebanyak 0,5; 1,0; 1,6; 2,0;
dan 2,5 ml, masing-masing dimasukkan ke dalam labu tentukur 10 ml, diencerkan
dengan fase gerak hingga garis tanda sehingga diperoleh konsentrasi 50, 100, 160,
200 dan 250 mcg/ml, disaring, kemudian filtratnya masing-masing diinjeksikan ke
sistem KCKT dengan volume penyuntikan 20 µl dengan laju aliran (flow rate) 2
luas area kromatogram yang diperoleh dibuat kurva kalibrasi lalu hitung
persamaan regresinya. (Hasil dapat dilihat pada gambar 4.12 dan lampiran 7 di
halaman 38 dan 54-55).
3.4.6.1.2 Kurva kalibrasi trimetoprim BPFI
Dipipet larutan induk baku trimetoprim sebanyak 0,1; 0,2; 0,32; 0,4; dan
0,5 ml, masing-masing dimasukkan ke dalam labu tentukur 10 ml, diencerkan
dengan fase gerak hingga garis tanda sehingga diperoleh konsentrasi 10, 20, 32,
40 dan 50 mcg/ml, disaring, kemudian filtratnya masing-masing diinjeksikan ke
sistem KCKT dengan volume penyuntikan 20 µl dengan laju aliran (flow rate) 2
ml/menit, deteksi dilakukan pada panjang gelombang 254 nm. Selanjutnya dari
luas area kromatogram yang diperoleh dibuat kurva kalibrasi lalu hitung
persamaan regresinya (Hasil dapat dilihat pada gambar 4.13 dan lampiran 7
halaman 39 dan 55-56).
3.4.7 Perlakuan Sampel
Dipipet 2 ml sampel suspensi, dimasukkan ke dalam labu tentukur 50 ml,
lalu dilarutkan dengan pelarut metanol 30 ml. Sonikasi selama 10 menit,
cukupkan volume sampai garis tanda, dikocok dan sentrifuge. Dipipet 5 ml
supernatan, dimasukkan ke dalam labu tentukur 50 ml yang kedua encerkan
dengan fase gerak sampai garis tanda sehingga diperoleh larutan dengan
konsentrasi 160 mcg/ml. Dilakukan pengulangan sebanyak 6 kali lalu
masing-masing disaring dengan membran Whatman PTFE 0,2 μm. Kemudian dinjeksikan
rate) 2,0 ml/menit dan deteksi dilakukan pada panjang gelombang 254 nm,
kemudian dihitung kadarnya.
3.4.7.1 Penetapan Kadar sampel
Dinjeksikan 20 μL larutan sampel ke sistem KCKT dengan laju alir (flow
rate) 2,0 ml/menit dan deteksi dilakukan pada panjang gelombang 254 nm.
Diamati puncak yang muncul dalam kromatogram.
Luas area (luas puncak) dari kromatogram sampel (Y) disubsitusikan ke
persamaan garis regresi yang diperoleh dari kurva kalibrasi (Y = aX + b),
sehingga diperoleh konsentrasi sampel (X) dan dihitung kadarnya (data dapat
dilihat pada lampiran 14-20 halaman 73-89).
3.4.8 Penentuan Spektra Infra Red
3.4.8.1 Penentuan Spektra Infra Red Sukfametoksazol
Dicampur serbuk sulfametoksazol dengan serbuk KBr dalam lumpang,
kemudian dipasang pasang DRS 8000 (Diffuse Reflectance Measuring) pada
tempat sampel, lalu dimasukkan campuran sampel KBr ke sample pan, diletakkan
ke tempat dudukan sample pan, kemudian dianalisis spektrumnya.
3.4.8.2 Penentuan Spektra Infra Red Trimetoprim
Dicampur serbuk trimetoprim dengan serbuk KBr dalam lumpang,
kemudian dipasang pasang DRS 8000 (Diffuse Reflectance Measuring) pada
tempat sampel, lalu dimasukkan campuran sampel KBr ke sample pan, diletakkan
ke tempat dudukan sample pan, kemudian dianalisis spektrumnya.
3.4.9 Prosedur Validasi
Dipipet 2 ml suspensi kotrimoksazol, kemudian dimasukkan dalam labu
tentukur 50 ml. Lalu Ditambahkan dengan 20 ml LIB sulfametoksazol dan 4 ml
dengan metanol sampai garis tanda, setelah itu disentrifuge selama 10 menit.
Diperoleh supernatant dan endapan, kemudian dipipet supernatan sebanyak 5 ml,
dimasukkan ke labu 50 ml, lalu diencerkan dengan fase gerak sampai garis tanda.
Kemudian disaring melalui membran PTFE 0,2 µ. Disuntikkan sebanyak 20 µl
pada sistem KCKT , lalu di peroleh hasilnya dan dicatat.
3.4.10 Penentuan Limit of Detection ( LOD ) dan Limit of Quantitation (LOQ)
Batas deteksi atau Limit of Detection ( LOD ) adalah jumlah terkecil analit
dalam sampel yang dapat dideteksi. Batas kuantitasi atau Limit of Quantitation
(LOQ) merupakan kuantitas terkecil analit dalam sampel.
Untuk menentukan batas deteksi (LOD) dan batas kuantitasi (LOQ)
digunakan rumus: SD = 1
)
( 2
n Yi Y
LOD =
Slope XSD
3
LOQ =
Slope XSD
10
Keterangan :
SD = Standar Deviasi
LOD = Batas Deteksi
LOQ = Batas Kuantitasi ( Harmita, 2004 )
3.4.11 Analisis Statistik Penolakan Hasil Pengamatan
Kadar Campuran Sulfametoksazol dan Trimetoprim sebenarnya dalam
sampel dapat diketahui dengan menggunakan uji Q test. Cara untuk melakukan
analisis terhadap data yang menyimpang adalah dengan Dixon’s Q-test yang
terendah nilai
tertinggi nilai
terdekat yang
nilai dicurigai yang
nilai Qhitung
Jika nilai Qhitung lebih kecil dari nilai Qkritis maka hipotesis nol diterima
berarti tidak ada perbedaan antara nilai yang dicurigai dengan nilai-nilai yang lain
( Rohman, 2007 ).
Hasil pengujian atau nilai Q yang diperoleh ditinjau terhadap daftar harga
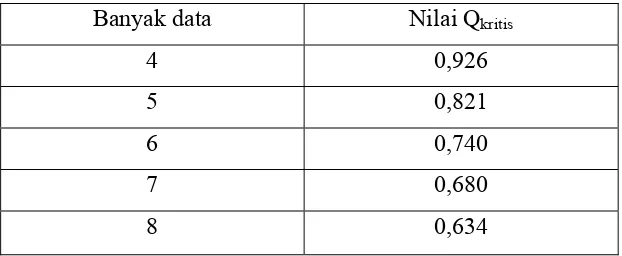
[image:40.595.157.468.287.415.2]Q pada Tabel 2.1, apabila Q > Q0,99 maka data tersebut ditolak.
Tabel 3.1. Nilai Qkritis pada Taraf Kepercayaan 99%
Banyak data Nilai Qkritis
4 0,926
5 0,821
6 0,740
7 0,680
8 0,634
BAB IV
HASIL DAN PEMBAHASAN
Suspensi kotrimoksazol merupakan kombinasi antara sulfametoksazol dan
trimetoprim dengan perbandingan (5:1), dimana kedua senyawa ini bersifat semi
polar dan mudah larut dalam alkohol sehingga penetapan kadarnya dapat
dilakukan secara Kromatografi Cair Kinerja Tinggi (KCKT) dengan fase gerak
campuran air : asetonitril : trietylamin (1400 : 400 : 2) v/v dengan metode
isokratik.
Pada`penelitian ini prosedur penetapan kadar secara Kromatografi Cair
Kinerja Tinggi menggunakan prosedur yang terdapat dalam USP edisi XXXI
(2008) dengan kolom yang berbeda yaitu kolom yang digunakan adalah kolom
Shimpac VP-ODS (4,6 mm x 25 cm) dan deteksi dilakukan pada panjang
gelombang 254 nm serta sensitivitas 1,000 AUFS.
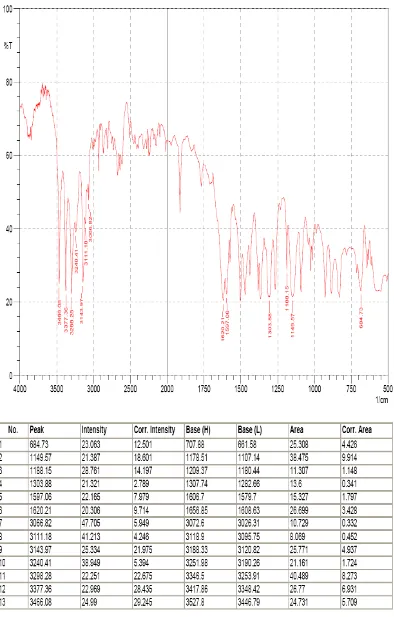
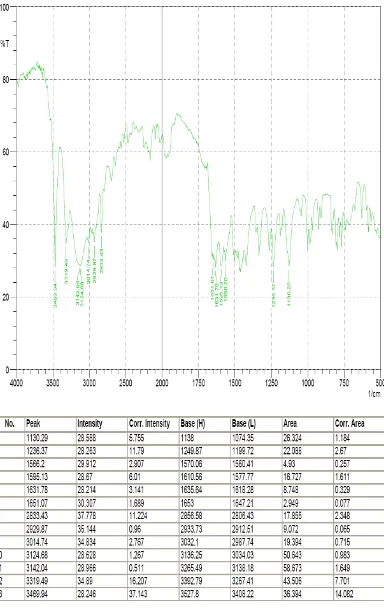
Hasil uji identifikasi Sulfametoksazol BPFI dan Trimetoprim BPFI yang
dilakukan dengan Spektrofotometer IR dan KCKT diperoleh hasil sebagai berikut,
dari hasil spektrum Sulfametoksazol dan Trimetoprim diperoleh bentuk spektrum
yang hampir sama dengan spektrum pembanding yang terdapat pada library
(dapat dilihat pada lampiran). Bilangan gelombang pada daerah sidik jari juga
hampir sama dengan bilangan gelombang yang terdapat pada literatur yaitu untuk
Sulfametoksazol pada bilangan gelombang 1145, 1160, 1599, 1621, 685, 1306
cm-1 dan untuk Trimetoprim pada bilangan gelombang 1126, 1630, 1596, 1235,
1650, 1565 cm-1 (Clarke’s, 2005).
Pada daerah gugus fungsi dari spektrum Sulfametoksazol terlihat beberapa
gugus amin primer dan pada 3298.28 – 3240.41 menunjukkan gugus amin
sekunder, pada bilangan gelombang 3143.97 – 3066.82 cm-1 menunjukkan cincin
aromatis. Sedangkan pada daerah gugus fungsi spektrum Trimetoprim terlihat
beberapa peak yaitu pada bilangan gelombang 3469.94 cm-1 yang menunjukkan
gugus amin primer, pada bilangan gelombang 3142.04 – 3124.68 cm-1
menunjukkan =C – H aromatis.
Dari data spektrum yang diperoleh, dapat diambil kesimpulan bahwa baku
yang diidentifikasi adalah Sulfametoksazol dan Trimetoprim.
Hasil uji identifikasi menggunakan KCKT diperoleh waktu retensi yaitu
menit ke-2 untuk sulfametoksazol dan menit ke-6 untuk trimetoprim. Hal ini
terjadi karena perbedaan kepolaran kedua komponen, dimana pada metode KCKT
komponen yang non polar sedikit tertahan di dalam kolom dibandingkan dengan
komponen yang lebih polar sehingga waktu retensinya juga lebih cepat. Maka
dapat disimpulkan bahwa sulfametoksazol bersifat lebih polar daripada
trimetoprim berdasarkan waktu retensi kedua komponen. Hasil pengujian untuk
suspensi yang terdapat dalam perdagangan baik dengan nama generik maupun
nama dagang juga sama. Hal ini berarti bahwa sampel yang terdapat
diperdagangan mengandung sulfametoksazol dan trimetoprim. Kromatogram
Gambar 4.3 Hasil Kromatogram dengan Metode Kromatografi Cair Kinerja Tinggi dengan Fase Gerak acetonitril : air (25 : 75) v/v mengandung ammonium acetat 1% dengan laju alir 1 ml/menit dan UV detektor pada 254 nm
Acquired by : Admin
Method File Name : campuran baku.Icm Report File Name : Simple Single.Icr Sample Type : Unknowm
Level : 1
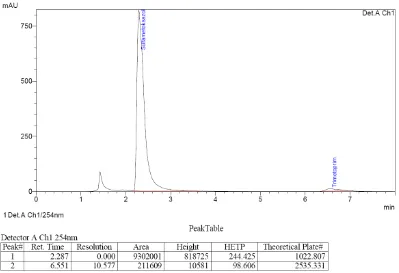
Peak Table Detector A Ch1 254nm
Peak# Ret. Time Resolution Area Height HETP Theoretical Plate#
- Hasil Kromatogram dengan metode Kromatografi Cair Kinerja Tinggi menggunakan kolom ODS (4.6 mm x 25 cm) dengan fase gerak campuran air, asetonitril dan trietylamina (1400 : 400 : 2) v/v, dengan laju alir (flow rate) 2 ml/menit, volume penyuntikan 20 µl dan UV detektor pada 254 nm
Gambar 4.4 Kromatogram hasil penyuntikan larutan Sulfametoksazol BPFI
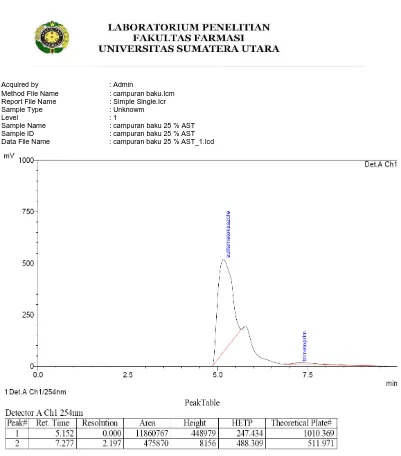
[image:48.595.121.512.449.743.2]Gambar 4.6 Kromatogram hasil penyuntikan larutan Baku campur sulfametoksazol dan trimetoprim BPFI dengan konsentrasi masing-masing 160 mcg/ml dan 32 mcg/ml, yang dianalisis secara KCKT
Untuk memilih metode dengan 2 fase gerak berbeda dilakukan dengan
baku campur sulfametoksazol dan trimetoprim, hasil dapat dilihat pada gambar
dibawah. Dari gambar 4.3 terlihat bahwa penelitian dengan mempergunakan fase
gerak asetonitril : air : ammonium acetat menghasilkan kromatogram yang kurang
baik, karena kromatogram yang dihasilkan saling bergabung, dengan demikian
penelitian dengan menggunakan fase gerak tersebut dihentikan dan dilanjutkan
dengan menggunakan metode dengan fase gerak air : asetonitril : trietylamin yang
menghasilkan kromatogram yang lebih baik dibandingkan kromatogram
menggunakan fase gerak pertama.
Hasil kromatogram larutan sampel dengan konsentrasi masing-masing 160
mcg/ml dan 32 mcg/ml, yang dianalisis secara KCKT dengan fase gerak air :
[image:49.595.113.511.88.393.2]Gambar 4.7 Kromatogram hasil penyuntikan larutan suspensi Sanprima dengan penambahan spike baku trimetoprim
[image:50.595.118.511.417.675.2]Gambar 4.9 Kromatogram hasil penyuntikan larutan suspensi sanprima
[image:51.595.116.509.427.701.2]Gambar 4.11 Kromatogram hasil penyuntikan larutan suspensi Cotrimoksazol. Penentuan linieritas kurva kalibrasi Sulfametoksazol BPFI ditentukan
berdasarkan luas puncak pada rentang konsentrasi 50 sampai 250 mcg/ml,
diperoleh hubungan linearitas dengan koefisien kolerasi (r) = 0,9997 dan
persamaa garis regresi Y = 46709,25327 X + 46088,31281. Hasil linieritas kurva
kalibrasi larutan Sulfametoksazol BPFI dapat dilihat pada gambar 4.12.
Gambar 4.12. Kurva kalibrasi sulfametoksazol BPFI
Penentuan linieritas kurva kalibrasi trimetoprim BPFI ditentukan
[image:52.595.113.512.86.359.2] [image:52.595.184.438.527.662.2]diperoleh hubungan yang linier dengan koefisien korelasi, r = 0,9997 dan
persamaan regresi Y = 5800,13118X + 5576,943053. Hasil penentuan kalibrasi
dapat dilihat pada gambar 4.13.
Gambar 4.13. Kurva kalibrasi trimetoprim BPFI
Dari pengolahan data, dapat dihitung kadar Sulfametoksazol dan
Trimetoprim dalam sediaan suspensi berdasarkan luas puncak. Kadar
Sulfametoksazol dalam sampel dapat dihitung menggunakan persamaan regresi Y
= 46709,25327 X + 46088,31281 yaitu mensubsitusikan Y dengan luas puncak
sampel. Sedangkan untuk kadar Trimetoprim dalam sampel dapat dihitung dengan
mensubsitusikan Y dengan luas puncak sampel dengan menggunakan persamaan
garis regresi Y = 5800,13118 X + 5576,943053
Hasil perhitungan diketahui harga X (kadar sampel) dan pengolahan data
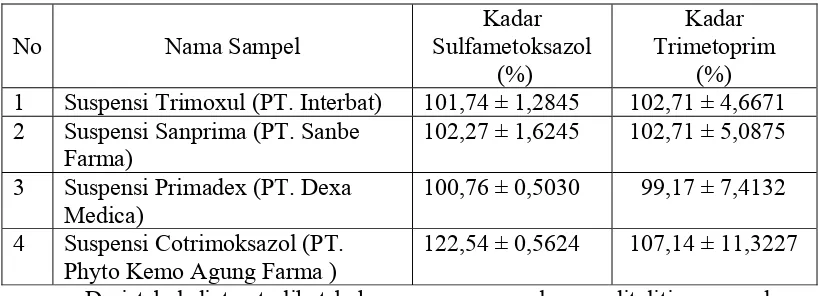
Tabel 4.1 Data hasil penetapan kadar Sulfametoksazol dan Trimetoprim dalam sediaan suspensi
No Nama Sampel
Kadar Sulfametoksazol
(%)
Kadar Trimetoprim
(%) 1 Suspensi Trimoxul (PT. Interbat) 101,74 ± 1,2845 102,71 ± 4,6671 2 Suspensi Sanprima (PT. Sanbe
Farma)
102,27 ± 1,6245 102,71 ± 5,0875
3 Suspensi Primadex (PT. Dexa Medica)
100,76 ± 0,5030 99,17 ± 7,4132
4 Suspensi Cotrimoksazol (PT. Phyto Kemo Agung Farma )
122,54 ± 0,5624 107,14 ± 11,3227
Dari tabel diatas terlihat bahwa semua sampel yang diteliti mengandung
sulfametoksazol memenuhi persyaratan kadar yang tertera dalam USP XXXI
(2008) yaitu mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0%
dari jumlah yang tertera pada etiket sulfametoksazol (C10H11N3O3S) dan
Trimetoprim (C14H18N4O3), kecuali sulfametoksazol pada suspensi cotrimoksazol
yang tidak memenuhi persyaratan USP XXXI (2008). Sedangkan untuk
Trimetoprim memenuhi persyaratan kadar yang tertera dalam USP XXXI (2008) .
Pada penelitian ini dilakukan uji validasi metode dengan metode
penambahan bahan baku (standard addition methode) terhadap sampel suspensi
Trimoxul (PT. Interbat) meliputi uji akurasi dengan parameter persen perolehan
kembali (% recovery) dan uji presisi dengan parameter Standar Deviasi (SD) dan
RSD (Relatif Standar Deviasi), batas deteksi (LOD) dan batas kuantitasi (LOQ).
(Harmita, 2004).
Uji akurasi dengan parameter persen perolehan kembali dilakukan dengan
menambahkan 80 mcg/mg Sulfametoksazol BPFI, dan 16 mcg/mg Trimetoprim
BPFI. Data hasil pengujian perolehan kembali Sulfametoksazol dengan metode
Tabel 4.2 Data hasil pengujian perolehan kembali Sulfametoksazol dan Trimetoprim dengan metode penambahan bahan baku (standard addition methode)
Penambahan zat aktif Luas Puncak
Persen perolehan kembali
(%)
Sulfametoksazol
11525560 102,2
11545207 102,73 11665932 105,96 11633103 105,08 11521556 102,1
11502947 101,61
Kadar rata-rata (%) 103,28
Standar Deviasi (SD) 1,7929
Relatif Standar Deviasi (RSD) (%) 1,7359
Trimetoprim
284719 96,63 287376 99,44 288279 100,44
285514 97,44 286429 98,44 287534 99,63
Kadar rata-rata (%) 98,67
Standar Deviasi (SD) 1,4405
Relatif Standar Deviasi (RSD) (%) 1,4599
Dari data diatas diperoleh persen perolehan kembali Sulfametoksazol
103,28%. Persen perolehan kembali ini dapat diterima karena memenuhi syarat
akurasi, rentang rata-rata hasil persen perolehan kembali adalah 80 - 110%. Hasil
uji presisi dengan parameter standar deviasi (SD) sebesar 1,7929 dan relative
standar deviasi (RSD) 1,7359%. Nilai RSD yang diizinkan adalah ≤ 2%. Batas
deteksi (LOD) dan batas kuantitasi (LOQ) yang diperoleh dari penelitian ini
sebesar 13,47 mcg/ml dan 44,89 mcg/ml.
Persen perolehan kembali trimetoprim 98,67%. Persen perolehan kembali
ini dapat diterima karena memenuhi syarat akurasi, rentang rata-rata hasil persen
perolehan kembali adalah 80 - 110%. Hasil uji presisi dengan parameter standar
RSD yang diizinkan adalah ≤ 2%. Batas deteksi (LOD) dan batas kuantitasi
(LOQ) yang diperoleh dari penelitian ini sebesar 4,51 mcg/ml dan 15,03 mcg/ml.
Dari hasil yang diperoleh dapat disimpulkan bahwa metode yang
digunakan memenuhi persyaratan uji validasi sehingga dapat digunakan untuk
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Dari penelitian yang telah dilakukan maka penetapan kadar
Sulfametoksazol dan Trimetoprim dalam sediaan suspensi dapat dilakukan secara
Kromatografi Cair Kinerja Tinggi (KCKT), menggunakan fase gerak air :
asetonitril : triethylamin (1400 : 400 : 2) v/v, dengan laju alir 2 ml/menit, pada
panjang gelombang 254 nm.
Hasil penetapan kadar Suspensi Sulfametoksazol dan Trimetoprim dari
empat sampel dengan nama dagang dan generik, terdapat satu sampel dengan
nama generik yang tidak memenuhi persyaratan yang ditetapkan oleh USP edisi
XXXI tahun 2008, yaitu tidak kurang dari 90,0 % dan tidak lebih dari 110,0 %
dari jumlah yang tertera pada etiket, yaitu untuk sediaan suspensi dengan nama
dagang Trimoxul (PT. Interbat), Sulfametoksazol = 102,49% ± 1,28, dan
Trimetoprim = 102,51% ± 4,65, Sanprima (PT. Sanbe Farma), Sulfametoksazol =
103,04% ± 1,63, Trimetoprim = 102,51% ± 5,07, Primadex (PT. Dexa Medica),
Sulfametoksazol = 101,51% ± 0,48, Trimetoprim = 98,97% ± 7,39 untuk sediaan
dengan nama generik Cotrimoksazole (PT. Phyto Kemo Agung Farma),
sulfametoksazol = 123,45% ± 0,56, trimetoprim = 106,93% ± 11,31.
Dari hasil uji validasi menunjukkan bahwa metode yang telah dilakukan
memenuhi persyaratan uji validasi yang meliputi ujia akurasi dan uji presisi,
sehingga metode ini dapat digunakan untuk penetapan kadar sulfametoksazol dan
5.2 Saran
Disarankan agar dilakukan penelitian lebih lanjut terhadap penetapan
DAFTAR PUSTAKA
De Lux Putra, E. (2007). Dasar-dasar Kromatografi Gas & Kromatografi Cair
Kinerja Tinggi. Fakultas Farmasi USU-Medan. Hal. 88-91.
DitJen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta. Departemen Kesehatan RI. Hal. 769-771.
Gandjar, I. G., dan A.Rohman. (2007). Kimia Farmasi Analisis. Yogyakarta. Penerbit Pustaka Pelajar. Hal. 378- 379, 406.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara
Perhitungannya. Departemen Farmasi FMIPA UI. Hal. 117-132.
Johnson, E.L., and Stevenson, R (1991). Basic Liquid Chromatography. Penerjemah Kosasih Padmawinata. Dasar Kromatografi Cair. Penerbit ITB Bandung. Hal. 291-302.
Katzung, B, G. (1898). Farmakologi Dasar dan Klinik. Edisi III. Penerbit Buku Kedokteran ECG. Jakarta. Hal : 655 - 660
Katzung, B, G. (2004). Farmakologi Dasar dan Klinik. Edisi VIII. Penerbit Buku Kedokteran ECG. Jakarta. Hal : 73 - 80
Lunn, G and Schmuff, N. R. (1997). HPLC Methods for Pharmaceutical Analysis. John Wiley & Sons, Inc. Page. 17 -19.
Mariana, J. (1995). Sulfonamid dan Trimetoprim-Sulfametoksazol. Dalam Farmakologi dan Terapi. Edisi keempat. Bagian Farmakologi FKUI. Jakarta. Penerbit Universitas Indonesia Press. Hal. 460, 470-471.
Roos, R. W. And Lau-Cam, C.A. (1986). General Reversed-Phase High-Performance Liquid Chomatographic Method for the Separation of Drugs
using Triethylamine as aC ompeting Base. Page. 403-418
Silverstein, et all. (1986). Penyidikan Spektrometrik Senyawa Organik. Edisi Ke Empat. Jakarta. Penerbit Erlangga. Hal : 95 – 181.
Tjay, T.H., dan Rahardja, K. (2002). Obat-Obat Penting. Edisi V. Cetakan ke-2. PT. Gramedia. Jakarta. Hal : 80 – 81.
USP Pharmacopeia, (2008). The National Formulary. 31th Edition . The United States Pharmacopeial Convention. Page. 3300– 3301.
Lampiran 1. Gambar alat KCKT dan syringe 100 µl
Gambar 1. Alat KCKT (Shimadzu) di laboratorium Farmasi Kuantitatif USU
[image:60.595.131.530.466.631.2]Lampiran 2.Gambar alat ultrasonic cleaner dan penyaring
Gambar 3. Alat Ultrasonic Cleaner di laboratorium Farmasi Kuantitatif USU
[image:61.595.185.490.467.694.2]Lampiran 3. Gambar alat sentrifuge
Lampiran 4. Spektrum Inframerah Sulfametoksazol pada literatur Pharmaceutical Sub stance (UV/IR)
Lampiran 4. Kromatogram dari larutan Sulfametoksazol dan Trimetoprim BPFI
Lampiran 5. Spektrum Inframerah Trimetoprim pada literatur Pharmaceutical Sub stance (UV/ IR)