DETEKSI Mycobacterium avium subspesies paratuberculosis
PADA SAPI PERAH, SUSU PASTURISASI, DAN SUSU FORMULA
LANJUTAN DI WILAYAH BOGOR
WIDAGDO SRI NUGROHO
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
BOGOR
2008
PERNYATAAN MENGENAI DESERTASI DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa disertasi Deteksi Mycobacterium avium
subspesies paratuberculosis pada Sapi Perah, Susu Pasturisasi, dan Susu Formula Lanjutan di Wilayah Bogor adalah karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
Bogor, 11 November 2008
Widagdo Sri Nugroho NRP B063040031
WIDAGDO SRI NUGROHO. Detection of Mycobacterium avium subspecies paratuberculosis in Dairy Cows, Pasteurized Milk, and Growing-up Formula
Milk in Bogor. Under the direction of MIRNAWATI SUDARWANTO, DENNY
WIDAYA LUKMAN, EWALD USLEBER, and SURACHMI SETIYANINGSIH
Indonesia has been importing dairy cows and milk products from countries which have endemic disease of paratuberculosis or Johne’s disease. This disease is caused by Mycobacterium avium subspecies paratuberculosis (MAP) and has big impact in economic losses of dairy industry. The bacterium has been suggested to cause Crohn’s disease that can be transmitted via milk and milk products. In the last few years, paratuberculosis has been detected serologically in Indonesia. This situation suggests a potential spread of the disease in the national dairy herds, and may pose a public health risk. In the other aspect, Indonesia needs the diagnostic tools to isolate MAP cheaply but quite accurate. The Ogawa medium is a cheap medium, which is commonly used to isolate Mycobacterium tuberculosis in Indonesia and could be improved as growth medium for MAP.
The objectives of the current study were (1) to evaluate capability of modified Ogawa medium (MOM) as a growth medium for MAP, (2) to detect MAP in dairy herd and as good as to evaluate the association between farm management factors and the presence of the bacteria, (3) to detect MAP in pasteurized and growing up formula milk in Bogor.
The study was done in Bogor region. Milk and feces samples were taken from 62 dairy cows (with estimated prevalence of 5%) in Cibungbulang. Fourty two pasteurized milk samples produced by 7 distributors and 50 growing up formula milk produced by 5 distributors were purchased in supermarkets.
Detection methods used MOM, herrold’s egg yolk medium with and without
mycobactin J, mycobacterium growth indicator tube, Ziehl-Neelsen staining, and conventional polymerase chain reaction (PCR) using primers IS900 and F57. Performance of MOM as growth medium for MAP and Mycobacterium avium
subspecies avium (MAV) was evaluated by agreement test (Kappa). The association between herd management factors and the presence of Mycobacterium sp. was evaluated using Odds Ratio (OR). The presence of MAP in raw, pasteurized, and growing up formula milk were analyzed descriptively.
The modified Ogawa medium showed very poor performance as growth medium for MAP (Kappa=0) but was useful for MAV (Kappa=1).There were no MAP isolated from raw milk and feces of dairy cows. Fifteen Mycobacterium sp. could be isolated from 15 dairy cows, but none of them was identified as either MAP or M. tuberculosis. The study suggests that the prevalence of MAP among dairy cattle in Bogor was less than 5%. The existence of Mycobacterium sp. in faeces associated with body weight (OR 1.9), individual cases of diarrhoea (OR 1.8), age (OR 1.7), daily milk product (0.5), and personal hygiene (0.3). Similarly, there was no evidence of life MAP contamination in pasteurized and growing up formula milks, but nested PCR using F57 detected MAP DNA in 5 samples from 3 growing-up formula milk producers.
Further study needs to be done to improve the formulation of MOM suitable for MAP. In addition, an observational study in dairy cattle, goat, sheep, and rabbit is necessary to achieve the comprehensive information on paratuberculosis in Indonesia. And from the public health point of view, a comprehensive and sustainable study on MAP in milk and milk products, as well as in human is of particularly important.
Key words: Mycobacterium avium subspecies paratuberculosis modified Ogawa medium, raw milk, pasteurized milk, growing-up formula milk.
RINGKASAN
WIDAGDO SRI NUGROHO. Deteksi Mycobacterium avium subspesies paratuberculosis pada Sapi Perah, Susu Pasturisasi, dan Susu Formula
Lanjutan di Wilayah Bogor. Dibimbing oleh MIRNAWATI SUDARWANTO, DENNY
WIDAYA LUKMAN, EWALD USLEBER, dan SURACHMI SETIYANINGSIH
Indonesia merupakan pengimpor sapi perah maupun produk susu olahan dari beberapa negara endemis penyakit paratuberkulosis atau Johne’s disease (JD). Penyakit yang disebabkan oleh bakteri Mycobacterium avium subspesies
paratuberculosis (MAP) ini sangat merugikan ekonomi perternakan dan diduga kuat menularkan penyakit Crohn pada manusia melalui produk susu dan susu olahannya. Beberapa tahun terakhir, paratuberkulosis terdeteksi secara serologis pada sapi perah di Jawa Tengah dan Jawa Barat. Selama ini belum pernah dilakukan kajian yang mendalam terhadap paratuberkulosis di Indonesia sehingga sangat dikhawatirkan akan menyebar dan menimbulkan masalah bagi dunia peternakan dan kesehatan masyarakat. Di lain pihak, media isolasi MAP yang mahal dan langka menjadi salah satu kendala lain untuk mendiagnosis penyakit ini. Media Ogawa selama ini dikenal sebagai media isolasi dan pertumbuhan Mycobacterium
tuberculosis yang murah dan mudah dibuat. Media ini sangat berpotensi untuk
dikembangkan menjadi media isolasi dan pertumbuhan untuk MAP dengan melakukan modifikasi komponen penyusunnya.
Penelitian ini dilakukan untuk (1) menguji media Ogawa modifikasi (MOM) sebagai media isolasi dan pertumbuhan MAP (2) mendeteksi kasus MAP pada sapi perah dan mengukur asosiasi tatacara beternak dengan keberadaan bakteri tersebut (3) mendeteksi MAP pada susu pasturisasi dan susu formula lanjutan yang dijual di wilayah Bogor.
Kajian deteksi MAP pada sapi perah dilakukan di wilayah Bogor dengan asumsi prevalensi 5%. Contoh susu dan feses diambil dari 62 sapi perah Cibungbulang Bogor yang tergabung dalam Koperasi Produksi Susu dan Usaha Peternakan (KPS) Bogor. Deteksi MAP juga dilakukan 42 kemasan (180-250 ml) susu pasturisasi yang berasal dari 7 produsen dan 50 kemasan (120-200 g) susu formula lanjutan yang berasal dari 5 produsen. Seluruh produk susu olahan tersebut dibeli dari supermarket di Wilayah Bogor dengan target konsumen adalah anak-anak.
Pengujian dilakukan menggunakan MOM, media herrold’s egg yolk medium
yang diperkaya dan tidak diperkaya mycobactin J, mycobacterium growth indicator tube, dan polymerase chain reaction (PCR) konvensional dengan primer IS900 dan F57. Analisis hasil uji MOM dilakukan dengan uji kesesuaian (Kappa), analisis faktor keberadaan bakteri Mycobacterium sp. dilakukan dengan Odds Ratio (OR), dan deteksi MAP pada susu segar, susu pasturisasi, dan susu formula lanjutan dilakukan secara deskriptif.
Media Ogawa modifikasi mampu menumbuhkan Mycobacterium avium
subspesies avium namun belum sesuai untuk menumbuhkan MAP. Tidak ditemukan isolat MAP dari seluruh contoh susu segar dan feses sapi perah. Pada penelitiani ini diperoleh 15 isolat Mycobacterium sp. yang tumbuh dari contoh 15 feses sapi perah. Limabelas isolat Mycobacterium sp. tersebut setelah dikonfirmasi dengan PCR tidak teridentifikasi sebagai MAP dan berdasarkan uji kimia tidak teridentifikasi pula sebagai M. tuberculosis. Hasil analisis asosiasi dan Odds Ratio atas keberadaan
Mycobacterium sp. pada feses dengan tatacara beternak memperlihatkan beberapa
faktor yang terkait. Faktor-faktor dapat digunakan sebagai indikasi untuk membantu diagnosis kasus infeksi Mycobacterium sp. Faktor-faktor tersebut adalah berat badan (OR 1.9), kasus diare (OR 1.8), umur (OR 1.7) produksi susu per hari (OR 0.5), dan kebersihan pemerah (OR 0.3). Tidak ditemukannya bakteri MAP dalam penelitian ini mengindikasikan bahwa prevalensi kasus MAP di Bogor kurang dari 5%.
Hasil deteksi terhadap MAP pada susu olahan yaitu susu pasturisasi dan susu formula lanjutan menunjukkan tidak adanya isolat MAP yang tumbuh dari seluruh
berdasarkan uji PCR F57 nested diperoleh DNA target dari 5 contoh susu yang berasal dari 3 produsen susu formula lanjutan. Temuan ini merupakan indikasi adanya jejak keberadaan MAP dalam susu formula lanjutan tersebut namun tidak ditemukannya isolat yang tumbuh membuktikan bahwa tidak ada bakteri MAP yang hidup dalam produk tersebut.
Hasil penelitian ini memberikan data awal terhadap keberadaan MAP di Indonesia dan masih perlu tindak lanjut kajian untuk memberikan gambaran yang komprehensif status MAP. Kajian perlu dilanjutkan untuk mendapatkan formula media Ogawa modifikasi yang tepat sebagai media pertumbuhan MAP. Kajian observasional perlu dilakukan pada peternakan sapi perah, kambing, domba, serta kelinci untuk mendapatkan gambaran lengkap paratuberkulosis di Indonesia. Kajian menyeluruh dan berkelanjutan juga harus dilakukan pada susu dan hasil olahannya dengan jumlah sampel yang lebih besar dan bervariasi termasuk pada manusia untuk menjamin keamana pangan bagi masyarakat Indonesia. Di lain pihak dengan ditemukannya isolat Mycobacterium sp. maka perlu diaktifkan kembali tuberkulinasi pada sapi perah sebagai upaya pemantauan kasus tuberkulosis sapi.
Kata kunci: Mycobacterium avium subspesies paratuberculosis, media Ogawa modifikasi, susu segar, susu pasturisasi, susu formula lanjutan.
© Hak Cipta milik IPB, tahun 2008
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB. Dilarang mengumumkan atau memperbanyak sebagian atau seluruh karya tulis dalam bentuk apapun tanpa seizin IPB
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas rahmat dan
hidayahNya sehingga desertasi ini berhasil diselesaikan. Penelitian ini berorientasi
pada kesehatan ternak dan keamanan pangan bagi kesehatan masyarakat dengan
topik Mycobacterium avium subspesies paratuberculosis yang sangat jarang diteliti di Indonesia. Bakteri ini memiliki potensi menjadi ancaman yang besar bagi
peternakan dan kesehatan manusia di Indonesia.
Penulis mengucapkan terimakasih sebesar-besarnya kepada Prof. Dr. drh. Hj.
Mirnawati Sudarwanto, Prof. Dr. Ewald Usleber, Dr. drh. Denny Widaya Lukman, M.
Si. dan drh. Surachmi Setiyaningsih, Ph.D. selaku pembimbing yang memberi
kesempatan penulis untuk melakukan sebagian penelitian di Jerman. Kepada drh.
Rochman Naim, Ph.D. yang telah memberikan masukan di awal penelitian ini.
Terimakasih juga disampaikan kepada Prof. drh. Setyawan Budiharta, M.P.H., Ph.D.
dan Prof. Dr. drh. Bambang Sumiarto, S.U., M.Sc. yang telah mengarahkan dan
mendukung penulis untuk melanjutkan pendidikan doktor dengan program sandwich,
kepada Dr. drh. I Wayan Teguh Wibawan, M.S. dan Dr. Ir. Rarah R.A. Maheswari,
D.E.A. selaku penguji luar komisi, kepada drh. Muhammad Fahruddin, Ph.D. dan
drh. Ni Wayan Kurniani Karja, M.P., Ph.D. atas dukungan akomodasi kepada penulis
selama di Bogor, kepada Dr. Abdulwahed Ahmed Hassan dan seluruh staf
Laboratorium Kesehatan Susu, Universitas Justus-Liebig Jerman yang telah
membantu penulis melakukan penelitian selama di Jerman. Terimakasih kepada
para peternak KPS Bogor, para kolega pengajar dan laboran di Bagian/Laboratorium
Kesehatan Masyarakat Veteriner FKH UGM dan FKH IPB, staf di Laboratorium
Terpadu Ilmu Penyakit Hewan dan Kesehatan Masyarakat Veteriner, yang telah
membantu penelitian ini. Terimakasih kepada drh. Maya Purwanti, M.S., drh.
Nurliana, M.Si, dan drh. Rahmat Setya Adji, M.Si. atas kerjasamanya selama
penelitian. Departemen Pendidikan Nasional yang telah memberikan beasiswa
pendidikan doktor melaui program BPPS dan Deutsche Akademische
Austauschdienst (DAAD) atas beasiswa sandwich kepada penulis. Terimakasih dan penghargaan penulis sampaikan pula kepada almarhum Bapak dan Ibu
Martopratiknyo, Bapak Djohansyah (alm), Ibu Rusimah, drg. Eka Rusmeida dan
Wikasita Najmi Nariswari, kakak-kakak, adik-adik, dan keponakan tercinta atas
dukungan doa, moral, dan material selama ini.
Semoga tulisan ini dapat bermanfaat sebanyak-banyaknya bagi kesejahteraan
peternak khususnya dan masyarakat pada umumnya.
Bogor, 11 November 2008
Widagdo Sri Nugroho
RIWAYAT HIDUP
Penulis adalah anak bungsu dari 7 bersaudara putra Bapak Doellah
Satari Martopratiknyo dan Ibu Sri Kawit Martopratiknyo, dilahirkan di Surakarta
19 Desember 1970. Pendidikan dasar sampai menengah dijalani di Sekolah
Dasar Pangudiluhur Surakarta 1976-1983, Sekolah Menengah Pertama Negeri 1
Surakarta tahun 1983-1986, dan Sekolah Menengah Atas Negeri 3 Surakarta,
1986-1989. Pendidikan dokter hewan pada Fakultas Kedokteran Hewan
Universitas Gadjah Mada diselesaikan tahun 1996. Setelah lulus dari FKH UGM,
bekerja pada satu industri perunggasan multinasional sebagai poultry health
supervisor. Sejak tahun 2000 dipanggil untuk mengabdikan diri sebagai staf
pengajar di Fakultas Kedokteran Hewan Universitas Gadjah Mada. Pada tahun
2000-2003 mendapatkan beasiswa pendidikan pascasarjana Departemen
Pendidikan Nasional untuk melanjutkan pendidikan Magister Pertanian (Strata 2)
pada program Sain Veteriner dengan mengambil konsentrasi Ilmu Kesehatan
Masyarakat Veteriner di Program Pascasarjana Universitas Gadjah Mada. Tahun
2004 kembali mendapat beasiswa pendidikan pascasarjana Departemen
Pendidikan Nasional untuk menempuh pendidikan program Doktor (Strata 3)
pada Program Studi Sain Veteriner, Sekolah Pascasarjana Institut Pertanian
Bogor dengan mengambil konsentrasi Ilmu Kesehatan Masyarakat Veteriner.
Pada tahun 2006 mendapatkan beasiswa dari Deutsche Akademische Austausch Dienst (DAAD) untuk program sandwich ke Universitas Justus–Liebig Jerman, dalam rangka penelitian disertasi ini.
Sejak menjadi siswa hingga mahasiswa terlibat aktif dalam banyak
kegiatan pada organisasi siswa dan mahasiswa. Setelah lulus dokter hewan
bergabung pada organisasi profesi Perhimpunan Dokter Hewan Indonesia
cabang Yogyakarta dan menjadi Sekretaris I pada tahun 2001-2005. Penulis juga
anggota Asosiasi Kesehatan Masyarakat Veteriner Indonesia (Askesmaveti) dan
pernah menjadi Sekretaris Jenderal periode 2002-2006. Beberapa tulisan terkait
topik desertasi ini telah diterbitkan pada beberapa Jurnal Nasional terakreditasi
antara lain Detection of Mycobacterium avium subspecies paratuberculosis in
Formula Milk From Bogor Using PCR IS900 pada Medical Journal of Indonesia
Fakultas Kedokteran Univeristas Indonesia, Deteksi Mycobacterium avium
DAFTAR ISI
Mycobacterium avium subspesies paratuberculosis ... 4
Paratuberkulosis pada hewan ... 9 Penyakit Crohn dan Mycobacterium avium subspesies paratuberculosis ... 12
BAHAN DAN METODE Waktu dan Tempat ... 17
Tahapan Penelitian ... 17
MODIFIKASI MEDIA OGAWA SEBAGAI MEDIA TUMBUH Mycobacterium avium subspesies paratuberculosis Abstrak ……….. 26
Abstract ………. 26
Pendahuluan ……….... 27
Bahan dan Metode ……….. 29
Hasil dan Pembahasan ... 30
Kesimpulan dan Saran ... 36
3
DETEKSI Mycobacterium avium subspesies paratuberculosis PADA SUSU PASTURISASI YANG DIJUAL DI BOGOR
66
DETEKSI Mycobacterium avium subspesies paratuberculosis PADA SUSU FORMULA LANJUTAN YANG DIJUAL DI BOGOR
75
Kesimpulan dan Saran ... 84
PEMBAHASAN UMUM
85 Paratuberkulosis dan Peternakan Rakyat Sapi Perah di Bogor……
Cemaran Mycobacterium avium subspesies paratuberculosis
pada Susu dan Penyakit Crohn ... 88
Potensi Kasus Infeksi Mycobacterium avium subspesies
paratuberculosis dan Kajian Terkait di Masa Mendatang………….. 92
DAFTAR TABEL
Halaman Populasi sapi dan produksi susu nasional ... 1 1
Rataan insidensi kasus CD (per 100000 orang/tahun) selama tahun 1991-1994 di Eropa ... 2
14
Hasil uji kesesuaian media MOM A dan MOM B terhadap HEYMj atas pertumbuhan MAP... 3
32
4 Hasil uji kesesuaian media MOM A dan MOM B terhadap HEYMj
atas pertumbuhan MAV... 32
5 Pertumbuhan bakteri MAP dan MAV pada media HEYMj... 43
6 Hasil lengkap deteksi MAP dari susu dan feses sapi perah di Bogor...
56
7 Asosiasi faktor ternak dengan keberadaan Mycobacterium sp.
pada feses……….. 59
8 Hasl pengujian MAP pada susu pasturisasi di Wilayah Bogor... 71
9 Hasil analisis MAP dengan berbagai metode pada susu formula
5
DAFTAR GAMBAR
Halaman
Tahapan penelitian deteksi Mycobacterium avium subspesies
paratuberculosis pada sapi perah dan produk susu olahan di Bogor.... 1
18
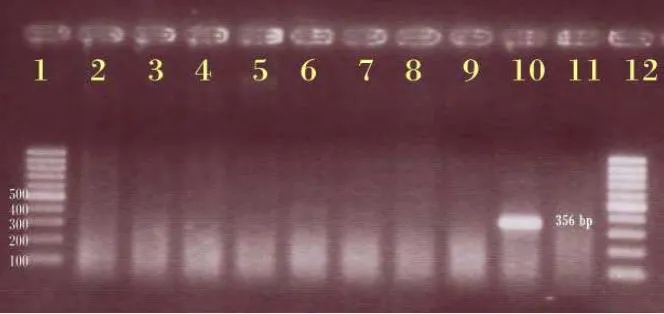
2 Hasil PCR konvensional untuk mengetahui spesifisitas primer IS900... 41
Hasil PCR konvensional untuk mengetahui sensitivitas primer IS900...
3 42
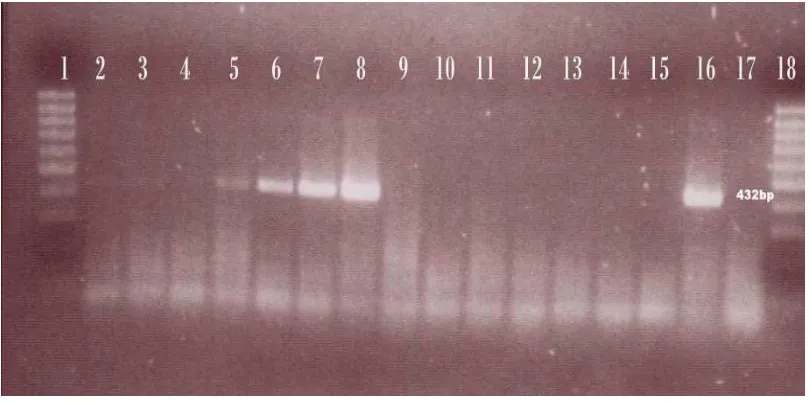
4 Hasil PCR konvensional untuk mengetahui sensitivitas primer F57... 42
5 Isolat Mycobacterium sp. yang tumbuh dari contoh feses pada media
HEYMj dan HEYM... 53
6 Perbandingan Mycobacterium sp. isolat F56 dan MAP referensi... 54
7 Hasil PCR F57 dari ekstraksi langsung contoh susu segar ... 55
8 Hasil PCR F57 dari isolat Mycobacterium sp. yang diperoleh dari
contoh feses... 55
9 Hasil PCR 57 konvensional terhadap contoh susu formula lanjutan... 80
DETEKSI Mycobacterium avium subspesies paratuberculosis
PADA SAPI PERAH, SUSU PASTURISASI, DAN SUSU FORMULA
LANJUTAN DI WILAYAH BOGOR
WIDAGDO SRI NUGROHO
DISERTASI
sebagai salah satu syarat untuk memperoleh gelar
Doktor pada
Program Studi Sain Veteriner
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
7
Judul Disertasi : Deteksi Mycobacterium avium subspesies paratuberculosis Pada Sapi Perah, Susu Pasturisasi, dan Susu Formula Lanjutan di Wilayah Bogor Nama : Widagdo Sri Nugroho
NIM : B063040031
Disetujui
Komisi Pembimbing
Prof. Dr. drh. Mirnawati Sudarwanto Dr. drh. Denny Widaya Lukman, M. Si.
Ketua Anggota
Prof. Dr. Ewald Usleber drh. Surachmi Setiyaningsih, Ph. D. Anggota Anggota
Diketahui
Ketua Program Studi Sain Veteriner Dekan Sekolah Pascasarjana IPB
Tanggal Ujian: 11 November 2008 Tanggal Lulus:
Penguji luar komisi pada ujian tertutup : Dr. drh. I Wayan Teguh Wibawan, M.S.
Penguji luar komisi pada ujian terbuka : Prof. Dr. drh. Bambang Sumiarto, S.U.,M.Sc.
Dr. Ir. Rarah RA. Maheswari, D.E.A.
PENDAHULUAN
Pemenuhan kebutuhan susu nasional dilakukan dengan berbagai cara
seperti meningkatkan populasi sapi perah dan produktivitasnya serta
mendatangkan susu dan hasil olahannya. Upaya peningkatan produksi susu
dalam negeri dilakukan dengan memperbaiki mutu genetik, pembinaan sumber
bibit ternak, pembinaan pakan ternak, pengamanan ternak, dan hasil-hasil ternak
yang meliputi pencegahan, pengendalian, dan pemberantasan penyakit ternak
serta pembinaan usaha peternakan (Sudarwanto 1999). Populasi sapi perah
nasional tahun 2007 tercatat sebanyak 377772 ekor yang menyumbang produksi
susu sebanyak 6368957 ton atau hanya sekitar 25-30% dari kebutuhan nasional,
sehingga masih diperlukan import susu dan produk olahannya. Perkembangan
populasi dan produksi susu segar dalam negeri selama 5 tahun terakhir dapat
dilihat pada Tabel 1.
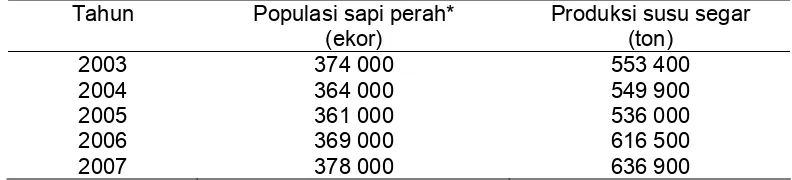
Tabel 1 Populasi sapi dan produksi susu nasional (DitJen Peternakan 2007)
Tahun Populasi sapi perah* Produksi susu segar
(ekor) (ton)
2003 374 000 553 400
2004 364 000 549 900
2005 361 000 536 000
2006 369 000 616 500
Keterangan: * angka dibulatkan ke atas
2007 378 000 636 900
Populasi sapi perah tersebut mayoritas dikelola oleh peternak rakyat yang
rata-rata hanya memiliki sapi produksi 3-5 ekor. Rerata produksi susu yang
dihasilkan setiap sapi masih di bawah 10 liter perhari walaupun menggunakan
bibit sapi perah unggul. Usaha meningkatkan produksi susu dilakukan dengan
menambah jumlah sapi, namun hal ini tidak diikuti peningkatan kualitas
pengelolaan peternakan sehingga hasilnya tidak optimal. Beberapa faktor terkait
dengan pengelolaan adalah sulitnya mendapatkan pakan hijauan, konsentrat
serta lahan yang semakin sempit (Yusdja 2005). Faktor lain yang mempengaruhi
rendahnya produksi susu adalah keberadaan penyakit yang menyerang
peternakan.
Penyakit pada sapi perah dapat dikelompokkan menjadi penyakit tidak
menular, serta penyakit menular primer dan sekunder. Beberapa penyakit pada
epizootica (ngorok), bovine viral disease, infectious bovine rhinotracheitis, dan cacingan masih menjadi permasalahan yang sering dilaporkan terjadi di
Indonesia. Seringkali kasus kronis kurang menjadi perhatian peternak sehingga
tanpa disadari ada kerugian dalam usaha peternakan tersebut akibat produksi
sapi tidak optimal (Sudarwanto 1999; Putra 2006). Salah satu penyakit kronis
yang berpotensi menjadi ancaman bagi usaha peternakan yaitu paratuberkulosis
atau Johne’s disease (JD) yang disebabkan oleh Mycobacterium avium
subspesies paratuberculosis (MAP). Saat ini penyakit tersebut masih belum menjadi perhatian pemerintah maupun peternak. Kasus MAP pernah terdeteksi secara serologis dan dilaporkan pada tahun 1951, 1998, dan terakhir 2004 (Adji
2004), dikhawatirkan kasus ini akan meluas mengingat lingkungan peternakan di
Indonesia memungkinkan tumbuhnya bakteri MAP.
Kejadian diare pada sapi perah seringkali dianggap biasa oleh peternak,
terlebih pada saat pergantian musim atau pakan. Peternak sering tidak
menyadari kejadian diare pada diri atau keluarganya terkait dengan kesehatan
sapi yang dipelihara. Banyak penyakit yang ditandai gejala diare namun belum
banyak yang menghubungkannya dengan infeksi MAP baik pada sapi atau
manusia.
Mycobacterium avium subspesies paratuberculosis diduga kuat berkaitan dengan kasus Crohn’s disease (CD) yaitu penyakit radang kronis saluran pencernaan bagian bawah pada manusia. Paparan MAP pada manusia
umumnya terjadi pada umur 15-24 tahun dan kadang justru terjadi pada keluarga
dengan status sosial baik. Kasus CD juga dikaitkan dengan susu dan produk
olahannya terutama dari ternak yang terinfeksi MAP. Beberapa survei di negara
Eropa menunjukkan tingkat cemaran MAP yang tinggi pada susu segar dan
olahannya seperti susu pasturisasi, susu formula, dan keju (SCAHAW 2000).
Sumber bibit sapi perah dan bahan baku industri susu nasional
didatangkan dari negara-negara penghasil susu khususnya Australia dan New
Zealand. Dua negara tersebut dan beberapa negara Eropa seperti Jerman,
Inggris, dan Swiss tercatat memiliki prevalensi kasus JD cukup tinggi (>15%).
Pengawasan terhadap infeksi MAP pada ternak impor di Indoneseia sudah
dilakukan, namun mengingat masa inkubasinya yang panjang, maka infeksi pada
hewan tidak mudah terdeteksi dengan uji serologis. Bahan baku susu bubuk dan
susu olahan impor selama ini juga belum pernah diperiksa terhadap keberadaan
3
menyebarnya kasus JD pada peternakan nasional serta ancaman penularan
MAP pada masyarakat Indonesia.
Kajian terhadap MAP di Indonesia belum pernah dilakukan, sehingga
penelitian ini benar-benar merupakan sesuatu yang baru di Indonesia. Geografi
Indonesia yang berada di daerah tropis, memungkinkan MAP hidup dan
berkembang di wilayah ini. Dugaan ini didukung fakta masih tingginya kejadian
tuberkulosis (disebabkan Mycobacterium tuberculosis) dan penyakit lepra (disebabkan Mycobacterium leprae) di Indonesia(WHO 2003).
Tantangan lain berkaitan dengan MAP adalah media diagnosis. Isolasi
MAP pada umumnya dilakukan dengan Herrold’s egg yolk media (HEYM) dan
Löwenstein-Jensen (LJ) yang cukup mahal. Di Indonesia, sudah banyak dipakai media Ogawa untuk mengisolasi Mycobacterium tuberculosis di laboratorium-laboratorium rumah sakit paru atau saluran pernafasan. Media ini relatif murah
dan sangat mudah dibuat namun sampai saat ini belum banyak dimodifikasi
sebagai media tumbuh MAP. Penelitian ini juga akan memodifikasi media
Ogawa untuk mengisolasi MAP dengan menambahkan mycobactin ke dalam media. Mycobactin merupakan senyawa yang membantu mikroorganisme menyerap logam yang sangat terbatas ketersediaannya di lingkungan. Bakteri
MAP sangat membutuhkan senyawa mycobactin karena tidak mampu
menghasilkan senyawa ini.
Penelitian ini bertujuan untuk (1) menguji media Ogawa modifikasi sebagai
media isolasi MAP, (2) mendeteksi MAP pada sapi perah dan mengukur asosiasi
tatacara beternak dengan keberadaan bakteri tersebut, serta (3) mendeteksi
MAP pada susu pasturisasi dan susu formula lanjutan.
Hipotesis penelitian ini adalah (1) ditemukan bakteri MAP pada sapi perah
di Bogor dengan prevalensi kasus sebesar 5%, (2) Bakteri MAP dapat ditemukan
pada susu segar, susu pasturisasi, dan susu fromula lanjutan.
Hasil penelitian ini diharapkan dapat menyediakan data yang berharga bagi
para pengambil kebijakan bidang kesehatan hewan dan kesehatan masyarakat.
Rekomendasi dari penelitian ini diharapkan membantu para pemangku
kepentingan industri susu untuk menyikapi dan mengambil langkah pencegahan
kasus JD maupun CD. Hasil lain yang penting adalah diperolehnya media
Mycobacterium avium subspesies paratuberculosis
Pada tahun 1895, Johne dan Frothingham menemukan bakteri tahan asam
yang menyebabkan bentuk atypical tuberculosis pada sapi di Jerman (Griffiths 2003). Pada tahun 1910, bakteri tersebut diberi nama Mycobacterium enteritidis
chronicae pseudotuberculosis bovis johne yang selanjutnya dikelompokkan ke
dalam Mycobacterium aviumcomplex dan terakhir disebut Mycobacterium avium
subspesies paratuberculosis. Bakteri ini merupakan patogen obligat pada mamalia khususnya ruminansia yang menyebabkan radang granulomatosa
saluran pencernaan yang dikenal sebagai paratuberkulosis atau Johne’s Disease
(JD) (SCAHAW 2000).
Morfologi dan Karakter
Mycobacterium avium subspesies paratuberculosis (MAP) adalah bakteri Gram positif, berbentuk batang lurus atau sedikit bengkok dan terkadang
bercabang dengan ukuran 0.2-0.7 X 1.0-10 μm. Dinding sel MAP tersusun dari lapisan lipida kompleks yang tebal. Bakteri ini bersifat aerobik, tidak bergerak
aktif (non-motile) dan tidak berspora (Gallagher & Jenkins 1998; Harris & Barletta 2001). Kemampuan tumbuh Mycobacterium dikenal dua macam yaitu tumbuh cepat (koloni tampak dalam waktu kurang dari 7 hari) dan tumbuh lambat (koloni
baru terlihat setelah 7 hari). Secara umum Mycobacterium memiliki waktu tumbuh 2-60 hari (Holt et al. 1994) namun untuk MAP dapat mencapai 18 bulan untuk isolat lapang (Shanahan 1994). Koloni memiliki permukaan halus atau
kasar, tumbuh pada pada suhu 25-45 °C dengan suhu optimal 39 °C, bakteri ini
juga mampu hidup di dalam makrofag, tahan pada pH 5.5, alkohol dan panas,
membutuhkan senyawa mycobactin untuk mengikat zat besi lingkungan (Griffiths 2003).
Sifat tahan panas MAP berbeda dengan Mycobacterium lainnya. Pasturisasi umumnya mampu mematikan Mycobacterium tuberculosis, M. bovis,
dan lainnya namun hal ini kurang berhasil untuk MAP (Sung et al. 2004). Beberapa penelitian memperlihatkan MAP mampu bertahan pada suhu
pasturisasi low temperature long time (LTLT) 63-63.3 °C selama 30 menit dan
5
dengan protein 65kDa, GroES, antigen α, dan Ag 85B yang dimiliki MAP (El-Zaatari et al. 1995; Sung et al. 2004)
Bakteri umumnya membutuhkan zat besi untuk keperluan metabolisme,
demikian halnya dengan Mycobacterium. Senyawa besi kompleks dikelasi bakteri melalui perantara senyawa siderofor untuk diangkut menembus membran
hingga masuk ke sitoplasma. Dua jenis siderofor yang dikenal yaitu mycobactin
yang larut lemak dan eksokelin (exochelin) yang larut air. Eksokelin merupakan protein bermolekul kecil yang terdapat pada cairan ekstraseluler. Zat besi dalam
tubuh hewan pada umumnya disimpan dalam bentuk ferritin dan molekul transpor yang digunakan adalah transferrin dan lactoferrin. Eksokelin yang dihasilkan Mycobacterium akan mengkelasi zat besi dan membawanya melintasi membran sel. Selanjutnya zat besi diangkut oleh mycobactin masuk ke dalam sel bakteri. Kemampuan menghasilkan eksokelin dan myobactin hanya dimiliki oleh Mycobacteria dan Nocardia sehingga hal ini menjadi faktor penting dalam taksonomi bakteri ini. Pada umumnya Mycobacterium memiliki dua senyawa siderofor tersebut namun MAP dan beberapa strain MAV tidak mampu
menghasilkan mycobactin. Ketergantungan terhadap mycobactin ini menjadi penanda khas untuk MAP meskipun saat ini Mycobacterium avium subspesies
silvaticum dan beberapa MAV juga teridentifikasi memiliki ciri tersebut (Cocito et al. 1994).
Mycobacteriaceae memiliki 4 genus yaitu Corynebacterium,
Mycobacterium, Nocardia, dan Rhodococcus. Spesies Mycobacterium avium
yang termasuk dalam genus Mycobacterium saat ini terbagi menjadi 3 subspesies yaitu Mycobacterium avium subspesies avium, Mycobacterium avium
subspesies silvaticum, dan Mycobacterium avium subspesies partuberculosis. Komposisi basa dari genom masing-masing genus merupakan parameter
taksonomi (Cocito et al. 1994).
Saat ini dipakai metode biofisika (thermal profile atau buoyant density) dan dinyatakan dalam bentuk prosentase guanine+cytosine (G+C) dalam DNA. Komposisi basa (G+C) dari genom Corynebacterium adalah 48-59%,
Rhodococcus 63-73%, Mycobacterium 62-70%, dan Nocardia 64-69%.
Komposisi basa untuk beberapa spesies Mycobacterium antara lain M. leprae
besar dibandingkan spesies lain seperti MAV 3.5X106 bp, M tuberculosis 3.0 X106 sampai 4.2X10 bp, 6 M. leprae 2.0X106 sampai 3.30X10 bp (Harris & 6 Barletta 2001; Cocito et al. 1994).
Deteksi dan Identifikasi MAP
Identifikasi fenotipik MAP dilakukan dengan menggunakan beberapa media
seperti Herrold’s egg yolk medium (HEYM), Modified Dubos’s medium,
Middlebrook 7H9, 7H10, 7H11, 7H12 Bactec medium, dan Löwenstein–Jensen
medium (LJ) (Holt et al. 1994; OIE 2004).
Pada media biakan seperti HEYM, LJ, atau Middlebrook 7H9 agar yang
diperkaya mycobactin J, koloni akan terlhat halus atau kasar. Pada uji biokimia, MAP tidak menghasilkan niasin, peroksidase, nitrat reduktase, urease,
arisulfatase, penisilinase, beta-glukosidase, dan tidak menghidrolisis Tween 80
dalam 10 hari. Beberapa strain menghasilkan sedikit katalase termo resisten dan
semua strain susunan asam mikolak (mycolic acid) dan resisten terhadap
thiophene-2-carboxylic acid hydrazide, dan isoniazid (SCAHAW 2000).
Kelemahan dari metode isolasi adalah keberadaan bakteri yang tidak selalu
dapat ditemukan dalam feses, susu, atau jaringan atau organ. Kelemahan lain
adalah waktu pertumbuhan MAP yang lama yaitu 3-24 minggu, bahkan dapat
mencapai 18 bulan (Shanahan 1994, Griffiths 2003) sehingga metode ini sulit
memberikan keputusan yang cepat.
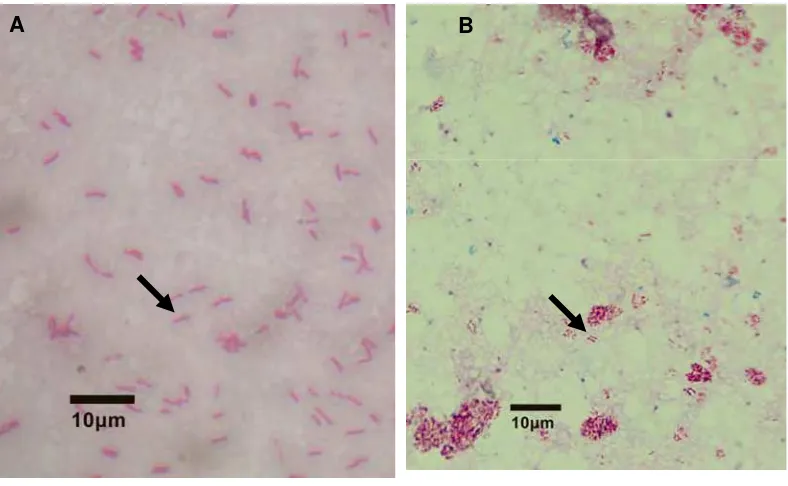
Identifikasi bakteri dapat pula dilakukan dengan mewarnai ulas bakteri
dengan pewarnaan tahah asam Ziehl-Neelsen (ZN). Metode ini dapat dilakukan dari contoh ulas dari organ terutama kelenjar limfoid saluran pencernaan/usus,
feses, maupun susu penderita. Pada pewarnaan ZN ini MAP akan terlihat
berbentuk batang dan berwarna merah (OIE 2004). Bakteri MAP sulit dibedakan
dengan Mycobacterium sp. lainnya dengan teknik pewarnaan karena ukuranya yang tidak jauh berbeda.
Deteksi terhadap MAP berdasarkan uji serologis dilakukan dengan
complement fixation test (CFT), enzyme linked immunosorrbent assay (ELISA), agar gel immunodiffusion (AGID). Reaksi tanggap kebal humoral mulai dapat terdeteksi pada fase pre-klinis tanpa disertai pengeluaran bakteri di dalam
fesesnya (McKenna et al. 2005; Roussel et al. 2007). McKenna et al. (2005) menjelaskan bahwa hasil uji ELISA berkaitan erat dengan fase perkembangan
7
sangat rendah dan akan meningkat pada fase klinis seiring reaksi tanggap kebal
inang. Pendapat Osterstock et al. (2007) sejalan dengan Roussel et al. (2007) yang menyebutkan bahwa spesifisitas ELISA relatif tinggi yaitu 91-95% dengan
melakukan absorbsi serum menggunakan M. phlei. Prosedur ini cukup baik meskipun masih memungkinkan terjadinya reaksi silang dengan MAC,
khususnya M. intraselular sehingga dihasilkan reaksi positif palsu. Hal ini seringkali menyebabkan hasil uji serologis tidak sejalan dengan hasil isolasi
bakteri dari feses.
Identifikasi genotipik merupakan satu metode yang sangat membantu
mengenali MAP dengan cepat. Insertion sequence (IS) merupakan elemen genetik yang bergerak dan hanya mengandung gen-gen terkait fungsi insersi.
Lokasi IS berada di dalam struktur gen yang dapat menyebabkan terjadinya
mutasi insersional (Lida et al. 1983 diacu oleh Green et al. 1989). Pengelompokan IS dilakukan berdasarkan pada kemiripan dan perbedaan
struktur, organisasi, dan nukleotida serta protein sekuen terkait. Letak IS pada
lokasi tertentu yang stabil dalam kromosom menjadikan mereka sebagai
penanda dalam kajian restriction fragment length polymorphism (RFLP) untuk penentuan spesies dan kajian epidemiologi. Struktur IS tersusun dari
transposon, dalam kajian lebih lanjut IS ini berkaitan dengan fungsi patogenik
dan virulensi agen. Sejak dipublikasikan tahun 1989 penelitian terkait IS sangat
banyak dan hingga tahun 1998 telah diidentifikasi sekitara 500 IS (Mahillon &
Chandler 1998).
Penggunaan polymerase chain reaction (PCR) sebagai salah satu metode diagnosis sangat membantu dalam penelitian tentang MAP. Green et al. (1989) berhasil mendapatkan sekuen elemen DNA untuk diagnosis MAP yang kemudian
dikenal sebagai insertion sequence (IS) 900. Sekuen tersebut dikelompokkan dalam keluarga IS110, dengan ukuran 1451 bp dan komposisi G+C sebesar
66%. Insertion sequence ini memiliki mayor open reading frames (ORF) sejumlah 1197 nukleotida yang diprediksi mengkode 399 protein dan dapat
mengkopi 15-20 genom MAP. Sumber IS900 tidak diketahui tetapi diduga dibawa
oleh mycobacteriophage. Pohon genetik IS900 menunjukkan bahwa MAP masuk dalam kelompok Mycobacterium avium. Keunikan perangkat IS900 ini adalah tidak memiliki terminal inverted dan direct repeats. Insertion sequence
900 memiliki daya pembeda yang tinggi untuk mengidentifikasi MAP secara tepat
Perkembangan selanjutnya primer IS900 yang spesifik MAP ini digunakan
sebagai rujukan identifikasi MAP baik untuk konfirmasi isolat maupun diagnosis
cepat. Penggunaan primer IS900 juga digunakan untuk mendeteksi MAP
langsung pada beberapa contoh seperti susu segar, susu pasturisasi, dan keju
(Grant et al. 1998; Giese & Ahrens 2000; Pillai & Jayarao 2002), feses (Motiwala
et al. 2004; Strickland et al. 2005), maupun biopsi jaringan (Taddei et al. 2004; Hermon-Taylor et al. 1998). Sekuen genom lengkap MAP berhasil dipetakan oleh Li et al. (2005) sehingga akan dapat dijadikan rujukan dalam pengembangan metode deteksi dan produk biologis untuk pengendalian penyakit
JD di masa mendatang.
Harris dan Barletta (2001) menyatakan bahwa primer IS900 yang
dirancang Vary et al. (1990) memiliki kelemahan yaitu adanya 229 wilayah amplifikasi yang tumpang tindih dengan IS1626 dari M. avium sehingga sering diperoleh hasil positif palsu. Cousins et al. (1999) juga mendapatkan hasil amplifikasi dari Mycobacterium lingkungan non-MAP menggunakan primer ini. Secara tegas Semret et al. (2006) menyatakan bahwa amplifikasi dari IS900 tidak cukup mewakili MAP. Kelemahan-kelemahan ini diidentifikasi oleh Bull et
al. (2000) dan kemudian mengembangkan beberapa variasi IS900 yang dikenal sebagai multiplex PCR of IS900 loci (MPIL) untuk memperbaiki kinerja primer ini. Variasi MPIL didasarkan pada sekuen genom DNA dan didapatkan 14 variasi
primer IS900 yang berbeda pada genom MAP. Temuan ini diharapkan mampu
mengurangi hasil positif palsu.
Selain pengembangan IS900 sebagai primer MAP, beberapa peneliti juga
mengembangkan primer lain seperti yang dilakukan Cocito et al. (1994) yang mengembangkan F57. Primer ini dikloning dari segmen DNA MAP dalam satu
vektor transkripsi. Klon F57 rekombinan terbukti spesifik untuk identifikasi agen
JD. Sekuen F57 menghasilkan satu segmen 620 bp dengan kandungan G+C
sebesar 58%. Primer F57 mampu mengidentifikasi MAP dengan baik dari
jaringan hewan penderita JD yang telah diparafin (Coetsier et al. 2000). Pengembangan F57 sebagai primer identifikasi MAP dikembangkan oleh
Vansnick et al. (2004) dengan target gen F57 yang memiliki panjang 424-432 bp. Kinerja primer F57 dengan metode nested PCR sangat baik dengan kemampuan
deteksi hingga 1 CFU per PCR dan daya pembeda yang sangat baik.
Penggunaan F57 untuk deteksi MAP pada susu dengan metode RT-PCR juga
9
(Tasara & Stephan 2005). Berdasarkan berbagai hasil penelitian di atas para
peneliti menganjurkan penggunaan metode deteksi lebih dari 1 macam termasuk
pada analisis molekular dengan menggunakan setidaknya 2 primer.
Paratuberkulosis pada Hewan
Paratuberkulosis pada hewan terutama terjadi pada ruminansia seperti
sapi, domba, dan kambing namun dapat terjadi pula pada satwa liar seperti
bison, kijang, kelinci, dan kadang ditemukan pula pada burung-burung liar meski
tidak menimbulkan gejala klinis (Cocito et al. 1994; Buergelt et al. 2000; Acha & Szyfres 2003). Hewan penderita paratuberkulosis akan menunjukkan gejala
sakit 2-5 tahun setelah infeksi. Penderita paratuberkulosis subklinis akan
merugikan peternak karena penurunan produksi susu dan rendahnya kinerja
reproduksi. Kerugian industri peternakan sapi perah di Amerika Serikat karena
penyakit ini diperkirakan mencapai US $ 1.5 milyar per tahun (Stabel 1996).
Epidemiologi dan Penyebaran Penyakit
Sejak dikenal pertamakali, kasus JD telah diketahui tersebar di berbagai
tempat. Pada tahun 1934 sebuah penelitian di Perancis memperlihatkan bahwa
prevalensi kasus JD hanya 0.8%. Berbagai survei yang dilakukan pada
peternakan sapi di negara-negara Eropa memperlihatkan prevalensi JD yang
bervariasi seperti di Inggris sekitar tahun 1950 mencapai 11-17%, di Denmark
pada tahun 1965 sebesar 2.3% dan meningkat pada tahun 1972 yang mencapai
9.8%. Di Amerika Serikat survei tahun 1980 memperlihatkan tingkat penyakit
pada peternakan sapi sebesar 1.2% (SCAHAW 2000). Laporan tahun 1997
menunjukkan peningkatan prevalensi JD di Amerika yang mencapai 21.6% dan
40% dari peternakan yang terinfeksi tersebut memiliki lebih dari 300 sapi
penderita (Gonda et al. 2006).
Tingginya prevalensi menunjukkan penyakit ini sulit dikendalikan. Faktor
lingkungan sangat berperan dalam kelangsungan penyakit ini. Raizman et al. (2004) melakukan penelitian untuk mengetahui distribusi MAP di lingkungan
peternakan sapi perah di Minnesota. Hasil penelitian ini memperlihatkan
prevalensi peternakan yang tercemar MAP mencapai 53-73%, sedangkan
distribusi keberadaan bakteri di peternakan terdapat pada lokasi–lokasi seperti
pada gang/jalan ternak 77%, penampungan pupuk/kotoran 68%, lokasi
3%. Pergantian musim terbukti tidak mempengaruhi terjadinya kasus JD pada
peternakan (Strickland et al. 2005). Hal ini sejalan dengan temuan Whan et al. (2005) yang sepanjang musim dapat menemukan MAP dari air yang tidak diberi
perlakuan (untreated) di Irlandia Utara. Tingginya kejadian juga diduga karena keberadaan kelinci liar sebagai vektor biologis MAP yang menularkannya ke
peternakan sapi perah dan hewan liar lain (Judge et al. 2006).
Patogenesis Paratuberkulosis
Mycobacterium avium subspesies paratuberculosis menyebabkan Johnes disease (JD) yaitu penyakit radang granulomatosa usus yang bersifat kronis dan sulit disembuhkan pada hewan. Setelah tertelan, bakteri ini akan segera
menembus permukaan mukosa saluran pencernaan dan difagosit oleh makrofag.
Kemampuan MAP bertahan di dalam makrofag merupakan suatu kelebihan
bakteri ini dalam mengganggu inang dan bakteri mampu bertahan dan terlindung
dari mekanisme kekebalan humoral (Stabel et al. 1998).
Hewan mammalia secara aktif akan membatasi suplai zat besi kepada
bakteri patogen. Fungsi sitokin pada makrofag diduga untuk membatasi secara
aktif konsentrasi besi di dalam sel sehingga perkembangan bakteri terhambat.
Makrofag teraktivasi akan menurunkan kerja reseptor transferin dan mengurangi
konsentrasi zat besi. Bakteri Mycobacterium menghasilkan siderofor mycobactin
larut lemak dan siderofor eksokelin larut air dalam rangka mencari zat besi yang
terbatas jumlahnya dalam sel inang. Kedua siderofor ini sangat berkaitan dengan
patogenisitas Mycobacterium dan menjadi perangkat penting bakteri dalam bertahan dan bereplikasi di dalam makrofag (Harris & Barletta 2001).
Lesi granulomatosa mulai muncul pada lokasi peyer patches. Luka ini akan bertahan dalam keadaan laten untuk waktu yang lama. Pada perkembangan
infeksi selanjutnya dari peyer patche akan menyebar ke seluruh usus dan menimbulkan radang granulomatosa pada usus dan kondisi paling ekstrim
adalah terbentuknya lubang (perforasi) pada usus. Lesi-lesi ini jelas akan
mengganggu absorbsi makanan. Hal ini akan berakibat pada kondisi umum
hewan sehingga akan memperlihatkan gejala-gejala klinis yang akan muncul
sekitar 2-5 tahun sejak infeksi bakteri ke dalam inang (SCAHAW 2000).
Gejala Klinis
Pedet yang terinfeksi MAP seringkali tidak memperlihatkan gejala klinis
11
8
kolostrum yang tercemar MAP. Jumlah bakteri sebanyak 5x10 CFU mampu
menimbulkan penyakit pada kambing umur 3 bulan dan gejala klinis muncul
setelah 11 bulan kemudian (Begg et al. 2005).
Perkembangan penyakit paratuberkulosis dibagi menjadi 3 stadium.
Stadium 1 adalah stadium subklinik, hewan tidak menunjukkan gejala klinis,
tanggap kebal seluler tinggi tetapi tidak ada pengeluaran MAP dalam feses.
Pada stadium 2, hewan dalam kondisi subklinik dengan tanggap kebal seluler
dan humoral yang sedang. Fase ini juga ditandai dengan peningkatan
konsentrasi MAP pada mukosa usus dan ruang usus. Stadium 3 (fase terminal)
merupakan fase hewan menunjukkan gejala klinik yang ditandai adanya diare
kronis, gejala infeksi umum seperti emasiasi, penurunan produksi susu, edema
difus, anemia, dan infertilitas yang merupakan tanda akhir yang dominan (Cocito
et al. 1994). Aborsi dan alopesia merupakan tanda yang terlihat pada stadium lanjut dan hewan mati dengan status kaheksia. Pada fase klinis jumlah bakteri
yang dikeluarkan melalui feses dapat mencapai 1010 CFU/g feses. Distribusi
MAPselain pada organ pencernaan juga dapat terdapat pada organ reproduksi
hewan jantan dan betina terinfeksi. Organisme ini dapat diisolasi dari fetus yang
berasal dari sapi penderita meskipun penularan melalui intrauteri belum dapat
dibuktikan (Stabel 1998).
Metode Diagnosis
Organisasi Kesehatan Hewan Dunia (Office International des
Epizootica/OIE) telah mengeluarkan panduan diagnosis paratuberkulosis.
Diagnosis dapat dilakukan dengan identifikasi agen, uji serologis, dan test of
cell-mediated immunity. Identifikasi agen dapat dilakukan dengan melakukan
nekropsi, pemeriksaan mikroskopik, biakan bakteri, dan pelacakan DNA.
Pengujian serologi dapat dilakukan dengan complement fixation test, ELISA, dan AGID sedangkan untuk test of cell-mediated immunity dilakukan dengan gamma interferon assay dan delayed type hypersensitivity (OIE 2004).
Diagnosis Paratuberkulosis berdasarkan gejala klinis cukup sulit dilakukan
karena perjalanan penyakit yang cukup lama. Pada umumnya gejala klinis
terlihat pada saat hewan sudah dalam kondisi terinfeksi parah. Cocito et al.
(1994) menjelaskan bahwa stadium perkembangan penyakit berpengaruh
terhadap metode diagnosis klinik maupun laboratorik.
Diagnosis laboratorik MAP sampai saat ini masih dikembangkan untuk
dilakukan adalah dengan enzyme-linked immunosorbent assay (ELISA). Variasi sensitivitas uji ELISA sangat tergantung pada fase respon sistem kekebalan
inang dan reaksi silang bila inang terinfeksi M. avium complex (MAC). Sensitivitas ELISA untuk mendeteksi MAP ini bervariasi 42-88% sehingga
seringkali diperoleh hasil yang berbeda antara uji ini dengan uji isolasi (Collins
2002; McKenna et al. 2005).
Diagnosis MAP dapat dilakukan berdasarkan uji cell-mediated immunity yaitu dengan gamma interferon assay dan delayed-typed hipersensitivity test
(DTH). Uji DTH menggunakan purified protein derivative (PPD) johnin dan akan menghasilkan rekasi penebalan pada kulit setelah 72 jam diinjeksi intradermal
dengan PPD johnin (OIE 2004).
Primer IS900 menjadi satu alat deteksi molekuler yang cukup banyak
membantu diagnosis MAP. Beberapa hasil penelitian menggunakan primer IS900
memperlihatkan adanya positif palsu. Salah satu sebabnya adalah tingkat
homologi DNA MAP dengan MAC yang mencapai 97% (Bannantine et al. 2002). Pengembangan primer untuk deteksi MAP kemudian dilakukan untuk
mendapatkan tingkat akurasi yang tinggi. Beberapa primer kemudian ditemukan
seperti F57 (Cocito et al. 1994), ISMap02 (Stabel & Bannantine 2005), dan ISMav2 (Wells et al. 2006) namun banyak peneliti tetap merekomendasikan untuk mengkombinasikannya dengan primer IS900. Penelitian Vansnick et al. (2004) menunjukkan bahwa dari 53 isolat Mycobacterium non MAP tidak satupun yang teramplifikasi dengan primer ini. Primer IS900 mampu mendeteksi MAP
sampai 1 CFU per PCR namun demikian dalam beberapa penelitian diperoleh
beberapa hasil yang bervariasi tergantung dari jenis sampel yang diuji. Stabel et al. (2004) dengan metode konvensional mampu mendeteksi 12 dari 165 sampel feses yang mengandung MAP 1 CFU/g. Metode real-time PCR (RT-PCR) yang dilakukan O’Mahony dan Hill (2004) mampu mendeteksi MAP dalam susu segar
hingga konsentrasi <100 CFU/ml. Kinerja primer IS900 mendeteksi MAP sangat
baik dan direkomendasikan oleh OIE untuk digunakan sebagai salah satu
metode identifikasi (OIE 2004).
Penyakit Crohn dan Mycobacterium avium subspesies paratuberculosis
Penyakit Crohn (Crohn’s disease/CD) adalah penyakit yang dideskripsikan oleh Crohn, Ginzberg, dan Oppenheimer pada tahun 1932 sebagai peradangan
13
semacam ini sebenarnya telah diketahui sejak abad 16 namun baru Crohn dan
teman-temannya yang menjelaskan secara spesifik (Chiodini 1989). Di Eropa
insidensi kasus CD sebesar 5.6 kasus per 100000 orang per tahun dan hingga
tahun 2000 diperkirakan telah mencapai 200000 penderita. Kerugian ekonomi
yang ditimbulkan cukup besar seperti yang dialami pemerintah Swedia yang
harus mengeluarkan dana € 40 juta (sekitar 560 miliar rupiah) untuk pengobatan
dan penanganan kasus CD pada tahun 1994 (SCAHAW 2000).
Etiologi Crohn’s Disease
Penyebab CD secara pasti hingga saat ini masih dalam perdebatan.
Chamberlin dan Naser (2006) menjelaskan ada tiga teori penyebab CD yaitu
teori autoimun(immune dysregulation theory), teori defisiensi kekebalan (immune deficiency), dan teori mikobakterial (mycobacterial theory). Teori autoimun menjelaskan bahwa terjadinya CD sebagai akibat ketidaktepatan aktivasi sistem
kekebalan mukosa usus secara terus menerus yang dipicu oleh keberadaan flora
normal di dalam lumen. Teori defisiensi kekebalan menekankan timbulnya CD
karena cacat bawaan sistem kekebalan yang menyebabkan tanggap kebal yang
berlebihan dengan penyebab yang belum teridentifikasi. Teori mikobakterial
mengungkapkan bahwa kejadian CD merupakan hasil interaksi Mycobacterium
avium subspesies paratuberculosis dengan sistem kekebalan tubuh inang.
Dugaan bakteri MAP sebagai penyebab CD muncul saat Dalziel pada
tahun 1913 menemukan perubahan patologi usus pasiennya berupa keradangan
granulomatosa yang sangat mirip dengan perubahan patologis usus sapi
penderita JD. Saat itu Dalziel belum berhasil mengisolasi bakteri tahan asam
seperti halnya pada penderita JD. Semula penyakit ini dikenal hanya terjadi
pada ileum, namun tahun 1960 Lockart-Mummery dan Morson mengidentifikasi
adanya radang pada kolon dan membentuk granuloma, karena daerah radang
yang lebih banyak pada usus besar maka sering juga disebut sebagai chronic inflamatory bowels disease (IBD)(SCAHAW 2000).
Temuan bakteri MAP pada darah pasien CD (Naser et al. 2004) menguatkan dugaan MAP sebagai penyebab CD. Collins et al. (2000) melakukan penelitian yang menggunakan beberapa alat uji untuk mengidentifikasi adanya
infeksi MAP pada penderita inflammatory bowel disease (IBD) dan menyimpulkan adanya keterkaitan kuat antara MAP dan CD. Pendapat tersebut
menimbulkan radang kronis yang terjadi pada penderita CD dan hal ini secara
jelas membuktikan hubungan sebab akibat antara MAP dengan CD.
Epidemiologi dan Distribusi Penyakit Crohn
Pada awal kasus CD dikenali, kejadian penyakit banyak dialami oleh
masyarakat Eropa Utara dan etnis Anglo-Saxon dibandingkan dengan
masyarakat Eropa Selatan, Asia, dan Afrika. Perkembangan selanjutnya
keberadaan imigran Asia menjadi pembawa penyakit ini ke daerah Asia.
Kajian-kajian epidemiologi CD cukup banyak dilakukan di Eropa dan Amerika namun
sebagian besar berupa kajian retrospektif yang datanya didasarkan dari
laporan-laporan dan kurang didukung identifikasi etiologi agen secara akurat.
Tabel 2 Rataan insidensi kasus CD (per 100000 orang/tahun) selama tahun 1991-1994 di Eropa (SCAHAW 2000)
Pusat Kajian Laki-laki Perempuan Total Daerah utara
Kajian prospektif mulai dilakukan tahun 1991 hingga 1994 oleh para
15
untuk memperoleh gambaran dan insidensi kasus secara lebih tepat. Hasil
kajian tersebut memperlihatkan bahwa jenis kelamin tidak berpengaruh terhadap
peluang kejadian (Shivananda et al. diacu oleh SCAHAW 2000) dan dapat dilihat pada Tabel 2.
Tabel 2 menunjukkan kasus CD yang telah menyebar di Eropa dengan
insidensi kasus di setiap daerah di atas 5 kasus per 100000 orang per tahun.
Belanda sebagai negara pengekspor susu dan produk olahannya memiliki
insidensi CD cukup tinggi (9.1). Laporan Hruska et al. (2005) menyebutkan angka insidensi CD semakin meningkat 50-150 kasus per 100000 orang per
tahun dan di negara yang memiliki kasus paratuberkulosis pada sapi perah,
kambing, dan ternak lainya juga memiliki prevalensi CD yang tinggi.
Potensi MAP Sebagai Foodborne Disease
Kemiripan perubahan patologi organ penderita CD dengan JD pada sapi
menimbulkan dugaan potensi penularan MAP dari hewan ke manusia. Media
penularan yang paling dicurigai adalah susu sapi dan produk olahannya seperti
susu pasturisasi, keju, dan susu formula. Banyak sekali informasi keberadaan
MAP dalam komoditi tersebut. Taylor et al. (1981) berhasil mengisolasi MAP dari susu segar yang dihasilkan sapi penderita JD klinis, namun Sweeney et al. (1992) mendapatkan 9 isolat MAP dari susu segar sapi penderita JD subklinis.
Pengolahan susu dengan pasturisasi teryata belum mampu memusnahkan
MAP seperti pada Listeria monocytogenes maupun Mycobacterium bovis (Collins 1996). Millar et al. (1996) menggunakan metode PCR IS900 mendeteksi MAP pada susu high temperature short time (HTST) sebanyak 7% dari 312 contoh yang diuji. Temuan MAP pada susu HTST juga ditemukan di Inggris (Grant et al. 2002a), di Irlandia (O’Reilly et al. 2004) dan Republik Ceska (Ayele et al. 2005). Produk susu olahan seperti susu formula dan keju juga masih dapat
terkontaminasi MAP.
Hruska et al. (2005) berhasil mendeteksi bakteri tersebut dengan metode PCR pada susu formula bayi,sedangkan penelitian Akineden et al. (2006) selain mendeteksi dengan PCR juga mendapatkan isolat MAP dari makanan bayi.
Donaghy et al. (2004) secara laboratorik memperlihatkan bahwa MAP masih dapat hidup pada keju cheddar, demikian juga temuan Ikonomopoulos et al. (2005) yang mendeteksi keberadaan MAP pada keju yang dijual di ritel Yunani
Banyaknya data memperlihatkan bahwa MAP memiliki kemampuan
bertahan dalam perlakuan panas. Chiodini dan Hermon-Taylor (1993)
melaporkan bahwa MAP lebih tahan panas dibandingkan dengan M. bovis. Pada skala laboratorium, sebanyak 3-10% dari MAP yang dikotaminasikan pada susu
segar dengan dosis 104 CFU/ml mampu bertahan setelah dipanaskan pada suhu
71.7 oC selama 15 detik (HTST). Sung dan Collins (1998) mendapatkan waktu
yang dibutuhkan untuk menurunkan 1 log 10 bakteri (nilai D) MAP pada suhu 71
o o
C adalah 11.67 detik, sedangkan untuk suhu 68 C adalah 21.8 detik, pada suhu
65 oC adalah 47.8 detik dan 62 oC adalah 228.8 detik. Penelitian Sung dan
Collins (1998) tersebut juga memperlihatkan bahwa MAP akan tetap dapat
ditemukan dalam susu meskipun telah dipasturisasi apabila pada susu
mentahnya mengandung lebih dari 101 sel/ml.
Sung et al. (2004) berhasil mengidentifikasi beberapa protein dari bakteri MAP yang diduga mengendalikan kemampuan tahan panas. Beberapa protein
tersebut adalah GroES, Ag85, dan antigen α. Protein GroES yang juga dikenal sebagai heat shock protein bertanggungjawab melindungi sel dari panas yang dengan cepat memperbaiki denaturasi atau kesalahan pelipatan protein. Antigen
BAHAN DAN METODE
Waktu dan Tempat Penelitian
Penelitian dilakukan dari Agustus 2006 sampai Mei 2008. Contoh susu
dan feses diambil dari sapi-sapi peternakan rakyat yang tergabung dalam
Koperasi Produksi Susu dan Usaha Peternakan (KPS) di perkampungan
peternakan sapi perah Cibungbulang Bogor. Contoh susu pasturisasi dan susu
formula lanjutan dibeli di supermarket di wilayah Bogor.
Pemeriksaan contoh dilakukan di Laboratorium Terpadu Departemen Ilmu
Penyakit Hewan dan Kesehatan Masyarakat Veteriner Fakultas Kedokteran
Hewan Institut Pertanian Bogor dan Laboratorium Kesehatan Susu Fakultas
Kedokteran Hewan Universitas Justus-Liebig Jerman.
Tahapan Penelitian
Penelitian ini pada prisipnya terdiri dua tahap yaitu tahap verifikasi metode
dan alat diagnostik, dan tahap pengujian contoh. Tahap verifikasi metode dan
alat diagnostik yaitu menguji kemampuan media isolasi yaitu Herrold’s egg yolk
medium diperkaya mycobactin J (HEYMj) dan Ogawa modifikasi serta primer
IS900 dan F57 untuk PCR konvensional. Tahap pengujian contoh dilakukan
setelah diketahui batas kemampuan deteksi metode dan alat diagnostik yang
akan digunakan. Contoh yang diuji meliputi susu segar, feses, dan contoh susu
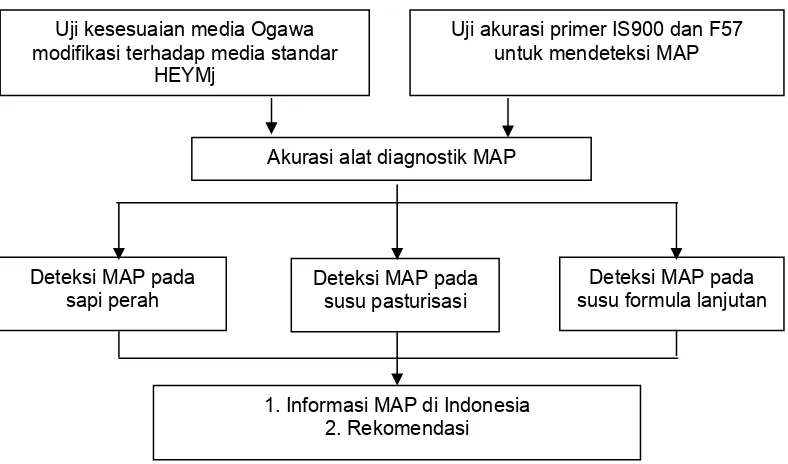
olahan yaitu susu pasturisasi dan susu formula lanjutan. Tahapan penelitian
dapat dilihat pada Gambar 1.
Modifikasi Media Ogawa Sebagai Media Tumbuh Mycobacterium avium
subspesies paratuberculosis
Penelitian ini bertujuan untuk menguji media Ogawa yang dimodifikasi
sebagai media tumbuh Mycobacterium avium subspesies paratuberculosis. Penelitian dilakukan dengan membandingkan kemampuan antara media Ogawa
modifikasi terhadap media standar sebagai media tumbuh MAP. Media
pertumbuhan MAP terdiri dari 3 kelompok yaitu Herrold’s egg yolk medium yang diperkaya mycobactin J (HEYMj), Ogawa tanpa mycobactin J (MOM A), Ogawa dengan mycobactin J (MOM B). Inokulat penguji media yang digunakan adalah
Uji kesesuaian media Ogawa modifikasi terhadap media standar
HEYMj
Uji akurasi primer IS900 dan F57 untuk mendeteksi MAP
Deteksi MAP pada sapi perah
Deteksi MAP pada susu pasturisasi
Deteksi MAP pada susu formula lanjutan
1. Informasi MAP di Indonesia 2. Rekomendasi Akurasi alat diagnostik MAP
Gambar 1 Tahapan penelitian deteksi Mycobacterium avium subspesies
paratuberculosis pada sapi perah dan produk susu olahan di Bogor.
Media standar yang digunakan adalah HEYMj siap pakai yang sudah
diperkaya mycobactin J, vancomisin dan asam nalidiksik produksi BBL Becton Dickinson (Germany).
Modifikasi media Ogawa A (MOM A) yang mengandung 9.0 g pepton
kasein (pancreatic) (Merck USA), 2.7 g ekstrak daging (Merck USA), 9.0 g
KH2PO4 (Sigma USA), 3.0 g sodium glutamat (Ubena Gewürzvetrieb Germany),
18.0 ml glycerol (Sigma USA), 18.0 ml malachite green 2% (Merck USA ), 16.0 g
agar-agar (Merck USA), 100.0 ml emulsi kuning telur (Oxoid England), 864.0 ml
aquades (pH akhir 5.7).
Modifikasi media Ogawa B (MOM B) dengan komposisi seperti MOM A
dan ditambahkan 0.002 g mycobactin J (Synbiotics France).
Penyiapan stok bakteri dilakukan dengan mengambil satu ose bakteri
kemudian dilarutkan dalam 1.5 ml PBS Tween-20 0.05% (Sigma USA) dalam
tabung Eppendorf. Suspensi dihomogenkan dengan vorteks selanjutnya
digunakan untuk membuat stok bakteri 107 sel/ml. Stok bakteri tersebut dibuat
dengan mengukur kepekatan suspensi dalam tabung kuvet menggunakan
spektrofotometer (Shimadzu UV-1601) pada panjang gelombang 660 nM dan
tingkat adsorbensi 10%. Pada skala tersebut maka suspensi setara dengan
19
Pengenceran seri dibuat dengan mengambil 1 ml larutan stok bakteri dan
dimasukkan ke dalam 9 ml PBS Tween-20 0.05% kemudian dihomogenkan.
Konsentrasi bakteri pada larutan baru setara dengan 106 sel/ml. Pengenceran
dilanjutkan dengan mengambil 1 ml larutan dari tabung pengenceran
sebelumnya (106 sel/ml) dan masukkan ke dalam 9 ml PBS Tween dan tahapan
diulang sampai diperoleh larutan dengan konsentrasi bakteri setara 100 sel/ml.
0 6
sel/ml - 10
Inokulasi dilakukan dari setiap pengenceran 10 sel/ml dengan
dosis 250 μl. Masing-masing pengenceran diinokulasikan secara duplo (dua ulangan) pada setiap media tumbuh HEYMj, MOM A, dan MOM B.
Kesesuaian media Ogawa dengan media standar (uji Kappa) dianalsis
menggunakan perangkat lunak statistix® for windows (Analytical Software 2000).
Akurasi Primer IS900 dan F57 Untuk Mendeteksi Mycobacterium avium
subspesies paratuberculosis dengan Metode PCR Konvensional
Penelitian ini bertujuan untuk mengetahui akurasi primer IS900 dan primer
F57 dalam mendeteksi bakteri Mycobacterium avium subspesies
paratuberculosis.
Primer yang digunakan yaitu IS900 dan F57. Susunan oligonukleotida
IS900 seperti didiskripsikan oleh Bull et al. (2003) yaitu TJ1 (forward) 5’-GCT GAT CGC CTT GCT CAT-3’ dan TJ2 (reverse) 5’-CGG GAG TTT GGT AGC
CAG TA-3’). Oligonukleotida primer F57 mengacu pada Vansnick et al. (2004) yaitu F57 (forward) 5’-CCT GTC TAA TTC GAT CAC GGA CTA GA-3’ dan R57
(reverse) 5’-TCA GCT ATT GGT GTA CCG AAT GT-3’ ).
Sediaan bakteri yang digunakan adalah Mycobacterium avium subspesies
paratuberculosis (442) dan Mycobacterium avium subspesies avium (J14),
Escherichia coli, Listeria ivanovii, Pseudomonas aeruginosa, Streptococcus agalactiae, Klebsiella pneumoniea, Staphylococcus hyicus, Streptococcus infatis, Listeria monocytogenes yang telah dikarakterisasi, milik Laboratorium Kesehatan Susu Universitas Justus-Liebeig, Jerman.
Pengukuran sensitivitas primer IS900 dan F57 terhadap MAP dilakukan
dengan menggunakan pengeceran seri seperti yang dilakukan pada penelitian di
atas. Bakteri dari setiap pengeceran dari 10 sel/ml hingga 10 sel/ml kemudian 0 6
diekstraksi.
Pengujian spesifisitas primer IS900 dan F57 dilakukan dengan
menggunakan seluruh sediaan bakteri di atas. Satu ose bakteri diambil dari
Germany) dalam tabung Eppendorf dan dihomogenkan. Suspensi dari setiap
bakteri selanjutnya diekstraksi.
Ekstraksi DNA dilakukan dengan mengambil 1000 µl suspensi setiap
sediaan di atas baik untuk uji sensitivitas maupun uji spesifisitas diambil dan
dimasukkan ke dalam tabung Eppendorf 2 ml. Suspensi kemudian disentrifus
pada kecepatan 13300 X g selama 30 menit. Supernatan dibuang sebanyak 950
µl dan pelet ditambahkan larutan penyangga TE 180 µl kemudian dihomogenkan
dan diinkubasi pada suhu 37 °C selama 1 jam. Suspensi dipanaskan pada
penangas air dengan suhu 100 °C selama 10 menit kemudian setelah
didinginkan, ditambahkan 30 µl proteinase K (Qiagen, Germany) dan 200 µl AL
Buffer (Qiagen, Germany). Suspensi dihomogenkan dan diinkubasi pada suhu
56 °C selama 2 jam. Tahapan selanjutnya mengikuti prosedur dari produsen
DNeasy® Tissue Kit (Qiagen, Germany).
Amplifikasi menggunakan dua primer yaitu IS900 (TJ1/TJ2) dan F57
(F57/R57). Amplifikasi dilakukan untuk masing-masing primer dengan formulasi
yang sama. Formulasi untuk amplifikasi PCR masing-masing primer yaitu 50 µl
larutan reaksi yang tersusun dari1.5 µl masing-masing primer (10 pmol/µl), 1.5
µl dNTP-mix (10 mmol) (MBI Fermentas, Germany), 5 µl GeneAmp 10x PCR
Gold Buffer (150 mM Tris-HCL, 500 mM KCL, pH 8.0) (Applied Biosystem,
Germany), 3.0 µl MgClB2 (25 mM) (Applied Biosystem, Germany), 0.35 µl
AmpliTaq Gold polymerase (5 U/µl, Applied Biosystem, Germany), 32.15 µl
aquades steril, dan ditambahkan 5.0 µl DNA template.
®
Program amplifikasi PCR yang digunakan adalah 1 siklus of 94 °C selama
10 menit kemudian 40 siklus pada 94 °C selama 1 menit, 58 °C selama 1 menit,
dan 72 °C selama 3 menit, dan dilanjutkan dengan 1 siklus pada 72 °C selama 7
menit.
Visualisasi hasil PCR dilakukan dengan mencampur 13 µl amplikon dengan
2 µl loading dye solution (MBI Fermentas, Germany). selanjutnya diseparasi menggunakan 2% gel agarose electrophoresis (Biozyme, Germany) pada tegangan 120 V selama 50 menit di dalam larutan 1x TAEbuffer (0.04 mol/l Tris,
0.001 mol/l EDTA, pH 7.8). Marker yang digunakan adalah 100 bp DNA ladder
(MBI Fermentas, Germany). Pewarna menggunakan ethidium bromide 5 µl/ml (Sigma, Germany) dan gambar didokumentasikan dengan menggunakan UV
(245 nm) trans-illuminator (Biorad, Germany).
21
Kajian Deteksi Mycobacterium avium subspesies paratuberculosis pada
Sapi Perah di Bogor
Kajian ini bertujuan mendeteksi MAP pada sapi perah di peternakan rakyat
Bogor dan menganalisis faktor tatacara berternak terkait keberadaan bakteri
tersebut pada ternak. Desain penelitian yang dipakai adalah kajian deteksi
penyakit.
Kajian dilakukan terhadap sapi perah peternakan rakyat di desa
Cibungbulang Bogor yang tergabung dalam Koperasi Produksi Susu dan Usaha
Peternakan (KPS) Bogor.
Penghitungan jumlah contoh hewan berdasarkan rumus Canon dan Roe
(diacu oleh Martin et al. 1987):
1/D
Keterangan
n : jumlah contoh yang diambil α : tingkat kepercayaan
D :jumlah hewan sakit
N :populasi hewan
Se: sensitivitas
Populasi sapi perah di Bogor sebanyak 5841 ekor (komunikasi pribadi
2005) dan asumsi prevalensi 5% dengan tingkat kepercayaan (CI) 95% dan
sensitivitas 95% maka diperoleh jumlah contoh sebanyak 62 ekor. Contoh
hewan dipilih secara purposif dengan kriteria hewan berumur diatas 2 tahun,
sering mengalami diare/berulang, produksi susu tidak stabil( tinggi sekali atau
rendah sekali), serta kondisi badan yang kurus.
Contoh yang diambil yaitu susu segar 500 ml langsung dari pemerahan
pagi dan feses segar per rektal. Selain pengambilan contoh susu dan feses, juga
dilakukan pengumpulan data pendukung berdasarkan wawancara dengan
peternak/pegawai kandang. Kuesioner terhadap peternak terpilih berupa
pertanyaan tertutup dan terbuka, meliputi: umur, bangsa, berat badan, produksi
susu, frekuensi diare, status mastitis, frekuensi pemerahan, sanitasi kandang dan
ternak, higiene peternak, sumber air minum.
Pemeriksaan laboratorik terhadap contoh susu segar dan feses meliputi
isolasi bakteri menggunakan HEYMj dan HEYM (BBL Becton Dickinson,
Germany), pewarnaan tahan asam Ziehl-Neelsen (ZN), dan analisis PCR konvensional menggunakan primer IS900 dan F57. Pemeriksaan contoh
dilakukan di Laboratorium Terpadu Ilmu Penyakit Hewan dan Kesehatan
Masyarakat Veteriner FKH IPB.
Seratus mililiter masing-masing contoh dihomogenkan kemudian dituang
ke dalam 2 buah tabung gelas sentrifus steril (ukuran 50 ml). Susu disentrifus
(Serovall Super T21, USA ) pada kecepatan 2500 X g selama 15 menit. Fraksi
cair susu dibuang, dan pelet dari masing-masing tabung diresuspensi dengan 1
ml aquades steril dan disatukan (dari asal contoh yang sama). Satu mililiter
larutan dimasukkan ke dalam tabung Eppendorf 1.5 ml untuk dibiakan.
Penyiapan contoh feses dilakukan mengacu pada Stabel et al. (2002) yang dimodifikasi. Feses seberat 3 g dilarutkan dengan 35 ml air destilasi steril,
dikocok dan didiamkan pada suhu ruang selama 30 menit. Supernatan kemudian
diambil sebanyak 30 ml dan dipindahkan ke dalam tabung sentrifus 50 ml dan
disentrifus pada kecepatan 1500 X g (Serovall Super T21, USA) selama 15
menit. Larutan kemudian disentrifus pada 2500 X g selama 15 menit. Supernatan
dibuang sedangkan pelet diresuspensi kembali dengan 2 ml aquades steril
kemudian 1 ml larutan diambil dan ditempatkan pada tabung Eppendorf 1.5 ml
untuk analisis PCR sedangkan sisanya digunakan untuk analisis biakan.
Inokulasi untuk mendapatkan biakan dilakukan dengan menggunakan
media HEYMj dan HEYM. Sebanyak 1 ml suspensi yang telah diperoleh dari
tahap sebelumnya dipindahkan ke dalam tabung gelas steril. Suspensi
didekontaminasi dengan menambahkan sebanyak 10 ml 0.75%
hexadecilpyridinium chloride (HPC) (Biomedical, USA) kemudian didiamkan pada suhu kamar selama 5 jam untuk contoh susu segar dan 24 jam untuk contoh
feses. Suspensi yang telah didekontaminasi kemudian disentrifus pada
kecepatan 2500 X g selama 15 menit. Supernatan dibuang dan pelet
diresuspensi menggunakan 1000 µl PBS steril (Invitrogen, New Zealand).
Inokulasi dilakukan dengan memasukkan sebanyak 250 µl inokulat ke dalam 2
tabung HEYMj dan 1 tabung HEYM. Media yang telah diinokulasi kemudian
diinkubasi pada suhu 37 °C selama 20 minggu.
Pengamatan pertumbuhan bakteri dilakukan setiap minggu dan koloni yang
tumbuh pada media HEYMj maupun HEYM selanjutnya dibuat preparat ulas
untuk pemeriksaan mikroskopik dengan pewarnaan tahan asam ZN. Isolat yang
diperoleh dan teridentifikasi sebagai Mycobacterium kemudian dikonfirmasi terhadap MAP dengan PCR konvensional. Isolat tersebut juga diuji biokimia