ABSTRAK
KAJIAN SEBARAN LOGAM BERAT Cd DAN Cr PADA SEDIMEN DI PESISIR PANTAI WAY KUALA BANDAR LAMPUNG
Oleh
DWI PUJI ASTUTI
Telah dilakukan kajian sebaran logam berat Cd dan Cr pada sedimen di muara sungai dan di pesisir pantai Way Kuala Bandar Lampung. Konsentrasi logam Cd dan Cr ditentukan dengan menggunakan spektofotometer serapan atom (SSA) dengan menggunakan dua validasi metode yaitu, presisi (ketelitian), dan linieritas. Hasil analisis menunjukkan konsentrasi logam Cd pada sedimen di muara sungai dan di pesisir pantai Way Kuala Bandar Lampung yaitu pada rentang 0 ppm sampai 0,2522 ± 0,011ppm. Konsentrasi logam berat Cr pada sampel sedimen di muara sungai dan di pesisir pantai Way Kuala Bandar Lampung yaitu pada rentang 1,243 ± 0,056 ppm sampai 1,361 ± 0,047 ppm. Validasi metode pada penentuan kadar Cd dan Cr pada sedimen menunjukkan presisi dengan nilai RSD < 5 %; koefisien korelasi untuk masing-masing logam Cd dan Cr adalah; 0,999 dan 0,995.
ABSTRACT
STUDY OF DISTRIBUTION OF HEAVY METALS Cd AND Cr IN SEDIMENTS ON COASTAL REGION OF WAY KUALA
BANDAR LAMPUNG
By
DWI PUJI ASTUTI
This Study was carried out to insvestigate distribution of heavy metals Cd dan Cr in sediments of estuary and coastal region of Way Kuala Bandar lampung. Metals concentration were measured using Atomatic absorption spectroscopy (AAS), with two validation methods namely precision and linearity.
I. PENDAHULUAN
A. Latar Belakang
Bandar Lampung merupakan pusat kegiatan pemerintahan, sosial politik, pendidikan dan kebudayaan serta pusat kegiatan perekonomian. Sektor industri pengolahan merupakan sektor tertinggi yang membangun perekonomian kota Bandar Lampung yaitu sebesar 29,82 % pada tahun 2000 (BPS, 2002). Hasil identifikasi yang telah dilakukan oleh Wiryawan dkk, pada tahun 2002,
Pencemaran perairan di wilayah pesisir telah menjadi isu utama yang dihadapi oleh pemerintah dan masyarakat di Kota Bandar Lampung. Sumber pencemaran yang utama berasal dari limbah industri dan domestik yang mengalir melalui sungai-sungai yang bermuara ke laut di sepanjang pantai Kota Bandar Lampung. Selain itu, sampah- sampah domestik diperkirakan juga berasal dari wilayah lain yang dibawa oleh arus laut dan terdampar di sepanjang pantai (Yudha, 2007). Mengingat sampai saat ini Bandar Lampung belum memiliki Instalasi Pengolahan Air Limbah (IPAL) terpadu, dimungkinkan bahwa limbah industri yang
merupakan limbah B3 (Bahan Beracun Berbahaya) yang dihasilkan dari proses produksi dialirkan langsung ke pesisir pantai Way Kuala (Wiryawan dkk., 1999). Limbah B3 merupakan limbah yang mengandung logam berat seperti Cd dan Cr. Selain limbah industri, pencemaran logam berat juga berasal dari limbah domestik seperti: limbah alat elektronik rumah tangga, korosi pipa-pipa air yang
mengandung Cd dan Cr (Connel and Miller, 1995).
Untuk mengatasi masalah pencemaran air sungai, pemerintah Kota Bandar Lampung melalui BPPLH (Badan Pengelola dan Pengendali Lingkungan Hidup) dan Dinas Tata Kota setiap tahun melakukan program kali bersih (Prokasih). Hanya saja, upaya pembersihan yang dilakukan sejak 2001 hingga kini belum berhasil. Total bahan pencemar tetap tinggi karena peningkatan kapasitas pengelolaan industri dan ketidakmampuan mengurangi dampak polutan
199,9 dan 71,96 mg/L (Yudha, 2007). Menurut Yudha (2007) kandungan logam berat pada air sungai Way Kuala masih memenuhi persyaratan untuk baku mutu air kelas III. Logam berat dapat membentuk senyawa kompleks atau teradsorpsi dengan partikulat senyawa organik dan anorganik yang terdapat dalam air sungai (Forstner and Prosi, 1987).
Faktor yang dapat mempengaruhi lingkungan pesisir yakni, seperti: pertambahan jumlah penduduk, kegiatan-kegiatan manusia, pencemaran, sedimentasi,
overeksploitasi sumberdaya alam. Sedimentologi adalah ilmu yang mempelajari sedimen atau endapan (Ward dkk., 2004). Adanya gaya gravitasi menyebabkan partikulat tersebut mengendap membentuk sedimen pada dasar sungai. Hal ini menyebabkan kadar logam berat pada sedimen sungai lebih besar dibandingkan air sungai.
Unsur kromium (Cr) merupakan unsur yang bersifat karsinogen bila terakumulasi dalam jumlah berlebih pada tubuh. Kromium (VI) dapat menyebabkan tumor pada perut. Keracunan logam berat Cd dapat menyebabkan tekanan darah tinggi, kerusakan jaringan testikular, kerusakan ginjal dan kerusakan sel-sel darah merah (Pallar, 1994). Konsentrasi rata-rata logam Cd pada sedimen di muara sungai Way Kuala berada pada rentang 20,73 ± 0,18 sampai 23,00 ± 0,81 ppm (Novita, 2010), berada di atas baku mutu yang telah ditetapkan oleh National Sediment Quality Survey USEPA (2004) yaitu pada rentang 0,65-2,49 ppm. Pada penelitian logam Cd yang diteliti oleh Novita di bulan Juli 2010,tepatnya pada musin
Dari uraian di atas, perlu dilakukan kajian sebaran logam berat Cd dan Cr pada sedimen di pesisir pantai Way Kuala sehingga dapat mencerminkan tingkat pencemaran yang sesungguhnya. Logam berat Cd dan Cr dianalisis dengan menggunakan Spektrofotometer Serapan Atom (SSA) dimana alat ini dapat digunakan untuk menentukan unsur di dalam suatu bahan dengan kepekaan, ketelitian serta selektifitas yang tinggi (Gunandjar, 1990). Prinsip metode spektrofotometri serapan atom adalah absorbsi cahaya oleh atom pada panjang gelombang tertentu tergantung pada sifat unsurnya (Skoog, 1985).
B. Tujuan
Adapun tujuan dari penelitian ini adalah menentukan kadar logam berat Cd dan Cr pada sedimen di pesisir pantai Way Kuala Bandar Lampung.
C. Manfaat
KAJIAN SEBARAN LOGAM BERAT Cd DAN Cr PADA SEDIMEN DI PESISIR PANTAI WAY KUALA BANDAR LAMPUNG
(Skripsi)
Oleh
Dwi Puji Astuti
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
II. TINJAUAN PUSTAKA
A. Pesisir Pantai Way Kuala
Wilayah pesisir Kota Bandar Lampung merupakan daerah yang rentan terhadap pencemaran yang berasal dari limbah domestik maupun limbah industri yang mengalir melalui sungai-sungai yang bermuara ke wilayah perairan laut. Hasil identifikasi yang telah dilakukan oleh Wiryawan dkk., (2002), memberikan informasi bahwa setidaknya terdapat 9 sungai yang bermuara ke pesisir pantai Kota Bandar Lampung yang berpotensi mencemarkan wilayah pantai tersebut. Dataran kota Bandar Lampung sebagian besar dialiri oleh sungai yang tidak terlalu panjang yaitu antara 2 sampai 14 km, di mana hulu sungai berada pada bagian barat dan hilir sungai berada pada bagian selatan yaitu pada dataran pantai (Anonim 1, 2009).
B. Sedimen
Sedimen yang ada terangkut sampai di suatu tempat yang disebut cekungan. Sedimen sangat besar kemungkinan terendapkan karena daerah tersebut relatif lebih rendah dari daerah sekitarnya dan karena bentuknya yang cekung ditambah akibat gaya gravitasi dari sedimen, maka sedimen akan susah sekali bergerak melewati cekungan. Semakin banyaknya sedimen yang diendapkan, maka cekungan akan mengalami penurunan dan membuat cekungan tersebut semakin dalam sehingga semakin banyak sedimen yang terendapkan. Penurunan cekungan sendiri banyak disebabkan oleh penambahan berat dari sedimen yang ada dan juga dipengaruhi oleh struktur yang terjadi di sekitar cekungan seperti adanya patahan (Siaka, 2008).
Transportasi sedimen dapat terjadi melalui tiga cara, yaitu (Prothero and Schwab, 1999):
1. Suspension: umumnya terjadi pada sedimen-sedimen yang sangat kecil ukurannya (seperti lempung) sehingga mampu diangkut oleh aliran air atau angin yang ada.
3. Saltation: umumnya terjadi pada sedimen berukuran pasir dimana aliran fluida yang ada mampu menghisap dan mengangkut sedimen pasir sampai akhirnya karena gaya gravitasi yang ada mampu mengembalikan sedimen pasir tersebut ke dasar.
Pada saat kekuatan untuk mengangkut sedimen tidak cukup besar dalam membawa sedimen-sedimen yang ada maka sedimen tersebut akan jatuh atau mungkin tertahan akibat gaya gravitasi yang ada. Setelah itu proses sedimentasi dapat berlangsung sehingga mampu mengubah sedimen-sedimen tersebut menjadi suatu batuan sedimen. Material yang menyusun batuan sedimen adalah lumpur, pasir, kerikil, kerakal, dan sebagainya. Sedimen ini akan menjadi batuan sedimen apabila mengalami proses pengerasan.
Secara umum, sedimen atau batuan sedimen terbentuk dengan dua cara, yaitu (Ward and Stanley, 2004):
1. Batuan sedimen yang terbentuk dalam cekungan pengendapan atau dengan kata lain tidak mengalami proses pengangkutan. Sedimen ini dikenal sebagai sedimen Autochthonous. Kelompok batuan Autochhonous antara lain adalah batuan evaporit (halit) dan batu gamping.
Selain kedua jenis batuan diatas, batuan sedimen dapat dikelompokkan pada beberapa jenis berdasarkan cara dan proses pembentukannya yaitu (Prothero and Schwab, 1999):
1. Terrigenous (Detrital atau Klastik).
Batuan sedimen klastik merupakan batuan yang berasal dari suatu tempat yang kemudian diangkut dan diendapkan pada suatu cekungan. Contoh batuan
Terrigenous adalah konglomerat atau breksi, batu pasir, batu lanau dan lempung.
2. Sedimen kimiawi (Chemical)/biokimia (Biochemical).
Batuan sedimen kimiawi atau biokimia adalah batuan hasil pengendapan dari proses kimiawi suatu larutan dan organisme bercangkang yang mengandung mineral silika atau fosfat. Contoh batuan sedimen kimiawi adalah evaporit, batuan sedimen karbonat (batu gamping dan dolomit), batuan sedimen bersilika (rijang) dan endapan organik (batubara).
3. Batuan volkanoklastik (Volcanoclastic Rocks).
Batuan volkanoklastik merupakan batuan yang berasal dari aktivitas gunung berapi. Debu dari aktivitas gunung berapi ini akan terendapkan seperti
sedimen yang lain. Adapun kelompok batuan volkanoklastik adalah batu pasir tufa dan aglomerat.
1. Batuan sedimen klastik
Batuan yang terbentuk dari hasil rombakan batuan yang sudah ada (batuan beku, metamorf, atau sedimen) yang kemudian diangkut oleh media (air, angin, gletser) dan diendapkan di suatu cekungan. Proses pengendapan sedimen terjadi terus menerus sesuai dengan berjalannya waktu sehingga endapan sedimen semakin lama semakin bertambah tebal. Beban sedimen yang semakin tebal mengakibatkan endapan sedimen mengalami kompaksi. Sedimen yang terkompaksi kemudian mengalami proses diagenesa, sementasi dan akhirnya mengalami pembatuan menjadi batuan sedimen.
2. Batuan sedimen non-klastik
Batuan sedimen yang pembentukannya berasal dari proses kimiawi atau sedimen yang berasal dari sisa-sisa organisme yang telah mati. Kandungan logam berat pada sedimen umumnya rendah pada musim kemarau dan tinggi pada musim penghujan. Penyebab tingginya kadar logam berat dalam
sedimen pada musim penghujan kemungkinan disebabkan oleh tingginya laju erosi pada permukaan tanah yang terbawa ke dalam badan sungai, sehingga sedimen dalam sungai yang diduga mengandung logam berat akan terbawa oleh arus sungai menuju muara dan pada akhirnya terjadi proses sedimentasi (Nammiinga and Wilhm, 1977; Siaka, 2008).
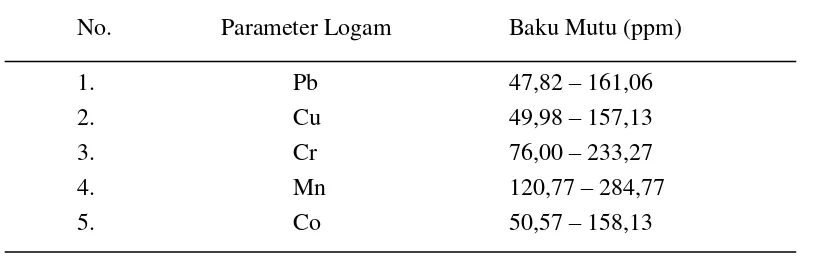
Tabel 1. Baku mutu kandungan logam berat dalam sedimen
No. Parameter Logam Baku Mutu (ppm)
1. Pb 47,82 – 161,06
2. Cu 49,98 – 157,13
3. Cr 76,00 – 233,27
4. Mn 120,77 – 284,77
5. Co 50,57 – 158,13
Akumulasi logam berat ke dalam sedimen dipengaruhi oleh jenis sedimen, dimana kandungan logam berat pada lumpur > lumpur berpasir > abu pasir
(Korzeniewski and Neugabieuer, 1991). Secara alamiah, kandungan logam berat dalam air adalah kurang dari 1g/L.
Tabel 2. Klasifikasi partikel sedimen menurut skala wenworth (Buchanan, 1984)
Ukuran partikel
partikel tersuspensi akan menuju dasar perairan, menyebabkan kandungan logam di air menjadi lebih rendah. Hal ini tidak menguntungkan bagi organisme yang hidup di dasar seperti kerang (oyster) dan kepiting, partikel sedimen ini akan masuk ke dalam sistem pencernaannya (Ford, 1999).
C. Logam Berat
Logam merupakan bahan pertama yang dikenal oleh manusia dan digunakan sebagai alat-alat yang berperan penting dalam sejarah peradaban manusia (Darmono, 1995). Logam juga didefinisikan sebagai unsur alam yang dapat diperoleh dari laut, erosi batuan tambang, vulkanisme dan sebagainya (Clark, 1986). Umumnya logam-logam di alam ditemukan dalam bentuk persenyawaan dengan unsur lain, sangat jarang yang ditemukan dalam elemen tunggal.
1995). Dalam neraca global, sumber yang berasal dari alam sangat sedikit dibandingkan dengan pembuangan limbah akhir di laut (Yudha, 2007).
Logam berat adalah suatu terminologi umum yang digunakan untuk menjelaskan sekelompok elemen-elemen logam yang kebanyakan berbahaya apabila masuk ke dalam tubuh. Logam berat adalah unsur-unsur yang mempunyai nomor atom dari 22- 92 dan terletak di dalam periodik tiga dalam susunan berkala, mempunyai densitas lebih besar dari 5 gram/ml (Hutagalung, 1991). Logam berat umumnya berada di sudut kanan bawah pada susunan berkala, seperti unsur-unsur Pb, Cd, dan Hg. Kebanyakan dari logam-logam tersebut mempunyai afinitas sangat besar terhadap belerang (Siaka, 2008).
Dalam perairan, logam berat dapat ditemukan dalam bentuk terlarut dan tidak terlarut. Logam berat terlarut adalah logam yang membentuk kompleks dengan senyawa organik dan anorganik, sedangkan logam berat yang tidak terlarut merupakan partikel-partikel yang berbentuk koloid dan senyawa kelompok metal yang teradsorbsi pada partikel-partikel yang tersuspensi (Razak, 1998).
Pencemaran logam berat ini menimbulkan berbagai permasalahan diantaranya: 1. Berhubungan dengan estetika (perubahan bau, warna dan rasa air).
2. Berbahaya bagi kehidupan tanaman dan binatang. 3. Berbahaya bagi kesehatan manusia.
4. Menyebabkan kerusakan pada ekosistem.
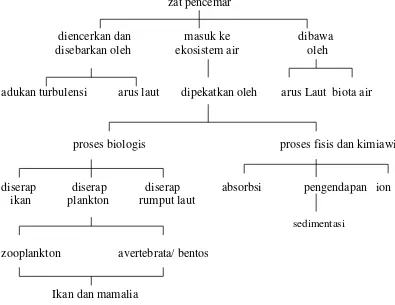
toksisitas lingkungan, biasanya berasal dari limbah yang sangat berbahaya dan memiliki toksisitas yang tinggi. Limbah industri merupakan salah satu sumber pencemaran logam berat yang potensial bagi perairan. Pembuangan limbah industri secara terus-menerus tidak hanya mencemari lingkungan perairan tetapi menyebabkan terkumpulnya logam berat dalam sedimen dan biota perairan, seperti yang terlihat pada gambar dibawah ini
zat pencemar
diencerkan dan masuk ke dibawa disebarkan oleh ekosistem air oleh
adukan turbulensi arus laut dipekatkan oleh arus Laut biota air
proses biologis proses fisis dan kimiawi
diserap diserap diserap absorbsi pengendapan ion ikan plankton rumput laut
zooplankton avertebrata/ bentos
Ikan dan mamalia
Gambar 1. Skema proses alami yang terjadi jika polutan logam berat masuk ke dalam lingkungan air (Hutagalung, 1991).
Pencemaran logam berat di perairan dapat berasal dari kegiatan alam maupun industri. Secara alamiah pencemaran logam berat dapat diakibatkan adanya pelapukan batuan pada cekungan perairan atau adanya kegiatan gunung berapi
(Connel and Miller, 1995). Proses industri yang menghasilkan limbah berupa logam berat seperti Cd dan Cr merupakan sumber utama pencemaran di perairan.
Selain limbah industri, pencemaran logam berat juga berasal dari limbah rumah tangga seperti sampah-sampah metabolik, korosi pipa-pipa air yang mengandung Cd dan Cr (Connel and Miller, 1995). Logam berat seperti Cd dan Cr yang masuk dalam perairan akan mengalami pengendapan yang dikenal dengan istilah
sedimen (Pallar, 1994). Logam berat dapat terakumulasi dalam sedimen karena dapat terikat dengan senyawa organik dan anorganik melalui proses adsorpsi dan pembentukan senyawa kompleks (Forstner and Prosi, 1987; Tarigan dkk., 2003).
Pada umumnya logam berat yang terakumulasi pada sedimen tidak terlalu berbahaya bagi makhluk hidup di perairan, tetapi oleh adanya pengaruh kondisi akuatik yang bersifat dinamis seperti perubahan pH akan menyebabkan logam-logam yang terendapkan dalam sedimen terionisasi ke perairan. Hal inilah yang merupakan bahan pencemar dan akan memberikan sifat toksik terhadap organisme yang hidup bila ada dalam jumlah berlebih dan akan membahayakan kesehatan manusia yang mengkomsumsi organisme tersebut. Sifat toksik logam berat dapat dikelompokkan menjadi 3 yaitu; toksik tinggi yang terdiri dari unsur-unsur Hg, Cd, Pb, Cu dan Zn; toksik sedang terdiri dari unsur-unsur Cr, Ni dan Co; toksik rendah terdiri dari unsur Mn dan Fe (Connel and Miller, 1995; Siaka, 1998).
D. Kadmium (Cd)
dunia fotografi. Selain itu, Cd juga banyak digunakan dalam industri-industri ringan, seperti pada mesin pengolahan roti, mesin pengolahan ikan, dan mesin pengolahan air minum meskipun dalam konsentrasi rendah (Pallar, 1994).
1. Sumber Pencemaran Logam Cd
Kandungan logam Cd terdapat di daerah-daerah penimbunan sampah dan aliran air hujan. Menurut National Research Council dalam Yuliasari (2003), sampah dari kota mengandung Cd yang cukup besar sehingga penggunaan sampah yang mengandung Cd tinggi untuk pemupukan tanaman, baik
tanaman untuk manusia atau hewan memperlihatkan peningkatan kandungan Cd secara substansial ke dalam makanan hewan dan manusia.
Selain dari aktivitas manusia, organisme yang hidup di perairan tersebut juga dapat meningkatkan konsentrasi melalui biomagnifikasi. Biomagnifikasi adalah kemampuan yang dimiliki oleh organisme perairan untuk
meningkatkan konsentrasi bahan pencemar baik dalam bentuk logam berat atau persenyawaan kimia beracun lainnya, yang melebihi keseimbangan penyerapan dalam tubuh organisme tersebut (Gobas et al., 1999). 2. Toksisitas Logam Cd
Dampak keracunan Cd dapat menyebabkan tekanan darah tinggi, kerusakan jaringan testikular, kerusakan ginjal dan kerusakan sel darah merah.
3. Sifat Fisik dan Kimia Cd
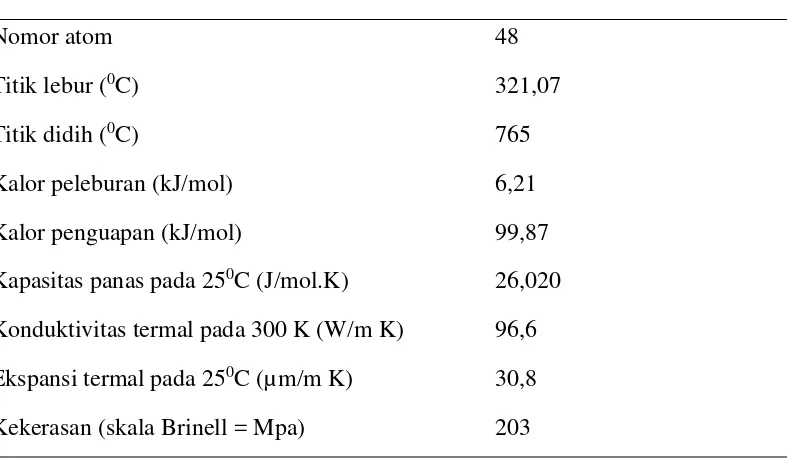
Kadmium (Cd) adalah salah satu logam berat dengan penyebaran yang luas di alam; logam ini bernomor atom 48; berat atom 112,40. Kadmium (Cd) di alam bersenyawa dengan belerang (S) sebagai Greennocckite (CdS) yang ditemukan bersamaan dengan senyawa Spalerite (ZnS). Kadmium merupakan logam lunak (Ductile) berwarna putih perak dan mudah teroksidasi oleh udara bebas dan gas amoniak. Beberapa sifat fisik dari Cd dapat dilihat pada Tabel
Tabel 3. Sifat Fisik Logam Cd (Anonim 3, 2009)
Nomor atom 48
Titik lebur (0C) 321,07
Titik didih (0C) 765
Kalor peleburan (kJ/mol) 6,21 Kalor penguapan (kJ/mol) 99,87 Kapasitas panas pada 250C (J/mol.K) 26,020 Konduktivitas termal pada 300 K (W/m K) 96,6 Ekspansi termal pada 250C (µm/m K) 30,8 Kekerasan (skala Brinell = Mpa) 203
E. Kromium (Cr)
Menurut Anonim 2 (2010) penggunaan logam kromium dalam industri antara lain 1. Logam kromium (Cr) digunakan sebagai pelapis baja atau logam. Kromium
merupakan bahan paduan baja yang menyebabkan baja bersifat kuat dan keras. 2. Kromium (Cr) digunakan dalam industri penyamakan kulit. Senyawa
3. Logam kromium (Cr) dimanfaatkan sebagai bahan pelapis (platting) pada bermacam-macam peralatan, mulai dari peralatan rumah tangga sampai peralatan mobil. Bahan paduan steinless steel (campuran Cr dengan Ni) digunakan pada industri pembuatan alat dapur.
4. Senyawa CrO3 yang berwarna coklat gelap, bersifat konduktor listrik yang tinggi dan bersifat magnetik, digunakan pada pita rekaman.
5. Senyawa Na2Cr2O7 sebagai oksidan dalam industri kimia.
6. Persenyawaan kromium (senyawa-senyawa kromat dan dikromat) dimanfaatkan dalam industri tekstil untuk pencelupan dan zat warna.
Penjualan produk atau bahan kimia yang mengandung kromium dan bahan bakar fosil menyebabkan terjadinya pembakaran ke udara, tanah dan air. Partikel
kromium ada di udara dalam waktu kurang dari 10 hari, kemudian akan menempel pada partikel tanah dan air tetapi kelarutannya rendah.
1. Sumber Pencemaran Logam Cr
Logam kromium (Cr) juga beracun bagi manusia. Sumber pencemaran logam berat Cr dibagi menjadi dua sumber yaitu sumber alami dan sumber buatan. Sumber alami :
1. Berasal dari daerah pantai (coastal supply), yang bersumber dari sungai, abrasi pantai oleh aktifitas gelombang.
2. Berasal dari logam yang dibebaskan oleh aktivitas gunung berapi dan logam yang dibebaskan oleh proses kimiawi.
ditransportasi oleh ikan dari atmosfir berupa partikel debu (Wordpress.com, 2009).
2. Toksisitas Cr
Kromium dapat berbentuk cairan, padatan maupun gas dan terdapat di alam dalam 3 jenis valensi yaitu kromium (0), kromium (III) dan kromium (VI). Kromium (III) merupakan unsur esensial yang dibutuhkan tubuh dalam reaksi enzimatis untuk metabolisme gula, protein dan lemak. Kromium (III) memiliki sifat toksisitas yang rendah dibandingkan dengan kromium (VI). Pada bahan baku makanan dan tumbuhan mobilitas krom relatif rendah dan diperkirakan konsumsi harian kromium (III) pada manusia di bawah 100 μg, berasal dari makanan, sedangkan dari air dan udara dalam tingkat yang rendah. Kromium (VI) lebih mudah diserap oleh tubuh dibandingkan dengan kromium (III). Namun, setelah di dalam tubuh kromium(VI) segera mengalami reduksi menjadi kromium (III), (TNR.R, 2008).
Akumulasi kromium dalam tubuh manusia dapat mengakibatkan kerusakan dalam sistem organ tubuh. Efek toksisitas kromium (Cr) dapat merusak serta mengiritasi hidung, paru-paru, lambung, dan usus. Konsumsi makanan mengandung
inhalasi tubuh dapat menyebabkan kanker paru-paru. Kromium (VI) yang terdapat dalam air minum dapat menyebabkan tumor pada perut manusia dan hewan (TNR.R, 2008).
Akumulasi kromium (VI) dalam jumlah 7,5 mg/L pada manusia menyebabkan toksisitas akut berupa kematian sedangkan bila terjadi akumulasi kromium (VI) pada dosis 0,57 mg/kg perhari dapat menyebabkan kerusakan pada hati (TNR.R, 2008), gangguan perut serta kematian pada penduduk. Hal ini akibat terjadinya pencemaran air sungai oleh industri yang menyebabkan konsentrasi kromium (VI) dalam air sungai mencapai 20 mg/L (Zhang et al., 1987).
Menurut(TNR.R, 2008) batas konsentrasi kromium yang membahayakan bagi kesehatan manusia adalah :
1. EPA (Environmental Protection Agency) menetapkan batas maksimal konsentrasi kromium (III) dalam air minum adalah 1 mg/L untuk konsumsi air minum selama 10 hari.
2. OSHA (The Occupational Health and Safety Administration) menetapkan batas maksimal bagi pekerja yang terpapar dengan kromium secara langsung adalah 0,005 mg/m3 untuk kromium (VI) dan 0,5 mg/m3 untuk kromium (III) dan 1 mg/m3 untuk kromium (0) selama 8 jam kerja sehari dan 40 jam kerja selama 1 minggu.
3. FDA menetapkan batas maksimal konsentrasi maksimal kromium (III) yang digunakan dalam botol air minum adalah 1 mg/L.
3. Sifat Fisik dan Kimia Kromium (Cr).
logam di alam ditemukan dalam bentuk persenyawaan dengan unsur lain dan sangat jarang ditemukan dalam bentuk unsur tunggal. Logam kromium (Cr) di alam ditemukan dalam bentuk chromite (FeCr2O3). Kromium adalah logam yang berwarna putih, tak begitu liat, dan tak dapat ditempa. Logam kromium (Cr) larut dalam asam klorida encer atau pekat.
Jika tidak terkena udara, akan terbentuk ion-ion kromium.
Cr (S) + 2 HCl (aq) Cr2+ (aq) + 2Cl- (aq) + H2 (g)
Logam kromium tidak dapat teroksidasi oleh udara yang lembab dan proses pemanasan cairan. Logam ini larut juga oleh H2SO4, dan asam perklorat. Ion kromium yang telah membentuk senyawa, mempunyai sifat yang berbeda sesuai dengan tingkat oksidasinya.
Tebel 4. Sifat Fisik Logam Kromium (Cr) (Anonim 3, 2010)
Nomor atom 24
Densitas (g/cm3) 13,11
Titik lebur (0C) 1765
Titik didih (0C) 1810
Kalor fusi (kJ/mol) 4,90
Kalor penguapan (kJ/mol) 190,5 Kapasitas panas pada 250C (J/mol.K) 21,650
Menurut Svehla (1985) dalam larutan air, kromium (Cr) membentuk tiga jenis ion yaitu :
1. Ion kromium(II) atau kromo (Cr2+)
merupakan zat pereduksi yang kuat dan dapat menguraikan air perlahan-lahan dengan membentuk hidrogen. Oksigen di udara akan mengoksidasi Cr2+ menjadi ion kromium(III), ion ini membentuk larutan yang berwarna biru. Senyawa yang terbentuk dari ion logam Cr2+ bersifat basa.
2. Ion kromium(III) atau kromi (Cr3+)
Ion kromium(III) memiliki bilangan oksidasi +3 dan bersifat stabil. Dalam larutan, ion-ion ini bewarna hijau. Senyawa yang terbentuk dari ion logam Cr3+ bersifat amfoter.
3. Ion kromium(VI) atau kromat (CrO42-) dan dikromat (Cr2O72-)
Ion kromium(VI) memiliki bilangan oksidasi +6. Ion-ion kromat berwarna kuning sedangkan dikromat bewarna jingga. Senyawa yang terbentuk dari ion kromium(VI) bersifat asam. Ion-ion kromat dan dikromat merupakan zat pengoksidasi yang kuat sedangkan jika sedimen yang mengandung ion kromium diasamkan, akan membentuk ion-ion dikromat.
F. Spektrofotometri Serapan Atom (SSA)
1. Prinsip Dasar
Spektrum atom yang karakteristik untuk setiap unsur biasanya terdiri dari
sejumlah garis-garis tertentu, diantaranya terdapat garis-garis resonansi di dalam metode ini. Panjang gelombang pada garis-garis resonansi inilah yang digunakan dalam pengukuran, hal ini disebabkan karena kebanyakan atom-atom netral dihasilkan oleh alat atomisasi berada dalam keadaan dasar.
Adapun keunggulan dari Spektroskopi Serapan Atom yaitu memiliki kepekaan yang tinggi karena dapat mengukur kadar logam sampai konsentrasi yang sangat kecil, memiliki selektifitas yang tinggi karena dapat menentukan beberapa unsur sekaligus dalam larutan sampel tanpa perlu pemisahan. Prinsip metode
spektrofotometri serapan atom adalah absorbsi cahaya oleh atom pada panjang gelombang tertentu tergantung pada sifat unsurnya (Skoog, 1985).
Kelemahannya yaitu dengan pengaruh kimia, dimana SSA tidak mampu menguraikan zat menjadi atom, misalnya pengaruh fosfat pada pengukuran Ca. Selain itu adanya pengaruh ionisasi yaitu bila atom tereksitasi (tidak hanya terdisosiasi), sehingga menimbulkan emisi pada panjang gelombang yang sama, serta pengaruh matriks misalnya pelarut (Razak, 1998).
2. Analisis Kuantitatif
Pada dasarnya hubungan antara absorpsi atom dengan konsentrasi di dalam metode SSA dapat dinyatakan dengan hukum Lambert-Beer, yaitu secara matematika, persamaannya adalah sebagai berikut:
I = Ioe−
A = a. b. c
Keterangan:
Io : Interaksi Cahaya yang datang (mula-mula) I : Interaksi cahaya yang ditransmisikan
a : Absorpsotivitas, yang besarnya sama untuk sistem atau larutan yang sama (g/L)
b : Panjang jalan cahaya atau tebalnya medium penyerap yang besarnya tetap untuk alat yang sama (cm)
c : Konsentrasi atom yang mengabsorpsi A : absorbansi = log Io/I
Dari persamaan di atas, nilai absorbansi sebanding dengan konsentrasi untuk panjang jalan penyerapan dan panjang gelombang tertentu. Ada dua cara untuk mengetahui konsentrasi cuplikan yang telah diketahui nilai absorbansinya, yaitu (1) cara deret waktu, dengan membandingkan nilai absorbansi terhadap kurva kalibrasi dari standar-standar yang diketahui, (2) cara penambahan standar yaitu dengan membandingkan konsentrasi dengan perpotongan grafik terhadap sumbu dengan konsentrasi dari data absorbansi.
3. Gangguan-Gangguan pada Spektofotometer Serapan Atom (SSA)
Beberapa gangguan yang sering terjadi pada SSA adalah sebagai berikut (Ismono, 1984):
adalah; tegangan permukaan, berat jenis, tekanan uap pelarut. Untuk mengatasi gangguan ini maka perlu diusahakan agar sifat fisik larutan cuplikan sama dengan larutan standar.
b. Gangguan kimia
Gangguan ion disebabkan karena terhambatnya pembentukan atom-atom netral dari unsur yang analisis pada tingkat energi dasar, hal ini terjadi karena:
1) Pembentukan senyawa-senyawa yang yang bersifat refraktori seperti Ca-fosfat, fosfat, sillikat dan oksida dari logam alkali tanah dan Mg. Untuk mengatasi gangguan ini dapat dilakukan dengan berbagai cara, antara lain:
Menggunakan nyala yang lebih tinggi suhunya, karena
senyawa-senyawa yang refraktori dapat terurai pada suhu yang tinggi.
Penambahan unsur penyangga kepada cuplikan yang akan dianalisis.
Unsur penyangga ini misalnya Sr atau La yang akan mengikat gugus yang mengganggu (aluminat, fosfat, silikat dan sebagainya). Unsur yang akan dianalisis tidak akan diikat oleh gugus ini, dengan demikian unsur-unsur yang dianalisa dapat teratomisasi dengan sempurna meskipun di dalam nyala yang suhunya lebih rendah.
Mengekstraksi unsur yang akan dianalisis, terutama cuplikan yang
sangat kompleks.
2) Ionisasi atom-atom pada tingkat dasar
gangguan ini, suhu nyala yang digunakan harus serendah mungkin dimana atomisasi masih dapat berlangsung secara sempurna. Penambahan unsur lain yang mempunyai potensial ionisasi lebih rendah daripada unsur yang dianalisis juga dapat mengurangi gangguan itu. Contoh unsur penyangga adalah Sr dan Li pada penempatan kalsium, juga terdapat fosfat.
c. Gangguan oleh serapan bukan atom
Gangguan ini bahwa penyerapan cahaya dari lampu katoda berongga dan berukuran bukan dari atom-atom netral melainkan dari molekul-molekul, hal ini terutama akan terjadi apabila konsentrasi sampel tinggi dan juga bila suhu nyala kurang tinggi. Cara mengatasi gangguan ini yaitu dengan
menggunakan nyala api yang suhunya lebih tinggi dan mempercepat hasil konsentrasi molekuler dari larutan sampel.
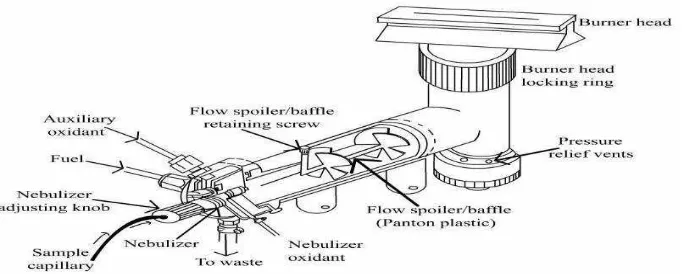
4. Instrumentasi Spektrofotometer Serapan Atom (SSA)
Spektrofotometer Serapan atom memiliki komponen-komponen sebagai berikut (Slavin, 1978):
a. Sumber Sinar
Sumber radiasi Spektofotometer Serapan Atom (SSA) adalah Hollow Cathode Lamp (HCL). Setiap pengukuran dengan SSA harus menggunakan Hollow Cathode Lamp khusus misalnya untuk menentukan konsentrasi tembaga dari suatu cuplikan, maka digunakan Hollow Cathode khusus untuk tembaga.
Hollow Cathode Lamp terdiri dari katoda cekung yang silindris yang terbuat dari unsur yang sama dengan yang akan dianalisis dan anoda yang terbuat dari tungsten. Pemberian tegangan pada arus tertentu, menyebabkan logam mulai memijar dan atom-atom logam katodanya akan teruapkan dengan pemercikan. Atom akan tereksitasi kemudian mengemisikan radiasi pada panjang
gelombang tertentu. Diagram lampu katoda cekung dapat dilihat pada Gambar 2.
Gambar 2. Diagram Lampu Katoda Cekung (Khopkar, 1990). Sumber radiasi lain yang sering dipakai adalah ”Electrodless Discharge
Lamp.” Lampu ini mempunyai prinsip kerja hampir sama dengan Hollow
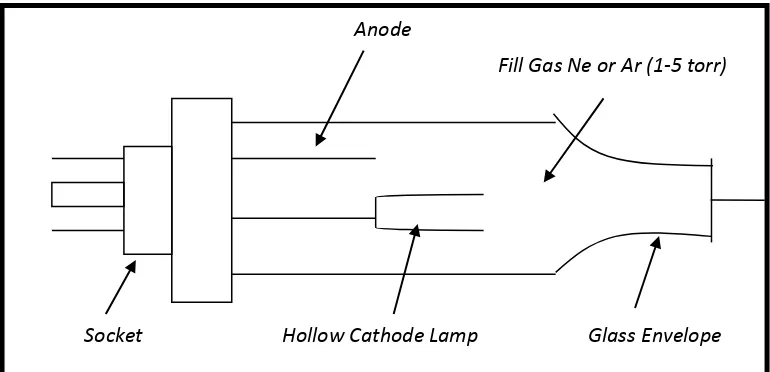
Cathode Lamp (lampu katoda cekung), tetapi mempunyai output radiasi lebih tinggi dan biasanya digunakan untuk analisis unsur-unsur As dan Se, karena lampu HCL untuk unsur-unsur ini mempunyai signal yang lemah dan tidak stabil yang bentuknya dapat dilihat pada Gambar 3.
Socket
Anode
Hollow Cathode Lamp
Fill Gas Ne or Ar (1-5 torr)
Gambar 3. Electrodless Discharge Lamp (Anonim 4, 2003) b. Sumber atomisasi
Sumber atomisasi dibagi menjadi dua yaitu sistem nyala dan sistem tanpa nyala. Kebanyakan instrumen sumber atomisasinya adalah nyala dan sampel diintroduksikan dalam bentuk larutan. Sampel masuk ke nyala dalam bentuk aerosol. Aerosol biasa dihasilkan oleh nebulizer (pengabut) yang
dihubungkan ke nyala oleh ruang penyemprot (Chamber spray). Jenis nyala yang digunakan secara luas untuk pengukuran analitik adalah udara-asetilen dan nitrous oksida-asetilen. Dengan kedua jenis nyala ini, kondisi analisis yang sesuai dengan jenis nyala ini, untuk kebanyakan analit dapat ditentukan dengan menggunakan metode emisi, absorbsi dan juga fluorosensi. Diagram sumber atomisasi dapat dilihat pada Gambar 4.
Nyala udara asetilen.
Biasanya menjadi pilihan untuk analisis mengunakan SSA (Spektrofotometer Serapan Atom). Temperatur nyalanya yang lebih rendah mendorong
terbentuknya atom netral dan dengan nyala yang kaya bahan bakar maka pembentukan oksida dari banyak unsur dapat diminimalkan.
Nitrous oksida-asetilen.
Biasanya digunakan untuk penentuan unsur-unsur yang mudah membentuk oksida dan sulit terurai. Hal ini disebabkan karena temperatur nyala yang dihasilkan relatif tinggi. Unsur-unsur tersebut adalah: Al, B, Mo, Si, So, Ti, V, dan W.
c. Monokromator
Monokromator merupakan alat yang berfungsi untuk memisahkan radiasi yang tidak diperlukan dari spektrum radiasi lain yang dihasilkan oleh Hollow Cathode Lamp .
d. Detektor
Detektor merupakan alat yang mengubah energi cahaya menjadi energi listrik, yang memberikan suatu isyarat listrik berhubungan dengan daya radiasi yang diserap oleh permukaan yang peka.
e. Sistem pengolah
f. Sistem pembacaan
Sistem pembacaan merupakan bagian yang menampilkan suatu angka atau gambar yang dapat dibaca oleh mata.
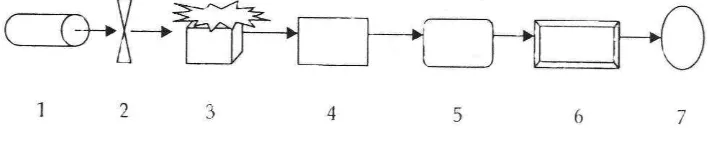
Gambar 5. Skema Instrumentasi Spektrofotometer Serapan Atom (Syahputra, 2004; Azis, 2007)
Keterangan :
1. Sumber sinar 2. Pemilah (Chopper)
3. Nyala
4. Monokromator 5. Detektor 6. Amplifier
MENGESAHKAN
1. Tim Penguji
Ketua : Diky Hidayat, M.Sc. …………..
Sekretaris : Ni Luh Gede Ratna Juliasih, M.Si. ………...
Penguji
Bukan Pembimbing : Dr. Eng. Suripto Dwi Yuwono, M.T. ………...
2. Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Prof. Suharso, Ph.D. NIP 196905301995121001
Judul Skripsi : Kajian Sebaran Logam Berat Cd dan Cr Pada Sedimen di Pesisir Pantai Way Kuala Bandar Lampung
Nama Mahasiswa : Dwi Puji Astuti
Nomor Pokok Mahasiswa : 0717011032
Jurusan : Kimia S1
Fakultas : Matematika dan Ilmu Pengetahuan Alam
MENYETUJUI 1. Komisi Pembimbing
Diky Hidayat, M.Sc. Ni Luh Gede Ratna Juliasih, M.Si.
NIP 197406092005011002 NIP 197707132009122002
2. Ketua Jurusan Kimia
Sesungguhnya bersama kesulitan ada kemudahan
(Q.S. Al-insyirah ayat 8)
Sebaik-baik manusia adalah yang bermanfaat untuk
orang lain. (Hr.Bukhari)
“Kegagalan adalah keberhasilan yang tertunda”
“No Days Without study and pray”
“Tak ada kata
menyerah sebelum mencoba untuk
menjadi yang terbaik”
Hidup Itu adalah pilihan, sukses atau tidak
nantinya, tergantung dari diri kita yang
meyakininya, sesungguhnya Allah bersama kita.
Jadikan diri kita berbeda dari yang lain, jadilah diri
sendiri, maka kita akan SUKSES nantinya.
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta, pada tanggal 2 Sepetember 1989, sebagai anak kedua dari dua bersaudara. Ibu bernama Muhaya, A.P., bapak bernama Sulasman, kakak bernama Hari Febriansyah, S.Pd.I., dan adik bernama Muhammad Ikbal. Jenjang pendidikan diawali dari Taman Kanak-Kanak (TK Aisyiah) tahun1995. Sekolah Dasar (SD) di SD Negeri Bahagia 04 diselesaikan pada tahun 2001. Sekolah Menengah Pertama (SMP) di SMP Negeri 1 Babelan, Bekasi diselesaikan pada tahun 2004, dan Sekolah Menengah Atas (SMA) di SMA Negeri 10 Kota bekasi diselesaikan pada tahun 2007. Tahun 2007, penulis terdaftar sebagai Mahasiswa Jurusan Kimia FMIPA Universitas Lampung melalui jalur SPMB (Seleksi Penerimaan Mahasiswa Baru).
Pemenang Lomba Program Kreativitas Mahasiswa Bidang Penelitian (PKMP), DIKTI, DEPDIKNAS RI tahun 2009; Pemenang Lomba Program Kreativitas Mahasiswa Bidang Penelitian (PKMP), DIKTI, DEPDIKNAS RI tahun 2010; Pemenang Penyeleksian Program Mahasiswa Wirausaha (PMW), DIKTI, DEPDIKNAS RI tahun 2011; Finalis Lomba Proposal Bisnis BEM Unila Tahun 2011; Lolos menjadi 5 Finalis Terbaik perwakilan Lampung, dalam Lomba Inovasi Pemuda IPTEK Nasional, KEMENPORA RI tahun 2011; dan Nominasi Lomba Sociopreneur Nasional ITB FAIR tahun 2012.
Bandar Lampung, 7 Februari 2012
Dwi Puji Astuti, S.Si.
PERSEMBAHAN
Kupersembahkan karya sederhana ini kepada :
Kedua orang tuaku Sulasman dan Muhaya yang selalu menjadi motivator utamaku, terima kasih atas doa, nasihat
dan kasih sayang tulus yang kau berikan sehingga mampu menguatkan aku di saat-saat sulit
.
Kakak dan adikku tersayang
Hari Febriansyah, S.Si., dan Muhammad Ikbal.
Diky Hidayat, M.Sc, Dr. Eng. Suripto Dwi Yuwono, M.T.,. dan Ni Luh Gede Ratna Juliasih, M.Si terima kasih untuk
bimbingannya selama ini.
Segenap Keluarga besarku yang selalu menyemangati dan mendoakan keberhasilanku.
Sahabat ku “dumblee” dan teman-teman kimia 2007 yang selalu berbagi kebahagiaan.
Seseorang yang kelak akan mendampingiku,
SANWACANA
Assalamu’alaikum Wr. Wb.
Alhamdulillah Puji dan syukur Penulis ucapkan atas kehadirat Allah SWT, karena atas segala rahmat dan karunia-Nya skripsi ini dapat diselesaikan.
Skripsi dengan judul "Kajian Sebaran Logam Berat Cd dan Cr Pada Sedimen di Pesisir Pantai Way Kuala Bandar Lampung" adalah salah satu syarat untuk memperoleh gelar Sarjana Sains pada Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung.
Dalam pelaksanaan dan penulisan skripsi ini tidak lepas dari kesulitan dan rintangan, namun itu semua dapat penulis lalui berkat rahmat dan ridha Allah SWT serta bantuan dan dorongan semangat dari orang-orang yang hadir dikehidupan penulis. Dalam kesempatan ini, penulis mengucapkan terima kasih sebesar-besarnya kepada :
skripsi ini terselesaikan dengan baik.
3. Yuli Ambarwati M.Si., selaku pembahas dalam seminar Usul Penelitian yang telah memberikan kritik, saran dan arahan kepada penulis sehingga skripsi ini terselesaikan dengan baik.
4. Dr. Eng. Suripto Dwi Yuwono, M.T. selaku pembahas dalam seminar Hasil Penelitian yang telah memberikan kritik, saran dan arahan kepada penulis sehingga skripsi ini terselesaikan dengan baik.
5. Prof. Dr. Tati Suhartati, M.S., selaku pembimbing Akademik dan ibu yang telah memberikan bimbingan, bantuan, nasehat dan motivasi serta ilmu yang yang bermanfaat kepada penulis.
6. Andi Setiawan, Ph.D., selaku pembimbing dan motivator untuk semua bantuan, kritik dan saran
7. Dian Septiani Pratama, M.Sc. yang telah memberikan bambingan dan bantuan kepada penulis sehingga skripsi ini dapat terselesaikan dengan baik. 8. Seluruh dosen FMIPA Unila yang telah mendidik, memberikan ilmu
pengetahuan dan motivasi yang sangat berguna kepada penulis selama kuliah.
9. Andi Setiawan, Ph.D., selaku ketua Jurusan Kimia FMIPA Unila.
10. Prof. Suharso, Ph.D., selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
dan mendoakan keberhasilanku, serta senyum yang menjadi penyemangatku. Segala hal terbaik dan semua yang telah diberikan kepadaku takkan bisa terganti oleh apapun (maaf Bapak dan ibuku, baru ini yang puji bisa berikan untuk kalian).
12. Kakak dan adikku tersayang, Hari Febriansyah, S.Pd.I., dan Muhammad Ikbal, serta keluarga besarku, terima kasih atas motivasi, doa, keceriaan canda dan tawa keberadaan kalian sangat berarti dalam hidupku.
13. Temen Seperjuanganku dalam penelitian Hafizah Helma, S.Si., dan Yohanes Wikan Agung, S.Si., yang telah bersama menyelesaikan skripsi ini.
14. Sahabat-sahabat terbaikku yang tersayang : “Dumbless”, Andi Yuli Firtiani, S.Si. (yuccy), Eka Sulis Sundari, S.Si., Hade Sastra Wiyana, S.Si. (uni), Clara Citra Resmie (lala), Eka Eprianti, S.Si (mami), Nurtika Kurniati (loned), Halimah, S.Si (umi), Mega Dewi F.S., S.Si (ega), Tristian Martika (Tibo) dan Gia Yustika K.A, S.Si (cikibip), terima kasih atas persahahabatan terhebat, motivasi luar biasa, aku sangat bersyukur dan bangga mengenal kalian, kalian adalah keberhasilanku. “SALAM SUKSES”.
menjalankan perkuliahan, tetap semangat, perjuangan kita masih panjang, sukses selalu untuk kita.
16. Mbak Uyun 06 (makasih pH meternya) mbak Lince 06, mba Eka Eva, mbak Inda, S.Si, Mbak Putri 06, bunda Iin, dan Teman-teman Kimia 2005, 2006, 2008, 2009, 2010 dan 2011 FMIPA Unila Ronny Pramuji dan Anisa Nurfitriyanah terimakasih atas semangatnya, SALAM SUKSES.
17. Sahabat-sahabatku di HIMAKI, BEM FMIPA, UKM-F NATURAL, ROIS FMIPA, FISTEK Unila, TFT MU, Bimbel Salemba Lampung, Bidik Misi Unila, terimakasih untuk kerjasama, kebersamaan, canda tawa, dan pengalaman yang luar biasa.
18. Team NASA PLUS (Munadah, S.P. dan Triyono, A.Md.), terimakasih atas
nasehat dan motivasinya selama ini, “SALAM SUKSES”.
19. Semua pihak yang telah membantu dan mendukung penulis dalam penyusunan skripsi ini.
20. Akhir kata, Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan. Penulis berharap semoga skripsi yang sederhana ini dapat berguna dan bermanfaat bagi kita semua. Amin.
Bandar Lampung, 7 Februari 2012 Penulis
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan hasil analisis dan pembahasan pada penelitian ini, maka dapat disimpulkan sebagai berikut:
1. Konsentrasi logam Cd pada sedimen di muara sungai dan di pesisir pantai Way Kuala Bandar Lampung yaitu pada rentang 0 ppm sampai 0,2522 ± 0,011 ppm.
2. Konsentrasi logam berat Cr pada sampel sedimen di muara sungai dan di pesisir pantai Way Kuala Bandar Lampung yaitu pada rentang 1,243 ± 0,056 ppm sampai 1,361 ± 0,047 ppm.
3. Validasi metode pada penentuan kadar Cd dan Cr pada sedimen menunjukkan presisi dengan nilai RSD < 5 %; koefisien korelasi untuk masing-masing logam Cd dan Cr adalah; 0,999 dan 0,995.
B. Saran
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Maret sampai dengan bulan Agustus 2011 di laboratorium Kimia Analitik Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung dan Laboratorium Kimia Analitik Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Gadjah Mada.
B. Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini adalah : Spektrofotometer Serapan Atom (SSA), eckmen grab Wildco Wildlife Supply Company, ® orbital shaker
gallenhamp®, neraca analitik, botol sampel, kertas saring, pH-meter, termometer, mortar dan peralatan gelas yang umum digunakan di laboratorium.
Bahan-bahan yang digunakan adalah sampel sedimen, HCl pekat, HNO3 pekat, HNO3 1 N, CrCl3·6 H2O , Cd(NO3)2.4H2O dan akuades.
C. Prosedur kerja
1. Pembuatan Larutan
Sebanyak 31,25 mL HNO3 pekat dimasukkan ke dalam labu ukur 500 mL, kemudian ditambahkan akuades sampai tanda batas dan dihomogenkan.
b. Larutan induk Cr 1000 ppm.
Sebanyak 0,5124 gram CrCl3.6 H2Odimasukkan ke dalam labu ukur 100 mL, kemudian ditambahkan akuades hingga tanda batas dan dihomogenkan.
c. Larutan induk Cd 1000 ppm
Sebanyak 0,2744 gram Cd(NO3)2.4H2O dimasukkan ke dalam labu ukur 100 mL, kemudian ditambahkan akuades hingga tanda batas dan dihomogenkan.
2. Metode Pengambilan Sampel
a. Persiapan Pengambilan Sampel
Sebelum melakukan pengambilan sampel, semua wadah dicuci dengan sabun dan dibilas merata dengan air sampai busanya habis, kemudian dibilas dengan HNO3 1 N untuk menghilangkan kontaminasi logam yang menempel dalam wadah sampel. Proses pengeringan dan penyimpanan dilakukan dalam keadaan tertutup sampai digunakan (Sulistiani, 2009).
b. Titik Pengambilan Sampel
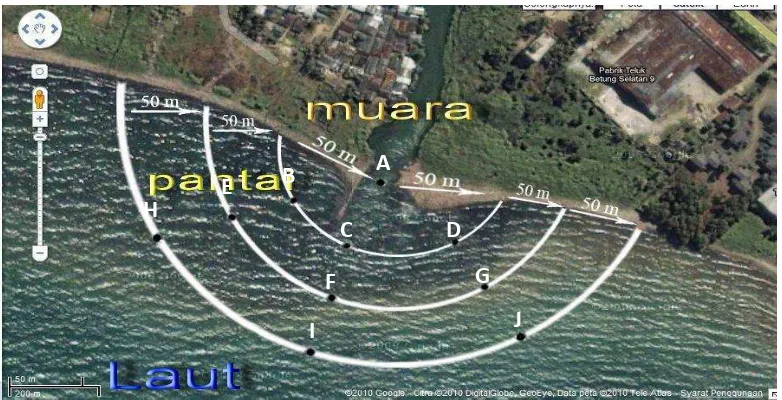
Metode pengambilan sampel sedimen dilakukan dengan stratified sampling,
sedimen diambil hingga kedalaman kurang dari 10-15 meter. Pengambilan sampel sedimen di setiap titik dilakukan pengulangan masing-masing 4 kali. Berikut ini adalah gambar titik pengambilan sampel sedimen.
Gambar 6. Titik Pengambilan Sampel
Keterangan : X° = Titik Koordinat berdasarkan derajat Y’ = Waktu dalam satuan menit
Z “= Waktu dalam satuan detik (google earth, 2011).
Proses pengambilan sampel menggunakan alat EckmenGrabWildco Wildlife Supply Company dilakukan sebanyak 2 kali, yaitu pada minggu kedua di bulan Maret dan minggu ketiga di bulan Mei. Pada saat pengambilan sampel, kondisi iklim di kota Bandar Lampung sedang mengalami musim hujan. Secara umum, iklim merupakan faktor yang berpengaruh terhadap konsentrasi logam berat dalam suatu badan perairan. Kandungan logam berat pada sedimen umumnya tinggi pada musim kemarau dan rendah pada musim penghujan. Tingginya kadar logam berat dalam sedimen pada musim penghujan disebabkan oleh tingginya proses erosi pada permukaan tanah yang terbawa ke dalam badan sungai, sehingga sedimen dalam sungai yang diduga mengandung logam berat akan terbawa oleh arus sungai menuju muara dan pesisir pantai dan pada akhirnya terjadi proses sedimentasi.
3. Preparasi Sampel
Gambar 7. EckmenGrab Wildco Wildlife Supply Company
Selanjutnya sampel ditempatkan ke dalam plastik transparan, sehingga tidak akan terkontaminasi dengan senyawa lain. Sampel sedimen yang telah disiapkan kemudian dikeringkan dalam 2 tahap, yaitu tahap pengeringan di bawah sinar matahari langsung selama 6 jam dan tahap kedua dengan menggunakan oven pada temperatur 120 0C selama 4 jam. Kedua tahap proses pengeringan tersebut
dilakukan karena sampel sedimen yang didapatkan banyak mengandung air sehingga dengan 2 tahap pengeringan akan lebih cepat diperoleh sedimen kering. Sampel sedimen yang telah kering selanjutnya dihaluskan kemudian diayak menggunakan ayakan dengan ukuran 125 mesh. Sampel sedimen yang telah dihaluskan akan memudahkan proses peleburan (leaching).
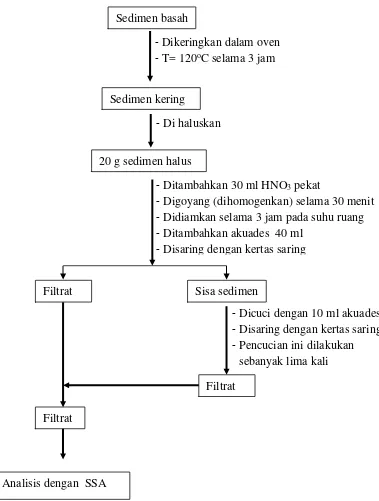
a. Preparasi Sampel Untuk Menentukan Kadar Logam Cd
Sedimen basah dikeringkan dalam oven 120 oC hingga diperoleh berat konstan. Sedimen kering dihaluskan dan disaring dengan ukuran pori 125 mesh,
dimasukkan ke dalam elemeyer kemudian ditambahkan 30 ml HNO3 pekat dan digoyangkan selama 30 menit, kemudian didiamkan selama 3 jam pada suhu ruang. Setelah didiamkan selama 3 jam ditambahkan 40 ml akuades kemudian disaring dengan menggunakan kertas saring. Sisa sedimen pada kertas saring dicuci dengan 10 ml akuades sebanyak lima kali pengulangan sampai pH berkisar 2-3. Filtrat yang dihasilkan kemudian dianalisis dengan
Spektrofotometer Serapan Atom.
b. Preparasi Sampel Untuk Menentukan Kadar Logam Cr
Sedimen basah dikeringkan dalam oven 120 oC hingga diperoleh berat konstan. Sedimen kering dihaluskan dan disaring dengan ukuran pori 125 mesh,
kemudian ditimbang dengan teliti 20. Sedimen yang telah dihaluskan dimasukkan ke dalam gelas piala kemudian ditambahkan HCl dan HNO3 dengan perbandingan 3 :1 dan total jumlah volume 50 mL sampai pH berkisar antara 2-3 dan digoyangkan selama 30 menit, kemudian didiamkan selama 3 jam pada suhu ruang. Setelah didiamkan selama 3 jam, ditambahkan 50 mL akuades kemudian disaring dengan menggunakan kertas saring. Sisa sedimen pada kertas saring dicuci dengan 10 mL akuades sebanyak lima kali
pengulangan. Filtrat yang dihasilkan kemudian diukur dengan Spektrofotometer Serapan Atom untuk menentukan kadar logam Cr.
4. Penentuan Konsentrasi Cd dan Cr pada Sedimen dengan SpektrofotometerSerapan Atom (SSA)
didapat dari manual alat. Pada grafik kurva standar terdapat korelasi antara Konsentrasi (x) dengan Absorbansi (y). Persamaan regresi linier digunakan untuk menentukan konsentrasi dari sampel dengan perhitungan:
y = a+bx
Keterangan :
y : Absorbansi Sampel b : Slope
x : Konsentrasi sampel a : Intersep
Setelah konsentrasi pengukuran diketahui, maka konsentrasi sebenarnya dari Cd dan Cr dalam sampel kering dapat ditentukan dengan persamaan berikut (Siaka, 2008) :
M = CregB. V. F
Keterangan :
M : Konsentrasi logam dalam sampel (mg/Kg)
Creg : konsentrasi yang diperoleh dari kurva kalibrasi (mg/L)
V : Volume larutan sampel (mL) B : Massa sampel (g)
5. Validasi Metode
Penelitian mengenai Kajian Sebaran Logam Berat Cd dan Cr pada sedimen di pesisir pantai Way Kuala Bandar Lampung menggunakan validasi metode. Validasi metode analisis yang digunakan yaitu presisi.
Presisi (ketelitian)
Presisi merupakan ukuran drajat keterulangan dari metode analisis yang
memberikan hasil yang sama pada beberapa perulangan, dinyatakan simpangan baku relatif (RSD) dan simpangan baku (SD). Simpangan baku (SD) dan simpangan baku relatif (RSD) dapat ditentukan dengan persamaan berikut:
SD = √∑ M − M̅ n −
Keterangan :
SD : Standar Deviasi (simpangan baku) M : Konsentrasi hasil analisis
n : Jumlah pengulangan analisis M̅ ∶ konsentrasi rata-rata hasil analisis
RSD = ��
M̅ x %
Keterangan :
Gambar 8. Preparasi Sampel Untuk Logam Cd Sedimen basah
Sedimen kering
-Dikeringkan dalam oven -T= 120oC selama 3 jam
20 g sedimen halus
-Ditambahkan 30 ml HNO3 pekat
-Digoyang (dihomogenkan) selama 30 menit -Didiamkan selama 3 jam pada suhu ruang -Ditambahkan akuades 40 ml
-Disaring dengan kertas saring -Di haluskan
Filtrat Sisa sedimen
-Dicuci dengan 10 ml akuades -Disaring dengan kertas saring -Pencucian ini dilakukan
sebanyak lima kali
Filtrat
Filtrat
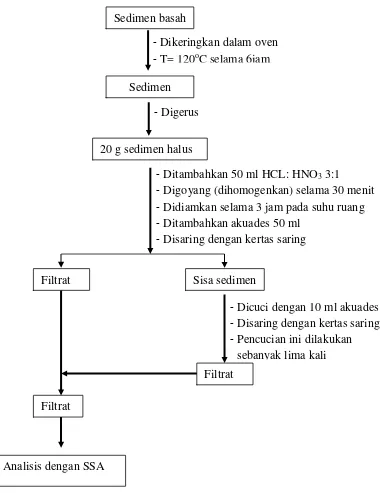
Gambar 9. Preparasi Sampel Untuk Logam Cr Sedimen basah
Sedimen
-Dikeringkan dalam oven -T= 120oC selama 6jam
20 g sedimen halus
-Ditambahkan 50 ml HCL: HNO3 3:1
-Digoyang (dihomogenkan) selama 30 menit -Didiamkan selama 3 jam pada suhu ruang -Ditambahkan akuades 50 ml
-Disaring dengan kertas saring -Digerus
Filtrat Sisa sedimen
-Dicuci dengan 10 ml akuades -Disaring dengan kertas saring -Pencucian ini dilakukan
sebanyak lima kali
Filtrat
Filtrat