UIN SYARIF HIDAYATULLAH JAKARTA
UJI ANTIFERTILITAS EKSTRAK N-HEKSANA BIJI JARAK
PAGAR (Jatropha curcas L.) PADA TIKUS PUTIH JANTAN
(Rattus novergicus) GALUR Sprague Dawley SECARA IN VIVO
SKRIPSI
INDAH FADLUL MAULA
NIM : 109102000037
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI
UIN SYARIF HIDAYATULLAH JAKARTA
UJI ANTIFERTILITAS EKSTRAK N-HEKSANA BIJI JARAK
PAGAR (Jatropha curcas L.) PADA TIKUS PUTIH JANTAN
(Rattus novergicus) GALUR Sprague Dawley SECARA IN VIVO
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
INDAH FADLUL MAULA
NIM : 109102000037
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI
Skripsiiniadalahhasilkaryasayasendiri,
dansemuasumberbaik yang dikutipmaupundirujuk
telahsayanyatakandenganbenar.
Nama :Indah Fadlul Maula
NIM : 109102000037
Tandatangan :
Nama : Indah Fadlul Maula Program Studi : Farmasi
Judul Skripsi :Uji Antifertilitas Ekstrak n-heksana Biji Jarak Pagar (Jatropha curcas L.) Pada Tikus Putih Jantan (Rattus Novergicus) Galur Sprague Dawley Secara In Vivo
Penelitian ini dilakukan untuk mengevaluasi pengaruh pemberian ekstrak n-heksanabiji jarak pagar (Jatropha curcasL.) pada beberapa parameterreproduksi tikus jantan. Beberapa penelitian terkait topik ini sudah dilakukan dalam ekstrak etanol dan etil asetat, sedangkan dalam penelitian kali ini yang digunakan adalah ekstrak n-heksana. Ekstrak diberikan secara oral sekali sehari dalam 48 hari. Sampel terdiri dari 20 ekor tikus galur Sprague Dawley yang dibagi 4 kelompok yaitu kelompok I, II (5mg/kg BB), III (25mg/kg BB), dan IV (50 mg/kg BB). Kelompok I merupakankontrol negatif dengan perlakuan Na CMC1 %. Data dianalisa menggunakan analisis one way Anova dan dilanjutkan dengan uji Multiple Comparisons jenis LSD. Hasil penelitian menunjukkan pemberian ekstrak n-heksana biji jarak pagar dengan dosis 5 mg/kg BB, 25 mg/kg BB, dan 50 mg/kg BB memberikan penurunan yang bermakna (p≤0,05) terhadap konsentrasi spermatozoa, berat testis, dan diameter tubulus seminiferus. Jumlah spermatosit pakiten dihitung pada seluruh tahapan dan perbandingan jumlah spermatosit pakiten per sel Sertoli masing-masing dihitung dalam tahap II,VII dan XII dari siklus epitel seminiferus. Hasil menunjukkan perbedaan yang bermakna antara kelompok kontrol dan kelompok perlakuan dosis 25 mg/kg BB dan 50 mg/kg BB berupa penurunan jumlah spermatosit pakiten pada kelompok perlakuan (p≤ 0,05). Ekstrak n-heksana biji jarak pagar dosis 5 mg/kg BB dan 25 mg/kgBB tidak menunjukkan penurunan jumlah spermatosit pakiten per sel Sertoli secara bermakna (p≥0,05) dalam setiap tahapan, namun dosis 50 mg/kgBB dapat menurunkan jumah spermatosit pakiten per sel Sertoli dalam setiap tahapan secara tidak bermakna (p ≥ 0,05).Kedepan diharapkan hasil penelitian dapat dikembangkan sebagai bahan kontrasepsi pria.
Name : Indah Fadlul Maula Program Study : Pharmacy
Title : Study of Antifertility Effect of n-hexane Extract of Jatropha curcas seeds in White Male (Rattus novergicus) Sprague Dawley
Rats In Vivo
The present study is conducted to evaluate the antifertile effect of n-hexane extract of Jatropha curcas seed on reproductive parameters of male rats. Several studies towards the same topic had done in an ethanolic and ethyl acetate extract, while this study used n-hexane extract which owned a non polar characteristic. The extract was given orally once a day in 48 days. The sample consisted of 20 rats Sprague Dawley strain that were divided four groups: control group, treatment I (5 mg/Kg body weight), II (25 lowering the sperm concentration, testis weight, and diameter of seminiferous tubules (p≤0,05). Numbers of pachytene per Sertoli cell were also counted in all stages and the numbers of pachytene per Sertoli cell were counted in stages II,VII and XII of the cycle of the seminiferous epithelium.The results showed significant difference between the control, treatment with 25 mg/Kg body weight dosage and treament with 50 mg/Kg body weightdosage group which existed as the decreasing numbers of pachyten spermatocytes in treatment groups (p≤ 0,05).n-heksana extract of Jatrophacurcas seed 5 mg /Kg body weight dosage and 25 mg/Kg body weight showed no decreasing effect in the numbers of pachytene spermatocytes per Sertoli cells, significantly (p≥0,05), in every stage. While 50 mg/Kg body weight dosage decreasing the numbers of pachytene spermatocytes per Sertoli cells in each stage,unsignificantly (p≥0,05). It is expected that the result of this study can be developed into a male contraception.
Puja dan puji syukur senantiasa saya panjatkan kehadirat Ilahi Rabbi, Tuhan Yang Maha Esa, atas segala rahmat, karunia, hidayah, serta inayah-Nya, saya dapat menyelesaikan penulisan skripsi ini. Penulisan skripsi ini dilakukan dalam rangka untuk memenuhi tugas akhir sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Kedokteran dan Ilmu Kesehatan Program Studi Farmasi Universitas Islam Negeri (UIN) Syarif Hidayatullah, Jakarta.
Dalam proses penelitian dan penyusunan skripsi ini penulis menyadari banyak pihak yang membantu dan sangat memberikan kontribusi kepada penulis. Maka pada kesempatan ini penulis ingin menyampaikan rasa terima kasih dan penghargaan kepada :
1. Prof. Dr. (hc) dr. M. K. Tadjudin, Sp.And, Dekan Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta sekaligus bertindak selaku pembimbing I, terima kasih atas ilmu, arahan, bimbingan dan kesabaran dalam meluangkan waktu, pikiran dan tenaga untuk membimbing penulis selama ini.
2. Drs. Umar Mansur M.Sc, Apt selaku Ketua Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta
3. Azrifitria, M.Si, Apt sebagai pembimbing II, terimakasih telah banyak memberikan ilmu, pengarahan, bimbingan, dukungan serta perhatian yang begitu besar kepada penulis selama menyusun skripsi ini.
4. Bapak dan Ibu Dosen Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan atas ilmu yang telah diberikan kepada penulis.
5. Seluruh kakak laboran (kak eris, kak tiwi, kak lisna, dll) yang sangat membantu penulis selama penelitian di kampus.
6. Kedua orang tua, abah saya Maftuh Aziz dan umi saya Masiroh, yang senantiasa memberikan pengertian, dorongan, semangat, dukungan dan perhatian terbesar bagi penulis baik secara moril dan materiil.
7. Adik – adik tercinta, Muhammad Nazieh Elfikar, Kanza Rufaida, dan Matswa Akrimi atas setiap motivasi, doa dan dukungannya bagi penulis.
8. Mbak yuyun sekeluarga yang telah membantu penulis mendapatkan sampel penelitian, serta kak Widya Dwi Arini yang telah membantu dan membimbing penulis selama penelitian.
9. Gian pertela, yang telah menjadi rekan, sahabat, sekaligus keluarga terbaik bagi penulis.
11.Sahabat-sahabat tersayang yang selalu ada (Nadya, Arif, Irsyad, Puput, Emma, Bella, Ulfa, Zia, Caca, Neneng, Dyah, Cucut, Nisa, Zil Ardi) yang tak henti memberikan doa, semangat dan masukan untuk kelancaran penyusunan skripsi.
12.Sahabat Al-muna, (Acan, Syifa, Isma, Fanny, Lita, Noveline, Mbak Nia, Masna) atas setiap dukungan kepada penulis selama penyusunan skripsi.
13.Sahabat tersayang, Sujatna, Nurul Pradana sari, Arina Aisyalhana, Soraya Reza, Matlaun Huda, Dhanang ML, Faris Aziz, Muhammad Khairiskam, atas kebaikan, doa, dan dukungan selama proses penyusunan skripsi.
14.Keluarga besar BEM Farmasi 2012 dan BIMKES 2013 atas segala pengertian, dukungan dan doa yang diberikan kepada penulis.
15.Teman-teman Farmasi 2009 yang tidak dapat saya sebutkan satu persatu, terima kasih atas doa, dukungan, dan persaudaraannya selama ini.
16.Pihak-pihak yang tidak dapat disebutkan satu-satu oleh penulis, yang telah membantu penyelesaian skripsi.
Akhirnya dengan segala kerendahan hati, penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, maka penulis mengharapkan kritik dan saran pembaca yang bersifat membangun guna memperbaiki kemampuan penulis.
Jakarta, 1 Januari 2014
TUGAS AKHIR UNTUK KEPENTINGAN AKADEMIS
Sebagai civitas akademik Universitas Islam Negeri (UIN) Syarif
Hidayatullah Jakarta, saya yang bertanda tangan di bawah ini :
Nama : Indah Fadlul Maula
NIM : 109102000037
Program Studi : Farmasi
Fakultas : Kedokteran dan Ilmu Kesehatan
Jenis karya : Skripsi
Demi kepentingan ilmu pengetahuan, saya menyetujui skripsi /
karya ilmiah saya dengan judul :
Uji Antifertilitas Ekstrak n-heksana Biji Jarak Pagar (Jatropha curcas L.) pada Tikus Putih Jantan (Rattus novergicus) Galur
Sprague Dawleysecara In Vivo
untuk dipublikasikan atau ditampilkan di internet atau media lain
yaitu Digital Library Perpustakaan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta untuk kepentingan akademik sebatas
sesuai dengan Undang-undang Hak Cipta.
Demikian pernyataan persetujuan publikasi karya ilmiah ini saya
buat dengan sebenarnya.
Dibuat di : Jakarta
Tanggal : Januari 2014
Yang menyatakan :
Halaman
HALAMAN JUDUL ... ii
HALAMAN PERNYATAAN ORISINALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ... iv
HALAMAN PENGESAHAN SKRIPSI... v
ABSTRAK ... vi
ABSTRACT ... vii
KATA PENGANTAR ... viii
HALAMAN PERSETUJUAN PUBLIKASI ... x
DAFTAR ISI ... xi
2.5Sistem Reproduksi Tikus Jantan ... 16
2.5.1 Produksi Sperma ... 18
BAB 3 METODE PENELITIAN ... 23
3.4.1 Pemeriksaan Simplisia (Determinasi) ... 25
3.4.2 Penyiapan Simplisia ... 25
3.4.3 Pembuatan Ekstrak ... 25
3.4.4 Penapisan Fitokimia ... 25
3.4.5 Parameter Spesifik dan Non Spesifik Ekstrak ... 28
3.4.6Persiapan Hewan Uji ... 29
3.4.7 Pemberian Perlakuan ... 30
3.4.8 Pembuatan Preparat ... 30
3.4.9 Pengukuran Bobot Testis ... 31
3.4.10. Pengukuran Konsentrasi Spermatozoa ... 31
3.4.11 Pengukuran Jumlah Sel Germinal & Diameter Tubulus Seminiferus ... 33
3.5Analisis Data ... 34
BAB 4 : HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian ... 35
4.1.7 Perhitungan Konsentrasi Spermatozoa ... 38
4.1.8 Pengukuran Diameter Tubulus Seminiferus ... 40
4.1.9 Perhitungan Jumlah Spermatosit Pakiten dan Sel Sertoli ... 42
4.2 Pembahasan ... 45
BAB 5 : KESIMPULAN DAN SARAN ... 53
5.1 Kesimpulan ... 53
5.2 Saran ... 53
Tabel Halaman
1. Data Biologis Tikus ... ... 15
2. Pengenceran yang Dilakukan dan Kotak yang Dihitung………... ... 32
3. Cara Pengenceran ... ... 32
4. Rumus Konsentrasi Spermatozoa... 33
5. Hasil Penapisan Fitokimia Serbuk dan Ekstrak n-heksana Biji Jarak Pagar ... 35
6. Parameter Standar Simplisia dan Ekstrak ... 36
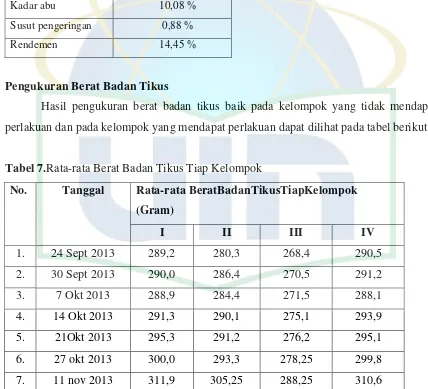
7. Rata-rata Berat Badan Tikus Tiap Kelompok ... 36
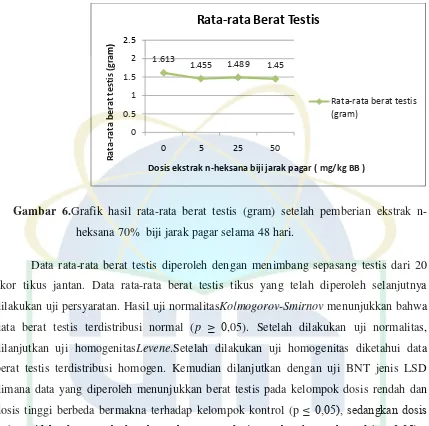
8. Rata-rata Berat Testis Tikus Kelompok Kontrol dan Kelompok Perlakuan ... 37
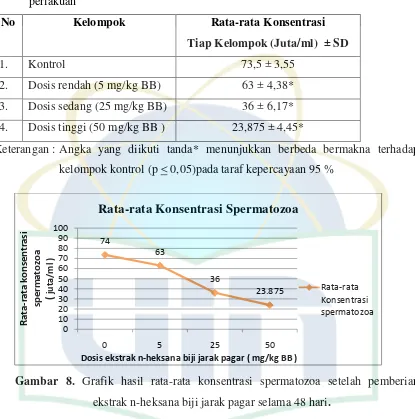
9. Rata-rata Konsentrasi Spermatozoa Tikus Kelompok Kontrol dan Kelompok Perlakuan ... 39
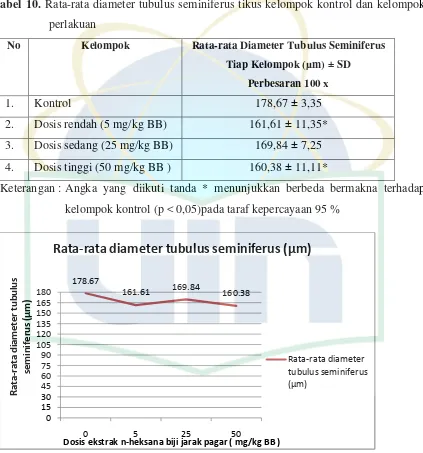
10.Rata-rata Diameter Tubulus Seminiferus Tikus Kelompok Kontrol dan Kelompok Perlakuan ... 40
11.Rata-rata Jumlah Spermatosit Pakiten... 43
12.Rata-rata Jumlah Sel Sertoli ... 44
13.Berat Badan Tikus Tiap Kelompok ... 45
14.Hasil Pengukuran Bobot Testis ... 72
15.Hasil Perhitungan Konsentrasi Spermatozoa ... 73
16.Hasil Pengukuran Diameter Tubulus Seminiferus ... 74
17.Hasil Perhitungan Jumlah Spermatosit Pakiten per Sel Sertoli... 75
18.Hasil Perhitungan Jumlah Spermatosit Pakiten ... 76
19.Hasil Uji Normalitas Berat Testis Tikus ... 77
20.Hasil Uji Homogenitas Berat Testis Tikus ... 77
21.Hasil Uji BNT Berat Testis Tikus ... 78
22.Hasil Uji Normalitas Konsentrasi Spermatozoa... 79
23.Hasil Uji Homogenitas Konsentrasi Spermatozoa ... 80
24.Hasil Uji BNT Konsentrasi Spermatozoa ... 81
25.Hasil Uji Normalitas Diameter Tubulus Seminiferus ... 82
26.Hasil Uji Homogenitas Diameter Tubulus Seminiferus ... 83
27.Hasil Uji ANOVA Diameter Tubulus Seminiferus... 84
28.Hasil Uji BNT Diameter Tubulus Seminiferus ... 85
29.Hasil Uji Normalitas Jumlah Spermatosit Pakitendansertoli ... 86
30.Hasil Uji Homogenitas Jumlah Spermatosit Pakiten ... 87
31.Hasil Uji ANOVA Jumlah Spermatosit Pakiten ... 87
Gambar Halaman
1. Bunga, buah dan biji Jatropha curcas L ... 9
2. Anatomi sistem reproduksi tikus jantan……… .... 16
3. Spermatozoa tikus... ... 18
4. Tahapan dari siklus sel spermatogenesis pada tikus ... 19
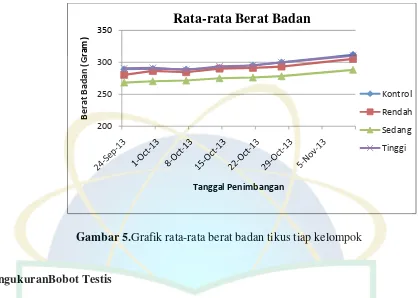
5. Grafik rata-rata berat badan tikus tiap kelompok ... 37
6. Grafik hasil rata-rata berat testis setelah pemberian ekstrak n-heksana biji jarak pagar selama 48 hari ... 38
7. Grafik hasil rata-rata konsentrasi spermatozoa (juta/ml) setelah pemberian ekstrak n-heksana biji jarak pagar selama 48 hari ... 39
8. Grafik hasil rata-rata diameter tubulus seminiferus setelah pemberian ekstrak n-heksana biji jarak pagar selama 48 hari... 40
9. Grafik hasil rata-rata jumlah spermatosit pakiten setelah pemberian ekstrak n-heksana biji jarak pagar selama 48 hari ... 43
10.Grafik hasil rata-rata jumlah selsertoli setelah pemberian ekstrak n-heksana biji jarak pagar selama 48
17.Serbuk simplisia biji jarak pagar ... 63
18.Tikus putih jantan galur Sprague Dawley ... 63
19.n-heksana ... 63
20.Ekstrak kental n-heksan biji jarak pagar ... 63
21.Larutan Na CMC 1%... 63
28.Timbangan berat badan hewan uji (Ohauss) ... 64
32.Freeze dry (Eyela FDU 1200)) ... 65
33.Mikropipet ukuran 200 µl ... 65
34.Mikropipet ukuran 10-20 µl ... 65
35.Mikroskop optik (Motic BA310) ... 65
36.Haemositometer Improved Neubeur ... 65
37.Penimbangan serbuk simplisia biji jarak pagar ... 66
38.Maserasi serbuk simplisia biji jarak pagar dengan n-heksan ... 66
39.Pemekatan maserat ... 66
40.Penyaringan maserat ... 66
41.Proses freeze dry ekstrak cair n-heksan biji jarak pagar ... 66
42.Pembuatan larutan Na CMC 1% ... 66
43.Pemberian makan hewan uji ad libitum ... 66
44.Pemberian minum hewan uji ad libitum ... 66
45.Penimbangan berat badan hewan uji ... 67
46.Pemberian ekstrak secara oral menggunakan alat pencekok oral ... 67
47.Pembiusan hewan uji ... 67
48.Pembedahan hewan uji ... 67
49.Pengeluran cairan sperma dari cauda epididymis dengan bantuan cairan NaCl ... 67
50.Pencucian organ testis dengan larutan NaCl fisiologis ... 67
51.Epididimis ... 68
52.Pengawetan organ testis ... 68
53.Penimbangan organ testis ... 68
54.Organ testis dan epididymis ... 68
55.Pengambilan cairan spermatozoa ... 68
56.Pengenceran spermatozoa dengan larutan george ... 68
57.Spermatozoa pada kamar hemositometer ... 68
58.Pengamatan spermatozoa di bawah mikroskop dengan perbesaran 400x ... 68
59.Kontrol,tahap II, Perbesaran 400x... 90
60.Kontrol,tahap VII, Perbesaran 400x ... 90
61.Kontrol,tahap XII, Perbesaran 400x ... 90
62.Perlakuan Ekstrak n-heksan Biji Jarak Pagar (5 mg/kg BB), tahap II, Perbesaran 400x ... 91
63.Perlakuan Ekstrak n-heksan Biji Jarak Pagar (5 mg/kg BB), tahap VII, Perbesaran 400x` ... 91
tahap VII, Perbesaran 400x ... 92 67.Perlakuan Ekstrak n-heksan Biji Jarak Pagar (25 mg/kg BB),
tahap XII,
Perbesaran 400x ... 92 68.Perlakuan Ekstrak n-heksan Biji Jarak Pagar (25 mg/kg BB),
Perbesaran 400x ... 93 69.Perlakuan Ekstrak n-heksan Biji Jarak Pagar (50 mg/kg BB),
tahap II, Perbesaran 400x ... 94 70.Perlakuan Ekstrak n-heksan Biji Jarak Pagar (50 mg/kg BB),
tahap VII, Perbesaran 400x ... 94 71.Perlakuan Ekstrak n-heksan Biji Jarak Pagar (50 mg/kg BB),
tahap XII, Perbesaran 400x ... 94 72.Perlakuan Ekstrak n-heksan Biji Jarak Pagar (50 mg/kg BB),
Lampiran Halaman
1. Hasil Determinasi Tanaman ... 61
2. Hasil Penapisan Fitokimia Ekstrak n-heksan Biji Jarak Pagar ... 62
3. Gambar Bahan dan Alat Penelitian ... 63
4. Gambar Kegiatan Penelitian Uji Antifertilitas Ekstrak n-heksan Biji Jarak Pagar ... 66
5. Pengamatan Parameter Ekstrak ... 69
6. Alur penelitian ... 70
7. Perhitungan Dosis Uji Ekstrak Biji Jarak ... 71
8. Hasil Pengukuran Bobot Testis ... 72
9. Hasil Perhitungan Konsentrasi Spermatozoa ... 73
10.Hasil Pengukuran Diameter Tubulus Seminiferus ... 74
11.Hasil Perhitungan Jumlah Spermatozoa Pakiten per Sel Sertoli ... 75
12.Analisis Data Berat Testis ... 77
13.Analisis Data Konsentrasi Spermatozoa ... 79
14.Analisis Data Diameter Tubulus Seminiferus ... 82
15.Analisa Data Jumlah Spermatosit Pakiten dan Sel Sertoli ... 86
16.Histologi Tubulus Seminiferus Testis Tikus Kontrol ... 90
17.Histologi Tubulus Seminiferus Testis Tikus Perlakuan Ekstrak n-heksan Biji Jarak Pagar (5 mg/kgBB) ... 91
18.Histologi Tubulus Seminiferus Testis Tikus Perlakuan Ekstrak n-heksan Biji Jarak Pagar (25 mg/kgBB) ... 92
BAB I
PENDAHULUAN
1. 1. LATAR BELAKANG
Kepadatan kependudukan di Indonesia merupakan suatu permasalahan
yang mengalami perkembangan kompleksitas disetiap tahunnya, terlebih
mengenai permasalahan yang mengacu pada aspek pengendalian kuantitas
penduduk. Data terakhir menunjukkan angka pertumbuhan di Indonesia
bertambah 32,5 juta jiwa, dengan rata-rata pertumbuhan 1,49 % pada sensus yang
dilakukan tahun 2010. Dengan persen rata – rata pertumbuhan sebesar 1,49, jika tidak disertai aspek pengendalian kuantitas penduduk, peningkatan kualitas
penduduk dan pengarahan mobilitas penduduk, Indonesia berpotensi mengalami
ancaman ledakan penduduk kedepan. (BKKBN, 2012). Keluarga Berencana (KB),
program yang merupakan bagian dari pembangunan nasional, memegang peranan
penting dalam mengatasi permasalahan tersebut melalui pelaksanaan fungsi
kontrol terhadap ketiga aspek yang telah dipaparkan diatas.
Optimalisasi pelaksanaan program Peserta KB idealnya dicapai dengan
peningkatan peran serta penduduk, baik pria maupun wanita, dalam ber-KB. Akan
tetapi pada kenyatannya di Indonesia masih didominasi oleh
perempuan.Pemerintah dengan berbagai sumber daya yang ada telah berupaya
untuk meningkatkan kesertaan pria dalam ber-KB. Namun hasilnya belum seperti
yang diharapkan. (BKKBN, 2008). Keikutsertaan pria dalam ber-KB masih
minim, pilihannya masih berbatas pada penggunaan salah satu cara atau metode
pencegahan kehamilan, seperti kondom, vasektomi, serta KB alamiah yang
melibatkan pria/suami (metode sanggama terputus dan metode pantang berkala)
(Bhakti Ekarini, 2008).
Di Indonesia, terdapat berbagai tanaman yang berkhasiat menghasilkan
aktifitas antifertilitas (Hartini, 2011). Hal ini dapat menjadi solusi, mengingat
animo masyarakat Indonesia belakangan ini lebih memilih alternatif
lebih aman dari efek samping dibandingkan dengan obat sintetik (Andria, 2012).
Animo ini juga didukung dengan kondisi alam Indonesia yang kaya akan sumber
daya tanaman obat, sehingga mempunyai peluang untuk memperoleh kontrasepsi
tikus jantan yang berasal dari tanaman. Penelitian diharapkan tidak hanya
berfokus pada perkembangan efektivitas dan keamanan kontrasepsi priatetapi
jugasecara ideal memiliki khasiat jangka lama, tetapi bersifat reversibel dalam hal
menyebabkan azoospermia (tidak adanya sperma didalam semen)(BKKBN, 2006).
Beberapa penelitian telah dilakukan menggunakan beberapa jenis tanaman
yang kemudian diteliti efeknya terhadap organ reproduksi pria. Di Indonesia,
terdapat beberapa jenis tanaman yang telah diteliti efeknya terhadap organ
reproduksi jantan. Beberapa tanaman tersebut adalah ekstrak etanol batang
manggarsih dimana selama 35 hari mampu menyebabkan penurunan jumlah
spermatosit sekunder dan jumlah spermatozoa mencit namun tidak mampu
menyebabkan penurunan berat testis, diameter tubulus seminiferous testis, jumlah
spermatogonium, jumlah spermatosit primer, dan jumlah spermatid
(Ulimaz,2010).
Dari penelitian Yurnadi dkk (2002) diketahui bahwa penyuntikan ekstrak
biji pepaya selama 20 hari (1,5 siklus epitel seminiferus) pada berbagai dosis
terhadap tikus belum dapat menurunkan konsentrasi spermatozoa vas deferen,
akan tetapi dapat menurunkan populasi sel spermatogonium A dan spermatosit
primer preleptoten. Selain itu, pada tanaman Momordica charantia L. dengan pemberian selama 20 hari memberikan hasil penurunan pada jumlah spermatozoa
dan pada 40 hari memberikan hasil penurunan jumlah spermatozoa yang lebih
banyak. Namun, pada pemberian Momordica charantia L. selama 60 hari tidak memberikan perubahan yang bermakna (Saptogino & Juniarto, 2010)
Salah satu penelitian yang juga mengambil fokus pada tanaman yang
pengobatan yang besar. Ekstrak tanaman dapat digunakan untuk mengobati alergi,
luka bakar, peradangan, kusta, leucoderma, kudis dan cacar. (Sachdeva et al.,
2012).Penggunaanobattradisional untukekstrakdari bijijarak pagar diantaranya
sebagai pencahar, abortivum, antipiretik, antihelmintik, serta pengobatan gout dan
gonorrhea (Barceloux, 2008).). Menurut Ejelonu et al. (2010), hasil skrining
fitokimia dari biji jarak pagar positif mengandung terpenoid, alkaloid, cardenolid,
dan steroid. Kandungan lainnya adalah lemak, protein, karbohidrat, dan air (Tim
Departemen Teknologi Pertanian, 2005).Dalam suatu penelitian dilaporkan bahwa
dengan pemberian ekstrak n-heksanbiji jarak pagar diberikan secara oral
mempunyai aktivitas antifertilitas pada tikus betina. (Ahirwar et al., 2010).
Sebelumnya, penelitian tentang tanaman jarak pagar dan potensinya
terhadap antifertilitas pada tikus jantan secara tradisional belum banyak diteliti di
Indonesia, disamping itu penggunaan biji jarak pagar pada sistem reproduksi tikus
jantan pun masih belum dilaporkan. Penelitian yang dilakukan oleh Widya Dwi
Arini tersebut adalah untuk mengetahui aktivitas antifertilitas dari ekstrak
n-heksan biji jarak pagar (Jatropha curcas L. ) pada fungsi reproduksi tikus jantan ditinjau dari karakteristik sperma, konsentrasi sperma, serta ukuran diameter
tubulus seminiferus testis.Dari penelitian tersebut dikemukakan kesimpulan
bahwa biji jarak pagar dapat menyebabkan infertilitas sehingga dapat
dikembangkan sebagai bahan dasar obat kontrasepsi tradisional tikus jantan.
Makin besar dosis yang diberikan, makin besar pula pengaruhnya terhadap
penuruanan konsentrasi spermatozoa, bobot testis dan diameter tubulus
seminiferus.
Penelitian yang dilakukan oleh Widya Dwi Arini menarik untuk ditindak
lanjuti, mengingat aspek yang diamati baru sampai pada tingkat ekstrak etanol
dari sampel, atau dengan kata lain masih berkonsentrasi pada fase polar. Belum
ada penelitian yang dilaporkan menindaklanjuti penelitian terkait biji jarak pagar
dan aktivitas antifertilitasnya terhadap tikus jantan ini sampai ke fase non-polar
dan semi-polarnya. Beberapa data yang sudah ada mengacu masih terbatas pada
tikus betina sebagai objeknya, seperti yang diungkapkan pada Ahirwar et al.,
steroid (Ahirwar et al., 2010) kandungan kimia dari biji jarak adalah senyawa
seperti viteksin, isoviteksin (Aregheore et.al., 2003), beta-sitosterol dan curcin
(Mastiholimath, 2008), saponin (Punsuvona et. al., 2012). Seperti diketahui bahwa
senyawa beta-sitosterol termasuk dalam golongan senyawa sterol tumbuhan.
Senyawa sterol merupakan turunan dari senyawa steroid.
Hal ini melatarbelakangi perlunya penelitian lebih lanjut pengaruh aktifitas
antifertilitas biji jarak terhadap organ reproduksi tikus jantan pada fase
non-polarnya, dimana dalam hal ini pelarut yang digunakan adalah n-heksana. Dengan
menggunakan pelarut yang berbeda ini diharapkan dapat memberikan gambaran
perbandingan signifikansi aktifitas antifertilitas biji jarak terhadap tikus putih
jantan dalam berbagai ekstrak, dari pelarut yang bersufat polar (yang telah dilakukan) hingga non polar. Maka penelitian “Uji Antifertilitas Ekstrak n-heksana Biji Jarak Pagar (jatropha curcas l.) pada Tikus Putih Jantan (Rattus novergicus) Galur Sprague Dawley Secara In Vivo” ini adalah untuk menguji aktivitas antifertilitas dari ekstrak n-heksana biji jarak pagar (Jatropha curcas L.)
pada fungsi reproduksi tikus jantan ditinjau dari konsentrasi sperma, berat testis,
ukuran diameter tubulus seminiferus testis, serta jumlah spermatosit pakiten dan
sel sertoli.
1.2. RUMUSAN MASALAH
Berdasarkan uraian dari latar belakang, maka rumusan masalah adalah
sebagai berikut :
1. Laju pertumbuhan penduduk indonesia mengalami kenaikan angka
yang signifikan dan berpotensi menimbulkan ledakan penduduk
2. Hingga saat ini, penggunaan kontrasepsi pada pria masih terbatas pada
pilihan kondom dan vasektomi, belum dilaporkan adanya pilihan
antifertilitas dalam bentuk sediaan oral
3. Penelitian terkait aktivitas antifertilitas dari sampel tanaman jarak
4. Hingga saat ini belum ada penelitian yang melakukan penelitian
terkait keberadaan komponen senyawa yang berkhasiat terhadap
aktivitas antifertilitas dari biji jarak pada tikus jantan pad ekstrak
n-heksana
1.3. TUJUAN PENELITIAN
Tujuan dari penelitian uji antifertilitas ekstrak n-heksana biji jarak
pagar ( Jatropha curcas L. ) pada tikus jantan galur Sprague Dawley secara in vivo sebagai berikut :
1. Untuk mengetahui aktivitas ekstrak n-heksana biji jarak pagar
(Jatropha curcas L. ) terhadap konsentrasi spermatozoa tikus jantan (Rattus Novergicus) galur Sprague Dawley secara in vivo
2. Untuk mengetahui aktivitas ekstrak n-heksana biji jarak pagar
(Jatropha curcas L. ) terhadap bobot testis tikus jantan (Rattus Novergicus) galur Sprague Dawley secara in vivo
3. Untuk mengetahui aktivitas ekstrak n-heksana biji jarak pagar
(Jatropha curcas L. ) terhadap tahapan spermatogenesis tikus jantan (Rattus Novergicus) galur Sprague Dawley secara in vivo
4. Untuk mengetahui aktivitas ekstrak n-heksana biji jarak pagar
(Jatropha curcas L. ) terhadap diameter tubulus seminiferus pada tikus jantan galur Sprague Dawley secara in vivo
1.4. HIPOTESIS
Hipotesis dari penelitian uji antifertilitas ekstrak n-heksana biji
jarak pagar ( Jatropha curcas L. ) pada tikus jantan galur Sprague Dawley secara in vivo sebagai berikut :
1. Pemberian ekstrak n-heksana biji jarak pagar (Jatropha curcas L.) dapat menurunkan konsentrasi spermatozoa tikus jantan galur
Sprague Dawley
3. Pemberian ekstrak n-heksanabiji jarak pagar (Jatropha curcas L.) mempunyai efek terhadap berkurangnya diameter tubulus
seminiferus pada tikus jantan galur Sprague Dawley
4. Pemberian ekstrakn-heksana biji jarak pagar (Jatropha curcas L.) dapat mengganggu tahapan spermatogenesistikus jantan galur
Sprague Dawley
1.5. MANFAAT PENELITIAN
Dari penelitian uji antifertilitas ekstrakn-heksana biji jarak pagar (
Jatropha curcas L. ) pada tikus jantan galur Sprague Dawley secara in vivodiharapkan dapat memberi manfaat sebagai berikut :
1. Memberi kontribusi terhadap penegakan program KB sebagai
bagian dari upaya mencegah terjadinya ledakan penduduk dengan
memberikan pilihan obat kontrasepsi bagi pria
2. Memberikan informasi kepada masyarakat luas tentang manfaat
biji jarak pagar (Jatropha curcas L. ) sebagai obat antispermatogenik
3. Memberikan informasi yang bermanfaat dalam pengembangan
ilmu reproduksi yang kemudian dapat digunakan sebagai obat
kontrasepsi alami
4. Memberikan informasi keberadaan komponen senyawa yang
berkhasiat terhadap aktivitas antifertilitas pada tikus jantan pada
ekstrak n-heksana
5. Melengkapi hasil penelitian sebelumnya yang telah lebih dulu
dilakukan, yakni aktifitas antifertilitas ekstrak biji jarak yang sudah
ada dalam ekstrak etanol dan etil asetat, sehingga dapat
memberikan informasi yang utuh mengenai pada ekstrak mana biji
TINJAUAN PUSTAKA
2.1 Jarak Pagar (Jatropha curcas L ) 2.1.1 Sejarah dan Sinonim
Tanaman jarak pagar mulai banyak ditanam di Indonesia semenjak masa penajajahan
Jepang. Pada waktu itu, rakyat diperintah oleh pemerintah Jepang untuk membudidayakan
tanaman jarak. Oleh karenanya, dalam waktu singkat tanaman jarak menyebar cukup luas,
khususnya di Jawa Tengah dan Jawa Timur. Wilayah Jawa Tengah meliputi daerah Semarang
serta Solo dan sekitarnya. Sementara, wilayah Jawa Timur meliputi Madiun, Lamongan, Besuki,
dan Malang. Dalam perkembangan selanjutnya, tanaman jarak meluas sampai di Kawasan
Indonesia Timur, seperti Nusa Tenggara, Sulawesi, dan sebagainya. Jadi, nama-nama lokal untuk
jarak pagar dapat ditemukan di daerah-daerah(Nurcholis dan Sumarsih, 2007). Meskipun
banyak terdapat di Indonesia, tanaman jarak pagar bukan berasal dari Indonesia. Tanaman ini
berasal dari Meksiko dan Amerika Tengah, tetapi tumbuh di sebagian besar negara tropis.
Tanaman ini tumbuh di Amerika Tengah, Amerika Selatan, Asia Tenggara, India, dan Afrika.
Jatropha berasal dari kata Yunani, iatrós yang berarti medis dan trophé yang berarti makanan(Bartoli, 2008). Di Indonesia, jarak pagar juga dikenal dengan nama jarak kosta, jarak
paer, atau jarak wolanda. Nama tanaman jarak pagar dengan daerahnya antara lain: physic nut,
purging nut (English); pourghère, pignon d’Inde (French); purgeernoot (Dutch); Purgiernuß, Brechnuß (German); purgueira (Portuguese); fagiola d’India (Italian); dand barrî, habel meluk (Arab);bagbherenda, jangliarandi, safed arand (Hindi); kadam (Nepal); yu-lu-tzu (Chinese);
sabudam (Thailand); túbang-bákod (the Philippines); bagani (Côte d’Ivoire); kpoti (Togo); tabanani (Senegal); mupuluka (Angola); butuje (Nigeria) (Heller, 1996).
Genus Jatropha memiliki 175 spesies, dari jumlah ini lima spesies tumbuh di Indonesia,
2.1.2 Klasifikasi
Tanaman jarak pagar mempunyai nama latin Jatropha curcasL. Dalam sistematika (taksonomi) tumbuhan, kedudukan tanaman jarak pagar diklasifikasikan sebagai berikut :
Kingdom : Plantae
Subkingdom : Trachebionta (tumbuhan vascular) Superdivision : Spermatophyta (tumbuhan berbiji) Division : Magnoliophyta (tumbuhan berbunga) Class : Magnoliopsida (Dicotyledonae) Subclass : Rosidae
Order : Euphorbiales Family : Euphorbiaceae Genus : Jatropha L.
Species : Jatropha curcas L. (Bartoli, 2008)
2.1.3 Morfologi
Jarak pagar berupa pohon kecil atau perdu. Tanaman ini dapat mencapai umur 50 tahun.
Tinggi tanaman pada kondisi normal adalah 1,5-5 meter. Percabangannyatidak teratur, dengan
bulatdan tebal. Kulit batang berwarna keabu-abuan atau kemerah-merahan. Apabila ditoreh,
batang mengeluarkan getah seperti latex berwarna putih atau kekuning-kuningan.
Daun jarak pagar cukup besar, panjang helai 6-16 cm dan lebar 5-15 cm. Helaian daun
berbentuk bulat telur dengan pangkal berbentuk jantung, bersudut atau berlekuk 3-5 dan tepi
daun gundul. Warna daun hijau atau hijau muda.
Bunga jarak pagar mulai muncul saat tanaman mulai berumur 3-4 bulan. Pembungaan
umumnya terjadi pada musim kemarau. Walaupun demikian, pada musim hujan juga dapat
berbunga. Bunga terdiri atas bunga jantan dan bunga betina. Dalam setiap helai terdapat bunga
jantan dan bunga betina. Bunga betina bertangkai tebal dan berambut seperti sarang laba-laba.
Ukurannya lebih besar daripada bunga jantan.
Biji yang sudah tua berbentuk bulat panjang. Ukuran panjang rata-rata 18 mm ( berkisar
antara 11-30mm) dan lebar rata-rata 10mm (berkisar antara 7-11mm). Biji jarakbercangkang
kering penuh retal-retak kecil. Jika belum tua, warna biji lebih cerah atau kecokelat-cokelatan,
dengan permukaan halus. Jika kulit buah telah kering, biji dapat terlepas sendiri dari buah.
Bijimatang ditandai dengan perubahan warna kulit buah dari hijau menjadi kuning.
Buah jarak pagar banyak dihasilkan pada musim kering, pada saat jumlah daun
berkurang karena banyak yang kering atau gugur. Sekitar 2-3 bulan setelah pemupukan, pada
umumnya tanaman dewasa sudah berbuah. Buah tersusun dalam tandan buah. Setiap tandan
berisi 10 buah atau lebih. Bentuk buah membulat, beukuran panjang 2-3 cm. Permukaan buah
rata (halus). Apabila buah mongeringdan kemudian pecah menurut ruang, dalam setiap buah
terdapat 3 biji ( Nurcholis dan Sumarsih, 2007).
Gambar 2.1. Bunga ,buah dan biji Jatropha curcas L. ( IEEJ, 2009 )
2.1.4 Kandungan Bahan Aktif
Tanaman jarak mengandung senyawa-senyawa aktif seperti alpha-amirin, kampesterol,
iso-viteksin viteksin, kampesterol, dan HCN. ( Agromedia, 2008). Selain itu tanaman ini juga
mengandung beta-sitosterol, stigmasterol, curcin, flavonoid dan 12-deoksil-16-hidroksiforbol
akar, daun, batang, buah, biji serta minyak hasil pengepresan. Ekstrak forbol ester memiliki
kemampuan membunuh serangga, fungi, dan moluska sehingga berpotensi sebagai antimikroba.
Flavonoid yang tekandung dalam ekstrak kulit batang jarak memiliki aktivitas biologi seperti
antimikroba, anti alergi dan antioksidan. Lateks dari jarak yang mengandung komponen alkaloid
digunakan sebagai anti kanker (Nurmillah, 2009).
Setiap 100 g biji mengandung 6,6 g H2O, 18,2 g protein, 3,8 g lemak, 33,5 g total
karbohidrat, 15,15 g serat dan 4,5 g abu. Biji dilaporkan juga mengandung sakarosa, raffinosa,
stachyosa, glukosa, fruktosa, galaktosa, protein, minyak, curcasin, arachidic, oleat, linoleat,
miristik, palmitat dan asam stearat (Mahmud, 2007). Senyawa toksik dalam biji jarak pagar
adalah lektin dan phorbolester. Senyawa lektin maupun phorbolester dapat terdegradasi sehingga
toksisitasnya berkurang bahkan hilang, yaitu dengan pemanasan dan dengan reaksi kimia. Selain
itu, juga terdapat agensia antifertilitas yang disebut jatrophone, yang dilaporkan berperan dalam mempengaruhi fertilitas (Muliani, 2011).
2.1.5 Kegunaan
Olahan dari semua bagian tanaman termasuk biji, daun dan kulit kayu, segar atau sebagai
air rebusandigunakan dalam pengobatan tradisional. Minyak dari biji memilikitindakan pencahar
yang kuat dan juga banyak digunakan untuk penyakit kulit dan untuk meredakan rasa sakit
sepertiyang disebabkan oleh rematik. Getah yang keluar dari batang digunakan untuk
menghentikan pendarahan dari luka. Rebusan dari daun digunakan untuk batuk dan sebagai
antiseptik setelah kelahiran (Heller,1996). Lateks memiliki sifat antibiotik terhadap beberapa
bakteri ; diterapkan langsung pada luka dan dapat digunakan sebagai antiseptik seperti pada
ruam, luka bakar, dan infeksi kulit (Bartoli,2008).
Dengan menggunakan ekstrak dari biji jarak pagar dapat mengobati penyakit seperti
hernia, kanker, gonorhoea. Hal ini yang pernah dicoba oleh penduduk di Colombia untuk
mengobati penyakit kelamin. Di Mesir, biji digunakan untuk pengobatan arthritis, gout dan
jaundice. Biji tanaman ini juga telah digunakan secara tradisional untuk pengobatan banyak
penyakit termasuk luka bakar, kejang, demam dan peradangan (Prasad et al., 2012). Beberapa
negara seperti, Kamboja, Vietnam dan India telah menggunakan biji jarak sebagai agensia
aborsi, sedangkan di Sudan telah menggunakan biji jarak sebagai agensia kontrasepsi (Cambie
2.2 Simplisia dan Ekstrak 2.2.1 Simplisia
Simplisia tumbuhan obat merupakan bahan baku proses pembuatan ekstrak, baik sebagai
bahan obat atau produk. Dalam buku Materia Medika lndonesia ditetapkan definisi bahwa
simplisia adalah bahan alamiah yang dipergunakan sebagai obat yang belum mengalami
pengolahan apapun juga dan kecuali dikatakan lain, berupa bahan yang telah dikeringkan.
Simplisia dibedakan.simplisia nabati, simplisia hewani, dan simplisia pelikan (mineral).
Simplisia nabati adalah simplisia yang berupa tumbuhan utuh, bagian tumbuhan atau eksudat
tumbuhan. Eksudat tumbuhan ialah isi sel yang secara spontan keluar dari tumbuhan atau isi sel
yang dengan cara tertentu dikeluarkan dari selnya atau senyawa nabati lainnya yang dengan cara
tertentu dipisahkan dari tumbuhannya dan belum berupa senyawa kimia murni ( Anonim, 2000).
2.2.2 Ekstrak
Ekstrak adalah sediaan kental yang diperoleh dengan mengekstraksi senyawa aktif dari
simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau
hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian
hingga memenuhi baku yang telah ditetapkan (Anonim, 2000).
Ada beberapa jenis ekstrak yakni : ekstrak cair, ekstrak kental dan ekstrak kering.
Ekstrak cair adalah sediaan dari simplisia nabati yang mengandung etanol sebagai pelarut atau
sebagai pengawet. Jika tidak dinyatakan lain pada masing-masing monografi tiap ml ekstrak
mengandung senyawa aktif dari 1 g simplisia yang memenuhi syarat. Ekstrak cair jika hasil
ekstraksi masih bisa dituang biasanya kadar air lebih 30%. Ekstrak kental jika memilki kadar
air antara 5-30%. Ekstrak kering jika mengandung kadar air kurang dari 5% (Saifudin dkk,
2011).
2.3 Ekstraksi 2.3.1.Cara dingin
1. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut
dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan (kamar).
pada keseimbangan. Maserasi kinetik berarti dilakukan pengadukan yang kontinu
(terus-menerus). Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah
dilakukan penyaringan maserat pertama, dan seterusnya.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna
(exhaustive extraction) yang umumnya dilakukan pada temperatur ruangan. Proses
terdiri dari tahapan pengernbangan bahan, tahap maserasi antara, tahap perkolasi
sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai diperoreh ekstrak
(perkolat) yang jumlahnya 1- 5 kali bahan.
2.3.2 Cara panas 1. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama
waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya
pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai
3-5 kali sehingga dapat termasuk proses ekstraksi sempurna.
2. Soxhlet
Soxhlet adalah ekstraksi menggunakan pelarut yang selalu baru yang umumnya
dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut
relatif konstan dengan adanya pendingin balik.
3. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur
yang lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada
temperatur 40-50oC.
4. Infus
lnfus adalah ekstraksi dengan pelarut air pada temperatur penangas air (bejana
infus tercelup dalam penangas air mendidih, temperatur terukur 96-980C) selama waktu
tertentu (15 - 20 menit).
5. Dekok
Dekok adalah infus pada waktu yang lebih lama (> 300C ) dan temperatur sampai
2.3.3 Destilasi uap
Destilasi uap adalah ekstraksi senyawa kandungan menguap (minyak atisiri) dari bahan
(segar atau simplisia) dengan uap air berdasarkan peristiwa tekanan parsial senyawa kandungan
menguap dengan fase uap air dari ketel secara kontinu sampai sempurna diakhiri dengan
kondensasi fase uap campuran (senyawa kandungan menguap ikut terdestilasi) menjadi destilat
air bersama senyawa kandungan yang memisah sempurna atau memisah sebagian.
Destilasi uap, bahan (simplisia) benar-benar tidak tercelup ke air yang mendidih, namun
dilewati uap air sehingga senyawa kandungan menguap ikut terdestilasi. Destilasi uap dan air,
bahan (simplisia) bercampur sempurna atau sebagian dengan air mendidih, senyawa kandungan
menguap tetap kontinu ikut terdestilasi.
2.3.4 Cara ekstraksi lainnya
1. Ekstraksi berkesinambungan
Proses ekstraksi yang dilakukan berulang kali dengan pelarut yang berbeda atau
resirkulasi cairan pelarut dan prosesnya tersusun berturutan beberapa kali. Proses ini
dilakukan untuk meningkatkan efisiensi (jumlah pelarut) dan dirancang untuk bahan
dalam jumlah besar yang terbagi dalam beberapa bejana ekstraksi.
2. Super kritikal karbondioksida
Penggunaan prinsip superkritik untuk ekstraksi serbuk simplisia, dan umumnya
digunakan gas karbondioksida. Dengan variabel tekanan dan temperatur akan diperoleh
spesifikasi kondisi polaritas tertentu yang sesuai untuk melarutkan golongan senyawa
kandungan tertentu. Penghilangan cairan pelarut dengan mudah dilakukan karena
karbondioksida menguap dengan mudah, sehingga hampir langsung diperoleh ekstrak
3. Ekstraksi Ultrasonik
Getaran ultrasonik (> 20.000 Hz.) memberikan efek pada proses ekstrak dengan
prinsip rneningkatkan permiabilitas dinding sel, menimbulkan gelembung spontan
(cavitation) sebagai stres dinamik serta menimbulkan fraksi interfase. Hasil ekstraksi
tergantung pada frekuensi getaran, kapasitas alat dan lama proses ultrasonikasi.
4. Ekstraksi energy listrik
Energi listrik digunakan dalam bentuk medan listrik, medan magnet serta
prinsip menimbulkan gelembung spontan dan menyebarkan gelombang tekanan
berkecepatan ultrasonik.
2.4 Tinjauan Hewan Percobaan
2.4.1 Klasifikasi Tikus Putih (Rattus norvegicus)
Menurut Krinke (2000) klasifikasi Tikus putih (Rattus norvegicus) adalah sebagai berikut:
Kingdom : Animalia Phylum : Chordata Subphylum : Vertebrata Class : Mammalia Order : Rodentia Family : Muridae Genus : Rattus Species : norvegicus
2.4.2 Biologis Tikus Putih (Rattus norvegicus)
Hewan laboratorium atau hewan percobaan adalah hewan yang sengaja dipelihara dan
diternakkan untuk dipakai sebagai hewan model guna mempelajari dan mengembangkan
berbagai macam bidang ilmu dalam skala penelitian atau pangamatan laboratorium. Tikus
termasuk hewan mamalia, oleh sebab itu dampaknya terhadap suatu perlakuan mungkin tidak
jauh berbeda dibanding dengan mamalia lainnya Selain itu, penggunaan tikus sebagai hewan
percobaan juga didasarkan atas pertimbangan ekonomis dan kemampuan hidup tikus hanya 2-3
tahun dengan lama reproduksi 1 tahun.
Kelompok tikus laboratorium pertama-tama dikembangkan di Amerika Serikat antara
tahun 1877 dan 1893. Keunggulan tikus putih dibandingkan tikus liar antara lain lebih cepat
dewasa, tidak memperlihatkan perkawinan musiman, dan umumnya lebih cepat berkembang
biak. Kelebihan lainnya sebagai hewan laboratorium adalah sangat mudah ditangani, dapat
ditinggal sendirian dalam kandang asal dapat mendengar suara tikus lain dan berukuran cukup
besar sehingga memudahkan pengamatan. Secara umum, berat badan tikus laboratorium lebih
g, dan berat dewasa rata-rata 200-250 g, tetapi bervariasi tergantung pada galur. Galur Sprague Dawley merupakan galur yang paling besar diantara galur yang lain.
Terdapat beberapa galur tikus yang sering digunakan dalam penelitian. Galur-galur
tersebut antara lain : Wistar, Sprague-Dawley, Long Evans, dan Holdzman. Dalam penelitian ini digunakan galur Sprague-Dawley dengan ciri-ciri berwarna putih, berkepala kecil dan ekornya lebih panjang daripada badannya (Smith dan Mangkoewidjojo 1988). Tikus ini pertama kali
diproduksi oleh peternakan Sprague Dawley. Tikus Sprague Dawley merupakan jenis outbred tikus albino serbaguna secara ekstensif dalam riset medis. Keuntungan utamanya adalah
ketenangan dan kemudahan penanganannya. Adapun data biologis tikus sebagai berikut :
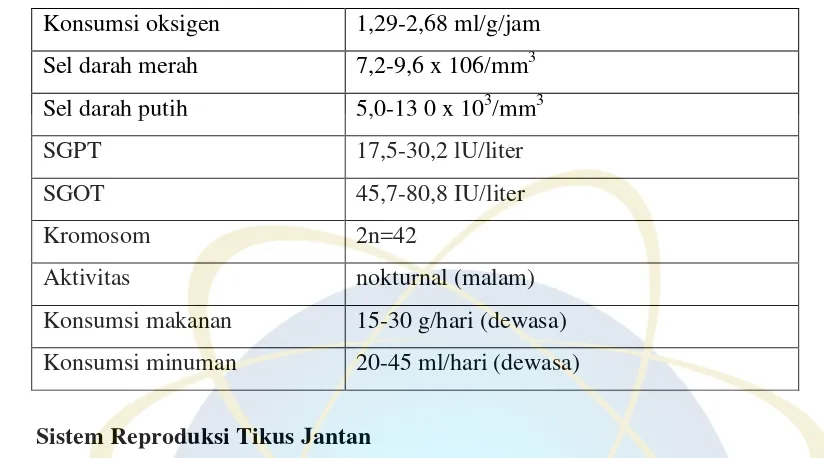
Tabel 2.1. Data biologis tikus (Smith dan Mangkoewidjojo, 1988).
Lama hidup 2-3 tahun, dapat sampai 4 tahun
Lama produksi ekonomis I tahun
Lama bunting 20-22 hari
Umur dewasa 40-60 hari
Umur dikawinkan 8-10 minggu (jantan dan betina)
Siklus kelamin Poliestrus
Siklus estrus (berahi 4-5 hari
Lama estrus 9-20 jam
Perkawinan Pada waktu estrus
Ovulasi 8- 11 jam sesudah timbul estrus, spontan
Ferilisasi 7-10 jam sesudah kawin
Implantasi 5-6 hari sesudah fertilisasi
Berat dewasa 300-400 g jantan; 250-300 g betina
Suhu (rektal) 36-39oC (rata-rata 37,5oC)
Pernapasan 65-115/menit, turun menjadi 50 dengan
anestesi, naik sampai 150 dalam stress
Denyut jantung 330-480/menit, turun menjadi 250 dengan
anestesi, naik sampai 550 dalam stress
Tekanan Darah 90-180 sistol, 60-145 diastol, turun menjadi
2.5 Sistem Reproduksi Tikus Jantan
Sistem reproduksi tikus jantan terdiri atas testis dan skrotum, epididimis, duktus deferens,
kelenjar aksesori (kelenjar vesikulosa, prostat dan bulbouretralis), uretra dan penis.. Selain uretra
dan penis, semua struktur ini berpasangan. Duktus yang menjadi testis, duktuli eferentes bersama duktus epididymis, suatu duktus konvolusi bergelung untuk membuat epididimis, suatu organ
yang terletak pada permukaan posterior testis.
Dari epididimis, duktus deferen yang lurus panjang naik dari skrotum dan melalui aknalis
inguinalis masuk ke dalam pelvis, tempat duktus ini berlanjut dengan duktus ejakulatorius, suatu segmen terminal dari system duktus yang membuka ke arah uretra prostatic. Berhubungan
dengan system duktus adalah tiga kelenjar asesorius, vesikula seminalis, prostat, dan kelenjar
bulboureta. Spermatozoa dari epididymis, bersama dengan hasil sekretorius kelenjar ini,
merupakan semen yang dikeluarkan melalui uretra penis (Fawcett & Bloom, 2002).
Gambar 2.2. Anatomi sistem reproduksi tikus jantan (Suckow, 2006) Konsumsi oksigen 1,29-2,68 ml/g/jam
Sel darah merah 7,2-9,6 x 106/mm3
Sel darah putih 5,0-13 0 x 103/mm3
SGPT 17,5-30,2 lU/liter
SGOT 45,7-80,8 IU/liter
Kromosom 2n=42
Aktivitas nokturnal (malam)
Konsumsi makanan 15-30 g/hari (dewasa)
Pada hewan yang melakukan fertilisasi secara interna organ reproduksinya dilengkapi
dengan adanya organ kopulatori, yaitu suatu organ yang berfungsi menyalurkan spermatozoa
dari organisme jantan ke betina. Peranan hewan jantan dalam hal reproduksi terutama adalah
memproduksi spermatozoa dan sejumlah kecil cairan untuk memungkinkan sel spermatozoa
masuk menuju rahim (William, 2005).
Ketiga kelenjar asesorius mensekresi zat-zat makanan bagi spermatozoa. Vesikula
seminalis merupakan kelenjar berlekuk-lekuk yang terletak di belakang kantung kemih. Dinding
vesikula seminalis menghasilkan zat makanan yang merupakan sumber makanan bagi sperma.
Kelenjar Cowper (kelenjar bulbouretra) merupakan kelenjar yang salurannya langsung menuju
urethra. Kelenjar Cowper menghasilkan getah yang bersifat alkali (basa). Prostat terletak di
pelvis, tepatnya di posterior dan inferior vesika urinaria dekat dengan rektum. Fungsi dari
kelenjar prostat adalah memproduksi cairan prostat yang mengandung kolesterol, garam dan
fosfolipid yang merupakan komponen utama dari semen yang bersifat basa ( Faranita, 2009 ).
Testis memiliki dua fungsi, yaitu sebagai tempat spermatogenesis dan produksi andogen.
Oleh sebab itu, maka testis dapat juga dikatakan sebagai kelenjar ganda, karena secara
fungsional bersifat endokrin dan juga eksokrin. Fungsi endokrin terletak pada sel Leydig yang
menghasilkan androgen, terutama testosteron. Fungsi eksokrin terletak pada epitelium semiferus
yang menghasilkan spermatozoa (Fawcett & Bloom, 2002).
Spermatogenesis terjadi di dalam suatu struktur yang disebut tubulus seminiferous.
Tubulus ini berlekuk-lekuk dalam lobules yang semua duktusnya kemudian meninggalkan testis
dan masuk ke dalam epididymis. Produksi andogen terjadi di dalam kantung dari sel khusus yang
terdapat di daerah interstitial antara tubulus. Tubulus seminferus dilapisi oleh epitelium
bertingkat yang sangat kompleks yang mengandung sel spermatogenik dan sel-sel yang
menunjang. Sel-sel penunjang berjenis tunggal disebut dengan sel Sertoli.
Tubulus seminiferus di kelilingi oleh membran basal. Di dekat membran basal ini
terdapat sel progenitor untuk produksi spermatozoa. Epitel yang mengandung spermatozoa yang
sedang berkembang di sepanjang tubulus disebut epitel seminiferus atau epitel germinal. Pada
potongan melintang testis, spermatosit dalam tubulus berada dalam berbagai tahap pematangan.
Di antara spermatosit terdapat sel Sertoli. Sel ini berperan secara metabolik dan struktural untuk
yang telah dikeluarkan. Sel ini merupakan satu-satunya sel nongerminal dalam epitel
seminiferous. Semua sel Sertoli berhubungan dengan membrane basal pada satu kutubnya dan
mengelilingi spermatozoa yang sedang berkembang pada kutub yang lain. Sel Sertoli memilki
jari-jari sitoplasma yang besar dan kompleks yang dapat mengelilingi banyak spermatozoa dalam
satu waktu.
Sel ini juga berfungsi pada proses aromatisasi prekursor androgen menjadi estrogen,
suatu produk yang menghasilkan pengaturan umpan balik lokal pada sel Leydig yang
memproduksi androgen. Selain itu sel Sertoli juga menghasilkan protein pengikat androgen.
Produksi androgen sendiri terjadi di dalam kantong dari sel khusus (sel Leydig) yang terdapat di
daerah interstitial antara tubulus-tubulus seminiferus (Heffner & Schust, 2005).
2.5.1 Produksi Sperma
Produksi sperma tiap hari per testis pada tikus adalah 35,4 x 106/mL, tidak berbeda
signifikan dengan manusia yakni sebesar 45,5 x 106/mL. Tubulus seminiferus tikus lebih tebal
dari manusia yakni 347+5 µm vs 262+9 µm , tetapi pembatas tubulus pada tikus lebih jauh tipis
dibanding manusia ( 1,4+1 µm vs 15,9+3,4 µm ). Epitel seminiferus tikus mengandung 40%
lebih sel spermatogenik dari volumenya, dua kali leboh banyak dari epitel seminiferus manusia (
Ilyas, 2007).Spermatozoa pada tikus panjangnya sekitar 150 – 200 mm. Kepala sperma pada tikus berbentuk kail hal ini sama seperti pada hewan pengerat lainnya (Krinke, 2000).
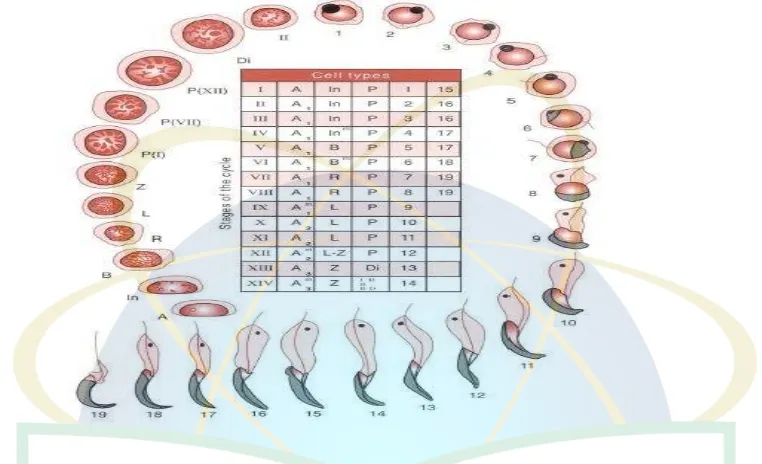
2.5.2 Spermatogenesis Pada Tikus
Gambar 2.4. Tahapan dari siklus sel spermatogenesis pada tikus, dimulai dari kiri bawah searah
jarum jam. A, tipe spermatogonium A; In , spermatogonium tipe intermediet; B, tipe
spermatogonium B; R, spermatosit primer resting; L, spermatosit leptotene; Z, spermatosit
zygotene; P(I), P(VII), P (XII), awal, pertengahan dan akhir spermatosit pachytene. Angka
romawi menunjukkan tahap siklus di mana mereka ditemukan; Di, diplotene; II, spermatosit
sekunder; 1-19, tahap spermiogenesis. Tabel di tengah memberikan komposisi sellular dari
tahapan siklus pada epitel seminiferus (l-XIV). Penulisan m menunjukkan terjadinya mitosis (
Clermont, 1962).
Dasar pengetahuan yang cukup telah dibangun tentang spermatogenesis pada
tikus. Sel primodial germinal yang telah berhenti bermigrasi diliputi oleh sel Sertoli dan
membran basal yang menonjol dalam tubulus seminiferus pada alat kelamin tikus jantan.
Sel kelamin jantan tetap tidak aktif sampai sebelum masa pubertas, yaitu dimana sekitar
50 hari setelah kelahiran. Pada tahap itu mereka mulai membelah dan menjadi
spermatogonium, dan kemudian terus membelah sampai hewan kehilangan kemampuan
untuk memproduksi spermatozoa.
Sel-sel spermatogenik berkembang dalam tubulus seminiferus testis melalui
Spermatogenesis memerlukan suatu seri komplek dimana spermatozoa dihasilkan melalui
tahap mitosis, meiosis, dan diferensiasi sel untuk menjadi spermatozoa matang.
Perubahan morfologi dari spermatid menjadi spermatozoa disebut dengan
spermiogenesis. Selanjutnya spermatozoa dilepaskan ke dalam lumen tubulus. Proses
pelepasan tersebut dikenal dengan proses spermiasi (Ilyas, 2007).
Spermatogonium secara garis besar diklasifikasikan ke dalam tiga jenis: tipe A,
tipe intermediet dan tipe B. Tipe spermatogonia A ini dibagi lagi menjadi tipe AO (
disebut juga sel induk) dan tipe Al-A4. Tipe spermatogonium AO tetap pada membran
basal di tubulus seminiferus dan memiliki kemampuan untuk membelah menjadi dua sel
anak, salah satunya menjadi spermatogonium A1, yang seterusnya lebih lanjut dalam
proses spermatogenesis, sedangkan yang lainnya sebagai sel induk. Pada tikus,
spermatogonium A1 kemudian memiliki enam pembelahan mitosis, dan kemudian
mereka menjadi spermatosit prelepton. Kemudian spermatosit dalam fase meiosis, di
mana berkembang menjadi leptolene, zygotene dan pakiten untuk menjadi spermatosit
sekunder di komponen adluminal dari sel Sertoli dalam tubulus seminiferous. Selama
fase meiosis, masing-masing spermatosit membelah menjadi satu dari empat spermatid
haploid, yang kemudian memasuki fase akrosom, selama akrosom berkembang.
Kondensasi inti dan perpanjangan terjadi berikutnya, diikuti oleh fase eliminasi dan
pelepasan sitoplasma.
Pada tikus, 14 tahapan siklus spermatogenesis terjadi di dalam tubulus
seminiferus. Tubulus memiliki susunan ruas, dan setiap potongan melintang tubula
menunjukkan tahapan yang seragam yang melibatkan empat atau lima generasi di sel
germinal dengan sesuai. Tubulus seminiferus di tikus dikarakterisasi oleh struktur ruas,
sedangkan pada manusia dan hewan domestik lainnya biasanya menunjukkan pola
mosaic di beberapa tahap. Pada tikus, dibutuhkan 12 hari untuk menyelesaikan satu siklus
yang terdiri dari 14 tahap. Spermatogonium tikus membutuhkan empat siklus sampai
akhirnya membentuk spermatozoa, sehingga diperlukan 48 hari untuk menyelesaikan
2.5.3 Peran Hormon Pada Spermatogenesis
Proses spermatogenesis dipengaruhi oleh hormon-hormon yang dihasilkan oleh organ
hipotalamus, hipofisis dan testis sendiri. Testes memproduksi sejumlah hormone jantan yang
kesemuanya disebut androgen. Yang paling poten dari androgen adalah testosterone. Fungsi
testosterone adalah merangsang pendewasaan spermatozoa yang terbentuk dalam tubulus
seminiferous, merangsang pertumbuhan kelenjar-kelenjar asesori dan merangsang pertumbuhan
sifat jantan ( Partodihardjo,1980)
Spermatogenesis dan pematangan sperma sewaktu bergerak di sepanjang epididymis dan
vas deferens memerlukan androgen. Androgen juga mengontrol pertumbuhan dan fungsi
vesikula seminalis serta kelenjar prostat. Spermatogenesis hampir seluruhnya terjadi dibawah
pengaruh hormon-hormon yang berasal dari hipofisa, terutama FSH. Hal ini mirip dengan apa
yang terjadi pada ovarium, dimana terjadi pembentukan folikel di bawah pengaruh FSH.
Spermiogenesis adalah lanjutan spermatogenesis yang berlangsung di bawah peranan LH dan
testosterone. Tanpa testosterone spermatozoa tidak dapat mencapai pendewasaan yang baik.
Spermatogenesisdimulaipada saatpubertaskarena adanyapeningkatan
sekresigonadotropin(FSHdan LH) dari hipofisisanterior.FSHdianggaphormonpentinguntuk
induksispermatogenesis danmerangsang secara langsungpada tubulusseminiferus, karena
spermatogenesislengkappada tikushyposectomizeddipulihkanoleh perlakuanFSHdalamkombinasi denganLHdan testosteron.Di sisi lain, efek spermatogenesis dari LH, kadang-kadang disebut
hormonselinterstisial yangmerangsang(ICSH) pada tikus jantan karena
tindakanandrogenikpadasel-sel Leydigdiinterstitium, dianggap dimediasi olehandrogen,
setidaknya pada tikus.Dalam konteks ini,sekresi LHjuga merangsangsintesistestosteron di
selLeydigpada testis.
Aksi FSH pada spermatogenesis mungkin dimediasi oleh sel Sertoli, karena hormon
peptida tidak dapat secara langsung mencapai spermatosit dan spermatid melintasi sawar darah
testis, yang terbentuk selama 16 - 19 hari setelah kelahiran. Sebaliknya, testosteron dapat dengan
mudah melewati sawar darah testis dengan difusi (dan mungkin juga oleh beberapa sistem
transportasi). Telah dilaporkan bahwa tingkat testosteron di dalam cairan interstisial (lebih dari
cairan vena perifera (kurang dari 10 ng / ml ), menunjukkan aksi parakrin atau autokrin dari
testosteron pada spermatogenesis di testis.
Salah satu peran untuk sel Sertoli adalah produksi androgen yang mengikat protein,
dimana dirangsang oleh FSH dan testosteron. Ini juga telah menunjukkan bahwa terdapat
beberapa faktor yang tidak diketahui yang dikeluarkan dari sel Sertoli, sebagai respon untuk
BAB III
METODE PENELITIAN
3.1. Tempat dan Waktu Penelitian 3.1.1. Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Product Natural Analysis dan di Laboratorium
Farmakologi (Laboratorium Bioavailabilitas dan Bioekivalensi Farmasi), Fakultas Kedokteran
dan Ilmu Kesehatan, UIN Syarif Hidayatullah Jakarta.
3.1.2. Waktu Penelitian
Penelitian berlangsung dalam waktu 4 bulan, terhitung dari bulan September sampai
dengan Desember 2013.
3.2. Alat dan Bahan 3.2.1. Hewan Uji
Hewan uji yang akan digunakan dalam penelitian ini adalah tikus putih jantan galur
Sprague-Dawley yang sehat berumur 9 minggu dengan berat 250-350 g dan fertil yang diperoleh
dari Badan Pengawasan Obat dan Makanan.
3.2.2. Bahan Uji
Bahan uji yang akan digunakan adalah biji jarak pagar (Jatropha curcas L.) yang diperoleh dari Balai Penelitian Tanaman Pemanis dan Serat Malang.Sebelum dilakukan
penelitian, tanaman di determinasi terlebih dahulu di Herbarium Bogoriense Bidang Botani Pusat
Penelitian Biologi-LIPI Bogor.
3.2.3. Bahan Kimia
Bahan-bahan yang dipergunakan dalam penelitian ini adalah pakan tikus berupa pellet,
aquades steril, larutan NaCl, alkohol 70%,80%, dan 96% , n-heksana 70% dan 95%, ammoniak 1
% dan 25 %. larutan HCl, kloroform, pereaksi Dragendroff, pereaksi Mayer, serbuk Mg, amil
alkohol, larutan NaOH, FeCl3, eter, petroleum eter, larutan Hematoksilin, larutan Bouin (asam
pikrat, formaldehid 4%, asam asetat), larutan xilol, larutan Eosin, larutan George, paraffin.
Alat yang digunakan dalam penelitian ini meliputi : labu erlenmeyer, labu kocok, gelas
ukur, ayakan mesh 40, timbangan analitik, mortir, tabung reaksi, cawan penguap, hot plate, corong, kertas Whatman, batang pengaduk, perangkat vacuum rotary evaporator, botol sampel, kandang hewan, tempat makan danminum tikus, timbangan hewan, alat pencekok oral(sonde), beaker glass, gelas kaca, object glass, kertas saring, Hemositometer Improved Neubeur, pipet tetes, mikro pipet, seperangkat alat bedah, mikrotom, dan mikroskop optik.
3.3. Rancangan Penelitian
Rancangan penelitian yang digunakan adalah eksperimen murni dengan Rancangan
Acak Lengkap (RAL). Perlakuan di kelompokkan menjadi 4 kelompok dengan masing-masing
terdiri dari 5 ekor tikus putih jantan strain Sprague Dawley (WHO, 2000). Perlakuan yang digunakan adalah kontrol (tanpa perlakuan) dan tikus yang diberi ekstrak biji jarak pagar (
Jatropha curcas L.) dengan 3 dosis yang berbeda.). Acuan dosis yang digunakan berdasarkan penelitian yang dilakukan oleh Arini, Dwi Widya(2011). Perlakuan yang digunakan terdiri dari:
1. Kelompok I : Kelompok pembanding tanpa perlakuan sebanyak 5 ekor tikus diberi pembawa
(Na CMC 1%)sebanyak 1 ml serta makan dan minum.
2. Kelompok II : Kelompok perlakuan sebanyak 5 ekor tikus yang diberi suspensiekstrak ekstrak
n-heksana biji jarak pagar ( Jatropha curcas L.) dengan dosis rendah yaitu 5 mg/kg BB, makan dan minum.
3. Kelompok III : Kelompok perlakuan sebanyak 5 ekor tikus yang diberi suspensiekstrak
n-heksana ekstrak jarak pagar ( Jatropha curcas L.) dengan dosis sedang yaitu 25 mg/kg BB, makan dan minum.
4. Kelompok IV : Kelompok perlakuan sebanyak 5 ekor tikus yang diberi suspensi ekstrak
ekstrak n-heksana jarak pagar ( Jatropha curcas L.) dengan dosis tinggi yaitu 50 mg/kg BB, makan dan minum.
3.4. Kegiatan Penelitian
Sebelum dilakukan penelitian, biji jarak pagar terlebih dahulu di determinasi di
Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi-LIPI Bogor untuk memastikan
kebenaran simplisia.
3.4.2. Penyiapan Simplisia
Biji jarak pagar yang telah dikeringkan dengan kadar air sebesar 8,15 % diperoleh dari
Kebun Induk Jarak Pagar Balitri Sukabumi. Biji jarak pagar lalu dirajang kemudian diblender.
Kemudian dilakukan pengayakan dengan menggunakan ayakan mesh 40 untuk mendapatkan
serbuk simplisia. Serbuk simplisia disimpan dalam wadah yang kering, tertutup rapat dan
terlindung dari cahaya.
3.4.3. Pembuatan Ekstrak
Pada pembuatan ekstrak biji jarak pagar digunakan metode ekstraksi cara dingin dengan
maserasi dan menggunakan n-heksanasebagai pelarut.
Serbuk simplisa ditimbang kemudian dimaserasi dengan pelarut n-heksanahingga sampel
terendam. Pelarut diganti setiap 3 hari sekali. Hasil maserasi disaring sehingga diperoleh filtrat.
Proses maserasi dilakukan hingga larutan mendekati tidak berwarna.
Filtrat yang diperoleh dipekatkan dengan menggunakan rotary evaporator sampai diperoleh ekstrak kental. Ekstrak kental yang dihasilkan kemudian ditimbang dan dicatat
beratnya dan selanjutnya disimpan dalam lemari pendingin atau freezerdan digunakan untuk perlakuan.
3.4.4. Penapisan Fitokimia
Pada penapisan fitokimia dilakukan pemeriksaan terhadap kandungan golongan
senyawa kimia dari simplisia dan ekstrak n-heksana biji jarak pagar seperti alkaloid,
flavonoid, saponin, tanin dan polifenol, dan steroid/terpenoid.
1. Identifikasi Golongan Alkaloid
Metoda Culvernor-Fitzgerald
Gerus 2-4 g biji jarak yang telah bersih potong-potong masukan kedalam mortar dan
kloroform amoniakal diaduk rata. Campuran disaring kedalam tabung reaksi dengan cara
memerasnya memakai kain kasa untuk memindahkan ekstrak. Kemudian tambahkan 0.5 ml
I M asam sulfat dan kocok baik-baik, biarkan beberapa saat. Pipet lapisan atas yang jernih
kedalam 2 tabung reaksi kecil. Salah satunya diberikan pereaksi Dragendorff"s dan tabung
lainnya pereaksi Mayer's (2-3 tetes). Reaksi positif apabila menunjukkan endapan kuning
jingga (orange) dengan pereaksi Drogendorff's danendapan putih dengan pereaksi Mayer's.
Catatan hail sebagai berikut:
(+) sedikit keruh
(++) sangat keruh
(+++) terjadi endapan (Chairul,2003).
2. Identifikasi Golongan Flavonoid
Pembuatan ekstrak
Ekstrak lebih kurang 10 g material tumbuhan dengan etanol 80 %, saring dan
keringkan diatas penangas air. Kemudian lemaknya dihilangkan denganpencucian
etanol70% beberapa kali sehingga warna pigmen hilang atau larutan
heksanatidakberwarnalagi. Panaskan residu yangbebas lemak diatas penangas air untuk
memindah sisa etanol.Tambahkan residu dengan 20 ml n-heksanadan pindahkan
masing-masing 10 ml kedalam 2 tabung reaksi. Masing-masing-masing tabung reaksi ditambahkan 0,5 ml
asam klorida pekat dan dilakukan uji dengan pereaksi Wilstatter (Chairul,2003).
Pereaksi Wilstatter
Salah satu tabung reaksi yang telah berisikan asam klorida pekat ditambahkan 3-4
butir logam magnesium (Mg). Amati perubahan warna yang terjadi dalam 10 menit. Apabila
terbentuk warna, diencerkan dengan air secukupnya dan tambahkan 1 ml oktil alkohol.
Kocok kuat-kuat kemudian diamkan dan amati perubahan wama pada masing-masing
lapisan pelarut. Apabila terjadi pembentukan atau perubahan warna menunjukkan reaksi
positif terhadap flavonoida (Chairul,2003).
3. Identifikasi Golongan Saponin