AKTIVITAS ANTIOKSIDAN EKSTRAK METANOLIK
DAUN BELUNTAS (
Pluchea indica Less
) DAN FRAKSINYA SERTA
KEMAMPUAN MENCEGAH
WARMED OVER FLAVOR
PADA
DAGING ITIK YANG TELAH DIPANASKAN
PAINI SRI WIDYAWATI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI DISERTASI DAN SUMBER
INFORMASI
Dengan ini saya menyatakan bahwa disertasi berjudul aktivitas antioksidan ekstrak metanolik daun beluntas (Pluchea indica Less) dan fraksinya serta kemampuan mencegah warmed over flavor pada daging itik yang telah dipanaskan merupakan hasil karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir disertasi ini.
Bogor, November 2011
Paini Sri Widyawati F261070041
ABSTRACT
PAINI SRI WIDYAWATI 2011. Antioxidant activity of Pluchea indica Less
leaves methanolic extractand its fraction and their capacity to inhibit cooked duck meat warmed over flavor. Under direction of C. HANNY WIJAYA, PENI SUPRAPTI HARDJOSWORO, and DONDIN SAJUTHI.
Pluchea indica Less is a herb commonly used as food and traditional medicine. Its leaves have antioxidant activity due to its various phytochemical compounds. The antioxidant activity of methanolic extract of Pluchea leaves to prevent cooked duck meat warmed over flavor (WOF) is still under explored. The objective of this study was to investigate the antioxidant activity of methanolic extract of Pluchea leaves and its fraction (ethyl acetate, water, and n-butanol) by using different analysis approaches test systems (2,2-phenyl-1-picrylhydrazyl (DPPH), superoxide and hydroxyl radical-scavenging activities, hydrogen peroxide scavenging activity, ferric reducing power, iron chelating capacity, and -carotene-linoleic acid bleaching assay). Furthermore, their application as inhibitor to cooked duck meat WOF has also been conducted. Antioxidant activity of Pluchea leaves was obtained by dividing its leaves into 3 groups, i.e 1-3, 4-6 and >6. The methanolic extract of those groups contained phytochemical compounds, such as tannin, sterol, phenol hydroquinone, and flavonoid. The methanolic extract of 1-6 Pluchea leaves (EMB) had more potential source of DPPH free radical scavenging activity. In addition, this extract was fractionated by various solvents with different polarity, such as ethyl acetate, n-butanol, and water. The result showed that ethyl acetate fraction (FEA) had higher antioxidant activity than EMB and the other fraction, but its activity was lower than methanolic extract of green tea (EMT). The antioxidant activity assay of EMB and FEA was compared to BHT and -tocopherol by using different analysis approaches test systems. It showed that FEA had superoxide radical-scavenging activity, iron chelating capacity and ferric reducing power, while EMB had superoxide radical-scavenging activity, ferric reducing power and -carotene– linoleic acid bleaching assay. FEA at 250 ppm concentration was more effective to prevent the formation of cooked duck meat WOF than FEA at 600 ppm concentration and EMB. This fraction significantly inhibited the oxidation of PUFA (linoleic and arachidonic acids) and the formation of malondialdehide (MDA) and hexanal content. In comparison with FEA, EMB showed less potent antioxidant activity. However, the volatile compounds in EMB extract had an effect in improving sensory properties of duck meat, mainly by increased hedonic-preference scores on acceptance sensory test and also suppressed green and grassy aromatic intensities of duck meat during cooking and storage.
RINGKASAN
PAINI SRI WIDYAWATI 2011. Aktivitas antioksidan ekstrak metanolik daun beluntas (Pluchea indica Less) dan fraksinya serta kemampuan mencegah warmed over flavor pada daging itik yang telah dipanaskan. Dibimbing oleh C. HANNY WIJAYA, PENI SUPRAPTI HARDJOSWORO, dan DONDIN SAJUTHI.
Beluntas (Pluchea indica Less) merupakan famili Asteraceae yang telah dimanfaatkan masyarakat sebagai pangan dan sediaan obat bahan alam. Senyawaan fitokimia yang terkandung dalam daun beluntas mempunyai aktivitas antioksidan. Ekstrak etanolik daun beluntas telah terbukti mampu menangkap radikal bebas 1,1-difenil-2- pikrilhidrasil (DPPH) dan asam 2,2'-azino-bis-(3-etil bensotiasolin-6-sulfonat) (ABTS), mereduksi ion besi, dan menghambat pembentukan malondialdehida (MDA). Penelitian sebelumnya menginformasikan bahwa metanol merupakan pelarut yang efektif untuk mengekstrak senyawa fenolik tanaman sehingga diperoleh aktivitas antioksidan tinggi. Sejauh ini ekstrak metanolik daun beluntas (EMB) dan fraksinya belum diketahui aktivitas antioksidannya serta kemampuannya mencegah warmed over flavor (WOF) pada daging itik yang telah dipanaskan. Penggunaan daging itik pada penelitian ini disebabkan komoditas tersebut mudah mengalami penurunan kualitas selama pemanasan dan penyimpanan karena reaksi oksidasi. Salah satu indikasi kerusakan akibat reaksi oksidasi adalah munculnya WOF.
Penelitian ini secara garis besar difokuskan pada 3 tahapan, yaitu: 1) tahap seleksi daun beluntas yang berpotensi sebagai sumber antioksidan alami; 2) tahap pengujian aktivitas antioksidan ekstrak metanolik daun beluntas dan fraksinya yang berpotensi sebagai antioksidan alami secara in vitro, meliputi kemampuan menangkap spesies oksigen reaktif (SOR) (hidrogen peroksida, radikal superoksida dan hidroksil), mereduksi dan mengkelat ion besi, dan menghambat oksidasi asam linoleat- -karoten; dan 3) tahap pengujian aktivitas antioksidan EMB dan fraksinya yang paling berpotensi sebagai antioksidan alami dalam mencegah WOF daging itik.
Pada seleksi daun beluntas sebagai sumber antioksidan alami didasarkan pada perbedaan tingkat ketuaan daun dan perbedaan jenis pelarut. Hasil seleksi berdasarkan tingkat ketuaan daun diperoleh informasi bahwa daun beluntas mengandung senyawaan fitokimia, meliputi grup senyawa tanin, flavonoid, sterol, dan fenol hidrokuinon. Pada seleksi ini daun beluntas dibagi menjadi 3 kelompok, yaitu daun 1-3, 4-6, dan >6. Berdasarkan intensitas deteksi bahwa senyawaan fitokimia pada daun beluntas lebih terkonsentrasi pada daun yang lebih muda, hal ini seiring dengan kadar total fenol (TP) dan total flavonoid (TF) untuk daun 1-3> daun 4-6 > daun >6. Kadar TP dan TF daun menentukan kemampuannya menangkap radikal DPPH, secara berturutan nilai IC50 daun 1-3 sama dengan
daun 4-6 > daun >6.
tanin, flavonoid, dan fenol hidrokuinon ditemukan pada EMB, fraksi etil asetat (FEA), fraksi n-butanol (FNB), dan fraksi air (FA), sedangkan grup senyawa sterol tidak ditemukan pada FA. Pengujian ini juga memberikan informasi bahwa sebagian besar senyawa fenolik penyusun EMB bersifat semipolar, yang ditandai dengan kadar TP dan TF pada FEA lebih tinggi dari kedua fraksi yang lain. Kandungan senyawa fenolik tersebut menentukan aktivitas FEA menangkap radikal bebas DPPH. Hasil menunjukkan bahwa FEA lebih berpotensi menangkap radikal DPPH dibandingkan dengan EMB dan kedua fraksi yang lain. Namun demikian aktivitasnya masih lebih rendah dibandingkan ekstrak metanolik teh hijau (EMT). Potensi FEA sebagai antioksidan didasarkan pada konsentrasi yang dibutuhkan untuk menurunkan aktivitas DPPH sebesar 50% (IC50) maupun
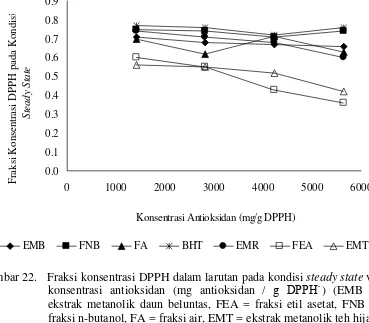
konsentrasi dan waktu yang diperlukan untuk mereduksi aktivitas DPPH sebesar 50% pada kondisi steady state (AE).
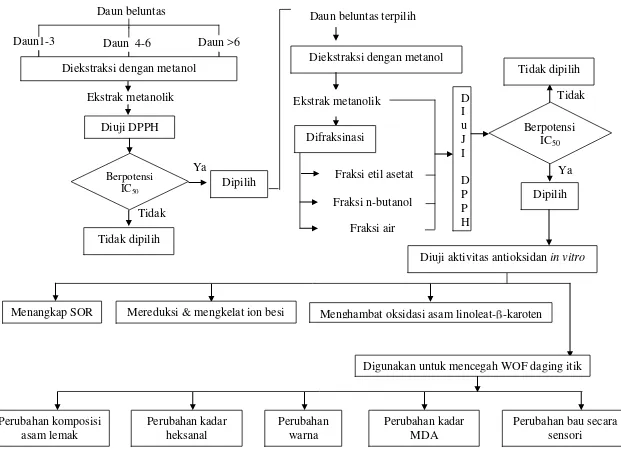
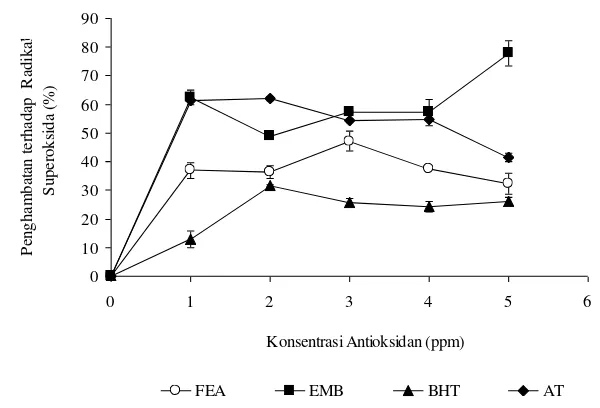
Potensi FEA sebagai antioksidan ditentukan aktivitasnya dalam berbagai sistem uji in vitro dibandingkan EMB dan antioksidan pembanding (BHT dan -tokoferol (AT)). Hasil menunjukkan bahwa FEA mempunyai aktivitas antioksidan melalui kemampuan menangkap radikal superoksida, mereduksi dan mengkelat ion besi. Sedangkan EMB mempunyai aktivitas antioksidan berdasarkan kemampuan menangkap radikal superoksida, mereduksi ion besi, dan menghambat oksidasi asam linoleat- -karoten.
Penambahan FEA konsentrasi 250 ppm lebih berpotensi mencegah terjadinya WOF pada daging itik dibandingkan EMB pada konsentrasi yang sama. Penambahan FEA dan EMB pada konsentrasi 250 ppm lebih efektif sebagai antioksidan dibandingkan konsentrasi 600 ppm. Keefektifan FEA dalam mencegah WOF pada daging itik masih lebih rendah dibandingkan BHT dan lebih tinggi dibandingkan AT. FEA dapat menghambat oksidasi asam lemak tak jenuh ganda (ALTJG) (asam linoleat dan arakidonat), mencegah pembentukan MDA, dan mereduksi kandungan heksanal. EMB kurang berpotensi sebagai antioksidan dibandingkan FEA, akan tetapi kandungan senyawa volatil pada ekstrak tersebut diduga dapat memperbaiki sensori daging itik sehingga mampu meningkatkan skor kesukaan hedonik pada uji sensori penerimaan, dan juga mampu menekan intensitas green dan grassy yang kurang disukai yang muncul pada daging itik selama pemanasan dan penyimpanan.
Kata Kunci : antioksidan, beluntas (Pluchea indica Less), warmed over flavor
(WOF), daging itik.
© Hak Cipta milik Institut Pertanian Bogor, tahun 2011
Hak cipta dilindungi
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
AKTIVITAS ANTIOKSIDAN EKSTRAK METANOLIK
DAUN BELUNTAS (
Pluchea indica Less
) DAN FRAKSINYA SERTA
KEMAMPUAN MENCEGAH
WARMED OVER FLAVOR
PADA
DAGING ITIK YANG TELAH DIPANASKAN
PAINI SRI WIDYAWATI
Disertasi
Sebagai salah satu syarat untuk memperoleh gelar Doktor pada
Program Studi Ilmu Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji pada Ujian Tertutup : 1. Prof. Dr. Maria Bintang, MS 2. Dr. Ir. Joko Hermanianto
Judul Disertasi : Aktivitas Antioksidan Ekstrak Metanolik Daun Beluntas (Pluchea indica Less) dan Fraksinya serta Kemampuan Mencegah Warmed Over Flavor pada Daging Itik yang telah Dipanaskan
Nama : Paini Sri Widyawati NIM : F261070041
Disetujui, Komisi Pembimbing
Prof. Dr. Ir. C. Hanny Wijaya, M.Agr. Ketua
Prof. Em. Dr. Peni Suprapti H, M.Sc Prof. drh. Dondin Sajuthi, M.ST, PhD.
Anggota Anggota
Diketahui,
Ketua Program Studi Ilmu Pangan Dekan Sekolah Pascasarjana
Dr. Ir. Ratih Dewanti Haryadi, M.Sc. Dr. Ir. Dahrul Syah, M.Sc.Agr.
PRAKATA
Segala puji dan syukur penulis persembahkan kepada Allah Bapa di Surga atas kasih dan karuniaNya yang selalu dilimpahkan sehingga karya ilmiah yang berjudul aktivitas antioksidan ekstrak metanolik daun beluntas (Pluchea indica Less) dan fraksinya serta kemampuan mencegah warmed over flavor pada daging itik yang telah dipanaskan berhasil diselesaikan.
Pada kesempatan ini penulis menyampaikan banyak terima kasih kepada : 1. Komisi pembimbing Prof. Dr. Ir. C. Hanny Wijaya, M.Agr., Prof. Em. Dr.
Peni Suprapti Hardjosworo, M.Sc dan Prof. drh. Dondin Sajuthi, M.ST, PhD. yang selalu dengan sabar dan bijaksana memberikan bimbingan, arahan, masukan dan motivasi kepada penulis dalam menyelesaikan karya ilmiah ini. 2. Rektor Institut Pertanian Bogor dan stafnya yang telah memberikan
kesempatan kepada penulis untuk sekolah di Program Studi Ilmu Pangan Sekolah Pascasarjana IPB.
3. Rektor Unika Widya Mandala Surabaya atas kesempatan dan dukungannya dalam beasiswa lanjutan yang diberikan kepada penulis sehingga dapat melanjutkan studi S3 di Program Studi Ilmu Pangan Sekolah Pascasarjana IPB. 4. Direktorat Jenderal Tinggi (DIKTI) atas beasiswa BPPS, program Sandwich
like dan bantuan dana penelitian melalui program Hibah Bersaing 2008-2010 yang diberikan sehingga penulis dapat melanjutkan studi S3 di Sekolah Pascasarjana IPB dan menyelesaikan penelitian disertasi ini.
5. Dr. Leong Lai Peng selaku dosen pembimbing selama penulis mengikuti program Sandwich like di Food Science and Technology Programme, Chemistry Department, National University of Singapore.
6. Keluarga besar Bpk Noto Prawiro di Klaten dan Keluarga besar Mama AE. Napitupulu di Medan, kakak tercinta Fransika Romana Sutarni, serta suami tercinta Melvin Emil Simanjuntak yang selalu mendukung, memotivasi serta mendoakan sehingga penulis selalu semangat untuk menyelesaikan studi ini. 7. Teman-temanku angkatan 2007, Rahman Karnila, Endang Purwani, Nurhayati,
Emma Rochima dan Emma Hastarini serta teman sekerja di Laboratorium Kimia SEAFAST IPB, Triana Kusumawardhani, Yuzda Salimi, Procula Rudlof Matitaputty, Isaac Silamba, Silvana D. Harikedua, Asi Febrina Cecilia, Rukmiasih, Rafitah Hasanah, Dwi Wahyu Utomo, Victoria Kristina Ananingsih, Tami Trinh, Religiana yang selalu memotivasi dan mendukung serta menjadi tempat berbagi suka dan duka selama menyelesaikan studi S3 di Program Studi Ilmu Pangan.
8. Staf Laboratorium dan administrasi SEAFAST dan Fateta IPB, Bapak/Ibu Tofik, Ariyanti, Sari, Maryati, Sobirin, Rojak, Wahid, Sri dsb yang selalu membantu dan mendukung penyelesaian studi S3 ini.
Semoga karya ilmiah ini bermanfaat.
Bogor, November 2011
DAFTAR RIWAYAT HIDUP
Penulis dilahirkan di Klaten, Jawa Tengah, pada 23 April 1973 sebagai anak keempat dari 5 bersaudara dari Bapak Mugimin Nata Prawira dan Ibu Painem Nata Prawira, menikah dengan Melvin Emil Simanjuntak. Sekolah dasar hingga menengah penulis selesaikan di Klaten, Jawa Tengah. Pendidikan sarjana dimulai pada tahun 1991 pada Program Studi Produksi Ternak Fakultas Peternakan Universitas Jenderal Soedirman Purwokerto, kemudian pindah ke Program Studi Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Gadjah Mada Yogyakarta, lulus pada tahun 1997. Pada Tahun 1998, penulis memperoleh beasiswa URGE/Kerjasama Pemerintah RI-Jepang untuk melanjutkan pendidikan di Program Studi Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Gadjah Mada Yogyakarta, lulus pada tahun 2000. Program Doktor dengan beasiswa BPPS dan beasiswa Yayasan Widya Mandala Surabaya di Sekolah Pascasarjana IPB penulis memulainya pada tahun 2007 pada Program Studi Ilmu Pangan.
Penulis pernah berkarya sebagai staf R & D di PT Kesatuan Hasil Industri pada tahun 1997. Setelah menyelesaikan program master, penulis pernah menjadi anggota peneliti parakuat di Laboratorium Kimia Fisika Pusat UGM pada tahun 2000. Sejak tahun 2001 hingga sekarang penulis merupakan staf pengajar di Fakultas Teknologi Pertanian UnikaWidya Mandala Surabaya.
Selama mengikuti pendidikan program doktor ini, penulis menjadi anggota Masyarakat Perkelapasawitan Indonesia (MAKSI). Pada bulan Oktorber 2009 hingga Januari 2010, penulis mengikuti program Sandwich like di Food Science and Technology Programme, Chemistry Department National University of Singapore. Program ini diikuti penulis untuk menunjang penyelesaian penelitian disertasi ini. Pada Bulan Agustus 2010 penulis menyajikan karya ilmiah dengan judul “Pengaruh ekstraksi dan fraksinasi terhadap sifat antioksidatif daun beluntas(Pluchea indica Less)” di Seminar Nasional Rekayasa dan Proses Kimia di FTK UNDIP. Pada Bulan 11-15 Oktober 2010 penulis menyajikan karya ilmiah dengan judul “Antioxidant activity of phytochemicals from beluntas (pluchea indica less) leaves extract and its fractions” dalam bentuk poster pada ISNFF international conference di Bali. Sebuah artikel berjudul “Aktivitas antioksidan berbagai fraksi dan ekstrak metanolik daun beluntas (Pluchea indica Less)”, telah diterima untuk diterbitkan pada jurnal Agritech Volume 32 Nomor 3 pada bulan Agustus 2012. Karya-karya ilmiah tersebut merupakan bagian dari disertasi penulis. Selama menyelesaikan program doktor, penulis juga aktif mengikuti beberapa seminar nasional maupun lokal IPB serta pelatihan yang menunjang pendidikan doktor yang ditempuh.
Halaman
Daftar Gambar……… xiv
Daftar Tabel……… xvii
Daftar Lampiran………. xviii
Daftar Singkatan………. xxii
PENDAHULUAN……….. 1
Latar Belakang………. 1
Perumusan Masalah………. 4
Tujuan Penelitian………. 4
Manfaat Penelitian……… 5
Hipotesa……… 5
Ruang Lingkup Penelitian……… 5
TINJAUAN PUSTAKA………. 7
Daging Itik……… 7
Antioksidan……….. 14
Senyawa Fenolik……….. 16
Beluntas (Pluchea indica Less)……… 19
Evaluasi Sensori………... 21
Daftar Pustaka……….. 23
SELEKSI DAUN BELUNTAS (Pluchea indica Less) SEBAGAI SUMBER ANTIOKSIDAN ALAMI …………...…...……….. 31
Abstrak ……… 31
Abstract……… 31
Pendahuluan………. 32
Bahan dan Metode……… 33
Waktu dan Tempat Penelitian……….. 33
Bahan Penelitian……….. 33
Metode Penelitian………. 34
Analisis Data……… 36
Hasil dan Pembahasan……….. 37
Seleksi Daun Beluntas sebagai Sumber Antioksidan Berdasarkan Perbedaan Tingkat Ketuaan Daun... 37
Seleksi Daun Beluntas sebagai Sumber Antioksidan Berdasarkan Perbedaan Jenis Pelarut……… 42
Simpulan………... 53
xii
Kemampuan Fraksi Etil Asetat Menangkap Radikal Superoksida.. 61
Kemampuan Fraksi Etil Asetat Menangkap Radikal Hidroksil…... 65
Kemampuan Fraksi Etil Asetat Menangkap Hidrogen Peroksida… 66 Kemampuan Fraksi Etil Asetat Mereduksi Ion Besi……….... 67
Kemampuan Fraksi Etil Asetat Mengkelat Ion Besi (II) dan Ion
AKTIVITAS ANTIOKSIDAN FRAKSI ETIL ASETAT DAN EKSTRAK METANOLIK DAUN BELUNTAS DALAM MENCEGAH WARMED OVER FLAVOR (WOF) DAGING ITIK ... 78
Perubahan Komposisi Kimia Daging Itik selama Perlakuan………. 87 Perubahan Komposisi Asam Lemak Tak Jenuh Ganda (ALTJG) pada Daging Itik selama Perlakuan……... 89 Pembentukan Malondialdehida (MDA) pada Daging Itik selama Perlakuan………... 91 Kandungan Heksanal pada Daging Itik selama Perlakuan……….. 95
Perubahan Warna pada Daging Itik selama Perlakuan ………..…. 98
Karakteristik Sensori Daging Itik yang Ditambahkan Antioksidan selama Perlakuan……….. 101
Simpulan……….. 107
Daftar Pustaka………. 108
xiii Saran………
DAFTAR PUSTAKA………. 119
xiv
1 Bagan alir ruang lingkup penelitian………... 6
2 Itik lokal dan daging itik... 7
3 Mekanisme reaksi oksidasi lemak... 9
4 Pembentukan produk sekunder dari reaksi dekomposisi hidroperoksida.. 10
5 Mekanisme induksi besi (II) mioglobin dalam memacu oksidasi lemak……….. 11
6 Pembentukan heksanal dari dekomposisi asam linoleat……… 12
7 Reaksi TBA dengan MDA………. 14
8 Penghambatan reaksi otooksidasi lemak... 16
9 Potensial oksidasi elektrokimia senyawa fenolik………... 17
10 Struktur dasar flavonoid………. 17
11 Potensi flavonoid sebagai penangkap radikal……… 19
12 Tanaman beluntas... 20
13 Pengelompokan daun beluntas berdasarkan perbedaan tingkat ketuaan daun... 34
14 Kenampakan ketiga kelompok daun beluntas... 34
15 Diagram alir proses ekstraksi dan pengujian aktivitas ekstrak metanolik daun beluntas dan fraksinya……….. 35
16 Penentuan intensitas warna pada pengujian grup senyawa sterol……... 38
17 Kemampuan menangkap radikal bebas DPPH dari ketiga kelompok daun beluntas……….. 41
18 Kemampuan menangkap radikal bebas DPPH dari senyawa antioksidan. 46 19 Penurunan Absorbansi vs waktu dari DPPH˙ pada penambahan antioksidan pada konsentrasi 0.05 mg/ml dan 0.10 mg/ml……….. 48
xv 22 Fraksi konsentrasi DPPH dalam larutan pada kondisi steady state vs
konsentrasi antioksidan (mg antioksidan/g DPPH˙)……….. 51
23 Kemampuan senyawa antioksidan menangkap radikal superoksida…….. 61 24 Mekanisme senyawa antioksidan dalam menangkap radikal bebas……... 63 25 Struktur molekul tanin terhidrolisis dan tanin terkondensasi………. 64 26 Kemampuan senyawa antioksidan menangkap radikal hidroksil……….. 65 27 Kemampuan senyawa antioksidan menangkap hidrogen peroksida…….. 66 28 Kemampuan senyawa antioksidan mereduksi ion besi……….. 67 29 Kemampuan senyawa antioksidan mengkelat ion besi………. 69 30 Kemampuan senyawa antioksidan mengkelat ion besi pada
hemoglobin………. 69
31 Mekanisme senyawa flavonoid mengkelat ion logam………... 70 32 Mekanisme senyawa tanin mengkelat ion logam………..
70
33 Pembentukan senyawa kompleks antara EDTA dan ion logam………… 71 34 Struktur molekul hemoglobin……… 72 35 Kemampuan senyawa antioksidan menghambat oksidasi asam
linoleat--karoten……… 73
36 Proses pemotongan dan persiapan daging itik giling………. 83 37 Proses pengujian aktivitas antioksidan ekstrak metanolik daun beluntas
dan fraksi etil asetat dalam mencegah WOF daging itik pada berbagai perlakuan... 84
38 Pengaruh penambahan senyawa antioksidan terhadap perubahan kadar asam linoleat pada daging itik di berbagai perlakuan……… 90 39 Pengaruh penambahan senyawa antioksidan terhadap perubahan kadar
asam arakidonat pada daging itik di berbagai perlakuan………... 91 40 Pengaruh penambahan senyawa antioksidan terhadap kadar TBARS
xvi
pada daging itik di berbagai perlakuan………... 96 43 Kromatogram GC senyawa volatil dari minyak atsiri daun beluntas
segar)………..
97
44 Pengaruh penambahan senyawa antioksidan terhadap perubahan nilai merah (a) pada daging itik di berbagai perlakuan……….. 98 45 Pengaruh penambahan senyawa antioksidan terhadap perubahan nilai
kuning (b) pada daging itik di berbagai perlakuan………. 99 46 Pengaruh penambahan senyawa antioksidan terhadap perubahan nilai
kecerahan (L) pada daging itik di berbagai perlakuan………... 100 47 Skor kesukaan terhadap aroma daging itik di berbagai perlakuan………. 102 48 Skor intensitas green dan grassy pada daging itik di berbagai
xvii
Halaman
1 Senyawa aldehida hasil otooksidasi asam lemak tak jenuh (ALTJ)…... 13 2 Pembagian senyawa flavonoid berdasarkan perbedaan struktur kimia... 18
3 Potensial oksidasi beberapa senyawa fenolik yang terukur dengan
elektroda karbon gelas……… 19
4 Kandungan fitokimia pada ketiga kelompok daun beluntas…………... 38 5 Kadar air dan rendemen pada ketiga kelompok daun beluntas………... 39 6 Kadar total fenol, total flavonoid, IC50 ketiga kelompok daun beluntas 40
7 Kadar rendemen, total fenol, dan total flavonoid ekstrak metanolik
daun beluntas dan fraksinya……… 43
8 Fitokimia yang terkandung pada ekstrak metanolik daun beluntas dan
fraksinya……….. 44
9 Kemampuan penghambatan (IC50) dari senyawa antioksidan uji……... 47
10 Kemampuan penghambatan (EC50) dan efisien antiradikal (AE) dari
senyawa antioksidan uji….………. 52
11 Kemampuan penghambatan oksidasi (IC50) dari senyawa antioksidan
uji di berbagai sistem uji in vitro………. 62
12 Rancangan percobaan………. 85
13 Rancangan percobaan………. 86
14 Perubahan komposisi kimia daging itik giling di berbagai
perlakuan………. 87
15 Senyawa volatil yang terdeteksi pada ekstrak metanolik daun beluntas (EMB) dan fraksi etil asetat (FEA) yang mempunyai aroma………….. 97
16 Deskripsi aroma pada daging itik selama perlakuan, ekstrak metanolik daun beluntas (EMB), fraksi etil asetat (FEA), dan -tokoferol (AT)…
103
xviii
1 Prosedur analisis kadar air tepung daun beluntas……… 123 2 Hasil analisa varians (Anova) kadar air ketiga kelompok daun
beluntas……… 123
3 Prosedur analisis rendemen……….……… 124 4 Hasil analisa varians (Anova) rendemen ketiga kelompok daun
beluntas……… 124
5 Prosedur analisis total fenol...……….……… 125 6 Hasil analisa varians (Anova) total fenol (TP) ketiga kelompok daun
beluntas………... 125 7 Prosedur analisis total flavonoid……….……… 126 8 Hasil analisa varians (Anova) total flavonoid ketiga kelompok daun
beluntas………...……… 126
9 Prosedur analisis kemampuan menangkap radikal bebas DPPH……… 127 10 Hasil analisa varians (Anova) IC50 ketiga kelompok daun
beluntas……… 128
11 Hasil analisa varians (Anova) total fenol (TP) pada ekstrak metanolik
daun beluntas dan fraksinya………..………….. 129 12 Hasil analisa varians (Anova) total flavonoid pada ekstrak metanolik
daun beluntas dan fraksinya……… 130
13 Hasil analisa varians (Anova) IC50 dari kemampuan menangkap
radikal bebas DPPH oleh ekstrak metanolik daun beluntas, dan
fraksinya serta antioksidan pembanding……….… 131 14 Prosedur analisis kemampuan menangkap radikal hidroksil………….. 132 15 Hasil analisa varians (Anova) IC50 dari kemampuan menangkap
radikal hidroksil oleh ekstrak metanolik daun beluntas, dan fraksinya
xix 18 Prosedur analisis kemampuan menangkap hidrogen peroksida………. 136 19 Hasil analisa varians (Anova) IC50 dari kemampuan menangkap
hidrogen peroksida oleh ekstrak metanolik daun beluntas dan
fraksinya serta antioksidan pembanding……….……… 136 20 Prosedur analisis kemampuan mengkelat ion besi (II)………...………. 137 21 Hasil analisa varians (Anova) IC50 dari kemampuan mengkelat ion
besi oleh ekstrak metanolik daun beluntas, dan fraksinya serta
antioksidan pembanding……….. 137
22 Prosedur analisis kemampuan mengkelat ion besi pada hemoglobin…. 138 23 Hasil analisa varians (Anova) IC50 dari kemampuan mengkelat ion
besi pada hemoglobin (Hb) oleh ekstrak metanolik daun beluntas dan
-fraksinya serta antioksidan pembanding... 138
24 Prosedur analisis kemampuan menghambat oksidasi asam linoleat
-karoten………...………. 139
25 Hasil analisa varians (Anova) IC50 dari kemampuan menghambat
oksidasi asam linoleat- -karoten oleh ekstrak metanolik daun
beluntas, dan fraksinya serta antioksidan pembanding………... 140
26 Prosedur analisis kemampuan mereduksi ion besi ….………...………. 141 27 Hasil analisa varians (Anova) kemampuan mereduksi ion besi oleh
ekstrak metanolik daun beluntas, dan fraksinya serta antioksidan
pembanding………. 141
28 Prosedur analisis kadar air (AOAC 1990)……….. 142 29 Hasil analisa varians (Anova) kadar air daging itik di berbagai
perlakuan... 142
30 Prosedur analisis kadar abu………...……….. 143 31 Hasil analisa varians (Anova) kadar abu daging itik di berbagai
perlakuan………. 143
xx
34 Prosedur analisis total lemak… ……….. 146 35 Hasil analisa varians (Anova) kadar lemak daging itik di berbagai
perlakuan………. 146
36 Prosedur analisis total ion besi..……….. 147 37 Hasil analisa varians (Anova) kadar besi total daging itik di berbagai
perlakuan………. 147
38 Prosedur analisis pH…………..……….. 148 39 Hasil analisa varians (Anova) perubahan pH daging itik di berbagai
perlakuan………. 148
40 Contoh kuesioner uji kesukaan terhadap aroma daging itik…………... 149 41 Hasil analisa varians (Anova) skor kesukaan terhadap aroma daging
itik pada berbagai perlakuan...……… 150
42 Contoh kuesioner uji deskripsi dan pengenalan larutan standar penentu
WOF pada daging itik………. 151
43 Contoh kuesioner uji intensitas green dan grassy pada daging itik
dengan skala tidak terstruktur………. 152
44 Hasil analisa varians (Anova) skor intensitas green dan grassy daging
itik di berbagai perlakuan…………..………... 153 45 Prosedur analisis warna……… ……….. 154 46 Hasil analisa varians (Anova) nilai merah (a) pada daging itik
diberbagai perlakuan…………..………... 155
47 Hasil analisa varians (Anova) nilai kuning (b) pada daging itik di
berbagai perlakuan…………..………... 157
48 Hasil analisa varians (Anova) nilai kecerahan (L) pada daging itik di
berbagai perlakuan…………..………... 159
49 Prosedur analisis kadar TBARS……….. 161 50 Hasil analisa varians (Anova) kadar TBARS daging itik pada berbagai
xxi
perlakuan………. 167
53 Data analisis asam-asam lemak pada daging itik dipanaskan suhu 70
o
C selama 50 menit di berbagai perlakuan……….……….. 168 54 Data analisis asam-asam lemak pada daging itik dipanaskan suhu 70
o
C selama 50 menit dan disimpan di refrigerator suhu 4 oC selama 5
hari di berbagai perlakuan………...……… 169 55 Data analisis asam-asam lemak pada daging itik dipanaskan suhu 70
o
C selama 50 menit, disimpan di refrigerator suhu 4 oC selama 5 hari dan dipanaskan kembali suhu 70 oC selama 10 menit di berbagai
perlakuan………. 170
xxii
a Nilai merah AE Efisiensi antiradikal AL Asam lemak
ALTJ Asam lemak tak jenuh ALTJG Asam lemak tak jenuh ganda AT -tokoferol konsentrasi 300 ppm
b Nilai kuning bb Basis basah b/b Berat per berat BHA Butil hidroksi anisol
BHT Butil hidroksi toluena konsentrasi 200 ppm bk Basis kering
CE Ekuivalen katekin
C Kontrol
DPPH 1,1-difenil-2-pikrilhidrasil DM Daging itik giling mentah DMSO Dimetil sulfoksida
DNA Asam deoksi ribonukleat
DP DM yang dipanaskan suhu 70 oC selama 50 menit
DPP DP yang dipanaskan kembali suhu 70 oC selama 10 menit DPS DP yang disimpan di refrigerator suhu 4 oC, selama 5 hari DPSP DPS yang dipanaskan kembali suhu 70 o C selama 10 menit
EC50 Konsentrasi efektif penghambatan aktivitas biologis sebesar 50% (satuan b/b)
EDTA Asam etilena diamina tetra asetat EMB Ekstrak metanolik daun beluntas
EMB1 Ekstrak metanolik daun beluntas konsentrasi 250 ppm EMB2 Ekstrak metanolik daun beluntas konsentrasi 600 ppm EMR Ekstrak metanolik rosemari
xxiii FEA2 Fraksi etil asetat daun beluntas konsentrasi 600 ppm
FNB Fraksi n-butanol daun beluntas GAE Ekuivalen asam gallat
GPx Glutathion peroksidase
GSH Glutathion reduktase
Hb Hemoglobin
IC50 Konsentrasi penghambatan aktivitas biologis sebesar 50% (satuan b/v)
L Nilai kecerahan LB Liebermann-Burchard MDA Malondialdehida
NADH Nikotinamida adenin dinukleotida NBT Nitroblue tetrazolium
nd Not detected (Tidak terdeteksi) PMS Fenazin metoksulfat
PUFA Polyunsaturated fatty acid
SNR Spesies nitrogen reaktif SOD Superoksida dismutase
SOR Spesies oksigen reaktif TBA Asam tiobarbiturat
TBARS Senyawa reaktif asam tiobarbiturat/Thiobarbituric acid reactive substances
TBHQ Tersier butil hidrokuinon
TEC50 Waktu yang diperlukan untuk mencapai konsentrasi efektif penghambatan
aktivitas biologis sebesar 50% TF Total flavonoid
TP Total fenol UV Ultra violet UV-Vis Ultra violet-visible
PENDAHULUAN
Latar Belakang
Itik lokal merupakan komoditas nasional yang berpotensi sebagai sumber daging (Hendayana 2009). Kontribusi itik sebagai penyedia daging hingga saat ini masih sangat rendah, yaitu sekitar 1.73% (0.1 kg/kapita/tahun dari konsumsi daging nasional yang mencapai 5.79 kg/kapita/tahun) (Ditjennak 2006), sedangkan Ditjennak (2009) menginformasikan bahwa suplai daging yang berasal dari itik lokal hanya sekitar 217.7 ton. Populasi itik di Indonesia menempati urutan keempat di dunia (FAO 2006), sedangkan berdasarkan BPS (1999) bahwa populasi itik lokal di Indonesia cukup tinggi, yaitu 26.3 juta ekor. Itik umumnya dibudidayakan sebagai penghasil telur (Sujana et al. 2009). Oleh karena itu daging itik yang ada di pasaran masih sangat terbatas, biasanya berasal dari betina afkir sebanyak 54.35%, jantan afkir sebanyak 35.41%, jantan dan betina muda sebanyak 18%, dan entok sebanyak 2% (Hardjosworo et al. 2001).
Kendala yang dihadapi dalam pengembangan daging itik, yaitu bertekstur liat (Oteku et al. 2006), memiliki kadar lemak lebih tinggi dari ayam pedaging (Kim et al. 2009), kadar asam lemak tak jenuh (ALTJ) sekitar 60% dari total asam lemak (AL) (Estevez et al. 2007), dan serabut daging berwarna merah karena mengandung pigmen heminik (hemoglobin dan mioglobin) yang cukup tinggi (Baeza 2006; Kim et al. 2009).
2011). Menurut Hoac et al. (2009) bahwa pemanasan daging itik pada suhu 60 dan 80 oC terjadi kerusakan glutathion peroksidase (GPx) masing-masing sebesar 20% dan 80%.
Salah satu akibat dari proses oksidasi adalah munculnya warmed over flavor (WOF), yaitu indikasi penyimpangan flavor daging yang telah dipanaskan dan disimpan di refrigerator selama 48 jam pada suhu 4 oC (Jayathilakan et al. 2007). Indikator terjadinya WOF pada daging adalah terbentuknya senyawa volatil, seperti heksanal, pentanal, 2,4-dekadienal, 2,3-oktanadion, 2-oktenal (Juntachote et al. 2007), 2,4-nonadienal, trans 2-dekenal (Konopka et al. 1995). Heksanal merupakan aldehida jenuh hasil oksidasi sekunder asam linoleat (C18:2
-6) yang sering digunakan sebagai marker oksidasi daging (Pignoli et al. 2009). Antioksidan dapat digunakan untuk mencegah terbentuknya WOF pada daging. Pemakaian antioksidan sintetis pada produk pangan mulai mengalami penurunan dengan semakin meningkatnya kesadaran masyarakat terhadap kesehatan (Valentão et al. 2010). Berbagai penelitian tentang potensi bahan alami sebagai sumber antioksidan untuk produk daging telah dilakukan, diantaranya bawang putih (Mielnik 1997), ekstrak buah anggur (Vitis vinifera) (Pazos et al.
2005), ekstrak etanolik dan bubuk galagal (Juntachote et al. 2007). Penggunaan tanaman herba dan rempah-rempah yang kaya akan senyawa polifenol pada produk pangan menunjukkan aktivitas antioksidatif, seperti kemampuan menangkap radikal bebas dan spesies oksigen reaktif (SOR) (Mielnik et al. 2008), mengkelat dan mereduksi ion logam besi (Arabshahi-Delouee & Urooj 2007), menghambat oksidasi asam linoleat- -karoten (Subhasree et al. 2009). Oleh karena itu usaha pencarian sumber antioksidan baru terutama yang berasal dari tanaman asli Indonesia terus dilakukan.
satunya aktivitas antioksidan. Hasil penelitian sebelumnya telah menginformasikan bahwa ekstrak etanolik daun beluntas telah terbukti mempunyai kemampuan menangkap radikal bebas 1,1-difenil-2-pikrilhidrasil (DPPH) (Widyawati 2004), asam 2,2'-azino-bis-(3-etilbensotiasolin-6-sulfonat) (ABTS), mereduksi ion besi, dan menghambat oksidasi asam linoleat (Andarwulan et al. 2010).
Pada penelitian ini dilakukan ekstraksi daun beluntas dengan metanol dan selanjutnya dilakukan fraksinasi dengan beberapa pelarut dengan tingkat kepolaran yang berbeda, meliputi etil asetat, n-butanol, dan air. Pertimbangan penggunaan metanol dalam ekstraksi daun beluntas berdasarkan informasi sebelumnya bahwa metanol secara efisien mengekstrak senyawa fenolik sehingga dihasilkan rendemen dan aktivitas antioksidan yang tinggi pada daun spesies
etlingera (Chan et al. 2007a) dan daun mulberry (Arabshahi-Delouee & Urooj 2007; Yen et al. 1996). Selain itu metanol efektif mengekstrak fenolik pada sel tanaman dengan berat molekul rendah dan tingkat kepolaran sedang (Yu Lin et al.
2009), serta melarutkan flavonoid aglikon (Dehkharghanian et al. 2010).
Fraksinasi ekstrak metanolik dengan berbagai pelarut yang berbeda tingkat kepolaran, seperti etil asetat, n-butanol, dan air dapat dilakukan untuk mendapatkan fraksi yang mengandung senyawa antioksidan dengan komposisi sesuai sifat pelarut (kepolaran dan viskositas) (Lai et al. 2009). Etil asetat dilaporkan dapat mengekstrak senyawa alkaloid, aglikon, dan glikosida (Houghton & Raman 1998) serta senyawa fenolik dengan berat molekul rendah hingga tinggi (Mariod et al. 2010). n-Butanol dapat mengekstrak senyawa polar seperti glikosida, aglikon, dan gula (Liu et al. 2011). Sedangkan air dapat mengekstrak senyawa polar seperti glikosida, asam amino, dan gula (Houghton & Raman 1998) serta senyawa polar aglikon (Liu et al. 2011).
superoksida dan hidroksil), mereduksi dan mengkelat ion besi, dan menghambat oksidasi asam linoleat- -karoten.
Perumusan Masalah
Berdasarkan latar belakang di atas diperoleh permasalahan yang memerlukan pengkajian lebih lanjut sebagai berikut :
1. Daging itik mudah mengalami oksidasi karena pemanasan, oleh karenanya perlu dikaji tingkat penurunan kualitas selama penyimpanan daging itik yang telah dipanaskan.
2. Proses pemanasan dapat memacu munculnya WOF, maka perlu dikaji pengaruh pemanasan terhadap munculnya WOF selama penyimpanan daging itik.
3. Daun beluntas telah diketahui mempunyai aktivitas antioksidan, perlu diketahui aktivitas ekstrak metanolik dan fraksinya yang diharapkan akan lebih mampu menangkap SOR (hidrogen peroksida, radikal superoksida dan hidroksil), mereduksi dan mengkelat ion besi, dan menghambat oksidasi asam linoleat- -karoten serta mencegah WOF pada daging itik yang telah dipanaskan.
Tujuan Penelitian
Tujuan Umum
Tujuan umum penelitian ini adalah untuk mempelajari aktivitas antioksidan ekstrak metanolik daun beluntas dan fraksinya serta kemampuan mencegah WOF pada daging itik yang telah dipanaskan.
Tujuan Khusus
Penelitian ini secara khusus dilakukan untuk :
1. Memperoleh ekstrak metanolik daun beluntas dan fraksinya yang berpotensi sebagai sumber antioksidan berdasarkan kemampuannya menangkap radikal bebas 1,1-difenil-2-pikrilhidrasil (DPPH), menangkap SOR (hidrogen peroksida, radikal superoksida dan hidroksil), mereduksi dan mengkelat ion
besi, dan menghambat oksidasi asam linoleat- -karoten.
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi tentang :
1. Tersedianya informasi tentang aktivitas antioksidan ekstrak metanolik daun beluntas dan fraksinya dalam menangkap SOR (hidrogen peroksida, radikal superoksida dan hidroksil), mereduksi dan mengkelat ion besi, dan
menghambat oksidasi asam linoleat- -karoten.
2. Tersedianya informasi tentang kemampuan antioksidan ekstrak metanolik daun beluntas dan fraksinya dalam mencegah WOF pada daging itik yang telah dipanaskan sehingga dapat mempertahankan kualitas daging itik dan tingkat penerimaan konsumen terhadap daging itik meningkat.
3. Dalam jangka panjang untuk mempertahankan pangan nasional dengan melestarikan dan memanfaatkan sumberdaya lokal.
Hipotesis
Hipotesis yang dapat diajukan pada penelitian ini adalah :
1. Ekstrak metanolik daun beluntas dan fraksinya berpotensi sebagai antioksidan berdasarkan kemampuannya menangkap radikal bebas DPPH.
2. Ekstrak metanolik daun beluntas dan fraksinya mempunyai kemampuan menangkap SOR (hidrogen peroksida, radikal superoksida dan hidroksil), mereduksi dan mengkelat ion besi, dan menghambat oksidasi asam linoleat -karoten.
3. Ekstrak metanolik daun beluntas dan fraksinya mempunyai aktivitas antioksidan yang dapat mencegah WOF pada daging itik yang telah dipanaskan.
Ruang Lingkup Penelitian
Daun beluntas
Diuji aktivitas antioksidan in vitro
Menangkap SOR Mereduksi & mengkelat ion besi Menghambat oksidasi asam linoleat- -karoten
Digunakan untuk mencegah WOF daging itik
TINJAUAN PUSTAKA
Daging Itik
Deskripsi Daging Itik
Klasifikasi zoologis menggolongkan itik ke dalam kelas Aves, ordo
Arseriformes, famili Anatidae, genus Anas,dan spesies Platyhynchos (Srigandono, 1996). Itik terdiri atas dua tipe, yaitu pedaging dan petelur. Keduanya dibedakan berdasarkan postur tubuh. Dada itik pedaging lebih sejajar dengan lantai sedangkan itik petelur lebih tegak lurus terhadap lantai. Pada umumnya itik lokal yang dibudidayakan oleh masyarakat untuk menghasilkan telur dan masih jarang yang dibudidayakan untuk diambil dagingnya.
Gambar 2. Itik lokal dan daging itik.
Daging itik sebagian besar tersusun atas daging merah dengan kadar pigmen heminik (hemoglobin dan mioglobin) relatif tinggi (Baéza 2006; Kim et al.
2009). Daging bagian dada tersusun atas daging merah sebanyak 84% dan daging putih 16% (Smith et al. 1993), sedangkan daging ayam pedaging 100% berisi serabut putih. Warna merah daging itik meningkat seiring dengan bertambahnya kadar ion besi. Kandungan Fe daging merah pada itik sebesar 2.40 mg/100 g daging mentah termasuk kulit, sedangkan kandungan Fe daging putih pada ayam pedaging sebesar 0.90 mg/100 g daging mentah termasuk kulit (Staldeman et al.
Daging itik mengandung protein berkisar antara 18.6-19.6% dan lemak berkisar antara 2.7-6.8% (Jun et al. 1996), sedangkan Farrell (2000) menyatakan bahwa protein karkas berkisar antara 14-17% dan lemak berkisar antara 16-23%. Kadar protein daging merah lebih rendah dari daging putih (Soeparno 2005). Kadar protein dan lemak pada daging itik sangat dipengaruhi oleh genetik, jenis kelamin, pakan, dan umur (Baéza 2006). Daging itik tersusun atas ALTJ sebesar 60% dari total asam lemak yang terakumulasi pada jaringan otot dan adiposa (Chartrin et al. 2006).
Daging itik mempunyai ukuran serabut otot lebih besar dari daging ayam (Lukman 1998) maupun daging entok (Sudjatinah 2000), sehingga menyebabkan daging itik teksturnya lebih keras (liat). Perbedaan komposisi kimia daging itik dapat mempengaruhi off flavor yang dihasilkan (Smith et al. 1993). Daging itik mempunyai sensasi off flavor, seperti bau amis, bau darah, apek, tengik, bau seperti kentang rebus, dan bau seperti telur asin (Hustiany 2001) cenderung tidak disukai konsumen. Oteku et al. (2006) menyatakan bahwa tingkat penerimaan masyarakat terhadap daging itik masih rendah dengan skor penerimaan dari kurang suka hingga tidak suka mencapai 57.8%.
Kerusakan Oksidasi pada Daging Itik
Oksidasi lemak adalah penyebab utama kerusakan daging dan produk olahannya, sehingga mempengaruhi masa simpannya (Gatellier et al. 2007). Oksidasi lemak melibatkan reaksi serah terima elektron dari radikal bebas dan spesies oksigen reaktif (SOR) (Živković et al. 2008). SOR adalah ion atau molekul yang sangat kecil dan reaktif, terdiri atas spesies radikal [hidroksil (OH ),
superoksida (O2-), dan peroksil (ROO )] dan non radikal [hidrogen peroksida
(H2O2), oksigen singlet (1O2), dan ozon (O3)] (Gulcin 2010). Radikal bebas
merupakan molekul atau ion yang mempunyai elektron tidak berpasangan dan cenderung menangkap elektron dari senyawa lain untuk menjadi netral. Radikal bebas ini biasanya tidak stabil, reaktif, dan mempunyai waktu paruh pendek (Moein et al. 2007).
secara mekanik, penggilingan, proses pengolahan, pemasakan, dan lama penyimpanan) (Gatellier et al. 2007). Pemotongan, pencacahan, dan perebusan daging dapat memacu reaksi oksidasi sehingga penurunan kualitas daging lebih cepat dibandingkan dengan kondisi utuh dan mentah selama penyimpanan (Lee et al. 2006). Terjadinya reaksi oksidasi dapat menurunkan penerimaan konsumen dan kualitas nutrisi, karena hilangnya sejumlah asam lemak esensial, vitamin, karbohidrat, protein, perubahan warna, tekstur, flavor, dan aroma pada pangan selama penyimpanan (Estevez et al. 2007).
RH + •O-O• → R• + •OOH (tahap inisiasi)
R• + •O-O• → ROO• (tahap propagasi)
ROO• + RH → ROOH + R•
R• + •OOH → ROOH (tahap terminasi)
R• + R• → RR
R•+ ROO• → ROOR
ROO•+ ROO• → ROOR + •O-O•
ROOH → RO• + •OH (tahap inisiasi sekunder)
β ROOH → RO• + ROO• + H2O
Gambar 3. Mekanisme reaksi oksidasi lemak (RH = ALTJ, ROO• = radikal
peroksil, R• = radikal alkil, RO• = radikal alkoksil) (Farhoosh 2005).
Reaksi oksidasi ALTJ pada daging merupakan reaksi berantai yang melibatkan 3 tahap reaksi, yaitu tahap permulaan (inisiasi), perambatan (propagasi), dan penghentian (terminasi) (Gambar 3 dan 4). Pada tahap permulaan, radikal bebas lemak terbentuk akibat pemutusan atom H dari gugus ALTJ (RH) pada atom C dengan energi ikatan terendah (posisi bis metilen/ karbon -metilen). Radikal yang terbentuk dapat menjadi inisiator reaksi otooksidasi antara radikal
peroksida (ROO•) dengan ALTJ (RH) menghasilkan hidroperoksida (ROOH) dan radikal hidrokarbon (R•) yang baru. Pada tahap terminasi terjadi penggabungan
seperti alkohol, keton, aldehida, asam karboksilat, ester maupun hidrokarbon
Gambar 4. Pembentukan produk sekunder dari reaksi dekomposisi hidroperoksida
(R”, R’ = gugus alkil dengan panjang rantai berbeda, R”CHOOHR’ = senyawa peroksida, R”CHO R’ = radikal alkoksil, R”CHO = senyawa
aldehida, R”COOH, RCOOH= senyawa asam karboksilat, R”CHOHR’ =senyawa alkohol sekunder, R”COR’ = senyawa keton, RH = senyawa
hidrokarbon, ROH = senyawa alkohol primer) (Pokorny et al. 2001).
Reineccius (2006) menyatakan bahwa pigmen heme (mioglobin dan hemoglobin) dapat sebagai katalis utama oksidasi lemak pada daging merah mentah, sedangkan non heme berfungsi sebagai prooksidan pada daging yang telah dimasak. Masqood & Benjakul (2011) juga menginformasikan bahwa hemoglobin dapat menjadi sumber oksigen aktif terjadinya reaksi otooksidasi. Ion besi pada cincin heme yang berada dalam bentuk Fe2+ dapat berubah menjadi Fe3+ melalui proses otooksidasi. Strlic et al. (2002) menyatakan bahwa ion Fe3+ dapat bereaksi secara otooksidasi dengan hidroperoksida menghasilkan senyawa volatil dengan mendonorkan elektron membentuk radikal alkoksil, yang selanjutnya memacu pembentukan senyawa yang mampu menginisiasi dan mempropagasi oksidasi lemak. Oksimioglobin dan metmioglobin dapat menghasilkan ferrilmioglobin (metmioglobin teraktivasi) dengan adanya hidrogen peroksida atau lipid hidroperoksida dan merupakan inisiator oksidasi lemak.
penyimpangan flavor daging ini dikenal dengan warmed over flavor (WOF) (Pokorny et al. 2001). WOF terjadi pada produk daging disebabkan reaksi otooksidasi lemak menghasilkan hidroperoksida, yang selanjutnya terdekomposisi menghasilkan sejumlah senyawa volatil (Jayathilakan et al. 2007). WOF dapat terjadi pada bahan pangan berbasis lemak yang telah digoreng atau dimasak dan disimpan di suhu rendah, selama penyimpanan senyawa hasil oksidasi yang bersifat volatil diserap oleh bahan pangan tersebut. Ketika bahan pangan tersebut dipanaskan kembali maka senyawa volatil tersebut akan dilepaskan (Herschowitz
et al. 2003).
MbO2Fe(II) + O2 MbFe(III) + 2O2-
MbO2Fe(II) + RH HmbFe(II) + R + O2
MbO2Fe(II) + ROOH HmbFe(II) + ROO + O2
MbFe(III) + RH HmbFe(III) + R
MbFe(III) + ROOH HmbFe(III) + ROO
MbFe(III) + H2O2 Mb Fe(IV)=O + -OH + H
Mb Fe(IV)=O + RH MbFe(IV)=O + R + H+
MbO2Fe(II) + H2O2 MbFe(IV)=O + H2O + O2
Gambar 5. Mekanisme induksi besi (II) mioglobin dalam memacu oksidasi lemak (MbFe(II) = deoksimioglobin, MbO2Fe(II) = oksimioglobin,
HmbFe(II) = hemokrom, HmbFe(III) = hemikrom, MbFe(III) = metmioglobin, Mb Fe(IV)=O = perferilmioglobin, MbFe(IV)=O = ferrilmioglobin) (Huang et al. 2010).
Pemanasan dapat mempercepat terjadinya WOF, karena pemanasan menyebabkan denaturasi protein heme, kerusakan struktur membran sel, dan pencampuran komponen penyusun sel (Reineccius 2006). WOF akan berkembang cepat selama daging disimpan di refrigerator dengan karakteristik sensori yang tidak diinginkan, ditandai adanya bau paint atau wet cardboard (Jayathilakan et al. 2007), oxidized/rancid, fishy, stale, dan metallic (Grigioni et al. 2000). Flavor
100 kkal/mol 50 kkal/mol 75 kkal/mol
CH3─(CH2)3─CH2─CH=CH─CH2─CH=CH─CH2─(CH2)6─COOH
14 13 12 11 10 9
- H (Tahap inisiasi)
CH3─(CH2)4─CH─CH=CH─CH=CH─(CH2)7─COOH
CH3─(CH2)4─CH─CH=CH─CH=CH─(CH2)7─COOH
O O
CH3─(CH2)4─CH─CH=CH─CH=CH─(CH2)7─COOH
O O H
CH3─(CH2)4─CH─CH=CH─CH=CH─(CH2)7─COOH
O
CH3-CH2-CH2-CH2-CH2-CHO + CH=CH-CH=CH(CH2)7COOH
Heksanal (Tahap terminasi)
Gambar 6. Pembentukan heksanal dari dekomposisi asam linoleat (Verlet et al. 2007).
Pokorny et al. (2001) menyatakan bahwa terjadinya WOF dipengaruhi oleh faktor endogenus dan eksogenus. Faktor endogenus, meliputi tipe daging dan spesies (genetik), antioksidan aktif dalam daging (dipeptida, tokoferol dsb), dan enzim pendeaktif SOR, seperti superoksida dismutase (SOD) dan glutathion reduktase (GSH), serta prooksidan, seperti ion besi heme, non heme, dan SOR. Faktor eksogenus, terdiri atas jenis pengolahan, teknik dan lama pemasakan, kondisi pemasakan awal dan akhir, lama dan suhu penyimpanan, sistem pengemasan, dan penggunaan antioksidan.
(Tahap propagasi) + O2
+ H
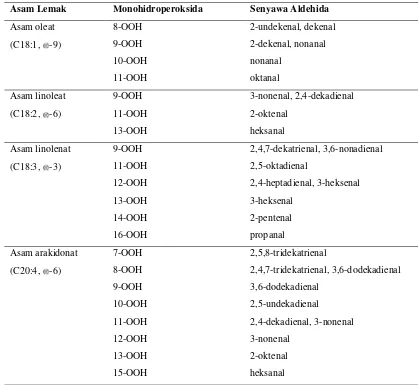
Tabel 1. Senyawa aldehida hasil otooksidasi asam lemak tak jenuh (ALTJ)
Asam Lemak Monohidroperoksida Senyawa Aldehida
Asam oleat
Senyawa volatil yang menjadi indikator munculnya WOF, meliputi heksanal, pentanal, (E,E)-2,4-dekadienal, 2,3-oktanadion, 2-oktenal (Junthachote
et al. 2007), 1-okten-3-on, (E,E)-2,4-nonadienal, trans-4,5-epoksi-(E)-2-dekenal (Konopka et al. 1995). Senyawa aldehida volatil adalah komponen utama yang berkontribusi terjadinya off flavor pada bahan pangan (Pignoli et al. 2009). Heksanal adalah salah satu jenis senyawa flavor volatil yang dapat digunakan sebagai indikator WOF pada daging itik, akibat oksidasi ALTJG ( -6), terutama asam linoleat dan arakidonat (Gambar 6 & Tabel 1).
deoksinukleat (DNA), amino dari fosfolipid, dan asam amino melalui basa schiff
terkonjugasi yang mempunyai karakteristik sistem fluoromorfik N-C=C-C=N (Rababah et al. 2004; Ganhao et al. 2011).
Gambar 7. Reaksi TBA dengan MDA (Fernindez et al. 1997).
MDA terbentuk dari oksidasi ALTJG dengan ikatan rangkap paling sedikit 3 buah. Senyawa ini dapat bereaksi dengan asam 2-thiobarbiturat (TBA)
membentuk larutan berwarna merah yang dapat terdeteksi pada 532–535 nm. Intensitas warna yang terukur menunjukkan konsentrasi MDA, yang berkorelasi dengan sensori dan WOF (Mendes et al. 2009). Gorelik et al. (2008) menyatakan bahwa MDA tidak merupakan indikator stoikiometri reaksi oksidasi lemak, meskipun akumulasi MDA menyatakan intensitas terjadinya proses oksidasi lemak. Hal ini disebabkan senyawa produk oksidasi yang lain (2,4-alkadienal/2,4-dekadienal, protein, produk pencoklatan Maillard, dan produk degradasi gula) dapat bereaksi dengan TBA (Igene et al. 1985). Oleh karena itu penentuan nilai TBA selalu dinyatakan dengan senyawa reaktif terhadap TBA (TBARS/thiobarbituric acid reactive substances) (Tokur et al. 2006).
Antioksidan
Deskripsi Antioksidan
Antioksidan adalah senyawa atau bahan yang digunakan pada konsentrasi lebih rendah dari substratnya secara signifikan dapat menunda atau mencegah oksidasi (Moein et al. 2007). Penggunaan antioksidan pada daging atau produk olahannya dapat menghambat ketengikan oksidatif, mempertahankan warna daging, dan memperpanjang masa simpan (Choe et al. 2011). Ketengikan (off flavor) daging yang kaya ALTJG dapat diminimalkan dengan mengkombinasikan
Kromagen TBA
Malondialdehida TBA
antioksidan yang mampu menangkap radikal bebas, mengkelat dan mereduksi ion logam (Ganhao et al. 2010).
Pengelompokan Antioksidan
Antioksidan berdasarkan fungsinya dibedakan menjadi tiga kelompok, yaitu antioksidan primer, sekunder dan tersier. Antioksidan primer dapat mencegah pembentukan radikal bebas dan memutus rantai reaksi radikal bebas dengan cara mendonorkan atom hidrogen, diantaranya SOD, katalase, GSH,
fenolik maupun vitamin E ( -tokoferol). Antioksidan sekunder berfungsi mendekomposisi peroksida lemak, mengkelat ion logam, menangkap oksigen, mengubah hidrogen peroksida menjadi senyawa non radikal, mengabsorbsi radiasi ultra violet (UV), atau mendeaktivasi oksigen singlet, meliputi vitamin C (asam
askorbat), vitamin E, -karoten, asam urat, bilirubin, dan albumin. Antioksidan tersier berperan memperbaiki kerusakan sel-sel dan jaringan yang diakibatkan oleh radikal bebas, meliputi methionin sulfoksida reduktase yang berfungsi untuk memperbaiki asam deoksiribonukleat (DNA) pada inti sel (Pokorny et al. 2001).
Antioksidan berdasarkan asalnya dibagi menjadi dua, yaitu antioksidan alami dan sintetik. Antioksidan alami diperoleh dari hasil ekstraksi bahan alami atau terbentuk dari reaksi-reaksi kimia selama proses pengolahan (Trilaksani 2003), meliputi fenol dan turunannya, karotenoid, tokoferol, dan asam askorbat (Cahyadi 2005). Antioksidan sintetik diperoleh sebagai hasil sintesis reaksi kimia (Trilaksani 2003), seperti butil hidroksi anisol (BHA), butil hidroksi toluena (BHT), dan tersier butil hidrokuinon (TBHQ). Penggunaan antioksidan sintetik masih dikuatirkan akan efek sampingnya (Juntachote et al. 2007). BHA dapat menimbulkan pembengkakan organ hati, mempengaruhi aktivitas enzim dalam hati, menyebabkan pendarahan fatal pada organ pernapasan, pencernaan, dan organ testes epididimus serta pankreas (Farago et al. 1989), luka pada kandung kemih, dan kerongkongan pada hewan coba (Gharan & El-Kadi 2005). BHT dapat menyebabkan perubahan pada tiroid tikus, stimulasi sintesis DNA, dan induksi enzim (Farago et al. 1989).
Mekanisme Antioksidatif
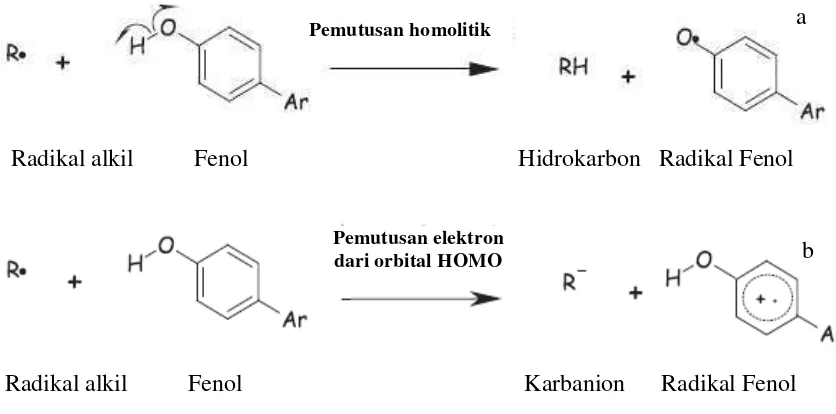
menghambat pembentukan oksidan reaktif, menghambat kofaktor dan enzim oksidatif (Saraf et al. 2007). Banu et al. (1985) menyatakan bahwa mekanisme senyawa antioksidan dalam menghambat reaksi pembentukan radikal bebas, melalui kemampuan mendonorkan hidrogen atau elektron, mengkelat dan mereduksi ion logam.
A–H + R-O-O• → A• + R-O-OH A–H + R-O• → A• + R-OH
A• + R-O-O• → A-O-OR
A• + R-O• → A-OR
A• + A• → A-A
A• + O2 → A-O-O• A• + R-H → A-H + R
A-H + ROOH A + RO + H2O
A-H + O2 A + HO2
AOOR AO + RO
Gambar 8. Penghambatan reaksi otooksidasi lemak (RH = asam lemak tak jenuh, AH = antioksidan, ROO = radikal peroksil, RO = radikal alkoksil, R = radikal alkil, A = radikal antioksidan) (Pokorny 2001).
Senyawa Fenolik
Senyawa fenolik adalah metabolit sekunder tanaman dengan struktur molekul bervariasi dan bertanggung jawab pada sifat organoleptik pada pangan atau minuman, terutama warna, flavor, rasa, nutrisi, astringency, dan bitterness
(Tapas et al. 2008). Secara fisiologis senyawa fenolik mempunyai beberapa aktivitas biologis, seperti antialergi, antiinflammasi, antimikrobial, antibakterial, antioksidan, antitrombotik, kardioprotektif, dan efek vasodilatori (Aberoumand & Deokule 2008).
mudah mengalami oksidasi sehingga menyebabkan fenolik mampu menangkap radikal bebas (Benbrook 2005).
Gambar 9. Potensial oksidasi elektrokimia senyawa fenolik (Simic et al. 2007).
Flavonoid adalah kelompok terbesar dari fenolik dengan kapasitas antioksidan yang kuat (Aberoumand & Deokule 2008). Flavonoid termasuk kelompok benzo- -piron dengan struktur umum difenilpropan (C6-C3-C6) terdiri dari 2 (dua) cincin aromatis yang dihubungkan oleh 3 (tiga) atom karbon membentuk heterosiklik teroksigenasi, ditandai dengan A, B, C (Filipiak 2001). Berdasarkan perbedaan strukturnya, flavonoid dibedakan atas flavonol, flavon, flavanol, isoflavon, flavanon, flavanonol, anthosianidin, dan proanthosianidin (Lugasi et al. 2003).
Gambar 10. Struktur dasar flavonoid (Filipiak 2001).
Tabel 2. Pembagian senyawa flavonoid berdasarkan perbedaan struktur kimia
Efektivitas flavonoid sebagai penangkap radikal dan pengkelat ion logam ditentukan oleh adanya struktur (katekol) ortho dihidroksi pada cincin B, ikatan rangkap pada C2-3 yang terkonjugasi dengan gugus fungsi C4 okso, gugus OH
pada C3 di cincin C, dan gugus OH pada C5 di cincin A (Tapas et al. 2008).
Kombinasi gugus C3-OH dan C5-OH dengan C4-karbonil dan ikatan rangkap C2-3
Tabel 3. Potensial reduksi beberapa senyawa fenolik yang terukur dengan elektroda karbon gelas
Jenis Senyawa Fenolik Potensial Reduksi (Volt)
Erioduktiol + 0.51 ; + 1.20
Katekin + 0.53 ; + 0.88
Asam kafeat + 0.53
Asam gallat + 0.54 ; + 0.87
Hidrokuinon + 0.57
Pirokatekin + 0.61
Asam siringat + 0.75
Guaiakol + 0.77
Siringaldehida + 0.81
Asam ferulat + 0.82
Asam p-koumarat + 0.85
Asam vanilat + 0.88
Asetovanilon + 0.89
Vanilin + 0.92
Resorsinol + 0.94
Fenol + 0.98
Asam o-hidroksi fenil asetat + 9.98 Asam m-hidroksi fenil asetat + 1.02 Asam p-hidroksi fenil asetat + 1.02 Asam p-hidroksi bensoat + 1.15 2,4-Dihidroksi asetofenon + 1.15
2-Hidroksi asetofenon + 1.25
Sumber : Chaviari et al. (1988)
Gambar 11. Potensi flavonoid sebagai penangkap radikal (Amic et al. 2003).
Beluntas (Pluchea indica Less)
Deskripsi Beluntas
penyakit (sakit perut, asma, batuk, reumatik, wasir, penyakit kulit, keseleo, encok, sakit pinggang, demam, datang bulan tidak teratur, dan keputihan) (Manan 2002; Raharjo & Horsten 2008).
Gambar 12. Tanaman beluntas
Tanaman ini dapat tumbuh liar di daerah kering dengan tekstur tanah keras dan berbatu serta memerlukan cukup cahaya matahari. Beluntas termasuk tanaman perdu, berkayu, dan bercabang dengan rusuk halus, dan berbulu lembut. Tanaman ini dapat diperbanyak dengan cara stek dan tingginya dapat mencapai 2 meter. Berbunga sepanjang tahun dan mempunyai akar tunggang. Berdaun tunggal dengan tangkai pendek, letaknya berseling, bentuk bundar seperti telur sungsang. Ujung daun bundar, tepi bergerigi sampai bergigi dengan pertulangan menyirip, berwarna hijau terang, berkelenjar dengan panjang 2.5-9 cm dan lebar 1-5.5 cm, berbau harum dan berasa agak getir. Berbunga majemuk dengan bentuk malai rata yang keluar dari ujung cabang dan ketiak daun. Bunga bercabang banyak, berbentuk bonggol, bergagang atau duduk, bentuknya seperti silinder dengan panjang 5-6 mm, berbulu lembut, berwarna ungu, dan pangkalnya berwarna ungu muda. Kepala sari menjulur dan berwarna ungu. Kepala putik berwarna putih atau putih kekuningan. Putik berbentuk jarum dengan panjang ± 6 mm. Buah beluntas berbentuk seperti gasing, warnanya coklat dengan sudut-sudut putih, dan lokos (gundul atau licin). Ukuran buah relatif kecil, keras, dan berwarna coklat dengan panjang 1 mm. Biji kecil dan berwarna coklat keputih-putihan (Dalimarta 2003; Raharjo & Horsten 2008).
Komposisi Kimia Beluntas
Biswas et al. 2007). Hal ini disebabkan beluntas mengandung senyawa aktif, seperti lignan, seskuisterpena, fenilpropanoid, bensoid, monoterpena, triterpena, sterol, alkana, fenol hidrokuinon, vitamin A dan C, alkaloid, flavonoid, tanin, minyak atsiri, asam klorogenik, asam amino (leusin, isoleusin, triptofan, dan treonin) (Luger et al. 2000; Dalimarta 2003; Ardiansyah et al. 2003).
Biswas et al. (2005) menyatakan bahwa ekstrak metanolik akar beluntas mengandung senyawa stigmasterol (+ sitosterol), stigmasterol glikosida (+ -sitosterol-glikosida), 2-(prop-1-unil)-5-(5,6-dihidroksi heksa-1,3-diunil)-tiofena, dan (-)-katekin. Traithip (2005) menyatakan bahwa daun beluntas juga mengandung sejumlah senyawa volatil kelompok terpena, seperti boehmeril asetat, HOP-17 (21)-en 3 -asetat, linaloil glukosida, linaloil apiosil glukosida, linaloil hidroksi glukosida, pluseosida C, kuauhtermona, 3-(β’-γ’-diasetoksi-β’ -metil-butiril), pluseol A, pluseol B, pluseosida A, pluseosida B, pluseosida E, dan pterokarptriol.
Ekstrak etanolik dan minyak atsiri daun beluntas menunjukkan aktivitas antioksidan dalam sistem asam linoleat- -karoten dan mampu menangkap radikal bebas DPPH (Widyawati 2004). Menurut Andarwulan et al. (2010) bahwa daun beluntas mengandung senyawa flavonol, meliputi mirisetin, kuersetin, dan
kaemferol, yang mampu menangkap radikal DPPH dan ABTS2+ , mereduksi ion besi,, dan menghambat pembentukan MDA.
Evaluasi Sensori
disingkirkan (Gasong 2005). Menurut Mielgaard et al. (2007) ada 3 (tiga) kelompok variabel yang harus dikontrol untuk mendapatkan perbedaan nyata antar sampel yang terukur, yaitu : 1). Pengontrolan terhadap proses pengujian, meliputi lingkungan, tempat pengujian, penggunaan booth atau meja diskusi, pencahayaan, sistem ventilasi udara, ruang persiapan, pintu masuk dan keluar, 2). Pengontrolan produk, meliputi penggunaan peralatan, cara penyiapan, pemberian kode, dan cara penyajian, 3). Pengontrolan terhadap panel, meliputi prosedur yang digunakan oleh panelis dalam mengevaluasi sampel.
Evaluasi sensori berdasarkan tujuan pengujiannya dapat dibedakan menjadi 3 (tiga), yaitu uji afektif, uji pembedaan, dan uji deskriptif. Uji afektif bertujuan untuk menilai respon pribadi (kesukaan atau penerimaan) dari produk tertentu atau karakteristik produk spesifik tertentu. Uji Pembedaan bertujuan untuk menilai perbedaan sensori antara sampel yang diuji atau atribut X yang berbeda diantara sampel. Uji deskriptif adalah metode yang melibatkan deteksi (diskriminasi) dan deskripsi antara aspek sensori kualitatif dan kuantitatif dari produk (Meilgaard et al. 2007).
Analisis deskriptif secara luas digunakan untuk pengembangan produk dan pengontrolan kualitas produk (Abdi & Valentin 2007). Metode ini melibatkan panelis terlatih, yang diperoleh melalui hasil training berdasarkan kemampuan sensorinya untuk mendeskripsikan dan mengevaluasi perbedaan sensori antara produk yang diuji. Panelis dipilih dari sumber yang tidak terlibat dalam pembuatan produk untuk mengurangi bias dari produk. Kriteria yang harus dipenuhi dalam pemilihan panelis, yaitu individu yang mengkonsumsi produk dengan frekuensi rata-rata atau lebih akan lebih sensitif dibandingkan dengan yang jarang mengkonsumsi dan kemampuan pembedaan terhadap produk uji memberi hasil yang lebih terarah secara berturut-turut (Stone & Sidel 1998; Carpenter et al. 2000). Pelatihan panelis menggunakan produk dan senyawa standar (reference) dengan tujuan untuk menstimulasi penurunan istilah-istilah. Pelatihan bertujuan untuk mengembangkan istilah yang konsisten, tetapi panelis bebas untuk memperkirakan skor yang akan diberikan, menggunakan skala garis 15 cm (Gacula 1997; Meilgaard et al. 2007).
kemampuan tinggi dalam mendeteksi dan mendeskripsikan off flavor harus dilakukan melalui seleksi, pelatihan, dan uji panelis. Uji yang dapat dilakukan untuk mengetahui intensitas off flavor pada daging itik adalah uji skoring, uji skalar garis dan uji deskripsi. Uji skalar garis adalah uji yang dilakukan oleh panelis untuk memberikan penilaian skala intensitas off flavor dimulai dari garis sebelah kiri menuju ke arah kanan. Semakin ke kanan intensitas off flavor yang terdeteksi semakin meningkat (Mielgaard et al. 2007).
Daftar Pustaka
Abdi H, Valentine D. 2007. Some New and Easy Ways to Describe, Compare and Evaluate Products and Assessors. In: SPISE 2007, editor. New Trends in Sensory Evaluation of Food and Non-Food Products. Vietnam : Ho Chi Minh.
Aberoumand A, Deokule SS. 2008. Comparison of phenolic compounds of some edible plants of Iran and India. Pakistan Journal of Nutrition 7 (4) : 582-585. Ahmadi F, Kadivar M, Shahedi M. 2007. Antioxidant activity of Kelussia odoratissima Mozaff in model and food systems. Food Chemistry 105 : 57–64. Amic D, Davidovic-Amic D, Beslo D, Trinajsti N. 2003. Structure-radical scavenging activity relationships of flavonoids. Croatica Chemica Acta 76(1) : 55-61.
Andarwulan N et al. 2010. Short communication flavonoid content and antioxidant activity of vegetables from Indonesia. Food Chemistry 121 : 1231– 1235.
Arabshahi-Delouee S, Urooj A. 2007. Antioxidant properties of various solvent extracts of mulberry (Morus indica L.) Leaves. Food Chemistry 102 : 1233–1240. Ardiansyah, Nuraida L, Andarwulan N. 2003. Aktivitas antimikroba daun beluntas (Pluchea indica Less) dan stabilitas aktivitasnya pada berbagai konsentrasi garam dan tingkat pH. Jurnal Teknologi dan Industri Pangan 14(2) : 90-97.
Baéza E. 2006. Effects of Genotype, Age and Nutrition on Intramuscular Lipids and Meat Quality. In: Symposium COA/INRA Scientific Cooperation in Agriculture, Tainan, 7-10 November 2006. Taiwan : ROC.
Bailey ME, Rourke TJ, Gutheil RA, Wang CYJ. 1992. Undesirable flavour of meat. Di dalam: Off flavour in Food and Beverages, editor. New York : G.Charalambous-Elsevier.
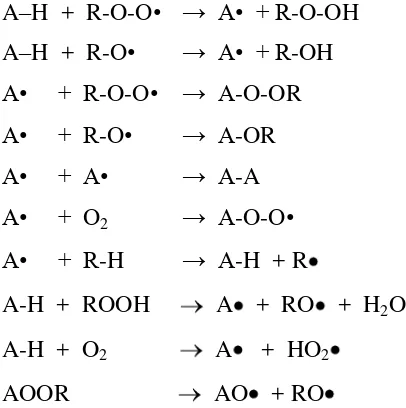

![Gambar 25. Struktur molekul tanin terhidrolisis (a, b, e) dan tanin terkondensasi (c, d, f), a = asam gallat, b = asam ellagat, c = epikatekin, d = katekin, e = -1,2,3,4,6-pentagaloil-O-D-glikosa, f = epikatekin-[(4->8)-epikatekin]15-(4->8)-katekin](https://thumb-ap.123doks.com/thumbv2/123dok/779821.372029/88.595.98.470.157.645/gambar-struktur-terhidrolisis-terkondensasi-epikatekin-pentagaloil-epikatekin-epikatekin.webp)