KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA DAN ISOLASI SENYAWA FLAVONOIDA DARI DAUN TANAMAN EKOR NAGA
(Rhaphidophora pinnata Schott.)
SKRIPSI
Oleh: NURHANIFAH
071524046
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA DAN ISOLASI SENYAWA FLAVONOIDA DARI DAUN TANAMAN EKOR NAGA
(Rhaphidophora pinnata Schott.)
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh: NURHANIFAH
071524046
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
Pengesahan Skripsi
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA DAN ISOLASI SENYAWA FLAVONOIDA DARI DAUN TANAMAN EKOR NAGA
(Rhaphidophora pinnata Schott.) Oleh:
NURHANIFAH NIM 071524046
KATA PENGANTAR
Puji dan Syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan hidayah-Nya, sehingga penulis dapat menyelesaikan penelitian dan penulisan skripsi ini untuk memenuhi syarat guna mencapai gelar sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini dengan segala kerendahan hati, penulis mengucapkan terima kasih yang tiada hentinya kepada Ayahanda Holil Nasution dan Ibunda Misni serta Kakanda Muri Alamsyah dan Yusri alamsyah yang telah memberikan kasih sayang, doa serta dorongan kepada penulis selama ini.
Penulis menyadari bahwa skripsi ini tidak akan terwujud tanpa adanya bantuan dari berbagai pihak, untuk itu penulis mengucapkan terimakasih yang tulus kepada :
1. Ibu Dra. Misra Gaffar M.S., Apt., dan Ibu Dra. Aswita Hafni Lubis MSi, Apt., selaku dosen pembimbing yang telah membimbing penulis dengan penuh kesabaran dan keikhlasan selama penelitian hingga selesainya penulisan skripsi ini
2. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara yang telah mensahkan dan memberikan pengarahan dalam penyusunan skripsi ini
penguji yang telah memberikan masukan dan saran kepada penulis hingga selesainya penulisan skripsi ini
5. Ibu Kepala Laboratorium Fitokimia Farmasi atas segala fasilitas yang diberikan hingga penelitian ini dapat terselesaikan
6. Bapak/Ibu dosen Fakultas Farmasi USU yang telah memberikan didikan dan bimbingan selama penulis menuntut ilmu di Fakultas Farmasi USU 7. Teman – teman farmasi ekstensi stambuk 07 evi, irus, delly, iza, rena,
puji, reni, rani, ike, lely, k’yayuk, nanda, silmi dan masih banyak lagi yang tidak bisa disebutkan satu persatu.
8. Teman-teman seperti mamak, k’muteh, siti, kak aing, bang ubit, kak wanda, andre, rani hrp yang banyak membantu
9. Serta semua pihak yang langsung maupun tidak langsung telah banyak membantu dalam penyelesaian skripsi ini
Semoga Allah SWT memberikan balasan yang berlipat ganda atas segala kebaikan yang telah diberikan. Akhirnya penulis berharap semoga skripsi ini bermanfaat bagi kita semua. Amin
Medan, Januari 2010 Penulis
(Nurhanifah)
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA DAN ISOLASI SENYAWA FLAVONOIDA DARI DAUN TANAMAN EKOR NAGA
(Rhaphidophora pinnata Schott.) ABSTRAK
Flavonoida merupakan salah satu golongan fenol alam terbesar, dan terdapat dalam semua tumbuhan hijau. Ekor naga (Rhaphidophora pinnata Schott.) adalah salah satu tanaman yang banyak mengandung flavonoida banyak digunakan dalam pengobatan tradisional sebagai antikoagulan, antioksidan, anti hipertensi, antivirus, anti inflamasi dan anti sariawan. Untuk mengetahui karakterisasi simplisia, mengetahui golongan senyawa kimia, dan isolasi senyawa flavonoida dengan cara spektrofotometri ultraviolet dengan menggunakan pereaksi geser (Shift reagent) merupakan tujuan penelitian.
Hasil karakterisasi simplisia diperoleh kadar air 7,30%, kadar sari yang larut dalam air 11,70%, kadar sari yang larut dalam etanol 10,99%, kadar abu total 5,32% dan kadar abu yang tidak larut dalam asam 0,43%.
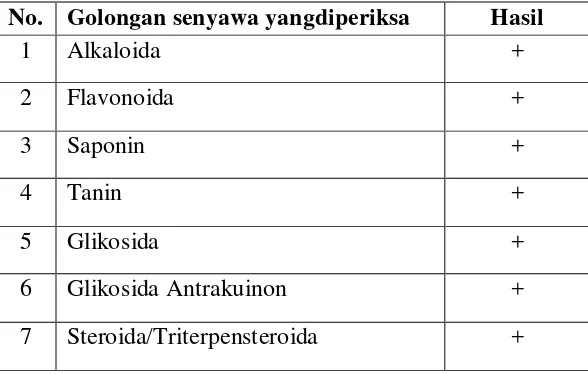
Hasil skrining fitokimia menunjukkan adanya senyawa golongan alkaloida, flavonoida, saponin, tanin, glikosida dan steroida/triterpenoida.
Ekstraksi dilakukan dengan cara sokletasi menggunakan pelarut etanol, ekstrak etanol kemudian difraksinasi berturut-turut menggunakan n-heksana, kloroform, dan etil asetat. Fraksi etil asetat kemudian dikromatografi kertas menggunakan berbagai fase gerak dan perbandingan untuk mencari pengembang yang terbaik. Selanjutnya fraksi etil asetat dipisahkan dengan kromatografi kertas preparatif menggunakan fase gerak asam asetat 50%, hasil kromatografi kertas diperoleh 3 isolat yaitu F1, F2, dan F3, selanjutnya isolat ini dikromatografi dua arah, dari hasil kromatogram diketahui bahwa isolat F1 dan F2 sudah murni, sedangkan isolat F3 belum murni.
Hasil penafsiran ultraviolet dengan pereaksi geser (shift reagent)dari F1 diperoleh absorpsi maksimum dengan panjang gelombang 354 nm yang menunjukkan senyawa flavonol dengan gugus 5 hidroksi dan F2 diperoleh absorbsi maksimum dengan panjang gelombang 330 nm menunjukkan adanya senyawa flavonol dengan gugus 5 hidroksi.
CHARACTERISTICS, PHYTOCHEMICAL SCREENING AND ISOLATION FLAVONOIDA COMPOUND OF “EKOR NAGA” (Rhaphidophora pinnata
Schott.)
ABSTRACT
Flavonoida is one of faction of biggest natural fenol, and there are in all greenery. Ekor naga (Rhaphidophora Pinnata Schott.) is one of plant which containing many flavonoida that used for many traditional medication as anticoagulan, antioxidan, anti hypertension, antivirus, anti inflammation and anti sprue. To knowing simplex characteristic, knowing chemical compound faction, and compound insulation of flavonoida by ultraviolet spektrofotometri by using Reagent shift is representing the target of research.
The result of Rhapidophora leaf simplicia characteristics obtained water value 7,30%, the water soluble extract value 11,70%, the etanol soluble extract value 10,99%, the total ash value 5,32%, the acid insoluble ash value 0,43%.
The result of phytochemical screening is flavonoida, alcaloida, saponin, tannin, glycocida, antraquinon glycocida, and steroid/triterpen steroida,
The extraction with soxhletation was carried out by using ethanol, ethanol extract fractionated by using mixture n-heksane, chloroform and ethyl acetate. Continous partition with ethyl acetate then were done paper chromatography with various developing solvent. Isolates were done identified by ultraviolet spctrophotometry in the presence of shift reagent. The result of preparative paper chromatography produced three spots those are F1, F2 and F3. The F1 and F2 were then identificated by ultraviolet spectrophotometric. And then the spot have two direction chromatography, and gave the result spot F1 and F2 have been pure, but spot F3 not pure.
The interpretation of ultraviolet spectrophotometric result from F1 with maximum absorbption at 354 nm, wavelength indicated the presence of flavonol with 5 hydroxyl group. F2 with maximum absorption at 330 nm and wavelength indicated the presence of flavonol too with 5 hydroxyl group.
DAFTAR ISI
Halaman
JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... v
ABSTRAK ...vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR LAMPIRAN ... x
DAFTAR BAGAN ... xi
DAFTAR GAMBAR ... xii
DAFTAR TABEL ... xiii
DAFTAR KROMATOGRAM ... xiv
DAFTAR SPEKTRUM ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesa ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
2.4.10 Flavanonol ... 15
BAB III METODOLOGI PENELITIAN ... 22
3.3.11 Pereaksi Kloralhidrat jenuh ... 25
3.5.1 Pemeriksaan Makroskopik ... 27
3.5.2 Pemeriksaan Mikroskopik ... 27
3.5.3 Penetapan Kadar Air ... 28
3.5.4 Penetapan Kadar Sari yang larut dalam air ... 29
3.5.5 Penetapan Kadar Sari yang Larut dalam etanol ... .29
3.5.6 Penetapan Kadar Abu total ... 30
3.5.7 Penetapan Kadar Abu yang tidak larut dalam asam ... 30
3.6 Skiring Fitokimia ... 30
3.6.1 Pemeriksaan Alkaloida ... 30
3.6.2 Pemeriksaan Steroida/triterpenoida ... 31
3.6.3 Pemeriksaan Tanin ... 31
3.6.4 Pemeriksaan Saponin ... 32
3.6.5 Pemeriksaan Flavonoida ... 32
3.6.6 Pemeriksaan Glikosida... 32
3.7 Pembuatan Ekstrak ... 33
3.8 Ekstraksi Cair-Cair Senyawa Flavonoida dari Ekstrak Etanol ... 34
3.9 Analisis Senyawa Flavonoida dari Ekstrak Hasil Fraksinasi dengan Cara Kromatografi kertas ... 34
3.10 Pemisahan Senyawa Flavonoida dari Fraksi Etil asetat dengan Cara Kromatografi Kertas Preparatif ... 35
3.11 Uji Kualitatif terhadap senyawa Flavonoida Hasil Kromatografi Kertas Preparatif ... 36
3.12 Uji Kemurnian Senyawa Flavonoida dari Hasil Kromatografi Kertas Preparatif ... 36
3.13 Karakterisasi Senyawa Hasil Isolasi ... 37
BAB IV HASIL PENELITIAN DAN PEMBAHASAN………...38
BAB V KESIMPULAN DAN SARAN... 45
4.1 Kesimpulan ... 45
4.2 Saran ... 45
DAFTAR PUSTAKA ... 46
DAFTAR LAMPIRAN
Lampiran Halaman
1. Determinasi Tanaman ... 47
2. Gambar... 48
3. Bagan ... 55
4. Tabel ... 59
5. Kromatogram ... 65
DAFTAR BAGAN
DAFTAR GAMBAR
Gambar Halaman
1. Tanaman ekor naga (Rhaphidophora pinnata Schott.) ... 48
2. Daun tanaman ekor naga Rhaphidophorae pinnatae Folium ... 48
3. Simplisia daun tanaman ekor naga Rhaphidophorae pinnatae Folium ... 49
4. Alat Soklet ... 50
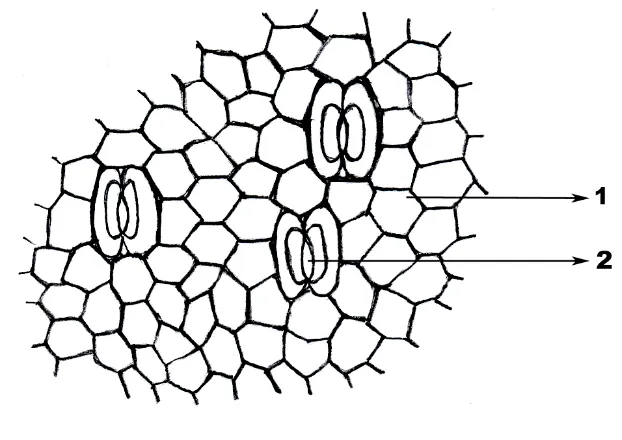
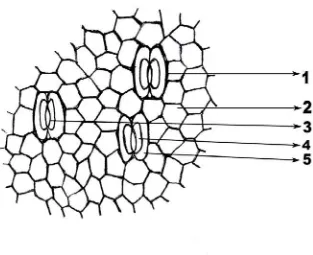
5. Pemeriksaan mikroskopik sayatan melintang daun tanaman ekor naga Rhaphidophorae pinnatae Folium ... 51
6. Pemeriksaan mikroskopik sayatan membujur atas daun tanaman ekor naga Rhaphidophorae pinnatae Folium ... 52
7. Pemeriksaan mikroskopik sayatan membujur bawah daun tanaman ekor naga Rhaphidophorae pinnatae Folium ... 53
DAFTAR TABEL
Tabel Halaman
1. Hasil pemeriksaan karakterisasi simplisia daun tanaman ekor naga Rhaphidophorae pinnatae Folium ... 59
DAFTAR KROMATOGRAM
Kromatogram Halaman
1. Kromatogram Hasil Fraksinasi dengan Kromatografi Kertas dengan
menggunakan Fase Gerak BAA ... 65
2. Kromatogram Hasil Fraksinasi dengan Kromatografi Kertas menggunakan Fase Gerak Forestal ... 66
3. Kromatogram Hasil Fraksinasi dengan Kromatografi Kertas menggunakan Fase Gerak Asam asetat 50% ... 67
4. Kromatogram Ekstrak Etanol dengan Kromatografi Kertas ... 68
5. Kromatogram Fraksi n-heksana dengan Kromatografi Kertas ... 69
6. Kromatogram Fraksi Kloroform dengan Kromatografi Kertas ... 70
7. Kromatogram Fraksi Etil asetat dengan Kromatografi Kertas ... 71
8. Kromatogram Fraksi Air dengan Kromatografi Kertas ... 72
9. Kromatogram Fraksi Etil asetat dengan Kromatorafi Kertas Preparatif ... 73
10.Kromatogram Pita F1 dengan Kromatografi Kertas menggunakan Pengembang Asam Asetat 50% ... 74
11. Kromatogram Pita F1 dengan Kromatografi Kertas menggunakan Fase Gerak BAA ... 75
12. Kromatogram Pita F1 dengan Kromatografi Kertas menggunakan Fase Gerak Forestal ... 76
Fase Gerak BAA ... 78 15. Kromatogram Pita F2 dengan Kromatografi Kertas menggunakan
Fase Gerak Asam Asetat 50% ... 79 16. Kromatogram Pita F3 dengan Kromatografi Kertas menggunakan
Fase Gerak Asam Asetat 50% ... 80 17. Kromatogram Pita F3 dengan Kromatografi Kertas menggunakan
Fase Gerak BAA ... 81 18. Kromatogram Pita F3 dengan Kromatografi Kertas menggunakan
Fase Gerak BAA ... 82 19. Kromatogram Hasil Uji Kemurnian Isolat dengan Kromatografi Kertas Dua Arah ... 83 20. Kromatogram Hasil Uji Kemurnian Isolat F2 dengan Kromatografi
DAFTAR SPEKTRUM
Halaman 1. Spektrum Isolat F1 dalam Metanol ... 85 2. Spektrum Isolat F1 dalam Metanol dengan Penambahan NaOH
dibandingkan dengan spektrum isolat dalam metanol ... 86 3. Spektrum Isolat F1 dalam Metanol dengan Penambahan NaOH
setalah 5 menit dibandingkan dengan spektrum isolat F1 dalam
metanol dengan penambahan NaOH ... 87 4. Spektrum Isolat F1 dalam Metanol dan setelah Penambahan
AICl3/HCl dibandingkan dengan isolat dalam metanol ... 88
5. Spektrum Isolat F1 dalam Metanol dengan Penambahan AICl3/HCl dibandingkan
dengan spektrum isolat F1 dalam dengan
penambahan AlCl3 ... 89
6. Spektrum Isolat F1 dalam Metanol dan setelah penambahan
natrium asetat ... 90 7. Spektrum isolat F1 dalam metanol dengan penambahan natrium
asetat dibandingkan dengan spektrum isolat F1 dalam metanol ... 91 8. Spektrum isolat F2 dalam metanol ... 92 9. Spektrum Isolat F2 dalam metanol dengan penambahan NaOH
dibandingkan dengan spektrum isolat F2 dalam metanol ... 93 10. Spektrum Isolat F2 dalam metanol dengan penambahan NaOH
11. Spektrum Isolat F1 dalam Metanol dan setelah Penambahan
AICl3/HCl dibandingkan dengan isolat dalam metanol ... 95
11. Spektrum Isolat F1 dalam Metanol dengan Penambahan AICl3/HCl dibandingkan
dengan spektrum isolat F1 dalam dengan
penambahan AlCl3 ... 96
12. Spektrum Isolat F1 dalam Metanol dan setelah penambahan
natrium asetat ... 97 13. Spektrum isolat F1 dalam metanol dengan penambahan natrium
KARAKTERISASI SIMPLISIA, SKRINING FITOKIMIA DAN ISOLASI SENYAWA FLAVONOIDA DARI DAUN TANAMAN EKOR NAGA
(Rhaphidophora pinnata Schott.) ABSTRAK
Flavonoida merupakan salah satu golongan fenol alam terbesar, dan terdapat dalam semua tumbuhan hijau. Ekor naga (Rhaphidophora pinnata Schott.) adalah salah satu tanaman yang banyak mengandung flavonoida banyak digunakan dalam pengobatan tradisional sebagai antikoagulan, antioksidan, anti hipertensi, antivirus, anti inflamasi dan anti sariawan. Untuk mengetahui karakterisasi simplisia, mengetahui golongan senyawa kimia, dan isolasi senyawa flavonoida dengan cara spektrofotometri ultraviolet dengan menggunakan pereaksi geser (Shift reagent) merupakan tujuan penelitian.
Hasil karakterisasi simplisia diperoleh kadar air 7,30%, kadar sari yang larut dalam air 11,70%, kadar sari yang larut dalam etanol 10,99%, kadar abu total 5,32% dan kadar abu yang tidak larut dalam asam 0,43%.
Hasil skrining fitokimia menunjukkan adanya senyawa golongan alkaloida, flavonoida, saponin, tanin, glikosida dan steroida/triterpenoida.
Ekstraksi dilakukan dengan cara sokletasi menggunakan pelarut etanol, ekstrak etanol kemudian difraksinasi berturut-turut menggunakan n-heksana, kloroform, dan etil asetat. Fraksi etil asetat kemudian dikromatografi kertas menggunakan berbagai fase gerak dan perbandingan untuk mencari pengembang yang terbaik. Selanjutnya fraksi etil asetat dipisahkan dengan kromatografi kertas preparatif menggunakan fase gerak asam asetat 50%, hasil kromatografi kertas diperoleh 3 isolat yaitu F1, F2, dan F3, selanjutnya isolat ini dikromatografi dua arah, dari hasil kromatogram diketahui bahwa isolat F1 dan F2 sudah murni, sedangkan isolat F3 belum murni.
Hasil penafsiran ultraviolet dengan pereaksi geser (shift reagent)dari F1 diperoleh absorpsi maksimum dengan panjang gelombang 354 nm yang menunjukkan senyawa flavonol dengan gugus 5 hidroksi dan F2 diperoleh absorbsi maksimum dengan panjang gelombang 330 nm menunjukkan adanya senyawa flavonol dengan gugus 5 hidroksi.
CHARACTERISTICS, PHYTOCHEMICAL SCREENING AND ISOLATION FLAVONOIDA COMPOUND OF “EKOR NAGA” (Rhaphidophora pinnata
Schott.)
ABSTRACT
Flavonoida is one of faction of biggest natural fenol, and there are in all greenery. Ekor naga (Rhaphidophora Pinnata Schott.) is one of plant which containing many flavonoida that used for many traditional medication as anticoagulan, antioxidan, anti hypertension, antivirus, anti inflammation and anti sprue. To knowing simplex characteristic, knowing chemical compound faction, and compound insulation of flavonoida by ultraviolet spektrofotometri by using Reagent shift is representing the target of research.
The result of Rhapidophora leaf simplicia characteristics obtained water value 7,30%, the water soluble extract value 11,70%, the etanol soluble extract value 10,99%, the total ash value 5,32%, the acid insoluble ash value 0,43%.
The result of phytochemical screening is flavonoida, alcaloida, saponin, tannin, glycocida, antraquinon glycocida, and steroid/triterpen steroida,
The extraction with soxhletation was carried out by using ethanol, ethanol extract fractionated by using mixture n-heksane, chloroform and ethyl acetate. Continous partition with ethyl acetate then were done paper chromatography with various developing solvent. Isolates were done identified by ultraviolet spctrophotometry in the presence of shift reagent. The result of preparative paper chromatography produced three spots those are F1, F2 and F3. The F1 and F2 were then identificated by ultraviolet spectrophotometric. And then the spot have two direction chromatography, and gave the result spot F1 and F2 have been pure, but spot F3 not pure.
The interpretation of ultraviolet spectrophotometric result from F1 with maximum absorbption at 354 nm, wavelength indicated the presence of flavonol with 5 hydroxyl group. F2 with maximum absorption at 330 nm and wavelength indicated the presence of flavonol too with 5 hydroxyl group.
BAB I PENDAHULUAN 1.1. Latar belakang
Indonesia sangat kaya akan jenis tumbuhan yang dapat dimanfaatkan untuk tujuan peningkatan kesehatan, pencegahan penyakit maupun pengobatan berbagai penyakit. Tumbuhan mengandung berbagai jenis senyawa kimia, mulai dari struktur dan sifat sederhana sampai yang sangat rumit dan unik. Beragam jenis dari senyawa kimia yang terkandung dalam tumbuhan berkhasiat obat penelitiannya telah lama dilakukan, baik untuk memperoleh senyawa baru maupun keaneka ragaman senyawa yang telah ada (Endjo, D & Hernani, 2004).
Berdasarkan pengalaman turun-temurun, penggunaan tanaman herbal dianggap cukup manjur untuk mengobati berbagai macam penyakit. Rendahnya pengetahuan tentang kandungan senyawa obat sehingga menimbulkan keraguan bagi yang belum membuktikannya. Saat ini masih banyak misteri dibalik kandungan dan manfaat tanaman obat yang belum terungkap, pada akhirnya tanaman obat herbal tersebut harus dipertanggung jawabkan secara medis dan ilmiah (Mangan, 2003).
Salah satu tanaman obat yang digunakan secara tradisional oleh masyarakat Indonesia adalah ”tanaman ekor naga” (Rhaphidophora pinnata Schott.). Tanaman ini merupakan tumbuhan merambat, batang bulat, mempunyai akar pelekat dan akar gantung, serta mempunyai banyak kegunaan (Heyne, 1987).
mendorong munculnya paradigma baru dalam dunia kedokteran modern, yaitu back to nature. Contohnya daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) suku araceae yang mengandung senyawa flavonoida, saponin, glikosida, steroida/triterpenoida. (Mangan, 2003; Anonim, 2008).
Flavonoida merupakan salah satu golongan fenol alam terbesar. Flavonoida terdapat pada semua tumbuhan hijau dan banyak digunakan dalam pengobatan tradisional sebagai antikoagulan, antioksidan, anti hipertensi, antivirus, anti inflamasi, anti sariawan (Farnsworth, 1966; Robinson, 1995).
Untuk memisahkan senyawa flavonoida dari daun tumbuhan ekor naga (Rhaphidophorae pinnatae Folium) digunakan kromatografi kertas (KKt), KKt merupakan cara kromatografi yang paling umum dan berguna, yang dilakukan oleh kimiawan pada saat ini (Markham, 1988).
1.2.Perumusan Masalah
Berdasarkan latar belakang di atas dapat diambil perumusan masalah yaitu: 1. Apakah karakterisasi simplisia daun tanaman ekor naga (Rhaphidophorae
pinnatae Folium) yang diteliti dapat digunakan sebagai bahan pembanding. 2. Apakah kandungan metabolit sekunder lain selain flavonoida dapat ditelaah
dari daun tanaman ekor naga (Rhaphidophorae pinnatae Folium)
3. Apakah jenis senyawa flavonoida dapat diisolasi dari ekstrak etanol daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) dan diidentifikasi secara spektrofotometri Ultraviolet menggunakan pereaksi geser (shift reagent).
1.3.Hipotesis
Berdasarkan perumusan masalah diatas maka dibuat hipotesis yaitu:
1. Diduga daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) memenuhi persyaratan karakterisasi simplisia yang dapat digunakan sebagai bahan pembanding.
2. Diduga daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) mengandung senyawa metabolit sekunder lain selain flavonoida, seperti steroida/triterpenoida, glikosida, glikosida antrakinon, tanin, alkaloida, minyak atsiri dan lain-lain.
1.4.Tujuan Penelitian
Adapun tujuan penelitian ini adalah :
1. Untuk mengetahui karakterisasi simplisia daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) yang dapat digunakan sebagai bahan pembanding.
2. Untuk mengetahui golongan metabolit sekunder daun tanaman ekor naga (Rhaphidophorae pinnatae Folium)
3. Untuk mengetahui cara mengisolasi senyawa flavonoida daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) kemudian diidentifikasi secara spektrofotometri ultraviolet dengan menggunakan pereaksi geser (Shift reagent).
1.5.Manfaat Penelitian
Manfaat dalam penelitian ini adalah:
1. Merupakan bahan informasi tentang karakterisasi simplisia daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) yang dapat digunakan sebagai bahan pembanding.
2. Mengetahui golongan metabolit sekunder daun tanaman ekor naga (Rhaphidophorae pinnatae Folium)
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tanaman ekor naga
Tanaman ekor naga sejenis tanaman merambat yang besar, memanjat, tingginya mencapai 5-15 m, daun berbentuk bulat memanjang, daun berbagi-bagi, mempunyai toreh, dalamnya melebihi setengah panjang tulang daun yang berjumlah 7-12, ujung daunnya meruncing, dengan batang yang bulat, dan mempunyai akar pelekat dan akar gantung yang panjang bergantungan seperti ular yang meliliti pohon. Tanaman ini berasal dari Himalaya sampai Australia dan Pasifik (Burkill, 1935, Heyne, 1987).
2.1.1 Sinonim (Lemmens and Bunyapraphatsa, 2003)
Epipremnun pinnatum (L.) Engl, Scindapsus pinnatus (L.) schott,
Rhaphidophora merillii Engl.
2.1.2 Nama Daerah (Heyne, 1987)
Indonesia : Tapanawa tairis (Mal.) Sunda : Lolo munding, Lolo tali Jawa : Jalu mampang, Sulang Bali : Samblung
2.1.3 Sistematika Tanaman Ekor Naga (Arthur, 1981) Divisi : Spermatophyta
Kelas : Monocotyledoneae Bangsa : Arales
Famili : Araceae
Genus : Rhaphidophora
Spesies : Rhaphidophora pinnata Schott.
2.1.4 Kegunaan Tanaman Ekor Naga
Kulit akar gantung dikunyah dengan pinang dan kapur, berguna untuk menguatkan akar gigi dan dapat menghitamkan gigi sebagai efek sampingnya. Batang digiling dapat menyembuhkan anggota badan yang salah urat (terkilir). Di Singapura, daunnya digunakan sebagai teh herbal untuk mengobati reumatik dan kanker. Di Pilipina, getah dari batang tanaman digunakan untuk mengobati gigitan ular beracun. Di Vietnam, tanaman ini berguna untuk mengobati batuk, paralisis dan konjungtivitis (Heyne, 1987; Lemmens and Bunyapraphatsara, 2003).
2.2 Uraian Kimia 2.2.1 Alkaloida
Pereaksi yang umum untuk uji alkaloida adalah pereaksi Bouchardat (Iodium dalam kalium iodida), pereaksi Mayer (Kalium Merkuri Iodida), dan Dragendorff (Kalium Bismuth Iodida).
Kebanyakan alkaloida berupa zat padat yang berbentuk kristal. Alkaloida biasanya tidak berwarna dan mempunyai rasa pahit, sangat sukar larut dalam air, tetapi garamnya yang terbentuk dengan asam selalu mudah larut dalam air, Alkaloida bebas mudah larut dalam eter, kloroform dan pelarut lainnya yang bersifat non polar (Tyler et al, 1988).
2.2.2 Glikosida
Glikosida merupakan senyawa yang mengandung komponen gula dan bukan gula. Komponen gula dikenal dengan nama glikon dan komponen bukan gula dikenal sebagai aglikon. Dari segi biologi, glikosida memiliki peranan penting di dalam kehidupan tumbuhan dan terlibat di dalam pertumbuhan dan perlindungan tumbuhan tersebut. Beberapa glikosida mengandung lebih dari satu jenis gula dalam bentuk disakarida atau trisakarida.
Pengelompokan glikosida berdasarkan ikatan antara glikon dan aglikon dapat dibagi menjadi empat, yaitu:
1. O-glikosida, jika glikon dan aglikonnya dihubungkan oleh atom O, contohnya : salisin.
2. S-glikosida, jika glikon dan aglikonnya dihubungkan oleh atom S, contohnya : sinigrin.
3. N-glikosida, jika glikon dan aglikonnya dihubungkan oleh atom N, contohnya kronotosida.
4. C-glikosida, jika glikon dan aglikonnya dihubungkan oleh atom C, contohnya : barbaloin (Farnsworth, 1966).
2.2.3 Glikosida Antrakinon
Glikosida antrakinon adalah glikosida yang bila dihidrolisa akan menghasilkan aglikon, di-, tri-, atau tetra-hidroksi antrakinon. Glikosida antrakinon umumnya digunakan sebagai pencahar dan bekerja dengan meningkatkan gerakan otot polos pada dinding usus besar saluran pencernaan (Tyler et al, 1988).
2.2.4 Saponin
2.2.5 Flavonoida
Flavonoida merupakan senyawa polifenol yang mempunyai struktur dasar C6
-C3-C6. Golongan terbesar flavonoida mempunyai cincin piral yang menghubungkan
rantai karbonnya (Robinson, 1995).
Senyawa flavonoida selalu terdapat pada tumbuhan dalam bentuk glikosida dimana satu atau lebih gugus hidroksi fenol berikatan dengan gula. Gugus hidroksil selalu terdapat pada atom C 5 dan 7 pada cincin A dan juga pada atom C3’, 4’ dan 5’ pada cincin B (Ikan, 1969).
Flavonoida berupa senyawa yang larut dalam air dan tetap ada dalam lapisan air setelah ekstrak ini dikocok dengan eter minyak bumi. Flavonoida berupa senyawa fenol, karena itu warnanya berubah bila ditambahkan basa atau amonia. Flavonoida mengandung sistem aromatik yang terkonjugasi dan karena itu menunjukkan pada pita serapan kuat pada daerah spektrum sinar UV dan spektrum sinar tampak. Flavonoida umumnya terdapat dalam tumbuhan, terikat pada gula sebagai glikosida. Flavonoida merupakan senyawa golongan fenol alam bersifat antibakteri (Harborne, 1996).
2.2.6 Tanin
Tanin merupakan senyawa yang memiliki sejumlah gugus hidroksi fenolik yang banyak terdapat pada tumbuh-tumbuhan. Terdapat pada bagian tertentu dari tumbuhan, seperti daun, buah dan batang. Tanin terbagi dalam dua golongan, yaitu:
1. Berasal dari turunan pyrogallol
2. Berasal dari turunan pyrocatechol
Adanya 2 gugus hidroksil pada inti aromatis.
Pyrogallol dan catechol merupakan hasil peruraian glikosida tanin yangdapat digunakan sebagai anti bakteri dan anti fungi dengan adanya gugus –OH. Tanin merupakan senyawa yang tidak dapat dikristalkan, dan membentuk senyawa tidak larut yang berwarna biru gelap atau hitam kehijauan dengan garam besi (Tyler et al, 1988).
2.2.7 Triterpenoida/Steroida
Triterpenoida adalah senyawa yang kerangka karbonnya berasal dari enam satuan isoprena dan secara biosintesis diturunkan dari hidrokarbon C30 asiklik, yaitu
skualena. Triterpenoida banyak terdapat pada tumbuhan dan hewan, dapat berada dalam bentuk bebas, maupun dalam bentuk glikosida.
2.3 Metode Ekstraksi
Ekstraksi merupakan suatu proses penarikan senyawa kimia dari jaringan tumbuhan ataupun hewan dengan menggunakan penyari tertentu. Terdapat beberapa macam metode ekstraksi, diantaranya adalah maserasi, perkolasi dan sokletasi (Depkes RI, 1979).
A. Cara Dingin 1. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan (kamar).
Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus menerus). Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama dan seterusnya.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna yang umum dilakukan pada temperatur ruangan. Proses terdiri dari tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetasan/penampungan ekstrak), terus-menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali bahan.
B. Cara Panas 1. Refluks
adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi sempurna. 2. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
3. Digesti
Digesti adalah maserasi kinetik (dengan adanya pengadukan kontinu pada temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada temperatur 40-50◦ C.
4. Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas air (bejana infus tercelup dalam penangas air mendidih, temperatur terukur 96-98◦C) selama waktu tertentu (15-20 menit).
5. Dekok
Dekok adalah infus pada waktu yang lebih lama (≥30◦C) dan temperatur sampai titik didih air (Depkes RI, 2000).
Senyawa Flavonoida
2.4.1 Distribusi, Sifat dan Klasifikasi Flavonoida
dua cincin aromatik yang dihubungkan oleh satuan tiga karbon yang dapat atau tidak dapat membentuk cincin ketiga. (Markham, 1988).
Flavonoida sering terdapat sebagai glikosida. Golongan terbesar Flavonoida berciri mempunyai cincin yang menghubungkan rantai tiga karbon dengan salah satu dari cincin benzena. Flavonoida mencakup banyak pigmen dan terdapat pada tumbuhan mulai dari fungus sampai angiospermae. Pada tumbuhan tinggi, flavonoida terdapat baik dalam bagian vegetatif maupun bunga. Sebagai pigmen bunga, flavonoida berperan dalam menarik burung dan serangga penyerbuk bunga. Beberapa flavonoida tidak berwarna tetapi menyerap sinar ultraviolet. Beberapa kemungkinan fungsi flavonoida untuk tumbuhan yang mengandungnya ialah pengatur tumbuh, pengatur fotosintesis, kerja anti mikroba, anti virus dan kerja terhadap serangga (Robinson, 1995).
Flavonoida sering terdapat dalam tumbuhan sebagai campuran dari flavonoida yang berbeda golongan dan jarang sekali dijumpai hanya flavonoida tunggal dalam jaringan tumbuhan (Harborne, 1987).
Penggolongan senyawa flavonoida menurut Robinson (1995) adalah
antosianin, leukoantosianin, flavonol,flavon, khalkon, auron, flavanon, isoflavon dan flavononol.
2.4.2 Antosianin
pada tumbuhan tinggi. Sebagian besar antosianin adalah glikosida dan aglikonnya disebut antosianidin, salah satu contohnya adalah pelargonidin (Harborne, 1987)
2.4.3 Leukoantosianin
Leukoantosianin merupakan sumber dari antosianin. Leukuantosianin adalah jenis flavonoida yang tidak berwarna dan terdapat dalam daun tumbuhan berkayu (Harborne, 1987)
2.4.4 Flavonol
Flavonol tersebar luas dalam tumbuhan, baik dalam bunga, dan daun. Flavonol sering terdapat dalam bentuk aglikon. Ada aglikon flavonol yang umum yaitu kaemferol, kuersetin, dan mirisetin (Harborne, 1987)
2.4.5 Flavon
Flavon berbeda dengan flavonol karena pada flavon tidak terdapat penyulihan 3 hidroksi. Hal ini mempengaruhi serapan ultravioletnya, serta reaksi warnanya. Hanya ada dua flavon yang umum yaitu apigenin dan luteolin. (Harborne, 1987)
2.4.6 Khalkon
2.4.7 Auron
Seperti Khalkon senyawa ini tampak pada karmotogram kertas berupa bercak kuning dengan sinar UV. (Harborne, 1987)
Auron berupa pigmen kuning emas yang terdapat dalam bunga tertentu. Dikenal hanya lima aglikon, tetapi hidroksilasi senyawa ini umumnya serupa dengan pola pada flavonoida lain, begitu pula bentuk yang dijumpai adalah bentuk glikosida. Dalam larutan basa senyawa ini menjadi merah ros (Robinson, 1995).
2.4.8 Flavanon
Flavanon adalah senyawa tidak berwarna dan sering terdapat aglikon. Contoh senyawa flavanon adalah naringenin dan hesperitin. Uji warna yang penting ialah reduksi dengan serbuk Mg dan HCl pekat, diantara flavonoida hanya flavonon yang memberikan warna merah ceri kuat (Harborne, 1987).
2.4.9 Isoflavon
Isoflavon sukar dicirikan karena reaksinya tidak khas dengan pereaksi warna mana pun. Beberpa isoflavon memberikan warna biru muda cemerlang dengan sinar UV bila diuapi amonia (Harborne, 1987).
2.4.10 Flavanonol
Flavanonol merupakan flavonoida yang kurang dikenal, senyawa ini dikenal berkhasiat sebagai antioksidan (Robinson, 1995).
Kromatografi
Prosedur kromatografi merupakan metode pemisahan. Dibandingkan metode pemisahan klasik seperti destilasi, kristalisasi, dan lain-lain, mempunyai keuntungan dalam pelaksanaan yang lebih sederhana, penggunaan waktu yang singkat, mempunyai kepekaan dan kemampuan memisah yang tinggi (Blaschke, 1998).
Istilah kromatografi mula-mula ditemukan oleh Michael Tswett (1908), seorang ahli botani Rusia. Ia memisahkan klorofil dan pigmen-pigmen lain dari ekstrak tanaman dengan cara ini. Meskipun dasar kromatografi adalah suatu proses pemisahan, namun banyak diantar cara ini dapat digunakan untuk analisis kuantitatif. Jenis-jenis kromatografi yang bermanfaat dalam analisis kualitatif dan kuantitatif adalah kromatografi kertas (KKt), kromatografi lapis tipis (KLT), kromatografi kolom, kromatografi gas, kromatografi cair kinerja tinggi. KKt dan KLT umumnya lebih bermanfaat untuk tujuan identifikasi, karena lebih mudah dan sederhana, kromatografi gas memerlukan alat yang lebih rumit tapi sangat berguna untuk identifikasi dan penetapan kadar (Blaschke, 1998).
2.5.1 Kromatografi Kertas
hanya pada lembaran kertas saring yang berlaku sebagai medium pemisahan. Pada KKt, senyawa biasanya dideteksi sebagai bercak berfluoresensi ultraviolet setelah direaksikan dengan penampak bercak (Markham,1988).
Pada kromatografi kertas sebagai fase diam digunakan sehelai kertas dengan susunan serabut tebal yang cocok. Pemisahan dapat dilakukan menggunakan pelarut tunggal dan proses analog dengan kromatografi penyerapan atau menggunakan dua pelarut yang tidak dapat bercampur dengan proses analog dengan kromatografi pembagian, fase gerak merambat perlahan-lahan melalui fase diam yang membungkus serabut kertas (Depkes RI, 1995).
Proses kromatografi disebut pengembangan, pada kromatografi kertas dibedakan 2 jenis pengembangan (Blasche, 1998).
1. Kromatografi kertas menaik
Untuk kromatografi menaik, ujung bawah kertas dicelupkan kedalam bejana berisi fase gerak, sehingga memungkinkan fase gerak merambat naik pada kertas.
2. Kromatografi kertas menurun
Dipakai bejana yang lebih besar dilengkapi dengan wadah pelarut yang dipasang pada penopang, kertas kromatografi dicelupkan kedalam fase gerak yang diberati oleh batang kaca supaya tetap pada tempatnya dan fase gerak dibiarkan merambat turun pada kertas.
bercak ini kecepatannnya cukup, maka kromatografi lewat kembang dapat memisahkannya dengan lebih baik (Markham, 1988).
Gerakan noda suatu senyawa dalam pengembang tertentu disebut bilangan Rf senyawa itu dalam pengembang tersebut. Bilangan Rf didefenisikan sebagai jarak yangditempuh oleh senyawa dibagi dengan jarak yang ditempuh oleh garis depan fase gerak (diukur dari garis awal). Karena itu bilangan Rf selalu lebih kecil dari 1,0. Pembanding bilangan flavonoida yang belum dikenal dengan Rf yang telah dikenal dan sejenis merupakan cara yang berguna untuk membandingkan flavonoida yang sedang diidentifikasi dengan flavonoida yang tidak ada dilaboratorium (Markham, 1988).
Cara yang lebih efektif yang dilaksanakan untuk mengisolasi flavonoida adalah kromatografi kertas preparatif, merupakan cara yang cocok dalam pemisahan komponen. Ekstrak tidak ditotolkan sebagai bercak bundar pada garis awal tetapi berupa pita lebar 1-3 cm. Setelah pengembangan, pita yang terjadi dapat dipotong-potong dan diekstraksi dengan pelarut (Markham, 1988).
2.6 Spektrofotometri UV
dengan satu ikatan rangkap saja idak menyerap didaerah sinar ultraviolet (Hart, 2003).
Spektrofotometer ultraviolet adalah pengukuran panjang gelombang dan intensitas sinar ultraviolet diabsorbsi oleh isolet. Sinar ultraviolet memiliki energi yang cukup untuk mempromosikan elektron pada kulit terluar ketingkat energi yang lebih tinggi. Spektrofotometer ultraviolet pada umumnya digunakan untuk menentukan jenis kromofor, ikatan rangkap yang terkonyugasi, menjelaskan informasi dari struktur berdasarkan panjang gelombang maksimum suatu senyawa (Dachrianus, 2004).
Ketika suatu atom atau molekul menyerap cahaya maka energi tersebut akan menyebabkan tereksitasinya electron pada kulit terluar ke tingkat energi yang lebih tinggi. Tipe eksitasi tergantung pada panjang gelombang cahaya yang terserap. Sinar ultraviolet akan menyebabkan electron tereksitasi ke orbital yang lebih tinggi.
Terjadinya penyerapan sinar pada daerah gelombang cahaya ultraviolet atau cahaya tampak tergantung pada mudahnya promosi electron. Molekul-molekul yang memerlukan lebih banyak energi untuk promosi electron ke tingkat yang lebih tinggi akan menyerap pada panjang gelombang yang lebih pendek. Molekul yang memerlukan energi lebih sedikit akan menyerap pada panjang gelombang yang lebih panjang (Fessenden dan Fessenden, 1982).
1. Kromofor ; merupakan gugus yang tak jenuh yang bertanggung jawab terhadap terjadinya absorbsi elektronik.
2. Auksokrom ; merupakan gugus jenuh dengan adanya electron bebas (tidak terikat), dimana jika gugus ini bergabung dengan kromofor, akan mempengaruhi panjang gelombang dan intensitas absorban.
3. Pergeseran batokromik ; merupakan pergeseran absorban ke daerah panjang gelombang yang lebih panjang karena danya substitusi atau efek pelarut. 4. Pergeseran hipsokromik ; merupakan pergeseran absorban ke daerah panjang
gelombang yang lebih pendek karena adanya substitusi atau efek pelarut 5. Efek hiperkromik ; merupakan peningkatan intensitas absorban.
6. Efek hiperkromik ; merupakan penurunan intensitas absorban.
Spekroskopi serapan ultraviolet adalah cara yang berguna untuk menganalisis struktur flavonoida. Cara tersebut digunakan untuk membantu mengidentifikasi jenis flavonoida dan menentukan pola oksigenasi. Disamping itu kedudukan gugus hidroksil fenol bebas pada inti flavonoida dapat ditentukan dengan penambahan pereaksi geser kedalam larutan cuplikan dan mengamati pergeseran puncak serapan yang terjadi (Markham, 1988).
2.6.1 Spektrum Natrium Metoksida
Natrium metoksida adalah merupakan basa kuat yang dapat mengionisasi hampir semua gugus hidroksil yang terdapat pada inti flavonoida. Spektrum ini biasanya merupakan petunjuk sidik jari pola hiroksilasi. Degradasi atau pengurangan kekuatan spektrum setelah waktu tertentu merupakan petujuk baik akan adanya gugus yang peka tehadap basa. Pereaksi pengganti natrium metoksida adalah larutan natrium hidroksida 2 N dalam air (Markham, 1988).
2.6.2 Spektrum Natrium Asetat
Natrium asetat hanya menyebabkan pengionan yang berarti pada gugus hidroksil flavonoida. Natrium asetat digunakan terutama untuk mendeteksi adanya gugus 7 hidroksil (Markham, 1988).
2.6.3 Spektrum natrium asetat/asam borat
Menjembatani kedua gugus hidroksil pada gugus orto-dihidroksi dan digunakan untuk mendeteksinya (Markham, 1988).
2.6.4 Spektrum AlCl3/HCl
Karena membentuk kompleks antara gugus hidroksil dan keton yang bertetangga dan membentuk kompleks dengan gugus orto-dihidroksil, pereaksi ini dapat digunakan untuk mendeteksi kedua gugus tersebut. Jadi spekrum AlCl3
BAB III
METODOLOGI PENELITIAN
Metode penelitian adalah metode eksperimental yang meliputi identifikasi tumbuhan, pengumpulan bahan tumbuhan, pengolahan sampel, karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak, analisis kromatografi kertas,uji kemurnian dan identifikasi senyawa hasil isolasi secara spektrofotometri ultraviolet menggunakan pereaksi geser (shift reagent).
3.1 Alat-alat yang digunakan
Alat-alat yang digunakan dalam penelitian adalah: alat-alat gelas laboratorium, blender (national), lampu sinar ultraviolet (Nimura), neraca kasar (Ohaus), neraca listrik (Sartorius), penangas air (Yenaco), rotary evaporator (Buchi 461), seperangkat alat kromatografi kertas dan spektrofotometer ultraviolet (Shimadzu UV-1240), mikroskop, kaca objek, kaca penutup.
3.2 Bahan-bahan yang digunakan
naftol, timbal asetat, dragendorff, mayer, bouchardat, kertas Whatman No.1 dan No. 3, kloralhidrat, floroglusinol.
3.3 Pembuatan Larutan pereaksi 3.3.1 Pereaksi Dragendorff
Sebanyak 8,0 g bismut (III) nitrat dilarutkan dalam 20 ml asam nitrat dan dilarutkan 27,2 g, kalium iodida dalam 50 ml air suling. Campur kedua larutan dan diamkan sampai memisah sempurna. Diambil larutan jernih dan diencerkan dalam air secukupnya hingga 100 ml ( Depkes RI, 1980).
3.3.2 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida dilarutkan dalam air suling secukupnya sampai KI larut dengan sempurna, lalu ditambahkan 2 g iodium sedikit demi sedikit dan dicukupkan dengan air suling hingga volume 100 ml ( Depkes RI,1979).
3.3.3 Pereaksi Mayer
3.3.4 Pereaksi Besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling hinnga 100 ml (Depkes RI, 1989).
3.3.5 Pereaksi Asam klorida 6 N
Sebanyak 50 ml asam klorida pekat diencerkan dalam air suling hingga 100 ml (Depkes RI, 1979).
3.3.6 Pereaksi Asam klorida 2N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling hingga 100 ml (Depkes RI, 1979).
3.3.7 Pereaksi Aluminium klorida 5 %
Sebanyak 5 g aluminium klorida ditimbang, kemudian dilarutkan dalam metanol hingga 100 ml (Harborne, 1989).
3.3.8 Pereaksi Natrium Hidroksida 2 N
Sebanyak 8,002 g natrium hidroksida dilarutkan dalam air suling bebas karbondioksida hingga 100 ml (Depkes RI, 1979).
3.3.9 Pereaksi Asam Sulfat 2 N
3.3.10 Pereaksi Molish
Sebanyak 3 g α- naftol dilarutkan dalam asam nitrat 0,5 N hingga diperoleh 100 ml larutan (Depkes RI, 1989).
3.3.11 Pereaksi Timbal (II) Asetat 0,4 M
Sebanyak 15,17 g Timbal (II) Asetat dilarutkan dalam air suling bebas karbondioksida hingga 100 ml (Depkes RI, 1989).
3.3.12 Pereaksi Kloralhidrat jenuh
Sebanyak 50 g kloralhidrat dilarutkan didalam 20 ml air suling (Depkes RI, 1989).
3.3.13 Pereaksi Floroglusinol HCl
1 g floroglusinol ditambah beberapa tetes HCl pekat sampai memerahkan lignin (Depkes RI, 1989).
3.3.14 Air suling bebas karbondioksida
Sebanyak 500 ml sulingan dididihkan selama tidak kurang dari 10 menit, sambil mencegah sesempurna mungkin dengan udara, dinginkan, dimasukkan kedalam wadah bertutup kedap (Depkes RI, 1979).
3.4 Penyiapan Sampel 3.4.1 Pengambilan sampel
tanaman ekor naga (Rhaphidophorae pinnatae Folium) segar yang diperoleh dari Komplek Bea Cukai No. 22 Kecamatan Padang Selatan, Kota Madya Padang, Provinsi Sumatera Barat.
3.4.2 Determinasi Tumbuhan
Determinasi tanaman dilakukan oleh lembaga Ilmu Pengetahuan Indonesia (LIPI) Pusat Penelitian Biologi, Bogor (Frans, 2007). Hasil determinasi dapat dilihat pada lampiran 1 halaman 28.
3.4.3 Pengolahan Sampel
Sebanyak 6 kg daun tanaman ekor naga (Rhaphidophorae pinnatae Folium yang segar dibersihkan dari pengotoran, dicuci bersih, ditiriskan. Selanjutnya dikeringkan dengan cara diangin-anginkan diudara terbuka terhindar dari sinar matahari langsung, setelah kering diserbukkan dengan blender dan serbuk disimpan dalam wadah plastik.
3.5 Pemeriksaan Karakterisasi Simplisia
3.5.1 Pemeriksaan Makroskopik Simplisia
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk,ukuran, warna, rasa dan bau dari simplisia daun tanaman ekor naga (Rhaphidophorae pinnatae Folium).
3.5.2 Pemeriksaan Mikroskopik Simplisia
Sebelum dilakukan pemeriksaan mikroskopik dari serbuk simplisia maka dilakukan pemeriksaan mikroskopik pada tanaman segar.
- Sayatan melintang daun tanaman ekor naga (Rhaphidophorae pinnatae Folium)
Cara kerja: Pada kaca objek ditetesi kloralhidrat, diletakkan sayatan melintang daun tanaman ekor naga, dipanaskan diatas lampu spiritus, tidak sampai kering, dicuci dengan beberapa tetes akuades, kemudian ditetesi beberapa tetes floroglusinol HCl, didiamkan selama 10 menit, ditutup dengan kaca penutup, kemudian diamati dibawah mikroskop.
- Sayatan membujur (atas dan bawah) daun tanaman ekor naga (Rhaphidophorae pinnatae Folium)
Simplisia
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia daun tanaman ekor naga. Serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi larutan kloral hidrat kemudian ditutup dengan kaca penutup, kemudian diamati pada mikroskop. Hasil mikroskopik serbuk simplisia daun tanaman ekor naga dapat dilihat pada lampiran 8 halaman 35.
3.5.3 Penetapan Kadar Air a. Penjenuhan Toluen
Sebanyak 200 ml toluen dan 2 ml air suling dimasukkan kedalam labu alas bulat, dipasang alat penampung dan pendingin, kemudian di destilasi selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,05 ml (WHO, 1992).
b. Penetapan kadar air
volume air dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen (WHO, 1992).
3.5.4 Penetapan kadar sari yang larut dalam air
Sebanyak 5 g serbuk yang telah dikeringkan diudara di maserasi selama 24 jam dalam 100 ml air-kloroform (2,5 ml kloroform dalam air sampai 1 liter) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, kemudian dibiarkan selama 18 jam, lalu disaring. Sebanyak 20 ml filtrat diuapkan sampai kering dalam cawan dangkal berdasar rata yang telah ditara, dan sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari larut dalam air dihitung terhadap bahan yang telah dikeringkan di udara (Depkes RI, 1989).
3.5.5 Penetapan kadar sari yang larut dalam etanol
3.5.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian diratakan. Krus dipijarkan pada suhu 600oC sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah dikeringkan diudara (Depkes RI, 1989; WHO, 1992).
3.5.7 Penetapan kadar abu yang tidak larut dalam asam
Sebanyak 25 ml asam klorida encer dimasukkan abu yang telah diperoleh dalam penetapan kadar abu total, kemudian didihkan selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring bebas abu kemudian dicuci dengan air panas. Residu dan kertas saring dipijarkan pada suhu 600oC sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu tidak larut dalam asam dihitung terhadap bahan yang dikeringkan diudara (WHO, 1992).
3.6 Skrining Fitokimia
Skrining fitokimia dari serbuk simplesia meliputi pemeriksaan senyawa golongan alkaloida, steroida/ triterpenoida, tannin, saponin, flavonoida, glikosida dan glikosida antrakuinon, minyak atsiri.
3.6.1 Pemeriksaan Alkaloida
a. Sebanyak 3 tetes filtrat ditambahkan 2 tetes larutan pereaksi Mayer, maka akan terbentuk endapan menggumpal berwarna putih atau putih kekuningan. b. Sebanyak 3 tetes filtrat ditambahkan 2 tetes larutan pereaksi Bouchardat, akan
terbentuk endapan berwarna coklat sampai hitam.
c. Sebanyak 3 tetes filtrat ditambah dengan 2 tetes larutan pereaksi Dragendroff, akan terbentuk endapan merah atau jingga.
Alkaloida positif jika terjadi endapan atau kekeruhan paling sedikit dua dari tiga percobaan di atas (Depkes RI, 1989).
3.6.2 Pemeriksaaan Steroida/ triterpenoida
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml n-heksan selama 2 jam. Kemudian maserat yang diperoleh disaring, lalu filtrat diuapkan dalam cawan penguap, dan pada sisanya ditambahkan 20 tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat (pereaksi Lieberman-Bourchard). Apabila terbentuk warna biru kehijauan atau merah ungu menunjukkan adanya steroida/triterpenoida bebas (Harborne, 1987).
3.6.3 Pemeriksaan Tanin
3.6.4 Pemeriksaan Saponin Uji Busa
Sebanyak 0,5 g serbuk simplesia dimasukkan kedalam tabung reaksi, lalu ditambahkan 10 ml air panas dan didinginkan, kemudian dikocok kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1 sampai 10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan asam klorida 2 N menunjukkan adanya saponin (Depkes RI, 1989)
3.6.5 Pemeriksaan Flavonoida
Sebanyak 10 g serbuk simplisia ditambahkan 100 ml air panas, didihkan selama 5 menit dan disaring dalam keadaan panas. Kedalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol,dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah, kuning, jingga pada lapisan amil alkohol (Farnsworth, 1996).
3.6.6 Pemeriksaan Glikosida
reaksi, selanjutnya diuapkan diatas penangas air. Pada sisa ditambahkan 2 ml air suling dan 5 tetes pereaksi Molish. Tambahkan hati-hati secara 2 ml asam sulfat pekat melalui dinding tabung terbentuk cincin ungu pada batas kedua cairan, menunjukkan adanya glikosida (Depkes RI, 1989).
3.6.7 Pemeriksaan Glikosida Antrakuinon
Sebanyak 0,2 g serbuk simplisia ditambah dengan 5 ml asam sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzena, dikocok dan didiamkan. Lapisan benzena dipisahkan dan disaring. Kocok lapisan benzena dengan 2 ml NaOH 2 N, didiamkan. Lapisan ini berwarna merah dan lapisan benzena tidak berwarna menunjukkan adanya antrakuinon (Depkes RI, 1989).
3.7 Pembuatan Ekstrak
Pembuatan ekstrak dilakukan secara sokletasi mengunakan pelarut etanol Prosedur pembuatan ekstrak :
Sebanyak 150 g serbuk simplisia dibungkus dengan kertas saring, diletakkan kedalam tabung soklet, kemudian pelarut dimasukkan kedalam labu sebanyak 2/3 bagian dari volume labu, selanjutnya alat dirangkai, dibuka kran air masuk.
seterusnya. Aliran pelarut ini disebut dengan 1 (satu) kali sirkulasi pada alat soklet. Ekstraksi sempurna ditandai bila cairan yang melewati pipa kapiler sifon tidak berwarna. Ekstrak yang diperoleh dikumpulkan dan dipekatkan. Bagan ekstraksi serbuk simplisia dapat dilihat pada lampiran 10 halaman 56.
3.8 Ekstraksi Cair-Cair Senyawa Flavonoida Dari Ekstrak Etanol
Ekstraksi cair-cair senyawa flavonoida dari ekstrak etanol dilakukan berturut-turut dengan pelarut n-heksana, kloroform dan etil asetat. Caranya: ekstrak etanol ditambah 10 ml etanol, kemudian dilarutkan dalam air panas sebanyak 100 ml, dan dimasukkan kedalam corong pisah, mula-mula di fraksinasi dengan pelarut n- heksana sebanyak 100 ml, diperoleh fraksi n-heksana dan fraksi air. Fraksi air kemudian difraksinasi dengan pelarut kloroform 100 ml, diperoleh fraksi kloroform dan fraksi air. Fraksi air kemudian difraksinasi lagi dengan 100 ml etil asetat, diperoleh fraksi etil asetat dan fraksi air. Hasil fraksinasi dipekatkan dengan penguap vakum putar (Markham, 1988). Bagan ekstraksi cair-cair dari ekstrak etanol dapat dilihat pada lampiran 11 halaman 57.
3.9 Analisis Senyawa Flavonoida dari Ekstrak Hasil Fraksinasi dengan Cara Kromatografi Kertas
Ekstrak etanol, fraksi n-heksana, kloroform, etil asetat, dan air. Masing-masing di totolkan pada kertas whatman, kemudian dimasukkan kedalam bejana yang telah dijenuhkan dengan masing-masing fase gerak, dielusi dengan jarak rambat 20 cm, kertas diangkat dan dikeringkan, diamati dibawah lampu ultraviolet. Hasil disemprot dengan AlCl3 5% dan diamati dibawah lampu ultraviolet. Diantara ekstrak
etanol dan semua fraksi, diperoleh bercak yang paling banyak dan terpisah dengan baik adalah fraksi etil asetat. Hasil kromatogram dengan KKt dari ekstrak etanol, fraksi n-heksana, fraksi kloroform, fraksi etil asetat, fraksi air dapat dilihat pada lampiran 19-26 halaman 65-72.
3.10 Pemisahan Senyawa Flavonoida dari Fraksi Etil asetat dengan Cara Kromatografi Kertas Preparatif
Terhadap fraksi etil asetat dilakukan pemisahan secara kromatografi kertas preparatif dengan fase gerak asam asetat 50%, dan fase diam kertas whatman No.3 dengan ukuran 15x20 cm.
Cara kerja:
3.11 Uji Kualitatif terhadap Senyawa Flavonoida Hasil Kromatografi Kertas Preparatif
1. Reaksi warna Cara kerja :
Terhadap senyawa flavonoida hasil isolasi ditambah serbuk Mg dan 1 ml HCL pekat kemudian diamati perubahan warna yang terjadi (Farnsworth, 1966). 2. Kromatografi kertas menggunakan berbagai fase gerak (BAA, asam asetat 50%, dan forestal), sebagai fase diam digunakan kertas whatman No. 1 berukuran 3x25 cm, penampak bercak AlCl3.
Isolat dilarutkan kemudian ditotolkan pada kertas whatman no 1, kemudian dimasukkan kedalam bejana yang telah jenuh dengan fase gerak kemudian dielusi, selanjutnya kertas dikeluarkan dan dikeringkan. Hasilnya dilihat dibawah lampu ultraviolet pada panjang gelombang 366 nm kemudian disemprot dengan penampak bercak AlCl3 5% dan dilihat dibawah sinar ultraviolet. Hasil kromatogram dengan
KKt kualitatif isolat dapat dilihat pada lampiran 28-36 halaman 74-82.
3.12 Uji Kemurnian Senyawa Flavonoida dari Hasil Kromatografi Kertas Preparatif
Cara kerja:
Isolat ditotolkan pada kertas whatman No.1 yang berukuran 15x20 cm, dimasukkan kedalam bejana yang telah jenuh dengan uap fase gerak I lalu dielusi, kertas diangkat dan dikeringkan, selanjutnya dielusi kembali dengan fase gerak II dengan arah yang berbeda, kemudian kertas diangkat dan dikeringkan, bercak diamati dibawah sinar ultraviolet. Hasil kromatogram dengan KKt dua arah dari isolat dapat dilihat pada lampiran 37-38 halaman 82-83.
3.13 Karakterisasi Senyawa Hasil Isolasi
Identifikasi senyawa hasil isolasi dilakukan secara spektrofotometri UV menggunakan pereaksi geser (shift reagent) menurut Markham (1988).
Cara kerja:
1. Isolat dilarutkan dengan metanol dalam kuvet lalu diukur spektrumnya, kemudian ditambahkan tiga tetes natrium hidroksida 2 N, lalu diukur spektrumnya. Pengukuran spektrum diulang kembali setelah lima menit.
2. Pereaksi aluminium klorida enam tetes ditambahkan kedalam larutan isolat, lalu diukur spektrumnya, ditambahkan 3 tetes asam klorida 6 N, lalu diukur spektrumnya.
BAB IV
HASIL DAN PEMBAHASAN
Hasil determinasi tanaman yang dilakukan di Pusat Penelitian dan Pengembangan Biologi Bogor adalah tanaman ekor naga (Rhaphidopora pinnata Schott.) famili Araceae.
Hasil pemeriksaan karakterisasi serbuk simplisia dapat digunakan sebagai bahan pembanding, diperoleh kadar air simplisia 7,3%, menunjukkan bahwa simplisia telah memenuhi persyaratan yaitu tidak lebih dari 10%. Kadar sari yang larut dalam air 11,70%, kadar sari yang larut dalam etanol 10,99%.Kadar abu total yaitu 5,32%, kadar abu yang tidak larut dalam asam 0,43%.
Hasil skrining fitokimia daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) golongan senyawa yang positif adalah flavonoida, alkaloida, tanin, glikosida, glikosida antrakinon dan steroida/triterpenoida.
Ekstraksi dilakukan dengan cara sokletasi menggunakan pelarut etanol, hasil sokletasi 150 g serbuk daun ekor naga diperoleh ekstrak 23,405 g. Dilakukan ekstraksi cair-cair secara berturut-turut menggunakan pelarut n-heksana dan air, dari 3 g ekstrak diperoleh fraksi n-heksana 90 ml, fraksi air di fraksinasi dengan kloroform, dan diperoleh fraksi kloroform 75 ml, selanjutnya fraksi air difraksinasi lagi dengan etil asetat sehingga diperoleh fraksi etil asetat 20,1 ml dan fraksi air 13 ml.
sinar lampu Ultraviolet dan AlCl3 5%. Pada fraksi etil asetat diperoleh pemisahan
yang baik dengan fase gerak asam asetat 50% yang memberikan empat bercak dengan sinar lampu UV 366 nm, kromatogram dibaca dari bawah keatas yaitu warna ungu (Rf = 0,27), biru (Rf= 0,63), kuning (Rf = 0,7), ungu (Rf = 0,74). Menurut Markham (1988) senyawa flavonoida yang memberikan fluoresensi warna ungu dan biru dengan sinar lampu ultraviolet menunjukkan senyawa flavonoida golongan flavon, isoflavon, flavanon dan flavonol.
Terhadap fraksi etil asetat ini kemudian dilakukan pemisahan dengan kromatografi kertas preparatif dengan fase gerak asam asetat 50 % dan fase diam kertas whatman no.3, pita-pita dipisahkan berdasarkan fluoresensinya dibawah sinar lampu UV 366 nm, hasilnya diperoleh 3 pita yaitu isolat F1, berfluoresensi ungu; F2 berfluoresensi biru dan F3 berfluoresensi kuning ungu. Selanjutnya dilakukan uji kualitatif terhadap isolat tersebut. Hasil uji kualitatif terhadap isolat F1 dan F2 dengan penambahan serbuk Mg dan HCl pekat memberikan warna merah, ini menunjukkan senyawa flavonoida tersebut adalah golongan flavonol (Fransworth, 1966). Uji kulitatif juga dilakukan dengan kromatografi kertas dengan fase gerak asam asetat 50%, forestal dan BAA. Penampak noda digunakan sinar lampu UV 366 nm, uap ammonia dan AlCl3 5%, ternyata F1 menunujukkan satu bercak berwarna
memiliki dua warna yang berbeda yaitu warna kuning dan ungu (fase gerak asam asetat 50%, Rf = 0,37; BAA, Rf = 0,81; forestal, Rf = 0,77).
Hasil uji kemurnian isolat F1 dan F2 menggunakan kromatografi kertas dua arah dengan fase gerak I adalah BAA (n-butanol:asam asetat:air = 4:1:5) dan asam asetat 50 % sebagai fase gerak II, hasilnya menunjukkan satu bercak jika dilihat dibawah sinar lampu UV 366 nm dan setelah diberi AlCl3 5 % masih menunjukkan satu bercak yaitu F1 (Rf = 0,78) fluoresensi ungu, F2 (Rf = 0,91) fluoresensi biru muda.
Penafsiran spektrum ultraviolet dilakukan untuk isolat F1 dan F2, dengan merujuk pada Markham (1988).
Penafsiran spektrum ultraviolet untuk isolat F1:
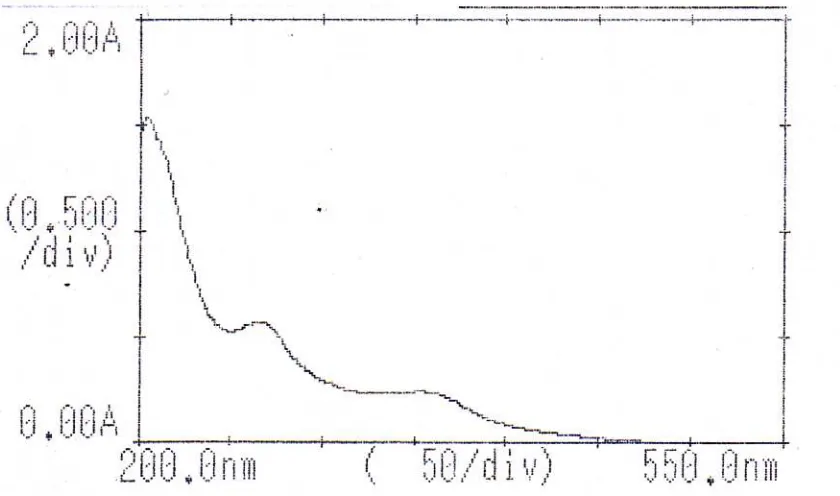
1. Hasil spektrum F1 dalam metanol memberikan pita absorpsi maksimum pada pita I yaitu 354 nm, sedangkan untuk pita II 267 nm. Absorpsi maksimum pada pita I ini sesuai untuk senyawa Flavonol yang panjang gelombang absorpsi maksimum pada pita I adalah 350-385 nm, dengan demikian diduga senyawa flavonoida tersebut adalah flavonol.
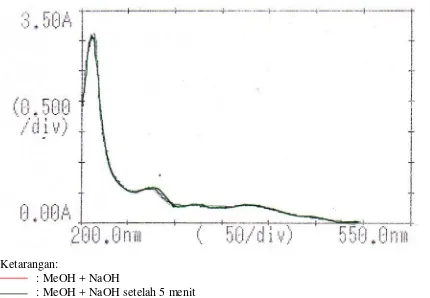
2. Pada spektrum F1 dalam metanol dengan penambahan NaOH dibandingkan dengan spektrum yang telah diukur setelah 5 menit terlihat adanya penguraian yang ditandai intensitas meningkat, dimana pergeseran panjang gelombang pada pita I dari 354 nm menjadi 378 nm jadi diperoleh perubahan panjang gelombang pada pita 24 nm.
terjadi pada pita I sebesar 23 nm. Pergesaran batokromik 20-26 nm menunjukkan gugus 5-OH (dihidroflavonol). Dengan demikian dijumpai gugus 5-OH pada golongan flavonol ini. Pada spektrum isolat dengan penambahan AlCl3 terjadi
pergeseran hiperkromik 1 nm pada pita 1 bila dibandingkan terhadap spektrum dalam metanol dengan penambahan AlCl3/HCl.
4. Hasil spektrum F1 dalam metanol dengan panambahan natrium asetat (NaOAc) menunjukkan adanya pergeseran hipsokromik pada pita II sebesar 1 nm jika dibandingkan dengan spektrum dalam metanol, Jika terjadi pergeseran sebesar 5-20 nm pada pita II, maka terdapat gugus 7-OH pada cincin A, maka pada senyawa flavonol ini tidak dijumpai adanya gugus 7-OH.
5. Pada spektrum F1 dalam metanol dengan penambahan NaOAc/H3BO3 dibandingkan terhadap spektrum dalam metanol menunjukkan pergeseran pada pita I sebesar 11 nm, jika terjadi pergeseran sebesar 12-36 nm pada pita I, maka terdapat gugus orto- dihidroksi pada cincin B, dengan demikian pada senyawa flavonol ini tidak terdapat gugus orto-dihidroksi pada cincin B.
Hasil penafsiran spektrum ultraviolet dengan penambahan pereaksi geser terhadap isolat F2 dapat disimpulkan bahwa senyawa flavonoida ini diduga senyawa flavonol yang mempunyai gugus hidroksi pada posisi 5-OH.
Penafsiran spektrum ultraviolet untuk isolat F2 :
pita I adalah 330-360 nm, dengan demikian senyawa flavonoida tersebut adalah golongan flavonol.
2. Pada spektrum F2 dalam metanol dengan penambahan NaOH menunjukkan adanya pergeseran batokromik pada pita I yaitu 43 nm tanpa penurunan intensitas. Pergesarn batokromik pada pita I ini sesuai untuk senyawa flavonol yaitu sebesar 45-60 nm, tanpa adanya penurunan intensitas, ini menunjukkan bahwa pada F2 tidak dijumpai gugus 4’-OH bebas.
3. Pada spektrum F1 dalam metanol dengan penambahan NaOH dibandingkan dengan spektrum yang telah diukur setelah 5 menit terlihat adanya penguraian yang ditandai intensitas meningkat, dimana pergeseran panjang gelombang pada pita I dari 373 nm menjadi 378 nm jadi diperoleh perubahan panjang gelombang pada pita 5 nm.
4. Pada spektrum F2 dalam metanol dengan penambahan AlCl3/HCl terjadi pergeseran batokromik bila dibandingkan spektrum dalam metanol. Pergeseran batokromik ini terjadi pada pita I sebesar 46 nm. Jika terjadi pergeseran batokromik sekitar 35-55 nm menunjukkan gugus 5-OH pada cincin A, dengan demikian dijumpai adanya gugus 5-OH bebas. Pada spektrum isolat dengan penambahan AlCl3 terjadi pergeseran hiperkromik 1 nm pada pita 1 dibandingkan
terhadap spektrum dalam metanol dengan penambahan AlCl3/HCl3.
maka terdapat gugus 7-OH pada cincin A dengan demikian pada senyawa flavonol ini tidak dijumpai gugus 7-OH.
6. Pada spektrum F2 dalam metanol dengan panambahan NaOAc/H3BO3 bila dibandingkan spektrum isolat dalam metanol menunjukkan pergeseran batokromik pada pita I, senyawa flavonol yang mempunyai gugus orto- dihidroksi pada cincin B biasanya menunjukkan pergeseran batokromik pada pita I dengan NaOAc/H3BO3 dengan demikian pada senyawa flavonol ini dijumpai adanya tidak adanya gugus orto-dihidroksi pada cincin B.
BAB V
KESIMPULAN DAN SARAN A. Kesimpulan
a. Hasil Karakterisasi serbuk simplisia daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) diperoleh kadar air simplisia 7,3%,kadar sari yang larut dalam air 11,70%, kadar sari yang larut dalam etanol 10,99%,kadar abu total 5,32%, kadar abu yang tidak larut dalam asam 0,43%.
b. Hasil skrining fitokimia serbuk simplisia daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) golongan senyawa yang positif adalah flavonoida, alkaloida, tanin, glikosida, glikosida antrakinon dan steroida/triterpenoida.
c. Hasil isolasi diperoleh 3 senyawa yaitu isolat F1 harga Rf = 0,29 berfuluoresensi ungu; F2 harga Rf = 0,56 berfluoresensi biru; F3 harga Rf = 0,37 berfluoresensi kuning ungu dibawah sinar lampu ultraviolet.
d. Hasil karakteristisasi isolat I (Rf = 0,78) dari data spektrofotometri ultraviolet dengan pereaksi geser adalah golongan flavonol, dengan gugus hidroksi pada posisi 5 hidroksi dan isolat II (Rf = 0,91) dengan spektrofotometer ultraviolet dengan pereaksi geser juga menunjukkan golongan flavonol, dengan gugus hidroksi pada posisi 5 hidroksi.
C. Saran
DAFTAR PUSTAKA
Anonim 04 Des 2008. Rhaphidophora pinnata. E Prints@llSc.
http: /
Arthur, C. (1981). An Integrated System Of Classification Of Flowering Plants. Columbia University Press. Pages. 477 and 481
Blasche, H.G (1998). Analisis Farmasi. Gadjah Mada University Press. Yogyakarta. Hal. 413-416
Burkill, I.H. (1935). A Dictionary Of The Economic Products Of The Malay Peninsula. Volume II. London. Pages. 889
Gembong, T. (1990). Morfologi Tumbuhan. Cetakan keenam. Gadjah Mada University Press. Yogyakarta. Hal. 54-58
Dachrianus, Drs. (2002). Analisis Struktur Senyawa Organik Secara Spektroskopi. Andalas University Press. Padang. Hal. 1-7
Djahauriya dan Hernani. (2004). Gulma Khasiat Obat. Seri Agrisehat. Jakarta. Hal 24
Departemen Kesehatan RI. (1979). Farmakope Indonesia. Edisi III. Jakarta. Hal. 748, 891.
Departemen Kesehatan RI. (1979). Materia Medika Indonesia. Jilid III. Jakarta. Hal. 131,133, 135, 138, 141, 167, 168, 169, 170
Farnsworth, N.R. (1996). Biological and Phytochemical screening of Plants. Journal of Pharmaceutical Science. Volume 55. Number 3. Chicago. Rheins Chemical Company. Pages. 264
Fessenden, R. J. Fessenden, J. S. (1995). Kimia Organik. Penerjemah : Pudjaatmaka. A. H. Jilid kedua. Edisi ketiga. Penerbit Erlangga. Jakarta. Hal. 407-409, 418, 437-439, 454-454.
Hart H. (2003). Kimia Organik. Edisi Kesebelas. Penerbit Erlangga. Surabaya. Hal 375, 389
Heyne, K. (1987). Tumbuhan Berguna Indonesia. Jilid I. Cetakan I. Penerjemah : Badan Litbang Kehutanan. Penerbit Yayasan Sarana Wanajaya. Jakarta. Hal. 493-494
Hosttmann, K. Hostettmann, M. dan Marston, A. (1995). Cara Kromatografi Preparatif. Penggunaan Pada Isolasi Senyawa Alam. Penerjemah: Padmawinata, K. Penerbit ITB. Bandung. Hal 9-12, 33-34
Ikan, R. (1994). Natural Product. Second Printing. Academic-Press. London. Pages. 146-147
Lemmens and N. Bunyapraphatsara. (2003). Plant Resources Of South-East Asia. Backhuys Publisher. Leiden. Pages.189
Mabry, T.J. Markham. K.R. dan Thomas, M.B. (1970). The Systematic Identification of Flavonoids. New York: Springer-Verlag. Pages. 43-54
Mangan, Y. (2003). Cara Bijak menaklukkan kanker. Cetakan I. Jakarta. Penerbit PT. agromedia Pustaka. Hal. 28-32.
Markham, K.R. (1988). Cara Mengidentifikasi Flavonoida. Penerjemah: K Padmawinata. Bandung: Penerbit ITB-Press. Hal. 1,15-27,32-33, 38-49
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Edisi keenam. Terjemahan K. Padmawinata, Bandung : ITB. Hal. 191-192, 195-197, 203 Sastrohamidjojo, H. (1985). Kromatografi. Edisi I. Yogyakarta. Penerbit Liberty.
Hal. 1-5, 13-25
Tyler, V.E, et al. (1988). Pharmacognosy. Ninth Edition. Lea and Febiger. Philadelphia. Pages. 57-59, 67, 77-78,186-187
Wijayakusuma, H.S. (1996). Tanaman Berkhasiat obat di Indonesia. Cetakan kedua. Jakarta: Pustaka Kartini. Hal.7
Lampiran 1
Lampiran 2
Gambar 1. Tanaman ekor naga (Rhaphidophora pinnata Schott.)
Lampiran 3
Lampiran 4
Gambar 4. Alat Soklet Keterangan:
1. Pendingin balik 5. Tabung soklet 2. Statif dan klem 6. Labu alas bulat
3. Air keluar 7. Mantel pemanas
1 2
3
4
5
Lampiran 5
Gambar 5. Pemeriksaan mikroskopik sayatan melintang daun tanaman ekor naga (Rhaphidophorae pinnatae Folium)
Keterangan :
1. Kutikula 2. Epidermis atas
3. Kristal kalsium oksalat bentuk druse 4. Jaringan palisade
5. Berkas pembuluh
Lampiran 6
Gambar 6. Pemeriksaan mikroskopik sayatan membujur atas daun tanaman ekor naga (Rhaphidophorae pinnatae Folium)
Keterangan :
1. Sel epidermis
Lampiran 7
Gambar 7. Pemeriksaan mikroskopik sayatan membujur bawah daun tanaman ekor naga (Rhaphidophoreae pinnataFolium)
Keterangan :
1. Stomata tipe parasitik 2. Sel epidermis
Lampiran 8
Gambar 8. Mikroskopik serbuk simplisia daun tanaman ekor naga (Rhaphidophoreae pinnata Folium)
Keterangan:
1. Kristal kalsium oksalat bentuk druse 2. Stomata tipe parasitik
Lampiran 9
Bagan 1. Penyiapan simplisia daun tumbuhan ekor naga Ditimbang
Daun tanaman ekor naga (Rhaphidophorae pinnatae Folium) Disortasi basah
Serbuk simplisia = 820 g
Dicuci, ditiriskan
Ekstraksi Skrining fitokimia (± 7 g)
- Alkaloid
Karakteristik Simplisia (± 2 g) - Kadar air
- Kadar sari yg larut dalam air - Kadar sari yang larut dalam
etanol
- Kadar abu total & tidak larut dlm asam
K d b id k l dl Ditimbang