SEL BETA PANKREAS TIKUS WISTAR JANTAN MODEL DIABETES MELLITUS TIPE 2 YANG DIBERI PAKAN TINGGI
LEMAK DAN STREPTOZOTOCIN DOSIS RENDAH
T E S I S
OLEH
NINGRUM WAHYUNI 117008006/BM
PROGRAM STUDI MAGISTER (S-2) ILMU BIOMEDIK FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA MEDAN
BETA PANKREAS TIKUS WISTAR JANTAN MODEL DIABETES MELLITUS TIPE 2 YANG DIBERI PAKAN TINGGI LEMAK DAN
STREPTOZOTOCIN DOSIS RENDAH
T E S I S
Untuk melengkapi persyaratan memperoleh Gelar Magister Biomedik
dalam Program Studi Magister Ilmu Biomedik
pada Fakultas Kedokteran Universitas Sumatera Utara
Oleh
NINGRUM WAHYUNI 117008006/ BM
PROGRAM STUDI MAGISTER (S-2) ILMU BIOMEDIK FAKULTAS KEDOKTERAN
UNIVERSITAS SUMATERA UTARA MEDAN
PANKREAS TIKUS WISTAR JANTAN MODEL DIABETES MELLITUS TIPE 2 YANG DIBERI PAKAN TINGGI LEMAK DAN STREPTOZOTOCIN DOSIS RENDAH
Nama : NINGRUM WAHYUNI
Nomor Pokok : 117008006
Program Studi : ILMU BIOMEDIK
Menyetujui Komisi Pembimbing,
(Prof.Dr.Drs.Syafruddin Ilyas, M. Biomed) (dr.Alya Amila Fitrie,M.Kes,Sp.PA) Ketua Anggota
Ketua Program Studi Biomedik, Dekan,
(dr. Yahwardiah Siregar, Ph.D) (Prof. dr. Gontar A.Siregar,SpPD,KGEH) NIP : 195508071985032001 NIP : 195402201980111001
PANITIA PENGUJI TESIS
KETUA : Prof. Dr. Drs. Syafruddin Ilyas, M. Biomed Anggota : 1. dr. Alya Amila Fitrie, M.Kes, Sp.PA
RENDAH
ABSTRAK
Latar belakang: Selama lebih dari 30 tahun terakhir, jumlah penderita diabetes melitus meningkat dua kali lipat secara global. Menurut data Global Prevalence of Diabetes
(2000), jumlah penderita DM di Indonesia diperkirakan mencapai angka 21,3 juta pada tahun 2030. Disfungsi jaringan adiposa berperan penting pada kejadian resistensi insulin. Jaringan adiposa menghasilkan TNF ; dihubungkan dengan timbulnya resistensi insulin, obesitas dan diabetes. Jamur secara tradisional juga telah digunakan untuk pencegahan diabetes. Penelitian ini bertujuan untuk mengetahui efek antioksidan dari jamur Pleurotus ostreatus terhadap sel beta pankreas.
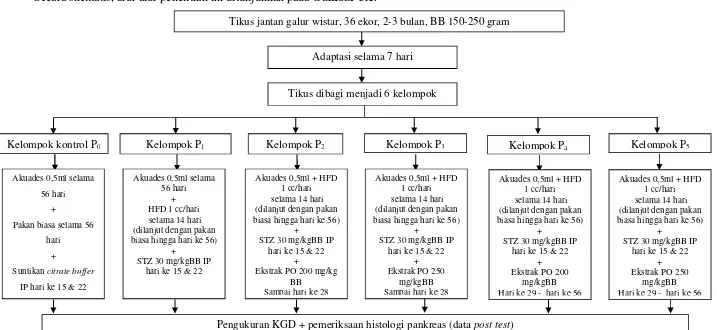
Metode: Penelitian ini adalah penelitian eksperimental dengan rancangan posttest only control goup design. Subjek penelitian ini adalah 24 ekor tikus Wistar jantan, dibagi menjadi enam kelompok (n = 4 ekor/perlakuan). Grup P0 diberi akuades dan citrate
buffer. Grup P1 diberi pakan tinggi lemak dan STZ dosis rendah (30 mg/kgBB). Grup P2 dan P3 diberi pakan tinggi lemak dan STZ dosis rendah bersamaan dengan ekstrak etanol Pleurotus ostreatus (200mg/kgBB/hari dan 250mg/kgBB/hari). Grup P4 dan P5 diberi pakan tinggi lemak dan STZ dosis rendah, setelah itu diberi ekstrak etanol
Pleurotus ostreatus (200 mg/kgBB/hari dan 250mg/kgBB/hari). Pengukuran KGD dan perhitungan area sel beta pankreas dilakukan pada hari ke 57 setelah perlakuan. Data yang diperoleh kemudian dianalisis dengan uji one way ANOVA.
Hasil: Hasil uji one way ANOVA menunjukkan adanya perbedaan yang bermakna antara keenam kelompok (p<0,05). Hasil uji Post Hoc menunjukkan adanya perbedaan KGD dan jumlah area sel beta pankreas antara kelompok P0 dengan kelompok P1, dan juga antara kelompok P2 dan P3 dengan kelompok P1. Sementara kelompok P4 dan P5 tidak berbeda bermakna dengan P1.
Kesimpulan: Ekstrak etanol jamur Pleurotus ostreatus dapat mencegah kerusakan sel beta pankreas pada dosis 200 dan 250 mg/kgBB tikus namun tidak dapat memperbaiki kerusakan sel beta.
STREPTOZOTOCIN
ABSTRACT
Background: Over the last 30 years, the amount of DM incident has been increased. According to Global Prevalence of Diabetes (2000) DM incident in Indonesia estimated about 21.3 million in 2030. Adipose tissue dysfunction plays a significant role in the insulin resistance. Adipose tissue produces TNF lead to the insulin resistance incident, obesity, and diabetes. Traditionally, mushroom has been used to prevent diabetes. This study aimed to perceive the antioxidant effect of Pleurotus ostreatus to the beta cell pancreas.
Methods: This research was an experimental study using randomized control group posttest only design. Subjects of this research were 24 male Wistar rats and divided into six groups (n=4 rats/treatment). Group P0 just received aquadest and buffer citrate.
Group P1 received high fat diet and low dose STZ. Group P2 and P3 received high fat
diet and low dose STZ together with ethanolic extract of Pleurotus ostreatus (respectively 200mg/body weight/day and 250mg/body weight/day). Group P4 and P5
received high fat diet and low dose STZ, then treated with ethanolic extract of Pleurotus ostreatus (respectively 200mg/body weight/day and 250mg/body weight/day). Blood glucose level measurement and beta cell area calculation were done at 57 day after treatment. Data from this research was analyzed using one way ANOVA.
Results: There were significant difference among six groups (p<0,05). The result of Post Hoc test for blood glucose level and beta cell area showed the significant difference between P0 with P1, and between P2 and P3 to P1. And P4 and P5 didn’t show
significant difference to P1.
Conclusion: Ethanolic extract of Pleurotus ostreatus prevented beta cell pancreas damage at 200 and 250 mg/bodyweight but did not ameliorate the beta cell damage.
Puji dan syukur penulis ucapkan kepada Allah SWT atas segala rahmat dan
karunia-Nya penulis dapat menyelesaikan tesis ini dengan judul ”Efek Jamur Tiram Putih
(Pleurotus ostreatus) terhadap Sel Beta Pankreas Tikus Wistar Jantan Model Diabetes Mellitus tipe 2 yang Diberi Pakan Tinggi Lemak dan Streptozotocin Dosis Rendah”, sebagai salah satu syarat dalam menyelesaikan jenjang pendidikan Magister pada
program studi Ilmu Biomedik Fakultas Kedokteran Universitas Sumatera Utara. Proses
penulisan tesis ini tidak lepas dari bimbingan, bantuan, dukungan dan doa dari berbagai
pihak. Pada kesempatan ini ucapan terima kasih yang sebesar-besarnya saya sampaikan
dengan hormat kepada :
1. Prof. Dr. Syahril Pasaribu, DTMH, MSc (CTM), SpA(K), Rektor Universitas
Sumatera Utara
2. Prof. dr. Gontar A. Siregar, SpPD-KGEH., Dekan Fakultas Kedokteran
Universitas Sumatera Utara.
3. Dr. Yahwardiah Siregar, PhD., Ketua Program Studi Biomedik, yang memberi
banyak masukan kepada penulis.
4. Prof. DR. Drs. Syafrudin Ilyas, M. Biomed, Ketua Komisi Pembimbing yang
senantiasa bersedia meluangkan waktu untuk membimbing, memberikan
masukan dan pemikiran dengan penuh kesabaran kepada penulis untuk
menyelesaikan tesis ini.
5. dr. Alya Amila Fitrie, M.Kes, Sp.PA, anggota Komisi Pembimbing yang telah
banyak memberikan bimbingan, masukan, motivasi dan dukungan kepada
penulis untuk menyelesaikan tesis ini.
6. DR. M. Pandapotan Nasution, MPS, Apt., Dosen Pembanding yang juga turut
meluangkan waktu dan banyak memberikan masukan, dan motivasi kepada
penulis untuk perbaikan tesis ini.
7. dr. Mardianto, Sp.PD-KEMD, FINASIM, Dosen Pembanding yang juga turut
meluangkan waktu memberikan masukan untuk perbaikan tesis ini.
8. dr. Mutiara Indah Sari, M.Kes., sekretaris program studi yang banyak
menyelesaikan pendidikan ini.
10.Kepada keluarga saya, terutama suami yang telah bersabar dan mendoakan
kemudahan untuk penyelesaian tesis ini hingga rampung.
11.Kepada sahabat-sahabat saya, terima kasih atas pengertian, perhatian, dukungan
dan doa sehingga saya bisa menyelesaikan pendidikan ini.
12.Kepada teman-teman seangkatan 2011 yang banyak memberikan dorongan dan
motivasi.
13.Kepada seluruh staf Anatomi – Histologi FK UISU yang telah banyak
memberikan dukungan, doa dan semangat serta motivasi yang besar.
Masih banyak lagi saudara/i ku yang lain yang tidak mungkin saya sebutkan satu
persatu, terima kasih untuk semuanya. Penulis berharap, semoga proses pendidikan
yang penulis jalani memberikan manfaat baik bagi penulis sendiri dan bagi orang lain.
Penulis berterima kasih atas masukan, saran dan kritikan dari semua pihak guna
perbaikan dari penelitian ini.
Medan, Agustus 2014
Penulis
Nama : Ningrum Wahyuni
Tempat/Tgl Lahir : Medan, 5 April 1984
Agama : Islam
Alamat : Jl. Polonia Komp. Flamingo no-J-11
Medan 20157
Telp : 081265022696
Ayah : Tri Marsono
Ibu : Sudarmawan
Anak ke : 1 dari 3 bersaudara
Email : ningrumwahyuni@gmail.com
PENDIDIKAN:
SD Angkasa 2 Lanud Medan : Tahun 1990-1996
MTs Muhammadiyah Kwalamadu Binjai : Tahun 1996-1999
SMU Negeri 1 Medan : Tahun 1999-2002
Fakultas Kedokteran UISU Medan : Tahun 2003- 2009
PEKERJAAN :
Dosen Tetap Kontrak FK-UISU staff Anatomi Histologi dari tahun 2010 s/d sekarang
BAB V. KESIMPULAN DAN SARAN ... 71
5.1. Kesimpulan ... 71
5.2. Saran ... 71
DAFTAR PUSTAKA ... 73
Tabel Halaman
2.1. Klasifikasi Diabetes Melitus ... 7
2.2. Kriteria Diagnosis Diabetes Melitus ... 9
2.3. Faktor Resiko DM tipe 2 ... 10
4.1. Hasil Identifikasi dan Klasifikasi Jamur Tiram Putih ... 53
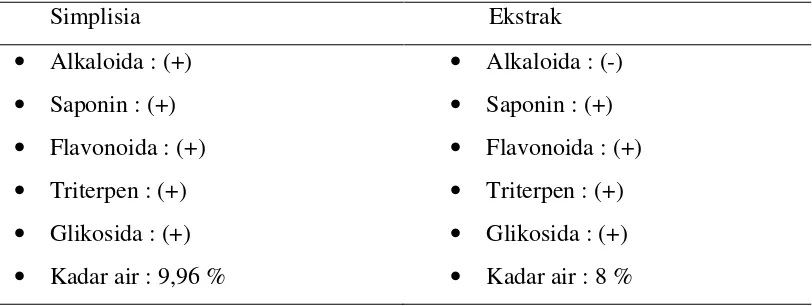
4.2. Hasil Skrining Fitokimia untuk Simplisia dan Ekstrak ... 53
4.3. Hasil Standarisasi Simplisia Jamur Pleurotus ostreatus ... 54
4.4. Rerata Pengukuran KGD pada Kelompok Preventif (mg/dl) ... 54
4.5. Rerata Perhitungan Area Sel Beta pada Kelompok Preventif (%) ... 59
4.6. Rerata Pengukuran KGD pada Kelompok Kuratif (mg/dl) ... 61
Gambar Halaman
1.1. Gambar kerangka konsep ... 6
2.1. Jalur transduksi sinyal insulin di otot polos ... 15
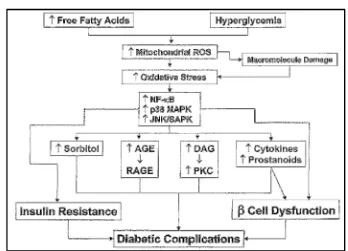
2.2. Hubungan antara peningkatan FFA dan hiperglikemia menghasilkan patofisiologi DM melalui pembentukan ROS ... 18
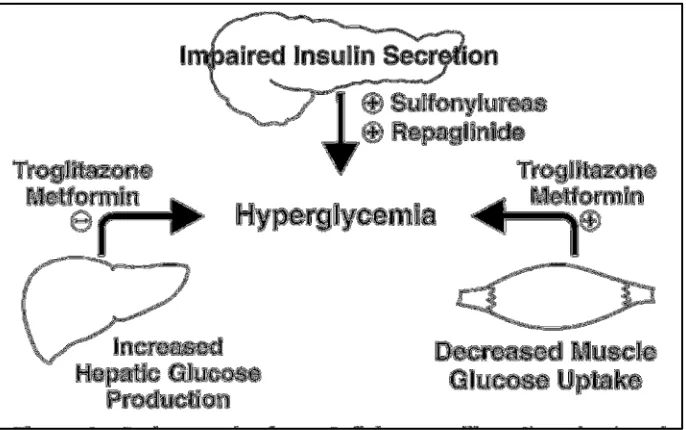
2.3. Tempat kerja obat oral yang diindikasikan ... 22
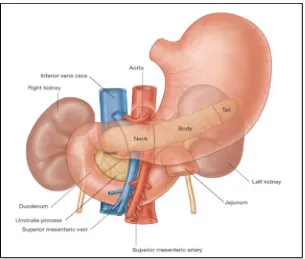
2.4. Posisi anatomi pankreas ... 23
4.1. Grafik Rerata KGD Tikus pada Kelompok Preventif ... 55
4.2. Gambaran Imunohistokimia Antibodi Anti-Insulin Pankreas Tikus Kelompok P0 yang Diberi Citrate Buffer ... 57
4.3. Gambaran Imunohistokimia Antibodi Anti-Insulin Pankreas Tikus Kelompok P1 yang Diberi Diet Tinggi Lemak dan STZ dosis rendah .. 57
4.4. Gambaran Imunohistokimia Antibodi Anti-Insulin Pankreas Tikus Kelompok P2 yang Diberi Diet Tinggi Lemak dan STZ dosis rendah bersamaan dengan Ekstrak Jamur PO 200 mg/kgBB ... 58
4.5. Gambaran Imunohistokimia Antibodi Anti-Insulin Pankreas Tikus Kelompok P3 yang Diberi Diet Tinggi Lemak dan STZ dosis rendah bersamaan dengan Ekstrak Jamur PO 250 mg/kgBB ... 58
4.9. Gambaran Imunohistokimia Antibodi Anti-Insulin Pankreas Tikus Kelompok P1 yang Diberi Diet Tinggi Lemak dan STZ dosis rendah .. 64
4.10. Gambaran Imunohistokimia Antibodi Anti-Insulin Pankreas Tikus Kelompok P2 yang Diberi Diet Tinggi Lemak dan STZ dosis rendah, lalu diberi Ekstrak Jamur PO 200 mg/kgBB ... 65
4.11. Gambaran Imunohistokimia Antibodi Anti-Insulin Pankreas Tikus Kelompok P2 yang Diberi Diet Tinggi Lemak dan STZ dosis rendah, lalu diberi Ekstrak Jamur PO 250 mg/kgBB ... 65
Nomor Judul Halaman 1. Hasil Identifikasi dan Klasifikasi Jamur Tiram Putih (Pleurotus ostreatus) 82
2. Hasil Skrining Fitokimia Simplisia ... 83
3. Hasil Skrining Fitokimia Ekstrak ... 87
4. Cara Perhitungan Dosis Ekstrak Jamur PO ... 89
5. Uji Normalitas terhadap Kadar Gula Darah (KGD) Tikus pada Kelompok Preventif ... 89
6. Uji Kesamaan Varians terhadap KGD Tikus pada Kelompok Preventif ... 89
7. Uji post hoc Bonferroni Perbandingan data KGD pada Kelompok Preventif ... 90
8. Uji Normalitas terhadap Area Sel Beta Pankreas Tikus pada Kelompok Preventif ... 91
9. Uji Kesamaan Varians terhadap Area Sel Beta Pankreas Tikus Kelompok Preventif ... 91
10. Uji post hoc Bonferroni Perbandingan data Area Sel Beta Pankreas pada Kelompok Preventif ... 92
11. Uji Normalitas terhadap Kadar Gula Darah (KGD) Tikus pada Kelompok Kuratif ... 92
12. Uji Kesamaan Varians terhadap KGD Tikus pada Kelompok Kuratif .... 93
13. Grafik Slope dan Power untuk Menentukan Rumus Transformasi data KGD Tikus pada Kelompok Kuratif ... 93
14. Uji Kesamaan Varians Data dan Uji ANOVA Hasil Transformasi pada Kelompok Kuratif ... 94
15. Hasil bootstrap Data Kadar Gula Darah pada Kelompok Kuratif ... 94 16. Uji post hoc Bonferroni Perbandingan data KGD Kelompok Kuratif ... 95
19. Uji post hoc Bonferroni Perbandingan Data Area Sel Beta Pankreas pada Kelompok Kuratif ... 97
20. Surat Ethical Clearance ... 98
21. Penjelasan Prosedur Penggunaan Kit Pemeriksaan Kadar Gula Darah .... 99
22. Foto Jamur Tiram Putih yang Digunakan pada Penelitian ... 101
Akt : Protein Kinase B
ALT : Alanine transaminase
AMPK : 5' Adenosine Monophosphate-Activated Protein Kinase
AST : Aspartate aminotransferase
CGA : Chlorogenic acid
CRP : C Reactive Protein
DAG : Diacylglycerol
DM : Diabetes Melitus
DNA : Deoxyribonucleic acid
DPPH : Diphenyl-picrylhydralazyl
FFA : Free Fatty Acid
GDM : Gestational Diabetes Mellitus
GLUT : Glucose Transporter
HDL : High Density Lipoprotein
HFD : High Fat Diet
IFG : Impaired Fasting Glucose
IGT : Impaired Glucose Tolerance
IL : Interleukin
IMT : Indeks Massa Tubuh
iNOS : inducible Nitric Oxide Synthase
IRS : Insulin Receptor Substrate
ISSR : Inter Simple Sequence Repeat
KGD : Kadar Gula Darah
LDL : Low Density Lipoprotein
MDA : Malondialdehyde
MODY : Maturity Onset Diabetes of The Young
mRNA : messenger Ribonucleic acid
NADPH : Nicotinamide adenine dinucleotide phosphate
NF- B :Nuclear Factor Kappa-Light-Chain-Enhancer Of Activated B Cells
OH : Hidroksil
PAC : Protocatechuic acid
PCO : Polycystic Ovary Syndrome
PI3K : Phospphatidyl Inositol 3 Kinase
PKC : Protein Kinase C
PO : Pleurotus ostreatus
PPAR : Peroxisome proliferator-activated receptor
ROS : Reactive Oxygen Species
STZ : Streptozotocin
TG/TAG : Trigliserida/Triacylglycerol
RENDAH
ABSTRAK
Latar belakang: Selama lebih dari 30 tahun terakhir, jumlah penderita diabetes melitus meningkat dua kali lipat secara global. Menurut data Global Prevalence of Diabetes
(2000), jumlah penderita DM di Indonesia diperkirakan mencapai angka 21,3 juta pada tahun 2030. Disfungsi jaringan adiposa berperan penting pada kejadian resistensi insulin. Jaringan adiposa menghasilkan TNF ; dihubungkan dengan timbulnya resistensi insulin, obesitas dan diabetes. Jamur secara tradisional juga telah digunakan untuk pencegahan diabetes. Penelitian ini bertujuan untuk mengetahui efek antioksidan dari jamur Pleurotus ostreatus terhadap sel beta pankreas.
Metode: Penelitian ini adalah penelitian eksperimental dengan rancangan posttest only control goup design. Subjek penelitian ini adalah 24 ekor tikus Wistar jantan, dibagi menjadi enam kelompok (n = 4 ekor/perlakuan). Grup P0 diberi akuades dan citrate
buffer. Grup P1 diberi pakan tinggi lemak dan STZ dosis rendah (30 mg/kgBB). Grup P2 dan P3 diberi pakan tinggi lemak dan STZ dosis rendah bersamaan dengan ekstrak etanol Pleurotus ostreatus (200mg/kgBB/hari dan 250mg/kgBB/hari). Grup P4 dan P5 diberi pakan tinggi lemak dan STZ dosis rendah, setelah itu diberi ekstrak etanol
Pleurotus ostreatus (200 mg/kgBB/hari dan 250mg/kgBB/hari). Pengukuran KGD dan perhitungan area sel beta pankreas dilakukan pada hari ke 57 setelah perlakuan. Data yang diperoleh kemudian dianalisis dengan uji one way ANOVA.
Hasil: Hasil uji one way ANOVA menunjukkan adanya perbedaan yang bermakna antara keenam kelompok (p<0,05). Hasil uji Post Hoc menunjukkan adanya perbedaan KGD dan jumlah area sel beta pankreas antara kelompok P0 dengan kelompok P1, dan juga antara kelompok P2 dan P3 dengan kelompok P1. Sementara kelompok P4 dan P5 tidak berbeda bermakna dengan P1.
Kesimpulan: Ekstrak etanol jamur Pleurotus ostreatus dapat mencegah kerusakan sel beta pankreas pada dosis 200 dan 250 mg/kgBB tikus namun tidak dapat memperbaiki kerusakan sel beta.
STREPTOZOTOCIN
ABSTRACT
Background: Over the last 30 years, the amount of DM incident has been increased. According to Global Prevalence of Diabetes (2000) DM incident in Indonesia estimated about 21.3 million in 2030. Adipose tissue dysfunction plays a significant role in the insulin resistance. Adipose tissue produces TNF lead to the insulin resistance incident, obesity, and diabetes. Traditionally, mushroom has been used to prevent diabetes. This study aimed to perceive the antioxidant effect of Pleurotus ostreatus to the beta cell pancreas.
Methods: This research was an experimental study using randomized control group posttest only design. Subjects of this research were 24 male Wistar rats and divided into six groups (n=4 rats/treatment). Group P0 just received aquadest and buffer citrate.
Group P1 received high fat diet and low dose STZ. Group P2 and P3 received high fat
diet and low dose STZ together with ethanolic extract of Pleurotus ostreatus (respectively 200mg/body weight/day and 250mg/body weight/day). Group P4 and P5
received high fat diet and low dose STZ, then treated with ethanolic extract of Pleurotus ostreatus (respectively 200mg/body weight/day and 250mg/body weight/day). Blood glucose level measurement and beta cell area calculation were done at 57 day after treatment. Data from this research was analyzed using one way ANOVA.
Results: There were significant difference among six groups (p<0,05). The result of Post Hoc test for blood glucose level and beta cell area showed the significant difference between P0 with P1, and between P2 and P3 to P1. And P4 and P5 didn’t show
significant difference to P1.
Conclusion: Ethanolic extract of Pleurotus ostreatus prevented beta cell pancreas damage at 200 and 250 mg/bodyweight but did not ameliorate the beta cell damage.
BAB I PENDAHULUAN 1.1 Latar Belakang
Diabetes tipe 2 merupakan kelainan heterogen yang ditandai dengan
menurunnya kerja insulin secara progresif (resistensi insulin), yang diikuti dengan
ketidakmampuan sel beta untuk mengkompensasi resistensi insulin (disfungsi sel
beta pankreas) (Srinivasan et al., 2005). Selama lebih dari 30 tahun terakhir, jumlah penderita diabetes melitus meningkat dua kali lipat secara global, dan
menjadi tantangan dalam bidang kesehatan di beberapa negara (Chen et al., 2011). Diabetes melitus (DM) tipe 2 ini merupakan tipe yang paling banyak diantara
bentuk diabetes lainnya (Bi et al., 2012), bahkan pada tahun 2010 mencapai 90% dari total kejadian penyakit diabetes (Chen et al., 2011). Prevalensi DM tipe 2 telah mencapai proporsi epidemi di seluruh dunia dan menjadi ancaman kesehatan
global ( Bi et al., 2012; Ramachandran & Snehalatha, 2012). Di Amerika Serikat, DM tipe 2 mengenai kira-kira 16 juta orang, di seluruh dunia mengenai 135 juta
orang dan diperkirakan mencapai angka 300 juta pada tahun 2025 (Choi et al., 2005).
Masalah diabetes melitus saat ini berada pada negara berkembang
dibandingkan negara maju, dengan 80% penderita berada di negara berkembang.
Diantara 10 negara dengan prediksi jumlah penderita DM tipe 2 terbanyak pada
tahun 2030, lima diantaranya adalah negara di Asia, yaitu China, India, Pakistan,
Indonesia, dan Bangladesh (Chen et al., 2011). Di negara berkembang, mayoritas penderita diabetes berada pada rentang umur 45 – 64 tahun. Sebaliknya di negara
Prevalence of Diabetes, jumlah penderita DM di Indonesia pada tahun 2000 sebanyak 8,4 juta dan diperkirakan mencapai angka 21,3 juta pada tahun 2030
(Wild et al., 2004). DM tipe 2 meningkat angka kejadiannya pada anak-anak, remaja dan dewasa muda (Chen et al., 2011).
Sejumlah faktor mempengaruhi angka kejadian DM tipe 2, antara lain pola
diet yang menyebabkan obesitas, kerentanan gen, merokok dan konsumsi alkohol
( Chen et al., 2011; Ramachandran & Snehalatha, 2012), gaya hidup yang kurang gerak dan terlalu banyak duduk (Bi et al., 2012), gangguan tidur dan depresi (Chen et al., 2011). Peranan diet lemak pada kejadian DM tipe 2 telah mejadi perhatian klinis selama beberapa dekade (Risérus et al., 2009).
Obesitas secara klinis didefinisikan sebagai Indeks Massa Tubuh (IMT) 30
kg/m2, merupakan penyakit yang memiliki prevalensi tinggi di segala usia dan
dengan cepat mencapai proporsi pandemi (Tataranni, 2002). Studi terkini
menemukan hubungan antara obesitas dengan DM tipe 2 yang melibatkan sitokin
proinflamasi (TNF dan IL-6), resistensi insulin, terganggunya metabolisme asam
lemak, dan proses seluler seperti disfungsi mitokondria (Eckel et al., 2011). Kualitas diet lemak sebagian besar mempengaruhi komposisi asam lemak
membran sel dan karenanya mempengaruhi fungsi membran sel. Komposisi asam
lemak membran sel diduga merubah sejumlah fungsi sel, termasuk ketidakstabilan
membran, permeabilitas ion, dan afinitas/ikatan reseptor insulin (Risérus et al., 2009).
Pengaruh obesitas terhadap resiko DM tipe 2 tidak hanya ditentukan oleh
derajat obesitas, namun juga dipengaruhi oleh dimana terjadinya akumulasi
terlihat pada rasio pinggang-panggul dikaitkan dengan sindroma metabolik, DM
tipe 2, dan penyakit kardiovaskular (Eckel et al., 2011). Disfungsi jaringan adiposa memainkan peranan penting pada kejadian resistensi insulin (Snel et al., 2012). Jaringan adiposa menghasilkan TNF bersama monosit dan limfosit;
dimana TNF terlibat dalam respon inflamasi dan dihubungkan dengan timbulnya
resistensi insulin, obesitas dan diabetes (Bi et al., 2012).
Resistensi insulin merupakan abnormalitas metabolik utama pada sebagian
besar pasien dengan DM tipe 2 (Glass & Olefsky, 2012), dimana baik pada hewan
coba maupun manusia terdapat akumulasi lipid intrasel pada otot skeletal dan
liver. Akumulasi lipid ini dapat menyebabkan hambatan GLUT4, yang kemudian
menekan masuknya glukosa kedalam sel dan menghambat oksidasi glukosa dan
sintesis glikogen (Wolf, 2008).
STZ telah digunakan sebagai agen alkilasi kemoterapi untuk pengobatan
tumor sel pulau Langerhans metastasis. Pada tahun 1963 Rakieten melaporkan
bahwa STZ merupakan diabetogenik dan sejak saat itulah STZ digunakan sebagai
zat penginduksi DM di laboratorium hewan (Lenzen, 2007). Pada pemberian STZ,
tanda-tanda DM yang terjadi seperti meningkatnya asupan makanan dan air, berat
badan tidak bertambah, dan meningkatnya KGD (Wei et al., 2003). Pada pengamatan mikroskopis mencit yang diinduksi dengan STZ terlihat abnormalitas
pankreas secara histomorfologi. Pulau Langerhans berbentuk tidak teratur dan
ukurannya berkurang. Jumlah sel endokrin pankreas berkurang (Tian et al., 2010). Diabetes dapat dikontrol dengan manajemen diet yang tepat. Obat tradisional
seperti jamur sangat bermanfaat untuk penatalaksanaan sejumlah masalah
diabetes, obesitas, penyakit jantung, konstipasi, kanker dan hipertensi (Agrawal &
Chopra, 2010). Polisakarida (beta glucan) yang terdapat dalam jamur, secara khusus, dapat mengembalikan fungsi jaringan pankreas dengan
meningkatan pelepasan insulin oleh sel fungsional, yang menurunkan kadar gula
darah dan juga tampaknya dapat memperbaiki sensitivitas sel perifer terhadap
insulin sirkulasi (Rathee & Rathee, 2012; Silva et al., 2012).
Spesies Pleurotus merupakan anggota filum Basidiomycota. Manfaat terapeutik dari Pleurotus ostreatus antara lain: antimikroba, antivirus, antineoplasma, antioksidan, antilipidemik, hipoglikemik, hipotensif, antiinflamasi,
hepatoprotective, hipokolesterolemik. Efek hipoglikemiknya diduga karena
adanya senyawa guanide yang bisa diekstrak dari jamur ini. Sementara efek antioksidannya karena adanya peran pleuran (beta glucan) yang pada penelitian sebelumnya menunjukkan efek positif terhadap lesi pra-kanker. Pleurotus ostreatus meningkatkan enzim antioksidan yang mengurangi kerusakan oksidatif pada manusia. Pleurotus ostreatus juga mengandung senyawa polifenol yang memiliki kemampuan untuk menghambat efek mutagen dan karsinogen (Patel et al., 2012). Pada penelitian Ikrimah pada tahun 2012, dibuktikan bahwa ekstrak jamur tiram terbukti mampu meregenerasi sel pulau Langerhans yang dilihat dari
berat pankreas dan menurunkan kadar gula darah (Ikrimah & Permatasari, 2012).
Berdasarkan uraian diatas peneliti tertarik untuk meneliti efek ekstrak jamur
tiram putih terhadap sel pankreas tikus yang diinduksi DM tipe 2 dengan
1.2 Perumusan Masalah
Bagaimanakah efek pemberian ekstrak etanol jamur tiram putih (Pleurotus ostreatus) terhadap sel beta pankreas yang mengalami degenerasi disebabkan resistensi insulin oleh induksi pakan tinggi lemak dan STZ dosis rendah?
1.3 Tujuan Penelitian 1.3.1 Tujuan Umum
Tujuan umum penelitian ini adalah untuk mengetahui efek ekstrak etanol
jamur tiram putih terhadap sel pankreas tikus wistar jantan yang diberi
pakan tinggi lemak dan streptozotocin dosis rendah.
1.3.2 Tujuan Khusus
1. Mendapatkan ekstrak etanol jamur tiram putih (Pleurotus ostreatus) untuk digunakan dalam penelitian ini serta mengetahui kandungannya secara
kualitatif.
2. Mengetahui efek pemberian ekstrak etanol jamur tiram putih (Pleurotus ostreatus) dalam menurunkan kadar gula darah tikus Wistar jantan yang diinduksi dengan pakan tinggi lemak dan streptozotocin dosis rendah.
3. Mengamati efek ekstrak etanol jamur tiram putih Pleurotus ostreatus
terhadap sel pankreas pada tikus Wistar jantan yang diinduksi dengan
pakan tinggi lemak dan streptozotocin dosis rendah.
1.4 Hipotesis Penelitian
Ekstrak etanol jamur tiram putih (Pleurotus ostreatus) dapat mencegah dan memperbaiki kerusakan sel pankreas tikus Wistar jantan DM tipe 2 yang
1.5 Manfaat Penelitian
1.5.1 Menyediakan informasi ilmiah mengenai jamur tiram putih (Pleurotus ostreatus) dan efeknya terhadap DM tipe 2
1.5.2 Penelitian ini dapat dijadikan tambahan informasi untuk pengembangan
bahan obat dari alam.
1.6 Kerangka Konsep
Gambar 1.1 Gambar kerangka konsep DM tipe 2
High fat diet
+
Streptozotocin dosis rendah
Tikus Wistar jantan
Ekstrak etanol Pleurotus ostreatus
- Kadar Gula Darah <<< - Morfologi sel pankreas
BAB II
TINJAUAN PUSTAKA
2.1 Diabetes Melitus tipe 2 2.1.1 Definisi
Diabetes melitus (DM) merupakan sekelompok kelainan heterogen secara
genetis dan klinis yang ditandai dengan kadar gula didalam darah yang meningkat
secara tidak normal. Kelainan ini terjadi, baik ketika pankreas tidak bisa
memproduksi insulin yang cukup maupun saat tubuh tidak dapat menggunakan
insulin yang dihasilkan secara efektif. Pada kelainan ini, biasanya juga terjadi
gangguan metabolisme karbohidrat, lipid dan protein (Harris, 2004; WHO, 2013).
2.1.2 Klasifikasi
Secara umum diabetes dibagi menjadi 4 subkelas, yaitu DM tipe 1, DM tipe 2,
DM gestasional dan tipe DM tipe khusus. Lebih jelasnya dapat dilihat pada tabel
dibawah ini:
Tabel 2.1 Klasifikasi Diabetes Melitus (Goldman & Bennet, 2000)
I. DM tipe 1. Sebelumnya disebut sebagai insulin-dependent diabetes mellitus (IDDM) atau “juvenile onset diabetes”
II. DM tipe 2. Sebelumnya disebut sebagai non-insulin-dependent diabetes mellitus (NIDDM) atau “adult onset diabetes”
III. DM tipe khusus
A. Kerusakan genetik fungsi sel (misal: maturity onset diabetes of the young (MODY) tipe 1 – 3 dan point mutation pada DNA mitokondria) B. Kerusakan genetik kerja insulin
C. Penyakit eksokrin pankreas (pankreatitis, trauma, pankreatektomi, neoplasma, cystic fibrosis, hemokromatosis, fibrocalculous pancreatopathy)
diazoksid, pentamidin, vacor, hormon tiroid, fenitoin, agonis , kontrasepsi oral)
F. Infeksi (rubella kongenital, sitomegalovirus)
G. Bentuk diabetes immune-mediated yang jarang (sindroma “stiff-man”, antobodi reseptor anti-insulin)
H. Sindroma genetik lainnya (sindroma Down, Klinefelter, Turner, penyakit Huntington, distrofi miotonik, lipodistrofi, ataksia-telangiektasia)
IV. DM gestasional
2.1.3 Epidemiologi
Jumlah orang yang menderita DM di seluruh dunia sudah bertambah dua kali
lipat selama 30 tahun terakhir. Pada tahun 2010 diperkirakan 285 juta orang
diseluruh dunia menderita DM, dimana 90%-nya mengidap DM tipe 2. Jumlah ini
diperkirakan akan meningkat hingga 439 juta pada tahun 2030, yang mewakili
7,7% populasi dewasa total didunia yang berusia 20 – 79 tahun. (Chen et al., 2011). Di Amerika Serikat prevalensinya meningkat 10 – 15% pada orang yang
berusia 50 tahun keatas. Penyakit ini sering tidak terdiagnosa, diperkirakan ada 1
kasus yang tidak terdiagnosa untuk setiap 2 kasus yang terdiagnosa (Goldman &
Bennet, 2000).
Sejumlah ahli memperdebatkan bahwa beberapa negara di Asia muncul
sebagai pusat dari epidemi DM. Sejumlah wilayah di Asia terdiri dari beberapa
negara dengan penduduk terbanyak di dunia, dan mengalami perubahan nyata
secara demografi, epidemiologi, dan sosioekonomi selama beberapa dekade
terakhir. Negara dengan penduduk terbanyak adalah Cina dan kedua adalah India.
India dan Cina memiliki jumlah penderita DM dalam jumlah yang besar.
Meningkatnya DM tipe 2 di Asia berbeda dengan negara lain, dimana
perkembangannya relatif dalam waktu yang singkat dan pada kelompok usia yang
lemak tubuh dan obesitas abdomen lebih menonjol pada orang Asia dibandingkan
dengan orang Eropa pada nilai IMT yang sama. Karakteristik ini memiliki arti
bahwa orang Asia memiliki predisposisi resistensi insulin pada derajat obesitas
yang lebih rendah dibandingkan orang-orang keturunan Eropa (Yoon et al., 2006). DM tipe 2 juga meningkat pada orang Asia yang berimigrasi ke Amerika Serikat.
Perubahan ini dihubungkan dengan ketidakmampuan orang Asia beradaptasi
secara metabolik terhadap pola perilaku barat yang cenderung beraktivitas rendah
dengan asupan kalori yang lebih tinggi (Goldman & Bennet, 2000).
2.1.4 Diagnosis
Diagnosis biasanya langsung ditegakkan dengan munculnya gejala klasik
poliuria, polidipsi, dan turunnya berat badan. Hal ini dikonfirmasi dengan
melakukan pemeriksaan kadar gula darah sewaktu yang diambil dari pembuluh
darah vena yaitu sebesar 200 mg/dL atau lebih (Goldman & Bennet, 2000).
The National Diabetes Data Group dan World Health Organization telah menerbitkan kriteria diagnosis untuk DM yang dirangkum pada tabel berikut:
Tabel 2.2 Kriteria Diagnosis Diabetes Mellitus (Harrison, 2005)
• Gejala-gejala diabetes ditambah konsentrasi KGD random 11,1 mmol/L (200 mg/dL) atau
lingkungan memainkan peranan penting dalam memicu perkembangan DM,
diharapkan prevalensi DM lebih rendah di daerah pedesaan, dimana orang-orang
ini terbukti ketika membandingkan beda prevalensi DM di perkotaan dan
pedesaan di India, Filipina dan Kamboja. Di India, angka prevalensi di perkotaan
8,2% sementara di pedesaan prevalensinya 2,4%. Tapi perbedaan prevalensi tidak
didapati di Korea dan Thailand. Hal ini bisa saja disebabkan oleh urbanisasi
komunitas pedesaan (Yoon et al., 2006).
Faktor-faktor yang berkontribusi terhadap peningkatan prevalensi DM di Asia
salah satunya adalah urbanisasi dan transisi sosioekonomi. Sementara faktor
resiko lainnya termasuk usia, karakteristik antropometrik, merokok, alkohol, gaya
hidup tanpa olahraga dan kerentanan gen (Bi et al., 2012; Ramachandran & Snehalatha, 2012).
Mengkonsumsi makanan tinggi lemak ternyata berhubungan dengan
meningkatnya resiko DM tipe 2 (Marshall & Bessesen, 2002). Jadi, meskipun DM
tipe 2 sangat dipengaruhi olah gaya hidup dan kerentanan gen, komposisi
makanan bisa mempengaruhi perkembangan dan komplikasi DM tipe 2 ini. Asam
lemak mempengaruhi metabolisme glukosa dengan merubah fungsi membran sel,
aktivitas enzim, sinyal insulin dan ekspresi gen (Risérus et al., 2009). Tabel 2.3 Faktor resiko DM tipe 2 (Harrison, 2005)
• Riwayat keluarga diabetes (misal: orang tua atau saudara kandung dengan DM tipe 2)
• Obesitas (IMT 25 kg/m2) • Kebiasaan fisik yang tidak aktif
• Ras/etnis (misal: Afro-Amerika, Asia-Amerika, Amerika asli)
• Sebelumnya diidentifikasi dengan IFG (Glukosa Puasa Terganggu) atau IGT (Toleransi Glukosa Terganggu)
• Riwayat GDM (DM gestasional) atau melahirkan bayi > 4 kg • Hipertensi (KGD 140/90 mmHg)
• Kadar kolesterol HDL 35 mg/dL (0.9 mmol/L) dan/atau kadar trigliserida 250 mg/dL (2,82 mmol/L)
• Riwayat penyakit vaskular
2.1.6 Konsumsi Lemak dan DM tipe 2
Sejumlah peneliti menemukan kaitan antara konsumsi makanan tinggi lemak
dan asam lemak jenuh yang memiliki hubungan terhadap meningkatnya resiko
DM (Marshall & Bessesen, 2002). Hubungan ini bahkan telah ditemukan selama
lebih dari 60 tahun (Lichtenstein & Schwab, 2000). Studi terbaru telah
menemukan hubungan antara obesitas dan DM tipe 2 yang melibatkan sitokin
proinflamasi, resistensi insulin dan terganggunya metabolisme asam lemak serta
gangguan proses seluler (Eckel et al., 2011; Meyer et al., 2001). Diet lemak terutama mempengaruhi komposisi asam lemak membran sel, dan akibatnya
mempengaruhi fungsi membran sel. Komposisi asam lemak didalam membran sel
diduga mempengaruhi sejumlah fungsi sel, salah satunya adalah mengganggu
afinitas/ikatan reseptor insulin dengan cara interaksi GLUT dengan second messenger. Hal ini akan mempengaruhi sensitivitas insulin seluruh tubuh dan jaringan (Risérus et al., 2009).
a. Jaringan adiposa
Semakin banyak bukti yang menunjukkan bahwa jaringan adiposa, dengan
cara menghasilkan hormon dan energi, merupakan suatu organ penting dalam
patogenesis resistensi insulin pada DM tipe 2 (McPhee & Ganong, 2006).
Jaringan adiposa merupakan jaringan yang paling merata dalam tubuh manusia.
Jaringan ini biasanya ditemukan dalam jaringan ikat longgar subkutan, dan juga
jaringan ini melingkupi organ internal. Jaringan adiposa ini dibagi menjadi 2
subtipe: lemak putih dan lemak coklat. Lemak putih tersebar luas dan merupakan
coklat relatif jarang dan peranan utamanya adalah mempertahankan suhu tubuh.
Jaringan adiposa putih merupakan cadangan energi utama dan fungsi utamanya
adalah menyimpan trigliserida (TG) saat kelebihan energi dan melepas energi
dalam bentuk asam lemak bebas selama kekurangan energi. Jaringan adiposa
melepaskan sejumlah peptida, sitokin, dan faktor komplemen, yang berperan
sebagai autokrin dan parakrin untuk mengatur metabolisme dan pertumbuhan
adiposit, juga sinyal insulin untuk mengatur homeostasis energi (Niemelä &
Miettinen, 2008). Meningkatnya serum TG menyebabkan akumulasi DAG di otot
dan hepar, yang merupakan aktivator kuat protein kinase C (PKC) yang nantinya
akan mengaktifkan jalur fosforilasi threonine/serine, menyebabkan translokasi GLUT4 yang menurunkan penyimpanan glukosa ke dalam otot yang nantinya
mengurangi oksidasi glukosa dan sintesis glikogen. Hasil akhirnya berupa
tanda-tanda resistensi insulin: berkurangnya oksidasi glukosa dan sintesis glikogen di
otot rangka, dan berkurangnya sintesis glikogen dan lebih banyak
glukoneogenesis di hepar (Wolf, 2008)
Adiposit merupakan komponen seluler utama dari jaringan adiposa dan
sebagai tempat penyimpanan energi utama dalam bentuk TG. Sebagian kecil
adiposit berperan sebagai buffer kuat, yang secara berkala menyerap FFA (asam lemak bebas) dan TG pada periode post prandial. Namun saat adiposit dalam jumlah berlebihan, malah menyebabkan fungsinya tidak bekerja, yang akan
menyebabkan resistensi insulin, hiperlipolisis, dan resisten terhadap efek
anti-lipolitik insulin (Ibrahim, 2010). Adiposit mensekresikan sejumlah faktor yang
memainkan peranan dalam respon imunologi, penyakit vaskular, dan pengaturan
faktor komplemen, yang berperan mengatur metabolisme dan pertumbuhan
adiposit, juga sinyal endokrin untuk mengatur homeostasis energi (Niemelä &
Miettinen, 2008).
Adipokin adalah protein yang disekresikan dari adiposit dan juga disintesa
oleh adiposit. Yang menjadi bagian dari adipokin yang berpengaruh terhadap
homeostasis glukosa antara lain sitokin (TNF , IL-6), adiponektin, resistin, CRP
(Trayhurn & Wood, 2004; Hajer et al., 2008; Ibrahim, 2010). Adiponektin meningkatkan sensitivitas insulin dengan cara menghambat produksi glukosa
hepar (Hajer et al., 2008). Kondisi obesitas menurunkan jumlah adiponektin (Ibrahim, 2010). TNF meningkatkan fosforilasi serine IRS-1 (Insulin Receptor Substrate – 1) dan mengurangi ekspresi GLUT4 (Glucose Transporter – 4) yang membantu terbentuknya resistensi insulin (Saini, 2010). TNF juga menginduksi
lipolisis, mengaktivasi NF- B dan meningkatkan pelepasan asam lemak bebas
(FFA) dari jaringan adiposa (Al-Dahr & Jiffri, 2010). IL-6 menurunkan sinyal
insulin dan merupakan sitokin utama yang mengatur produksi CRP (Trayhurn &
Wood, 2004; Ibrahim, 2010).
b. Resistensi insulin
Resistensi insulin dapat didefinisikan sebagai suatu kondisi berkurangnya respon terhadap kadar insulin sirkulasi yang normal, atau dengan kata lain
berkurangnya respon metabolisme glukosa terhadap insulin (Wolf, 2008).
Peningkatan kadar insulin dengan glukosa plasma normal dapat diindikasikan
sebagai resistensi insulin. Seiring dengan meningkatnya adipositas, khususnya
insulin. Jaringan target menurunkan jumlah reseptor insulin pada permukaan sel
sebagai respon terhadap peningkatan kadar sirkulasi insulin berkepanjangan,
kemungkinan dengan peningkatan degradasi intraselular. Saat kadar insulin
rendah, disisi lain, ikatan reseptor meningkat. Kondisi terkait kadar insulin tinggi
dan menurunnya ikatan insulin-reseptor diantaranya termasuk obesitas, konsumsi
tinggi karbohidrat, dan insulinisasi eksogen berlebih yang berkepanjangan.
(Gardner & Shoback, 2007).
Etiologi resistensi insulin telah dipelajari secara khusus, dan telah diketahui
bahwa inflamasi jaringan kronik merupakan penyebab utama resistensi insulin
yang diinduksi oleh obesitas. Salah satu bukti utama hubungan tersebut berasal
dari pengamatan tanpa sengaja bahwa TNF- , sebuah sitokin yang berhubungan
dengan kaheksia pada kanker, ternyata meningkat dalam jaringan adiposa obesitas
pada rodensia dan hambatan terhadap sitokin ini memperbaiki toleransi glukosa
dan sensitivitas insulin (Glass & Olefsky, 2012). Resistensi insulin menghalangi
penggunaan glukosa oleh jaringan sensitif-insulin dan meningkatkan keluaran
glukosa hepar; keduanya menyebabkan kondisi hiperglikemia. Pada resistensi
insulin jumlah reseptor insulin dan aktifitas tyrosine-kinase berkurang, namun perubahan ini lebih disebabkan kondisi sekunder dari hiperinsulinemia dan bukan
merupakan kerusakan primer. Karena itu, kerusakan post receptor diyakini berperan predominan pada resistensi insulin. Polimorfisme IRS-1 juga
berhubungan dengan intoleransi glukosa. Saat ini patologi resistensi insulin
berfokus pada kerusakan sinyal PI3K yang mengurangi translokasi GLUT4 ke
Gambar 2.1. Jalur transduksi sinyal insulin di otot polos (Harrison, 2005). FFA sudah lama diketahui memiliki peranan dalam hal menghilangkan
sensitivitas insulin, yang nantinya menyebabkan resistensi insulin dan DM tipe 2
(Bhattacharya et al., 2007; Saini, 2010). FFA dapat mengganggu penggunaan glukosa dalam otot polos, memicu produksi glukosa oleh hepar, dan merusak
fungsi sel beta pankreas (Harrison, 2005). FFA yang meningkat didalam plasma
berasal dari lipolisis TG didalam jaringan adiposa ataupun sebagai akibat dari
kerja lipoprotein lipase selama penyimpanan TG plasma kedalam jaringan
(Murray et al., 2006). Telah dipostulasikan bahwa peningkatan metabolit asam lemak dalam konsentrasi intraselular mengaktifkan kaskade serine-kinase, yang menyebabkan defek pada sinyal reseptor insulin. Sebagai tambahan, rangkaian
adipokin kompleks, dilepaskan dari jaringan adiposa mengubah respon jaringan
terhadap insulin. Dari banyaknya molekul yang terlibat dalam proses sinyal
intraseslular oleh insulin, reseptor insulin substrat-2 (IRS-2), protein kinase B
(Akt) dan faktor transkripsi forkhead Foxo 1a merupakan molekul yang menarik perhatian, sebagaimana data terkini memberikan bukti kuat bahwa disfungsi
Meningkatnya serum trigliserida menyebabkan akumulasi DAG intrasel di
otot dan hepar. DAG aktivator kuat protein kinase C, khususnya protein kinase-theta di otot dan protein kinasae-epsilon di hepar. Aktifnya protein kinase ini mengawali kaskade fosforilasi serine/threonine yang memfosforilasi insulin receptor substrate-1 (IRS-1), menghambat fosforilasi tirosin IRS-1 dan mengaktifkan PI3K (phosphatidyl inositol-3-kinase), dan sebagai akibatnya, mengurangi fosforilasi dan aktivasi Akt2. Menurunnya aktivitas Akt2
mempengaruhi translokasi GLUT4 dan menyebabkan menurunnya ambilan
glukosa ke dalam sel otot dan, karenanya, oksidasi glukosa dan sintesis glikogen
berkurang. Di hepar, berkurangnya aktivitas Akt2 menurunkan sintesis glikogen
hepar dan meningkatkan glukoneogenesis. Hasil akhirnya merupakan tanda khas
resistensi insulin: berkurangnya oksidasi glukosa dan sintesis glikogen pada otot
rangka dan berkurangnya sintesis glikogen dan lebih berkurang lagi
glukoneogenesis di hepar (Wolf, 2008). Sel pankreas mengkompensasi
resistensi insulin dengan meningkatkan sekresi insulin. Kegagalan sel dan DM
yang merupakan lanjutan dari kompensasi sel dapat menyebabkan ekspansi
massa sel in-adekuat atau kegagalan massa sel yang ada untuk memberi
respon terhadap glukosa. Berkurangnya massa sel pada mencit diabetes dengan
resistensi insulin bisa disebabkan kerusakan pada perkembangan siklus sel
(Kasuga, 2006).
c. Reactive Oxygen Species (ROS)
Pada sebuah penelitian DM pada hewan coba, ditemukan perubahan genetik
pada tikus yang DM (fragmentasi DNA, hilangnya sejumlah pasangan basa DNA
disebabkan oleh adanya kondisi hiperglikemia, yang pada sejumlah penelitian
ternyata merupakan faktor utama yang memicu produksi berlebih ROS. ROS
menyerang membran sel, nukleus dan materi genetik lainnya menyebabkan
modifikasi DNA dan protein (Ghaly et al., 2011). Pada kondisi diabetes, hiperglikemia menghasilkan ROS yang menyebabkan penurunan ekspresi dan
sekresi gen insulin yang pada akhirnya menyebabkan apoptosis. Pada kondisi
diabetes, ROS terinduksi dan terlibat dalam toksisitas glukosa sel . Karena hal
tersebut, tampaknya ROS terlibat dalam perburukan sel pankreas yang
ditemukan pada DM tipe2 (Kaneto et al., 2010). Meningkatnya glukosa (hiperglikemia) menyebabkan peningkatan produksi oxidative stress dari ROS di mitokondria, glikasi non-enzimatik protein dan auto-oksidasi glukosa.
Meningkatnya FFA dapat menyebabkan peningkatan produksi ROS karena
peningkatan pemisahan mitokondria dan oksidasi- . Hiperglikemia dan FFA
menginduksi oxidative stress menyebabkan aktivasi jalur sinyal sensitif-stres. Hal ini memperburuk sekresi dan aksi insulin, memperjelas DM tipe 2 (Evans, 2002).
Sumber ROS
Ada banyak sumber potensial ROS didalam sel. Satu penghasil penting
oksidan intraselular adalah sekelompok enzim yang terikat membran yang
bergantung pada NADPH untuk bisa aktif (Finkel, 2011). Perkembangan DM
yang diciri-cirikan dengan tingginya kadar glukosa serum, molekul pro-oksidan
bisa menjadi asal produksi berlebihan dari ROS. Tingginya KGD dapat memicu
produksi superoksida dan hidrogen peroksida, prekursor radikal bebas reaktif,
yang mampu merangsang penurunan sistem antioksidan, secara langsung merusak
Sumber penting utama ROS pada kondisi hiperglikemia adalah rantai transpor
elektron mitokondria dan NADPH oksidase (Son, 2012; Fernández-Mejía, 2013).
Peranan ROS pada disfungsi sel pankreas
Pada kondisi DM, hiperglikemia dan produksi ROS menurunkan sekresi dan
ekspresi gen insulin yang pada akhirnya menyebabkan apoptosis. ROS terlibat
dalam proses degradasi sel . Juga telah diketahui lipotoksisitas terlibat dalam
degradasi sel karena terpapar dengan FFA, ROS terinduksi, yang menyebabkan
pengurangan sekresi insulin dan disfungsi sel . FFA memperantarai induksi
iNOS dan NO berlebih yang terlibat dalam kerusakan sel . Karena NO
intraseluler merupakan mediator penting apoptosis sel , ada kemungkinan bahwa
hilangnya sel pada DM tipe 2 disebabkan oleh apoptosis yang diinduksi oleh
NO (Kaneto et al,. 2010).
2.1.7. Pencegahan dan Pengobatan Diabetes Melitus tipe 2
Telah dijelaskan sebelumnya, mengkonsumsi makanan tinggi lemak ternyata
berhubungan dengan meningkatnya resiko DM tipe 2 (Marshall & Bessesen,
2002). Jadi, meskipun DM tipe 2 sangat dipengaruhi olah gaya hidup dan
kerentanan gen, komposisi makanan bisa mempengaruhi perkembangan dan
komplikasi DM tipe 2 ini. Asam lemak mempengaruhi metabolisme glukosa
dengan merubah fungsi membran sel, aktivitas enzim, sinyal insulin dan ekspresi
gen (Risérus et al., 2009).
Kebanyakan intervensi yang ditargetkan pada pencegahan DM tipe 2
bertujuan untuk mencapai dan mempertahankan berat badan yang sehat melalui
kombinasi ukuran diet dan aktivitas fisik pada individu yang sudah memiliki
toleransi glukosa terganggu, khususnya kelompok dengan resiko tinggi.
Rekomendasi diet pada berbagai macam studi cukup mirip, dengan menekankan
pada pengurangan asupan lemak dan peningkatan konsumsi sayuran dengan
pengurangan kalori sekedarnya pada populasi obesitas (Klein et al., 2005; Alberti
et al., 2007). Pengaturan pola makan yang dilakukan bersamaan dengan aktivitas fisik, memainkan peranan dalam pencegahan DM tipe 2. Anjuran pengaturan pola
makan untuk mengurangi kelebihan berat badan dan obesitas merupakan
komponen penting dalam pencegahan diabetes. Aktivitas fisik berkala untuk
meningkatkan pengeluaran energi harian memainkan peranan penting dalam
mempertahankan atau mengurangi berat badan dan memperbaiki resistensi insulin
(Wyness, 2009).
komplikasi mikrovaskular dan neuropati jangka panjang sembari menghindari
kejadian hipoglikemik yang parah (Ismail-Beigi, 2012; Barag, 2011).
Mempertahankan kadar glikemik sebisa mungkin pada rentang non-diabetik
memperlihatkan efek yang sangat bermanfaat dalam mengurangi komplikasi
mikrovaskular pada DM tipe 2 (Nathan et al., 2009). Tujuan manajemen gula darah umumnya dinilai dengan menggunakan kadar HbA1c sebagai indeks (Kim
et al., 2012). Target yang direkomendasikan oleh American Diabetes Association
secara umum adalah kadar HbA1c dibawah 7%. Sementara menurut International
Diabetes Federation target kadar HbA1c adalah kurang dari 6,5% (Nathan et al., 2009). Data United Kingdom Prospective Diabetes Study (UKPDS), yang memusatkan studi pada DM tipe 2, telah membuktikan bahwa manajemen gula
darah yang ketat berhasil menurunkan kadar HbA1c sebesar 1% dan mampu
mengurangi terjadinya komplikasi mikrovaskular sebesar 37%. Karenanya,
manajemen gula darah ketat penting untuk menurunkan angka kejadian dan
memperlambat berkembangnya komplikasi terkait diabetes (Kim et al., 2012) a. Diet & Olahraga
Pada kebanyakan pasien DM tipe 2, pengaturan pola nutrisi dan olahraga
merupakan kunci atau satu-satunya intervensi terapeutik yang dibutuhkan untuk
mengembalikan kontrol metabolik (Goldman & Bennet, 2000). Pola nutrisi yang
seimbang merupakan unsur dasar pada terapi diabetes. Setengah dari pasien
diabetes gagal mengatur pola makannya. Pada pasien DM tipe 2 membatasi
asupan karbohidrat dan mengganti sejumlah kalori dengan lemak tidak jenuh
obesitas dan DM tipe 2, mengurangi berat badan dengan restriksi kalori
merupakan tujuan penting pengaturan makanan (Gardner & Shoback, 2007).
Olahraga memiliki sejumlah keuntungan positif termasuk mengurangi resiko
kardiovaskular (Goldman & Bennet, 2000; Harrison, 2005), mengurangi tekanan
darah, mempertahankan massa otot, mengurangi lemak tubuh, dan menurunkan
berat badan (Harrison, 2005). Olahraga yang teratur pada DM tipe 2 menurunkan
kadar VLDL dan meningkatkan kadar HDL dan aktivitas fibrinolitik pada DM
tipe 2 (Goldman & Bennet, 2000).
b. Obat Anti Diabetes Oral
Sejumlah kelas obat tersedia untuk pengobatan DM tipe 2. Obat-obatan ini
umumnya efektif pada pasien yang diet dan olahraganya gagal mencapai tujuan
pengobatan (Goldman & Bennet, 2000). Klasifikasi obat tersebut adalah sebagai
berikut (Gardner & Shoback, 2007):
1. Obat yang bekerja pada kompleks reseptor sulfonilurea, antara lain:
sulfonylurea (glibenclamid dan glydiazinamide), analog meglitinide
(rapiglinide dan mitiglinide), derivat -phenylalanine (nateglinide)
2. Obat yang bekerja pada jaringan target insulin antara lain: metformin, agonis
peroxisome proliferator-activated receptor (rosiglitazone dan pioglitazone) 3. Obat yang mempengaruhi penyerapan glukosa, yaitu penghambat
-glukosidase (acarbose dan miglitol)
4. Incretin, antara lain agonis reseptor GLP-1 (exanetide dan liraglutide),
Gambar 2.3. Tempat kerja obat oral yang diindikasikan. Tanda (-) menunjukkan hambatan dan tanda (+) menunjukkan stimulasi (Defronzo 1999).
c. Terapi Insulin
Insulin diindikasikan pada pasien DM tipe 1 juga pasien DM tipe 2 yang
kondisi hiperglikemianya tidak berespon terhadap diet, olahraga dan obat anti
diabetes oral (Gardner & Shoback, 2007). Insulin tidak boleh digunakan sebagai
terapi lini pertama pada pasien tidak patuh yang enggan memonitor KGD-nya
ataupun pada pasien yang beresiko tinggi terjadi hipoglikemia (Goldman &
Bennet, 2000).
2.2 Pankreas 2.2.1 Anatomi
Pankreas merupakan kelenjar aksesoris pencernaan yang memanjang, terletak
retroperitoneal dan secara transversal melewati dinding belakang abdomen,
posterior dari gaster, terletak antara duodenum, di kanan, dan lien, di kiri.
Pankreas menghasilkan sekresi eksokrin yang memasuki duodenum, dan sekresi
endokrin yang masuk kedalam darah (Moore & Agur, 2007). Pankreas dibagi
terluas dari kelenjar ini dilingkupi oleh kurva C duodenum. Bagian inferior dari
caput pankreas, processus uncinatus, meluas dari posterior ke superior vena
mesenterica superior. Collum pankreas terletak di anterior dari arteri dan vena
mesenterica superior, di bagian posterior dari collum pankreas vena mesenterica superior dan vena lienalis menyatu untuk membentuk vena porta. Corpus
pankreas merupakan sambungan dari collum dan terletak di sebelah kiri dari vena dan arteri mesenterica superior. Sementara cauda pankreas sangat dekat dengan
hilum lienalis dan flexura colica sinistra. Cauda ini relatif mobile dan lewat diantara lapisan ligamentum splenorenal dan arteri-vena lienalis. (Drake et al., 2007; Moore & Agur 2007).
Gambar 2.4. Posisi Anatomis Pankreas (Drake et al., 2007)
Pankreas secara makroskopis berlobus-lobus dan berada dalam pembungkus
yang tipis; lobus pankreas ini terdiri dari alveoli sel sekretori serosa yang
inilah terdapat pulau Langerhans yang mensekresikan insulin. Ductus pancreaticus mayor (Wirsung) berjalan di sepanjang kelenjar ini dan biasanya bermuara ke ampula Vater bersama dengan ductus biliaris communis; kadang terpisah. Ductus pancreaticus accesorius (Santorini) berjalan di bagian bawah
caput pankreas didepan ductus pancreaticus mayor, saling berhubungan dan kemudian bermuara ke duodenum di bagian atas ampula Vater. Kadang-kadang
ductus pancreaticus accesorius ini tidak ada (Ellis, 2006).
Gambar 2.5. Ductulus pankreas dan muaranya (Drake et al., 2007) 2.2.2 Histologi
Sekelompok sel endokrin ditemukan di lautan sel eksokrin pankreas.
Merupakan sekelompok epitel bervaskular, yang disebut dengan pulau
Langerhans; pertama kali ditemukan oleh Paul Langerhans, 1847-1888. Sel
eksokrin pankreas dan sel pulau Langerhans memiliki struktur yang berbeda dan
diwarnai berbeda (Kuehnel, 2003). Bagian endokrin pankreas terdiri atas 1-2 juta
pulau Langerhans. Pulau Langerhans yang berbentuk bulat atau oval berisi sel-sel
hormon kedalam darah (Kuehnel, 2003). Hormon penting disekresikan dari pulau
Langerhans, insulin oleh sel , glukagon oleh sel dan somatostatin oleh sel
(Faller et al., 2004).
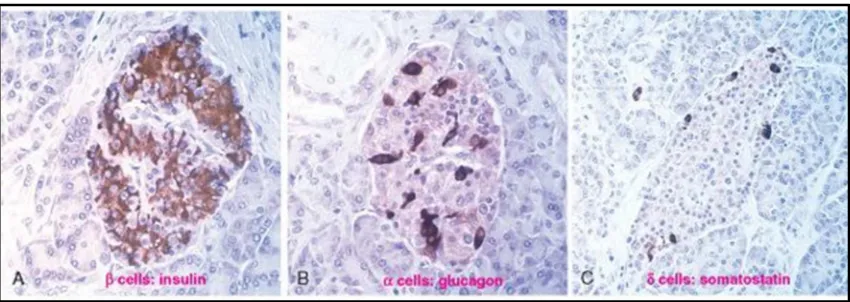
Gambar 2.6. Sel , sel dan sel pada pewarnaan imunoperoksidase (Kumar et al., 2010)
2.2.3 Insulin
Insulin sendiri didefinisikan sebagai hormon peptida yang disekresikan oleh
sel dari pulau Langerhans pankreas dan mempertahankan kadar gula darah
normal dengan cara memudahkan penyimpanan glukosa seluler, pengaturan
metabolisme karbohidrat, lemak dan protein dan mendukung pembelahan dan
pertumbuhan sel melalui efek mitogeniknya. Pelepasan insulin dipicu oleh
peningkatan kadar glukosa didalam darah (Wilcox, 2005). Insulin pertama kali
diisolasi dari pankreas pada tahun 1922 oleh Banting dan Best. Dalam sejarahnya,
insulin telah dihubungkan dengan gula darah, insulin memiliki efek yang sangat
besar pada metabolisme karbohidrat. Insulin memiliki pengaruh terhadap
metabolisme protein dan lemak hampir sama besarnya dengan pengaruh insulin
terhadap metabolisme karbohidrat itu sendiri. Insulin merupakan protein yang
satu sama lain oleh jembatan disulfida. Jika kedua rantai asam amino terpisah,
aktivitas fungsional molekul insulin hilang (Guyton & Hall, 2006).
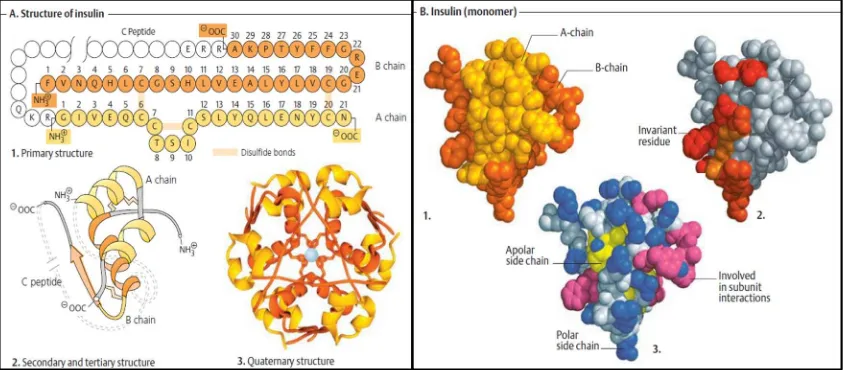
Gambar 2.7. A. Struktur insulin; B. Insulin 3 Dimensi (Koolman & Röhm, 2005)
2.3 Streptozotocin (STZ)
Streptozotocin (STZ) adalah agen antimikroba yang berasal dari
mikroorganisme Streptomyces achromogenes. STZ telah digunakan sebagai agen alkilasi kemoterapi untuk pengobatan tumor sel pulau Langerhans metastasis dan
untuk pengobatan keganasan lainnya. Pada tahun 1963 Rakieten melaporkan
bahwa STZ merupakan diabetogenik. Sejak itu STZ telah digunakan sebagai zat
penginduksi DM di laboratorium hewan (Lenzen, 2007). Pada pemberian STZ,
tanda-tanda DM terjadi seperti meningkatnya asupan makanan dan air, berat
badan tidak bertambah, dan meningkatnya KGD. Pada hewan coba juga
ditemukan adanya disfungsi cardiac diastole, katarak dan neuropati, namun tidak ditemukan adanya aterosklerosis dan tikus tetap normotensif (Wei et al., 2003). Pemberian STZ juga memperlihatkan terjadinya pengurangan protein GLUT2
Pengurangan GLUT2 tergantung dosis dan rentang waktu pemberian (Z. Wang &
Gleichmann, 1998). Pada pengamatan mikroskopis mencit yang diinduksi dengan
STZ terlihat abnormalitas pankreas secara histomorfologi (Tian et al., 2010). Dimana pulau Langerhans berbentuk tidak teratur, terdapat perubahan nekrotik
pada sel endokrin pulau Langerhans, berkurangnya area sel beta (Smirnov et al., 2012) dan juga amiloidosis pulau Langerhans pankreas juga diamati. Jumlah sel
endokrin pankreas berkurang. Infiltrat limfositik interstisial yang terlokalisasi juga
diamati pada perifer pulau Langerhans mencit yang DM (Tian et al., 2010). Pada penelitian lain yang membuktikan efek STZ terhadap parameter biokimia
memperlihatkan terjadinya peningkatan KGD, AST dan ALT secara signifikan
(Ragbetli & Ebubekir, 2010). Pada penelitian yang menggunakan kombinasi STZ
dan nikotinamid memperlihatkan perubahan histopatologi yang ditandai dengan
hilangnya sejumlah sel pankreas dari jaringan hewan coba yang diberi STZ
tunggal, sementara pemberian STZ yang dikombinasi dengan nikotinamid,
kerusakan morfologinya dapat dicegah, menunjukkan efek protektif nikotinamid
terhadap sel pankreas. Pada uji protein yang terkait dengan sinyal insulin
memperlihatkan ekspresi IRS-1, IRS-2 dan PI3K di hepar hewan coba yang diberi
STZ tunggal terlihat penurunan hingga 10–40% (Nakamura et al., 2006). Sebuah penelitian lain menggunakan high fat diet (HFD) bersama dengan STZ dosis rendah menginduksi kadar ekspresi gen yang terlibat dalam metabolisme energi
pada pengaturan metabolisme utama jaringan (H. J. Wang et al., 2007). Pada penelitian lain yang menggunakan kombinasi HFD/STZ menilai kadar
pada kelompok yang mendapat ekstrak bawang kupas dibandingkan dengan
kelompok yang mendapat HFD/STZ (Jung et al., 2011). 2.4 Jamur Tiram Putih (Pleurotus ostreatus)
Sebagai salah satu sumber hayati, jamur (mushroom) diketahui hidup liar di alam. Selama ini jamur banyak dimanfaatkan sebagai bahan pangan, selain juga
ada yang memanfaatkannya untuk obat. Selain dikonsumsi, ada banyak jenis
jamur yang diketahui berkhasiat obat, terutama di negara Cina dan Jepang. Dalam
ramuan tradisional Cina dapat ditemukan jamur Cordyceps sinensis, Ganoderma aplanatum, atau Ganoderma lucidum (Gunawan, 2008). Beberapa jamur banyak digunakan sebagai obat karena memiliki efek antitumor, anti jamur dan
antikolesterol (Chirinang & Intarapichet, 2009).
Jamur, secara alami tumbuh di alam (Bhatti et al., 2007; Iwalokun & Usen, 2007). Jamur tiram putih (Pleurotus ostreatus) merupakan salah dari sekian banyak jamur yang mudah dipanen. Jamur ini juga mudah untuk tumbuh di
sejumlah media yang berbeda (Abrefah et al. 2011). Pleurotus ostreatus memiliki khasiat anti-hiperkolesterolemik (Alam et al., 2011; Schneider et al., 2011),
anti-aging (Jayakumar et al., 2010), anti katarak (Isai et al., 2009), anti hipertensi (Choudhury & Rahman, 2013), anti hiperglikemi (Krishna et al., 2009; Choudhury & Rahman, 2013) dan antioksidan (Jayakumar et al., 2006; Alam et al., 2010; Vamanu et al., 2011; Kim et al., 2009). Dalam sebuah penelitian DM yang menggunakan hewan coba, ekstrak PO ternyata mampu meregenerasi sel-sel
pulau Langerhans yang ditandai dengan meningkatnya jumlah pulau Langerhans
dan juga meningkatnya berat pankreas setelah pemberian ekstrak PO (Ikrimah &
2.4.1 Efek Hipoglikemik Jamur Tiram Putih (Pleurotus ostreatus)
Pleurotus ostreatus (PO) memiliki efek hipoglikemik (Krishna et al., 2009). PO meningkatkan glikogen hepar yang mungkin disebabkan oleh peningkatan laju
glikogenesis (Choudhury & Rahman, 2013). Polisakarida yang diekstraksi dari
badan buah Pleurotus spp memiliki efek peningkatan glutathion peroxidase yang memiliki efek anti-hiperglikemi (Patel et al., 2012). Pada sebuah penelitian DM menggunakan tikus, pemberian ekstrak PO menyebabkan berkurangnya
perubahan genetik (fragmentasi DNA, hilangnya sejumlah pasangan basa dari
fragmen DNA dan kelainan kromosom). Hal ini mungkin disebabkan oleh
berkurangnya kondisi hiperglikemia dengan pemberian PO sehingga secara
bertahap mengurangi potensi pembentukan ROS dan memungkinkan perbaikan
bagi kelainan genetik (fragmentasi DNA, hilangnya sejumlah pasangan basa dari
fragmen DNA dan kelainan kromosom) (Ghaly et al., 2011)..
2.4.2 Efek Antioksidan Jamur Tiram Putih (Pleurotus ostreatus)
Kerusakan oksidatif yang disebabkan oleh radikal bebas bisa saja berhubungan
dengan aging dan penyakit, seperti aterosklerosis, diabetes, kanker, dan sirosis. Meskipun seluruh organisme memperlihatkan sistem pertahanan dan perbaikan
antioksidan yang terlibat dalam perlindungan diri melawan kerusakan oksidatif,
sistem ini tidak cukup untuk mencegah kerusakan secara keseluruhan. Namun,
suplemen antioksidan ataupun makanan yang mengandung antioksidan bisa
membantu tubuh manusia mengurangi kerusakan oksidatif (Alam et al., 2010). Berdasarkan hasil penelitian Chirinang 2009, PO memiliki kandungan serat
45,5% dan lipid < 1%. Senyawa polifenol merupakan senyawa antioksidan utama
2009). PO juga memiliki kemampuan untuk menangkal radikal bebas yang diuji
dengan DPPH (diphenyl-picrylhydralazyl) (Chirinang & Intarapichet, 2009). Kemampuan menangkal radikal bebas PO jauh lebih tinggi dibandingkan dengan
spesies Pleurotus lain dan juga dibandingkan dengan antioksidan lainnya (Neldawati, 2006; Neelam & Singh, 2013), semisal -tocoferol (Neelam & Singh,
2013).
Konsentrasi senyawa polifenol paling banyak yang terdapat dalam PO adalah
protocatechuic acid (PCA) (Alam et al., 2010; Reis et al., 2012), diikuti oleh
gallic acid dan chlorogenic acid (CGA). Senyawa polifenol sebagai antioksidan menghambat aktivitas penangkalan-radikal bebas secara luas sebagai donor
hidrogen atau sebagai alat donor-elektron, juga sebagai pengikat ion logam. Gallic acid merupakan merupakan penghambat aktivitas tirosinase yang efektif (Alam et al., 2010). Uji penangkalan aktivitas DPPH oleh protocatechuic acid (PCA) memperlihatkan efek antioksidan dengan cara mendonorkan atom hidrogen untuk
membentuk molekul DPPH-H yang stabil. Pada uji aktivitas penangkalan radikal
hidroksil (OH) dan anion superoksida (O2-), PCA menghambat pembentukan
kedua radikal bebas yang paling penting didalam sel hidup, dimana kedua radikal
bebas ini meningkat seiring dengan proses metabolisme dalam tubuh (Li et al., 2011). PCA juga menghambat jalur sinyal Akt/NF- B/PKC (Lin et al., 2011), dimana jalur tersebut terlibat dalam mekanisme molekuler resistensi insulin
(Saini, 2010). Sebuah studi memperlihatkan efek CGA dalam menurunkan kadar
gula darah puasa hewan coba, dan merangsang trasnpor glukosa kedalam otot dan