AKIBAT PROSES PENGOLAHAN
YUNITA PUSPA DEWI
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
YUNITA PUSPA DEWI. C34080035. Perubahan Kandungan Asam Lemak dan Kolesterol Keong Mas (Pomacea Canaliculata) Akibat Proses Pengolahan. Dibimbing oleh SRI PURWANINGSIH dan ELLA SALAMAH.
Keong mas (Pomacea canaliculata) merupakan moluska air tawar yang belum dimanfaatkan secara optimal. Keong mas banyak dimanfaatkan sebagai pakan dan terbatas dimanfaatkan sebagai bahan pangan, padahal keong mas memiliki kandungan gizi yang cukup bagus, antara lain mineral, protein, dan asam lemak tak jenuh. Pemanfaatan keong mas sebagai bahan pangan oleh masyarakat kebanyakan hanya menggunakan metode perebusan. Proses pengolahan dengan panas akan mempengaruhi komposisi kimia keong mas, sehingga perlu dilakukan penelitian untuk mengetahui pengaruh metode pengolahan terhadap kandungan gizi (meliputi kandungan proksimat, asam lemak, dan kolesterol) keong mas.
Tujuan penelitian ini adalah menentukan rendemen keong mas, menganalisis komposisi kimia daging keong mas segar dan setelah proses pengolahan, menganalisis pengaruh pengolahan terhadap kandungan asam lemak dan kolesterol keong mas, serta menentukan metode pengolahan terbaik untuk mendapatkan kandungan asam lemak tertinggi dan kandungan kolesterol terendah.
Penelitian ini diawali dengan identifikasi keong mas, penentuan morfometrik, serta penentuan rendemen cangkang, jeroan, dan daging keong mas. Penelitian pendahuluan dilakukan untuk menentukan waktu pengolahan dan konsentrasi garam. Penelitian ini menerapkan uji hedonik parameter rasa untuk menentukan konsentrasi garam terbaik. Penelitian utama dilakukan untuk mengetahui komposisi proksimat, asam lemak, dan kolesterol daging keong mas segar, rebus, rebus dalam air garam terpilih (konsentrasi 2,5 %), dan daging keong kukus. Rancangan percobaan yang digunakan adalah Kruskal Wallis dan Multiple Comparison untuk uji hedonik, serta uji kenormalan data Anderson Darling, Rancangan Acak Lengkap, dan uji lanjut Duncan untuk uji analisis kimia.
YUNITA PUSPA DEWI C34080035
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar sarjana Perikanan pada Departemen Teknologi Hasil Perairan
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
Nama Mahasiswa : Yunita Puspa Dewi Nomor Pokok : C34080035
Program Studi : Teknologi Hasil Perairan
Menyetujui
Pembimbing I Pembimbing II
Dr. Ir. Sri Purwaningsih, M.Si Dra. Ella Salamah, M.Si NIP. 1965 0713 1990 02 2 001 NIP.1953 0629 1988 03 2 001
Mengetahui
Ketua Departemen Teknologi Hasil Perairan.
Dr. Ir. Ruddy Suwandi, MS, M.Phil NIP. 1958 0511 1985 03 1 002
Dengan ini saya menyatakan bahwa skripsi dengan judul “Perubahan Kandungan Asam Lemak dan Kolesterol Keong Mas (Pomacea canaliculata) Akibat Proses Pengolahan” adalah benar karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Bogor, Mei 2012
Yunita Puspa Dewi
NRP. C34080035
Puji syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa, atas anugerahNya sehingga penulis dapat menyelesaikan skripsi dengan cukup baik dan lancar. Skripsi ini disusun sebagai salah satu syarat untuk mendapatkan Gelar
Sarjana di Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Skripsi hasil penelitian ini berjudul “Perubahan Kandungan Asam Lemak dan Kolesterol Keong Mas (Pomacea canaliculata) Akibat Proses Pengolahan”.
Penulisan skripsi ini tidak lepas dari bimbingan, dukungan, dan bantuan dari berbagai pihak. Penulis sangat berterima kasih pada:
1. Dr. Ir. Sri Purwaningsih, M.Si dan Dra. Ella Salamah, M.Si sebagai Dosen Pembimbing yang telah membimbing dan memberikan arahan dengan penuh kesabaran.
2. Dr. Ir. Agoes Mardiono Jacoeb Dipl.Biol, sebagai Dosen Penguji atas saran yang telah diberikan.
3. Dr. Ir. Ruddy Suwandi, M.S, M.Phil sebagai Ketua Departemen Teknologi Hasil Perairan.
4. Ibu Ivana Nervosa Inasesybelly, Bapak Mardi Santoso, Andy Loran Kassandra, dan Dinar Winia Mahandhira atas perhatian dan dukungannya. 5. Rhesa Agung Maulana atas saran, semangat, dan bantuannya.
6. Ramli Baharman, Regina Agustin, Syinta Melani Suherman, Dinial Lavi, Roy Rimansyah, M. Ferry, Ellis Permatasari, Zara Tahira Insanabella, dan M. Andi Rahman atas kebersamaan dan semangat yang diberikan.
7. Teman-teman THP 45 atas kenangan indah yang telah terukir.
8. Kakak-kakak kelas THP 44, 43, dan 42 atas saran yang sangat membantu. Penulis menyadari penulisan skrpsi ini masih belum sempurna. Penulis sangat terbuka atas saran maupun kritik yang membangun. Semoga skripsi ini dapat bermanfaat bagi semua pihak yang memerlukan.
Bogor, Mei 2012
Penulis dilahirkan di Jember pada tanggal 21 Juni 1990 sebagai anak kedua dari tiga bersaudara pasangan Bapak Mardi Santoso dan Ibu Ivana Nervosa Inasesibelly. Pendidikan formal terakhir yang dijalani penulis yaitu di SMAN 1 Jember dan lulus tahun 2008. Penulis melanjutkan pendidikan di Institut Pertanian Bogor melalui jalur USMI pada tahun yang sama.
Penulis aktif di beberapa organisasi kemahasiswaan, antara lain Koran Kampus IPB, Klub Cinta Lingkungan, IPB Debatting Community, dan Himpunan Mahasiswa Hasil Perikanan (HIMASILKAN) Divisi Kewirausahaan. Penulis membuat karya tulis PKM Penelitian dan berhasil didanai oleh DIKTI pada tahun 2012. Penulis juga terlibat dalam beberapa kegiatan asistensi maupun praktikum, antara lain Asisten Sosiologi Umum 2010/2011, Asisten Luar Biasa Ekologi Hasil Perairan 2010/2011, Asisten Metodologi Statistika 2010/2011, Asisten Praktikum Biokimia Hasil Perairan 2010/2011, Asisten Praktikum Penanganan dan Transportasi Biota Perairan 2011/2012, Asisten Praktikum Fisiologi, Formasi, dan Degradasi Metabolit Hasil Perairan 2011/2012, serta Asisten Praktikum Biotoksikologi Hasil Perairan 2011/2012.
Halaman
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
1 PENDAHULUAN ... 1.1 Latar Belakang ... 1
1.2 Tujuan ... 3
2 TINJAUAN PUSTAKA ... 2.1 Deskripsi dan Klasifikasi Keong Mas (Pomacea canaliculata) ... 4
2.2 Komposisi Kimia Keong Mas (Pomecea canaliculata) ... 5
2.3 Lemak ... 6
2.4 Asam Lemak ... 8
2.5 Kolesterol ... 10
2.6 Pengaruh Pengolahan terhadap Nilai Gizi ... 12
2.7 Kromatografi Gas ... 13
3 METODE PENELITIAN ... 3.1 Waktu dan Tempat Pelaksanaan ... 15
3.2 Bahan dan Alat ... 15
3.3 Tahap Penelitian ... 15
3.4 Pengukuran dan Analisis ... 17
3.4.1 Pengukuran morfometrik dan rendemen keong mas ... 17
3.4.2 Uji hedonik (SNI-01-234-2006) ... 17
3.4.3 Analisis kimia ... 18
3.5 Rancangan Percobaan ... 23
3.5.1 Rancangan percobaan uji hedonik ... 23
3.5.2 Rancangan percobaan analisis kimia ... 24
4 HASIL DAN PEMBAHASAN ... 4.1 Karakteristik Keong Mas ... 27
4.2 Rendemen Keong Mas ... 28
4.3 Penetapan Waktu Pemasakan dan Konsentrasi Garam ... 29
4.4 Komposisi Kimia Keong Mas ... 30
4.4.1 Kadar air ... 31
vii
4.5 Kandungan Asam Lemak Keong Mas ... 37
4.6 Kandungan Kolesterol Keong Mas ... 49
4.7 Penentuan Metode Pengolahan Terbaik ... 51
5 KESIMPULAN DAN SARAN ... 5.1 Kesimpulan ... 53
5.2 Saran ... 53
DAFTAR PUSTAKA ... 54
Nomor Teks Halaman
1 Kandungan mineral keong mas ... 5
2 Komposisi kimia keong mas ... 6
3 Berat dan ukuran keong mas (Pomacea canaliculata) ... 27
4 Hasil analisis proksimat keong mas (Pomacea canaliculata) ... 30
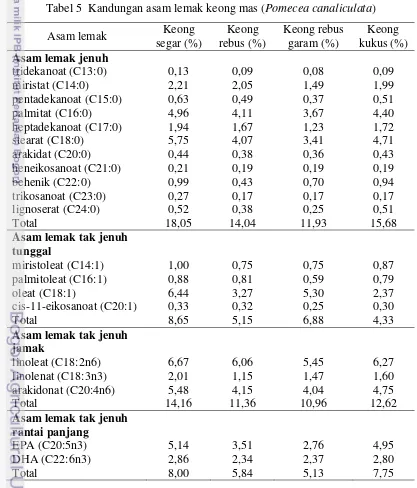
5 Kandungan asam lemak keong mas (Pomecea canaliculata) ... 38
Nomor Teks Halaman
1 Keong mas (Pomacea canaliculata) ... 4
2 Struktur kimia lemak berdasarkan jumlah asam lemak ... 6
3 Skema autooksidasi asam lemak tidak jenuh ... 7
4 Struktur kimia EPA dan DHA ... 9
5 Struktur kimia kolesterol ... 11
6 Diagram alir penelitian ... 16
7 Kromatografi gas dan recorder ... 21
8 Pengukuran morfometrik keong mas ... 27
9 Rendemen keong mas segar ... 28
10 Diagram batang nilai rata-rata parameter rasa keong mas ... 29
11 Diagram batang kadar air keong mas ... 31
12 Diagram batang kadar abu keong mas ... 33
13 Diagram batang kadar protein keong mas ... 35
14 Reaksi hidrolisis protein ... 35
15 Diagram batang kadar lemak keong mas ... 36
16 Diagram batang kandungan asam stearat keong mas ... 39
17 Diagram batang kandungan asam oleat keong mas ... 40
18 Diagram batang kandungan asam linoleat keong mas ... 42
19 Diagram batang kandungan asam linolenat keong mas ... 43
20 Proses pembentukan asam lemak ... 44
21 Diagram batang kandungan asam arakidonat keong mas ... 45
22 Diagram batang kandungan EPA keong mas ... 46
23 Diagram batang kandungan DHA keong mas ... 48
Nomor Halaman
1 Keong mas utuh, cangkang, jeroan, dan daging keong mas ... 61
2 Morfometrik keong mas ... 62
3 Hasil uji hedonik parameter rasa keong mas ... 63
4 Hasil uji Kruskal Wallis parameter rasa keong mas ... 64
5 Hasil uji Multiple Comparisson parameter rasa keong mas ... 64
6 Analisis proksimat daging keong mas ... 64
7 Grafik uji kenormalan galat analisis proksimat keong mas ... 65
8 Analisis ragam kadar air keong mas ... 67
9 Uji Duncan kadar air ... 67
10 Analisis ragam kadar abu keong mas ... 67
11 Uji Duncan kadar abu ... 67
12 Analisis ragam kadar protein keong mas ... 67
13 Uji Duncan kadar protein ... 68
14 Analisis ragam kadar lemak keong mas ... 68
15 Uji Duncan kadar protein ... 68
16 Kromatogram asam lemak standar ... 68
17 Kromatogram asam lemak keong mas segar ... 70
18 Kromatogram asam lemak keong mas rebus ... 73
19 Kromatogram asam lemak keong mas rebus garam ... 76
20 Kromatogram asam lemak keong mas kukus ... 79
21 Contoh perhitungan asam lemak ... 82
22 Grafik uji kenormalan galat analisis asam lemak keong mas ... 83
23 Analisis ragam kandungan asam stearat keong mas ... 86
24 Uji Duncan kandungan asam stearat ... 86
25 Analisis ragam kandungan asam oleat keong mas ... 86
26 Uji Duncan kandungan asam oleat ... 87
27 Analisis ragam kandungan asam linoleat keong mas ... 87
28 Uji Duncan kandungan asam linoleat ... 87
29 Analisis ragam kandungan asam linolenat keong mas ... 87
xi
32 Uji Duncan kandungan asam arakidonat ... 88
33 Analisis ragam kandungan EPA keong mas ... 88
34 Uji Duncan kandungan EPA ... 88
35 Analisis ragam kandungan DHA keong mas ... 88
36 Uji Duncan kandungan DHA ... 89
37 Hasil uji kolesterol keong mas ... 89
38 Kurva standar kolesterol keong mas ... 89
39 Grafik uji kenormalan galat analisis kolesterol keong mas ... 90
40 Analisis ragam kandungan kolesterol keong mas ... 90
1 PENDAHULUAN
1.1 Latar Belakang
Era modern menuntut manusia bekerja lebih cepat, sehingga manusia
kurang memperhatikan kebutuhan gizi tubuh dan kandungan gizi dalam makanan.
Masyarakat era modern cenderung lebih menyukai makanan instan dan makanan
cepat saji (fast food). Jenis makanan tersebut cukup merugikan tubuh manusia, karena mengandung asam lemak jenuh dan kolesterol yang tinggi. Pola hidup
masyarakat tersebut dapat menimbulkan berbagai resiko kesehatan, misanya
jantung koroner, stroke, dan hiperkolesterol.
Asam lemak merupakan asam organik berantai panjang dan mempunyai
gugus karboksil (COOH) di salah satu ujungnya dan gugus metil (CH3) di ujung
lainnya (Almatsier 2006). Asam lemak dibedakan atas asam lemak jenuh dan
asam lemak tak jenuh. Asam lemak jenuh cenderung menimbulkan pengaruh
kurang sehat bagi tubuh, sedangkan asam lemak tak jenuh memiliki beberapa
manfaat bagi kecerdasan otak dan pertumbuhan. Asam lemak tak jenuh yang
paling dikenal masyarakat adalah linoleat (omega-6) dan linolenat (omega-3).
Asam linolenat memiliki turunan yaitu asam eikosapentanoat dan asam
dokosaheksanoat. Asam lemak tak jenuh ini banyak ditemukan pada beberapa
pangan hasil laut (Akoh & Min 2008).
Kolesterol merupakan senyawa golongan steroid dan hanya terdapat dalam
lemak hewan. Kolesterol berperan penting untuk membentuk membran sel dan
komponen sel otak maupun syaraf. Tubuh manusia mengandung kolesterol
sebanyak + 0,2 % dari total berat tubuh. Kolesterol berperan sebagai prekursor
hormon steroid seperti progesteron, testosteron, dan kortisol
(Hames & Hooper 2005). Kelebihan asupan kolesterol dapat mempengaruhi
kesehatan, menimbulkan kegemukan, serta penyakit degeneratif.
Penyakit-penyakit yang disebabkan oleh tingginya kandungan kolesterol dalam darah
tersebut dapat dicegah dengan mengonsumsi pangan rendah kolesterol dan kaya
asam lemak tak jenuh, seperti komoditas perairan yang kaya akan asam lemak tak
perairan yang cukup potensial dimanfaatkan sebagai pangan dan memiliki asam
lemak jenuh dan kolesterol rendah, salah satunya adalah keong.
Keong mas (Pomacea canaliculata) merupakan moluska air tawar yang terdapat di sepanjang Sungai Paraguay dan Parana yang memotong Paraguay,
Brazil, Bolivia dan Argentina. Keong mas pertama kali dikenal sebagai hama
padi di Taiwan sejak tahun 1979, dan kini telah menjadi hama padi paling
berbahaya di negara-negara penyedia beras, antara lain Filipina, Vietnam,
Thailand, dan Indonesia (Joshi 2005). Keong mas telah banyak dimanfaatkan
sebagai sumber pangan dan pakan. Keong mas diberikan sebagai pakan pada
ternak itik, ayam broiler, burung puyuh, budidaya ikan patin, ikan gabus, ikan
sidat, udang, kepiting dan lobster air tawar. Daging keong mas mulai
dimanfaatkan dalam bidang pangan untuk fortifikasi beberapa produk pangan,
misalnya cracker, kerupuk, kecap, hingga sate keong dan pepes keong. Pemanfaatan keong mas saat ini tidak terbatas sebagai bahan pangan dan pakan
saja, tetapi juga sebagai obat untuk penyakit liver (Sulistiono 2010).
Keong mas umumnya diolah dengan metode pengolahan yang
menggunakan panas, antara lain pengukusan dan perebusan. Pengaruh pemanasan
terhadap komponen daging keong mas dapat menyebabkan perubahan fisik dan
kimia keong mas. Beberapa penelitian menunjukkan bahwa proses pemanasan
terhadap produk perikanan dapat mempengaruhi kadar air, kadar protein, dan
kadar lemak dalam ikan. Kandungan asam lemak dan kolesterol dalam keong mas
juga dapat berubah akibat proses pengolahan dengan panas. Pengetahuan tentang
besarnya perubahan komposisi kimia yang terjadi akibat proses pengolahan yakni
perebusan, perebusan dalam air garam, dan pengukusan perlu diketahui untuk
menentukan metode pengolahan yang tepat.
Informasi mengenai kandungan asam lemak, kolesterol, serta pengaruh
berbagai proses pengolahan yaitu dengan perebusan, perebusan dalam air garam,
dan pengukusan pada keong mas masih terbatas. Penelitian ini dilakukan untuk
mengetahui perubahan kandungan gizi keong mas. Dengan mengetahui
perubahan asam lemak dan kolesterol dalam daging keong mas setelah proses
pengolahan yang tepat, sehingga keong mas dapat dijadikan sebagai sumber
pangan alternatif kaya gizi.
1.2 Tujuan
Tujuan umum penelitian ini adalah mengetahui pengaruh metode
pengolahan terhadap kandungan gizi keong mas (Pomacea canaliculata). Adapun tujuan khusus penelitian ini antara lain:
1) menentukan rendemen keong mas
2) menganalisis komposisi kimia (air, protein, abu, dan lemak) daging keong
mas segar dan setelah proses pengolahan
3) menganalisis pengaruh pengolahan (perebusan, perebusan dalam air garam,
dan pengukusan) terhadap kandungan asam lemak dan kolesterol keong mas
2 TINJAUAN PUSTAKA
2.1 Deskripsi dan Klasifikasi Keong Mas (Pomacea canaliculata)
Keong mas (Pomacea canaliculata) adalah siput sawah dengan warna cangkang keemasan yang dianggap sebagai salah satu hama dalam produksi padi.
Keong mas disebut hama karena menjadi pemakan tanaman padi di areal
persawahan dan telurnya yang menempel pada batang padi menyebabkan tanaman
padi mati. Keong mas memiliki karakteristik khusus yang dapat digunakan untuk
membedakan dengan keong-keong jenis lain yang hidup pada habitat yang sama.
Keong mas dewasa memiliki cangkang berwarna coklat dan daging berwarna
putih krem hingga kemerah-merahan. Ukuran tubuhnya bervariasi dan tergantung
pada ketersediaan makanan. Makanan keong mas umumnya berupa tanaman yang
masih muda dan lunak, misalnya bibit padi, sayuran, dan enceng gondok
(Budiyono 2006). Morfologi keong mas disajikan pada Gambar 1.
b a
Gambar 1 Keong mas (Pomacea canaliculata) a) (Afrianty 2010)
b) (Sarwoedi 2009)
Ukuran diameter cangkang keong mas dapat mencapai 4 cm dengan berat
10-20 gram. Keong mas memiliki umbilicus terbuka. Operkulum yang menutupi lubang aperture terbuat dari kitin dan merupakan operkulum tipe konsentris. Keong mas dikategorikan sebagai hewan omnivora. Klasifikasi keong mas
Filum : Moluska
Kelas : Gastropoda
Subkelas : Prosobranchiata
Ordo : Mesogastropoda
Famili : Ampullariidae
Genus : Pomacea
Spesies : Pomacea canaliculata
Keong mas hidup di kolam, sawah beririgasi dan kanal. Keong mas
membenamkan diri pada tanah lembab selama musim kering. Keong mas dapat
bertahan hidup hingga 6 bulan dengan cara menutup operkulum dan
membenamkan diri dalam tanah. Keong mas menjadi aktif kembali ketika tanah
tempat hidupnya tergenang air. Keong mas dapat bertahan hidup pada kondisi
lingkungan yang keras, misalnya pada perairan tercemar atau perairan yang
memiliki kandungan oksigen terlarut rendah, karena keong mas memiliki insang
(ctenidium) dan organ menyerupai paru-paru, sehingga dapat bertahan hidup di dalam dan di luar air (DA-PhilRice 2001).
2.2 Komposisi Kimia Keong Mas (Pomecea canaliculata)
Keong mas cukup potensial sebagai sumber protein hewani. Keong mas
memiliki kandungan gizi lain yakni kalori dan karbohidrat. Keong mas juga
mengandung vitamin dan mineral yang dibutuhkan oleh tubuh. Beberapa mineral
yang ditemukan dalam daging keong mas antara lain kalsium, natrium, kalium,
fosfor, magnesium, seng, dan zat besi. Tabel 1 berikut menunjukkan kandungan
mineral daging keong mas (Pambudi 2011).
Tabel 1 Kandungan mineral keong mas
Komposisi mineral makro Kadar (bk) (mg/100 gr) Komposisi mineral mikro Kadar (bk) (mg/100 gr)
Kalsium 7593,81 Besi 44,16
Natrium 620,84 Seng 20,57
Kalium 824,84 Selenium Tidak terdeteksi
Fosfor 1454,32 Tembaga Tidak terdeteksi
Komposisi kimia keong mas dinyatakan dalam persentase dari unsur-unsur
air, abu, protein, dan lemak. Komposisi kimia bahan baku sangat bervariasi,
tergantung pada ukuran, kelamin, tingkat kematangan seksual, maupun waktu
penangkapan biota. Komposisi kimia daging keong mas disajikan pada Tabel 2.
Tabel 2 Komposisi kimia keong mas
Komposisi kimia Nurjanah et al. (1996) Susanto (2010) Pambudi (2011) Kadar air 84,70 % (bb) 81,19 % (bb) 81,50 % (bb) Kadar protein 9,33 % (bb) 10,30 % (bb) 7,58 % (bk) Kadar lemak 0,91 % (bb) 0,51 % (bb) 2,10 % (bk) Kadar abu 1,43 % (bb) 4,07 % (bb) 9,03 % (bk)
2.3 Lemak
Lemak merupakan senyawa organik yang tidak larut dalam air tetapi dapat
diekstraksi dengan pelarut nonpolar. Senyawa organik ini terdapat dalam semua
sel dan berfungsi sebagai sumber energi, komponen struktur sel, sebagai simpanan
bahan bakar metabolik, sebagai komponen pelindung dinding sel, dan juga
sebagai komponen pelindung kulit vertebrata (Girindra 1987). Lemak juga
berperan sebagai sumber energi dan pelarut vitamin. Babu et al. (2010) menyatakan bahwa lemak menyumbangkan 9,45 kcal/g dan bertindak sebagai
carrier untuk vitamin A, D, E, dan K.
Suatu molekul lemak tersusun dari satu hingga tiga asam lemak dan satu
gliserol. Jumlah asam lemak pada gugus gliserol membuat molekul lemak
diklasifikasikan menjadi monogliserida, digliserida, dan trigliserida. Gambar 2
menunjukkan struktur lemak berdasarkan jumlah asam lemak gugus gliserol.
Lemak pada daging keong mas akan mengalami beberapa perubahan
setelah keong mas mati, salah satunya adalah autooksidasi lemak. Autooksidasi yang terjadi menyebabkan perubahan bau, warna dan tekstur. Ketengikan merupakan indikator utama dari kerusakan lemak dan minyak. Proses oksidasi lemak yang menimbulkan aroma tengik membuat makanan menjadi tidak enak.
Proses autooksidasi lipid melalui tiga tahap reaksi yaitu inisiasi, propagasi
dan terminasi. Inisiasi ditandai dengan terlepasnya atom hidrogen dari molekul
asam lemak (LH) sehingga terbentuk radikal bebas alkil (L-). Tahap propagasi
yaitu saat radikal bebas alkil yang terbentuk pada tahap inisiasi bereaksi dengan
oksigen atmosfer membentuk radikal bebas peroksi (LOO-). Radikal bebas
peroksi yang terbentuk bereaksi dengan atom hidrogen yang terlepas dari asam
lemak tidak jenuh lain membentuk hidroperoksida (LOOH). Antioksidan (AH)
dapat memberikan atom oksigen pada radikal bebas peroksi (LOO-) dan
membentuk radikal lemak yang lebih stabil (LOOH). Turunan radikal antioksidan
(A-) juga bersifat stabil sehingga tidak membentuk radikal yang baru. Tahap
terminasi terjadi saat adanya penggabungan radikal-radikal bebas membentuk
produk non radikal yang stabil (Akoh & Min 2008). Skema autooksidasi asam
lemak tidak jenuh disajikan pada Gambar 3.
Gambar 3 Skema autooksidasi asam lemak tidak jenuh (Sampaio et al. 2006)
senyawa rantai karbon yang lebih pendek berupa beberapa aldehid, keton, alkohol, dan alkana yang mudah menguap dan potensial bersifat toksik (Almatsier 2000). Anand et al. (2010) menambahkan bahwa jumlah lemak di dalam bahan pangan hasil laut sangat rendah namun kaya akan asam lemak tak jenuh majemuk.
Asam lemak tak jenuh mengandung dua atau lebih ikatan rangkap dan sebagian
besar memiliki peranan yang penting bagi tubuh manusia. Oleat, linoleat, dan
linolenat merupakan contoh asam lemak tak jenuh yang juga tergolong sebagai
asam lemak esensial. Asam lemak esensial merupakan asam lemak yang tidak
dapat disintesis oleh tubuh dan harus tersedia dari luar, yaitu berasal dari asupan
makanan. Asam lemak esensial sangat diperlukan tubuh, antara lain untuk
menjaga bagian struktural membran sel dan untuk membuat bahan-bahan hormon.
2.4 Asam Lemak
Asam lemak merupakan senyawa organik polar yang mengandung
4 hingga 24 atom karbon (C) dengan gugus fungsional utamanya adalah gugus
karboksil (-COOH). Setiap atom karbon pada asam lemak akan berikatan dengan
hidrogen atom karbon lainnya. Asam lemak berperan sebagai senyawa penyusun
berbagai lipid, termasuk lipid sederhana, fosfogliserida, glikolipid, stingolipid,
ester kolesterol, hingga lilin. Asam lemak memiliki gugus karboksil tunggal dan
ujung hidrokarbon nonpolar yang panjang, sehingga hampir semua lipid bersifat
tidak larut air dan tampak berminyak atau berlemak (Lehninger 1992).
Rantai karbon pada struktur asam lemak menyebabkan lemak digolongkan
menjadi asam lemak jenuh dan asam lemak tak jenuh. Asam lemak jenuh disusun
oleh rantai atom karbon penyusunnya yang berikatan tunggal, sedangkan asam
lemak tak jenuh mengandung satu atau lebih atom karbon yang berikatan ganda
(Kusnandar 2010). Asam lemak jenuh memiliki titik cair lebih tinggi daripada
asam lemak tak jenuh. Lemak yang tersusun oleh asam lemak jenuh akan
berbentuk padat pada suhu kamar, sedangkan lemak yang tersusun oleh asam
lemak tak jenuh akan bersifat cair (Akoh & Min 2008).
Perbedaan konfigurasi asam lemak disebabkan oleh perbedaan letak ikatan
rangkap dalam struktur kimia asam lemak. Bila ikatan rangkap asam lemak
Sebaliknya asam lemak trans apabila asam lemak memiliki ikatan rangkap di sisi
yang berlawanan. Mahaffey (2004) menyatakan bahwa asam lemak trans dapat
meningkatkan resiko penyakit jantung koroner. Asam lemak tak jenuh jamak
yang ideal adalah asam lemak cis yang berasal dari alam, yakni asam lemak
omega-3 cis yang berasal dari ikan.
Asam lemak esensial sangat diperlukan tubuh, antara lain untuk menjaga
bagian-bagian struktural membran sel dan untuk membuat bahan-bahan hormon
eikosanoid. Eikosanoid berperan untuk membantu tekanan darah, proses
pembekuan darah, dan kadar lemak dalam darah. Asam lemak rantai panjang
omega-3, terutama EPA dan DHA tergolong asam lemak esensial karena tidak
dapat disintesis oleh tubuh, namun dapat diperoleh dari makanan. Asam lemak
omega-3 ini memiliki ikatan rangkap pada atom C ketiga jika dihitung dari gugus
metil. Asam lemak kelompok omega-3 yaitu α-linolenic acid (ALA), docosahexanoic acid (DHA), dan eicosapentanoic acid (EPA). Gambar 4 berikut menunjukkan struktur kimia EPA dan DHA (Akoh & Min 2008).
Gambar 4 Struktur kimia EPA dan DHA (Visentainer et al. 2005)
Eicosapentanoic acid dan docosahexanoic acid merupakan turunan dari asam linolenat. De Castro et al. (2007) menyatakan bahwa tubuh manusia tidak cukup efisien mengubah asam linolenat menjadi EPA dan DHA, sedangkan ikan
dapat mengubah asam linolenat menjadi EPA dan DHA. Ikan kaya akan EPA dan
DHA yang dapat mereduksi timbulnya resiko arterosklerosis. Asam lemak EPA
dan DHA juga dapat mencegah penyakit jantung koroner dan memiliki pengaruh
anti-inflamatori.
pada retina mata, dan pada sperma. Organ-organ tersebut membutuhkan DHA
dalam perkembangannya. Sidhu (2003) mengemukakan bahwa defisiensi dan
kehilangan asam lemak omega-3 ini akan menyebabkan melemahnya daya ingat,
berkurangnya ketajaman penglihatan, dan terganggunya sistem reproduksi.
Kandungan EPA berperan dalam mencegah penyakit degeneratif sejak
janin dan pada saat dewasa, membantu pembentukan sel pembuluh darah, dan
membantu perkembangan jantung selama janin dalam kandungan. Saat dewasa,
EPA berperan dalam mendukung mekanisme pembuluh darah dan kerja jantung,
sehingga kekurangan omega-3 dapat meningkatkan resiko terkena penyakit
jantung (Budiman 2009).
Fungsi asam lemak esensial yang terdapat dalam tubuh sebagai fosfolipid
menurut Muchtadi et al. (1993) adalah sebagai berikut:
1) memelihara integritas dan fungsi membran seluler dan subseluler
2) mengatur metabolisme kolesterol
3) merupakan prekursor dari senyawa yang memiliki fungsi pengatur fisiologis
dalam tubuh
4) dibutuhkan untuk aksi piridoksin (vitamin B6) dan asam pantotenat
5) dibutuhkan untuk pertumbuhan dan perkembangan bayi.
2.5 Kolesterol
Kolesterol merupakan golongan sterol (steroid alkohol) yang paling
dikenal oleh masyarakat. Kolesterol adalah sterol utama pada jaringan hewan.
Kolesterol dan senyawa turunan esternya adalah komponen penting dari plasma
lipoprotein dan dari membran sel sebelah luar (Lehninger 1992).
Kolesterol di dalam tubuh mempunyai fungsi ganda, yaitu di satu sisi
diperlukan dan di sisi lain dapat membahayakan, bergantung berapa banyak
terdapat di dalam tubuh dan di bagian mana. Kolesterol dapat membahayakan
tubuh apabila terdapat dalam jumlah terlalu banyak di dalam darah, sehingga
membentuk endapan pada dinding pembuluh darah dan menyebabkan
penyempitan pembuluh darah (arterosklerosis). Kolesterol diperlukan dalam
pembentukan asam empedu, asam folat, dan progesteron. Kolesterol dalam darah
kolesterol dalam tubuh terjadi dalam hati dengan bahan utama karbohidrat,
protein, dan lemak. Kadar kolesterol yang disintesis tergantung jumlah kebutuhan
dan jumlah kolesterol dari makanan (Achadi 2007). Struktur kimia kolesterol
disajikan pada Gambar 5.
Gambar 5 Struktur kimia kolesterol (Hames & Hooper 2005)
Kolesterol tidak dapat disirkulasikan dalam aliran darah dengan sendirinya
karena kolesterol tidak larut dalam cairan darah, oleh karena itu agar dapat
diedarkan ke seluruh tubuh koleterol dikemas bersama protein menjadi partikel
lipoprotein. Lipoprotein ini dianggap sebagai pembawa kolesterol dalam darah.
Menurut Colpo (2005) ada dua jenis lipoprotein yang membawa kolesterol dalam
darah, yaitu:
1) Low Density Lipoprotein (LDL)
Lipoprotein ini berbahaya karena mengangkut kolesterol paling banyak di
dalam darah. Level LDL yang tinggi menyebabkan pengendapan kolesterol
dalam arteri. Tingginya kadar LDL dalam plasma darah merupakan faktor
resiko utama penyakit jantung koroner.
2) High Density Lipoprotein (HDL)
Lipoprotein ini tidak berbahaya karena mengangkut kolesterol lebih
sedikit dari LDL. High Density Lipoprotein (HDL) dapat membuang kelebihan kolesterol di pembuluh darah arteri dan kembali ke hati untuk diproses atau
dibuang. Lipoprotein berdensitas tinggi ini dapat mencegah kolesterol
mengendap di arteri dan melindungi pembuluh darah dari proses arterosklerosis.
Kolesterol mempunyai peranan penting untuk mengatur fungsi tubuh.
Kolesterol menjalankan 3 fungsi utama, yaitu (Freeman & Junge 2005):
1) kolesterol membentuk selubung luar sel
2) kolesterol membentuk asam empedu yang mencerna makanan di usus
3) kolesterol memungkinkan tubuh membentuk vitamin D dan hormon-hormon
penting dalam tubuh.
2.6 Pengaruh Pengolahan terhadap Nilai Gizi
Pemanasan merupakan suatu perlakuan suhu tinggi yang diberikan pada
suatu bahan pangan yang bertujuan untuk mengurangi populasi mikroorganisme
atau membunuh mikroorganisme dalam bahan pangan. Perlakuan-perlakuan
pemanasan biasanya dikombinasikan dengan perlakuan lainnya untuk mencegah
rekontaminasi oleh mikroorganisme (Tamrin & Prayitno 2008).
Proses pengolahan bahan pangan umumnya akan diikuti oleh kerusakan
lemak yang terkandung dalam bahan pangan. Tingkat kerusakan lemak sangat
bervariasi tergantung suhu yang digunakan serta lamanya waktu proses
pengolahan. Semakin tinggi suhu yang digunakan, maka kerusakan lemak akan
semakin besar. Bahan pangan yang diolah dengan panas juga mengalami
kerusakan kandungan gizi yang lain, seperti protein, mineral, dan vitamin. Hal ini
dikarenakan gizi yang terdapat dalam bahan pangan peka terhadap pH larutan,
oksigen, cahaya, dan panas atau kombinasinya (Harris dan Karmas 1989).
Perebusan adalah cara memasak makanan dalam cairan yang sedang
mendidih (100 oC). Perebusan dipakai dalam pengolahan makanan, sayuran, atau
bahan bertepung. Faktor waktu dan suhu perebusan memegang peranan penting
dalam perubahan kandungan gizi bahan pangan. Semakin tinggi suhu yang
digunakan dan semakin lama waktu perebusan akan menurunkan kandungan gizi
bahan pangan dalam jumlah besar (Widyati 2001).
Pengukusan merupakan proses pemanasan yang sering diterapkan pada
sistem jaringan sebelum pembekuan, pengeringan, atau pengalengan. Pengukusan
sebelum pengeringan terutama bertujuan untuk menginaktifkan enzim yang akan
menyebabkan perubahan warna, cita rasa, atau nilai gizi yang tidak dikehendaki
untuk mengurangi kadar air dalam bahan baku, sehingga tekstur bahan menjadi
kompak.
Pengukusan akan mengurangi zat gizi bahan pangan. Penurunan zat gizi
karena proses pengukusan tergantung dari cara mengukus dan jenis bahan pangan
yang dikukus. Proses pengolahan dengan pengukusan memiliki nilai susut gizi
yang lebih kecil dibandingkan dengan perebusan (Harris & Karmas 1989).
2.7 Kromatografi Gas
Kromatografi gas adalah teknik yang digunakan untuk memisahkan
campuran berdasarkan sifat volatilitas masing-masing komponennya. Pemisahan
ini terjadi karena adanya interaksi antara komponen sampel dengan fase gerak dan
fase diam pada kromatografi gas. Komponen volatil tersebut akan dibawa oleh
fase gerak (carrier) berupa gas yang bersifat inert seperti gas helium dan nitrogen. Fase diam pada kromatografi gas berfungsi untuk mempartisikan komponen yang
dipisahkan berdasarkan interaksinya dengan fase diam. Fase diam pada
kromatografi gas dapat berupa padatan, yang disebut dengan kromatografi gas
padat (Gas Solid Chromatography / GSC) ataupun padatan yang dilapisi dengan cairan, yang disebut dengan Gas Liquid Chromatography (GLC) (Herawati et al. 2011).
Pemisahan sampel dalam campuran pada GLC dilakukan secara partisi di
antara fase gerak dan fase diam. Sampel bergerak dalam kolom dengan kecepatan
yang tergantung pada derajat kelarutan dalam cairan pada fase diam dan volatilitas
dari masing-masing komponen. Komponen yang cenderung larut dalam fase diam
akan tertahan sedangkan komponen yang tidak larut dalam fase diam akan lebih
dahulu bergerak, demikian juga dengan komponen yang cenderung lebih volatil
akan lebih dulu bergerak keluar kolom (Adnan 1997).
Senyawa yang tidak stabil secara termal ataupun tidak mudah menguap,
dapat juga dianalisis dengan kromatografi gas dengan cara mengubahnya menjadi
turunan-turunannya yang lebih mudah menguap dan stabil, misalnya asam lemak
dapat diubah menjadi ester metilik atau metil ester melalui esterifikasi dengan BF3
Keuntungan analisis pangan menggunakan kromatografi gas menurut
McNair & Bonelli (1988) antara lain:
1) Kecepatan
Penggunaan gas sebagai fase gerak mempunyai keuntungan, yaitu cepat
tercapainya kesetimbangan antara fase gerak dan fase diam, dan dapat digunakan
kecepatan-gas-pembawa yang tinggi.
2) Resolusi (daya pisah)
Daya resolusi kromatografi gas sangat tinggi yaitu dapat memisahkan
komponen yang sukar dipisahkan dengan cara lain, walaupun dengan titik didih
yang hampir sama, karena kromatografi gas menggunakan fase cair yang selektif.
3) Analisis kualitatif
Waktu retensi atau waktu tambat adalah waktu sejak penyuntikan sampai
maksimum puncak. Dengan menggunakan aliran yang tepat dan mengendalikan
suhu, waktu tambat tersebut cukup singkat.
4) Kepekaan
Kromatografi gas memiliki kepekaan yang tinggi. Keuntungan tambahan
dari kepekaan yang tinggi ini adalah sampel yang diperlukan hanya sedikit untuk
menganalisis secara lengkap.
5) Kesederhanaan
Kromatografi gas mudah dijalankan dan mudah dipahami. Penafsiran data
3 METODE PENELITIAN
3.1 Waktu dan Tempat Pelaksanaan
Penelitian dilaksanakan pada bulan November 2011 sampai Januari 2012
bertempat di Laboratorium Biokimia Hasil Perairan (preparasi sampel dan analisis
komposisi kimia) dan Laboratorium Preservasi dan Pengolahan Hasil Perairan
(proses perlakuan pengolahan), Departemen Teknologi Hasil Perairan, Fakultas
Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor, Laboratorium Terpadu
Fakultas Peternakan (analisis kolesterol), dan Laboratorium Terpadu Baranang
Siang (analisis asam lemak).
3.2 Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini meliputi keong mas
(Pomacea canaliculata), akuades, HCl, NaOH, katalis selenium, H2SO4, H3BO3, n-heksana, iso-oktan, larutan standar internal asam lemak dan kolesterol, larutan
NaOH 0,5 N dalam metanol, larutan BF3 16%, larutan NaCl jenuh, isooktan,
Na2SO4 anhidrat, etanol, petroleum eter, alkohol, asetat anhidrat, dan kloroform.
Alat-alat yang digunakan pada penelitian ini antara lain meja preparasi,
pisau, timbangan analitik, cawan porselen, oven, desikator, tanur, tabung reaksi,
erlenmeyer, tabung soxhlet, tabung Kjeldahl, destilator, buret, kromatografi gas
SupelcoTM 37 Component FAME Mix, penangas, tabung bertutup teflon, pipet mikro, pipet tetes, bulb, spektrofotometer, sentrifuse, tabung sentrifuse, dan vorteks.
3.3 Tahap Penelitian
Penelitian terdiri dari penelitian pendahuluan dan penelitian utama.
Penelitian pendahuluan terdiri dari pengukuran morfometrik dan rendemen keong
mas, pengolahan, dan uji hedonik. Penelitian utama terdiri dari pengujian
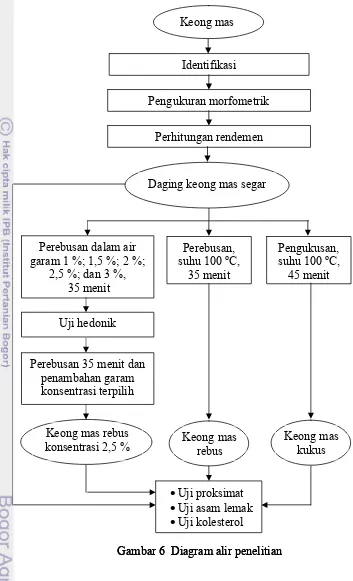
proksimat, asam lemak, dan kolesterol. Diagram alir penelitian disajikan pada
Keong mas
Identifikasi
Pengukuran morfometrik
Perhitungan rendemen
Daging keong mas segar
Perebusan dalam air garam 1 %; 1,5 %; 2 %;
2,5 %; dan 3 %, 35 menit
Perebusan, suhu 100 oC,
35 menit
Pengukusan, suhu 100 oC,
45 menit
Uji hedonik
Perebusan 35 menit dan penambahan garam konsentrasi terpilih
Keong mas rebus
konsentrasi 2,5 % Keong masrebus Keong mas kukus
•Uji proksimat •Uji asam lemak
Uji kolesterol •
Gambar 6 Diagram alir penelitian Gambar 6 Diagram alir penelitian
Proses pengolahan yang dilakukan meliputi perebusan, pengukusan, dan
perebusan dalam air garam. Pengolahan dilakukan hingga daging keong mas
matang. Pengecekan dilakukan setiap 5 menit untuk mengetahui tingkat
kematangan daging keong mas. Daging keong mas dinyatakan matang apabila Proses pengolahan yang dilakukan meliputi perebusan, pengukusan, dan
perebusan dalam air garam. Pengolahan dilakukan hingga daging keong mas
matang. Pengecekan dilakukan setiap 5 menit untuk mengetahui tingkat
sudah terasa empuk dan kenyal. Perebusan keong mas dilakukan selama 35 menit
pada suhu 100 oC. Pengukusan dilakukan selama 45 menit pada suhu 100 oC.
Perebusan dalam air garam dilakukan dengan penambahan konsentrasi garam
terpilih selama 35 menit pada suhu 100 oC. Daging keong mas yang telah
dimasak selanjutnya diangkat dan ditiriskan. Daging keong disimpan dalam botol
kaca dan dilapisi alumunium foil untuk selanjutnya dilakukan pengujian komposisi kimia, asam lemak, dan kolesterol.
Tahap ini juga bertujuan untuk menentukan konsentrasi garam terbaik
yang akan digunakan dalam proses perebusan dalam air garam. Sampel yang diuji
adalah daging keong mas yang telah direbus dalam air garam berkonsentrasi 1 %;
1,5 %; 2 %; 2,5 %; dan 3 %.
3.4 Pengukuran dan Analisis
3.4.1 Pengukuran morfometrik dan rendemen keong mas
Keong mas (Pomacea canaliculata) diambil dari daerah persawahan Situ Gede, Bogor. Keong mas sebanyak 30 ekor diukur panjang, lebar, dan tingginya
menggunakan penggaris. Keong mas lalu dipisahkan cangkang, jeroan, dan
dagingnya kemudian dihitung rendemen masing-masing.
Perhitungan rendemen daging keong mas adalah sebagai berikut:
Rendemen daging % Bobot total keong mas gram Bobot daging gram %
3.4.2 Uji hedonik (SNI-01-234-2006)
Uji hedonik dilakukan oleh 30 orang panelis semi terlatih menggunakan
lembar penilaian uji hedonik berdasarkan SNI-01-234-2006. Panelis memberikan
penilaian secara subjektif terhadap rasa keong mas yang telah direbus dengan
konsentrasi garam berbeda-beda. Parameter yang dinilai memiliki rentang 1-9,
dimana angka 1= amat sangat tidak suka, 2= sangat tidak suka, 3= tidak suka,
4= agak tidak suka, 5= netral, 6= agak suka, 7= suka, 8= sangat suka, dan
3.4.3 Analisis kimia
1) Analisis kadar air (AOAC 2005)
Cawan porselen dikeringkan dalam oven pada suhu 105 oC selama 1 jam.
Cawan tersebut diletakkan ke dalam desikator (kurang lebih 15 menit) dan
dibiarkan sampai dingin kemudian ditimbang. Cawan tersebut ditimbang kembali
hingga beratnya konstan. Sebanyak 5 gram contoh dimasukkan ke dalam cawan
tersebut, kemudian dikeringkan dengan oven pada suhu 105 oC selama 5 jam,
kemudian cawan dimasukkan ke dalam desikator sampai dingin dan selanjutnya
ditimbang kembali.
Perhitungan kadar air:
% kadar air B A B C %
Keterangan:
A = Berat cawan kosong (gram)
B = Berat cawan dengan sampel (gram)
C = Berat cawan dengan sampel setelah dikeringkan (gram)
2) Analisis kadar abu (AOAC 2005)
Cawan pengabuan dikeringkan di dalam oven selama 1 jam pada suhu
600 oC, kemudian didinginkan selama 15 menit di dalam desikator dan ditimbang
hingga didapatkan berat yang konstan. Sampel sebanyak 5 gram dimasukkan ke
dalam cawan pengabuan dan dipijarkan di atas nyala api hingga tidak berasap lagi.
Setelah itu dimasukkan ke dalam tanur pengabuan dengan suhu 600 oC selama
1 jam, kemudian ditimbang hingga didapatkan berat yang konstan.
Perhitungan kadar abu:
% kadar abu C AB A %
Keterangan:
A = Berat cawan abu porselen kosong (gram)
B = Berat cawan abu porselen dengan sampel (gram)
3) Analisis kadar protein (AOAC 2005)
Tahap-tahap yang dilakukan dalam analisis protein terdiri dari tiga tahap,
yaitu destruksi, destilasi, dan titrasi. Pengukuran kadar protein dilakukan dengan
metode mikro Kjeldahl. Sampel ditimbang sebanyak 0,25 gram, kemudian
dimasukkan ke dalam labu Kjeldahl 100 ml, lalu ditambahkan satu butir kjeltab
dan 3 ml H2SO4 pekat. Contoh didestruksi pada suhu 410 oC selama kurang lebih
1 jam sampai larutan jernih lalu didinginkan. Setelah dingin, ke dalam labu
Kjeldahl ditambahkan 50 ml akuades dan 20 ml NaOH 40 %, kemudian dilakukan
proses destilasi dengan suhu destilator 100 oC. Hasil destilasi ditampung dalam
labu Erlenmeyer 125 ml yang berisi campuran 10 ml asam borat (H3BO3) 2 % dan
2 tetes indikator bromcherosol green-methyl red yang berwarna merah muda. Setelah volume destilat mencapai 40 ml dan berwarna hijau kebiruan, maka
proses destilasi dihentikan. Lalu destilat dititrasi dengan HCl 0,1 N sampai terjadi
perubahan warna merah muda. Volume titran dibaca dan dicatat. Larutan blanko
dianalisis seperti contoh. Kadar protein dihitung dengan rumus sebagai berikut :
% N ml HCl ml Blankomg sampelN HCl fp %
% kadar protein % N fk
Keterangan:
fp = Faktor pengenceran = 10 fk = Faktor konversi = 6,25
4) Analisis kadar lemak (AOAC 2005)
Contoh seberat 5 gram dimasukkan ke dalam kertas saring pada kedua
ujung bungkus ditutup dengan kapas bebas lemak dan selanjutnya sampel yang
telah dibungkus dimasukkan ke dalam labu lemak yang sudah ditimbang berat
tetapnya dan disambungkan dengan tabung Soxhlet. Selongsong lemak
dimasukkan ke dalam ruang ekstraktor tabung Soxhlet dan disiram dengan pelarut
lemak (n-heksana), kemudian dilakukan refluks selama 6 jam. Pelarut lemak yang
ada dalam labu lemak didestilasi hingga semua pelarut lemak menguap. Pada saat
sehingga tidak kembali ke dalam labu lemak, selanjutnya labu lemak dikeringkan
dalam oven pada suhu 105 oC, setelah itu labu didinginkan dalam desikator
sampai beratnya konstan.
Kadar lemak dihitung dengan rumus sebagai berikut :
% Kadar lemak W WW % Keterangan :
W1 = Bobot sampel (gram)
W2 = Bobot labu lemak kosong (gram) W3 = Bobot labu lemak dengan lemak (gram)
5) Analisis asam lemak (AOAC 2005)
Metode analisis yang digunakan memiliki prinsip mengubah asam lemak
menjadi turunannya, yaitu metil ester sehingga dapat terdeteksi oleh alat
kromatografi. Gas Chromatography (GC) memiliki prinsip kerja pemisahan antara gas dan lapisan tipis cairan berdasarkan perbedaan jenis bahan
(Fardiaz 1989). Jenis alat kromatografi yang digunakan dalam penelitian ini
adalah SupelcoTM 37 Component FAME Mix. Hasil analisis akan terekam dalam
suatu lembaran yang terhubung dengan rekorder dan ditunjukkan melalui
beberapa puncak pada waktu retensi tertentu sesuai dengan karakter
masing-masing asam lemak. Sebelum melakukan injeksi metil ester, terlebih dahulu
lemak diekstraksi dari bahan lalu melakukan metilasi sehingga terbentuk metil
ester dari masing-masing asam lemak yang didapat.
a. Tahap ekstraksi
Tahap pertama dilakukan ekstraksi soxhlet untuk memperoleh asam
lemak, dan ditimbang sebanyak 20-30 mg lemak dalam bentuk minyak.
b. Tahap metilasi
Tahap metilasi dimaksudkan untuk membentuk senyawa turunan dari
asam lemak menjadi metil esternya. Asam-asam lemak diubah menjadi ester-ester
metil atau alkali yang lainnya sebelum disuntikkan ke dalam kromatografi gas
(Fardiaz 1989).
Tahap metilasi diawali dengan hidrolisis, yaitu dengan merefluks lemak di
dipanaskan selama 20 menit. Tahap selanjutnya adalah proses metilasi dengan
menambahkan 2 ml BF3 16 % dalam metanol kemudian dipanaskan kembali
selama 20 menit dan didinginkan. Sampel yang telah didinginkan selanjutnya
ditambahkan 2 ml NaCl jenuh dan 1 ml isooktan, kemudian dihomogenkan dan
bagian atas lapisan isooktan dipindahkan ke dalam tabung reaksi yang berisi
0,1 gram Na2SO4 anhidrat lalu dibiarkan 15 menit. Larutan disaring dengan
mikrofilter untuk memisahkan fase cairnya sebelum diinjeksikan ke dalam
kromatografi gas. Sampel sebanyak 1 µl selanjutnya diinjeksikan ke dalam
kromatografi gas. Asam lemak yang ada dalam metil ester akan diidentifikasi
oleh flame ionization detector (FID) atau detektor ionisasi nyala dan respon yang ada akan tercatat melalui kromatogram (peak).
c. Identifikasi asam lemak
Identifikasi asam lemak dilakukan dengan menginjeksikan metil ester pada
kromatografi gas SupelcoTM 37 Component Fame Mix dengan kondisi sebagai berikut: gas yang digunakan sebagai fase bergerak adalah gas nitrogen dengan
aliran bertekanan 20 ml/menit, sebagai bahan pembakar adalah hidrogen dengan
aliran bertekanan 30 ml/menit, dan oksigen dengan aliran 200-300 ml/menit,
kolom yang digunakan adalah kolom kapiler (capillary column) dB-23 berisi cyanopropil methylsil sepanjang 60 m dengan diameter dalam 0,25 mm, dengan tebal lapisan film 0,25 µm. Temperatur terprogram sebesar 125 oC, kemudian
suhu dinaikkan 5 oC per menit hingga suhu akhir 225 oC, suhu injektor 220 oC,
dan suhu detektor 240 oC. Alat kromatografi gas yang digunakan dalam penelitian
ini disajikan pada Gambar 7.
a b
Gambar 7 (a) Kromatografi gas
[image:34.595.328.476.574.699.2]d. Perhitungan jumlah asam lemak
Prinsip analisis komposisi asam lemak dengan kromatografi gas adalah
dengan mengubah komponen asam lemak pada lemak/minyak menjadi senyawa
volatil metil ester lemak yang akan dideteksi oleh detektor ionisasi nyala api
dalam bentuk respon berupa peak kromatogram. Jenis dan jumlah asam lemak yang ada pada contoh dapat diidentifikasi dengan membandingkan peak kromatogram contoh dengan peak kromoatogram asam lemak standar yang telah diketahui jenis dan konsentrasinya, kemudian dihitung kadar asam lemaknya.
Pengujian asam lemak ini menggunakan metode eksternal standar dimana
pengukuran contoh dan standar dilakukan secara terpisah dan tanpa adanya
penambahan larutan standar ke dalam contoh. Kadar asam lemak sampel dengan
metode eksternal standar dapat dihitung sebagai berikut:
% asam lemak b/b
Area sampel
Area standar C V %
gram contoh lemak
6) Analisis kolesterol (Liebermann Burchard 1974)
Analisis kadar kolesterol dilakukan menggunakan spektrofotometer.
Sampel keong mas sebanyak + 0,1 gram sampel dimasukkan ke dalam tabung
sentrifuse ditambah 8 ml campuran etanol dan potreleum eter dengan
perbandingan 3:1 dan diaduk sampai homogen. Pengaduk dibilas dengan larutan
yang sama sebanyak 2 ml, kemudian disentrifuse 4.000 rpm selama 10 menit.
Supernatan dituang ke dalam beaker glass 100 ml dan diuapkan di penangas air. Residu dilarutkan dengan kloroform sedikit demi sedikit sambil
dituangkan ke dalam tabung berskala hingga mencapai volume 5 ml. Selanjutnya
ditambahkan 2 ml asetat anhidrat dan 0,2 ml H2SO4 pekat, lalu dihomogenkan
dengan vorteks dan dibiarkan di tempat gelap selama 15 menit. Absorbansi
dibaca menggunakan spektrofotometer pada panjang gelombang 420 nm yang
ditunjukkan dengan warna hijau tua. Kadar kolesterol dihitung dengan rumus:
3.5 Rancangan Percobaan
Rancangan percobaan dilakukan untuk mengamati dan mengidentifikasi
perubahan yang disebabkan variabel atau perlakuan. Rancangan percobaan yang
digunakan pada penelitian ini dibedakan atas rancangan percobaan untuk uji
hedonik dan rancangan percobaan untuk analisis kimia.
3.5.1 Rancangan Percobaan uji hedonik
Rancangan percobaan uji hedonik menggunakan uji Kruskal Wallis untuk mengetahui pengaruh perbedaan konsentrasi garam terhadap rasa daging keong
mas. Uji Multiple Comparison selanjutnya dilakukan untuk mengetahui perlakuan yang memberikan pengaruh nyata terhadap rasa keong mas.
1) Uji Kruskal Wallis
Pengujian organoleptik rasa pada penelitian ini dilakukan oleh 30 orang
panelis semi terlatih. Cara penilaian organoleptik rasa dapat dilihat pada
Lampiran 3. Apabila nilai asymp. sig < 0,05 maka dinyatakan tolak H0 (perbedaan konsentrasi garam memberikan pengaruh nyata pada rasa keong mas).
Pengujian Krusk Wal allis menggunakan rumus berikut (Steel & Torrie 1993):
(1) H =
∑
R n(2) FK = ∑T
(3) H’ = H
FK
Keterangan ni
banyaknya pengamatan tiap perlakuan atau jumlah panelis
N = banyaknya data
Ri = jumlah rata-rata tiap perlakuan ke-i
T = banyaknya pengamatan yang seri dalam tiap ulangan
H’ = H terkoreksi
FK = faktor terkoreksi
2) Uji Multiple Comparison
Apabila hasil uji Kruskal Wallis menunjukkan bahwa perlakuan memberikan pengaruh nyata terhadap rasa keong mas, maka pengujian
R
'
i
−
R
'
j
><
Z
a/k(k−1)N
(
N
+
1)
12
1
ni
+
1
nj
⎡
⎣
⎢
⎤
⎦
⎥
Keterangan:R’i = Rata-rata rangking perlakuan ke-i R’j = Rata-rata rangking perlakuan ke-j N = Banyaknya data
K = Banyaknya perlakuan ni = Jumlah data perlakuan ke-i nj = Jumlah data perlakuan ke-j
3.5.2 Rancangan percobaan analisis kimia
Rancangan percobaan yang digunakan untuk menguji pengaruh metode
pengolahan terhadap komposisi proksimat, asam lemak, dan kolesterol adalah
rancangan acak lengkap (RAL) dengan satu faktor dan 4 taraf (sampel segar,
perebusan, perebusan dalam air garam, dan pengukusan). Data dianalisis dengan
ANOVA (Analysis Of Variant) menggunakan uji F, sebelum dilakukan uji F terlebih dahulu diuji kenormalan data.
1) Uji kenormalan Anderson-Darling
Uji kenormalan adalah pengujian untuk mengetahui apakah galat data
yang digunakan menyebar normal, sehingga dapat digunakan dalam statistika
parametrik. Uji kenormalan data yang digunakan dalam penelitian ini adalah uji
Anderson-Darling. Uji Anderson-darling berdasarkan pada fungsi distribusi
empirik. Model statistik uji Anderson-Darling adalah sebagai berikut
(Anderson & Darling 1952):
Keterangan:
A = Nilai uji statistik Anderson-Darling N = Jumlah data
F = Fungsi distributif kumulatif Y = Data yang telah diurutkan
Penghitungan menghasilkan nilai A2 hitung dan Pvalue. Bila nilai
posisi kurva sumbu X, sedangkan standar deviasi menggambarkan sebaran varian
(Anderson & Darling 1952).
2) Uji ANOVA
Data yang telah dinyatakan berdistribusi secara normal, dapat dinyatakan
dalam selang sebagai berikut:
Keterangan: x = Rata-rata = 1,96 z
µ
= Simpangan baku = (1-α) 100 %
n = Banyak data
Data selanjutnya dianalisis menggunakan model rancangan ANOVA
(Analysis Of Variant) atau uji F dengan formulasi (Steel & Torrie 1993):
Yij = μ + τi + εij
Keterangan :
Yij = Nilai pengamatan pada taraf ke-i dan ulangan ke-j (j=1,2) μ = Nilai tengah atau rataan umum pengamatan
τi = Pengaruh metode pengolahan pada taraf ke-i (i=1,2,3) εij = Galat atau sisa pengamatan taraf ke-i dengan ulangan ke-j
Hipotesa terhadap data hasil uji komposisi kimia pada berbagai metode
pengolahan adalah sebagai berikut:
H0 = Metode pengolahan tidak memberikan pengaruh terhadap komposisi kimia.
H1 = Metode pengolahan memberikan pengaruh terhadap komposisi kimia.
Hipotesa terhadap data hasil analisis kandungan asam lemak pada berbagai
metode pengolahan adalah sebagai berikut:
H0 = Metode pengolahan tidak memberikan pengaruh terhadap kandungan asam lemak.
Hipotesa terhadap data hasil analisis kadar kolesterol pada berbagai
metode pengolahan adalah sebagai berikut:
H0 = Metode pengolahan tidak memberikan pengaruh terhadap kadar kolesterol. H1 = Metode pengolahan memberikan pengaruh terhadap kadar kolesterol.
3) Uji lanjut Duncan
Jika uji F pada ANOVA memberikan pengaruh yang berbeda terhadap
komposisi kimia, kandungan asam lemak, dan kadar kolesterol, maka dilanjutkan
dengan uji Duncan, dengan rumus sebagai berikut:
Duncan t / ; KTSr
Keterangan :
4 HASIL DAN PEMBAHASAN
4.1 Karakteristik Keong Mas
Tubuh keong mas terdiri atas cangkang, jeroan, dan daging. Cangkang keong mas bundar dan berwarna coklat kehitaman. Cangkang ini tersusun dari kalsium karbonat sehingga bertekstur keras. Cangkang mencakup bagian operkulum yang berbentuk lingkaran dan menempel pada otot kaki. Operkulum berwarna coklat gelap, tersusun dari kitin, tipis, dan mudah dipatahkan. Jeroan keong mas yang berwarna hitam dengan bintik-bintik putih merupakan alat pencernaan, sedangkan bagian jeroan berwarna merah muda merupakan bagian gonad. Bagian jeroan ini bertekstur lunak dan mudah hancur saat ditekan. Daging keong mas bertekstur kenyal dan berwarna krem kecoklatan. Pengukuran morfometrik keong mas disajikan pada Gambar 8.
Lebar
Panjang
Tinggi
Gambar 8 Pengukuran morfometrik keong mas (Wood et al. 2006)
Data berat dan ukuran dari 30 sampel keong mas yang digunakan dalam penelitian ini disajikan pada Lampiran 2. Adapun berat dan ukuran rata-rata keong mas disajikan dalam Tabel 3.
Tabel 3 Berat dan ukuran keong mas (Pomacea canaliculata)
No Parameter Nilai
1. Panjang (cm) 2,56 ± 0,19
2. Lebar (cm) 1,84 ± 0,19
3. Tinggi (cm) 1,45 ± 0,13
4. Bobot (gram) 4,54 ± 0,80
4.2 Rendemen Keong Mas
Rendemen merupakan perbandingan antara bobot produk yang dapat dimanfaatkan dengan bobot total keseluruhan produk. Rendemen menunjukkan efektivitas suatu bahan. Semakin besar nilai rendemen, semakin besar pula bagian bahan baku yang dapat dimanfaatkan. Rendemen daging keong mas dihitung berdasarkan persentase perbandingan bobot daging terhadap bobot keong utuh. Rendemen yang dihitung meliputi cangkang, jeroan, dan daging keong mas. Diagram lingkaran rendemen keong mas disajikan pada Gambar 9.
Daging 21,84%
Jeroan 24,19%
Cangkang 53,97%
Gambar 9 Rendemen keong mas segar
Rendemen keong mas segar tertinggi yaitu pada bagian cangkang sebesar 53,97 %. Cangkang keong mas memiliki persentase terbesar karena cangkang keong pada umumnya tebal dan mengandung kalsium karbonat (CaCO3) maupun
zat tanduk. Rendemen jeroan keong mas memiliki persentase sebesar 24,19 % dan rendemen daging keong mas sebesar 21,84 %. Bagian jeroan keong mas memiliki persentase rendemen yang lebih besar dibandingkan rendemen daging. Hal ini diduga terkait dengan kebiasaan makan keong mas.
Cangkang keong terdiri atas tiga lapisan, yaitu lapisan nacre yang tipis, lapisan prismatik yang mengisi hingga 90% cangkang mengandung CaCO3, serta
maupun partikel lain dalam saluran pencernaan dan bagian jeroan kemungkinan disebabkan oleh cara keong mas mengambil makanan tersebut (Turgeon 1988).
4.3 Penetapan Waktu Pemasakan dan Konsentrasi Garam
Metode pengolahan yang dilakukan dalam penelitian ini adalah perebusan, perebusan dalam air garam, dan pengukusan. Lamanya waktu pemasakan ditentukan terlebih dahulu sehingga diperoleh waktu pemasakan terbaik hingga daging keong mas matang. Kematangan daging keong mas yang direbus maupun dikukus diperiksa setiap 5 menit sekali dan diperkirakan tingkat kematangannya hingga mencapai taraf kematangan terbaik. Keong mas yang direbus akan matang pada suhu 100 oC selama 35 menit, sedangkan keong mas yang dikukus akan matang pada suhu 100 oC selama 45 menit.
Penentuan konsentrasi garam yang digunakan dalam perlakuan perebusan dalam air garam, dilakukan dengan metode uji hedonik. Uji hedonik dilakukan oleh 30 orang panelis semi terlatih. Panelis mendapatkan sampel daging keong mas yang telah mengalami proses perebusan dalam air garam dengan konsentrasi garam sebesar 1%, 1,5%, 2%, 2,5%, dan 3% (Lampiran 3). Panelis kemudian menilai rasa daging keong mas secara subjektif menggunakan score sheet menurut SNI 01-234-2006. Diagram batang rata-rata uji hedonik rasa keong mas disajikan pada Gambar 10.
Gambar 10 menunjukkan bahwa uji hedonik parameter rasa daging keong mas rebus garam berkisar antara 4,57 hingga 6,20. Nilai tersebut menunjukkan bahwa panelis menilai rasa daging keong mas dengan kisaran “netral” hingga “agak suka”. Nilai rata-rata uji hedonik tertinggi terhadap rasa keong mas yaitu sebesar 6,20 (agak suka), dicapai oleh keong mas yang direbus dengan konsentrasi garam 2,5%.
Hasil uji Kruskal Wallis tentang konsentrasi garam (Lampiran 4) menunjukkan bahwa pada tingkat kepercayaan 95% konsentrasi garam yang berbeda memberikan pengaruh terhadap rasa keong mas. Hasil uji Multiple Comparisson (Lampiran 5) menunjukkan bahwa konsentrasi garam 2,5% memberikan pengaruh berbeda terhadap konsentrasi garam 1%, konsentrasi 1,5%, konsentrasi 2%, dan konsentrasi 3%. Berdasarkan hasil yang diperoleh, maka konsentrasi garam 2,5% adalah konsentrasi garam terbaik untuk perlakuan perebusan dalam air garam.
Penggunaan konsentrasi garam 2,5% ini relevan dengan pernyataan bahwa penambahan garam berkonsentrasi 1-3% berfungsi sebagai bumbu yang memberi cita rasa gurih pada bahan pangan. Penambahan konsentrasi garam yang terlalu tinggi dihawatirkan memberikan efek negatif bagi tubuh (Zaitsev et al. 1969).
4.4 Komposisi Kimia Keong Mas
Informasi mengenai kandungan gizi yang terdapat dalam bahan pangan dapat diketahui dengan analisis komposisi kimia atau proksimat bahan pangan tersebut. Analisis proksimat secara umum menunjukkan persentase dari unsur pokok berupa air, abu, protein, dan lemak. Kandungan gizi yang terkandung dalam suatu bahan pangan berbeda-beda karena adanya perbedaan makanan, spesies, jenis kelamin, dan umur bahan (Kusumo 1997). Hasil analisis proksimat daging keong mas disajikan padaTabel 4.
Tabel 4 Komposisi kimia keong mas (Pomacea canaliculata)
Parameter Kandungan (% bb)
Segar Rebus Rebus air garam Kukus
Kadar air 77,40 68,36 67,20 64,23
Kadar abu 5,44 4,40 6,67 4,00
Kadar protein 14,04 10,86 8,36 11,71
Tabel 4 menunjukkan hasil analisis proksimat daging keong mas segar dan setelah diberikan perlakuan pengolahan. Data kemudian diuji kenormalan galatnya menggunakan metode uji kenormalan Anderson Darling. Berdasarkan uji kenormalan Anderson Darling (Lampiran 7), semua perlakuan mempunyai galat yang menyebar normal sehingga dapat dilakukan analisis ragam.
4.4.1 Kadar air
Air merupakan komponen yang penting dalam bahan makanan, karena air dapat memberikan pengaruh pada penampakan, tekstur, serta cita rasa (Winarno 2008). Kadar air keong mas segar pada penelitian ini sebesar 77,40 % (bb). Hal ini tidak berbeda jauh dengan hasil penelitian Susanto (2010) yang menyatakan bahwa kadar air keong mas sebesar 81,19 % (bb).
Hasil analisis ragam kadar air (Lampiran 8) pada tingkat kepercayaan 95% menunjukkan bahwa pengolahan memberikan pengaruh terhadap kadar air keong mas. Nilai signifikansi < 0,05 dari analisis ragam, menunjukkan diperlukannya uji lanjut untuk mengetahui perlakuan yang memberikan pengaruh berbeda. Hasil uji lanjut Duncan (Lampiran 9) menunjukkan bahwa kadar air keong mas segar berbeda dengan kadar air keong mas setelah dilakukan perebusan, perebusan dalam air garam, dan pengukusan. Pengolahan menyebabkan penurunan kadar air pada proses perebusan sebesar 11,68%, perebusan dalam air garam sebesar 13,18%, dan pengukusan sebesar 17,02%. Diagram batang kadar air keong mas disajikan pada Gambar 11.
Gambar 11 menunjukkan bahwa metode pengolahan dengan panas memberikan kadar air yang berbeda dengan keong mas segar. Pengolahan dengan perebusan memiliki kadar air yang tidak berbeda dengan perebusan dalam air garam. Metode pemasakan yang hampir mirip, yakni perebusan, membuat kadar air yang dihasilkan tidak berbeda secara signifikan. Hal ini sesuai dengan pernyataan Prabandari et al. (2005) bahwa waktu dan suhu pengolahan dapat mempengaruhi nilai kadar air suatu bahan pangan. Semakin lama waktu pengolahan dan semakin tinggi suhu yang digunakan akan mengakibatkan banyak air dalam bahan pangan keluar.
Perebusan memberikan penurunan yang paling kecil terhadap kadar air. Pengolahan dengan perebusan membuat keong mas kontak langsung dengan air sehingga tidak terlalu banyak mengurangi kadar air. Hal ini sesuai dengan penelitian Weber et al. (2008) yang menyatakan bahwa pengolahan dengan panas menurunkan kadar air fillet ikan lele silver dan perlakuan perebusan memiliki persentase penurunan kadar air paling kecil.
Metode pengolahan dengan pengukusan menurunkan kadar air paling besar dari daging keong mas segar. Hal ini sesuai dengan penelitian Jamasuta et al. (1996) yang menyatakan bahwa kadar air ikan pindang yang dikukus lebih kecil dibandingkan dengan kadar air pindang yang direbus. Pengukusan menguapkan air lebih besar dibandingkan dengan perebusan karena pengukusan menggunakan metode yang membuat bahan pangan tidak langsung bersinggungan dengan air seperti pada proses perebusan.
4.4.2 Kadar abu
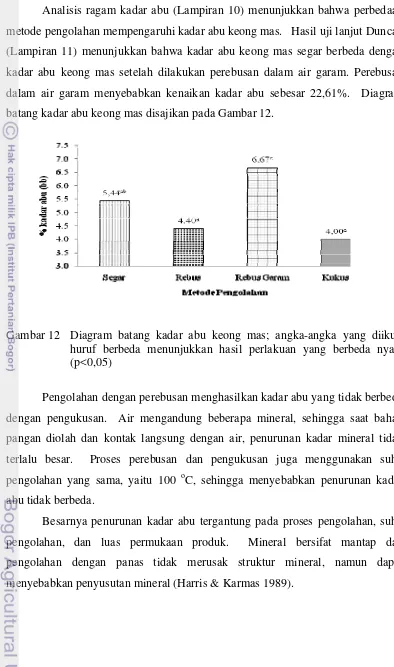
Analisis ragam kadar abu (Lampiran 10) menunjukkan bahwa perbedaan metode pengolahan mempengaruhi kadar abu keong mas. Hasil uji lanjut Duncan (Lampiran 11) menunjukkan bahwa kadar abu keong mas segar berbeda dengan kadar abu keong mas setelah dilakukan perebusan dalam air garam. Perebusan dalam air garam menyebabkan kenaikan kadar abu sebesar 22,61%. Diagram batang kadar abu keong mas disajikan pada Gambar 12.
Gambar 12 Diagram batang kadar abu keong mas; angka-angka yang diikuti huruf berbeda menunjukkan hasil perlakuan yang berbeda nyata (p<0,05)
Pengolahan dengan perebusan menghasilkan kadar abu yang tidak berbeda dengan pengukusan. Air mengandung beberapa mineral, sehingga saat bahan pangan diolah dan kontak langsung dengan air, penurunan kadar mineral tidak terlalu besar. Proses perebusan dan pengukusan juga menggunakan suhu pengolahan yang sama, yaitu 100 oC, sehingga menyebabkan penurunan kadar abu tidak berbeda.
[image:46.595.107.501.82.749.2]Proses pengolahan dengan perebusan dalam air garam menyebabkan kadar abu dalam daging keong mas bertambah, karena garam yang mengandung beberapa mineral seperti yodium, natrium, magnesium, dan lainnya terserap oleh bahan pangan yang direbus. Kadar mineral yang bertambah ditunjukkan dengan kadar abu yang naik pula.
Hal tersebut sesuai dengan pernyataan bahwa kadar abu mempunyai hubungan dengan mineral suatu bahan. Garam mempunyai unsur-unsur mineral seperti NaCl, MgCl, Na2SO4, CaCl2, hingga KCl sehingga meningkatkan kadar
abu bahan pangan yang ditambahkan garam (Budiono 2010). Penelitian lain yang mendukung yaitu Unlusayin et al. (2010) yang menyatakan bahwa kadar abu udang segar Penaeus semisulcatus sebesar 7,68 % (bk) meningkat menjadi 9,40 % (bk) setelah udang direbus dalam air garam.
4.4.3 Kadar protein
Protein merupakan sumber asam-asam amino yang mengandung unsur C, H, O, dan N yang tidak dimiliki oleh lemak dan karbohidrat (Lehninger 1992). Kadar protein yang didapat dari penelitian ini yaitu sebesar 14,04 % (bb), tidak berbeda jauh dengan hasil penelitian Budiyono (2006) bahwa kadar protein keong mas sebesar 12 %.
Gambar 13 Diagram batang kadar protein keong mas; angka-angka yang diikuti huruf berbeda menunjukkan hasil perlakuan yang berbeda nyata (p<0,05)
Diagram batang tersebut menunjukkan bahwa metode pengolahan dengan panas memberikan kadar protein yang berbeda dengan keong mas segar. Hal ini sesuai dengan pernyataan Georgiev et al. (2008) bahwa protein daging bersifat tidak stabil dan dapat terdenaturasi dengan adanya perubahan suhu lingkungan.
[image:48.595.120.460.89.264.2]Pengolahan dengan perebusan menghasilkan kadar protein yang tidak berbeda dengan perebusan dalam air garam. Keduanya merupakan metode pengolahan yang kontak langsung dengan air perebusnya. Protein larut air dalam daging keong mas lebih banyak keluar sehingga kadar protein daging keong yang direbus lebih kecil dibandingkan daging keong yang dikukus. Hal tersebut sesuai dengan pernyataan Harikedua (1992) bahwa penurunan kadar protein disebabkan proses hidrolisis protein dalam air rebusan, sehingga protein keluar bersama drip daging. Hidrolisis protein terjadi karena adanya molekul air bergabung ke dalam rantai protein dan ikatan antar asam amino terputus menjadi rantai protein yang lebih pendek. Reaksi hidrolisis protein disajikan pada Gambar 14.
Gambar 14 Reaksi hidrolisis protein (Winarno 2008)
juga dapat mengabsorbsi air dari jaringan daging, memecah ikatan molekul air, dan mengubah sifat alami protein. Hal ini didukung oleh penelitian Selcuk et al. (2010) yang menyatakan bahwa kadar protein, baik bobot basah maupun bobot kering, dapat berubah tergantung jenis spesies dan metode pengolahan. Penelitian lain yang mendukung yaitu Unlusayin et al. (2010) bahwa kadar protein udang segar Penaeus semisulcatus sebesar 83,81% (bk) menurun menjadi 79,15% (bk) setelah mendapat perlakuan perebusan dalam air garam. 4.4.4 Kadar lemak
Lemak merupakan sumber energi yang lebih efektif dibandingkan dengan karbohidrat dan protein karena menyumbang kalori sebesar 9 Kkal/gram atau 2 ¼ kali energi dari karbohidrat dan protein (Kusnandar 2010). Kadar lemak daging keong mas yang dianalisis dari penelitian ini yaitu sebesar 0,99% (bb). Nilai tersebut tidak terlalu berbeda dibandingkan penelitian Mulyaningtyas (2011) bahwa kandungan lemak remis sebesar 0,73% (bb).
Analisis ragam kadar lemak (Lampiran 14) menunjukkan perbedaan metode pengolahan mempengaruhi kadar lemak keong mas. Uji lanjut Duncan menunjukkan kadar lemak keong mas segar berbeda dengan kadar lemak keong mas setelah dilakukan perebusan, perebusan dalam air garam, dan pengukusan. Pengolahan menyebabkan penurunan kadar lemak pada proses perebusan sebesar 29,29%, perebusan dalam air garam sebesar 59,60%, dan pengukusan sebesar 20,00%. Diagram batang kadar lemak keong mas disajikan pada Gambar 15.
Gambar 15 menunjukkan bahwa metode pengolahan dengan panas menghasilkan kadar lemak berbeda dengan keong mas segar. Kadar lemak daging keong mas segar berbeda dengan kadar lemak daging keong mas yang telah mengalami perebusan, perebusan dalam air garam, dan pengukusan. Pernyataan tersebut didukung oleh Tapotubun et al. (2008) bahwa suhu dan waktu pemanasan memberikan pengaruh pada kadar lemak bahan pangan. Lemak yang berwujud padat pada suhu kamar akan mencair atau bahkan menguap saat terkena panas.
Perebusan dan pengukusan diduga mengakibatkan penyusutan kadar lemak. Prabandari et al. (2005) menyatakan bahwa proses pengolahan dengan pemanasan akan memecah komponen-komponen lemak menjadi produk volatil seperti aldehid, keton, alkohol, asam, dan hidrokarbon yang akan menguap saat pemanasan. Penelitian lain yang mendukung yaitu Weber et al. (2008) yang meneliti bahwa kadar lemak silver catfish (Rhamdia quelen) mengalami penurunan sebesar 0,06% setelah direbus, dan Baker et al. (2010) meneliti bahwa ikan Scomberomorus guttatus mengalami penurunan kadar lemak sebesar 0,05% setelah dikukus.
4.5 Kandungan Asam Lemak Keong Mas
Asam lemak adalah komponen penyusun lipid berantai panjang yang terdiri dari rantai hidrokarbon, gugus karboksil tunggal, dan memiliki ujung hidrokarbon non polar. Struktur asam lemak tersebut menyebabkan hampir semua lipid tampak berminyak dan tidak larut dalam air. Karakteristik asam lemak tergantung pada panjang rantai dan jumlah ikatan rangkapnya (Hames & Hooper 2005).
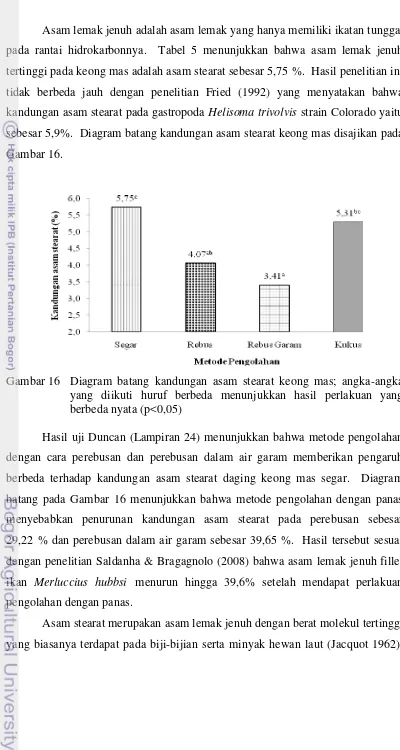
Kandungan asam lemak jenuh pada daging keong mas segar yaitu 18,05%, asam lemak tak jenuh tunggal yaitu 8,65%, asam lemak tak jenuh jamak yaitu 14,16%, dan asam lemak tak jenuh jamak r