PEMERIKSAAN RESIDU KLORAMFENIKOL DALAM
IKAN GURAMI (Osphronemus goramy) DAN IKAN MAS
(Cyprinus carpio) SECARA KROMATOGRAFI CAIR
KINERJA TINGGI (KCKT)
SKRIPSI
OLEH:
RIKHA ANDRYSSHA
NIM 091524022
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMERIKSAAN RESIDU KLORAMFENIKOL DALAM
IKAN GURAMI (Osphronemus goramy) DAN IKAN MAS
(Cyprinus carpio) SECARA KROMATOGRAFI CAIR
KINERJA TINGGI (KCKT)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
RIKHA ANDRYSSHA
NIM 091524022
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PEMERIKSAAN RESIDU KLORAMFENIKOL DALAM IKAN GURAMI
(Osphronemus goramy) DAN IKAN MAS (Cyprinus carpio) SECARA
KROMATOGRAFI CAIR KINERJA TINGGI (KCKT)
OLEH:
RIKHA ANDRYSSHA NIM 091524022
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Juni 2011
Medan, Juni 2011
Disetujui oleh:
Pembimbing I, Panitia Penguji,
Drs. Fathur Rahman Harun, M.Si.,Apt. NIP. 195201041980031002
Dra. Saleha Salbi, M.Si., Apt. Dra. Saleha Salbi, M.Si., Apt. NIP 194909061980032001 NIP 194909061980032001
Disetujui oleh:
Pembimbing II, Drs. Muchlisyam, MSi., Apt. NIP 195006221980021001
Prof. Dr. rer. nat. Effendy De Lux Putra, SU, Apt. NIP 195306191983031001
Drs. Maralaut Batubara, M.Phill.,Apt. NIP 195101311976031003
Dekan,
KATA PENGANTAR
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta Shalawat dan Salam kepada Nabi Allah: Rasulullah
Muhammad SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan
judul:“Pemeriksaan Residu Kloramfenikol dalam Ikan Gurami
(Osphronemus goramy)” dan Ikan Mas (Cyprinus carpio) Secara
Kromatografi Cair Kinerja Tinngi.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada:
1. Ayahanda Hendry dan ibunda Rosmala yang telah memberikan cinta dan kasih
sayang yang tidak ternilai dengan apapun, doa yang tulus serta pengorbanan
baik materi maupun non-materi.
2.Ibu Dra. Saleha Salbi, M.Si., Apt. dan bapak Prof. Dr. rer. nat. Effendy De Lux
Putra, SU, Apt. yang telah membimbing dan memberikan petunjuk serta
saran-saran selama penelitian hingga selesainya skripsi ini.
3. Bapak Prof. Dr. Sumadio Hadisahputra, Apt selaku Dekan, staf pengajar dan
staf administrasi Fakultas Farmasi yang telah mendidik penulis selama masa
perkuliahan dan membantu kemudahan administrasi.
4. Ibu Dra. Sudarmi, M.Si., Apt selaku Kepala Laboratorium Kimia Farmasi
Kuantitatif Farmasi USU yang telah memberikan izin dan fasilitas untuk
5. Kak Mustika Puri dan bang Abdi selaku penanggung jawab Laboratorium, Kak
Evi, Kak Tina selaku Operator Laboratorium Penelitian yang telah membantu
fasilitas kepada penulis selama melaksanakan penelitian.
6. Kakanda tercinta (Retno Sugianto) dan abangku (Muhamad Yusuf Mustawwa),
adikku tersayang (Almarhumah Farah Dinna Andryssha, Abdillah Shafanda
Mustawwa, Nadia Shafira Andryssha, Rahmawati) serta seluruh keluarga yang
selalu mendoakan dan memberikan semangat.
7. Spesial untuk sahabat-sahabat ku Tentuwin (Kak Winda, Kak Ira Veronika,
Ernal, Desmi, Sri, Emil, Ipit, Vivi Ke, Iezzha, Anita), Sahabat di Lab.
Penelitian (Mirna, Harti, Melati, Midah) Kak Ve,, Bayu, Taqin, Zega, Hendra,
K’Ira S, K’Mariani, K’Okta, K’Maria, Hetty, Kak Maria dan seluruh
teman-teman Ekstensi angkatan 2009 dan 2008, terima kasih untuk perhatian,
semangat, doa, dan kebersamaannya selama ini.
8. Serta seluruh pihak yang telah ikut membantu penulis namun tidak tercantum
namanya.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini.
Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat
bagi kita semua.
Medan, Juni 2011 Penulis,
PEMERIKSAAN KADAR RESIDU KLORAMFENIKOL DALAM IKAN GURAMI (Osphronemus goramy) DAN IKAN MAS (Cyprinus carpio)
SECARA KROMATOGRAFI CAIR KINERJA TINGGI (KCKT)
Abstrak
Kloramfenikol adalah antibiotik berspektrum luas yang bekerja dengan cara menghambat sintesis protein bakteri dan menjadi obat pilihan pada penyakit Tifoid salmonellosis. Penggunaan kloramfenikol banyak digunakan dalam budidaya ikan gurami (Osphronemus goramy) dan ikan mas (Cyprinus carpio) baik untuk pencegahan maupun pengobatan beberapa penyakit. Diberikan melalui makanan, perendaman ataupun penyuntikan. Tujuan dari penelitian ini adalah untuk memeriksa residu kloramfenikol dalam daging ikan. Penetapan kadar dilakukan secara kromatografi cair kinerja tinggi menggunakan kolom C18 (250 mm x 4,60 mm), dengan fase gerak metanol - air (55:45) dan laju alir 1 ml/menit, detektor UV pada panjang gelombang 278 nm.
Hasil penelitian menunjukkan terdapat residu kloramfenikol dalam ikan gurami dan ikan mas dari keempat pasar yang berbeda di kota Binjai, dengan kadar berturut- turut PG1, PG2, PG3, PG4 dan PM1, PM2, PM3, PM4 adalah 0,2092±0,0073, 0,0587±0,0016, 0,0786±0,0045, 0,1190±0,0111, 0,07675±0,0048 dan 0,0676±0,0035, 0,0734±0,0094, 0,2169±0,0448. Berdasarkan Rancangan Standar Nasional Indonesia No. 05 – TAN - 1996 batas maksimum residu dalam daging sebesar 0,01 mg/kg. Dari hasil penelitian, disimpulkan bahwa kadar residu kloramfenikol dalam sampel tidak memenuhi persyaratan.
Validasi metode menunjukkan bahwa prosedur penelitian yang dilakukan memiliki akurasi dan presisi yang baik yakni dengan persen perolehan kembali kloramfenikol sebesar 95,49%, (RSD = 9,96%). Dengan batas deteksi (LOD) dan batas kuantitasi (LOQ) berturut-turut adalah 0,0165 µg/ml dan 0,0550 µg/ml.
EXAMINATION OF CHLORAMPHENICOL RESIDUE IN CARP
(Osphronemus goramy) AND GOLDFISH (Cyprinus carpio) BY HIGH
PERFORMANCE LIQUID CHROMATOGRAPHY
Abstract
Chloramphenicol is a broad spectrum antibiotic that inhibit synthesis of bacterial protein and it has been used as a drug of choice in treatment of salmonellosis tiffoid diseases. Chloramphenicol was widely used in farming on carp (Osphronemus goramy) and goldfish (Cyprinus carpio) as well to prevent and treat of several diseases it was provided through food, soaking or injection. The aim of this study was to examine the residues of chloramphenicol in fish flesh. Determination of chloramphenicol levels was conducted by using high performance liquid chromatography, involving C-18 column with mobile phase of methanol - water (55:45) and flow rate 1ml/minute, UV detector at 278 nm, was used to quantity chloramphenicol residue.
The results showed that there were chloramphenicol residues in the carp and goldfish that were collected from four different market in Binjai they were PG1, PG2, PG3, PG4 dan PM1, PM2, PM3, PM4 adalah 0.2092±0.0073, 0.0587±0.0016, 0.0786±0.0045, 0.1190±0.0111, 0.07675±0.0048 dan 0.0676±0.0035, 0.0734±0.0094, 0.2169±0.0448, respectively. Based on Program Standart National Indonesian No. 05-TAN-1996. maximum level of chloramphenicol residue in meat is 0.01 mg/kg. From this result, it can be concluded that the level of chloramphenicol in samples did not meet the requirement.
Method validation showed that procedure have a good accuracy and precision with percentage of recovery 95.49%, relative standard deviation (RSD = 9,96%). Limit of detection (LOD) and limit of quantization (LOQ) were 0.0165 µg/ml and 0.0550 µg/ml, respectively.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
ABSTRAK ... iii
ABSTRACT... ... ... iv
DAFTAR ISI ... v
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... xi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB III TINJAUAN PUSTAKA ... 5
2.1 Kloramfenikol ... 5
2.1.1 Sifat Fisiko Kimia ... 5
2.1.2 Kegunaan Umum.... ... ... 5
2.1.3 Farmakokinetika ... 6
2.2 Ikan... 6
2.2.1 Ikan Gurami (Osphronemus gouramy) ... 7
2.2.2 Ikan Mas (Cyprinus carpio) ... 8
2.2.3 Penyakit Ikan.... ... 9
2.3 Kromatografi ... 13
2.3.1 Pembagian Kromatografi ... 14
2.3.2 Kromatografi Cair Kinerja Tinggi ... 14
2.3.3 Jenis Kolom ... 16
2.3.4 Jenis Pompa ... 16
Kolom... 17
2.3.6 Proses Pemisahan Dalam Kromatografi Cair ... 19
2.4 Validasi Metode... 21
2.4.1 Akurasi (Kecermatan) ... 21
2.4.2 Presisi (Keseksamaan) ... 21
2.4.3 Spesifisitas (Selektivitas) ... 22
2.4.4 Batas Deteksi (Limit of Detection/LOD) ... 22
2.4.5 Batas Kuantitasi (Limit of Quantitation/LOQ) ... 22
2.4.6 Linearitas ... 22
2.4.7 Kekuatan (Robustness) ... 23
BAB III METODOLOGI PENELITIAN ... 24
3.1 Waktu dan Tempat Penelitian ... 24
3.2 Alat-alat ... 24
3.3 Bahan-bahan ... 24
3.4 Pengambilan Sampel ... 24
3.5 Prosedur Penelitian ... 25
3.5.1 Penyiapan Bahan ... 25
3.5.1.1 Pembuatan Fase Gerak Metanol - Air ... 25
3.5.1.2 Pembuatan Pelarut.... ... 25
3.5.2 Penentuan Panjang Gelombang Maksimum.... ... 25
3.5.3 Prosedur Analisis ... 25
3.5.3.1 Penyiapan Alat Kromatografi Cair Kinerja Tinggi ... 25
3.5.3.2 Pembuatan Larutan Induk Baku Kloramfenikol ... 26
3.5.3.3 Penentuan Perbandingan Fase Gerak yang optimum untuk analisa ... 26
3.5.3.4 Pembuatan Kurva Kalibrasi Kloramfenikol Baku .... 26
3.5.3.5 Preparasi Sampel ... 27
3.5.3.6 Penetapan Kadar Residu Kloramfenikol dalam Sampel ... 27
3.5.3.7 Analisis Data Secara Statistik ... 30
3.5.4 Metode Validasi ... 31
3.5.4.2 Presisi ... 32
3.5.4.3 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ) ... 33
BAB IV HASIL DAN PEMBAHASAN... 34
4.1 Penentuan Kondisi Kromatografi untuk Mendapatkan Hasil Analisis yang Optimum ... 34
4.2Penentuan Linieritas Kurva Kalibrasi Kloramfenikol BPFI…….. 35
4.3 Penenetapan Kadar Residu Kloramfenikol dalam Sampel ... 35
4.4 Hasil Uji Validasi ... 39
BAB V KESIMPULAN DAN SARAN ... 42
5.1 Kesimpulan ... 42
5.2 Saran ... 42
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Halaman
Tabel 1. Data Hasil Analisis Kloramfenikol Baku 10 ppm Pada Berbagai
Perbandingan Komposisi Fase Gerak ... 37
Tabel 2. Hasil Penetapan Kadar Kloramfenikol dalam Sampel Ikan gurami
dan ikan mas Secara Statistik ... 39
DAFTAR GAMBAR
Halaman
Gambar 1. Rumus Bangun Kloramfenikol ... 5
Gambar 2. Ikan Gurami Yang Tidak Terserang Penyakit (A) dan Ikan
Gurami Yang Terserang Penyakit Bercak Merah (B) ... 11
Gambar 3. Pengukuran Derajat Asimetri Puncak ... 19
Gambar 4. Ilustrasi Pemisahan Yang Terjadi di Dalam Kolom KCKT ... 20
Gambar 5.Bagan Prosedur Penetapan Kadar Residu Kloramfenikol dalam Sampel ... 30
Gambar 6.Kurva Serapan Kloramfenikol Baku 15 ppm Secara Spektrofotometri UV ... 34
Gambar 7. Kurva Kalibrasi Kloramfenikol BPFI ... 35
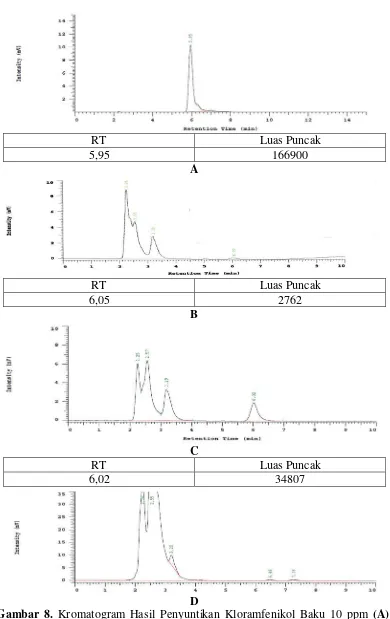
Gambar 8. Kromatogram Hasil Penyuntikan Kloramfenikol Baku 10 ppm (A), Larutan Sampel Ikan (B), dan Larutan Sampel yang telah di-spike dengan Larutan Baku Pembanding Kloramfenikol (C) Larutan Sampel Blanko (D) dengan
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Kromatogram Penyuntikan Kloramfenikol Baku untuk
Mencari Perbandingan Fase Gerak ... 45
Lampiran 2. Kromatogram Penyuntikan Kloramfenikol Baku Pada
Pembuatan Kurva Kalibrasi ... 49
Lampiran 3. Perhitungan Persamaan Regresi dari Kurva Kalibrasi
Kloramfenikol ... 52
Lampiran 4. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi
(LOQ) Baku Kloramfenikol ... 54
Lampiran 5. Data Hasil Perhitungan Kadar Residu Kloramfenikol dalam
Ikan Gurami dan Ikan Mas ... 55
Lampiran 6. Contoh Perhitungan Hasil Penetapan Kadar Kloramfenikol
Dalam Sampel Menggunakan Persamaan Garis Regresi ... 56
Lampiran 7. Kromatogram Hasil Penyuntikan dari Ikan Gurami PG1 ... 57
Lampiran 8. Analisis Data Secara Statistik Untuk Mencari Kadar
Sebenarnya dari Penyuntikan Ikan Gurami PG1 ... 58
Lampiran 9. Kromatogram Hasil Penyuntikan dari Ikan Gurami PG2 ... 60
Lampiran10. Analisis Data Secara Statistik Untuk Mencari Kadar
Sebenarnya Dari Penyuntikan Ikan Gurami PG2 ... 61
Lampiran11. Kromatogram Hasil Penyuntikan dari Ikan Gurami PG3 ... 64
Lampiran12. Analisis Data Secara Statistik Untuk Mencari Kadar
Sebenarnya dari Penyuntikan Ikan Gurami PG3 ... 65
Lampiran13. Kromatogram Hasil Penyuntikan dari Ikan Gurami PG4 ... 69
Lampiran 14. Analisis Data Secara Statistik Untuk Mencari Kadar
Sebenarnya dari Penyuntikan Ikan Gurami PG4 ... 70
Lampiran 15. Kromatogram Hasil Penyuntikan dari Ikan Mas PM1 ... 74
Lampiran 16. Analisis Data Secara Statistik Untuk Mencari Kadar
Sebenarnya Dari Penyuntikan Ikan Mas PM1 ... 75
Lampiran 17. Kromatogram Hasil Penyuntikan dari Ikan Mas PM2 ... 79
Lampiran 18. Analisis Data Secara Statistik Untuk Mencari Kadar
Lampiran 19. Kromatogram Hasil Penyuntikan dari Ikan Mas PM3 ... 84
Lampiran 20. Analisis Data Secara Statistik Untuk Mencari Kadar Sebenarnya Dari Penyuntikan Ikan Mas PM3 ... 85
Lampiran 21. Kromatogram Hasil Penyuntikan dari Ikan Mas PM4 ... 88
Lampiran 22. Analisis Data Secara Statistik Untuk Mencari Kadar Sebenarnya Dari Penyuntikan Ikan Mas PM4 ... 89
Lampiran 23. Kromatogram Hasil Penyuntikan Sampel Tanpa Penambahan Kloramfenikol Baku ... 92
Lampiran 24. Kromatogram Hasil Perolehan Kembali Kloramfenikol Baku yang Ditambahkan pada sampel (Metode Penambahan Baku) .. 94
Lampiran 25. Perhitungan Persen Perolehan Kembali ... 99
Lampiran 26. Analisis Data Secara Statistik Persen Perolehan Kembali Kloramfenikol pada Ikan ... 101
Lampiran 27. Gambar Kromatografi Cair Kinerja Tinggi (KCKT) dan vial autosampler ... 102
Lampiran 28. Gambar Perangkat Pendukung Penelitian Lainnya ... 103
Lampiran 29. Nilai Distribusi t ... 106
Lampiran 30. Sertifikat Taksonomi Ikan Gurami ... 107
Lampiran 31. Sertifikat Taksonomi Ikan Mas ... 108
Lampiran 32. Sertifikat Analisis Kloramfenikol BPFI ... . 109
PEMERIKSAAN KADAR RESIDU KLORAMFENIKOL DALAM IKAN GURAMI (Osphronemus goramy) DAN IKAN MAS (Cyprinus carpio)
SECARA KROMATOGRAFI CAIR KINERJA TINGGI (KCKT)
Abstrak
Kloramfenikol adalah antibiotik berspektrum luas yang bekerja dengan cara menghambat sintesis protein bakteri dan menjadi obat pilihan pada penyakit Tifoid salmonellosis. Penggunaan kloramfenikol banyak digunakan dalam budidaya ikan gurami (Osphronemus goramy) dan ikan mas (Cyprinus carpio) baik untuk pencegahan maupun pengobatan beberapa penyakit. Diberikan melalui makanan, perendaman ataupun penyuntikan. Tujuan dari penelitian ini adalah untuk memeriksa residu kloramfenikol dalam daging ikan. Penetapan kadar dilakukan secara kromatografi cair kinerja tinggi menggunakan kolom C18 (250 mm x 4,60 mm), dengan fase gerak metanol - air (55:45) dan laju alir 1 ml/menit, detektor UV pada panjang gelombang 278 nm.
Hasil penelitian menunjukkan terdapat residu kloramfenikol dalam ikan gurami dan ikan mas dari keempat pasar yang berbeda di kota Binjai, dengan kadar berturut- turut PG1, PG2, PG3, PG4 dan PM1, PM2, PM3, PM4 adalah 0,2092±0,0073, 0,0587±0,0016, 0,0786±0,0045, 0,1190±0,0111, 0,07675±0,0048 dan 0,0676±0,0035, 0,0734±0,0094, 0,2169±0,0448. Berdasarkan Rancangan Standar Nasional Indonesia No. 05 – TAN - 1996 batas maksimum residu dalam daging sebesar 0,01 mg/kg. Dari hasil penelitian, disimpulkan bahwa kadar residu kloramfenikol dalam sampel tidak memenuhi persyaratan.
Validasi metode menunjukkan bahwa prosedur penelitian yang dilakukan memiliki akurasi dan presisi yang baik yakni dengan persen perolehan kembali kloramfenikol sebesar 95,49%, (RSD = 9,96%). Dengan batas deteksi (LOD) dan batas kuantitasi (LOQ) berturut-turut adalah 0,0165 µg/ml dan 0,0550 µg/ml.
EXAMINATION OF CHLORAMPHENICOL RESIDUE IN CARP
(Osphronemus goramy) AND GOLDFISH (Cyprinus carpio) BY HIGH
PERFORMANCE LIQUID CHROMATOGRAPHY
Abstract
Chloramphenicol is a broad spectrum antibiotic that inhibit synthesis of bacterial protein and it has been used as a drug of choice in treatment of salmonellosis tiffoid diseases. Chloramphenicol was widely used in farming on carp (Osphronemus goramy) and goldfish (Cyprinus carpio) as well to prevent and treat of several diseases it was provided through food, soaking or injection. The aim of this study was to examine the residues of chloramphenicol in fish flesh. Determination of chloramphenicol levels was conducted by using high performance liquid chromatography, involving C-18 column with mobile phase of methanol - water (55:45) and flow rate 1ml/minute, UV detector at 278 nm, was used to quantity chloramphenicol residue.
The results showed that there were chloramphenicol residues in the carp and goldfish that were collected from four different market in Binjai they were PG1, PG2, PG3, PG4 dan PM1, PM2, PM3, PM4 adalah 0.2092±0.0073, 0.0587±0.0016, 0.0786±0.0045, 0.1190±0.0111, 0.07675±0.0048 dan 0.0676±0.0035, 0.0734±0.0094, 0.2169±0.0448, respectively. Based on Program Standart National Indonesian No. 05-TAN-1996. maximum level of chloramphenicol residue in meat is 0.01 mg/kg. From this result, it can be concluded that the level of chloramphenicol in samples did not meet the requirement.
Method validation showed that procedure have a good accuracy and precision with percentage of recovery 95.49%, relative standard deviation (RSD = 9,96%). Limit of detection (LOD) and limit of quantization (LOQ) were 0.0165 µg/ml and 0.0550 µg/ml, respectively.
BAB I
PENDAHULUAN
1.1Latar Belakang
Ikan gurami (Osphronemus goramy) dan ikan mas (Cyprinus carpio)
merupakan komoditi perikanan air tawar yang banyak dibudidayakan di
Indonesia. Salah satu sektor perikanan yang memiliki peluang pasar yang cukup
baik adalah budidaya ikan gurami. Hal ini karena harga ikan gurami merupakan
yang paling tinggi dibandingkan dengan ikan air tawar lainnya seperti ikan mas,
nila dan mujair. Namun, masa pemeliharaan ikan gurami mulai dari menetas telur
hingga mencapai ukuran konsumsi (500 g/ekor) adalah 1,5 tahun sedangkan
pemeliharaan ikan mas dari menetas telur hingga mencapai ukuran 500 g/ekor
hanya membutuhkan waktu sekitar 6 bulan (Pertamawati, 2006).
Akan tetapi, serangan penyakit dan gangguan hama dapat menyebabkan
pertumbuhan ikan menjadi lambat (kekerdilan), konversi pakan menjadi tinggi,
periode pemeliharaan lebih lama, yang dapat meningkatkan biaya produksi,
sehingga dapat menyebabkan menurunnya hasil panen serta kegagalan panen
(Kordi, 2004).
Para peternak ikan menambahkan obat-obatan seperti antibiotik untuk
menghindari masalah tersebut, karena dianggap sangat praktis, efektif dan murah.
Menurut Martadinata (2002), penggunaan antibiotik saat ini telah meluas, tidak
saja pada manusia, juga pada ternak ikan. Antibiotik selain digunakan untuk
mencegah dan mengobati, juga dimanfaatkan untuk merangsang pertumbuhan dan
produksi ternak. Jika pemberian antibiotik tidak sesuai dengan aturan medis dapat
dapat mengganggu kesehatan manusia. Menurut Kordi (2004), salah satu contoh
antibiotik yang sering digunakan oleh peternak ikan, yaitu kloramfenikol.
Kloramfenikol diberikan melalui makanan, perendaman atau penyuntikan.
Kloramfenikol merupakan antibiotik berspektrum luas bekerja dengan cara
menghambat sintesis protein bakteri dan menjadi obat pilihan pada penyakit
Tifoid salmonellosis. Efek samping penggunaan kloramfenikol adalah, dapat
menyebabkan terjadinya gangguan saluran cerna, anemia aplastik, gray sindrom,
alergi, dan resistensi (Wattimena, dkk., 1999 ; Hadisahputra dan Harahap, 1994).
Menurut Rancangan Standar Nasional Indonesia (RSNI) No. : 05 – TAN –
1996 batas kadar residu kloramfenikol yang masih diperbolehkan adalah 0,01
mg/kg.
Mutakin dkk, (2010) telah menentukan kadar residu kloramfenikol dalam
jaringan ikan mas dengan metode kromatografi cair kinerja tinggi di Universitas
Padjajaran, menggunakan kolom Lichosper C-18, laju alir 1-2 ml/ menit dan fase
gerak air – metanol (75 : 25) dengan waktu retensi 10 menit.
Menurut SNI (Standar Nasional Indonesia) 7541.1:2009, metode pengujian
residu kloramfenikol dalam daging, telur, susu, dan olahannya dilakukan secara
kromatografi cair kinerja tinggi menggunakan kolom C18, detektor UV panjang
gelombang 270 nm dengan fase gerak metanol-air (1:1) dan laju alir 1 ml/menit.
Oleh karena itu, peneliti tertarik untuk mengetahui kadar residu kloramfenikol
pada ikan gurami dan ikan mas di keempat pasar di kota Binjai menggunakan
metode pengujian SNI 7541.1:2009 secara kromatografi cair kinerja tinggi
Metode identifikasi kloramfenikol pada ikan gurami dan ikan mas secara
KCKT dilakukan dengan membandingkan parameter waktu tambat dari sampel
terhadap waktu tambat kloramfenikol BPFI sedangkan penetapan kadarnya
dilakukan dengan mensubstitusikan luas puncak kloramfenikol yang diperoleh ke
persamaan regresi. Untuk menguji keabsahan metode yang digunakan dilakukan
validasi. Parameter validasi yang diuji meliputi akurasi (kecermatan), presisi
(keseksamaan), batas deteksi (LOD) dan batas kuantitasi (LOQ).
1.2 Perumusan Masalah
1. Apakah terdapat residu kloramfenikol dalam ikan gurami dan ikan mas
dari keempat pasar di kota Binjai.
2. Berapakah kadar residu kloramfenikol dalam ikan gurami dan ikan mas
dari keempat pasar di kota Binjai memenuhi persyaratan RSNI No. : 05 –
TAN – 1996.
1.3 Hipotesis
1. Terdapat residu kloramfenikol dalam ikan gurami dan ikan mas dari
keempat pasar di kota Binjai.
2. Kadar residu kloramfenikol dalam ikan gurami dan ikan mas dari keempat
pasar di kota Binjai, tidak memenuhi persyaratan RSNI No. : 05 – TAN –
1.4 Tujuan Penelitian
1. Untuk mengetahui adanya residu kloramfenikol dalam ikan gurami dan
ikan mas dari keempat pasar di kota Binjai.
2. Untuk mengetahui kesesuaian kadar residu kloramfenikol dalam ikan
gurami dan ikan mas dari keempat pasar di kota Binjai dengan persyaratan
RSNI No. : 05 – TAN – 1996.
1.5 Manfaat Penelitian
Hasil penelitian ini, diharapkan dapat memberikan informasi kepada
masyarakat mengenai keberadaan residu kloramfenikol yang terdapat dalam ikan
BAB II
TINJAUAN PUSTAKA
2.1 Kloramfenikol
2.1.2 Sifat Fisiko Kimia
Sinonim kloramfenikol adalah dichloroasetamide, amphicol, anacetin, fenicol,
cloramicol, cloromycetin, Kemicetine, (Winholdz, 1983). Merupakan hablur
halus berbentuk jarum atau lempeng memanjang; putih sampai putih kelabu
atau putih kekuningan; tidak berbau; rasa sangat pahit. Larut dalam lebih kurang
400 bagian air, dalam 2,5 bagian etanol (95%) P dan dalam 7 bagian
propilenglikol P; sukar larut dalam kloroformP dan dalam eter. Dapat menyerap
sinar Ultraviolet didalam air pada panjang gelombang 278 nm. Berkhasiat sebagai
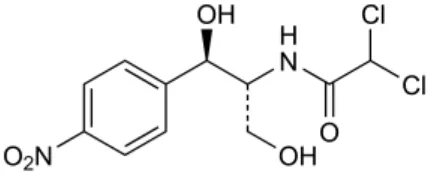
antibiotikum (Ditjen POM, 1979). Memiliki rumus molekul C11H12Cl2N2O5 dan
rumus bangun, seperti yang ditunjukkan pada gambar 1.
Gambar 1. Rumus Bangun Kloramfenikol (sumber: USP, 2006)
2.1.3 Kegunaan Umum
Kloramfenikol digunakan sebagai antibiotik bersifat bakteriostatik dan
mempunyai spektrum luas. Merupakan obat pilihan untuk pengobatan demam
tifoid akut yang disebabkan oleh salmonella sp. Kloramfenikol pada awalnya
Burkholder pada tahun 1947 dari contoh tanah yang diambil dari Venezuela,
sekarang telah dapat dibuat melalui sintesis total, yang metodenya relatif lebih
sederhana dan biayanya lebih murah. Kloramfenikol efektif terhadap riketsia dan
konjungtivitis akut yang disebabkan oleh mikoroorganisme, termasuk
Pseudomonas sp kecuali Pseudomonas aeruginosa. Senyawa ini juga efektif
untuk pengobatan infeksi berat yang disebabkan oleh bakteri gram positif dan
gram negative (Siswandono dan Soekardjo, 1995).
2.1.4 Farmakokinetika
Penyerapan obat melalui saluran cerna cukup baik (75-90%), kadar plasma
tertinggi dicapai dalam 2-3 jam. Waktu paruh kloramfenikol pada orang dewasa ±
3 jam, sedang pada bayi di bawah 1 bulan 12-24 jam (Siswandono dan Soekardjo,
1995).
2.1.5 Toksikologi
Efek samping yang ditimbulkan kloramfenikol antara lain adalah depresi
sumsum tulang belakang, yang menimbulkan kelainan darah yang serius, seperti
anemia aplastik, granulositopenia, trombositopenia. Selain itu, obat ini juga dapat
menyebabkan gangguan saluran cerna dan reaksi hipersensitivitas. Oleh karena itu
kloramfenikol tidak boleh digunakan untuk pengobatan infeksi yang bukan
indikasinya,seperti influenza, infeksi kerongkongan atau untuk pencegahan infeksi
(Siswandono dan Soekardjo, 1995 ; Watimena, dkk, 1999).
2.2 Ikan
Ikan merupakan salah satu bahan makanan yang mengandung berbagai macam
zat, selain harga yang umumnya lebih murah, absorpsi ikan lebih tinggi
daging ikan mempunyai serat-serat protein lebih pendek dari pada serat-serat
protein daging sapi atau ayam. Jenisnya pun sangat beragam dan mempunyai
beberapa kelebihan, diantaranya adalah mengandung omega 3 dan omega 6, dan
kelengkapan komposisi asam amino. Ikan juga dapat menurunkan kolesterol
darah, menurunkan kadar trigliserida darah, meningkatkan kecerdasan anak dan
meningkatkan kemampuan akademik, menurunkan resiko kematian karena
penyakit jantung, mengurangi gejala rematik, menurunkan aktivitas pertumbuhan
sel kanker dan juga mengandung omega 3 dan omega 6 (Anonim, 2008).
2.2.1 Ikan Gurami (Osphronemus gouramy)
Gurami adalah ikan air tawar yang banyak menghuni rawa-rawa, danau, atau
daerah perairan tenang. Sebagai ikan hasil budi daya, gurami banyak dipilih petani
karena mampu berbiak secara alami dan mudah dalam pemberian pakan. Dari
aspek bisnis keuntungan yang bisa didapat adalah harga jual yang cukup tinggi
dan relatif stabil. Gurami sangat peka terhadap suhu dingin. Suhu air optimal
untuk pertumbuhaannya adalah 24-280C. Bentuk fisik gurami sangat khas.
Tubuhnya pipih dan agak panjang. Bagian dahi gurami dewasa terdapat tonjolan
mirip cula. Tonjolan ini tidak ditemukan pada gurami muda (anakan). Pada
gurami anakan terdapat ciri khas berupa garis-garis hitam yang melintang
ditubuhnya. Rata-rata ikan gurami memiliki mulut yang kecil dengan bibir bagian
bawah terlihat sedikit lebih panjang dibandingkan bibir atas. Panjang gurami
dewasa dapat mencapai 65 cm dan berat 10 kg,. Secara alami pertumbuhan paling
pesat terjadisaat mencapai 3-5 tahun. Gurami memiliki kemampuan mengambil
oksigen dari udara karena adanya labirin yang terletak diatas atau dibelakang
permukaan air. Dengan kemampuannya ini, gurami dapat hidup di perairan yang
kandungan oksigennya terbatas (Agus, dkk., 2002).
Klasifikasi ikan gurami berdasarkan ilmu taksonomi adalah sebagai berikut :
Kingdom : Animalia
Filum : Chordata
Kelas : Pisces
Ordo : Anabantoidei
Famili : Osphronemidae
Marga : Osphronemus
Jenis : Osphronemus goramy
2.2.2 Ikan Mas (Cyprinus carpio)
Ikan mas merupakan jenis ikan darat yang hidup di perairan dangkal yang
mengalir tenang dengan suhu sejuk. Jenis ikan konsumsi air tawar ini banyak
digemari masyarakat karena rasa dagingnya gurih dan memiliki kadar protein
tinggi. Ikan mas yang lazim disebut ikan karper terkenal cukup mudah
pemeliharaannya. Ini disebabkan pertumbuhannya yang relatif cepat, tahan
terhadap penyakit dan parasit, adaptif terhadap lingkungan yang terbatas, dan
kelambatan permulaan matang kelamin. Ikan mas tergolong jenis ikan yang sangat
toleran terhadap fluktuasi suhu air antara 14-230C. Namun, suhu air optimum
yang baik untuk pertumbuhan ikan mas berkisar 22-280C . Ikan mas mampu
beradaptasi terhadap perubahan kandungan oksigen terlarut dalam perairan. Ikan
mas juga tidak sensitif terhadap perlakuan fisik seperti seleksi, penampungan,
penimbangan, dan pengangkutan. Karena sifatnya yang sangat adaptif terhadap
ikan mas dapat dilakukan setelah ikan berumur 3-4 bulan terhitung sejak benih
mulai ditebar di kolam pembesaran. Ikan Mas memiliki bentuk tubuh yang agak
memanjang dan sedikit memipih ke samping. Sebagian besar tubuh ikan mas di
tutupi oleh sisik. Moncongnya terletak di ujung tengah dan dapat di sembulkan.
Pada bibirnya yang lunak terdapat dua pasang sungut dan tidak bergerigi. Pada
bagian dalam mulut terdapat gigi kerongkongan sebanyak tiga baris berbentuk
geraham (Bachtiar, 2003).
Klasifikasi ikan gurami berdasarkan ilmu taksonomi adalah sebagai berikut :
Kingdom : Animalia
Filum : Chordata
Kelas : Pisces
Ordo : Cypriniformes
Famili : Cyprinidae
Genus : Cyprinus
Species : Cyprinus carpio
2.2.3 Penyakit Ikan
Penyakit ikan dapat didefenisikan sebagai segala sesuatu yang dapat
menimbulkan gangguan suatu fungsi atau struktur dari alat tubuh atau sebagian
alat tubuh, baik secara langsung maupun tidak langsung. Penyakit yang
menyerang ikan tidak datang begitu saja, melainkan melalui proses hubungan
antara tiga faktor, yaitu kondisi lingkungan, kondisi inang, dan adanya jasad
patogen. Dengan demikian, timbulnya serangan penyakit merupakan hasil
interaksi yang tidak serasi antara lingkungan, ikan, dan jasad/organism penyakit.
pertahanan diri yang dimilikinya menjadi lemah dan akhirnya mudah diserang
oleh penyakit (Kordi, 2004).
Pada umumnya penyakit infeksi bersifat musiman, terutama pada daerah
tropis. Di daerah sub – tropis, seperti Amerika Serikat, wabah penyakit infeksi
umumnya terjadi pada bulan Maret – Juni dan September – Oktober, ketika suhu
air mencapai 20-28oC. Kisaran suhu tersebut merupakan suhu optimum bagi
sebagian besar pathogen ikan (Irianto, 2005).
Menurut Kordi, 2004, penyakit yang disebabkan oleh bakteri yang
menyerang ikan-ikan budidaya, baik dipelihara di kolam, tambak, keramba, dan
wadah-wadah dan cara penanggulangannya adalah sebagai berikut:
1. Bakteri perusak sirip
Bakteri perusak sirip adalah jenis bakteri Mycobacter sp, Vibrio sp, Pseudomonas
sp, dan bakteri coccus gram negatif. Ikan yang terserang bakteri ini mengalami
kerusakan sirip-sirip terutama pada ujung-ujungnya.
Cara penanggulangan :
Ikan yang terserang penyakit direndam dengan kloramfenikol 50 ppm
selama 2 jam.
2. Penyakit Bercak merah
Penyakit bercak merah disebabkan oleh Aeromonas hydrophila. Bakteri
Aeromonas hydrophila menyerang hampir semua jenis ikan air tawar yang
dipelihara di tambak bersalinitas rendah. Kerugian yang ditimbulkan sangat besar,
sebab dalam waktu relatif singkat puluhan ton ikan mati secara masal, baik ukuran
benih maupun induk. Serangan bakteri ini bersifat laten, jadi tidak
Serangan bakteri ini baru terlihat apabila ketahanan tubuh ikan menurun akibat
stress yang disebabkan oleh penurunan kualitas air, kekurangan pakan atau
penanganan ikan yang kurang baik.
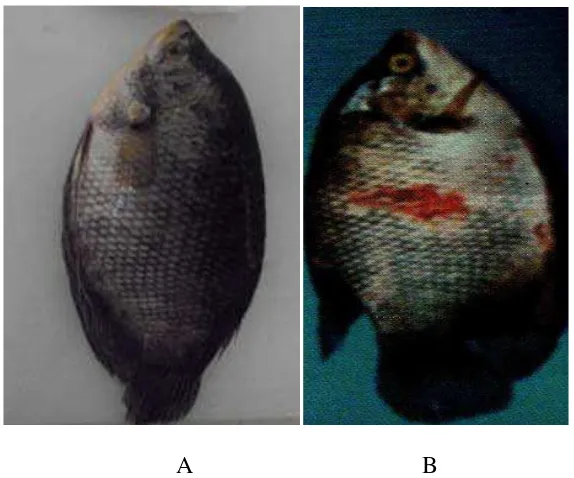
A B
Gambar 2. Ikan gurami yang tidak terserang penyakit (A) Ikan gurami yang
terserang penyakit bercak merah (B) (sumber: Irianto, 2005)
Cara penanggulangan :
Cara penanggulanagannya dapat dilakukan dengan penyuntikan menggunakan
kloramfenikol 20-60 mg/kg.
3. Columnaris
Penyakit columnaris disebabkan oleh bakteri Flexibacter columnaris.
Bakteri Columnaris menyerang hampir semua jenis ikan air tawar. Gejala yang
timbul ditandai dengan ikan kehilangan nafsu makan, terbentuknya luka terutama
di kepala, sirip, kulit badan bagian belakang, ekor dan insang. Pada mulanya luka
yang terbentuk cukup kecil, kemudian berwarna keputih-putihan,
rontok. Jika organisme ini menyerang insang, sering menyebabkan kematian
massal.
Cara penanggulangan:
Penanggulangan dilakukan dengan cara merendam Kloramycetin 5-10 ppm
selama 1-2 menit
4. Vibrosis
Penyakit vibrosis disebabkan oleh bakteri Vibrio sp. Bakteri Vibrio sp
menyerang ikan air tawar dan ikan-ikan laut budidaya. Umumnya ikan yang
diserang vibrosis memperlihatkan gejala-gejala seperti, ikan kehilangan nafsu
makan, kulit ikan menjadi gelap, insang ikan pucat, sering terjadi pembengkakan
pada kulit yang lama kelamaan akan pecah menjadi bisul dan mengeluarkan
cairan nanah berwarna kuning kemerah-merahan, terjadi perdarahan pada dinding
perut dan permukaan jantung, dan jika dilakukan pembedahan akan terlihat
pembengkakan dan kerusakan pada jaringan hati, ginjal, limpa.
Cara penanggulangan:
Penanggulangan dilakukan dengan cara memberikan kloramfenikol 0,2 g/kg
pakan selama 4 hari berturut-turut.
5. Furuncolosis
Penyakit furuncolosis disebabkan oleh bakteri Aeromonas salmonicia.
Ikan yang terserang penyakit ini menunjukkan gejala-gejala seperti, ikan
kehilangan nafsu makan, kulit ikan melepuh, insang terlihat pucat, mata menonjol,
dan terdapat perdarahan pada kulit dan insang. Bila dibedah, maka organ-organ
Cara penanggulangan:
Ikan yang telah terserang penyakit di obati dengan memberikan pakan
yang dicampurkan dengan kloramfenikol sebanyak 1 g /Kg pakan dan diberikan
selama 10 hari berturut-turut.
2.3 Kromatografi
Kromatografi merupakan suatu proses pemisahan yang mana analit-analit
dalam sampel terdistribusi antara dua fase, yaitu fase diam dan fase gerak. Fase
diam dapat berupa bahan padat atau porus dalam bentuk molekul kecil atau dalam
bentuk cairan yang dilapiskan pada pendukung padat atau dilapiskan pada dinding
kolom. Fase gerak dapat berupa gas atau cairan. Jika gas digunakan sebagai fase
gerak, maka prosesnya dikenal sebagai kromatografi gas. Dalam kromatografi cair
dan juga kromatografi lapis tipis, fase gerak yang di gunakan selalu cair (Rohman,
2009).
2.3.1 Pembagian Kromatografi
Menurut (Rohman, 2009), kromatografi dapat dibedakan atas berbagai
macam, tergantung pada pengelompokannya. Berdasarkan pada mekanisme
pemisahannya, kromatografi dibedakan menjadi :
a. Kromatografi adsorbsi
b. Kromatografi partisi
c. Kromatografi pasangan ion
d. Kromatografi penukar ion
e. Kromatografi ekslusi ukuran
Berdasarkan alat yang digunakan, kromatografi dapat dibagi atas :
a. Kromatografi kertas
b. Kromatografi lapis tipis
c. Kromatografi cair kinerja tinggi
d. Kromatografi gas
2.3.2 Kromatografi Cair Kinerja Tinggi
Kromatografi Cair Kinerja Tinggi atau KCKT atau biasa juga disebut
dengan HPLC (High Performance Liquid Chromatography) dikembangkan pada
akhir tahun 1960-an dan awal tahun 1970-an. Saat ini, KCKT merupakan teknik
pemisahan yang diterima secara luas untuk analisis dan pemurnian senyawa
tertentu dalam suatu sampel pada sejumlah bidang, antara lain: farmasi,
lingkungan, bioteknologi, polimer, dan industri-industri makanan. Kegunaan
umum KCKT adalah untuk pemisahan sejumlah senyawa organik, anorganik,
maupun senyawa biologis; analisis ketidak murnian (impurities); analisis
senyawa-senyawa tidak mudah menguap (non-volatil); penentuan
molekul-molekul netral, ionic, maupun zwitter ion; isolasi dan pemurnian senyawa;
pemisahan senyawa yang strukturnya hampir sama; pemisahan
senyawa-senyawa dalam jumlah sekelumit, dalam jumlah banyak, dan dalam skala proses
industri. KCKT merupakan metode yang tidak destruktif dan dapat digunakan
baik untuk analisis kualitatif maupun kuantitatif.
KCKT paling sering digunakan untuk menetapkan kadar senyawa-senyawa
tertentu seperti asam-asam amino, asam-asam nukleat, dan protein-protein dalam
cairan fisiologis; menentukan kadar senyawa-senyawa aktif obat, produk hasil
memonitor sampel-sampel yang berasal dari lingkungan, memurnikan senyawa
dalam suatu campuran; kontrol kualitas; dan mengikuti jalannya reaksi sintesis.
Kromatografi merupakan teknik yang mana solut atau zat-zat terlarut terpisah oleh
perbedaan kecepatan elusi, dikarenakan solute-solut ini melewati suatu kolom
kromatografi. Pemisahan solut-solut ini diatur oleh distribusi solut dalam fase
gerak dan fase diam. Penggunaan kromatografi cair secara sukses terhadap suatu
masalah yang dihadapi membutuhkan penggabungan secara tepat dari berbagai
macam kondisi operasional seperti jenis kolom., fase gerak, suhu kolom, dan
ukuran sampel (Rohman, 2007).
Maksud dan tujuan analisis dengan KCKT hanya ada dua hal yaitu didapatnya
pemisahan yang baik dalam waktu proses yang relatif singkat.
Menurut, Mulja dan Suharman, 1995, untuk tercapainya maksud dan tujuan
analisis dengan KCKT diatas maka diperlukan penatalaksanaan yang betul-betul
sudah dipersiapkan dan diperhitungkan, antara lain :
- Diplih pelarut pengembang atau pelarut pengembang campur yang sesuai
untuk komponen yang dipisahkan
- Berkaitan dengan pemilihan pelarut pengembang (solvent) maka kolom
yang dipakai juga harus diperhatikan.
- Detektor yang memadai
- Pengetahuan dasar KCKT yang baik serta pengalaman dam keterampilan
kerja yang baik
- Keuntungan metode Kromatografi Cair Kinerja Tinggi antara lain :
- dapat dilaksanakan pada suhu kamar
- pelarut pengembang yang dapat dipakai berulangkali, demikian juga
dengan kolomnya.
- ketepatan dan ketelitiannya relative tinggi dijajaran teknik analisis
fisiko-kimia.
2.3.3 Jenis Kolom
Dilihat dari jenis fase diam dan fase gerak, maka kromatografi cair kinerja
tinggi (kolomnya) dibedakan atas :
a. Kromatografi Fase Normal
Kromatografi dengan kolom konvensional dimana fase diamnya “normal”
bersifat polar, misalnya silika gel, sedangkan fase geraknya bersifat non
polar.
b. Kolom fase terbalik (Reversed Phase Colomn)
Kromatografi dengan kolom yang fase diamnya bersifat non polar,
sedangkan fase geraknya bersifat polar, kabalikan dari fase normal.
Kromatografi fase terbalik sebenarnya sudah lama dipikirkan oleh Boscott
(1947), tetapi baru sekitar tahun 1948 Boldingh berhasil memisahkan
asam-asam lemak dengan rantai panjang melalui suatu kolom yang berisi
bahan karet (non polar) dan dielusi dengan larutan pengembang campur
yang polar yaitu campuran air-metanol-aseton (Mulja dan Suharman,
1995).
2.3.4. Jenis Pompa
Sistem pompa kromatografi cair kinerja tinggi sudah diprogram untuk
dapat melakukan elusi dengan satu atau lebih macam pelarut. Dikenal dua sistem
1. Sistem Elusi Isokratik
Pada sistem ini elusi dilakukan dengan satu macam larutan pengembang
atau lebih dari satu macam larutan pengembang (pelarut pengembang campur)
dengan perbandingan yang tetap.
2. Sistem Elusi Gradien
Pada system ini elusi dilakukan dengan pelarut pengembang campur yang
perbandingannya berubah dalam waktu tertentu (Suharman dan Mulja, 1995).
2.3.5 Faktor-Faktor Yang Digunakan Untuk Evaluasi kinerja kolom
Kualitas pemisahan dengan kromatografi kolom dapat dikontrol dengan
melakukan serangkaian uji kesesuaian sistem yang meliputi:
1. Efisiensi kolom
2. Resolusi atau daya pisah
3. Simetrisitas puncak
4. Faktor retensi atau kapasitas kolom
1. Efisiensi Kolom
Salah satu karakteistik system kromatografi yang paling penting adalah
efisiensi atau jumlah lempeng teoritis (N). Ukuran efisiensi kolom adalah jumlah
lempeng (plate number, N) yang didasarkan pada konsep lempeng teoritis pada
distilasi. Bilangan lempeng (N) yang tinggi disyaratkan untuk pemisahan yang
baik yang nilainya sebanding dengan semakin panjangnya kolom (L) dan semakin
kecilnya nilai H. Istilah nilai H merupakan tinggi ekivalen lempeng teoritis atau
HETP (High Eqivalent Theoritical Plate), yang mana merupakan panjang kolom
yang dibutuhkan untuk menghasilkan satu lempeng teoritis. Kolom yang baik
mempunyai nilai H yang rendah. Semakin kecil ukuran partikel, maka semakin
tinggi bilangan lempeng teoritis. Kondisi optimum diperoleh dengan melihat
hubungan antara tinggi lempeng teoritis dan kecepatan alir.
2. Resolusi (daya pisah)
Kolom yang lebih efisien akan mempunyai resolusi yang baik. Tingkat
pemisahan komponen dalam suatu campuran dengan metode kromatografi
direfleksikan dalam kromatogram yang dihasilkan. Untuk hasil pemisahan yang
baik, puncak-puncak dalam kromatogram harus terpisah secara sempurna dari
puncak lainnya dengan sedikit tumpang tindih atau tidak tumpang tindih.
3. Faktor Asimetri
Suatu situasi yang menunjukkan kinerja kromatografi yang kurang baik
adalah ketika ditemukan suatu puncak yang mengalami pengekoran (tailing)
sehingga menyebabkan puncak tidak setangkup atau tidak simetri. Kromatogram
yang memberikan harga TF=1 menunjukkan bahwa kromatogram tersebut bersifat
setangkup atau simetris. Harga TF>1 menunjukkan bahwa kromatogram
mengalami pengekoran (tailing). Semakin besar harga TF maka kolom yang
dipakai semakin kurang efisien. Dengan demikian harga TF dapat digunakan
untuk melihat efisiensi kolom kromatografi (Rohman, 2009).
Ada dua cara yang digunakan untuk pengukuran derajat asimetri puncak,
yakni factor ikutan dan factor asimetris. Faktor ikutan/tailing factor (Tf) seperti
yang diterangkan dalam Farmakope Amerika Serikat (USP) Edisi Ketigapuluh
dihitung dengan menggunakan lebar puncak pada ketinggian 5% (W0,05),
rumusnya dituliskan sebagai berikut:
Tf=
a b a
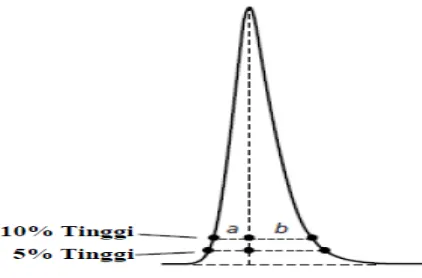
Dengan nilai a dan b merupakan setengah lebar puncak pada ketinggian 5%
[image:35.595.186.397.149.288.2]seperti yang ditunjukkan pada gambar 5
Gambar 3. Pengukuran derajat asimetri puncak (sumber Dolan, 2003).
Sementara itu, factor asimetri/asymmetry factor (As) dihitung dengan
rumus berikut:
As=
a b
Namun, nilai a dan b dalam perhitungan faktor asimetri merupakan setengah lebar
puncak pada ketinggian 10% seperti yang ditunjukkan di Gambar 5. Jika nilai a
sama dengan b, maka faktor ikutan dan asimetri bernilai 1. Kondisi ini
menunjukkan bentuk puncak yang simetris sempurna (Dolan, 2003).
2.3.6 Proses Pemisahan dalam Kolom Kromotografi Cair
Pemisahan dalam kromatografi cair disebabkan oleh distribusi kesetimbangan dari
senyawa-senyawa yang berbeda antara partikel fase diam dan larutan fase gerak
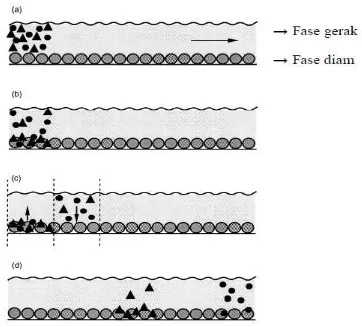
(Synder dan Kirkland, 1979). Contohnya, campuran dua komponen dimasukkan
kedalam sistem kromatografi (partikel dan ) (Gambar 4a). Di mana
komponen cenderung menetap di fase diam dan komponen lebih
cenderung didalam fase gerak (Gambar 4b). Masuknya eluen (fase gerak) yang
dalam fase gerak diadsorpsi sebagian oleh permukaan fase diam berdasarkan pada
koefisien distribusinya, sedangkan molekul yang sebelumnya diadsorpsi akan
mumcul kembali di fase gerak (Gambar 4c). Setelah proses ini terjadi berulang
kali, kedua komponen akan terpisah. Komponen yang lebih suka dengan fase
gerak akan berpindah lebih cepat daripada komponen yang cenderung
menetap di fase diam, sehingga komponen akan muncul terlebih dahulu dalam
kromatogram, kemudian baru diikuti oleh komponen akan muncul terlebih
dahulu dalam kromatogram, kemudian baru diikuti oleh komponen (Gambar
[image:36.595.138.500.351.678.2]4c) (Meyer, 2004).
Gambar 4. Ilustrasi proses pemisahan yang terjadi di dalam kolom KCKT.
2.4 Validasi Metode
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter
tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa
parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Menurut Farmakope Amerika Serikat (USP/United State Pharmacopeia) Edisi
Ketigapuluh, ada 8 karakteristik utama yang digunakan dalam validasi metode,
yakni akurasi, presisi, spesivisitas, batas deteksi, batas kuantitasi, linearitas,
rentang dan kekuatan.
2.4.1 Akurasi (Kecermatan)
Akurasi adalah ukuran yang menunjukkan derajat kedekatan hasil analisis
dengan kadar analit yang sebenarnya, kecermatan dinyatakan sebagai persen
perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan
dengan dua cara yaitu metode simulasi (spike placebo recovery) dan metode
penambahan baku (standard addition method).
2.4.2 Presisi (Keseksamaan)
Presisi biasanya dinyatakan sebagai simpangan baku relatif dari jumlah
sampel yang berbeda signifikan secara statistic (Rohman, 2007). Berdasarkan
rekomendasi ICH (The International Conference on the Harmonisation),
karakteristik presisi dilakukan pada 3 tingkatan, yakni keterulangan
(repeatability), presisi antara (intermediate precision), dan reprodusibilitas
(reproducibility). Keterulangan dilakukan dengan cara menganalisis sampel yang
sama oleh analisis yang sama menggunakan instrumen yang sama dalam periode
Sedangkan reprodusibilitas dikerjakan oleh analis yang berbeda dan
dilaboratorium yang berbeda (Epshtein, 2004).
2.4.3 Spesifisitas (Selektivitas)
Spesifisitas suatu metode adalah kemampuannya yang hanya mengukur at
tertentu saja secara cermat dan seksama dengan adanya komponen lain yang
mungkin ada dalam matriks sampel (Harmita, 2004).
2.4.4 Batas Deteksi (Limit of Detection/LOD)
Batas deteksi didefenisikan sebagai konsentrasi analit terendah dalam
sampel yang masih dapat dideteksi, meskipun tidak selalu dapat dikuantitasi.
Batas deteksi merupakan batas uji yang secara spesifik menyatakan apakah analit
diatas atau dibawah nilai tertentu (Rohman, 2009).
2.4.5 Batas Kuantitasi (Limit of Quantitation/ LOQ)
Batas kuantitasi didefenisikan sebagai konsentrasi analit terendah dalam
sampel yang dapat ditentukan dengan presisi dan akurasi yang dapat diterima pada
kondisi operasional metode yang digunkan (Rohman, 2009).
2.4.6 Linearitas
Linearitas dapat ditentukan secara langsung dengan pengukuran analit atau
sampel yang di-spiked pada konsentrasi sekurang-kurangnya lima titik konsentrasi
yang mencakup seluruh rentang seluruh konsentrasi kerja (Ermer, 2005).
2.4.7 Rentang
Rentang metode adalah pernyataan batas terendah dan tertinggi analit yang
sudah ditunjukkan dapat ditetapkan dengan kecermatan, keseksamaan, dan
2.4.8 Kekuatan (Robustness)
Kekuatan dievaluasi dengan melakukan perubahan parameter dalam
melakukan metode analitik seperti pH larutan dapar, suhu kolom KCKT, waktu
pengekstraksian analit, komposisi pengekstaksi, perbandingan konsentrasi fase
gerak, laju alir fase gerak dan tipe kolom serta pabrik pembuat kolom (Epshtein,
2004)
BAB III
METODE PENELITIAN
3.1Waktu dan Tempat Penelitian
Penelitian dilakukan di laboratorium Penelitian Fakultas Farmasi Universitas
Sumatera Utara pada bulan Januari sampai Maret 2011.
3.2 Alat - Alat
Alat-alat yang digunakan dalam penelitian ini adalah seperangkat instrumen
KCKT lengkap (Hitachi) dengan pompa (L-2130), injektor autosampler L-2200,
kolom Luna Phenomenex 5µ m C18 (250 mm x 4,60 mm), detektor UV-Vis
L-2420, degasser (DGU 20 AS), wadah fase gerak, vial khusus autosampler,
sonifikator (Branson 1510), pompa vakum (Gast DOA - P604 – BN), neraca
analitik (Mettler Toledo), penyaring PTFE 0,5 µm, penyaring nitrat selulosa 0,45
µ m dan 0,2 µ m, seperangkat alat-alat gelas, spektrofotometer UV-Vis (Shimadzu
uv 1800), blender, vortex (Boeco-Germany), sentrifus (Hitachi CF16RXII).
3.3 Bahan - Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah asetonitril pro
analisa (E. Merck), n-heksan pro analisa (E. Merck), metanol gradient grade for
liquid chromatography (E. Merck), NaCl pro analisa (E. Merck), aquabidestilata
(PT. Ikapharmindo Putramas), kloramfenikol Baku Pembanding Farmakope
Indonesia (BPFI), kloramfenikol baku pabrik (PT. Varia Sekata), ikan gurami dan
ikan mas.
3.4 Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif di empat lokasi yaitu, Pasar
dan Pasar Modern (PG4 dan PM4). (Untuk ikan gurami diberi kode PG dan ikan
mas diberi kode PM).
3.5 Prosedur Penelitian
3.5.1 Penyiapan Bahan
3.5.1.1 Pembuatan Pelarut
Pelarut terdiri dari campuran metanol HPLC grade dan air dengan
perbandingan 55 : 45 (perbandingan fase gerak hasil optimasi).
3.5.1.2 Pembuatan Fase Gerak Metanol - Air
Metanol 500 ml disaring dengan menggunakan penyaring PTFE 0,5 µm
dan diawaudarakan selama 30 menit.
Air 500 ml disaring dengan menggunakan penyaring nitrat selulosa 0,45
µ m dan diawaudarakan selama 30 menit.
3.5.2 Penentuan Panjang Gelombang Maksimum
Sejumlah 50 mg bahan baku kloramfenikol ditimbang seksama, dimasukkan
ke dalam labu tentukur 50 ml, dilarutkan dengan 5 ml metanol lalu dicukupkan
sampai garis tanda dengan air dan dikocok sampai homogen, sehingga diperoleh
larutan dengan konsentrasi 1000 µg/ml, larutan induk baku I (LIB I). Dipipet
sebanyak 1,5 ml LIB I, dimasukkan ke dalam labu tentukur 100 ml, dicukupkan
sampai garis tanda dengan air dan dikocok sampai homogen, sehingga diperoleh
larutan dengan konsentrasi 15 µg/ml. Larutan diukur serapannya pada panjang
gelombang 200 - 400 nm.
3.5.3 Prosedur Analisis
Masing-masing unit diatur, kolom yang digunakan C18 (250 mm x 4,60
mm), detektor UV-VIS pada panjang gelombang analisis yang diperoleh. Pompa
menggunakan mode aliran tetap dengan sistem elusi isokratik.
Setelah alat KCKT dihidupkan, maka pompa dijalankan dan fase gerak
dibiarkan mengalir selama 30 menit sampai diperoleh garis alas yang datar,
menandakan sistem tersebut telah stabil.
3.5.3.2 Pembuatan Larutan Induk Baku Kloramfenikol
Sejumlah 50 mg Baku Pembanding kloramfenikol ditimbang seksama,
dimasukkan ke dalam labu tentukur 250 ml, dilarutkan dengan 5 ml metanol
kemudian dicukupkan sampai garis tanda dengan pelarut dan dikocok sampai
homogen, sehingga diperoleh larutan dengan konsentrasi 200 µg/ml, Larutan
Induk Baku (LIB I).
3.5.3.3 Penentuan Perbandingan Komposisi Fase Gerak yang Optimum untuk Analisa
Larutan Induk Baku kloramfenikol dipipet5 ml dan dimasukkan ke dalam
labu tentukur 100 ml, dicukupkan dengan pelarut hingga garis tanda dan dikocok
sampai homogen sehingga diperoleh larutan kloramfenikol dengan konsentrasi 10
µg/ml, disaring dengan penyaring nitrat selulosa 0,2 µm, diawaudarakan selama
10 menit, kemudian diinjeksikan ke dalam sistem KCKT menggunakan vial
autosampler sebanyak 10 µ l, menggunakan fase gerak metanol - air, dengan
perbandingan (40 : 60), (50 : 50), (55 : 45), (60 : 40), (65 : 35), (70 : 30), dan (75 :
25), dengan laju alir 1 ml/menit, dan dideteksi pada panjang gelombang 278 nm.
3.5.3.4 Pembuatan Kurva Kalibrasi Kloramfenikol Baku
Larutan Induk Baku (LIB I) dipipet sebanyak 5 ml, dimasukkan ke dalam
hingga homogen sehingga diperoleh larutan kloramfenikol dengan konsentrasi 10
µg/ml, Larutan Induk Baku II (LIB II). Larutan Induk Baku II dipipet 0,3 ; 0,7 ; 1
; 3 ; 5 ml dimasukkan ke dalam labu tentukur 100 ml, diencerkan dengan pelarut
hingga garis tanda, dikocok sampai homogen sehingga diperoleh konsentrasi 0,03
; 0,07 ; 0,1 ; 0,3 ; 0,5 µg/ml. Kemudian masing-masing larutan disaring dengan
penyaring nitrat selulosa 0,2 µm, dan diinjeksikan ke sistem KCKT menggunakan
vial autosampler sebanyak 10 µ l dideteksi pada panjang gelombang maksimum
yang dipilih 278 nm. Selanjutnya dari luas area yang diperoleh pada kromatogram
dibuat kurva kalibrasi, dihitung persamaan garis regresi dan faktor korelasinya.
3.5.3.5 Preparasi Sampel
Ikan gurami dan ikan mas dengan berat 500 g, dicuci bersih, sisiknya
dibersihkan, dipisahkan seluruh bagian daging dari tulangnya, dikumpulkan
seluruh dagingnya, dihaluskan dengan blender, diaduk agar homogen, ditimbang
kurang lebih sebanyak 5 g.
3.5.3.6 Penetapan Kadar Residu Kloramfenikol dalam Sampel
Sampel yang telah homogen dan ditimbang sebanyak 5 g, dimasukkan ke
dalam tabung sentrifus bertutup, ditambahkan 10 ml asetonitril dikocok dengan
vortex selama 30 detik, dan disentrifus dengan kecepatan 3000 rpm selama 10
menit. Supernatan dipisahkan dari endapan. Kemudian ditambahkan Asetonitril
10 ml ke dalam endapan, dikocok dengan vortex selama 30 detik, dan disentrifus
dengan kecepatan 3000 rpm selama 10 menit. Supernatan dipisahkan dari endapan
dan digabungkan dengan supernatan pertama. Gabungan supernatan ditambahkan
1,5 g NaCl, dikocok dengan vortex selama 1 menit, dan disentrifus dengan
Supernatan ditambahkan 5 ml n-heksana, dikocok dengan vortex selama 30 detik,
dan didiamkan sampai terpisah sempurna hingga terbentuk 2 lapisan, yaitu lapisan
n-heksan di bagian atas dan lapisan asetonitril di bagian bawah. Lapisan n-heksan
dibuang dengan menggunakan pipet secara hati-hati. Perlakuan n-heksan diulangi
sekali lagi. Lapisan asetonitril dikeringkan dengan alat penguap. Ekstrak
dilarutkan hingga 5 ml dengan pelarut kemudian disaring dengan penyaring nitrat
selulosa 0,2 µ m, dan diawaudarakan selama 10 menit, kemudian diinjeksikan
sebanyak 10 µ l ke sistem KCKT menggunakan vial autosampler dan dideteksi
pada panjang gelombang maksimum yang dipilih 278 nm dengan perbandingan
fase gerak metanol : air (55:45) dan laju alir 1 ml/menit. Dilakukan sebanyak 6
kali pengulangan untuk setiap sampel. Kadar dapat dihitung dengan
mensubtitusikan luas area sampel pada Y dari persamaan regresi : Y = aX + b.
Bagan penetapan kadar residu kloramfenikol dalam sampel dapat dilihat pada
Berdasarkan metode SNI 7541.1:09, bagan penetapan kadar residu kloramfenikol
dalam ikan adalah sebagai berikut:
5 gram ikan yang telah dihomogenkan
ditambah 10 ml asetonitril
disentrifus 10 menit
dikocok 30 detik dengan vortex
supernatan I endapan
ditambah 10 ml asetonitril
dikocok 30 detik dengan vortex
disentrifus 10 menit
supernatan II endapan
kumpulan supernatan I dan II
ditambah 1,5 g NaCl
dikocok 60 detik dengan vortex
disentrifus 5 menit
endapan supernatan
ditambah 5 ml n-heksan
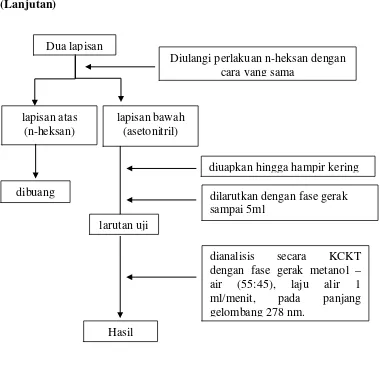
(Lanjutan)
[image:46.595.113.493.88.453.2]
Gambar 5. Bagan Prosedur Penetapan Kadar Residu Kloramfenikol dalam Sampel.
3.5.3.7 Analisis Data Secara Statistik
Menurut Usman dan Purnomo (2006) data perhitungan kadar dianalisis
secara statistik menggunakan uji t.
Rumus yang digunakan untuk menghitung simpangan baku adalah:
1 ) ( 2 − − =
∑
n X X SDSedangkan untuk mendapatkan thitung digunakan rumus:
t hitung
n SD X X / − = Dua lapisan lapisan atas (n-heksan) lapisan bawah (asetonitril)
diuapkan hingga hampir kering
dilarutkan dengan fase gerak sampai 5ml
larutan uji
Diulangi perlakuan n-heksan dengan cara yang sama
Hasil
dianalisis secara KCKT dengan fase gerak metanol – air (55:45), laju alir 1 ml/menit, pada panjang gelombang 278 nm.
Data diterima jika -t tabel < t hitung < t tabel pada interval kepercayaan 95% dengan
derajat kebebasan dk= n-1 dan nilai α = 0,05
Keterangan :
SD = Standard deviation/simpangan baku
X = Kadar dalam satu perlakuan
X = Kadar rata-rata dalam satu sampel
n = Jumlah perlakuan
Untuk menghitung kadar kloramfenikol dalam sampel secara statistik
dapat digunakan rumus:
Kadar Kloramfenikol (μ)= X
n SD x t(1−1/2α).dk
±
Keterangan:
μ = Kadar sebenarnya
X = Kadar sampel
n = Jumlah perlakuan
t = Harga ttabel sesuai dengan derajat kepercayaan
dk= Derajad kebebasan.
3.5.4 Metode Validasi
3.5.4.1 Akurasi
Menurut Harmita (2004), Akurasi adalah ukuran yang menunjukkan
derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Akurasi
dinyatakan dengan persen perolehan kembali (recovery) analit yang ditambahkan.
Dalam hal ini persen perolehan kembali ditentukan dengan menggunakan metode
penambahan baku (The Method of Standard Additives) yakni kadar kloramfenikol
dalam sampel ikan ditentukan terlebih dahulu, selanjutnya dilakukan penentuan
100% dan 150%. Masing-masing dilakukan sebanyak 3 kali pengulangan
kemudian dianalisis dengan perlakuan yang sama seperti pada penetapan kadar
sampel. Persen perolehan kembali dapat dihitung dengan menggunakan rumus
berikut:
% Perolehan Kembali= x 100%
Keterangan :
CF = Konsentrasi total sampel yang diperoleh dari pengukuran
CA = Konsentrasi sampel sebenarnya
C*A = Konsentrasi analit yang ditambahkan
3.5.4.2 Presisi
Menurut Rohman (2007), presisi merupakan ukuran keterangan metode
analisis dan biasanya diekspresikan sebagai simpangan baku relative dari
sejumlah sampel yang berbeda signifikan secara statistik.
Standar deviasi relatif (relative standard deviation, RSD) yang juga
dikenal dengan koefisien variansi merupakan ukuran ketepatan relatif dan
umumnya dinyatakan dalam persen. RSD dirumuskan dengan persamaan:
% 100 x X SD RSD=
Keterangan :
RSD= Relatif Standar Deviasi
SD = Standar Deviasi
X = Rata-rata
Sementara itu, SD dihitung dengan :
SD =
(
)
(
)
2
1 −
−
∑
n X X
Keterangan :
X = Nilai dari masing-masing pengukuran
X = Rata-rata (mean) dari pengukuran
N = Frekuensi penetapan
N-1 = Derajat kebebasan
3.5.4.3 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Menurut Harmita (2004), Batas Deteksi (Limit Of Detection /LOD) dan
Batas Kuantitasi (Limit Of Quantitation/LOQ) dapat dihitung dengan menggunakan
rumus sebagai berikut :
Sl SB x
LOD=3
Sl SB x
LOQ=10
(Hasil perhitungan batas deteksi (LOD) dan batas kuantitasi (LOQ) dapat dilihat
BAB IV
HASIL DAN PEMBAHASAN
4.1 Penentuan Kondisi Kromatografi untuk Mendapatkan Hasil Analisis yang Optimum
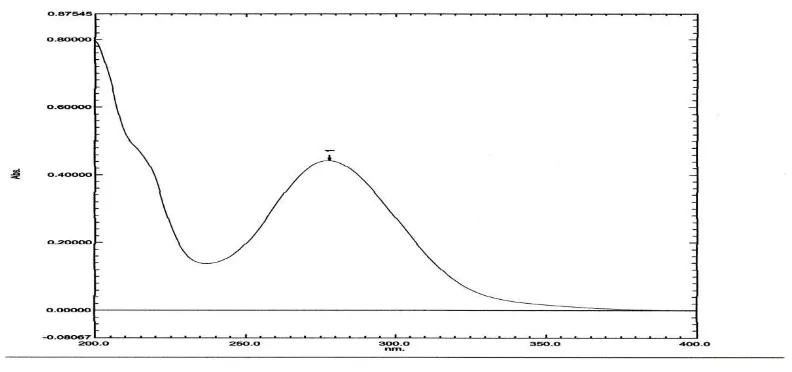
Panjang gelombang analisis ditentukan dengan membuat kurva serapan
kloramfenikol baku menggunakan spektrofotometer Ultraviolet (UV). Spektrum
hasil pengukuran kloramfenikol baku dapat dilihat pada gambar 6
Gambar 6. Kurva Serapan Kloramfenikol Baku 15 ppm Secara Spektrofotometri UV
Dari kurva diatas, dapat dilihat bahwa kloramfenikol memberikan serapan
pada panjang gelombang 278 nm. Hasil yang diperoleh berbeda dengan panjang
gelombang yang digunakan dalam prosedur SNI 7541.1:2009 yang menjadi
pedoman pada penelitian ini. Dimana menurut SNI 7541.1:2009, panjang
gelombang kloramfenikol yang digunakan adalah 270 nm. Namun menurut Ditjen
POM (1979) dan Moffat et all (2005), kloramfenikol memberikan serapan
[image:50.595.114.510.248.434.2]maksimum yang didapat adalah 8 nm. Berdasarkan hal tersebut maka analisis
kloramfenikol dalam penelitian ini digunakan panjang gelombang 278 nm.
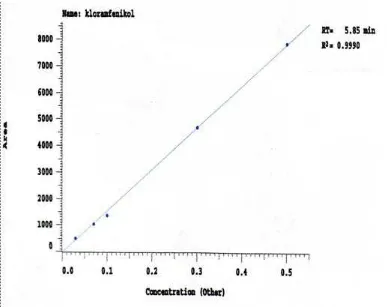
4.2 Penentuan Linearitas Kurva Kalibrasi Kloramfenikol Baku
Kurva kalibrasi kloramfenikol Baku dibuat dengan konsentrasi 0,03 ; 0,07 ;
0,1 ; 0,3 ; 0,5 µg/ml. Dari kurva kalibrasi diperoleh hubungan yang linier antara
luas area dan konsentrasi dengan koefisien korelasi (r) = 0,9997. Koefisien
korelasi yang diperoleh ini masih dalam batas penerimaan nilai koefisien korelasi
yaitu r = 0,995 (Moffat, et all). Dari hasil perhitungan, diperoleh persamaan
regresi Y=15754,4589X −44,5765. Kurva kalibrasi kloramfenikol dapat dilihat
[image:51.595.115.502.362.669.2]pada gambar 7.
Kromatogram hasil penyuntikan larutan kloramfenikol Baku untuk penentuan
kurva kalibrasi dapat dilihat pada lampiran 2. Hal. 49 dan perhitungan persamaan
regresi dapat dilihat pada lampiran 3, Hal. 52.
4.3 Penetapan Kadar Residu Kloramfenikol dalam Sampel
Penetapan kadar residu kloramfenikol dalam ikan gurami dan ikan mas telah
dilakukan mengikuti prosedur SNI 7541.1:2009, menggunakan fase gerak metanol
– air dengan perbandingan (50:50). Tetapi dari hasil penelitian tidak diperoleh
kondisi yang sesuai dan hasil yang kurang baik, dimana waktu tambat yang
dihasilkan terlalu lama dan jumlah lempeng yang kurang begitu besar. Oleh
karena itu, di lakukan optimasi fase gerak dengan memvariasikan komposisi
metanol dan air. Waktu tambat kloramfenikol yang diperoleh pada perbandingan
(50:50) adalah 7,71 menit dengan nilai asimetris 2,05 sedangkan pada
perbandingan (55:45) diperoleh waktu tambat yang relatif singkat yaitu 5,95 menit
dengan nilai asimetri 1,83 dan nilai lempeng teoritis yang paling besar diantara
perbandingan fase gerak lainnya. Menurut Rohman, 2007, Jumlah lempeng
merupakan salah satu parameter yang digunakan untuk menilai kualitas
pemisahan kromatografi yakni efisiensi. Oleh karena itu, semakin besar jumlah
lempeng yang dihasilkan akan menunjukkan bahwa kolom mampu memisahkan
komponen dalam campuran dengan baik berarti efisiensi kolom besar.
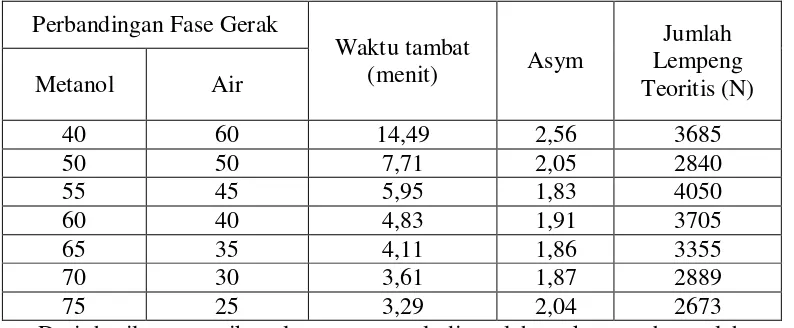
Berdasarkan hal tersebut maka perbandingan komposisi fase gerak yang
digunakan dalam penelitian ini adalah metanol – air (55:45) dengan laju alir
1ml/menit. Data hasil analisis perbandingan komposisi fase gerak dapat dilihat
pada tabel 1. Kromatogram kloramfenikol baku untuk mencari perbandingan
Tabel 1. Data Hasil Analisis Kloramfenikol Baku 10 ppm pada Berbagai Perbandingan Komposisi Fase Gerak
Perbandingan Fase Gerak
Waktu tambat
(menit) Asym
Jumlah Lempeng Teoritis (N)
Metanol Air
40 60 14,49 2,56 3685
50 50 7,71 2,05 2840
55 45 5,95 1,83 4050
60 40 4,83 1,91 3705
65 35 4,11 1,86 3355
70 30 3,61 1,87 2889
75 25 3,29 2,04 2673
Dari hasil penyuntikan larutan sampel diperoleh waktu tambat salah satu
puncak yaitu 6,02 menit. Waktu tambat ini berdekatan dengan waktu tambat
kloramfenikol baku yang dianalisis dengan KCKT pada kondisi yang sama yaitu
5,96 menit. Meskipun waktu tambat yang dihasilkan tidak sama persis, namun
puncak yang diamati dalam kromatogram sampel dapat diterima sebagai puncak
kloramfenikol karena waktu tambat 6,02 menit masih berada pada rentang waktu
tambat yang diterima dan pada sampel blanko tidak terlihat adanya puncak
kloramfenikol pada menit 5-6 (gambar 8D ). Menurut Wetson and Brown (1997),
rentang waktu tambat yang dapat diterima yaitu ± 5% dari waktu tambat baku.
Kedua kromatogram hasil analisis KCKT dapat dilihat pada gambar 8A dan 8B.
Maka untuk mempertegas hal tersebut, ditambahkan sedikit larutan
kloramfenikol baku ke dalam larutan sampel (spiking method), lalu dianalisis
kembali dengan KCKT pada kondisi yang sama. Hasil analisis menunjukkan
terjadi peningkatan luas dan tinggi puncak kloramfenikol dari yang diamati
sebelumnya. Jadi dapat disimpulkan bahwa puncak yang diamati dalam larutan
sampel adalah benar merupakan puncak kloramfenikol. Kromatogram larutan
RT Luas Puncak
5,95 166900
A
RT Luas Puncak
6,05 2762
B
C
RT Luas Puncak
6,02 34807
D
[image:54.595.117.507.77.696.2]Hasil pengolahan data penyuntikan larutan sampel secara KCKT menggunakan
kolom C18 (Phenomenex) dengan perbandingan fase gerak metanol - air (55 : 45),
volume penyuntikan 10 µ l, laju alir 1 ml/menit, detektor UV-Vis (L - 2420) pada
panjang gelombang maksimum yang diperoleh 278 nm. Kadar residu
kloramfenikol dapat dihitung dengan mensubtitusikan luas area pada Y dari
persamaan regresi Y=15754,4589X −44,5765. Hasil perhitungan residu
[image:55.595.112.506.302.586.2]kloramfenikol dalam sampel setelah diuji secara statistik dapat dilihat pada tabel2.
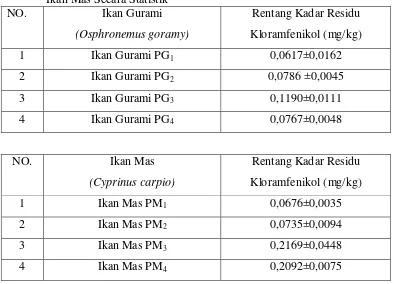
Tabel 2. Hasil Penetapan Kadar Kloramfenikol dalam Sampel Ikan Gurami dan Ikan Mas Secara Statistik
NO. Ikan Gurami
(Osphronemus goramy)
Rentang Kadar Residu
Kloramfenikol (mg/kg)
1 Ikan Gurami PG1 0,0617±0,0162
2 Ikan Gurami PG2 0,0786 ±0,0045
3 Ikan Gurami PG3 0,1190±0,0111
4 Ikan Gurami PG4 0,0767±0,0048
NO. Ikan Mas
(Cyprinus carpio)
Rentang Kadar Residu
Kloramfenikol (mg/kg)
1 Ikan Mas PM1 0,0676±0,0035
2 Ikan Mas PM2 0,0735±0,0094
3 Ikan Mas PM3 0,2169±0,0448
4 Ikan Mas PM4 0,2092±0,0075
Berdasarkan data tersebut, residu kloramfenikol yang di peroleh dari empat
pasar di kota Binjai tidak memenuhi persyaratan yang telah ditetapkan oleh RSNI
No. : 05 – TAN – 1996.
4.4 Hasil Uji Validasi
Pada penelitian ini dilakukan uji validasi metode, validasi metode dilakukan