BAB II
TINJAUAN PUSTAKA
2.1. Gastritis
2.1.1. Definisi Gastritis
Definisi gastritis adalah proses inflamasi pada mukosa dan submukosa lambung secara histopatologi. Sedangkan definisi lain dari gastritis adalah proses inflamasi pada mukosa dan submukosa lambung sebagai respon terhadap jejas (injury) yang dapat bersifat akut maupun kronik.1,16
Mukosa lambung terdiri dari sel-sel yang memproduksi asam dan enzim. Asam dan enzim ini akan berperan dalam pencernaan makanan, sedangkan mukus berperan dalam melindungi mukosa lambung dari asam. Ketika mukosa mengalami inflamasi, maka produksi asam, enzim dan mukus akan terganggu. Sampai saat ini masih belum jelas hubungan antara gambaran mikroskopi (histopatologi) dengan keluhan pada lambung. Hubungan antara gambaran mikroskopi dengan endoskopi juga tidak konsisten. Pada kebanyakan pasien dengan gambaran gastritis pada pemeriksaan PA sering tidak meunjukkan kelainan saat endoskopi.17
2.1.2. Epidemiologi Gastritis
Gastritis merupakan masalah kesehatan yang umum ditemui dalam pelayanan klinis. Sekitar 10% kunjungan pada unit gawat darurat merupakan kasus gastritis. Berdasarkan penelitian WHO (Word Health Organization) dilaporkan prevalensi gastritis dibeberapa negara sebagai berikut: Inggris 22%, China 31%, Jepang 14,5%, Kanada 35% dan Perancis 29,5%. Sekitar 1,8-2,1 juta penduduk mengalami gastritis setiap tahunnya.5,7,8
2.1.3. Etiologi Gastritis
Terdapat beberapa penyebab gastritis diantaranya infeksi kuman H.pylori, gangguan fungsi sistem imun, infeksi virus seperti: enteric rotavirus, calicivirus dan cytomegalovirus, infeksi jamur seperti: candida species, histoplasma capsulatum dan mukonacea serta obat anti inflamasi nonsteroid, konsumsi
alkohol, usia, stress oleh karena trauma, tindakan operatif, luka bakar, dll. 7,8 Infeksi kuman H.pylori merupakan penyebab gastritis yang sangat penting. Prevalensi infeksi H.pylori pada orang dewasa di negara berkembang ± 90%. Di Indonesia, prevalensi kuman H.pylori yang dinilai melalui pemeriksaan urea breath test cukup tinggi pada pasien dispepsia.9,10
Etiologi gastritis oleh Rugge atas dasar agen yang ditransmisikan yaitu : kimiawi, fisik, faktor imun, dan idiopatik. Rugge juga membagi etiologi gastritis berdasarkan 3 bentuk utama antara lain gastritis H.pylori, gastritis kimiawi, dan gastritis autoimun. Lalu Toljamo (2012) mengelompokkan etiologi gastritis menjadi 3 kelompok yaitu agen kimiawi, penyakit, dan faktor fisik/mekanik. Adapun Adibi menuliskan etiologi gastritis menjadi 2 bagian besar yaitu gastritis H. pylori dan gastritis non H. pylori. 9
Sampai saat ini belum ada klasifikasi gastritis yang dapat diterima secara luas. Salah satu klasifikasi yang digunakan oleh banyak ahli adalah the Sydney System yang diperbaharui. Klasifikasi tersebut dapat dilihat pada tabel berikut : 10
2.1.4 Patofisiologi Gastritis secara Umum
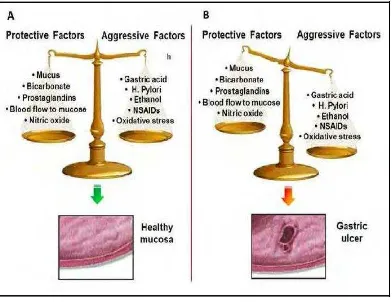
Terjadinya gastritis secara umum karena ketidakseimbangan faktor agresif dan defensif, di mana faktor agresif lebih dominan daripada faktor defensif. Yang termasuk faktor agresif antara lain asam lambung, pepsin, refluks bilier, nikotin, alkohol, NSAID, kortikosteroid, H.pylori, dan adanya radikal bebas. Yang termasuk faktor defensif antara lain mikrosirkulasi mukosa, sel epitel permukaan, prostaglandin, fosfolipid, mukus, bikarbonat, dan motilitas saluran pencernaan. 27
Gambar 2.1. Patofisiologi gastritis 26
Keterangan : (A) mukosa gaster normal akibat adanya keseimbangan antara faktor agresif dan pertahanan mukosa. (B) pembentukan ulkus gaster karena ketidakseimbangan faktor agresif dan faktor pertahanan mukosa.
2.2 Gastritis H.Pylori
panjang 1-3 µm dan lebar 0,3-0,6 µm serta berflagella pada satu ujung polenya. Bakteri ini memiliki adaptasi yang sangat baik pada kondisi asam. H.pylori mengekskresikan urease yang berperan dalam merubah urea menjadi amonia sehingga pH gaster meningkat. H.pylori juga dapat menghindari kontak dengan gastric juice yang bersifat asam melalui crossing lapisan tebal dari mukus dengan
menggunakan flagelnya. 22
Epidemiologi H.pylori sekitar 50% populasi di dunia. Di negara barat seperti USA, prevalensi H.pylori < 30% pada usia < 30 tahun dan > 75% pada usia > 60 tahun. Di Asia, prevalensi H.pylori sangat tinggi .22
Infeksi kronik dari H.pylori biasanya menyebabkan atrofi serta metaplasia dan juga diplasia serta ca gaster. H.pylori dapat menyebabkan ulkus peptikum (70%) dan ulkus duodeni (90%). Transmisi infeksi H.pylori melalui mulut ke mulut atau feses ke mulut. 22,24
2.3. Virulensi H.Pylori
Kebanyakan kasus gastritis H pylori, infeksi yang terjadi merupakan asimtomatik dan manifestasi yang terjadi hanya 10-15 % individu yang terinfeksi. Hal ini tergantung dari virulensi dari strain H pylori, serta respon imun terhadap bakteri ini. Perbedaan klinis dapat dijelaskan berdasarkan faktor bakteri dan respon imun yang mendasari.26
Dua faktor virulensi yang telah terlibat dalam proses Gastritis H.pylori adalah cytotoxin-associated gene A (CagA) dan vacuolating cytotoxin A (Vaca), yang
disekresikan oleh H. pylori. Kedua faktor virulensi ini polimorfik dan mempengaruhi banyak jalur. CagA dan vacuolating cytotoxin A (Vaca), juga telah terbukti mempengaruhi keadaan penyakit, dan kemungkinan faktor virulensi yang paling baik dipelajari dari H. pylori. 11
selanjutnya tergantung kemampuan virulensi dari strain H pylori menginduksi terjadinya perubahan morfologi, vakuolisasi dan degenerasi sel epitel lambung. 11
Saat ini makin bertambah adanya bukti-bukti mengenai pengaruh faktor-faktor CagA, VacA, alel s1m1 dan adesin A2 ( BabA2) terhadap manifestasi klinik yang dihubungkan peningkatan risiko gastritis lebih berat, atropi lambung dan/ atau kanker lambung. 11
Strain H pylori dapat dibagi atas 2 kelompok yaitu strain tipe 1 dan tipe 2. Strain tipe 1 dengan CagA dan VacA (+) sedangkan tipe 2 dengan CagA (-) dan sistesis VacA yang in aktif. Dibandingkan dengan tipe 2, tipe 1 lebih berperan dalam timbulnya ulkus peptikum, radang dan kerusakan jaringan. 11
Protein Vac A diproduksi sebagai protoksin 140-kDa yang dipecah menjadi bentuk matang 95-kDa untuk disekresi. Walaupun semua strain H pylori membawa gen VacA namun aktivitasnya bervariasi. 8,11
Aktivitas protein VacA termasuk membuat lubang membran sel-sel epitel, mengganggu aktifitas endosomal dan lisosom, menghambat fungsi sitoskleton, induksi apoptosis dan mengatur imunitas. 7,8,11
karsinoma lambung, sementara itu genotype s2m1 dan s2m2 hanya dijumpai pada ulkus lambung7,20
Gen VacA pada H. Pylori memiliki genetik heterogenenicity yang signifikan, sehingga menghasilkan hasil klinis yang berbeda. Toksin VacA diberikan kode oleh gen VacA untuk menginduksi vakuola sitoplasma dan meningkatkan permeabilitas, yang mengarah ke kerusakan sel epitel lambung. 3,11,20
Sekitar 50 % dari semua strain H.Pylori mengeluarkan VacAprotein 95 -kDa sangat imunogenik yang menginduksi vacuolization besar dalam sel epitel in vitro. Protein VacA berperan penting dalam pogenesis pada ulkus peptikum dan kanker lambung. 2,11
Gen CagA dengan segmen DNA 40 kb ditemukan pada salah satu ujung cytotoxin-associated gene pathogenicity island (CagPAI), tepatnya yang mengkode sistem sekresi tipe IV (T4SS). CagPAI dijumpai pada 95-100 % strain H pylori di Asia. Salah satu strain spesifik yang paling penting mempengaruhi patogenesis H pylori adalah CagPAI. Protein CagA sangat imunologik dan ditemukan sekitar
50-70 % dari strain H pylori. Pada perlekatan H pylori dengan sel epitel lambung, protein CagA ditranslokasi ke membrana sel-sel epitel melalui sistem sekresi tipe IV. Pada membran sel epitel, Cag A menyebabkan redistribusi protein perlekatan antar sel yang menyebabkan kebocoran sel. Selain itu, Cag A juga disebutkan dapat mengubah struktur sel lambung, sehingga membuat bakteri melekatkan diri lebih mudah. Dalam waktu panjang, toxin tersebut menyebabkan inflamasi kronis. 11,20
Pada dasarnya CagA merupakan kunci dari faktor virulensi masuknya H pylori kedalam sel host. Adanya CagA dihubungkan dengan beratnya penyakit. Bahkan, pasien kanker setidaknya dua kali lebih mungkin terinfeksi dengan strain H. pylori yang CagA positif daripada CagA negatif. 15
CagA juga dapat menimbulkan respon proinflamasi, dan mengaktifkan signal transduser dan aktivasi jalur transkripsi 3 (STAT3) yang berperan terhadap cancerogenesis pada lambung. 11
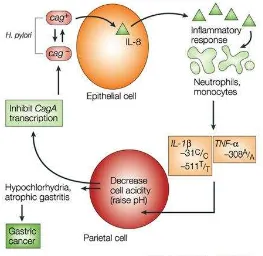
IL-1 dibandingkan dengan infeksi CagA (-), sehingga mungkin mencerminkan respon sitokin dengan strain yang spesifik. Beberapa penelitian invitro yang menggunanakan sel epitel lambung menunjukkan bahwa respon epitelial IL-8 diamati lebih spesifik dengan strain CagA (+). 13,14
Gambar 2.2 Perbedaan Patofisiologi Cag A (+), CagA (-) pada Gastritis H pylori6
2.4. Patofisologi Gastritis H pylori
H pylori memiliki flagela yang memungkinkan bergerak dan dapat menembus lapisan mukus epitel lambung. Selubung flagela sebagai pelindung terhadap asam lambung. Hal ini mendukung persistensi infeksi H pylori dalam lambung. Pergerakan flagela dirangsang aktifitas kemotaksis berbagai senyawa termasuk glutamin, histidin, lisin, alanin, musin, urea, bikarbonas dan natrium klorida.7,8,12
Penularan infeksi H pylori terjadi antar manusia secara langsung baik melalui oral-oral maupun feko-oral sehingga H pylori ditemukan pada saliva, muntahan dan tinja. 7,8,12
Di dalam lambung H pylori berhadapan dengan imunitas bawaan sel epitel lambung sebagai faktor anti mikroba berupa molekul protektif non spesifik seperti laktoferin, lisosim dan defensin. Faktor anti mikroba lain yang tersedia yaitu asam lambung. H pylori dapat beradaptasi terhadap lingkungan asam dengan memproduksi enzim urease. Urease menghidrolisis urea menjadi amoniak dan karbamat. Karbamat secara spontan pecah menjadi amoniak dan asam karbonat, yang akan meningkatkan pH lambung. 7,8
Faktor lain yang memungkinkan H pylori dapat beradaptasi terhadap lingkungannya adalah sifat bakteri tersebut mikroaerofilik, yang mempunyai pertahanan terhadap stres oksidatif akibat respons radang mukosa. Setelah berhasil beradaptasi, H pylori akan adesi pada permukaan epitel lambung dengan menggunakan adesin babA dan sabA. Namun kurang dari 1 % H pylori dapat beradesi dengan sel epitel lambung, sebagaian besar pada lapisan mukus atau dibersihkan oleh peristaltik atau pengosongan lambung. Adesi yang erat H pylori pada sel-sel epitel lambung akan memfasilitasi proses pengiriman toksin dan proses induksi respons imun, yang keduanya menyebabkan kerusakan sel-sel epitel. 7,8,12
2.5. Pemeriksaan diagnostik H.pylori
Metode diagnostik untuk mendeteksi kuman H.pylori dibagi menjadi pemeriksaan invasif dan pemeriksaan non invasif. Beberapa metode telah dikembangkan untuk mendeteksi keberadaan infeksi kuman H. pylori, yang dapat dilihat pada tabel di bawah ini.24,26
Tabel 2.2. Pemeriksaan diagnostik untuk H. pylori 26
Selain tabel di atas, terdapat keuntungan dan kerugian dari penggunaan masing-masing test untuk diagnostik H.pylori. Keuntungan dan kerugian tersebut dapat dilihat pada tabel berikut :
Tabel 2.3. Keuntungan dan kerugian test H.pylori 26
Test endoskopi Keuntungan Kerugian
1. Histologi Sensitifitas dan
spesifisitas tinggi
Mahal, memerlukan infrastruktur & personal training
Test non endoskopi
3.Faecal antigent test Identifikasi aktif H.pylori, NPV &
H.pylori dapat dideteksi dari endoskopi melalui histologi, kultur, maupun tes
urease, dengan kelebihan dan kekurangannya masing-masing. Semua metode berbasis biopsi tersebut dapat mengalami kesalahan pengambilan sampel karena infeksi tersebut bersifat patchy. Sekitar 14% pasien tidak mengalami infeksi di antrum namun memiliki H.pylori di suatu tempat di lambung, terutama jika pasien tersebut mengalami atrofi gaster, metaplasia intestinal, ataupun refluks empedu. Selain itu, pasca-eradikasi dengan efektivitas parsial, infeksi dalam kadar rendah dapat terlewatkan pada biopsi melalui endoskopi. Hal ini menimbulkan overestimasi efikasi eradikasi dan tingkat reinfeksi. Penghambat pompa proton mempengaruhi pola kolonisasi H.pylori di lambung dan mengurangi akurasi biopsi di antrum. Oleh karena itu, pedoman konsensus merekomendasikan untuk dilakukan biopsi multipel dari antrum dan korpus untuk histologi dan satu untuk metode lain (baik kultur maupun pemeriksaan urease).26
2.5.1. Pemeriksaan invasif 1. Histologi
secara histologi selain dapat disimpan, irisan dari biopsi dapat diperiksa kapanpun; dan adanya gastritis, atrofi, ataupun metaplasia intestinal dapat pula diperiksa. Spesimen biopsi dari bagian lain lambung dapat disimpan dalam formalin untuk diproses hanya jika histologi antrum tidak dapat disimpulkan.26
2. Kultur
Isolasi mikrobiologi adalah baku emas teoritis untuk identifikasi infeksi bakteri, namun kultur H.pylori kurang dapat dipercaya. Risiko pertumbuhan berlebih maupun kontaminasi membuatnya kurang sensitif, dan metode ini adalah metode yang paling tidak mudah dikerjakan bersama endoskopi. Meskipun hanya sedikit pusat kesehatan yang secara rutin menawarkan isolasi mikrobiologis H.pylori, prevalensi strain multiresisten membuat metode kultur dan uji sensitivitas terhadap antibiotik menjadi persyaratan bagi pasien dengan infeksi persisten dengan kegagalan terapi.26
3. Uji urease
Metode ini bersifat cepat dan sederhana untuk deteksi infeksi H.pylori namun hanya menunjukkan ada atau tidaknya infeksi. Pemeriksaan CLO dan pemeriksaan urease yang lebih murah ternyata memiliki sensitivitas dan spesifisitas yang serupa. Namun, sensitivitas pemeriksaan urease seringkali lebih tinggi dibanding metode berbasis biopsi karena seluruh spesimen biopsi ditempatkan di dalam media sehingga dapat menghindari sampel tambahan ataupun kesalahan proses terkait histologi maupun kultur. Sensitivitas pemeriksaan urease biopsi terlihat jauh lebih rendah (sekitar 60%) pada pasien dengan perdarahan saluran cerna atas. Namun kondisi tersebut dapat diperbaiki dengan menempatkan beberapa sampel biopsi di dalam satu vial untuk pemeriksaan. 26
2.5.2. Pemeriksaan non-invasif 1. Serologi
terhadap sampel yang disimpan. Metode ini banyak digunakan dalam studi epidemiologi, termasuk studi retrospektif untuk menentukan prevalensi maupun insiden infeksi. Individu sangat bervariasi terkait respon antibodi terhadap antigen H.pylori, dan tidak ada antigen yang sama yang dapat dikenali melalui serum dari
semua subyek. Oleh karena itu akurasi pemeriksaan serologis bergantung kepada antigen yang digunakan sehingga penting untuk melakukan validasi lokal terhadap ELISA H.pylori. Pada orang tua dengan infeksi yang telah berlangsung lama, gastritis atrofi dikaitkan dengan hasil negatif palsu. Konsumsi obat anti-inflamasi non-steroid juga dilaporkan mempengaruhi akurasi ELISA. Titer antibodi turun secara perlahan pasca-keberhasilan eradikasi sehingga serologi tidak dapat digunakan untuk menentukan eradikasi H.pylori ataupun untuk menentukan tingkat reinfeksi. Meskipun titer antibodi IgM terhadap H.pylori menurun seiring bertambahnya usia, tidak ada assay yang menunjukkan akuisisi baru. Karena infeksi ini biasanya asimtomatik, sulit untuk mengidentifikasi dan menegakkan jalur transmisi. Keuntungan metode serologi adalah perkembangan uji finger prick yang menggunakan assay fase solid terfiksir untuk mendeteksi adanya imunoglobulin H.pylori. Near patient test (NPT) dapat dilakukan di pusat kesehatan primer dan lebih sederhana dibanding 13C-urea breath test yang merupakan satu-satunya NPT yang digunakan saat ini. Namun akurasi NPT serologis lebih rendah dibanding yang dilaporkan untuk pemeriksaan ELISA standar menggunakan preparat antigen yang sama. Pemeriksaan ini sering digunakan untuk menenangkan pasien, namun saat ini belum ada studi yang membandingkan akurasi, efektivitas biaya, dan nilai jaminan dari 13C-urea breath test dengan NPT serologis di pusat kesehatan primer.26
2. Urea breath test (UBT)
14
C-urea breath test mirip dengan 13C-urea breath test namun bersifat radioaktif dan
tidak dapat dilakukan di pusat kesehatan primer.26 3. Faecal antigen test
Dalam pemeriksaan antigen di feses, ELISA sandwich sederhana digunakan untuk mendeteksi keberadaan antigen H. pylori yang terbungkus feses. Studi melaporkan sensitivitas dan spesifisitas yang mirip dengan 13C-urea breath test (>90%) dan teknik ini berpotensi untuk dikembangkan sebagai NPT. Keutungan utama dari pemeriksaan ini adalah dalam studi epidemiologi berskala besar terhadap akuisisi H. pylori pada anak.26
2.6 Peranan Sitokin Inflamasi terhadap Gastritis H.pylori
Inflamasi kronis H pylori melibatkan netrofil, limfosit (sel T dan B), sel plasma, dan makrofag, sesuai dengan tingkat degenerasi dan kerusakan selnya. Mekanisme inflamasi lainnya melalui kontak langsung dengan sel epitel lambung dan merangsang pembentukan serta pelepasan sitokin inflamasi. Adanya inflamasi karena H pylori dapat ditunjukkan dengan peningkatan IL-1 , IL-2, IL-6, IL-8 dan TNF-α. 26
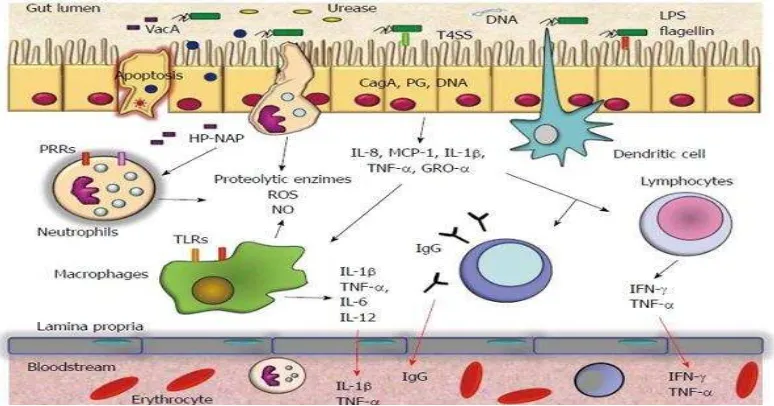
Inflamasi lambung ditemukan bervariasi pada pasien yang terinfeksi dengan H pylori tergantung dari respon imun pejamu terhadap organisme. Mekanisme
inflamasi terhadap infeksi H pylori melibatkan respon imun spesifik dan imun non spesifik, seperti terlihat pada gambar di bawah ini. 25
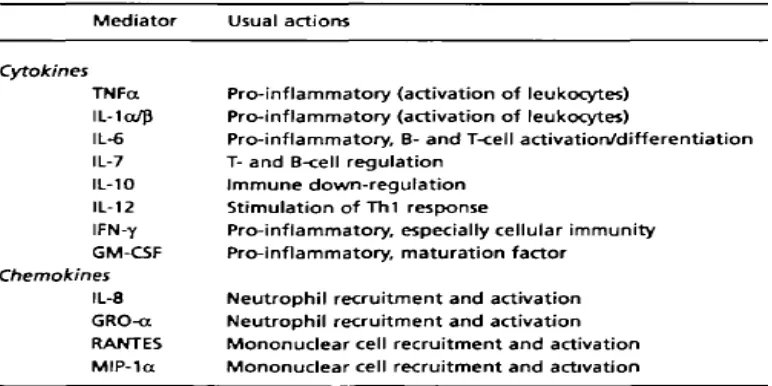
Tabel 2.4. Sitokin yang dihasilkan sebagai implikasi dari gastritis H. pylori18
TNF-α berperan untuk meningkatkan reaksi inflamasi dan diyakini berperan penting dalam kerusakan mukosa gaster akibat H.pylori. TNF-α menyebabkan kaskade inflamasi terhadap infeksi, respons inflamasi berlebihan di mukosa gaster yang berhubungan dengan inhibisi sekresi asam lambung dan kerentanan yang lebih tinggi terhadap Ca gaster.20 Pada gastritis kronis terjadi inflamasi pada mukosa lambung selama >2 minggu sehingga terjadi peningkatan sitokin pada darah.23
Infeksi H.pylori berkontribusi terhadap rekrutmen neutrofil dan limfosit yang menyebabkan kerusakan epitel melalui pelepasan sitokin, salah satunya TNF-α. Bodger et al melaporkan bahwa ada hubungan signifikan antara IL-6, IL-8, TNF-α pada pasien yang terinfeksi H.pylori. Sitokin ini berkorelasi dengan derajat inflamasi dan aktivitas neutrofil, di mana makin tinggi kadar sitokin sebanding dengan peningkatan derajat inflamasi dan aktivitas neutrofil.26
TNF-α merupakan sitokin utama pada respons inflamasi akut. Infeksi yang berat dapat memicu produksi TNF dalam jumlah besar yang menimbulkan reaksi sistemik. TNF disebut TNF-α atas dasar historis dan untuk membedakannya dari TNF- atau limfotoksin. 25
TNF-α diproduksi oleh neutrofil, limfosit yang diaktifkan, makrofag sel NK, dan beberapa sel non limfoid seperti astrosit, sel endotel dan sel otot polos, sementara TNF- nampaknya hanya diproduksi oleh sel T. 23
LPS (lipopolysakarida) adalah endotoxin dari H pylori yang merupakan rangsangan poten untuk mensekresi TNF. IFN- yang diproduksi oleh sel T dan sel NK juga merangsang makrofag antara lain meningkatkan sintesis TNF. TNF memiliki efek biologik antara lain pengerahan neutrofil dan monosit ke tempat infeksi serta mengaktifkan sel-sel tersebut untuk menyingkirkan mikroba, memacu ekspresi molekul adesi sel endotel vaskular terhadap leukosit, merangsang makrofag mensekresi kemokin dan menginduksi kemotaksis dan pengerahan leukosit, merangsang fagosit mononuklear. 24
TNF-α adalah sitokin proinflamasi yang berperan penting dalam respon baik akut maupun kronis pada infeksi virus, bakteri, dan parasit. Bioaktivitas TNF-α terjadi melalui terikatnya TNF-α pada reseptor seluler spesifik TNF-R, TNF-R1 (p55) dan TNF-R2 (p75), yang berbeda berat molekul, lokasi, dan fungsinya. TNF-R1 tersebar di banyak tempat, sementara TNF-R2 lebih terbatas distribusinya, yaitu pada sel-sel asal hematopoietin. TNF-R1 memperantarai kebanyakan respon seluler yang diinduksi TNF-α, termasuk aktivasi faktor traskripsi seperti NF-κB dan apoptosis 25