UJI ANGKA KAPANG/KHAMIR (AKK) DAN ANGKA LEMPENG TOTAL (ALT) PADA JAMU SERBUK JAHE MERAH
(Zingiber officinale Rosc. var. rubrum) YANG DIJUAL DI PASAR BERINGHARJO YOGYAKARTA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Agustina Kristiani
NIM : 168114147
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2021
ii
Persetujuan Pembimbing
UJI ANGKA KAPANG/KHAMIR (AKK) DAN ANGKA LEMPENG TOTAL (ALT) PADA JAMU SERBUK JAHE MERAH
(Zingiber officinale Rosc. var. rubrum) YANG DIJUAL DI PASAR BERINGHARJO YOGYAKARTA
Skripsi yang diajukan oleh:
Agustina Kristiani NIM : 168114147
telah disetujui oleh:
Pembimbing Utama
(Dr. apt. Erna Tri Wulandari) Tanggal, 24 Februari 2020
iii
Pengesahan Skripsi Berjudul
UJI ANGKA KAPANG/KHAMIR (AKK) DAN ANGKA LEMPENG TOTAL (ALT) PADA JAMU SERBUK JAHE MERAH
(Zingiber officinale Rosc. var. rubrum) YANG DIJUAL DI PASAR BERINGHARJO YOGYAKARTA
Oleh:
Agustina Kristiani NIM : 168114147
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma Pada tanggal 29 Maret 2021
Mengetahui Fakultas Farmasi Universitas Sanata Dharma
Dekan
(Dr. apt. Yustina Sri Hartini)
Panitia Penguji Tanda Tangan
1. Dr. apt. Erna Tri Wulandari ………….
2. Dr. apt. Yustina Sri Hartini ………….
3. apt. Maywan Hariono, Ph.D. ………….
iv
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan ini sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila dikemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang- undangan yang berlaku.
Yogyakarta, 17 Januari 2021 Penulis,
Agustina Kristiani
v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan dibawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Agustina Kristiani Nomor Mahasiswa : 168114147
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
“UJI ANGKA KAPANG/KHAMIR (AKK) DAN ANGKA LEMPENG TOTAL (ALT) PADA JAMU SERBUK JAHE MERAH
(Zingiber officinale Rosc. var. rubrum) YANG DIJUAL DI PASAR BERINGHARJO YOGYAKARTA”
Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 17 Januari 2021 Yang menyatakan
Agustina Kristiani
vi
HALAMAN PERSEMBAHAN
Karya ini kupersembahkan untuk : Tuhan Yesus Kristus
Bapak, Ibu, dan Adik yang selalu memberikan doa dan semangat Sahabat dan Teman yang selalu menemani dan memberikan semangat
Almamater tercinta Universitas Sanata Dharma
vii PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas, berkat, rahmat, dan penyertaan-Nya sehingga penulis dapat menyelesaikan penilitian dan penyusunan naskah skripsi yang berjudul “Uji Angka Kapang/Khamir (AKK) dan Angka Lempeng Total (ALT) pada Jamu Serbuk Jahe Merah (Zingiber officinale Rosc. var. rubrum) yang Dijual di Pasar Beringharjo Yogyakarta”
Skripsi ini disusun untuk memenuhi salah satu syarat dalam memperoleh gelar Sarjana Farmasi (S.Farm) Fakultas Farmasi Universitas Sanata Dharma Yogyakarta. Penyusunan skripsi telah melibatkan banyak pihak baik langsung maupun tidak langsung. Oleh karena itu, pada kesempatan ini, penulis ingin menyampaikan terimakasih kepada:
1. Ibu Dr. Apt.Yustina Sri Hartini. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta dan Dosen Penguji
2. Ibu Dr. Apt. Christine Patramurti. selaku Ketua Program Studi Fakultas Farmasi Universitas Sanata Dharma.
3. Ibu Dr. Apt. Erna Tri Wulandari. selaku Dosen Pembimbing Skripsi yang telah membimbing serta memberikan dukungan kepada penulis
4. Ibu Damiana Sapta Candrasari, M. Sc. selaku Kepala Penanggung Jawab Laboratorium Fakultas Farmasi USD dan Dosen Penguji yang telah memberikan ijin dalam menggunakan fasilitas laboratorium dan saran yang sangat membantu dalam penyusunan skripsi ini.
5. Bapak apt. Maywan Hariono, Ph.D. selaku Dosen Penguji Skripsi yang telah membimbing serta memberikan saran dalam penyusunan skripsi ini.
6. Ibu apt Dina Christin Ayuning Putri. selaku Dosen Pembimbing Akademik yang selalu membimbing, memberikan masukan dan motivasi selama penulis menempuh perkuliahan di Fakultas Farmasi USD
7. Bapak Kunto selaku Laboran laboratorium yang telah membantu penulis selama proses penelitian
viii
8. Seluruh Civitas Akademika Universitas Sanata Dharma yang telah membimbing, memberikan ilmu pengetahuan dan arahan selama penulis menempuh perkuliahan di Fakultas Farmasi USD.
9. Keluarga tersayang, Simbah Wijiningsih, Bapak Fransiscus Widiarsono Wijayanto, Ibu Puji Rahayu, dan adik Fransisca Widya Adiwitya, serta para saudara yang telah memberikan doa dan dukungan
10. Teman-teman seper-JAMU-an (Ambros, Pulung, dan Ichak). Terimakasih atas kebersamaan dan bantuan selama penelitian di laboratorium
11. Teman-teman FSMD 2016 tercinta. Terimakasih atas kebersamaan, dukungan, dan telah berbagi suka duka selama masa perkuliahan
12. Para “Sahabat Typo Autocorrect” dan “Pejuang Bolot Saru”, Ancis, Agnes, Ayu, Bano, Beta, Dita, Lia, Mbak Cimol, Mbak Cynthia, Mbak Tantri, Mbak Pita, Mas Angie, Mas Danu, Mas Hugo, Mas Rio, Mas Randy, Mbak Kunti, Mbak Novi, Yakuza yang selama ini telah memberikan keceriaan, semangat, doa, dan dukungan selama menjalankan perkuliahan.
13. Masyarakat Dextro SMF Angkatan 49 yang saling mendukung dan memotivasi
14. Apotek Lunar Group yang sudah memberikan kesempatan kepada penulis untuk belajar dan berdinamika bersama.
15. Semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah mendukung penulis dalam menyelesaikan penyusunan naskah skripsi ini.
Penulis menyadari bahwa masih banyak kelemahan dan kekurangan dalam penulisan naskah skripsi ini. Oleh karena itu, penulis mengharapkan adanya kritik dan saran yang membangun dari semua pihak. Akhir kata, penulis berharap semoga naskah skripsi ini dapat bermanfaat bagi semua pihak terutama dibidang ilmu Farmasi.
Yogyakarta, 17 Januari 2021
Penulis
ix DAFTAR ISI
Halaman
HALAMAN JUDUL... i
HALAMAN PERSETUJUAN PEMBIMBING... ii
HALAMAN PENGESAHAN... iii
PERNYATAAN KEASLIAN KARYA... iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI... v
HALAMAN PERSEMBAHAN... vi
PRAKATA... vii
DAFTAR ISI... ix
DAFTAR TABEL... x
DAFTAR GAMBAR... xi
DAFTAR LAMPIRAN... xii
ABSTRAK... xiii
ABSTRACT... xiv
PENDAHULUAN... 1
METODE PENELITIAN... 5
Jenis dan Rancangan Penelitian... 5
Alat dan Bahan... 5
Tata Cara Penelitian... 5
Teknik Pengumpulan Data dan Analisis Hasil... 8
HASIL DAN PEMBAHASAN... 12
Pemilihan dan Pengambilan Sampel... 12
Sterilisasi Alat, Media, dan Ruangan... 13
Persiapan Sampel... 14
Homogenisasi Sampel... 14
Pengenceran Sampel... 15
Uji Angka Kapang Khamir... 15
Uji Angka Lempeng Total... 18
KESIMPULAN DAN SARAN... 22
DAFTAR PUSTAKA... 23
BIOGRAFI PENULIS... 65
x
DAFTAR TABEL
Tabel 1. AKK Jamu Serbuk Jahe Merah... 17
Tabel 2. ALT Jamu Serbuk Jahe Merah... 20
Tabel 3. Perhitungan SD dan CV AKK Sampel A... 33
Tabel 4. Perhitungan SD dan CV AKK Sampel B... 38
Tabel 5. Perhitungan SD dan CV AKK Sampel C... 43
Tabel 6. Perhitungan SD dan CV ALT Sampel A... 50
Tabel 7. Perhitungan SD dan CV AKK Sampel B... 56
Tabel 8. Perhitungan SD dan CV AKK Sampel C... 63
xi
DAFTAR GAMBAR
Gambar 1. Jahe Merah, Jahe Gajah, dan Jahe Emprit...
Gambar 2. Kontrol Media dan Pengencer AKK...
1 17
Gambar 3. Kontrol Media dan Pengencer ALT... 19
Gambar 4. AKK Jamu Serbuk Jahe Merah Sampel A Replikasi 1... 29
Gambar 5. AKK Jamu Serbuk Jahe Merah Sampel A Replikasi 2... 30
Gambar 6. AKK Jamu Serbuk Jahe Merah Sampel A Replikasi 3... 31
Gambar 7. AKK Jamu Serbuk Jahe Merah Sampel B Replikasi 1... 34
Gambar 8. AKK Jamu Serbuk Jahe Merah Sampel B Replikasi 2... 35
Gambar 9. AKK Jamu Serbuk Jahe Merah Sampel B Replikasi 3... 36
Gambar 10. AKK Jamu Serbuk Jahe Merah Sampel C Replikasi 1... 39
Gambar 11. AKK Jamu Serbuk Jahe Merah Sampel C Replikasi 2... 40
Gambar 12. AKK Jamu Serbuk Jahe Merah Sampel C Replikasi 3... 41
Gambar 13. ALT Jamu Serbuk Jahe Merah Sampel A Replikasi 1... 44
Gambar 14. ALT Jamu Serbuk Jahe Merah Sampel A Replikasi 2... 45
Gambar 15. ALT Jamu Serbuk Jahe Merah Sampel A Replikasi 3... 46
Gambar 16. ALT Jamu Serbuk Jahe Merah Sampel B Replikasi 1... 51
Gambar 17. ALT Jamu Serbuk Jahe Merah Sampel B Replikasi 2... 52
Gambar 18. ALT Jamu Serbuk Jahe Merah Sampel B Replikasi 3... 53
Gambar 19. ALT Jamu Serbuk Jahe Merah Sampel C Replikasi 1... 57
Gambar 20. ALT Jamu Serbuk Jahe Merah Sampel C Replikasi 2... 58
Gambar 21. ALT Jamu Serbuk Jahe Merah Sampel C Replikasi 3... 59
xii
DAFTAR LAMPIRAN
Lampiran 1. Sampel Jamu Serbuk Jahe Merah... 28
Lampiran 2. Sampel Jamu Serbuk Jahe Merah dalam Wadah... 28
Lampiran 3. Uji AKK Jamu Serbuk Jahe Merah Sampel A... 29
Lampiran 4. Perhitungan AKK Jamu Serbuk Jahe Merah Sampel A... 32
Lampiran 5. Uji AKK Jamu Serbuk Jahe Merah Sampel B... 34
Lampiran 6. Perhitungan AKK Jamu Serbuk Jahe Merah Sampel B... 37
Lampiran 7. Uji AKK Jamu Serbuk Jahe Merah Sampel C... 39
Lampiran 8. Perhitungan AKK Jamu Serbuk Jahe Merah Sampel C... 42
Lampiran 9. Uji ALT Jamu Serbuk Jahe Merah Sampel A... 44
Lampiran 10. Perhitungan ALT Jamu Serbuk Jahe Merah Sampel A... 47
Lampiran 11. Uji AKK Jamu Serbuk Jahe Merah Sampel B... 50
Lampiran 12. Perhitungan AKK Jamu Serbuk Jahe Merah Sampel B... 54
Lampiran 13. Uji AKK Jamu Serbuk Jahe Merah Sampel C... 57
Lampiran 14. Perhitungan AKK Jamu Serbuk Jahe Merah Sampel C... 60
Lampiran 15. Kontrol Media dan Kontrol Pengencer AKK dan ALT... 64
xiii ABSTRAK
Jahe merah (Zingiber officinale Rosc.var. rubrum) merupakan tanaman yang digunakan sebagai rempah, penghangat, dan bahan baku obat tradisional.
Tujuan penelitian ini adalah untuk mengetahui cemaran mikroba pada jamu serbuk jahe merah yang dijual di Pasar Beringharjo Yogyakarta secara cluster sampling berdasarkan jumlah angka kapang khamir (AKK) dan angka lempeng total (ALT).
Penelitian ini merupakan penelitian non eksperimental deskriptif komparatif yaitu mendeskripsikan AKK dan ALT pada sediaan jamu serbuk jahe merah serta membandingkan dengan Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 12 Tahun 2014. Penentuan uji ALT menggunakan media Plate Count Agar (PCA) dan AKK menggunakan media Potato Dextrose Agar (PDA). Analisis hasil pengujian dilakukan sesuai dengan ketentuan pada PPOMN tahun 2006. Pertumbuhan koloni bakteri diinokulasikan dengan metode pour plate pada suhu 37°C selama 24-48 jam dan pada suhu 20- 25°C selama lima hari untuk kapang khamir. Hasil AKK yang diperoleh yaitu < 10 koloni/g dan ALT 2,4 x 102 koloni/ g. Jamu serbuk jahe merah ini memenuhi ketentuan PerKaBPOM RI No. 12 Tahun 2014 yang menyatakan bahwa persyaratan mutu pada serbuk simplisia yaitu nilai AKK yang diperbolehkan adalah
≤ 104 koloni/g dan ALT yang diperbolehkan adalah ≤ 106 koloni/g.
Kata kunci: jahe merah, angka kapang khamir, angka lempeng total
xiv ABSTRACT
Red ginger (Zingiber officinale Rosc.var. Rubrum) is a plant used as a spice, warmer, and raw material for traditional medicine. The purpose of this study was to determine the microbial contamination of the red ginger powder herbs that trading in Yogyakarta Beringharjo Market by cluster sampling based on the number of yeast molds (MYN) and total plate count (TPC).
This research was a comparative descriptive non experimental study that described MYN and TPC in red ginger powder herbal and compared them with the Regulation of the Food and Drug Monitoring Agency (BPOM) Republic of Indonesia Number 12 of 2014. Determination of the TPC test used Plate Count Agar (PCA) as a media and yeast mold number used media Potato Dextrose Agar (PDA).
Analysis of the test results was carried out in accordance with the provisions of PPOMN 2006. Growth of bacterial colonies was inoculated by the pour plate method at 37°C for 24-48 hours and at 20-25°C for five days of yeast molds. The MYN results obtained were <10 colonies/g and ALT 2,4 x 102 colonies/g. This red ginger herb powder complies with the provisions of the Republic of Indonesia Regulation No. 12 of 2014 which states that the quality requirements for simplicia powders, namely the allowable AKK value is ≤ 104 colonies/g and the allowed ALT is ≤ 106colonies / g.
Keywords: red ginger, mold/ yeast number, total plate count
1 PENDAHULUAN
Tumbuhan merupakan salah satu sumber terbesar dari alam yang digunakan sebagai obat tradisional dan menjadi objek penelitian dalam pencarian obat baru. Pemanfaatan tanaman untuk obat tradisional memiliki kelebihan tersendiri yaitu toksisitasnya rendah, mudah diperoleh, murah harganya dan kurang menimbulkan efek samping (Lallo, 2018). Tanaman obat juga merupakan sumber daya alam hayati yang memiliki nilai ekonomi yang tinggi (Sukmawati, Proborini, dan Kawuri, 2012). Kelebihan ini telah dibuktikan secara empiris pada penggunaan langsung oleh manusia secara tradisional. Hal inilah yang menjadi salah satu motivasi untuk melirik kembali potensi alam untuk mengupayakan penanggulangan berbagai penyakit atau gangguan kesehatan yang sering muncul termasuk dalam proses pencegahannya (Lallo, 2018).
Persentasi penggunaan tanaman obat di Indonesia berturut-turut adalah jahe (50,36%), diikuti kencur (48,77%), temulawak (39,65%), meniran (13,93%) dan pace (11,17%) (MENKES RI, 2017). Ada beberapa jenis jahe yang dibudidayakan di Indonesia, salah satunya adalah jahe merah (Zingiber officinale Rosc. var.
rubrum) (Wasito, 2011). Berdasarkan bentuk, warna, dan bau jahe dapat dibedakan menjadi 3 varietas yaitu Z. officinale var. officinale (jahe badak atau jahe gajah atau jahe putih besar) yang berukuran besar, berwarna putih, bau dan serat lebih sedikit;
Z. officinale var. amarum (jahe emprit atau jahe putih kecil) yang berukuran kecil, berwarna putih, bau tajam, dan lebih banyak serat; serta Z. officinale var. rubrum (jahe merah atau jahe sunti) yang berukuran kecil, berwarna merah, bau tajam dan lebih banyak serat (Setyawan et al., 2014; Wibowo, Mariani, Hasanah, Aulifa, 2020).
Gambar 1. Jahe merah, jahe gajah, dan jahe emprit
(Maimunah, 2018).
2
Kandungan kimia khas dari jahe adalah gingerol dan shogaol (Adnyana dan Suciati, 2016). Senyawa kimia aktif dalam jahe merah yang berefek farmakologis terhadap kesehatan, antara lain minyak atsiri dengan kandungan zat aktif zingiberin, kamfena, lemonin, borneol, shogaol, sineol, fellandren, zingiberol, gingerol, dan zingeron (Aryanta, 2019). Jahe merah banyak dipilih sebagai bahan baku obat tradisional dan industri obat-obatan karena kandungan minyak atsiri, oleoresin, serat jahe merah lebih tinggi jika dibandingkan dengan jenis jahe yang lain (Hapsoh, Hasanah, dan Julianti, 2010). Kandungan minyak atsiri jahe merah yaitu 2,58 - 2,72%, menyusul jahe gajah dengan kandungan minyak atsiri 0,82 - 1,68% , dan jahe emprit dengan kandungan minyak atsiri 1,5 – 3,3% (Santoso, 2008; Aryanta, 2019). Kandungan oleoresin jahe merah 3% (Hapsoh, Hasanah, dan Julianti, 2010). Selain itu, kandungan gingerol dan shogaol pada jahe merah juga lebih tinggi dibandingkan jenis jahe lainnya (Adnyana dan Suciati, 2016). Aroma harum jahe disebabkan oleh minyak atsiri, sedangkan oleoresin menyebabkan rasa pedas. Komponen utama minyak atsiri jahe yang menyebabkan bau harum adalah zingiberen dan zingiberol (Handrianto, 2016).
Jahe merah berkhasiat mengobati batuk, membangkitkan nafsu makan, perut kembung, gatal, dan sakit kepala (Wasito, 2011). Manfaat lain jahe merah dalam pengobatan tradisional yaitu dapat digunakan untuk ramuan selesma dan sakit pinggang (MENKES RI, 2017). Terdapat pula aktivitas farmakologi jahe merah antara lain efek antioksidan (gingerol, seskuiterpen, shogaol), antifungi (gingerol, shogaol, zingiberol, eugenol, senyawa monoterpen), antimikroba (zingiberene), imunomodulator (6-shogaol dan 1-dehydro-6-gingerdione), antiinflamasi (gingerol), antinyeri (gingerol, shogaol, zingerone, diarylheptanoids dan derivatnya terutama paradol), antihipertensi dan dislipidemia (polifenol) (Oboh, Akinyemi, and Ademiluyi, 2012; Sitepu, Suniti, Singarsa, 2019;
Handrianto, 2016; Nordin et al., 2013; Levita, Syafitri, Supu, Mutakin, Megantara, Febrianti, Diantini, 2018; Azkiya, Ariyani, Nugraha, 2017; Akinyemi, Ademiluyi, Oboh, 2014).
Obat tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik) atau campuran
3
dari bahan tersebut yang secara turun temurun telah digunakan untuk pengobatan, dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat (MENKES RI, 2014). Salah satu kelompok obat tradisional adalah jamu. Jamu sudah dikenal di Indonesia, khususnya di Pulau Jawa sebagai sarana perawatan kesehatan sehari- hari maupun sebagai sarana pemulihan kesehatan dari sakit (Sukmawati, Proborini, Kawuri, 2012). Obat tradisional dibuat dari bahan alam yang memiliki jenis serta sifat zat berkhasiat yang terkandung di dalamnya sangat beragam, sehingga dalam pembuatan dan pengolahan obat tradisional untuk menjamin mutu, keamanan, dan kemanfaatan obat tradisional maka diperlukan Cara Pembuatan Obat Tradisional yang Baik yang selanjutnya disingkat CPOTB (MENKES RI, 2013).
Pemerintah menjamin ketersediaan sediaan farmasi yang beredar di Indonesia aman, bermutu, dan bermanfaat/ berkhasiat, tersedia dalam jumlah yang cukup, serta terjangkau (Diniarti dan Iljanto, 2017). Keamanan obat tradisional (jamu) merupakan suatu tuntutan yang telah dikemukakan sejak munculnya gangguan kesehatan manusia akibat cemaran mikroorganisme, maka penting dilakukan pengujian cemaran mikroorganisme dalam sediaan obat tradisional, antara lain uji Angka Lempeng Total (ALT) dan Angka Kapang Khamir (AKK).
Uji ALT adalah pengujian yang dilakukan untuk menghitung angka bakteri aerob mesofil yang terdapat dalam suatu sampel. Perhitungan AKK untuk menentukan jumlah koloni kapang dan khamir yang terdapat dalam suatu sampel (Radji, 2009).
Apabila jamu serbuk tercemar dan terus-menerus dikonsumsi dapat menghasilkan toksin yang menyebabkan berbagai penyakit diantaranya diare, muntah, demam, dan infeksi yang timbul pada pencernaan karena infeksi bakteri.
Kapang dan khamir akan berkembang biak bila tempat tumbuhnya cocok untuk pertumbuhan, disamping itu kapang tertentu ada yang menghasilkan zat racun (toksin) seperti jamur Aspergilus flavus yang dapat menghasilkan aflatoksin (Saweng, Sudimartini, Suartha, 2020). Komponen beracun yang diproduksi oleh kapang maupun jamur disebut mikotoksin yang dapat menyebabkan penyakit yang kadang-kadang fatal dan beberapa diantaranya bersifat karsinogenik. Aflatoksin dalam jumlah tinggi dapat menyebabkan terjadinya aflatoksikosis akut yang dapat menimbulkan manifestasi hepatoksisitas atau kasus berat dapat menyebabkan
4
kematian. Bila aflaktosikosis ini berkelanjutan maka akan muncul sindrom penyakit yang ditandai dengan muntah, diare, nyeri perut, kejang, koma, dan kematian akibat edema otak serta perlemakan hati, ginjal dan jantung (Sari, Dewi, Wilson, 2020).
Menurut Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 12 Tahun 2014 dikatakan bahwa persyaratan mutu pada serbuk simplisia yang diseduh dengan air panas sebelum digunakan yaitu AKK yang diperbolehkan adalah ≤ 104 koloni/g dan ALT yang diperbolehkan adalah ≤ 106 koloni/g (MENKES RI, 2014). Nilai AKK dan ALT dapat digunakan sebagai petunjuk dalam pembuatan obat tradisional sesuai CPOTB. Semakin kecil AKK dan ALT bagi setiap produk yang dihasilkan menunjukkan semakin tinggi nilai penerapan CPOTB dalam pembuatan obat tradisional tersebut (Wasito, 2011).
Pasar Beringharjo merupakan salah satu pasar terbesar di Yogyakarta dan paling ramai dikunjungi oleh pedagang maupun pembeli. Letak Pasar Beringharjo ini strategis yaitu berada di tengah kota. Selain itu, di Pasar Beringharjo terdapat blok toko penjual obat tradisional dengan 3 los dan 24 toko obat tradisional baik dalam bentuk rajangan simplisia, serbuk simplisia, jamu serbuk seduhan, dan kemasan obat tradisional lainnya. Dari total 24 toko tersebut, terdapat 12 toko yang menjual jamu serbuk jahe merah produksi X. Secara purposive sampling, diambil 9 sampel jamu serbuk jahe merah dari 3 toko obat tradisional. Masing-masing los dipilih 1 toko obat tradisional secara acak dan dari masing-masing toko dilakukan 3 kali pengambilan sampel. Berdasarkan hasil observasi yang dilakukan peneliti kepada penjual jamu, salah satu jamu serbuk yang paling banyak diminati konsumen adalah jamu serbuk jahe merah. Hal tersebut mendorong peneliti melakukan uji AKK dan ALT pada jamu serbuk jahe merah yang dijual di Pasar Beringharjo. Penelitian ini diharapkan dapat diketahui nilai AKK dan ALT pada jamu serbuk jahe merah yang merupakan salah satu parameter keamanan jamu serbuk secara mikrobiologi.
5 METODE PENELITIAN
Jenis dan Rancangan Penelitian
Penelitian ini merupakan penelitian non eksperimental dengan rancangan penelitian deskriptif komparatif yaitu mendeskripsikan AKK dan ALT pada sediaan jamu serbuk jahe merah yang dijual di Pasar Beringharjo, Yogyakarta, serta membandingkan dengan Peraturan Kepala Pengawas Obat dan Makanan Republik Indonesia Nomor 12 Tahun 2014 yang menyatakan bahwa ALT yang diperbolehkan adalah ≤ 𝟏𝟎𝟔 koloni/g dan AKK yang diperbolehkan adalah ≤ 𝟏𝟎𝟒 koloni/g
Bahan Penelitian
Bahan yang digunakan adalah jamu serbuk jahe merah produksi X yang diperoleh dari penjual obat tradisional di Pasar Beringharjo Yogyakarta. Media yang digunakan untuk pengujian AKK adalah Potato Dextrose Agar (Merck).
Media yang digunakan untuk pengujian ALT adalah Plate Count Agar (Merck).
Kloramfenikol (Brataco Chemika), BPW (Merck), Aquades steril, Etanol 70 % (Onemed)
Alat Penelitian
Alat-alat yang digunakan dalam penelitian antara lain Biological Safety Cabinet (BSC), Laminar Air Flow (LAF), autoklaf, inkubator, oven, blue tip, mikropipet, mikroskop, colony counter, pipet tetes, pipet volume, glassfirn, tabung reaksi, gelas beaker, gelas ukur, labu ukur, batang pengaduk, cawan petri, erlenmeyer, bunsen, neraca analitik,
Pemilihan dan Pengambilan Sampel
Sampel jamu serbuk jahe merah diperoleh dari toko penjual obat tradisional di Pasar Beringharjo Yogyakarta. Di blok obat tradisional terdapat 3 los toko obat tradisional dengan total 24 toko yang menjual berbagai bentuk sediaan seperti rajangan, serbuk simplisia, dan jamu lainnya. Teknik pengambilan sampel dilakukan dengan teknik purposive sampling . Purposive sampling adalah pengambilan sampel secara sengaja sesuai dengan persyaratan atau kriteria tertentu yang ditentukan oleh peneliti (Larici dan Adawiyah, 2017). Dipilih toko yang menjual jamu serbuk jahe merah produksi X dan dipilih toko yang dekat dengan
6
persimpangan pada los toko obat tradisional karena merupakan tempat yang lebih ramai dikunjungi dan dilewati pembeli. Dari total 24 toko tersebut, terdapat 12 toko yang menjual jamu serbuk jahe merah produksi X. Dipilih 1 toko dari masing- masing los toko obat tradisional yang berbeda dan dari masing-masing toko dilakukan 3 kali pengambilan sampel sebagai replikasi untuk dapat mewakili keseluruhan penjual obat tradisional yang berada di pasar tersebut, sehingga diperoleh 9 sampel jamu serbuk dari 3 toko. Sampel kemudian disimpan dalam wadah yang tertutup rapat, kering, dan sudah disterilkan dengan alkohol.
Sterilisasi Alat, Media, dan Ruangan
Sterilisasi dilakukan menggunakan autoklaf pada suhu 121°C selama 15 menit. Pada penelitian ini autoklaf digunakan untuk sterilisasi media dan alat, oven untuk sterilisasi peralatan gelas seperti tabung reaksi, pipet volume, dan alat gelas lainnya, serta alkohol digunakan untuk sterilisasi ruang dan meja yang digunakan dalam penelitian. Dalam pengerjaan perlu memperhatikan teknik steril dan teknik aseptis untuk mencegah cemaran mikroorganisme kontak langsung dengan tangan dan alat-alat yang kurang steril melalui udara.
Persiapan Sampel
Persiapan sampel sampai dengan uji AKK dan ALT dilakukan di Biological Safety Cabinet (BSC). Disiapkan sebanyak 9 botol plastik jamu serbuk jahe merah.
Bagian wadah atau kemasan jamu serbuk jahe merah dibuka secara aseptis Homogenisasi Sampel
Diambil sebanyak tiga per empat sendok sampel dari masing-masing botol jamu serbuk jahe merah, sesuai cara pembuatan jamu yang tertera pada kemasan.
Kemudian jamu serbuk jahe merah dilarutkan dengan 100 ml aquades steril panas.
Diambil 1 ml dari larutan sampel tersebut dan dimasukkan dalam labu ukur 10 ml, kemudian ditambahkan larutan pengencer BPW hingga tanda batas sehingga diperoleh pengenceran 10-1.
Pengenceran sampel untuk uji AKK
Disiapkan tiga buah labu ukur 10 ml, masing-masing telah diisi dengan 9 ml BPW. Dipipet 1 ml sampel pengenceran 10-1 dan dimasukkan ke dalam tabung
7
pertama yang telah berisi BPW hingga diperoleh pengenceran 10-2 lalu dikocok homogen. Dibuat pengenceran berikutnya sampai 10-4.
Pembuatan Larutan Kloramfenikol
Ditimbang sebanyak 1 gram kloramfenikol dan dilarutkan ke dalam 100 ml aquadest steril.
Pembuatan Larutan Media Potato Dextrose Agar (PDA)
Disuspensikan 39 gram serbuk PDA dalam 1000 ml aquadest, kemudian dipanaskan dan diaduk dengan stirrer diatas hotplate. Disterilisasi dengan autoklaf selama 15 menit pada suhu 121°C. Kemudian dituang ke dalam cawan petri dan dibiarkan memadat.
Uji Angka Kapang Khamir
Dipipet sebanyak 1 ml dari masing-masing pengenceran ke dalam cawan petri steril secara duplo. Dipipet sebanyak 1 ml larutan kloramfenikol ke dalam cawan petri tersebut. Media PDA yang telah dicairkan (suhu 45±1°C) sebanyak 20 ml dituangkan ke dalam cawan petri dan digoyangkan sehingga campuran tersebut merata. Setelah agar memadat, cawan petri dibalik dan diinkubasikan pada suhu 25°C atau pada suhu kamar selama 5 hari. Dilakukan pengamatan setiap hari sampai hari ke-5. Dihitung koloni kapang dan khamir setelah 5 hari. Dilakukan uji sterilitas media dengan menuangkan media PDA dalam cawan petri dan dibiarkan memadat.
Dilakukan uji sterilitas pengencer dengan cara menuangkan media PDA dan 1 ml pengencer (BPW) lalu dibiarkan memadat.
Pengenceran sampel untuk uji ALT
Disiapkan sebanyak 5 buah labu ukur 10 ml, masing-masing telah diisi dengan 9 ml pengencer BPW. Dipipet 1 ml pengenceran 10-1 dari hasil homogenisasi pada penyiapan sampel dan dimasukkan ke dalam tabung pertama yang telah diisi 9 ml BPW hingga diperoleh pengenceran 10-2 dan dihomogenkan.
Kemudian dibuat pengenceran selanjutnya hingga 10-6. Pembuatan Media Plate Count Agar (PCA)
Ditimbang sebanyak 22,5 gram PCA dan dicampurkan dengan 1000 ml aquades, dipanaskan dan diaduk dengan stirrer pada hotplate hingga larutan jernih.
Kemudian disterilkan dengan autoklaf selama 15 menit pada suhu 121°C.
8
Pembuatan Larutan Pengencer Buffered Pepton Water (BPW)
Dilarutkan sebanyak 25,5 gram serbuk BPW dalam 1000 ml air suling dan diukur pH 7,0 ± 1. Kemudian disterilkan dengan menggunakan autoklaf selama 15 menit pada suhu 121°C.
Uji Angka Lempeng Total
Dipipet 1 ml dari masing-masing pengenceran ke dalam cawan petri steril secara duplo. Dalam setiap cawan petri dituangkan sebanyak 15 ml media PCA yang telah dicairkan yang bersuhu 45 ± 1°C dalam waktu 15 menit dari pengencerkan pertama. Cawan petri digoyangkan dengan hati-hati agar sampel tersebut merata kemudian dibuat diplo. Dilakukan pula uji kontrol untuk mengetahui sterilitas media dan pengencer. Uji sterilitas media dilakukan dengan cara menuangkan media PCA dalam suatu cawan petri dan dibiarkan memadat.
Seluruh cawan petri diinkubasikan terbalik pada suhu 37°C selama 24 jam hingga 48 jam. Jumlah koloni yang tumbuh diamati dan dihitung.
Teknik Pengumpulan Data dan Analisis Hasil 1. Uji Angka Kapang/ Khamir
Cara menganalisis hasil pengujian untuk nilai Angka Kapang/Khamir sesuai dengan ketentuan PPOMN (2006) yaitu : cawan petri yang menunjukkan jumlah koloni antara 10-150 dari satu pengenceran dipilih dan dihitung jumlah koloni dari kedua cawan lalu dikalikan dengan faktor pengencerannya. Bila pada cawan petri dari dua tingkat pengenceran yang berurutan menunjukkan jumah antara 10-150, maka dihitung jumlah koloni dan dikalikan dengan faktor pengenceran, kemudian diambil angka rata-rata. Hasil dikalikan sebagai Angka Kapang/Khamir dalam tiap gram atau mililiter sampel.
Beberapa kemungkinan lain yang berbeda dari pernyataan diatas, maka diikuti petunjuk sebagai berikut :
a. Bila hanya salah satu diantara kedua cawan petri dari pengenceran yang menunjukkan jumlah antara 10-150 koloni, dihitung jumlah koloni dari kedua cawan dan dikalikan dengan faktor pengenceran.
9
b. Bila pada tingkat pegenceran yang lebih tinggi didapat jumlah koloni lebih besar dari dua kali jumlah koloni pada pengenceran dibawahnya, maka dipilih tingkat pengenceran terendah (Misal: pada pengenceran 10−2 diperoleh 60 koloni dan pada pengenceran 10−3 diperoleh 30 koloni, maka dipilih jumlah koloni pada pengenceran 10−2 yaitu 60 koloni). Bila pada pengenceran yang lebih tinggi didapat jumlah koloni kurang dari dua kali jumlah koloni pengenceran dibawahnya, maka diambil angka rata-rata dari jumlah koloni kedua pengenceran tersebut. Hasil dinyatakan sebagai Angka Kapang dan Khamir dalam tiap gra, sampel
(Misal pada pengenceran 10−2 diperoleh 60 koloni dan pada pengenceran 10−3 diperoleh 10 koloni, maka Angka Kapang Khamir adalah:
6+10
2 x 103 = 8 x 103)
c. Bila dari seluruh cawan petri tidak ada satupun yang menunjukkan jumlah antara 10-150 koloni, maka dicatat angka sebenarnya dari tingkat pengenceran terendah dan dihitung sebagai Angka Kapang/Khamir perkiraan.
d. Bila tidak ada pertumbuhan pada semua cawan dan bukan disebabkan karena faktor inhibitor, maka Angka Kapang/Khamir dilaporkan sebagai kurang dari satu dikalikan faktor pengenceran terendah (<1 x faktor pengenceran terendah).
2. Uji Angka Lempeng Total
Cara menganalisis hasil pengujian sesuai untuk nilai Angka Lempeng Total sesuai dengan ketentuan PPOMN (2006) yaitu :
a. Pilih cawan petri dari satu pengenceran yang menunjukkan jumlah koloni antara 25-250 setiap cawan. Semua koloni dalam cawan petri dihitung dengan menggunakan alat penghitung koloni (Colony counter). Jumlah koloni dihitung rata-rata dan dikalikan dengan faktor pengenceran. Hasilnya dinyatakan sebagai jumlah bakteri per mililiter atau gram.
b. Jika salah satu dari dua cawan petri terdapat jumlah koloni lebih kecil dari 25 atau lebih besar dari 250, dihitung rata-rata jumlah koloni dan dikalikan dengan faktor pengenceran. Hasilnya dinyatakan sebagai jumlah bakteri per mililiter atau gram.
10
c. Jika hasil dari dua pengenceran jumlahnya berturut-turut terletak antara 25-250 koloni, jumlah koloni dari masing-masing pengenceran dihitung seperti yang pada poin a dan poin b diatas, dan dihitung rata-rata jumlah koloni dari kedua pengenceran tersebut. Jika jumlah yang tertinggi lebih besar dari dua kali jumlah yang terkecil,dinyatakan jumlah yang lebih kecil sebagai jumlah bakteri per mililiter atau gram.
d. Jika rata-rata jumlah koloni masing-masing cawan petri tidak terletak antara 25-250 koloni, dihitung jumlah koloni seperti pada poin a dan poin b diatas, dan dinyatakan sebagai jumlah bakteri per mililiter atau gram
e. Jika jumlah koloni dari semua pengenceran lebih dari 250 koloni, maka setiap dua cawan petri dengan pengenceran tertinggi dibagi ke dalam 2, 4, atau 8 sektor. Jumlah koloni dihitung dalam satu bagian atau lebih. Untuk mendapatkan jumlah koloni dalam satu cawan petri, dihitung rata-rata jumlah koloni dan dikalikan dengan faktor pembagi dan pengencer. Hasil dinyatakan sebagai jumlah bakteri perkiraan per mililiter atau gram.
f. Jika dalam 1/8 bagian cawan petri terdapat lebih dari 200 koloni, maka jumlah koloni yang didapat = 8 x 200 (1600), dikalikan dengan faktor pengenceran dan hasilnya dinyatakan sebagai jumlah bakteri perkiraan per mililiter atau gram lebih besar dari jumlah yang didapat (>1600 x faktor pengenceran).
g. Jika tidak ada koloni yang tumbuh dalam cawan petri, dinyatakan jumlah bakteri perkiraan lebih kecil dari satu dikalikan dengan faktor pengenceran yang terendah (<10).
h. Menghitung koloni perambat (spreader)
Ada 3 macam koloni perambatan pada koloni, yaitu : (1) Merupakan rantai yang tidak terpisah-pisah
(2) Perambatan yang terjadi diantara dasar cawan petri dan perbenihan (3) Perambatan yang terjadi pada pinggir atau permukaan perbenihan
Jika terjadi hanya 1 perambatan (seperti rantai) maka koloni dianggap 1. Tetapi jika 1 atau lebih rantai terbentuk dan yang berasal dari sumber yang terpisah- pisah, maka setiap sumber dihitung sebagai 1 koloni. Bila (2) dan (3) terjadi
11
maka sebaiknya pemeriksaan diulangi karena koloni dalam keadaan semacam ini agak sulit dihitung
i. Menghitung dan membulatkan angka
Dalam melaporkan jumlah koloni atau jumlah koloni perkiraan hanya 2 angka penting yang digunakan, yaitu angka yang pertama dan kedua (dimulai dari kiri), sedangkan angka ketiga diganti dengan 0, apabila <5 dan apabila 5 atau lebih dijadikan 1 yang ditambah pada angka yang kedua.
Contoh : 523.000 dilaporkan sebagai 520.000 (5,2 x 105) 86.300 dilaporkan sebagai 84.000 (8,4 x 104)
12 HASIL DAN PEMBAHASAN
Jamu merupakan salah satu kelompok obat tradisional yang sudah dikenal di Indonesia sebagai sarana perawatan kesehatan sehari-hari maupun sebagai sarana pemulihan kesehatan dari sakit. Ramuan yang ada dalam jamu terdiri dari berbagai bagian tanaman yang saling bekerja sama membantu perawatan dan untuk mencegah penyakit (Sukmawati, Proborini, dan Kawuri, 2012). Jamu serbuk yang beredar dan dikonsumsi oleh masyarakat harus memenuhi standar kualitas dan keamanannya secara mikrobiologis untuk dikonsumsi. Hal tersebut didasarkan pada ketentuan dari BPOM sehingga jamu perlu diuji dan dianalisis kelayakan konsumsinya berdasarkan kualitas mikrobiologinya (BPOM RI, 2019). Uji cemaran mikroba dilakukan untuk menentukan cemaran mikrobiologi yang terkandung pada jamu tidak melebihi batas yang telah ditetapkan sehingga dapat diketahui kualitas dan keamanan dari bahan baku yang akan dijadikan sediaan farmasi. Cemaran mikroba yang tinggi dapat menyebab efek yang buruk bagi kesehatan (Saweng, Sudimartini, Suartha, 2020).
Salah satu bentuk penyajian jamu yang ada di Indonesia diantaranya berupa jamu serbuk, yaitu sediaan obat tradisional berupa butiran homogen dengan derajat halus yang sesuai, terbuat dari simplisia atau campuran dengan ekstrak yang cara penggunaannya diseduh dengan air panas. Keuntungan dari jamu serbuk ini adalah produknya mempunyai daya simpan yang lebih lama dibandingkan jamu gendong, penampilan yang lebih baik, pemasaran yang lebih luas, bobot pada saat penjualan lebih ringan, dan mudah dalam penyajian, namun khasiat dan rasanya masih dapat dipertahankan (Samran dan Fatimah, 2018; Permata dan Sayuti, 2016). Adapun Pemilihan dan Pengambilan Sampel
Sampel yang digunakan dalam penelitian ini adalah serbuk jamu jahe merah produksi X yang dijual di Pasar Beringharjo Yogyakarta. Jamu jahe merah dipilih karena berdasarkan survey peneliti di Pasar Beringharjo, jamu jahe merah merupakan salah satu jamu yang banyak diminati oleh masyarakat. Hal ini sesuai dengan Formularium Ramuan Obat Tradisional Indonesia yaitu persentasi penggunaan tanaman obat paling banyak digunakan dalah jahe (50,36%) (MENKES, 2017). Selain itu, jamu jahe merah dapat bermanfaat untuk mengobati
13
batuk, membangkitkan nafsu makan, masuk angin, gatal, sakit kepala, gangguan pencernaan, analgesik, antipiretik, antiinflamasi, selesma dan lain-lain.
Pasar Beringharjo dipilih sebagai tempat pengambilan sampel karena Pasar Beringharjo merupakan pasar terbesar di Yogyakarta dan terletak di pusat kota.
Selain itu, Pasar Beringharjo juga merupakan pasar pusat penjualan bahan baku jamu seperti rimpang, simplisia, serbuk simplisia, serta merupakan pasar dengan penjual obat tradisional terbanyak di Yogyakarta.
Berdasarkan survey yang dilakukan peneliti, terdapat tiga los penjual obat tradisional. Peneliti mengambil 9 sampel dari 3 toko obat tradisional yang dipilih secara acak. Dipilih 1 toko dari masing-masing los toko obat tradisional, kemudian dilakukan 3 kali pengambilan sampel sebagai replikasi yang dianggap dapat mempresentasikan penjual obat tradisional di pasar tersebut. Sampel yang sudah diambil kemudian disimpan dalam wadah yang kering, tertutup rapat, dan sudah dibersihkan dengan alkohol. Wadah disterilkan dengan alkohol terlebih dahulu karena alkohol sangat efektif membunuh bakteri dengan mendenaturasi protein.
Selain itu, alkohol dapat bekerja cepat dan menguap dengan cepat tanpa meninggalkan residu. Alkohol yang digunakan yaitu etanol 70% karena konsentrasi etanol 65-95% juga dapat membunuh dengan sama baiknya, sedangkan etanol murni kurang efektif dibandingkan dengan campuran etanol dan air karena denaturasi membutuhkan air (Radji 2009).
Sterilisasi Alat, Media, dan Ruangan
Sterilisasi merupakan proses penghilangan semua jenis organisme hidup, dalam hal ini adalah mikroorganisme yang terdapat pada suatu benda. Sterilisasi penting dilakukan untuk membebaskan peralatan dan media dari mikroba (Rizal, Sumaryani, Suprihana, 2016). Apabila tidak dilakukan sterilisasi maka tidak dapat dibedakan cemaran mikroba yang tumbuh berasal dari sampel atau dari peralatan dan media yang digunakan.
Peralatan dan media yang digunakan dalam penelitian disterilisasi terlebih dahulu. Peralatan yang terbuat dari kaca dan tahan terhadap panas dibungkus, kemudian dilakukan proses sterilisasi ke dalam autoklaf pada suhu 121 ˚C selama 20 menit. Media yang sudah dicampur dengan aquadest, dihomogenkan dengan
14
stirrer dan dipanaskan hingga jernih dalam hotplate kemudian dilakukan proses sterilisasi dengan autoklaf pada suhu 121 ˚C selama 15 menit (Saweng, Sudimartini, Suartha, 2020).
Autoklaf adalah alat pemanas tertutup yang digunakan untuk mensterilkan suatu benda menggunakan uap bersuhu dan bertekanan tinggi 121˚C selama kurang lebih 15 menit. Penurunan tekanan pada autoklaf tidak dimaksudkan untuk membunuh mikroorganisme, melainkan meningkatkan suhu dalam autoklaf. Suhu yang tinggi inilah yang akan membunuh mikroorganisme. Autoklaf terutama ditujukan untuk membunuh endospora, yaitu sel resisten yang diproduksi oleh bakteri, sel ini tahan terhadap pemanasan, kekeringan, dan antibiotik. Endospora dapat dibunuh pada suhu 100˚C, yang merupakan titik didih air pada tekanan atmosfer normal. Pada suhu 121˚C , endospora dapat dibunuh dalam waktu 4 – 5 menit, dimana sel vegetatif bakteri dapat dibunuh hanya dalam waktu 6 – 30 detik pada suhu 65˚C (Rizal, Sumaryati, Suprihana, 2016).
Sterilisasi ruangan dilakukan dengan mengelap permukaan meja kerja menggunakan alkohol 70 %. Pengujian dilakukan secara aseptis untuk meminimalkan kontaminasi sehingga bakteri yang tumbuh pada media benar-benar berasal dari sampel jamu jahe merah (Andriani, 2016).
Persiapan Sampel
Kemasan sampel jamu dibersihkan terlebih dahulu dengan alkohol 70%
kemudian kemasan sampel dibuka secara aseptis. Jamu serbuk jahe merah yang sudah dibuka, kemudian diambil dan dilarutkan dengan aquades steril.
Homogenisasi sampel
Homogenisasi adalah suatu cara penyajian sampel pemeriksaan untuk memperoleh distribusi mikroba sebaik mungkin di dalam sampel yang akan diperiksa. Tujuan homogenisasi adalah membebaskan sel-sel bakteri atau jamur yang mungkin terlindung di dalam bahan pemeriksaan dan untuk menormalkan kembali sel-sel bakteri dan jamur yang mungkin viabilitasnya berkurang karena kondisi yang kurang menguntungkan dalam sediaan farmasi yang akan diperiksa (Radji, 2009). Homogenisasi sampel dilakukan dengan cara mencampur 1 ml
15
larutan sampel jamu jahe merah dengan 9 ml pengencer BPW dalam labu ukur 10 ml, kemudian dihomogenkan. Ini diperoleh pengenceran 10−1
Pengenceran sampel
Pengenceran dilakukan dengan mengambil 1 mL dari pengenceran 10−1 dan ditambahkan 9 mL larutan pengencer, kemudian diperoleh pengenceran 10−2. Pengencer yang digunakan untuk uji ALT dan AKK adalah BPW (Buffered Peptone Water). BPW berfungsi dalam mendukung pH pertumbuhan akibat adanya perubahan pH yang disebabkan oleh pertumbuhan dan metabolisme mikroorganisme, serta menjaga agar mikroorganisme tidak rusak akibat perubahan pH tersebut. Kandungan pepton pada larutan BPW ini berfungsi sebagai sumber karbon, nitrogen, vitamin dan mineral bagi pertumbuhan bakteri. Selain itu kandungan NaCl pada larutan BPW berfungsi dalam menjaga keseimbangan osmotik medium pertembuhan (Soesetyaningsih, Azizah, 2020).
Pengenceran AKK dilakukan sampai 10−4, sedangkan pengenceran ALT dilakukan sampai 10−6. Tujuan dari pengenceran bertingkat yaitu untuk memperkecil atau mengurangi jumlah mikroba yang tersuspensi dalam jamu sehingga koloni yang tumbuh tidak menumpuk dan mempermudah dalam perhitungan jumlah koloni (Yunita, Hendrawan, Yulianingsih, 2015; Saweng, Sudimartini, Suartha, 2020).
Uji Angka Kapang Khamir
Uji Angka Kapang Khamir merupakan suatu pengujian yang dilakukan untuk menghitung jumlah koloni kapang/khamir pada sampel yang diteliti (Saweng, Sudimartini, Suartha, 2020). Media yang digunakan untuk uji AKK adalah PDA (Potato Dextrose Agar) (Afifi dan Sugiarti, 2016). PDA mengandung ekstrak potato, glukosa, dan agar. Glukosa dan potato/kentang merupakan sumber energi untuk memproduksi konidia dari kapang/khamir. Agar merupakan polisakarida asam yang diekstraksi dari ganggang merah tertentu (Putri, Sudimartini, Dharmayudha, 2020). Potato Dextrose Agar merupakan media yang umum digunakan untuk pertumbuhan jamur karena memilki pH 4,5 - 5,6 sehingga dapat menghambat pertumbuhan bakteri yang membutuhkan lingkungan dengan pH 7,0 dan suhu optimum untuk pertumbuhan antara 25-30° C (Cappucino, 2014).
16
Media Potato Dextrosa Agar (PDA) dibuat dengan menimbang serbuk PDA dan ditambahkan aquadest, kemudian dipanaskan hingga larutan jernih.
Selanjutnya disterilkan menggunakan autoklaf pada suhu 121°C selama 15 menit.
Selain itu, media PDA ditambahkan dengan kloramfenikol untuk menghambat pertumbuhan bakteri pada media, sehingga diharapkan yang tumbuh pada media adalah kapang/ khamir. Kloramfenikol adalah antibiotik spektrum luas bakteriostatik yang aktif melawa baik organisme gram positif dan gram negatif aerob dan anaerob yang menghambat kuat sintesis protein dengan mengikat secara reversibel ke subunit 50S dari ribosom bakteri dan menghambat pembentukan ikatan peptida (Katzung and Trevor, 2015).
Setiap cawan petri, dituang sebanyak 12-15 ml media PDA yang dicairkan pada suhu 45˚±1˚C. Pada uji AKK dilakukan pula kontrol media dengan cara menuangkan media PDA pada cawan petri dan membiarkannya memadat tanpa diisi pengencer BPW untuk memastikan bahwa bakteri yang tumbuh murni berasal dari sampel. Serta dilakukan kontrol pengencer dengan cara menuangkan media PDA dan pengencer BPW pada cawan petri dan membiarkannya memadat untuk menjamin bahwa sampel tidak terdapat kontaminan (Saweng, Sudimartini, Suartha, 2020). Seluruh cawan petri diinkubasikan dengan suhu 25°C karena kapang dan khamir bersifat mesofilik yang dapat tumbuh pada suhu 25-30°C selama 5 hari dengan posisi terbalik. Jumlah koloni yang tumbuh diamati sampai hari ke-5 (Saweng, Sudimartini, Suartha, 2020).
Data yang diperoleh dalam penelitian ini merupakan data yang bersifat kuantitatif yaitu dengan cara penghitungan jumlah mikroba yang muncul pada media yang telah diujikan. Hasil dianalisis dan dibandingkan dengan standar cemaran mikroba yang termuat dalam persyaratan Mutu Obat Tradisonal yang sesuai dengan Peraturan Kepala Bidang Pengawas Obat dan Makanan (BPOM) Republik Indonesia Nomor 12 Tahun 2014. Koloni kapang yang dihitung adalah berbentuk serabut seperti kapas dan untuk khamir berbentuk bulat dan keduanya merupakan koloni yang tunggal atau terpisah (Saweng, Sudimartini, Suartha, 2020).
17
Kontrol Media Kontrol Pengencer
Gambar 2. Kontrol Media dan Kontrol Pengencer Uji AKK
Pada uji AKK dilakukan uji kontrol media dan kontrol pengencer untuk mengetahui sterilitas media dan pengencer. Hasil dari uji kontrol media dan kontrol pengencer dapat dilihat pada Gambar 1. yaitu tidak terdapat pertumbuhan jamur yang menunjukkan bahwa tidak ada kontaminan dari media dan pelarut yang digunakan. Hasil rata-rata replikasi AKK setelah inkubasi sampai hari ke-5 ditunjukkan pada Tabel 1.
Tabel 1. Angka Kapang Khamir pada jamu serbuk jahe merah setelah inkubasi
Sampel AKK (koloni/g) SD CV
Sampel A (pedagang 1)
< 10 koloni/ g 0 0%
Sampel B (pedagang 2)
< 10 koloni/ g 0 0%
Sampel C (pedagang 3)
< 10 koloni/ g 0 0%
Hasil uji AKK setelah inkubasi 5 hari yaitu tidak ada kapang atau khamir pada sampel jamu serbuk jahe merah, maka nilai AKK dilaporkan sebagai kurang dari satu dikalikan faktor pengenceran terendah (<1 x faktor pengenceran terendah) (PPOMN, 2006). Dipilih pengenceran 10−1, sehingga nilai AKK yang diperoleh berdasarkan Tabel.1 yaitu < 10 koloni/ g. Nilai tersebut sesuai dengan persyaratan yang ditetapkan oleh Peraturan Kepala Bidang Pengawas Obat dan Makanan
18
(BPOM) Republik Indonesia Nomor 12 Tahun 2014, yaitu AKK yang diperbolehkan adalah ≤ 104 koloni/g. Hal ini menunjukkan bahwa jamu serbuk jahe merah telah dibuat dengan memperhatikan CPOTB (Cara Pembuatan Obat Tradisional yang Baik) dengan baik. Selain itu menunjukkan pula bahwa penjual jamu serbuk telah melakukan penyimpanan dengan baik yaitu disimpan dalam tempat yang kering, tidak lembab, dan tidak terkena sinar matahari langsung untuk menghindari pertumbuhan jamur.
Pada penelitian uji AKK ini didapatkan nilai Standar Deviasi (SD) untuk masing-masing sampel A, B, dan C berturut-turut yaitu sebesar 0 , 0, dan 0. Nilai Koefisien Variasi (CV) untuk masing-masing sampel A, B, dan C berturut-turut yaitu sebesar 0 % , 0 %, 0 %. Berdasarkan nilai CV tersebut, dapat diketahui bahwa hasil analisis data ini memiliki tingkat ketelitian yang sangat teliti (CV = ≤ 1 %) (Kumalasari, Panggabean, Akkas, 2017).
Uji Angka Lempeng Total
Uji ALT merupakan metode untuk menghitung angka cemaran bakteri aerob mesofil yang terdapat dalam sampel dengan metode cara tuang (pour plate) pada media padat dan diinkubasi selama 24-48 jam pada suhu 35-45°C dengan posisi dibalik (Tivani, Amananti, Purgiyanti, 2018).Bakteri yang tergolong mesofil adalah bakteri yang mempunyai suhu pertumbuhan 20-40°C dengan suhu minimum pertumbuhan 10-20°C, dan suhu maksimum 40-45°C (Saweng, Sudimartini, Suartha, 2020).
Prinsip dari metode ALT adalah menumbuhkan sel-sel mikroba yang masih hidup pada suatu atau beberapa media sehingga sel tersebut berkembang biak dan membentuk koloni-koloni yang dapat dilihat langsung dengan mata telanjang tanpa menggunakan mikroskop, dan koloni dapat dihitung menggunakan colony counter (Yunita, Hendrawan, Yulianingsih, 2015)
Media yang digunakan adalah media PCA karena mengandung nutrisi yang cukup untuk pertumbuhan mikroorganisme (Saweng, Sudimartini, Suartha, 2020).
Media PCA mengandung triptone 5.0 gr/L, ekstrak ragi 2.5 gr/L, glukosa 1.0 gr/L dan agar 9.0 gr/L untuk nutrisi pertumbuhan bakteri dengan pH 7,0±0,2. Media ini tidak mengandung agen inhibitor yang hanya membatasi pertumbuhan mikroba
19
tertentu saja, sehingga hampir semua mikroba mesofil aerob dapat tumbuh pada media ini. (Putri, Sudimartini, Dharmayudha, 2020).
Media plate count agar (PCA) ditimbang, dicampur dengan aquadest steril, dan dipanaskan hingga larutan kuning jernih. Selanjutnya media disterilkan meggunakan autoklaf selama 15 menit pada suhu 121˚C. Pada ALT digunakan metode pour plate yaitu dengan mengambil 1 ml sampel (semua seri pengenceran secara duplo) dan dituangkan ke dalam cawan petri steril. Setiap cawan petri, dituang sebanyak ± 15 ml media PCA yang dicairkan pada suhu 45˚±1˚C. Setelah itu media diratakan dengan menggoyangkan cawan petri dan diinkubasi pada suhu 35-45°C selama 24 hingga 48 jam dalam posisi terbalik (Soesetyaningsih, Azizah, 2020).
Kontrol media dilakukan dengan cara menuangkan media PCA pada cawan petri dan membiarkanya memadat tanpa di isi pengenceran. Media PCA dikatakan steril apabila tidak ada pertumbuhan koloni bakteri dan kapang/khamir (Saweng, Sudimartini, Suartha, 2020). Kontrol pengencer dilakukan dengan cara menuangkan media PCA dan pengencer BPW pada cawan petri dan membiarkannya memadat untuk menjamin bahwa sampel tidak terdapat kontaminan dari pengencer. Jumlah koloni yang tumbuh diamati dan dihitung menggunakan colony counter (Yunita, Hendrawan, Yulianingsih, 2015).
Kontrol Media Kontrol Pengencer
Gambar 3. Kontrol Media dan Kontrol Pengencer Uji ALT
Pada uji ALT dilakukan pula uji kontrol media dan kontrol pengencer. Hasil uji kontrol media dan kontrol pengencer dapat dilihat pada Gambar 2. yaitu tidak terdapat bakteri atau cemaran yang menandakan bahwa tidak ada kontaminan dari
20
media dan pengencer yang digunakan. Hasil pengamatan rata-rata replikasi ALT selama inkubasi ditunjukkan pada Tabel.2
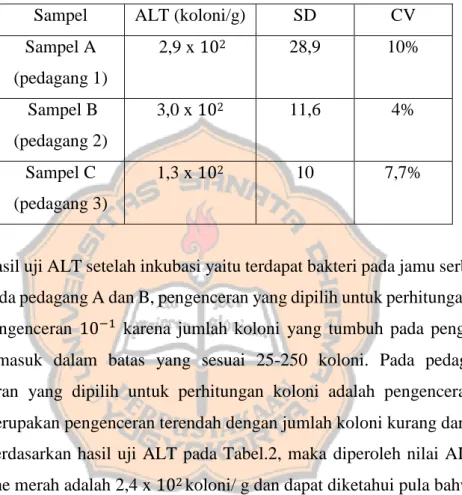
Tabel 2. Angka Lempeng Total pada jamu serbuk jahe merah setelah inkubasi
Sampel ALT (koloni/g) SD CV
Sampel A (pedagang 1)
2,9 x 102 28,9 10%
Sampel B (pedagang 2)
3,0 x 102 11,6 4%
Sampel C (pedagang 3)
1,3 x 102 10 7,7%
Hasil uji ALT setelah inkubasi yaitu terdapat bakteri pada jamu serbuk jahe merah. Pada pedagang A dan B, pengenceran yang dipilih untuk perhitungan koloni adalah pengenceran 10−1 karena jumlah koloni yang tumbuh pada pengenceran tersebut masuk dalam batas yang sesuai 25-250 koloni. Pada pedagang C, pengenceran yang dipilih untuk perhitungan koloni adalah pengenceran 10−1 karena merupakan pengenceran terendah dengan jumlah koloni kurang dari 25.
Berdasarkan hasil uji ALT pada Tabel.2, maka diperoleh nilai ALT jamu serbuk jahe merah adalah 2,4 x 102 koloni/ g dan dapat diketahui pula bahwa jamu serbuk jahe merah memenuhi persyaratan yang ditetapkan oleh Peraturan Kepala Bidang Pengawas Obat dan Makanan (BPOM) Republik Indonesia Nomor 12 Tahun 2014, yaitu ALT yang diperbolehkan adalah ≤ 106 koloni/g. Apabila angka lempeng total terlalu tinggi dapat berbahaya bagi kesehatan karena bakteri ini dapat menghasilkan toksin yang menyebabkan penyakit diantaranya muntah, diare, demam dan infeksi (Saweng, Sudimartini, Suartha, 2020).
Nilai Standar Deviasi (SD) untuk masing-masing sampel A, B, dan C berturut-turut yaitu sebesar 28,9; 11,6; dan 10. Nilai Koefisien Variasi (CV) untuk masing-masing sampel A, B, dan C berturut-turut yaitu sebesar 10 % , 4 %, 7,7 %.
Berdasarkan nilai CV tersebut, dapat diketahui bahwa hasil analisis data ini
21
memiliki tingkat ketelitian yang sedang (2 % < CV < 5 %) dan ketelitian yang rendah (CV = > 5 %) (Kumalasari, Panggabean, Akkas, 2017). Hal ini terjadi karena pengukuran jumlah koloni hanya dilakukan sekali, setidaknya dilakukan 3 kali pengukuran masing-masing sampel untuk menghindari subjektivitas dalam pengamatan atau analisis, pengambilan sampel hanya dilakukan pada 3 toko, dan tempat penyimpanan serbuk jamu yang berbeda dari masing-masing penjual.
Adanya cemaran bakteri pada jamu serbuk jahe merah dapat berhubungan dengan pemilihan bahan baku jahe merah, proses pengolahan serbuk jamu, pengemasan produk jamu serbuk, dan penyajian kaitannya dengan pekerja dan lingkungan. Higiene atau masalah kesehatan dan kebersihan syarat penting bagi pembuat jamu. Kesehatan dan kebersihan pembuat jamu yang terjaga akan menjamin dihasilkannya jamu yang bebas mikroba atau tidak tercemar (Hadijah, 2015). Selain itu, cemaran bakteri dapat terjadi karena adanya pencemaran dari air, udara, faktor kelembaban saat penyimpanan, penyimpanan serbuk jamu jahe merah pada etalase toko obat yang bercampur dengan sediaan obat tradisional lainnya, serta kebersihan dari toko obat yang masih kurang.
Peneliti tidak melakukan identifikasi lebih lanjut pada sampel jamu serbuk jahe merah sehingga tidak diketahui dengan pasti koloni bakteri apa yang tumbuh pada media tersebut. Perlu dilakukan identifikasi bakteri lebih lanjut menggunakan media selektif terhadap bakteri patogen yang mungkin terdapat pada jamu serbuk jahe merah.
22 KESIMPULAN DAN SARAN
Kesimpulan
1. Nilai AKK pada jamu serbuk jahe merah yang dijual di Pasar Beringharjo Yogyakarta sebesar < 10 koloni/ g, maka jamu serbuk jahe merah memenuhi persyaratan KaBPOM 2014 yang menyatakan bahwa angka kapang khamir yang diperbolehkan ≤ 104 koloni/g.
2. Nilai ALT pada jamu serbuk jahe merah yang dijual di Pasar Beringharjo Yogyakarta sebesar 2,4 x 102 koloni/ g, maka jamu serbuk jahe merah memenuhi persyaratan KaBPOM 2014 yang menyatakan bahwa angka lempeng total yang diperbolehkan ≤ 106 koloni/g.
Saran
1. Perlu dilakukan penelitian lebih lanjut mengenai identifikasi jenis cemaran mikroba yang ditemukan pada ALT sediaan jamu serbuk, seperti bakteri Escherichia coli, Salmonella spp, Pseudomonas aeruginosa, dan Staphylococcus aureus.
23
DAFTAR PUSTAKA
Adnyana, I.K. & S.W. Suciyati, 2016. Napak tilas jahe gajah (Zingiber officinale Roscoe var officinalum) dan jahe merah (Zingiber officinale var rubrum).
Jurnal Farmasi Galenika, 3(1), 1-7.
Afifi, C., Sugiarti, L., 2016. Analisis Mikrobiologis Jamu Tujuh Angin dan Sari Asih PT. Jamu Air Mancur Surakarta dengan Metode ALT dan AKK.
Jurnal Keperawatan dan Kesehatan Masyarakat. Vol. 1. No. 5.
Akinyemi, A.J., Ademiluyi, A.O., Oboh, G., Inhibition of Angiotensin-1- Converting Enzyme Activity by Two Varieties of Ginger (Zingiber officinale) in Rats Fed a High Cholesterol Diet. Journal Of Medicinal Food, 17(3). 321-322.
Andriani, R., 2016. Pengenalan Alat-Alat Laboratorium Mikrobiologi Untuk Mengatasi Keselamatan Kerja dan Keberhasilan Praktikum. Jurnal Mikrobiologi, 1(1), 2-4.
Aryanta, 2019. Manfaat Jahe Untuk Kesehatan. E-Jurnal Widya Kesehatan, 1(2), 40.
Azkiya, Z., Ariyani, H., Nugraha, T.S., 2017. Evaluasi Sifat Fisik Krim Ekstrak Jahe Merah (Zingiber officinale Rosc. var. rubrum) sebagai Anti Nyeri (Evaluation of Physical Properties Cream from Red Ginger Extract (Zingiber officinale Rosc var rubrum) As Anti Pain). Journal of Current Pharmaceutica Sciences, 1(1), 13.
Cappuccino, J. G., Sherman, N., 2014. Microbiology : A Laboratory Manual. 10th edition. Pearson Education, Inc., USA.
Departemen Kesehatan Republik Indonesia, 2017. Peraturan Menteri Kesehatan nomor HK.01.07/MENKES/187/2017 tentang Formularium Ramuan Obat Tradisional Indonesia. Departemen Kesehatan Republik Indonesia.
Jakarta.
Diniarti, I. dan Iljanto, S., 2017. Strategi Peningkatan Daya Saing Industri Obat Tradisional (IOT) Tahun 2017. Jurnal Kebijakan Kesehatan Indonesia, 6(3), 184-192.
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 2014. Peraturan Kepala Badan Pengawas Obat dan Makanan RI nomor 12 tahun 2014 tentang Persyaratan Mutu Obat Tradisional. Departemen Kesehatan Republik Indonesia, Jakarta.
24
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 2013. Peraturan Kepala Badan Pengawas Obat dan Makanan RI nomor 35 tahun 2013 tentang Tata Cara Sertifikasi Cara Pembuatan Obat Tradisional Yang Baik.
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 2019. Peraturan Kepala Badan Pengawas Obat dan Makanan RI nomor 32 tahun 2019 tentang Persyaratan Keamanan dan Mutu Obat Tradisional.
Hadijah, S., 2015. Deteksi Cemaran Bakteri pada Jamu Tradisional yang Dijajakan di Kelurahan Banta-Bantaeng, BIOTEK, 3(1), 109.
Handrianto, P., 2016. Uji Antibakteri Ekstrak Jahe Merah Zingiber Officinale Var.
Rubrum Terhadap Staphylococcus Aureus dan Escherichia Coli. 2(1). 3.
Hapsoh, Hasanah, Y. dan Julianti, E., 2010. Budidaya dan Teknologi Pascapanen Jahe. USU Press. Medan. 14.
Katzung and Trevor, 2015. Basic & Clinical Pharmacology. Thirteenth Edition.
McGraw-Hill Education, pp. 1166
Kumalasari, A., Panggabean, A.S., Akkas, E., 2017. Pengembangan Metode Rapid Test dalam Penentuan Ash Content dan Calorific Value Batubara di Laboratorium PT Jasa Mutu Indonesia. Jurnal Atomik, 2(1), 126.
Lallo, S., Mirwan, M., Palino, A., Nursamsiar, Hardianti, B., 2018. Aktifitas Ekstrak Jahe Merah Dalam Menurunkan Asam Urat Pada Kelinci Serta Isolasi Dan Identifikasi Senyawa Bioaktifnya. Jurnal Fitofarmaka Indonesia, 5 (1), 271-278
Larici, A. dan Adawiyah, R., 2017. Inventarisasi Jenis Tumbuhan Berkhasiat Obat di Desa Lahei Kecamatan Muara Lahei Kabupaten Barito Utara. Jurnal Pendidikan Hayati, 3(2), 42.
Levita, J., Syafitri, D.M., Supu, R.D., Mutakin, Megantara, S., Febrianti, M., Diantini, A., 2018. Pharmacokinetics of 10-gingerol and 6-shogaol in the plasma of healthy subjects treated with red ginger (Zingiber officinale var.
Rubrum) suspension. Biomedical Repots, Vol. 9, 474.
Maimunah, 2018. Identifikasi Jenis Jahe Berdasarkan Warna Menggunakan Jaringan Syaraf Tiruan. Information System For Educators And Professionals. 2(2). 147.
Nordin, N. I., 2012. Immunomodulatory Effects of Zingiber officinale Roscoe var.
rubrum (Halia Bara) on Inflammatory Responses Relevant to Psoriasis.
Queen Mary University of London, London, 92.
Oboh, G., Akinyemi, A. J., Ademiluyi, A. O., 2012. Antioxidant and Inhibitory Effect of Red Ginger (Zingiber officinale var. Rubra) and White Ginger
25
(Zingiber officinale Roscoe) on Fe2+ Induced Lipid Peroxidation in Rat Brain In Vitro. Experimental and Toxicologic Pathology, Vol. 64, 34-35.
Permata, D. A. Dan Sayuti, K., 2016. Pembuatan Minuman Serbuk Instan Dari Berbagai Bagian Tanaman Meniran (Phyllanthus Niruri). Jurnal Teknologi Pertanian Andalas, 20(1). 44
Putri, Sudimartini, Dharmayudha, 2020. Standarisasi Cemaran Mikrob Daun Sirsak (Annona muricata L.) sebagai Bahan Baku Sediaan Obat Tradisional.
Indonesia Medicus Veterinus, 9(3), 311.
Radji, M., 2009. Buku Ajar Mikrobiologi : Panduan Mahasiswa Farmasi dan Kedokteran. Penerbit Buku Kedokteran EGC. Jakarta. 64-65, 269.
Rizal, Sumaryati, Suprihana, 2016. Pengaruh Waktu dan Suhu Sterilisasi Terhadap Susu Sapi Rasa Coklat. Jurnal Ilmu-Ilmu Pertanian “Agrika” , 10(1), 2-3.
Samran, Fatimah, C., 2018. Prosiding Seminar Nasional Hasil Pengabdian.
Pembuatan Sediaan Temu Lawak dan Minuman Sehat Bentuk Serbuk Instan Kering. Universitas Muslim Nusantara Al-Washliyah, Medan, pp.
5.
Santoso, H.B. 2008. Ragam & Khasiat Tanaman Obat. PT Agromedia Pustaka.Yogyakarta.
Sari, R.I., Dewi, S.S., Wilson, W., Total Mikrobia Jamu Serbuk Kemasan Dan Tanpa Kemasan Produk Banjarmasin. Jurnal Media Analisis Kesehatan,11(1), 2.
Saweng, C.F.I.J., Sudimartini, L.M., dan Suartha, I.N., 2020. Uji Cemaran Mikroba pada Daun Mimba (Azadiractha Indica A. Juss) Sebagai Standarisasi Bahan Obat Herbal. Indonesia Medicus Veterinus, 9(2), 272-273.
Setyawan, A.D., Wiryanto, Suranto, Bermawie N., 2014. Variation in isozymic pattern of germplasm from three of ginger (Zingiber officinale) varieties.
Nusantara Bioscience, 6(1), 86.
Sitepu, M., Suniti, N. W., Singarsa, I.D.P., 2019. Uji Efektivitas Ekstrak Beberapa Jenis Rimpang Jahe (Zingiber officinale Rosc.) Terhadap Patogen Phytophthora palmivora Butl. Penyebab Busuk Buah Kakao. Jurnal Agroekoteknologi Tropika, 8(3). 317
Soesetyaningsih, E. dan Azizah, 2020. Berkala Sainstek, 8(3), 76-78.
Sukmawati, P. A., Proborini, M. W., dan Kawuri, R., 2012. Identifikasi Fungi dan Total Bakteri pada Jamu Tradisional Di Pasar Kedonganan Kelurahan Jimbaran Kabupaten Badung Provinsi Bali. Jurnal Biologi, 16(2), 31-35.
26
Tivani, I., Amananti, W., dan Purgiyanti., 2018. Uji Angka Lempeng Total (ALT) pada Jamu Gendong Kunyit Asem di Beberapa Desa Kecamatan Talang Kabupaten Tegal. Pancasakti Science Education Journal, 3(1), 3
Wasito, H., 2011. Obat Tradisional Kekayaan Indonesia. Edisi Pertama. Graha Ilmu. Yogyakarta. 13-15. 41-43. 51. 70-71.
Wibowo, D.P., Mariani, R., Hasanah, S.U., Aulifa, D.L., 2020. Chemical Constituents, Antibacterial Activity and Mode of Action of Elephant Ginger (Zingiber officinale var. officinale) and Emprit Ginger Rhizome (Zingiber officinale var. amarum) Essential Oils. Pharmacogn J., 12(2), 404.
Yunita, M., Hendrawan, Y., Yulianingsih, R., 2015. Analisis Kuantitatif Mikrobiologi Pada Makanan Penerbangan (Aerofood ACS) Garuda Indonesia Berdasarkan TPC (Total Plate Count) dengan Metode Pour Plate. Jurnal Keteknikan Pertanian Tropis dan Biosistem, 3(3). 240-241.
27
LAMPIRAN
28 Lampiran 1. Sampel jamu serbuk jahe merah
Lampiran 2. Sampel jamu serbuk jahe merah dalam wadah
29
Lampiran 3. Uji AKK jamu serbuk jahe merah sampel A
A1 A2 B1 B2
C1 C2 D1 D2
Gambar 4. AKK jamu serbuk jahe merah sampel A replikasi 1 Keterangan :
A1 : Sampel jamu A replikasi 1 pengenceran 10-1 (cawan 1) A2 : Sampel jamu A replikasi 1 pengenceran 10-1 (cawan 2) B1 : Sampel jamu A replikasi 1 pengenceran 10-2 (cawan 1) B2 : Sampel jamu A replikasi 1 pengenceran 10-2 (cawan 2) C1 : Sampel jamu A replikasi 1 pengenceran 10-3 (cawan 1) C2 : Sampel jamu A replikasi 1 pengenceran 10-3 (cawan 2) D1 : Sampel jamu A replikasi 1 pengenceran 10-4 (cawan 1) D2 : Sampel jamu A replikasi 1 pengenceran 10-4 (cawan 2)
30
A1 A2 B1 B2
C1 C2 D1 D2
Gambar 5. AKK jamu serbuk jahe merah sampel A replikasi 2 Keterangan :
A1 : Sampel jamu A replikasi 2 pengenceran 10-1 (cawan 1) A2 : Sampel jamu A replikasi 2 pengenceran 10-1 (cawan 2) B1 : Sampel jamu A replikasi 2 pengenceran 10-2 (cawan 1) B2 : Sampel jamu A replikasi 2 pengenceran 10-2 (cawan 2) C1 : Sampel jamu A replikasi 2 pengenceran 10-3 (cawan 1) C2 : Sampel jamu A replikasi 2 pengenceran 10-3 (cawan 2) D1 : Sampel jamu A replikasi 2 pengenceran 10-4 (cawan 1) D2 : Sampel jamu A replikasi 2 pengenceran 10-4 (cawan 2)
31
A1 A2 B1 B2
C1 C2 D1 D2
Gambar 6. AKK jamu serbuk jahe merah sampel A replikasi 3 Keterangan :
A1 : Sampel jamu A replikasi 3 pengenceran 10-1 (cawan 1) A2 : Sampel jamu A replikasi 3 pengenceran 10-1 (cawan 2) B1 : Sampel jamu A replikasi 3 pengenceran 10-2 (cawan 1) B2 : Sampel jamu A replikasi 3 pengenceran 10-2 (cawan 2) C1 : Sampel jamu A replikasi 3 pengenceran 10-3 (cawan 1) C2 : Sampel jamu A replikasi 3 pengenceran 10-3 (cawan 2) D1 : Sampel jamu A replikasi 3 pengenceran 10-4 (cawan 1) D2 : Sampel jamu A replikasi 3 pengenceran 10-4 (cawan 2)