TUGAS KIMIA ORGANIK ASAM KARBOKSILAT
Makalah ini disusun untuk memenuhi tugas kimia organic semester genapJurusan teknik kimia universitas riau
DISUSUN OLEH :
1.
Afriandi
2.
Ahmed Al-syaid
3.
Amalia Ardiana
4.
Anggi Pratama
5.
M.Taufik Kurniawan
6.
Rio Andika
DOSEN PEMBIMBING :Drs. Irdoni HS, MS.
TEKNIK KIMIA FAKULTAS TEKNIK UNIVERSITAS RIAU PEKANBARU 2010KATA PENGANTAR
Senyawa Asam Karboksilat Page 2
Puji dan syukur kami sampaikan kehadirat Tuhan Yang Maha Esa, karena berkat Karunia-Nya kami dapat menyelesaikan makalah ini.
Makalah ini kami buat dan kami susun dengan maksud untuk memenuhi tugas yang diberikan serta untuk menambah pengetahuan pembaca tentang Asam Karboksilat pada mata kuliah Kimia Organik.
Kami haturkan terima kasih kepada bapak Drs. Irdoni HS, MS. yang telah membimbing kami dalam mempelajari mata kuliah Kimia Organik, kemudian kepada teman-teman sejawat yang telah membantu kami dalam penyelesaian makalah ini.
Kami menyadari bahwa makalah ini masih banyak kekurangan. Tetapi kami berharap makalah ini dapat bermanfaat bagi siapapun yang membacanya.
Oleh karena itu, kami mohon maaf atas segala kekurangan dalam penyajian makalah ini, maka dari itu kritik dan saran sangat kami harapkan.
Pekanbaru, Maret 2010
Kelompok
Senyawa Asam Karboksilat Page 3
Kata Pengantar 2
Daftar Isi 3
Daftar Tabel 5
Daftar Flow Chart 6
BAB I PENDAHULUAN 7
I.1 Latar Belakang 7
I.2 Rumusan Masalah 7
I.3 Tujuan Penulisan 8
BAB II PEMBAHASAN 9
II.1 Definisi Asam Karboksilat 9
II.2 Penamaan Asam Karboksilat 9
II.3 Isomer Asam Karboksilat 12
II.4 Sifat-sifat Asam Karboksilat 13
II.4.1 Sifat Spektral Asam Karboksilat 15
II.4.2 Bagaimana Struktur Mempengaruhi Kuat Asam 17
II.5 Keasaman dan Ketetapan Keasaman 33
II.6 Reaksi-reaksi Pembuatan Asam Karboksilat 35
II.7 Reaksi-reaksi Senyawa Asam Karboksilat 43
II.7.1 Reaksi Asam Karboksilat dengan Basa 46
Senyawa Asam Karboksilat Page 4
II.7.3 Reduksi Asam Karboksilat 54
II.8 Kegunaan Asam Karboksilat 55
BAB III KESIMPULAN DAN SARAN 59
BAB IV PERTANYAAN 60
Senyawa Asam Karboksilat Page 5
Daftar Tabel
1. Tabel II.1 Asam-asam karboksilat alifatik 11
2. Tabel II.2 Sifat fisik beberapa asam karboksilat 15 3. Tabel II.3 Resapan inframerah karakteristik untuk asam-asam karboksilat 17
4. Tabel II.4 Harga pKa beberapa asam karboksilat 18
5. Tabel II.5 Harga pKa untuk beberapa asam benzoate 30
Senyawa Asam Karboksilat Page 6
Daftar Flow Chart
1. Flow Chart II.1 reaksi-reaksi pembuatan asam karboksilat 36 2. Flow Chart II.2 reaksi-reaksi senyawa asam karboksilat 44
Senyawa Asam Karboksilat Page 7
Daftar Gambar
1. Gambar 1. Ikatan Hidrogen pada Asam Karboksilat 15
2. Gambar 2. Kenaikan Kekuatan Asam 18
3. Gambar 3. Halida Asam bereaksi dengan H2O 19
4. Gambar 4. Kenaikan keelektronegatifan unsure 20
5. Gambar 5. Kenaikan Kuat Asam 20
6. Gambar 6. Kenaikan Kuat Basa 21
7. Gambar 7. Kenaikan Jari-Jari Atom 22
8. Gambar 8. Kenaikan Kuat Basa 22
9. Gambar 9. Kenaikan Kekuatan Asam 23
10.Gambar 10. Kenaikan Kekuatan Basa 23
11.Gambar 11. Pengaruh Muatan Positif 24
12.Gambar 12. Pengaruh Muatan Positif dan Negatif 25
13.Gambar 13. Kekuatan Asam 26
14.Gambar 14. Pengaruh –Cl dan –COOH 27
15.Gambar 15. Kenaikan Kereaktifan Alkohol 52
16.Gambar 16. Kenaikan Kereaktifan Alkohol Berdasarkan Gugus Samping 52
Senyawa Asam Karboksilat Page 8
BAB I
PENDAHULUAN
I.1 Latar Belakang Asam Karboksilat
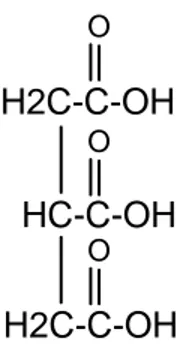
Asam karboksilat disebut golongan asam alkanoat. Asam karboksilat merupakan senyawa karbon yang mempunyai gugus karboksil –COOH. Istilah karboksil berasal dari dua gugus, yaitu gugus karbonil (-CO-) dan gugus hidroksil (-OH). Asam karboksilat merupakan turunan dari alkana dimana sebuah atom H dari alkana diganti gugus –COOH. Rumus umum asam karboksilat adalah R-COOH atau CnH2nO2.
Asam karboksilat adalah suatu senyawa organik yang mengandung gugus karbonil (-COOH ), misalnya : asam formiat, asam asetat, asam propionnat, asam butirat, dan lain-lain. Asam asetat dapat dihasilkan dengan mereaksikan Na-asetat dengan K-hidrosulfat. Suatu ester karboksilat adalah suatu senyawa yang mengandung gugus -COOR dengan R yang berupa alkil atau aril. Ester ini dapat di bentuk dengan mereaksikan langsung suatu asam karboksilat dengan suatu alkohol. Reaksi ini di sebut reaksi esterifikasi, yang berkataliskan asam dan bersifat reversibel.
I.2 Rumusan Masalah Asam Karboksilat
Apa yang dimaksud dengan asam karboksilat ?
Bagaimana sifat fisik dan sifat kimia asam karboksilat ?
Bagaimana cara penulisan tata nama asam karboksilat ?
Bagaimana reaksi-reaksi pembuatan asam karboksilat ?
Apa saja reaksi-reaksi senyawa asam karboksilat ?
Senyawa Asam Karboksilat Page 9 I.3 Tujuan Pembelajaran Asam Karboksilat
Mengetahui definisi dari asam karboksilat
Mengetahui sifat fisik dan sifat kimia asam karboksilat
Mengerti akan cara penulisan tata nama asam karboksilat
Mengerti akan reaksi-reaksi pembuatan asam karboksilat
Mengetahui reaksi-reaksi asam karboksilat
Mengetahui kegunaan dari asam karboksilat
Senyawa Asam Karboksilat Page 10
BAB II
PEMBAHASAN
II.1 DEFINISI ASAM KARBOKSILAT
Asam organic yang paling penting adalah asam-asam karboksilat. Gugus fungsinya adalah gugus karboksil . Kependekan dari dua bagian yaitu gugus karboksil dan hidroksil. Asam karboksilat juga merupakan senyawa karbon turunan alkana. Rumus umum asam karboksilat dapat dipanjangkan atau dipendekan seperti :
O O
–C-OH R – C – OH atau RCOOH atau RCO2H
gugus karboksil tiga cara untuk menulis asam karboksilat
II.2 PENAMAAN ASAM KARBOKSILAT
1. Nama IUPAC
Pada system IUPAC nama asam diturunkan dari nama alkana, akhiran a diganti dengan oat di depannya ditambah kata asam, jadi senyawa ini disebut golongan asam alkanoat.
Untuk senyawa yang mempunyai isomer, tata namanya sama seperti pada aldehid karena gugus fungsinya sama-sama berada pada ujung rantai C. Cara penamannya sebagai berikut .
(a) Rantai pokok adalah rantai yang paling panjang yang mengandung gugus fungsi. Nama alkanoat sesuai nama rantai pokok diberi akhiran oat.
Senyawa Asam Karboksilat Page 11 (c) Penulisan nama dimulai dengan nama cabang atau gugus lain yang diisusun menurut abjad kemudian nama rantai pokok. Karena gugus fungsi pasti nomor satu, jadi nomor gugus fungsi tidak perlu disebutkan.
Contoh : CH3-CH-C-OH CH3 Asam 2-metilpropanoat O Asam 2-amino-4-metilpentanoat CH3 NH2 O CH3-CH-CH2-CH-C-OH Cl O Asam 3-klorobutanoat CH3-CH-CH2-C-OH CH3-CH-CH2- C C-OH Asam 4-hidroksi-2,2-dimetilpentanoat O CH3 CH3 OH
Asam karboksilat yang mempunyai dua gugus fungsi disebut asam alkanadioat. Sedangkan, asam yang mempunyai tiga gugus fungsi disebut asam alkanatrioat.
Contoh :
Asam 1,2-etanadioat (asam oksalat)
HO-C-C-OH O O
Asam 1,3-propanadioat (asam malonat)
HO-C-CH2-C-OH O O
Senyawa Asam Karboksilat Page 12
Asam 1,3,5-pentanatrioat (asam sitrat)
HC-C-OH H2C-C-OH O O O H2C-C-OH Asam 2,2-dimetilpropanoat CH3-C C-OH O CH3 CH3
2. Nama Lazim ( Trivial)
Nama lazim asam karboksilat diambil dari nama asal asam tersebut di alam.
Tabel II.1 Asam-asam karboksilat alifatik
Atom-atom karbon
Rumus Sumber Nama
Biasa
Nama IUPAC
1 HCOOH Semut (Latin, formica) Asam
rformat
Asam metanoat
2 CH3COOH Cuka`(Latin, acetum) Asam
asetat Asam etanoat 3 CH3CH2COOH Susu(Yunani,protos pion=lemak pertama) Asam propionate Asam propanoat 4 CH3(CH2)2 COOH Mentega (Latin,
butyrum)
Asam butirat
Asam butanoat
5 CH3(CH2)3COOH Akat Valerian (Latin, valere = kuat)
Asam valerat
Asam pentanoat
Senyawa Asam Karboksilat Page 13
caper) kaproat heksanoat
7 CH3(CH2)5 COOH Bunga anggur
(Yunani, oenanthe)
Asam enantat
Asam heptanoat 8 CH3(CH2)6 COOH Kambing (Latin,
caper)
Asam kaplirat
Asam oktanaoat 9 CH3(CH2)7 COOH Pelaronium (Yunani,
pelargos)
Asam pelargonat
Asam nonanoat 10 CH3(CH2)8 COOH Kambing (Latin,
caper)
Asam kaprat
Asam dekanoat
II.3 ISOMER ASAM KARBOKSILAT
Seperti alkanal, asam karboksilat juga tidak mempunyai isomer posisi karena gugus fungsinya di ujung rantai C. Karena yang dapat berubah hanya stuktur alkil maka isomernya adalah isomer struktur. Isomer struktur asam karboksilat dimulai dari asam butanoat.
Contoh :
O
1) Isomer struktur C4H9C – OH ada dua, yaitu :
CH3-CH2-CH2-C-OH O Asam Butanoat O CH3-CH2-CH-C-OH CH3 Asam 2-metilbutanoat
Senyawa Asam Karboksilat Page 14
O
2) Isomer struktur C5H11-C-OH ada 4 (empat), yaitu :
CH3-CH2-CH-C-OH O CH3 Asam 2-metilbutanoat CH3-CH-CH2-C-OH O CH3 Asam 3-metilbutanoat Asam 2,2-dimetilpropanoat CH3-C C-OH O CH3 CH3
II.4 SIFAT FISIS dan SIFAT KIMIA ASAM KARBOKSILAT
Anggota-anggota pertama dari asam karboksilat adalah cairan tak berwarna dengan bau yang menyengat. Cuka adalah larutan 4 atau 5% asam asetat, baud an rasanya khas. Asam butirat berasal dari mentega tengik, asam-asam kaproat,kaprilat, dan kaprat berbau kambing.
Sebagaimana diramalkan dari strukturnya, asam karboksilat bersifat polar seperti halnya alcohol. Asam karboksilat membentuk ikatan hydrogen dengan sesamanya atau dengan molekul lain. Karena itu titik didihnya lebih tinggi dibandingkan dengan alcohol dengan bobot molekul yang hampir sama. Misalnya, asam asetat dan n-propil alcohol mempnuyai bobot molekul sama (60) tetapi titik didihnya berturut-turut 118⁰C dan
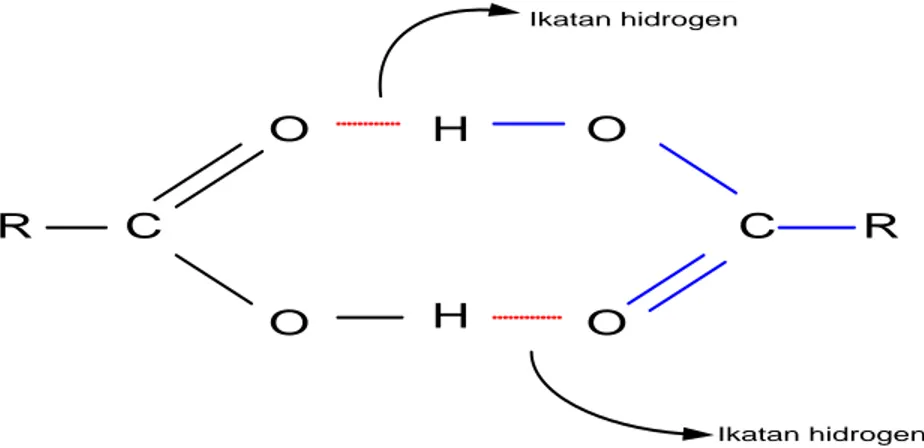
Senyawa Asam Karboksilat Page 15 97⁰C. penetapan bobot molekul menunjukan bahwa asm-asam format dan asetat merupakan dimer dalam pelarut non polar, sekalipun dalam keadaan gasnya. Dua molekul saling berpegangan melalui ikatan hydrogen.
C R Ikatan hidrogen R C H O O H O O Ikatan hidrogen
Gambar 1. Ikatan hidrogen pada asam karboksilat
Ikatan hydrogen juga menjelaskan sifat-sifat kelarutan air pada asam-asam karboksilat berbobot molekul rendah.
Beberapa point tentang sifat fisis dan kimia asam karboksilat , diantaranya adalah
Mengandung gugus COOH yang terikat pada gugus alkil (R-COOH) maupun gugus aril (Ar-COOH)
Asam dengan jumlah C 1 – 4 : larut dalam air Asam dengan jumlah C = 5 : sukar larut dalam air Asam dengan jumlah C > 6 : tidak larut dalam air
Larut dalam pelarut organik seperti eter, alkohol, dan benzen TD asam karboksilat > TD alkohol dengan jumlah C sama.
Suku-suku rendah mudah larut dalam air. Makin banyak atom C dalam molekul kelarutan akan semakin berkurang. Senyawa yang berwujud padat tidak larut dalam air.
Titik didih dan titik lelehnya tinggi, karena antara molekulnya terdapat ikatan hydrogen. Merupakan asam lemah. Makin panjang rantai C makin lemah kekuatan asamnya.
Senyawa Asam Karboksilat Page 16 Tabel II.2 Sifat fisik beberapa asam karboksilat
Nama Td ⁰C tl ⁰C Kelarutan g/100 g H2O pada 25⁰C Format 101 8 Asetat 118 17 Propanoat 141 -22 Bercampur (∞) Butanoat 164 -8 Kaproat 205 -1.5 10 Kaprilat 240 17 0.06 Kaprat 270 31 0.01 Benzoate 249 122 0.4(but 6,8 at 95⁰C)
II.4.1 Sifat Spektral Asam Karboksilat
a. Spektra Inframerah
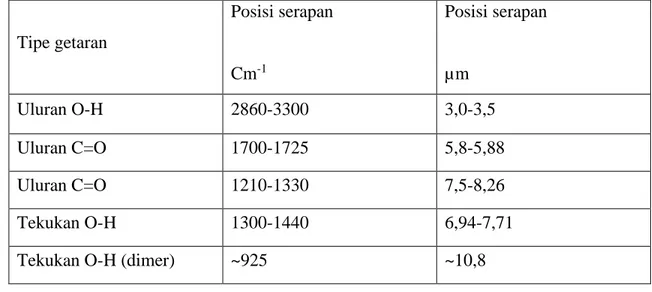
Asam karboksilat, baik sebagai cairan ataupun dalam larutan dengan konsentrasi di atas 0,01 M, berada terutama dalam bentuk dimer berikatan-hidrogen, bukannya dalam bentuk monomer diskrit (discrete). Karena itu spectrum inframerah asam karboksilat adalah spectrum dari dinernya. Karena adanya ikatan hydrogen, resapan uluran OH (dari) asam-asam karboksilat sangat lebar dan intensif. Resapan OH ini mulai sekitar 3300 cm-1 (3,0 µm) dan melandai ked lam daerah resapan karbon-hidrogen alifatik (lihat gambar II.1). Lebarnya pita OH asam karboksilat seringkali dapat mengaburkan resapan CH aromatic dan alifatik, maupun resapan OH atau NH lainnya didalam spectrum itu.
Senyawa Asam Karboksilat Page 17 Resapan karbonil dijumpai pada kira-kira 1700-1725 cm-1 (5,8-5,88 µm), dengan intensitas yang cukup kuat. Konjugasi menggeset resapan ini frekuensi yang lebih rendah: 1680-1700 cm-1 (5,9-5,95 µm).
Daerah sidik jari dalam spectrum inframerah suatu asam karboksilat seringkali menunjukan uluran C – O dan tekukan OH ( lihat table II.3). Getaran tekukan OH lainnya (dari) dimer itu menimbulkan resapan lebar di dekat 925 cm-1 (10,8 µm).
b. Spektra nmr
Dalam spectrum nmr, resapan proton asam (dari) suatu asam karboksilat nampak sebagai suatu singlet jauh dibawah medan (δ = 10-13 ppm), diuar skala dari rentang spectra yang biasa. Proton alfa hanya sedikit sekali dipengaruhi oleh gugus C=O; resapnnya sedikit dibawah medan (sekitar 2,2 ppm) karena efek induktif (dari) karbon karbonil yang positif parsial. Tidak terdapat pola penguraian yang unikk, yang dikaitkan dengan gugus asam karboksilat, karena proton karboksilat tidak mempunyai tetangga proton.
Tabel II.3 Resapan inframerah karakteristik untuk asam-asam karboksilat
Tipe getaran Posisi serapan Cm-1 Posisi serapan µm Uluran O-H 2860-3300 3,0-3,5 Uluran C=O 1700-1725 5,8-5,88 Uluran C=O 1210-1330 7,5-8,26 Tekukan O-H 1300-1440 6,94-7,71
Senyawa Asam Karboksilat Page 18 II.4.2 Bagaimana Struktur Mempengaruhi Kuat Asam
Hanya asam karboksilat, asam sulfonat (RSO3H), dan alkil hydrogen sulfat (ROSO3H) yang merupakan kelompok-kelompok senywa organic yang lebih asam daripada asam karbonat (H2CO3). Dari ketiga kelas ini, sejauh ini asam karboksilat adalah yang paling lazim.
RCH3
RNH2 RC CH
ROH
H2O
ArOH H2CO3
RCOOH
Naiknya kuat asam
Gambar 2. Kenaikan kekuatan asam
Kuat asam adalah suatu istilah yang menjelaskan sejauh mana ionisai suatu asam Bronsted dalam air; makin besar ionisasinya, makin banyak ion hydrogen yang terbentuk dan makin kuat asam itu. Kuat asam dinyatakan oleh Ka atau pKa –nya
(lihat table II.4). Dalam sub-bab ini, akan kita bahas sifat-sifat struktur umum yang menpengaruhi kuat asam suatu senyawa organic. Akan ditekankan pada asam karboksilat, tetapi pembahasan tidak dibatasi hanya untuk senyawa ini.
Reaksi suatu asam lemah dengan air bersifat reversible. Kesetimbangan terletak pada sisi persamaan, yang energinya lebih rendah. Sifat struktur apa saja yang menstabilkan anion dibandingkan dengan asam konjugasinya, akan menambah kuat asam dengan cara menggeser letak kesetimbangan kea rah sisi H3O dan anion (A-).
Senyawa Asam Karboksilat Page 19 Tabel II.4 Harga pKa beberapa asam karboksilat
Nama Trivial Struktur pKa
Format HCO2H 3,75 Asetat CH3CO2H 4,75 Propionat CH3CH2CO2H 4,87 Butirat CH3(CH2)2CO2H 4,81 Trimetilasetat (CH3)3CCO2H 5,02 Fluoroasetat FCH2CO2H 2,66 Kloroasetat ClCH2CO2H 2,81 Bromoasetat BrCH2CO2H 2,87 Iodoasetat ICH2CO2H 3,13 Dikloroasetat Cl2CHCO2H 1,29 Trikloroasetat Cl3CCO2H 0,7 α-kloropropionat CH3CHClCO2H 2,8 β-kloropropionat ClCH2CH2CO2H 4,1 Laktat CH3CHCO2H 3,87 Vinilasetat CH2=CHCH2CO2H 4,35
Gambat 3. Halida asam bereaksi dengan H2O
Faktor-faktor utama yang mempengaruhi kestabilan A-, dan dengan demikian juga mempengaruhi kuat asam HA, adalah: (1) keelektronegativan atom yang mengemban muatan negative dalam A-; (2)ukuran A-; (3) hibridisasi atom yang mengemban muatan negative dalam A-;(4) efek induktif atom-atom atau gugus-gugus lain yang terikat pada atom negative dalam A-; (5) stabilisasi-resonansi A-; dan (6) solvasi A-Secara bergiliran sifat-sifat ini akan dibahas
HA + H2O
H30
++ A
-Energi lebih rendah berarti HA asam yang
Senyawa Asam Karboksilat Page 20 dibawah ini, namun perlu selalu diingat bahwa sifat-sifat ini tidak bekerja sendiri-sendiri tanpa berkaitan.
A. keelektronegatifan
Sebuah atom yang lebih elektronegatif mengikat electron-elektron ikatan dengan lebih erat daripada atom yang kurang elekronegatif. Dalam pembandingan anion, anion dengan atom yang lebih stabil. Oleh karena itu, bila dimulai dari kiri ke kanan dalam Daftar Berkala, akan dijumpai bahwa unsure-unsur membentuk anion yang makin stabil dan bahwa konjugasinya makin kuat.
F
O
N
C
Meningkatnya keelektronegatifan unsur
Gambar 4. Kenaikan keelektronegatifan unsur
R2N-H
RO-H
F-H
R3C-H
Naiknya kuat asam
Gambar 5. Kenaikan kuat asam
Kuat basa (dari) basa konjugasinya justru terbalik. Anion suatu asam y ang sangat lemah merupakan basa yang sangat kuat, sedangkan anion asam yang lebih kuat akan merupakan basa yang lebih lemah.
Senyawa Asam Karboksilat Page 21
Naiknya kuat basa
R2N
-R3C
-RO
-F
-Gambar 6. Kenaikan kuat basa
Sebagai contoh, perhatikan reaksi ionisasi dari etanol dan HF dalam air. Sebagai suatu unsure, F lebih eletronegatif daripada O. Jadi, ion fluoride lebih mampu mengemban muatan negative daripada ion alkoksida. Meskipun HF suatu asam lemah, tetapi merupakan asam yang jauh lebih kuat daripada etanol. Sebaliknya ion fluoride merupakan basa yang lebih lemah daripada ion etoksida.
CH3CH2OH + H20
CH3CH2O
-+ H3O
+Asam lebih lemah pKa = 16
Senyawa Asam Karboksilat Page 22
HF + H2O
F
-+ H3O
+Asam lebih kuat pKa = 3,45
basa lebih lemah
B. Ukuran
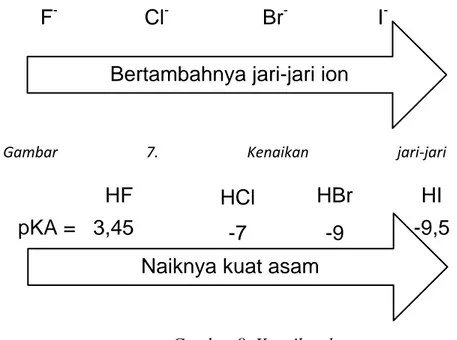
Atom yang lebih besar mampu menyebar suatu muatan negative ddengan baik daripada atom kecil. Penyebaran muatan akan menyebabkan penstabilan. Jadi makin besar ukuran atom yang mengikat H dalam suatu deret senyawa dalam grup mana saja dari Daftar Berkala, kestabilan anionnya akan bertambah, demikian pula kuat asamnya. Karena ukuran atom fluor yang kecil itu, HF merupakan asam yang lebih lemah daripada hydrogen halide lain,, meskipun fluor lebih elektronegatif dibandingkan halogen lain.
F
-Bertambahnya jari-jari ion
Cl
-Br
-I
-Gambar 7. Kenaikan jari-jari atom
HCl
HF
HBr
HI
-7
pKA = 3,45
-9
-9,5
Naiknya kuat asam
Gambar 8. Kenaikan kuat asam C. Hibridisasi
Bertambahnya karakter s orbital halide (dari) karbon dalam deret sp3→ sp2→ sp berarti bertambahnya keeletronegatifan karbon tersebut, dan dengan demikian
Senyawa Asam Karboksilat Page 23 bertambahnya polaritas ikatan CH dan bertambahnya kuat asan. Keelektrobegatifan yang lebih besar (dari) atom yang mengikat H juga akan menmbah kestabilan anion dan dengan demikian keasaman senyawa. Karena alas an-alasan ini, maka suatu proton alkunil lebih bersifat asam daripada proton alkenil, yang selanjutnya juga lebih bersifat asam daripada proton sebuah alkana.
Gambar 9. Kenaikan kekuatan asam
Sekali lagi, asam terkuat dalam suatu deret akan menghasilkan anion yang bersifat basa terlemah.
CH3CH2
-CH2=CH
-CH
C
-Naiknya kuat basa
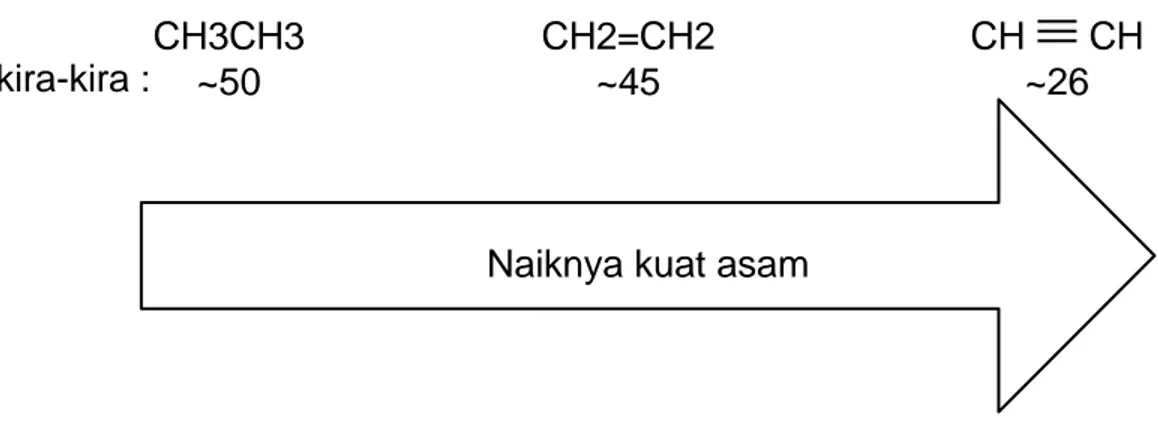
Gambar 10. Kenaikan kekuatan basa CH2=CH2 ~45 pKa kira-kira : CH3CH3 ~50 CH CH ~26
Senyawa Asam Karboksilat Page 24 D. Efek induktif
Sejauh ini telah dibahas bagaimana atom yang terikat langsung pada suatu hydrogen mempengaruhi kuat asam. Namun, bagian-bagian lain dari sebuah molekul juga dapat mempengaruhi kuat asam. Bandingkan harga pKa untuk
asam asetat dan asam kloroasetat berikut:
CH3CO2
Asam asetat pKa 4,75ClCH2CO2H
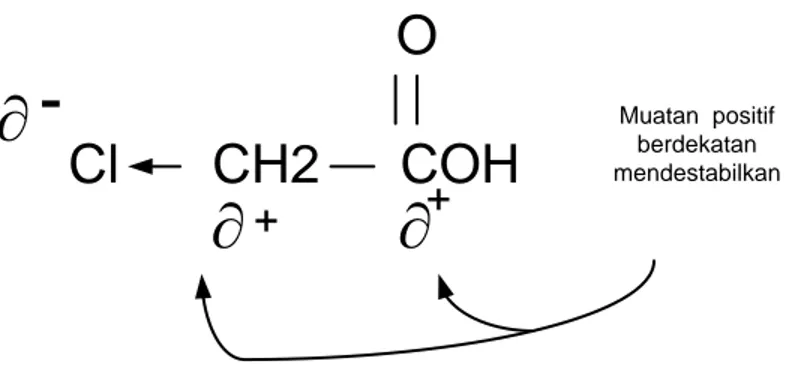
Asam kloroasetat pKa 2,81Sebagai asam, asam kloroasetat jauh lebih kuat daripada asam asetat. Keasaman yang diperbesar ini timbul dari efek induktif klor yang elektronegatif itu. Dalam asam karboksilat yang tak terionkan, Cl yang menarik electron mengurangi rapatan electron dari karbon α. Akibatnya ialah struktur berenergi-tinggi karena muatan-muatan positif berdekatan.
Cl
COH
O
CH2
+
-
+
Muatan positif berdekatan mendestabilkanGambar 11. Pengaruh muatan positif
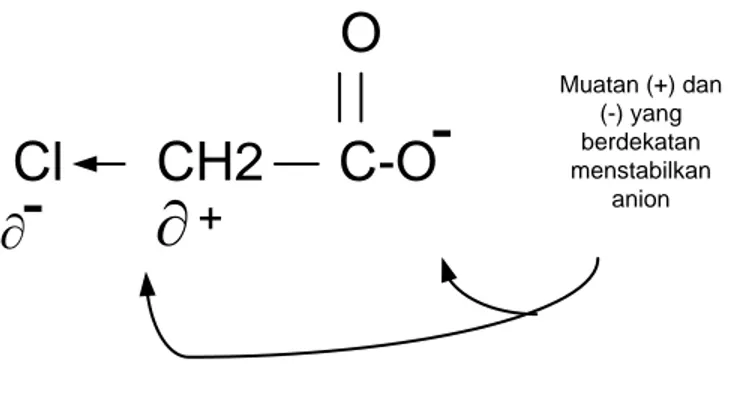
Namun, dengan adanya klor akan mengurngi energy anion. Dalam hal ini, muatan negative gugus karboksilat sebagian tersebar oleh muatan δ+ di dekatnya.
Senyawa Asam Karboksilat Page 25
Cl
C-O
O
CH2
+
-
Muatan (+) dan (-) yang berdekatan menstabilkan anion-Gambar 12. Pengaruh muatan positif dan negatif
Efek suatu gugs elektronegatif di dekat gugus karboksil adalah memperkuat sifat asam dengan cara mendestabilkan asam itu dan menstabilkan anionnya, relative satu terhadap yang lain.
ClCH2COH + H2O
ClCH2CO
-+ H3O
+O
O
Kurang stabil dibandingkan CH3CO2H Lebih stabil dibandingkanCH3CO2-Berikut ini daftar gugus dalam urutan daya menarik elektronnya:
N i l a
CH3- H- CH2=CH- C6H5- HO- CH3O- I- Br- Cl-
Senyawa Asam Karboksilat Page 26 nilai pKa asam-asam karboksilat beikut ini mencerminkan selisih penrikan-elektron oleh gugus-gugus yang terikat pada –CH2CO2H:
Gambar 13. Kekuatan asam
Gugus-gugus penarik electron tambahaan akan menggandakan efek induktif itu. Asam dikloroasetat merupakan asam yang lebih kuat daripada asam kloroasetat, dan asam trikloroasetat merupakan asam terkuat di antara ketiganya. P e n g a
ruh efek induktif pada kuat asam akan berkurang dengan makin banyaknya atom yang berada antara gugus karboksil dan gugus elektronegatif itu. Asam 2-klorobutanoat cukup lebih kuat daripada asam butanoat sendiri; namun asam 4-klorobutanoat mempunyai harga pKa yang mendekati harga pKa asam tak tersubstitusi.
CH3CH2CO2H CH3CO2H CH2=CHCH2CO2H C6H5CH2CO2H HOCH2CO2H ClCH2CO2H pKa : 4,87 4,75 4,35 4,31 3,87 2,81
Bertambahnya kuat asam
ClCH2CO2H Asam kloroasetat pKa 2,81 Cl2CHCO2H Asam dikloroasetat pKa 1,29 Cl3CCO2H Asam trikloroasetat pKa 0,7
Senyawa Asam Karboksilat Page 27 Gambar 14. Pengaruh –Cl dan -COOH
E. Stabilisasi-resonansi
Alkohol, fenol. Dan asam karboksilat ketiganya mengandung gugus OH. Meskipun demikian ketiga kelas senyawa ini beranekaragam secara dramatis dalam hal kuat-asamnya. Perbedaan ini dapat disebabkan langsung oleh adanya (atau tak-adanya) stabilisasi-resonansi anion, relative terhadap asam konjugasinya.
ROH ArOH RCOOH
pKa kira-kira
15-19 10 5
Dalam hal alcohol, anionnya tidak terstabilkan oleh resonansi. Muatan negative suatu ion alkoksida tinggal seluruhnya pada oksigen dan tidak didelokalisasikan. Pada ujung lain (dari) skala terdapat asam karboksilat. Muatan negative ion karboksilat dibagi secara sama oleh dua atom oksigen yang elektronegatif itu, Fenol terletak di tengah, antara asan karboksilat dan alcohol dalam hal keasaman. Oksigen suatu ion fenoksida berdekatan dengan cincin aromatic dan muatan negative itu sebagian terdelokasikan oleh awan piaromatik.
suatu alkoksida :
CH3CH2O
- tidak adastabilisasi-resonansi CH3CH2CH2CO2H pKa 4,8 CH2CH2CH2CO2H 4,5 Cl CH3CHCH2CO2H 4,0 Cl CH3CH2CHCO2H 2,9 Cl
Senyawa Asam Karboksilat Page 28 O-
-
O O -O -Penyumbang utama Suatu fenoksida :Suatu karboksilat :
CH3C-O- CH3C=O
Penumbang sama besarO
O
-F. Solvasi
Solvasi anion dapat memainkan peranan utama dalam keasaman suatu senyawa. Dengan berasosiasi dengan sebuah anion, molekul-molekul pelarut menstabilakan anion dengan cara membantu menyebar muatan negative lewat antaraksi dipol-dipol. Setiap factor yang menambah derajat solvasi dari anion itu akan menambah keasaman senyawa itu dalam larutan. Misalnya, air mempunyai kemampuan yang lebih besar untuk mensolvasi ion daripada etanol, dengan factor sekitar 105!
G. Kuat asam dari asam benzoate tersubstitusi
Mungkin diharapkan bahwa stabilisasi-resonansi oleh awan pi aromatic memainkan peranan besarr dalam hal kuat asam relative dari asan benzoate dan asam-asam benzoate tersubstitusi – namun, etrnyata tidak demikian. Muatan negative ion karboksilat terbagi oleh keedua atom oksigen karboksilat, ttapi muatan ini tidak dapat dideloalikasikan secara efektif oleh concon aromatic. (Oksigen-oksigen anion karboksilat tidak langsung berdekatan dengan cincin aronatik; struktur-struktur resonansi yang padanya muatan negative didelokalisasikan oleh cinicn tak dpat digambar).
Senyawa Asam Karboksilat Page 29 Meskipun muatan negative ion benzoate tidak didelokalisasikan oleh cincin benzene, asam benzoate lebih kuat daripada fenol. Dalam ion benzoate, muatan negative dibagi secara sama oleh dua atom oksigen elektronegatif. N
a m u n
dalam ion fenoksida, sebagian besar mmuatan terletak pada atom oksigen tinggal itu.
Karena cincin benzene tidak mengambil bagian dalam stabilisasi-resonanso dari gugus karboksilat, substituent pada cincin benzene mempengaruhi keasaman terutama dengan efek induktifnya. Tanpa memperhatikan posisi s u b s t i t u s i
, suatu gugus penarik-elektron biasanya akan menaikkan keasaman suatu asan benzoate (Tabel II.6)
C
O
-O
C
O
O
-Cl CO2H CO2H Cl Cl CO2HSenyawa Asam Karboksilat Page 30 Alasan mengapa substituent elektronegatif menaikkan kuat asam, sekali lagi, adalah adanya destabilisasi asamnya dan stabilisasi anionnya,
S u a
tu substituent alkil yang melepas-elektron yakni yang berposisi -m atau –p terhadap gugus karboksil, mengurangi kuat asam (dari) sebuah asam benzoate. Dengan melepaskan electron, substituent itu menstabilkan asam yang tak terionkan dan mendestabilkan anionnya.
T a b O2N CO2 -O2N CO2H -H + R
COOH R COOH Gugus alkil m- atau p- mengurangi kuat asam
Senyawa Asam Karboksilat Page 31 Tabel II.5 Harga pKa untuk beberapa asam benzoate
Asama Posisi substi tusi dari pKa Orto Posisi substit usi dari pKa Meta Posisi substi tusi dari pKa Para
COOH
4,2 4,2 4,2 CH3 COOH 3,9 4,3 4,4 HO COOH 3,0 4,1 4,5 CH3O COOH 4,1 4,1 4,5 Br COOH 2,9 3,8 4,0Senyawa Asam Karboksilat Page 32 Cl COOH 2,9 3,8 4,0 O2N COOH 2,2 3,5 3,4
Hampir semua substituent –orto (baik pelepas-elektron maupun penarik-elektron) Menaikkan kuat asam (dari) suatu asam benzoate. Alasan efek –orto ini, agaknya Merupakan gabungan antara factor sterik dan elektronik.
X
COOH
Subtituen -o menaikkan kuat asam
Senyawa Asam Karboksilat Page 33 Contoh Soal :
Dalam table II.6 tampak bahwa asam p-hidroksibenzoat lebih lemah daripada Asam benzoate, meskipun gugs hidroksil bersifat menarik-elektron. Sarankan Penjelasannya. (Petunjuk: Tulis struktur-struktur resonansi untuk anionnnya yang menunjukan delokalisasi electron-elektron menyendiri pada OH oleh cincin benzene).
Jawab:
Penentuan kuat asam adalah suatu contoh destabilisas-resonansi (dari) anion benzoate. Kuncinya terletak dalam struktur yang dilingkari dibaewah ini, dalam mana muatan negative berdekatan dengan gugus –CO2-. Struktur resonansi memberikan sedikit sumbangan kepada struktur sebenarnya dari hibrida resonansi.
Senyawa Asam Karboksilat Page 34 HO CO2- HO+ CO2
-HO+-
CO2- HO+ CO2-II. 5 KEASAMAN DAN TETAPAN KEASAMAN
Asam karboksilat mengurai dalam air menghasilkan anion karboksilat dan ion hidronium.
+ O+ H H H Ion hidronium R C O -O Ion karboksilat HOH + R C O OH ( II.1)
Keasaman diukur secara kuantiatif dengan tetapan keasaman atau ionisasi, Ka . nilai Ka suatu asam dinyatakan
(RCO2-)(H2O+) Ka =
Senyawa Asam Karboksilat Page 35 Yaitu tetapan kesetimbangan untuk reaksi pers. II.1 . konsentrasi air diabaikan dari pembagi (air adalah pelarut dalam pengukuran ini, jumlahnys sangat banyak sehingga tidak dipengaruhi oleh sejumlah kecik asam yang terlarut). Makin besar nilai Ka , makin kuat suatu asam (makin besar Ka,, makin besar pembilang pada pers. II.2, atau makin besar konsentrasi H3O+). Asam dengan Ka sebesar 10-4 adalah 10 kali lebih kuat daripada asam dengan nilai Ka 10-5.
Karena Ka biasanya dinyatakan dengan bilangan eksponen, keasaman sering dinyatakan dalam pKa, logaritma negative dari Ka (pKa = -log Ka). misalnya, jika Ka = 10-5. Maka pKa = 5. Tabel 1.2 memuat tetapan keasaman beberapa asam karboksilat dan beberapa asam. Dalam membandingkan data dalam table ini, perlu diingat, bahwa semakin besar nilai Ka, semakin kecil nilai pKa,, atau semakin kuat suatu asam.
Contoh :
Manakah lebih kuat asam format atau asam asetat dan berapa kali lipat kekuatannya?
Jawab
Asam format lebih kuat karena Ka-nya lebih besar, perbandingan keasamannya ialah:
2,1 x 10-4 1,8 x 10-5
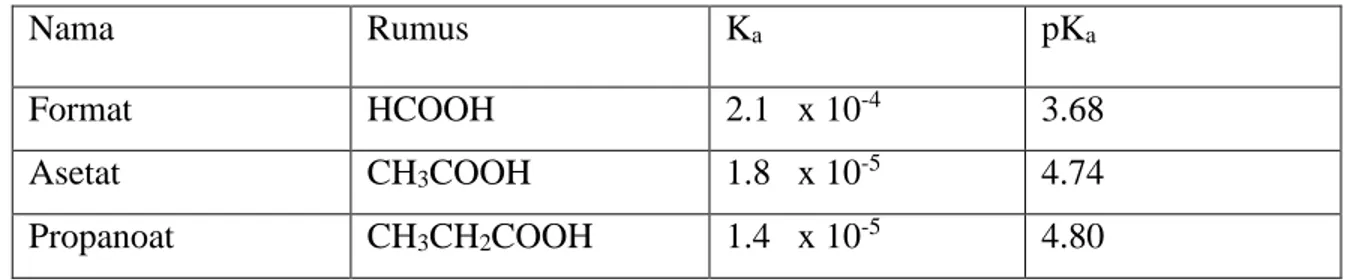
Tabel II.6 Tetapan ionisasi beberapa asam
Nama Rumus Ka pKa
Format HCOOH 2.1 x 10-4 3.68
Asetat CH3COOH 1.8 x 10-5 4.74
Senyawa Asam Karboksilat Page 36 Butanoat CH3CH2CH2COOH 1.6 x 10-5 2.82 Kloroasetat ClCH2COOH 1.5 x 10-3 1.30 Dikloroasetat Cl2CHCOOH 5.0 x 10-2 0.70 Trikloroasetat CCl3COOH 2.0 x 10-1 2.85 2-klorobutanoat CH3CH2CH2ClCOOH 1.4 x 10-3 4.05 3-klorobutanoat CH3CHClCH2COOH 8.9 x 10-5 4.18
Asam benzoate C6H5COOH 6.6 x 10-5 2.90
o-klorobenzoat o-Cl-C6H4COOH 12.5 x 10-4 3.80 m-klorobenzoat m-Cl-C6H4COOH 1.6 x 10-4 4.00 p-klorobenzoat p-Cl-C6H4COOH 1.0 x 10-4 10.0 p-nitrobenzoat P-NO2-C6H4COOH 4.0 x 10-4 5.40 Fenol C 6H5OH 1.0 x 10-10 10.0 Etanol CH3CH2OH 1.0 x 10-16 16.0
II.6 REAKSI-REAKSI PEMBUATAN ASAM KARBOKSILAT
Flow Chart II.1 reaksi-reaksi pembuatan asam karboksilat
reaksi-reaksi pembuatan Asam Karboksilat Hidrolisis Ester Amida Anhidrida Halida Asam Nitril Oksidasi Alkohol Primer Aldehid Alkena Alkilarena Metil Keton Reaksi Grignard
Senyawa Asam Karboksilat Page 37 Sejumlah besar jalur sintetik untuk mendapatkkan asam karboksilat dapat dikelompokkan dalam tiga tipe reaksi : (1) hidrolisis derivate asam karboksilat
(2) reaksi oksidasi (3) reaksi Grignard
(1) Hidrolisis derivate asam karboksilat.
Hidrolisis derivate asam karboksilat terjadi dari serangan air atau OH- pada karbon kabonil (atau karbon –CN pada suatu nitril) dari derivate itu. Hidrolisis suatu ester yang menghasilkan suatu asam karboksilat dan alcohol adalah khas dari kelompok reaksi ini.
a. Ester
RC-OR’ + H2O
RCOOH + HOR’
O
H+ atau OH -b. AmidaRC-NR’ + H2O
RCOOH + HNR2’
O
H+ atau OH -c. AnhidridaSenyawa Asam Karboksilat Page 38
RC-OCR’ + H2O
H+ atau OH-RCOOH + HO2CR’
O
O
d. Halida AsamRC-X + H2O
RCOOH + X
-O
H+ atau OH -e. NitrilRC N + H2O
HRCOOH + NH3
+ atau OH-(2) Oksidasi alcohol primer dan aldehida.
Kekurangan utama dari oksidasi alcohol ialah diperlukannya zat pengoksidasi yang kuat sehingga dalam molekul itu tak boleh ada gugus fungsional yang dapat dioksidasi (kecuali bila gugus itu dilindungi oleh suatu gugus blockade, seperti dibromida dari suatu alkena atau asetal dari suatu aldehida). Bahkan dengan kekurangan ini, oksidasi alcohol primer merupakan prosedur oksidatif yang paling
Senyawa Asam Karboksilat Page 39 sering dilakukan untuk memperoleh asam karboksilat karena selalu tersedianya alcohol.
H2CrO4
RCH2OH RCOOH
Tidak ada ikatan rangkap yang tak terintangi, aldehid, gugus benzil atau
gugus -OH lain
Oksidasi aldehida berlangsung dengan zat pengoksidasi lembut (seperti Ag+) yang tidak mengoksidasi gugus lain; namun, aldehida tidak tersedia semudah alcohol primer.
Oksidasi alkena terutama digunakan sebagai alat analitis, tetapi dapat juga dimanfaatkan untuk mensintetis asam karboksilat. Seperti alcohol, alkena memerlukan zat pengoksidasi yang kuat.
MnO4 kalor
HO2CCH2CH2CH2CH2CO2H
Asam heksanadioat
Sikloheksana
Oksidasi alkilbenzena tersubstitusi merupakan jalan yang bagus untuk memperoleh asam-asam benzoate tersubstitusi. Suatu gugus fungsi karbonil adalah pengarah-meta, tetapi suatu gugus alkil adalah pengaruh o-p. Substitusi elektrofilik suatu alkilbenzena, yang disusul dengan oksidasi, meghasilkan asam benzoate tersubstitusi-o dan p.
Senyawa Asam Karboksilat Page 40
NO2
O2N
CH3
NO2
NO2
NO2
O2N
CO2H
H2CrO4 kalor2,4,6-trinitrotoluena Asam 2,4,6-trinitrobenzoat
a. Alkohol primer
RCH2OH
KMnO4/H2CrO4RCOOH
b. Oksidasi Aldehid
RCH
RCOOH
O
Ag+
c. Oksidasi Alkena
RCH=CR2
KMnO4/H2CrO4RCOOH + R2C=O
Senyawa Asam Karboksilat Page 41
Ar-R
KMnO4/H2CrO4ArCOOH
e. Oksidasi Metil Keton
RCCH3 + X2
RCOOH + CHX3
O
OH-(3) Reaksi Grinard S u a t ureaksi Grignard antara suatu reagensia Grignard (primer, sekunder, tersier, vinilik atau aril) dan karbon dioksida (berbentuk gas atau es kering) seringkali merupakan metode terpilih untuk membuat suatu asam karboksilat.
MgBr
CO2COOH
H2O
Fenil magnesium bromida Asam benzoat
Berikut ini ringkasan jalur-jalur sintetik yang lazim untuk mendapatkan asam karboksilat, dipandang dari segi lain – yakni dilihat dari apa yang terjadi pada
RX
RMgX
R
RCOOH
Mg CO2 eter H+O
OMgX
C
Senyawa Asam Karboksilat Page 42 molekul itu sebagai suatu keseluruhan. Sintesis dari suatu alkil halide lewat nitril atau reagensia Grignard menghasilkan asam karboksilat yang satu karbon lebih banyak daripada alkil halidanya.
Pemanjangan rantai :
1
0RX RCN RCOOH
CN- H2O, H+ SN2Oksidasi alcohol primer (atau aldehida) tidak mengubah panjang rantai, demikian pula hidrolisis suatu derivate asam karboksilat.
RCH2OH
KMnO4/H2CrO4RCOOH
RC-OR’ + H2O
RCOOH + HOR’
O
H+ atau OH-RX
RMgX
RCOOH
Mg CO2 eter H+Senyawa Asam Karboksilat Page 43 Oksidasi suatu alkena (kecuali bila alkena itu siklik) menyebabkan fragmentasi rantai induk.
RCH=CR2 RCO2H + O=CR2
MnO4 -Kaor
Senyawa Asam Karboksilat Page 44 II.7 REAKSI-REAKSI SENYAWA ASAM KARBOKSILAT
( Flow Chart II.2 Reaksi-reaksi senyawa asam karboksilat)
1. Netralisasi
2. Estersifikasi
3. Pembentukan Klorida Asam
Reaksi-reaksi senyawa asam karboksilat
Netralisasi Estersifikasi
Pembentukan Klorida Asam Pembentukan Amida Reduksi menjadi Alkohol Subtistusi Gugus alkil/aril
Dekarboksilasi
RCOOH + NaOH
H2ORCOONa + H2O
RCOOH + R’OH
H+RCOOR’ + H2O
RCOOH + SOCl2 atau PCl
RCCl
O
Senyawa Asam Karboksilat Page 45 4. Pembentukan Amida
5. Reduksi menjadi alcohol
RCOOH
LiAlH4RCH2OH
6. Subtitusi gugus alkil/aril
a. Alfa halogenasi pada asam alifatik O OH + NH3 C O ONH4 C O R R R NH2 C H2O
Senyawa Asam Karboksilat Page 46
R-CH2-COOH + X2
R-CH-COOH + HX
X
P
X2 = Cl2, Br2
b. Subtitusi pada ring dari asam aromatic. Gugus –COOH, kurang mengaktifkan dan mengarahkan subtitusi pada kedudukan –m dalm subtitusi elektro filik
COOH
HNO3/H2SO4COOH
NO2
7. DekarboksilasiRCCR’2COOH
kalorRCCHR’2
O
Senyawa Asam Karboksilat Page 47 II.7.1 Reaksi Asam Karboksilat dengan Basa
Reaksi suatu asam karboksilat dengan suatu basa akan menghasilkan garam.Suatu garam organic mempunyai babyak sifat fisis dari garam anorganik padanannnya. Seperti NaCl atau KNO3, suatu garam organic meleleh pada tempratur tinggi, larut dalam aur, dan tak berbau.
HCO2H + Na
+OH
-HCO
-Na
++ H2O
Asam format natrium format
Anion karboksilat diberi nama dengan menghilangkan kata asam –it dan mengubah akhirannya menjadi –at (Inggris: -ic acid menjadi –ate). Pada nama garam, nama kation mendahului anion sebagai kata terpisah.
Na+ + H2O + CO2 Na+ HCO3
-CO2H + CO2
-Asam
sikloheksana-karboksilat Natrium
Senyawa Asam Karboksilat Page 48 Ion karboksilat merupakan basa lemah dan dapat bertindak sebagai suatu nukleofil. Ester, misalnya dapat dibuat dengan mereaksikan alkil halide yang reaktif dan karboksilat.
CH3CO2H
Asam asetatCH3CO2Na
natrium asetatCOOH
Asam benzoatCOONH4
+ Amonium benzoatHOCCH2CH2CHCO2H
Asam glutamatSuatu asam amino yang dijumpai dalam protein
NH2
HO2CCH2CH2CHCO2
-Na
+Mononatrium glutamat
Suatu zat penyedap (MSG)
NH2
Senyawa Asam Karboksilat Page 49
CH3CO2
-+ CH2-Br C6H5CH2O2CCH3 + Br
Ion asetat benzil bromida benzil asetat(suatu ester)
C6H5
Karena lebih asam daripada asam karbonat, suatu asam karboksilat mengalami reaksi asam-basa dengan natrium bikarbonat maupun basa-basa yang lebih kuat seperti NaOH.
CH3COH + HCO3- CH3CO- + [H2CO3] H2O + CO2 O
O
Sementara asam karboksilat dapdat bereaksi dengan natrium bikarbonat, fenol memerlukan NaOH basa yang lebih kuat, dan alcohol membutuhkan basa yang kebih kuat lagi, seperti NaNH2.
Dalam NaHCO3 :
RCOOH RCO2- + CO2 + H2O
ArOH dan ROH
HCO3 tidak ada reaksi yang berarti
-Senyawa Asam Karboksilat Page 50
Dalam NaOH:
RCOOH RCO2
-+ H2O
ArOH ArO
-+ H2O
ROH
Tidak ada reaksi yang berarti
OH-Perbedaan antara fenol dan asam karboksilat dalam kereaktifaannya terhadapa NaOH dan NaHCO3 merupakan dasar klasifikasi sederhana dan prosedur pemisahan. Jika suatu senywa yang tak larut dalam air, larut dalam larutan NaOH, tetapi tidak ked lam larutan NaHCO3, maka senyawa itu mungkin sekali adalah fenol. Sebalikanya, bila melarut ke dalam keduanya, agaknya senyawa itu adalah suatu asam karboksilat.
Suatu asam karboksilat dapat diekstrak dari dalam suatu campuran senyawa organic yang tak larut dalam air, dengan larutan natrium bikarbonat. Asam itu membentuk garam natrium dan menjadi larut dalam air, sedangkan senyawa organic lain tetap tidak larut. Asam karboksilat bebas akan diperoleh dari larutan air dengan pengasaman.
Bila digunakan sebagai suatu uji atau prosedur pemisahan, reaksi dnegan natrium bikarbonat ini mempunyai pembatasan. Jiak bagian hidrokarbon dari asam karboksilat itu panjang, maka senyawa itu mungkin tidak larut dalam larutan NaHCO3, bahkan juga tidak dalam larutan NaOH. Disamping itu, beberapa fenol, seperti nirtofenol, mempunyai keasaman yang sepadan dengan asam karboksilat; fenol-fenol ini akan larut baik dalam larutan NaHCO3 maupun dalam NaOH.
Senyawa Asam Karboksilat Page 51 II.7.2 Estersifikasi Asam Karboksilat
Suatu ester asam karboksilat ialah suatu senyawa yang mengandung gugus – CO2R dengan R dpat berbentuk alkil atau aril. Suatu ester dapat dibentuk
dengan reaksi langsung antara suatu asam karboksilat dan suatu alcohol, suatu reaksi yang disebut reaksi estersifikasi. Estersifikasi berkatalikan asam daan merupakan reaksi yang reversible.
H+
RCOOH + R’OH
RCOOR’ + H2O
Suatu asam
karboksilat Suatu alkohol
Suatu ester
+ HO
COOH COO + H2O
H+
CH3COOH + CH3CH2OH CH3COOCH2CH3 + H2O
Senyawa Asam Karboksilat Page 52 Laju estersifikasi suatu asam karboksilat bergantung terutama pada halangan sterik dalam alcohol dan asam karboksilatnya. Kuat asam dari asam karboksilat hanya memainkan peranan kecil dalam laju pembentukan eter.
Kereaktivan alcohol terhadap esterifikasi :
Gambar 15.kenaikan Kereaktifan alkohol
Kereaktivan asam karboksilat terhadap esterifikasi :
Gambar 16. Kenaikan kereaktifan alkanoat berdasarkan gugus sampingnya
Seperti banyak reaksi aldehida dan keton,estersifikasi suatu asam karboksilat berlangsung melalui serangkaian tahap protonasi dan deprotinasi. Oksigen karbonil diprotonasi, alcohol nukleofilik menyerang karbon positif, dan eleminasi air akan menghasilkan ester yang dimaksud.
Mekanisme ini dapat diringkas sebagai berikut:
ROH tersier ROH sekunder ROH primer CH3OH
Bertambahnya kereaktifan
R3CCO2H R2CHCO2H RCH2CO2H CH3CO2H HCOOH
Senyawa Asam Karboksilat Page 53 Gambar 17. Pembuatan ester
Perhatikan bahwa dalam reaksi esterifikasi, ikatan yang terputus adalah ikatan C-O (dari) asam karnoksilatlah dan bukan ikatan C-O-H dari asam atau ikatan C-C-O dari alcohol. Bukti untk mekanisme ini ialah reaksi suatu alcohol bertanda seperti CH3 18OH dengan suatu asam karboksilat. Dalam kasus ini,18O itu tetap bersama gugus metil.
Reaksi esterifikasi bersifat reversible. Untuk memperoleh rendemen tinggi dari ester itu, kesetimbangan harus digeser ke arah sisi ester. Satu teknik untuk mencapai adalah menggunakan salah satu zat pereaksi yang murah secara
R-C-OH
OH
OR’
RCOR’ + H2O
Suatu esterO
RCOH + R’OH
Suatu asam karboksilat
O
H+
COOH + CH3
18OH
O
Ikatan C-O tidak putus
OH
COH
18OCH3
H
+C-
18OHCH3 + H2O
O
Senyawa Asam Karboksilat Page 54 berlebihan. Teknik lain ialah membuang salah satu produk dari dalam campuran reaksi (misalnya, dengan deatilasi air secara aerotropik).
Dengan bertambahnya halangan sterik dalam zat-antara, laju pembentukan ester akan menurun. Rendemen esternya pun berkurang. Alasannya ialah karena esterifikasi itu merupakan suatu reaksi yang bersifat reversible dan spesi yang kurang terintangi (pereaksi) akan lebih disukai. Jika suatu eter yang meluah (bulky) harus dibuat, maka lebi baik digunakan jalur sintetik lain, seperti reeaksi antara suatu alcohol dan suatu anhidrida asam atau suatu klorida asam, yang lebih reaktif daripada asam karboksilat dan yang bereaksi dnegna alcohol secara tak reversible.
Ester fenil (RCO2C6H5) umumnya tidak dibuat secara langsung dai fenol dan asam karboksilat karena kesetimbangan lebih cenderung dapat diperoleh dengan menggunakan derivate asam yang lebih reaktif.
II.7.3 Reduksi Asam Karboksilat
Karbon karbonil suatu asam karboksilat berada pada keadaan oksidasi tertinggi yang dapat dicapai oleh karbon dan mamsih tetap merupakan bagian dari suatu molekul organic. (keadaan oksidasi lebih tinggi berikutnya adalah dalam C02). Kecuali terhadap pembakaran atau oksidasi oleh reagensia yang sangat kuat, seperti H2SO4 – CrO3 panas (larutan pembersih), gugus asam karboksilat bersifat lamban ke arah reaksi oksidatif.
Mengherankan bahwa gugus asam karboksilat itu juga lamban (inert) terhadap kebanyakan zat pereduksi (seperti hydrogen plus katalis). Kelambanan ini menyebabakan perlunya dikembangkan metode reduksi alternative, seperti mengubah asam karboksilat menjadi ester dan kemudian ester itu direduksi. Namun, degan diperkenalkannya litium alumunium hidrida (LAH) pada akhir
Senyawa Asam Karboksilat Page 55 tahun 1940-an menyebabkan reduksi itu dapat disederhanakan karena LiAlH4 meredukis gugus karboksil langsung menjadi gugus –CH2OH.
CH3CO2H CH3CH2OH
Asam asetat etanol
LiAlH4/H2O
COOH
LiAlH4/H2OCH2OH
Ringkasan reaksi asam karboksilat adalah sebagai berikut:
RCOOH Suatu asam larboksilat Dimana R=alkil,aril,H,dan sebagainya
Suatu basa seperti
-OH,-OR,atau HCO3
-R’O-H,H+
,kalor
Untuk asam tak terintangi dan alkohol (reaksi reversible)
LiAlH4 H2O, H+ RCOO- Suatu asam karboksilat RCOOR’ Suatu ester RCH2OH suatu alkohol primer
Senyawa Asam Karboksilat Page 56 II.8 KEGUNAAN ASAM KARBOKSILAT
Beberapa asam karboksilat yang banyak digunakan dalam kehidupan sehari-hari adalah
1. Asam formiat (asam semut/asam metanoat)
Asam formiat merupakan zat cair yang tidak berwarna, mudah larut dalam air dan berbau tajam. Dalam jumlah sedikit terdapat dalam keringat, oleh karena itu keringat baunya asam. Asam ini juga menyebabkan lecet atau lepuh pada kulit. Sifat khusus yang dimiliki asam formiat, yaitu dapat mereduksi, karena mempunyai gugud aldehida.
Sifat-sifat reaksi :
-zat cair yang dapat merusak kulit. -bersifat reduktor
Hg(OOCH)2 HC-OH
O
+ HgO Hg(OOCH) + CO2 PUTIH + HC-OH
O
2Hg(OOCH) 2Hg + HCOCH + CO2
Bila dipanaskan dapat terurai menurut 2 macam cara:
HCOOH CO2 + H2
kat= Pd, Cu, Ni, ZnO, SnOHCOOH CO + H2O
kat= H2SO4, Al2O3, SiO2Kegunaan asam formiat, yaitu untuk menggumpalkan lateks, penyamaan kulit, dan pada proses pencelupan tekstil.
Senyawa Asam Karboksilat Page 57 2. Asam asetat (asam cuka/asam etanoat)
Asam asetat dibuat dengan oksidasi alcohol encer oleh O2 udara dengan adanya mikroorganisme (mycroderma acetil).
Suatu larutan alcohol encer (5- 10 %) diteteskan ke dalam kolom yang berisi potongan-potongan kayu, dimana ditempatkan mikroorganisme tersebut.
Dari bawah dapat dipompakan udara. Larutan alcohol waktu turun akan mengalami oksidasi. Temperature harus dipertahankan 25-35⁰C.
Cara lain dari asteilena
HC CH + H2O CH4-C
HgSO4O
H
CH3COOH
Larutan cuka sebagai bahan makanan yang umumnya digunakan sehari-hari mempunyai kadar 25 % volume asam asetat. Asam asetat murni disebut asam asetat
CH3CH2OH CH3C
O
Senyawa Asam Karboksilat Page 58 glacial digunakan untuk membuat selulosa dalam industry rayon, plastic, dalam film fotografi, dan industry obat-obatan.
3. Asam laktat pada susu
Asam laktat merupakan senyawa tidak berwarna, dapat dibuat fermentasi tepung, gula, atau air didih. Dihasilkan dalam susu oleh fermentasi laktosa, sehingga susu menjadi asam. Asam laktat digunakan pada pembuatan keju, minuman ringan, dan asinan.
4. Asam sitrat pada jeruk
Asam sitrat merupakan senyawa putih padat, larut dalam air dan sedikit larut dalam pelarut organic. Banyak ditemukan pada tumbuhan dan hewan, tetapi kandungan paling banyak terdapat pada jeruk. Asam sitrat ditambahkan pada makanan dan minuman untuk memberikan rasa asam, digunakan dalam indsutri obat-obatan, pembuatan kertas, dan tekstil.
5. Asam tartrat pada anggur
Asam tartrat digunakan untuk memberikan rasa pada makanan dan minuman. Digunakan juga dalam fotografi, penyamakan, dan sebagai natrium kalium tartrat yang dikenal sebagai garam Rochelle digunakan untuk obat pencahar.
Senyawa Asam Karboksilat Page 59 6. Asam glutamate pada kecap
Garam glutamate dikenal dengan nama MSG atau monosodium glutamate dipakai untuk penyedap masakan.
Senyawa Asam Karboksilat Page 60
BAB III
KESIMPULAN dan SARAN
Kesimpulan yang dapat diambil adalah asam karboksilat merupakan salah satu turunan dari senyawa alkana, dimana satu atom H dari alkana dig anti dengan gugus karboksil.
Karena kedudukan dari gugus fungsi karboksi (-COOH) tidak boleh berubah atau tetap di ujung rantai karbon maka isomer yang terjadi pada senyawa asam karboksilat adalah isomer struktur. Jadi, yang memungkinkan untuk berubah adalah rantai karbon alkilnya.
Asam karboksilat merupakan jenis asam lemah. Kekuatan asamnya ditentukan oleh haraha konstanta kesetimbangan asamnya (Ka). Dengan basa kuat, asam karboksilat akan bereaksi membentuk garam.
Titik didih asam karboksilat lebih tinggi dibandingkan senyawa alcohol yang memiliki jumlah ataom C yang sama. Titk didih dari asam karboksilat akan terus meningkat sesuai dengan bertambahnya atom C.
Senyawa Asam Karboksilat Page 61
BAB IV
PERTANYAAN
Pertanyaan pada saat presentasi diantaranya adalah
1. Apa perbedaan dari asam askorbat dan asam sitrat ?
Asam askorbat merupakan vitamin C yang biasanya berasal dari jeruk, sama hal nya dengan asam sitrat juga berasal dari jeruk, namun asam sitrat ini biasanya digunakan untuk penambah rasa masam pada makanan ringan atau minuman. Jadi,asam asrkobat dengan asam sitrat berbeda pada penggunaannya dan strukturnya.
2. Kenapa senyawa asam aromatik, asam –asam tersubstitusi dan derivat-derivat asam malonat mudah didekarboksilasi ?
3. Mengapa asam butirat menyebabkan bau tengik ?
Indol, skatol dan asam butirat menyebabkan bau normal pada tinja. Bau busuk didapatkan jika dalam usus terjadi pembusukan protein yang tidak dicerna dan dirombak oleh
kuman. Reaksi tinja menjadi lindi oleh pembusukan semacam itu. Tinja yang berbau tengik atau asam disebabkan oleh peragian gula yang tidak dicerna seperti pada diare. Reaksi tinja pada keadaan itu menjadi asam.
4. Kenapa titik didih asam karboksilat lebih tinggi disbanding dengan alcohol, sedangkan Mr nya hampir sama antara alcohol dengan asam karboksilat ?
Titik didih asam karboksilat lebih tinggi dari pada alcohol yang massa atom relatifnya hampir sama karena asam karboksilat memiliki double ikatan hydrogen sehingga butuh energy yang banyak untuk memutuskannya sehingga titik didihnya tinggi. Sedangkan alcohol tak memerlukan energi tinggi untuk di pisahkan, sehingga ikatan hidrogennya terputus pada suhu yang lebih rendah dari pada asam karboksilat.seperti yang terlihat pada gambar.
Senyawa Asam Karboksilat Page 62 C R Ikatan hidrogen R C H O O H O O Ikatan hidrogen
5. Jelaskan kelarutan yang terjadi pada asam karboksilat ?
Masalah kelarutan dimana C1-C4 larut dalam air, C=5 sukar larut dalam air dan C>5 tidak larut air, ini terjadi karena perbedaan kepolaran, semakin paanjang rantai C maka kepolarannya semakin bertambah sehingga momen dipolnya semakin besar.
6. Jelaskan tentang radikal bebas yang terjadi pada hidrolisis halide asam ?
Radikal bebas yang terjadi pada proses hidrolisis halide asam akan ditarik oleh ion H+ yang masih bebas sehingga hasil nya adalah HX bukan X-.
RC-X + H2O
RCOOH + X
-O
H+ atau OH
-7. Berasal dari bagian tubuh kambing yang manakah asam koprat, kaprilat, dan kaproar ? Bagian tubuh kambing yang menghasilkan asam koprat, asam kaprilat dan asam kaproat adalah keringat kambing itu sendiri
Senyawa Asam Karboksilat Page 63 8. Apa fungsi asam karboksilat pada proses penyabunan ?
Senyawa Asam Karboksilat Page 64
Daftar Pustaka
1. http://www.chem-is-try.org/materi_kimia/kimia-smk/kelas_xi/asam-karboksilat-dan-turunannya/ (23 -3 -2010 1:24 PM)
2. Kuswati, Tine Maria, dkk. 2007. Sains Kimia. Jakarta: Bumi Aksara
3. Respati, Ir. 1986. Pengantar Kimia Organik. Jakarta: Aksara Baru