PERBEDAAN KEKASARAN PERMUKAAN ENAMEL
GIGI PADA PENGGUNAAN KARBAMID
PEROKSIDA 16% DENGAN JUS BUAH TOMAT
(Lycopersicum esculentum Mill,var.commune) SEBAGAI
BAHAN PEMUTIH GIGI
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi syarat guna memperoleh gelar Sarjana Kedokteran Gigi
Disusun oleh: Venosha Rajen NIM : 130600159
Fakultas Kedokteran Gigi
Departemen Ilmu Konservasi Gigi
Tahun 2017 Venosha Rajen
Perbedaan Kekasaran Permukaan Enamel Gigi Pada Penggunaan Karbamid Peroksida 16% Dan Jus Buah Tomat (Lycopersicum esculentum Mill,var.commune) sebagai Bahan Pemutih Gigi
xi + 64 halaman
Penggunaan karbamid peroksida 16% sebagai bahan pemutih gigi menimbulkan efek samping pada enamel gigi. Salah satu efek samping yang terjadi adalah meningkatkanya kekasaran enamel. Permukaan enamel yang kasar akan menjadi tempat perlekatan dan kolinisasi bakteri yang akhirnya akan meningkatkan demineralisasi. Salah satu bahan alami yang mempunyai kemampuan untuk mencerahkan warna gigi adalah buah tomat yang mempunyai kandungan hidrogen peroksida.Tujuan penelitian ini untuk mengetahui perbedaan kekasaran permukaan enamel gigi pada pengunaan karbamid peroksida 16% dengan jus buah tomat sebagai bahan pemutih gigi.
Penelitian dilakukan dengan 30 sampel (15 sampel gigi molar tiga dibagi menjadi 2 bagian) gigi post-ekstraksi, kemudian dilakukan pengukuran kekasaran permukaan enamel gigi menggunakan profilometer. Seluruh akar diolesi dengan cat kuku bening dan direndam dalam saliva buatan. Sampel dibagi menjadi tiga kelompok, kelompok 1 direndam dalam jus tomat 100% yang pembuatannya dengan 200 gram buah tomat dihaluskan tanpa air, kelompok 2 direndam dalam jus tomat 50% dengan 200 gram buah tomat dihaluskan tanpa air kemudian diencerkan menggunakan rumus V1C1=V2C2. Perendaman selama 5 menit setiap 6 jam 3 kali
sehari selama 2 minggu. Kelompok 3 diaplikasikan gel karbamid peroksida 16% selama 6 jam setiap hari selama 2 minggu. Setelah 2 minggu dilakukan pengukuran
Hasil penelitian menunjukkan adanya peningkatan kekasaran permukaan enamel pada masing-masing kelompok. Uji normalitas dengan menggunakan Shapiro-Wilk menunjukkan data hasil penelitian tidak memenuhi asumsi normalitas. Pada uji Kruskall-Wallis didapat p = 0,068 yang menunjukkan tidak ada perbedaan yang signifikan antara penggunaan karbamid peroksida 16% dan jus buah tomat dengan konsentrasi 50% dan 100%. Maka dapat disimpulkan bahwa baik karabamid peroksida 16% maupun jus buah tomat dengan konsentrasi 50% dan 100% dapat menyebabkan peningkatan kekasaran permukaan enamel gigi.
Kata kunci : jus buah tomat, kekasaran permukaan gigi, pemutihan gigi Daftar rujukan : 42 (2003-2016)
PERBEDAAN KEKASARAN PERMUKAAN ENAMEL
GIGI PADA PENGGUNAAN KARBAMID
PEROKSIDA 16% DENGAN JUS BUAH TOMAT
(Lycopersicum esculentum Mill,var.commune) SEBAGAI
BAHAN PEMUTIH GIGI
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi syarat guna memperoleh gelar Sarjana Kedokteran Gigi
Disusun oleh: Venosha Rajen NIM : 130600159
PERNYATAAN PERSETUJUAN
Skripsi ini telah disetujui untuk dipertahankan di hadapan tim penguji skripsi
Medan, 11 Oktober 2017
Pembimbing: Tanda tangan
1. Bakri Soeyono, drg .………
NIP. 19450702 197802 1 001
2. Widi Prasetia, drg ……….
TIM PENGUJI SKRIPSI
Skripsi ini telah dipertahankan di hadapan tim penguji
pada tanggal 11 Oktober 2017
TIM PENGUJI
KETUA
ANGGOTA
: Bakri Soeyono, drg
KATA PENGANTAR
Puji syukur kepada Tuhan Yang Maha Esa telah memberikan rahmat dan karunia-Nya sehingga dapat menyelesaikan skripsi ini sebagai salah satu syarat untuk mendapatkan gelar Sarjana Kedokteran Gigi pada Fakultas Kedokteran Gigi Universitas Sumatera Utara.
Pada kesempatan ini, penulis ingin menyampaikan terima kasih kepada kedua orang tua, Bapak Rajen dan Ibu Sathiavany sebagai tanda hormat, rasa sayang dan terima kasih yang tak terhingga atas kasih sayang, perhatian, dukungan, kesabaran, semangat, kerja keras dan doanya selama ini.
Dalam penelitian dan penulisan skripsi ini, penulis mendapatkan banyak bantuan dan bimbimgan dari berbagai pihak. Untuk itu, dengan segala kerendahan hati dan penghargaan yang tulus, penulis menyampaikan rasa terima kasih kepada :
1. Dr. Trelia Boel, M.Kes Sp.RKG selaku Dekan Fakultas Kedokteran Gigi Universitas Sumatera Utara.
2. Cut Nurliza, drg., M.Kes.,Sp.KG selaku Ketua Departemen Ilmu Konservasi Gigi Fakultas Kedokteran Gigi Universitas Sumatera Utara.
3. Bakri Soeyono, drg., selaku dosen pembimbing skripsi yang telah meluangkan waktu, tenaga, pemikiran, dukungan, kesabaran, bimbingan dan semangat kepada penulis.
4. Widi Prasetia, drg., selaku dosen pembimbing skripsi yang telah meluangkan waktu, tenaga, pemikiran, dukungan, kesabaran, bimbingan dan semangat sehingga skripsi ini dapat terselesaikan.
5. Cut Nurliza,drg.,M.Kes.,Sp.KG selaku dosen penguji yang telah meluangkan waktu, memberi ide dan saran kepada penulis.
6. Siti Salmiah.,drg.,Sp.KGA selaku dosen penasehat akademik yang telah membimbing dan mengarahkan penulis selama menjalani pendidikan di Fakultas
7. Seluruh staf pengajar dan tenaga administrasi FKG USU terutama Departemen Ilmu Konservasi Gigi yang telah memberikan bantuan, bimbingan dan saran kepada penulis.
8. Prof. Dr. Sutomo Kasiman, Sp.PD.,Sp.JP(K) selaku Ketua Komite Etik Penelitian Bidang Kesehatan Universitas Sumatera Utara yang telah memberikan izin untuk melakukan penelitian.
9. Idham Kami, ST, MT., selaku Ketua Jurusan Teknik Politeknik Negeri Medan dan Drs. Moch. Agus Zaenuri, MT selaku Dosen Pembimbing Laboratorium CNC Politeknik Negeri Medan atas dukungan dan bantuan yang telah diberikan selama penulis melaksanakan penelitian.
10. Maya Fitria, SKM., M.Kes., selaku staf pengajar di Departemen Kependudukan dan Biostatistik FKM USU yang telah memberikan bimbingan mengenai analisa statistika kepada penulis.
11. Sahabat terbaik penulis, Jeevitha Dewi serta teman-teman skripsi di Departmen Konservasi Gigi yang telah memberikan dukungan, semangat, doa, harapan dan kebersamaan selama penulis mendapatkan pendidikan di Fakultas Kedokteran Gigi Universitas Sumatera Utara.
12. Semua pihak yang telah banyak membantu penulisan skripsi ini yang tidak dapat saya sebutkan satu persatu.
Penulis menyadari bahwa skripsi ini jauh dari sempurna, untuk itu diharapkan saran dan kritik yang membangun. Semoga skripsi ini dapat memberikan sumbangan pikiran yang berguna bagi fakultas, pengembangan ilmu dan bermanfaat bagi masyarakat.
Medan, 11 Oktober 2017
Penulis
( Venosha ) NIM 130600159
DAFTAR ISI Halaman HALAMAN JUDUL ... HALAMAN PERSETUJUAN... KATA PENGANTAR ... iv DAFTAR ISI... vi DAFTAR TABEL... ix DAFTAR GAMBAR ... x DAFTAR LAMPIRAN... xi BAB 1 PENDAHULUAN 1.1 Latar Belakang ... 1 1.2 Rumusan Masalah ... 5 1.3 Tujuan Penelitian ... 5 1.4 Manfaat Penelitian ... 5
BAB 2 TINJAUAN PUSTAKA 2.1 Struktur Enamel ... 7
2.2 Demineralisasi………... 8
2.3 Perubahan Warna Gigi……... 9
2.4 Pemutihan Gigi……….………... 10
2.5 Mekanisme Pemutihan Gigi... 11
2.6 Bahan Pemutih Gigi... 12
2.6.1 Hidrogen Peroksida………... 13
2.6.2 Karbamid Peroksida... 13
2.7 Indikasi dan Kontraindikasi Bleaching... 15
2.8 Efek Samping Bleaching... 15
2.9 Tomat………... 16
2.9.1 Morfologi Tomat………... 17
2.9.2 Kandungan Tomat... 18
2.11 Metode Pengukuran Kekasaran Permukaan Gigi ... 22
2.12 Kerangka Teori ... 24
BAB 3 KERANGKA KONSEP DAN HIPOTESIS PENELITIAN 3.1 Kerangka Konsep... 25
3.2 Hipotesis Penelitian ... 25
BAB 4 METODOLOGI PENELITIAN 4.1 Jenis Penelitian... 26
4.2 Tempat dan Waktu Penelitian ... 26
4.3 Populasi dan Sampel ... 26
4.3.1 Populasi... 26 4.3.2 Sampel... 26 4.3.3 Besar Sampel ... 27 4.4 Variabel Penelitian... 27 4.4.1 Variabel Bebas.. ... 27 4.4.2 Variabel Tergantung ... 28 4.4.3 Variabel Terkendali ... 28
4.4.4 Variabel Tidak Terkendali ... 28
4.4.5 Identifikasi Variabel Penelitian... 29
4.5 Definisi Operasional ... 30
4.6 Alat dan Bahan Penelitian... 31
4.6.1 Alat Penelitian... 31
4.6.2 Bahan Peneltian ... 31
4.7 Metode Pengumpulan Data/Prosedur Penelitian... 33
4.7.1 Persiapan Sampel ... 33
4.7.2 Perlakuan Terhadap Sampel... 33
4.7.3 Pengukuran Kekasaran Permukaan Gigi... 35
4.8 Analisis Data ... 35
BAB 5 HASIL PENELITIAN 5.1 Hasil Penelitian ... 36
5.1.1 Kekasaran Permukaan Sampel Kelompok 1 ... 36
5.1.2 Kekasaran Permukaan Sampel Kelompok 2 ... 37
5.1.3 Kekasaran Permukaan Sampel Kelompok 3 ... 37
5.2 Analisis Hasil Penelitian ... 38
5.2.1 Uji Kruskal-Wallis……... 38
5.2.2 Uji Mann--Whitney... 39
BAB 7 KESIMPULAN DAN SARAN
7.1 Kesimpulan 46 7.2 Saran 46 DAFTAR PUSTAKA ... 47 LAMPIRAN
DAFTAR TABEL
Halaman
Tabel 1 Kandungan Gizi Buah tomat 18
Tabel 2. Definisi Operasional 28
Tabel 3. Nilai kekasaran permukaan kelompok 1 36
Tabel 4. Nilai kekasaran permukaan kelompok 2 37
Tabel 5. Nilai kekasaran permukaan kelompok 3 38
Tabel 6. Hasil uji Kruskall-Wallis 38
10
DAFTAR GAMBAR
Halaman
Gambar 1 Struktur enamel 8
Gambar 2 Mekanisme pemutihan gigi 12
Gambar 3 Buah tomat 17
Gambar 4 Stylus profilometer 23
Gambar 5 Gambar alat dan bahan 32
Gambar 6 Gigi dipotong 33
Gambar 7 Sampel gigi dibagi 2 bagian 33
Gambar 8 Buah tomat ditimbang 34
Gambar 9 Jus buah tomat 34
Gambar 10 Perendaman sampel gigi 35
Gambar 11 Aplikasi Karbamid Peroksida 16% 35
11 DAFTAR LAMPIRAN Lampiran 1 Alur penelitian Lampiran 2 Biaya Penelitian
Lampiran 3 Gants Chart Lampiran 4 Surat LIPI Bogor
Lampiran 5 Ethical
Clearance
Lampiran 6 Surat Keterangan Politeknik Negeri Medan Lampiran 7 Lembar Hasil Uji Statistik
12
BAB 1 PENDAHULUAN
1.1. Latar belakang
Keinginan masyarakat masa kini terhadap kualitas tampilan gigi mereka sudah semakin meningkat.1 Gigi tidak cukup terlihat rapi tetapi juga harus putih.1 Perubahan warna pada satu atau sekelompok gigi akan terus memberikan sebuah dampak negatif pada keharmonisan senyum seseorang.2 Meskipun warna gigi hanya merupakan salah satu aspek yang terlibat dalam keharmonian wajah, namun tetapi memainkan sebuah peran yang penting karena perubahan pada warna gigi dapat segara dilihat dibandingkan aspek-aspek lain.2
Warna gigi seseorang itu ditentukan oleh warna dentin dan enamelnya. Selain itu, dapat juga dipengaruhi oleh kombinasi dari warna intrinsik dan adanya stain ekstrinsik yang menempel pada pemukaan gigi.1,2,3 Setiap perubahan pada enamel, dentin atau struktur pulpa koronal dapat menyebabkan perubahan transmisi cahaya pada warna gigi.3 Penyebab utama perubahan warna secara ekstrinsik pada gigi adalah kromogen yang berasal dari asupan sumber diet, seperti, kopi, teh, wortel,coklat, atau dari tembakau, larutan kumur, atau plak pada permukaan gigi. Penyebab perubahan warna gigi secara intrinsik antara lain, yaitu : penyebab sistemik, metabolisme ,genetik, serta lokal.1,3
Beberapa metode dan pendekatan dapat dilakukan untuk meningkatkan warna gigi menjadi lebih putih yaitu dengan pasta gigi pemutih, bleaching internal pada gigi non vital, bleaching eksternal pada gigi vital dan scalling.1,3-4 Prosedur bleaching merupakan suatu proses pemutihan gigi yang berubah
13 warna sampai mendekati warna gigi asli dengan proses perbaikan secara kimiawi.3,5 Ada dua metode penggunaan pemutihan gigi, yaitu pemutihan gigi sendiri di rumah (home bleaching) dan pemutihan gigi yang dilakukan dokter gigi (office bleaching).2,5
Bahan pemutih gigi yang biasa digunakan adalah hidrogen peroksida dan karbamid peroksida.5-6 Kedua bahan ini sama-sama menggunakan hidrogen peroksida yang akan terurai menjadi H2O dan O2.5-7
Hidrogen peroksida pada konsentrasi sangat tinggi dapat bersifat mutagenik dan agen pengoksidasi yang kuat melalui pembentukan radikal
bebas. Karbamid peroksida merupakan kombinasi hidrogen peroksida dan urea.5-7 Pemutihan gigi dengan menggunakan karbamid peroksida terdapat dua
macam yaitu home bleaching dengan karbamid peroksida 10-22% karena bahan aman dan efektif yang disetujui oleh American Dental Association (ADA) dan office bleaching yang pemutihannya dilakukan oleh dokter gigi di ruang praktek dengan menggunakan karbamid peroksida 30-37% yang diperlukan aktivasi cahaya (seperti halogen, LED, laser) untuk mempercepat proses pemutihan gigi serta mendapatkan hasil yang efektif.1,5-6
Bahan pemutih gigi yang digunakan pada saat perawatan pemutihan gigi memang masih tergolong aman untuk digunakan. Namun ternyata penggunaan bahan pemutih gigi senyawa kimia masih diperdebatkan karena menimbulkan efek samping pada jaringan gigi dan mulut. Beberapa penelitian menyimpulkan tidak ada efek samping dari penggunaan bahan pemutih gigi pada permukaan gigi, namun ada juga penelitian yang menyimpulkan sebaliknya. Salah satu efek samping yang terjadi adalah perubahan morfologi permukaan enamel seperti meningkatnya porositas enamel, berkurangnya kekerasan enamel dan meningkatnya kekasaran enamel.7
14 demineralisasi pada permukaan enamel gigi. Larutnya prisma-prisma enamel akibat berkontak dengan bahan pemutih gigi akan menyebabkan perubahan kekasaran permukaan enamel. Penggunaan karbamid peroksida 16% dapat menyebabkan terbentuknya porus dan hilangnya komponen kalsium dan fosfor dari permukaan enamel.8
Kekasaran permukaan enamel menjadi suatu studi yang penting, karena permukaan enamel yang kasar akan menjadi tempat perlekatan dan kolonisasi bakteri yang akhirnya akan meningkatkan demineralisasi dan infeksi gingiva.9 Penelitian Soares DG dkk, menyatakan bahan pemutih gigi karbamid peroksida 16% menyebabkan demineralisasi serta meningkatnya kekasaran permukaan enamel.10 Bistey dkk, dalam penelitiannya juga menyimpulkan bahan pemutih gigi baik dengan teknik home bleaching maupun in-office bleaching dapat menyebabkan perubahan morfologi
enamel.11 Penelitian Cavalli V dkk, menunjukkan bahwa penggunaan
karbamid peroksida dengan konsentrasi rendah yang berbeda telah mengakibatkan peningkatan yang signifikan terhadap kekasaran permukaan enamel gigi dan evaluasi SEM mengungkapkan bahwa produk pemutih gigi memiliki potensi efek demineralisasi pada permukaan enamel gigi.12
Adapun kerugian ini membuat para peneliti mencari bahan pemutih gigi alami yang lebih aman.3,7 Bahan alami yang saat ini dapat digunakan untuk memutihkan gigi yang telah berubah warna adalah hidrogen peroksida yang dapat diperoleh dari buah-buahan. Hidrogen peroksida mempunyai kemampuan untuk mencerahkan warna gigi. Hidrogen peroksida akan berdifusi melalui enamel ke dentin dan bertindak sebagai oksidator kuat yang menghasilkan radikal bebas yang cukup reaktif. Radikal bebas ini akan menyerang molekul organik di gigi untuk mencapai stabilitas. Hidrogen peroksida juga mampu mengoksidasi berbagai senyawa organik dan anorganik berwarna,sehingga
15 menyebabkan perubahan warna.13 Hidrogen peroksida dapat terkandung dalam bahan alami seperti pir dan madu. Penelitian yang dilakukan oleh Utami DR dkk menyimpulkan buah pir yang mengandung hidrogen peroksida dapat digunakan sebagai bahan alternatif yang aman pada proses pemutihan gigi.14 Istanti SF dkk dalam penelitiannya menyimpulkan bahwa terdapat peningkatan warna gigi setelah dilakukan perendaman gigi di dalam madu.15
Buah lain yang mengandung hidrogen peroksida adalah buah tomat. Buah tomat (Lycopersicum Esculentum Mill.) merupakan salah satu tanaman yang sangat dikenal oleh masyarakat Indonesia. Hidrogen peroksida dapat ditemukan pada pericarp buah tomat sebanyak 4000nmol.13 Penelitian Pratiwi SA telah membuktikan adanya efektivitas jus buah tomat terhadap perubahan warna gigi pada proses pemutihan gigi secara in vitro dengan metode perendaman selama 3 hari.16 Penelitian Anggarawati dkk, telah dilakukan dengan metode perendaman gigi dalam ekstrak tomat dengan konsentrasi 50%, 75% dan 100% selama 4 hari dan menunjukan adanya perubahan warna gigi.17 Penelitian Mulky dkk, telah membuktikan efek bleaching dari buah tomat dengan metode smear dan inkubasi selama 3 hari.13 Semakin lama waktu perendaman diduga akan menyebabkan meningkatkan porositas pada gigi. Meningkatnya porositas enamel terjadi karena adanya proses dimineralisasi oleh asam yang dapat menembus enamel. Dimineralisasi enamel dapat terjadi apabila enamel berada pada lingkungan pH dibawah 5,5 Nilai pH berperan dalam dimineralisasi karena pH yang rendah akan meningkatkan konsentrasi ion hidrogen dan ion ini akan merusak hidroksiapatit enamel gigi serta kemungkinan mempengaruhi kekasaran permukaan enamel dengan sifatnya yang asam.8-9
16 dapat menyebabkan perubahan kekasaran permukaan enamel. Penurunan kadar kalsium dan fosfor pada enamel yang signifīkan dapat dilihat pada gigi setelah aplikasi karbamid peroksida 16%. Pada penelitian ini penulis tertarik untuk membandingkan bagaimana perubahan kekasaran permukaan enamel yang terjadi setelahnya. Dalam penelitian ini digunakan jus buah tomat dan karbamid peroksida 16%.
1.2.Rumusan Masalah
Apakah ada perbedaan kekasaran permukaan enamel gigi pada penggunaan karbamid peroksida 16% dan jus buah tomat (Lycopersicum
esculentum Mill,var.commune) dengan konsentrasi 50% dan 100% sebagai
bahan pemutih gigi.
1.3.Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui perbedaan kekasaran permukaan enamel gigi pada penggunaan karbamid peroksida 16% dan jus buah tomat (Lycopersicum esculentum Mill,var.commune) dengan konsentrasi 50% dan 100% sebagai bahan pemutih gigi.
1.4. Manfaat Penelitian 1.4.1. Manfaat Teoritis
1. Sebagai wawasan tambahan dan pengetahuan bagi peneliti, dokter gigi dan masyarakat tentang manfaat buah tomat bagi kesehatan gigi dan mulut.
2. Sebagai pengetahuan bagi peneliti, dokter gigi dan masyarakat tentang perubahan kekasaran permukan enamel gigi setelah aplikasi karbamid peroksida dan jus buah tomat.
17 3. Sebagai dasar penelitian lebih lanjut tentang efek samping buah tomat terhadap permukaan enamel gigi dan penanggulangnya sebagai alternatif bahan pemutih gigi.
1.4.2. Manfaat Praktis
Memperoleh bahan pemutih alami dengan tingkat kekasaran yang masih dapat ditolerir gigi sebagai alternatif bahan pemutih gigi yang bermanfaat bagi masyarakat luas.
1.4.2. Manfaat Klinis
Memperoleh bahan pemutih gigi alami yang dapat menggantikan bahan kimia sehingga efek samping penggunaanya dapat dihindari.
18
BAB 2
TINJAUAN PUSTAKA
Gigi terdiri dari enamel, dentin dan rongga pulpa. Enamel merupakan struktur keras dalam tubuh. Komposisi enamel terdiri atas bahan anorganik dan bahan organik.18
2.1 Struktur Enamel
Enamel gigi merupakan jaringan terluar gigi yang menutupi anatomis
mahkota gigi manusia dan memiliki ketebalan yang berbeda pada setiap area gigi. Bila dibandingkan dengan jaringan gigi yang lain, enamel adalah jaringan yang paling keras dan paling kuat.18 Oleh karena itu enamel merupakan pelindung yang paling kuat bagi gigi terhadap rangsangan-rangsangan.18
Enamel terdiri dari 96%-98% bahan anorganik serta 2%-8% air dan bahan
organik.19 Bahan-bahan anorganik dari enamel mengandung komponen-komponen mineral antara lain: PO4 55,5%, Ca 37%, CO3 3,5%, Na 0,5% dan lain-lain.19 Bahan-bahan mineral ini biasanya tersusun dalam kristal hidroxiapatit dengan rumus kimia Ca10(PO4)6(OH) atau flouroapatit (Ca10(PO4)6F2) dengan struktur heksagonal.19
Bagian dari enamel meliputi enamel rod dan rod sheath.19 Enamel rod atau prisma enamel merupakan struktur utama dari enamel yang terbentuk dari kristal-kristal hidroksiapatit.19 Rod sheath merupakan bagian luar enamel rod yang sebagian besar merupakan substansi fibrosa organik.19 Enamel pada gigi mempunyai ketebalan yang berbeda pada tiap bagian dan bervariasi diantara jenis gigi, maksimum 2,5 mm.19
Dilihat dari sifat fisiknya, enamel memiliki sifat yang sangat keras karena bahan mineralnya.11 Meskipun demikian, enamel bersifat permeabel terhadap ion-ion dan molekul yang dapat mengalami penetrasi sebagian atau
19 kompleks. Enamel dapat larut ketika berkontak dengan asam, sehingga
larutnya sebagian atau keseluruhan mineral enamel akan mempengaruhi
11
permukaan enamel.
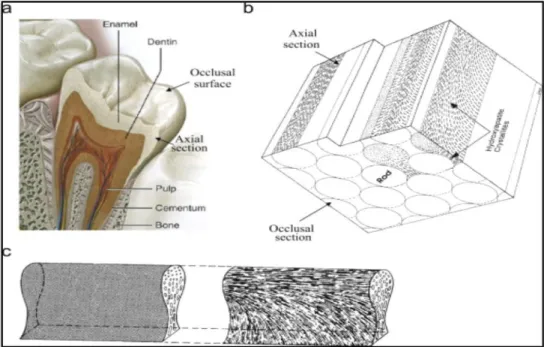
Gambar 1. (a) Gigi dengan struktur pendukung. (b) Struktur enamel gigi. (c) Struktur Rod 18
2.2 Demineralisasi Enamel
Demineralisasi merupakan proses hilangnya kandungan mineral pada
enamel. Kandungan mineral yang tinggi pada enamel membuat enamel
menjadi rentan terhadap proses demineralisasi oleh asam. Demineralisasi akan terjadi bila pH dari rongga mulut berada di bawah pH kritis hidroksiapatit (pH= 5,5). pH berperan pada proses demineralisasi karena pH yang rendah akan meningkatkan konsentrasi ion hidrogen dan ion ini akan
20 merusak hidroksiapatit enamel gigi yang menyebabkan terurainya ion kalsium dan fosfat. Selain dipengaruhi oleh pH, proses demineralisasi juga tergantung pada substansi gigi (enamel dan dentin), konsentrasi asam, frekuensi dan durasi gigi terpapar oleh asam.20,21
Proses demineralisasi akan dimulai pada saat rongga mulut dalam keadaan asam. Hidroksiapatit (Ca10 (PO4)6 (OH)2) dan Flouroapatit (Ca10 (PO4)6 F2) yang merupakan mineral dari enamel gigi akan larut menjadi Ca2+, PO4-9 , dan F atau OH- . Ion H+ akan bereaksi dengan gugus PO4 -9 , dan F-atau OH- yang akan membentuk HSO4 - , H2SO4 - , HF atau H2O, sedangkan yang kompleks terbentuk CaHSO4, CaPO4 dan CaHPO4. Mengingat bahwa kalsium merupakan komponen utama dalam struktur gigi dan demineralisasi enamel terjadi akibat lepasnya ion kalsium dari enamel gigi, maka pengaruh asam pada enamel gigi merupakan reaksi penguraian. Demineralisasi yang terus-menerus akan membentuk porositas pada permukaan enamel yang sebelumnya tidak ada. Saliva yang mengandung kalsium dan fosfat dengan konsentrasi yang cukup dapat melindungi enamel dari proses demineralisasi.20,21
2.3 Perubahan warna gigi
Perubahan warna dapat berlangsung secara fisiologi maupun patologi.1 Perubahan warna fisiologi terjadi seiring dengan bertambahnya usia, karena dentin lebih tebal, akibat pembentukan dentin sekunder.1 Perubahan warna secara patologis dapat secara ekstrinsik dan intrinsik.1 Perubahan warna secara ektrinsik dapat disebabkan oleh deposit yang terjadi pada permukaan gigi.1 Sementara perubahan warna gigi secara intrinsik disebabkan oleh faktor dari dalam jaringan pulpa.1
21 umumnya dapat digolongkan dalam dua macam faktor penyebab pewarnaan, yaitu pewarnaan karena faktor dari luar (ekstrinsik) dan pewarnaan karena faktor dari dalam (intrinsik):1
1. Diskolorisasi yang disebabkan faktor ekstrinsik
Perubahan warna secara ekstrinsik dapat disebabkan oleh adanya deposit yang melekat atau pada permukaan gigi.Biasanya terjadi karena perlekatan warna makanan, minuman ataupun rokok yang meninggalkan tar berwarna kecoklatan pada gigi, yang terjadi secara perlahan-lahan dalam jangka waktu yang cukup panjang. Selain itu keadaan kebersihan mulut yang buruk, dimana plak mengandung produk bakteri kromogenik yang dapat menyebabkan perubahan warna pada gigi, misalnya pada pengguna alat ortodontik. Diskolorisasi karena faktor-faktor tersebut dapat dihilangkan dengan skeling dan pemolesan pada saat melakukan tindakan profilaksis tanpa harus melakukan prosedur bleaching. Jenis lain diskolorisasi ekstrinsik adalah noda nitrat perak yang sukar dihilangkan dengan bahan-bahan kimiawi karena stain memasuki permukaan mahkota gigi. Noda dapat dihilangkan dengan proses bleaching.
2. Diskolorisasi yang disebabkan faktor intrinsik
Perubahan warna secara intrinsik disebabkan oleh faktor dari dalam jaringan gigi atau jaringan pulpa.Pewarnaan dari dalam disebabkan oleh bahan-bahan restorasi gigi (amalgam), karies, trauma, infeksi, obat-obatan (pemakaian tetracycline dan fluorida dalam dosis besar selama beberapa tahun), gangguan selama kehamilan faktor genetik dan penyakit herediter yang memengaruhi perkembangan dan pematangan enamel dan dentin, penyakit sistemik pada periode pembentukan gigi.
22
2.4 Pemutihan gigi (bleaching)
Pemutihan gigi atau yang lebih dikenal dengan istilah bleaching adalah suatu cara pemutihan kembali gigi yang berubah warna sampai mendekati warna alami gigi dengan proses perbaikan secara kimiawi, yang tujuan utamanya adalah mengembalikan fungsi estetika manusia.21 Ada berbagai macam prosedur untuk pemutihan.1 Pemutihan gigi dapat dikerjakan di klinik oleh dokter gigi secara langsung atau dilakukan di rumah dengan pantauan dokter gigi.1
Terdapat 2 macam teknik pemutihan gigi:1,2,22 1. Teknik eksternal
Teknik eksternal ini terdapat dua macam yaitu office bleaching dan home
bleaching
Office bleaching dilakukan langsung dipraktek oleh dokter gigi. Digunakan untuk menghilangkan stein pada gigi (contoh : stein tetrasiklin atau karena penuaan).
Home bleaching merupakan teknik yang sangat mudah, setelah konsultasi awal dengan dokter gigi, tray yang dibuat untuk pasien untuk memutihkan gigi dirumah. Pasien mengaplikasikan bahan pemutih gigi pada tray. Tray dipakai selama beberapa jam selama 1 hari.
2. Teknik internal
Teknik internal terdapat dua macam yaitu teknik termokatalik (peletakan bahan oksidator di dalam kamar pulpa dan penggunaan panas) dan teknik
walking bleach (dipakai dalam semua keadaan yang memerlukan teknik
pemutihan secara internal dan teknik ini dapat dilakukan pada kunjungan yang sama pada obturasi).
23
2.5 Mekanisme pemutihan gigi
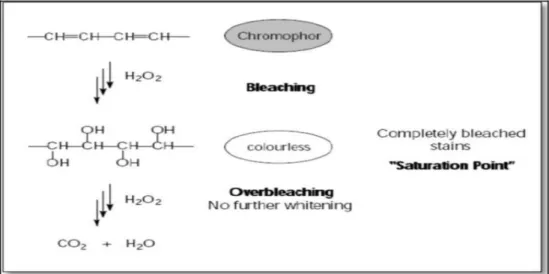
Proses perubahan warna gigi dengan menggunakan teknik bleaching apapun dan dengan konsentrasi peroksida yang berbeda merupakan proses reaksi kimia oksidasi dan reduksi. Pada proses ini terjadi reaksi antara zat pewarna pada gigi (sebagai pereduksi) dengan molekul bahan bleaching (sebagai oksidator).23 Pada awal proses pemutihan, cincin karbon yang terpigmentasi akan terbuka menjadi ikatan tidak jenuh. Kemudian cincin karbon yang terbuka akan berikatan dengan radikal bebas dari bahan pemutih. Radikal bebas merupakan elektron yang tidak berpasangan dan akan terus bereaksi sampai staining terurai menjadi molekul- molekul sederhana yang bersifat sedikit merefleksikan cahaya spesifik dari stain, yaitu terjadi pengurangan atau elimination discoloration. Sampai suatu saat akan dicapai suatu titik dimana molekul-molekul sederhana yang terbentuk maksimum, keadaan ini disebut dengan saturation point (titik jenuh). Pada titik ini kerusakan struktur gigi dimulai, kehilangan email menjadi lebih cepat. Oleh karena itu pemutihan gigi harus segera dihentikan ketika titik jenuh dicapai untuk meminimalkan kerapuhan gigi dan meningkatnya porositas. Selanjutnya reaksi kimia bahan-bahan organik yang diakhir reaksinya akan menghasilkan CO2 dan air (gambar 2).24
24
Gambar 2. Mekanisme pemutihan gigi. Diskolorosasi yang disebabkan kromofor makanan atau minuman, peroksida mengoksidasi kromofor, pemecahan kromofor sehingga menjadi molekul sederhana.24
2.6 Bahan pemutih gigi
Bahan pemutih dapat berperan sebagai oksidator atau reduktor dan kebanyakan adalah oksidator. Oksidator yang makin kuat akan meningkatkan daya pemutihan gigi.6 Kandungan utama bahan pemutih gigi tergantung dari produsen pembuatnya, diantaranya hidrogen peroksida, karbamid peroksida atau urea peroksida atau sistem non-hidrogen peroksida yang mengandung sodium klorida, oksigen dan natrium fluorida. Beberapa produk mengandung bahan tambahan potasium nitrat dan fluoride untuk membantu mengurangi sensitivitas gigi.1
2.6.1 Hidrogen peroksida
Hidrogen Peroksida merupakan suatu senyawa kimia jernih, tidak berwarna, tidak berbau, dan tidak mudah terbakar yang umumnya digunakan
25 untuk memutihkan gigi pada konsentrasi 30%.25 Hidrogen peroksida merupakan bahan radikal yang mempunyai elektron yang tidak berpasangan, dan merupakan bahan yang tidak stabil yang akan menyerang molekul organik lainnya yang akan mencapai kestabilan, kemudian menghasilkan radikal yang lain. Radikal ini mampu bereaksi dengan ikatan yang tak jenuh, kemudian terjadi perpecahan konjugasi elektron dan terjadinya perubahan absorbsi energi molekul organik pada enamel gigi.26
Radikal bebas ini akan bereaksi dengan ikatan tidak jenuh dan menyebabkan gangguan konjugasi elektron dan perubahan penyerapan energi pada molekul organik dalam struktur gigi (enamel, dentin). Molekul gigi berubah struktur kimianya dengan tambahan oksigen dan akan membentuk molekul organik email yang lebih kecil dengan warna yang lebih terang sehingga menghasilkan efek pemutihan dan gigi menjadi lebih bercahaya.22
2.6.2 Karbamid peroksida
Karbamid peroksida adalah senyawa perpaduan antara hidrogen peroksida dan urea. Konsentrasi hidrogen peroksida yang terdapat dalam karbamid peroksida adalah 1/3 dari total konsentrasi karbamid peroksida. Konsentrasi karbamid peroksida yang umum digunakan untuk memutihkan gigi berkisar 10%- 22%.25
Bahan oksidasi yang sering digunakan mengandung karbamid peroksida 10%dengan rata-rata pH antara 5-6,5. Karbamid peroksida mengandung gliserin atau propylene glycol, sodium stannate, phosphoric atau asam sitrat serta memiliki bau yang khas. Karbamid peroksida mempunyai sifat tidak stabil dan dapat langung pecah menajadi urea, amoniak, karbon monoksida dan hidrogen peroksida 3%-5%. Karbamid peroksida
26 digunakan untuk bleaching ekstra koronal dan pemakaiannya harus dengan pengawasan dari dokter gigi.
Karbamid peroksida (CH6N2O3) juga dikenal sebagai hidrogen peroksida urea, yang terdiri dari kristal putih atau bubuk yang mengkristal yang berisi sekitar 35% H2O2. Terbentuk dari H2O2 dan urea yang menyatu menjadi larutan yang encer. Bahan ini merupakan bahan yang paling sering digunakan dalam teknik home-bleaching dengan konsentrasi kisaran 10% sampai 30%, tapi dari keseluruhan konsentrasi 10% adalah konsentrasi yang paling sering digunakan. 22
Reaksi dari karbamid peroksida dalam proses pemutihan sebagai berikut:23
Karbamid peroksida Hidrogen peroksida + Urea
CH2N2OH2O2 H2O2 CH2N2O
Hidrogen peroksida Air + Oksigen
H2O2 H2O O2
Urea Amonia + Karbon dioksida
27 Urea dalam karbamid peroksida berperan sebagai penstabil agar efek bahan tersebut lebih panjang dan berperan memperlambat proses pelepasan hidrogen peroksida. Agar efek karbamid peroksida maksimal, dibutuhkan waktu yang lama untuk berkontak dengan gigi. Urea dalam karbamid peroksida dengan berat molekul yang rendah dapat bergerak bebas ke dalam email dan dentin pada saat proses degradasi ammonia, dan karbondioksida akan dilepas sehingga akan meningkatkan pH. Proses buffer dapat meningkatkan efek pemutihan karena produksi ion perhidrol meningkat sehingga proses oksidasi juga akan bertambah. Selain itu, urea juga mempunyai efek pembersih untuk menetralkan asam dan menghilangkan noda-noda pada gigi.23
2.7 Indikasi dan kontraindikasi bleaching
Indikasi perawatannya untuk penderita dengan perubahan warna yang disebabkan proses penuaan, konsumsi makanan, minuman, obat antara lain tetrasiklin, serta fluorosis.1
Kontra indikasi penggunaan bahan pemutih gigi adalah penderita yang alergi terhadap komponen bahan pemutih gigi atau bahan sendok cetak, penderita dengan gigi sangat sensitif, wanita hamil.1
2.8 Efek samping bleaching
Pemakaian bahan pemutih gigi dapat menyebabkan terjadinya efek samping, yaitu pada jaringan keras, mukosa, dan sensitifitas gigi.22
Antara efek samping yang ditimbulkan dari bleaching:
Gigi yang sensitif
28 waktu singkat, ditanggulangi dengan memendekkan waktu proses pemutihan setiap harinya, pengulasan fluor, potasium nitrat atau bahan
desentizing lain.
Iritasi pada mukosa
Iritasi pada mukosa gingival dan tenggorokan biasanya disebabkan bahan pemutih yang berlebihan, keluar dari sendok cetak sehingga mengiritasi mukosa atau kemungkinan tertelan.
Perubahan morfologi enamel
Perendaman sampel gigi dalam karbamid peroksida dan hidrogen peroksida menunjukkan adanya perubahan gambaran enamel menjadi lebih kasar, berpori- pori dan adanya bercak putih akibat penggunaan bahan tersebut dilihat secara mikroskopis.
2.9 Tomat
Tomat (Lycopersicon esculentum Mill) merupakan sayuran buah yang tergolong tanaman semusim berbentuk perdu dan termasuk ke dalam famili Solanaceae.27 Tomat (Lycopersico esculentum Mill.) adalah sangat bermanfaat bagi tubuh karena mengandung vitamin dan mineral yang diperlukan untuk pertumbuhan dan kesehatan. Buah tomat juga mengandung karbohidrat, protein, lemak dan kalori. Buah tomat merupakan komoditas multiguna yang berfungsi sebagai sayuran, bumbu masak, buah meja, penambah nafsu makan, bahan pewarna makanan, sampai kepada bahan kosmetik dan obat-obatan.28
Klasifikasi botani tanaman tomat adalah sebagai berikut:29 Kingdom
Devisi
Subdevisi
: Plantae (Tumbuh-tumbuhan)
: Spermatophyta (Tumbuhan berbiji)
29 Kelas : Tubiflorae
Ordo : Solanaceae
Famili : Lycopersicum
Genus : Lycopersicum esculentum Mill
Gambar 3. Buah tomat 30
2.9.1 Morfologi tomat
Tanaman tomat terdiri dari akar, batang, daun, bunga dan biji. Tinggi tanaman tomat mencapai 2-3 meter.31
1. Batang
Sewaktu masih muda, batang tanaman tomat berbentuk bulat dan teksturnya lunak, tapi setelah tua batangnya berubah jadi bersudut dan bertekstur keras berkayu. Ciri khas batang tomat adalah tumbuhnya bulu-bulu halus diseluruh permukaannya.
30 2. Akar
Berbentuk serabut yang menyebar kesegala arah. Kemampuannya menembus lapisan tanah terbatas terbatas yakni pada kedalaman 30-70 cm.
3. Daun
Berwarna hijau dan berbulu mempunyai panjang sekitar 20-30 cm dan lebar 15-20 cm. Daun tomat tumbuh didekat dahan atau cabang. Sementara tangkai daunnya berbentuk bulat memanjang sekitar 7-10 cm dan ketebalan 0-3-0,5 cm.
4. Bunga
Berwarna kuning dan tersusun dalam dompalan dengan jumlah 5-10 bunga bunga per dompalan atau tergantung dari varietasnya. Kuntum bunganya terdiri dari lima helai mahkota. Bunga tomat dapat melakukan penyerbukan sendiri karena tipe bunganya berumah satu. Tapi tidak menutup kemungkinan terjadi penyerbukan silang.
5. Biji
Berbentuk pipih, berbulu, dan diselimuti daging buah. Warna bijinya ada yang putih, putih kekuningan, serta kecoklatan. Biji inilah yang digunakan untuk perbanyakan tanaman.
6. Buah
Buah tomat berbentuk bulat, bulat lonjong, bulat pipih atau oval. Buah yang masih muda berwarna hijau muda sampai hijau tua. Sementara itu, buah yang sudah tua berwarna merah cerah atau gelap, merah kekuning-kuningan atau merah kehitaman. Selain itu ada juga tomat yang berwarna kuning.
31
2.9.2 Kandungan tomat :
Tanaman tomat (Lycopersicon lycopersicum L.) merupakan salah satu jenis tanaman hortikultura yang mempunyai prospek cukup cerah untuk dibudidayakan.Buah tomat mengandung serat makanan alami yang sangat baik bagi pencernaan manusia dan juga adanya protein dalam buah tomat menjadikannya buah yang sangat sarat gizi.Asam sitrat adalah asam utama dalam jus tomat.32
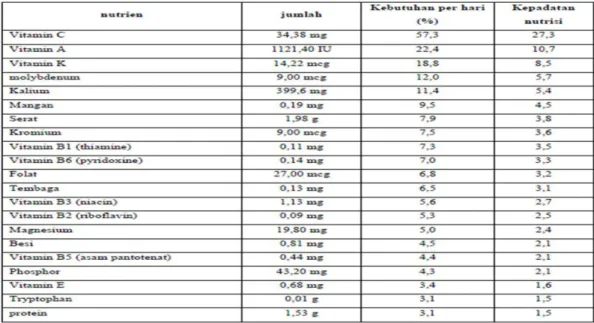
Sebagai sumber vitamin, buah tomat sangat baik untuk mencegah dan mengobati berbagai macam penyakit, seperti sariawan karena kekurangan vitamin C, xeropthalmia pada mata akibat kekurangan vitamin A, beri-beri, radang syaraf, lemahnya otot-otot, dermatitis, bibir menjadi merah dan radang lidah akibat kekurangan vitamin B. Sebagai sumber mineral, buah tomat dapat bermanfaat untuk pembentukan tulang dan gigi (zat kapur dan fosfor), sedangkan zat besi (Fe) yang terkandung didalam buah tomat dapat berfungsi untuk pembentukan sel darah merah atau hemoglobin. Buah tomat juga mengandung serat yang berfungsi memperlancar proses pencernaan makanan didalam perut dan membantu memudahkan buang kotoran. Selain itu, tomat mengandung zat potassium yang sangat bermanfaat untuk menurunkan gejala tekanan darah tinggi.31
Salah satu agen untuk memutihkan gigi juga dapat ditemukan dalam buah tomat iaitu hidrogen peroksida sebanyak 4000 nmol. Enzim ini terdapat pada pericarp buah tomat dan berfungsi sebagai agen oksidasi dan senyawa tersebut mampu merusak molekul-molekul zat warna sehingga warna menjadi netral dan menyebabkan efek pemutihan.8
32
Tabel 2. Kandungan gizi buah tomat segar (matang) tiap 180 gram bahan.32
2.9.3 Potensi buah tomat sebagai bahan pemutih gigi
Buah tomat mengandung hidrogen peroksida yang diperoleh dari reaksi oksidasi 8 Selain itu, buah tomat mengandung enzim peroksidase, dimana enzim ini dapat diidentifikasi di dalam pericarp buah tomat.8 Proses pemutih gigi melalui hidrogen peroksida yang merupakan senyawa yang bersifat oksidator kuat dimana dalam penelitian ini sifat oksidator ini akan dimanfaatkan untuk mendegradasi agen penghasil warna atau kromofor yang menyebabkan gigi mengalami diskolorisasi.9 Proses dalam mendegradasi kromofor tersebut terjadi setelah hidrogen peroksida diubah menjadi radikal bebas atau diubah menjadi molekul oksigen yang reaktif.9 Radikal bebas atau molekul oksigen yang reaktif ini akan menembus lapisan struktur enamel dan masuk ke dalam tubuli dentin dan akan rusak ikatan ikatan konjungasi yang telah terbentuk antara zat pewarna dengan struktur gigi9. Sehingga akibatnya gigi menjadi terbebas dari ikatan zat pewarna dan menjadi tampak lebih putih.8
33 Terdapat penelitian sebelumnya yang membuktikan efektivitas buah tomat sebagai bahan pemutih gigi antaranya penelitian Pratiwi SA telah membuktikan adanya efektivitas jus buah tomat terhadap perubahan warna gigi pada proses pemutihan gigi secara in vitro dengan metode perendaman selama 3 hari.10 Penelitian Anggarawati dkk telah dilakukan dengan metode perendaman gigi dalam ekstrak tomat dengan konsentrasi 50%,75% dan 100% selama 4 hari dan menunjukan adanya perubahan warna gigi.11 Penelitian Mulky dkk telah membuktikan efek bleaching dari buah tomat dengan metode smear dan inkubasi selama 3 hari.8
2.10 Kekasaran permukaan enamel gigi
Enamel terdiri atas kristal hidroksit apatit yang tersusun rapat dan beraturan membentuk prisma email. Kristal ini saling melekat erat satu sama lain, namun sebenarnya masing-masing kristal dipisahkan satu dengan lainnya oleh daerah intercrystalline yang sangat tipis dan disebut dengan enamelins. Daerah ini banyak mengandung air dan material organik. Ketika email terpapar oleh asam baik karena hasil produksi mikrobial biofilm ataupun karena konsumsi oral, mineral yang ada di permukaan kristal akan mengalami reaksi demineralisasi yang kemudian akan larut dan mengecilkan ukuran kristal, sehingga hal ini dapat memperbesar jarak intercrystalline dan pada akhirnya jaringan menjadi porus.33
Peningkatan porositas permukaan enamel secara klinis dapat dilihat dengan adanya white spot. Pola kelarutan enamel tergantung dari arah kristal hidroksiapatit sebagai penyusun enamel. Kristal dengan arah sumbu panjang tegak lurus pada garis permukaan akan mengalami kelarutan lebih cepat dibandingkan dengan kristal yang arah sumbu panjangnya sejajar dengan garis permukaan enamel. Perbedaan kecepatan kelarutan ini akan menyebabkan
34 timbulnya permukaan enamel yang tidak merata. Jaringan enamel yang porus dan permukaan yang tidak rata akan menghasilkan permukaan enamel yang kasar.33
Selain itu, ditemukan bahwa demineralisasi awal ditandai dengan pelunakan permukaan dengan adanya pelarutan tepi prisma tanpa terbentuk lesi dibawahnya.34 Kemudian bila proses berlanjut terus, maka akan terjadi kekasaran permukaan enamel. Kekasaran permukaan enamel mempunyai peran penting dalam adhesi enamel. Pada permukaan kasar bakteri dilindungi terhadap gaya geser, sehingga perubahan dari perlekatan reversibel menjadi ireversibel lebih mudah dan lebih sering terjadi. Kontak antara permukaan yang kasar dengan gingiva dapat menimbulkan rasa tidak nyaman. Selain itu, permukaan yang kasar dapat memudahkan perlekatan bakteri dan menyulitkan pengangkatannya dengan cara alami atau bahkan dengan metode-metode pembersihan rongga mulut. Kekasaran permukaan juga mempengaruhi penampilan estetik, stabilitas warna, dan pembentukan biofilm.13,35
Kekasaran permukaan adalah ukuran ketidakteraturan dari permukaan dan diukur dengan satuan mikrometer (μm). Nilai ini merupakan ukuran deviasi vertikal suatu permukaan dari bentuk idealnya. Apabila deviasi ini besar, maka permukaan tersebut kasar apabila deviasi ini kecil, maka permukaan tersebut halus. Kekasaran dianggap sebagai komponen dari permukaan yang telah diukur dengan frekuensi yang tinggi dan panjang gelombang yang pendek.36,37
Kekasaran enamel yang normal pada bagian oklusal akibat adanya kontak dengan gigi anatagonis yaitu sekitar 0,64±0.25 µm.38 Penelitian yang dilakukan pada permukaan gigi insisivus mandibular,bagaian labial mendapatkan rerata kekasaran 1,64±0.62 µm.39 Penelitian lain yang
35 melakukan uji kekasaran pada permukaan enamel gigi molar mendapatkan rerata 1,72±0,56 µm.40
2.11 Metode pengukuran kekasaran permukaan gigi
Gambar 4 : Profilometer Mahr Surftest
Kekasaran permukaan dapat diukur dengan dua metode, antara lain metode sentuhan (contact method) dan metode tanpa sentuhan (non-contact method). Metode sentuhan dilakukan dengan menarik suatu stylus pengukuran sepanjang permukaan. Alat untuk metode sentuhan ini disebut profilometer.Permukaan adalah suatu batas yang memisahkan benda padat dengan sekitarnya, Profil yaitu garis hasil pemotongan secara normal atau serong dari suatu penampang permukaan. Dengan melihat profil maka bentuk dari suatu permukaan pada dasarnya dapat dibedakan menjadi dua yaitu permukaan yang kasar (roughness) dan permukaan yang bergelombang (waviness). Untuk memperoleh profil suatu permukaan, digunakan suatu alat ukur yang disebut surface tester, dimana jarum peraba (Stylus) dari alat ukur akan bergerak mengikuti lintasan yang berupa garis lurus dengan jarak yang ditentukan terlebih dahulu. Bagian dari panjang ukuran yang dilakukan analisa profil permukaan disebut sebagai panjang sampel.38
36 Parameter kekasaran yang biasa dipakai dalam proses produksi untuk mengukur kekasaran permukaan benda adalah kekasaran rata-rata (Ra) nilai satuan µm.39 Salah satu alat Surface Roughness Tester yang portable dan telah digunakan secara luas adalah Mahr Surftest, Japan. Dengan komponen di dalamnya yaitu standar detector dengan stylus, drive unit yang berisi menu sistem operasi, display unit yang akan menampilkan hasil pengukuran,
2.12 Kerangka Teori
Enamel gigi
Perubahan warna gigi (Diskolorisasi)
Pemutihan gigi (Bleaching)
Bahan pemutih gigi
Bahan Kimia Karbamid Peroksida Hidrogen Peroksida ( H2O2) Urea ( CH2N2O ) Efek Pemutihan Stabilisator H2O2 H2O + O+ H2O H + + HO- ( H+ ) Suasana Asam Bahan alami Hidrogen
BAB 3
KERANGKA KONSEP DAN HIPOTESIS PENELITIAN
38
3.1 Kerangka Konsep
- Jus buah tomat 100% Kekasaran permukaan
- Jus buah tomat 50% enamel gigi
- Karbamid peroksida 16%
3.2 Hipotesis Penelitian
Ada perbedaan kekasaran permukaan enamel gigi pada penggunaan karbamid peroksida 16% dengan jus buah tomat (Lycopersicon esculentum
39
BAB 4
METODE PENELITIAN
4.1 Jenis penelitian : Eksperimental laboratorium in vitro Rancangan penelitian : Pre and Post test group design 4.2 Tempat dan Waktu Penelitian
4.2.1 Tempat Penelitian
Laboratorium Politeknik USU
4.2.2 Waktu Penelitian
Penelitian ini dilaksanakan pada bulan September 2016 – Juli 2017
4.3 Populasi dan Sampel 4.3.1 Populasi
Populasi yang digunakan adalah gigi molar tiga
4.3.2 Sampel
Sampel yang digunakan pada penelitian ini adalah permukaan bagian bukal dan lingual/palatal gigi molar tiga dengan kriteria inklusi sebagai berikut: Kriteria inklusi:
a. Mahkota masih utuh dan akar sudah terbentuk sempurna b. Tidak karies
c. Tidak tambalan
a. Gigi yang fraktur.
40
4.3.3 Besar Sampel
Jumlah besar sampel pada penelitian eksperimen secara sederhana dapat dihitung dengan rumus Federer sebagai berikut :
( t – 1 ) ( r – 1 ) ≥ 15
Dimana ; t = jumlah perlakuan dalam penelitian r = jumlah sampel
Dalam penelitian ini terdapat 4 kelompok sampel yang diberi perlakuan. Berdasarkan rumus diatas, maka jumlah sampel tiap kelompok dapat ditentukan sebagai berikut :
( 3 – 1 ) ( r – 1 ) ≥ 15 ( 2 ) ( r – 1 ) ≥ 15
r ≥ 8.5
Jumlah sampel (r) yang digunakan dalam penelitian ini adalah 10 sampel. Kelompok 1 : sampel direndam dalam jus tomat 100%
Kelompok 2 : sampel direndam dalam jus tomat 50%
Kelompok 3 : sampel direndam dalam karbamid peroksida 16%
= 10 sampel = 10 sampel = 10 sampel
Jadi, total jumlah sampel yang digunakan dalam penelitian ini adalah 30 sampel (15 gigi molar yang dibagi menjadi 2 bagian).
4.4 Variabel Penelitian 4.4.1 Variabel bebas
· Jus buah tomat 100% · Jus buah tomat 50% · Karbamid peroksida 16%
41
4.4.2 Variabel tergantung
· Kekasaran permukaan enamel gigi
4.4.3 Variabel terkendali
· Gigi molar tiga
· Lama perendaman gigi dalam jus buah tomat yaitu 2 menit. Dilakukan 3 kali dalam sehari dengan selang waktu 6 jam selama 2 minggu (14 hari).
· Konsentrasi jus buah tomat 100% dan 50% · Karbamid peroksida 16%
· Media penyimpanan menggunakan saliva buatan · Suhu ruangan
· Masa/jangka waktu pencabutan gigi molar, kurang dari 3 bulan · Lama waktu penghalusan jus tomat
· Keadaan buah tomat
4.4.4 Variabel tidak terkendali
· Perlakuan terhadap buah tomat selama tumbuh · Ketebalan enamel / struktur enamel
43
4.5 Definisi Operasional
Tabel 1 Definisi operasional
No Variabel Definisi Skala Ukur Alat Ukur Operasional
Variabel Bebas
1 Jus buah tomat 200 g buah tomat
100% yang dihaluskan
tanpa air. Nominal Gelas Ukur
2 Jus buah tomat 200 g buah tomat
50% yang dihaluskan Nominal Gelas Ukur
tanpa air. Setelah didapatkan jus tomat maka
dicampur dengan air matang yang rumus V1.C1=V2.C2
3 Karbamid peroksida Bahan pemutih gigi
16% yang digunakan Nominal Sesuai
dalam metode home petunjuk
bleaching yang telah pabrik
disetujui oleh
American Dental Association
No Variabel Definisi Skala Ukur Alat Ukur Operasional
Variabel Tergantung
1 Kekasaran Suatu
permukaan enamel ketidakteraturan Ratio Profilometer
gigi pada permukaan
enamel gigi yang diukur dengan alat ukur surface roughness tester.
44
4.6 Alat dan Bahan Penelitian 4.6.1 Alat penelitian
1. Surface Roughness tester (Mahr Surf, Amerika) 2. Wadah plastic (Tupperware,Malaysia)
3. Alat penghalus (National, Japan) 4. Gelas ukur (Pyrex,Germany) 5. Pinset (Dentica,Indonesia) 6. Alarm (Casio,Malaysia) 7. Mikromotor (Strong, China) 8. Carborundum (Dia Bur,China) 9. Tisu (Premier,Indonesia) 10. Alat tulis (Pilot,Indonesia) 11. Spidol (Artline 100,Indonesia)
4.6.2 Bahan penelitian
1. Jus buah tomat 100% & 50% (Berastagi,Medan)
2. Karbamid peroksida 16% (Zoom Nite White,Philips,USA) 3. Air (Aqua,Indonesia)
4. Saliva buatan (UGM,Indonesia) 5. Cat kuku (Elianto,Indonesia)
45
A B C
D E F
Gambar 5. A. Carborundum (Dia Bur,China); B. Profilometer (Mahr Surf,Amerika); C. Gelas ukur (Pyrex,Germany); D. Alat penghalus (Miyako,Indonesia); E. Mikromotor (Strong,China); F. Karbamid Peroksida 16% ( Zoom Nite White,Philips)
46
4.7 Metode pengumpulan data / pelaksanaan penelitian 4.7.1 Persiapan sampel/bahan coba
Sampel yang digunakan adalah gigi molar tiga yang sesuai dengan kriteria inklusi dan eksklusi. Pertama-tama semua sampel gigi dibersihkan, lalu gigi dibagi menjadi 2 bagian (bagian bukal dan lingual/palatal). Setiap gigi bagian akar sampel ditutup dengan cat kuku untuk mencegah masuknya karbamid peroksida serta jus buah tomat melalui tubulus dentin dan bagian apikal gigi. Kemudian lakukan pengukuran dan pencatatan kekasaran permukaan enamel sebelum gigi direndam/diberikan perlakuan.
Gambar 6.Gigi dipotong dua bagian Gambar 7. Sampel gigi yang dipotong dua bagian
4.7.2 Perlakuan terhadap sampel
Bahan alami pemutih gigi yang digunakan untuk membuat jus adalah buah tomat (Lycopersicon esculentum Mill) yang diperoleh dari P a s a r a ya Pondok Buah, Medan . Buah tomat yang dipilih adalah buah tomat yang masih segar dan sudah masak. Dimana dalam buah tomat terdapat kandungan hidrogen peroksida yang memutihkan gigi. Setiap perlakuan diperlukan
47 buah tomat sebanyak 400 gram yang dimanfaatkan menjadi jus dengan cara 200 gram tomat dihaluskan tanpa air dan dihasilkan jus buah tomat dengan konsentrasi 100% yang digunakan untuk sampel Kelompok 1. Kemudian, 200 gram tomat dihaluskan tanpa air lagi lalu dilakukan pengenceran menggunakan air matang dengan menggunakan rumus pengenceran yang digunakan untuk sampel kelompok 2 yaitu sebagai berikut:
V1. C1 = V2. C2
Setiap hari jus tomat dalam wadah percobaan tersebut harus diganti. Proses aplikasi bahan pemutih gigi pada kelompok 1 dan 2 yaitu dengan cara gigi setiap kelompok perlakuan dikeluarkan dari wadahnya masing-masing yang berisi saliva buatan, dicuci di bawah air mengalir dan dikeringkan dengan tisu. Lalu gigi direndam dalam wadah yang sesuai dengan kelompok perlakuannya masing- masing. Kelompok sampel terbagi menjadi kelompok 1 : 10 sampel direndam dalam jus buah tomat 100%, kelompok 2 : 10 sampel direndam dalam jus buah tomat 50%. Gigi kemudian dicuci dibawah air mengalir, keringkan dengan tisu dan direndam kembali dalam saliva buatan. Setiap hari saliva buatan dalam wadah tersebut harus diganti. Prosedur ini diulang 3 kali sehari dengan selang 6 jam selama 2 menit dalam waktu 2 minggu/ 14 hari.
Pada kelompok 3 diaplikasikan karbamid peroksida 16% sesuai dengan petunjuk pabrik, setelah itu dicuci kembali dibawah air mengalir, keringkan dengan tisu dan rendam dalam saliva buatan. Pengaplikasian dilakukan selama 2 minggu.
48
Gambar 8. Penimbangan Gambar 9. Jus buah tomat
buah tomat
4.7.3 Pengukuran kekasaran permukaan gigi
Setelah 2 minggu/ 14 hari, gigi dikeluarkan dari wadahnya masing-masing, dicuci dibawah air mengalir dan dikeringkan dengan tisu lalu dilakukan pengukuran kekasaran permukaan enamel dengan menggunakan profilometer. Hasil pengukuran pada masing-masing gigi dicatat kemudian didapatkan hasil tingkat kekasaran permukaan dari masing-masing kelompok perlakuan yang akan dibandingkan dengan uji Kruskall-Wallis.
Gambar 10. Sebagian sampel gigi yang direndam dalam jus buah tomat 50% dan 100%
Gambar 11. Gigi diaplikasi gel karbamid peroksida 16%
49
4.8 Analisa Data
Data yang telah terkumpul dari hasil pengukuran kekasaran permukaan enamel gigi dianalisis secara uji Kruskall -Wallis yang menunjukkan perbedaan maka dilanjutkan uji analisis Mann Whitney untuk melihat perbedaan antar kelompok.
50
BAB 5
HASIL PENELITIAN
5.1 Hasil Penelitian
5.1.1 Kekasaran Permukaan Sampel Kelompok 1
Kelompok 1 merupakan kelompok yang diberikan perlakuan perendaman jus buah tomat dengan konsentrasi 100%. Nilai kekasaran permukaan sampel diperoleh dengan menghitung selisih dari pengukuran sebelum dan setelah diberikan perlakuan dari setiap sampel kelompok 1 yang diukur dengan menggunakan alat stylus profilometer. Nilai peningkatan kekasaran permukaan sampel menunjukkan nilai terbesar 1,465 µm. (Tabel 3).
Tabel 2. Nilai kekasaran permukaan kelompok 1
Sebelum (µm) Sesudah (µm) Selisih (µm)
0,549 0,782 0,233 1,058 1,391 0,333 1,327 2,007 0,680 1,162 1,893 0,731 1,690 1,455 - 0,235 1,759 1,890 0,131 0,623 2,088 1,465 0,627 0,728 0,101 2,135 1,848 - 0,287 0,448 0,715 0,267
51
5.1.2 Kekasaran Permukaan Sampel Kelompok 2
Kelompok 2 merupakan kelompok yang diberikan perlakuan perendaman jus buah tomat dengan konsentrasi 50%. Nilai kekasaran permukaan sampel diperoleh dengan menghitung selisih dari pengukuran sebelum dan setelah diberikan perlakuan dari setiap sampel kelompok 2 yang diukur dengan menggunakan alat stylus profilometer. Nilai peningkatan kekasaran permukaan sampel menunjukkan nilai terbesar 1,155 µm (Tabel 4).
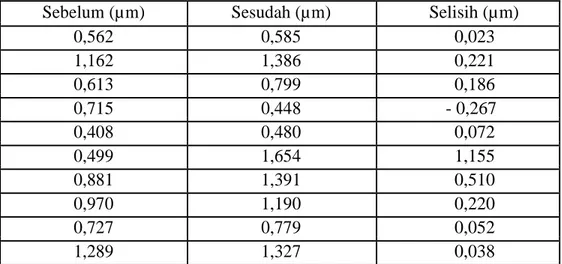
Tabel 3. Nilai kekasaran permukaan kelompok 2
Sebelum (µm) Sesudah (µm) Selisih (µm)
0,562 0,585 0,023 1,162 1,386 0,221 0,613 0,799 0,186 0,715 0,448 - 0,267 0,408 0,480 0,072 0,499 1,654 1,155 0,881 1,391 0,510 0,970 1,190 0,220 0,727 0,779 0,052 1,289 1,327 0,038
5.1.3 Kekasaran Permukaan Sampel Kelompok 3
Kelompok 3 merupakan kelompok yang diaplikasikan bahan home
bleaching karbamid peroksida 16%. Nilai kekasaran permukaan sampel
diperoleh dengan menghitung selisih dari pengukuran sebelum dan setelah pengaplikasian dari setiap sampel kelompok 3 yang diukur dengan menggunakan alat stylus profilometer. Nilai peningkatan kekasaran permukaan sampel menunjukkan nilai terbesar 1,340 µm. (Tabel 5).
52
Tabel 4. Nilai kekasaran permukaan kelompok 3
Sebelum (µm) Sesudah (µm) Selisih (µm)
0,727 1,281 0,554 0,755 0,682 - 0,073 1,281 2,621 1,340 0,602 0,928 0,326 1,759 1,890 0,131 1,342 1,583 0,241 0,433 0,730 0,297 0,662 0,518 - 0,144 1,235 1,524 0,289 1,654 1,982 0,328
5.2 Analisis Hasil Penelitian
Data hasil penelitian dianalisis secara statistik dengan pertama menggunakan tes normalitas yaitu Shapiro-Wilk dimana ketahui nilai p = 0,307 > 0,05 , p = 0.027 < 0,05 , p = 0,024 < 0,005 , maka didapati data perubahan kekasaran enamel gigi tidak memenuhi asumsi normalitas dan dilakukan pengujian selanjutnya dengan menggunakan uji Kruskal-Wallis .
5.2.1 Uji Kruskal-Wallis
Tabel dibawah ini menunjukkan rata-rata kekasaran permukaan dan standard deviasi kelompok 1,2 dan 3.
Tabel 6. Tabel hasil uji Kruskal-Wallis
Kelompok N x (µm) ±SD P
1 10 0,342 0,516
0,068
53
Dari tabel Kruskal-Wallis diperoleh nilai signifikasi 0,0628 (p>0,05) dengan demikian tidak terdapat perbedaan kekasaran permukaan gigi yang signifikan pada penggunaan karbamid peroksida 16% dan jus buah tomat sebagai bahan pemutih gigi. Untuk mengetahui perbedaan nilai kekasaran permukaan sampel diantara masing-masing kelompok 1,2 dan 3, maka dilanjutkan dengan Uji Mann-Whitney.
5.2.2 Uji Mann-Whitney
Tabel 7. Hasil uji Mann-Whitney
Kelompok P
Kelompok Tomat 100% - Kelompok Tomat 50% 0,326
Kelompok Tomat 100% - Kelompok Karbamid Peroksida 16% 0,850 Kelompok Tomat 50% - Kelompok Karbamid Peroksida 16% 0,226
*Terdapat perbedaan yang bermakna pada p<0,05
Pada tabel 7 (hasil Uji Mann-Whitney) diatas perbandingan kelompok tomat 100% dan kelompok tomat 50% diperoleh signifikasi sebesar 0,326 (p>0,05), perbandingan kelompok tomat 100% dan kelompok karbamid peroksida 16% sebesar 0,850 (p>0,05) serta perbandingan antara kelompok tomat 50% dan kelompok karbamid peroksida 16% diperoleh signifikasi sebesar 0,226 (p>0,05). Hal ini berarti tidak terdapat perbedaan yang bermakna antara kelompok tomat 100% dan kelompok tomat 50%, kelompok tomat 100% dan kelompok karbamid peroksida 16% serta kelompok tomat 50% dan kelompok karbamid peroksida 16%.
54
BAB 6 PEMBAHASAN
Penelitian ini merupakan jenis penelitian eksperimental laboratorium dengan desain penelitian pre and post test with group design. Pada penelitian sampel yang digunakan adalah gigi molar tiga yang diekstraksi dengan menetapkan beberapa kriteria yaitu mahkota masih utuh dan akar sudah terbentuk sempurna, tiada karies dan tiada tambalan. Jumlah sampel yang digunakan adalah sebanyak 15 gigi molar tiga yang akan dibagi menjadi dua bagian sehingga terdapat 30 buah sampel bagi penelitian ini yang dibagi kedalam tiga kelompok yaitu kelompok pertama yang akan dilakukan perendaman dalam jus buah tomat dengan konsentrasi 100%, kelompok kedua perendaman dalam jus buah tomat dengan konsentrasi 50% dan kelompok 3 diaplikasikan Karbamid Peroksida 16%.
Sampel-sampel kemudian dilakukan pengukuran dan pencatatan kekasaran permukaan enamel sebelum gigi direndam/diberikan perlakuan. Setiap perlakuan diperlukan buah tomat sebanyak 400 gram yang dimanfaatkan menjadi jus dengan cara 200 gram tomat dihaluskan tanpa air dan dihasilkan jus buah tomat dengan konsentrasi 100% yang digunakan untuk sampel kelompok 1. Kemudian, 200 gram tomat dihaluskan tanpa air lagi lalu dilakukan pengenceran menggunakan air matang dengan menggunakan rumus pengenceran yang digunakan untuk sampel kelompok 2 yaitu V1C1=V2C2. Setiap hari jus tomat dalam wadah percobaan tersebut harus diganti, gigi setiap kelompok perlakuan dikeluarkan dari wadahnya masing-masing yang berisi saliva buatan, dicuci di bawah air mengalir dan
55 dikeringkan dengan tisu. Lalu gigi direndam dalam wadah yang sesuai dengan kelompok perlakuannya masing- masing. Setiap hari saliva buatan dalam wadah tersebut harus diganti. Prosedur ini diulang 3 kali sehari dengan selang 6 jam selama 2 menit dalam waktu 2 minggu/ 14 hari. Pada kelompok 3 diaplikasikan karbamid peroksida 16% sesuai dengan petunjuk pabrik, setelah itu dicuci kembali dibawah air mengalir, keringkan dengan tisu dan rendam dalam saliva buatan. Pengaplikasian dilakukan selama 2 minggu. Setelah 2 minggu/ 14 hari, gigi dikeluarkan dari wadahnya masing-masing, dicuci dibawah air mengalir dan dikeringkan dengan tisu lalu dilakukan pengukuran kekasaran permukaan enamel dengan menggunakan profilometer. Sebagian besar gigi dalam masing-masing kelompok sampel mengalami peningkaatn kekasaran permukaan setelah diberikan perlakuan.
Dalam kelompok 1 yang diberi perlakuan jus buah tomat 100% dan kelompok 2 yang diberi perlakuan jus buah tomat 50% terdapat gigi mengalami peningkatan kekasaran permukaan enamel. Nilai rata-rata peningkatan kekasaran yang didapat sebesar 1,465 µm pada kelompok 1 dan 1,155 µm pada kelompok 2 . Peningkatan kekasaran permukaan enamel dapat disebabkan karena sifat asam dari jus buah tomat 100% dan 50% yang dapat menyebabkan perubahan pada permukaan enamel. Jus buah tomat 100% dengan nilai pH ± 4,5 dan jus buah tomat 50% dengan nilai pH ± 5,5 mengandung asam yang dapat menyebabkan hilangnya struktur mineral dari enamel.
Nilai pH yang rendah juga akan meningkatkan konsentrasi ion hidrogen yang dapat merusak hidroksiapatit pada enamel gigi. Pada saat berkontak dengan asam terjadinya pembesaran jalur interkristalin. Interkristalin merupakan batas antara kristal hidroksiapatit yang terdapat pada prisma enamel.17 Pembesaran jalur interkristalin dapat menyebabkan
56 mineral enamel lebih mudah untuk berdifusi keluar dan memudahkan penetrasi asam ke dalam lapisan subsurface enamel. Hal ini dapat menyebabkan kerusakan sampai ke bagian gigi yang lebih dalam dan menyebabkan peningkatan kekasaran permukaan enamel gigi.17
Pada kelompok 1 dan kelompok 2 juga terdapat beberapa gigi yang tidak mengalami peningkatan kekasaran. Hal ini dapat terjadi karena komposisi kimia dan ketebalan enamel yang berbeda-beda pada setiap gigi. Buah tomat juga mengandung berbagai mineral seperti kalsium. Kalsium merupakan komponen utama pembentuk tulang dan gigi. Kalsium juga dapat berperan dalam proses remineralisasi.31,32
Pada kelompok 3 yang diberi perlakuan karbamid peroksida 16% terdapat gigi yang mengalami peningkatan kekasaran. Nilai rata-rata kekasaran enamel yang terjadi adalah sebesar 1,340 µm. Hasil penelitian ini sejalan dengan penelitian Soares dkk dimana penggunaan karbamid peroksida 16% menyebabkan hilangnya struktur mineral enamel yang menyebabkan perubahan pada permukaan enamel menjadi lebih kasar.10 Penelitian Martin JMH dkk, menyatakan bahwa asam dari bahan pemutih dapat meningkatkan kekasaran permukaan enamel.41 Penelitian Cavalli V dkk, menunjukkan bahwa penggunaan karbamid peroksida dengan konsentrasi rendah yang berbeda telah mengakibatkan peningkatan yang signifikan
terhadap kekasaran permukaan enamel gigi dan evaluasi SEM mengungkapkan bahwa produk pemutih gigi memiliki potensi efek demineralisasi pada permukaan enamel gigi.12
Nilai pH karbamid peroksida yang dipakai pada perawatan home bleaching berkisar antara 4 – 6,5.6 Pelepasan urea setelah 15 menit aplikasi akan menyebabkan pH karbamid peroksida turun dari nilai awalnya.
57 Penurunan nilai pH tersebut dapat menyebabkan larutnya komponen-komponen prisma enamel hingga membentuk porus dan meningkatkan kekasaran permukaan enamel.6
Penurunan kekasaran permukaan enamel yang terjadi pada kelompok 3 kemungkinan dapat terjadi karena proses remineralisasi yang terjadi selama sampel disimpan dalam saliva artifisial. Klaric dkk dalam penelitianya menyimpulkan penggunaan saliva artifisial dapat memulihkan sedikit komponen apatit pada enamel yang terpapar asam.42 Saliva secara langsung akan menetralkan suasana asam yang terjadi. Saliva juga mengandung ion kalsium dan fosfat yang dapat meremineralisasi permukaan enamel gigi.42
Secara umum peningkatan kekasaran lebih besar dilihat pada kelompok 1. Baik tomat maupun karbamid, keduanya mempunyai sifat asam yang dapat menyebabkan perubahan permukaan enamel.10 Pada saat berkontak dengan asam,bagian ujung dari kristal enamel akan larut terlebih dahulu dan kemudian meluas di sepanjang kristal enamel. Kecepatan melarutnya enamel dipengaruhi oleh derajat keasaman(pH), konsentrasi asam, waktu melarut dan kehadiran ion sejenis kalsium dan fosfat.10,16
Hasil uji normalitas pada data hasil pengukuran kekasaran gigi pada kelompok 1 yang direndam dalam jus tomat 100% menunjukkan nilai p = 0,307 > 0,05. Pada kelompok 2 menunjukkan nilai p = 0,027 < 0,05 dan pada kelompok 3 menunjukkan nilai p = 0,024 < p. Maka asumsi normalitas pada data selisih kekasaran permukaan enamel tidak terpenuhi. Karena itu analisis data dilanjutkan dengan uji Kruskall-Wallis dan uji Mann-Whitney.
Uji Kruskall-Wallis dilakukan dengan membandingkan nilai peningkatan kekasaran permukaan enamel antara kelompok jus tomat 100%, kelompok jus tomat 50% dan karbamid peroksida 16%. Berdasarkan hasil uji
58 Kruskall-Wallis didapat nilai p = 0,068 dimana terdapat perbedaan yang tidak signifikan pada p < 0,05. Selanjutnya dilakukan Uji Mann-Whitney untuk melihat perbedaan antar kelompok, hasil perbandingan kelompok tomat 100% dan kelompok tomat 50% diperoleh signifikasi sebesar 0,326 (p>0,05), perbandingan kelompok tomat 100% dan kelompok karbamid peroksida 16% sebesar 0,850 (p>0,05) serta perbandingan antara kelompok tomat 50% dan kelompok karbamid peroksida 16% diperoleh signifikasi sebesar 0,226 (p>0,05). Hal ini berarti tidak terdapat perbedaan yang bermakna antara kelompok tomat 100% dan kelompok tomat 50%, kelompok tomat 100% dan kelompok karbamid peroksida 16% serta kelompok tomat 50% dan kelompok karbamid peroksida 16%.Hal ini mungkin disebabkan nilai pH jus buah tomat dan karbamid peroksida 16% tidak terlalu jauh berbeda.
Selain itu, setiap kelompok juga disimpan dalam saliva buatan dan memungkinkan dapat terjadi proses remineralisasi setelah diberikan perlakuan. Remineralisasi merupakan reaksi kebalikan dari demineralisasi. Saliva dapat berperan sebagai buffer untuk mentralkan suasana asam rongga mulut dan mencegah larutnya kristal enamel.42 Saliva dapat berperan sebagai buffer alami untuk menetralkan suasana asam rongga mulut dan mencegah larutnya kristal enamel. Saliva kaya akan ion kalsium dan fosfat. Pada saat rongga mulut berada pada pH 5,5 saliva akan menetralkan pH rongga mulut dengan dan ion kalsium akan menggantikan ion fosat yang terlepas dari enamel gigi.42
Meningkatnya kekasaran permukaan enamel akan mengakibatkan risiko perlekatan dan kolonisasi bakteri yang akhirnya akan meningkatkan demineralisasi dan infeksi gingiva.9Permukaan yang kasar dapat memudahkan perlekatan bakteri dan menyulitkan pengakatannya dengan cara alami atau