ANALISIS KADAR ANGKA PERMANGANAT PADA AIR MINUM DAN AIR BERSIH DI BALAI DINAS KESEHATAN MEDAN
KARYA ILMIAH
MAI FRANSISKA BARUTU 092401054
PROGRAM STUDI DIPLOMA III KIMIA DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
ANALISIS KADAR ANGKA PERMANGANAT PADA AIR MINUM DAN AIR BERSIH DI BALAI DINAS KESEHATANMEDAN
KARYA ILMIAH
Diajukan Untuk Melengkapi Tugas dan Memenuhi Syarat Memperoleh Gelar Ahli Madya
MAI FRANSISKA BARUTU
092401054
PROGRAM STUDI DIPLOMA III KIMIA DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : ANALISIS KADAR ANGKA PERMANGANAT
PADA AIR MINUM DAN AIR BERSIH DI BEBERAPA DAERAH MEDAN
Kategori : TUGAS AKHIR
Nama : MAI FRANSISKA BARUTU
NIM : 092401054
Program Studi : DIPLOMA III KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM UNIVERSITAS SUMATERA UTARA
Disetujui di :
Medan , April 2012
Diketahui/Disetujui Oleh :
Departemen Kimia FMIPA USU
Ketua Program Studi D3 Kimia Analis Dosen Pembimbing,
Dra. Emma Zaidar Nasution, M.Si Drs.Adil Ginting,MSc.
NIP : 195512181987012001 NIP :195307041980031002
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
ANALISIS KADAR ANGKA PERMANGANAT PADA AIR MINUM DAN AIR BERSIH DI BALAI DINAS KESEHATAN MEDAN
KARYA ILMIAH
Saya mengakui bahwa Karya Ilmiah ini adalah hasil kerja saya sendiri. Kecuali beberapa kutipan dari ringkasan yang masing-masing disebutkan sumbernya.
Medan, April 2012
PENGHARGAAN
Puji syukur kehadirat Allah SWT yang senantiasa melimpahkan berkah dan rahmat Nya sehingga penulisan karya ilmiah yang berjudul “ANALISIS KADAR ANGKA PERMANGANAT PADA AIR MINUM DAN AIR BERSIH DI BEBERAPA DAERAH MEDAN” akhirnya dapat penulis selesaikan. Dalam penyusunan karya ilmiah ini penulis ingin mengucapkan terima kasih dari beberapa pihak yang telah banyak membantu baik moril maupun materil. Maka dengan segala kerendahan hati penulis menyampaikan rasa terima kasih yang sebesar-besarnya kepada :
1. Orang tua tercinta (Ayahanda K.Barutu dan Ibunda P.Munthe) yang telah memberikan doa restunya yang tiada terhingga, dan telah banyak memberikan pengorbanan moril maupun materil serta kesabaran yang tulus, kakak dan abang saya yang selalu memberikan semangat untuk penulis sehingga selalu termotivasi ingin menyelesaikan Tugas Akhir dengan baik. serta seluruh keluarga saya yang telah memberikan dukungan kepada penulis.
2. Bapak Drs. Adil Ginting MSc sebagai dosen pembimbing yang telah banyak meluangkan waktu dalam memberikan bimbingan kepada penulis.
3. Ibu Dr. Rumondang Bulan MS, selaku Ketua Departemen Kimia FMIPA USU, dan Ibu Dra. Emma Zaidar MSi, selaku Ketua Program Studi D3 Kimia Analis.
4. Ibu Dra Ernawati Apt. selaku pembimbing PKL serta seluruh pegawai di Balai DINAS KESEHATAN Pancing Medan yang telah banyak meluangkan waktu dan memberikan banyak masukan kepada penulis. 5. Partner saya saat Praktek Kerja Lapangan (Tatiana Rizka,Nurhamida
Sagala,Yessi Juniar Samosir,Masryana Ikawani Girsang) terima kasih buat pengertian dan bantuan yang diberikan saat Praktek Kerja Lapangan masih berlangsung sampai Tugas Akhir penulis terselesaikan.
6. Rekan-rekan mahasiswa/i Kimia Analis D3 angkatan 2009 serta sahabat-sahabat yang lain yang tidak dapat saya sebutkan satu persatu yang telah memberikan dukungan sehingga penulis dapat
menyelesaikan Karya Ilmiah ini.
semua pihak yang dapat menjadi bahan masukan bagi penulis. Semoga penulisan Karya Ilmiah ini dapat bermanfaat bagi para pembaca.
Medan, April 2012
ABSTRAK
ANALYSIS OF RATE LEVELS PERMANGANATE IN DRINGKING WATER AND CLEAN WATER IN DINAS KESEHATAN MEDAN
ABSTRACT
DAFTAR ISI
Halaman
PERSETUJUAN ii PERNYATAAN iii PENGHARGAAN iv
ABSTRAK vi
ABSTRACT vii
DAFTAR ISI viii
DAFTAR TABEL x BAB 1 PENDAHULUAN 1
1.1 Latar Belakang 1 1.2 Permasalahan 3
1.3 Tujuan 3
1.5 Manfaat 3
BAB 2 TINJAUAN PUSTAKA 4
2.1 Air 4
2.1.1 Sifat Umum Air 4
2.1.2 Sumber-sumber Air 5
2.1.3 Pembagian Air 8 2.1.4Golongan-golongan Air 11
2.2 Air minum/Air Bersih 11
2.2.1 Pengertian Air minum/Air bersih 11
2.2.2 Syarat-syarat Air minum/Air bersih 11
2.3 Pencemaran Air 12 2.3.1 Defenisi Pencemaran Air 12 2.3.2 Beberapa Parameter Untuk Menilai Pencemaran Air 13 2.3.3 Sumber-sumber Pencemaran Air 13 2.3.4 Faktor-faktor yang mempengaruhi pencemaran Air 15 2.3.5 Dampak yang ditimbulkan oleh pencemaran Air 16 2.4 Manfaat Air bagi kesehatan 16 2.5 Zat Organik (sebagai KMnO4) 17 2.6 Titrimetri 18 2.6.1 Pengertian Titrimetri 18 2.6.2 Larutan Baku/peniter 19 2.6.3 Penggolongan Titrimetri 19 2.7 Angka permanganat 21 2.8 Permanganometri 21 2.8.1 Oksidasi Dengan Kalium Permanganat 22
2.8.2 Sumber Kesalahan Permanganometri 23
BAB 3 BAHAN DAN METODE 24
3.1 Alat dan Bahan 24
3.1.1 Alat 24
3.1.2 Bahan 24
3.2 Penyediaan Sampel 24
BAB 4 HASIL DAN PEMBAHASAN 26
4.1 Data Percobaan 26
4.2 Perhitungan 27
4.3 Pembahasan 29
BAB 5 KESIMPULAN DAN SARAN 30
5.1 Kesimpulan 30
5.2 Saran 30
DAAFTAR PUSTAKA 31
DAFTAR TABEL
Halaman
ABSTRAK
ANALYSIS OF RATE LEVELS PERMANGANATE IN DRINGKING WATER AND CLEAN WATER IN DINAS KESEHATAN MEDAN
ABSTRACT
BAB 1 PENDAHULUAN
1.1Latar Belakang
Air merupakan suatu sarana utama untuk meningkatkan derajat kesehatan
masyarakat, karena air merupakan salah satu media dari berbagai macam penularan,
terutama penyakit perut. seperti yang telah kita ketahui bahwa penyakit perut adalah
penyakit yang paling banyak terjadi di Indonesia.
Melalui penyediaan air bersih baik dari segi kualitas maupun kuantitasnya di
suatu daerah, maka penyebaran penyakit menular dalam hal ini adalah penyakit perut
diharapkan bisa ditekan seminimal mungkin. Penurunan penyakit perut ini didasarkan
atas pertimbangan bahwa air merupakan salah satu mata rantai penularan penyakit
perut. Agar seseorang menjadi tetap sehat sangat dipengaruhi oleh adanya kontak
manusia tersebut dengan makanan dan minuman.
Peningkatan kualitas air minum dengan jalan mengadakan pengelolaan
terhadap air yang akan diperlukan sebagai air minum dengan mutlak diperlukan
terutama apabila air tersebut berasal dari air permukaan pengolahan yang dimaksud
bisa dimulai dari yang sangat sederhana sampai yang pada pengolahan yang mahir
dan lengkap, sesuai dengan tingkat kekotoran dari sumber asal air tersebut (Sutrisno,
2006).
Pengunaan air yang utama dan sangat vital bagi kehidupan adalah sebagai air
sendiri. Di dalam tubuh manusia air diperlukan untuk melarutkan berbagai jenis zat
yang diperlukan tubuh.
Mengingat pentingnya peran air, sangat di perlukan adanya sumber air yang
dapat menyediakan air yang baik dari segi kuantitas dan kualitasnya. Di Indonesia,
umumnya sumber air minum bersal dari air permukaan (surface water), air tanah
(ground water), dan air hujan (rain water) (Mulia, 2005).
Kehidupan mikroorganisme, seperti ikan dan hewan lainnya, tidak terlepas
dari kandungan oksigen yang terlarut di dalam air, tidak berbeda dengan manusia dan
mahluk hidup lainnya yang ada di darat, yang juga memerlukan oksigen dari udara
agar tetap dapat bertahan. Air yang tidak mengandung oksigen tidak akan
memberikan kehidupan bagi mikroorganisme, ikan dan hewan air lainnya. Oksigen
yang terlarut di dalam air sangat penting artinya bagi kehidupan (Ardana, 2001).
Peningkatan air minum dengan jalan mengadakan pengelolaan terhadap air
yang akan diperlukan sebagai air minum dengan mutlak diperlukan terutama apabila
air tersebut berasal dari permukaan. Pengelolaan yang dimaksud bisa dimulai dari
yang sangat sederhana sampai yang pengelolaan yang lengkap, sesuai dengan tingkat
kekotoran dari sumber asal air tersebut. Oleh karena itu, dalam praktek sehari-hari
maka pengelolaan air menjadi pertimbangan yang utama untuk menentukan apakah
sumber tersebut bisa dipakai sebagai sumber persediaan atau tidak. Untuk itu
diperlukan analisa kadar permanganat untuk mengetahui kualitas air bersih yang
1.2Permasalahan
Berapakah kadar angka permanganat pada air minum dan air bersih yang akan
digunakan di daerah Medan apakah memenuhi standar kualitas air bersih.
1.3 Tujuan
Untuk mengetahui kadar angka permanganat dari air minum dan air bersih di daerah
Medan yang akan di gunakan oleh masyarakat.
1.3Manfaat
Memberikan informasi mengenai kandungan kadar Angka permanganat pada air
minum dan air air bersih di daerah Medan, serta memberikan wawasan dan
pengetahuan penulis terhadap penerapan ilmu kimia analisis dalam pemeriksaan
BAB 2
TINJAUAN PUSTAKA
2.1 Air
Air merupakan zat kimia yang penting bagi semua bentuk kehidupan yang
diketahui sampai saat ini di bumi. Air adalah senyawa kimia dengan rumus kimia
H2O: satu molekul air tersusun dari dua atom hidrogen yang terikat secara kovalen
pada satu atom oksigen. Pada kondisi standar, air bersifat tidak berwarna, tidak berasa
dan tidak berbau yaitu pada tekanan 100 kPa (1 bar) dan temperature 273,15 K (0oC).
Zat kimia ini merupakan suatu pelarut yang penting, yang memiliki kemampuan untuk
melarutkan banyak zat kimia lainnya, seperti garam-garam, gula, asam, beberapa jenis
gas dan banyak macam molekul organik (Kusmayadi, 2008).
2.1.1 Sifat Umum Air − Sifat Fisik
Titik beku 0oC;
Masa jenis es (0oC) 0,92 g/cm3;
Masa jenis air (0oC) 1,00 gr/cm3;
Panas lebur 80 kal/gram;
Titik didih 100oC;
Panas penguapan 540 kal/gram;
Temperatur kritis 347oC;
Tekanan kritis 217 Atm;
Konstanta dielektrikum (25oC).
Perlu diketahui bahwa air laut mempunyai titik beku (-1,9oC), massa jenis air tawar
terbesar pada 4oC, sedangkan air laut (kadar garam 35%) mempunyai masa jenis
terbesar pada
(-3,5oC).
− Sifat Kimia
Baik air laut, air hujan ,maupun air tanah/air tawar mengandung mineral.
Macam-macam mineral yang terkandung dalam air tawar bervariasi tergantung
struktur tanah dimana air itu diambil. Sebagai contoh mineral yang terkandung
dalam air itu bukan melalui suatu reaksi kimia melainkan terlarut dari suatu
subtansi misalnya dari batu andesit (dari batu vulkanis). Sifat kimia yang lain
yaitu konduktivitas listrik pada air paling seikit 1000 kali lebih besar daripada
cairan non metalik pada suhu ruangan.
Air dapat terurai oleh pengaruh arus listrik engan reaksi:
H2O → H+ + OH-
Air merupakan pelarut yang baik
Air dapat bereaksi dengan basa kuat dan asam kuat
Air bereaksi dengan berbagai subtansi membentuk senyawa padat dimana
air terikat dengannya, misalnya senyawa hidrate (Gabriel, 2001).
2.1.2 Sumber-Sumber Air
Sumber-sumber air minum diantaranya adalah:
1. Air laut.
3. Air permukaan.
4. Air tanah.
1.Air laut.
Mempunyai sifat asin, karena mengandung garam NaCl.kadar garam NaCl dalam
air laut 3 %. Dengan keadaan ini maka air laut tak memenuhi syarat untuk air minum.
2.Air atmosfir, air meteriologik.
Alam dalam keadaan murni sangat bersih karena dengan adanya pengotoran
udara yang disebabkan olah kotoran-kotoran industri/debu dan lain sebgainya. Maka
untuk menjadikan air hujan sebagai sumber air minum hendaknya pada waktu
menampung air hujan jangan dimulai pada saat hujan mulai turun, karena masih
mengandung banyak kotoran.
Selain itu air hujan mempunyai sifat agresif terutama terhadap pipa-pipa
penyalur maupun bak-bak reservoir, sehingga hal ini akan mempercepat terjainya
korosi(karatan). juga air hujan ini mempunyai sifat lunak, sehingga akan boros
terhadap pemakaian sabun.
3.Air permukaan.
Adalah air hujan yang mengalir di permukaan bumi.pada umumnya air
permukaan ini hanya mendapat pengotoran selama pengalirannya, misalnya oleh
lumpur,batang-batang kayu, daun-daun, kotoran industri kota dan sebagainya.
Beberapa pengotoran ini untuk masing-masing air permukaan akan
berbeda-beda, tergantung pada daerah pengaliran air permukaan ini. jenis pengotorannya
Setelah mengalami suatu pengotoran, pada suatu saat air permukaan itu akan
mengalami suatu proses pembersihan sendiri yang dapat dijelaskan sebagai berikut:
Udara yang mengandung oksigen atau gas O2 akan membantu mengalami
proses pembusukan yang terjadi pada air permukaan yang telah mengalami
pengotoran, karena selama dalam perjalanan, O2 akan meresap kedalam air
permukaan.
4.Air tanah
Terbagi atas:
a.air tanah dangkal.
Terjadi karena daya proses peresapan air dari permukaan tanah.lumpur akan
tertahan demikian pula dengan sebagian bakteri, sehingga air tanah akan jernih tetapi
lebih banyak mengandung zat kimia (garam-garam yang terlarut) karena mempunya
lapisan tanah yang mempunyai unsure-unsur kimia yang tertentu untuk lapisan tanah.
Lapis tanah disini berfungsi sebagai saringan. Disamping penyaringan, pengotoran
juga masih terus berlangsung, terutama pada muka air yang dekat dengan muka tanah,
setelah menemui lapisan rapat air, air akan terkumpul merupakan air tanah dangkal
dimana air tanah ini dimanfaatkan untuk sumber air minum melalui sumur-sumur
dangkal.
Air tanah dangkal ini dapat pada kedalaman 15,00 m. sebagai sumur air
minum, air tanah dangkal ini ditinjau dari segi kualitas agak baik. kuantitas kurang
b.Air tanah dalam.
Terdapat setelah lapisan rapar air yang pertama. pengambilan air tanah dalam,
tak semudah pada air tanah dangkal.
Kualitas dari air tanah dalam pada umumnya lebih baik dari air dangkal,
karena penyaringannya lebih sempurna dan bebas dari bakteri. susunan unsur-unsur
kimia tergantung pada lapis-lapis tanah yang dilalui. Jika melalui tanah kapur, maka
air itu akan menjadi sadah, karena mengandung Ca (HCO3)2 dan Mg (HCO3)2.jika
melalui batuan granit, maka air itu lunak dan agresif karena mengandung gas CO2 dan
Mn (HCO3)2.
c.Mata air
Adalah air tanah yang ke luar dengan sendirinya ke permukaan tanah. Mata air
yang berasal dari tanah dalam, hampir tidak terpengaruh oleh musim dan kualitas
/kuantitasnya sama dengan keadaan air dalam.
Berdasarkan keluarnya (munculnya permukaan tanah) terbagi atas:
− Rembesan, di mana air ke luar dari lereng-lereng
− Umbul, di mana air ke luar ke permukaan pada suatu dataran (Sutrisno, 2006).
2.1.3 Pembagian Air
Pembagian air berdasarkan analisis
a. Air kotor/air tercemar
Air yang bercampur dengan satu atau berbagai campuran hasil buangan disebut
air tercemar/air kotor.
Menurut lokasi pencemaran maka air tercemar ini digolongkan dalam 2 lokasi
yaitu:
Air tercemar di pedesaan. Sumber pencemar adalah hasil sampah rumah
tangga, hasil kotoran hewan, hasil industri kecil.
Air tercemar perkotaan bersumber dari hasil sampah rumah tangga, pusat
perbelanjaan, industri kecil, industry besar, hotel, restoran, tempat keramaian.
b. Air bersih
Air bersih adalah air yang sudah terpenuhi syarat fisik, kimia, namun
bakteriologi belum terpenuhi. Air bersih ini diperoleh dari sumur gali, sumur
bor, air hujan, air dari sumber mata air.
Pemanfaatan air bersih
Secara umum dapat dikatakan penggunaan air bersih sebagai berikut: Akan diolah menjadi air siap minum
Untuk keperluan keluarga (cuci, mandi)
Sarana pariwisata
Pada industri (sarana pendingin)
Sebagai alat pelarut (dalam bidang farmasi/kedokteran)
Pelarut obat-obatan dan infuse (apabila air tersebut telah diolah menjadi air
steril)
Sebagai sarana irigasi
Sebagai sarana peternakan
c. Air siap diminum/air minum
Air siap minum/air minum ialah air yang sudah terpenuhi syarat fisik, kimia,
bakteriologi serta level kontaminasi maksimum (LKM) (Maximum
Contaminant Level).
Level kontaminasi maksimum meliputi sejumlah zat kimia, kekeruhan dan
bakteri koliform yang diperkenankan dalam batas-batas aman. Lebih jelas lagi,
bahwa air siap minum/air minum yang berkualitas harus terpenuhi syarat
sebagai berikut:
Harus jernih, transparan dan tidak berwarna
Tidak dicemari bahan organik maupun bahan anorganik
Tidak berbau, tidak berasa, kesan enak bila diminum
Mengandung mineral yang cukup sesuai dengan standard
Bebas kuman/LKM coliform dalam batas aman (Gabriel, 2001).
2.1.4 Golongan-golongan Air
Peraturan pemerintah No. 20 tahun 1990 mengelompokkan kualitas air menjadi beberapa golongan menurut peruntukannya. Adapun penggolongan air menurut
peruntukannya adalah sebagai berikut.
1. Golongan A, yaitu air yang dapat digunakan sebagai air minum secara
langsung, tanpa pengolahan terlebih dahulu.
2. Golongan B, yaitu air yang dapat digunakan sebagai air baku air minum.
3. Golongan C, yaitu air yang dapat digunakan untuk keperluan perikanan dan
peternakan.
4. Golongan D, yaitu air yang dapat digunakan untuk keperluan pertanian, usaha
2.2 Air Minum/Air bersih
2.2.1 Pengertian Air Minum/Air bersih
Menurut Peraturan Menteri Kesehatan RI No. 907 /Menkes/SK/VII/2002, air
minum adalah air yang melalui proses pengolahan atau tanpa proses pengolahan yang
memenuhi syarat kesehatan dan dapat langsung diminum. Jenis air minum meliputi :
1. Air yang didistribusikan melalui pipa untuk keperluan rumah tangga
2. Air yang didistribusikan melalui tangki air
3. Air kemasan
4. Air yang digunakan untuk produksi bahan makanan dan minuman yang disajikan
kepada masyarakat Air minum merupakan salah satu kebutuhan manusia yang paling
penting. Seperti diketahui, kadar air tubuh manusia mencapai 68 persen dan untuk
tetap hidup air dalam tubuh tersebut harus dipertahankan. Kebutuhan air minum setiap
orang bervariasi dari 2,1 liter hingga 2,8 liter per hari, tergantung pada berat badan
dan aktivitasnya. Namun, agar tetap sehat, air minum harus memenuhi persyaratan
fisik, kimia, maupun bakteriologis (Suriawiria, 1995).
2.2.2 Syarat-syarat Air Minum/Air bersih
Air minum yang ideal seharusnya jernih, tidak berwarna, tidak berasa, dan tidak berbau. Air minumpun seharusnya tidak mengandung kuman pathogen dan segala
makhluk yang membahayakan kesehatan manusia. Tidak mengandung zat kimia yang
dapat mengubah fungsi tubuh, tidak dapat diterima secara estetis, dan dapat merugikan
secara ekonomis. Air itu seharusnya tidak korosif, tidak meninggalkan endapan pada
seluruh jaringan distribusinya. Pada hakekatnya, tujuan ini dibuat untuk mencegah
terjadinya serta meluasnya penyakit bawaan air. Air minum yang memenuhi persyaratan
(LKM). Level kontaminasi maksimum meliputi sejumlah zat kimia, kekeruhan dan
bakteri Coliform yang diizinkan dalam batas-batas maksimum (Slamet, 1994).
Dari segi kualitas air minum harus memenuhi :
a. Syarat fisik
Adapun syarat-syarat fisik yang ditentukan, yaitu :
- Air tak boleh berwarna
- Air tak boleh berasa
- Air tak boleh berbau
- Suhu air hendaknya (suhu udara ± 3o C)
- Air harus jernih.
b. Syarat kimia
Air minum tidak boleh mengandung racun, zat-zat mineral atau zat-zat kimia tertentu
dalam jumlah melampaui batas yang telah ditentukan. (Sutrisno, 2006).
c. Syarat biologi
Kualitas air ditentukan oleh kehadiran dan jumlah Coli didalamya, yaitu air minum
dan untuk air lainnya. Penentuan kehadiran mikroba didalam air, berdasarkan
kebutuhannya untuk mengetahui ada tidaknya jenis yang berbahaya sebagai penyebab
penyakit, penghasil toksin dan penyebab pencemaran air. (Suriawiria, 1993)
2.3 Pencemaran Air
2.3.1 Definisi Pencemaran Air
Menurut peraturan mentri kesehatan RI no. 173/Menkes/VII/77
Pencemaran air adalah suatu peristiwa masuknya zat ke dalam air yang
atau membahayakan kesehatan masyarakat.
Menurut peraturan perintah RI no. 20 tahun 1990
Pencemaran air adalah masuknya atau dimasukkannya makhluk hidup, zat, enenrgi
dan atau komponen lain kedalam air oleh kegiatan manusia, sehingga kualitas air
turun sampai ke tingkat tertentu yang membahayakan yang mengakibatkan air tidak
berfungsi lagi sesuai dengan peruntuknya (Mukono,2006).
2.3.2 Beberapa Parameter Untuk Menilai Pencemaran Air
Turbidity
Temperatur
pH
Dissolved Oksigen
Biological Oxygen Demand
Total Solid
Phosfat
Nitrat
Bacteri-coli
Biologis (Sutrisno, 2006)
2.3.3 Sumber-sumber Pencemaran Air Domestik (Rumah Tangga)
Yaitu berasal dari pembuangan air kotor dari amar mandi, kakus dan dapur. Industri
Secara umum jenis polutan air dapat dikelompokkan sebagai berikut:
Pasir atau lumpur yang tercampur dalam limbah air.
b.kimia
Bahan pencemar yang berbahaya: Merkuri (Hg), cadmium (Cd), Timah hitam
(Pb), pestisida dan jenis logam berat lainnya.
c.Mikrobioligi
Berbagai macam bakteri, virus, parasit dan lain-lainnya. Misalnya yang
berasal dari pabrik yang mengolah hasil ternak, rumah potong dan tempat
pemerahan susu sapi.
d.Radioaktif
Beberapa bahan radioaktif yang dihasilkan oleh pembangkit Listrik Tenaga
Nuklir (PLTN) dapat pula menimbulkan pencemaran air. Pertanian dan perkebunan
Polutan air dari pertanian/perkebunan dapat berupa:
a.Zat kimia
Misalnya berasal dari penggunaan pupuk, pestisida seperti (DDT, Dieldrin dan
lain-lain)
b.Mikrobiologi
misalnya virus, bakteri, parasit yang berasal dari kotoran ternak dan cacing
tambang di lokasi perkebunan.
c.Zat Radioaktif
Berasal dari penggunaan zat radioaktif yang dipakai dalam proses pematangan
2.3.4 Faktor-Faktor Yang Mempengaruhi Pencemaran Air
Mikroorganisme
Salah satu indikator bahwa air tercemar adalah adanya mikroorganisme patogen
dan non patogen didalamnya. Danau atau sungai yang terkontaminasi/tercemar
mempunyai spesies mikroorganisme yang berlainan dari air yang bersih. Air yang
tercemar umumnya mempunyai kadar bahan organic yang tinggi sehingga pada
umumnya banyak mengandung mikroorganisme heterotropik. Mikroorganisme
heterotropik akan menggunakan bahan organik tersebut untuk metabolism,
misalnya bakteri koliform.
Curah Hujan
Curah hujan di suatu daerah akan menentukan volume dari badan air dalam rangka
mempertahankan efek pencemaran terhadap setiap bahan buangan di dalamnya
(deluting effects). Curah hujan yang cukup tinggi sepanjang musim dapat lebih
mengencerkan (mendispersikan) air yang tercemar.
Kecepatan Aliran Air (Stream Flow)
Bila badan air memiliki aliran yang cepat, maka keadaan itu dapat memperkecil
kemungkinan timbulnya pencemaran air karena bahan polutan dalam air akan
lebih cepat terdispersi.
Kualitas Tanah
Kualitas tanah (Pasir atau lempung) juga mempengaruhi pencemaran air, ini
berkaitan dengan pencemaran tanah yang terjadi di dekat sumber air. Beberapa
logam berat dan sejenisnya serta penimbunan sampah secara besar-besaran
(misalnya open dumping).
2.3.5 Dampak Yang Ditimbulkan Oleh Pencemaran Air Disebabkan oleh mikrobiologi dalam air
Contoh penyakit yang ditimbulkan antara lain:
1.Tifoid, disebabkan oleh kuman salmonella thyphosa
2.kolera, disebabkan oleh bakteri vibrio kolera
3.Leptospirosis, disebabkan oleh spirochaeta
4.Giardiasis, disebabkan oleh sejenis protozoa
5.Disentri, disebabkan oleh Entamoeba histolitytica Disebabkan Oleh Pestisida
Tercemarnya air oleh pestsida dapat menyebabkan kanker kulit, keracunan,
kerusakan jaringan dan pada konsentrasi tertentu bisa menimbulkan kematian
(Mukono, 2006).
2.4 Manfaat Air Bagi Kesehatan
Air minum dalam tubuh manusia berfungsi untuk menjaga keseimbangan
metabolisme dan fisiologi tubuh. Setiap waktu, air perlu dikonsumsi karena setiap saat
tubuh bekerja dan berproses. Di samping itu, air juga berguna untuk melarutkan dan
mengolah sari makanan agar dapat dicerna. Tubuh manusia terdiri dari berjuta-juta sel
dan komponen terbanyak sel-sel itu adalah air. Jika kekurangan air, sel tubuh akan
menciut dan tidak dapat berfungsi dengan baik. Begitu pula, air merupakan bagian
ekskreta cair (keringat, air mata, air seni), tinja, uap pernafasan, dan cairan tubuh
2.5 Zat Organik (Sebagai KMnO4)
Zat organik yang terdapat di alam bisa berasal dari :
a. Alam misalnya minyak, tumbuh-tumbuhan, serat-serat minyak dan lemak hewan,
alkohol, selulosa, gula, pati dan sebagainya.
b. Sintesa misalnya berbagai persenyawaan dan buah-buahan yang dihasilkan dari
proses-proses dalam pabrik.
c. Fermentasi misalnya alkohol, aseton, gliserol, antibiotik, asam-asam dan sejenisnya
yang berasal dari kegiatan mikroorganisme terhadap bahan-bahan organik.
Dengan melihat proses asal terjadinya bahan-bahan organik tersebut dapat
diketahui bahwa sumber utama dari bahan-bahan tersebut adalah kegiatan-kegiatan
rumah tangga dan proses-proses industri, tanpa mengkesampingkan adanya
bahan-bahan organik yang berasal dari kegiatan-kegiatan dalam bidang pertanian, peternakan
dan pertambangan.
Adanya bahan-bahan organik dalam air erat hubungannya dengan terjadinya
perubahan sifat fisik dari air, terutama dengan timbulnya warna, bau dan rasa dan
kekeruhan yang tidak diinginkan. Adanya zat organik dalam air dapat diketahui
dengan menentukan angka permanganatnya. Walaupun KmnO4 sebagai oksidator
yang dipakai tidak dapat mengoksidasi semua zat organik yang ada, namun cara ini
sangat praktis dan cepat pengerjaanya. Standar kandungan bahan organik dalam
air-minum menurut Dep. Kes. R.I. maksimal yang diperbolehkan adalah 10 mg/L.
Pengaruh terhadap kesehatan yang dapat ditimbulkan oleh penyimpangan terhadap
standar ini adalah timbulnya bau yang tidak sedap pada air minum, dan dapat
2.6 TITRIMETRI
2.6.1 Pengertian Titrimetri
Titrimetri atau volumetric adalah salah satu cara pemeriksaan jumlah zat yang luas pemakainya. Pada analisa titrimetri sangat menguntngkan karena cara ini lebih
akurat dan teliti serta dapat digunakan untuk menentukan konsentrasi zat lain.
Pada dasarnya cara titrimetri ini terdiri dari pengukuran volume larutan
pereaksi yang dibutuhkan untuk bereaksi secara stokiometri dengan zat yang
ditentukan. Larutan pereaksi itu biasanya diketahui konsentrasinya dengan pasti dan
disebut pentiter atau larutan baku. Titrasi adalah proses penambahan peniter kedalam
zat yang akan ditentukan konsentrasinya dengan menggunakan bantuan alat yang
disebut buret. Pada proses titrasi juga ditambahkan larutan untuk menunjukkan titik
akhir titrasi. Pada proses titrasi juga dikenal dua titik yaitu titik kesetaraan (ekuivalen)
dan titik akhir titrasi. Titik kesetaraan akan dicapai bila jumlah zat peniter dan zat
yang akan ditentukan telah bereaksi secara stoikiometri. Sedangkan titik akhir titrasi
adalah titik dimana titrasi dapat dihentikan dengan adanya perubahan warna dari
larutan dengan adanya penambahan indikator.
Agar proses titrasi dapat berjalan dengan baik sehingga memberikan hasil
pemeriksaan yang tepat dan teliti maka persyaratan berikut perlu diperhatikan :
1. Interaksi antara peniter dan zat yang ditentukan harus berlangsung secara
stoikiometri
dengan faktor stoikiometrisnya berupa bilangan bulat.
3. Interaksi antara peniter dan zat yang ditentukan hars berlangsung secara
terhitung.
2.6.2 Larutan baku / peniter
Larutan baku adalah larutan yang konsentrasinya atau kepekatannya telah
diketahui dan dapat digunakan untuk menentukan konsentrasi zat yang lain yang
digunakan dalam analisa voumetris.
Larutan baku ini dapat dibagi dua yaitu larutan baku primer dan larutan baku
skunder. Larutan baku primer adalah larutan yang konsentrasinya telah diketahui dan
dapat dibuat hanya dengan cara penimbangan dan pengenceran yang teliti. contoh
larutan baku primer antara lain : H2C2O4, Na2B4O7, Ba(OH)2, dan lain-lain.
Sedangkan larutan baku sekunder adalah larutan baku yang konsentrasinya
dapat diketahui dengan cara menstandarisasikannya dengan mengunakan larutan baku
primer, contohnya NaOH, HCL, dan lain-lain.
2.6.3 Penggolongan Titrimetri
Pemeriksaan kimia secara titrimetri dapat digolongkan dengan berbagai cara tergantung pada jenis interaksi kimia yang terjadi, cara melakukan titrasi dan jumlah
cuplikan yang digunakan dalam pemeriksaan.
Penggolongan titrimetri berdasarkan pertidaksamaan kimia dapat dibedakan
menjadi empat bagian, yaitu :
1. Titrasi asam basa
Titrasi asam basa adalah didasrkan pada reaksi perpindahan proton antara
Dengan metode ini berbagai senyawa organic dan anorganik dapat ditentukan
dengan mudah.
Untuk titrasi basa digunakan larutan baku asam kuat,misalnya HCL, H2SO4.
Sedangkan asam dititrasi dengan larutan baku basa kuat, misalnya NaOH,
KOH. Titik akhir titrasi ditetapkan dengan bantuan indikator asam-basa yang
sesuai, atau secara potensimetri.
2. Titrasi Kompleksiometri
Titrasi kompleksiometri adalah didasarkan pada reaksi zat-zat pengkompeks
organik tertentu dengan ion-ion logam, menghasilkan senyawa kompleks yang
mantap. Zat pengkompleks yang paling sering digunakan adalah asam
etilendiaminatetra asetat (EDTA), yang membentuk senyawa kompleks yang
mantap dengan beberapa ion logam. Titik akhir titrasi ditetapkan dengan
indikator logam secara potensiometri dan spektrofotometri.
3. Titrasi Pengendapan
Titrasi pengendapan adalah didasarkan pada reaksi pembentukan endapan yang
sukar larut, misalnya ion-ion halida (kecuali flourida), sering ditentukan dengan
cara titrasi dengan larutan perak nitrat. Titik akhir titrasi ini juga ditentukan
dengan bantuan indikator khusus atau secara potensiometri.
4. Titrasi Oksidasi – Reduksi
Titrasi oksidasi – reduksi merupakan titrasi yang didasarkan pada proses
perpindahan elektron antara zat pengoksidasi dengan zat pereduksi. Zat
pengoksidasi dititrasi dengan larutan baku zat pereduksi kuat, misalnya
Na2S2O3,asam askorbat. Sebaliknya, zat pereduksi dititrasi dengan larutan baku
zat pengoksidasi kuat, misalnya KMnO4, KBrO3, K2Cr2O7. Titik akhir titrasi
potensiometri. Sedangkan pada titrasi iodometri (salah satu metode oksidasi
reduksi) digunakan larutan kanji sebagai indikator khusus (Rivai, 1995).
2.7 Angka Permanganat
Kalium Permanganat (KMnO4) telah lama dipakai sebagai oksidator pada penentuan konsumsi oksigen untuk mengoksidasi bahan organik, yang dikenal sebagai
parameter nilai permanganat atau sering disebut sebagai bahan organik total atau
TOM (Total Organic Matter). Akan tetapi, kemampuan oksidasi oleh permanganat
sangat bervariasi, tergantung pada senyawa-senyawa yang terkandung di dalam air
(Effendi, 2002).
Uji coba ini dengan cepat menunjukkan kebutuhan langsung oksigen yang di
sebabkan oleh zat-zat anorganik yang dioksidasi, seperti nitrit, sulfida, sulfit dan
sebagainya, maupun oleh zat-zat organik yang dapat dioksidasi dengan mudah. Uji
coba permanganat, yang dapat dikerjakan dengan cepat, dengan demikian, dapat
dipergunakan untuk memberikan gambaran kasar tentang BOD. Uji coba permanganat
selama empat jam merupakan uji coba kimia murni dan mengukur jumlah zat
pencemar yang dioksidasi secara kimiawi oleh potasium permangananat. Uji coba
permanganat menunjukkan jumlah yang sesungguhnya dari pada kotoran-kotoran
organik di dalam suatu contoh (Mahida, 1984).
2.8 Permanganometri
Permanganometri merupakan titrasi yang dilakukan berdasarkan reaksi oleh
kalium permanganat (KMnO4). Reaksi ini difokuskan pada reaksi oksidasi dan reduksi
yang terjadi antara KMnO4 dengan bahan baku tertentu. Titrasi dengan KMnO4 sudah
atas alat yang dapat dioksidasi seperti Fe2+, asam atau garam oksalat yang dapat larut
dan sebagainya. Beberapa ion logam yang tidak dioksidasi dapat dititrasi secara tidak
langsung dengan permanganometri seperti:
1. Ion-ion Ca, Ba, Sr, Pb, Zn, dan Hg (I) yang dapat diendapkan sebagai oksalat.
Setelah endapan disaring dan dicuci, dilarutkan dalam H2SO4 berlebih sehingga
terbentuk asam oksalat secara kuantitatif. Asam oksalat inilah yang akhirnya dititrasi
dan hasil titrasi dapat dihitung banyaknya ion logam yang bersangkutan.
2. Ion-ion Ba dan Pb dapat pula diendapkan sebagai garam kromat. Setelah disaring,
dicuci, dan dilarutkan dengan asam, ditambahkan pula larutan baku FeSO4 berlebih.
Sebagian Fe2+ dioksidasi oleh kromat tersebut dan sisanya dapat ditentukan
banyaknya dengan menitrasinya dengan KMnO4.
2.8.1 Oksidasi Dengan Kalium Permanganat
Zat pengoksidasi yang yang berharga dan sangat kuat ini paling mula
diperkenalkan dalam analisis titrimetri oleh F. Margueritte untuk titrasi besi (II),
dalam larutan-larutan asam, reduksi ini dapat dinyatakan dengan persamaan berikut :
MnO4- + 8H+ + 5e → Mn2+ + 4H2O
Sehingga ekuivalennya adalah seperlima mol, yaitu 158,03/5, atau 31,606. Potensial
standar dalam larutan asam menurut perhitungan adalah 1,51 volt, maka ion
permanganat dalam larutan asam adalah zat pengoksidasi yang kuat.
Asam sulfat adalah asam yang paling sesuai, karena tak bereaksi terhadap
permanganat dalam larutan encer. Dengan asam klorida, ada kemungkinan terjadi
reaksi :
2MnO4- + 10Cl- + 16H+→ 2Mn2+ + 5Cl2 + 8H2O
Kalium permanganat bukanlah suatu standar primer. Zat ini sukar diperoleh sempurna
mungkin mengandung zat-zat pereduksi (runutan bahan-bahan organik, dan
sebagainya), yang akan bereaksi dengan kalium permanganat itu dengan mangan
oksida. Adanya zat yang disebut diakhir ini sangatlah mengganggu, karena ia
mengkatalisis penguraian sendiri dari larutan permanganat setelah didiamkan. (Vogel, 1994)
2.8.2 Sumber Kesalahan Permanganometri
Sumber-sumber kesalahan pada titrasi permanganometri, antara lain terletak
pada larutan pentiter KMnO4 pada buret. Apabila percobaan dilakukan dalam waktu
yang lama, larutan KMnO4 pada buret yang terkena sinar akan terurai menjadi MnO2
sehingga pada titik akhir titrasi akan diperoleh pembentukan presipitasi coklat yang
seharusnya adalah larutan berwarna merah rosa. Pemberian KMnO4 yang terlalu cepat
pada larutan H2C2O4 yang telah ditambahkan H2SO4 dan telah dipanaskan cenderung
menyebabkan reaksi antara MnO4- dengan Mn2+ :
MnO4- + 3Mn2+ + 2H2O ↔ 5MnO2 + 4H+
Pemberian KMnO4 yang terlalu lambat pada larutan H2C2O4 yang telah ditambahkan
H2SO4 dan telah dipanaskan mungkin akan terjadi kehilangan oksalat karena
membentuk peroksida yang kemudian terurai menjadi air.
BAB 3
BAHAN DAN METODE
3.1 Alat dan Bahan
3.1.1 Alat
− Buret digital
− Pipet ukur 10 mL
− Gelas ukur 100 mL
− Labu Erlenmeyer 250 mL
− Hot plate
− Botol aquades
3.1.2 Bahan
− Akuades
− KMnO4 0,01 N
− H2SO4 8 N
− H2C2O4 0,01 N
− Air minum
− Air bersih
3.2 Penyediaan Sampel
Adapun sampel disediakan dari Laboratorium DINAS KESEHATAN Medan
3.3 Prosedur Air Bersih
− diukur 100 ml sampel
− ditambahkan 2-3 tetes KMnO4 0.01 N hingga berwarna merah muda
− ditambahkan 5 ml H2SO4 8 N
− dipanaskan hingga menguap
− ditambahkan 100 ml KMnO4 0.01 n
− dipanaskan kembali hingga mendidih selama tepat 10 menit
− ditambahkan 10 ml H2C2O4 0.01 N
− dititrasi dengan menggunakan larutan standart KMnO4 0.01 N
sampai terbentuk warna merah muda. − Dicatat volume KMnO4 yang terpakai.
Dengan cara yang sama dilakukan untuk air minum.
BAB 4
HASIL DAN PEMBAHASAN
4.1 Data Percobaan
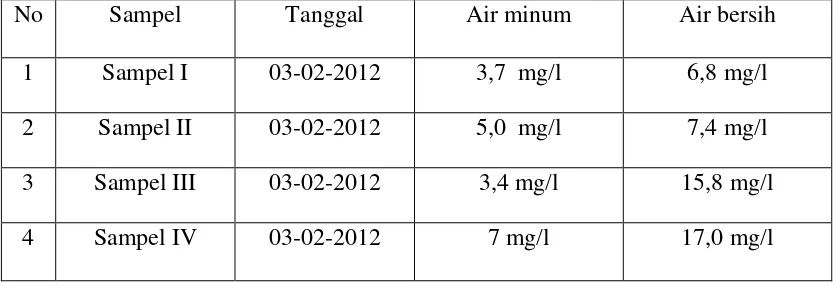
[image:39.595.107.527.278.421.2]Dari hasil analisis yang dilakukan diperoleh kadar angka permanganat dari air minum, dan air bersih di Balai Laboratorium Dinas Kesehatan Medan.
Tabel 4.1 Kadar Angka permanganat dari air minum dan air bersih
No Sampel Tanggal Air minum Air bersih
1 Sampel I 03-02-2012 3,7 mg/l 6,8 mg/l
2 Sampel II 03-02-2012 5,0 mg/l 7,4 mg/l
3 Sampel III 03-02-2012 3,4 mg/l 15,8 mg/l
4.2 Perhitungan
Penentuan kadar Angka Permanganat
KMnO4mg/l =
(10+a)b−cx31,6x1000
volumesampel x Fp
Dimana : a = Volume KMnO4 yang terpakai
b = Normalitas KMnO4
c = Normalitas asam oksalat
Fp= Faktor pengenceran
Untuk sampel air minum
Sampel I
KMnO4=
(10+1,2 )0,01−0,1x31,6x1000 100
= 0.012x31600
100 = 3,7 mg/l Sampel II
KMnO4=
(10+1,6 )0,01−0,1x31,6x1000 100
= 0.016x31600 100 = 5,0 mg/l Sampel III
KMnO4=
(10+1,1 )0,01−0,1x31,6x1000 100
Sampel IV
KMnO4=
(10+2,2 )0,01−0,1x31,6x1000 100
= 0.022x31600 100 = 7 mg/l
Untuk sampel air bersih
Sampel I
KMnO4=
(10+2,1 )0,01−0,1x31,6x1000 100
= 0.021x31600 100 = 6,8 mg/l Sampel II
KMnO4=
(10+2,4 )0,01−0,1x31,6x1000 100
= 0.024x31600 100 = 7,4 mg/l Sampel III
KMnO4=
(10+5 )0,01−0,1x31,6x1000 100
= 0.05x31600 100 = 15,8 mg/l
Sampel IV
KMnO4=
(10+5,4 )0,01−0,1x31,6x1000 100
4.3pembahasan
Analisa kadar permanganat pada air minum dan air bersih di Dinas Kesehatan Medan dilakukan secara titrimetri, yaitu berdasarkan titrasi redoks. Metode yang digunakan untuk menentukan kandungan zat organik yang terdapat pada air berdasarkan pembentukan warna merah muda pada titik akhir titrasi. Dimana zat organik pada air dioksidasi oleh kalium permanganat dalam 1000 ml air pada kondisi mendidih. Dari hasil analisis, diperoleh kadar Angka permanganat dari air minum yaitu pada sampel I sebesar 3,7 mg/l, sampel II = 5,0 mg/l, sampel III = 3,4 mg/l, sampel IV = 7 mg/l. Dan Kadar Angka Permanganat pada air bersih pada sampel I sebesar 6.8 mg/L, sampel II -= 7,4 mg/L, sampel III = 15,8 mg/L, sampel IV = 17,0 mg/L. Dapat ditunjukkan bahwa keempat sampel pada air minum dan air bersih pada sampel I dan sampel II masih layak di gunakan karena kadar angka permanganat pada air ini tidak melewati batas peraturan Menteri Kesehatan RI Nomor 416 / MENKES / PER IX / 1990. Sedangkan air bersih pada sampel III dan sampel IV tidak layak digunakan karena kadar angka permanganat pada air ini telah melewati batas
peraturan Menteri Kesehatan RI Nomor 416 / MENKES / PER IX / 1990 yaitu sebesar 10 mg/L.
BAB 5
KESIMPULAN DAN SARAN
5.1. KESIMPULAN
Dari analisis yang dilakukan kadar angka permanganat pada keempat sampel air minum dan dua sampel pada air bersih, yaitu pada sampel I dan sampel II tidak melewati baku mutu sedangkan kadar angka permanganat air bersih pada sampel III dan sampel IV telah melewati baku mutu menurut peraturan Menteri Kesehatan RI NO 416 / MENKES/ PER/ IX/ 1990 Tentang Standar kualitas Air Bersih.
5.2. SARAN
− Air minum dan air bersih yang akan digunakan sebaiknya diteliti kadar angka permanganatnya, karena jika kadar angka permanganat tinggi hal ini menunjukkan adanya pencemaran organik pada air tersbut.
DAFTAR PUSTAKA
Ardana. W. 2001. Dampak Pencemaran Lingkungan. Yogyakarta : Andi.
Depkes RI, 2006. Pedoman Pelaksanaan Penyelenggaraan Hygiene Sanitasi Depot Air Minum. Jakarta: Depkes RI.
Effendi. H. 2002. Telaah Kualitas Air. Jakarta : Kanisius.
Gabriel. J. F. 2001. Fisika Lingkungan. Cetakan I. Jakarta : Hipokrates.
http://id.wikipedia.org/wiki/Permanganometri.
Kusmayadi, A. 2008. Mengolah Air Bersih. Bogor: Regina.
Mahida, U. N. 1984. Pencemaran Air dan Pemanfaatan Limbah Industri. Cetakan I. Jakarta: C.V Rajawali.
Mukono,H.J. 2006.Prinsip Dasar Kesehatan Lingkungan Hidup. Edisi 2. Surabaya:Airlangga-press.
Mulia. R. 2005. Kesehatan Lingkungan. Yogyakarta : Penerbit Graha Ilmu.
Rivai, H. 1995. Asas Pemeriksaan Kimia. Cetakan Pertama. Jakarta: UI-press.
Slamet, J. (1994). Kesehatan Lingkungan. Bandung: Gadjah Mada University Press.
Suriawiria, U. 1993. Mikrobiologi Air. Cetakan pertama. Edisi Kedua. Bandung:
Alumni.
Suriawiria, U. 1995. Pengantar Mikrobiologi Umum. Bandung: Penerbit Angkasa.
Sutrisno, C.T. 2006. Teknologi Penyediaan Air bersih. Cetakan Keenam. Jakarta: Rineka Cipta.
Lampiran 1
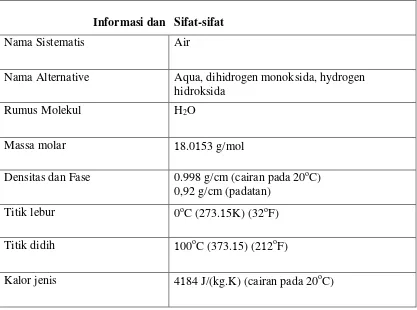
Sifat – sifat kimia fisika dari air adalah sebagai berikut:
Informasi dan Sifat-sifat
Nama Sistematis Air
Nama Alternative Aqua, dihidrogen monoksida, hydrogen
hidroksida
Rumus Molekul H2O
Massa molar 18.0153 g/mol
Densitas dan Fase 0.998 g/cm (cairan pada 20oC)
0,92 g/cm (padatan)
Titik lebur 0oC (273.15K) (32oF)
Titik didih 100oC (373.15) (212oF)
Kalor jenis 4184 J/(kg.K) (cairan pada 20oC)
[image:45.595.109.526.141.451.2]Kusmayadi (2008). Lampiran 2
Tabel Tentang Standar Kualitas Air Bersih Sifat Fisika
Parameter Satuan Kadar Maksimum
Yang Diperoleh
Keterangan
Bau − − Tidak Berbau
Jumlah Zat Padat Terlarut
mg/L 1000 −
Kekeruhan Skala NTU 5 −
Rasa − − Tidak Berbau
Suhu 0oC Suhu Udara 3oC −
Sifat Kimia a Kimia Anorganik
Parameter Satuan Kadar Maksimum
Yang Diperoleh
Keterangan
Air raksa mg/L 0.001
Arsen mg/L 0.05
Besi mg/L 1.0
Flourida mg/L 1.5
Kadmium mg/L 0.005
Kesadahan(CaCO3) mg/L 500
Klorida mg/L 600
Kromium, Valensi 6 mg/L 0.05
Mangan mg/L 0.5
Nitrat, sebagai N mg/L 10
Nitrit, sebagai N mg/L 1.0
pH mg/L 6.5-8.5
Selenium mg/L 0.01
Seng mg/L 15
Sianida mg/L 0.1
Sulfat mg/L 400
b Kimia Organik
Parameter Satuan Kadar Maksimum
Yang Diperoleh
Keterangan
Aldrin dan dieldrin mg/L 0.0007
Benzene mg/L 0.01
Benzo(a)pyrene mg/L
Cloroform (Total isomer)
mg/L 0.03
2,4-D mg/L
DDT mg/L 0.03
Detergen mg/L 0.5
1,2-Dichloroethene mg/L 0.01
1,1- Dichloroethene mg/L 0.0003
Heptachlor dan Heptavhlor Eposide
mg/L 0.003
Hexachlorobenzene mg/L 0.00001
Gamma-HCH (Lindane)
mg/L 0.004
Methoxychlor mg/L 0.1
Pentachloropenol mg/L 0.01
Pestisida Total mg/L 0.1
2,4,6-Tricloropenol mg/L 0.01
Zat Organik (KMnO4) mg/L 10
Cloroform (Total Isomer)
c Mikrobiologi
Parameter Satuan Kadar
Maksimum Yang Diperoleh
Keterangan
Total Coliform (MPN) Jumlah per
100 mL
0 Bukan Air Pipaan
Coliform Tinja Belum Diperiksa
Jumlah per 100 mL
0 Bukan Air Pipaan
Peraturan Menteri Kesehatan RI Tahun 1990 No 416/MENKES/PER/IX/1990.
Lampiran 3
Standard air minum menurut WHO:
1. Syarat Fisik a.Rasa b.Bau
c.Sisa zat padat d.Derajat kekeruhan e.Warna f.pH Tidak berasa Tidak berbau 500-1000 ppm
Tidak melebihi 5-15 unit (Turbidity Unit)
5-30 Unit (skala platina-Cobalt) 7-8,5 atau 6,5-9,5
2. Zat yang tidak mengganggu tetapi tidak boleh melebihibatas yang ditentukan Besi Mangan Seng Calsium Magnesium Sulfat Chlorida Nitrogen-Nitrat NO3
0,3-1,0 mg/L 0,1-0,3 mg/L 1,0-1,5 mg/L 75-200 mg/L 50-150 mg/L 200-500 mg/L 200-600 mg/L 0,001 mg/L
50 ppm