LAPORAN MINGGUAN
PRAKTIKUM KIMIA DASAR
REAKSI-REAKSI KIMIA
Oleh :
Nama
: Ernalia Rosita
NRP
: 133020175
Kelompok
: G
Meja
: 11 (Sebelas)
Tanggal Percobaan : 16 Oktober 2013
Asisten
: Vanidya Afsarah Permadi
LABORATORIUM KIMIA DASAR
JURUSAN TEKNOLOGI PANGAN
FAKULTAS TEKNIK
UNIVERSITAS PASUNDAN
BANDUNG
2013
ERNALIA ROSITA 133020175
Jurusan Teknologi Pangan, Fakultas Teknik, Universitas Pasundan
ABSTRAK
Reaksi merupakan salah satu cara untuk mengetahui sifat-sifat kimia dari satu atau berbagai jenis zat. Perubahan kimia disebut juga reaksi kimia. Ada beberapa hal yang menandai terjadinya reaksi kimia, diantaranya terjadi perubahan warna, bau, suhu, timbulnya gas dan endapan. Reaksi kimia ada yang berlangsung cepat, ada pula yang berlangsung lambang. Reaksi kimia yang berlangsung cepat misalnya meledaknya bom dan terbakarnya bensin sedangkan yang berlangsung lambat misalnya besi berkarat. Tujuan percobaan ini adalah untuk mengetahui dan mempelajari jenis dan sifat (sifat kimia atau fisika) dari zat yang direaksikan, serta untuk mencari rumus senyawa dengan cara mereaksikan dua buah zat atau lebih yang dibuktikan adanya perubahan warna, bau, suhu, timbulnya gas dan endapan. Prinsip dari percobaan ini adalah berdasarkan penggabungan molekul terbagi menjadi dua bagian atau lebih. Molekul yang kecil atau atom-atom dalam molekul. Reaksi kimia selalu melibatkan terbentuk dan terputusnya ikatan kimia. Berdasarkan Hukum Kekekalan Massa yang dikemukakan oleh Lavoisier: “Massa zat sebelum dan sesudah reaksi adalah sama” dan berdasarkan Hukum Perbandingan Tetap (Hukum Proust): “Dalam setiap persenyawaan perbandingan massa unsur-unsur selalu tetap”. Berdasarkan Bronsted Lowry: “Asam sebagai setiap zat sembarang yang menyumbang proton dan basa sebagai setiap zat sembarang yang menerima proton”.
Key words: Reaksi Kimia, Hukum Kekekalan Massa, Hukum Perbandingan Tetap, Bronsted Lowry. PENDAHULUAN
Reaksi merupakan salah satu cara untuk mengetahui sifat-sifat kimia dari satu atau berbagai jenis zat. Perubahan kimia disebut juga reaksi kimia. Ada beberapa hal yang menandai terjadinya reaksi kimia, diantaranya terjadi perubahan warna, bau, suhu, timbulnya gas dan endapan. Reaksi kimia ada yang berlangsung cepat, ada pula yang berlangsung lambang. Reaksi kimia yang berlangsung cepat misalnya meledaknya bom dan terbakarnya bensin sedangkan yang berlangsung lambat misalnya besi berkarat.
Tujuan percobaan ini adalah untuk mengetahui dan mempelajari jenis dan sifat (sifat kimia atau fisika) dari zat yang direaksikan, serta untuk mencari rumus senyawa dengan cara mereaksikan dua buah zat atau lebih yang dibuktikan adanya perubahan warna, bau, suhu, timbulnya gas dan endapan.
Prinsip dari percobaan ini adalah berdasarkan penggabungan molekul terbagi menjadi dua bagian atau lebih. Molekul yang kecil atau atom-atom dalam molekul. Reaksi kimia selalu melibatkan terbentuk dan terputusnya ikatan kimia. Berdasarkan Hukum Kekekalan Massa yang dikemukakan oleh Lavoisier: “Massa zat sebelum dan sesudah reaksi adalah sama” dan berdasarkan Hukum Perbandingan Tetap (Hukum Proust): “Dalam setiap persenyawaan perbandingan massa unsur-unsur selalu tetap”. Berdasarkan Bronsted Lowry: “Asam sebagai setiap zat sembarang yang menyumbang proton dan basa sebagai setiap zat sembarang yang menerima proton”.
METODOLOGI Bahan dan Alat
Bahan yang digunakan dalam percobaan reaksi kimia ini adalah: NaOH 0,05 M, 0,1 M dan 1 M, CH3COOH 0,05 M, HCl 0,1 M, K2CrO4 0,1 M, Al2(SO4)3
0,1 M, NH4OH 2 M, ZnSO4 0,1 M, (NH4)2SO4, Pb(NO3)2
0,1 M, NaCl 0,1 M dan 0,5 M, NH4OH 1 M, AgNO3 0,1
M, BaCl2 0,1 M, K2Cr2O7 0,1 M, CaCO3, Ba(OH)2,
H2C2O4, H2SO4, KMnO4 0,05 M, Larutan Fe2+ dan Fe3+,
CuSO4 0,05 M, KSCN 0,1 M, Na3PO4, indikator
phenolphthalein, indikator metil merah, dan kertas lakmus merah. Sedangkan alat-alat yang digunakan untuk melakukan percobaan reaksi kimia adalah tabung reaksi, pipet, rak tabung, pipa U, penjepit tabung reaksi, dan pembakar bunsen.
Metode Percobaan 1. a. NaOH 0,05 M + 1 tetes phenolphthalein (PP) b. NaOH 0,05 M + 1 tetes metil merah (MM)
c. HCl 0,1 M + 1 tetes phenolphthalein (PP) d. HCl 0,1 M + 1 tetes metil merah (MM) 2. a. CH3COOH 0,05 M + 1 tetes phenolphthalein (PP) b. CH3COOH 0,05 M + 1
tetes metil merah (MM) c.
NaOH 1 M + 1 tetes phenolphthalein (PP) d.
NaOH 1 M + 1 tetes metil merah (MM) 3. a. + NaOH 0,05 M (pp) HCl 0,1 M (pp) b. + NaOH 0,05 M (mm) HCl 0,1 M (mm) c. + NaOH 0,05 M (pp) CH3COOH 0,05 M (pp) d. + NaOH 0,05 M (mm) CH3COOH 0,05 M (mm) 4. a. + K2CrO4 0,1 M HCl 0,1 M b. + K2CrO4 0,1 M NaOH 0,1 M 5. a. + K2C2O7 0,1 M HCl 0,1 M b. + K2C2O7 0,1 M NaOH 0,1 M 6. Al2(SO4)3 0,1 M + 1 tetes NaOH 1 M 7. Al2(SO4)3 0,1 M + 1 tetes
NaOH 1 M + tetes demi tetes NH4OH 2 M 8. a. ZnSO4 0,1 M + 5 tetes NaOH 1 M b. ZnSO4 0,1 M + 5 tetes
NaOH 1 M + tetes demi tetes NH4OH 1 M 9. Tabung pertama: (NH4)2SO4 + NaOH 0,05 M Tabung kedua: Tabung Merah 10. Pb(NO3)2 0,1 M+NaCl 0,1 M
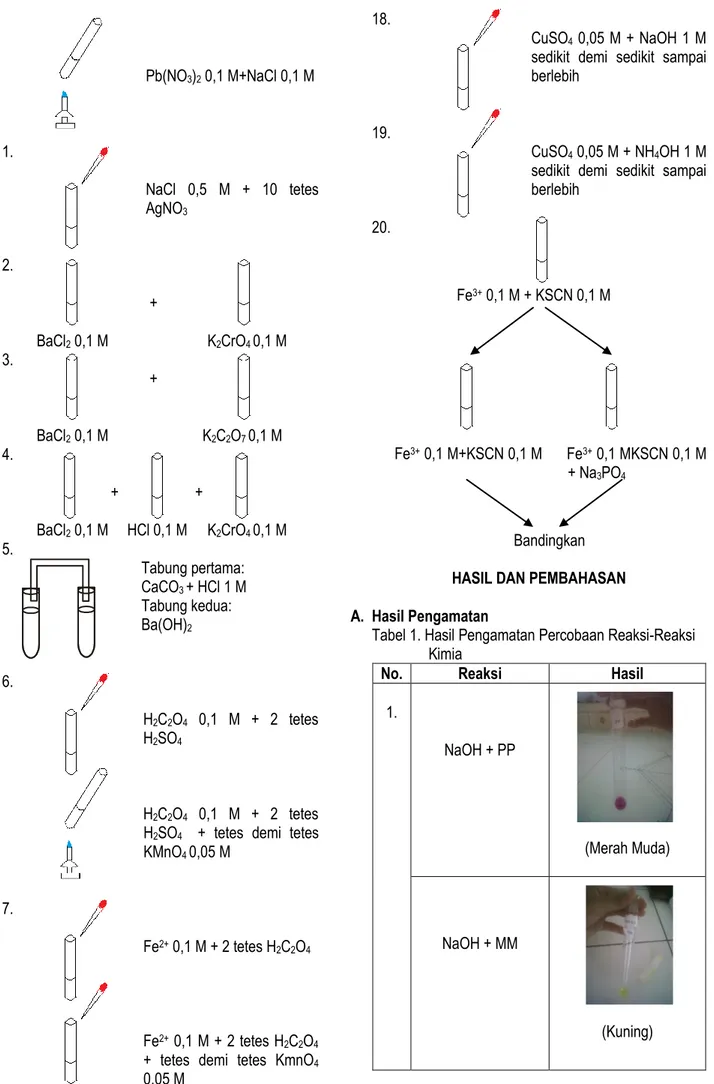
Pb(NO3)2 0,1 M+NaCl 0,1 M 11. NaCl 0,5 M + 10 tetes AgNO3 12. + BaCl2 0,1 M K2CrO4 0,1 M 13. + BaCl2 0,1 M K2C2O7 0,1 M 14. + + BaCl2 0,1 M HCl 0,1 M K2CrO4 0,1 M 15. Tabung pertama: CaCO3 + HCl 1 M Tabung kedua: Ba(OH)2 16. H2C2O4 0,1 M + 2 tetes H2SO4 H2C2O4 0,1 M + 2 tetes
H2SO4 + tetes demi tetes
KMnO4 0,05 M
17.
Fe2+ 0,1 M + 2 tetes H2C2O4
Fe2+ 0,1 M + 2 tetes H2C2O4
+ tetes demi tetes KmnO4
0,05 M
CuSO4 0,05 M + NaOH 1 M
sedikit demi sedikit sampai berlebih
19.
CuSO4 0,05 M + NH4OH 1 M
sedikit demi sedikit sampai berlebih 20. Fe3+ 0,1 M + KSCN 0,1 M Fe3+ 0,1 M+KSCN 0,1 M Fe3+ 0,1 MKSCN 0,1 M + Na3PO4 Bandingkan
HASIL DAN PEMBAHASAN A. Hasil Pengamatan
Tabel 1. Hasil Pengamatan Percobaan Reaksi-Reaksi Kimia
No. Reaksi Hasil
1.
NaOH + PP
(Merah Muda)
NaOH + MM
HCl + PP (Bening) HCl + MM (Merah Muda) 3. NaOH(pp) + HCl(pp) (Bening) NaOH(mm) + HCl(mm) (Merah Muda) 5. K2Cr2O7 + HCl (Kuning Keemasan) K2Cr2O7 + NaOH (Kuning Cerah) 7. Al2(SO4)3 + NaOH +NH4OH
(Putih keruh dan ada endapan putih) 9.
(NH4)2SO4 + NaOH Lakmus Merah
(Larutan tetap bening dan lakmus menjadi
biru) 11.
NaCl + AgNO3
(Putih dan ada endapan putih) 13.
BaCl2 + K2Cr2O7
(Kuning tua dan endapan kuning muda) 15.
CaCO3 + HCl
Ba(OH)2
(Ada gelembung gas dan tabung menjadi
17.
Fe2++ H2C2O4 +
KMnO4
(Coklat tua dan ada endapan coklat
kekuningan) 19.
CuSO4 + NH4OH
(Biru dan ada endapan biru)
(Sumber: Ernalia Rosita, 133020175, Meja 11, Kelompok G, 2013)
B. Pembahasan
Berdasarkan hasil praktikum reaksi-reaksi kimia diperoleh bahwa larutan NaOH jika ditambah phenolphthalein (PP) menjadi warna merah muda dan jika ditambah Metil Merah (MM) menjadi warna kuning.
Larutan HCl dan CH3COOH jika ditambah
phenolphthalein (PP) menjadi warna bening dan jika ditambah Metil Merah (MM) menjadi warna merah muda. Larutan NaOH(pp) ditambah HCl(pp) dengan reaksi
NaOH(pp) + HCl(pp) → NaCl + H2O menjadi warna
bening sedangkan jika NaOH(mm) ditambah HCl(mm)
dengan reaksi NaOH(mm) + HCl(mm) → NaCl + H2O
menjadi warna merah, larutan NaOH(pp) ditambah
CH3COOH(pp) dengan reaksi NaOH(pp) + CH3COOH(pp
→ CH3COONa + H2O menjadi warna kuning
sedangkan NaOH(mm) ditambah CH3COOH(mm) dengan
reaksi NaOH(mm) + CH3COOH(mm) → CH3COONa +
H2O menjadi warna merah. Larutan K2CrO4 ditambah
HCl dengan reaksi K2CrO4 + HCl → 2KCl + H2CrO4
menjadi warna kuning keemasan sedangkan jika K2CrO4 ditambah NaOH dengan reaksi K2CrO4 + NaOH
→ 2KOH + Na2CrO4 menjadi warna kuning cerah.
Larutan K2Cr2O7 ditambah HCl dengan reaksi K2Cr2O7 +
HCl → 2KCl + H2Cr2O7 menjadi warna kuning
keemasan sedangkan jika K2Cr2O7 ditambah NaOH
dengan reaksi K2Cr2O7 + NaOH → 2KOH + Na2Cr2O7
menjadi warna kuning cerah. Larutan Al2(SO4)3
ditambah NaOH dengan reaksi Al2(SO4)3+NaOH →
2Al(OH)3 + 3Na2SO4 menjadi warna putih keruh.
Larutan Al2(SO4)3 + NaOH ditambah NH4OH dengan
2Al(OH)3 + NaOHmenjadi warna putih keruh dan ada
endapan putih. Larutan ZnSO4 ditambah NaOH dengan
reaksi ZnSO4 + NaOH → Zn(OH)2 + Na2SO4 menjadi
warna putih keruh sedangkan jika ZnSO4 + NaOH
ditambah NH4OH dengan reaksi ZnSO4 + NaOH +
2NH4OH → (NH4)2SO4 + Zn(OH)2 + NaOH menjadi
warna putih keruh dan ada endapan putih. Larutan (NH4)2SO4 + NaOH pada tabung pertama dengan
reaksi (NH4)2SO4 + 2NaOH → NH3 + H2O +
Na2SO4 dan juga lakmus merah di tabung kedua
hasilnya lakmus di tabung kedua berubah menjadi lakmus biru dan larutan tetap bening. Larutan Pb(NO3)2
ditambah NaCl dengan Pb(NO3)2 + 2NaCl →
PbCl2 + 2Na2NO3 menjadi warna bening dan
bergelembung. Larutan NaCl ditambah AgNO3 dengan
reaksi NaCl + AgNO3 → AgCl + NaNO3 menjadi warna
putih dan ada endapan putih. Larutan BaCl2 ditambah
K2CrO4 dengan reaksi BaCl2 + K2CrO4 → BaCrO4 +
2KCl menjadi warna kuning susu. Larutan BaCl2
ditambah K2Cr2O7 dengan reaksi BaCl2 + K2CrO7 →
BaCr2O7 + 2KCl menjadi warna kuning tua dan ada
endapan. Serbuk CaCO3 ditambah HCl di tabung
pertama dan Ba(OH)2 di tabung kedua dengan
persamaan reaksi CaCO3 + 2HCl + Ba(OH)2 →
Ca(OH)2 + BaCl2 + H2CO3 menjadi panas dan terdapat
gelembung gas. Larutan H2C2O4 + H2SO4 ditambah
KMnO4 dengan reaksi H2C2O4 + H2SO4 + KMnO4 →
K2C2O4 + HMnO4 menjadi warna bening. Larutan Fe2+
+ H2SO4 ditambah KMnO4 dengan reaksi Fe2+ + H2SO4
+ KMnO4 → Fe2+ + K2SO4 + HMnO4 menjadi warna
orange. Larutan CuSO4 ditambah NaOH dengan reaksi
CuSO4 + NaOH → Cu(OH)2 + Na2SO4 menjadi warna
biru dan ada endapan berwarna hijau lumut. Larutan CuSO4 ditambah NH4OH dengan reaksi CuSO4 +
NH4OH →Cu(OH)2 + (NH4)2SO4 menjadi warna bening
dan ada endapan biru. Terakhir, larutan Fe3+ ditambah
KSCN dengan reaksi Fe3+ + KSCN → Fe(SCN)3 + K+
menjadi warna merah darah sedangkan jika Fe3+ +
KSCN + Na3PO4 → FePO4 + NaSCN + K+ menjadi
warna coklat.
Dari hasil percobaan diatas, larutan 1, 2, 3, 4, 5, 9 dapat dikelompokan sebagai reaksi asam-basa, larutan 6, 7, 8, 11, 12, 13, 18, 19 dikelompokan sebagai reaksi pengendapan. Reaksi pembentukan gas terdapat pada nomor 10 dan 15. Reaksi kompleksometri terdapat pada nomor 4, 5, 6, 7, 8, 10, 11, 12, dan 13. Reaksi pertukaran ganda terdapat pada nomor 4, 5, 6, dan 7. Reaksi redoks terdapat pada nomor 10, 11, 12, 15, 16, 18, dan 19. Reaksi sintesis terdapat pada nomor 12 sampai 20.
Reaksi kimia merupakan salah satu cara untuk mengetahui sifat-sifat kimia dari suatu zat. Reaksi kimia terdiri dari berbagai jenis, diantaranya:
1. Sintesis
Dalam reaksi kombinasi langsung atau sintesis, dua atau lebih senyawa sederhana bergabung membentuk senyawa baru yang lebih kompleks. Dua reaktan atau lebih yang bereaksi menghasilkan satu produk juga merupakan salah satu cara untuk mengetahui kalau itu reaksi sintesis. Contoh dari reaksi ini adalah gas hidrogen bergabung dengan gas oksigen yang hasilnya adalah air :
2 H2 + O2 → 2 H2O
2. Dekomposisi
Reaksi dekomposisi atau analisis adalah kebalikan dari reaksi sintesis. Sebuah senyawa yang lebih kompleks akan dipecah menjadi senyawa yang lebih sederhana. Contohnya adalah molekul air yang dipecah menjadi gas oksigen dan gas hidrogen, dengan persamaan reaksi:
2 H2O → 2 H2 + O2
3. Penggantian Tunggal
Dalam reaksi penggantian tunggal atau substitusi sebuah elemen tunggal menggantikan elemen tunggal lainnya di suatu senyawa. Contohnya adalah logam natrium yang bereaksi dengan asam klorida akan menghasilkan natrium klorida atau garam dapur, dengan persamaaan reaksi:
2 Na(s) + 2 HCl(aq) → 2 NaCl(aq) + H2(g)
4. Penggantian Ganda
Dalam reaksi penggantian ganda, dua senyawa saling berganti ion atau ikatan untuk membentuk senyawa baru yang berbeda. Hal ini terjadi ketika kation dan anion dari 2 senyawa yang berbeda saling berpindah tempat, dan membentuk 2 senyawa baru.
Contoh dari reaksi penggantian ganda adalah timbal(II) nitrat bereaksi dengan kalium iodida untuk membentuk timbal(II) iodida dan kalium nitrat, dengan persamaan reaksi:
Pb(NO3)2 + 2 KI → PbI2 + 2 KNO3
5. Oksidasi dan Reduksi (Redoks)
Reaksi redoks dapat dipahami sebagai transfer elektron dari salah satu senyawa
(disebut reduktor) ke senyawa lainnya
(disebut oksidator). Contoh reaksi redoks adalah: S2O32−(aq) + I2(aq) → S4O62−(aq) + 2 I−(aq)
6. Reaksi Asam-Basa (Netralisasi)
Reaksi asam basa adalah reaksi yang mendonorkan proton dari sebuah molekul asam ke molekul basa. Disini asam berperan sebagao akseptor proton. Reaksi asam basa, HA: asam, B: Basa, A–: basa konjugasi, HB+: asam konjugasi.
Contohnya:
HCl + H2O → H3O+ + Cl-
7. Reaksi Pengendapan
Reaksi pengendapan adalah reaksi antara zat-zat atau ion logam yang sukar larut dalam air, sehingga terbentuklah endapan.
Contohnya pada reaksi antara AgNO3 dengan NaCl menyebabkan semua ion pemisah tidak dihilangkan. Endapan hasil reaksi disebut juga presipitat.
NaCl + AgNO3 AgCl + NaNO3 Adapun tanda-tanda terjadinya reaksi kimia. Tanda-tanda atau indikator terjadinya reaksi kimia adalah sebagai berikut:
1. Terjadinya perubahan suhu atau perubahan panas.
Reaksi kimia terkadang ditandai dengan adanya perubahan suhu. Suhu yang terjadi bisa menjadi lebih tinggi atau lebih rendah. Reaksi kimia yang disertai dengan kenaikan suhu disebut eksoterm sedangkan reaksi kimia yang disertai penurunan suhu disebut endoterm.
2. Terjadinya perubahan warna
Reaksi kimia terkadang ditandai dengan perubahan warna. Perubahan warna bsa diamati secara langsung dengan mudah.
3. Terbentuknya endapan
Reaksi kimia terkadang ditandai dengan pembentukan endapan. Seperti halnya perubahan warna, pembentukan endapan dapat diamati secara langsung dengan mudah.
4. Terbentuknya gas
Pembentukan gas biasanya menunjukan bahwa reaksi sedang berlangsung. Reaksi pembentukan gas ditandai dengan adanya gelembung-gelembung udara, atau bau yang tercium ataupun tampak asap keluar dari sebuah reaksi dan mengembangnya suatu reaktan.
Pada saat mengamati reaksi kimia yang terjadi pada suatu zat, praktikan dianjurkan untuk mengetahui hal-hal yang dapat mempengaruhi laju reaksi. Berikut adalah hal-hal yang mempengaruhi laju reaksi:
1. Luas Permukaan
Luas permukaan dalam reaksi kimia adalah luas permukaan zat-zat pereaksi yang bersentuhan untuk menghasilkan reaksi. Dalam reaksi kimia, tidak semua luas permukaan zat yang bereaksi dapat bersentuhan hingga terjadi reaksi, hal ini bergantung pada bentuk partikel zat-zat yang bereaksi. Suatu reaksi dapat saja melibatkan pereaksi dalam bentuk padatan. Luas permukaan zat ini akan berkaitan dengan bidang sentuh zat tersebut.
2. Konsentrasi Larutan
Jika konsentrasi suatu larutan makin besar, larutan akan mengandung jumlah partikel semakin banyak sehingga partikel-partikel tersebut akan
konsentrasinya lebih rendah. Susunan partikel yang lebih rapat memungkinkan terjadinya tumbukan semakin banyak dan kemungkinan terjadi reaksi lebih besar. Makin besar konsentrasi zat, makin cepat laju reaksinya.
3. Suhu
Partikel-partikel dalam zat selalu bergerak. Jika suhu zat dinaikkan, maka energi kinetik partikel-partikel akan bertambah sehingga tumbukan antar partikel akan mempunyai energi yang cukup untuk melampaui energi pengaktifan. Hal ini akan menyebabkan lebih banyak terjadi tumbukan yang efektif dan menghasilkan reaksi. Di samping memperbesar energi kinetik, ternyata peningkatan suhu juga meningkatkan energi potensial suatu zat. Dengan semakin besarnya energi potensial zat, maka semakin besar terjadinya tumbukan yang efektif, sehingga laju reaksi semakin cepat.
4. Katalis
Katalis adalah zat yang pada umumnya ditambahkan dalam ke dalam suatu sistem reaksi untuk mempercepat reaksi. Pada akhir reaksi, katalis diperoleh kembali dalam bentuk zat semula. Katalis bekerja dengan cara turut terlibat dalam setiap tahap reaksi, tetapi pada akhir tahap, katalis terbentuk kembali. Jika suatu campuran zat tidak dapat bereaksi, penambahan katalis pun tidak akan membuat reaksi terjadi. Dengan kata lain, katalis tidak dapat memicu reaksi, tetapi hanya membantu reaksi yang berlangsung lambat menjadi lebih cepat. Katalis bekerja secara khusus. Artinya, tidak semua reaksi dapat dipercepat dengan satu macam katalis. Dengan kata lain, katalis bekerja hanya pada satu atau dua macam reaksi, tetapi untuk reaksi yang lain tidak dapat digunakan.
Ada beberapa faktor kesalahan yang dapat terjadi pada saat percobaan dalam praktikum berlangsung. Faktor-faktor kesalahan yang dapat terjadi pada saat praktikum berlangsung diantaranya:
1. Faktor Ketelitian
Kesalahan yang sering terjadi pada saat melakukan percobaan adalah kekurang telitian praktikan dalam mengamati reaksi kimia yang terjadi pada zat yang direaksikan seperti terbentuknya gas, endapan atau perubahan suhu dan warna. praktikan harus lebih teliti dalam melakukan pengamatan agar tidak terjadi kesalahan pada hasil pengamatan.
2. Faktor Kebersihan
Kebersihan alat-alat yang digunakan pada saat praktikum dapat mempengaruhi hasil pengamatan dari zat yang sedang diamati. Alat-alat yang kurang bersih dapat mempengaruhi atau merubah reaksi yang sedang dilakukan. Oleh
alat-alat yang dipakai pada saat praktikum sudah benar-benar bersih.
3. Faktor Lingkungan
Faktor lingkungan seperti tinggi rendahnya suhu ruangan dapat mempengaruhi proses reaksi kimia. Oleh sebab itu, praktikan harus melakukan pengamatan di tempat dengan suhu yang pas agar pengamatan yang dilakukan berjalan dengan lancar tanpa kesalahan.
Dalam pengamatan reaksi asam dan basa, digunakan indikator phenolphthalein atau biasa disebut PP dan metil merah atau MM. Indikator phenolphthalein adalah indikator yang digunakan untuk mengetahui konsentrasi asam atau basa yang tidak diketahui berdasarkan reaksi dengan asam atau basa yang telah diketahui konsentrasinya. Indikator phenolphthalein mempunyai sifat: jika diteteskan pada larutan asam, larutan tidak akan menghasilkan perubahan warna (larutan tetap jernih), sebaliknya, jika diteteskan pada larutan basa, larutan akan berubah warna menjadi warna merah muda. Indikator metil merah atau MM adalah senyawa organik yang memiliki rumus kimia C15H15N3O2 yang banyak dipakai pada titrasi asam
basa. Indikator ini mempunyai sifat: jika dalam lingkungan asam akan berwarna merah, sedangkan jika dalam lingkungan basa akan berwarna kuning.
Aplikasi di bidang pangan dari reaksi-reaksi kimia adalah pada fermentasi tempe, proses pengendapan tahu, pembakaran gula/glukosa, fotosintesis pada tumbuhan untuk menghasilkan oksigen dan glukosa, proses pembuatan garam, proses respirasi dan inspirasi, proses pembuatan kecap, dll.
KESIMPULAN
Berdasarkan hasil pengamatan dari reaksi kimia dapat disimpulkan bahwa apabila suatu zat direaksikan dengan zat lain, maka akan diperoleh zat baru dengan ciri-ciri perubahan warna, suhu, timbulnya endapan dan munculnya gas dan bau. Untuk meminimalisir tingkat kesalahan dan perbedaan mengenai hasil, praktikan harus lebih teliti dalam melakukan percobaan.
DAFTAR PUSTAKA
Anonim. 2013. Reaksi Kimia. http://mafia.mafiaol.com Diakses: 19 Oktober 2013.
Chang, R. 2004. Kimia Dasar Konsep-Konsep Inti. Erlangga: Jakarta.
Septiarini, Dina. 2012. Perhitungan pH Larutan dengan Indikator. http://dinaseptember.blogspot.com. Diakses: 20 Oktober 2013.
Sutrisno, E. T. dan Nurminabari, I. S. 2013. Penuntun Praktikum Kimia Dasar. Universitas Pasundan, Bandung.