1
ANALISIS PARASETAMOL DAN PROPIFENAZON SECARA SPEKTROFOTOMETRI UV DAN KEMOMETRIKA
TANPA TAHAP PEMISAHAN
I MADE MUDIARCANA, ABDUL ROHMAN, FLORENTINUS DIKA, O. R FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
YOGYAKARTA INTISARI
Kontrol kualitas sediaan farmasi merupakan suatu keharusan untuk menjamin mutu sediaan farmasi. Kontrol kualitas sediaan farmasi biasanya dilakukan dengan metode spektrofotometri dan kromatografi. Akan tetapi metode analisis spektrofotometri untuk analisis senyawa campuran secara simultan memiliki keterbatasan karena adanya overlapping spektra senyawa. Dengan bantuan kemometrika, masalah overlapping pada metode spektrofotometri dalam analisis senyawa campuran parasetamol (PCT) dan propifenazon (PPZ) dapat teratasi.
Analisis sediaan farmasi dengan metode spektrofotometri yang dikombinasikan dengan kemometrika memanfaatkan suatu model kalibrasi multivariat partial least square (PLS) yang divalidasi dari nilai koefisien determinasi (R2) dan kesalahan pemodelan (RMSE, root mean square error) dan kesalahan prediksi (PRESS, predicted residual error sum of square).
Diperoleh model kalibrasi PLS dengan nilai R2 PCT 0,9999 dan PPZ 0,9999. Nilai RMSEC sebesar 0,0043µg/mL untuk PCT dan 0,0031 µg/mL untuk PPZ, nilai R2 dan RMSEC tersebut menunjukkan kemampuan prediksi model yang tinggi. Pada proses validasi internal diperoleh nilai R2 PCT 0,9955 dan PPZ 0,9912 dengan nilai RMSECV untuk PCT 0,1027 µg/mL dan PPZ 0,0782 µg/mL. Nilai PRESS untuk PCT 0,2112 dan PPZ 0,1225. Pada proses validasi eksternal diperoleh nilai R2 PCT sebesar 0,9922 dan PPZ 0,9886 dengan nilai RMSECP PCT 0,3813 dan PPZ 0,2509. Nilai kadar rata-rata yang diperoleh dari tahap penetapan kadar untuk PCT dan PPZ adalah sebesar 299,861 mg/mg dan 197,95? mg/mg, dengan persentase kedekatan kadar sebesar 99,95% dan 98,96%.Metode analisis spektrofotometri UV-PLS merupakan metode yang valid dan dapat digunakan untuk menetapkan kadar senyawa campuran parasetamol dan propifenazon dalam sediaan tablet.
2
ANALISIS PARASETAMOL DAN PROPIFENAZON SECARA SPEKTROFOTOMETRI UV DAN KEMOMETRIKA
TANPA TAHAP PEMISAHAN
I MADE MUDIARCANA, ABDUL ROHMAN, FLORENTINUS DIKA, O. R FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
YOGYAKARTA ABSTRACT
Quality control of pharmaceutical dosage was a must. Quality control of pharmaceutical dosage usually done by spectrophotometric and chromatographic methods. Spectrophotometric analysis method for simultaneous analysis of mixtures compound has limitations because of the overlapping spectra. A mixture of paracetamol (PCT) and prophyphenazon (PPZ) has overlapping spectra. With the aid of chemometrics, overlapping problems that encountered by the spectrophotometric method can be resolved.
Analysis of pharmaceutical dosage by spectrophotometric method combined with chemometrics utilizing a calibration model multivariate partial least square (PLS) were validated from the coefficient of determination (R2) and modeling errors (RMSE, root mean square error) and the prediction error (PRESS, predicted residual sum of square error).
PLS calibration model was shown good with high predictive ability, which shown by the value of R2 for both PCT and PPZ was 0.9999. The RMSEC value of PCT 0.0043% and PPZ 0.0031%. In the internal validation process R2 values of PCT was 0,9958 and for PPZ was 0.9946. The RMSECV values of PCT was 0.1027 and 0.0782 for PPZ. PRESS value of the PCT and PPZ was 0.2112 and 0.1225 respectively. In the external validation process R2 values of PCT was 0.9922 and for PPZ was 0.9986, the RMSECP value of PCT and PPZ was 0,3813 and 0,2509 respectively. PCT and PPZ assay was successfully performed by the percentage recovery range for PCT was 99.95% and for PPZ was 98.96%. Spectrophotometric UV-PLS analysis methods was a valid method than can be used for analyzing mixture compound of paracetamol and propifenazon in pharmaceutical tablet dosage.
ANALISIS PARASETAMOL DAN PROPIFENAZON SECARA SPEKTROFOTOMETRI UV DAN KEMOMETRIKA
TANPA TAHAP PEMISAHAN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana (S.Farm.)
Program Studi Farmasi
Oleh : I Made Mudiarcana
NIM : 118114182
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
ANALISIS PARASETAMOL DAN PROPIFENAZON SECARA SPEKTROFOTOMETRI UV DAN KEMOMETRIKA
TANPA TAHAP PEMISAHAN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana (S.Farm.)
Program Studi Farmasi
Oleh : I Made Mudiarcana
NIM : 118114182
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
“Ananyas cintayanto mam ye janan paryupasate
Tesam nityambhiyuktanam yoga-ksemam vahamu aham”
Orang yang selalu menyembah-Ku dengan bhakti tanpa tujuan lain dan bersemedipada bentuk rohani-Ku, Aku akan bawakan apa yang dibutuhkannya, dan Aku memelihara apa yang dimilikinya (Bhagawaghita, Sloka 9.22)
“Life is a journey, not a destination”– Ralp Waldo Emerson
“Those who are given more in life must not cling to it but risk it all at every
moment.”– Huskar, Sacred Warrior.
“I wonder what awaits me at the end of everything.”– Lone Druid
Sebuah karya yang kupersembahkan kepada…
vii PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan atas segala anugerah dan penyertaan-Nya yang begitu besar kepada penulis selama proses penelitian dan penyusunan naskah skripsi ini.
Skripsi berjudul “Analisis Parasetamol dan Propifenazon Secara Spektrofotometri UV dan Kemometri Tanpa Tahap Pemisahan” ini disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S.Farm.) Program Studi Ilmu Farmasi Universitas Sanata Dharma.
Selama proses penelitian dan penyusunan naskah ini, tidak terlepas dari dukungan banyak pihak yang telah memberikan dukungan, semangat, kritik dan sarannya kepada penulis, maka pada kesempatan kali ini, penulis mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Aris Widayati, M.Si., Ph.D., Apt., selaku Dekan Fakultas Famasi Universitas Sanata Dharma.
2. Prof. Dr. Abdul Rohman, M.Si., Apt., selaku dosen pembimbing yang dengan penuh kesabaran memberikan informasi, pengarahan, masukan, dukungan, semangat, kritik dan saran, serta waktu dan tenaga untuk membimbing penulis selama proses penelitian maupun penyusunan naskah ini.
3. Florentinus Dika Octa Riswanto, M.Si., selaku dosen pembimbing pendamping yang dengan penuh kesabaran memberikan masukan, pengarahan, dukungan, semangat, kritik dan saran selama penelitian maupun penyusunan naskah ini. 4. Dr. Christine Patramurti, M.Si., Apt., dan Jeffry Julianus, M.Si., Selaku dosen
penguji yang dengan penuh kesabaran memberikan masukan, pengarahan, kritik dan saran yang sangat membantu kemajuan naskah ini.
5. Yohanes Dwiatmaka, M.Si., selaku Dosen Pembimbing Akademik yang telah membantu penulis selama proses perkuliahan.
6. Agustina Setiawati, M.Sc., Apt., selaku Kepala Laboratorium Fakultas Farmasi Universitas Sanata Dharma.
viii
8. Seluruh dosen dan karyawan Fakultas Farmasi Universitas Sanata Dharma yang telah memberikan ilmu, bimbingan, pengarahan, pengalaman, dan masukan selama perkuliahan.
9. Mas Bimo, Mas Kethul, dan Mas Ottok selaku Laboran, Karyawan Laboratorium Kimia Analisis Instrumental, dan Pengelola Gudang Laboratorium yang telah banyak memberikan bantuan dan kemudahan waktu kepada penulis selama proses penelitian.
10.Orang tuaku yang sangat kuhormati I Ketut Artana dan Ni Wayan Windri yang tak pernah berhenti mendoakan, mendukung baik dalam moral dan material serta memberi semangat sampai akhirnya skripsi ini selesai.
11.Arif, Jalaq, dan Erfan sebagai sahabat dan rekan kerja yang telah menyediakan waktu dan tenaga untuk memberikan semangat, bantuan, dukungan, kritik dan saran dalam pengumpulan data dan penyusunan tugas akhir serta diskusi panjang tentang hal – hal yang menyenangkan.
12.Devina dan Ophi sebagai rekan kerja yang telah sepenuh hati membantu memberikan bantuan, dukungan, kritik dan saran dalam hal penyusunan tugas akhir.
13.Teman-teman FST B 2011 dan seluruh teman-teman angkatan 2011 atas kebersamaan yang telah kita lalui bersama.
14.Rekan, kerabat, dan sahabat yang telah membantu penulis selama proses penelitian dan penyusunan naskah ini, baik secara langsung maupun tidak, yang tidak dapat penulis sebutkan satu per satu.
Akhir kata, penulis berharap semoga skripsi ini dapat bermanfaat bagi pembaca dan bagi pengembangan ilmu pengetahuan, serta dapat menjadi acuan bagi penelitian-penelitian selanjutnya.
Yogyakarta, 30 November 2015
ix DAFTAR ISI
HALAMAN JUDUL ……….………..… i
HALAMAN PERSETUJUAN ……….…...….…... ii
HALAMAN PENGESAHAN………... iii
HALAMAN PERSEMBAHAN ……….……. iv
PERNYATAAN KEASLIAN KARYA ………...…. v
LEMBAR PERNYATAAN PUBLIKASI ……….. vi PRAKATA ………...……...…..………. vii
DAFTAR ISI ………...…...…………..…... ix
DAFTAR TABEL ………...……….……. x
DAFTAR GAMBAR ………..………...……… xii DAFTAR LAMPIRAN ………...………...…...……. xvi
INTISARI ………...…….………..……….……….. xviii
ABSTRACT ……….……..……….……... xix
BAB I. PENGANTAR ………..……….………..…… 1
A. Latar Belakang ………...……….………...…… 1
1. Rumusan Masalah ………....………… 2
2. Keaslian Penelitian ……….…..………...…… 3
3. Manfaat Penelitian ………..………..……….. 4
B. Tujuan Penelitian ………..……… 4
BAB II. PENELAAHAN PUSTAKA ………..………..… 6
A. Karakteristik Senyawa ……….……….…….…...……. 6
x
2. Propifenazon ……….……….…....….…...….. 7
B. Spektrofotometri Ultraviolet ………...……. 8
C. Kemometrika ………...…….. 12
D. Validasi Metode Analisis ……….………...………..….……..…… 16
1. Validasi Metode Kalibrasi Multivariat ………..….…....…. 16
2. Parameter Validasi Metode Analisis Multivariat …………..…….……. 18
a. Presisi ………...……….……....……. 18
b. Akurasi ………..……….……….……. 19
E. Landasan Teori ………...………...…………. 20
F. Hipotesis ………...………...……….…… 21
BAB III. METODOLOGI PENELITIAN ……….………...…..…. 22
A. Jenis dan Rancangan Penelitian ………...………..……. 22
B. Variabel Penelitian ………...……….……..… 22 1. Variabel Bebas ………..………...…………..…... 22
2. Variabel Tergantung ………..…………...…………..……… 22
3. Variabel Pengacau ………..……….…..…. 22
C. Definisi Operasional ………..……….... 22
D. Bahan ……….…..……….…..…. 23
E. Alat ……….………..……..…...….. 24
F. Tata Cara Penelitian ………..…….….…….... 24
G. Analisis Data ………...……...…… 31
BAB IV. HASIL DAN PEMBAHASAN ………. 33
xi
B. Validasi Metode Kalibrasi Multivariat partial least square(PLS) …….… 38
C. Penetapan Kadar Sediaan Farmasi ………..… 45
BAB V. KESIMPULAN DAN SARAN ………..…....……… 50
A. Kesimpulan ………..……..………..…...………… 50
B. Saran ………..………...……… 50
DAFTAR PUSTAKA ……….………...…………..….… 51
LAMPIRAN ………..………...………... 54
xii
DAFTAR TABEL
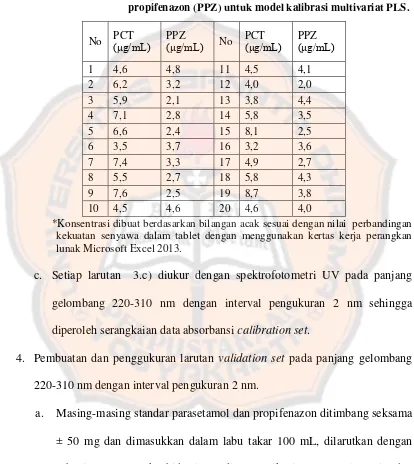
Tabel I. Komposisi campuran sintetik parasetamol (PCT) dan propifenazon (PPZ) untuk model kalibrasi multivariat PLS ………..…… 26
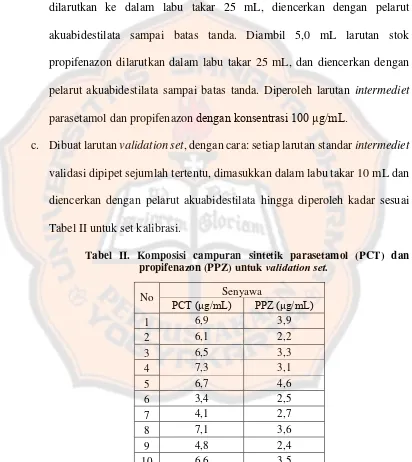
Tabel II. Komposisi campuran sintetik parasetamol (PCT) dan propifenazon (PPZ) untuk validation set……….……. 27
Tabel III. Evaluasi nilai sebenarnya dan terhitung hasil kalibrasi PLS dari
calibration set yang mengandung parasetamol (PCT) dan propifenazon (PPZ) tanpa validasi silang (cross validation) pada panjang gelombang 220-310 nm ……….……….. 35 Tabel IV. Evaluasi nilai sebenarnya dan terhitung hasil kalibrasi PLS dari
calibration set yang mengandung parasetamol (PCT) dan propifenazon (PPZ) validasi silang (cross validation) pada panjang gelombang 220-310 nm ………..….……….. 39 Tabel V. Evaluasi nilai sebenarnya dan terhitung hasil kalibrasi PLS dari 10
larutan validation set yang mengandung parasetamol (PCT) dan propifenazon (PPZ) ………..….………...….. 42 Tabel VI. Rekapitulasi parameter validasi metode spektrofotometri UV-PLS………. 44
Tabel VII. Konsentrasi larutan akhir setelah ditetapkan dengan model kalibrasi PLS yang telah tervalidasi ….………...………...…. 47 Tabel VIII. Hasil penetapan kadar prediksi parasetamol (PCT) dalam sediaan
xiii
xiv
DAFTAR GAMBAR
Gambar 1. Struktur parasetamol ………..……….... 6 Gambar 2. Struktur propifenazon ……….……….….. 7 Gambar 3. Penyerapan sinar UV oleh larutan ………...….…...…….. 9 Gambar 4. Gambar skematis spektrofotometer UV-vis …...……..…...….. 11 Gambar 5. Overlay spektra UV parasetamol (PCT), propifenazon (PPZ), dan
campuran kedua senyawa pada konsentrasi 5 µg/mL, yang diukur pada 200 –400 nm ………..………...….…… 33
Gambar 6. Kurva hubungan nilai sebenarnya dengan nilai terhitung pada model kalibrasi multivariat PLS parasetamol ……….…...…... 36
Gambar 7. Kurva hubungan nilai sebenarnya dengan nilai terhitung pada model kalibrasi multivariat PLS propifenazon…..……..……... 37 Gambar 8. Kurva hubungan nilai sebenarnya dengan nilai terhitung pada
model kalibari multivariat PLS parasetamol yang teleh tervalidasi
cross validation leave one out…….………….………. 41
Gambar 9. Kurva hubungan nilai sebenarnya dengan nilai terhitung pada model kalibari multivariat PLS propifenazon yang teleh tervalidasi
cross validation leave one out……….. 41
xv
xvi
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat analisis baku parasetamol …………...….…...……….55 Lampiran 2. Sertifikat analisis baku profipenazo ...………..……...………. 56 Lampiran 3. Data penimbangan baku pembanding untuk campuran sintetik
sampel kalibrasi………....…………...……… 58 Lampiran 4. Data penimbangan sampel tablet untuk penetapan kadar sediaan
tablet……….…………...………...…..………. 58 Lampiran 5. Data pengukuran spektrofotometer UV 20 campuran sintetik untuk
model PLS pada panjang gelombang 220 – 310 nm yang diukur dengan interval pengukuran 2 nm………..….… 59 Lampiran 6. Output Minitab hasil kalibrasi multivariat partial least square
(PLS) parasetamol dari sampel kalibrasi 20 campuran sintetik tanpa validasi internal……….…………..……...…… 63 Lampiran 7. Output Minitab hasil kalibrasi multivariat partial least square
(PLS) propifenazon dari sampel kalibrasi 20 campuran sintetik tanpa validasi internal ………...………...…… 64 Lampiran 8. Output Minitab hasil kalibrasi multivariat partial least square
(PLS) parasetamol dari sampel kalibrasi 20 campuran sintetik validasi internal ……… 65 Lampiran 9. Output Minitab hasil kalibrasi multivariat partial least square
xvii
Lampiran 10. Data nilai koefisien dari model PLS parasetamol dan propifenazon………... 67 Lampiran 11. Data pengukuran 10 sampel validasi eksternal pada panjang
gelombang 220-310 nm yang diukur dengan interval 2 nm ….. 68 Lampiran 12. Data penetapan kadar 10 larutan validasi dengan koefisien model kalibrasi PLS parasetamol dan propifenazon ……….… 70 Lampiran 13. Data pengukuran spektrofotometri UV enam replikasi sampel pada
panjang gelombang 220 – 310 nm yang diukur dengan interval pengukuran 2 nm……….………..…………...….. 80 Lampiran 14. Perhitungan kadar parasetamol terprediksi darri sampel obat sakit
xviii INTISARI
Kontrol kualitas sediaan farmasi merupakan suatu keharusan untuk menjamin mutu sediaan farmasi. Kontrol kualitas sediaan farmasi biasanya dilakukan dengan metode spektrofotometri dan kromatografi. Akan tetapi metode analisis spektrofotometri untuk analisis senyawa campuran secara simultan memiliki keterbatasan karena adanya overlapping spektra senyawa. Dengan bantuan kemometrika, masalah overlapping pada metode spektrofotometri dalam analisis senyawa campuran parasetamol (PCT) dan propifenazon (PPZ) dapat teratasi.
Analisis sediaan farmasi dengan metode spektrofotometri yang dikombinasikan dengan kemometrika memanfaatkan suatu model kalibrasi multivariat partial least square (PLS) yang divalidasi dari nilai koefisien determinasi (R2) dan kesalahan pemodelan (RMSE, root mean square error) dan kesalahan prediksi (PRESS, predicted residual error sum of square).
Diperoleh model kalibrasi PLS dengan nilai R2 PCT 0,9999 dan PPZ 0,9999. Nilai RMSEC sebesar 0,0043µg/mL untuk PCT dan 0,0031 µg/mL untuk PPZ, nilai R2 dan RMSEC tersebut menunjukkan kemampuan prediksi model yang tinggi. Pada proses validasi internal diperoleh nilai R2 PCT 0,9955 dan PPZ 0,9912 dengan nilai RMSECV untuk PCT 0,1027 µg/mL dan PPZ 0,0782 µg/mL. Nilai PRESS untuk PCT 0,2112 dan PPZ 0,1225. Pada proses validasi eksternal diperoleh nilai R2 PCT sebesar 0,9922 dan PPZ 0,9886 dengan nilai RMSECP PCT 0,3813 dan PPZ 0,2509. Nilai kadar rata-rata yang diperoleh dari tahap penetapan kadar untuk PCT dan PPZ adalah sebesar 299,861 mg/mg dan 197,95? mg/mg, dengan persentase kedekatan kadar sebesar 99,95% dan 98,96%.Metode analisis spektrofotometri UV-PLS merupakan metode yang valid dan dapat digunakan untuk menetapkan kadar senyawa campuran parasetamol dan propifenazon dalam sediaan tablet.
xix ABSTRACT
Quality control of pharmaceutical dosage was a must. Quality control of pharmaceutical dosage usually done by spectrophotometric and chromatographic methods. Spectrophotometric analysis method for simultaneous analyisis of mixtures compound has limitations because of the overlapping spectra. A mixture of paracetamol (PCT) and prophyphenazon (PPZ) has overlapping spectra. With the aid of chemometrics, overlapping problems that encountered by the spectrophotometric method can be resolved.
Analysis of pharmaceutical dosage by spectrophotometric method combined with chemometrics utilizing a calibration model multivariate partial least square (PLS) were validated from the coefficient of determination (R2) and modeling errors (RMSE, root mean square error) and the prediction error (PRESS, predicted residual sum of square error).
PLS calibration model was shown good with high predictive ability, which shown by the value of R2 for both PCT and PPZ was 0.9999. The RMSEC value of PCT 0.0043% and PPZ 0.0031%. In the internal validation process R2 values of PCT was 0,9958 and for PPZ was 0.9946. The RMSECV values of PCT was 0.1027 and 0.0782 for PPZ. PRESS value of the PCT and PPZ was 0.2112 and 0.1225 respectively. In the external validation process R2 values of PCT was 0.9922 and for PPZ was 0.9986, the RMSECP value of PCT and PPZ was 0,3813 and 0,2509 respectively. PCT and PPZ assay was successfully performed by the percentage recovery range for PCT was 99.95% and for PPZ was 98.96%. Spectrophotometric UV-PLS analysis methods was a valid method than can be used for analyzing mixture compound of paracetamol and propifenazon in pharmaceutical tablet dosage.
1 BAB I PENGANTAR
A. Latar Belakang
Kontrol kualitas suatu sediaan farmasi mutlak diperlukan untuk menjamin bahwa sediaan obat mengandung bahan dengan mutu dan jumlah yang telah ditetapkan, sehingga menunjang efek terapeutik yang diharapkan. Kontrol kualitas sediaan farmasi dilakukan secara rutin sehingga memerlukan metode analisis yang handal dan cepat. Spektrofotometri UV sejauh ini adalah salah satu metode instrumental yang dipilih oleh laboratorium industri untuk analisis sediaan farmasi. Spektrofotometri UV dipilih karena merupakan metode yang sederhana selain itu juga tidak membutuhkan biaya yang besar. Analisis sediaan farmasi multikomponen secara simultan sangat sulit dilakukan dengan metode spektrofotometri UV biasa dikarenakan adanya permasalahan spektra yang tumpang tindih antar komponen. Oleh karena itu perlu dilakukan pengolahan data secara statistik agar diperoleh suatu metode yang mampu memenuhi kebutuhan kontrol kualitas sediaan farmasi secara rutin.
PLS dipilih dikarenakan memiliki kemampuan dalam mengolah data dengan jumlah banyak dan memberikan model kalibrasi berkemampuan prediksi tinggi.
Parasetamol dan propifenazon merupakan obat yang secara luas digunakan dalam penanganan rasa nyeri (analgetika) dan demam (antipiretika) (Tan & Rahardja, 2007). Campuran parasetamol dan propifenazon tidak dapat dianalisis dengan metode spektrofotometri UV biasa dikarenakan terjadi spektra yang tumpang tindih antar kedua senyawa. Metode spektrofotometri UV yang dikombinasikan dengan kalibrasi multivariat PLS diharapkan mampu digunakan untuk menganalisis sediaan tablet farmasi multikomponen parasetamol dan propifenazon. Metode analisis spektrofotometri UV yang dikombinasikan dengan kalibrasi multivariat PLS diharapkan memiliki model kalibrasi yang optimal serta validitas yang baik sehingga mampu digunakan untuk kontrol kualitas sediaan farmasi secara rutin.
1. Rumusan Masalah
Berdasarkan pada latar belakang permasalahan yang telah diuraikan di atas, maka dapat diuraikan beberapa rumusan masalah sebagai berikut :
1. Apakah metode spektrofotometri UV yang dikombinasikan dengan teknik kalibrasi multivariat PLS untuk analisis sediaan tablet parasetamol dan propifenazon adalah metode yang optimal?
3. Apakah metode spektrofotometri UV yang dikombinasikan dengan teknik kalibrasi mulivariat PLS dapat digunakan untuk penetapan kadar parasetamol dan propifenazon dalam sediaan tablet?
2. Keaslian Penelitian
Berdasarkan studi pustaka yang telah peneliti lakukan, belum ditemukan penelitian yang menggunakan metode spektrofotometri UV dengan kalibrasi multivariat untuk menentukan kadar sediaan tablet farmasi dengan kombinasi parasetamol dan propifenazon. Beberapa penelitian yang telah berhasil menetapkan kadar senyawa mulikomponen dengan metode kalibrasi multivariat PLS adalah sebagai berikut :
a. Kombinasi spektrofotometri UV dan kalibrasi multivariat untuk analisis parasetamol, guafenesin, dan klorfeniramin maleat secara simultan tanpa proses pemisahan oleh Yani (2014).
b. Campuran obat bronkodilator secara simultan menggunakan metode spektrofotometri dan KCKT serta pendekatan kemometrika oleh El-Gindy
et al., (2006).
c. Penetapan kadar parasetamol, ibuprofen, dan kafein secara simultan dengan kombinasi spektrofotometri UV dan pendekatan kalibrasi multivariat Khosayand et al., (2008).
3. Manfaat Penelitian a. Manfaat Metodologis.
Penelitian ini diharapkan dapat memberikan sumbangan ilmiah tentang penggunaan metode spektrofotometri UV yang digabungkan dengan teknik kalibrasi multivariat seperti partial least square (PLS) dalam analisis kadar sediaan tablet dengan komposisi parasetamol dan propifenazon yang memiliki sistem optimal dan memenuhi persyaratan validasi yang baik.
b. Manfaat praktis.
Penelitian ini diharapkan dapat memberikan suatu alternatif metode baru untuk analisis kadar sediaan tablet dengan komposisi parasetamol dan propifenazon yang beredar di pasaran.
c. Manfaat teoritis.
Penelitian ini diharapkan memberikan informasi dan pengetahuan mengenai analisis parasetamol dan propifenazon dalam sediaan tablet menggunakan metode spektrofotometri UV yang dikombinasikan dengan kalibrasi multivariat PLS.
B. Tujuan Penelitian
2. Mengetahui validitas metode spektrofotometri UV yang dikombinasikan dengan teknik kalibrasi multivariat PLS untuk analisis sediaan tablet parasetamol dan profiopenazon.
6 BAB II
PENELAAHAN PUSTAKA
A. Karakteristik Senyawa 1. Parasetamol
Menurut Moffat (2011) Parasetamol (Gambar 1) memiliki rumus molekul C8H9NO2 dengan berat molekul 151,16.
Gambar 1. Struktur parasetamol
Parasetamol berbentuk kristal putih atau serbuk kristal putih yang larut dalam air dingin, larut dalam air mendidih, larut dalam etanol, metanol, dimetilformamid, etilen diklorida, aseton dan etil asetat, larut baik dalam kloroform dan eter, sedikit larut dalam petroleum eter, pentana, dan benzene (Moffat,2011). Parasetamol larut 70 bagian air, dalam 7 bagian etanol (95%), dalam 13 bagian aseton P, dalam 40 bagian gliserol P, dan 9 dalam propilenglikol P (Depkes RI,1979). Parasetamol memberikan serapan maksimum dalam pelarut asam pada panjang gelombang 245 nm dengan nilai % = dan dalam pelarut basa memberikan serapan maksimal pada
panjang gelombang 257 nm dengan nilai % = (Moffat,2011).
dianggap sebagai zat penghilang rasa nyeri (analgetika) yang paling aman. Efek analgetika dari parasetamol dapat diperkuat oleh kafein hingga 50%. Dalam hati zat ini diuraikan menjadi metabolit toksis sebagai konjugat glukoronida sulfide. Pada dosis tinggi mengakibatkan nekrosis hati yang tidak reversibel. Dosis yang berlebihan (overdose) menimbulkan mual dan muntah (Tan & rahardja, 2007). 2. Propifenazon
Propifenazon (Gambar 2) rumus molekul C14H18N2O dan berat molekul 230,30. Propifenazon berbentuk kristal putih atau serbuk kristal putih, setiap 1 gram propifenazon larut dalam 400 ml air, larut dengan mudah dalam etanol dan kloroform, dan larut dalam eter. Propifenazon memberikan serapan maksimum dalam pelarut asam pada panjang gelombang 240 nm dengan nilai % = dan dalam pelarut basa memberikan serapan maksimal pada
panjang gelombang 245 dengan nilai % = (Moffat, 2011).
Gambar 2. Struktur propifenazon
B. Spektrofotometri Ultraviolet
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari spektrometer dan fotometer. Spektrometer menghasilkan sinar spektrum dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi. Jadi, spektrofotometer digunakan untuk mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan, atau diemisikan sebagai fungsi panjang gelombang (Khopkar, 2008). Bila cahaya (monokromatik maupun campuran) jatuh pada suatu medium homogen, sebagian dari sinar masuk akan dipantulkan sebagian diserap medium itu, dan sisanya diteruskan (Basset, dkk., 1994).
Radiasi elektromagnetik pada sinar ultraviolet dan sinar tampak (visibel) dianggap sebagai energi yang merambat dalam bentuk gelombang. Panjang gelombang merupakan jarak linier dari suatu titik pada satu gelombang ke titik yang bersebelahan pada gelombang yang berdekatan (Watson, 2003).
Spektrofotometri dapat dianggap sebagai perluasan suatu pemeriksaan visual, yang dengan studi lebih mendalam dari absorpsi energi radiasi oleh macam-macam zat kimia sehingga dilakukannya pengukuran ciri-ciri serta kuantitatifnya dengan ketelitian yang lebih besar (Day dan Underwood, 1983). Dalam aspek kuantitatif spektrofotometer Uv-Vis, suatu radiasi dikenakan pada larutan (sampel) dan intensitas sinar radiasi yang diteruskan diukur besarnya. Radiasi yang diserap oleh sampel (Gambar 3) ditentukan dengan membandingkan intensitas sinar yang diteruskan dengan yang diserap. Serapan terjadi jika radiasi/foton yang mengenai sampel memiliki energi yang sama dengan energi yang diperlukan untuk perubahan tenaga. Kekuatan radiasi dapat mengalami penurunan dengan adanya penghamburan dan pemantulan cahaya (Sudjaji dan Rohman, 2007).
Gambar 3. Penyerapan sinar UV oleh larutan (Watson, 2003)
Perhitungan besarnya serapan cahaya oleh suatu molekul dalam larutan mengikuti Hukum Lambert-Beer dengan rumus:
Log I0/It = A = ε b c (1) I0 adalah intensitas sinar awal; It adalah intensitas sinar setelah melalui larutan dengan ketebalan b; A adalah absorbansi terukur (besarnya/sejumlah cahaya
Sampel
yang diserap oleh sampel); ε adalah konstanta serapan tiap 1M analit dalam larutan;
b adalah ketebalan kuvet (biasanya 1cm); dan c adalah konsentrasi analit (Watson, 2003).
Hubungan antara nilai A % cm dengan absorptivitas molar (ε) adalah:
ε = A % cm x BM (2)
Keterangan:
Ε = absorptivitas molar
% = absorptivitas molekul dalam satuan konsentrasi (g/100 mL) BM = bobot molekul
(Sudjaji dan Rohman, 2007). Hukum Lambert-Beer menyatakan bahwa instensitas yang diteruskan oleh larutan zat penyerap sebanding dengan tebal dan konsentrasi larutan. Dalam hukum ini terdapat pembatasan yaitu: sinar yang digunakan dianggap monokromatis; tidak terjadi fluoresensi atau fosforesensi; indeks bias tidak tergantung pada konsentrasi larutan; penyerapan terjadi dalam suatu volume yang mempunyai penampang luas sama; dan senyawa yang menyerap tidak tergantung kepada senyawa lain dalam larutan (Sudjaji dan Rohman, 2007).
Gambar 4. Gambar skematis spektrofotometer UV-Vis (Watson, 2003) Sumber energi pada spektrofotometer harus dapat memberikan intenitas radiasi elektromagnetik secara stabil pada daerah spektrum elektromagnetik. Sumber energi dibagi menjadi dua yaitu sumber energi continuum dan sumber energi line. Sumber energi continuum merupakan sumber energi yang memancarkan lebih dari satu panjang gelombang dengan intensitas bervariasi dari masing-masing panjang gelombang. Sumber energi line merupakan sumber energi yang memancarkan satu panjang gelombang yang selektif. Pada spektrofotometer Uv-Vis menggunakan sumber energi continuum, sehingga membutuhkan monokromator sebagai selektor filter untuk membatasi jumlah panjang gelombang radiasi elektromagnetik yang akan masuk (Harvey, 2000).
Panjang gelombang radiasi yang masuk melalui monokromator akan melewati sampel. Pada saat panjang gelombang radiasi melewati sampel, akan terjadi pengurangan sejumlah radiasi, sehingga panjang gelombang radiasi yang keluar ditangkap oleh detektor akan lebih kecil dari panjang gelombang radiasi
Slit Slit
Monokromator
Detektor
Sampel dalam kuvet kuarsa Lampu deuterium dan
yang masuk. Banyaknya jumlah radiasi yang berkurang berbanding lurus dengan konsentrasi analit dalam sampel (Harvey, 2000).
C. Kemometrika
Permasalahan dalam analisis senyawa multikomponen secara simultan dengan menggunakan metode spektrofotometri adalah adanya overlapping spektra satu senyawa dengan senyawa lainnya (Ragno et al., 2004). Analisis masing-masing komponen senyawa dalam campuran yang mempunyai spektra overlapping
hanya dapat diatasi dengan metode pemisahan secara kromatografi atau metode spektrofotometri yang dikombinasikan dengan kalibrasi multivariat (Miller & Miller, 2010).
Kemometrika adalah ilmu pengetahuan yang menghubungkan pengukuran yang dibuat pada suatu proses atau sistem kimiawi melalui penggunaan ilmu matematika dan statistika (Rohman, 2014). Kemometrika berfokus pada ekstraksi informasi yang relevan dari data kimiawi dengan memanfaatkan ilmu matematika dan statistika (Kurt, 2009). Kemometrika banyak berkaitan dengan pengukuran data multivariat. Data multivariat adalah data yang dihasilkan dari pengukuran banyak variabel pada satu sampel yang sama (Rohman, 2014). Uji statistik multivariat merupakan alat yang sangat baik digunakan untuk menganalisis data yang diperoleh dari suatu pengukuran kimia dan untuk membuat suatu model matematika empirik untuk secara instan dapat memprediksi suatu nilai yang tidak dapat diukur secara langsung (Kurt, 2009).
yang mana koordinat-koordinat titik memberikan suatu nilai oleh 2 variabel. Nilai– nilai tersebut dapat ditentukan sebagai suatu vektor. Data yang mempunyai sifat serupa akan mempunyai vektor yang sama sehingga data-data ini akan terletak secara rapat satu sama lain dalam suatu ruang yang ditentukan dengan beberapa variabel (Rohman, 2014).
Metode-metode kemometrika adalah metode yang dipergunakan untuk mereduksi data dan mengelompokkan data-data tersebut dalam suatu kelompok dengan karakter data yang sama. Dalam hal ini, ada dua jenis cara pengelompokkan yakni: (1) pengelompokkan yang tidak disupervisi (unsupervised pattern recognition) seperti analisis komponen utama (principle component analysis,
PCA), analisis kluster (cluster analysis); dan (2) pengelompokkan yang disupervisi (supervised pattern recognition) seperti analisis diskriminan (discriminant analysis) (Rohman, 2014).
Dalam prakteknya, model aditif/penjumlahan sederhana ini tidak dapat menggambarkan keadaan sebenarnya secara sempurna. Terdapat dua alasan untuk hal ini. Pertama, analit yang dikehendaki dapat terganggu dengan satu sama lain secara kimiawi sedemikian rupa sehingga akan mempengaruhi spektra analit yang dituju. Kedua, sampel dari sumber sebenarnya dapat mengandung senyawa lain selain senyawa-senyawa (analit) yang akan dianalisis, yang berkontribusi pada nilai absorbansi yang dihasilkan. Pada keadaan ini, lebih baik menggunakan suatu kalibrasi terbalik dan mengkalibrasi dengan spesimen sebenarnya. Istilah “kalibrasi
terbalik” berarti bahwa konsentrasi analit (Ct) dimodelkan sebagai fungsi spektrum
(yakni sebagai kebalikan kalibrasi klasik). Dengan demikian persamaan regresi terbalik mempunyai bentuk: = + + + ⋯ + . Kalibrasi terbalik merupakan kalibrasi yang sesuai karena konsentrasi tidak dipertimbangkan sebagai variabel terkendali (Rohman, 2014).
Berdasarkan hal di atas, seringkali kalibrasi multivariat dibedakan menjadi: (1) kalibrasi biasa/normal ( = + + + ⋯ + ), dan metode yang termasuk jenis ini adalah metode kuadrat terkecil klasik (classical least square) dan (2) kalibrasi terbalik ( = + + + ⋯ + . Yang termasuk dalam kalibrasi terbalik adalah: (i) stepwise multiple linear regression, (ii) principle component regression, dan (iii) partial least square
(Rohman,2014).
koordinat matrik data. Variabel ini kemudian disebut dengan “latent variable”
(Land et al., 2011). Metode ini menggunakan suatu kombinasi linier dari variabel prediktor daripada menggunakan variabel biasa. Variabel yang memberikan korelasi tinggi terhadap variabel response dipilih karena akan memberikan prediksi yang lebih efektif. Dalam hal ini, PLS membuat suatu kombinasi linier dari variabel prediktor yang memberikan korelasi yang tinggi terhadap variabel response dan juga menjelaskan variasi di dalam variabel respons (Miller, 2010). “Latent variabel” ini diperoleh dari dua tahapan penting yaitu loading weight dan
regression coofesion. Loading weight adalah proses seleksi variabel-variabel dengan nilai korelasi yang signifikan, proses ini menitik beratkan pada pemberian suatu nilai loading weightpada setiap variabel yang bisa diseleksi berdasarkan nilai tetapan signifikansi dari uji Hotelling’s T2 yang dikombinasikan dengan Jacknifing. Dari proses ini dapat diperoleh variabel-variabel yang memberikan pengaruh kuat dan bertanggung jawab terhadap kemampuan prediksi dari model. Proses kedua adalah regression coofesion, tahap ini merupakan tahap yang sangat rumit. Sekali lagi, variabel-variabel yang telah diseleksi dengan Loading Weigh diberikan nilai yang diperoleh dari prosedur bootstrapping atau jackknifing. Nilai regression coofesion adalah nilai yang menghubungkan antara variabel dan response. Nilai ini bertanggung jawab secara langsung untuk proses prediksi (Mehmood et al., 2012). Persamaan linear PLS dinotasikan sebagai berikut :
= � + � (3)
Keterangan :
ε = kesalahan pengukuran pemodelan.
(Haenlein, 2004). Kelebihan metode PLS dibandingkan dengan metode kalibrasi lain adalah: a. Dibandingkan dengan LSR, PLS jauh lebih cepat dan lebih mudah diimplementasikan. Kemungkinan terjadinya over-fitting pada PLS jauh lebih kecil dibandingkan dengan metode kalibrasi lain.
b. PLS memiliki kemampuan tinggi ketika diterapkan pada data dengan dimensi yang luas.
(Land et al., 2011).
D. Validasi Metode Analisis 1. Validasi metode kalibrasi multivariat
Validasi metode analisis merupakan suatu prosedur yang digunakan untuk membuktikan apakah suatu metode analisis memenuhi persyaratan yang ditentukan atau tidak, sehingga hasil analisis dapat dipertanggungjawabkan. Tujuan utama validasi metode adalah untuk memberikan hasil analisis yang paling baik (United States Pharmacopeial Covention, 2007).
memenuhi persyaratan untuk diterapkan dalam analisis senyawa atau sediaan yang bersangkutan (Satiadarma, dkk., 2004).
Menurut Richard Kramer (2005), suatu metode kemometrika bisa divalidasi dengan dua cara; (1) Dengan adanya sampel validasi eksternal; (2) Dengan menggunakan cross validation. Sampel validasi eksternal akan semakin baik jika semakin banyak jumlahnya. Idealnya, sampel eksternal hendaknya memberikan konsentrasi terhitung yang seakurat mungkin dengan nilai sebenarnya. Secara umum, suatu sampel validasi memiliki nilai simpangan tidak lebih dari ±5%. Sampel validasi masih dapat dipercaya apabila nilai simpangan tidak lebih dari ±10%. Namun, sampel validasi eksternal tidak perlu diterapkan apabila nilai simpangan mencapai ±20% dan disarankan untuk melakukan cross validation.
Validasi dengan sampel eksternal atau juga sering disebut dengan test set validation dilakukan dengan memproses sejumlah data (training set) dengan metode yang sama pada saat memproses data calibration set. Dalam hal ini, ada dua kelompok data yang berbeda yaitu data training set yang manamerupakan sejumlah data tambahan yang bukan merupakan calibration set. Hasil pengolahan statistik kedua kelompok data baik dari calibration set dan training set dibandingkan untuk melihatkemampuan sebuah model dalam mengekstrak suatu populasi data dengan jumlah data yang berbeda. Hal ini bertujuan untuk mengukur seberapa optimal model mampu menentukan komponen pembeda dari jumlah data yang berbeda. Diharapkan terjadi kesamaan hasil antara data
baik untuk melakukan test set validation. Oleh karena itu bisa digunakan sebagian dari calibration set untuk melakukan validasi, dan hal ini disebut dengan cross validation (Kim, 2002).
Standard cross validation melibatkan sebuah data dari bagian populasi yang diujikan pada populasi data yang sama untuk mengevalusasi kemampuan prediksi dari sebuah model. Metode validasi standard cross validation
memisahkan populasi data menjadi dua bagian (tidak harus dengan jumlah yang sama) untuk melihat kemampuan model terhadap satu bagian yang memvalidasi model tersebut (Esposito et al., 2010).
Tahap pengerjaan suatu cross validation bisa digambarkan sebagai berikut; (1) memisahkan satu data dari kelompok data atau populasi; (2) memisahkan satu data secara bergilir dari kelompok data atau populasi; (3) menetapkan data yang terpisah sebagai suatu sampel dan kelompok data yang tersisa sebagai predictor. Perbedaan nilai sebenarnya dengan nilai prediksi digambarkan sebagai nilai PRESS (predivtive residual error sum of squares)
(Reyment, 2002).
2. Parameter Validasi Metode Analisis Multivariat a. Presisi
Predicted residual error sum of square (PRESS) merupakan selisih antara nilai sebenarnya dengan nilai terhitung (y) kemudian dihitung jumlah kuadrat dari selisih tersebut. Persamaan PRESS dijabarkan dengan :
Ketidakpastian kalibrasi dan prediksi dari konsentrasi yang tidak diketahui dapat dihitung dengan root mean standard error of calibration
(RMSEC), dengan persamaan:
� = √∑��=� �� � ℎ� ��− �� � �� �� , 2
(5)
Dan root mean square prediction (SEP):
� � � � = √∑��=� �� � ℎ� ��− �� � �� �� , 2
(6)
Dimana, �(sebenarnya,cs) adalah kadar sebenarnya dari sampel kalibrasi, �(sebenarnya,ts) merupakan kadar sebenarnya dari sampel validasi, dan �(terhitung) adalah kadar prediksi sampel (Danzer et al, 2004).
b. Akurasi
Ada tidaknya suatu kesalahan sistematik dapat dilihat pengujian secara umum dengan melihat fungsi recovery yang dinyatakan oleh koefisien determinasi (R2). Kadar terprediksi dari kurva kalibrasi (ĉ dibandingkan dengan kadar sebenarnya dari sampel kalibrasi (c), dengan persamaan regresi sebagai berikut:
ĉ = + c (7) Koefisien regresi ideal adalah jika nilai = dan =
E. Landasan Teori
Parasetamol dan propifenazon sering dikombinasikan sebagai zat aktif dalam suatu sediaan tablet dengan indikasi analgetika dan antipiretika untuk mengatasi sakit kepala dan keluhan nyeri lainnya yang sering dialami oleh masyarakat.
Analisis suatu campuran senyawa secara simultan dengan metode spektrofotometri UV memiliki kendala overlapping antara senyawa satu dengan senyawa lainnya sehingga metode spektrofotometri UV harus dikombinasikan dengan kemometrika agar masalah overlapping mampu diatasi. Kemometrika adalah ilmu pengetahuan yang menghubungkan pengukuran yang dibuat pada suatu proses atau sistem kimiawi melalui penggunaan ilmu matematika dan statistika. Kemometrika sering dihubungkan dengan pengolahan data multivariat. Data multivariat adalah data yang dihasilkan dari pengukuran banyak variabel pada satu sampel yang sama. Metode yang biasa digunakan untuk mengolah data multivariat adalah kalibrasi multivariat. Kalibrasi multivariat pada umumnya adalah metode yang memiliki prinsip mereduksi jumlah data menjadi suatu kelompok data yang lebih kecil. Salah satu metode kalibrasi multivariat adalah partial least square
(PLS).
PLS merupakan metode yang mengkombinasikan korelasi antara koordinat dalam matrik data sehingga diperoleh “latent value”. Latentvalue merupakan nilai
bisa dievaluasi berdasarkan parameter akurasi dan presisi. Parameter akurasi diperoleh melalui koefisien determinasi (R2) dan parameter presisi diperoleh dari nilai predicted residual error sum of square (PRESS) dan root mean square of error
(RMSE).
F. Hipotesis
Berdasarkan landasan teori yang telah dikemukakan di atas, maka dapat ditarik hipotesis sebagai berikut:
1. Spektrofotometri UV yang dikombinasikan dengan teknik kalibrasi multivariat PLS memiliki kemampuan prediksi yang optimal.
2. Spektrofotometri UV yang dikombinasikan dengan teknik kalibrasi multivariat PLS merupakan metode yang valid.
22 BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Jenis penelitian ini termasuk penelian non eksperimental dengan rancangan penelitian deskriptif. Jenis penelitian non eksperimental karena tidak ada perlakuan terhadap subjek penelitian. Rancangan penelitian deskripstif karena penelitian hanya mendeskripsikan keadaan yang ada.
B. Variabel Penelitian 1. Variabel Penelitian
a. Variabel Bebas
Variabel bebas dari penelitian ini adalah variasi konsentrasi larutan campuran senyawa parasetamol dan propifenazon.
b. Variable Tergantung
Variabel tergantung dari penelitian ini adalah konsentrasi sampel parasetamol dan propifenazon.
c. Variabel Pengacau
Variabel pengacau dari penelitian ini adalah pengukuran data absorbansi yang tidak informatif. Dikendalikan dengan pemusatan pengukuran pada panjang tertentu.
2. Definisi Oprasional
c. R-sq atau R2 merupakan koefisien determinasi yang menggambarkan kemampuan nilai konsentrasi dalam menjelaskan hubungan terhadap nilai terhitung.
d. RMSE (root mean square of error) merupakan simpangan dari sebuah pemodelan yang menjelaskan seberapa mungkin suatu model kalibrasi melakukan kesalaan dalam memprediksikan sampel.
e. PRESS (predicted error sum of square) merupakan nilai kesalahan yang dilakukan saat prediksi sampel oleh model kalibrasi dalam proses cross validation leave-one-out.
f. Calibration set atau kelompok larutan validasi internal merupakan 20 larutan kalibrasi yang digunakan untuk pembuatan model kalibrasi multivariat partial least square (PLS) untuk senyawa parasetamol dan propifenazon.
g. Validation set atau kelompok larutan validdasi eksternal merupakan 10 larutan validasi yang digunakan pada tahap validasi eksternal.
h. Overlapping merupakan keadaan spektra yang tumpang tindih dalam campuran senyawa.
i. Overfitting merupakan keadaan model tampak sempurna namun tidak mewakili populasi data secara keseluruhan.
C. Bahan
lampiran 1-2), akuabidestilata, metanol teknis, sediaan tablet obat sakit kepala dengan merk paten produksi perusahaan farmasi Indonesia dibeli dari apotek di Yogyakarta. Komposisi zat aktif pada sediaan farmasi tersebut adalah parasetamol 300 mg dan propifenazon 200 mg, kertas saring.
D. Alat
Spektrofotometer uv/vis (Shimadzu) tipe UV-1800 dengan kuvet kwarsa merk Hellma®, alat ultrasonikasi, timbangan analitik (Ohauss) tipe PAJ1003 dengan kepekaan 0,1 mg (maksimal 120 gram, minimal 0,001 gram), pipet mikro dengan skala 20-200 L merk Socorez®, stamper dan mortir serta gelas-gelas yang lazim digunakan dalam laboratorium analisis kimia yang terdapat di laboratorium Fakultas Farmasi Universitas Sanata Dharma.
E. Tata Cara Penelitian
1. Pembuatan larutan dan pengamatan spektra pada panjang gelombang 220-400 nm untuk parasetamol, propifenazon dan campuran senyawa dengan.
a. Standar parasetamol dan propifenazon masing-masing ditimbang seksama ± 50 mg dan dimasukkan dalam labu takar 100 mL, dilarutkan dengan sebagian pelarut akuabidestilata, diultrasonikasi selama 15 menit, dan diencerkan dengan pelarut sampai batas tanda (larutan stok standar konsentrasi 500 g/mL).
2. Pemilihan rentang panjang gelombang dan interval pengukuran calibration set
dengan spektrofotometri UV.
a. Dilihat hasil pengamatan spektra campuran parasetamol dan propifenazon. Rentang panjang gelombang pengukuran dipilih berdasarkan spektra dari campuran senyawa mulai memberikan serapan hingga spektra menunjukkan serapan mendekati nilai 0.
b. Dari hasil pengamatan spektra campuran parasetamol dan propifenazon dipilih rentang panjang gelombang pengukuran 220-310 nm. Interval pengukuran 2 nm dipilih agar diperoleh data yang tidak terlalu banyak namun tetap berdekatan satu dengan yang lainnya.
3. Pembuatan dan penggukuran larutan calibration set pada panjang gelombang 220-310 nm dengan interval pengukuran 2 nm.
a. Dilakkukan pembuatan larutan intermediet dengan mengencerkan masing-masing larutan baku standar (larutan baku standar dibuat pada proses 1.a) hingga konsentrasi 100 g/mL dengan pelarut akuabidestilata. Diambil 5,0
mL larutan stok parasetamol dilarutkan ke dalam labu takar 25 mL, diencerkan dengan pelarut akuabidestilata sampai batas tanda. Diambil 5,0 mL larutan stok propifenazon dilarutkan dalam labu takar 25 mL, dan diencerkan dengan pelarut akuabidestilata sampai batas tanda. Diperoleh larutan intermediet parasetamol dan propifenazon dengan konsentrasi 100
g/mL.
b. Dibuat larutan model kalibrasi, dengan cara: setiap larutan standar
dan diencerkan dengan pelarut akuabidestilata hingga diperoleh kadar sesuai Tabel I untuk set kalibrasi.
Tabel I. Komposisi campuran sintetik parasetamol (PCT) dan propifenazon (PPZ) untuk model kalibrasi multivariat PLS.
No PCT ( g/mL) PPZ ( g/mL) No PCT ( g/mL) PPZ ( g/mL)
*Konsentrasi dibuat berdasarkan bilangan acak sesuai dengan nilai perbandingan kekuatan senyawa dalam tablet dengan menggunakan kertas kerja perangkan lunak Microsoft Excel 2013.
c. Setiap larutan 3.c) diukur dengan spektrofotometri UV pada panjang gelombang 220-310 nm dengan interval pengukuran 2 nm sehingga diperoleh serangkaian data absorbansi calibration set.
4. Pembuatan dan penggukuran larutan validation set pada panjang gelombang 220-310 nm dengan interval pengukuran 2 nm.
b. Dilakkukan pembuatan larutan intermediet validasidengan mengencerkan masing-masing larutan baku standar validasi hingga konsentrasi 100 g/mL dengan pelarut akuabidestilata. Diambil 5,0 mL larutan stok parasetamol dilarutkan ke dalam labu takar 25 mL, diencerkan dengan pelarut akuabidestilata sampai batas tanda. Diambil 5,0 mL larutan stok propifenazon dilarutkan dalam labu takar 25 mL, dan diencerkan dengan pelarut akuabidestilata sampai batas tanda. Diperoleh larutan intermediet
parasetamol dan propifenazon dengan konsentrasi 100 g/mL.
c. Dibuat larutan validation set, dengan cara: setiap larutan standar intermediet
validasi dipipet sejumlah tertentu, dimasukkan dalam labu takar 10 mL dan diencerkan dengan pelarut akuabidestilata hingga diperoleh kadar sesuai Tabel II untuk set kalibrasi.
Tabel II. Komposisi campuran sintetik parasetamol (PCT) dan propifenazon (PPZ) untuk validation set.
No Senyawa
d. Setiap larutan 4.c) diukur dengan spektrofotometri UV pada panjang gelombang 220-310 nm dengan interval pengukuran 2 nm sehingga diperoleh serangkaian data absorbansi validation set.
5. Pembuatan dan pengukuran larutan sampel pada panjang gelombang 220-310 nm dengan interval pengukuran 2 nm.
a. Ditimbang 20 sampel tablet secara seksama, lalu dicatat bobot setiap tablet, kemudian dilakukan pengujian keseragaman bobot tablet, digerus sampai homogen.
b. Ditimbang seksama serbuk dengan jumlah tertentu yang setara dengan 30 mg parasetamol dan 20 mg propifenazon larutkan dalam labu takar 100 mL, dilarutkan dalam sebagian pelarut akuabidestilata, lalu diultrasonikasi selama 15 menit, dan diencerkan dengan pelarut sampai batas tanda. Sebagian larutan disaring dengan penyaring Whatman ke dalam gelas beker. c. Dari larutan yang telah disaring, dipipet sebanyak 5,0 mL dan dimasukkan ke dalam labu takar 50 mL, kemudian ditambahkan pelarut sampai batas tanda.
d. Dari larutan c) tersebut dipipet sebanyak 5,0 mL dan dimasukkan dalam labu takar 25 mL, kemudian ditambahkan pelarut sampai batas tanda. e. Tahap b) hingga d) dilakukan sebanyak enam kali untuk memperoleh
replikasi sebanyak 6 sampel replikasi. Konsentrasi sampel dihitung dengan model kalibrasi multivariat partial least square (PLS).
6. Pengolahan data statistik dengan partial least square (PLS) dengan perangkat lunak Minitab 16.
a. Model Kalibrasi Partial Least Square (PLS).
1) Data konsentrasi dan absorbansi set kalibrasi yang diperoleh dari proses 2.d) dilampirkan dalam kertas kerja perangkat lunak Microsoft Excel 2013.
2) Perangkat lunak Minitab 16 dibuka, kemudian data set kalibrasi dipindahkan dengan fungsi copy-paste dari perangkat lunak Microsoft Excel 2013 ke dalam kertas kerja perangkat lunak Minitab 16.
3) Pengolahan data statistik partial least square (PLS) dengan menggunakan pilihan Stat pada panel kerja, kemudian dipilih
regression partial least square.
4) Untuk pembuatan model PLS parasetamol, kolom responses dipilih variabel konsentrasi PCT dan kolom model dipilih variabel absorbansi dengan panjang gelombang 220-310 nm.
5) Untuk pembuatan model PLS propifenazon, kolom responses dipilih variabel konsentrasi PPZ dan kolom model dipilih variabel absorbansi dengan panjang gelombang 210-310 nm.
dipindahkan ke dalam kertas kerja perangkat lunak Microsoft Excel 2013 dengan fungsi copy-paste.
7) Kemampuan prediksi model dievaluasi dengan dicari nilai R2 dan nilai RMSEC dengan dibuat hubungan linier antara konsentrasi dan absorbansi. Diperoleh nilai R2 serta persamaan linier y=bx+a. Persamaan linier dipakai untuk menentukan nilai RMSEC.
b. Validasi Internal Cross Validation Leave-one-out
1) Data dipindahkan dari kertas kerja perangkat lunak Microsoft Excel 13 dengan menggunakan fungsi copy-paste ke dalam kertas kerja perangkat lunak Minitab 16.
2) Dipilih model kalibrasi PLS dengan menekan pilihan stat pada panel kerja, kemudian dipilih regression partial least square.
3) Untuk validasi parasetamol, kolom responses dipilih variabel konsentrasi PCT dan kolom model dipilih variabel absorbansi dengan panjang gelombang 210-320 nm. Kemudian tekan tombol option yang selanjutnya dipilih tahap leave-one-out.
4) Untuk validasi propifenazon, kolom response dipilih variabel konsentrasi PPZ dan kolom model dipilih variabel absorbansi dengan panjang gelombang 210-320 nm. Kemudian tekan tombol option yang selanjutnya dipilih tahap leave-one-out.
6) Akurasi dan Presisi model kalibrasi dievaluasi dari nilai R2 dan nilai RMSECV dengan membuat hubungan linier antara nilai sebenarnya dan nilai terhitung. Diperoleh persamaan linear y=bx+a yang akan dipergunakan untuk memperoleh nilai RMSECV.
F. Analisis Data
1. Validitas model kalibrasi multivariat dinyatakan secara statistik dengan nilai R2 untuk akurasi dan untuk presisi dinyatakan dengan nilai RMSE dan PRESS. 2. Konsentrasi sampel dihitung dengan koefisien dari masing-Xmasing model
untuk senyawa parasetamol dan propifenazon sesuai dengan persamaan :
= � + � + ⋯ + � + �
3. Kadar sampel dihitung dengan menggunakan rumus :
Kadar µ�/ = ( �ℎ� � µg/mL �) X �Ẋ mg)
Keterangan :
4. Kadar rata-rata sampel dihitung dengan menggunakan rumus :
� � % = Ẋ� �
Ẋ � =
�
Ẋ � %
Keterangan :
Kadar = Kadar rata-rata sampel terhadap keseluruhan sampel tablet (%)
Ẋ Kadar = Rata-rata kadar (mg)
Ẋ Berat tablet = Berat rata – rata penimbangan keseluruhan sampel tablet (mg)
Etiket = Informasi kekuatan senyawa sesuai dengaetiket (mg)
5. Akurasi dari proses penetapan kadar ditetapkan dengan persen perolehan kembali dengan rentang yang dapat diterima menurut Gonzales dan Herrador (2007) adalah sebesar 80-110 %.
33 BAB IV
HASIL DAN PEMBAHASAN
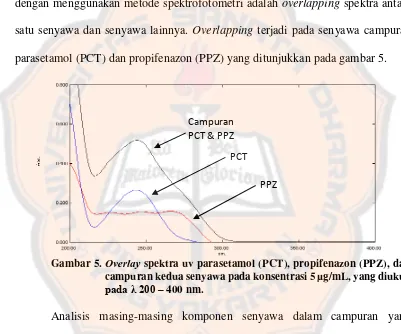
A. Optimasi Kalibrasi Multivariat Menggunakan Partial Least Square (PLS) Permasalahan dalam analisis senyawa multikomponen secara simultan dengan menggunakan metode spektrofotometri adalah overlapping spektra antara satu senyawa dan senyawa lainnya. Overlapping terjadi pada senyawa campuran parasetamol (PCT) dan propifenazon (PPZ) yang ditunjukkan pada gambar 5.
Gambar 5. Overlay spektra uv parasetamol (PCT), propifenazon (PPZ), dan campuran kedua senyawa pada konsentrasi 5 µg/mL, yang diukur
pada λ 200 – 400 nm.
Analisis masing-masing komponen senyawa dalam campuran yang mempunyai spektra overlapping hanya dapat diatasi dengan metode pemisahan secara kromatografi atau metode spektrofotometri yang dikombinasikan dengan kalibrasi multivariat. Permasalahan overlapping pada senyawa PCT dan PPZ dapat diatasi dengan adanya kombinasi antara spektrofotometry UV dengan kemometrika.
Campuran PCT & PPZ
PCT
Metode kemometrika yang dipilih dalam penelitian ini adalah kalibrasi multivariat partial least square (PLS). PLS memiliki keunggulan dalam menghasilkan model kalibrasi dengan kemampuan tinggi untuk jumlah data yang banyak. Pembuatan model PLS menggunakan 20 larutan calibration set yang dibuat berdasarkan nilai acak, bisa dilihat pada Tabel I. Bilangan acak dibuat dengan menggunakan kertas kerja perangkat lunak Microsoft Excel 2013 dengan memanfaatkan fungsi =RAND()*(perbandingan kekuatan senyawa). 20 larutan
calibration set diukur menggunakan spektrofotometri UV pada panjang gelombang 220-310 nm dengan interval pengukuran sebesar 2 nm menghasilkan serangkaian data absobansi (Lampiran 5). Menurut El Gindy (2006), pemilihan panjang gelombang pada PLS sangat diperlukan supaya kinerja model dapat optimum.
Pemusatan pengukuran pada panjang gelombang 220-310 nm bertujuan untuk mengurangi sebagian data yang mungkin bersifat tidak informatif dan dapat mengganggu dalam proses pengolahan data. Pemilihan panjang gelombang dalam pengukuran calibration set bertujuan untuk mendapatkan model kalibrasi dengan kemampuan prediksi yang optimum.
Data absorbansi dari calibration set (Lampiran 5) diolah menggunakan
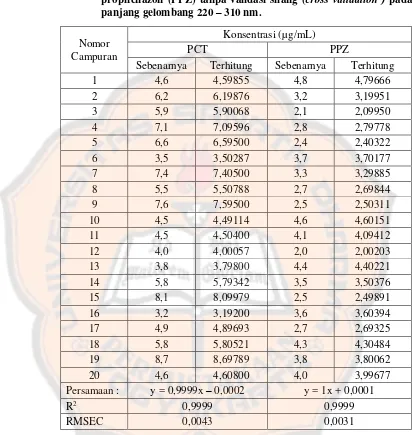
Tabel III. Evaluasi nilai sebenarnya dan terhitung hasil kalibrasi PLS dari
calibration set yang mengandung parasetamol (PCT) dan propifenazon (PPZ) tanpa validasi silang (cross validation ) pada
Sebenarnya Terhitung Sebenarnya Terhitung 1 4,6 4,59855 4,8 4,79666
Tabel III merupakan hasil pengolahan data yang diperoleh dari pembuatan model kalibrasi parasetamol dan propifenazon. Nilai sebenarnya merupakan nilai konsentrasi yang dibuat berdasarkan bilangan acak pada tahap pembuatan
dan nilai RMSEC. Diperoleh persamaan y=0,9999x-0,0002 untuk PCT dengan nilai R2-PCT sebesar 0,9999 dan nilai RMSEC-PCT sebesar 0,0043. Persamaan linier hubungan nilai sebenarnya dengan nilai terhitung untuk PPZ y=1x+0,0001 dengan nilai R2-PPZ sebesar 0,9999 dan nilai RMSEC-PPZ sebesar 0,0031. Menurut Danzer (2004) akurasi model kalibrasi bisa dideskripsikan dari persamaan garis y=bx+a, y merupakan kadar terhitung dihubungkan dengan x yang merupakan kadar sebenarnya. Jika nilai a mendekati 0 dan nilai b mendekati 1 maka dapat dinyatakan akurasi dari pemodelan baik. Model dinyatakan memiliki kemampuan prediksi tinggi dengan nilai R2 untuk kedua senyawa yang mendekati 1 serta memiliki kemungkinan kesalahan prediksi yang rendah ditunjukkan RMSEC yang mendekati 0. Data Tabel III bisa digambarkan dengan kurva hubungan antara nilai sebenarnya dan nilai terhitung untuk kedua senyawa bisa dilihat pada gambar 6 dan 7.
Gambar 6. Kurva hubungan nilai Sebenarnya dengan nilai terhitung pada model kalibrasi multivariat PLS parasetamol.
y = 0.9999x - 0.0002
0.00000 2.00000 4.00000 6.00000 8.00000 10.00000
Kurva Hubungan Nilai Sebenarnya vs
Gambar 7. Kurva hubungan nilai Sebenarnya dengan nilai terhitung pada model kalibrasi multivariat PLS propifenazon.
Informasi secara visual mengenai kemampuan prediksi model kalibrasi bisa dilihat pada gambar 6 dan gambar 7. Sesuai dengan nilai R2 dari masing-masing senyawa yang bernilai 0,9999 menunjukkan hubungan yang sangat baik antara nilai sebenarnya terhadap nilai terhitung dan memberikan pola garis lurus yang melewati setiap titik.
Model kalibrasi multivariat diharapkan memiliki kemampuan prediksi tinggi agar mampu menetapkan kadar sedekat mungkin dengan kadar sebenarnya dari suatu sampel. Kemampuan prediksi dari model kalibrasi multivariat divalidasi dengan dua proses yaitu validasi internal dan validasi eksternal. Validasi internal atau cross validation bertujuan untuk menangani masalah overfitting yang seringkali terjadi dalam proses pembuatan model. Validasi eksternal bertujuan untuk menentukan validitas dari model yang telah melewati proses cross validation.
y = 1x + 0,0001 R² = 0,9999
0.00000 1.00000 2.00000 3.00000 4.00000 5.00000 6.00000
0.00000 1.00000 2.00000 3.00000 4.00000 5.00000 6.00000
Kurva Hubungan Nilai Sebenarnya vs
B. Validasi Model Kalibrasi Multivariat Partial Least Square (PLS) Terjadinya over-fitting merupakan halangan yang mungkin terjadi pada suatu pembuatan model kalibrasi partial least square (PLS). Over-fitting
merupakan keadaan model yang nampak sempurna dengan nilai korelasi yang tinggi dan kesalahan yang kecil, namun tidak mampu memberikan hasil yang baik pada kelompok data yang berbeda (Faber and Rajko, 2007). Dengan kata lain, model kalibrasi yang over-fitting merupakan model kalibrasi yang nampak sempurna namun data dalam pembuatan model tidak seluruhnya representatif terhadap populasi data. Over-fitting dapat diatasi dengan melakukan proses validasi silang (cross-validation) dan salah satu jenis validasi silang adalah leave-one-out. Metode validasi cross-validation adalah metode yang memisahkan populasi data menjadi dua kelompok data. Kelompok data pertama berperan sebagai model kalibrasi PLS yang akan dipergunakan untuk mengkoreksi kelompok data kedua. Untuk leave-one-out, salah satu data dikeluarkan dari populasi yang nantinya akan dikoreksi. Proses leave-one-out terjadi terus menerus sampai semua data mengalami proses yang sama. Prosedur ini memungkinkan adanya pemerataan perlakuan terhadap keseluruhan populasi data. Proses cross-validation
menghasilkan nilai PRESS (predicted error sum of square) menunjukkan kesalahan prediksi yang terjadi selama proses leave-one-out.
V). Nilai PRESS merupakan kesalahan prediksi yang mungkin terjadi saat proses
leave-one-out sehingga model kalibrasi yang baik ditunjukkan dengan nilai kesalahan yang kecil.
Tabel IV. Evaluasi nilai sebenarnya dan terhitung hasil kalibrasi PLS dari
calibration set yang mengandung parasetamol (PCT) dan propifenazon (PPZ) validasi silang (cross validation ) pada panjang gelombang 220 – 310 nm.
Nomor Campuran
Konsentrasi (µg/mL)
PCT PPZ
sebelumnya, sementara itu nilai terhitung diperoleh dari nilai prediksi yang dilakukan pada proses leave-one-out.
Diperoleh persamaan linier hubungan nilai sebenarnya dan nilai terhitung untuk parasetamol y=1,0022x-0,0166 dengan nilai R2-PCT sebesar 0,9958, nilai RMSEC-PCT sebesar 0,1027 serta nilai PRESS-PCT sebesar 0,2112. Untuk propifenazon memiliki persamaan linier y=1,0069x-0,0253 dengan nilai R2-PPZ sebesar 0,9946, nilai RMSEC-PPZ sebesar 0,1027 serta nilain PRESS-PPZ sebesar 0,1225.
Gambar 8. Kurva hubungan nilai Sebenarnya dengan nilai terhitung pada model kalibrasi multivariat PLS parasetamol yang telah tervalidasi cross validation leave-one-out.
Gambar 9. Kurva hubungan nilai Sebenarnya dengan nilai terhitung pada model kalibrasi multivariat PLS propifenazon yang telah tervalidasi cross validation leave-one-out.
Gambar 8 dan 9 merupakan bentuk visual dari Tabel IV untuk senyawa parasetamol. Diperoleh garis lurus yang menunjukkan adanya hubungan yang baik
y = 1.0022x - 0.0166
0.00000 2.00000 4.00000 6.00000 8.00000 10.00000
Kurva Hubungan Nilai Sebenarnya vs
Terhitung Model PLS Parasetamol
Cross-0.00000 1.00000 2.00000 3.00000 4.00000 5.00000 6.00000
Kurva Hubungan Nilai Sebenarnya vs
antara nilai sebenarnya dan nilai terhitung meskipun garis tidak melewati keseluruhan titik secara sempura.
Selain melakukan validasi internal, juga dilakukan validasi eksternal dengan menetapkan konsentrasi 10 larutan validasi dengan hasil yang dapat dilihat pada Tabel V. Nilai sebenarnya merupakan nilai yang dibuat pada proses penentuan konsentrasi lauran, sementara itu nilai terhitung merupakan nilai yang diperoleh dari penetapan konsentrasi larutan dengan koefisien model kalibrasi yang telah melewati proses validasi internal (Lampiran 11). Validasi eksternal bertujuan untuk mengetahui kemampuan prediksi dari keseluruhan model kalibrasi multivariat PLS dengan menetapkan konsentrasi larutan yang telah diketahui. Dalam hal ini, penetapan kadar dilakukan dengan memperlakukan 20 calibration set sebagai model kalibrasi dan 10 validation set sebagai sampel validasi dengan hasil yang tertera pada Tabel V.
Tabel V. Evaluasi nilai sebenarnya dan terhitung hasil kalibrasi PLS dari 10 larutan validation set yang mengandung parasetamol (PCT) dan propifenazon (PPZ).
No PCT PPZ
Data yang diperoleh dari Tabel V menjelaskan kemampuan prediksi dari model kalibrasi PLS yang diperoleh setelah tahap cross validation leave-one-out. Kemampuan prediksi yang masih dapat diterima pada validasi eksternal terlihat dengan nilai R2 yang diperoleh untuk parasetamol dan propifenazon sebesar 0,9922 dan propifenazon senilai 0,9886 serta nilai RMSECP parasetamol 0,3813 dan propifenazon 0,2509. Korelasi antara nilai sebenarnya dan terhitung pada Tabel V bisa diamati secara visual pada gambar 10 dan 11. Secara visual digambarkan hubungan yang baik dari nilai sebenarnya dan nilai terhitung pada proses validasi internal dengan adanya garis lurus yang berada tidak jauh dari sekitaran titik dan ada beberapa titik yang tepat dilewati garis.
Gambar 10. Kurva hubungan nilai sebenarnya dengan nilai terhitung pada model kalibrasi multivariat PLS parasetamol validasi eksternal.
y = 1.0037x + 0.0369