i
OPTIMASI KOMPOSISI FASE GERAK PADA PEMISAHAN CAMPURAN DEKSAMETASON DAN DEKSKLORFENIRAMIN MALEAT SECARA
KROMATOGRAFI LAPIS TIPIS DENSITOMETRI
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh: Lucia Shinta Ratnaningtyas
NIM : 098114113
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
Halaman Persembahan
My Lovely Father and Mother
yang selalu setia dan tulus ikhlas menemani penulis dalam keadaan apapun,baik suka
maupun duka, atas doa dan restu dalam pencapain cita-cita penulis.
My Lovely Brother
Yang menjadi partner dalam berbagi pengalaman dan pemacu semangat penulis
untuk selalu berjuang dan berpikir positif dalam berkarya.
"When a person really desires something, all the universe conspires to help that person to realize his dream" Paulo Coelho “Bermimpi saja tidak akan pernah cukup. Sebuah impian
memang seharusnya tidak perlu terlalu banyak dibicarakan, tetapi diperjuangkan.”
― Donny Dhirgantoro
vii PRAKATA
Puji dan syukur kepada Tuhan Yang Maha Esa atas kasih, semangat, talenta,
cinta dan berkat penyertaanNya yang begitu besar, sehingga penulis dapat
menyelesaikan penelitian dan penyusunan skripsi berjudul “Optimasi Komposisi
Fase Gerak Pada Pemisahan Campuran Deksametason Dan Deksklorfeniramin
Maleat Secara Kromatografi Lapis Tipis Densitometri”
Penulis menyadari bahwa penelitian dan penyusunan skripsi ini dapat
terselesaikan oleh karena kritikan, saran, diskusi, arahan, dan bimbingan dari
berbagai pihak. Penulis mengucapkan terima kasih kepada :
1. Ipang Djunarko, M.Sc., Apt selaku dekan Fakultas Farmasi Universitas Sanata
Dharma yang memberikan kesempatan kepada saya untuk menuntut ilmu di
fakultas ini.
2. Prof. Dr. Sudibyo Martono, M.S., Apt. selaku dosen pembimbing pertama atas
kesabaran dan waktunya dalam memberikan arahan, kritik, saran, dan kesediaan
beliau untuk memberikan pencerahan pemikiran saya.
3. Dra. M.M. Yetty Tjandrawati, M.Si. selaku dosen pembimbing kedua dan DPA
Farmasi C 2009 atas pendampingannya dari awal sampai akhir kuliah, serta
viii
4. Jeffry Julianus, M.Si selaku dosen penguji atas masukan, kritik membangun dan
bimbingannya.
5. Lucia Wiwid Wijayanti, M.Si. selaku dosen penguji atas masukan, kritik
membangun dan bimbingannya.
6. Metri Setyadhiani Karunawati dan Sisilia Mirsya Anastasia sebagai rekan kerja
dalam penelitian ini. Terima kasih atas kesabaran, kerjasama, persahabatan,
canda, dan semangat selama ini.
7. Rendy Putra Wijaya yang telah sabar dan tulus setia mendampingi penulis dalam
suka maupun duka selama melakukan penelitian ini.
8. Eric Antonius, Is Sumitro, Demas, Novia Sarwoningtyas, Victor Purnama Jati,
Agnes Mutiara, Leonardus Nito Kristiyanto, Ina Juni Natasia, Topan Pamungkas,
Kristina Nety, dan Johannes Dharma sebagai teman seperjuangan dalam satu
lantai laboratorium Analisis Instrumental. Terima kasih atas diskusi, semangat,
dan keceriaan selama kita bekerja bersama-sama.
9. Konco Dolan FST 2009, FST suka-suka, dan Kepoers ( christine, devita galuh
ajeng, inggrid silli, dan amalia) untuk penghiburannya di sela-sela pusingnya
ix
10.Rekan praktikum (Wisnu, Nindi, Friska, Teti, Arvi, Haris, Ade, Saka, Novia)
yang telah mengajari penulis untuk terus semangat pantang menyerah dan sabar
dalam menyelsaikan tugas perkuliahan apapun yang terjadi.
11.PT. Ifars dan PT. Konimex yang telah memberikan baku deksklorfenirami maleat
dan deksametason kepada peneliti.
12.Grup request paper ilmiah di google tulisan-ilmiah@googlegroups.com dan
Indonesia-International Collaborative Research Forum yang selalu membantu
penulis dalam mendownload sumber ilmu dari paper-paper berkualitas dengan
sukarela dan tulus ikhlas.
13.Agnes Ardiyanti, Agatha Lena, Felicia Putri Hernat, Sanjayadi, Florentinus Dika
Octa Riswanto, dan Kenny Ryan Limanto atas bantuannya akses artikel ilmiah
dan diskusi membangun untuk kelancaran penelitian ini
14.Bimo Adithya, Parlan, Kunto, Fransiskus Otok dan segenap staf laboran yang
senantiasa siap membantu dan meluangkan waktunya dalam penyediaan bahan dan
alat selama penelitian
15.Semua dosen dan karyawan Fakultas Farmasi Universitas Sanata Dharma atas
x
16.Teman-teman Farmasi Angkatan 2009 atas suka, duka dan ceria selama 4 tahun
bersama “Together We Can”. Keberuntungan yang sangat berlimpah dirasakan
penulis atas kebersamaan selama ini.
17.Semua pribadi yang tidak dapat disebutkan satu persatu, atas segala bantuan,
semangat dan doa yang menyertai penulis dari awal penelitian sampai akhir
terselesaikannya penulisan skripsi.
Penulis membuka diri untuk menerima saran yang membangun dari semua
pihak. Akhir kata, penulis mempersembahkan skripsi ini dengan demi majunya ilmu
pengetahuan farmasi. Terima kasih.
xi
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... ... v
PERNYATAAN KEASLIAN KARYA ... ... vi
xiii
BAB II. PENELAHAAN PUSTAKA ... ... 7
A. Deksklorfeniramin maleat ... ... 7
B. Deksametason ... ... 9
3. Aplikasi Penotolan Sampel ... ... 14
4. Penilaian Kromatogram... ... 14
BAB III. METODE PENELITIAN ... ... 24
A. Jenis dan Rancangan Penelitian ... ... 24
xiv
1. Pembuatan larutan baku deksametason... ... 26
a. Pembuatan larutan baku deksametason 3,75 mg/mL...26
b. Pembuatan larutan baku deksametason 0,3 mg/mL...26
2. Pembuatan larutan baku deksklorfeniramin maleat ... ...26
a. Pembuatan larutan baku deksklorfeniramin maleat 5,0 mg/mL ... 26
b. Pembuatan larutan baku deksklorfeniramin maleat 1,0 mg/mL ... 26
3. Pembuatan larutan baku campuran deksametason dan deksklorfeniramin maleat... ... 27
4. Penentuan panjang elusi ... ... 27
5. Penentuan panjang gelombang pengamatan deksametason dan deksklorfeniramin maleat ... ... 27
6. Optimasi metode KLT densitometri .. ... 28
a. Pembuatan fase gerak ... 28
xv
c. Pembuatan larutan sediaan kaplet X® ... 29
d. Reprodusibilitas dari fase gerak hasil optimasi ... 29
G. Analisis Hasil ... 30
A.Penentuan Fase Gerak ... 32
B.Penentuan Larutab Baku ... 34
C. Pembuatan Panjang Jarak Elusi ... 35
D. Optimasi Metode Pemisahan Deksametason dan Deksklorfeniramin Maleat dalam sediaan tablet X® dengan Kromatografi Lapis Tipis Densitometri .. 36
1. Penentuan panjang gelombang pengamatan deksametason dan deklorfeniramin maelat ... ...36
2. Optimasi fase gerak untuk pemisahan deksametason dan deksklorfeniramin maleat dalam sediaan tablet® dengan KLT densitometri...39
a. Hasil elusi larutan blanko dengan fase gerak etil asetat p.a : metanol p.a : larutan amonia 25% p.a (25 :4 :1)...42
xvi
BAB V. KESIMPULAN DAN SARAN ...57
A.Kesimpulan ...57
B.Saran ...57
Daftar pustaka ... ... 58
Lampiran ... ... 61
xviii
DAFTAR TABEL
Tabel I. Sifat/karakteristik yang dimiliki deklorfeniramin maleat
...7
Tabel II. Sifat/karakteristik yang dimiliki deksametason...9
Tabel III. Karakteristik lapisan fase diam yang digunakan untuk TLC...12
Tabel IV. Nilai sifat pelarut...13
Tabel V. Komposisi Fase Gerak...28
Tabel VI. Nilai Rf, As, Rs, dan lama pengelusian larutan baku campuran deksametason dan deksklorfeniramin maleat...35
Tabel VII. Data pengukuran panjang gelombang pengamatan deksametason dan deksklorfeniramin maleat...38
Tabel VIII. Nilai Rf dan As larutan baku deksametason (D) dan deksklorfeniramin maleat (DM) pada berbagai komposisi fase gerak...41
Tabel IX. Nilai Rf dan As larutan baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat : metanol (25:4)...44
Tabel X. Nilai Rf dan As larutan baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat : metanol: larutan amonia 25% p.a (8 :20 :2)...45
xix
Tabel XII. Nilai Rf dan As larutan baku deksametason dan deksklorfeniramin maleat
dengan fase gerak etil asetat : metanol: larutan amonia 25% p.a (25 :4
:2)...47
Tabel XIII. Nilai Rf dan As larutan baku deksametason dan deksklorfeniramin maleat
dengan fase gerak etil asetat : metanol: larutan amonia 25% p.a
(25:6:1)...48
Tabel XIV. Nilai Rf dan As larutan baku deksametason dan deksklorfeniramin maleat
dengan fase gerak etil asetat : metanol: larutan amonia 25% p.a
(27:4:1)...49
Tabel XV. Nilai Rf dan As larutan baku deksametason dan deksklorfeniramin maleat
dengan fase gerak etil asetat : metanol: larutan amonia 25% p.a
(23:4:1)...50
Tabel XVI. Nilai Rf dan As larutan baku deksametason dan deksklorfeniramin maleat
dengan fase gerak etil asetat : metanol: larutan amonia 25% p.a
(25:2:1)...51
Tabel XVII. Nilai Rf, As, Rs dan AUC larutan baku campuran deksametason (D) dan
deksklorfeniramin maleat (DM) serta sampel kaplet X® dengan fase gerak
etil asetat p.a : metanol p.a : larutan amonia 25% p.a
xx
DAFTAR GAMBAR
Gambar 1. Struktur Deksklorfeniramin maleat ... ... 7
Gambar 2. Spektra Deksklorfeniramin maleat... ... 8
Gambar 3. Struktur Deksametason... ... 9
Gambar 4. Spektra Deksametason ... ... 10
Gambar 5. Struktur silika gel...13
Gambar 6. Ilustrasi pengaruh difusi Eddy pada pelebaran puncak... 16
Gambar 7. Ilustrasi pengaruh difusi longitudinal pada pelebaran puncak ... ... 17
Gambar 8. Ilustrasi pengaruh transfer massa pada pelebaran puncak. ... 17
Gambar 9. Isoterm sorpsi dan profil puncak...18
Gambar 10. Pemisahan dua senyawa... ... 19
Gambar 11. Ilustrasi skematis model deteksi ... 21
Gambar 12. Menentukan puncak asimetriss dan faktor pengukuran ... 30
Gambar 13. Gugus kromofor deksametason ... 37
Gambar 14. Gugus kromofor dan auksokrom deksklorfeniramin maleat ... 37
Gambar 15.Pola spektra absorbsi seri larutan rendah, sedang, dan tinggi senyawa campuran deksametason dan deksklorfeniramin maleat..38
Gambar 16. Puncak larutan blanko dengan fase gerak etil asetat : metanol : larutan amonia 25% (25 :4 :1)...42
xxi
Gambar 18. Puncak baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat p.a : metanol p.a : larutan amonia 25% p.a
(8 :20 :2) ... 44
Gambar 19. Puncak baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat : metanol : larutan amonia 25% p.a (20 : 8 : 2) ... 46
Gambar 20. Puncak baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat : metanol : larutan amonia 25% p.a (25 :4 :2) ... 47
Gambar 21. Puncak baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat : metanol : larutan amonia 25% p.a (25 :6 :1) ... 48
Gambar 22. Puncak baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat : metanol : larutan amonia 25% p.a (27 :4 :1) ... 49
Gambar 23. Puncak baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat : metanol : larutan amonia 25% p.a (23 : 4 : 1) ... 50
Gambar 24. Puncak baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat : metanol : larutan amonia 25% p.a (25 :2 :1) ... 51
Gambar 25. Puncak baku deksametason dan deksklorfeniramin maleat dengan fase gerak etil asetat : metanol : larutan amonia 25% p.a (25 :4 :1) ... ... ...52
xxii
DAFTAR LAMPIRAN
Lampiran 1. Certificate of Analysis Baku Deksklorfeniramin maleat...62
Lampiran 2. Certificate of Analysis Baku Deksametason...63
Lampiran 3. Data Penimbangan dan Pengambilan Baku dan Sampel serta Contoh Perhitungan Konsentrasi Baku...64
Lampiran 4. Contoh perhitungan Indeks Polaritas Fase Gerak...65
Lampiran 5. Sistem KLT-Densitometri yang Digunakan...67
Lampiran 6. Contoh densitogram hasil elusi dengan panjang track 15 cm...67
Lampiran 7. Contoh densitogram hasil elusi dengan panjang track 10 cm...68
Lampiran 8. Densitogram hasil elusi dengan fase gerak etil asetat p.a : metanol p.a (25:4)...68
Lampiran 9. Densitogram hasil elusi dengan fase gerak etil asetat p.a : metanol p.a : larutan amonia 25% p.a (8 :20 :2)...69
Lampiran 10. Densitogram hasil elusi dengan fase gerak etil asetat p.a: metanol p.a : larutan amonia 25% p.a (20 :8: 2) ...69
xxiii
Lampiran 12.Densitogram hasil elusi dengan fase gerak etil asetat p.a : metanol
p.a: larutan amonia 25% p.a (25 : 6: 1) ...70
Lampiran 13. Densitogram hasil elusi dengan fase gerak etil asetat p.a : metanol
p.a : larutan amonia 25% p.a (27 :4:1) ...71
Lampiran 14. Densitogram hasil elusi dengan fase gerak etil asetat p.a : metanol
p.a :larutan amonia 25% p.a (23 : 4 : 1)...71
Lampiran 15. Densitogram hasil elusi dengan fase gerak etil asetat p.a : metanol
p.a :larutan amonia 25% p.a (25 : 2 : 1)...72
Lampiran 16. Densitogram hasil elusi dengan fase gerak etil asetat p.a : metanol
p.a :larutan amonia 25% p.a (25 :4 :1)...72
Lampiran 17. Densitogram reprodusibilitas sampel...75
Lampiran 18. Perhitungan Nilai % KV AUC Baku dan Sampel...76
Lampiran 19. Contoh Perhitungan Nilai Rs (Resolusi) Puncak
Deksklorfeniramin maleat dan Deksametason ...77
Lampiran 20. Contoh Perhitungan Nilai Faktor Asimetris (As) Puncak
xxiv INTISARI
Kombinasi deksametason dan deksklorfeniramin maleat terdapat dalam sediaan kaplet X®. Penjaminan mutu menjadi hal yang penting untuk menjamin keamanan pemakaian sediaan kaplet X®. Salah satu usaha penjaminan mutu adalah penetapan kadar zat aktif yang akan mempengaruhi efek farmakologi obat. Metode kromatografi lapis tipis (KLT) densitometri adalah metode alternatif yang digunakan untuk memisahkan dan juga analisis kualitatif dan kuantitatif deksametason dan deksklorfeniramin maleat dalam waktu yang bersamaan.
Tujuan penelitian ini adalah untuk mengetahui kondisi optimal fase gerak dari KLT densitometri sehingga dapat menghasilkan pemisahan optimal dan dapat menetapkan kadar deksametason dan deksklorfeniramin maleat dalam sediaan kaplet X®.Penelitian ini merupakan jenis rancangan penelitian eksperimental yang pada subjek uji diberikan perlakuan yaitu jenis dan komposisi fase ferak. Sistem KLT yang digunakan fase normal menggunakan fase diam silika gel dan fase gerak optimal dari perbandingan etil asetat : metanol : larutan amonia 25%. Pembacaan dilakukan pada panjang gelombang 262 nm.
Sistem optimal komposisi dan jenis fase gerak yang diperoleh adalah etil asetat : metanol : larutan amonia 25% p.a (25 : 4 : 1) dengan jarak elusi 5 cm. Sistem memberikan bentuk puncak simetris, sempit, dan runcing (nilai faktor asimetris berada dalam kisaran 0,95-1,10), Range nilai Rf untuk deksametason adalah 0,60-0,68. Range Rf untuk deksklorfeniramin maleat adalah 0,40-0,48, dan %KV dari nilai AUC ≤ 2.
xxv ABSTRACT
Combinations of dexamethasone and dexchlorpheniramine maleate exist in X® tablet. Quality assurance becomes an essence since patient have to get the benefit of the safe medication. One kind of quality assurance involves the active substance quantifications related to the pharmalogical effect. Thin layer chromatography (TLC) densitometry is alternative method used for separation and also for qualitative and quantitative analysis of dexamethasone and dexchlorpheniramine maleate simultaneous.
The aim of this study is to determine optimal condition to produce the optimal separation and determine between dexamethasone and dexchlorpheniramine maleate in X® tablet. This study is an analytical experimental study that the test subjects are subjected by treatments consisted of different types and composition of mobile phase. The optimization of TLC-UV densitometric method was performed on ethyl acetate:methanol:larutan amonia 25% p.a with various compositions as the developing solvents. Detection was carried out at 262 nm.
The optimum system was confirmed by ethyl acetate : methanol : larutan amonia 25% p.a (25 : 4 : 1) as developing solvent with 5 cm elution distance. The systems gives symmetry, narrow, and pointed shaped peak (As = 0,95-1,10), Range Rf for dexamethasone are 0,60-0,68, Range Rf for dexamethasone are 0,40-0,48, and %CV of AUC ≤ 2.
Keywords : dexamethasone, dexchlorpheniramine maleate, thin layer chromatography, densitometric
1
BAB I PENGANTAR
A. Latar Belakang
Campuran deksametason dan deksklorfeniramin maleat (sediaan kaplet X®)
merupakan salah satu obat yang biasa digunakan untuk mengobati gangguan alergi
dan supresi inflamasi (Anonim1, 2009). Data World Allergy Organization (WAO)
2011 menyebutkan bahwa 22% penduduk dunia menderita alergi dan terus meningkat
setiap tahunnya. Hal ini menyebabkan penggunaan campuran deksametason dan
deksklorfeniramin maleat meningkat pula karena campuran deksametason dan
deksklorfeniramin maleat merupakan salah satu obat anti alergi yang menjadi
andalan.
Campuran deksametason dan deksklorfeniramin maleat merupakan produk
obat keras dan obat alergi andalan masyarakat. Oleh karena itu, penjaminan mutu
obat menjadi perhatian penting dalam penggunaan campuran deksametason dan
deksklorfeniramin maleat. Salah satu parameter obat dikatakan memenuhi standar
apabila kadar zat aktif yang terkandung di dalamnya memenuhi persyaratan standar
acuan. Deksametason dalam tablet mengandung tidak kurang dari 90,0 % dan tidak
lebih dari 110,0 % C22H29FO5 dari jumlah yang tertera pada etiket, sedangkan
deksklorfeniramin maleat dalam tablet mengandung tidak kurang dari 90,0% dan
tidak lebih dari 110,0% C20H23ClN2O4 dari jumlah yang tertera pada etiket (United
Penjaminan mutu kadar zat aktif yang terkandung dalam suatu obat dapat
diketahui melalui analisis kualitatif dan kuantitatif. Oleh karena itu, diperlukan
pengembangan metode analisis untuk memberikan metode alternatif. Pengembangan
metode alternatif penting karena variasi instrumen yang dimiliki laboratorium.
Metode analisis deksametason dan deksklorfeniramin maleat telah dilakukan
dengan menggunakan kromatografi cair (Maria dkk., 2005) dan spektrofluorometri
(El-Yazbi dkk., 2006). Penelitian menggunakan kromatografi cair dan
spektrofluorometri menghasilkan metode analisis yang akurat, simpel, dan
reprodusibel. Penelitian dengan menggunakan Kromatografi Lapis Tipis (KLT)
densitometri belum dikembangkan.
Peneliti ingin mengembangkan metode analisis alternatif obat yang
mengandung deksametason dan deksklorfeniramin maleat. Metode analisis yang akan
peneliti kembangkan adalah metode analisis campuran deksametason dan
deksklorfeniramin maleat dengan KLT densitometri. Salah satu kelebihan metode
KLT densitometri digunakan untuk analisis kualitatif dan kuantitatif dalam waktu
yang bersamaan dan dapat mengukur beberapa senyawa tidak hanya senyawa tunggal
(Martono, 1996).
Optimasi metode perlu dilakukan dalam penelitian ini karena terdapat
perbedaan zat aktif dan perbedaan instrumen analisis yang dilakukan dibandingkan
penelitian terdahulu. Optimasi metode ini diperlukan supaya tercapai pemisahan yang
optimal dari campuran deksametason dan deksklorfeniramin maleat.
Metode analisis yang optimal ditunjukkan dengan kualitas pemisahan.
Kualitas tersebut dapat dikontrol dengan melakukan serangkaian uji kesesuaian
sistem meliputi bentuk puncak, faktor retardasi, resolusi dan %KV nilai AUC. Bentuk
puncak yang baik yakni sempit dan simetris (nilai faktor asimetris (As) berada dalam
kisaran 0,95-1,10). Nilai faktor retardasi (Rf) zat aktif yang terletak antara 0,2-0,8
akan memaksimalkan pemisahan. Parameter lain dalam pemisahan senyawa dengan
metode kromatografi adalah nilai resolusi (Rs). Nilai resolusi harus bernilai lebih
besar sama dengan 1,5 (Rohman, 2009).
Penelitian ini merupakan dasar dalam rangkaian penelitian selanjutnya.
Penelitian ini diharapkan dapat diterapkan dalam pengembangan metode alternatif
1. Permasalahan
Bagaimanakah komposisi fase gerak yang dapat memberikan pemisahan KLT
yang baik dengan parameter-parameter bentuk puncak simetris dan sempit, nilai Rf
antara 0,2-0,8, nilai Rs ≥ 1,5, dan %KV nilai AUC ≤ 2 dalam pemisahan campuran
deksametason dan deksklorfeniramin maleat sebagai zat aktif dalam sediaan kaplet
X® menggunakan metode KLT densitometri dengan fase diam silika gel 60 F254 ?
2. Keaslian Penelitian
Penelitian mengenai identifikasi dan analisis kuantitatif deksametason
dilakukan oleh Krzek dan Maslanka (2005) dalam penelitiannya “Identification and
Quantitation of polymyxin B, framycetin, and dexamethasone in a ointment by using
thin-layer chormatograpfy with densitometry”. Plat dikembangkan dengan
sikloheksana-etil asetat (2 : 3 v/v).
Penelitian mengenai identifikasi dan kuantifikasi deksklorfeniramin maleat
dilakukan oleh Subarmaniyan dan Das (2004) dalam penelitiannya “Rapid
Identification and Quantification of Chlorpeniramine Maleate or Pheniramine
Maleate in Pharmaceutical Preparations by Thin Layer
Chromatography-Densitometry“ dengan menggunakan fase gerak sikloheksana : kloroform : metanol :
dietilamin (4,5 : 4 : 0,5 : 1 v/v).
Penelitian mengenai analisis kuantitatif deksametason dan klorfeniramin
maleat telah dilakukan Maria dkk.,(2005) dalam penelitiannya “Simultaneous
determination of chlorpheniramine maleate and dexamethasone in a tablet dosage
Penelitian El-Yazbi dkk.,2006) dalam penelitiannya yang berjudul “New
Spectrofluorometric Application For The Determination Of Ternary Mixtures Of
Drugs “memaparkan bahwa analisis campuran deksametason, deksklorfenirain
maleat, dan fluphenazine HCl dapat dilakukan dengan menggunakan
spektrofluorometri.
Penelitian yang akan dilakukan adalah optimasi komposisi fase gerak optimal
sebagai metode alternatif pemisahan campuran baku deksametason dan
deksklorfeniramin maleat dalam sediaan kaplet X® dengan menggunakan metode
KLT densitometri. Belum terdapat sistem KLT densitometri untuk pemisahan dan
kuantifikasi deksametason dan deksklorfeniramin maleat yang tercantum dalam
Farmakope Indonesia.
3. Manfaat Penelitian
a. Manfaat metodologis: Hasil penelitian diharapkan memberikan sumbangan
bagi pengembangan ilmu pengetahuan mengenai komposisi fase gerak yang
optimal sebagai metode alternatif pemisahan deksametason dan
deksklorfeniramin maleat dalam sediaan kaplet X® menggunakan KLT
densitometri.
b. Manfaat praktis: Hasil penelitian diharapkan memberikan informasi kondisi
pemisahan deksametason dan deksklorfeniramin maleat yang optimal untuk
penetapan kadar zat aktif sehingga menjamin keamanan pemakaian sediaan
B. Tujuan
Penelitian ini bertujuan untuk mengetahui komposisi fase gerak yang dapat
memberikan pemisahan KLT densitometri yang baik dengan parameter-parameter
bentuk puncak simetris dan sempit, nilai Rf antara 0,2-0,8, nilai Rs ≥ 1,5 dan %KV
nilai AUC ≤ 2 dalam pemisahan campuran deksametason dan deksklorfeniramin
maleat sebagai zat aktif dalam sediaan kaplet X® menggunakan metode KLT
7 BAB II
PENELAAHAN PUSTAKA A. Deksklorfeniramin Maleat
Gambar 1. Struktur Deksklorfeniramin maleat
Deksklorfeniramin maleat dalam tablet mengandung tidak kurang dari
90,0% dan tidak lebih dari 110,0% C20H23ClN2O4 dari jumlah yang tertera pada
etiket (United State Pharmacopeia, 2007). Deksklorfeniramin maleat (gambar 1.)
merupakan garam yang terdiri dari komponen basa deksklorfeniramin dan asam
maleat (Cox, 1979)
Tabel I. Sifat/ karakteristik yang dimiliki deksklorfeniramin maleat (Moffat, 2011)
No. Sifat/Karakteristik Keterangan
1 Titik didih 130 - 1350 C
2 Bobot molekul 390,9
3 pKa 9,13 (25°C)
4 Log P 0,08
Tabel I. menunjukkan karakteristik yang dimiliki deksklorfeniramin
maleat. Kelarutan deksklorfeniramin maleat yaitu mudah larut dalam air, larut
dalam etanol, dan dalam kloroform, sukar larut dalam benzena dan dalam eter
Deksklorfeniramin merupakan senyawa yang bersifat dibasic amine. Sifat
dibasic ini disebabkan adanya nitrogen pada gugus alifatik amin tersier dan
nitrogen piridin. Nitrogen pada gugus alifatik amin tersier memiliki kebasaan
yang lebih kuat dibandingkan dengan nitrogen piridin. Oleh karena itu, gugus
alifatik amin tersier akan memiliki kecenderungan lebih mudah terprotonasi untuk
membentuk garam.(Wilson dkk., 1966).
Berdasarkan struktur molekul, nitrogen pada cincin piridin
deksklorfeniramin memiliki pasangan elektron bebas. Pasangan elektron bebas ini
memiliki potensi untuk terprotonasi dan membentuk ion piridinium (Badger,
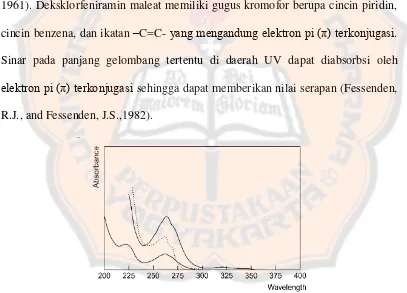
1961). Deksklorfeniramin maleat memiliki gugus kromofor berupa cincin piridin,
cincin benzena, dan ikatan –C=C- yang mengandung elektron pi (π) terkonjugasi.
Sinar pada panjang gelombang tertentu di daerah UV dapat diabsorbsi oleh
elektron pi (π) terkonjugasi sehingga dapat memberikan nilai serapan (Fessenden,
R.J., and Fessenden, J.S.,1982).
Gambar 2. Spektra Deksklorfeniramin maleat (Moffat, 2011)
Deksklorfeniramin maleat merupakan antihistamin yang memiliki
dengan reseptor akan menyaingi histamin sebagai agen alergi, sehingga reaksi
alergi dapat terhindarkan (Tjay dan Rahardja, 2002).
B. Deksametason
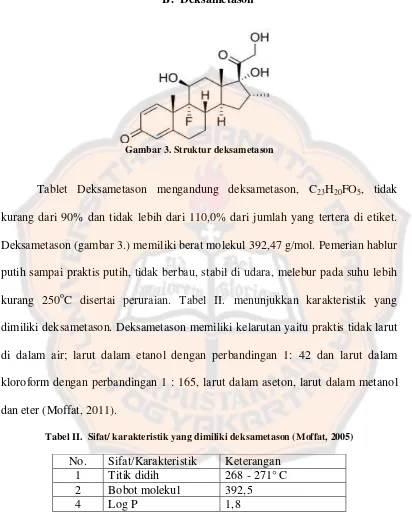
Gambar 3. Struktur deksametason
Tablet Deksametason mengandung deksametason, C23H20FO5, tidak
kurang dari 90% dan tidak lebih dari 110,0% dari jumlah yang tertera di etiket.
Deksametason (gambar 3.) memiliki berat molekul 392,47 g/mol. Pemerian hablur
putih sampai praktis putih, tidak berbau, stabil di udara, melebur pada suhu lebih
kurang 250oC disertai peruraian. Tabel II. menunjukkan karakteristik yang
dimiliki deksametason. Deksametason memiliki kelarutan yaitu praktis tidak larut
di dalam air; larut dalam etanol dengan perbandingan 1: 42 dan larut dalam
kloroform dengan perbandingan 1 : 165, larut dalam aseton, larut dalam metanol
dan eter (Moffat, 2011).
Tabel II. Sifat/ karakteristik yang dimiliki deksametason (Moffat, 2005)
No. Sifat/Karakteristik Keterangan
1 Titik didih 268 - 271° C
2 Bobot molekul 392,5
4 Log P 1,8
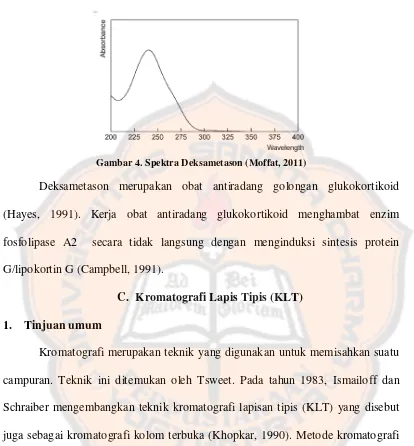
Berdasarkan struktur molekul, deksametason memiliki gugus kromofor
merupakan senyawa yang memiliki panjang gelombang maksimum 240 nm pada
pelarut metanol (Moffat, 2011).
Gambar 4. Spektra Deksametason (Moffat, 2011)
Deksametason merupakan obat antiradang golongan glukokortikoid
(Hayes, 1991). Kerja obat antiradang glukokortikoid menghambat enzim
fosfolipase A2 secara tidak langsung dengan menginduksi sintesis protein
G/lipokortin G (Campbell, 1991).
C. Kromatografi Lapis Tipis (KLT) 1. Tinjuan umum
Kromatografi merupakan teknik yang digunakan untuk memisahkan suatu
campuran. Teknik ini ditemukan oleh Tsweet. Pada tahun 1983, Ismailoff dan
Schraiber mengembangkan teknik kromatografi lapisan tipis (KLT) yang disebut
juga sebagai kromatografi kolom terbuka (Khopkar, 1990). Metode kromatografi
merupakan metode yang digunakan untuk menentukan jenis komponen terpisah
(analisis kualitatif) dan metode penentuan jumlah komponen-komponen tersebut
(analisis kuantitatif) (Harjadi, 1986).
Metode KLT memiliki kelebihan antara lain sederhana, pemisahannya
KLT-densitometri (Khopkar, 1990). Proses pengembangan kromatogram terjadi ketika
fase gerak melewati lokasi bercak dan fase diam (permukaan partikel-partikel/di
dalam pori-pori partikel maupun terbagi ke dalam sejumlah cairan yang terikat di
permukaan atau dalam pori). Sampel melintasi plat dengan bantuan aksi
kapilaritas fase gerak (Dean, 1995).
Mekanisme pemisahan yang terjadi pada kromatografi lapis tipis dengan
fase diam silika adalah mekanisme adsorpsi. Mekanisme tersebut merupakan
mekanisme pemisahan dengan penyerapan analit pada permukaan yang
melibatkan interaksi-interaksi elektrostatik seperti ikatan hidrogen, penarikan
dipol-dipol, dan penarikan yang diinduksi oleh dipol (Rohman, 2009). Jika
digunakan fase diam yang bersifat polar, fase gerak yang polar akan diadsorbsi
lebih kuat dibanding yang kurang polar. Hal ini berlaku sebaliknya pada fase diam
non polar. Kompetisi terjadi antara substansi yang dianalisis dan fase gerak pada
permukaan adsorben. Semakin polar substansi yang dikromatografi dibanding fase
gerak, maka substansi akan semakin kuat diadsorbsi dibanding fase gerak. Hal
sebaliknya, jika fase gerak lebih kuat diadsorbsi maka fase gerak akan
menggantikan molekul yang dikromatografi sehingga dapat dielusi bersama fase
gerak (Gasparic, 1978).
Kecepatan migrasi solut melalui fase diam ditentukan oleh perbandingan
distribusinya (D) dan besarnya D ditentukan afinitas relatif solut pada kedua fase.
Nilai D adalah perbandingan konsentrasi solut dalam fase diam (Cs) dan dalam
sebaliknya. Jika perbedaan perbandingan distribusi solut cukup besar maka
campuran-campuran solut akan mudah dan cepat dipisahkan (Rohman, 2009).
2. Sistem KLT a. Fase Diam
Biasanya sering digunakan sebagai materi adalah silika gel, bubuk
selulosa, tanah diatome, dan kieselguhr. Mekanisme sorpsi desorpsi yang utama
pada KLT adalah partisi dan adsorbsi (Rohman, 2009). Gel silika adalah bentuk
dari silikon dioksida (silika). Atom silikon dihubungkan oleh atom oksigen dalam
struktur kovalen yang besar. Struktur permukaan gel silika (gambar 5.)
menunjukkan bahwa atom silikon berlekatan pada gugus –OH.
Gambar 5. Struktur gel silika (Habtemariam, 2006)
b. Fase Gerak
Sistem paling sederhana dari fase gerak KLT adalah campuran 2 pelarut
organik yang diatur komposisinya sehingga memiliki daya elusi dan sifat tertentu
agar pemisahan optimal. Tabel 3. menunjukkan nilai sifat pelarut yang biasa
digunakan sebagai fase gerak. Menurut Rohman (2009), berikut adalah petunjuk
dalam memilih dan mengoptimasi fase gerak:
1. fase gerak harus mempunyai kemurnian yang sangat tinggi,
2. daya elusi fase gerak harus diatur sedemikian rupa sehingga nilai Rf solut
terletak antara 0,2-0,8 untuk memaksimalkan pemisahan,
3. pemisahan dengan fase diam polar seperti silika gel akan ditentukan pula
oleh polaritas fase gerak yang menentukan kecepatan migrasi solut
3. Aplikasi penotolan sampel
Hal yang harus diperhatikan dalam analisis dengan KLT adalah penotolan
sampel. Jika jumlah sampel yang ditotolkan dalam jumlah banyak dan secara
manual, maka waktu yang dibutuhkan untuk penotolan menjadi relatif lebih lama
dan reprodusibilitasnyarendah. Penotolan sampel secara otomatis dengan
menggunakan autosampler lebih dipilih daripada penotolan secara manual
terutama jika sampel yang ditotolkan lebih dari 15 L. Parameter aplikasi yang
direkomendasikan dalam penotolan sampel adalah secara otomatis dengan
diameter bercak 2 mm untuk volume sampel 0,5 L, konsentrasi sampel
0,02-0,2% dan banyaknya sampel 1-10 g untuk KLT konvensional, 0,1-1 g untuk
KLT kinerja tinggi. Untuk memperoleh reprodusibilitas yang baik, volume sampel
penotolan paling sedikit 0,5 L (Rohman, 2009). Volume sampel yang dapat
diaplikasikan sebagai titik adalah 0,5-5 L pada KLT konvensional (Sherma,
1996).
Penotolan sampel dapat dilakukan dalam bentuk bercak, pita, dan zig zag.
Bentuk penotolan sampel yang disarankan dalam analisis adalah bentuk pita.
Bentuk pita berada dalam bentuk yang sesempit mungkin dan menghasilkan
resolusi sampel terjamin (Gozan, 2002 cit. Rohman, 2009).
4. Penilaian kromatogram a. Faktor retardasi
Faktor Retardasi (Rf) adalah jarak yang ditempuh senyawa dibagi dengan
jarak yang ditempuh fase gerak. Jika dibandingkan senyawa berbeda dengan
kondisi sistem kromtografi yang sama, senyawa yang memiliki Rf lebih kecil
sedangkan senyawa dengan nilai Rf yang lebih besar bersifat kurang polar karena
berinteraksi kurang kuat terhadap fase diam polar dari plat KLT (Anonim2, 2010).
Nilai Rf berfungsi untuk mengidentifikasi senyawa. Nilai Rf untuk
senyawa yang diidentifikasi dapat dibandingkan dengan nilai Rf dari senyawa
standar baku (Clark, 2007).
Faktor yang mempengaruhi nilai Rf pada KLT adalah aktivitas lapisan,
ketebalan, keseragaman, jarak elusi, jumlah sampel yang diaplikasikan, pelarut,
kehadiran substansi lain, ukuran, bentuk chamber, dan perubahan temperatur.
Bercak yang dihasilkan dalam KLT dipengaruhi oleh beberapa faktor, yaitu
kelebihan jumlah sampel yang ditotolkan, penguapan fase gerak selama
pengembangan, kehadiran substansi lain dan perubahan temperatur (Gasparic,
1978).
b. Nilai Faktor Asimetris
Nilai Faktor Asimetris (As) adalah parameter yang digunakan untuk mengidentifikasi bentuk puncak. Nilai faktor asimetris diukur pada 10% tinggi
puncak dari dasar. Nilai untuk puncak simetris adalah 1. Nilai faktor asimetris
0,95-1,10 masih dikatakan baik (Rohman, 2009).
Hasil pemisahan kromatografi senyawa campuran akan berbentuk profil
Gaussian dalam arah aliran fase gerak. Bentuk profil ini berupa puncak atau pita.
Profil Gaussian secara perlahan akan melebar dan terkadang membentuk profil
yang asimetris. Profil yang asimetris terbentuk karena solut melanjutkan migrasi
ke fase diam. Beberapa penyebab terjadinya pelebaran pucak kromatografi, yaitu:
Keadaan di mana beberapa molekul meninggalkan kolom tidak bersamaan
akibat diversi selama perjalanan. Fenomena ini dapat dijelaskan dengan
gambar 6.
Gambar 6. Ilustrasi pengaruh difusi Eddy pada pelebaran puncak (Honrath, 1995)
2.) Difusi longitudinal
Spesies solut menyebar ke segala arah dengan difusi ketika berada di
dalam fase gerak. Difusi terjadi dengan arah yang sama dan berlawanan
dengan aliran fase gerak. Fenomena ini dapat dijelaskan dengan gambar 7.
Gambar 7. Ilustrasi pengaruh difusi longitudinal pada pelebaran puncak (Scott, 2008)
3.) Transfer massa
Transfer massa terjadi antara fase gerak, fase gerak stagnan, dan fase
diam. Profil konsentrasi dalam fase diam tertinggal sedikit dibanding
profil konsentrasi dalam fase gerak yang akan mengakibatkan adanya
pelebaran puncak. Desorpsi yang lambat juga menghasilkan puncak yang
antara partikel fase diam dalam gerakan laminar. Kecepatan alir fase gerak
lebih cepat jika melalui pusat saluran dibanding fase gerak di dekat
partikel fase diam (Rohman, 2009). Fenomena ini terlihat pada gambar 8.
Gambar 8. Ilustrasi pengaruh transfer massa pada pelebaran puncak (Scott, 2008)
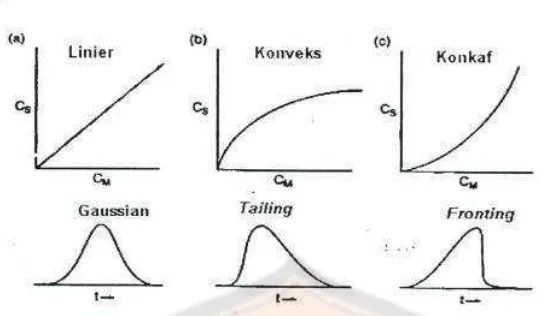
Profil konsentrasi solut yang bermigrasi akan simetris jika rasio distribusi
solut (D) konstan selama kisaran konsentrasi keseluruhan puncak, seperti
ditunjukkan oleh isoterm sorpsi yang linear berupa plot konsentrasi solut dalam
fase diam (Cs) tehadap konsentrasi solut dalam fase gerak (Cm). Gambar 9.
menunjukkan berbagai macam bentuk puncak pada kromatogram. Puncak
asimetris disebabkan oleh ukuran sampel yang dianalisis terlalu besar dan
interaksi yang kuat antara solut dengan fase diam. Solut menjadi sukar terelusi
sehingga menyebabkan terbentuknya puncak yang mengekor (Gandjar dan
Gambar 9. Isoterm sorpsi dan profil puncak. (a). isoterm linear (b). puncak tailing (c).puncak fronting (Gandjar dan Rohman, 2007)
c. Resolusi
Resolusi (Rs) adalah parameter yang menggambarkan rentang pemisahan
2 puncak yang saling berdekatan. Nilai Rs harus mendekati atau lebih dari 1,5
karena akan memberikan pemisahan puncak yang baik (baseline resolution)
(Gandjar dan Rohman, 2007).
(1)
Persamaan (1) menunjukkan komponen yang sangat berpengaruh terhadap
pemisahan. Komponen tersebut adalah ∆Rf yang merupakan selisih Rf maksimum
dari masing-masing solut (max Rf1 dan max Rf2) serta lebar puncak
masing-masing komponen yang dipisahkan (W1 dan W2). W1 dihitung dari selisih nilai
end Rf1 dikurangi start Rf1. W2 dihitung dari selisih nilai end Rf2 dikurangi start
Gambar 10. Pemisahan dua senyawa (Sherma dan Fried, 1996)
d. Presisi
Presisi merupakan ukuran derajat kesesuaian antara hasil uji individual
diukur melalui penyebaran hasil individual rata-rata jika prosedur diterapkan
secara berulang pada sampel-sampel yang diambil dari campuran yang homogen.
Presisi diukur sebagai simpangan baku atau simpangan baku relatif (koefisien
variansi). Kriteria seksama diberikan jika metode memberikan simpangan baku
relatif (RSD) atau koefisien variansi (KV) 2 % atau kurang (Riyadi, 2009).
D. Densitometri
Densitometri merupakan salah satu metode analisis KLT kuantitatif.
Metode ini dilakukan dengan cara mengukur kerapatan bercak senyawa uji yang
dipisahkan, dibandingkan dengan kerapatan bercak senyawa standar yang dielusi
bersama-sama. Syarat-syarat senyawa standar adalah murni, inert, dan stabil
(Hardjono, 1983).
Densitometri digunakan untuk pengukuran kuantitatif in situ dari substansi
yang terpisah pada KLT. Metode analisis instrumental ini didasarkan pada
interaksi radiasi elektromagnetik dengan analit berupa bercak hasil pemisahan
KLT. Densitometri mengevaluasi bercak analit hasil KLT dalam kadar kecil
secara kuantitatif. Bercak dideteksi dengan sumber sinar dalam celah (slit) yang
Rf1
dapat diatur panjang dan lebarnya. Sinar yang dipantulkan atau ditransmisikan
diukur dengan fotosensor. Banyaknya analit yang terbaca adalah berdasarkan
perbedaan antara sinyal optik daerah yang tidak mengandung bercak dengan
daerah yang mengandung bercak dalam lempeng yang sama (Rohman, 2009).
Substansi-substansi dipisahkan dengan KLT dikuantifikasi dengan
pengukuran absorbansi secara in situ cahaya sinar tampak, UV, atau sinar
fluoresensi. Absorpsi sinar UV dihitung baik pada lapisan yang mempunyai
kandungan fosfor yang mampu mendukung pengukuran ataupun pada lapisan
yang fosfornya tidak mendukung. Hasilnya memperlihatkan daerah gelap dengan
latar belakang yang berfluoresen (pemadaman fluoresen). Hanya substansi yang
spektra absorpsinya melampaui spektrum dari fosfor yang akan terlihat dengan
metode ini (Sherma, 1996).
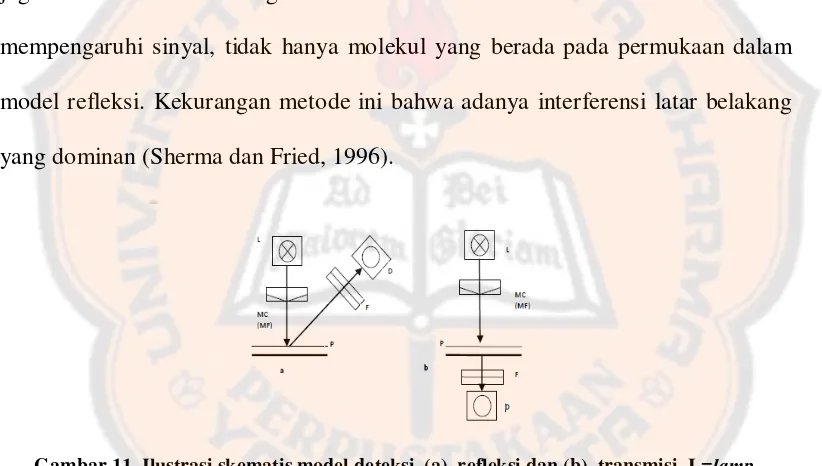
Secara umum, densitometri terbagi menjadi 2 model pembacaan yakni
model refleksi dan transmitan (Sherma dan Fried, 1996). Model refleksi
mengukur jumlah cahaya yang dipantulkan dari permukaan dengan menggunakan
lampu yang berbeda sebagai sumber cahaya UV/Vis. Lampu halogen dan tungsten
untuk menghasilkan cahaya visibel sedangkan lampu deuterium menghasilkan
cahaya UV. Lampu merkuri umumnya digunakan untuk menghasilkan cahaya
dalam kisaran UV dan visibel. Monokromator digunakan untuk menghasilkan
cahaya monokromatik. Cahaya yang direfleksikan kemudian diukur dengan
photomultiplier, fotodioda, dan fotoresistor. Hasil pembacaan dikonversikan ke
dalam sinyal tertentu. Kekurangan dari model ini adalah pengaruh posisi bercak
perbedaan konsentrasi profil sampel dan standar. Begitu pula perlakuan terhadap
plat setelah dikromatografi juga menyebabkan adanya variasi (Sherma dan
Fried,1996).
Model transmitan mengukur absorbansi substansi dalam kisaran visibel.
Detektor fotometrik mengukur intensitas cahaya yang ditransmisikan pada sisi
plat. Sinyal ini merupakan fungsi banyaknya molekul yang mengabsorbsi cahaya
dari lampu. Kelebihan model ini adalah fluktuasi transmisi yang diakibatkan
perbedaan posisi dari bercak dan gradien konsentrasi dapat diabaikan. Model ini
juga lebih sensitif dibanding model refleksi karena semua molekul dalam bercak
mempengaruhi sinyal, tidak hanya molekul yang berada pada permukaan dalam
model refleksi. Kekurangan metode ini bahwa adanya interferensi latar belakang
yang dominan (Sherma dan Fried, 1996).
Gambar 11. Ilustrasi skematis model deteksi. (a). refleksi dan (b). transmisi. L=lamp, D=detector, F=cut-off filter (for fluorescence), P=plate, MF=monochromatic filter,
E. Keterangan Empiris
Kombinasi deksametason dan deksklorfeniramin maleat digunakan untuk
mengobati alergi. Dekametason merupakan senyawa netral yang tidak larut dalam
air, agak sukar larut dalam aseton, dalam etanol, dalam dioksan dan dalam
metanol. Deksametason dalam tablet mengandung deksametason C23H20FO5 tidak
kurang dari 90,0 % dan tidak lebih dari 110,0 % dari jumlah tertera di etiket.
Deksametason dalam metanol memiliki maks 240 nm. Deksklorfeniramin
maleat dalam tablet mengandung tidak kurang dari 90,0 % dan tidak lebih dari
110,0 % C20H23CIN2O4 dari jumlah yang tertera pada etiket. Deksklorfeniramin
maleat adalah garam basa yang sangat mudah larut dalam air, larut dalam etanol
dan dalam kloroform. Deksklorfeniramin maleat dalam air memiliki maks 261
nm dan dalam 0,1 asam sulfat maks 265 nm.
Sistem yang digunakan dalam metode KLT densitometri pemisahan
kombinasi deksametason dan deksklorfeniramin adalah fase normal. Sistem ini
mengindikasikan bahwa fase diam yang digunakan lebih polar dibandingkan
dengan fase gerak. Senyawa deksametason memiliki kepolaran lebih kecil
dibandingkan dengan deksklorfeniramin maleat. Asumsi yang peneliti perkirakan
bahwa dalam metode pemisahan ini, deksametason akan terelusi lebih cepat
dibandingkan dengan deksklorfeniramin maleat.
Variasi dan optimasi jenis dan komposisi fase gerak akan berpengaruh
terhadap pemisahan senyawa dengan metode ini. Jenis fase gerak yang akan
digunakan merupakan modifikasi dan eksplorasi dari berbagai literatur tentang
tunggal. Penentuan komposisi fase gerak didasarkan pada trial dan error.
Parameter dalam pemisahan senyawa campuran deksametason dan
deksklorfeniramin maleat dengan metode KLT densitometri adalah bentuk puncak
yang simetris dan sempit (nilai faktor asimetris berada dalam kisaran 0,95-1,10),
24
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan jenis rancangan penelitian eksperimental analitik
yang pada subjek uji diberikan perlakuan yaitu jenis dan komposisi fase gerak.
B. Variabel Penelitian 1. Variabel bebas
Variabel bebas dalam penelitian ini adalah perbandingan komposisi fase gerak yang akan dioptimasi.
2. Variabel tergantung
Variabel tergantung pada penelitian ini adalah pemisahan deksametason dan
deksklorfeniramin dalam sediaan kaplet X® yang dilihat dari bentuk puncak
termasuk nilai faktor asimetris (As), nilai Rf, nilai Rs,dan %KV nilai AUC.
3. Variabel pengacau terkendali
a. Kemurnian pelarut yang digunakan, untuk mengatasinya digunakan
pelarut pro analysis.
b. Kemurnian bahan baku yang digunakan, untuk mengatasinya digunakan
bahan baku yang disertai dengan Certificate of Analysis.
c. Paparan cahaya akan mempengaruhi stabilitas dari deksametason
C. Definisi Operasional
1. Deksametason dan Deksklorfeniramin maleat merupakan senyawa aktif
yang sering berada dalam campuran sediaan kaplet X®.
2. Sistem kromatografi lapis tipis (KLT) yang digunakan adalah sistem KLT
fase normal dengan fase diam silika gel 60 F254 dan fase gerak hasil
optimasi.
3. Optimasi dilakukan dengan mengubah-ubah jenis dan komposisi fase gerak
4. Parameter pemisahan optimal komponen dengan KLT densitometri adalah
bentuk puncak termasuk nilai faktor asimetriss (As), nilai faktor retardasi
(Rf), nilai resolusi (Rs), dan %KV nilai AUC.
D. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini baku deksametason (Tianjin
Tianyao Pharmaceuticals Co., Ltd.) dengan kemurnian 99,4%, baku
deksklorfeniramin maleat (Siegfried Ltd.) dengan kemurnian 99,92%, etanol p.a
(E. Merck) , etil asetat p.a (E. Merck), larutan amonia 25 % p.a (E. Merck),
metanol p.a (E. Merck), aquabidest, lempeng KLT silika gel 60 F254 (E. Merck),
sediaan kaplet X®.
E. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah neraca analitik (OHAUS
Carat Series PAJ 1003), densitometer (CAMAG TLC Scanner 3 CAT. No
027.6485 SER. No. 160602), autosampler (Linomat 5 No. 170610), perangkat
lunak WinCats (V.1.4.4), mikropipet scorex, bejana kromatografi dan alat-alat
F. Tata Cara Penelitian 1. Pembuatan larutan baku Deksametason
a. Pembuatan larutan baku deksametason 3,75 mg/mL
Ditimbang seksama lebih kurang 37,5 mg baku deksametason,
dimasukkan ke dalam labu takar 10,0 mL, dilarutkan dengan etanol sampai batas
tanda, sehingga diperoleh larutan baku deksametason dengan konsentrasi 3,75
mg/mL.
b. Pembuatan larutan baku intermediet deksametason 0,30 mg/mL
Ambil larutan baku deksametason sebanyak 2,0 mL konsentrasi 3,75
mg/mL dimasukkan ke dalam labu takar 25,0 mL, dan dilarutkan dengan etanol
sampai batas tanda, sehingga diperoleh larutan baku deksametason dengan
konsentrasi 0,3 mg/mL.
2. Pembuatan larutan baku Deksklorfeniramin maleat
a. Pembuatan larutan baku deksklorfeniramin maleat 5,0 mg/mL
Ditimbang seksama lebih kurang 50,0 mg baku deksklorfeniramin maleat,
dimasukkan ke dalam labu takar 10,0 mL, dan dilarutkan dengan etanol sampai
batas tanda sehingga diperoleh larutan baku deksklorfeniramin maleat dengan
konsentrasi 5,0 mg/mL.
b. Pembuatan larutan baku intermediet deksklorfeniramin maleat 1,0 mg/mL
Ambil larutan baku deksklorfeniramin maleat sebanyak 5,0 mL dengan
konsentrasi 5,0 mg/mL dimasukkan ke dalam labu takar 25,0 mL, dan dilarutkan
dengan etanol sampai batas tanda, sehingga diperoleh larutan baku deksametason
3. Pembuatan larutan baku campuran deksametason dan deksklorfeniramin
telah berisi seri larutan baku deksklorfeniramin maleat. Seri larutan baku
dilarutkan dengan etanol sampai batas tanda, sehingga diperoleh seri larutan baku
campuran deksklorfeniramin maleat dan deksametason dengan konsentrasi 0,1 :
0,03 ; 0,3 : 0,09 dan 0,5 : 0,15 mg/mL.
4. Penentuan panjang elusi
Seri larutan campuran baku deksametason dan deksklorfeniramin maleat
0,3 : 1,0 mg/mL masing-masing ditotolkan sebanyak 1,0 µL pada lempeng silika
gel 60 F254. Semua penotolan dilakukan pada jarak 1 cm antar totolan. Plat
dikembangkan dalam bejana kromatografi yang telah dijenuhi dengan fase gerak
pada berbagai perbandingan campuran. Pengembangan dilakukan setinggi 5, 10,
dan 15 cm. Lempeng silika gel 60 F254 dikeluarkan dan dikeringkan. Bercak zat
aktif dideteksi pada panjang gelombang 254 nm dengan menggunakan KLT
densitometri.
5. Penentuan panjang gelombang pengamatan deksametason dan deksklorfeniramin maleat
Seri larutan campuran baku deksklorfeniramin maleat dan deksametason
0,1 : 0,03 ; 0,3 : 0,09 dan 0,5 : 0,15 mg/mL masing-masing ditotolkan sebanyak
cm antar totolan. Plat dikembangkan dalam bejana kromatografi yang telah
dijenuhi dengan fase gerak pada berbagai perbandingan campuran. Pengembangan
dilakukan setinggi 5 cm. Lempeng silika gel 60 F254 dikeluarkan dan dikeringkan.
Penentuan panjang gelombang dilakukan dengan merekam scanning pola spektra
absorbsi masing-masing zat aktif pada daerah panjang gelombang 200-400 nm
sehingga didapatkan panjang gelombang overlapping spektra deksametason dan
deksklorfeniramin maleat.
6. Optimasi metode KLT densitometri
a. Pembuatan fase gerak. Masing-masing fase gerak diambil sebanyak volume yang tertera pada tabel V. dan dicampur. Fase gerak yang digunakan untuk
optimasi seperti yang tertera pada tabel berikut:
Tabel V. Komposisi Fase Gerak
Komposisi Komposisi Fase Gerak
Etil asetat (mL) Metanol (mL) Larutan Amonia 25% (mL)
A 25 4 deksklorfeniramin maleat dalam sediaan kaplet X®.
Larutan baku campuran deksklorfeniramin maleat dan deksametason 0,3 :
1,0 mg/mL ditotolkan sebanyak 1,0 µL pada lempeng silika gel 60 F254.
bejana kromatografi yang telah dijenuhi oleh masing-masing jenis dan fase gerak
yang akan dioptimasi. Pengembangan dilakukan dengan panjang elusi yang
didapat dari hasil penentuan panjang elusi. Lempeng silika gel 60 F254
dikeluarkan, ditunggu kering dan bercak zat aktif dideteksi pada panjang
gelombang pengamatan yang telah ditentukan sebelumnya. Pembuatan larutan
campuran deksklorfeniramin maleat dan deksametason dilakukan sebanyak 3 kali
replikasi.
c. Pembuatan larutan sediaan kaplet X®
Satu buah tablet digerus kemudian diencerkan dengan 5 mL etanol dalam
labu takar 10,0 mL, lalu dilakukan sonifikasi selama 2 menit. Kemudian
ditambahkan etanol hingga tanda, selanjutnya larutan disaring.
d. Reprodusibilitas dari fase gerak hasil optimasi.
Tiga seri larutan baku campuran deksklorfeniramin maleat dan
deksametason masing-masing ditotolkan sebanyak 1,0 µL pada lempeng silika gel
60 F254. Tiga replikasi larutan sediaan kaplet X® yang telah dipreparasi juga
ditotolkan sebanyak 1,0 µL pada lempeng silika gel 60 F254 tersebut. Semua
penotolan dilakukan pada jarak 1 cm antar totolan. Plat dikembangkan dengan
bejana kromatografi yang telah dijenuhi oleh fase gerak. Pengembangan
dilakukan dengan menggunakan jarak elusi hasil optimasi. Lempeng silika gel 60
F254 dikeluarkan ditunggu kering dan bercak zat aktif dideteksi pada panjang
gelombang hasil pengamatan yang telah ditentukan sebelumnya. Parameter
puncak hasil pemisahan, dan %KV nilai AUC yang didapat dari 3 kali replikasi
larutan sediaan kaplet X®.
G. Analisis Hasil
Hasil optimasi metode pemisahan deksametason dan deksklorfeniramin
maleat dalam sediaan kaplet X® dinilai dari densitogram hasil pemisahan dengan
variasi jenis dan komposisi fase gerak. Parameter-parameter dasar KLT
densitometri untuk pemisahan yang baik dan optimal dilihat dari bentuk puncak,
faktor retardasi, resolusi dan %KV nilai AUC.
1. Bentuk puncak
Bentuk puncak yang simetris ditentukan dari nilai faktor asimetriss puncak
(As) dapat dihitung dengan cara sebagai berikut :
Gambar 12. Menentukan nilai faktor asimetris
dimana
As = nilai faktor asimetris
a = lebar setelah puncak pada ketinggian 10%dari bawah
b = lebar sebelum puncak pada ketinggian 10% dari bawah (Rohman, 2009 ).
3. Resolusi (Rs)
Nilai resolusi dapat dihitung dengan cara sebagai berikut :
Rs =
(2)
dimana :
Rs = nilai resolusi
t1 = jarak geometrik bagian tengah pada puncak 1
t2 = jarak geometrik bagian tengah pada puncak 2
W1 = lebar puncak pada puncak 1
W2 = lebar puncak pada puncak 2 (Gandjar dan Rohman, 2007).
4. % Koefisien Variasi (%KV)
%KV = x 100% (3)
dimana : %KV = koefisien variasi SD = standar deviasi
x = rata-rata (Riyadi, 2009).
2 (t2-t1)
W1+W2
32 BAB IV
HASIL DAN PEMBAHASAN
Penelitian ini bertujuan untuk mengetahui komposisi fase gerak yang
dapat memberikan pemisahan KLT densitometri yang baik dan optimal.
Parameter-parameter yang menunjukkan pemisahan densitometri yang baik dan
optimal adalah bentuk puncak simetris dan runcing, nilai Rf antara 0,2-0,8, nilai
Rs ≥ 1,5 dan %KV nilai AUC ≤ 2
A. Penentuan Fase Gerak
Optimasi komposisi fase gerak merupakan proses pengoptimalan salah
satu faktor yang mempengaruhi sistem kromatografi. Optimasi menjadi hal yang
penting karena efektivitas metode KLT sangat ditentukan oleh optimalnya suatu
prosedur zat aktif yang memungkinkan pemisahan suatu zat aktif terhadap zat
aktif yang lain. Variasi komposisi fase gerak akan memberikan perbedaan
interaksi antara senyawa campuran dengan fase gerak dan fase diam. Oleh karena
itu, perlu dilakukan optimasi komposisi fase gerak.
Modifikasi fase gerak bertujuan untuk menemukan komposisi fase gerak
yang mampu mengadsorpsi senyawa campuran diantara fase diam dan fase gerak
yang kepolarannya berbeda. Fase gerak dengan kepolaran yang optimal mampu
membentuk kesetimbangan sorpsi dan desorpsi senyawa pada fase diam dengan
optimal.Kesetimbangan ini dapat dicapai bila fase gerak yang digunakan optimal.
Penentuan fase gerak ini dilakukan dengan melakukan pembelajaran
deksametason adalah senyawa glukokortikoid, sedangkan deksklorfeniramin
maleat adalah senyawa garam amin.
Fase gerak yang digunakan dalam penelitian ini merupakan perbandingan
antara etil asetat, metanol, dan larutan amonia 25%. Jenis fase gerak tersebut
didapatkan dari modifikasi sistem kromatografi untuk kelompok basa-basa
nitrogen (Clarke,1969,1975). Sistem kromatografi yang digunakan adalah fase
diam berupa silika gel GF 254 tebal 0,25 mm yang dikeringkan pada suhu 110o
selama 1 jam dan fase gerak berupa metanol : amonia kuat (100 : 1,5).
Deksklorfeniramin maleat merupakan senyawa yang termasuk dalam kelompok
garam amin. Modifikasi dilakukan karena terdapat deksametason dalam senyawa
campuran yang ingin dipisahkan. Deksametason merupakan senyawa yang relatif
non polar. Modifikasi penambahan etil asetat yang merupakan pelarut dalam
proses ektraksi deksametason (Clarke,1969,1975) diharapkan bisa
mengoptimalkan pemisahan campuran deksametason dan deksklorfeniramin
maleat.
Larutan amonia 25% dalam komposisi fase gerak digunakan sebagai
modifiers. Larutan amonia 25% akan mengkondisikan pH fase gerak di keadaan
basa (± 6,5 – 11,95). Deksklorfeniramin maleat merupakan garam amin yang
memiliki mobilitas sangat rendah pada fase diam yang bersifat asam karena
senyawa deksklorfeniramin maleat akan terion di pH asam. Oleh karena itu,
penambahan larutan amonia 25% digunakan untuk menjaga agar senyawa
deksklorfeniramin maleat tetap dalam bentuk molekul. Deksklorfeniramin maleat
B. Pembuatan Larutan Baku
Pada penelitian ini digunakan baku deksametason (Tianjin Tianyao
Phamaceuticals) dengan kemurnian 99,4% dan baku deksklorfeniramin maleat
kemurnian 99,92% (Siegfried Ltd). Kedua baku ini dilarutkan dalam etanol.
Etanol p.a digunakan karena kedua baku tersebut dapat larut dalam etanol dan
menyerap pada panjang gelombang yang lebih rendah dari 185 nm, sehingga
dapat digunakan sebagai pelarut untuk pekerjaan dalam daerah UV dekat.
Larutan baku campuran dibuat untuk memastikan bahwa zat aktif yang
akan dianalisis dalam sampel memiliki kesamaan atau kedekatan spektra dengan
larutan baku. Selain itu, larutan baku campuran dibuat sebagai simulasi keadaan
zat aktif yang berada dalam sediaan kaplet X®.
Pembuatan baku campuran berfungsi untuk menemukan jenis dan
komposisi fase gerak yang optimal. Saat ditemukan fase gerak yang optimal,
dibuat level larutan baku campuran deksametason dan deksklorfeniramin maleat,
yaitu baku deksametason konsentrasi 0,03, 0,09 dan 0,15 mg/mL dan baku
deksklorfeniramin maleat dengan konsentrasi 0,1, 0,3 dan 0,5 mg/mL. Level
larutan baku ini diperoleh dari hasil orientasi.
Optimasi dilakukan pada larutan baku campuran karena apabila keadaan
sistem yang optimal telah ditetapkan pada baku campuran, maka kondisi yang
serupa juga diharapkan dapat diaplikasikan pada sampel untuk memperoleh
pemisahan dan bentuk puncak yang dinilai optimal. Penggunaan tiga level
campuran larutan ini digunakan untuk mengetahui respon detektor yang muncul
puncak zat aktif (Area Under Curve/AUC) pada fase gerak yang sudah
teroptimasi.
C. Penentuan Panjang Jarak Elusi
Dalam proses optimasi, penentuan panjang jarak elusi penting untuk
dilakukan. Semakin pendek jarak elusi, semakin singkat waktu pengembangan
oleh fase gerak. Hal itu akan memperkecil kemungkinan terjadinya difusi selama
pemisahan (Spangenberg dkk., 2010). Pemisahan senyawa campuran dengan jarak
lebih pendek dan sesuai dengan nilai parameter-parameter sistem yang akan
dipilih.
Tabel VI. Nilai Rf, Nilai Faktor Asimetris (As), Rs ,dan lama pengelusian larutan baku campuran deksametason dan deksklorfeniramin maleat
Tabel VI. menunjukkan bahwa panjang jarak elusi 5 cm menjadi pilihan
optimal karena semakin pendek jarak pengembangan, semakin singkat waktu
pengembangan oleh fase gerak. Hasil kromatogram juga menunjukkan kesesuaian
dengan nilai parameter sistem. Parameter dalam pemisahan senyawa campuran
deksametason dan deksklorfeniramin maleat dengan metode KLT densitometri
adalah bentuk puncak yang bentuk puncak simetris dan sempit (nilai As berada
dalam kisaran 0,95-1,10), nilai Rf antara 0,2-0,8, dan nilai Rs ≥ 1,5.
D. Optimasi Metode Pemisahan Deksametason dan Deksklorfeniramin Maleat dalam sediaan tablet X® dengan
Kromatografi Lapis Tipis Densitometri 1. Penentuan panjang gelombang pengamatan deksametason dan
deksklorfeniramin maleat
Penentuan panjang gelombang pengamatan bertujuan untuk menentukan
panjang gelombang optimal yang akan digunakan dalam deteksi bercak
deksametason dan deksklorfeniramin maleat. Densitometer yang digunakan akan
membaca kedua senyawa dalam satu kali deteksi. Penentuan panjang gelombang
pengamatan dilakukan dengan deteksi masing-masing baku deksametason dan
deksklorfeniramin maleat. Deteksi senyawa campuran dilakukan pada panjang
gelombang 200 – 400 dengan menggunakan lampu deuterium. Panjang
gelombang 200 – 400 nm termasuk dalam panjang gelombang ultraviolet (UV).
Oleh karena itu, syarat senyawa campuran yang akan dianalisis dengan panjang
gelombang tersebut harus memiliki gugus kromofor dan auksokrom (Rohman dan
Gandjar, 2007).
Gugus kromofor akan memberikan serapan ketika dipaparkan sinar UV
sehingga terbaca sebagai puncak dalam densitogram, sedangkan gugus auksokrom
berperan dalam pergeseran panjang gelombang dan intensitas serapan maksimal
senyawa. Berikut ini merupakan gugus kromofor dan auksokrom yang terdapat
Gambar 13. Gugus kromofor deksametason
Gambar 14. Gugus kromofor dan auksokrom deksklorfeniramin maleat
Keterangan:
Berikut adalah spektra serapan baku deksametason dan deksklorfeniramin maleat:
Gambar 15. Spektra serapan seri larutan rendah, sedang, dan tinggi senyawa campuran deksametason dan deksklorfeniramin maleat
Tabel VII. Data pengukuran panjang gelombang pengamatan deksametason dan deksklorfeniramin maleat
Deksklorfeniramin maleat merupakan senyawa yang memiliki panjang
gelombang serapan maksimal (λmaks) 265 nm pada pelarut asam (Moffat, 2011).
Pola spektra serapan (gambar 15.) menunjukkan adanya pergeseran sebesar 3 nm
antara panjang gelombang hasil pengamatan dan literatur. Pergeseran panjang
gelombang diakibatkan oleh perbedaan kondisi pengujian saat penelitian dengan
kondisi pengujian literatur seperti instrumen analisis dan pelarut. Dalam 245 nm
percobaan digunakan densitometer untuk mengukur λmaks deksklorfeniramin
maleat sedangkan dalam literatur digunakan spektrofotometer UV.
Deksametason, dilihat dari densitogram (gambar 14), memiliki panjang
gelombang serapan maksimal (λmaks) sebesar 245 nm. Deksametason merupakan
senyawa yang memiliki panjang gelombang maksimum 240 nm pada pelarut
metanol (Moffat, 2011). Hal ini menunjukkan adanya pergeseran panjang
gelombang karena pergantian pelarut dan instrumen analisis.
Panjang gelombang pengamatan ditentukan dengan melihat spektra hasil
perpotongan (spektra overlapping) deksametason dan deksklorfeniramin maleat.
Berdasarkan tabel VII, panjang gelombang pengamatan yang digunakan adalah
262 nm dengan pertimbangan bahwa pada panjang gelombang tersebut dapat
membaca serapan kedua zat aktif, yaitu deksametason dan deksklorfeniramin
maleat dalam satu kali deteksi.
2. Optimasi Fase gerak untuk pemisahan deksametason dan deksklorfeniramin maleat dalam sediaan tablet® dengan KLT densitometri
Optimasi dilakukan dengan KLT densitometri pada panjang gelombang
pengamatan 262 nm. Kromatografi teknik ascending digunakan dengan jarak
pengembangan 5 cm dalam chamber yang telah dijenuhkan dengan fase gerak.
Penjenuhan berfungsi untuk memastikan chamber telah jenuh dengan fase uap
yang dibentuk fase gerak organik, sehingga fase uap mampu melapisi fase diam
yang akan dielusi. Hal tersebut akan mempercepat proses elusi.
Fase diam yang digunakan adalah silika gel F254 karena silika gel memiliki
yang efisien. Permukaan silika gel memiliki situs adsorpsi (adsorption site)
berupa gugus silanol (Si-OH) dan gugus siloksan (Si-O- Si). Gugus silanol dapat
membentuk interaksi hidrogen dengan zat aktif. Selain dengan zat aktif, gugus
silanol dapat membentuk interaksi hidrogen dengan air yang membuat silika gel
terdeaktivasi. Oleh karena itu, silika gel harus dipanaskan pada suhu 120o selama
30 menit. Hal ini dilakukan untuk mengaktivasi kembali permukaan silika gel
sehingga gugus silanol dapat berinteraksi dengan zat aktif.
Puncak baku yang muncul dalam densitogram digunakan untuk analisis
data As, Rf, dan Rs sebagai respon untuk mendefinisikan kondisi yang optimal.
Sistem kromatografi yang digunakan dalam pemisahan deksametason dan
deksklorfeniramin maleat adalah fase normal, yang artinya fase diam bersifat
lebih polar dibandingkan fase gerak yang digunakan. Suatu zat dapat dipisahkan
dari zat lain dengan KLT densitometri bila zat memiliki interaksi dengan fase
diam dan fase gerak. Beberapa jenis dan komposisi fase gerak dan pengaruhnya
terhadap baku deksametason dan deksklorfeniramin maleat dipaparkan dalam
Tabel VIII. Nilai Rf dan As larutan baku deksametason (D) dan deksklorfeniramin maleat (DM) pada berbagai komposisi fase gerak
Jenis dan Komposisi
0,61-0,63 0,74-0,75 1,128 Fronting
Etil asetat p.a : metanol p.a : larutan amonia 25%
p.a (25:4:1)