APLIKASI METODE RATIO ABSORBANCE PADA
PENETAPAN KADAR ISONIAZID DAN VITAMIN B6 DALAM SEDIAAN TABLET SECARA SPEKTROFOTOMETRI
ULTRAVIOLET SKRIPSI
OLEH:
COKY F L SIMANJUNTAK NIM 141501118
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2019
APLIKASI METODE RATIO ABSORBANCE PADA
PENETAPAN KADAR ISONIAZID DAN VITAMIN B6 DALAM SEDIAAN TABLET SECARA SPEKTROFOTOMETRI
ULTRAVIOLET SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara
OLEH:
COKY F L SIMANJUNTAK NIM 141501118
PROGRAM STUDI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2019
KATA PENGANTAR
Puji dan syukur penulis ucapkan kepada Tuhan Yang Maha Esa atas segala limpahan rahmat dan karunia-Nya sehingga penulis dapat menjalani masa perkuliahan dan penelitian hingga akhirnya menyelesaikan penyusunan skripsi dengan judul “ Aplikasi Metode Ratio Absorbance Pada Penetapan Kadar Isoniazid dan Vitamin B6 Dalam Sediaan Tablet Secara Spektrofotometri Ultraviolet”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi dari Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini, penulis ingin menyampaikan terima kasih kepada Ibu Prof. Dr. Masfria, M.S., Apt., selaku Dekan Fakultas Farmasi dan Ibu Dr. Poppy Anjelisa Zaitun Hasibuan, M.Si., Apt., selaku Wakil Dekan I Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas selama masa pendidikan dan penelitian.
Rasa hormat dan terima kasih yang setulus-tulusnya penulis sampaikan kepada Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt., selaku pembimbing yang membimbing penulis dengan kesabaran, ketulusan, dan motivasi yang luar biasa selama masa penelitian dan penulisan skripsi, juga kepada Bapak Prof. Dr. Muchlisyam, M.Si., Apt., dan Bapak Drs. Nahitma Ginting, M.Si., Apt., selaku penguji yang telah meluangkan waktu untuk memberikan kritik, saran, dan nasihat yang membangun demi kesempurnaan skripsi ini.
Penulis menyampaikan rasa terima kasih serta penghargaan sebesar- besarnya khususnya kepada orang tua saya Bapak P. Simanjuntak dan Ibu R
Siahaan, dan saudari saya Putri L Simanjuntak, dan Deby C M Simanjuntak, serta seluruh keluarga saya yang senantiasa menyemangati dan memberikan dukungan penuh, doa, serta materil selama perkuliahan hingga penyelesaian skripsi ini.
Pada kesempatan ini juga, penulis ingin menyampaikan rasa terima kasih kepada teman-teman Kelompok Tumbuh Bersama “MIKHA” dan “Vionetta Kylamoreiza”, juga adik-adik kelompok kecil yang terkasih, Koordinasi UP FMIPA 2017 dan 2018, kelompok belajar (TG) Afrizal I Sinaga, Posman A Saragih, Raymond R Barus, Asael H Pardede, Roy I Bangar Siagian, kepada keluarga asuh dan Asisten Laboratorium Kimia Analisis Kualitatif dan lainnya yang telah mendoakan, membantu dan memberikan dukungan serta semangat selama penelitian dan penyusunan skripsi ini berlangsung.
Penulis menyadari bahwa skripsi ini masih memiliki banyak kekurangan dan oleh sebab itu, dengan segala kerendahan hati, penulis bersedia menerima kritik dan saran yang membangun untuk kesempurnaan skripsi ini pada waktu
\mendatang. Semoga skripsi ini dapat bermanfaat dan menjadi sumber informasi tambahan bagi kita semua khususnya bidang analisis farmasi.
Medan, Maret 2019 Penulis,
Coky F L Simanjuntak NIM 141501118
APLIKASI METODE RATIO ABSORBANCE PADA PENETAPAN KADAR ISONIAZID DAN VITAMIN B6 DALAM SEDIAAN TABLET
SECARA SPEKTROFOTOMETRI ULTRAVIOLET ABSTRAK
Latar Belakang : Banyak sediaan farmasi yang mengandung kombinasi bahan aktif. Isoniazid dan vitamin B6 sering dikombinasikan karena kombinasi obat ini memiliki keuntungan dimana vitamin B6 dalam kombinasi ini mencegah efek samping dari Isoniazid (anti tuberkulosis) yaitu efek neuritis perifer. Penentuan kadar isoniazid dan vitamin B6 menggunakan metode Ratio Absorbance merupakan salah satu metode spektrofotometri yang dapat digunakan untuk menentukan kadar obat dalam bentuk campuran. Metode ini menentukan titik isoabsorpsi (absorbsi yang sama) dan lainnya sebagai λmaks salah satu dari dua komponen obat pada kombinasi obat.
Tujuan : Tujuan penelitian ini adalah penetapan kadar campuran isoniazid dan vitamin B6 dengan spektrofotometri ultraviolet secara Ratio Absorbance.
Metode : Pembuatan Laruan Induk Baku isoniazid dan vitamin B6 dan kurva kalibrasi masing masing baku pada panjang gelombang maksimum kedua obat dan panjang gelombang pada tiik isoabsorpsi. Ditumpang tindihkan serapan maksimum isoniazid dan vitamin B6 untuk mendapatkan titik isoabsorpsi.
Dilakukan penetapan kadar pada tablet I dan P dan uji perolehan kembali dengan metode adisi standard dan diukur menggunakan spektrofotometri ultraviolet.
Hasil : Hasil penelitian menunjukkan pada pelarut asam, panjang gelombang maksimum isoniazid adalah 266,6 nm dan vitamin B6 adalah 290,4 nm. Hasil penetapan titik isoabsorpsi adalah 277,4 nm. Hasil kadar isoniazid dan vitamin B6
pada tablet I berturut-turut adalah (99,9689-100,8511)% dan (105,0439- 106,6961)% , dan untuk tablet P kadar masing-masing untuk isoniazid dan vitamin B6 (102,9174-103,7826)% dan (104,12286-107,6114)%. Hasil uji validasi memenuhi persyaratan validasi metode ,untuk isoniazid diperoleh % recovery = 99,84%, simpangan baku relatif/ relative standard deviation (RSD) = 1,10% dan untuk vitamin B6 diperoleh % recovery = 100,70%, simpangan baku relatif/
relative standard deviation (RSD) = 1,21%.
Kesimpulan : Metode spektrofotometri ultraviolet secara Ratio Absorbance dapat digunakan untuk menetapkan kandungan isoniazid dan vitamin B6 secara simultan, dapat digunakan pada campuran isoniazid dan vitamin B6 dan kadar yang diperoleh memenuhi persyaratan menurut Farmakope Indonesia Edisi V.
Kata kunci: Isoniazid, Vitamin B6, Rasio Absorbance, titik isoabsorpsi
APPLICATION OF RATIO ABSORBANCE METHODS ON DETERMINATION OF ISONIAZID AND VITAMIN B6 IN TABLET
DOSAGE BY SPECTROFOTOMETRY ULTRAVIOLET
ABSTRACT
Background : Many pharmaceutical preparations contain a combination of active ingredients. Isoniazid and vitamin B6 are often combined because this combination of drugs has the advantage that vitamin B6 in this combination prevents side effects from Isoniazid (anti tuberculosis), namely the effect of peripheral neuritis. Determination of the levels of isoniazid and vitamin B6 using the Ratio Absorbance method is one of the spectrophotometric methods that can be used to determine the drug content in a mixed form. This method determines the isoabsorption point (the same absorption) and others as λmax one of the two components of the drug in the combination drug.
Objective : The purpose of this study was to determine the content of the mixture of isoniazid and vitamin B6 with ultraviolet spectrophotometry in the Ratio Absorbance.
Method : Making isoniazid and vitamin B6 standard solution and calibration curves are each standard at the maximum wavelength of the two drugs and the wavelength in the isoabsorption tube. Overlapping isoniazid and vitamin B6 maximum uptake to obtain an isoabsorption point. Levels were determined on tablets I and P and the recovery test using the standard addition method was measured using ultraviolet spectrophotometry.
Result : The results showed that in acidic solvents, the maximum wavelength of isoniazid was 266.6 nm and vitamin B6 was 290.4 nm. The result of the isoabsorption point is 277.4 nm. The results of the levels of isoniazid and vitamin B6 in tablets I were (99,9689-100,8511)% and (105,0439-106,6961)%, respectively, and for tablets P the levels for isoniazid and vitamin B6 respectively (102,9174-103,7826)% and (104,1286-107,6114)%. The validation test results met the requirements for method validation, for isoniazid obtained% recovery = 99.84%, standard deviation relative / relative standard deviation (RSD) = 1.10%
and for vitamin B6% recovery = 100.70%, relative standard deviation (RSD) = 1.21%.
Conclusion : The ultraviolet spectrophotometric method by Ratio Absorbance can be used to determine the content of isoniazid and vitamin B6 simultan, can be used in a mixture of isoniazid and vitamin B6 and the levels obtained meet the requirements according to Indonesian Pharmacopoeia V. Edition.
Keywords: Isoniazid, Vitamin B6, Ratio Absorbance, Validation, isoabsorption point
DAFTAR ISI
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
SURAT PERNYATAAN... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
DAFTAR GAMBAR DALAM LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 5
1.5 Manfaat Penelitian ... 5
1.6 Kerangka Pikir Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 7
2.1 Uraian Bahan ... 7
2.1.1 Isoniazid ... 7
2.1.2 Vitamin B6 ... 8
2.2 Tablet Kombinasi Isoniazid dan Vitamin B6 ... 9
2.3 Spektrofotometri Ultraviolet-Visible(UV-Vis) ... 10
2.3.1 Pengertian Spektrofotometri Ultraviolet-Visible ... 10
2.3.2 Instrumen Spektrofotometer... 10
2.3.3 Kegunaan Spektrofotometri Ultraviolet-Visible ... 12
2.3.4 Hukum Lambert-Beer ... 13
2.4 Meode Rasio Absorbance ... 14
2.5 Metode Penambahan Standard ... 16
2.6 Validasi Metode ... 17
2.6.1 Akurasi ... 17
2.6.2 Presisi ... 18
2.6.3 LOD dan LOQ... 19
2.6.4 Linieritas ... 20
BAB III METODE PENELITIAN... 21
3.1 Jenis Penelitian ... 21
3.2 Tempat dan Waktu Penelitian ... 21
3.3 Alat ... 21
3.4 Bahan... 21
3.5 Pengambilan Sampel ... 21
3.6 Prosedur Penelitian... 22
3.6.1 Pembuatan Larutan Induk Baku ... 22
3.6.1.1 Pembuatan Larutan Induk Baku Isoniazid ... 22
3.6.1.2 Pembuatan Larutan Induk Baku Vitamin B6 ... 22
3.6.2 Pembuatan Spektrum Serapan Maksimum ... 22
3.6.2.1 Pembuatan Spektrum Serapan Maksimum Isoniazid ... 22
3.6.2.2 Pembuatan Spektrum Serapan Maksimum Vitamin B6 ... 23
3.6.3 Pembuatan Spektrum Serapan Baku ... 23
3.6.3.1 Pembuatan Spektrum Serapan Baku Isoniazid ... 23
3.6.3.2 Pembuatan Spektrum Serapan Baku Vitamin B6 ... 23
3.6.4 Penentuan Panjang Gelombang Isoabsorpsi dan Panjang Gelombang Maksimum Terpilih ... 23
3.6.4.1 Pembuatan Kurva Kalibrasi Metode Ratio Absorbance Isoniazid ... 24
3.6.4.2 Pembuatan Kurva Kalibrasi Metode Ratio Absorbance Vitamin B6 ... 24
3.6.5 Pembuatan Spektrum Campuran Baku Isoniazid dan Vitamin B6 ... 24
3.7 Penetapan Kadar Isoniazid dan Vitamin B6 ... 24
3.8 Analisis Data Secara Statistik ... 25
3.9 Validasi Metode ... 26
3.9.1 Uji Akurasi ... 26
3.9.2 Presisi ... 26
3.9.3 LOD dan LOQ... 27
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Hasil Penentuan Serapan Maksimum... 28
4.2 Hasil Penentuan Spektrum Serapan Isoniazid dan Vitamin B6 Pada Berbagai Konsentrasi ... 29
4.3 Hasil Spektrum Serapan Campuran Baku Isoniazid dan Vitamin B6 ... 31
4.4 Metode Rasio Absorbance ... 32
4.4.1 Hasil Meode Rasio Absorbance ... 32
4.5 Hasil Validasi Metode ... 34
BAB V KESIMPULAN DAN SARAN ... 38
5.1 Kesimpulan ... 38
5.2 Saran ... 38
DAFTAR PUSTAKA ... 39
LAMPIRAN ... 41
DAFTAR TABEL
4.1 Kadar Isoniazid dan Vitamin B6 dalam Tablet I ... 33
4.2 Kadar Isoniazid dan Vitamin B6 dalam Tablet P ... 33
4.3 Kadar Isoniazid dan Vitamin B6 dalam Tablet I Secara Statistik ... 33
4.4 Kadar Isoniazid dan Vitamin B6 dalam Tablet P Secara Statistik ... 34
DAFTAR GAMBAR
4.1 Spektrum Serapan Maksimum Isoniazid ... 28
4.2 Spekrum Serapan Maksimum Vitamin B6 ... 29
4.3 Spektrum Tumpang Tindih Serapan Maksimum Isoniazid dan Vitamin B6 .. 29
4.4 Spektrum Srapan Isoniazid Pada Berbagai Konsentrasi ... 30
4.5 Spektrum Serapan Vitamin B6 Pada Berbagai Konsentrasi ... 30
4.6 Spektrum Serapan Campuran Isoniazid dan Vitamin B6 ... 31
4.7 Titik isoabsorptif Isoniazid dan Vitamin B6 ... 32
4.8 Spektrum % Perolehan Kembali Rentang Spesifik 80% ... 35
4.9 Spektrum % Perolehan Kembali Rentang Spesifik 100% ... 35
4.10 Spektrum % Perolehan Kembali Rentang Spesifik 120% ... 36
4.11 Kurva Kalibrasi Isoniazid pada 266,6 dan 277,4 ... 37
4.12 Kurva Kalibrasi Vitamin B6 pada 290,4 dan 277,4... 37
DAFTAR LAMPIRAN
1. Perhitungan Pembuatan HCl 0,1 N ... 41
2. Bagan Alir Pembuatan Larutan Induk Baku dan Serapan Maksimum Isoniazid ... 42
3. Bagan Alir Pembuatan Larutan Induk Baku dan Serapan Maksimum Vitamin B6 ... 43
4. Bagan Alir Pembuatan dan Pengukurn Serapan Larutan Standar Isoniazid ... 44
5. Bagan Alir Pembuatan dan Pengukuran Serapan Larutan Standar Vitamin B6 ... 45
6. Bagan Alir Pembuatan Larutan Baku Campuran Isoniazid dan Vitamin B6 .. 46
7. Bagan Alir Penentuan Kadar Isoniazid dan Vitamin B6 dalam Sediaan Tablet I dan P ... 47
8. Bagan Alir Keseluruhan... 48
9. Data Perhitungan Kalibrasi, Persamaan Regresi, dan Koefisien Korelasi Isonazid ... 49
10. Data perhitungan Kalibrasi, Persamaan Regresi, dan Koefisien Korelasi Vitamin B6 ... 50
11. Perhitungan Penetapan Kadar ... 51
12. Contoh Perhitungan Konsentrasi Dengan Metode Rasio Absorbance Dari Isoniazid dan Vitamin B6 dalam Tablet I dan P... 53
13. Data Kadar Isoniazid dan Vitamin B6 Dalam Sediaan Tablet P ... 56
14. Data Kadar Isoniazid dan Vitamin B6 Dalam Sediaan Tablet I ... 57
15. Perhitungan Kadar Isoniazid dan Vitamin B6 Secara Statistik Pada Tablet I . 58 16. Pergitungan Kadar Isoniazid dan Vitamin B6 Secara Statistik Pada Tablet P 61 17. Contoh Perhitungan Kadar Perolehan Kembali Secara Satatistik ... 64
18. Data Hasil Persen Perhitungan Kadar Perolehan Kembali Isoniazid Secara Statistik ... 66
19. Data Hasil Persen Perhitungan Kadar perolehan Kembali Vitamin B6 Secara Statistik ... 67
20. Perhitungan Kadar Perolehan Kembali Isoniaid Secara Statistik ... 68
21. Perhitungan Simpangan Baku, Batas Deteksi (LOD), Batas Kuantitas (LOQ) Isoniazid ... 69
22. Perhitungan Kadar Perolehan kembali Vitamin B6 Secara Statistik... 70
23. Perhitungan Simpangan Baku, Batas Deteksi (LOD), Batas Kuantitas (LOQ) Vitamin B6 ... 71
24. Spektrum Serapan Isoniazid 5,6-16,80 µg/ml dan Vitamin B6 4,4-12,40 µg/ml ... 72
25. Spektrum Serapan Campuran Baku Isoniazid dan Vitamin B6 ... 73
26. Spektrum Serapan Sampel Tablet I dengan pengulangan 6 kali ... 74
27. Spektrum Serapan Uji Perolehan Kembali pada Tablet P ... 77
28. Gambar Alat alat ... 80
29. Gambar Sediaan Tablet I dan P ... 81
30. Sertifikat Pengujian Vitamin B6 ... 82
31. Sertifikat pengujian Isoniazid ... 83
DAFTAR GAMBAR DALAM LAMPIRAN
1 Spektrum Serapan Isoniazid 5,6-16,80 µg/mL ... 73
2 Spekrum Serapan Vitamin B6 4,4-12,4 µg/mL ... 73
3 Spektrum Serapan Campuran Baku Isoniazid (11,2 µg/mL) dan Vitamin B6 (8,40 µg/mL ... 74
4 Pengulangan 1 Spektrum Serapan Sampel Tablet I ... 75
5 Pengulangan 2 Spektrum Serapan Sampel Tablet I ... 75
6 Pengulangan 3 Spektrum Serapan Sampel Tablet I ... 76
7 Pengulangan 4 Spektrum Serapan Sampel Tablet I ... 76
8 Pengulangan 5 Spektrum Serapan Sampel Tablet I ... 77
9 Pengulangan 6 Spektrum Serapan Sampel Tablet I ... 77
10 Rentang Spesifik 80% (Sebelum Penambahan Baku) ... 78
11 Rentang Spesifik 80% (Sesudah Penambahan Baku) ... 78
12 Rentang Spesifik 100% (Sesudah Penambahan Baku) ... 79
13 Rentang Spesifik 100% (Sesudah Penambahan Baku) ... 79
14 Rentang Spesifik 120% (Sesudah Penambahan Baku) ... 80
15 Rentang Spesifik 120% (Sesudah Penambahan Baku) ... 80
16 Spektrofotometer UV-Visible (Shimadzu UV 1800) ... 81
17 Sonicator (Branson 1510) ... 81
18 Neraca Analitik (Boeco) ... 81
19 Tablet Inoxin ... 82
20 Tablet Inha ... 8
BAB I PENDAHULUAN 1.1 Latar Belakang
Menurut Undang-Undang Nomor 36 Tahun 2009, yang dimaksud dengan obat adalah bahan atau paduan bahan yang digunakan untuk mempengaruhi atau menyelidiki sistem fisiologi atau keadaan patologi dalam rangka penetapan diagnosis, pencegahan, penyembuhan, pemulihan, peningkatan kesehatan dan kontrasepsi untuk manusia (Anonim, 2009).
Isoniazid (INH) diperkenalkan pada tahun 1952 sebagai obat yang cukup efektif dalam pengobatan tuberkulosis (Tan dan Rahardja, 2010). INH memiliki kelarutan mudah larut dalam air; agak sukar larut dalam etanol; sukar larut dalam kloroform dan dalam eter (Ditjen POM Depkes RI, 1995).
Piridoksin yang oleh Birch dan kawan-kawan dan dinamakan vitamin B6 dikemukakan kira-kira 40 tahun yang lalu. Piridoksin memiliki kelarutan mudah larut dalam air; sukar larut dalam etanol; tidak larut dalam eter (Ditjen POM Depkes RI, 1995).
Suatu obat dikatakan bermutu jika obat yang digunakan tersebut mempunyai efek terapi yang baik dan aman dalam penggunaannya. Agar mutu obat tersebut tetap terjamin dan efektif dalam pengobatan, maka diperlukan suatu kadar zat aktif yang terkandung dalam sediaan obat tersebut. Untuk mengetahui kadar obat, perlu suatu metode penetapan kadar yang menunjukkan hasil yang baik dan terjamin ketepatan dan ketelitiannya (Armin dkk., 2012).
Campuran isoniazid dan vitamin B6 yang telah ditentukan kadarnya dengan metode spektrofotometri ultraviolet derivatif dengan menggunakan pelarut air suling diperoleh pada derivatif pertama pada panjang gelombang masing-
masing 263 nm dan 290 nm (Pawar dkk., 2012). Dalam buku Clarke’s Analysis of Drugs and Poisons (Moffat dkk., 2011) dituliskan bahwa isoniazid dan vitamin B6
diabsorbsi masing-masing pada panjang gelombang 266 nm dan 290 nm dalam larutan asam.
Metode spektrofotometri secara Ratio Absorbance adalah salah satu metode spektrofotometri yang dapat digunakan untuk analisis campuran beberapa zat secara langsung tanpa harus melakukan pemisahan dan derivatisasi terlebih dahulu walaupun dengan panjang gelombang yang berdekatan, serta dapat menganalisa sediaan obat yang mengandung tiga campuran zat aktif obat yang berbeda memberikan hasil yang baik dan akurat (Modak dkk., 2010). Bila dibandingkan dengan kromatografi cair kinerja tinggi (KCKT), metode spektrofotometri secara Ratio Absorbance relatif lebih sederhana, alat dan biaya operasionalnya lebih murah, waktu analisisnya lebih cepat, serta pengembangan metode spektrofotometri pada saat ini dapat melakukan pengukuran pada campuran zat aktif pada sediaan obat menggunakan lima metode spektrofotometri secara bersamaan (Abdel dkk., 2016).
Metode Ratio Absorbance melibatkan pengukuran absorbansi pada dua panjang gelombang, satu adalah λ max dari salah satu komponen (λ 2) dan yang lainnya adalah panjang gelombang absorptivitas yang sama dari dua komponen (λ 1) yang disebut titik isoabsorpsi.
Beberapa penelitian telah menggunakan metode Ratio Absorbance pada penetapan kadar campuran obat seperti penetapan kadar Paracetamol dan Salisilamida (Armin dkk., 2012), pengembangan dan validasi metode analisis Klorfeniramin Maleat dalam tablet dengan metode Absorbansi (Rivai dkk., 2017), pengembangan dan validasi metode analisis Ranitidin HCl tablet dengan metode
Absorbansi (Chandra dkk., 2016) memberikan hasil yang akurat, presisi dan selektif. Metode spektrofotometri secara ratio absorbance ini tidak memerlukan waktu preparasi sampel yang lama, pelarut yang banyak, perhitungan matematika yang rumit dan proses derivatisasi untuk penentuan nilai zero crossing (Chaudary dkk., 2011).
Persyaratan kadar untuk tablet isoniazid dan tablet vitamin B6 menurut Farmakope Indonesia Edisi V tahun 2014, masing-masing yaitu mengandung isoniazid, C6H7N3O, tidak kurang dari 90,0% dan tidak lebih dari 110,0% dan mengandung piridoksin hidroklorida, C8H11NO3.HCl, tidak kurang dari 95,0%
dan tidak lebih dari 115,0% dari jumlah yang tertera pada etiket.
Berdasarkan uraian diatas, peneliti tertarik umtuk melakukan analisis secara simultan kandungan isoniazid dan vitamin B6 dalam sediaan tablet dengan metode Ratio Absorbance secara spektrofotometri ultraviolet.
1.2.Perumusan Masalah
Berdasarkan latar belakang diatas, maka perumusan masalah dalam penelitian ini adalah sebagai berikut:
1. Apakah metode spektrofotometri ultraviolet secara Ratio Absorbance dapat digunakan untuk menetapkan kandungan isoniazid dan vitamin B6 secara simultan?
2. Apakah kadar campuran isoniazid dan vitamin B6 dalam sediaan tablet yang ditetapkan secara Ratio Absorbance memenuhi persyaratan kadar yang ditetapkan Farmakope Indonesia Edisi V (2014)?
3. Apakah uji validasi terhadap spektrofotometri ultraviolet secara Ratio Absorbance untuk menganalisa secara simultan kandungan isoniazid dan vitamin B6 pada sediaan tablet memenuhi syarat pengujian validasi?
1.3.Hipotesis
Berdasarkan perumusan masalah diatas, maka dibuat hipotesis sebagai berikut:
1. Metode Ratio Absorbance secara spektrofotometri ultraviolet dapat digunakan untuk menetapkan kadar Isoniazid dan Vitamin B6 secara simultan.
2. Kadar Isoniazid dan Vitamin B6 dalam sediaan tablet memenuhi persyaratan Farmakope Indonesia Edisi V (2014).
3. Hasil uji validasi terhadap metode spektrofotometri ultraviolet secara Ratio Absorbance untuk menganalisa secara simultan kandungan Isoniazid
dan Vitamin B6 pada sediaan tablet memenuhi syarat pengujian validasi.
1.4.Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah :
1. Untuk mengaplikasikan metode spektrofotometri ultraviolet secara Ratio Absorbance pada penetapan kandungan isoniazid dan vitamin B6 secara simultan.
2. Untuk mengetahui hasil yang diperoleh pada penetapan kadar campuran isoniazid dan vitamin B6 menggunakan metode spektrofotometri secara Ratio Absorbance dengan persyaratan Farmakope Indonesia Edisi V
(2014).
a. Untuk mengetahui hasil uji validasi terhadap metode spektrofotometri ultraviolet secara Ratio Absorbance kandungan isoniazid dan vitamin B6
secara simultan dalam sediaan tablet dapat memenuhi syarat pengujian validasi.
1.5 Manfaat Peneltian
Diharapkan metode hasil pengembangan dari penelitian ini dapat menjadi salah satu metode yang dapat diaplikasikan oleh industri farmasi terkait dalam menentukan secara simultan kandungan isoniazid dan vitamin B6 pada sediaan tablet.
1.6 Kerangka Pikir Penelitian
Penelitian ini meliputi orientasi panjang gelombang maksimum, titik isoabsorptif dan nilai Ratio Absorbance yang digunakan untuk mendapatkan kadar kemudian metode dan kondisi diaplikasikan terhadap sampel yang beredar dipasaran, selanjutnya metode divalidasi. Secara ringkasnya kerangka pikir penelitian dapat dilihat pada Gambar 1.1
Gambar 1.1 Kerangka pikir penelitian Nilai RA
λ analisis yang digunakan Metode Ratio
Absorbance Isniazid,
Vitamin B6 (BPFI)
Aplikasi pada Sampel
Tablet bermerek dagang yang mengandung : Isoniazid, Vitamin B6
Validasi Metode Linearitas (r) LOD
LOQ
Akurasi (% perolehan kembali) Variabel Terikat Absorbansi (Parameternya adalah
Kesalahan Fotometrik)
Variabel Bebas Jenis Pelarut:
-HCL 0,1 N
BAB II
TINJAUAN PUSTAKA 2.1 Uraian Bahan
2.1.1 Isoniazid
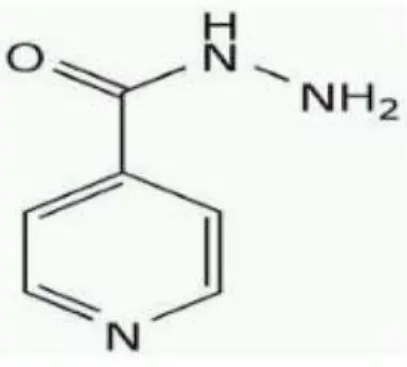
Menurut Kemenkes RI Ditjen BKAK (2014), monografi dari isoniazid adalah sebagai berikut:
Rumus struktur:
Gambar 2.1 Rumus Struktur Isoniazid Nama kimia : Asam isonikotianat hidrazida.
Rumus molekul : C6H7N3O.
Berat molekul : 137,14.
Kandungan : Mengandung tidak kurang dari 98% dan tidak lebih dari 102,% C6H7N30, dihitung terhadat zat yang telah dikeringkan.
Pemerian : Hablur putih atau tidak berwarna atau sebuk hablur putih; tidak berbau; perlahan – lahan dipengaruhi oleh udara dan cahaya.
Kelarutan : Mudah larut dalam air; agak sukar larut dalam etanol; sukar larut dalam kloroform dan dalam eter.
Spektrum ultraviolet : Dalam larutan asam – 266 nm; Dalam larutan alkali – 298 nm.
Isoniazid merupakan anti-mikobakterium lini pertama untuk penyakit tuberkulosis yang paling kuat terhadap Mycobacterium tuberculosis (dalam fase istirahat) dan bersifat bakterisid terhadap basil yang sedang tumbuh pesat. Dalam pengobatannya isoniazid dikombinasi dengan vitamin B6 karena penggunaan isoniazid untuk terapi jangka panjang dapat menyebabkan neuritis perifer misalnya parsites akibat defisiensi vitamin B6 (Tan dan Rahardja, 2010).
2.1.2 Vitamin B6
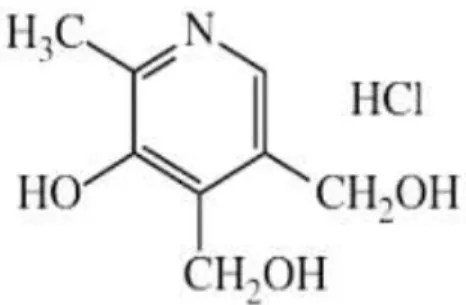
Menurut Kemenkes RI Ditjen BKAK (2014), monografi dari vitamin B6 adalah sebagai berikut:
Rumus struktur:
Gambar 2.2 Rumus Struktur Vitamin B6
Nama kimia : Piridoksol hidroklorida; Pyridoxini hydrochloridum.
Rumus molekul : C8H11NO3.HCl.
Berat molekul : 205,64.
Kandungan : Mengandung tidak kurang dari 98% dan tidak lebih dari 102,0% C8H11NO3.HCI, dihitung terhadap zat yang telah dikeringkan.
Pemerian : Hablur atau serbuk hablur putih atau hampir putih;
stabil di udara; secara perlahan-lahan dipengaruhi oleh cahaya matahari.
Kelarutan : Mudah larut dalam air; sukar larut dalam etanol;
tidak larut dalam eter.
Spektrum ultraviolet : Dalam larutan asam – 290 nm; dalam larutan buffer posfat (pH 6,88) – 254 nm; 324 nm.
Vitamin B6 dalam pengobatan digunakan untuk mencegah dan mengobati defisiensi vitamin B6 dengan gejala berupa kelainan kulit (dermatitis), peradangan lendir mulut dan lidah, kelainan susunan syaraf pusat dan gangguan eritropoetik berupa anemia hipokrom mikrosifer (Tan dan Rahardja, 2010).
2.2 Tablet Kombinasi Isoniazid dan Vitamin B6
Inoxin tablet merupakan kombinasi isoniazid dan vitamin B6. Isoniazid merupakan agen yang paling kuat terhadap penyakit tuberkulosis yang pada umumnya disebabkan oleh Mycobacterium tuberculosis, tetapi tidak pernah diberikan sebagai terapi tunggal dalam pengobatan tuberkulosis aktif. Vitamin B6
dalam terapi penyakit ini untuk mencegah efek samping penggunaan jangka panjang isoniazid yaitu efek neuritis perifer seperti parsitesia, seizures bahkan coma akibat defisiensi vitamin B6 (Tan dan Rahardja, 2010). Tablet isoniazid dan tablet vitamin B6 mengandung masing-masing yaitu isoniazid, C6H7N3O, tidak kurang dari 90,0% dan tidak lebih dari 110,0% dan piridoksin hidroklorida, C8H11NO3.HCl, tidak kurang dari 95,0% dan tidak lebih dari 115,0% dari jumlah yang tertera pada etiket (Kemenkes RI Ditjen BKAK, 2014).
2.3 Spektrofotometri Ultraviolet-Visible (UV-Vis)
2.3.1 Pengertian Spektrofotometri Ultraviolet-Visible
Spektrofotometri UV-Vis merupakan metode analisis berdasarkan pengukuran panjang gelombang dan intensitas sinar ultraviolet dan cahaya tampak yang diabsorpsi oleh sampel, sedangkan alat untuk mengukur transmitan atau absorban suatu sampel sebagai fungsi panjang gelombang disebut spektrofotometer yang terdiri dari spektrometer dan fotometer (Day dan Underwood, 1986). Tetapi spektrum ini sangat berguna untuk pengukuran secara kuantitatif. Sinar ultraviolet berada pada rentang panjang gelombang 200-400 nm sedangkan sinar tampak berada pada panjang gelombang 400-800 nm (Dachriyanus, 2004).
2.3.2 Instrumen Spektrofotometer
Komponen yang penting dari suatu spektrofotometer adalah sebagai berikut:
a. Sumber Cahaya
Sumber cahaya yang biasa digunakan ialah lampu hydrogen atau lampu deuterium untuk pengukuran daerah ultraviolet dan lampu tungsten atau lampu halogen kuarsa untuk pengukuran daerah sinar tampak (Dachriyanus, 2004).
b. Monokromator
Monokromator merupakan piranti optis untuk memencilkan suatu berkas radiasi dari suatu sumber berkesinambungan (Day dan Underwood, 1986).
Panjang gelombang dari sumber cahaya akan dibagi oleh pemisah panjang gelombang (wavelength separator) seperti prisma atau monokromator (Dachriyanus, 2004).
c. Sel
Senyawa yang dapat dianalisis dengan metode spektrofotometri yaitu dalam bentuk larutan tidak berwarna (ultraviolet) atau berwarna (sinar tampak) dan harus jernih sehingga wadah sampel yang digunakan adalah sel transparan untuk menaruh cairan kedalam berkas cahaya spektrofotometer. Sel itu haruslah meneruskan energi cahaya dalam daerah spektral yang diinginkan; sel kaca untuk daerah sinar tampak; sel kuarsa kaca silica untuk daerah ultraviolet. Sel cahaya tampak dan ultraviolet yang khas mempunyai tebal sebesar 1 cm, namun tersedia sel dengan ketebalan yang beragam, mulai dari yg sangat tipis kurang dari 1 mm, sampai 10 cm atau bahkan lebih dari 10 cm (Day dan Underwood, 1986). Pada instrumen berkas berganda, setiap pengukuran membutuhkan sepasang sel absorpsi yang sifat optiknya sama. Sel absorpsi tersebut disebut kembar, karena ukuran alur radiasi, tebal, dan bahan dinding selnya sama, agar sifat transmisi kedua sel itu sama. Sel kembar tidak akan menghasilkan perbedaan pada pembacaannya meskipun digunakan sebagai sel sampel atau sel acuan.
Kekembaran sel diuji dengan mengukur absorban dari sel berisi pelarut (blanko) dan berisi larutan yang mengabsorpsi panjang gelombang yang dipilih untuk penentuan. Perbedaan pembacaan absorban kedua buah sel absorpsi kembar tidak boleh lebih dari 0,002 (Satiadarma dkk., 2004).
d. Detektor
Detektor adalah input transducer, yaitu alat yang menerima sinyal dalam bentuk radiasi elektromagnetik, mengubah dan meneruskan dalam bentuk sinyal listrik ke rangkaian sistem penguat elektronika, dengan demikian sinyal radiasi yang terdeteksi itu dapat diukur kekuatannya (Satiadarma dkk., 2004). Macam- macam deteksi yang telah digunakan paling meluas, didasarkan pada perubahan
fotokimia (terutama fotografi), efek fotolistrik, dan efek termolistrik. Secara umum detektor fotolistrik digunakan dalam daerah tampak dan ultraviolet.
Detektor fotolistrik yang paling sederhana adalah tabung foton. Tabung pengganda foton (photomultiplier) lebih peka daripada tabung foton biasa karena penggandaan yang tinggi dicapai dengan tabung itu sendiri (Day dan Underwood, 1986).
2.3.3 Kegunaan Spektrofotometri Ultraviolet-Visible
Kegunaan utama spektrofotometri ultraviolet adalah untuk analisis kuantitatif. Apabila dalam spektrofotometer terdapat senyawa yang mengabsorpsi radiasi, akan terjadi pengurangan kekuatan radiasi yang mencapai detektor.
Parameter kekuatan energi khas yang diabsorpsi oleh molekul adalah absorban yang dalam batas konsentrasi terendah nilainya sebanding dengan banyaknya molekul yang mengabsorpsi radiasi dan merupakan dasar pemeriksaan kuantitatif (Satiadarma dkk., 2004). Identifikasi kualitatif sangat terbatas daripada daerah dalam inframerah karena pita serapan yang terbentuk terlalu lebar dan kurang terinci sehingga tidak semua gugus fungsi dapat diketahui, hanya gugus-gugus fungsional tertentu seperti karbonil, nitro dan karboksilat menunjukkan puncak yang karakteristik (Day dan Underwood, 1986).
Penyerapan energi cahaya oleh suatu atom atau molekul akan menyebabkan tereksitasinya elektron pada kulit terluar ke tingkat energi yang lebih tinggi. Tipe eksitasi tergantung panjang gelombang cahaya yang diserap.
Sinar ultraviolet dan sinar tampak akan menyebabkan elektron tereksitasi ke orbital lebih tinggi (Dachriyanus, 2004). Elektron yang terlibat pada penyerapan radiasi ultraviolet dan sinar tampak ini yaitu elektron phi (elektron pada ikatannya (pz) saling adu sisi (McMurry, 2008).
Spektrofotometer ini merupakan peralatan yang berbiaya murah sampai sedang dan mempunyai kepekaan analisis yang cukup tinggi. Karena luasnya ragam sediaan farmasi dan bahan biokimia yang menyerap radiasi ultraviolet- visible, maka metode ini banyak dipakai dalam analisis kadar dan analisis klinik
(Dachriyanus, 2004).
2.3.4 Hukum Lambert-Beer
Menurut hukum Lambert, serapan berbanding lurus terhadap ketebalan sel yang disinari, sedangkan menurut hukum Beer, serapan berbanding lurus dengan konsentrasi. Kedua hukum ini digabungkan dalam hukum Lambert-Beer, sehingga diperoleh bahwa intensitas yang diteruskan berbanding lurus terhadap konsentrasi dan ketebalan sel (Rohman, 2007). Hukum Lambert-Beer umumnya dikenal sebagai persamaan berikut:
A= A11. b. c (g/100 mL) atau A= a. b. c (g/L) atau
A= . b. c (mol/L) Keterangan:
A = serapan yang diukur
A11 = serapan larutan (1% b/v) dalam kuvet 1 cm a = absorptivitas
= absorptivitas molar b = ketebalan kuvet (cm) c = konsentrasi larutan
2.4. Metode Ratio Absorbance
Metode ini merupakan pengembangan dari cara simultan yang didasarkan atas hubungan antara harga perbandingan serapan ( “ratio absorbance” ) dengan
kadar suatu zat dalam campuran biner, bahwasanya harga perbandingan serapan suatu larutan pada dua panjang gelombang berbeda adalah tetap.
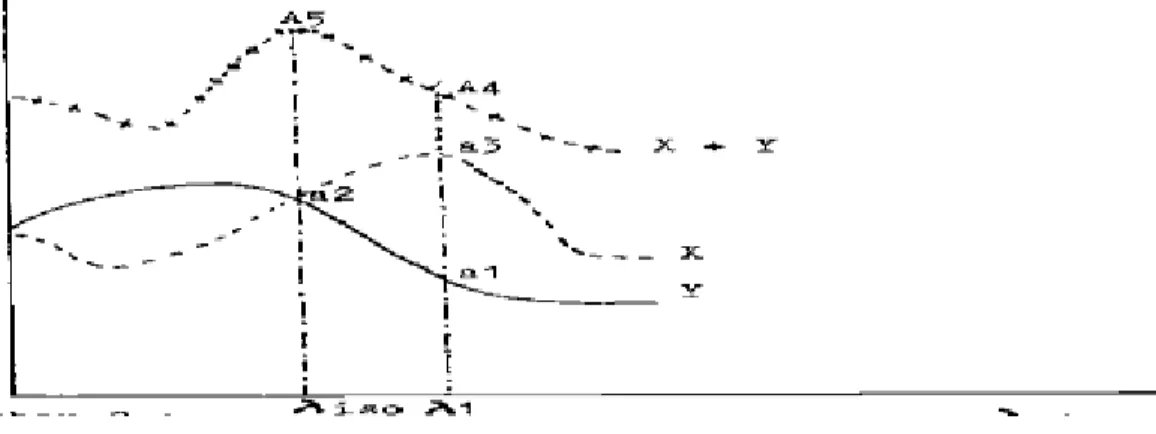
Untuk menjabarkan perhitungan kadar dari cara ini digunakan suatu model campuran biner zat X dan zat Y, dimana kurva spektranya seperti yang terlihat pada Gambar 2.4.
Gambar 2.4 Kurva serapan terhadap panjang gelombang zat X (- - -), zat Y ( ) dan campuran zat X dan Y (-+-+-)
λiso = panjang gelombang dimana daya serap zat X dan Y sama.
λ1 = panjang gelombang maksimum tertinggi.
A5 = daya serap campuran zat X dan Y pada panjang gelombang isoabsorpsi.
A4 = daya serap campuran zat X dan Y pada panjang gelombang maksimum terpilih.
a1 = daya serap zat Y pada panjang gelombang maksimum terpilih.
a2 = daya serap zat X dan Y pada panjang gelombang isoabsorpsi.
a3 = daya serap zat X panjang gelombang maksimum terpilih.
Metode ini melibatkan pengukuran absorbansi pada dua panjang gelombang, satu adalah λmax dari salah satu komponen (λ2) dan yang lainnya adalah panjang gelombang absorptivitas yang sama dari dua komponen (λ 1) yang
disebut titik isoabsorpsi. Konsentrasi masing – masing komponen dapat dihitung dengan persamaan matematis berikut:
Ca:
Cb:
Keterangan :
A = Absorbansi pada panjang gelombang isoabsorpsi
a1 dan a2 = Absorptivitas x dan y pada panjang gelombang isoabsorpsi Ca = Konsentrasi komponen x
Cb = Konsentrasi komponen y
Qm = A2
A1
Keterangan :
A2 = Absorbansi dari larutan sampel pada panjang gelombang maksimum dari suatu komponen (λ 2)
A1 = Absorbansi dari larutan sampel pada panjang gelombang maksimum isoabsorpsi dua komponen (λ 1)
Qx = ax2
ax1
Keterangan :
ax2 = Absorbansi dari baku x pada panjang gelombang maksimum dari satu komponen (λ 2)
ax1 = Absorbansi dari baku x pada panjang gelombang maksimum isoabsorpsi dua komponen (λ 1)
Qy = ay2
ay1
Keterangan :
ay2 = Absorbansi dari baku y pada panjang gelombang maksimum dari satu komponen (λ 2)
ay1 = Absorbansi dari baku y pada panjang gelombang maksimum isoabsorpsi dua komponen (λ 1) (Muchlisyam dan Pardede, 2017).
2.5 Metode Penambahan Standar
Metode penambahan standar adalah suatu metode dimana pada jumlah sampel yang sama ditambahkan larutan standar dengan konsentrasi yang berbeda, Menurut Day dan Underwood (1986), ada tiga teknik yang dapat digunakan dalam analisis secara spektrofotometri:
1. Metode Standar Tunggal
Metode ini menggunakan satu larutan standar yang telah diketahui konsentrasinya. Selanjutnya absorpsi larutan standar dan absorbansi larutan sampel diukur dengan spektrofotometri.
2. Metode Kurva Kalibrasi
Metode ini membuat suatu seri larutan standar dengan berbagai kosentrasi dan absorbansi kemudian dibuat kedalam grafik yang merupakan suatu garis lurus melewati titik nol. Konsentrasi larutan sampel dapat dicari setelah absorbansi larutan sampel diukur dan diintrapolasi kedalam kurva kalibrasi atau di masukkan kedalam persamaan garis lurus yang diperoleh dengan persamaan regresi linear.
3. Metode Adisi Standar
Metode ini digunakan secara luas karena mampu meminimalkan kesalahan yang disebabkan oleh perbedaan kondisi lingkungan (matriks) sampel dan standar. Dalam metode ini dua atau lebih sejumlah volume tertentu dari sampel dipindahkan kedalam labu
tentukur. Satu larutan diukur diencerkan sampai volume tertentu kemudian diukur absorbansinya tanpa ditambahkan dengan zat standar, sedangkan larutan yang lain sebelum diukur absorbansinya ditambah terlebih dahulu dengan sejumlah tertentu larutan standar dan diencerkan seperti pada larutan pertama.
2.6 Validasi Metode Analisis
Validasi metode adalah suatu proses yang menunjukkan bahwa prosedur analitik telah sesuai dengan penggunaan yang dikehendaki. Validasi metode analisis ditujukan untuk menjamin bahwa metode analisis memenuhi spesifikasi yang dapat diterima sesuai dengan tujuan yang diharapkan. Hal ini perlu dilakukan untuk menjamin bahwa setiap pengukuran serupa yang dilakukan dimasa yang akan datang akan menghasilkan nilai terhitung (calvulated value) yang cukup dekat atau sama dengan nilai sebenarnya dari jumlah analit yang terdapat dalam sampel. Adapun karakteristik dalam validasi yaitu akurasi/kecermatan, presisi/keseksamaan, spesifitas, batas deteksi, batas kuantitasi, linieritas, rentang, kekasaran dan ketahanan (robustness) (Gandjar dan Rohman, 2008).
2.6.1 Akurasi
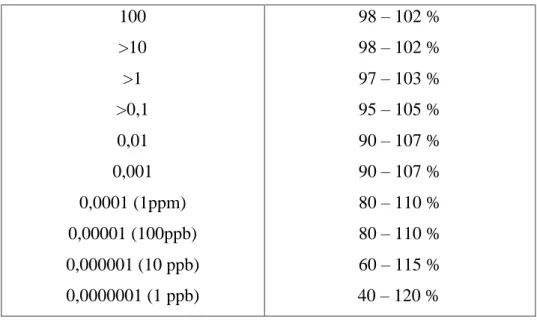
Akurasi atau kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analis dengan kadar analit yang sebenarnya. Range nilai % recovery analit yang dapat diterima adalah 90 – 110 %. Range tersebut bersifat fleksibel tergantung dari kondisi analit yang diperiksa, jumlah sampel dan kondisi laboratorium. Akurasi dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan (Harmita, 2004).
Analit pada matriks sampel (%) Daerahrecovery yang diperoleh
100
>10
>1
>0,1 0,01 0,001 0,0001 (1ppm) 0,00001 (100ppb) 0,000001 (10 ppb) 0,0000001 (1 ppb)
98 – 102 % 98 – 102 % 97 – 103 % 95 – 105 % 90 – 107 % 90 – 107 % 80 – 110 % 80 – 110 % 60 – 115 % 40 – 120 %
Tabel 2.3 Kriteria daerah recovery yang dapat diterima (Harmita, 2004)
% Perolehan Kembali = CF – CA x 100%
CA* Keterangan:
CF = konsentrasi sampel setelah penambahan baku CA = konsentrasi sebelum penambahan baku CA* = jumlah baku yang ditambahkan
2.6.2 Presisi
Presisi atau keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata- rata jika prosedur diterapkan secara berulang pada sampel – sampel yang diambil dari campuran yang homogen (Harmita, 2004). Presisi biasanya dinyatakan dalam koefisien variasi (KV). Suatu metode dapat dinyatakan memiliki presisi yang baik apabila memiliki KV < 2 % tetapi kriteria ini fleksibel tergantung dari kondisi analit yang diperiksa, jumlah sampel dan kondisi laboratorium.
Keterulangan yakni presisi pada kondisi percobaan yang sama (berulang) baik orangnya, peralatannya, tempatnya maupun waktunya. Presisi sering kali diekspresikan dengan SD atau standar deviasi relatif (RSD) dari serangkaian data.
Nilai RSD dirumuskan dengan:
RSD =
̅ ; dimana ̅ merupakan rata-rata, dan SD adlah standar deviasi serangkaian data, rumus menghitung SD adalah sebagai berikut:
SD = √∑( )
; dimana x adalah nilai dari masing-masing pengukuran;
̅ adalah rata-rata dari pengukuran; n adalah banyaknya data. Biasanya replikasi dilakukan 6-15 kali pada sampel tunggal untuk tiap konsentrasi (Gandjar dan Rohman, 2017).
2.6.3. Limit of Detection (LOD)
Menurut Harmita (2004), batas deteksi (Limit of Detection, LOD) adalah jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan dengan blangko. Batas deteksi merupakan parameter uji batas. Batas kuantitasi (Limit of Quantitation, LOQ) merupakan parameter pada analisis renik dan diartikan sebagai kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Sy/x = SD =
2 2
n
Yi Y
LOD =
slope SD x 3,3
LOQ =
slope SD x 10
Keterangan:
Sy/x = SD = Standart deviation/simpangan baku Slope = b (pada persamaan garis y = ax+b)
2.6.4 Linieritas
Menurut Harmita (2004), linearitas adalah kemampuan metode analisis yang memberikan respon yang secara langsung atau dengan bantuan transformasi matematik yang baik, proporsional terhadap konsentrasi analit dalam sampel.
BAB III
METODE PENELITIAN 3.1 Jenis Penelitian
Penelitian ini termasuk jenis penelitian eksperimental metode spektrofotometri secara Ratio Absorbance terhadap analisis simultan isoniazid dan vitamin B6 yang terkandung pada dua sediaan tablet.
3.2 Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan September-Desember 2018.
3.3 Alat
Alat-alat yang digunakan dalam penelitian ini adalah Spektrofotometer Ultraviolet-visibel (Shimadzu 1800) serta seperangkat Personal Computer (PC) yang dilengkapi dengan software UV-Probe 2.42, kuvet 1 cm, alat-alat gelas, lumpang dan alu, neraca analitik (Boeco Germany) serta alat-alat lainya yang diperlukan dalam preparasi sampel.
3.4 Bahan
Bahan yang digunakan dalam penelitian adalah baku isoniazid BPFI (Amsal Chem), baku vitamin B6 BPFI (Jiangxi Tianxin Pharmaceutical), air suling, HCl(p), HCl 0,1 N, tablet Inoxin 400 (PT Dexa Medica), dan tablet Inha 400 (PT Mersifarma TM)
3.5 Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif, yaitu ditentukan atas dasar pertimbangan bahwa sampel yang terambil mempunyai karakteristik yang sama dengan yang diteliti (Sudjana, 2005). Sampel yang digunakan yaitu tablet Inoxin
400 (PT Dexa Medica) yang mengandung 400 mg isoniazid; 10 mg vitamin B6 dan tablet Inha 400m(PT Mersifarma TM) yang mengandung 400 mg isoniazid;
10 mg vitamin B6 yang diperoleh dari apotek Haemes Jl. Darussalam.
3.6 Prosedur Penelitian
3.6.1 Pembuatan Larutan Induk Baku
3.6.1.1 Pembuatan Larutan Induk Baku Isoniazid
Ditimbang dengan seksama 0,1 g serbuk isoniazid BPFI kemudian dimasukkan kedalam labu tentukur 100 ml, dilarutkan dengan pelarut HCl 0,1 N dan dicukupkan sampai garis tanda sehingga diperoleh larutan dengan konsentrasi 1000 g/ml (LIB I). Dari LIB I dipipet 5 ml dimasukkan kedalam labu tentukur 50 ml, diencerkan dengan pelarut HCl 0,1 N sampai garis tanda sehingga diperoleh larutan dengan konsentrasi g/ml (LIB II).
3.6.1.2 Pembuatan Larutan Induk Baku Vitamn B6
Ditimbang dengan seksama 0,1 g serbuk vitamin B6 BPFI kemudian dimasukkan kedalam labu tentukur 100 ml, dilarutkan dengan pelarut HCl 0,1 N dan dicukupkan sampai garis tanda sehingga diperoleh larutan dengan konsentrasi 1000 g/ml (LIB I). Dari LIB I dipipet 5 ml dimasukkan kedalam labu tentukur 50 ml, diencerkan dengan pelarut HCl 0,1 N sampai garis tanda sehingga diperoleh larutan dengan konsentrasi 100 g/ml (LIB II).
3.6.2 Pembuatan Spektrum Serapan Maksimum
3.6.2.1 Pembuatan Spektrum Serapan Maksimum Isoniazid
Dipipet 1,12 ml larutan induk baku II ( LIB II) isoniazid, dimasukkan kedalam labu 10 ml, diencerkan dengan HCl 0,1 N hingga garis tanda, dikocok hingga homogen sehingga diperoleh larutan dengan konsentrasi 11,2 g/ml dan diukur serapan pada panjang gelombang 200-400 nm.
3.6.2.2 Pembuatan Spektrum Serapan Maksimum Vitamin B6
Dipipet 0,84 ml Larutan Induk Baku II ( LIB II) vitamin B6, dimasukkan kedalam labu 10 ml, diencerkan dengan HCl 0,1 N hingga garis tanda, dikocok hingga homogen sehingga diperoleh larutan dengan konsentrasi 8,4 g/ml, kemudian diukur serapan pada panjang gelombang 200-400 nm.
3.6.3 Pembuatan Spektrum Serapan Baku
3.6.3.1 Pembuatan spektrum serapan baku Isoniazid
Dipipet Larutan induk baku II (LIB II) isoniazid sebanyak 0,56 ml; 0,84 ml; 1,12 ml; 1,4 ml; dan 1,68 ml. Masing-masing dimasukkan kedalam labu tentukur 10 ml, diencerkan dengan dengan HCl 0,1 N hingga garis tanda. Dikocok sampai homogen sehingga diperoleh larutan dengan konsentrasi 5,6 g/ml; 8,4 g/ml; 11,2 g/ml; 14 g/ml; 16,8 g/ml.
3.6.3.2 Pembuatan spektrum serapan baku Vitamin B6
Dipipet Larutan induk baku II (LIB II) vitamin B6 sebanyak 0,44 ml; 0,64 ml; 0,84 ml; 1,04 ml; dan 1,24 ml. Masing-masing dimasukkan kedalam labu tentukur 10 ml, diencerkan dengan dengan HCl 0,1 N hingga garis tanda. Dikocok sampai homogen sehingga diperoleh larutan dengan konsentrasi 4,4 g/ml;
6,4 g/ml; 8,4 g/ml; 10,4 g/ml; 12,4 g/ml.
3.6.4 Pembuatan spektrum serapan dengan metode ratio absorbance terhadap panjang gelombang untuk penentuan panjang gelombang Isoabsorpsi dan panjang gelombang maksimum terpilih
Kurva ini dibuat dengan cara mendempetkan kurva serapan maksimum dari larutan Isoniazid dan Vitamin B6 diukur pada rentang panjang gelombang 200 – 400 nm. Dari kurva tersebut dapat ditentukan panjang gelombang isoabsorpsi (panjang gelombang dimana terjadi perpotongan keuda kurva) dan
panjang gelombang maksimum terpilih (panjang gelombang dengan absorbansi tertinggi dari kedua zat).
3.6.4.1 Pembuatan kurva kalibrasi metode Ratio Absorbance Isoniazid
Nilai ratio absorbance spektra pada panjang gelombang maksimum yang diperoleh, dihitung dan diplot dengan konsentrasi untuk mendapatkan persamaan garis regresinya
.
3.6.4.2 Pembuatan kurva kalibrasi metode Ratio Absorbance Vitamin B6
Nilai ratio absorbance spektra pada panjang gelombang maksimum yang diperoleh, dihitung dan diplot dengan konsentrasi untuk mendapatkan persamaan garis regresinya
.
3.6.5 Pembuatan Spektrum Serapan Campuran Baku Isoniazid dan Vitamin B6
Ditimbang masing-masing 0,010 g baku isoniazid dan vitamin B6, dimasukkan masing-masing kedalam labu tentukur 10 mL, dilarutkan dengan pelarut HCl 0,1 N sampai garis tanda, dan dihomogenkan. Kemudian dipipet 1,12 mL dari larutan isoniazid dan 0,84 mL dari larutan vitamin B6. Kedua larutan ini dicampurkan kedalam labu tentukur 10 mL, dicukupkan dengan pelarut HCl 0,1 N sampai garis tanda, dikocok hingga homogen. Kemudian dari campuran larutan tersebut dipipet 1 mL, dimasukkan kedalam labu tentukur 10 mL, dicukupkan hingga garis tanda dengan pelarut HCl 0,1 N dan dikocok sampai homogen.
Diukur serapan pada panjang gelombang 200-400 nm.
3.7 Penetapan Kadar Isoniazid dan Vitamin B6 dalam sediaan Tablet Ditimbang 0,04121 g sampel I dan 0,00318 g sampel P tablet mengandung Isoniazid dan Vitamin B6 (dilakukan sebanyak 6 kali)
kemudian masukkan secara kuantitatif dalam labu tentukur 50 ml.
Dilarutkan HCl 0,1 N kemudian dihomogenkan dengan sonikator selama 15 menit. Dicukupkan dengan HCl 0,1 N sampai garis tanda, dikocok hingga homogen. Larutan tersebut kemudian disaring, lebih kurang 10 ml filtrat pertama dibuang dan filtrat selanjutnya ditampung. Kemudian dari filtrat ini dipipet 0,224 ml dan dimasukkan kedalam labu tentukur 10 ml.
Ditambahkan 0,08 ml LIB II vitamin B6 (metode adisi standar), kemudian diencerkan dengan HCl 0,1 N sampai garis tanda sehingga diperoleh larutan yang mengandung 11,2 g/ml Isoniazid dan 8,4 g/ml Vitamin B6. Diukur serapan pada panjang gelombang 200-400, kemudian dicari nilai rasio absorbansi.
3.8 Analisis data secara statistik
Uji yang digunakan dalam penelitian ini adalah uji t. Distribusi data dihitung dengan menggunakan rumus:
thitung | X X̅ SD √n|
Kadar sebenarnya dengan taraf kepercayaan 99%, dihitung dengan menggunakan rumus:
µ X̅ t(1-1 2 )dk
SD
√n
Keterangan:
µ = interval kadar sebenarnya
̅ = kadar rata-rata sampel X = kadar sampel
t = harga t tabel sesuai dengan dk = n-1 dk = derajat kebebasan (n-1)
= tingkat kepercayaan SD = standar deviasi n = jumlah perlakuan 3.9 Validasi Metode 3.9.1 Uji akurasi
Uji akurasi dilakukan dengan metode penambahan baku (Standard Addition Method), yaitu dengan membuat konsentrasi analit sampel dengan rentang
spesifik 80%, 100%, dan 120%, dimana masing-masing dilakukan sebanyak tiga kali perlakuan. Setiap rentang mengandung 70% analit dan 30% baku pembanding, kemudian dianalisa dengan perlakuan yang sama seperti pada penetapan kadar sampel (Harmita, 2004). Spektrum serapan yang dihasilkan kemudian dibuat spektrum rasio untuk masing-masing isoniazid dan vitamin B6, kemudian dilanjutkan dengan pembuatan spektrum MCR dan dilakukan penetapan kadar seperti pada sampel. Berikut dibawah merupakan rumus persen perolehan kembali.
% Perolehan Kembali =
x 100%
Keterangan:
CF = Konsentrasi sampel setelah penambahan baku CA= Konsentrasi sampel sebelum penambahan baku
CA* = Jumlah baku yang ditambahkan (dikali pemurnian baku) 3.9.2 Presisi
Menurut Watson (2005), presisi suatu analisis sering dinyatakan sebagai ± simpangan baku relative (± SBR) dengan rumus sebagai berikut:
SBR =
̅ x 100%
Keterangan:
SBR = Simpangan Baku Relatif s = Simpangan baku
̅ = Rerata pengukuran
3.9.3 Linearitas, batas deteksi (Limit of Detection, LOD) dan batas deteksi (Limit of Quantification, LOQ)
Berdasarkan absorbansi pada λ analisis dilakukan pula perhitungan LOD dan LOQ sebagai berikut:
SD = √∑( ) LOD =
LOQ = Keterangan :
SD = Standard Deviation (Residual Standard Deviation) (Harmita, 2004).
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil Penentuan Spektrum Serapan Maksimum
Penentuan spektrum serapan maksimum dilakukan pada panjang gelombang 200-400 nm Penentuan spektrum serapan maksimum isoniazid adalah pada konsentrasi 11,20 µg mL dan vitamin B6 pada konsentrasi 8,40 µg mL.
Panjang gelombang maksimum untuk isoniazid dalam larutan asam adalah 266 nm dan vitamin B6 dalam larutan asam adalah 290 nm (Moffat, dkk., 2011).
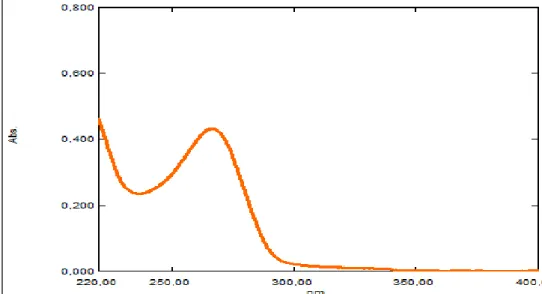
Spektrum serapan maksimum isoniazid dan vitamin B6 masing-masing dapat dilihat pada Gambar 4.1 dan Gambar 4.2.
Gambar 4.1 Panjang gelombang isoniazid serapan maksimum 266,6 nm.
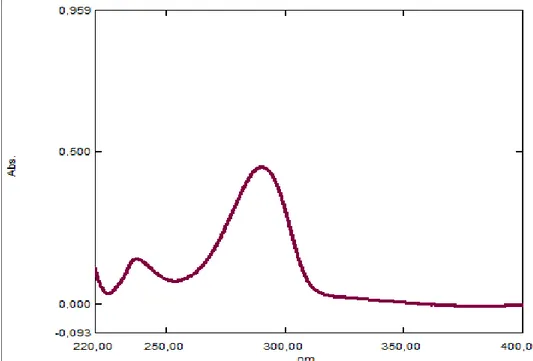
Gambar 4.2 Panjang gelombang vitamin B6 serapan maksimum 290,4 nm.
Gambar 4.3 Panjang gelombang maksimum isoniazid dan vitamin B6
4.2 Hasil Penentuan Spektrum Serapan Isoniazid dan Vitamin B6 Pada Berbagai Konsentrasi
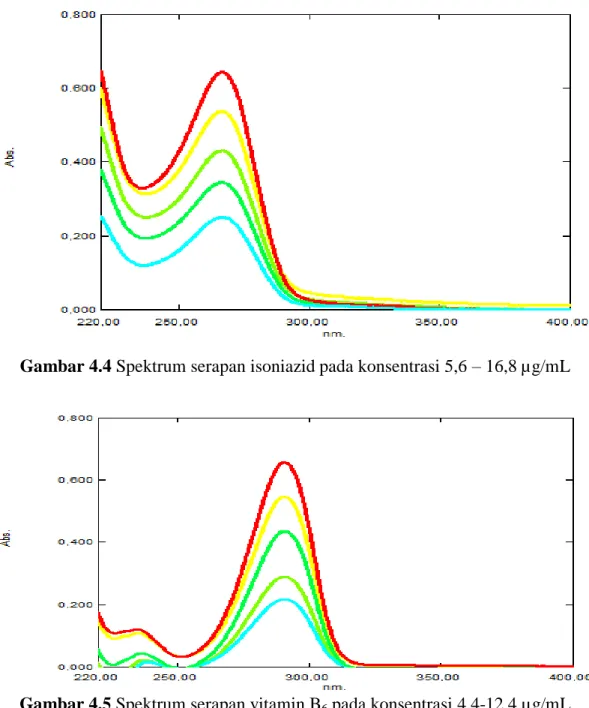
Spektrum serapan isoniazid dibuat pada konsentrasi 5,60 µg/mL; 8,40 µg/mL; 11,20 µg/mL; 14,0 µg/mL dan 16,80 µg/mL dan spektrum serapan
vitamin B6 dibuat pada konsentrasi 4,40 µg/mL; 6,40 g/mL; 8,40 µg/mL; 10,40 µg/mL dan 12,40 µg/mL, lalu diukur pada panjang gelombang 200-400 nm.
Spektrum serapan isoniazid dan vitamin B6 pada berbagai konsentrasi dapat dilihat pada Gambar 4.4 dan Gambar 4.5.
Gambar 4.4 Spektrum serapan isoniazid pada konsentrasi 5,6 – 16,8 µg/mL
Gambar 4.5 Spektrum serapan vitamin B6 pada konsentrasi 4,4-12,4 µg/mL
4.3 Hasil Spektrum Serapan Campuran Baku Isoniazid dan Vitamin B6
Spektrum serapan campuran baku isoniazid dan vitamin B6 dapat dilihat pada Gambar 4.6.
Gambar 4.6 Spektrum serapan campuran baku isoniazid dan vitamin B6
Spektrum serapan campuran baku isoniazid dan vitamin B6 dibuat dengan konsentrasi 11,20 µg mL untuk isoniazid dan 8,40 µg mL untuk vitamin B6. Spektrum campuran menghasilkan bentuk yang berbeda dengan spektrum isoniazid dan vitamin B6 masing-masing, karena spektrum serapan campuran adalah kombinasi dari spektrum penyusunnya.
Metode spektrofotometri ultraviolet konvensional tidak dapat digunakan untuk menetapkan kandungan Isoniazid dan Vitamin B6 dalam campuran, karena spektrum dari kedua zat saling tumpang tindih, sehingga absorbansi pada λ spektrum campuran Isoniazid dan Vitamin B6 tidak menggambarkan besar konsentrasi dari masing-masing zat tersebut dalam campurannya. Berbeda dengan metode spektrofotometri ultraviolet secara Ratio Absorbance yang memungkinkan untuk menetapkan kadar suatu zat dalam campuran zat tersebut
dengan zat lainnya, sehingga penetapan kadar zat tunggal dalam campurannya dapat dilakukan.
4.4 Metode Ratio Absorbance (Q-Ratio Method)
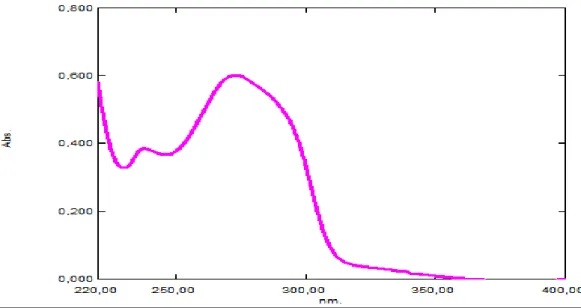
Metode ini menggunakan rasio dari absorbansi pada 2 panjang gelombang terpilih, dimana satu panjang gelombang merupakan titik isoabsorptif dan yang lainnya adalah panjang gelombang maksimum dari salah satu zat. Metode ini diawali dengan penentuan titik isoabsorptif dengan cara mendempetkan kurva serapan maksimum dari 2 zat. Hasil perpotongan dari kedua kurva disebut dengan titik isoabsorptif (panjang gelombang dimana kedua obat menunjukkan absorbansi yang sama) (Dinakaran, dkk.,2013).
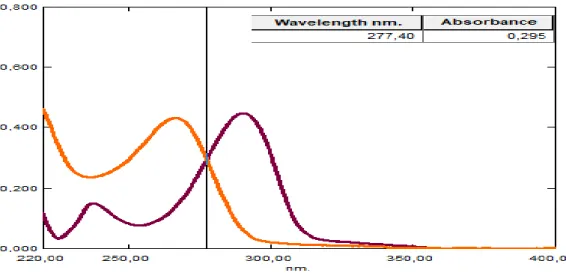
Gambar 4.7 Titik isoabsorptif isoniazid dan vitamin B6
Dari Gambar 4.7 dapat dilihat bahwa Isoniazid dan Vitamin B6
menghasilkan titik isoabsorptif pada panjang gelombang 277,4 nm dan panjang gelombang salah satu obat terpilih yaitu 266,6 nm yang merupakan panjang gelombang maksimum dari Isoniazid.
4.4.1 Hasil Metode Ratio Absorbance
Setelah mengetahui panjang gelombang isoabsorptif dari kedua campuran antara Isoniazid dan Vitamin B6, dapat dihitung konsentrasi masing-masing komponen dengan persamaan matematis berikut :
Ca =
Cb =
Dari hasil perhitungan konsentrasi hasil rasio absorbansi tersebut, diperoleh kadar Isoniazid dan Vitamin B6 sebagai berikut (Contoh perhitungan kadar dapat dilihat pada Lampiran 12).
Tabel 4.1 Data kadar isoniazid dan vitamin B6 dalam sediaan Tablet I
Peng ulang an
Isoniazid Vitamin B6
Konsentra si teori (µg/mL)
Konsentra si hasil
rasio absorbansi
(µg/mL)
Kadar (%)
Konsen trasi teori (µg/mL
)
Konsentrasi hasil rasio absorbansi
(µg/mL)
Kadar (%)
1 11,16 11,2589 100,68 8,3992 8,8348 104,97
2 11,16 11,2019 100,17 8,3992 8,8974 105,72
3 11,16 11,2175 100,31 8,4032 8,9426 106,20
4 11,16 11,2726 100,80 8,4032 8,9535 106,33
5 11,25 11,3108 100,34 8,4042 8,9116 105,83
6 11,27 11,3108 100,16 8,4042 8,9420 106,20
Tabel 4.2 Data kadar isoniazid dan vitamin B6 sediaan Tablet P Pengul
angan
Isoniazid Vitamin B6
Konsentr asi teori (µg/mL)
Konsentras i hasil
rasio absorbansi
(µg/mL)
Kadar (%)
Konsentr asi teori (µg/mL)
Konsentras i hasil
rasio absorbansi
(µg/mL)
Kadar (%)
1 11,33 11,7796 103,76 8,3992 8,7614 104,10
2 11,33 11,7450 103,45 8,3992 8,8658 106,10
3 11,41 11,8137 103,39 8,4032 8,9721 106,55
4 11,53 11,9454 103,39 8,4032 9,0331 107,28
5 11,53 11,9297 103,26 8,4032 8,9091 105,80
6 11,53 11,8943 102,95 8,4032 8,8658 106,10
Hasil penetapan kadar secara statistik isoniazid dan vitamin B6 dalam
sediaan tablet P dan tablet T dapat dilihat pada Tabel 4.3 dan Tabel 4.4.
Tabel 4.3 Kadar isoniazid dan vitamin B6 dalam Tablet I secara statistik
No. Obat Kadar Kandungan
dalam etiket Persyaratan kadar 1. Isoniazid (100,41 0,4411)% 400 mg (90-110)%
2. Vitamin B6 (105,87 0,8261 )% 10 mg (95-115)%
Rentang kadar isoniazid dan vitamin B6 pada tablet I masing-masing adalah 99,9689-100,8511% dan 105,0439-106,6961%. Kadar tersebut telah memenuhi persyaratan kadar yang tertera pada Farmakope Indonesia Edisi V.
Tabel 4.4 Kadar isoniazid dan vitamin B6 dalam Tablet P secara statistik
No. Obat Kadar Kandungan
dalam etiket
Persyaratan kadar 1. Isoniazid (103,35 ± 0,4326)% 400 mg (90-110)%
2. Vitamin B6 (105,87 1,7414)% 10 mg (95-115)%
Rentang kadar isoniazid dan vitamin B6 pada tablet P masing-masing adalah 102,9174-103,7826% dan 104,1286-107,6114%. Kadar tersebut telah memenuhi persyaratan kadar yang tertera pada Farmakope Indonesia Edisi V.
4.5 Hasil Validasi Metode
Parameter validasi yang diuji adalah akurasi (kecermatan), Linearitas, batas deteksi (LOD), dan batas kuantitas (LOQ). Uji akurasi dinyatakan dalam persen perolehan kembali (% recovery) yang ditentukan dengan metode adisi standar. Pada penelitian ini dilakukan uji validasi dengan metode adisi standar pada sampel tablet.
Uji akurasi dilakukan dengan membuat tiga konsentrasi sampel dengan rentang spesifik 80%, 100%, dan 120% dihitung dari kesetaraan pemipetan pada penetapan kadar sampel, masing-masing rentang spesifik terdiri dari tiga kali pengulangan yang mengandung 70% analit dan 30% baku. Spektrum serapan uji perolehan kembali dapat dilihat pada gambar berikut.
Gambar 4.8 Spektrum % perolehan kembali rentang spesifik 80%
Gambar 4.9 Spektrum % perolehan kembali rentang spesifik 100%
Gambar 4.10 Spektrum % perolehan kembali rentang spesifik 120%
Dari hasil perhitungan dapat dilihat pada lampiran 64 dan 65 bahwa uji
perolehan kembali ini memenuhi syarat akurasi yang telah ditetapkan. Akurasi yang diekspresikan dengan nilai perolehan kembali untuk senyawa obat dalam suatu campuran adalah kurang lebih 98%-102% (Gandjar dan Rohman, 2017).
Hasil uji perolehan kembali untuk Isoniazid adalah 99,84% dan 100,70% untuk Vitamin B6. Jika rata-rata hasil perolehan kembali berada pada rentang tersebut, maka persen perolehan kembali tersebut menunjukkan kecermatan kerja yang baik pada saat perlakuan penentuan kadar Isoniazid dan Vitamin B6.
Uji linieritas. Linearitas adalah kemampuan metode analisis yang memberikan respon yang secara langsung atau dengan bantuan transformarsi matematik yang baik, proporsional terhadap konsentrasi analit dalam sampel.
Rentang metode adalah pernyataan batas terendah dan tertinggi analit yang sudah ditunjukkan dapat ditetapkan dengan kecermatan, keseksamaan dan linearitas yang dapat diterima. Sebagai parameter adanya hubungan linear digunakan koefisien korelasi r pada analisis regresi linier Y = ax + b. Kurva kalibrasi dapat dilihat pada gambar berikut.
Gambar 4.10 Kurva kalibrasi Isoniazid pada 266,6 nm dan 277,4 nm
y = 0,039x + 0,002 R² = 0,999 pada 266,6 nm
y = 0,029x - 0,009 R² = 0,997 pada 277,4 nm -0.2
0 0.2 0.4 0.6 0.8
0 5 10 15 20
Axis Title
Isoniazid
Y Y
Gambar 4.11 Kurva kalibrasi Vitamin B6 pada 290,4 nm dan 277,4 nm
Berdasarkan kurva yang diperoleh, hubungan yang terjadi antara konsentrasi dengan absorbansi adalah linier, dengan koefisien korelasi (r) Isoniazid sebesar 0,99959 dan 0,99801 pada panjang gelombang 266,6 nm dan 277,4 nm secara berurutan dan Vitamin B6 sebesar 0,99973 dan 0,99330 pada panjang gelombang 290,4 nm dan 277,4 nm secara berurutan. Hubungan linier yang ideal dicapai jika nilai b = 0 dan r = +1 atau –1 bergantung pada arah garis.
Sedangkan, nilai a menunjukkan kepekaan analisis terutama instrumen yang digunakan (Harmita,2004).
Dari hasil perhitungan (tertera pada lampiran 21) dapat dilihat bahwa semua hasil yang diperoleh pada pengukuran sampel berada di atas batas deteksi (Limit of Detection, LOD) dan batas kuantitasi (Limit of Quantitation, LOQ).
Batas deteksi dan batas kuantitasi Isoniazid dan Vitamin B6 berturut-turut adalah 0,7443 µg/mL dan 2,4812 µg/mL untuk Isoniazid, sedangkan untuk Vitamin B6
berturut-turut adalah 1,2164 µg/mL dan 4,0547 µg/mL Konsentrasi yang terdapat di dalam batas kuantitasi atau LOQ merupakan konsentrasi minimum yang harus diukur dalam suatu sampel agar pembacaan absorbansi kuantitatif.
y = 0,053x + 0,001 R² = 0,999 pada 290,4 nm
y = 0,039x - 0,017 R² = 0,993 pada 277,4 nm -0.1
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7
0 2 4 6 8 10 12 14
Axis Title
Vitamin B6
Y X