LAPORAN PRAKTIKUM PENGANTAR KIMIA MEDISINAL
SEMESTER GANJIL 2016 - 2017PENENTUAN KOEFISIEN PARTISI MINYAK/AIR ASAM
SALISILAT
Hari / Jam Praktikum : Senin, pukul 10:00 – 13:00
Tanggal Praktikum : 19 September 2016
Kelompok : 2
Asisten : 1. Aulia Alfiana 2. Giovani Wijonarko
TENGKU RUHUL FAJRIA
260110160091
LABORATORIUM KIMIA MEDISINAL
FAKULTAS FARMASI
UNIVERSITAS PADJADJARAN
JATINANGOR
I. Tujuan
Untuk menentukan koefisien partisi asam salisilat dengan metode pengocokan.
II. Prinsip
1. Koefisien Partisi
Perbandingan kosentrasi dari suatu zat terlarut yang dilarutkan di dalam
dua pelarut yang tidak saling bercampur dengan perbandingan tersebut
adalah atau konstan. (cairns, Donald, 2004)
2. Titrasi asam basa
Titrasi berdasarkan penetralan asam-basa, larutan asam ditentukan dengan
menggunakan larutan basa yang telah diketahui kadarnya dan sebaliknya
kadar larutan bisa ditentukan dengan menggunakan arutan asam yang telah
diketahui kedarnya. (Michael, 2012)
3. Ekstrasi
Ekstrasi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan
pelarut cair. (Ditjen POM, 2000)
4. Like dissolve like
merupakan sifat kecenderungan senyawa pelarut yang hanya melarutkan
senyawa dengan sifat kepolaran sama. senyawa polar akan larut dalam
senyawa polar dan tidak larut dalam senyawa nonpolar, demikian juga
sebaliknya. (James, 2001)
IV. Teori Dasar
Asam salisilat merupakan bahan yang telah diketahui sejak lama dan salah satu
penggunaannya dalam sediaan obat luar untuk infeksi jamur ringan. Sering kali
asam ini dikombinasi dengan asam benzoat (salep Whitflied) dan belerang (sulfur
precipitatum) yang keduanya memiliki kerja fungistatis dan bakteriostatis. Asam
salisilat jika dalam bentuk mikroskopis dapat berupa bubuk kristal putih dengan
rasa manis, tidak berbau, dan stabil pada udara bebas. Bubuk asam salisilat sukar
larut jika dilarutkan dalam air. Sifat lipofilik asam salisilat (sukar bergabung
dengan air) membuat asam salisilat sukar dicampurkan dengan air. Namun asam
salisilat dapat mudah larut dalam lemak, dikarenakan asam salisilat bekerja sebagai
pelarut organik dan dapat menghilangkan ikatan kovalen lipid intraseluler yang
berikatan (Sulistyaningrum dkk, 2012).
Koefisien partisi atau koefisien distribusi menggambarkan pendistribusian obat
ke dalam pelarut sisstem dua fase, yaitu pelarut organik dengan air, koefisien partisi
semakin bear dan difusi trans menjadi lebihh mudah disebabkan molekul semakin
larut dalam lemak. Organisasi yang terdiri dari fase lemak dan air. Sehinggga bila
koefisien partisi tinggi atau rendah, maka hal ini akan menjadi hambatan pada
proses difusi zat aktif. Penentuan koefisien secara eksperimen dilakukan dengan
cara distribusi senyawa dalam jumlah tertentu ke dalam sistem kesetimbangan
termodinamika dua pelarut yang berbeda kepolaran yaitu h-optanal dan air. (Ansel,
Koefisien partisi adalah distribusi kesetimbangan dan analit dan
kesetimbangan dari perbandingan kadar zat dalam dua fase. Koefisien partisi
minyak air adalah suatu petunjuk sifat hipofilik/ hidrofilkdari molekul obat.
Lewatnya obat melalui lemak dan interaksi dengan makromolekul pada reseptor.
Adanya pemahaman tentang koefisien partisi dan pengaruh pH pada partisi akn
berpengaruh dalam hubungan dengan ekstrak dan komatograf obat. (Mochtar,
2007)
Sifat hidrofilik adalah sifat dimana suatu bagian yang menyukai air atau
bersifat polar. Sedangkan bagian hidrofobik adalah bagian yang tidak menyukai air
atau bersifat non polar (Wasis, 2008)
Pengetahuan tentang partisi untuk ahli farmasi, karena prinsip ini melibatkan
bebeapa bidang ilmu farmasetik. Termasuk disini pengawetan sistem minyak air,
kerja obat pada tempat yang tidak spesifik, absorbsi dan distribusi obat ke seluruh
tubuh (Marten, 2007)
Koefisien partisi senyawa organik sendiri adalah konsentrasi senyawa dalam
fase organik atau fase minyak dan (berair) adalah konsentrasi senyawa minyak
dalam fase air.
Sebagai contoh, perhatikan distribusi 100 mg obat dalam 50 ml pelarut organik
(misalnya eter, klorofoam, atau etanol)dan 50 ml air. Obat tersebut ditambahkan
kedu pelarut yang saling tidak bercampur dalam sebuah corong pemisah, dan
dibiarkan mencapai kesetimbangan. Ketika lapisan organik dianalisi, ditemukan
66,7 mg. Berdasarkan data tersebut, koefisien partisi dan persentase obat yang
terekstraksi ke dalam lapisan organik dapat dihitung.
Koefisien partisi sendiri merupakan suatu informasi yang penting karena dapat
digunakan untuk memperkirakan proses adsorbsi dan eliminasi obat di dalam tubuh.
Pengetahuan tentang koefisien partisi dapat digunakan untuk memperkirakan onset
kerja obat atau durasi kerja obat, atau untuk mengetahui apakah suaatu obat akan
bekerja secara aktif. Bagian kimiamedisinal, yaitu suatu disiplin ilmu pengetahuan
menggunakan koefisien partisi itu sendiri, dalam persamaan matematika yang
mencoba menghubungkan antara aktivitas biologis suatu obat dengan karakteristik
fisika dan kimianya.
Hukum koefisien partisi menyatakan bahwa senyawa tertentu pada suhu
tertentu akan memisahkan dirinya sendiri diantara dua pelarut yang saling tidak
bercampur pada perbandingan konsentrasi yang tetap. Perbandingan konsentrasi
yang tetapp itulah yang dikenal dengan koefisien partisi senyawa tersebut dan dapat
dinyatakan secara matematis sebagai berikut.
𝑝 =[Organik][Berair]
P adalah koefisien partisi senyawa, [Organik] adalah konsentrasi senyawa pada fase organik atau pada fase minyak, sedangkan [Berair] adalah konsentrasi senyawa pada fae air. (cairns, Donald, 2004)
Penentuan koefisien partisi cukup penting dilakukan dikarenakan ini bertujuan
untuk mendapatkan karakterisasi dan aktivasi biologis suatu obat. Penentuan
koefisien partisi biasanya diawali dengan percobaan terlebih dahulu. (Tahir, 2000)
Metode yang digunakan dalam praktikum ini ialah metode pengocokan atau
akrab dikenal dengan metode titrasi. Salah satu teori titrasi ialah teori asam-basa
Bronsted-Lowry. Berdasarkan teori ini dijelaskan bahwa sifat basa berlaku untuk
senyawa-senyawa hidroksida maupun senyawa-senyawa lain yang berkaitan dengan
hidroksida. Sifat asam menurut teori asam basa Bronsted-Lowry menjelaskan bahwa
asam dapat mendonorkan proton sedangkan basa bersifat sebagai akseptor atau
penerima proton. Persamaan reaksi menurut teori Bronsted-Lowry dapat dinyatakan
sebagai berikut:
HCl + H2O H2O+ + Cl
-(Suyatno dkk,2010)
Sedangkan Titrasi merupakan proses analisis dimana suatu volume larutan
tidak dikenal. Larutan standar adalah larutan yang konsentrasinya sudah diketahui
secara pasti. Berdasarkan kemurniannya dibedakan menjadi larutan standar primer
dan larutan standar sekunder. Larutan standar primer adalah larutan standar yang
dipersiapkan dengan menimbang dan melarutkan suatu zat tertentu dengan
kemurnian tinggi (konsentrasi diketahui dan massa-volume larutan). Larutan
standar sekunder adalah larutan standar yang disiapkan dengan menimbang dan
melarutkan suatu zat tertentu dengan kemurnian relative rendah sehingga
konsentrasi diketahui dari hasil standarisasi. (Day Underwood,1999)
V. Alat dan Bahan
5.1. Alat
1. Batang Pengaduk
2. Buret
3. Corong
4. Corong pemisah
5. Erlemeyer
6. Gelas beaker
7. Gelas ukur
8. Kertas Perkamen
9. Labu ukur
10.Pipet tetes
11.Spatula
12.Statif
13.Timbangan Analitis
5.2. Bahan
1. Aquades
2. Asam salisilat
3. Kloroform
4. Indikator fenoftalein
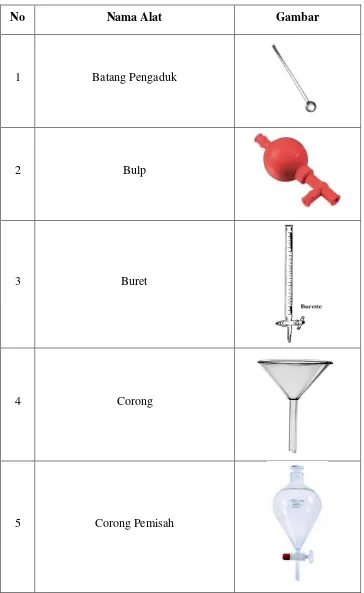
5.3. Gambar Alat
No Nama Alat Gambar
1 Batang Pengaduk
2 Bulp
3 Buret
4 Corong
6 Erlemeyer
7 Gelas Beaker
8 Gelas Ukur
9 Kertas Perkamen
10 Labu Ukur
12 Pipet Ukur
13 Spatula
14 Statif
15 Timbangan Analitik
VI. Prosedur
6.1Prosedur Pembuatan NaOH
Alat dan Bahan disiapkan. 1000 ml aquadest dituang ke dalam gelas
beaker. Aquadest dipanaskan sampai cukup panas/mendidih. NaOH
ditimbang sebanyak 4 gr. NaOH yang telah ditimbang dimasukkan ke
dalam 1000 ml aquadest yang telah dipanaskan. Aduk campuran NaOH
6.2 Pembakuan NaOH
Alat dan bahan disiapkan. Bagian dalam buret dibilas menggunakan
NaOH dan biarkan NaOH mengalir. Sebelumnya, keran buret
dipastikan tidak terbuka. 50 ml NaOH dituangkan ke dalam buret. 15
ml asam oksalat di dalam 2 labu ukur dituangkan ke dalam 2
erlenmeyer. Berikan 2 tetes indikator fenolftalein ke dalam
masing-masing larutan asam oksalat. Titrasi dilakukan sebnyak 2 kali dengan
metode pengocokan sampai larutan tersebut berubah warna menjadi
merah muda.
6.3Penimbangan asam salisilat
Alat dan bahan disiapkan terlebih dahulu. Timbangan analitik
dihidupkan terlebih dahulu, dan kertas perkamen diletakkan diatas
timbangan analitik. Maka, akan muncul berat dari kertas perkamen, tombol
“T’ ditekan agar berat dari kertas perkamen ditiadakan. Asam salisilat
diletakkan dengan bantuan spatula diatas kertas perkamen hingga mencapai
berat 1,38 g.
6.4pelarutan asam salisilat
Asam salisilat yang telah ditimbang dimasukkan kedalam
erlemeyer. Etanol sebanyak 10 ml ditambahkan kedalam erlemeyer yang
berisi asam salisilat, dan diaduk secara perlahan hingga asam salisilat larut
didalam etanol. Aquades ditambahkan sebanyak 90 ml dan diaduk hingga
semuanya tercampur.
6.5Titrasi asam salisilat dengan NaOH
Asam salisilat yang telah dilarutkan diambil sebanyak 15 ml dan
diletakkan kedalam erlemeyer. Sebanyak 20 ml aquades ditambahkan ke
dalam erlemeyer dan dikocok perlahan hingga bercampur. Selanjutnya,
dititrasi menggunakan NaOH sebanyak 50 ml. Saat titrasi, erlemeyer yang
berisi asam salisilat digoyangkan sedikit demi sedikit. Asam salisilat
dititrasi hingga berubah warna menjadi merah muda.
6.6 Ekstraksi
Larutan asam salisilat sebanyak 15 ml dicampur dengan 10 ml
kloroform dan dikocok didalam corong pemisah sampai terlihat dua lapisan.
Setelah dikocok, Lapisan air diambil dan dimasukan ke dalam erlenmeyer.
Lalu ditambahkan 20 mL air dan 2 tetes indikator fenolftalein. Kemudian
dititrasi dengan NaOH menggunakan buret dan diamati sampai warna
berubah.
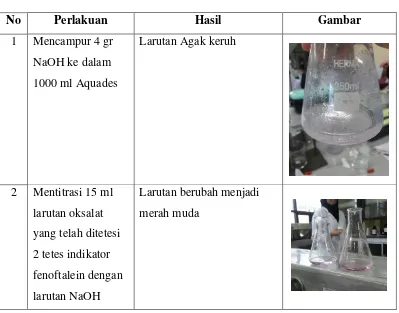
VII. Data Pengamatan
No Perlakuan Hasil Gambar
1 Mencampur 4 gr
NaOH ke dalam
1000 ml Aquades
Larutan Agak keruh
2 Mentitrasi 15 ml
larutan oksalat
yang telah ditetesi
2 tetes indikator
fenoftalein dengan
larutan NaOH
Larutan berubah menjadi
3 Menimbang asam
salisilat
Percobaan 1: 1,3819 gr
Percobaan 2 : 1,3809 gr
Percobaan 3 : 1,3812 gr 1,3819 + 1,3809 + 1,3812
3 =
4,144
3 = 1,3813 𝑔𝑟
4
Melarutkan 1,383
gr asam salisilat
kedalam 90 ml
aquades dan 10 ml
etanol
Larutan asam salisilat tidk
larut sepenuhnya, terdapat
5
1. Mengitung massa asam salisilat
M =
nV0,1 =
100mln n = 10 mmol𝑛 =
mrgrgr = n. Mr
= 10 mmol . 138
= 1380 mg
2. Menghitung konsentrasi NaOH
Diketahui :
V NaOH I = 17, 3 ml
V NaOH II = 16,5 ml
N1V1 = N2V2 N1V1 = N2V2
0,1 . 15 = N2 . 17,3 0,1 . 15 = N2 . 16,5
N2 = 1,5
17,3
N
2=
1,5 16,5
N2 = 0,087 N2 = 0,09
Rata-rata = 0,087+0,09
2 = 0,0885
3. Menghitung konsentrasi larutan asam salisilat + 20 ml air + 2 tetes
indikator fenoftalein
N1V1 = N2V2
N1 . 15 = 0,0885 . 3,5
N1 = 0,0885 . 3,5
15
N1 = 0,02065
4. Meghitung asam salisilat + pada lapisan bawah dari asam salisilat +
kloroform 10 ml + 20 ml aquades + 2 tetes indikator fenoftalein.
Menggunakan NaOh sebanyak 3,5 ml
N1V1 = N2V2
N1 . 30,2 = 0,0885 . 3,5
N1 =0,0885 . 3,5 30,2
5. Menghitung koefisien partisi
N asam salisilat fase kloroform = N asam salisilat – N fase air
[Organik] = 0,02065 – 0,01026
= 0,01039 M
[Berair] = 0,01065 M
𝑝 =[Organik][Berair] = 0,01039
0,01026 = 1.0126
Jadi, nilai p adalah 1.0126
6. Menghitung nilai log koefisien partisi
log1.0126 = 0.0547
IX. Pembahasan
Dalam pembuatan larutan NaOH, aquades yang digunakan perlu untuk
dipanaskan. Hal ini dikarenakan adanya molekul CO2 didalam aquades tersebut.
Keberadaan molekul CO2 di dalam aquades akan menyebabkan terbentuknya
molekul Na2CO3 sesuai dengan reaksi
2 NaOH + CO2 Na2CO3 + H2O (Undip, 2014).
Selain itu, NaOH yang telah dilarutkan perlu di tutup atau perlu untuk diplastic
wrap, ini dikarenakan NaOH memili sifat higroskopis. Sifat higroskopis ini
membuat NaOH mudah menyerap udara dan air dan mudah untuk meleleh.
Setelah larutan NaOH dibuat, maka perlu dilakukan pembakuan NaOH.
Pembakuan NaOH dilakukan karena NaOH merupakan zat baku sekunder. Zat
baku sekunder adalah zat baku yang konsentrasinya harus dibakukan dengan zat
baku primer. Zat baku sekunder sendiri memiliki normalitas yang nantinya akan
berubah jika disimpan dalam jangka waktu tertentu. Oleh karena itu perlu
Asam oksalat digunakan sebagai titran karena merupakan salah satu dari larutan
baku primer yang normalitasnnya telah stabil. Titrasi dilakukan sebanyak dua kali,
ini dilakukan untuk memperoleh nilai yang akurat.
Setelah volume NaOH didapat dari proses titrasi, maka normalitas dari NaOH
dapat diketahui dari perhitungan. Normalitas ini yang nantinya akan dijadikan
sebagai acuan dalam proses mencari konsentrasi zat organik maupun konsentrasi
zat cair nantinya.
Pada penimbangan asam salisilat hal yang perlu diperhatikan adalah
menyiapkan terlebih dahulu gelas beaker berdekatan dengan timbangan analitik
sebelum menimbang. Ini sangat dibutuhkan, karena setelah dilakukan
penimbangan, maka asam salisilat harus langsung dimasukkan kedalam gelas
beaker untuk menghindari hilangnya massa dari asam salisilat karena pengaruh
udara atau yang lainnya.
Penggunaan timbangan analitik pada percobaan memudahkan dalam banyak
hal. Timbangan analitik memiliki tingkat ketelitian yang tinggi. Selain itu
penggunaannya yang tidak begitu rumit lebih membuat efisien dalam hal waktu
maupun tenaga.
Pada pembuatan larutan asam salisilat, serbuk asam salisilat dilarutkan dengan
etanol. Hal ini dikarenakan sifat kelarutan dari asam salisilat yang mudah larut
pada etanol dan eter namun sukar larut dalam air (DepKes RI, 1995).
Dalam pembuatan asam salisilat tidak boleh dilarutkan langsung dengan
aquades. Sebelum dicampurnya asam salisilat dengan aquades terlebih dahulu
asam salisilat dilarutkan dengan etanol. Dilarutkan dahulu oleh etanol karena sifat
dari asam salisilat itu sendiri sukar larut dengan air, benzena, dan kloroform tetapi
mudah larut dalam eter dan etanol (Depkes RI, 1995).
Asam salisilat memiliki gugus polar dan gugus nonpolar. Gugus polar pada
asam ssalisilat adalah –OH sedangkan gugus nopolarnya adalah gugus cincin
benzen. Struktur tersebut yang menyebabkan asam salisilat dapat larut pada
memiliki gugus polar dan gugus nonpolar sekaligus dalam satu gugus, asam
salisilat sukar larut dalam pelarut polar saja atau dalam pelarut nonpolar saja. Asam
salisilat sukar larut pada air yang merupakan pelarut polar, tetapi mudah larut pada
etanol yang merupakan senyawa semi polar.
Pada saat dilakukan pelarutan, maka didapatkan hasil yang tidak sesuai, yaitu
munculnya kristalan putih atau semacam gumpalan didalam asam salisilat yang
telah dilartkan dengan air dan etanol. Ini terjadi karena kesalahn dalam
perbandingan antara air dan etanol atau adanya kontaminasi dengan lingkungan
luar. Akan tetapi, meskipun hasil yang didapat merupakan larutan etanol dengan
kristal atau gumpalan yang berwarna putih, tetap masih bisa diambil 15 ml larutan
asam salisilat yang akan digunakan untuk proses titrasi pada tahap selanjutnya.
Pada saat proses titrasi asam salisilat menggunakan larutan NaOH, maka
ditambahkan dua tetes indikator fenoftalein. Pemberian indikator fenoftalein
berfungsi untuk memberikan warna pada larutan setelah mencapai nilai
kesetimbangan. Indicator pp akan memberikan warna ungu pada keadaaan basa
dan tidak berwarna pada keadaan asam (Marwati,2014). Oleh karena itu, untuk
menemukan titik kesetimbangan, pengamatan terhadap perubahan warna harus
sangat teliti agar didapat warna yang sesuai, yaitu merah muda.
Indikator fenoftalein sendiri merupakan asam diprotik dan tak berwarna. Asam
diprotik sendiri adalah asam yang dapat melepaskan ion H+. Fenoftalein
mula-mula berdisosiasi menjadi suatu bentuk tak berwarna dan kemudian dengan
kehilangn hidrogen kedua menjadi ion dengan sistem terkonjugasikan, maka
dihasilkanlah warna merah muda. Fenoftalein berubah warna pada kira-kira titik
ekivalen atau titik seimbang. Fenoftalein selesai mengalami perubaahan warnanya
pada pH yang tepat dengan titik ekivalen pada saat untuk pertama kalinya natrium
hidrogenkarbonat terbentuk.
Pada saat dilakukannya titrasi asam ssalisilat, maka didapat sebanyak 3,5 ml
larutan NaOH yang harus ditambah kedalam larutan supaya mencapai nilai
Langkah selanjutnya adalah meenentukan normalitas asam salisilat pada fase
air. Langkah yang dilakukan yaitu pengocokan asam salisilat yang telah ditambah
kloroform di dalam corong pemisah hingga kedua larutan meengalami dispersi
yang ditandai dengan terpisahnya dua larutan pada corong pemisah tersebut.
Pengocokan dilakukan sampai asam saisilat dengan kloroform benar benar
tercampur dan setelah itu didiamkan. Maka, pada saat didiamkan, muncullah
larutan yang terdispersi tersebut. Setelah larutan terdisspersi, larutan asam salisilat
berada pada lapisan bawah, dan lapisan kloroform berada pada lapisan atas. Ini
disebabkan karena kerapatan atau massa jenis kloroform lebih kecil daripada
kerapatan asam salisilat.
Kloroform merupakan senyawa dari asam formiat dan termasuk senyawa
polihalogen yaitu senyawa turunan karboksilat yang mengikat lebih dari satu atom
halogen. Kloroform tidak larut dalam air, tetapi merupakan pelarut efektif untuk
senyawa organik. Selain kloroform, etil eter dan etanol juga merupakan pelarut
organik. Tetapi untuk etanol, lebih mendekati ke pelarut semi polar.
Langkah berikutnya adalah mentitrasi asam salisilat hasil dari corong pemisah
yang telah terdispersi sebelumnya. Seperti yang telah dilakukan sebelumnya,
diteteskan indikator fenoftalein sebanyak dua tetes dalam larutan asam salisilat
tersebut. Maka akan didapatkan larutan menjadi merah muda pada saat sudah
tertambah 3,5 ml NaOH. Pada langkah ini, diperkirakan NaOH yang masuk ke
dalam asam salisilat melalui proses titrasi mengalami kelebihan. Ini ditandai
dengan perubahan warna yang agak gelap dari yang sebenarnya, yaitu mendekati
ungu.
Dari serangkaian percobaan yang dilakukan telah dilakukan, maka didapat
hasil koefisien partisi adalah 1.0126. nilai ini dianggap benar karena dalam litertur
nilai ketetapan dari koefisien partisi asam salisilat yang baik berada lebih dari 1.
Dari nilai ini dapat diketahui pula nilai dari log nilai koefisien partisinya. Nilai
Berdasarkan nilai dari log koefisien tersebut dapat dilihat sifat lipofilisitas
asam salisilat yang nantinya akan menggambarkan hubungan antara asam salisilat
dengan enzim atau bahkan makromolekul lainnya yang ada di dalam tubuh. Nilai
0,0543 menunjukkan nilai yang baik untuk rentang suatu obat. Rentang obat yang
baik berada pada rentang -2 sampai dengan 4. Sedangkan nilai 0,0543
menunjukkan bahwa asam salisilat tergolong diantara obat yang bersifat lipofil
atau hidrofob. Semakin ke kiri (minus) nilai suatu log koefisien pasrtisi, maka akan
semakin bersifat hidrofil sedangkan semakin ke kanan akan bersifat lipofil.
Dengan nilai log yang menunjukkan niali yang bagus, maka pada percobaan
ini menyatakan bahwa asam salisilat dalam tubuh dapat menembus membran lipid
dengan baik sehingga tidak akan terperangkap dalam jaringan lipid tersebut.
X. Kesimpulan
Dari percobaan yang telah dilakukan, didapatkan koefisien partisi asam
salisilat adalah 1.0126. hasil dari koefisien partisi ini dianggap benar karena dalam
literature nilai ketetapan koefisien partisi asam salisilat yang baik berada diatas 1.
Sedangkan nilai dari log koefisien partisi menunjukkan angka 0.0543 yang
menunjukkan bahwa asam salisilat termasuk ke dalam golongan yang baik untuk
obat yaitu berada dalam renta -2 sampai dengan 4.
XI. Daftar Pustaka
Ansel, H. 1898. Kimia Farmasi. Jakarta :Universitas Indonesia.
Cairns, Donald. 2008. Intisari kimia Farmasi. Jakarta : Buku Kedokteran EGC.
Day, Underwood. 1999. Kimia Analisis Kuantitatif. Jakarta: Erlangga.
Departemen Kesehatan RI. 1995. Farmakope Indonesia. Edisi IV. Jakarta:
Ditjen POM. 2000. Parameter Standar Umum Ekstrak tumbuhan obat. Jakarta :
Departemen Kesehatan RI.
Gandjar, dkk. 2007. Kimia Farmasi Analisis. Yogyakarta: pustaka pelajar.
J.Gillespie, R dan Paul L.A.Popelier. (2001). Chemical Bonding and Molecular
Geometry. New York: Oxford University Press.
Martin, A. 1990. Dasar-Dasar Kimia Farmasi Fisik dalam Ilmu Farmasetika.
Jakarta : Universitas Indonesia.
Michael. 2012. 100 Tanya Jawab mengenai Diabetes. Jakarta: PT. Indeks.
Mochtar. 2007. Kimia farmasi Analisis. Jakarta : Universitas Indonesia.
R.T. Smedberg. 1994. J. Chem. Volume 3 No 71. Educ.
Sulistyaningrum, Sri dkk. 2012. Penggunaan Asam Salisilat Dalam Darmatologi.
Volume 62 No.7. tersedia online di Indonesian.digitaljournal.org (diakses
pada 16 September 2016)
Suyatno dkk. 2010. Kimia. Jakarta: Grasindo.
Tahir, iqmal. 2000. Komparasi nilai koefisien partisi teoritik berbagai senyawa
obat dengan metoda Hansch-Leo, metoda Rekker, dan penggunaan
program Clog. Tersedia online di iqmal.staff.ugm.ac.id [diakses pada 23
September 2016]
Undip. 2014. Absorpsi CO2 dengan Larutan NaOH. Tersedia online di
http://lab.tekim.undip.ac.id/proses/files [ diakses pada 25 September 2016].
Vogel. 1979. Buku teks analisis anorganik kualitatif makro dan semimakro.
Jakarta: PT kalman media pustaka
Wasis, dan Irianto, Sugeng Yuli. Ilmu Pengetahuan Alam jilid 2 Untuk SMP dan