IDENTIFIKASI KERAGAMAN GEN FOLLICLE STIMULATING
HORMONE RECEPTOR (FSHR|Alu-1) PADA SAPI LOKAL
INDONESIA DENGAN TEKNIK PCR-RFLP
SKRIPSI
RAYHANAH BEY NASUTION
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN
INSTITUT PERTANIAN BOGOR 2013
RINGKASAN
Rayhanah Bey Nasution. DI4080014. 2013. Identifikasi Keragaman Gen Follicle
Stimulating Hormone Receptor (FSHR|Alu-1) pada Sapi Lokal Indonesia dengan Teknik PCR-RFLP. Skripsi. Departemen Ilmu Produksi dan Teknologi Peternakan,
Fakultas Peternakan, Institut Pertanian Bogor.
Pembimbing Utama : Prof. Dr. Ir. Cece Sumantri, M.Agr.Sc. Pembimbing Anggota : Dr. Jakaria, S.Pt, M.Si.
Upaya perbaikan genetik terhadap mutu produktivitas ternak dapat dilakukan melalui seleksi pada tingkat molekuler. Perbaikan mutu genetik ternak terhadap nilai produktivitas terutama dalam reproduksi untuk menghasilkan fenotipe dan genotipe ternak yang lebih baik sangat dipengaruhi oleh keberadaan gen di dalamnya. Gen yang sangat berperan penting terhadap kemampuan fungsi reproduksi tersebut adalah gen Follicle Stimulating Hormone Receptor (FSHR). Sampel uji pelaksanaan penelitian ini dilakukan pada sapi lokal Indonesia yang terdiri atas sapi Bali, Aceh, Pesisir, PO, dan Katingan. Penelitian ini bertujuan untuk melihat keragaman Gen Follicle Stimulating Hormone Receptor (FSHR) dengan teknik Polymerase Chain Reaction-Restriction Fragment Length Polymorphism (PCR-RFLP).
Sampel yang digunakan dalam penelitian ini merupakan koleksi di Laboratorium Genetika dan Molekuler Ternak (LGMT), Fakultas Peternakan, Institut Pertanian Bogor. Total sampel yang diamati berjumlah 129 sampel DNA. Sampel tersebut terdiri dari 16 sampel sapi Bali, 12 sapi Aceh, 29 sapi Pesisir, 32 sapi PO, dan 40 sapi Katingan. Sampel tersebut berasal dari sejumlah tempat, seperti BIB (Balai Inseminasi Buatan) Lembang dan Singosari, BIBD (Balai Inseminasi Buatan Daerah) sapi Bali dan BPTU (Balai Pembibitan Ternak Unggul) sapi Bali.
Penelitian ini dilakukan dengan dua tahapan, yaitu amplifik asi DNA melalui proses Polymerase Chain Reaction (PCR) dan pemotongan DNA sel target dengan teknik Restriction Fragment Length Polymorphism (RFLP). Enzim restriksi yang digunakan adalah enzim Alu-1 yang memotong pada posisi basa spesifik AG|CT. Nilai keragaman gen FSHR diperoleh dengan analisis frekuensi genotipe, frekuensi alel, nilai heterozigositas pengamatan (Ho), dan nilai heterozigositas harapan (He).
Produk PCR yang dihasilkan dari proses amplifikasi gen FSHR dengan suhu annealing 60°C selama 45 detik mempunyai panjang fragmen sebanyak 306 pb. Pemotongan DNA terhadap produk PCR dengan teknik RFLP terhadap gen (FSHR|Alu-1) menghasilkan dua jenis alel (C dan G) dan menghasilkan tiga macam genotipe yaitu, CC (243 dan 63 bp), CG (243, 193, 63 dan 50 bp), dan GG (193, 50 dan 63 bp). Pendugaan nilai heterozigositas tertinggi ditemukan pada sapi Aceh dan heterozigositas terendah pada sapi Bali. Identifikasi keragaman gen FSHR|Alu-1 menujukkan bahwa sapi Bali, Aceh, Pesisir, PO, dan Katingan bersifat polimorifk dengan sapi Bali memiliki sifat gen homozigot (nilai genotipe CC dan GG).
ABSTRACT
Identification Polymorphism of The Follicle Stimulating Hormone Receptor (FSHR|Alu-1) Gene in Indonesian Cattle Using PCR-RFLP Technique.
Nasution, R. B., C. Sumantri and Jakaria
Polymerase chain reaction (PCR) is a technology to amplificate the specific fragments of DNA in vitro. PCR-RFLP is one of the PCR technic was developed to visualize the differences of DNA levels by using enzyme restriction. This research was conducted to identify polymorphism of Follicle Stimulating Hormone Receptor (FSHR) gene in Indonesian cattle, consits of Bali, Aceh, PO, Pesisir and Katingan. Follicle Stimulating Hormone Receptor (FSHR) gene is the one of the esensial hormone receptor in reproductivity animal system. It will induce the spermatogenesis and oogenesis process with spesific receptor interaction on male and female cell target. Total of sampels used in this reseach are 129 samples consist of Bali Cattle 16 heads, Aceh 12 heads, PO 29 heads, Pesisir 32 heads, and Katingan 40 heads. The result of this identify polymorphism showed that there are two alelles of C and G and three genotipes (CC, CG, and GG) in Aceh, PO, Pesisir, and Katingan cattle. Heterozygositas of each sample showed that heterozygositas expectation (He) is higher than heterozygositas observation (Ho). The higest heterozygosity value was found in Pesisir Aceh cattle, while the lower heterozygosity value was found in Bali cattle population. Based on the analysis, Indonesian cattle breed (Aceh cattle, Pesisir cattle, PO cattle, and katingan cattle) are polymorphic in FSHR gene with three genotipes (GG, GC, CC) and two alelles (G and C), while the Bali cattle is homozigot with only two genotipes CC and GG.
IDENTIFIKASI KERAGAMAN GEN FOLLICLE STIMULATING
HORMONE RECEPTOR (FSHR|Alu-1) PADA SAPI LOKAL
INDONESIA DENGAN TEKNIK PCR-RFLP
RAYHANAH BEY NASUTION D14080014
Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Peternakan pada
Fakultas Peternakan Institut Pertanian Bogor
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN
INSTITUT PERTANIAN BOGOR 2013
Judul : Identifikasi Keragaman Gen Follicle Stimulating Hormone Receptor (FSHR|Alu-1) pada Sapi Lokal Indonesia dengan Teknik PCR-RFLP Nama : Rayhanah Bey Nasution
NIM : D14080014
Menyetujui,
Mengetahui, Ketua Departemen
Ilmu Produksi dan Teknologi Peternakan
Prof. Dr. Ir. Cece Sumantri, M.Agr.Sc. NIP. 19591212 198603 1 004
Tanggal Ujian: 17 Desember 2012 Tanggal Lulus: Pembimbing Utama
Prof. Dr. Ir. Cece Sumantri, M.Agr.Sc. NIP. 19591212 198603 1 004
Pembimbing Anggota
Dr. Jakaria, S.Pt., M.Si. NIP. 19660105 199303 1 001
RIWAYAT HIDUP
Penulis bernama Rayhanah Bey Nasution, dilahirkan di kota Rantauprapat, Sumatera Utara pada tanggal 5 November 1990. Penulis merupakan anak pertama dari 5 bersaudara dari pasangan Busthamey Muhammad Nasution, BA dan Farida Hanum Dalimunthe, S.PdI. Pendidikan yang ditempuh Penulis dimulai dari Taman Kanak-kanak, SD Negeri 117470, MTs Negeri 1, SMA Negeri 3 yang semuanya dijalani di tempat kelahiran Penulis, Rantauprapat.
Penulis diterima sebagai mahasiswi Fakultas Peternakan di Departemen Ilmu Produksi dan Teknologi Peternakan, Institut Pertanian Bogor melalui jalur Undangan Seleksi Mahasiswa IPB (USMI). Aktivitas Penulis selama menjadi mahasiswi adalah sebagai mahasiswi aktif dan ikut bergabung di berbagai kepanitian dan organisasi. Penulis tercatat merupakan bagian dari kepengurusan Lembaga Dakwah Fakultas Peternakan Forum Aktivitas Mahasiswa Muslim Al-An’aam (FAMM Al-An’aam) sebagai Staf Informasi dan Komunikasi periode 2009-2010, Ketua Departemen Keputrian periode 2010-2011 dan Majelis Syuro periode 2011-2012. Penulis juga bergabung di Badan Eksekutif Mahasiswa Fakultas Peternakan (BEM D) dalam kabinet D’Knights sebagai Staf Departemen Riset dan Pengembangan Mahasiswa Eksternal periode 2009-2010.
Penulis pernah mengikuti Program Kreativitas Mahasiswa di bidang Kewirausahaan (PKM-K) yang didanai oleh Dikti dengan judul “Sabun Prasasti (Propolis Ekstra Susu Aroma Terapi) sebagai Produk Alternatif Kesehatan dan Kecantikan Kulit”. Penulis pun pernah mengikuti event International Conference of Sustainable Future for Human Security (Sustain 2011) yang mempresentasikan makalah Internasional dengan judul “Fermented Milk Yogurt With Antioxidant based on Fikosianin Biopigment from Spirulina fusiformis” di Universitas Kyoto, Jepang. Penulis pernah pula menjadi Asisten Praktikum Pendidikan Agama Islam pada periode 2010-2011 dan 2011-2012.
KATA PENGANTAR
Bismillahirrohmannirrohim, segala puji dan syukur kepada Ilahi Robbi yang menganugerahkan limpahan rahmat dan karunia sehingga Penulis mampu menyelesaikan penelitian dan penulisan skripsi yang berjudul Identifikasi
Keragaman Gen Follicle Stimulating Hormone Receptor (FSHR|Alu-1) pada Sapi Lokal Indonesia dengan Teknik PCR-RFLP. Sholawat dan salam untuk
Rosululloh Muhammad SAW yang menjadi teladan terbaik untuk seluruh ummat manusia. Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Peternakan pada Fakultas Peternakan, Institut Pertanian Bogor.
Pelaksanaan seleksi pada tingkat molekuler terhadap sumber daya genetik dapat dilakukan sebagai upaya perbaikan mutu genetik ternak. Perbaikan mutu genetik ternak terhadap nilai produktivitas terutama dalam reproduksi sangat dipengaruhi oleh keberadaan gen di dalamnya. Salah satu gen yang esensial dalam peningkatan produktivitas reproduksi pada ternak adalah gen Follicle Stimulating Hormone Receptor (FSHR). Follicle Stimulating Hormone (FSH) adalah salah satu hormon reproduksi yang penting pada sistem reproduksi. FSH menginduksi spermatogenesis dan oogenesis melalui interaksi reseptor spesifik pada sel target jantan dan betina yang disebut sebagai gen FSHR. Keberadaan gen FSHR tersebut dapat dideteksi melalui teknik Polymerase Chain Reaction-Restriction Fragment Length Polymorphism (PCR-RFLP).
Penelitian ini diharapkan dapat memberikan informasi mengenai identifikasi keragaman gen FSHR pada sapi lokal Indonesia yang terdiri atas sapi Bali, Aceh, Pesisir, PO, dan Katingan dengan menggunakan teknik PCR-RFLP dengan enzim restriksi Alu-1. Informasi mengenai keragaman FSHR diharapkan dapat menjadi dasar seleksi pada level DNA. Penulis menyadari masih terdapat banyak kekurangan, namun penulis berharap semoga skripsi ini dapat memberikan sumbangsih ilmu dan manfaat, khususnya bagi penulis dan pada pembaca secara umum, Amin.
Bogor, Januari 2013
DAFTAR ISI Halaman RINGKASAN……….... ii ABSTRACT.…....………... iii LEMBAR PERNYATAAN.………... iv LEMBAR PENGESAHAN.………... v RIWAYAT HIDUP.………... vi
KATA PENGANTAR.………... vii
DAFTAR ISI.………... iii
DAFTAR TABEL.………... x
DAFTAR GAMBAR.……….... xi
DAFTAR LAMPIRAN.………... xii
PENDAHULUAN.……….... 1 Latar Belakang.………... Tujuan.………... 1 1 TINJAUAN PUSTAKA ……….……. 2
Sumber Daya Genetik Sapi Lokal Indonesia...………... Gen Follicle Stimulating Hormone Receptor (FSHR)………….….... Polymerase Chain Reaction-Restriction Fragment Lenght Polymorphism (PCR-RFLP)………… ………....… 2 6 7 MATERI DAN METODE.………...… 9
Lokasi dan Waktu.………... Materi.………... Sampel.……….… Bahan dan Alat………... Prosedur.………...… Pengambilan Sampel...………... Ekstraksi DNA...………... Amplifikasi DNA...……..…………... Elektroforesis...………... Genotyping .………..…... Rancangan dan Analisis Data………... 9 9 9 9 10 10 10 11 12 13 14 HASIL DAN PEMBAHASAN.………...………...…... 15
Amplifikasi Gen FSHR|Alu-1.……...…...……...…...… Keragaman Gen FSHR|Alu-1………... Frekuensi Alel dan Frekuensi Genotipe Gen FSHR|Alu-1..... Heterozigositas………...………..…...
15 16 18 19
KESIMPULAN DAN SARAN..………....….. 22 Kesimpulan...………...………... Saran...………...
22 22
UCAPAN TERIMA KASIH.……....………... 23
DAFTAR PUSTAKA...…..……… 25
DAFTAR TABEL
Nomor Halaman
1. Karakteristik Fenotipik Sapi Lokal Indonesia …..……... 3 2. Jumlah Sampel Sapi yang Digunakan...…... 9 3. Frekuensi Alel dan Frekuensi Genotipe dari Gen FSHR|Alu-1... 19 4. Nilai Heterozigositas Pengamatan (Ho) dan Heterozigositas Harapan
(He) Gen FSHR|Alu-1... 20
DAFTAR GAMBAR
Nomor Halaman
1. Karakteristik Fenotipik Bangsa Sapi Lokal Indonesia. (a) Sapi Bali; (b) Sapi Aceh; (c) Sapi Pesisir; (d) Sapi PO; dan (e) Sapi Katingan...
5
2. Struktur Gen FSHR... 6 3. Posisi Penempelan Primer pada Sekuen Posisi Penempelan Primer
(Cetak Tebal) pada Sekuen Gen Follicle Stimulating Hormone Reseptor (FSHR) (Gene Bank Code: L22319.1)…...
12
4. Penentuan Genotipe Gen FSHR|Alu-1... 14 5. Hasil Amplifikasi Gen FSHR|Alu-1 pada Gel Agarose 1,5%... 16 6. Hasil Visualisasi PCR-RFLP Gen FSHR|Alu-1 pada Gel Agarose 2%... 18
DAFTAR LAMPIRAN
Nomor Halaman
PENDAHULUAN Latar Belakang
Potensi sumber daya genetik sapi lokal Indonesia sangat beragam dan belum dimanfaatkan secara optimal. Populasi sapi yang semakin berkembang di Indonesia telah menghasilkan sumber daya genetik yang lebih beragam pula. Sumber daya genetik yang semakin beragam akan membuat populasi tersebut semakin tahan untuk hidup dalam jangka waktu yang lebih lama dan semakin tinggi daya adaptasi populasi terhadap perubahan lingkungan (Frankham et al., 2002).
Pelaksanaan seleksi pada tingkat molekuler terhadap sumber daya genetik tersebut belum banyak dimanfaatkan. Pemanfaatan tersebut dilakukan sebagai upaya untuk mendapatkan ternak lokal unggul yang memiliki produktivitas tinggi dalam rangka meningkatkan kemampuan produksi dan reproduksi pada sapi lokal Indonesia.
Salah satu gen yang esensial dalam mempengaruhi sifat reproduksi pada ternak sapi lokal adalah gen Follicle Stimulating Hormone Receptor (FSHR). Keberadaan gen tersebut dapat membantu peningkatan produksi sperma dalam testis sapi jantan dan produksi sel ovum pada betina. Keterbatasan informasi dan teknologi terkait dengan pemanfaatan sumber daya genetik gen FSHR menyebabkan masih kecil sekali optimasi produksi yang dapat dihasilkan. Oleh karena itu, penelitiaan ini dilakukan untuk menelaah lagi keragaman gen FSHR pada sapi lokal agar dapat dijadikan salah satu acuan untuk pemanfaatan dalam peningkatan produktifitas maupun kelestarian plasma nutfah sapi lokal Indonesia.
Identifikasi keragaman gen FSHR pada sapi lokal ini salah satunya dapat dilakukan melalui teknik Polymerase Chain Reaction-Restriction Fragment Length Polymorphism (PCR-RFLP). Penelitian ini diamati pada ternak sapi Bali, Aceh, Pesisir, PO, dan Katingan.
Tujuan
Penelitian ini bertujuan untuk melihat keragaman gen Follicle Stimulating Hormone Receptor (FSHR|Alu-1) dengan menggunakan teknik PCR-RFLP pada sapi Bali, Aceh, Pesisir, PO, dan Katingan.
TINJAUAN PUSTAKA
Sumber Daya Genetik Sapi Lokal Indonesia
Ternak sapi di Indonesia dapat dikelompokkan ke dalam tiga kategori, yaitu terak asli, ternak yang telah beradaptasi dan ternak impor (Sarbaini, 2004). MacHugh (1996) mengemukakan bahwa sapi yang terdapat di Asia khususnya di Indonesia merupakan sapi yang termasuk dalam spesies Bos bibos dan sapi persilangan (cross breed) yang berbeda dari sapi domestikasi yang terdapat di Afrika dan Eropa, meskipun diduga bahwa pola penyebarannya berasal dari wilayah India (Bos indicus) yang merupakan tipe sapi berpunuk (Zebu). Hasil domestikasi spesies liar Bos bibos banteng adalah sapi Bali (Bos sundaicus) atau (Bos javanicus) yang sekarang telah menjadi bangsa ternak asli Indonesia (Directorate Generale of Livestock Service, 2003; Martojo, 2003).
Sumber daya genetik (ternak) yang merupakan wujud keanekaragaman hayati, ialah material genetik, yaitu bahan dari binatang/ternak yang mengandung unit-unit fungsional pewarisan sifat (hereditas). Kepentingan dan penggunaan sumber daya ini untuk kepentingan manusia, mencakup informasi yang berkenaan dengan ekspresi genetik untuk menambahkan nilai pemanfaatannya. Nilai pemanfaatan ini terkandung di dalam sifat-sifat yang terdapat pada dan proses-proses yang berlangsung di dalam makhluk hidup. Berdasarkan kandungan ini, sumber daya genetik mempunyai nilai manfaat, baik secara nyata maupun secara potensial (Setiadi et al., 2006).
Sumber daya genetik ternak adalah semua yang termasuk dalam spesies, bangsa dan strain (galur) ternak yang secara ekonomi, ilmiah dan budaya penting bagi umat manusia baik dalam bentuk makanan maupun produksi (Food Agriculture Organization, 2011). Departemen Pertanian (2006) menyatakan bahwa sumber daya genetik ternak adalah substansi yang terdapat dalam bentuk individu suatu populasi rumpun ternak secara genetik unik, terbentuk dalam proses domestikasi dari masing-masing spesies yang memiliki potensial serta dapat dimanfaatkan dan dikembangkan baik untuk menciptakan rumpun atau galur unggul.
Kergaman ternak sapi erat kaitannya dengan daya reproduksi ternak. Daya reproduksi ternak pada umumnya dipengaruhi oleh lama kehidupan, dimana lama kehidupan produktif sapi potong lebih lama bila dibandingkan dengan sapi perah
3 yaitu 10 sampai 12 tahun dengan produksi 6 sampai 8 anak. Faktor ini sangat penting bagi peternakan dan pembangunan peternakan, karena setiap penundaan kebuntingan ternak, mempunyai dampak ekonomis yang sangat penting (Toelihere, 1985). Tinggi rendahnya efisiensi reproduksi ternak dipengaruhi oleh lima hal yaitu, angka kebuntingan (conception rate); jarak antar kelahiran (calving interval); jarak waktu antara melahirkan sampai bunting kembali (service periode); angka kawin per kebuntingan (service per conception); angka kelahiran (calving rate) (Hardjopranjoto, 1995).
Keragaman ternak sapi di Indonesia merupakan hasil keragaman karakteristik fenotipik yang terdapat pada masing-masing individu ternak. Berikut disajikan karakteristik fenotipik pada sapi lokal Indonesia, yaitu sapi lokal Indonesia Bali, Aceh, Pesisir, PO Katingan (Tabel 1).
Tabel 1. Karakteristik Fenotipik Sapi Lokal Indonesia
Ternak Karakteristik Literatur
Sapi Bali Warna bulu merah bata, hitam, namun pada saat dewasa berubah menjadi hitam.
Hardjosubroto (1994).
Sapi berukuran sedang, berdada dalam dengan warna bulu merah kecoklatan. Bibir, kaki dan ekor berwarna hitam. Kakinya dari lutut ke bawah terdapat warna putih. Warna putih juga terdapat pada bagian bawah paha dan bagian pantatnya. Sapi jantan berwarna lebih coklat (gelap) dari pada sapi betina. Bila sapi jantan dikebiri maka akan berwarna merah kembali.
Panjaitan et al. (2003).
Sapi Aceh Warna tubuh dominan merah
kecoklatan, bagian kepala (mata, telinga bagian dalam dan bibir bagian atas berwarna keputih-putihan), leher lebih gelap pada ternak jantan, garis punggung cokelat kehitaman, paha belakang berwarna merah bata, bagian pantat berwarna cokelat muda, kaki berwarna keputih-putihan, ujung ekor berwarna hitam, rambut berwarnamerah bata hingga cokelat, bentuk muka dan punggung umumnya cekung, bentuk tanduk mengarah ke samping dan melengkung ke atas, bentuk telinga
Keputusan Menteri Pertanian (2011).
4 kecil dan mengarah ke samping tidak
terkulai.
Warna tubuh bervariasi, memiliki warna coklat yang lebih gelap pada bagian depan dibandingkan bagian belakang tubuhnya, pada ternak jantan gumba berukuran sedang.
Namikawa. et al. (1982), Otsuka et al. (1980), Adrial (2010).
Sapi Pesisir Memiliki bobot badan dan ukuran tubuh lebih kecil dibandingkan dengan sapi lokal lainnya, sapi pesisir jantan dewasa (umur 4-6 tahun) memiliki bobot badan 160 kg, jauh lebih rendah dibandingkan dengan bobot badan sapi lainnya.
Parker dalam Adrial (2002).
Warna bulu sapi pesisir memiliki pola tunggal. Warna bulu dikelompokkan menjadi lima warna utama, yaitu merah bata (34,35%), kuning (25,51%), coklat (19,96%), hitam (10,91%) dan putih (9,26%).
Anwar (2004).
Bersifat jinak sehingga mudah dikendalikan saat pemeliharaan. Sapi memiliki tanduk kecil, pendek dan mengarah ke luar seperti tanduk kambing. Sapi jantan memiliki kepala pendek dan membulat, sedangkan sapi betina mempunyai kepala agak panjang dan tipis, kemudi miring, pendek dan tipis.
Saladin (1983).
Sapi PO Punuk besar, terdapat lipatan kulit di leher dan perut, telinga panjang menggantung, kepala relatif pendek dengan profil melengkung, mata besar dan tenang, tanduk pendek, kadang-kadang hanya berupa “bungkul” kecil saja, mulai dagu sampai bagian dada terdapat gelambir yang lebar dan panjang. Bulu sapi ini berwarna putih kehitaman dengan warna hitam di sekitar lubang mata selebar 1 cm.
Sosoroamidjojo (1975), Wiliamson et al. (1978)
.
Sapi Katingan Sapi jantan memiliki ukuran tubuh yang tidak terlalu besar dibandingkan sapi betina, memiliki gumba yang cukup jelas, tonjolan pada kepala bagian atas pada betina, tanduk melengkung ke depan, warna bulu mata bervariasi, warna teracak didominasi warna hitam dan coklat kemerahan, warna bulu variasi putih sampai dengan hitam.
5 Karakterisik fenotipik pada ternak digunakan sebagai penciri atau pembeda antara jenis ternak. Perbedaan karakteristik fenotipik dari bangsa sapi lokal Indonesia yaitu sapi Bali, Aceh, Pesisir, PO, dan Katingan dapat dilihat pada Gambar 1.
(a) Sapi Bali
(b) Sapi Aceh (c) Sapi Pesisir
(d) Sapi PO (e) Sapi Katingan
Gambar 1. Karakteristik Fenotipik Bangsa Sapi Lokal Indonesia. (a) Sapi Bali; (b) Sapi Aceh; (c) Sapi Pesisir; (d) Sapi PO; dan (e) Sapi Katingan.
Sumber: (a) Saputra (2008); (b) Balai Pengkajian Teknologi Pertanian Aceh (2011); (c) Sarbaini (2004); (d) Jakaria (2011); (e) Balai PengkajianTeknologi Pertanian Kalimantan Tengah (2011).
6
Gen Follicle Stimulating Hormone Receptor (FSHR)
Keberadaan hormon FSH sangat dipengaruhi oleh adanya gen FSH dan gen FSHR. Gen FSH terbagi atas dua subunit yaitu α-subunit dan β-subunit dengan struktur yang berbeda (Alfredo, 1998). Salah satu fungdi FSH adalah merangsang pertumbuhan folikel pada ovarium dan menginisiasi serta meningkatkan kerja sel-sel sertoli pada proses spermatogenesis (Xing et al., 2001), fungsi tersebut didukung oleh aktivasi reseptor spesifik yang disebut FSH reseptor (Simoni et al., 1997)
Gen FSHR diperlukan untuk membawa gen FSH ke target jaringan sehingga dapat diterjemahkan menjadi protein hingga menjadi hormon FSH. Gen FSHR terdapat pada kromosom 11 dan terdiri dari 10 exon dan 9 intron dengan panjang 2375 bp (Houde et al., 1994).
Keterangan: = ekson = intron Ekson 1 = 251 bp Ekson 6 = 78 bp
Ekson 2 = 72 bp Ekson 7 = 69 bp Ekson 3 = 75 bp Ekson 8 = 75 bp Ekson 4 = 75 bp Ekson 9 = 186 bp Ekson 5 = 72 bp Ekson 10 = >1234 bp
Gambar 2. Struktur Gen FSHR Sumber: Leslie & Griswold, 2002
Sistem ekspresi gen reseptor FSH (FSHR) merupakan sel yang sangat spesifik yang berperan dalam siklus awal pada respon mutakhir sel Sertoli ke FSH. Respon sel yang sangat spesifik dan penting dari FSH ini terhadap proses spermatogenesis memperluas karakteristik pembawa dari gen FSHR (Heckert & Griswold, 2002).
Tombasco et al. (2000); Vasconcellos et al. (2003); dan Allan et al. (2007) melaporkan bahwa terdapat keragaman gen FSHR pada sapi Nelore yang berhubungan dengan produktivitas dan reproduktifitas. Rahal et al. (2000) menemukan dua situs mutasi gen FSHR pada sapi yang berhubungan pada sifat reproduksi. FSHR hanya terekspresi pada sel-sel granulosa di ovarium dan sel-sel sertoli di testis (Leslie et al. 1998).
7 FSH (Follicle Stimulating Hormone) yang dihasilkan di kelenjar hipofisis anterior akan memberikan pengaruh terhadap sel-sel sertoli yang terletak di dalam tubulus siminiferus. Pengaruh tersebut akan membantu untuk pemberian nutrien bagi sperma yang sedang berkembang dan mendukung spermatogenesis dalam penyediaan bahan makanan bagi sperma, serta melepaskan sel sperma yang telah matur di akhir proses spermatogenesis. Proses oogenesis, FSH akan merangsang perkembangan folikel (tempat berkembangnya ovum). Rangsangan perkembangan tersebut akan menghasilkan perkembangan hormon lainnya yang mendukung kerja oogenesis seperti dihasilkannya hormon estrogen dan progesteron (Yulianto, 2011).
Polymerase Chain Reaction-Restriction Fragment Lenght Polymorphism (PCR-RFLP)
Polymerase Chain Reaction (PCR) merupakan suatu teknologi untuk mengamplifikasi (memperbanyak) fragmen DNA spesifik secara in vitro (Mullis, 1986). Williams (2005), PCR merupakan suatu teknik yang dapat menggandakan jumlah molekul DNA pada ruas-ruas tertentu dan monomer-monomer nukleotida yang berjalan dengan bantuan primer dan enzim polymerase. Proses PCR terdiri atas tiga tahapan: (1) Denaturasi, yaitu perubahan struktur DNA utas ganda menjadi utas tunggal, (2) Annealing, yaitu penempelan primer pada sekuens DNA komplementer yang akan diperbanyak, dan (3) Ekstensi, yaitu pemanjangan primer oleh DNA polymerase (Muladno, 2002).
PCR merupakan suatu teknik untuk menggandakan jumlah molekul DNA pada ruas-ruas tertentu dan monomer-monomer nukleotida yang dilakukan secara in vitro. Proses ini berjalan dengan bantuan primer dan enzim polymerase. Primer merupakan oligonukleotida spesifik yang menempel pada bagian sampel DNA yang akan diperbanyak. Enzim polymerase merupakan enzim yang dapat mencetak urutan DNA baru. Hasil dari proses PCR dapat divisualisasikan dengan elektroforesis (Williams, 2005).
PCR-RFLP merupakan salah satu metode dalam PCR yang dikembangkan untuk memvisualisasikan perbedaan level DNA yang didasarkan oleh penggunaan enzim pemotong (restriction enzyme). Enzim restriksi ini dapat memotong DNA pada sekuens nukleotida spesifik (Montaldo dan Herrera, 1998). Metode PCR memanfaatkan urutan nukleotida yang dikenali oleh enzim restriksi dan disebut
8 dengan situs restriksi. Jika situs restriksi mengalami mutasi maka enzim restriksi tidak mampu mengenalinya. Analisis RFLP biasa digunakan untuk mendeteksi ada atau tidaknya keragaman pada gen yang berhubungan dengan sifat ekonomis (Sumantri et al., 2007).
MATERI DAN METODE Lokasi dan Waktu
Penelitian ini dilakukan di Laboratorium Genetika Molekuler Ternak, Bagian Pemuliaan dan Genetik Ternak, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut Pertanian Bogor. Penelitian telah dilaksanakan pada bulan Februari sampai Juli 2012.
Materi Sampel
Sampel darah yang digunakan berasal dari sapi lokal Indonesia yang terdiri atas sapi Bali, Aceh, Pesisir, PO, dan Katingan. Sampel tersebut merupakan koleksi Laboratorium Genetika Molekuler Ternak dengan jumlah seperti yang tertera pada Tabel 2 berikut.
Tabel 2. Jumlah Sampel Sapi yang Digunakan
No Ternak Sapi Asal n
1 Bali BIB Bali 16
2 Aceh Kab. Aceh Besar 12
3 Pesisir Kab. Pesisir Selatan 29
4 PO BIB Lembang 32
5 Katingan Kalimantan Tengah 40
Total 129
Keterangan: n = jumlah individu
Bahan dan Alat
Bahan yang digunakan untuk mengambil sampel adalah alkohol 70%, es batu dan kapas. Bahan yang digunakan untuk mengekstraksi DNA adalah sampel darah, Destilation Water (DW), NaCl, Proteinase-K, 1 x STE (5M NaCl, 2M tris HCl, 0,2M EDTA), SDS 10% (sodium dodesil sulfat), CIAA, ethanol absolute, ethanol 70%, phenol, dan buffer TE 80% (tris EDTA). Bahan yang digunakan untuk mengamplifikasi gen FSHR dengan teknik PCR-RFLP adalah sampel DNA, destilated water (DW), buffer, MgCl2, pasangan primer fragmen Gen FSHR|Alu-1, enzim Taq polymerase, dNTP (deoxy Nucleotida Triphosfat). dan enzim restriksi
10 Alu-1 serta buffernya. Bahan yang digunakan adalah produk PCR, agarose, loading dye, marker 100 pb, enzim restriksi Alu-1, 0,5 x TBE, dan Ethidium Bromide (EtBr). Bahan yang digunakan untuk elektroforesis produk PCR adalah produk PCR, agarose, loading dye, marker 100pb, 0,5 x TBE, dan Ethidium Bromide.
Alat yang digunakan untuk mengambil sampel adalah jarum venoject, tabung vacutainer 10 ml dan termos. Alat yang diperlukan untuk mengekstraksi DNA adalah tabung eppendorf 1,5 ml, satu set mikro pipet, tip, vortexmixer, autoclave, microsentrifuge, rotary mixer, inkubator, dan freezer. Alat yang digunakan untuk mengamplifikasi gen FSHR|Alu-1 adalah satu set pipet mikro, tip pipet, mesin sentrifuse, mesin thermosycler, rak dan tabung eppendorf, dan vortex. Alat yang digunakan untuk genotyping adalah tip pipet, mikropipet 10 P Gilson, gelas kimia, gelas ukur, stirrer, microwave, gel tray, pencetak untuk sumur (comb), power supply electrophoresis 100 volt, alat foto UV trans iluminator, dan sarung tangan. Alat yang digunakan untuk elektroforesis fragmen DNA adalah tip pipet, mikropipet, gelas kimia, gelas ukur, stirrer, microwave, gel tray, pencetak untuk sumur (comb), power supply electrophoresis 100 volt, alat foto UV trans iluminator, dan sarung tangan.
Prosedur Pengambilan Sampel
Pengambilan sampel dilakukan pada sapi lokal Indonesia, yaitu sapi Bali, Aceh, Pesisir, PO, dan Katingan. Sampel darah diambil melalui vena jugularis (pada bagian leher sapi) dengan menggunakan jarum venoject pada tabung vaccutainer yang ditambahkan ethanol absolute dengan perbandingan 1 : 2 dan disimpan dalam lemari es hingga akan digunakan lebih lanjut. Sampel yang digunakan dalam penelitian ini menggunakan data sekunder yang merupakan koleksi Laboratorium Genetika Molekuler Ternak. Sampel diperoleh dari berbagai tempat di Balai Inseminasi Buatan.
Ekstraksi DNA
Ekstraksi DNA dilakukan dengan menggunakan metode yang dikemukakan oleh Sambrook et al. (1989). Pengekstraksian DNA dimulai dengan persiapan sampel terlebih dahulu. Sebanyak 200 µl sampel darah dimasukkan ke dalam tabung 1,5 ml dan ditambahkan 1000 µl DW (destilation water). Campuran sampel darah
11 dan DW dikocok atau divortex dan didiamkan selama lima menit, kemudian disentrifuge selama lima menit dengan kecepatan 8000 rpm. Supernatan yang terbentuk dibuang dan seperti proses sebelumnya diulangi kembali. Tahapan selanjutnya adalah degradasi protein dalam DNA. Penambahan Proteinase-K sebanyak 10 µl, 350 µl 1xSTE (sodium tris-EDTA) serta 40 µl 10% SDS (sodium dodesil sulfat) ke dalam tip mix. Campuran tersebut selanjutnya diinkubasi pada suhu 55oC selama 2 jam sambil dikocok perlahan menggunakan alat pemutar.
Tahapan degradasi bahan organik dilakukan dengan cara menambahkan NaCl sebanyak 40 µl 5M, larutan fenol 400 µl dan 400 µl CIAA (chloroform iso amil alcohol), lalu dikocok pelan dalam suhu ruang selama satu jam. Bagian akhir dari tahapan ekstraksi DNA adalah presipitasi DNA. Proses ini dilakukan dengan sentifugasi larutan hasil degradasi bahan organik dengan kecepatan 12.000 rpm selama lima menit sehingga terbentuk fase DNA. Sebanyak 40 µl dari fase DNA yang terbentuk diambil dan dipindahkan ke dalam tabung baru 1,5 ml. NaCl 5 M sebanyak 40 µl dan ethanol absolute sebanyak 800 µl ditambahkan, kemudian dihomogenkan dan didiamkan over night pada suhu -20oC. Molekul DNA yang terbentuk selanjutnya dipisahkan dari ethanol absolute dengan cara disentrifugasi pada kecepatan 12.000 rpm selama lima menit dan supernatan yang diperoleh dibuang, kemudian ditambahkan kembali 800 µl ethanol absolute dan kembali disentrifugasi dengan kecepatan 12.000 rpm selama lima menit. Endapan molekul DNA diperoleh dengan cara membuang bagian supernatan yang terbentuk. Endapan tersebut kemudian didiamkan sampai kering dan disuspensikan dalam 100 µl 80% buffer TE (tris EDTA).
Amplifikasi DNA
Amplifikasi dilakukan menggunakan metode PCR-RFLP. 1 µl sampel DNA, 10,85 µl DW, 0,3 µl primer, 0,05 µl taq polymerase, 1,5 µl buffer, 0,3 µl dNTP dan 1 µl MgCl2 dicampurkan sebagai mix untuk mengamplifikasi DNA. Tahapan Amplifikasi invitro berlangsung sebanyak 35 siklus dengan menggunakan mesin thermocycler. Kondisi suhu yang terjadi yakni pada saat pra-denaturasi 94oC selama lima menit, 35 siklus dengan tahapan masing-masing siklus terdiri dari denaturasi 94oC selama 45 detik, anneling pada suhu 60oC selama 45 detik dan ekstensi pada
12 suhu 72oC selama satu menit. Tahap selanjutnya adalah ekstensi akhir 72oC selama lima menit.
Primer yang digunakan untuk mengamplifikasi gen FSHR|Alu-1 berdasarkan Houde et al. (1994) adalah forward: 5’-CTG CCT CCC TCA AGG TGC CCC TC-3’; dan reverse: 5’-CCC CCT AAG ACA TTT AGC CCA GAACT-3’ (Gambar 3).
Forward
1 atctctgcct ccctcaaggtgcccctcatc actgtgtcca agtcaaagatcctcctggtc 61 ctgttctacc ccatcaactcctgtgccaac cccttcctct atgccatcttcaccaagaac 121 ttccgcaggg atttcttcattctgctgagc aagtttggct gctatgaagtgcaagcccag 181 AC|CTataggt cagaaacctcatccactgcc cacaactttc atccaaggaacggccactgc 241 cccccAG|CTcccagggttactaatggttcc aattacacac ttatccccctaagacattta
301 gccaagaact aaaacacaat
Reverse
Keterangan :
: primer forward : primer reverse
AG|CT : situs pemotongan enzim Alu-I
Alel C : mempunyai basa C pada posisi basa ke 193 Alel G : mempunyai basa G pada posisi basa ke 193
Gambar 3. Posisi penempelan primer pada sekuen Posisi Penempelan Primer (cetak tebal) pada sekuen gen FSHR|Alu-1 (gene bank accses code: L22319.1). Keberhasilan suatu proses PCR sangat tergantung dari primer yang digunakan. Di dalam proses PCR, primer berfungsi sebagai pembatas fragmen DNA target yang akan diamplifikasi dan sekaligus menyediakan gugus hidroksi (-OH) pada ujung 3’ yang diperlukan untuk proses eksistensi DNA. Perancangan primer dapat dilakukan berdasarkan urutan DNA yang telah diketahui ataupun dari urutan protein yang dituju. Data urutan DNA atau protein bisa didapatkan dari database GenBank. Apabila urutan DNA maupun urutan protein yang dituju belum diketahui maka perancangan primer dapat didasarkan pada hasil analisis homologi dari urutan DNA atau protein yang telah diketahui mempunyai hubungan kekerabatan yang terdekat (Handoyo et al., 2001).
Elektroforesis
Tahapan proses elektroforesis produk PCR dilakukan dengan pembuatan gel agarose 1% terlebih dahulu, dengan cara melarutkan agarose sebanyak 0,30 g dengan larutan 0,5 x TBE 30 ml. Larutan tersebut kemudian dipanaskan dalam microwave selama lima menit dan distirer dengan menambahkan 2,5 µl EtBr. Larutan yang masih cair dituangkan ke dalam cetakan gel dan sisir cetakan
13 ditempatkan di bagian tepian gel, lalu dibiarkan mengeras. Apabila gel sudah mengeras, sisir cetakan gel diangkat sehingga terbentuk sumur-sumur. Tahapan berikutnya, sebanyak 5 µl produk PCR dicampur dengan 1 µl loading dye (bromothymol blue 0,01%, xylene cyanol 0,01% dan gliserol 50%) menggunakan mikropipet dan dimasukkan masing-masing ke dalam sumur gel. 2 µl marker dicampur dengan loading dye dan diletakkan di posisi paling kiri sumur yang berfungsi sebagai penanda. Gel tersebut kemudian diletakkan ke dalam gel tray elektroforesis yang berisi larutan buffer dan dialiri listrik 100 volt sekitar 30 menit. Molekul DNA yang bermuatan negatif pada pH netral akan bergerak (bermigrasi) ke arah positif. Gel agarose diangkat setelah proses elektroforesis selesai yang ditandai dengan garis biru yang telah mendekati ambang batas sumur gel. Hasil panjang pita DNA diamati dengan menggunakan sinar ultraviolet. Tahapan ini dilakukan dengan menarik garis lurus antara posisi pita dari masing-masing sampel DNA yang ingin diukur dengan posisi pita DNA marker.
Genotyping
Genotyping dilakukan dengan teknik analisis Restriction Fragment Lenght Polymorphism (RLFP). Tahapan awal proses ini adalah mencampurkan produk PCR sebanyak 5 µl ke dalam tabung 0,5 ml kemudian ditambahkan 0,2 µl enzim restriksi Alu-1. Mix tersebut kemudian diinkubasi selama 16 jam pada suhu 37oC.
Sampel DNA yang telah dipotong dengan enzim restriksi selama proses inkubasi dikeluarkan dari inkubator, kemudian masing-masing tip ditambahkan loading dye sebanyak 1 µl. Masing-masing sampel tersebut kemudian dielektroforesis kembali dengan tegangan 100 volt sekitar 30 menit pada gel agarose. Sampel DNA yang telah selesai dielektroforesis kemudian diangkat dan diamati panjang pita DNA yang terbentuk menggunakan sinar ultraviolet. Panjang pita yang terlihat dibandingkan dengan penanda marker untuk mengetahui panjangnya. Setiap pita DNA dari setiap sampel dibandingkan dengan marker untuk menentukan genotipe pita DNA. Satu posisi migrasi yang sama dianggap sebagai satu tipe atau alel yang bersifat homozigot.
14
Rancangan dan Analisis Data
Keragaman genotipe pada masing-masing sampel dapat dilihat dari pita-pita yang ditemukan. Masing-masing sampel dianalisis menggunakan pendekatan nilai frekuensi genotipe, frekuensi alel, dan nilai heterozigositas.
Frekuensi Genotipe dan Alel
Frekuensi genotipe dan alel gen FSHR|Alu-1dihitung berdasarkan rumus (Nei & Kumar, 2000) :
Frekuensi genotipe adalah
X
ii=
Keterangan :
xii = frekuensi genotipe ke-ii nii = jumlah individu bergenotipe ii N = jumlah individu sampel
Frekuensi alel adalah
X
i=
Keterangan :
xi = frekuensi alel ke-i
nii = jumlah individu bergenotipe ii nij = jumlah individu bergenotipe ij N = jumlah individu sampel
Heterozigositas
Pendugaan nilai heterozigositas pengamatan (Ho) dan heterozigositas harapan (He) dihitung menggunakan rumus Weir (1996) :
∑
Keterangan :
Ho = heterozigositas pengamatan (populasi) nij = jumlah individu heterozigot
N = jumlah individu yang diamati
∑
Keterangan :
He = nilai heterozigositas harapan xi = frekuensi alel
HASIL DAN PEMBAHASAN Amplifikasi Gen FSHR|Alu-1
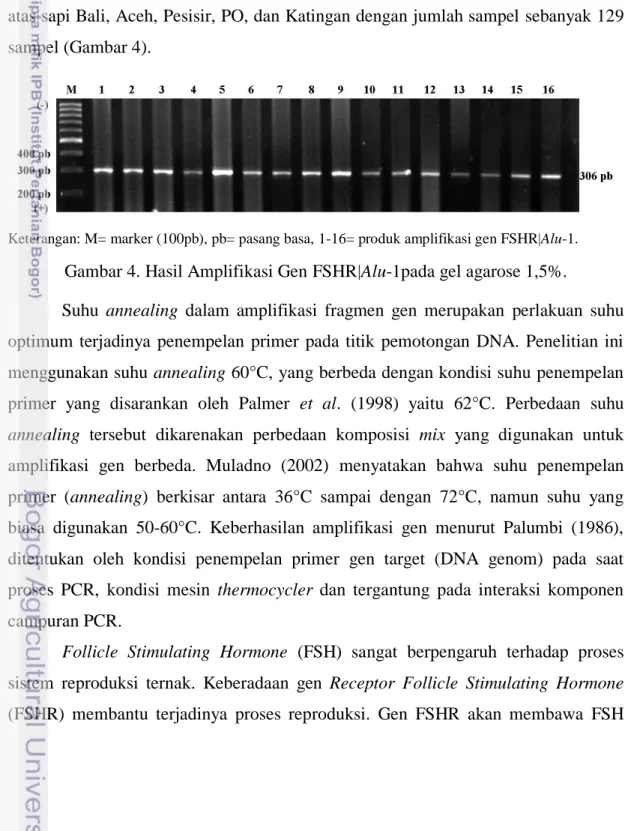
Amplifikasi fragmen gen FSHR|Alu-1 dengan metode Polymerase Chain Reaction (PCR) dilakukan dengan kondisi annealing 60°C selama 45 detik dan diperoleh produk PCR dengan panjang 306 pb yang divisualisasikan dengan menggunakan 1,5% gel agarose. Primer yang digunakan dalam proses PCR ini menggunakan rancangan Houde et al. (1994). Proses amplifikasi fragmen gen FSHR|Alu-1 berhasil dilakukan 100% pada sampel sapi lokal Indonesia yang terdiri atas sapi Bali, Aceh, Pesisir, PO, dan Katingan dengan jumlah sampel sebanyak 129 sampel (Gambar 4).
Keterangan: M= marker (100pb), pb= pasang basa, 1-16= produk amplifikasi gen FSHR|Alu-1. Gambar 4. Hasil Amplifikasi Gen FSHR|Alu-1pada gel agarose 1,5%.
Suhu annealing dalam amplifikasi fragmen gen merupakan perlakuan suhu optimum terjadinya penempelan primer pada titik pemotongan DNA. Penelitian ini menggunakan suhu annealing 60°C, yang berbeda dengan kondisi suhu penempelan primer yang disarankan oleh Palmer et al. (1998) yaitu 62°C. Perbedaan suhu annealing tersebut dikarenakan perbedaan komposisi mix yang digunakan untuk amplifikasi gen berbeda. Muladno (2002) menyatakan bahwa suhu penempelan primer (annealing) berkisar antara 36°C sampai dengan 72°C, namun suhu yang biasa digunakan 50-60°C. Keberhasilan amplifikasi gen menurut Palumbi (1986), ditentukan oleh kondisi penempelan primer gen target (DNA genom) pada saat proses PCR, kondisi mesin thermocycler dan tergantung pada interaksi komponen campuran PCR.
Follicle Stimulating Hormone (FSH) sangat berpengaruh terhadap proses sistem reproduksi ternak. Keberadaan gen Receptor Follicle Stimulating Hormone (FSHR) membantu terjadinya proses reproduksi. Gen FSHR akan membawa FSH
16 melalui impuls FSHR menuju sel target sehingga proses pembentukan sel ovum pada ternak betina dan sel spermatozoa pada ternak jantan dapat terjadi. Penempelan primer yang terjadi melalui primer forward dan reverse yang akan menjadi perhitungan panjang primer dari produk PCR yang dihasilkan. Amplifikasi DNA gen FSHR pada sampel sapi Bali, Aceh, Pesisir, PO, dan Katingan melalui proses PCR menghasilkan panjang produk amplifikasi DNA sepanjang 306 bp.
Keragaman Gen FSHR|Alu-1
Keragaman gen FSHR|Alu-1 dapat dideteksi dengan teknik PCR-RFLP menggunakan enzim restriksiAlu-1. Enzim restriksiAlu-1 memotong DNA dengan mengenali situs pemotongan AG|CT. Keragaman genetik berdasarkan frekuensi genotipe dan alel tersebut akan terdeteksi setelah terjadi pemotongan pada titik potong DNA.
Fragmen gen FSHR|Alu-1yang dihasilkan setelah proses PCR dan RFLP dari masing-masing sampel sapi diperoleh dua macam alel (C dan G) dan tiga macam genotipe (CC, CG, dan GG). Alel C merupakan titik potong yang dikenali oleh enzim restriksi dalam fragmen gen FSHR pada posisi basa ke 243 pb, sedangkan alel G berada pada posisi basa ke 193 pb dan 243 pb. Pemotongan alel C menghasilkan dua fragmen (243 pb dan 63 pb) dan pemotongan alel G menghasilkan tiga fragmen (193, 63 dan 50 pb).
Keragaman genotipe fragmen gen FSHR|Alu-1 yang dihasilkan menunjukkan kemunculan pita yang beragam dengan tiga macam genotipe, yaitu CC, CG, dan GG. Genotipe CC terdiri dari dua pita dengan panjang 243 dan 63 pb, genotipe CG terdiri dari empat pita dengan panjang 243, 193, 63, dan 50 pb, sedangkan genotipe GG terdiri dari tiga pita dengan panjang 193, 63, dan 50 pb (Marson, 2005).
Genotipe homozigot CC dan GG menujukkan bahwa masing-masing tetua menyumbangkan jumlah gen (alel) yang sama, sedangkan ternak dengan genotipe heterozigot (GC) menunjukkan bahwa ternak tersebut memiliki kombinasi gen yang berbeda dari kedua tetuanya.
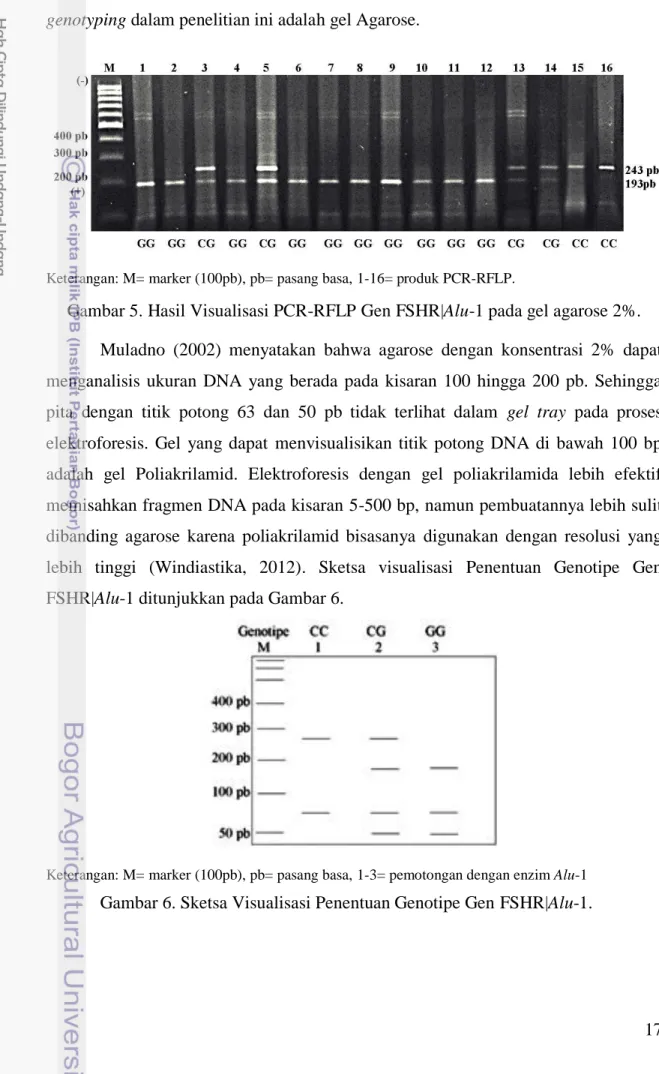
Hasil visualisasi produk PCR-RFLP pada gel agarose 2% ditampilkan pada Gambar 5. Hasil visualisasi tersebut menunjukkan pita yang terlihat adalah pita dengan panjang 243 dan 193 pb, sedangkan panjang pita 63 dan 50 pb tidak dapat
17 dilihat. Hal tersebut terjadi karena gel yang digunakan untuk menvisualisasikan hasil genotyping dalam penelitian ini adalah gel Agarose.
Keterangan: M= marker (100pb), pb= pasang basa, 1-16= produk PCR-RFLP.
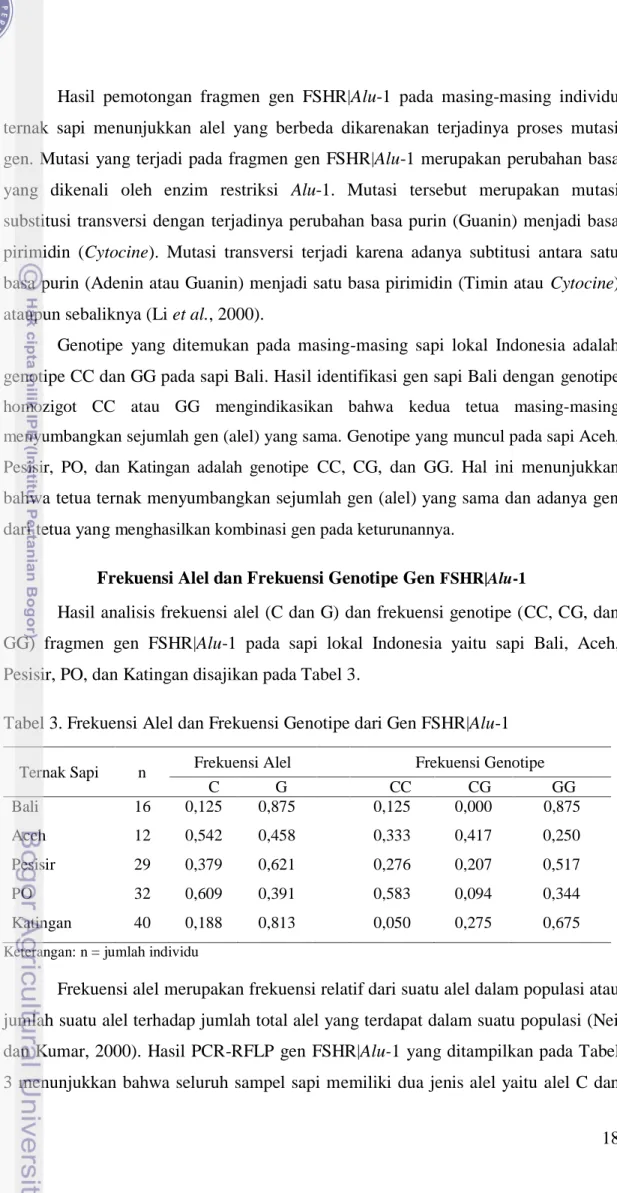
Gambar 5. Hasil Visualisasi PCR-RFLP Gen FSHR|Alu-1 pada gel agarose 2%. Muladno (2002) menyatakan bahwa agarose dengan konsentrasi 2% dapat menganalisis ukuran DNA yang berada pada kisaran 100 hingga 200 pb. Sehingga pita dengan titik potong 63 dan 50 pb tidak terlihat dalam gel tray pada proses elektroforesis. Gel yang dapat menvisualisikan titik potong DNA di bawah 100 bp adalah gel Poliakrilamid. Elektroforesis dengan gel poliakrilamida lebih efektif memisahkan fragmen DNA pada kisaran 5-500 bp, namun pembuatannya lebih sulit dibanding agarose karena poliakrilamid bisasanya digunakan dengan resolusi yang lebih tinggi (Windiastika, 2012). Sketsa visualisasi Penentuan Genotipe Gen FSHR|Alu-1 ditunjukkan pada Gambar 6.
Keterangan: M= marker (100pb), pb= pasang basa, 1-3= pemotongan dengan enzim Alu-1 Gambar 6. Sketsa Visualisasi Penentuan Genotipe Gen FSHR|Alu-1.
18 Hasil pemotongan fragmen gen FSHR|Alu-1 pada masing-masing individu ternak sapi menunjukkan alel yang berbeda dikarenakan terjadinya proses mutasi gen. Mutasi yang terjadi pada fragmen gen FSHR|Alu-1 merupakan perubahan basa yang dikenali oleh enzim restriksi Alu-1. Mutasi tersebut merupakan mutasi substitusi transversi dengan terjadinya perubahan basa purin (Guanin) menjadi basa pirimidin (Cytocine). Mutasi transversi terjadi karena adanya subtitusi antara satu basa purin (Adenin atau Guanin) menjadi satu basa pirimidin (Timin atau Cytocine) ataupun sebaliknya (Li et al., 2000).
Genotipe yang ditemukan pada masing-masing sapi lokal Indonesia adalah genotipe CC dan GG pada sapi Bali. Hasil identifikasi gen sapi Bali dengan genotipe homozigot CC atau GG mengindikasikan bahwa kedua tetua masing-masing menyumbangkan sejumlah gen (alel) yang sama. Genotipe yang muncul pada sapi Aceh, Pesisir, PO, dan Katingan adalah genotipe CC, CG, dan GG. Hal ini menunjukkan bahwa tetua ternak menyumbangkan sejumlah gen (alel) yang sama dan adanya gen dari tetua yang menghasilkan kombinasi gen pada keturunannya.
Frekuensi Alel dan Frekuensi Genotipe Gen FSHR|Alu-1
Hasil analisis frekuensi alel (C dan G) dan frekuensi genotipe (CC, CG, dan GG) fragmen gen FSHR|Alu-1 pada sapi lokal Indonesia yaitu sapi Bali, Aceh, Pesisir, PO, dan Katingan disajikan pada Tabel 3.
Tabel 3. Frekuensi Alel dan Frekuensi Genotipe dari Gen FSHR|Alu-1
Ternak Sapi n Frekuensi Alel Frekuensi Genotipe
C G CC CG GG Bali 16 0,125 0,875 0,125 0,000 0,875 Aceh 12 0,542 0,458 0,333 0,417 0,250 Pesisir 29 0,379 0,621 0,276 0,207 0,517 PO 32 0,609 0,391 0,583 0,094 0,344 Katingan 40 0,188 0,813 0,050 0,275 0,675
Keterangan: n = jumlah individu
Frekuensi alel merupakan frekuensi relatif dari suatu alel dalam populasi atau jumlah suatu alel terhadap jumlah total alel yang terdapat dalam suatu populasi (Nei dan Kumar, 2000). Hasil PCR-RFLP gen FSHR|Alu-1 yang ditampilkan pada Tabel 3 menunjukkan bahwa seluruh sampel sapi memiliki dua jenis alel yaitu alel C dan
19 G. Frekuensi alel sapi Aceh dan PO menunjukkan bahwa nilai frekuensi alel C yang lebih tinggi dibandingkan dengan alel G, sedangkan sapi Bali, Pesisir dan Katingan menunjukkan nilai frekuensi alel yang tertinggi adalah alel G dan alel yang terendah adalah alel C. Hasil keragaman gen FSHR|Alu-1 menunjukkan bahwa seluruh sampel sapi bersifat polimorfik. Hal tersebut dikarenakan, frekuensi alel masing-masing ternak sapi bernilai kurang dari 0,99. Menurut Nei (1987), suatu alel dikatakan polimorfik jika frekuensi alel bernilai sama dengan atau kurang dari 0,99 atau lebih dari 1% (Nei dan Kumar, 2000).
Identifikasi frekuensi genotipe gen FSHR|Alu-1 menunjukkan bahwa sapi Bali hanya menunjukkan dua macam genotipe yaitu genotipe CC dan GG. Hasil frekuensi genotipe sapi Aceh, Pesisir, PO, dan Katingan menunjukkan frekuensi genotipe yang lebih beragam, dengan ditemukannya ketiga macam genotipe yaitu CC, CG, dan GG. Sapi Aceh menunjukkan tiga macam genotipe dengan genotipe tertinggi adalah CG dan terendah adalah GG. Sapi Pesisir menghasilkan genotipe tertinggi adalah GG dan genotipe terendah CG. Frekuensi genotipe tertinggi sapi PO adalah CC dan terendah adalah GG, sedangkan sapi Katingan menunjukkan frekuensi genotipe tertinggi adalah GG dan terendah adalah CC. Frekuensi tertinggi yang ditemukan pada genotipe CC dan GG menunjukkan bahwa salah satu tetua menyumbangkan gen yang lebih dominan, sedangkan frekuensi genotipe CG menunjukkan bahwa ternak memiliki kombinasi gen yang sama besar dari kedua tetuanya.
Noor (2000), menyatakan jika frekuensi genotipe suatu populasi yang cukup besar akan selalu dalam keadaan seimbang bila tidak ada seleksi, migrasi, mutasi, dan genetic drift, selain itu silang dalam dan silang luar juga dapat mempengaruhi frekuensi genotipe. Frekuensi genotipe yang seringkali muncul pada individu ternak dapat dijadikan sebagai salah satu alel (penciri) spesifik pada semua bangsa sapi Indonesia.
Heterozigositas
Hasil analisis pendugaan nilai heterozigositas pengamatan (Ho) dan nilai heterozigositas harapan (He) gen FSHR|Alu-1 pada sapi lokal Indonesia yaitu sapi Bali, Aceh, Pesisir, PO, dan Katingan disajikan pada Tabel 4.
20 Tabel 4. Nilai Heterozigositas Pengamatan (Ho) dan Heterozigositas Harapan (He)
gen FSHR|Alu-1
Ternak Sapi n Heterozigositas
Ho He Bali 16 0,000 0,219 Aceh 12 0,417 0,497 Pesisir 29 0,207 0,471 PO 32 0,094 0,476 Katingan 40 0,275 0,305
Keterangan: n = jumlah individu
Keragaman genetik gen FSHR|Alu-1 dapat dilihat berdasarkan nilai heterozigositas. Nilai heterozigositas merupakan salah satu parameter yang digunakan untuk mengukur tingkat keragaman genetik dalam suatu populasi (Johari et al., 2007). Nilai heterozigositas merupakan cara yang paling akurat untuk mengukur variasi genetik, heterozigositas disebut juga sebagai keragaman gen (Nei, 1987). Perhitungan nilai heterozigositas menurut Nei (1987), adalah nilai heterozigositas yang memiliki nilai berkisar antara 0 (nol) sampai dengan 1 (satu), apabila heterozigositas sama dengan 0 (nol), maka diantara populasi yang diukur tersebut memilki hubungan genetik yang sangat dekat dan apabila nilai heterozigositas sama dengan 1 (satu), maka diantara populasi yang diukur tidak terdapat hubungan genetik atau pertalian genetik sama sekali.
Penetapan nilai heterozigositas ini didasarkan pada nilai frekuensi alel masing-masing sampel yang menghasilkan perbedaan persentasi nilai frekuensi genotipe. Nilai heterozigositas pengamatan (Ho) dan nilai heterozigositas harapan (He) dapat digunakan sebagai salah satu cara untuk menduga nilai koefisien biak dalam (inbreeding) pada suatu kelompok ternak (Hartl et al., 1997). Nilai heterozigositas pengamatan (Ho) dihitung berdasarkan nilai genotipe yang bersifat heterozigot, yaitu genotipe CG. Moioli et al. (2004) menjelaskan bahwa nilai heterozigositas harapan (He) merupakan pendugaan keragaman genetik yang tepat dalam populasi ternak karena perhitungannya didasarkan langsung pada frekuensi alel.
Perhitungan yang diperoleh dari berdasarkan Tabel 4 di atas menujukkan bahwa pendugaan nilai heterozigositas pengamatan (Ho) tertinggi terdapat pada sapi
21 Aceh (0,417). Tingginya nilai heterozigositas pada sapi Aceh menunjukkan keragaman genetik yang tinggi. Faktor yang mempengaruhi tingginya nilai heterozigositas pada populasi sapi Aceh disebabkan oleh perkawinan acak atau peluang inbreeding yang rendah (Mulliadi et al., 2010). Avise (1994) menyatakan jika semakin tinggi derajat heterozigositas dalam suatu populasi maka daya tahan populasi tersebut akan semakin tinggi.
Nilai heterozigositas pengamatan (Ho) terendah ditemukan pada sapi Bali (0,000). Javanmard et al. (2005) menyatakan bahwa heterozigositas dengan nilai di bawah 50% akan mengindikasikan rendahnya variasi suatu gen dalam populasi. Hal ini menunjukkan bahwa rendahnya keragaman gen FSHR|Alu-1 pada sapi Bali.
Hasil penelitian menunjukkan bahwa hasil PCR-RFLP gen FSHR|Alu-1 terhadap sampel sapi Bali, Aceh, Pesisir, PO, dan Katingan memiliki nilai heterosigositas pengamatan (Ho) yang lebih rendah dibandingkan nilai heterosigositas harapan (He). Machado et al. (2003) menyatakan jika nilai Ho lebih rendah dari nilai He, hal ini mengindikasikan adanya derajat endogami (perkawinan dalam kelompok) sebagai akibat proses seleksi yang intensif.
Apabila ditemukan perbedaan yang besar antara nilai heterozigositas pengamatan (Ho) dan nilai heterozigositas harapan (He) maka dapat dijadikan sebagai indikator adanya ketidakseimbangan genotipe pada populasi yang dianalisis (Tambasco et al., 2003). Sebaliknya dengan ditemukannya nilai Ho dan He yang relatif sama, maka menunjukkan keseimbangan genotipe pada populasi tersebut.
KESIMPULAN DAN SARAN Kesimpulan
Keragaman gen FSHR|Alu-1 pada sapi lokal Indonesia yang terdiri atas sapi Bali, Aceh, Pesisir, PO, dan Katingan bersifat polimorfik. Identifikasi frekuensi alel gen FSHR|Alu-1, ditemukan dua macam alel, yaitu alel C dan G. Nilai frekuensi genotipe yang diperoleh pada sapi Aceh, Pesisir, PO, dan Katingan adalah tiga macam genotipe, yaitu CC, CG, dan GG, sedangkan pada sapi Bali hanya ditemukan genotipe CC dan GG.
Saran
Penelitian mengenai keragaman gen FSHR dengan enzim restriksi Alu-1 perlu dilakukan dengan jumlah sampel yang lebih banyak lagi. Studi pustaka mengenai keragaman gen FSHR perlu diadakan kajian ulang sebagai representative hasil penelitian yang dapat dibandingkan dengan hasil telaah ilmiah.
UCAPAN TERIMA KASIH
Bismillahirrohmannirrohim, segala puji dan syukur kepada Ilahi Robbi yang menganugerahkan limpahan rahmat dan hikmah. Sholawat dan salam untuk Rosululloh Muhammad SAW yang menjadi teladan terbaik untuk seluruh ummat manusia. Ucapan terima kasih banyak Penulis sampaikan kepada Dosen Pembimbing Utama Skripsi Bapak Prof. Dr. Ir. Cece Sumantri, M.Agr.Sc. dan kepada Dosen Pembimbing Anggota Bapak Dr. Jakaria, S.Pt, M.Si. atas segala bimbingan, arahan dan ilmu yang diberikan kepada Penulis selama menempuh pendidikan di Fakultas Peternakan, khususnya selama berlangsungnya penelitian sampai dengan selesainya penulisan skripsi ini. Terima kasih pula kepada Dosen Pembimbing Akademik Bapak Bramada Winiar Putra, S.Pt., M.Si atas bimbingannya selama penulis menjalani studi di Fakultas Peternakan. Penulis juga mengucapkan terima kasih banyak kepada Ibu Dr. Ir. Sri Darwati, M.Si., Bapak Dr. Ir. Didid Diapari, M.S, dan Bapak Dr. Ir. Afton Atabany, M.Si yang telah memberikan banyak masukan dan saran untuk perbaikan skripsi penulis pada s aat ujian akhir.
Terima kasih kepada kedua orangtua yang bijak bestari penuh cinta kepada Ananda, Ibunda Farida Hanum, S.PdI dan Ayahanda Busthamey Muhammad Nasution, BA atas segala do’a, kasih sayang dan semangat yang selalu diberikan. Terima kasih pula untuk keempat orang adik yang selalu memberikan semangat untuk menjadi lebih baik, Nazhimah Bey Nasution, Hasienah Bey Nasution, Najmiyah Bey Nasution dan Muhammad Abdul Qoyyum Bey Nasution.
Terima kasih untuk sosok yang sudah banyak memberikan bantuan kepada Penulis; Kak Eryk, Kak Ferdy, Kak Irine, mb Santi, Bu Pipih, Bu Nena, dan Bu Harini. Terima kasih untuk sahabat di Laboratorium Genetika dan Molekuler Ternak (LGMT) atas segala kebersamaannya: Gya, Eka, Sri, Feby, Tessa, Isyana, Adil, Furqon, dan Menix.
Tak akan terlupakan sampai di penghujung usia untuk sahabat terbaik. Jazakumulloh khoir untuk sahabat terbaik IDers dari tahun ke tahun yang sudah memberikan pemahaman dan kesolidan azzam yang tak ternilai harganya. Wulan, Nunik, Zia, Tita, Siti, Dinis, Away, Akhyar, Dadan, Tegar. Begitu pun adik-adik terbaik FApeters atas segala keceriaan yang menginspirasi.
24 Jazakunalloh khoir teruntuk Murobbiyah dan kumpulan saudari Longlife Circle “manna”, sahabat 85ers yang tak pernah dimakan umur menahun, semua sahabat di FAA dan BEM Fapet, sahabat D’Technoduck IPTP 45, Rumah Qur’an IPB yang menjadi tempat bernaung cahaya keimanan, naungan Rumah Ramadhan di awal tahun perjuangan bermula, Salimah33 atas segala inspirasi keberaniannya. Adik-adik 47, 48 dan 49 yang selalu mengokohkan semangat dalam lingkaran-lingkaran kecil kita.
DAFTAR PUSTAKA
Adrial. 2010. Sapi lokal Kalimantan Tengah. BPTP Kalteng. http://kalteng.litbang.deptan.go.id/ind/index.php?option=com_content&view =article. [Oktober 2012].
Alfredo, U. A. & C. Timossi. 1998. Structure function relationship of follicle stimulating hormone and its receptor. J. Hum. Rep. 4 (3): 260-283.
Allan M. F., R. M. Thallman, R. A. Cushman, S. E. Echternkamp, S. N. White, L. A. Kuehn, E. Casas & T. P. L. Smith. 2007. Association of single nucleotide polymorphism in SPP1 with growt and twinning in a cattle population selected for twinning rate. Anim. Sci. 85: 341-347.
Anwar, S. 2004. Keragaman karakter eksternal dan DNA mikrosatelit sapi pesisir Sumatera Barat. Disertasi. Sekolah Pascasarjana, Institut Pertanian Bogor. Avise, J. C. 1994. Molecular Markers. Natural History Evolution. Chapman and
Hall, Inc., Washington.
Balai Pengkajian Teknologi Pertanian Aceh. 2011. Perlu upaya pembibitan dan pemurnia sapi Aceh. http://nad.litbang.deptan.go.id/. [Oktober 2012].
Balai Pengkajian Teknologi Pertanian Kalimantan Tengah. 2011. Sapi lokal katingan: adaptif, produktivitas dan keragaman fenotipik-genotipik tinggi. http://kalteng.litbang.deptan.go.id/. [Oktober 2012].
Departemen Pertanian. 2006. Peraturan Menteri Pertanian Nomor 35/Permentan/ OT.140/8/2006. Pedoman Pelestarian dan Pemanfaatan Sumber daya Genetik Ternak. Departemen Pertanian, Jakarta.
Directorate Generale of Livestock Service. 2003. National report on animal genetic resources Indonesia. Directorate of Livestock Breeding, Indonesia.
Food Agriculture Organization. 2011. The global strategy for the management of farm animal genetic resources: a call for action. FAO Publishing, Rome. Frankham, R., J. D. Ballou & D. A. Briscoe. 2002. Introduction to Conversation
Genetics. Cambridge University Press.
Handoyo, D. & A. Rudiretna. 2001. Prinsip umum dan pelaksanaan polymerase chain reaction (PCR). Pusat Studi Bioteknologi, Universitas Surabaya. Unitas, Vol. 9, No. 17-29.
Hardjopranjoto, S. 1995. Ilmu Kemajiran Pada Ternak. Airlangga University Press. Surabaya
Hardjosubroto, W. 1994. Aplikasi Pemuliabiakan Ternak di Lapangan. Gramedia Pustaka, Jakarta.
Hartl, D. L. & A. G. Clark. 2000. Principles of population genetics. 3rd Ed. Sinaeur Assosiatess, Inc., Publisher Sunderlands, Massachusetts.
26 Heckert, L. L. & M. D. Griswold. 2002. Introduction to conversation genetics.
Cambridge University Press.
Houde A., A. Lambert, J. Saumade & D. W. Silversides. 1994. Structure of the bovine follicle stimulating hormone receptor complementary DNA and expression in bovine tissues. Mol. Rep. Dev. 39: 127-135.
Jakaria, Muladno & M. Winugroho. 2011. Pembentukan bangsa sapi baru melalui persilangan sapi peranakan Ongole (PO) dengan sapi Wagyu sebagai pengayaan terhadap sumber daya genetik ternak sapi di Indonesia. Laporan Hasil Penelitian. Badan Penelitian dan Pengembangan Pertanian, Departemen Pertanian, Institut Pertanian Bogor, Bogor.
Javanmard, A., N. Asadazadeh, M. H. Banahazi & J. Tavakolian. 2005. The allele and genotype frequencies of bovine pituitary spesific transcription factor and leptin genes in Iranian cattle and buffalo population using PCR-RFLP. J. Irian. Biotech. 3: 104-108
Johari. S., E. Kurnianto, Sutopo & S. Aminah. 2007. Keragaman protein darah sebagai parameter biogenetik pada sapi jawa. J. Indonesian Trop. Agri., 32 [2] Juni 2007. Universitas Diponegoro. Semarang. Hal 112-118.
Johnson L., D.D. Varner, M. E. Roberts, T. L. Smith, G. E. Keillor & W. L. Sctruchfield. 2000. Eficiency of spermatogenesis: a comparative approach. Anim. Repro. Sci. 60-61: 471-480.
Keputusan Menteri Pertanian. 2011. Penetapan rumpun sapi Aceh. Nomor: 2907/Kpts/OT.140/6/2011.
Leslie L. H., A. F. Melissa & D. C. Jiangkai. 1998. Multiple promoter elements contribute to activity of the follicle stimulating hormone receptor (FSHR) gene in testicular sertoli cells. Mol. Endrocrinol. 10: 120-128.
Leslie L. H. & M. D. Griswold. 2002. The expression of the follicle stimulating hormone receptor in spermatogenesis. Mol. Rep. Dev. 2: 129-148.
Li, X., K. Li, B. Fan, Y. Gong, S. Zhao, Z. Peng & B. Liu. 2000. The Genetic diversity of seven pigs breeds in China, estimated by means of microsatellites. J. Anim. Sci9: 1193-1195.
Machado, M. A., I. Schuster, M. L. Martinez & A. L. Campos. 2003. Genetic diversity of four breed using microsatellite markers. Rev. Bras. De Zool. 32:93-98.
Machugh, D. E. 1996. Molecular Biogeoghraphy and Genetic Structure of Domestic Cattle. Thesis. University of Dubin. Irlandia.
Marson, E. P., B. S. Jose, V. M. Flavio, C. Julio, P. E. Joanir, G. Luis & B. M. Gerson. 2005. Genetic characterization of European Zebu composite bovine using RFLP markers. Genet. Mol. Res. 4 : 496-505.
27 Martojo, H. 2003. Indigenous Bali cattle: The best suited cattle breed for sustainable small farm in Indonesia. The Chinese Society of Animal Science. 112 Farm Road, Hsinhua, Tainan, Taiwan.
Moioli, B., F. Napolitano & G. Catillo. 2004. Genetic diversity between Piedmontese, Maremmana and Podolica cattle breeds. J. Hered. 95: 250-256. Muladno. 2002. Seputar Teknologi Rekayasa Genetika. Pustaka Wirausaha Muda
dan USESE Foundation, Bogor.
Montaldo, H. H. & C. A. M. Herrera. 1998. Use of molecular markers and major genes in genetic improvement of livestock. J. Biotech. 1 : 2.
Mulliadi, D. & J. Arifin. 2010. Pendugaan keseimbangan populasi dan heterozigositas menggunakan pola protein albumin darah pada populasi domba ekor tipis (Javanese Thin Tiled) di daerah Indramayu. Fakultas Peternakan, Universitas Padjadjaran. Jurnal Imu Ternak, Juni 2010 Vol. 10 No. 2, 65-72.
Mullis K. 1986. Specific enzymatic amplification of DNA in-vitro: the polymerase chain reaction. Cold Spring Harb Symp Quant Biol 51:263-273.
Namikawa T., Amano J., B. Pangestu & S. Natasasmita. 1982. Electrophoretic variations of blood protein and enzymes in Indonesia cattle and bantengs. The researchgroup of overseas scientific survey. Tokyo, Japan. 35-42.
Nei, M. 1987. Molecular Evolutionary Genetics. Columbia University Press, New York.
Nei, M. & S. Kumar. 2000. Molecular Evaluation and Phylogenetics. Oxford University Press, New York.
Noor, R. R. 2010. Genetika Ternak. Penebar Swadaya, Jakarta.
Otsuka, J., T. Namikawa, K. Nozawa & H. Martojo. 1982. Statistical analysis on the body measurements of East Asian native cattle and Bantengs: the origin and phylogeny of Indonesian native livestock (Part III).The Research Group of Overseas Scientific Survey.
Palmer, B. R., N. Roberts, J. G. H. Hickford & R. Bickerstaffe. 1998. Rapid communication: PCR-RFLP for Msp1and Nco1 in the ovine calpastatin gene. American Society. J. Anim. Sci. 76: 1499-1500.
Palumbi, S. R. 1986. Nucleic acid II: polymerase chain reaction. In: D.M. Hillis, C. Moritz dan B.K. Mable (Editor). Molecular Systematics. 2nd Edition. Sinauer Associates. Inc., Massachusetts USA.
Panjaitan, T. S., W. R. Sasongko, A. Muzani & W. Arief. 2003. Manajemen Terpadu Pemeliharaan Sapi Bali. Badan Penelitian dan Pengembangan Pertanian Balai Pengkajian Teknologi Pertanian, Nusa Tenggara Barat.
28 Rahal P. 2000 Polymorphisms in the bovine follicle stimulating hormone receptor
gene. Anim. Gen. 31: 280-291.
Saladin, R. 1983. Penampilan sifat-sifat produksi dan reproduksi sapi lokal Pesisir selatan di propinsi Sumatera Barat. Disertasi. Sekolah Pasca Sarjana, Institut Pertanian Bogor, Bogor.
Sambrook, J., E. F. Fritsch & J. F. Medrano. 1989. Moleculer Cloning: a laboratory maual. 2nd ed. Cold Spring Harbor Laboratory Press, New York.
Saputra, E. D. 2008. Sapi bali sebagai plasma nutfah Indonesia dan peranannya bagi petani. http://balivetman.wordpress.com/. [Oktober 2012]
Sarbaini. 2004. Kajian keragaman karakteristik eksternal dan DNA mikrosatelit sapi pesisir Sumatera Barat. Disertasi. Sekolah Pasca Sarjana, Institut Pertanian Bogor, Bogor.
Setiadi, B. & K. Dwiyanto. 2006. Pengelolaan berkelanjutan sumber daya genetik ternak. Lokakarya nasional pengelolaan dan perlindungan sumber daya genetik di Indonesia: Manfaat Ekonomi untuk Mewujudkan Ketahanan Nasional.
Simoni M., E. Nieschlag & J. Gromoll. 1997. The follicle stimulating hormone receptor: biochemistry, molecular biology, physiology, and pathophysiology. Endo. Rev. 18: 413-421.
Sumantri, C., A. Anggraeni, A. Farajallah & D. Perwitasari. 2007. Keragaman mikrosatelit DNA sapi perah FH di Balai Pembibitan Ternak Unggul; Baturaden. J. ITV 12: 124-133.
Tambasco, D. D., Paz, M. M. Alencar, Freitas, L. L. Coutinho, Packer & Regitano. 2003. Candidate genes for growth traits in beef cattle crosses Bos taurus x Bos indicus. J. Anim. Breed. Genet. 120: 51-60.
Tambasco, D. D., M. M. Alencar, & L. L. Coutinho. 2000. Characterization of Nelore cattle using microsatelite for gene candidate. Review. Zootec. Braz. 29: 1044-1049.
Toelihere, M. R, 1985. Fisiologi Reproduksi pada Ternak. Angkasa. Bandung.
Utomo, B.N., R.R. Noor, C. Sumantri, I. Supriatna & E.D. Gunardi. 2010. Keragaman morfometrik dan fenotipik sapi Katingan di Kalimantan Tengah. JITV. 15 (in Press).
Vasconcellos L. P. M. K. 2003. Genetic characterization of Aberden Angus cattle using molecular markers. Genet. Mol. Biol. 26: 133-137.
Weir, B. S. 1996. Genetic Data Analysis: Method for Discrete Population Genetic Data. 2nd ed. Sinauer associates. Sunderland, MA, USA.
29 Windiastika, G. 2012. Metode Uji Kualitatif DNA dengan Elektroforesis Gel Agarose. Balai Besar Perbenihan dan Proteksi Tanaman Perkebunan Surabaya, Surabaya.
Williamson, G. & W. J. A. Payne, 1978. An Introduction to Animal Husbandry in The Tropics, 2nd ed. ELBS and Longman Group Limited, London.
Williams, J. L. 2005 The use of marker-assisted selection in animal breeding and biotechnology. Rev. Sci. Tech. of. Int. Epiz., 24:379-391.
Xing W. & M. R. Sairam. 2001. Characterization of regulatory elements of Ovine follicle stimulating hormone (FSH) receptor gene: The Role of E-Box in the regulation of Ovine FSH Receptor expression. Bio. Rep. 64: 579-589.
Yulianto, E. 2011. http://konsepbiologi.wordpress.com/2011/05/23/sistem-reproduksi/. [Januari 2013].
31
Lampiran 1. Sekuens Gen FSHR (diakses dari Gen Bank No. L22319)
LOCUS BOVFSHR 2375 bp mRNA linear MAM 13-OCT-1994
DEFINITION Bovine follicle stimulating hormone receptor (FSHR) mRNA, complete
cds. ACCESSION L22319
VERSION L22319.1 GI:404671
KEYWORDS follicle stimulating hormone (FSH) receptor. SOURCE Bos taurus (cattle)
ORGANISM Bos taurus
Eukaryota; Metazoa; Chordata; Craniata; Vertebrata; Euteleostomi;
Mammalia; Eutheria; Laurasiatheria; Cetartiodactyla; Ruminantia; Pecora; Bovidae; Bovinae; Bos.
REFERENCE 1 (bases 1 to 2375)
AUTHORS Houde,A., Lambert,A., Saumande,J., Silversides,D.W. and Lussier,J.G.
TITLE Structure of the bovine follicle-stimulating hormone receptor complementary DNA and expression in bovine tissues
JOURNAL Mol. Reprod. Dev. 39 (2), 127-135 (1994) PUBMED 7826612
REFERENCE 2 (bases 1 to 2375) AUTHORS Lussier,J.G.
TITLE Direct Submission
JOURNAL Submitted (30-SEP-1993) Jacques G. Lussier, CRRA, Faculty of Veterinary Medicine, University of Montreal, P.O. Box 5,000, 3,200
Sicotte, St-Hyacinthe, Quebec, J2S 7C6, Canada
COMMENT Original source text: Bos taurus (strain Holstein) cDNA to mRNA. FEATURES Location/Qualifiers source 1..2375 /organism="Bos taurus" /mol_type="mRNA" /strain="Holstein" /db_xref="taxon:9913" /tissue_type="ovaries/testes" gene 1..2375 /gene="FSHR" 5'UTR 1..64 /gene="FSHR" CDS 65..2152 /gene="FSHR" /codon_start=1
/product="follicle stimulating hormone receptor" /protein_id="AAC37324.1" /db_xref="GI:404672" /translation="MALLLVALLAFLSLGSGCHHRLCHCSNGVFLCQESKVTEIPSDL PRDAVELRFVLTKLRVIPKGAFSGFGDLEKIEISQNDVLEVIEANVFSNLPKLHEIRI EKANNLLYIDPDAFQNLPNLRYLLISNTGIKHLPAVHKIQSLQKVLLDIQDNINIHTV ERNSFMGLSFESMTVWLSKNGIQEIHNCAFNGTQLDELNLSDNSNLEELPNDVFQGAS GPVILDISRTRIRSLPSYGLENLKKLRAKSTYRLKKLPSLEKFVTLVEASLTYPSHCC AFANWRRQTSDLHPICNKSILRQEVDDMTQARGQRVSLAEDDEPSYAKGFDVMYSEFD YDLCNEVVDVTCSPEPDAFNPCEDIMGDDILRVLIWFISILAITGNILVLVILITSQY KLTVPRFLMCNLAFADLCIGIYLLLIASVDVHTKTEYHNYAIDWQTGAGCDAAGFFTV