INTISARI
Penelitian ini merupakan optimasi formula gel UV Protection endapan perasan wortel (Daucus carota, Linn.) tinjauan terhadap humektan gliserol dan propilen glikol. Tujuan dari penelitian ini untuk memperoleh range komposisi optimum dari humektan gliserol dan propilen glikol sehingga dapat diperoleh gel yang mempunyai sifat fisik dan stabilitas gel yang baik.
Penelitian ini merupakan rancangan eksperimental bersifat eksploratif. Optimasi formula gel ini menggunakan metode Simplex Lattice Design dengan variasi komposisi humektan gliserol dan propilen glikol. Optimasi tersebut dilakukan terhadap parameter sifat fisik sediaan gel (daya sebar dan viskositas) serta stabilitas sediaan gel dalam penyimpanan selama 1 bulan. Uji mikromeritik juga dilakukan untuk memberikan informasi tentang ukuran partikel sehingga dapat memberikan nilai estetika yang tinggi.
Dari penelitian ini dilakukan optimasi formula gel UV Protection endapan perasan wortel (Daucus carota, Linn.) dengan sifat fisik meliputi daya sebar 3 cm sampai 5 cm, viskositas 310 d.Pa.s sampai 315 d.Pa.s, dan stabilitas gel yang ditunjukkan dengan persen pergeseran viskositas kurang dari 15%. Pada penelitian ini tidak dapat diperoleh range komposisi optimum terbatas pada komposisi humektan gliserol dan propilen glikol yang diteliti. Namun berdasarkan hasil percobaan dipilih formula III dengan komposisi humektan gliserol : propilen glikol (50% : 50%) sebagai formula optimum yang menghasilkan sifat fisik dan stabilitas gel paling baik.
ABSTRACT
This research was about optimization formula of UV Protection sediment carrot juice (Daucus carota, Linn.) gel review to glycerol and propylene glycol as
humectant. The aiming of this research was to obtain optimum composition range from glycerol and propylene glycol humectant to achieve a gel which had a good physical character and stability.
This research was including exploratively experimental design. This optimization formula gel used Simplex Lattice Design method with various compositions of glycerol and propylene glycol humectant. It was done to the parameter of physical characteristic of semisolid (spreadability and viscosity) and the stability during storing for a month. Micromeritic test was also done to give information about particle size so it could achieved a high aesthetics value.
From this research was done optimization the formulation of sediment extract carrot (Daucus carota, Linn.) UV Protection gel with physical character such as spreadability 3 cm to 5 cm, viscosity 310 d.Pa.s to 315 d.Pa.s, and gel stability which was shown with alteration of viscosity less than 15%. At this research, it could not be obtained optimum composition range that was limited to the compositions of glycerol and propylene glycol humectant had been done. But based on result of the research was selected the 3rd formula with composition of glycerol and propylene glycol humectant (50% : 50%) as optimum formula which achieved good physical character and stability.
OPTIMASI FORMULA GEL
UV PROTECTION
ENDAPAN PERASAN WORTEL (
Daucus carota
, Linn.) :
TINJAUAN TERHADAP
HUMEKTAN GLISEROL DAN PROPILEN GLIKOL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh :
Dian Kurniasari
NIM : 048114021
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
OPTIMASI FORMULA GEL
UV PROTECTION
ENDAPAN PERASAN WORTEL (
Daucus carota
, Linn.) :
TINJAUAN TERHADAP
HUMEKTAN GLISEROL DAN PROPILEN GLIKOL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh :
Dian Kurniasari
NIM : 048114021
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
Skripsi
OPTIMASI FORMULA GEL
UV PROTECTION
ENDAPAN PERASAN WORTEL (
Daucus carota
, Linn.) :
TINJAUAN TERHADAP
HUMEKTAN GLISEROL DAN PROPILEN GLIKOL
Yang diajukan oleh :
Dian Kurniasari
NIM : 048114021
telah disetujui oleh:
Pembimbing :
Sri Hartati Yuliani, M.Si., Apt.
God make a way very beautiful when the time is right
remember and believe that doesn’t matter how difficult your life
just wait and He will make a way for you
Jeremiah 29 : 11 -12
I alone know the plans I have for you, plans to bring you prosperity
and not disaster, plans to bring about the future you hope for.
Then you will call to me.
You will come and pray to me, and I will answer you
.
Matthew 19:26
This is impossible for man, but for God everything is possible
Karya ini kupersembahkan untuk orang-orang yang aku kasihi :
“Jesus Christ”
Papa, Mama, dan Dina Ko Edwin Baskara
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma :
Nama : Dian Kurniasari
Nomor Mahasiswa : 048114021
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
Optimasi Formula Gel
UV Protection
Endapan Perasan Wortel
(
Daucus carota,
Linn.): Tinjauan terhadap Humektan Gliserol dan
Propilenglikol
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, me-ngalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 28 Januari 2008
Yang menyatakan
PRAKATA
Puji syukur kepada Tuhan Yang Maha Pengasih atas segala kasih
karunia dan anugerah-Nya sehingga penulis dapat menyelesaikan skripsi dengan
judul “Optimasi Formula Gel UV Protection Endapan Perasan Wortel (Daucus
carota, Linn.) : Tinjauan terhadap Gliserol dan Propilen Glikol” dengan baik.
Skripsi ini dibuat untuk memenuhi salah satu syarat memperoleh gelar Sarjana
Farmasi (S. Farm.) pada Program Studi Farmasi di Universitas Sanata Dharma.
Penulis banyak mengalami kesulitan selama penyelesaian skripsi ini.
Tetapi dengan adanya bimbingan, bantuan dan dukungan dari berbagai pihak,
penulis dapat menyelesaikan skripsi ini. Oleh karena itu, penulis igin
mengucapkan terima kasih kepada :
1. “Jesus Christ” atas semua kasih karunia dan cinta-Mu, tanpa Engkau
penulis tidak akan mampu menyelseaikan skripsi ini.
2. Ibu Rita Suhadi, M.Si., Apt., selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
3. Ibu Sri Hartati Yuliani, M.Si., Apt., selaku Dosen Pembimbing yang telah
banyak meluangkan waktu, tenaga dan atas segala bimbingan dalam
penyusunan skripsi ini.
4. Ibu Rina Kuswahyuning, M.Si., Apt., selaku Dosen Penguji atas segala
kritik dan sarannya.
5. Ibu Agatha Budi Susiana L., M.Si., Apt., selaku Dosen Penguji atas segala
6. Pak Musrifin, Mas Agung, Mas Iswandi, Mas Ottok, Mas Parlan, Mas
Sarwanto, Mas Kunto serta laboran-laboran yang lain atas bantuannya
selama penulis menyelesaikan laporan akhir.
7. Papa, mama, dan Dina atas segala dukungan dan doa selama penyusunan
skripsi ini.
8. Ko Edwin Baskara atas segala doa, dukungan, perhatian, dan kasih sayang
yang telah diberikan selama ini.
9. Ineke, Desy, Cipi, Budiaji, Finza, Ela, dan Andryan atas kerjasama, canda
tawa dan keluh kesah selama penyusunan skripsi ini.
10.Semua teman-teman angkatan 2004, terima kasih atas segala semangat dan
kebersamaan kita yang indah.
11.Semua penghuni kost Amakusa atas kekompakan dan kebersamaannya.
12.Semua pihak yang telah banyak membantu penyusunan skripsi ini.
Penulis juga menyadari sepenuhnya penulisan skripsi ini tidak terlepas
dari keterbatasan dan kekurangan penulis. Untuk itu penulis mengharapkan saran
dan kritik yang membangun dari semua pihak. Akhir kata semoga skripsi ini dapat
berguna bagi pembaca.
Penulis
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 23 Januari 2008
Penulis
INTISARI
Penelitian ini merupakan optimasi formula gel UV Protection endapan perasan wortel (Daucus carota, Linn.) tinjauan terhadap humektan gliserol dan propilen glikol. Tujuan dari penelitian ini untuk memperoleh range komposisi optimum dari humektan gliserol dan propilen glikol sehingga dapat diperoleh gel yang mempunyai sifat fisik dan stabilitas gel yang baik.
Penelitian ini merupakan rancangan eksperimental bersifat eksploratif. Optimasi formula gel ini menggunakan metode Simplex Lattice Design dengan variasi komposisi humektan gliserol dan propilen glikol. Optimasi tersebut dilakukan terhadap parameter sifat fisik sediaan gel (daya sebar dan viskositas) serta stabilitas sediaan gel dalam penyimpanan selama 1 bulan. Uji mikromeritik juga dilakukan untuk memberikan informasi tentang ukuran partikel sehingga dapat memberikan nilai estetika yang tinggi.
Dari penelitian ini dilakukan optimasi formula gel UV Protection endapan perasan wortel (Daucus carota, Linn.) dengan sifat fisik meliputi daya sebar 3 cm sampai 5 cm, viskositas 310 d.Pa.s sampai 315 d.Pa.s, dan stabilitas gel yang ditunjukkan dengan persen pergeseran viskositas kurang dari 15%. Pada penelitian ini tidak dapat diperoleh range komposisi optimum terbatas pada komposisi humektan gliserol dan propilen glikol yang diteliti. Namun berdasarkan hasil percobaan dipilih formula III dengan komposisi humektan gliserol : propilen glikol (50% : 50%) sebagai formula optimum yang menghasilkan sifat fisik dan stabilitas gel paling baik.
ABSTRACT
This research was about optimization formula of UV Protection sediment carrot juice (Daucus carota, Linn.) gel review to glycerol and propylene glycol as humectant. The aiming of this research was to obtain optimum composition range from glycerol and propylene glycol humectant to achieve a gel which had a good physical character and stability.
This research was including exploratively experimental design. This optimization formula gel used Simplex Lattice Design method with various compositions of glycerol and propylene glycol humectant. It was done to the parameter of physical characteristic of semisolid (spreadability and viscosity) and the stability during storing for a month. Micromeritic test was also done to give information about particle size so it could achieved a high aesthetics value.
From this research was done optimization the formulation of sediment extract carrot (Daucus carota, Linn.) UV Protection gel with physical character such as spreadability 3 cm to 5 cm, viscosity 310 d.Pa.s to 315 d.Pa.s, and gel stability which was shown with alteration of viscosity less than 15%. At this research, it could not be obtained optimum composition range that was limited to the compositions of glycerol and propylene glycol humectant had been done. But
based on result of the research was selected the 3rd formula with composition of
glycerol and propylene glycol humectant (50% : 50%) as optimum formula which achieved good physical character and stability.
Key word : gel, sediment of extract carrot, UV Protection, humectant, Simplex
DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL... ii
HALAMAN PERSETUJUAN PEMBIMBING.... ... iii
HALAMAN PENGESAHAN... iv
HALAMAN PERSEMBAHAN ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS... vi
PRAKATA... vii
PERNYATAAN KEASLIAN KARYA ... ... ix
INTISARI ... x
ABSTRACT ... xi
DAFTAR ISI ... xii
DAFTAR TABEL ... xvi
DAFTAR GAMBAR ... xvii
DAFTAR LAMPIRAN ... xix
BAB I. PENGANTAR ... 1
A. Latar Belakang ... 1
B. Perumusan Masalah ... 4
C. Keaslian Karya ... 4
D. Manfaat Penelitian ... 5
BAB II. PENELAAHAN PUSTAKA... 6
A. Wortel (Daucus carota, Linn.)... 6
1. Uraian tanaman ... 6
2. Nama daerah... 6
3. Kandungan kimia ... 6
4. Kegunaan ... 7
B. Beta Karoten ... 7
C. Radikal Bebas ... 8
D. Antioksidan ... 9
E. Sinar Ultraviolet ... 9
F. Sun Protection Factor (SPF)... 10
G. Gel ... 12
1. Definisi gel ... 12
2. Karakteristik gel ... 13
H Carbopol... 15
I. Humektan... 17
1. Gliserol... 17
2. Propilen glikol... 18
J. Trietanolamin ... 19
K. Spektrofotometri Ultraviolet ... 20
L. Mikromeritik ... 21
M. Metode Simplex Lattice Design... 22
BAB III. METODOLOGI PENELITIAN ... 25
A. Jenis Rancangan Penelitian ... 25
B. Variabel dalam Penelitian ... 25
C. Definisi Operasional ... 26
D. Alat dan Bahan... 27
E. Tata Cara Penelitian ... 28
1. Ekstraksi kadar beta karoten dalam endapan perasan wortel (Daucus carota, Linn.)... 28
2. Penetapan kadar beta karoten dalam endapan perasan wortel (Daucus carota, Linn.)... 28
3. Uji Sun Protection Factor (SPF) ... 30
4. Optimasi pembuatan gel UV Protection... 30
5. Uji sifat fisik dan stabilitas fisik gel UV Protection... 32
6. Uji mikromeritik ... 32
F. Analisis Data dan Optimasi ... 33
BAB IV. HASIL DAN PEMBAHASAN ... 34
A. Ekstraksi Kadar Beta Karoten dalam Endapan Perasan Wortel (Daucus carota, Linn.)... 34
B. Penetapan Kadar Beta Karoten dalam Endapan Perasan Wortel (Daucus carota, Linn.)... 35
C. Uji Sun Protection Factor (SPF) ... 38
D. Optimasi Pembuatan Gel UV Protection... 39
F. Mikromeritik ... 53
G. Optimasi Formula... 55
BAB V. KESIMPULAN DAN SARAN …... 61
A. Kesimpulan ... 61
B. Saran... 61
DAFTAR PUSTAKA ... 62
LAMPIRAN ... 66
DAFTAR TABEL
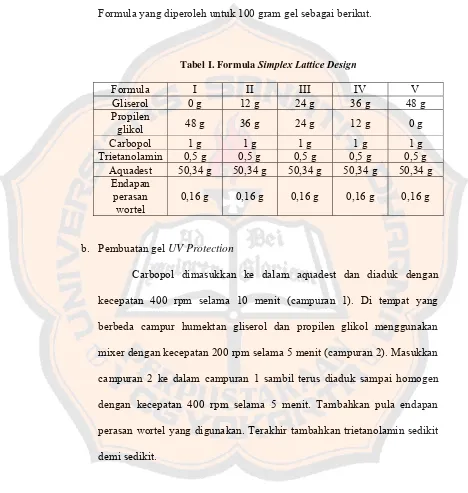
Tabel I. Formula Simplex Lattice Design...31
Tabel II. Kurva baku beta karoten dengan Spektrofotometer Genesis 10...36
Tabel III. Jumlah baku beta karoten dalam 1 gram endapan perasan wortel dengan dengan Spektrofotometer Genesis 10...37
Tabel IV. Hasil pengukuran SPF ...39
Tabel V. Kurva baku beta karoten dengan Perkin-Elmer Spektrofotomer UV-Vis Lambda 20...41
Tabel VI. Jumlah baku beta karoten dalam 1 gram endapan perasan wortel karoten dengan Perkin-Elmer Spektrofotomer UV-Vis Lambda 20...42
Tabel VII. Hasil pengukuran SPF dalam 100 gram gel. ...42
Tabel VIII. Hasil pengukuran sifat fisik dan stabilitas gel UV Protection...44
Tabel IX. Hasil perhitungan uji F pada daya sebar gel UV Protection...47
Tabel X. Hasil perhitungan uji F pada viskositas gel UV Protection...50
Tabel XI. Hasil perhitungan uji F pada pergeseran viskositas gel UV Protection...52
Tabel XII. Hasil uji pH gel UV Protection...53
Tabel XIII. Hasil pengukuran partikel gel UV Protection...54
DAFTAR GAMBAR
Gambar 1. Struktur molekul beta karoten...7
Gambar 2. Struktur molekul carbopol ...15
Gambar 3. Struktur molekul gliserol ...17
Gambar 4. Struktur molekul propilen glikol...18
Gambar 5. Struktur molekul trietanolamin ... 19
Gambar 6. Struktur beta karoten dengan sistem kromofor ...35
Gambar 7. Kurva baku beta karoten II...37
Gambar 8. Hasil scanning panjang gelombang serapan maksimum larutan baku beta karoten 2 ppm, 6 ppm, dan 10 ppm dengan pelarut aseton : heksan (1:9)...40
Gambar 9. Kurva baku beta karoten I ...41
Gambar 10. Hasil scanning larutan baku beta karoten dengan pelarut kloroform ...43
Gambar 11. Hasil scanning endapan perasan wortel dengan pelarut kloroform ...43
Gambar 12. Grafik hubungan antara humektan gliserol dan propilen glikol dengan respon daya sebar gel UV Protection endapan perasan wortel ...46
Gambar 14. Grafik hubungan antara humektan gliserol dan propilen glikol
dengan respon pergeseran viskositas gel UV Protection endapan
perasan wortel ...51
Gambar 15. Grafik distribusi ukuran partikel gel UV Protection endapan
perasan wortel ...55
Gambar 16. Contour plot respon daya sebar viskositas gel UV Protection
DAFTAR LAMPIRAN
Lampiran 1. Penetapan Kadar Beta Karoten dalam Endapan Perasan Wortel .66
Lampiran 2. Perhitungan Nilai SPF Beta Karoten ...71
Lampiran 3. Data Penimbangan Gel ...77
Lampiran 4. Data Sifat Fisik dan Stabilitas Gel ...78
Lampiran 5. Data pH Gel ...80
Lampiran 6. Persamaan Simplex Lattice Design...81
Lampiran 7. Uji F...85
Lampiran 8. Data Uji Mikromeritik ...91
BAB I
PENGANTAR
A. Latar Belakang
Radiasi UV dapat menyebabkan variasi efek biologis terhadap kulit
seperti eritema (kulit kemerahan), pigmentasi, dan imunomodulasi. Paparan UV
secara terus-menerus dapat menyebabkan skin aging dan meningkatkan resiko
kanker kulit. Reactive Oxygen Species (ROS) merupakan penyebab utama skin
aging dan penyakit kulit lainnya. Radikal bebas muncul setelah kulit terpapar
radiasi sinar ultraviolet. Lapisan epidermis mengandung antioksidan sehingga
dapat memberikan perlindungan awal untuk melawan radikal bebas. Tetapi kadar
antioksidan akan berkurang setelah terpapar UV terus-menerus. Oleh karena itu,
untuk mencegah kerusakan kulit akibat adanya radikal bebas dibutuhkan
antioksidan (Watson, 2001).
Salah satu antioksidan eksogen yang didapat dari luar tubuh adalah beta
karoten (Setiati, 2003). Beta karoten yang terdapat dalam wortel berfungsi sebagai
antioksidan (Watson, 2001). Beta karoten bereaksi dengan Reactive Oxygen
Species (ROS) untuk menetralkan oksigen singlet dan mencegah pembentukan
radikal peroksil (Paiva dan Russel, 1999). Oleh karena itu, dalam penelitian ini
menggunakan wortel sebagai bahan aktif dari sediaan UV Protection.
Baik antioksidan topikal maupun oral dapat mengontrol kelebihan
menyebabkan photo aging bahkan kanker (Morquio, A., Rivera-Megret, F., dan
Dajas, F., 2005). Saat ini suplemen beta karoten digunakan sebagai oral sun
protectant yang dapat mengurangi resiko kerusakan kulit akibat radiasi UV (Sies
dan Stahl, 2003; Weber, S.U., Saliou, C., Packer, L., Lodge, J.K., 2001). Hal
tersebut menarik minat penulis untuk membuat sediaan topikal UV Protection
karena sediaan tersebut langsung berinteraksi dengan kulit yang terpapar radiasi
UV.
Telah banyak sediaan UV Protection yang beredar di pasaran tetapi
produk-produk tersebut mengandung bahan aktif berupa senyawa sintetik. Akan
tetapi, penggunaan UV Protection dengan bahan aktif yang berasal dari bahan
alam lebih menguntungkan daripada senyawa sintetik karena produk-produk dari
bahan alam lebih aman dan memiliki toleransi yang baik terhadap kulit (Fridd,
1996). Oleh karena itu, dalam penelitian ini menggunakan bahan alam sebagai
alternatif dalam pembuatan UV Protection.
Bentuk sediaan UV Protection yang banyak dikembangkan berupa
cream dan lotion. Cream merupakan bentuk sediaan semisolid yang terdiri dari
dua fase, yaitu fase minyak dan fase air sehingga membentuk emulsi (Nairn,
1997). Bentuk sediaan ini dapat menimbulkan masalah kulit seperti jerawat
terutama pada orang yang memproduksi kelenjar sebacea berlebihan. Lotion
adalah bentuk sediaan cair yang dapat berbentuk suspensi di dalam air, tetapi
dapat juga berbentuk larutan atau emulsi (Nairn, 1997). Lotion mempunyai
viskositas yang cukup encer sehingga tidak dapat bertahan lama pada kulit dan
mengatasi kekurangan tersebut, maka perlu dikembangkan suatu bentuk sediaan
lain yaitu gel.
Menurut Barry (1993) gel merupakan sistem dua komponen dari sediaan
semipadat yang kaya akan cairan. Hidrogel adalah hidrofilik yang mengandung
85-95% air atau campuran aqueous-alcoholic dan gelling agent (Buchmann,
2001). Karakteristik gel secara estetika menarik karena transparan. Setelah kering,
gel akan meninggalkan lapisan tipis di kulit dan mempunyai daya lekat yang
tinggi. Akan tetapi gel tidak menyumbat pori-pori kulit sehingga tidak
merangsang timbulnya jerawat dan mudah dicuci dengan air. Oleh karena itu,
maka dalam penelitian ini dipilih bentuk sediaan yaitu hidrogel.
Setelah diaplikasikan, gel akan memberikan efek dingin karena adanya
evaporasi air. Evaporasi air yang cepat dapat mempengaruhi daya sebar sediaan
gel. Untuk memberikan proteksi terhadap kehilangan air tersebut, dapat digunakan
humektan. Selain itu, humektan juga dapat membantu menjaga kelembaban kulit
dengan cara menjaga kandungan air pada lapisan stratum corneum serta mengikat
air dari lingkungan ke kulit (Rawlings, Harding, Watkinson, Chandar, dan Scott,
2002). Dalam penelitian ini digunakan gliserol dan propilen glikol sebagai
humektan. Gliserol akan meningkatkan kelarutan solut lipofilik (Buchmann,
2001) sedangkan propilen glikol bersifat higroskopik (Anonim, 1979) sehingga
dapat menjaga konsistensi sediaan. Penggunaan gliserol dan proplen glikol secara
bersamaan akan meningkatkan sifat fisik dan stabilitas gel yang dihasilkan.
Penelitian ini bertujuan untuk mengetahui profil sifat fisik gel dengan
mendapatkan range komposisi optimum formula gel UV Protection endapan
perasan wortel (Daucus carota, Linn.) yang menghasilkan sifat fisik dan stabilitas
gel yang dikehendaki. Komposisi humektan gliserol dan propilen glikol
dioptimasi dengan menggunakan metode Simplex Lattice Design. Metode ini
dapat digunakan untuk mengetahui sifat-sifat fisik dari dua campuran dan
memprediksi sifat-sifat campuran tersebut pada semua perbandingan (Bolton,
1997).
B. Perumusan Masalah
1. Dapatkah ditemukan range komposisi optimum humektan gliserol dan
propilen glikol dalam formula gel UV Protection endapan perasan wortel
(Daucus carota, Linn.) yang menghasilkan sifat fisik dan stabilitas gel
yang dikehendaki?
2. Berapa jumlah komposisi humektan gliserol dan propilen glikol dalam
formula gel UV protection endapan perasan wortel (Daucus carota, Linn.)
yang menghasilkan formula optimum?
3. Bagaimana profil sifat fisik dan stabilitas gel UV Protection endapan
perasan wortel (Daucus carota, Linn.) dengan berbagai variasi komposisi
humektan gliserol dan propilen glikol?
C. Keaslian Karya
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian tentang
Linn.) : Tinjauan terhadap Humektan Gliserol dan Propilen Glikol belum pernah
dilakukan.
D. Manfaat Penelitian
Secara teoritis penelitian ini menambah informasi bagi ilmu pengetahuan,
khususnya dalam bidang kefarmasian mengenai aplikasi Simplex Lattice Design
pada proses optimasi formula gel UV Protection. Secara praktis penelitian ini
bermanfaat untuk mengetahui jumlah komposisi humektan gliserol dan propilen
glikol dalam formula gel UV protection endapan perasan wortel (Daucus carota,
Linn.) yang menghasilkan sifat fisik dan stabilitas gel yang dikehendaki.
E. Tujuan Penelitian
1. Untuk mendapatkan range komposisi optimum humektan gliserol dan
propilen glikol dalam formula gel UV Protection endapan perasan wortel
(Daucus carota, Linn.) yang menghasilkan sifat fisik dan stabilitas gel
yang dikehendaki.
2. Untuk mengetahui jumlah komposisi humektan gliserol dan propilen glikol
dalam formula gel UV protection endapan perasan wortel (Daucus carota,
Linn.) yang menghasilkan formula optimum.
3. Untuk mengetahui profil sifat fisik dan stabilitas gel UV Protection
endapan perasan wortel (Daucus carota, Linn.) dengan berbagai variasi
BAB II
PENELAAHAN PUSTAKA
A. Wortel (Daucus carota, Linn.)
1. Uraian tanaman
Semak semusim, tinggi kurang lebih kurang 1 meter. Batang tegak,
berbulu, warna hijau. Daun majemuk, menyirip, berselang, bentuk lonjong, tepi
bertoreh, ujung runcing, pangkal berlekuk, warna hijau. Perbungaan bentuk
cawan, terdapat di ujung batang, mahkota berbentuk bintang, berwarna putih.
Buah buni, lonjong, warna coklat. Biji lonjong, warna putih (Soedibyo, 1998).
2. Nama daerah
Sunda : bortol
Jawa : wertel, wertol, bortol
Madura : ortel
(Rukmana, 1995)
3. Kandungan kimia
Dalam setiap 100 gram mengandung 42 kalori; protein 1,2 gram;
lemak 0,3 gram; karbohidrat 9,3 gram; kalsium 39 miligram; fosfor 37
miligram; zat besi 0,8 miligram; vitamin A; vit BI 0,06 miligram; vitamin C 6
miligram (Arisandi Y., dan Andriani, Y., 2006). Kandungan lain yang penting
4. Kegunaan
Untuk keperluan kosmetik, wortel dapat digunakan untuk merawat
kecantikan wajah dan kulit, menjaga kelembaban kulit, melembutkan kulit,
memperlambat timbulnya kerutan pada wajah, dan antioksidan (Cahyono,
2002; Watson, 2001).
B. Beta Karoten
Karotenoid yaitu tetraterpenoid C40, merupakan golongan pigmen
yang larut lipid dan tersebar luas, terdapat dalam semua jenis tumbuhan.
Pada tumbuhan karotenoid mempunyai dua fungsi, yaitu sebagai pigmen
pembantu dalam fotosintesis dan sebagai pewarna dalam bunga dan buah.
Dalam bunga, karotenoid biasanya berupa zat warna kuning, sedangkan
dalam buah dapat juga berupa zat warna jingga atau merah (tomat dan cabe)
(Harborne, 1987). Karotenoid juga banyak terdapat di dalam wortel dan
sayuran berwarna hijau. Karotenoid bekerja sebagai antioksidan serta
penangkap radikal bebas, terutama untuk radikal peroksil (R-OO.) dan hidroksil
(.OH) serta oksigen singlet (02.) (Silalahi dan Tambunan, 2003). Beberapa
contoh karotenoid yang telah diketahui yaitu xantofil, β-karoten, α-karoten,
likopen, lutein, γ-karoten (Harborne, 1987).
Beta karoten larut dalam benzen, kloroform; cukup larut di eter,
petroleum eter dan sangat sedikit larut di metanol dan etanol. Sebanyak 100
ml heksan dapat melarutkan 109 mg beta karoten pada suhu 0°C (Anonim,
1989). Beta karoten berkhasiat sebagai antioksidan (Tjay dan Rahardja, 2002).
Beta karoten bereaksi dengan Reactive Oxygen Species (ROS) untuk menetralkan
oksigen singlet dan mencegah pembentukan radikal peroksil (Paiva dan Russel,
1999).
C. Radikal Bebas
Radikal bebas adalah suatu spesies yang mempunyai jumlah elektron
ganjil atau elektron yang tidak berpasangan tunggal pada lingkaran luarnya.
Elektron tidak berpasangan tersebut menyebabkan instabilasi dan bersifat reaktif,
karena selalu berusaha untuk mencari pasangan elektron lainnya agar menjadi
bentuk yang stabil. Radikal bebas akan merusak molekul yang elektronnya ditarik
oleh radikal bebas tersebut sehingga menyebabkan kerusakan sel, gangguan
fungsi sel, bahkan kematian sel. Molekul utama di dalam tubuh yang dirusak oleh
radikal bebas yaitu DNA, lemak, dan protein (Fessenden dan Fessenden, 1997;
Setiati, 2003).
Radikal bebas diproduksi secara eksogen dan secara endogen. Secara
endogen, radikal bebas diproduksi oleh mitokondria, membran plasma, lisosom,
retikulum endoplasma, dan intisel. Sedangkan secara eksogen, radikal bebas
berasal dari asap rokok, radiasi sinar UV, obat-obatan, dan pestisida (Setiati,
D. Antioksidan
Proses perusakan organ tubuh oleh radikal bebas dapat dihambat dengan
jalan memberikan antioksidan (Tjay dan Rahardja, 2002). Antioksidan adalah
senyawa yang mampu menghambat oksidasi, atau juga disebut dengan inhibitor
radikal bebas (Fessenden dan Fessenden, 1997).
Antioksidan dibedakan menjadi antioksidan eksogen dan antioksidan
endogen. Antioksidan endogen atau antioksidan primer terdiri atas enzim-enzim
dan berbagai senyawa yang disintesis dalam tubuh yang bekerja dengan cara
mencegah pembentukan radikal bebas baru. Antioksidan eksogen dikenal juga
sebagai antioksidan sekunder karena menangkap radikal dan mencegah reaksi
berantai. Contohnya adalah vitamin E (tokoferol), vitamin C (askorbat), karoten,
asam urat bilirubin, dan albumin (Setiati, 2003).
E. Sinar Ultraviolet
Berdasarkan panjang gelombangnya, sinar UV dibagi menjadi 3 yaitu :
1. UV A, mempunyai panjang gelombang 320 nm sampai 400 nm
2. UV B, mempunyai panjang gelombang 290 nm sampai 320 nm
3. UV C, mempunyai panjang gelombang 200 nm sampai 290 nm
(Harry, 1982)
Sinar UV A dilaporkan menyebabkan efek samping hilangnya kolagen,
menurunkan jumlah pembuluh darah, dan mengubah jaringan konektif pada
dermis. Sinar UV B bertanggung jawab terhadap sunburn setelah terpapar oleh
di kulit sehingga terbentuk melanin. Sinar UV C sangat berbahaya tetapi diserap
oleh lapisan ozon dan gas-gas lain yang ada di atmosfer (Walters, 1997).
F. Sun Protection Factor (SPF)
Sun Protection Factor (SPF) adalah tingkat perlindungan produk
sunscreen terhadap sinar matahari yang dapat menyebabkan sunburn (eritema).
SPF merupakan perbandingan MED (Minimal Erythema Dose) pada kulit manusia
yang terlindungi oleh sunscreen dengan MED tanpa perlindungan sunscreen
(Stanfield, 2003). Kondisi tes standar ditetapkan dosis sunscreen adalah 2 mg/
cm2.
SPF = sunscreen sunscreen a kulit tanp untuk MED ) cm / mg (2 dengan kulit untuk MED 2 (Walters, 1997)
MED ditentukan dengan membuat sebuah seri secara progresif untuk
meningkatkan dosis energi UV dan mengevaluasi respon setelah 22-24 jam. MED
merupakan dosis terkecil dari energi UV yang menghasilkan eritema dengan
batasan yang jelas pada bagian yang terpapar (Stanfield, 2003).
Meskipun pengukuran SPF dapat dilakukan secara alami dengan melihat
respon biologis yang tidak diketahui hubungannya dengan sifat kimia, tetapi dapat
diperkirakan hubungan sederhana antara absorbansi dan SPF, sebagai berikut :
⎥⎦ ⎤ ⎢⎣ ⎡ = SPF 1 log
-A 10 = log10SPF
Keterangan :
I0 = intensitas sinar yang sampai ke kulit tanpa adanya sunscreen
I = intensitas sinar yang sampai ke kulit dengan adanya sunscreen
A = serapan
(Walters, 1997)
Selain itu, serapan dari tiap-tiap panjang gelombang dapat dihitung sebagai
berikut :
A= - log
(Stanfield, 2003)
Kategori produk sunscreen dengan variasi nilai SPF yang dianjurkan
yaitu :
1. Minimal Sun Protection Product : nilai SPF 2-4, sangat kurang memproteksi
dari sunburning dan suntanning
2 Moderate Sun Protection Product : nilai SPF 4-6, cukup memproteksi dari
sunburning tapi beberapa suntanning
3. Extra Sun Protection Product : nilai SPF 6-8, proteksi ekstra dari sunburning
dan sedikit suntanning
4. Maximal Sun Protection Product : nilai SPF 8-15, proteksi maksimal dari
sunburning dan sedikit atau tidak suntanning
5. Ultra Sun Protection Product : nilai SPF >15, proteksi paling besar dari
sunburning dan tidak suntanning
Sunscreen dengan SPF 2 akan mentransmisikan 50% energi matahari
yang dapat menyebabkansunburn, SPF 15 mentransmisikan 6,7% energi matahari
yang dapat menyebabkan sunburn, dan SPF 30 mentransmisikan 3,3% energi
matahari yang dapat menyebabkan sunburn (Stanfield, 2003).
G. Gel
1. Definisi gel
Gel merupakan sistem semisolid terdiri dari suspensi yang dibuat dari
partikel anorganik yang kecil atau molekul organik yang besar, terpenetrasi oleh
cairan (Zatz dan Kushla,1996). Alexander dan Johnson (1949) mendefinisikan gel
sebagai sistem dua komponen dari sediaan semipadat yang kaya akan cairan. Pada
gel yang polar, polimer alam atau sintetik dengan konsentrasi rendah (biasanya
kurang dari 10%) membentuk matriks tiga dimensi melalui cairan hidrofilik.
Sistem yang terbentuk mungkin jernih atau keruh, karena gelling agent tidak
terlarut sempurna atau membentuk agregat (Barry, 1983).
Hidrogel mengandung dua unsur yaitu air dan susbstansi polimer yang
hidrofilik tetapi tidak larut air. Dengan adanya air, polimer kering akan
mengembang dan mengabsorbsi cairan. Salah satu alasan penggunaan hidrogel
adalah pelarut yang digunakan dalam pembuatan obat mempunyai kompatibilitas
2. Karakteristik gel
Sifat umum yang diinginkan dari sediaan semisolid adalah dapat
diterima oleh konsumen karena memiliki sifat tertentu yaitu mudah dikeluarkan
dari wadah, sensasinya ketika kontak dengan kulit, kemampuan melekat pada
tempat aplikasi selama waktu tertentu sebelum dibilas atau luntur, residu yang
tidak meninggalkan rasa lengket setelah aplikasi dan efikasi klinis yang terkait
pelepasan obat dan absorpsi. Hal ini terkait dengan daya sebar dan viskositas
sediaan sehingga perlu diperhatikan dalam formulasinya (Garg, A., Aggarwal, D.,
Garg, S., dan Singla, A.K., 2002).
a. Daya sebar
Daya sebar berhubungan dengan sudut kontak tiap tetes cairan atau
sediaan semisolid, yang berhubungan langsung dengan koefisien friksi.
Faktor-faktor yang mempengaruhi daya sebar adalah formulanya kaku atau tidak,
kecepatan dan lama tekanan yang menghasilkan kelengketan, temperatur tempat
aksi. Kecepatan penyebaran juga tergantung pada viskositas formula, kecepatan
evaporasi pelarut, dan kecepatan peningkatan viskositas karena evaporasi (Garg et
al., 2002).
Metode yang paling banyak digunakan untuk menentukan dan mengukur
daya sebar dari sediaan semisolid adalah parallel-plate method. Keuntungan
metode ini yaitu mudah dan relatif murah. Kelemahan metode ini yaitu kurang
b. Viskositas
Viskositas adalah suatu pernyataan tahanan dari suatu cairan untuk
mengalir. Semakin tinggi viskositas maka semakin besar tahanannya (Martin dan
Cammarata, 1993). Karakteristik formulasi yang penting dalam produk akhir
sediaan semisolid adalah viskositas, elastisitas, dan rheologi. Peningkatan
viskositas akan meningkatkan waktu retensi pada tempat aksi tetapi akan
menurunkan daya sebar (Garg et al., 2002). Jika konsentrasi gelling agent yang
digunakan terlalu tinggi atau dengan bobot molekul yang terlalu besar, maka akan
menghasilkan gel yang susah diaplikasikan (Zatz dan Kushla, 1996).
Thiksotropi merupakan suatu pemulihan yang isoterm dan lambat pada
pendiaman suatu bahan yang kehilangan konsistensinya karena shearing.
Thiksotropi hanya dapat diterapkan untuk bahan-bahan dengan tipe aliran plastis
dan pseudoplastis (Martin dan Cammarata, 1993). Dalam penyimpanannya, gel
dapat berupa thiksotropi, membentuk semisolid jika dibiarkan dan menjadi cair
pada pengocokan (Anonim, 1995).
c. Stabilitas
Ketidakstabilan gel pada kondisi normal menunjukkan perubahan
rheologi secara irreversible sehingga menyebabkan hasil akhir yang tidak dapat
diterima bila digunakan. Faktor yang bertanggungjawab terhadap pergeseran
viskositas adalah perubahan agen pembentuk viskositas, interaksi dengan sistem
pada kondisi istirahat, dan pertumbuhan partikel yang tergantung pada kandungan
perubahan ukuran partikel. Hasil depolimerisasi akan menurunkan rata-rata berat
molekul sehingga akan menurunkan viskositas (Zatz et al., 1996).
Peningkatan suhu penyimpanan dapat menyebabkan efek yang
berlawanan pada stabilitas polimer sehingga viskositas berubah dari waktu ke
waktu. Selama penyimpanan 2 bulan, terjadi pergeseran viskositas yang kecil
pada suhu ruangan atau pendingin. Akan tetapi, pada suhu 400C terjadi pergeseran
viskositas 15% atau lebih (Zatz et al., 1996).
H. Carbopol
Carbopol merupakan polimer sintesis dari kelompok acrylic polymers
yang membentuk rantai silang dengan polyalkenyl ether (Zatz dan Kushla, 1996).
Struktur molekul carbopol sebagai berikut :
C C
H
H H
COOH n
Gambar 2. Struktur molekul carbopol
Carbopol digunakan sebagai suspending agent pada konsentrasi sampai
0,4% dan basis gel (Anonim, 1999; Weiner dan Bernstein, 1989). Selain itu,
carbopol dapat menstabilkan emulsi dengan mengentalkan fase kontinyu sehingga
mengurangi creaming dan coalescence atau dengan berfungsi sebagai emulsifier
pada konsentrasi kurang dari 1% (Barry, 1983; Zatz dan Kushla, 1996). Carbopol
diaplikasikan pada kulit dan memberi lapisan minyak pada permukaan kulit.
Lapisan minyak ini tidak akan diemulsifikasikan kembali ketika bersentuhan
dengan air sehingga akan melekat pada kulit (Zatz dan Kushla, 1996). Carbopol
tidak toksik, tidak mensentisasi, dan tidak mempengaruhi aktivitas biologi obat
tertentu (Barry,1983).
Di dalam gel carbopol dapat digunakan untuk mengontrol dan
meningkatkan viskositas (thickener) pada pH antara 3,5 sampai 11 (Weiner dan
Bernstein, 1989). Carbopol 1% mempunyai pH 3. Pada pH 6-11 viskositas gel
akan meningkat. Viskositas gel akan menurun pada pH kurang dari 3 atau lebih
dari 12 dan bila terdapat elektrolit kuat. Viskositas gel berkurang dengan cepat
bila terpapar sinar matahari tetapi reaksi ini dapat dikurangi lajunya dengan
menambahkan antioksidan (Boyland, Cooper, dan Chowhan, 1986).
Jika didispersikan ke dalam air, carbopol membentuk larutan asam keruh
dengan pH 2,8 sampai 3,2 tetapi tidak larut dan dapat dinetralkan dengan basa
kuat seperti natrium hidroksida, amina (misalnya trietanolamin), atau basa
anorganik lemah (misalnya amonium hidroksida), sehingga meningkatkan
konsistensi dan menurunkan kekeruhan (Barry, 1983; Zatz, Berry, dan Alderman,
1996). Gel carbopol yang tidak dinetralkan dapat menurunkan viskositas lebih
banyak dibandingkan yang dinetralkan karena ikatan hidrogen pada struktur gel
yang tidak dinetralkan mudah putus (Barry, 1983).
Dalam suasana asam sebagian gugus karboksil pada rantai polimer putus
untuk membentuk gulungan yang lentur. Dengan penambahan basa, gugus
bagian-bagian yang diserang memperbesar molekul sehingga gel lebih kaku dan
mengembang. Bila penambahan basa berlebihan gel akan menjadi encer karena
kation-kation melindungi gugus karboksil dan gaya tolak menolak elektrostatik
berkurang (Barry, 1993).
I. Humektan
Humektan adalah bahan dalam produk kosmetik yang dimaksudkan
untuk mencegah hilangnya lembab dari produk dan meningkatkan jumlah air
(kelembaban) pada lapisan kulit terluar saat produk digunakan (Loden, 2001).
Humektan adalah bahan higroskopis yang mempunyai sifat menyerap uap air dari
udara lembab sehingga dapat mempertahankan kelembaban kulit (Johnson, 1992).
Humektan membantu menjaga kelembaban kulit dengan cara menjaga kandungan
air pada lapisan stratum corneum serta mengikat air dari lingkungan ke kulit
(Rawlings, Harding, Watkinson, Chandar, dan Scott, 2002).
1. Gliserol
C OH
H
H C OH
H C H
OH H
Gambar 3. Struktur molekul gliserol(Anonim, 1995)
Gliserol adalah cairan seperti sirup jernih dengan rasa manis. Gliserol
dan sering digunakan sebagai stabilisator dan sebagai suatu pelarut pembantu
dalam hubungannya bersama dengan air atau alkohol (Ansel, 1989). Gliserol
dapat digunakan sebagai emmolient dan humektan dengan konsentrasi
0,2%-65,7%. Selain itu, gliserol juga dapat digunakan sebagai plasticizer, pelarut, dan
pengisotonis dalam produk farmasetis (Smolinske, 1992). Penambahan gliserol
juga akan menurunkan polaritas solven dan meningkatkan kelarutan solut lipofilik
(Buchmann, 2001). Gliserol tidak mengiritasi dan sangat jarang mensensitisasi
kulit (Smolinske, 1992).
2. Propilen Glikol
C
H H
H C C
H OH
H OH
H
Gambar 4. Struktur molekul propilen glikol (Anonim, 1995)
Propilen glikol adalah cairan kental, jernih, tidak berwarna, rasa sedikit
tajam, dan higroskopik. Propilen glikol dapat dicampur dengan air, alkohol,
aseton, dan kloroform. Dapat larut dalam eter dan dapat melarutkan minyak
menguap, tetapi tidak dapat campur dengan minyak lemak (Anonim, 1979).
Propilen glikol dapat digunakan sebagai humektan dalam konsentrasi
sekitar 15%. Selain itu, propilen glikol dapat digunakan sebagai plasticizer,
pelarut, hygroscopic agent, desinfektan, stabilizer untuk vitamin, dan cosolvent
berfungsi sebagai pengawet (Boyland, Cooper, dan Chowhan, 1986; Anger,
Claude, B., Rupp, D., Lo, P.,1996). Propilen glikol digunakan sebagai gelling
agent pada konsentrasi 1% sampai 5%, stabil pada pH 3 sampai 6 dan harus
mengandung pengawet (Allen, 2002). Propilen glikol merupakan bahan yang
tidak berbahaya dan aman digunakan pada produk kosmetik dengan konsentrasi
lebih dari 50% (Loden, 2001).
J. Trietanolamin
N
HO OH
HO
Gambar 5. Struktur molekul trietanolamin
Trietanolamin merupakan campuran basis yang dibuat dari reaksi antara
etilen oksida dengan amonia (Stephenson, 2000). Trietanolamin adalah cairan
higroskopis yang bening, tidak berwarna atau berwarna kuning pucat, kental, tidak
berbau atau sedikit berbau amonia. Trietanolamin dapat bercampur dengan air dan
alkohol, larut dalam kloroform, sedikit larut dalam eter. Dalam air 10% larutan
trietanolamin bersifat basa terhadap kertas lakmus. Penyimpanan pada wadah
yang kedap udara, pada suhu < 50°C, dan terlindung dari sinar matahari
K. Spektrofotometri Ultraviolet
Spektrofotometri ultraviolet adalah anggota teknik analisis spektroskopik
yang memakai sumber radiasi elektromagnetik ultraviolet (190-380 nm) dengan
memakai instrumen spektrofotometer. Radiasi ultraviolet (100-190 nm) tidak
dipakai, sebab pada daerah radiasi tersebut diabsorbsi oleh udara (Mulja dan
Suharman, 1995).
Analisis dengan spektrofotometri UV selalu melibatkan pembacaan
serapan radiasi elektromagnetik oleh molekul atau radiasi elektromagnetik yang
diteruskan, yang disebut dengan serapan (A) tanpa satuan dan transmitan dengan
satuan persen (%T). Bouger, Lambert, dan Beer membuat formula secara
matematik hubungan antara transmitan atau serapan terhadap intensitas radiasi
atau konsentrasi zat yang dianalisis dan tebal larutan yang mengabsorpsi sebagai :
T = = 10-ε.c.b
A = log = ε.c.b
Keterangan :
T = persen transmitan
Io = intensitas radiasi yang datang
It = intensitas radiasi yang diteruskan
ε = serapan molar (Lt.mol-1 cm-1)
C = konsentrasi (mol. Lt-1)
b = tebal larutan (cm)
A = serapan
L. Mikromeritik
Mikromeritik adalah ilmu dan teknologi tentang partikel kecil. Dalam
bidang kefarmasian ada informasi yang perlu diperoleh dari partikel yaitu (1)
bentuk dan luas permukaan partikel serta (2) ukuran partikel dan distribusi ukuran
partikel (Martin dan Cammarata, 1993). Data tentang ukuran partikel diperoleh
dalam diameter partikel dan distribusi diameter partikel, sedangkan bentuk
partikel memberi gambaran tentang luas permukaan spesifik partikel dan
texture-nya (kasar atau halus permukaan partikel) (Martin dan Bustamante, 1993).
Ukuran partikel merupakan diameter rata-rata partikel dari suatu sampel.
Umumnya sifat sampel adalah polydisperse (heterogen) bermacam-macam
diameter dengan range atau rentang yang lebar. Sampel dengan ukuran partikel
yang sama disebut monodisperse tetapi sangat jarang ditemukan sampel yang
monodisperse. Dalam mikromeritik ada dua metode dasar untuk mengetahui
ukuran partikel yaitu metode mikroskopik dan metode pengayakan (Martin dan
Cammarata,1993).
Metode mikroskopik merupakan metode sederhana yang hanya
menggunakan satu alat yaitu mikroskop yang bukan merupakan alat yang rumit
dan memerlukan penanganan khusus (Martin dan Bustamante, 1993). Kerugian
dari metode mikroskopik adalah bahwa garis tengah yang diperoleh hanya dua
dimensi dari partikel tersebut, yaitu dimensi panjang dan lebar. Tidak ada
perkiraan yang diperoleh untuk mengetahui ketebalan partikel dengan memakai
metode ini. Selain itu jumlah partikel yang harus dihitung sekitar 300-500 partikel
membutuhkan waktu dan ketelitian. Namun pengujian mikroskopik dari suatu
sampel harus selalu dilaksanakan bahkan jika digunakan metode analisis ukuran
partikel lainnya, karena adanya gumpalan dan partikel-partkel lebih dari satu
komponen seringkali bisa dideteksi dengan menggunakan metode mikroskopik
(Martin dan Cammarata,1993).
M.Metode Simplex Lattice Design
Metode Simplex Lattice Design adalah suatau metode optimasi untuk
mengetahui sifat-sifat fisik dari dua campuran atau lebih. Dengan menggunakan
metode ini diharapkan faktor trial dan error dalam mendesain suatu formula dapat
dikurangi. Metode ini juga dapat memprediksi sifat-sifat campuran tersebut pada
semua perbandingan (Bolton, 1997).
Persamaan umum untuk Simplex Lattice Design dengan dua variabel bebas
adalah sebagai berikut :
Keterangan :
Y = B1(A) + B2(B) + B1 2(A)(B)
Y = respon atau hasil percobaan
A = konsentrasi (proporsi) komponen A
B = konsentrasi (proporsi) komponen B
B1, B2, B12 = koefisien yang dihitung dari pengamatan percobaan
Koefisien a, b, ab dapat dihitung dari asal percobaannya (Bolton, 1997).
Persamaan Simplex Lattice Design di atas untuk 2 komponen bisa
Percobaan 1 menggunakan 100% komponen A, percobaan II menggunakan 100%
komponen B, serta percobaan III menggunakan 50% komponen A dan 50%
komponen B (Bolton, 1997).
N. Keterangan Empiris
Beta karoten merupakan salah satu dari 600 karotenoid yang ada di alam.
Beta karoten yang terdapat pada wortel berpotensi sebagai antioksidan (Watson,
2001). Beta karoten bereaksi dengan Reactive Oxygen Species (ROS) untuk
menetralkan oksigen singlet dan mencegah pembentukan radikal peroksil (Paiva
dan Russel, 1999). Oleh karena itu, wortel dapat dibuat menjadi sediaan UV
Protection karena sifatnya sebagai antioksidan dan penggunaan bahan aktif
berupa bahan alam lebih disukai dibandingkan senyawa sintetik karena
produk-produk dari bahan alam lebih aman dan memiliki toleransi yang baik terhadap
kulit (Fridd, 1996).
Bentuk sediaan yang akan diteliti adalah hidrogel. Hal itu dikarenakan
konsistensinya yang lembut dan memberikan rasa dingin pada pemakaiannya
karena efek evaporasi dari air. Selain itu, hidrogel juga mudah diaplikasikan dan
memberi kelembaban secara instan tetapi pada penggunaan jangka panjang akan
membuat kulit kering sehingga membutuhkan humektan seperti gliserol dan
propilen glikol. Humektan dapat memberikan proteksi terhadap hilangnya air dan
mempertahankan kelembaban kulit (Johnson, 1992). Humektan membantu
menjaga kelembaban kulit dengan cara menjaga kandungan air pada lapisan
Watkinson, Chandar, dan Scott, 2002). Penggunaan gliserol dan proplenglikol
secara bersamaan akan meningkatkan sifat fisik dari sediaan. Gliserol akan
meningkatkan kelarutan solut lipofilik (Buchmann, 2001) sedangkan propilen
glikol bersifat higroskopik (Anonim, 1979) sehingga dapat menjaga konsistensi
sediaan.
Dalam penelitian ini dilakukan optimasi formula gel UV Protection
tinjauan terhadap humektan gliserol dan propilen glikol menggunakan metode
Simplex Lattice Design. Metode ini dapat digunakan untuk mengetahui sifat-sifat
fisik dari dua campuran dan memprediksi sifat-sifat campuran tersebut pada
semua perbandingan (Bolton, 1997). Sifat fisik dari formula dilihat dari formula
yang memiliki daya sebar dan viskositas yang baik sehingga dalam aplikasinya
pada kulit konsistensinya tidak terlalu encer dan tidak terlalu kental. Stabilitas
formula dilihat dari formula yang memiliki kestabilan selama penyimpanan.
Dengan metode ini diharapkan dapat ditemukan range komposisi optimum
humektan gliserol dan propilen glikol dalam formula gel UV Protection yang
BAB III
METODOLOGI PENELITIAN
A. Jenis Rancangan Penelitian
Penelitian ini merupakan rancangan eksperimental bersifat eksploratif
dengan menggunakan desain penelitian secara Simplex Lattice Design.
B. Variabel dalam Penelitian
1. Variabel bebas
Variabel bebas dalam penelitian ini adalah komposisi humektan gliserol dan
propilen glikol dalam formula gel UV Protection.
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah sifat fisik (viskositas dan daya
sebar) serta stabilitas (pergeseran viskositas).
43. Variabel pengacau terkendali
Variabel pengacau terkendali dalam penelitian ini adalah kecepatan dan lama
pengadukan serta metode kerja pembuatan gel UV Protection.
44. Variabel pengacau tak terkendali
Variabel pengacau tak terkendali dalam penelitian ini adalah suhu dan
C. Definisi Operasional
1. Gel UV Protection endapan perasan wortel adalah sediaan semisolid yang
berfungsi sebagai antioksidan yang dibuat dari endapan perasan wortel sesuai
formula yang telah ditentukan sesuai prosedur pembuatan gel pada penelitian
ini.
2. Endapan perasan wortel adalah endapan yang diperoleh dengan cara
mengambil perasan wortel dengan juicer lalu menyaring, mensentrifuge
dengan kecepatan 4000 rpm selama 15 menit, dan ditambahkan 0,2 % metil
paraben.
3. Daya sebar optimum adalah diameter penyebaran gel sebesar 3-5 cm pada
pengukuran massa gel 0,5 gram yang diberi beban 125 gram selama 1 menit.
4. Viskositas optimum adalah viskositas gel sebesar 310-315 d.Pa.s.
5. Stabilitas gel ditentukan dari besarnya nilai pergeseran viskositas antara
sebelum dan sesudah penyimpanan selama 1 bulan. Rumus yang digunakan
untuk pergeseran viskositas adalah :
awal as viskosit rata
-rata
bulan 1 viskositas awal
s viskosita rata
-rata −
x 100%
Pergeseran viskositas optimum dalam penelitian ini adalah ≤ 15%.
6. Respon adalah besaran yang diamati perubahan efek dan besarnya dapat
dikuantitatifkan, dalam penelitian ini adalah hasil penelitian sifat fisik gel
7. Contour plot adalah grafik yang merupakan hasil dari respon sifat fisik dan
stabilitas gel.
8. Contour plot super imposed adalah grafik pertemuan yang memuat semua
range komposisi humektan dalam contour plot respon sifat fisik dan stabilitas
gel yang dapat digunakan untuk melihat ada tidaknya prediksi range
komposisi optimum humektan dalam formula gel.
D. Alat dan Bahan
Alat-alat yang digunakan adalah Glasswares (Pyrex-Germany), Juicer
(Miyako), neraca analitik (Mettler Toledo GB 3002), magnetic stirrer, Mixer
(Cucina Phillips dan Power Supply IC Regulated model ad 01), alat uji daya
sebar, Viscotester seri VT 04 (Rion-Japan), Perkin-Elmer Spektrofotometer
UV-Vis Lambda 20, Spektrofotometer UV (Genesis 10), Hot Plate (Ikamag-Ret),
mikroskop (Olympus CH2-Japan), sentrifuge, alat pHmeter elektrik seri VT 03
(Rion-Japan), dan stopwatch.
Bahan-bahan yang digunakan adalah endapan perasan wortel, baku beta-
karoten (E. Merck), heksan (kualitas p.a.), aseton (kualitas p.a.), gliserol (kualitas
farmasetis), propilen glikol (kualitas farmasetis), Carbopol 940® (kualitas
E. Tata Cara Penelitian
1. Ekstraksi beta karoten dalam endapan perasan wortel (Daucus carota,
Linn.)
Menimbang kurang lebih 1 kg wortel segar yang telah dibersihkan dan
dipotong-potong kemudian diambil perasannya dengan menggunakan juicer
dan disaring. Hasilnya disentrifugasi dengan kecepatan 4000 rpm selama 15
menit, kemudian diambil endapannya.
Menimbang seksama 0,5 gram endapan perasan wortel lalu distrirrer
menggunakan 2x25 ml aseton dengan kecepatan 700 rpm selama 2,5 menit,
lalu disaring dengan kertas saring. Selanjutnya residu distrirrer menggunakan
25 ml heksan dengan kecepatan 700 rpm selama 1 menit, lalu disaring dengan
kertas saring.
Untuk menghilangkan aseton dari ekstrak, digunakan 5x100 ml
aquadest. Lapisan teratas (fraksi heksan) diambil lalu dimasukkan ke dalam
labu ukur 25 ml dan diencerkan dengan pelarut aseton : heksan (1:9) hingga
tanda (modifikasi Anonim, 1995).
2. Penetapan kadar beta karoten dalam endapan perasan wortel (Daucus
carota, Linn.)
a. Pembuatan larutan induk beta karoten
Menimbang seksama 10,0 mg baku beta karoten lalu dimasukkan
diaduk hingga larut sempurna. Kemudian dimasukkan ke dalam labu ukur
25 ml dan diencerkan dengan pelarut aseton : heksan (1:9) hingga tanda.
b. Pembuatan larutan intermediet beta karoten
Memipet 2,5 ml larutan induk beta karoten lalu dimasukkan ke
dalam labu ukur 25 ml dan diencerkan dengan pelarut aseton : heksan
(1:9) hingga tanda.
c. Pembuatan seri larutan baku beta karoten 2, 4, 6, 8, dan 10 ppm
Memipet 1,25 : 2,50 ; 3,75; 5,00; dan 6,25 ml larutan intermediet
beta karoten, masing-masing dimasukkan ke dalam labu ukur 10 ml dan
diencerkan dengan pelarut aseton : heksan (1:9) hingga tanda.
d. Penentuan panjang gelombang serapan maksimum beta karoten
Scanning serapan larutan baku beta karoten 2, 6, dan 10 ppm pada
panjang gelombang 390-500 nm. Bandingkan kurva hubungan panjang
gelombang lawan serapan dari ketiga seri larutan baku beta karoten.
Tentukan panjang gelombang saat serapan maksimum beta karoten dari
spektogram yang diperoleh. Panjang gelombang pada saat serapan
maksimum ditandai dengan nilai serapan yang paling besar.
e. Pembuatan kurva baku beta karoten
Seri larutan baku beta karoten 2, 4, 6, 8, dan 10 ppm diukur pada
panjang gelombang saat serapan maksimum dimulai dari kadar terkecil.
Kemudian menghitung persamaan regresi linier yang merupakan
f. Penetapan kadar beta karoten dalam endapan perasan wortel
Mengukur serapan endapan perasan wortel yang telah diekstraksi
beta karotennya pada panjang gelombang saat serapan maksimum. Kadar
beta karoten dalam endapan perasan wortel dapat dihitung berdasarkan
perhitungan persamaan regresi linier yang diperoleh.
3. Uji SPF (Sun Protection Factor)
Scanning serapan 0,04 gram endapan perasan wortel yang dilarutkan
dengan 25 ml kloroform pada panjang gelombang 365 nm dengan menggunakan
spektrofotometer UV. Serapan yang didapat dihitung sebagai nilai SPF
menggunakan rumus : = ⎢⎣⎡ ⎥⎦⎤
SPF 1 log
-A 10 =log10SPF
(Walters, 1997)
4. Optimasi pembuatan gel UV Protection
a. Formula gel UV Protection
Formula clear aqueous gel with dimethicone menurut Allen, Jr., Loyd.,
Popovich, N.G., dan Ansel, H.C. (2005) sebagai berikut:
Water 59,8 %
Carbomer 934 0,5 %
Triethanolamine 1,2
Glyceryn 34,2
Propylene glycol 2,0
Dalam optimasi formula ini dilakukan modifikasi formula dengan
variasi komposisi humektan menggunakan metode Simplex Lattice Design.
Formula yang diperoleh untuk 100 gram gel sebagai berikut.
Tabel I. Formula Simplex Lattice Design
Formula I II III IV V
Gliserol 0 g 12 g 24 g 36 g 48 g
Propilen
glikol 48 g 36 g 24 g 12 g 0 g
Carbopol 1 g 1 g 1 g 1 g 1 g
Trietanolamin 0,5 g 0,5 g 0,5 g 0,5 g 0,5 g
Aquadest 50,34 g 50,34 g 50,34 g 50,34 g 50,34 g
Endapan perasan
wortel
0,16 g 0,16 g 0,16 g 0,16 g 0,16 g
b. Pembuatan gel UV Protection
Carbopol dimasukkan ke dalam aquadest dan diaduk dengan
kecepatan 400 rpm selama 10 menit (campuran 1). Di tempat yang
berbeda campur humektan gliserol dan propilen glikol menggunakan
mixer dengan kecepatan 200 rpm selama 5 menit (campuran 2). Masukkan
campuran 2 ke dalam campuran 1 sambil terus diaduk sampai homogen
dengan kecepatan 400 rpm selama 5 menit. Tambahkan pula endapan
perasan wortel yang digunakan. Terakhir tambahkan trietanolamin sedikit
5. Uji sifat fisik dan stabilitas gel UV Protection
a. Uji daya sebar
Uji daya sebar sediaan gel UV Protection endapan perasan wortel
dilakukan segera setelah gel selesai dibuat dengan cara sebagai berikut :
gel ditimbang seberat 0,5 gram, diletakkan di tengah kaca bulat berskala.
Di atas gel diletakkan kaca bulat lain dan pemberat sehingga berat kaca
bulat dan pemberat 125 gram, didiamkan selama 1 menit, kemudian
dicatat diameter penyebarannya (modifikasi Garg et al., 2002).
b. Uji viskositas
Pengukuran viskositas menggunakan alat Viscotester Rion seri VT
04 dengan cara sebagai berikut : gel dimasukkan ke dalam wadah dan
dipasang pada portable viscotester. Viskositas gel diketahui dengan
mengamati gerakan jarum penunjuk viskositas. Uji ini dilakukan dua kali,
yaitu (1) segera setelah gel selesai dibuat dan (2) setelah disimpan selama
1 bulan (Instrustion Manual Viscotester VT-03E/VT-04E).
6. Uji mikromeritik
Penentuan ukuran partikel dengan metode mikroskopi. Alat yang
digunakan adalah mikroskop. Sebelum dilakukan pengukuran, terlebih dahulu
mengkalibrasi lensa mikroskop. Pengamatan ukuran partikel sebanyak 500 buah
F.Analisis Data dan Optimasi
Data uji daya sebar, viskositas, pergeseran viskositas yang terkumpul
dianalisis dengan menggunakan metode Simplex Lattice Design. Masing-masing
uji sifat fisik dan stabilitas gel dapat dibuat persamaan Simplex Lattice Design.
Selanjutnya dari respon yang diperoleh, dibuat contour plot masing-masing uji
sifat fisik dan stabilitas gel untuk menggambarkan garis respon yang diinginkan.
Dari masing-masing respon dihitung validitas persamaan Simplex Lattice Design.
dengan menganalisis secara statistik menggunakan uji F dengan taraf kepercayaan
95% untuk mengetahui validitas persamaan Simplex Lattice Design. Apabila
persamaan tersebut valid, maka persamaan tersebut dapat digunakan untuk
memprediksi respon tertentu dari campuran kedua humektan dalam berbagai
komposisi.
Masing-masing contour plot respon digabungkan menjadi satu contour
plot super imposed yang telah dipilih berdasar parameter kualitas yang ditentukan.
Range komposisi yang diperoleh selanjutnya diprediksi sebagai range komposisi
optimum humektan gliserol dan propilen glikol dalam formula gel UV Protection
BAB IV
HASIL DAN PEMBAHASAN
A. Ekstraksi Beta Karoten dalam Endapan Perasan Wortel
(Daucus carota, Linn.)
Sebelum mengekstraksi beta karoten, wortel diperas dengan
menggunakan juicer untuk memisahkan ampas dan perasan wortel. Dalam
penelitian ini ampas wortel tidak digunakan. Perasan wortel disaring untuk
menghilangkan serat-serat wortel yang masih terdapat di dalam perasan wortel.
Dalam penelitian ini hanya digunakan endapan perasan wortel sehingga perlu
dilakukan sentrifuge dengan kecepatan 4000 rpm selama 15 menit untuk
memisahkan filtrat dan endapan dari perasan wortel. Dengan kecepatan dan waktu
sentrifuge tersebut diharapkan sudah dapat memisahkan endapan dari filtrat
perasan wortel.
Endapan perasan wortel yang telah diperoleh diekstraksi dengan
menggunakan aseton dan heksan. Aseton digunakan untuk menyari senyawa polar
yang terdapat di dalam endapan perasan wortel. Heksan digunakan untuk menyari
senyawa non polar yang terdapat di dalam endapan perasan wortel. Beta karoten
merupakan senyawa non polar sehingga beta karoten tertarik ke dalam fraksi
heksan. Untuk menghilangkan aseton dari fraksi heksan, digunakan aquadest.
Lapisan teratas merupakan fraksi heksan yang akan ditetapkan kadar beta
B. Penetapan Kadar Beta Karoten dalam Endapan Perasan Wortel
(Daucus carota, Linn.)
Wortel mengandung senyawa beta karoten yang berwarna karena dalam
struktur molekulnya mempunyai sistem kromofor yang panjang sehingga dapat
ditetapkan kadarnya menggunakan spektrofotometri visibel.
Gambar 6. Struktur beta karoten dengan sistem kromofor
Keterangan
sistem kromofor
Pembuatan kurva baku bertujuan untuk memperoleh persamaan regresi
yang selanjutnya digunakan untuk menghitung kadar beta karoten dalam endapan
perasan wortel. Kurva baku dibuat dengan mengukur serapan dari 5 seri kadar
larutan beta karoten baku pada panjang gelombang serapan maksimum.
Panjang gelombang serapan maksimum adalah panjang gelombang di
mana senyawa memberikan serapan paling besar. Scanning panjang gelombang
dilakukan dengan menggunakan 3 seri kadar larutan baku beta karoten yaitu 2
ppm, 6 ppm, dan 10 ppm. Hal ini bertujuan untuk memastikan panjang gelombang
serapan maksimum beta karoten. Dari ketiga hasil scanning dengan
Spektrofotometer Genesis 10 tersebut, diperoleh panjang gelombang serapan
beta karoten dalam aseton : heksan (1:9) menurut Anonim (1995) adalah 436 nm.
Perbedaan panjang gelombang yang diperoleh ini dikarenakan adanya perbedaan
kondisi percobaan yang digunakan.
Kurva baku yang diperoleh dari tiap replikasi sebagai berikut.
Tabel II. Kurva baku beta karoten dengan Spektrofotometer Genesis 10
KURVA BAKU I KURVA BAKU II KURVA BAKU III
Kadar
(ppm) Serapan
Kadar
(ppm) Serapan
Kadar
(ppm) Serapan
2,174 0,262 2,160 0,243 2,056 0,336 4,348 0,541 4,320 0,626 4,112 0,570 6,522 0,930 6,480 0,986 6,168 0,980 8,696 1,200 8,640 1,291 8,224 1,320 10,870 1,509 10,800 1,629 10,280 1,622
Y = 0,14503 X + 0,0575 Y = 0,15912 X –0,0761 Y = 0,16158 X - 0,031
r = 0,99855 r = 0,99915 r = 0,99729
Dari 3 kurva baku tersebut dipilih salah satu kurva baku yang
mempunyai harga koefisien korelasi (r) yang paling mendekati ± 1. Persamaan
regresi linier dari ketiga kurva baku yang memiliki harga r yang paling besar akan
digunakan untuk menetapkan kadar beta karoten dalam endapan perasan wortel.
Kurva baku replikasi II mempunyai harga r paling besar bila dibandingkan dengan
kedua kurva baku lainnya sehingga korelasi antara peningkatan kadar dengan
peningkatan serapan adalah paling baik. Oleh karena itu dipilih persamaan regresi
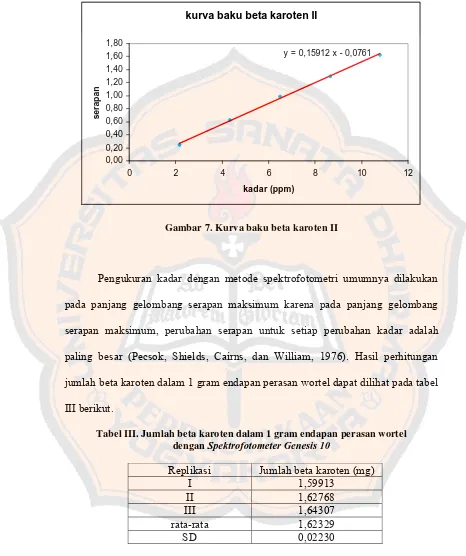
dari kurva baku II, yaitu Y = 0,15912 X –0,0761 untuk penetapan kadar beta
kurva baku beta karoten II
y = 0,15912 x - 0,0761
0,00 0,20 0,40 0,60 0,80 1,00 1,20 1,40 1,60 1,80
0 2 4 6 8 10 12
kadar (ppm)
ser
ap
an
Gambar 7. Kurva baku beta karoten II
Pengukuran kadar dengan metode spektrofotometri umumnya dilakukan
pada panjang gelombang serapan maksimum karena pada panjang gelombang
serapan maksimum, perubahan serapan untuk setiap perubahan kadar adalah
paling besar (Pecsok, Shields, Cairns, dan William, 1976). Hasil perhitungan
jumlah beta karoten dalam 1 gram endapan perasan wortel dapat dilihat pada tabel
III berikut.
Tabel III. Jumlah beta karoten dalam 1 gram endapan perasan wortel dengan Spektrofotometer Genesis 10
Replikasi Jumlah beta karoten (mg)
I 1,59913 II 1,62768 III 1,64307 rata-rata 1,62329
Berdasarkan hasil pengukuran dan perhitungan yang terdapat pada halaman 69,
didapatkan jumlah rata-rata beta karoten dalam 1 gram endapan perasan wortel
sebesar 1,62329 ± 0,02230 mg.
C. Uji Sun Protection Factor (SPF)
Uji SPF dilakukan untuk mengetahui tingkat perlindungan terhadap sinar
matahari yang dapat menyebabkan sunburn (eritema) (Stanfield, 2003). Penetapan
nilai SPF menurut Walters (1997) dilakukan dengan mengukur serapan endapan
perasan wortel yang dilarutkan dalam kloroform pada panjang gelombang 365
nm. Pemilihan panjang gelombang 365 nm ini dikarenakan untuk menyesuaikan
dengan lampu UV yang dimiliki untuk uji efikasi gel UV Protection endapan
perasan wortel (Daucus carota, Linn.) mempunyai panjang gelombang 365 nm.
Beta karoten sangat larut dalam kloroform (Anonim, 1989). UV cut off kloroform
di bawah 250 nm (Day and Underwood, 1996). Oleh karena itu, dalam penelitian
ini serapan endapan perasan wortel dapat diukur pada panjang gelombang 365
nm.
Dalam formulasi ini dibuat sediaan dengan nilai SPF antara 10 sampai
15 sehingga diharapkan dapat memberikan proteksi terhadap sunburning dan
suntanning. Pengukuran nilai SPF dengan kadar beta karoten 64,93160 ppm
Tabel IV. Hasil pengukuran SPF
Serapan (A) SPF
Replikasi Replikasi Kadar beta
karoten
(ppm) 1 2 3 1 2 3
SPF
rata-rata
51,94528 0,919 0,985 0,904 8,299 9,661 8,017 8,659
64,93160 1,152 1,038 1,028 14,191 10,914 10,666 11,924
Untuk mendapatkan gel UV Protection dengan nilai SPF 11,924, maka
jumlah beta karoten yang dibutuhkan dalam gel harus disesuaikan supaya kadar
beta karoten di dalam gel setara dengan 64,93160 ppm. Berdasarkan perhitungan,
jumlah beta karoten yang diperlukan untuk 100 gram gel supaya mempunyai nilai
SPF 11,924 adalah 6,49316 mg yang setara dengan 4 gram endapan perasan
wortel.
D. Optimasi Pembuatan Gel UV Protection
Pada pembuatan gel UV Protection dengan nilai SPF 11,924 dibutuhkan
4 gram endapan perasan wortel untuk 100 gram gel yang mengandung 6,49316
mg beta karoten. Secara teknologi hal tersebut masih dapat dilakukan, akan tetapi
hasil yang diperoleh tidak dapat diterima secara estetika karena warna gel UV
Protection yang dihasilkan terlalu mencolok.
Faktor penting yang perlu diperhatikan dalam formulasi gel UV
Protection adalah nilai estetika sediaan karena mempengaruhi tingkat penerimaan
konsumen. Oleh karena itu, dilakukan modifikasi terhadap jumlah endapan
perasan wortel yang dimasukkan dalam sediaan gel. Tujuan modifikasi ini untuk
penggunaannya oleh konsumen. Untuk alasan estetika tersebut, maka digunakan
0,28600 mg beta karoten di dalam 100 gram gel sehingga endapan perasan wortel
yang dimasukkan ke dalam sediaan gel menjadi 0,16 gram.
Endapan perasan wortel yang dimasukkan ke dalam sediaan gel berbeda
dengan sebelumnya sehingga diperlukan penetapan kadar beta karoten dalam
endapan perasan wortel. Scanning panjang gelombang dilakukan dengan
menggunakan 3 seri kadar larutan baku beta karoten yaitu 2 ppm, 6 ppm, dan 10
ppm. Hasil yang diperoleh dari scanning menggunakan Perkin-Elmer
Spektrofotometer UV-Vis Lambda 20 dapat dilihat pada spektogram berikut.
Gambar 8. Hasil scanning panjang gelombang serapan maksimum larutan baku beta karoten 2 ppm, 6 ppm, dan 10 ppm
Dari ketiga gambar spektogram tersebut, didapat panjang