i Teknologi Bioproses
Semester IV 2017/2018
Pembuatan Bioetanol Sebagai Bahan Bakar Rumah Tangga
Disusun oleh:
A. Nurul Rahmayani 33116012
Sutri Yulianti 33116033
Insan Kamil H. 33116052
Alfiani Wildasari 33116059
PROGRAM STUDI D3 TEKNIK KIMIA
JURUSAN TEKNIK KIMIA
POLITEKNIK NEGERI UJUNG PANDANG
ii
HALAMAN PENGESAHAN
Makalah yang berjudul “Pembuatan Bioetanol Sebagai Bahan Bakar Rumah Tangga” ini dibuat sebagai salah satu pemenuhan tugas mata kuliah Teknologi Bioproses.
Disusun Oleh:
A. Nurul Rahmayani/33116012
Sutri Yulianti/33116033
Insan Kamil H./33116052
Alfiani Wildasari/33116059
iii
KATA PENGANTAR
Syukur kami panjatkan atas semua limpahan rahmat Allah SWT karena-Nyalah sehingga kita masih diberi kesempatan dan kekuatan untuk menyelesaikan makalah yang
berjudul “Pembuatan Bioetanol Sebagai Bahan Bakar Rumah Tangga”. Makalah ini
disusun sebagai salah satu kelengkapan tugas mata kuliah Teknologi Bioproses.
Makalah ilmiah ini telah kami susun dengan maksimal dan mendapatkan bantuan dari berbagai pihak sehingga dapat memperlancar pembuatan makalah ini. Untuk itu kami menyampaikan banyak terima kasih kepada semua pihak yang telah berkontribusi dalam pembuatan makalah ini.
Terlepas dari semua itu, Kami menyadari sepenuhnya bahwa masih ada kekurangan baik dari segi susunan kalimat maupun tata bahasanya. Oleh karena itu dengan tangan terbuka kami menerima segala saran dan kritik dari pembaca agar kami dapat memperbaiki makalah ilmiah ini.
iv
3.3 Pengaplikasian Bioetanol Kepada Masyarakat... 7
VI PENUTUP ... 9
0 BAB I
PENDAHULUAN
1.1 Latar Belakang
Saat ini sumber energi yang paling banyak digunakan adalah energi fosil yang berupa bahan bakar minyak. Energi fosil tersebut terdiri atas adalah minyak bumi dan sisanya adalah gas dan batubara. Hampir semua kebutuhan masih sangat tergantung pada energi fosil. Berbagai kegiatan yang membutuhkan bahan bakar minyak seperti industri, rumah tangga, bahan bakar kendaraan, dan lain-lain.
Cadangan energi fosil (minyak bumi) yang tidak terbarukan sudah sangat menipis dan tidak akan bertahan selamanya. Maka dari itu diperlukan untuk melestarikan bahan bakar fosil tersebut. Dalam menghemat bahan bakar fosil diperlukan untuk melakukan hal-hal yang efektif yaitu dengan mengurangi atau menghemat jumlah pemakaian gas yang digunakan. Adapun energi alternatif telah dikembangkan dalam menghemat pemakaian energi fosil yaitu bioethanol.
Bioetanol adalah salah satu bahan bakar alternatif yang dibuat dari tumbuhan yang mengandung pati, gula dan serat selulosa. Bioetanol adalah cairan dari fermentasi gula yang bersumber dari karbohidrat dengan bantuan mikroorganisme. Bioetanol merupakan bahan bakar dari minyak nabati yang memiliki sifat menyerupai minyak premium.
Salah satu bahan yang dapat digunakan untuk membuat bioetanol ialah limbah tongkol jagung karena didalamnya terdapat kandungan gula. Limbah tongkol jagung biasanya hanya dianggap sebagai salah satu limbah industri rumah tangga yang belum termanfaatkan dengan baik, sehingga masyarakat membuangnya dan hal itu menjadi permasalahan yang akan menyebabkan pencemaran lingkungan.
1 1.2 Tujuan
1. Mencari bahan bakar alternatif (bioethanol) sebagai pengganti bahan bakar minyak untuk kebutuhan rumah tangga.
2. Cara pemanfaatan limbah organik sebagai bahan utama pembuatan bioetanol.
1.3 Rumusan Masalah
1. Bagaimana memanfaatkan limbah sebagai bahan pembuatan bioethanol?
2
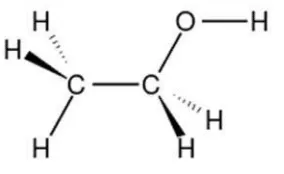
namun salah satu hidrogennya digantikan oleh gugus alkil. Gugus fungsional alkohol adalah gugus hidroksil (OH). Pemberian nama alkohol biasanya dengan menyebut nama alkil yang terikat pada gugus OH, kemudian menambahkan nama alkohol.
Karakteristik etanol meliputi: berupa zat cair, tidak berwarna, berbau spesifik, mudah terbakar dan menguap, dapat bercampur dengan air dalam segala perbandingan. Secara garis besar penggunaan etanol adalah sebagai pelarut untuk zat organik maupun anorganik, bahan dasar industri asam cuka, ester, spiritus, dan asetaldehid. Selain itu etanol juga digunakan untuk campuran minuman serta digunakan sebagai bahan bakar yang terbarukan.
Pembuatan etanol dalam industri dapat dibagi ke dalam 2 macam yaitu: 1) cara non fermentasi (sintetik), proses pembuatan alkohol yang tidak menggunakan enzim ataupun jasad renik, 2) cara fermenasi, merupakan proses metabolisme dimana terjadi perubahan kimia dalam substrat karena aktivitas enzim yang dihasilkan oleh mikroba.
Bioetanol adalah etanol yang diproduksi dengan cara fermentasi gula menggunakan ragi Saccharomyces cerevisiae. Bioetanol dapat dibuat dari pati tongkol jagung yang telah diproses menjadi glukosa. Secara teoritis, hidrolisis glukosa akan menghasilkan etanol dan karbondioksida.
Bioetanol bisa digunakan dalam bentuk murni atau sebagai campuran bahan bakar gasolin (bensin). Bioetanol memiliki sifat fisika tidak berwarna, cairan yang larut dalam air, kadang-kadang disebut alkohol padi-padian (grain) karena dapat diperoleh dengan cara fermentasi dari padi-padian. Fermentasi dari semua bahan yang mengandung karbohidrat seperti jagung, kentang, padi dan tanaman yang banyak mengandung karbohidrat lainnya akan menghasilkan etanol.
3 2.2.1 Tongkol Jagung
Jagung merupakan tanaman semusim (annual). Jagung memiliki bunga jantan dan bunga betina yang terpisah dalam satu tanaman. Tongkol terbungkus oleh kulit buah jagung. Secara morfologi, tongkol jagung adalah tangkai utama malai yang termodifikasi. Tongkol jagung muda, disebut juga babycorn, dapat dimakan dan dijadikan sayuran. Tongkol yang tua ringan namun kuat, dan menjadi sumber furfural, sejenis monosakarida. Tongkol jagung tersusun atas senyawa kompleks lignin, hemiselulose dan selulose. Masing-masing merupakan senyawa-senyawa yang potensial dapat dikonversi menjadi senyawa-senyawa lain secara biologi. Selulose merupakan sumber karbon yang dapat digunakan mikroorganisme sebagai substrat dalam proses fermentasi untuk mengahsilkan produk yang mempunyai nilai ekonomi tinggi.
2.2.2 Kulit Pisang
Kulit pisang kepok merupakan salah satu limbah industri rumah tangga yang belum termanfaatkan dengan baik. Kadar karbohidrat yang terkandung dalam kulit pisang yakni sebesar 18,50%.
2.2.3 Batang Padi
Jerami padi mengandung kurang lebih 39% selulosa dan 27,5% hemiselulosa (dasar berat kering). Kedua bahan polisakarida ini, dapat dihidrolisis menjadi gula sederhana yang selanjutnya dapat difermentasi menjadi bioethanol. Potensi produksi jerami padi per ha kurang lebih 10-15 ton, keadaan basah dengan kadar air kurang lebih 60%. Jika seluruh jerami per ha ini diolah menjadi ethanol fuel grade ethanol (FGE), maka potensi produksinya kurang lebih 766-1.148 liter/ha FGE (perhitungan ada di lampiran).
2.2.4 Nasi Aking
Nasi aking adalah istilah yang umum digunakan untuk menyebut makanan yang berasal dari nasi sisa yang tidak termakan. Umumnya nasi aking memiliki tampilan fisik berwarna agak kecoklatan, struktur kering, ditumbuhi jamur serta memiliki bau yang kurang sedap. Bau kurang sedap pada nasi aking akibat perkembangan jamur. Komposisi kimia yang terdapat dalam tepung nasi aking adalah karbohidrat 83,19% (b/b), amilose 29,70% (b/b), lemak 0,40% (b/b), protein 3,36% (b/b) serat 0,11% (b/b) dan air 12,37% (b/b). Kandungan karbohidrat yang cukup besar dalam nasi aking ini dapat dimanfaatkan sebagai bahan baku dalam pembuatan bioetanol dengan cara mengkonversi karbohidrat pada nasi aking menjadi alkohol melalui proses fermentasi.
2.2.5 Alga Laut
4
pengolahan limbah, serta sebagai sumber energi terbarukan [2]. Pada penelitian ini digunakan jenis Codium geppiorum yang tersebar di kawasan Nusa Lembongan dengan kandungan karbohidrat 69,10%.
2.2.6 Tetes Tebu (Molase)
5 BAB III
PEMBUATAN BIOETANOL
3.1 Prosedur Pengerjaan
3.1.1 Persiapan bahan baku
Tongkol jagung dicuci bersih terlebih dahulu. Kemudian dihancurkan dengan mesin penghancur. Lalu diayak dengan ayakan tepung dan diambil bagian terhalus (tepung tongkol jagung). Menimbang tepung tongkol jagung sebanyak 1 ton. Kemudian dimasukan kedalam wadah (drum besar).
3.1.2 Tahap Hidrolisis
Larutan tongkol jagung kemudian ditambahkan 1.000 L larutan HCl 0,1 N. Setelah itu dihidrolisis pada suhu 100°C selama 2 jam. Kemudian disaring dengan saringan manual untuk memisahkan filtrat dan residu.
3.1.3 Tahap Pembuatan Starter
Pada tahap ini, langkah-langkah yang dilakukan yaitu menambahkan 0,9 kg Ammonium sulfat dan 0,48 kg Urea sebagai nutrisi pada filtrat hasil hidrolisis yang memiliki kadar glukosa terbanyak lalu mengatur pH sekitar 4-4,5.
3.1.4 Tahap Fermentasi
Kemudian menyiapkan wadah lainnya dan pada wadah tersebut dimasukkan sampel (larutan campuran tepung tongkol jagung dan air). Setelah itu disterilisasi hingga suhu mencapai ±121°C. Kemudian didinginkan sampai suhunya turun hingga 30-40 (suhu kamar) selama ±24 jam. Kemudian ditambahkan mikroba Saccharomyces cerevisiae pada masing-masing wadah.
3.1.5 Tahap Destilasi
6
cukup tinggi, sekitar 74%. Jadi diperkirakan jika menggunakan tepung tongkol jagung tersebut dari 1000 kg tepung akan dihasilkan 44 liter bioethanol.
7 3.3 Pengaplikasian Bioetanol Kepada Masyarakat
Meskipun sudah ada energi alternatif untuk menggantikan minyak tanah yaitu LPG, tetapi produksi untuk LPG ternyata masih dibawah kebutuhan konsumsi LPG sehingga perlunya dikembangkan alternative bahan bakar lainnya salah satunya seperti kompor bioethanol. Kompor bioetanol merupakan kompor yang berbahan bakar bioethanol yang diolah dari tumbuhan (bahan organik) yang juga dapat berfungsi untuk mereduksi sampah sisa bahan organik dan juga kompor jenis ini ramah lingkungan.
8 BAB IV
PENUTUP
4.1 Kesimpulan
Berdasarkan hasil penelitian dan uraian pembahasan di atas maka dapat disimpulkan bahwa:
1. Kadar glukosa terbanyak terdapat pada sampel yang dihidrolisis menggunakan HCl 0,3 M yaitu 0,161%.
2. Kadar bioetanol terbanyak dihasilkan pada fermentasi hari ke 5 dan fermentasi hari ke 7.
3. Kadar bioetanol yang hasilkan pada hasil akhir fermentasi hari ke 3 (12,48%), fermentasi hari ke 5 (31,26%), fermentasi hari ke 7 (31,26%), dan fermentasi hari ke 9 (18,78%).
4.2 Daftar Pustaka
Wusnah, dkk.2016.”Proses Pembuatan Bioetanol Dari Kulit Pisang Kepok (Musa acuminata B.C) Secara Fermentasi”: Jurnal Teknologi Kimia Unimal 5:1 (2016) 57-65.Jurusan Teknik Kimia, Fakultas Teknik, Universitas Malikussaleh Lhokseumawe
Edward J. Dompeipen dan Riardi P. Dewa.2015.” Pengaruh Waktu Dan pH Fermentasi Dalam Produksi Bioetanol Dari Rumput Laut Eucheuma cotTonii Menggunakan Asosiasi Mikroba (Sacchromyces cerevisiae, Aspergilus niger dan Zymomonas mobilis)”: Majalah Biam Vol.11 No.2, Desember 2015, Hal 63-75.Balai Riset dan Standardisasi Industri Ambon, Jl. Kebun Cengkeh, Ambon.
Wayan Karta, Ni Made Puspawati, Yenni Ciawi.2015.” Pembuatan Bioetanol Dari Alga Codium geppiorum Dan Pemanfaatan Batu Kapur Nusa Penida Teraktivasi Untuk Meningkatkan Kualitas Bioetanol”: Cakra Kimia (Indonesian E-Journal of Applied Chemistry) Volume 3, Nomor 12, Mei 2015.Magister Kimia Terapan, Program Pascasarja Universitas Udayana, Jurusan Kimia Universitas Udayana,Jurusan Teknik Sipil Universitas Udayana.
9
10
Jurnal Teknologi Kimia Unimal 5:1 (2016) 57-65
Jurnal Teknologi Kimia Unimal
Jurnal
Teknologi
homepage jurnal: [email protected] Kimia
Unimal
PROSES PEMBUATAN BIOETANOL DARI KULIT PISANG
KEPOK (Musa acuminata B.C) SECARA FERMENTASI
Wusnah, Samsul Bahri, Dwi Hartono
Jurusan Teknik Kimia, Fakultas Teknik, Universitas Malikussaleh Lhokseumawe
Email: [email protected]
Abstrak
Kulit pisang kepok selama ini hanya dianggap sebagai salah satu limbah industri rumah tangga yang belum termanfaatkan dengan baik. Komposisi terbanyak kedua kulit pisang kepok adalah karbohidrat 18,50% dimana karbohidrat dapat dikonversi menjadi glukosa yang selanjutnya dapat digunakan sebagai bahan baku pembuatan bioetanol.Penelitian ini bertujuan membuat bioethanol dari kulit pisang kepok dengan variasi waktu fermentasi dan penambahan starter. Pada penelitian ini kulit pisang kepok dihidrolisis dengan mengunakan HCl 5% pada suhu 100oC selama 60 menit. Hasil penelitian menunjukkan bahwa semakin lama waktu fermentasi maka semakin banyak etanol yang dihasilkan.Pada variasi waktu fermentasi diperoleh waktu terbaik fermentasi pada waktu 7 hari dengan kadar etanol 40 % sebanyak 34ml.
11
1. Pendahuluan
Sumber daya energi konvensional bahan bakar fosil (minyak/gas bumi dan
batu bara) sebagai sumber energi yang tidak terbarukan dengan segala
permasalahannya, terutama kenaikan harga (price escalation) secara global setiap
terjadinya krisis energi akibat dari faktor-faktor seperti cadangan yang berkurang
sesuai dengan umur eksploitasinya, permintaan yang meningkat, jaminan pasokan
(supply security) yang terbatas dan pembatasan produksi serta penilaian dampak
lingkungan yang ketat terhadap pemanasan global (global warming), harus
dikurangi ketergantungannya denganmenggunakan sumber-sumber energi lainnya
sebagai bahan bakar alternatif.
Bioetanol merupakansalah satu sumber bahan bakar alternatif yang diolah
12
Wusnah, dkk / Jurnal Teknologi Kimia Unimal 5:1 (2016) 57–65
hingga 18 %. Menurut Balai Besar Teknologi Pati (B2TP) ada 3 kelompok tanaman sumber bioetanol: tanaman yang mengandung pati (seperti singkong, kelapa sawit, tengkawang, kelapa, kapuk, jarak pagar, rambutan, sirsak, malapari, dan nyamplung), bergula (seperti tetes tebu atau molase, nira aren, nira tebu, dan nira surgum manis) dan serat selulosa (seperti batang sorgum, batang pisang, jerami, kayu, dan bagas). Kulit pisang merupakan limbah yang banyak mengandung serat selulosa sehingga sangatefisien digunakan dari pada buahnya yang memiliki nilai jual yang tinggi.
Beberapa penelitian pembuatan bioetanol dengan menggunanakan kulit pisang kepok pernah dilakukan sebelumnya. Nityasa (2009), pembuatan bioetanol dari kulit pisang dengan proses ekstraksi. 5 kg kulit pisang dihaluskan dan ditambahkan air 2/3 dari jumlah kulit pisang, sehingga diperoleh bubur kurang lebih
1,5 liter. Bubur dihidrolisis dengan penambahan HCl 10% pada temperatur 60oC,
yang selanjutnya difermentasi dengan bantuan Saccharomyces cereviceae pada
temperatur 32oC sehingga dihasilkan 15% etanol per 1,5 L jumlah bubur.
Asteria (2013), kulit pisang dihidrolisis menggunakan laruan HCl 37%
pada pH 1. Hidrolisis dilakukan pada suhu 50, 60, 70, dan 80oC selama 1 jam.
Selanjutnya difermentasikan dengan Saccharomyces cereviceae dengan variabel nutrien Diamonium phospat 10, 20, dan 30 gr/l selama 12 hari. Hasil penelitian menunjukkan glukosa optimum yang didapat dari hidrolisis adalah 83,021 gr/l
pada suhu 70oC selama 1 jam. Kandungan bioetanol optimum didapat dari
fermentasi hari ke-8 sebesar 314.46 gr etanol/kg kulit pisang kering.
Dyah (2011), kulit pisang yang digunakan adalah kulit pisang yang telah
dikeringkan dan dihidrolisi menggunakan H2SO4 0,5 N. Hasil penelitian
13
Wusnah, dkk / Jurnal Teknologi Kimia Unimal 5:1 (2016) 57–65
13,5406%. Pada variasi penambahan berat ragi diperoleh kadar etanol 13,5353% dengan berat ragi 0,0624 gram.
Bioetanol adalah sebuah bahan bakar alternatif yang diolah dari tumbuhan,
dimana memiliki keunggulan mampu menurunkan emisi CO2 hingga 18 %. Ada 3
kelompok tanaman sumber bioetanol: tanaman yang mengandung pati (seperti singkong, kelapa sawit, tengkawang, kelapa, kapuk, jarak pagar, rambutan, sirsak, malapari, dan nyamplung), bergula (seperti tetes tebu atau molase, nira aren, nira tebu, dan nira surgum manis) dan serat selulosa (seperti batang sorgum, batang pisang, jerami, kayu, dan bagas). Bahan yang mengandung pati, glukosa, dan serat selulosa ini bisa dimanfaatkan sebagai bahan bakar (Arif, 2011).
Tidak ada perbedaan antara etanol biasa dengan bioetanol yang membedakannya hanyalah bahan baku pembuatan dan proses pembuatannya. Etanol adalah sejenis cairan yang mudah menguap, mudah terbakar, tak berwarna, dan merupakan alkohol yang paling sering digunakan dalam kehidupan sehari-hari. Senyawa ini merupakan obat psikoaktif dan dapat ditemukan pada minuman beralkohol dan termometer modern. Etanol termasuk
ke dalam alkohol rantai tunggal, dengan rumus kimia C2H5OH dan rumus
empiris C2H6O. Ia merupakan isomer konstitusional dari dimetil eter.
14
Bioetanol yang digunakan sebagai campuran bahan bakar merupakan etanol
(etil alcohol) dengan jenis yang sama dengan yang ditemukanpada minuman
beralkohol. Etanol seringkali dijadikan bahan tambahan bensin sehingga menjadi
biofuel. Produksi etanol dunia untuk bahan bakar transportasi meningkat 3 kali lipat
15
Wusnah, dkk / Jurnal Teknologi Kimia Unimal 5:1 (2016) 57–65
menjadi 52 miliar liter pada tahun 2007. Dari tahun 2007 ke 2008, komposisi etanol pada bahan bakar bensin di dunia telah meningkat dari 3.7% menjadi 5.4%. Penelitian ini bertujuan untuk mengkaji proses pembuatan bioetanol dari kulit pisang kepok dan menganalisa kadar bioetanol yang dihasilkan.
2. Bahan dan Metode
Bahan dan peralatan yang diperlukan dalam penelitian ini diantaranya kulit pisang kepok, ragi roti, aquades, gula, urea, NPK, CaO, HCl, NaOH dan seperangkat alat distilasi.
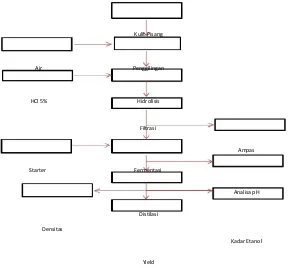
Penelitian ini terdiri atas lima tahap yaitu tahap hidrolisis, tahap persiapan/penumbuhan starter, tahap fermentasi, tahap distilasi dan tahap analisa. Variasi penelitian dilakukan terhadap perubahan volume starter dan waktu fermentasi. Adapun bagan penelitian dapat dilihat pada Gambar 2.
Tahap hidrolisis dilakukan dengan menghaluskan 300 gr kulit pisang kepok lalu dipanaskan sampai mendidih dengan menambahkan HCl 5% selama 60 menit.Tahap persiapan starter diawali dengan membuat larutan gula dengan kadar gula 14% lalu dimasukkan kedalam tempat pembiakan, ditambahkan pupuk urea sebanyak 0.5% dari kadar gula yang digunakan, ditambahkan pupuk NPK sebanyak 0.1% dari kadar gula yang digunakan, ditambahkan ragi roti sebanyak 0,2% dari kadar gula, lalu ditutup rapat dan disimpan dalam ruangan gelap dengan suhu kamar selama 24 jam. (Isroy, 2009). Tahap fermentasi diawali dengan menambahkan starter sesuai variabel yaitu (50, 150, 250 dan 350) ml dengan waktu fermentasi 3,5 dan 7 hari. Hasil fermentasi disaring untuk memisahkan ampasnya, kemudian dilakukan proses distilasi untuk memisahkan
bioetanol dengan air pada suhu 80oC selama 60 menit, lalu hasil distilasi
16
Wusnah, dkk / Jurnal Teknologi Kimia Unimal 5:1 (2016) 57–65
Kulit Pisang
Gambar 2. Skema Proses Pembuatan Bioetanol dari Kulit Pisang Kepok
3. Hasil dan Diskusi
3.1 Pengaruh Volume Starter Terhadap Kadar Bioetanol
17
18
Wusnah, dkk / Jurnal Teknologi Kimia Unimal 5:1 (2016) 57–65
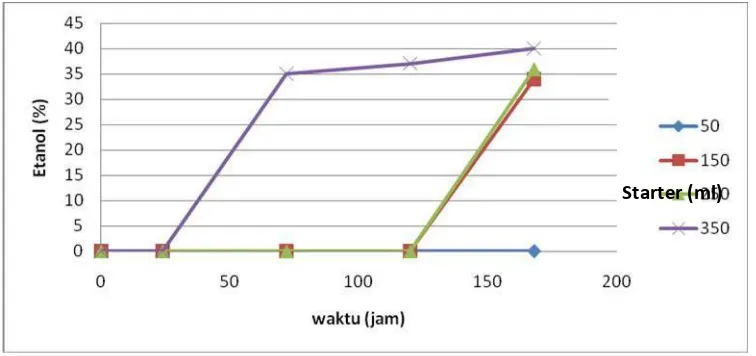
Starter (ml)
Gambar 3 Grafik Pengaruh Volume Starter Terhadap Kadar Bioetanol
Gambar 3 menunjukkan bahwa semakin besar volume starter yang digunakan maka bioetanol yang dihasilkan akan semakain banyak. Pada sampel dengan penambahan starter 50 ml tidak diperoleh bioetanol dari hasil fermentasi selama 168 jam. Sedangkan pada sampel dengan volume starter yang diberikan 350 ml bioetanol sudah terbentuk pada waktu fermentasi 72 jam dan semakin bertambah pada 120 jam dan 168 jam dengan kadar etanol tertinggi yaitu 40%. Pada sampel dengan volume starter 150 ml dan sampel 250 butuh waktu lama untuk menghasilkan bioetanol yaitu hingga pada hari terakhir yaitu 168 jam.
3.2 Pengaruh Yield Terhadap Bioetanol
Starter (ml)
19
Wusnah, dkk / Jurnal Teknologi Kimia Unimal 5:1 (2016) 57–65
Pada Gambar 4 dapat dilihat yield yang dihasilkan dengan semakin
bertambahnya volume starter yang digunakan maka semakin tinggi pula yield yang diperoleh. Dari grafik dapat kita lihat bahwa yield tertinggi diperoleh sampel dengan
volume starter terbanyak 350 ml dengan yield yang dicapai yaitu 11,33%.
2.3. Analisa Gas Chromatography
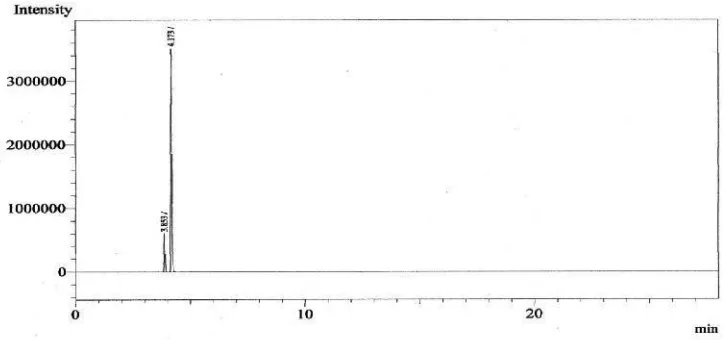
Gambar 5 Grafik HasilAnalisa Bioetanol dengan menggunakan Gas
Chromatography
Bioetanol diuji menggunakan alat gas chromatography untuk melihat senyawa yang terdapat pada sampel. Pada pengujian pertama dimenit 3,853 terbaca gelombang dengan tinggi 602504 µm dan luas area 1810908 µm be rupa metanol dengan konsentrasi 13,772%. Dan pada pengujian kedua terbaca gelombang kedua dengan tinggi 3504353 µm dan luas area 11337902 µm berupa etanol dengan konsentrasi 86,228%. Pada pengujian selanjutnya tidak ditemukan gelombang ketiga hingga akhir pengujian.
20
karbon dioksida, tidak ada senyawa lain yang dihasilkan jika reaksi fermentasinya berlangsung secara sempurna. Dalam proses fermentasi terkadang akan menghasilkan senyawa metanol dalam jumlah yang tidak terlalu signifikan,
Wusnah, dkk / Jurnal Teknologi Kimia Unimal 5:1 (2016) 57–65
senyawa tersebut tidak mengganggu kualitas bioetanol karena jumlahnya
yangsedikit dan sama-sama dapat digunakan sebagai bahan bakar mesin bermotor.
3. Kesimpulan
1. Sampel dengan penggunaan volume starter sebanyak 350 ml pada waktu fermentasi 7 hari mengghasilkan kadar etanol tertinggi yaitu 40%.
2. Selain etanol juga terbentuk metanol dengan jumlah yang sangat sedikit sebagai hasil produk samping proses fermentasi dari kulit pisang kepok.
4. Daftar Pustaka
Agus Krisno Budiyanto, M.Kes, (2011), “Pertumbuhan Microorganisme”
Pendidikan Biologi UMM.
Arif Yudiarto, (2011), Balai Besar Teknologi Pati (B2TP) – BPPT Lampung..
Asteria, Apriliani.S, Franky, Agustinus (2013), “Pembuatan Etanol Dari Kulit Pisang Secara Fermentasi”,Jurusan Teknik Kimia Fakultas Teknik Universitas Diponegoro,Semarang.
Dyah, Tri Retno. Wasir, Nuri, (2011), “Pembuatan Bioetanol Dari Kulit Pisang”,
Jurusan Teknik Kimia Fakultas Teknik Industri UPN “Veteran”,Yogyakarta.
21
Teknik Kimia Fakultas Teknik Universitas Malikussaleh,Lhokseumawe.
Kusnoputranto H. (1996). “Toksikologi Lingkungan Logam Toksik dan B3”
Jakarta: UI-Press.
Nityasa M H Y T, Hafidh Frian P, Nur Hasanah, Dr. Widyastuti, S.Sc., M.Sc
(2006), “Pemanfaatan Kulit Pisang Sebagai Bahan Baku Bioetanol Berbasis Fermentasi”.Institut Teknologi Sepuluh Nopember (ITS), Surabaya.
Saroso, Hadi, (1998), “Pemanfaatan Kulit Pisang Dengan Cara Fermentasi untuk
Pembuatan Alkohol”, Teknik Kimia Politeknik Universitas Brawijaya, Malang.
Soedarmadji, (2002), “Diktat Kuliah Mikrobiologi Industri”, Jurusan Teknik
Kimia Fakultas Teknik Universitas Diponegoro,Semarang.
Wusnah, dkk / Jurnal Teknologi Kimia Unimal 5:1 (2016) 57–65
Kurniawan, T.N., 2009, “Pembuatan Bioetanol Dari Nira Aren”,J u r u s a n
23
MAJALAH BIAM Vol.11 No.2, Desember 2015, Hal 63-75
PENGARUH WAKTU DAN pH FERMENTASI DALAM PRODUKSI
BIOETANOL
DARI
RUMPUT
LAUT
Eucheuma
cotTonii
MENGGUNAKAN ASOSIASI MIKROBA (Sacchromyces cerevisiae,
Aspergilus niger dan Zymomonas mobilis)
TIME EFFECT AND pH FERMENTATION OF BIOETHANOL
PRODUCTION FROM EUCHEUMA COTTONII USING MICROBA
ASSOCIATION (Sacchromyces cerevisiae, Aspergilus niger dan Zymomonas
mobilis)
Edward J. Dompeipen dan Riardi P. Dewa Balai Riset dan Standardisasi Industri Ambon, Jl. Kebun Cengkeh, Ambon Email : [email protected]
ABSTRACT
This research aims to determine of time effect and fermentation of pH as well as to determine concentrate of ethanol in bioethanol production from Eucheuma cottonii. Hydrolisis process that converts lignocelluloses from seaweed of Eucheuma cottonii into bioethanol by using microba association of aspergillus niger, Zymomonas mobilis, and Scharomyces cereviseae simultaneously. Method of this research using variation of pH 3.5; 4.0; 4.5; 5.0 and fermentation 4,5,6,7,8 days. Bioethanol concentration obtained 5,65% at pH 4,5; 7 days and temperature of 380 C.
Keyword : Fermentation, Saccharomyces cerevisiae, Zymomonas mobilis, Aspergilus Niger, Bioethanol
ABSTRAK
Penelitian ini bertujuan untuk mengetahui pengaruh waktu dan pH fermentasi serta menentukan kadar
etanol dalam produksi bioetanol dari rumput laut Eucheuma cotonii. Proses hidrolisis yang
mengkonversi lignoselulosa dari rumput laut Eucheuma cotonii menjadi bioetanol dilakukan dengan
menggunakan asosiasi mikroba Aspergillusniger, Zymomonas mobilis dan Sacchoromyces cerevisiae
secara serempak. Metode penelitian dilakukan variasipH 3,5 ; 4,0 ; 4,5 ; 5,0 dan waktu fermentasi 4,
5, 6, 7, 8 hari. Konsentrasi bioetanol yang diperoleh adalah 5,65% pada kondisi pH 4,5 ; waktu 7 hari dan temperatur 380C.
Kata Kunci : Asosiasi mikroba, Saccharomyces cerevisiae, Zymomonas mobilis, Aspergilus niger,
24
Pengaruh Waktu... (Edward J. Dompeipen dan Riardi P. Dewa)
PENDAHULUAN
Indonesia merupakan negara dengan konsumsi energi yang cukup tinggi di dunia. Berdasarkan data Direktorat Jenderal Energi Baru Terbarukan dan Konservasi Energi Kementerian ESDM, dalam beberapa tahun terakhir pertumbuhan konsumsi energi Indonesia mencapai 7% per tahun. Angka tersebut berada di atas pertumbuhan konsumsi energi dunia yaitu 2,6% per tahun. Konsumsi energi Indonesia tersebut terbagi untuk sektor industri (50%), transportasi (34%), rumah tangga (12%) dan komersial (4%) (ESDM, 2012). Konsumsi energi Indonesia yang cukup tinggi tersebut hampir 95% dipenuhi dari bahan bakar fosil. Dari total tersebut, hampir 50%-nya merupakan Bahan Bakar Minyak (BBM). Konsumsi BBM yang cukup tinggi ini menjadi masalah bagi Indonesia. Sebagai sumber energi tak terbarukan, cadangan BBM Indonesia sangat terbatas. Saat ini, Indonesia hanya memiliki cadangan terbukti minyak 3,7 miliar barel atau 0,3% dari cadangan terbukti dunia (ESDM, 2012). Untuk mengurangi ketergantungan pada bahan bakar fosil, pemerintah mengeluarkan Peraturan Presiden No.5 Tahun 2006 tentang kebijakan energi nasional untuk mendorong pengembangan sumber energi alternatif sebagai pengganti bahan bakar minyak. Pada tahun 2025 pemenuhan kebutuhan energi Indonesia diharapkan 17 % nya berasal dari energi baru terbarukan. Salah satunya dengan memanfaatkan etanol sebagai alternatif, khususnya bioetanol berbasis lignoselulosa.
Penggunaan etanol sebagai bahan bakar mempunyai beberapa keunggulan yaitu kandungan oksigen etanol tinggi (35%) sehingga menghasilkan bahan bakar yang bersih; kedua, hasil bersih ini ramah bagi lingkungankarenaemisigaskarbonmonoksida lebih rendah 19-25 persen dibanding BBM. Energi terbarukan ini tidak memberikan kontribusi pada akumulasi karbon dioksida di atmosfer; ketiga, daya hasil etanol lebih stabil. Angka oktan etanol tergolong tinggi sekitar 129 sehingga menghasilkan proses
pembakaran yang stabil. Proses pembakaran dengan daya yang lebih baik ini akan mengurangi emisi gas karbon monoksida; keempat, campuran bioetanol 3% saja mampu menurunkan emisi karbonmonoksida menjadi hanya 1,3% (Broto, S,K., 2010).
Krisis Bahan Bakar Minyak (BBM) dewasa ini menunjukkan cadangan energi fosil yang dimiliki Indonesia terbatas. Fakta menunjukkan konsumsi energi terus meningkat berbanding lurus dengan laju pertumbuhan ekonomi, pertambahan penduduk, peningkatan ilmu pengetahuan dan teknologi (Sudaryanto, 2008 ;Victor, 2010). Eksplorasi berbagai energi alternatif dari sumber daya alam yang dapat diperbaharui perlu dikembangkan. Sudah waktunya ketergantungan kebutuhan energi fosil non-renewable digantikan dengan energi renewable. Menurut Rikayana
dan Adam (2011) dalam Retmonando (2012), Salah satu energi renewable yang sangat penting adalah bioetanol. Bioetanol menjadi pilihan utama karenamudahteruraidanamanbagilingkungan karena tidak mencemari air dan pembakaran dari bioetanol hanya menghasilkan karbondiokasida dan air (Hambali et al., 2006). Bioetanol memiliki predikat clean energy karena mampu menurunkan emisi karbondioksida hingga18% (Fauzi, 2011).
25
26
MAJALAH BIAM Vol.11 No.2, Desember 2015, Hal 63-75
seperti rumput laut menjadi etanol, bagian yang terpenting adalah polisakarida. Karena polisakarida tersebut yang akan dihidrolisis menjadi monosakarida seperti glukosa, sukrosa, xilosa, arabinosa dan lain-lain sebelum dikonversi menjadi etanol (Arif Jumari, 2009). Secara umum sintesis bioetanol yang berasal dari biomassa terdiri dari dua tahap utama, yaitu hidrolisis dan fermentasi. Hidrolisis bertujuan untuk memecah polisakarida menjadi monosakarida. Polisakarida dapat diubah menjadi alkohol melalui proses biologi dan kimia (Broto.S.K, 2010).
Proses hidrolisis umumnya digunakan pada industri etanol adalah menggunakan hidrolisis dengan asam (acid hydrolysis) dengan menggunakan asam sulfat (H2SO4) atau dengan menggunakan asam klorida (HCl). Proses hidrolisis dapat dilakukan dengan menggunakan enzim yang sering disebut dengan enzymatic hydrolysis yaitu hidrolisis dengan menggunakan enzim jenis selulase atau jenis yang lain. Keuntungan dari hidrolisis dengan enzim dapat mengurangi penggunaan asam sehingga dapat mengurangi efek negatif terhadap lingkungan. Proses selanjutnya adalah fermentasi menggunakan jamur seperti Sacchromyces cerevisiae untuk
dikonversi menjadi etanol (Broto.S.K, 2010).
Penggunaan asam pekat pada proses hidrolisis selulosa dilakukan pada temperaratur yang lebih rendah daripada dalam asam encer. Konsentrasi asam yang digunakan adalah 10 - 30% (Zimbardi.,et. al.,2010). Sumber asam yang biasa digunakan adalah asam sulfat dengan temperatur reaksi adalah 100°C dan membutuhkan waktu reaksi antara 2 - 6 jam. Temperatur yang lebih rendah akan meminimalisasi degradasi gula. Keuntungan dari penggunaan asam pekat ini adalah konversi gula yang dihasilkan tinggi hingga mencapai konversi 90%. Kekurangan dari reaksi dengan penggunaan asam pekat adalah waktu reaksi yang dibutuhkan lebih lama dan membutuhkan proses pencucian yang baik untuk mencapai pH reaksi sebelum ditambahkan mikroba pada proses fermentasi
pembentukan etanol (Badger,2002).
Metode lain yang digunakan untuk menghidrolisis selulosa adalah secara enzimatis, yaitu dengan menggunakan enzim. Enzim merupakan protein alam yang dapat mengkatalisis reaksi tertentu. Untuk dapat bekerja, enzim harus kontak langsung dengan substrat yang akan dihidrolisa. Karena selulosa secara alami terikat oleh lignin yang bersifat permeable terhadap air sebagai pembawa enzim, maka untuk proses hidrolisis secara enzimatik membutuhkan pretreatmen sehingga enzim dapat berkontak langsung dengan selulosa. Pretreatmen dilakukan untuk memecah struktur kristalin selulosa dan memisahkan lignin sehingga selulosa dapat terpisah. Pretreatmen dapat dilakukan secara kimia maupun fisika. Metode fisika yang dapat dilakukan adalah dengan menggunakan temperatur dan tekanan tinggi, penggilingan, radiasi atau pendinginan, semuanya membutuhkan energi yang tinggi. Sedangkan metode pretreatmen secara kimia menggunakansolven untuk memecah dan melarutkan lignin (metode delignifikasi) (Badger,2002).
27
Z.mobilis merupakan jenis bakteri yang mampu menghasilkan selulase yang berguna untuk menghidrolisis dan dapat mengubah glukosa, fruktosa dan sukrosa menjadi etanol, sedangkan A. niger mampu menghasilkan amiloglukosidase yang berfungsi untuk
Pengaruh Waktu... (Edward J. Dompeipen dan Riardi P. Dewa)
menghidrolisis fraksi pati menjadi glukosa. Filtrat enzim selulase, AMG kasar dan kultur campuran dari Z.mobilis dan A. niger pada substrat hidrolisat asam diharapkan dapat meningkatkan hidrolisis fraksi disakarida menjadi glukosa yang selanjutnya dipergunakan sebagai substrat fermentasi oleh S. cerevisiae. Dengan demikian konsentrasi etanol akan meningkat jika dibandingkan dengan substrat yang hanya melalui hidrolisis menggunakan enzim amilolitik dan kultur tunggal S. cerevisiae.
Salah satu sumber daya laut Indonesia yang populer adalah rumput laut, memang pengembangan budidaya rumput laut yang cukup menjanjikan. Sayangnya, hanya 20
2.23% budidaya rumput laut di Indonesia menghasilkan bahan baku industri dan produk olahan dengan nilai tambah. Sampai saat ini pemanfaatan rumput laut Indonesia adalah sebagai sumber pangan antara lain Euchemacottoni, Eucheuma spinosum dan Gracilaria sp, Selain itu rumput laut
dimanfaatkan sebagai bahan kosmetika, obat obatan, pasta gigi, dll. Rumput laut kemudian mulai dilirik untuk dimanfaatkan sebagai sumber energi alternatif. Pemanfaatan rumput laut yang mudah dibudidayakan di Indonesia sebagai sumber energi alternatif merupakan hal yang baru dan patut didukung. Menurut data dari Inha Universitas di Republik Korea, satu hektare rumput laut dapat menghasilkan 58700 L biodiesel dengan asumsi kandungan minyak dalam rumput laut berkisar 30%.
Makroalga merupakan salah satu organisme yang dapat dinilai ideal dan potensial untuk dijadikan sebagai bahan baku produksi biofuel (Li, et al, 2008 ; Raja, et al., 2008 ; Gouveia and Oliveira, 2009). Secara kimia, rumput laut terdiri dari air (27,8%), protein (5,4%), karbohidrat (33,3%), lemak (8,6%), serat kasar (3%) dan abu (22,25%) (Harvey, 2009). Kadar karbohidrat makroalga tergolong tinggi (29-31% berat kering) lebih tinggi dari pada ubi singkong (23% berat kering) dan dengan memperhitungkan masa panen, secara matematis produktivitas bioetanolnya
mencapai lebih dari 100 kali lipat ubi singkong (Ansyori, 2008). Rumput laut jenis Eucheuma cottonii merupakan salah satu rumput laut dari jenis alga merah (Rhodophyta). Rumput laut dapat dijadikan sebagai sumber bahan baku utama dalam pembuatan bioetanol (biofuel). Rumput laut Eucheuma cottonii memiliki komposisi penyusun seperti polisakarida yaitu selulosa, karaginan, agar, lignin dan monosakarida yaitu glukosa, galaktosa.(Sinuraya, E.A, 2014).
Penelitian ini dilakukan untuk melihat pengaruh pH dan waktu selama fermentasi dalam produksi bioetanol dari rumput laut E. Cottonii. Sebagian besar karbohidratpada rumput laut E. cottonii berupa senyawa polisakarida sehingga diperlukan adanya proses hidrolisis untuk
menguraikan senyawa tersebut menjadi gula sederhana agar dapat dimanfaatkan sebagai sumber bahan baku bioetanol. Proses hidrolisis dilakukan dengan menggunakan asosiasi mikroba yaitu,
28 METODE PENELITIAN
Penelitian ini dilakukan pada bulan Juni sampai dengan Desember 2014 di Laboratorium Kimia, Jurusan Kimia Politeknik Negeri Makassar dan Laboratorium Mikrobiologi, Balai Riset dan Standardisasi Industri Ambon. Pengambilan sampel rumput laut Eucheuma cotonii di Desa Letvuan, Kabupaten Maluku Tenggara.
Persiapan Bahan dan Perlakuan Awal Rumput laut Eucheuma cotonii
sebanyak 10 Kg direndam dengan larutan KOH 2% dalam wadah plastik bertutup sampai terendam, diaduk dan kemudian dibiarkan selama 24 jam pada suhu kamar. Rumput laut dicuci dengan akuades sampai lignin yang berwarna hitam keluar semua. Proses pencucian dihentikan setelah cairan pencuci sudah jernih atau pH netral. Rumput laut yang telah bersih dipotong-potong sepanjang 1 cm kemudian dijemur hingga
MAJALAH BIAM Vol.11 No.2, Desember 2015, Hal 63-75
kadar air dibawah 10%. Rumput laut dihaluskan dengan crusher dengan kehalusan 100 mesh. Selanjutnya dilakukan analisis selulosa dan lignin dilakukan dengan metode Chesson (Datta, 1981)
Peremajaan mikroba dengan media agar miring
Bahan bahan seperti glukosa 2 g, bakto agar 2 g dan ekstrak toge 20% dicampur kemudian dipanaskan sambil diaduk hingga larut. Beberapa tabung reaksi disiapkan, kemudian dipipet 10 mL larutan ekstrak dimasukkan kedalam tiap tabung reaksi, disumbat dengan kapas dan alumunium foil. Proses selanjutnya sterilisasi pada 121oC selama 15 menit lalu didinginkan
dalam keadaan miring (media agar miring). Biakan murni mikroba Aspergillus niger dan Sacharomyces cerevisiae digoreskan secara zig-zag pada media agar miring dengan menggunakan jarum ose. Pengerjaan ini dilakukan dalam lemari sterilisasi (ent case) kemudian
ditumbuhkan dalam inkubator pada suhu 37oC selama 7 hari. Isolat Zymomonas mobilis
diremajakan dalam tabung reaksi yang berisi medium NA (Nutrien Agar) miring dan diinkubasi pada suhu 30oC selama 24 jam.
Pembuatan media inokulum (starter)
Pembuatan media inokulum (starter) untuk ketiga mikroba Zymomonas mobilis,
AspergillusnigerdanSacharomycescerevisiae dilakukan dalam media yang berbeda. Media starter
untuk mikroba Zymomonas mobilis adalah 1,50 g tepung rumput laut; 0,10 g Yeast extract; 0,05 g
MgSO4.7H2O; 0,01 g(NH4)2SO4, dan 18,50 gr Glukosa. Media starter untuk mikroba Aspergilus
niger adalah 1,50 g tepung rumput laut; 0,30 gKH2PO4; 0,35 g (NH4)2SO4 ;dan 18,50 gr Glukosa.
Media starter untuk mikroba Sacharomyces cerevisiae adalah 1,50 g tepung rumput laut; 0,30 g NPK; 0,35 g Urea dan 18,50 gr Glukosa.
29
Erlenmeyer ditutup dengan kapas dan aluminium foil lalu disterilkan dalam otoklaf pada suhu 12 oC selama 15 menit. Didinginkan lalu ditambahkan masing-masing kedalam Erlenmeyer stok
kultur murni Z.mobilis, A. niger dan S. cereviseae dengan menggunakan ose dalam ruang sterilisasi. Ditutup kembali dengan kapas dan aluminium foil lalu difermentasi pada inkubator shaker selama 3 haripadasuhu37oCdengankecepatan150rpm.
Pembuatan media fermentasi
Pembuatan media fermentasi untuk
ketiga mikroba Zymomonas mobilis, Aspergillus niger dan Sacharomyces cerevisiae dilakukan dalam media yangsama. Komposisi bahan untuk media fermentasi adalah 24,0 g tepung rumput laut; 1,00 g KH2PO4; ; 1,25 g (NH4)2SO 4; 1,00 g MgSO4.7H2O; 1,00 g CaCl2 ; 1,00 g NaCl;
2,50 g Ekstrak ragi; dan 62,50 g Glukosa.
Campuran bahan diatas dimasukkan kedalam beker gelas 2000 mL kemudian ditambahkan 400 mL air diaduk hingga larut. Atur pH larutan yaitu 3,5: 4,0: 4,5 dan 5,0 dengan buffer fospat lalu diencerkan hingga 500 mL. Disiapkan 20 buah Erlenmeyer 250 mL lalu ditambahkan 100 mL larutan kedalam tiap Erlenmeyer, disumbat dengan kapas dan aluminium foil dan disterilisasi dalam otoklaf selama 15 menit pada suhu 121oC.
Erlenmeyer dipindahkan kedalam ruang steril lalu tambahkan masing-masing 10 mL media inokulum A. niger .S. cereviseae dan Z.mobilis kedalam setiap Erlenmeyer dengan menggunkan
gelas ukur 25 mL yang steril. Erlenmeyer ditutup kembali dengan kapas lalu difermentasi pada shaker incubator selama, 4, 5, 6, 7 dan 8 hari pada suhu 29 oC dengan kecepatan 150 rpm. Setelah 4 hari salah satu Erlenmeyer pada media fermentasi diambil, disaring lalu didistilasi pada suhu 100 OC hingga diperoleh volume destilat 10 mL. Destilat dianalisis dengan alat refraktometer dan Gas Kromatorafi.
Analisis selulosa dan lignin
Analisis selulosa dan lignin dilakukan
Pengaruh Waktu... (Edward J. Dompeipen dan Riardi P. Dewa)
dengan metode Chesson (Datta, 1981). Sebanyak 1 g sampel kering ditambahkan 150 mL akuades, dipanaskan pada suhu 90
5.100 oC dengan water bath selama 1 jam. Hasilnya disaring, residu dicuci dengan air panas
(300 mL). Residu kemudian dikeringkan dengan oven sampai konstan kemudian ditimbang. Residu ditambahkan 150 mL H2SO4 1N kemudian dipanaskan dengan water bath selama 1 jam
pada suhu 90 - 100 oC. Hasilnya disaring dan dicuci dengan akuades sampai netral (300 mL)
30
H2SO4 1 N dan direfluks pada water bath selama 1 jam pada pendingin balik. Residu disaring dan dicuci dengan akuades sampai netral (400 mL) kemudian dipanaskan dalam oven pada suhu 105 oC
dan hasilnya ditimbang sampai bobot tetap, selanjutnya residu diabukan dan ditimbang. Perhitungan kadar selulosa dan kadar lignin sebagai berikut :
Kadar karagenan = (a - b)/a x 100
b = berat residu pada penimbangan kedua (gram) c = berat residu pada penimbangan ketiga (gram) d = berat residu pada penimbangan keempat (gram) e = berat abu (gram)
Karakterisasi Senyawa Bioetanol dengan Kromatografi Gas (GC)
Karakterisasi hasil fermentasi bioetanol dari kerja sinergisitas yang dilakukan oleh mikroba A. niger , S. cerevisiae dan Z. mobilis dengan menggunakan kromatografi gas. Kondisi operasi alat
Kromatografi Gas untuk analisis sampel bioetanol adalah sebagai berikut: tipe alat Shimadzu GC 2010, dengan gas pembawa ; N2, H2, kecepatan alir:30 mL/ menit, laju alir H2 :40 mL/menit, laju alir
N2 :400 mL/menit, temperatur injektor: 100oC, tekanan:100 kPa, total aliran: 50 mL/ menit,
purge flow: 3 mL/menit; Jenis kolom: RTX-WAX; Temperatur:100oC; Detektor : FID.
HASIL DAN PEMBAHASAN
Perlakuan Awal Sampel Rumput laut Eucheuma cotonii
31
Pencacahan dimaksudkan untuk memperkecil ukuran selulosa sehingga selulosa bisa berkontak secara efektif dengan katalis asam cair. Pencacahan dilakukan dengan menggunakan crusher sampai ukuran selulosa mencapai 60 mesh. Selanjutnya selulosa yang telah mencapai ukuran dikontakan dengan katalis asam dengan menambahkan aquadest sebagai zat cair pembawa untuk memudahkan kedua bahan (selulosa dan katalis) bercampur.
32
MAJALAH BIAM Vol.11 No.2, Desember 2015, Hal 63-75
dan selanjutnya dilakukan proses penepungan, seperti disajikan dalam gambar 1a dan 1b.
a.sebelumpenepunganb.sesudahpenepungan Gambar 1 (a) (b). Sampel Eucheuma cotonii
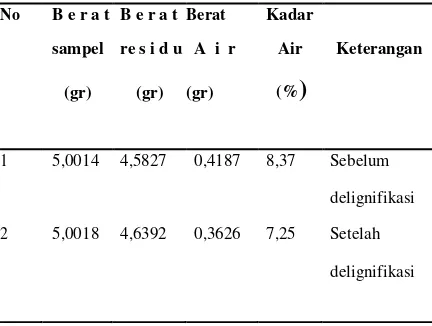
Setelah pencacahan diperoleh berat residu dan berat sampel sehingga dapat ditentukan kadar air dari tepung Eucheumacotonii, disajikan dalam Tabel 1.
Tabel 1. Penentuan kadar air tepung rumput laut Eucheuma cotonii
No B e r a t B e r a t Berat Kadar
Analisis Lignin dan Selulosa Pada Eucheuma cotonii
33 kandungan lignin harus rendah (Euis et al,2010).
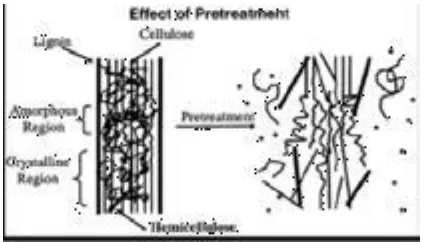
Secara garis besar ilustrasi proses penghancuran dinding lignin yang membungkus struktur hemiselulosa dalam proses pretreatment dapat dilihat pada :
Gambar 2. Proses Penghancuran Bahan Berlignoselullosa
Dari Gambar 2 Lignin laksana tembok yang kokoh yang dapat membungkus senyawa selulosa dalam satu matriks tumbuhan berlignoselulosa. Senyawa lignin inilah yang membuat sisi luar tanaman menjadi keras dan dapat berdiri kokoh. Namun menjadi masalah dalam proses fermentasi, dimana keberadaan lignin ini akan menyulitkan kerja dari enzim dan mikroba dalam fermentasi, sehingga proses konversi selulosa menjadi gula sederhana selanjutnya dikonversi menjadi etanol menjadi terhambat. Untuk itu diperlukan usaha luar untuk membantu usaha penghancuran dinding lignin sehingga akan diperoleh lebih banyak selulosa yang dapat dikonversi menjadi gula (Moiser, et al,2005).
Analisis kadar lignin rumput laut jenis Eucheuma cottonii dari hasil penelitian Samsul Rizal
(2005) yang melaporkan bahwa rumput laut jenis Eucheuma cottonii ternyata mengandung kadar
34
Pengaruh Waktu... (Edward J. Dompeipen dan Riardi P. Dewa)
dengan menggunakan bantuan senyawa katalis, salah satu caranya adalah dengan menggunakan katalis kimia berupa senyawa NaOH. Dari hasil penelitian Samsul Rizal (2005), penambahan konsentrasi katalis NaOH hingga 8% ternyata mampu meningkatkan kandungan selulosa dalam produksi pulp dari jerami, sehingga diperoleh hasil produksi optimum selulosa sekitar 91,4 % dengan sisa lignin dalam pulp yang hanya mencapai sekitar 1,2 % saja.
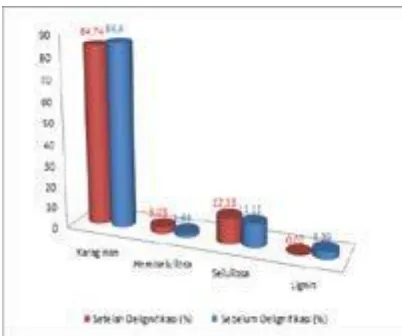
Pada penelitian ini kadar lignin yang diperoleh setelah proses delignifikasi adalah sebesar 0,02% atau terhidrolisis sebesar 59% dari kadar lignin sebelumnya. Semakin besar persentase lignin yang terhidrolisis baik untuk rekasi enzimatik selanjutnya dalam fermentasi untuk menghasilkan bioetanol, karena enzim yang dihasilkan oleh mikroba tidak mendapatkan halangan kontak untuk bereaksi dengan sisi aktif dari selulosa untuk menproduksi glukosa. Kadar selulosa sampel rumput laut Eucheuma cotonii setelah delignifikasi sebesar 12,13% dan untuk hemiselulosa 3,03%. Proses delignifikasi ini berhasil meghidrolisis ikatan 1,4 antara molekul monosakarida atau disakarida dengan molekul-molekul lignin. Kadar lignin, selullosa, hemiselullosa, karaginan sebelum dan setelah proses delignifikasi disajikan pada Gambar 3.
Gambar 3. Kadar Karaginan, Hemiselullosa, Selullosa dan Lignin Sebelum dan Sesudah delignifikasi
Pengaruh pH Substrat terhadap Produksi Bioetanol
Derajat keasaman (pH) merupakan satu diantara beberapa faktor penting yang mampu mempengaruhi proses pada fermentasi etanol. Derajat keasaman optimum untuk proses fermentasi adalah antara 4-5. Pada pH dibawah 3, proses fermentasi akan berkurang kecepatannya. Pada penelitian ini divariasikan kondisi pH pada proses fermentasi yaitu sebesar 3,5; 4,0; 4,5 dan 5,5. Proses hidrolisis selulosa Eucheuma cotonii menghasilkan monomer
glukosa olehmikroba A. niger dengan memutuskan ikatan glikosida dan selanjutnya difermentasi oleh mikroba Z. mobilis dan S. cerevisiae menjadi etanol dengan kondisi optimal diperhatikan
pengaruh pH dan waktu fermentasi terhadap konsentrasi bioetanol yang dapat dilihat glikosida dan selanjutnya difermentasi oleh mikroba Z. mobilis dan S. cerevisiae menjadi etanol dengan kondisi optimal diperhatikan pengaruh pH dan waktu fermentasi terhadap konsentrasi bioetanol.
35
secara sinergisitas untuk mengkatalisis reaksi hidrolisis glukosa menjadi etanol. Pada gambar 4 disajikan proses fermentasi starter mikroba campuran sampai terbentuknya etanol.
Pada penelitian ini digunakan A. niger yang memiliki kemampuan untuk memproduksi β
-glukosidase dan bekerja secara sinergis untuk menghasilkan enzim selulase yang dapat mengkonversi selebiosa yang telah terbentuk menjadi glukosa (Soeprijanto, 2004). Konsentrasi pH fermentasi optimal yaitu 3,5 yang menghasilkan kadar etanol sebesar 5,65%. Menurut Murphi, hal ini berpengaruh terhadap metode SSF dimana ada tiga mikroba yang bekerja dalam proses fermentasi, yaitu A. niger optimal pada pH 2,6-8,8 (Murphi, 1994) berperan
MAJALAH BIAM Vol.11 No.2, Desember 2015, Hal 63-75
merombak atau memecah selulosa menjadi glukosa. S. cerevisiae optimal pada pH 4-4,5 (Fardiaz, 1992), namun pada saat fermentasi berlangsungpHakanturunakibatterbentuknya CO2 dan asam-asam organik yang lain (Sugiarto, 1991). Z. mobilis dapat hidup pada pH 3,5--7,5 (Rahmanto dan Ambarwati, 2011) dan optimal pada pH 4-7, namun dapat hidup pada pH asam karena dapat memproduksi bakteriosin (protein anti mikroba) yang dapat menghambat pertumbuhan spesies lain yang berkerabat dekat.
36
polisakarida menjadi gula (glukosa, galaktosa, manosa dan sebagainya) yang difermentasikan lebih lanjut oleh S. cerevisiae dan Z. mobilis menjadi etanol. Enzim glukoamilase merupakan enzim
karbohidrase yang mengkatilasis pemecahan ikatan α (1-4) glikosidik pada polisakarida pati menjadi glukosa. Sementara Z. mobilis menghasilkan enzim yaitu glukokinase dan fruktokinase yang mampu
mengubah gula reduksi menjadi etanol (Purwoko, 2009) melalui 2-keto-3deoksi-6-fosfoglukonat membentuk piruvat, kemudian piruvat oleh piruvat dekarboksilase diubah menjadi asetaldehid yang kemudian direduksi menjadi etanol (Fardiaz, 1992).
Gambar 4. Proses Fermentasi Bioetanol dengan Mikroba Asosiasi
Karakterisasi Senyawa Bioetanol dengan Tabel 2. Komposisi campuran etanol standar
Kromatografi Gas (GC) dan pelarut akuabides dan luas
Pengujian kadar etanol hasil fermentasi area puncak etanol standard.
diawali dengan melakukan penentuan kurva standard etanol dengan deret konsentrasi
etanol adalah sebagai berikut: 20, 40, Konsentrasi Volume Volume Luas Puncak
60, 80 dan etnaol absolut 100%. Data
area luas puncak dan kadar etanol standar
yang diperoleh disajikan dalam Tabel 2. 20 0,2 0,8 1 61532401
37 garis regresi liniear yang menunjukan
60 0,6 0,4 1 194576884
hubungan antara luas puncak dengan
80 0,8 0,2 1 250412950
kadar etanol standar dalam persen (%),
100 1 0 1 295837554
38
Pengaruh Waktu... (Edward J. Dompeipen dan Riardi P. Dewa)
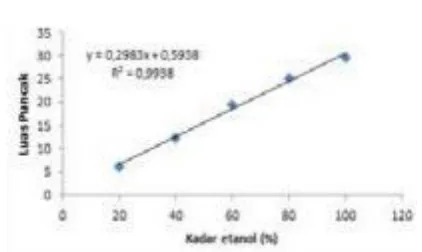
Gambar 5. Kurva Standar hubungan Luas Puncak dan Kadar Etanol Standar
Penentuan kadar bioetanol hasil fermentasi mikroba campuran pada hari ke 4, 5, 6, 7 dan 8 dilakukan berdasarkan data spektrum GC dan kurva standar etanol.
Spektrum GC bioetanol hasil fermentasi hari ke-4 menunjukan adanya 5 komponen yaitu pada waktu retensi 0,715; 1,052; 2,468 ; 2,623 dan 2,816 menit. Komponen utama terdapat pada waktu retensi 2,623 dengan luas area sebesar 5.997.425 yang dapat disimpulkan adalah merupakan senyawa etanol berdasarkan data spektrum etanol standard dan komponen yang lain merupakan senyawa pengotor. Konsentrasi bioetanol hasil fermentasi hari ke-4 diukur dengan memasukan nilai luas area yang diperoleh dari pengukuran ke dalam persamaan regresi linear yang membandingkan luas puncak dan kadar etanol standard.
Konsentrasi bioetanol hasil fermentasi hari ke empat sebesar 0,02% hal ini diakibatkan karena mikroba campuran masih dalam fase lag atau fase adaptasi yaitu fase di mana mikroba melakukan penyesuaain sel dengan lingkungan, pembentukan enzim-enzim untuk mengurai substrat. Pada hari ke empat diperkirakan campuran mikroba masih berkonsentrasi untuk beradaptasi untuk pertumbuhan sel sel penyusun dan pembentukan enzim pengurai. Penelitian dilakukan dengan metode Solid Sacarification Fermentation (SSF) dimana proses enzimatik pembentukan glukosa dan etanol berlangsung secara serempak dengan campuran mikroba yang sama. Pada hari ke empat enzim
glukoamilasedanglukosidasebelumterbentuk sehingga reaksi biokatalisis atau reaksi hidrolisis menjadi glukosa dan seterusnya menjadi etanol belum berlangsung
Konsentrasi bioetanol hasil fermentasi pada hari ke-5 dan hari ke-6 adalah sebesar 0,78 dan 0,95%. Pada hari ke-5 dan ke-6 diperkirakan S.cerevisiae, A.niger dan Z.mobilis masih dalam fase akselerasi yaitu suatu kondisi di dalam pertumbuhan mikroba dimana terjadinya proses pembelehan sel. Dalam fase ini diperkirakan belum terjadi reaksi enzimatik untuk degradasi dan hidrolisis substrat karena enzim pengurai belum terbentuk.
39
Kromatogram GC hasil fermentasi pada hari ke-6 menunjukan adanya tiga komponen yang ada pada hasil fermentasi campuran mikroba yaitu pada waktu retensi (Rt) : 2,476 M, 2,552M dan 2,635 M. Komponen senyawa pada Rt 2,635 merupakan komponen yang paling dominan dengan luas area 8.779.555 dan senyawa ini adalah etanol. Jumlah komponen yang terbentuk pada hari ke-5 dan 6 tidak mengalami pengurangan, tetapi terjadi perbedaan yang sangat kecil dalam waktu retensi setiap komponen hal ini diakibatkan karena senyawa senyawa yang terbentuk merupakan senyawa alkohol. Dengan demikian telah terjadi reaksi degradasi enzimatis karena tidak terbentuknya komponen yang lain selain senyawa senyawa alkohol.
Pada hari ke-7 fermentasi campuran mikroba S.cerevisiae, A.niger dan Z.mobilis dalam
40
MAJALAH BIAM Vol.11 No.2, Desember 2015, Hal 63-75
cotonii diperoleh konsentrasi bioetanolsebesar 5,65%. Konsentrasi bioetanol paada hari ke-7 merupakan kadar bioetanol hasil fermentasi campuran mikroba yang tertinggi karena pada waktu ini, campuran mikroba mengalami kondisi pada fase eksponensial dimana terjadi peningkatan dalam jumlah sel dan aktivitas mikroba serta merupakan fase yang penting dalam pertumbuhan mikroba. Diperkirakan pada fase ini terjadi reaksi reaksi enzimatik untuk produksi bioetanol.
Kromatogram GC hasil fermentasi pada hari ke-7 menunjukan adanya dua komponen yang ada pada hasil fermentasi campuran mikroba yaitu pada waktu retensi (Rt) : 2,475 M dan 2,631. Komponen senyawa pada Rt 2,631 merupakan komponen yang paling dominan dengan luas area 16.814.248 dan senyawa ini adalah etanol. Jumlah komponen senyawa yang terbentuk pada hari ke-
7 mengalami pengurangan dan perbedaan yang sangat kecil dalam waktu retensi setiap komponen
hal ini diakibatkan karena senyawa senyawa yang terbentuk merupakan senyawa alkohol. Dengan demikian telah terjadi reaksi degradasi enzimatis karena tidak terbentuk komponen lain selain senyawa senyawa alkohol. Luas area komponen pada Rt : 2,631 pada hari ke-7 dua kali lebih besar dengan Luas area komponen pada Rt : 2,635 pada hari ke-6.
Pada hari ke-8 fermentasi campuran mikroba S.cerevisiae, A.niger dan Z.mobilis dalam substrat tepung rumput laut Eucheuma cotonii diperoleh konsentrasibioetanol sebesar 0,01%. Terjadi penurunan yang sangat signifikan dalam produksi bioetanol hal ini diakibatkan karena mikroba sudah memasuki fase kematian dipercepat. Bioetanol yang dihasilkan pada fase sebelumnya akan bertindak sebagai racun terhadap mikroba sehingga mikroba-mikroba mengalami kematian.
41 Komponen ini adalah senyawa etanol. KESIMPULAN
Pembuatan bioetanol dari rumput laut Euchema cotonii dengan menggunakan
asosiasi mikroba Aspergillus niger, Zymomonas mobilis dan Sacchoromyces cerevisiae dapat dilakukan dengan metode Simultaneous Saccharification Fermentation (SSF). Proses hidrolisis dan enzimatis dapat mengkonversi lignoselulosa dari tepung rumput laut Eucheuma cotonii menjadi bioetanol. Penelitian dilakukan dengan metode pengaruh perbedaan pH dan waktu fermentasi terhadap konsentrasi bioetanol yang dihasilkan, dengan variasi pH 3,5 ; 4,0 ; 4,5 ; 5,0 dan waktu fermentasi 4, 5, 6, 7, 8 hari. Konsentrasi bioetanol tertinggi yang dihasilkan adalah 5,65% pada kondisi pH 4,5 dan lama waktu fermentasi 7 hari pada temperatur 38OC.
DAFTAR PUSTAKA
Ansyori. 2008. Etanol sebagai Bahan BakarAlternatif, Erlangga, Jakarta
Arif J,Wusana A. W, Handayani, Indika A. 2009. Pembuatan Etanol Dari Jambu Mete Dengan Metode Fermentasi.http://tk.uns.ac.id.Tanggal akses 17 November 2014.
Badger, P.C. 2002. Ethanol from cellulose.A general review p. 17-21. In J 8r ide’ and A. Whipkey (eds.), Trends in new crops and new uses. ASHS Press Alexandria, VA.
Broto S. K. 2010. Teknologi PembuatanEtanol Berbasis Lignoselulosa Tumbuhan Tropis untuk Produksi Biogasoline. Laporan Akhir Program Intensif Peneliti dan Perekayasa LlPI. Serpong.
Datta, R. 1981. Acidogenic fermentationof lignocellulose acid yield and
42
Pengaruh Waktu... (Edward J. Dompeipen dan Riardi P. Dewa)
conversion of components.Biotechnology and Bioengineering 23 (9): 2167-2170.
ESDM, 2012, “Laju Eksplorasi MinyakCadangan Indonesia Sangat Tinggi”, http://www. esdm . go . id/berita/ migas-laju-eksplorasi-cadangan-minyakindonesia-sangat-tinggi. html tanggal akses: 6 Juni 2012
Euis H, Djumali M, Titi C S, Ono S, Bambang P.2010. Pemanfaatan Biomassa Lignoselulosa Ampas Tebu Untuk Produksi Bioetanol.Jurnal Litbang Pertanian, 29(4).
Fardiaz, S. 1992. Mikrobiologi Pangan
Departemen Pendidikan dan Kebudayaan. Direktorat Jenderal Pendidikan Tinggi. PAU Pangan dan Gizi.Institut Pertanian Bogor. 119 pp.
Fauzi, A.F. 2011. Pemanfaatan Buah Pepaya (Carica papaya L.) Sebagai Bahan Baku Bioetanol dengan Proses Fermentasi dan Distilasi. (Skripsi). Program Diploma, Fakultas Teknik, Universitas Diponegoro, Semarang, 75 hlm.
Gouveia, L, Oliveira A.C. 2008. Microalgae as a raw material for biofuels production. J Ind Microbiol Biotechnol. 2009 Feb;36(2):269-74. doi: 10.1007/s10295-008-0495-6. Epub 2008 Nov 4.
Hamelinck, C. N, Hooijdonk, G. V, Faaij, A.P.2005.EtanolfromLignocellulosic B i o m a s s : Te c h n o E c o n o m i c Performance in Short, Middle, and Long-Term. Biomass and Bioenergy28(4), 384–410.
43
Harvey, M.,&Pilgrim,S. 2010. Battles Over Biofuels in Europe: NGOs and The Politics of Markets. University of Essex, Sociological Research Online, 15(3):4-16
Indyah N. 2005. Prospek Pengembangan BiofuelSebagaiSubtitusiBahanBakar MinyakdanTeknologiProsesProduksi Bioetanol. Jurnal Teknologi Proses.
Kadi, A., dan Atmadja,W.S. 1988. Rumput Laut (Algae) Jenis, Reproduksi, Produksi, Budidaya dan Pasca panen.Puslitbang Oseanologi – LIPI, Jakarta : 71 pp.
Kadir, S. 2003. Karakteristik Nata de Coco dari Starter Ampas Nenas Melalui Penambahan Sukrosa dan Keasaman Medium. Journal Agroland10 : 145–150
Mosier and Nathan. 2005. Features of
Promising Technologies for Pretreatment of Lignocellulosic Biomass. Bioresource Technology 96, pp. 673–686.
Murphy H. 1994. Pemanfaatan Kulit
Buah Pisang untuk Produksi Enzim
Selulase oleh Trichoderma viride,
Aspergillus niger dan Aspergillus
Oryzae. Institut Pertanian Bogor.
Bogor.
Purwoko,T. 2009. Fisiologi Mikroba. Bumi Aksara, Jakarta
Rahmanto, L,M., dan Ambarwati. 2011.
Pembuatan Bioetanol dari bagase dengan Hidrolisis Enzim, dan Fermentasi menggunakan
Saccaromyces Cerevisae dan Zymomonas Mobili Saccharomyces Jurusan Kimia, FMIPA Institut Teknologi Sepuluh Nopember. Surabaya.
44
MAJALAH BIAM Vol.11 No.2, Desember 2015, Hal 63-75
Retmonando. 2012. Pembuatan Bioetanol
dari Biji Kelor (Moringa oliefera Lamk) dengan Metode Fermentasi Ragi (Saccharomyces cerevisiae). Fakultas Keguruan dan Ilmu Pendidikan, Universitas Muhammadiyah Palembang, 34 hlm.
Sinuraya.E,A. 2014. Produksi substrat fermentasi bioetanol (biofuel) dari makroalga Eucheuma cottonii melalui hidrolisis menggunakan asam. Skripsi Teknologi Industri, Pertanian Fakultas Teknologi Pertanian, Universitas Gajah Mada.
Soegiarto, A., Sulistijo, W. S. Atmadja dan H. Mubarak. 1991. Rumput laut (algae). Manfaat, potensi, dan usaha budidaya. Lembaga OseanologiNasional – LIPI. Jakarta: 61 halaman.
Soeprijanto, Ratnaningsih, T., dan Prasetyaningrum I., 2004, Biokonversi Selulose dari Limbah Tongkol Jagung Menjadi Glukosa Menggunakan Jamur Aspergilus niger, Fakultas
Teknik Kimia Teknologi Industri, Institut Teknologi Sepuluh Nopember Surabaya
Sulistijo.1998. Pengaruh Salinitas Terhadap Pertumbuhan Zygote Rumput Laut Sargassum. Jour. Puslitbang Oseanologi-LIPI, Proceedings of the First Indonesian Seminar on Marine Biotechnology, Jakarta pp. 273-283.
Syamsu,K., R. Puspitasari., dan H. Roliadi. 2012. Penggunaan SelulosaMikrobial dari Nata De Cassava dan Sabut Kelapa Sebagai Pensubtitusi Selulosa Kayu Dalam Pembuatan Kertas. E-Jurnal AgroindustriIndonesia 1 (2): 118-124.
Victor. 2010. Pembuatan Bioetanol dariUbi Kayu (Manihot utilisima pohl)
dengan Jamur Aspergillus awamori dan Ragi Saccharomyces cerevisiae. Fakultas Farmasi, UniversitasSumatera Utara, Medan, 65 hlm.
Xiang. Y.Y, Qian. Lee, Par O. Pattersson, and W.T, Robert. 2003. Heterogeneous Aspects of Acid Hydrolysis of α-cellulase Applied. Biochemistry and Biotechnology. 107:1-3.
Yulianto, K., S. Wouthuyzen, Sulistijo dan D. Hindarti.2010. Percoban Produksi Alginat dengan Teknologi ’Meshsize Filtration’ dan Potensi Bahan Baku Sargassum duplicatum J. Agardh Serta Usaha Budidayanya.UPT Loka Pengembangan Kompetensi SDM Oseanografi Pulau
Pari, LIPI, Jakarta, 60 hlm.
45
Etanol dari Molasses. Jurusan Teknik
Kimia Universitas Diponegoro.
47
Cakra Kimia (Indonesian E-Journal of Applied Chemistry)
Volume 3, Nomor 12, Mei 2015
PEMBUATAN BIOETANOL DARI ALGA
Codium geppiorum
DAN PEMANFAATAN BATU KAPUR NUSA PENIDA TERAKTIVASI
UNTUK MENINGKATKAN KUALITAS BIOETANOL
I Wayan Karta1, Ni Made Puspawati2, Yenni Ciawi3
1
Magister Kimia Terapan, Program Pascasarja Universitas Udayana,
ABSTRAK: Penelitian ini bertujuan untuk mengetahui pengaruh variasi konsentrasi penambahan ragi tape dan waktu fermentasi terhadap kadar etanol dalam pembuatan bioetanol berbahan alga Codium geppiorum, dan pengaruh variasi suhu aktivasi dan massa batu kapur Nusa Penida dalam meningkatkan kadar etanol. Penelitian adalah True Experiment dengan Rancangan Acak Lengkap (RAL) pola faktorial 3 x 4 yang terdiri dari dua faktor. Kadar etanol diukur dengan Gas Chromatography Varian 3300 dan dianalisis dengan Anava dua jalur menggunakan software SPSS 17.0. Hasil penelitian pada kadar
etanol hasil fermentasi menunjukkan nilai Fhitung > Ftabel (38,212 > 2,51) dengan probabilitas 0,000 yang berarti adanya interaksi antara variasi konsentrasi ragi dan waktu fermentasi.
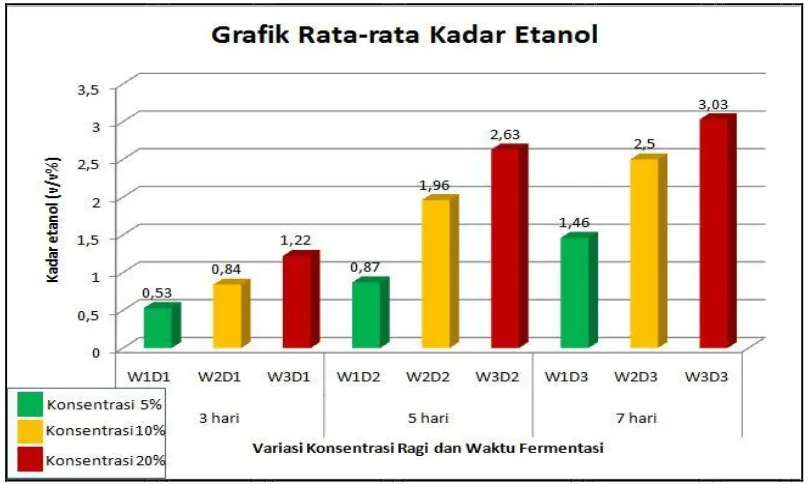
Perlakuan yang optimum diperoleh pada W3D3 (waktu 7 hari dan konsentrasi 20%) yaitu dengan rata-rata 3,03% dari massa sampel alga 25 gram. Hasil penelitian dehidrasi etanol
menunjukkan nilai Fhitung > Ftabel (3,082 > 2,51) dengan probabilitas 0,022 yang berarti terdapat interaksi antara suhu aktivasi dan massa batu kapur dalam dehidrasi etanol.
Perlakuan yang optimum adalah M1T1 (massa 50 gram dan suhu 800oC) dengan rata-rata kadar etanol 99,15 %. Aplikasi batu kapur dengan dehidrasi optimum mampu meningkatkan kadar bioetanol dari 28,92% menjadi 83,78%. Berdasarkan hasil penelitian disimpulkan bahwa variasi konsentrasi ragi tape dan waktu fermentasi berpengaruh signifikan terhadap kadar etanol yang dihasilkan pada pembuatan bioetanol berbahan alga Codium geppiorum; dan variasi suhu aktivasi dan massa batu kapur berpengaruh signifikan dalam meningkatkan kadar etanol.
48
ABSTRACT: The aims of this research are to determine the effect of the concentration ofyeast addition and length of fermentation on the amount of ethanol produced in the fermentation of algae Codium geppiorum and the effect of activation temperature and the amount of Nusa Penida’s limestone on the concentration of ethanol in the fermentation supernatant. The results showed that concerning the concentration of ethanol produced, Fvalue
6.Ftable with probability of 0.000 which means that there was interactions between yeast
concentration and duration of time of fermentation. The optimum result was obtained from W3D3 (7 day fermentation and 20% inoculum) by an average of ethanol concentration was 3.03% using 25 grams of algae sample. The results from the dehydration of ethanol showed that Fvalue > Ftable with a probability of 0.022 which means that there were interactions between activation temperature and amount of limestone used in the dehydration process.
49
Cakra Kimia (Indonesian E-Journal of Applied Chemistry) ISSN 2302-7274
Volume 3, Nomor 1, Mei 2015
that:concentration of yeast added and length of fermentation significantly affect the amount of ethanol produced the fermentation of Codium geppiorum and the activation temperature and the amount of limestone used in the dehydration process had significant effects on the increasing of ethanol concentration in the fermentation product.
Keywords: bioethanol, Codium geppiorum, dehydration, limestone, Saccharomyces
1. PENDAHULUAN
Bioetanol merupakan etanol yang terbuat dari hasil fermentasi tanaman yang mengandung karbohidrat dengan bantuan mikroorganisme. Bioetanol dikembangkan sebagai bahan bakar pengganti BBM dengan fuel grade ethanol ≥ 99,5 % untuk mengimbangi kelangkaan sumber minyak bumi. Bioetanol menjadi energi alternatif karena memiliki kandungan oksigen yang tinggi, bilangan oktan yang tinggi, mudah terurai, dan sumber energi diperbaharui. Kandungan oksigen yang tinggi akan meningkatkan efisiensi pembakaran dan mengurangi terjadinya pencemaran akibat gas buang seperti emisi hidrokarbon, karbon monoksida, dan emisi partikulat, ataupun gas-gas rumah kaca. Bioetanol memiliki bilangan oktan yang lebih tinggi dibandingkan dengan bensin sehingga dapat mengurangi terjadinya ketukan dan dapat menggantikan fungsi bahan aditif seperti metil tersier butil eter (MTBE) dan tetra etil timbale. Selain itu, bioetanol juga mempuyai batas sifat nyala yang lebih luas, kecepatan nyala yang lebih tinggi, dan kalor uap yang lebih tinggi dibandingkan dengan bensin. Hal ini akan memberikan perbandingan kompresi lebih tinggi, waktu bakar yang pendek dan bergantung pada pembakaran mesin [1].
Selama ini, sumber-sumber bahan bioetanol yang dimanfaatkan yaitu singkong, tebu, nira, sorgum, nira nipah, ubi jalar, dan lain-lain. Dalam penyediaannya, bahan baku tersebut memiliki kelemahan, yaitu penanamannya memerlukan lahan yang luas dan bioetanol yang diperoleh belum maksimal. Oleh karena itu, perlu upaya penggunaan bahan baku bioetanol alternatif, salah satunya dengan alga laut. Alga memiliki yield biomassa dan minyak yang tinggi, mampu dikembangkan secara luas, kurang berkompetisi dengan pertanian darat, menyerap CO2 dengan baik, cocok untuk pengolahan limbah, serta sebagai sumber energi terbarukan [2]. Pada penelitian ini digunakan jenis Codium geppiorum yang tersebar di kawasan Nusa Lembongan dengan kandungan karbohidrat 69,10% [3].
Proses pembuatan bioetanol meliputi perlakuan awal sampel, hidrolisis, fermentasi, dan pemurnian. Hidrolisis dapat dilakukan dengan penggunaan asam pekat, pelarutan dalam asam encer, atau dengan reaksi enzimatis [4]. Fermentasi sumber biomassa dilakukan dengan menambahkan mikroorganisme, dalam penelitian ini digunakan ragi tape jenis NKL. Mikroorganisme yang terdapat di dalam ragi tape adalah jenis kapang meliputi kapang Amylomyces rouxii, Mucor sp., dan Rhizopus sp.; khamir
Saccharomycopsis fibuligera,