LAPORAN PRAKTIKUM KIMIA FISIKA
PERCOBAAN II
KELRUTAN TIMBAL BALIK SISTEM BINER FENOL-AIR
Cahyo Fajar Handayani*, Aries Setyo Wibowo, Sasih Martiani Lab. Kimia Fisika Jurusan Kimia Universitas Negeri Semarang Gedung D8 Lt 2 Sekaran Gunungpati Semarang, Indonesia 50229[email protected] 085642158386
Abstrak
Sistem biner fenol – air merupakan sistem yang memperlihatkan sifat solubilitas timbal balik antara fenol dan air pada suhu tertentu dan tekanan tetap. Praktikum kelarutan timbale balik sistem biner fenol-air ini bertujuan untuk memperoleh kurva komposisi system fenol air terhadap suhu pada tekanan tetap dan untuk menentukan suhu kritis dari sitem tersebut. Metode yang dilakukan pada percobaan ini pada dasarnya adalah proses pemanasan dan pendinginan untuk memperoleh suhu kritis. Temperatur kritis adalah kenaikan temperatur tertentu dimana akan diperoleh komposisi larutan yang berada dalam kesetimbangan. Pada praktikum ini suhu kritis terjadi pada 66oC. sehingga kesimpulan dari praktikum ini adalah pada temperature/ suhu kritis, perubahan larutan dari keruh menjadi bening ataupun sebaliknya berlangsung pada rentang suhu yang berdekatan. Dalam percobaan ini, temperatur berbanding lurus dengan volume air yang digunakan. Pada suhu tersebut, persen massa fenol berbanding persen massa air adalah 50 banding 50. Massa fenol yang digunakan sebanyak 5 gram dan massa aquades yang digunakan 5 gram pula. Kata kunci: kelarutan; campuran; sollubilitas.
Abstract
Phenol binary system - a system that shows the water solubility properties of the tradeoffs between phenol and water at a certain temperature and pressure remain. Practicum reciprocal solubility of phenol-water binary system aims to obtain phenol-water system composition curve with respect to temperature at constant pressure and to determine the critical temperature of the sitem. The method used in this experiment is essentially a process of heating and cooling to obtain the critical temperature. Critical temperature is the temperature rise which would be obtained given the composition of the solution is in equilibrium. At this lab critical temperature occurs at 66oC. so the conclusion of this lab is the temperature / critical temperature, the solution changes from cloudy to clear, or vice versa takes place over a temperature range adjacent. In this experiment, the temperature is directly proportional to the volume of water used. At this temperature, mass percent phenol versus percent mass of water is 50 to 50. Mass of phenol is used as much as 5 grams and the mass 5 grams of distilled water used as well.
1. PENDAHULUAN 1.1 Latar Belakang
Kelarutan adalah kemampuan suatu zat kimia tertentu, zat terlarut (solute), untuk larut dalam suatu pelarut (solvent). Kelarutan dinyatakan dalam jumlah maksimum zat terlarut yang larut dalam suatu pelarut pada kesetimbangan. Larutan hasil disebut larutan jenuh. Zat-zat tertentu dapat larut dengan perbandingan apapun terhadap suatu pelarut. Contohnya adalah etanol di dalam air. Sistem biner fenol – air yang merupakan sistem yang memperlihatkan sifat solubilitas timbal balik antara fenol dan air pada suhu tertentu dan tekanan tetap. Sifat ini lebih dalam bahasa Inggris lebih tepatnya disebut miscible. Pelarut umumnya merupakan suatu cairan yang dapat berupa zat murni ataupun campuran (Darmaji, 2005).
1.2 Landasan Teori
Kelarutan timbal balik adalah kelarutan dari suatu larutan yang bercampur sebagian bila temperaturnya di bawah temperatur kritis. Jika mencapai temperatur kritis, maka larutan tersebut dapat bercampur sempurna (homogen) dan jika temperaturnya telah melewati temperatur kritis maka sistem larutan tersebut akan kembali dalam kondisi bercampur sebagian lagi. Salah satu contoh dari temperatur timbal balik adalah kelarutan fenol dalam air yang membentuk kurva parabola yang berdasarkan pada bertambahnya % fenol dalam setiap perubahan temperatur baik di bawah temperatur kritis (Sukardjo, 2003). Jika temperatur dari dalam kelarutan fenol aquadest dinaikkan di atas 50°C maka komposisi larutan dari sistem larutan tersebut akan berubah. Kandungan fenol dalam air untuk lapisan atas akan bertambah (lebih dari 11,8 %) dan kandungan fenol dari lapisan bawah akan berkurang (kurang dari 62,6 %). Pada saat suhu kelarutan mencapai 66°C maka komposisi sistem larutan tersebut menjadi seimbang dan keduanya dapat dicampur dengan sempurna.Temperatur kritis adalah kenaikan temperatur tertentu dimana akan diperoleh komposisi larutan yang berada dalam kesetimbangan. (Karyadi,2002).
Sistem biner fenol - air merupakan sistem yang memperlihatkan sifat kelarutan timbal balik antara fenol dan air pada suhu tertentu dan tekanan tetap. Disebut sistem biner karena jumlah komponen campuran terdiri dari dua zat yaitu fenol dan air. Fenol dan air kelarutanya akan berubah apabila dalam campuran itu ditambahan salah satu komponen penyusunnya yaitu fenol atau air. Jika komposisi campuran fenol air dilukiskan terhadap suhu akan diperoleh kurva sebagai berikut :
Gambar 1. Komposisi campuran fenol air
L1 adalah fenol dalam air, L2 adalah air dalam fenol, XA dan XF masing- masing adalah mol fraksi air dan mol fraksi fenol, XC adalah mol fraksi komponen pada suhu kritis (Tc). Sistem ini mempunyai suhu kritis (Tc) pada tekanan tetap, yaitu suhu minimum pada saat dua zat bercampur secara homogen dengan komposisi Cc. Pada suhu T1 dengan komposisi di antara A1 dan B1 atau pada suhu T2 dengan komposisi di antara A2 dan B2, sistem berada pada dua fase (keruh). Sedangkan di luar daerah kurva (atau diatas suhu kritisnya, Tc), sistem berada pada satu fase (jernih).
Temperatur kritis atas Tc adalah batas atas temperatur dimana nterjadi pemisahan fase.Diatas temperatur batas atas, kedua komponen benar-benar bercampur.Temperatur ini ada gerakan termal yang lebih besar menghasilkan kemampuan campur yang lebih besar pada kedua komponen, (Atkins PW, 1999).
1.3 Rumusan Masalah
1. Bagaimana cara memperoleh kurva komposisi sistem fenol-air terhadap suhu pada tekanan tetap?
2. Bagaimana cara menentukan suhu kritis kelarutan timbal balik sistem fenol-air.
1.4 Tujuan Praktikum
1. Memperoleh kurva komposisi sistem fenol-air terhadap suhu pada tekanan tetap. 2. Menentukan suhu kritis kelarutan timbal balik sistem fenol-air.
2. METODE 2.1 Alat
1. Tabung reaksi diameter 4 cm 1 buah
2. Pemanas 1 set
3. Pengaduk 1 buah
4. Gelas kimia 1 L 1 buah
5. Buret 50 mL 1 buah
6. Statif dan klem 1 buah
7. Termometer 1 buah
2.2 Bahan 1. Fenol 2. Aquades
2.3 Variabel Pengamatan - Variabel bebas : air - Variabel terikat : suhu
2.4 Cara Kerja
Langkah kerja yang pertama kali dilakukan adalah menimbang tabung reaksi (bersih dan kering). Kedua, tabung diisi dengan fenol sampai kira-kira massa fenol 5 gram.Ketiga, mengisi buret dengan aquades. Keempat, menyusun alat percobaan seperti gambar berikut :
Selanjutnya, menambahkan air melalui buret ke dalam tabung yang berisi fenol 1 ml atau sampai keruh. Kemudian memanaskan campuran dalam penangas (±90 ºC) sambil diaduk. Lalu mencatat suhu pada saat campuran berubah jernih (T1). Pemanasan diteruskan sampai
suhu menjadi (T1+4) ºC. Kemudian tabung dikeluarkan dan didinginkan. Suhu dicatat pada saat
campuran kembali keruh. Dan terakhir melalui buret ditambahkan lagi aquades 1 ml. Ulangi langkah tersebut. Percobaan dihentikan ketika volume aquades yang ditambahkan mencapai ±20 ml.
2.5 Cara Analisis Data
Menghitung Fraksi mol Fenol dan Fraksi mol Air
Massa Fenol = Kadar Fenol x massa fenol yang ditimbang Mr Fenol = 94 Mol Fenol = % massa fenol = x 100% Mr air = 18 Mol air = XAir = % massa fenol = x 100%
3 HASIL DAN PEMBAHASAN 3.1 Analisis Data
Pada percobaan ini kadar Fenol yang digunakan adalah 99.9% dan massa fenol yang ditimbang adalah 5.080 gram. Dari percobaan yang dilakukan diperoleh data pengamatan pada saat penambahan aquades, sampai terjadi kekeruhan pertama sebagai berikut :
Tabel 1. Penambahan aquades, sampai terjadi kekeruhan pertama
No. Aquades (ml) Pengamatan T1 T2 Trata-rata
1. 3.5 keruh 51 40 45.5
Dari table diatas dapat diketahui nilai dari % massa fenol dan %massa dari air pada saat penambahan aquades, sampai terjadi kekeruhan sebagai berikut :
% massa fenol =
x 100% = 59.2075% % massa air =
x 100% = 40.7925 %
Dari percobaan yang dilakukan juga diperoleh data pengamatan pada saat penambahan aquades, setelah terjadi kekeruhan sebagai berikut :
Tabel 2. Penambahan aquades, setelah terjadi kekeruhan
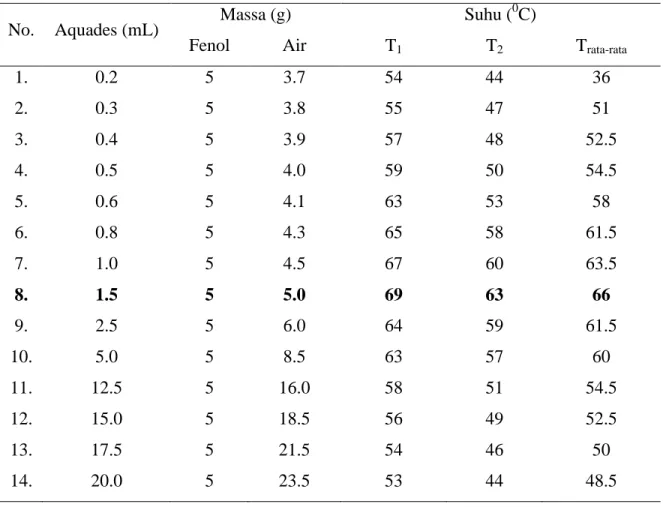
No. Aquades (mL) Massa (g) Suhu (
0 C)
Fenol Air T1 T2 Trata-rata
1. 0.2 5 3.7 54 44 36 2. 0.3 5 3.8 55 47 51 3. 0.4 5 3.9 57 48 52.5 4. 0.5 5 4.0 59 50 54.5 5. 0.6 5 4.1 63 53 58 6. 0.8 5 4.3 65 58 61.5 7. 1.0 5 4.5 67 60 63.5 8. 1.5 5 5.0 69 63 66 9. 2.5 5 6.0 64 59 61.5 10. 5.0 5 8.5 63 57 60 11. 12.5 5 16.0 58 51 54.5 12. 15.0 5 18.5 56 49 52.5 13. 17.5 5 21.5 54 46 50 14. 20.0 5 23.5 53 44 48.5
Dari table diatas dapat diketahui nilai dari % massa fenol dan % massa dari air pada saat penambahan aquades, setelah terjadi kekeruhan sebagai berikut :
Tabel 3. % massa fenol dan % massa dari air pada saat penambahan aquades, setelah terjadi kekeruhan
No. % massa fenol % massa air
1. x 100% = 57.47% x 100% = 42.53% 2. x 100% = 56.82% x 100% = 43.18% 3. x 100% = 56.18% x 100% = 43.82% 4. x 100% = 55.55% x 100% = 44.45% 5. x 100% = 54.94% x 100% = 45.06% 6. x 100% = 53.76% x 100% = 46.24% 7. x 100% = 52.63% x 100% = 47.37% 8. x 100% = 50.00% x 100% = 50.00% 9. x 100% = 45.45% x 100% = 54.55% 10. x 100% = 37.04% x 100% = 62.96% 11. x 100% = 23.81% x 100% = 76.19% 12. x 100% = 21.28% x 100% = 78.72% 13. x 100% = 19.23% x 100% = 80.77% 14. x 100% = 17.54% x 100% = 82.46%
Berikut ini merupakan perhitungan Fraksi mol Fenol dan Fraksi mol Air : Massa Fenol = 99.9 % x 5.080 = 5.0749 gram
Mr Fenol = 94 Mol Fenol = 0.054 mol Mr air = 18 1. Mol air = = 0.2056 XAir = 0.7921 2. Mol air = = 0.2111 XAir = 0.7962
3. Mol air = = 0.2167 XAir = 0.8006 4. Mol air = = 0.2222 XAir = 0.8044 5. Mol air = = 0.2278 XAir = 0.8084 6. Mol air = = 0.2389 XAir = 0.8157 7. Mol air = = 0.25 XAir = 0.8224 8. Mol air = = 0.2778 XAir = 0.8373 9. Mol air = = 0.3333 XAir = 0.8608 10. Mol air = = 0.4722 XAir = 0.8973 11. Mol air = = 0.8889 XAir = 0.9427 12. Mol air = = 1.0278 XAir = 0.9501 13. Mol air = = 1.1667 XAir = 0.9558 14. Mol air = = 1.3056 XAir = 0.9603
Dari data pengamatan dan hasil perhitungan diatas dapat diperoleh table hubungan antara suhu dengan fraksi mol air sebagai berikut :
Tabel 3. Hubungan Antara Suhu dengan Fraksi Mol Air
T (oC) Fraksi Mol Air T (oC) Fraksi Mol Air
36.0 0.7921 66.0 0.8373 51.0 0.7962 61.5 0.8608 52.5 0.8006 60.0 0.8973 54.5 0.8044 54.5 0.9427 58.0 0.8084 52.5 0.9501 61.5 0.8157 50.0 0.9558 63.5 0.8224 48.5 0.9603
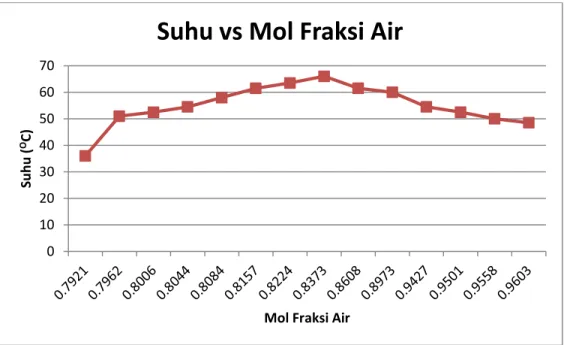
Dari data table 3 diatas dapat diperoleh grafik hubungan antara suhu dengan fraksi mol air sebagai berikut :
Gambar 1. Kurva komposisi fenol air hasil percobaan
3.2 Pembahasan
Tujuan dari percobaan ini yaitu untuk menetapkan (mencari) suhu kelarutan kritis (titik konsulat) system biner air- phenol. Pada percobaan ini dilakukan beberapa perbandingan empat belas perbandingan yaitu 5 : 3.7; 5 : 3.8; 5 : 3.9; 5 : 4.0; 5 : 4.1; 5 : 4.3; 5 : 4.5; 5 :
5.0; 5 : 6.0; 5 : 8.5; 5 : 16.0; 5 : 18.5; 5 : 21.5; 5 : 23.5. Dari perbandingan tersebut kita
dapat menentukan titik kritis (titik konsulat) dari system biner air-phenol. Temperatur kritis atas (Tc) adalah batas atas temperatur dimana nterjadi pemisahan fase. Diatas temperatur batas atas, kedua komponen benar- benar bercampur. Pada temperatur ini ada gerakan termal yang lebih besar, menghasilkan kemampuan campur yang lebih besar pada kedua komponen.
Tabung yang berisi air dan fenol dengan perbandingan yang telah ditentukan, dipanaskan sampai kedua zat tersebut bercampur atau membentuk system satu fasa yang ditandai dengan perubahan campuran dari keruh menjadi jernih. Dalam proses pemanasan campuran dilakukan pengocokan yang dimaksudkan untuk mencampurkan secara sempurna antara air dan phenol. Ketika dilakukan pengocokan tidak terbentuk campuran keruh dan tidak terbentuk dua lapisan, pemanasan dihentikan dan dicatat suhunya sebagai suhu dimana terbentuk system satu fasa. Ketika campuran kembali keruh suhunya juga dicatat sebagai suhu dimana terbentuk kembali system dua fase atau air dan phenol kembali tidak bercampur.
0 10 20 30 40 50 60 70 Su h u ( OC)
Mol Fraksi Air
Dalam percobaan ini, diperoleh larutan yang tidak saling bercampur, yang membentuk dua lapisan , lapisan atas air dan lapisan bawah adalah fenol, hal ini di sebabkan karena air memiliki massa jenis yang lebih rendah dari pada fenol. Setelah terjadi percampuran antara air dan fenol dalam tabung yang berbeda dengan perbandingan kompsisi yang berbeda pula, di lakukan pemanasan yang menyebabkan larutan menjadi bening yang sebelumnya keruh karena penambahan aquades kemudian dilakukan pendinginan yang menyebabkan larutan menjadi keruh kembali. Larutan keruh ini akan berubah kembali menjadi jernih (ketika dipanaskan) dan sebaliknya larutan jernih akan keruh kembali (ketika didinginkan). Hal ini menandakan kalau zat mengalami perubahan kelarutan yang dipengaruhi oleh perubahan suhu.
Pada percobaan ini komponen air selalu ditambahkan dan jumlah fenolnya tetap sehingga perubahan larutan dari jernih menjadi keruh atau sebaliknya terjadi pada suhu yang berubah-ubah. Perubahan suhu bergantung pada komposisi atau fraksi mol kedua zat. Kelarutan Fenol dan air akan berubah apabila ke dalam campuran itu ditambahkan dengan salah satu komponen penyusunnya.
Beradasarkan data percobaan, dapat dibuat grafik sistem biner fenol – air, yaitu antara fraksi mol vs suhu (T). Grafik ini berbentuk parabola dimana puncaknya merupakan suhu kritis (Tc) yang dicapai pada saat komponen mempunyai fraksi mol tertentu. Suhu kritis dalam percobaan ini adalah 66ºC dengan komposisi campurannya adalah fraksi mol fenol 0.1627 dan fraksi mol airnya 0.8373.
Grafik parabola yang diperoleh berdasarkan data percobaan sesuai dengan teori. Hal ini dibuktikan dengan naiknya temperature yang dihasilkan ketika ke dalam fenol ditambahkan air dengan volume yang berbeda. Semakin banyak volume air yang ditambahkan, semakin tinggi pula temperaturnya.
4. KESIMPULAN DAN SARAN 4.1 Simpulan
Dari hasil pembahasan dapat disimpulkan bahwa keadaan dimana terjadinya perubahan warna dari keruh menjadi jernih dan sebaliknya merupakan contoh kelarutan timbal balik. Dapat disimpulakan pula bahwa dalam percobaan ini, temperatur berbanding lurus dengan volume air yang digunakan. Serta dapat dismpulkan bahwa suhu kritis dalam percobaan kelarutan timbal balik sistem biner fenol-air yaitu 66oC dengan fraksi mol airnya 0.8373.
4.2 Saran
Sebelum melakukan percobaan, sebaiknya praktikan hendaknya melakukan persiapan secara matang dan juga saat melaksanakan percobaan, praktikan sebaiknya lebih teliti dalam melakukan pengamatan. Serta praktikan harus lebih hati-hati selama percobaan berlangsung, karena zat yang digunakan adalah fenol yang apabila terkena kulit dapat menyebabkan luka
5. DAFTAR PUSTAKA
Atkins PW. 1999. Kimia Fisika. “Ed ke-2 Kartahadiprodjo Irma I, penerjemah;Indarto Purnomo Wahyu, editor. Jakarta : Erlangga. Terjemahan dari:Physichal Chemistry. Castellan GW. 1982. Physichal Chemistry. Third Edition. NewYork : General Graphic
Services.
Darmaji.2005.Kimia Fisika I.Jambi : Universitas Jambi.
Karyadi.1990.Kimia Fisika II.Jakarta : Bumi Pustaka. Sutrisno.1999.Kimia Fisika untuk Mahasiswa.Malang : Universitas Brawijaya.
Sukarjo.1997. Kimia Fisika. Jakarta : Rineka Cipta.
Tim Dosen Kimia Fisik. 2013. Diktat Petunjuk Praktikum Kimia Fisik. Semarang : Jurusan Kimia FMIPA UNNES
Semarang, 19 November 2013 Mengetahui,
Dosen Pengampu Praktikan
Ir. Sri Wahyuni, M.Si Cahyo Fajar Handayani
JAWABAN PERTANYAAN
a. Tugas
1. Fenol mempunyai rumus kimia C6H6O dengan nilai Mr = 94. Rumus strukturnya sebagai berikut.
2. Jumlah mol fenol:
Massa fenol = 5,140 100 95 4,883 gram. Mol fenol = 94 883 , 4 Mr m 0,052 mol
3. Fase adalah bagian serba sama dari suatu zat yang dapat dipisahkan secara mekanik serta serba sama dalam sifat fisika dan kimia, sedangkan wujud merupakan bentuk zat pada suhu tertentu. Zat pada suhu yang berbeda mungkin mempunyai wujud yang berbeda. Misal air pada suhu -10ºC wujudnya padat, sedangkan pada suhu 10ºC wujudnya cair.
b. Pertanyaan
1. Komposisi campuran fenol dan air :
Massa fenol = 5g Fraksi mol fenol = 0,107
Massa air = 19 g Fraksi mol air = 0,893 Komposisi campuran dalam %
Fenol = 100 19 5 5 % = 20,8 % Air =5 19 100 19 % = 79,2 %
2. Komposisi campuran fenol air :
Komposisi campuran pada suhu 50ºC (diambil dari Trata2 = 54,5ºC) XF = 0,107
XA = 0,893
Sistem berada dalam 2 fase pada suhu di atas 64,5ºC. Sistem berada dalam 2 fase pada suhu di bawah 64,5ºC.