SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Lilis Dumaria Pasaribu NIM : 078114111
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Lilis Dumaria Pasaribu NIM : 078114111
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
Karya ini kupersembahkan kepada:
Tuhan Yesus Kristus,
Papa, Mama, Ka David, Hana dan Angel
yang selalu menyayangiku dan memberiku semangat,
sahabat-sahabat dan almamaterku.
God will make a way
When there seems to be no way
He works in way we cannot see
He will make a way for me
He will be my guide
Hold me closely to His side
With love and strength for each new day
He will make a way
vii
skripsi yang berjudul “Penetapan Kadar Kurkumin dalam Sedian Kapsul Lunak
Obat Herbal Terstandar Merk Rheumakur yang Beredar di Pasaran dengan Metode Kromatografi Lapis Tipis – Densitometri”. Skripsi ini disusun sebagai salah satu syarat untuk meraih gelar Sarjana Farmasi (S.Farm) di Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Pada kesempatan ini, penulis mengucapkan terima kasih atas bantuan yang diberikan baik secara moril maupun materiil kepada:
1. Ipang Djunarko, S.Si., Apt., M.Sc selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
2. Christine Patramurti, M.Si., Apt. selaku dosen pembimbing akademik dan dosen pembimbing yang dengan sabar memberikan pengarahan, masukan, kritik dan saran baik selama penelitian maupun penyusunan skripsi ini. 3. Yohanes Dwiatmaka, M.Si., selaku dosen penguji yang telah memberikan
masukan dan saran yang membangun.
4. Jeffry Julianus, M.Si. selaku dosen penguji yang telah memberikan kritik dan saran dalam penyusunan skripsi.
5. Prof. Dr. Sudibyo Martono, M.S., Apt., selaku dosen pengajar yang telah membantu memberikan senyawa baku kurkumin dalam penelitian ini. 6. Semua dosen-dosen yang telah memberikan ilmu selama penulis
viii
8. Theresia Kosasih dan Andreas Suseno selaku teman seperjuangan selama penelitian dan penyusunan skripsi.
9. Sahabat terbaikku, Veny Megawati Tambunan, Yemima Septiany Puraja, dan Agnes Anania yang selalu mendukung dalam doa dan semangat. 10.Teman-teman komsel dan pelayanan, Apo, Dhika, Ka Iva, Sanny, Irma,
Ka Sabrina, Ka Maria, Ka Mega, Ka Nina, Ka Jafet, dan Bu Susan yang selalu mengerti dan mendukung dalam doa.
11.Lala, Katiti, Toro, Benny, Dian, Katarina, Eliz, Yuyun selaku teman yang melakukan penelitian dalam satu tema yang sama, terima kasih atas dukungannya.
12.Teman-teman seperjuangan, khususnya Lia, Dinar, Fifi, dan Aji atas dukungannya.
13.Teman-teman FST angkatan 2007 dan teman KKN angkatan XL, atas pengalaman, kebersamaan dan kekompakan selama ini.
x
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
PERNYATAAN PERSETUJUAN PUBLIKASI ... vi
PRAKATA ... vii
B. Tujuan Penelitian ... 4
BAB II PENELAAHAN PUSTAKA... 5
xi
E. Obat Herbal Terstandar... 12
F. Rheumakur ... 13
G. Standarisasi Ekstrak ... 14
H. Cara Pembuatan Obat yang Baik ... 15
1. Personalia ... 15
9. Penanganan terhadap hasil pengamatan produk diperedaran ... 18
I. Kromatografi Lapis Tipis ... 19
J. Densitometri ... 24
K. Teknik Statistik Analisis Komparatif ... 26
L. Landasan Teori ... 27
M. Hipotesis ... 28
BAB III METODE PENELITIAN... 29
xii
3. Variabel pengacau terkendali ... 29
C. Definisi Operasional ... 29
1. Obat herbal terstandar ... 29
2. Kadar kurkumin ... 30
3. Kromatografi lapis tipis ... 30
D. Bahan ... 30
E. Alat ... 30
F. Tata Cara Penelitian ... 31
1. Pemilihan dan pengambilan sampel ... 31
2. Pembuatan metanol pH 4 ... 31
3. Pembuatan fase gerak ... 31
4. Penetapan panjang gelombang serapan maksimum ... 32
5. Pembuatan kurva baku kurkumin ... 32
6. Optimasi metode ekstraksi kurkumin dalam sampel Rheumakur ... 33
7. Penetapan kadar ... 34
G. Analisis Hasil ... 35
BAB IV HASIL DAN PEMBAHASAN ... 36
A. Pemilihan Sampel ... 36
B. Pembuatan Metanol pH 4 ... 39
xiii
2. Menggunakan ultrasonikator ... 46
F. Penetapan Kadar Kurkumin ... 50
BAB V KESIMPULAN DAN SARAN ... 55
A. Kesimpulan ... 55
B. Saran ... 55
DAFTAR PUSTAKA ... 56
LAMPIRAN ... 60
xiv
Tabel 2. Data pengukuran panjang gelombang serapan maksimum kurkumin ... 40
Tabel 3. Data kurva baku kurkumin ... 42
Tabel 4. Hasil pengukuran AUC sampel pada variasi waktu menggunakan magnetic stirer ... 46
Tabel 5. Hasil pengukuran AUC sampel pada variasi waktu menggunakan ultrasonikator ... 49
Tabel 6. Replikasi pengukuran AUC sampel pada waktu 15 menit menggunakan ultrasonikator ... 50
Tabel 7. Kadar kurkumin dalam setiap apotek pada sampel Rheumakur ... 51
Tabel 8. Nilai normalitas data apotek 1, 2, dan 3 ... 53
Tabel 9. Nilai varian apotek 1, 2, dan 3 ... 53
Tabel 10. Nilai uji statistik one way Anova apotek 1, 2, dan 3 ... 53
xv
Gambar 3. Bisdesmetoksikurkumin ... 7
Gambar 4. Struktur kurkumin ... 8
Gambar 5. Produk degradasi kurkumin pada pH alkali ... 9
Gambar 6. Produk fotodegradasi kurkumin ... 10
Gambar 7. Logo obat herbal terstandar ... 12
Gambar 8. Ilustrasi resolusi pada KLT: : (a) kromatogram; (b) profil kromatografi masing-masing bercak ... 23
Gambar 9. Gugus metilen aktif kurkumin. ... 39
Gambar 10. Gugus kromofor dan auksokrom pada struktur kurkumin ... 40
Gambar 11. Kromatogram panjang gelombang maksimum baku kurkumin ... 41
Gambar 12. Grafik hubungan antara konsentrasi kurkumin dengan AUC/50 (replikasi I) ... 42
Gambar 13. Perbandingan kromatogram baku dan kromatogram ekstraksi sampel menggunakan magnetic stirrer ... 45
xvi
Lampiran 2. Hasil uji pH stabilitas kurkumin ... 62
Lampiran 3. Hasil kromatogram pengukuran panjang gelombang serapan maksimum ... 63
Lampiran 4. Sistem KLT-Densitometri yang digunakan ... 64
Lampiran 5. Hasil uji keseragaman bobot... 66
Lampiran 6. Contoh perhitungan kadar kukumin ... 68
Lampiran 7. Data kurva baku kurkumin dan kromatogram baku kurkumin... 69
Lampiran 8. Kromatogram ekstraksi sampel menggunakan magnetic stirrer ... 70
Lampiran 9. Data perhitungan kadar sampel menggunakan magnetic stirrer ... 72
Lampiran 10. Kromatogram ekstraksi sampel menggunakan ultrasonikator... 73
Lampiran 11. Data perhitungan kadar sampel menggunakan ultrasonikator ... 75
Lampiran 12. Kromatogram replikasi ekstraksi sampel menggunakan ultrasonikator ... 76
Lampiran 13. Data perhitungan replikasi AUC sampel menggunakan ultrasonikator ... 78
Lampiran 14. Kromatogram penetapan kadar kurkumin dalam Rheumakur ... 79
Lampiran 15. Data perhitungan kadar kurkumin apotek 1, 2, dan 3 ... 85
xvii
terhadap perubahan pH dan cahaya. Sehingga perlu dilakukan penetapan kadar untuk mengetahui stabilitas kadar kurkumin selama distribusi dan penyimpanan.
Metode penetapan kadar pada penelitian ini menggunakan KLT – densitometri dengan sistem normal dan fase diam silika gel G60 serta fase gerak kloroform : asam asetat glasial : heksana (8,5 : 1,0 :0,5) yang diukur pada 425 nm. Analisis penetapan kadar kurkumin dalam Rheumakur® menggunakan nomor batch yang sama yang berasal dari 3 apotek yang berbeda.
Hasil penelitian yang didapat yaitu kadar rata-rata kurkumin dalam Rheumakur® untuk setiap apotek adalah apotek 1 yaitu 2,11316% (b/b), apotek 2 yaitu 2,06497% (b/b), dan apotek 3 sebesar 2,00917% (b/b). Kadar kurkumin dari ketiga apotek ini masuk dalam kadar kurkumin yang tertera pada label yaitu 1,785-2,142% b/b. Nilai CV antar apotek yaitu 2,35937%. Hal ini dapat disimpulkan kadar kurkumin pada setiap apotek tidak reprodusibel.
xviii
light. Determination necessarty to know the stability of curcumin content during distribution and storage.
Curcumin content determination method performed by TLC-Densitometry. TLC-Densitometry system used is a normal system with mobile phase chloroform: glacial acetic acid: hexane (8,5: 1,0: 0,5) v/v and stationary phase silica gel G 60 that was measured at 425 nm. Analytical determination of curcumin in Rheumakur using the same batch number derived from three different pharmacies.
Research results in to the average levels of curcumin in Rheumakur for each pharmacy is 2,11316% (b/b), 2,06497% (b/b), and 2,00917% (b/b). Curcumin content of the three pharmacies are included in the levels of curcumin are indicated on the label of 1,785-2,142% b/b. CV values among pharmacies is 2,35937%. It can be concluded levels of curcumin in every pharmacy is not reproducible.
BAB I PENGANTAR
A. Latar Belakang Masalah
Saat ini penggunaan bahan alam sebagai obat mengalami peningkatan. Selain harganya terjangkau, penggunaan obat tradisional dipercaya lebih aman karena memiliki efek samping yang tidak merugikan dibandingkan dengan penggunaan obat sintesis. Sehingga BPOM meningkatkan mutu obat tradisional melalui standarisasi bahan baku dan uji praklinik menjadi produk Obat Herbal Terstandar (OHT) (Kementerian Kesehatan Republik Indonesia, 1994).
Menurut BPOM (2005) pembuatan OHT harus mengikuti pedoman Cara Pembuatan Obat Tradisional yang Baik (CPOTB) sehingga dapat memenuhi persyaratan mutu. CPOTB yang dilakukan meliputi seluruh aspek yang menyangkut pembuatan obat tradisional.
Salah satu tanaman yang sering digunakan untuk bahan obat tradisional adalah Kunyit (Curcuma domestica Val) (Sumiati, 2010). Karena dalam kunyit terdapat senyawa aktif yang berkhasiat sebagai analgesik-antiinflamasi yaitu kurkumin.
Rheumakur® merupakan salah satu produk OHT dengan bentuk sediaan kapsul lunak yang dikeluarkan oleh PT Phytochemindo. Rheumakur® mengandung ekstrak yang setara dengan kurkuminoid 10 mg dan minyak atsiri dari ekstrak kunyit dan temulawak sebanyak 100 mg, sehingga kandungan kurkumin dengan rentang 1,785-2,142% b/b. Kurkumin memiliki stabilitas yang
rendah terhadap pH, suhu, serta cahaya (Kurnia, 2010). Hal ini akan berpengaruh terhadap stabilitas kurkumin dalam Rheumakur® yang mungkin terjadi selama proses distribusi dan penyimpanan. Perubahan stabilitas kurkumin yang terjadi untuk setiap tempat distribusi berbeda-beda tergantung dari kondisi penyimpanan. Adanya perubahan stabilitas kurkumin yang terjadi memungkinkan terjadi perubahan kadar sehingga akan mempengaruhi terhadap besarnya efek farmakologis yang dihasilkan. Untuk itu, perlu dilakukan penjaminan mutu terhadap stabilitas kurkumin dengan menetapkan kadar kurkumin dalam Rheumakur® dan melihat reprodusibilitas kadar dalam Rheumakur® yang berasal dari apotek yang berbeda dengan nomor batch yang sama.
Penelitian ini merupakan tahap akhir yang meliputi tahap optimasi, validasi, dan aplikasi. Dimana metode yang digunakan telah dioptimasi dan divalidasi terlebih dahulu. Metode yang digunakan pada penelitian ini yaitu kromatografi lapis tipis (KLT) – densitometri. Analisis dengan kromatografi lapis tipis sering digunakan karena prosedurnya sederhana, pemisahan cepat dan baik (Stahl, 1969). Dimana kadar kurkumin dapat ditetapkan menggunakan densitometer, setelah sampel dipisahkan menggunakan KLT terlebih dahulu. Reprodusibilitas kadar dalam kapsul lunak OHT merk Rheumakur® dapat dilihat
dari nilai CV, menurut Harmita (2004) nilai CV yang baik jika £ 2. 1. Permasalahan
b. Apakah terdapat perbedaan kadar kurkumin dalam sediaan kapsul lunak OHT merk Rheumakur® antar apotek dengan nomor batch yang sama?
2. Keaslian penelitian
Sejauh yang diketahui penulis penelitian mengenai penetapan kadar kurkumin dalam sediaan kapsul lunak OHT dengan metode kromatografi lapis tipis (KLT) – densitometri belum pernah dilakukan sebelumnya.
Penelitian yang pernah dilakukan yang berkaitan dengan penelitian ini yaitu penetapan kadar kurkumin secara kromatografi lapis tipis-densitometri (Martono, 1996), Occurance of curcuminoids in Curcuma longa: A quality standarization by HPTLC (M. Paramasivam dkk, 2008), penetapan kadar kurkumin dalam sediaan obat menggunakan kromatografi cair kinerja tinggi (KCKT) (Musfiroh dkk, 2010), dan penetapan kadar kurkumin dan piperin secara simultan dalam produk pangan dengan metode kromatografi cair untuk menggunakan diode array detection (Nagappan dkk, 2009).
3. Manfaat penelitian
a.Manfaat metodologis. Penelitian ini diharapkan mampu menambah pengetahuan dan informasi dalam bidang kefarmasian mengenai penetapan kadar kurkumin menggunakan metode KLT – densitometri.
B. Tujuan
1. Mengetahui kadar kurkumin yang terdapat dalam sediaan kapsul lunak OHT merk Rheumakur® yang beredar di pasaran.
BAB II
PENELAAHAN PUSTAKA
A. Kunyit
Gambar 1. Kunyit
Tanaman kunyit tumbuh dengan tinggi 40-100 cm. Batang merupakan batang semu, tegak, bulat, membentuk rimpang dengan warna hijau kekuningan dan tersusun dari pelepah daun (agak lunak). Daun tunggal, bentuk bulat telur (lanset) memanjang hingga 10-40 cm, lebar 8-12,5 cm dan pertulangan menyirip dengan warna hijau pucat. Berbunga majemuk yang berambut dan bersisik dari pucuk batang semu, panjang 10-15 cm dengan mahkota sekitar 3 cm dan lebar 1,5 cm, berwarna putih/kekuningan. Ujung dan pangkal daun runcing, tepi daun yang rata. Kulit luar rimpang berwarna jingga kecoklatan, daging buah merah jingga kekuning-kuningan (Shafwatunnida, 2009).
Kunyit mengandung senyawa yang berkhasiat obat, yang disebut kurkuminoid. Kandungan kurkuminoid yaitu kurkumin, demetoksikurkumin, bisdemetoksikurkumin, sisanya minyak asiri (keton sesquiterpen, turmeron, tumeon, zingiberen, felandren, sabinen, borneol, dan sineil), lemak, karbohidrat,
protein, pati, vitamin C, garam-garam mineral (zat besi, fosfor, dan kalsium) (Shafwatunnida, 2009).
Bagian yang sering dimanfaatkan adalah rimpangnya. Penggunaannya biasanya sebagai jamu karena berkhasiat menyejukkan, membersihkan, mengeringkan, menghilangkan gatal, dan menyembuhkan kesemutan. Disamping itu rimpang tanaman kunyit itu juga bermanfaat sebagai anti inflamasi, anti oksidan, anti mikroba, anti diabetes, pencegah kanker, anti tumor, mengobati tifus, usus buntu, disentri, memperlancar asi, dan menurunkan kadar lemak darah dan kolesterol, serta sebagai pembersih darah (Shafwatunnida, 2009).
Pemerian rimpang kunyit yaitu, bau khas aromatik; rasa agak pahit, agak pedas, lama kelamaan menimbulkan rasa tebal. Kadar minyak atsiri tidak kurang dari 3 % v/b (Direktorat Jenderal POM, 1995).
Ekstrak kental rimpang kunyit adalah ekstrak yang dibuat dari rimpang tumbuhan Curcuma domestica Val., mengandung minyak atsiri ≥ 3,2% dan
kurkuminoid ≥ 33,9% (Badan Pengawas Obat dan Makanan, 2004). Kandungan
dari ekstrak rimpang kunyit antara lain kurkuminoid, minyak atsiri, lemak 1 -3 %, karbohidrat 3%, protein 30%, pati 8%, vitamin C 45-55%, dan garam-garam mineral (Rukmana, 1994).
B. Kurkuminoid
merupakan komponen terbesar. Sering kadar total kurkuminoid dihitung sebagai % kurkumin, karena kandungan kurkumin paling besar dibanding komponen kurkuminoid lainnya (Sumiati, 2010).
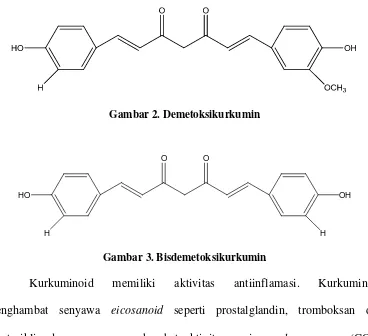
Gambar 2. Demetoksikurkumin
OH
H HO
H
O O
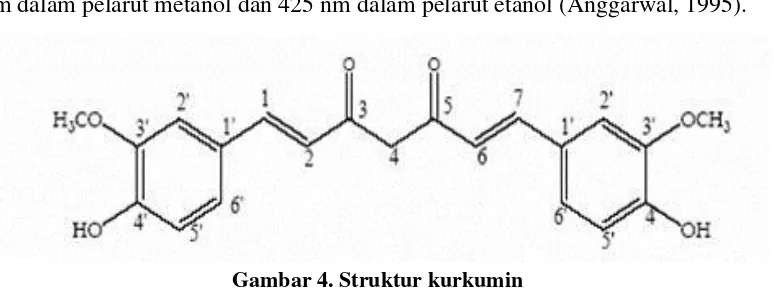
Gambar 3. Bisdemetoksikurkumin
Kurkuminoid memiliki aktivitas antiinflamasi. Kurkuminoid menghambat senyawa eicosanoid seperti prostalglandin, tromboksan dan prostasiklin dengan cara menghambat aktivitas enzim cyclooxygenase (COX) (Kohli, 2005).
C. Kurkumin
(Tonnesen & Karlsen, 1983). Kurkumin tidak larut dalam air dan eter, larut dalam etil asetat, metanol, etanol, benzena, asam asetat glasial, aseton, dan alkali hidroksida. Kurkumin memiliki panjang gelombang serapan maksimum pada 430 nm dalam pelarut metanol dan 425 nm dalam pelarut etanol (Anggarwal, 1995).
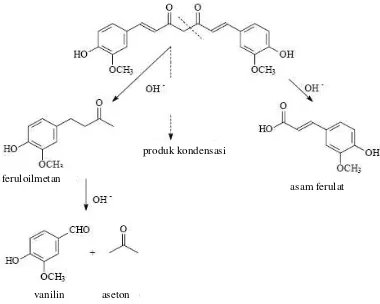
Gambar 4. Struktur kurkumin
Kurkumin merupakan senyawa yang peka terhadap lingkungan terutama karena pengaruh pH dan suhu serta cahaya. Sifat kurkumin yaitu dapat terjadi perubahan warna akibat perubahan pH lingkungan. Dalam suasana asam kurkumin berwarna kuning atau kuning jingga, sedangkan dalam suasana basa berwarna merah. Untuk mendapatkan stabilitas yang optimum dari sediaan kurkumin maka pH nya dipertahankan kurang dari 7 (Kurnia, 2010).
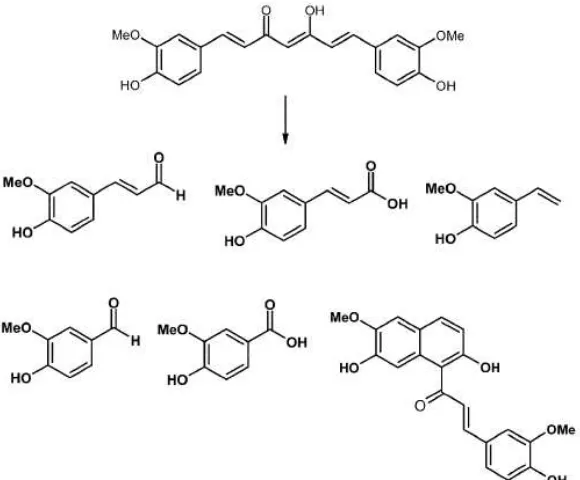
Dalam larutan berair dengan pH basa kurkumin mengalami reaksi degradasi yang disebabkan oleh adanya gugus metilen aktif pada senyawa tersebut menjadi asam ferulat, feruloilmetan, dan vanilin. Degradasi ini terjadi bila kurkumin berada dalam lingkungan pH 8,5 – 10,00 dalam waktu yang relatif lama (Tonnesen dan Karlsen, 1985a).
adalah vanilin dan aseton serta jumlahnya meningkat seiring bertambahnya waktu (Stankovic, 2004).
Gambar 5. Produk degradasi kurkumin pada pH alkali
Penelitian lain (Wang dkk, 1997) kurkumin diinkubasi pada 0,1 M buffer fosfat; pH 7,2 pada 37 ºC; dan sejumlah 90% terdekomposisi tidak kurang dari 30 menit. Vanilin, asam ferulat, dan feruloilmetan diidentifikasi sebagai produk degradasi minor. Pada bentuk netral, kurkumin tidak stabil pada larutan berair dengan pH >7 (Stankovic, 2004).
Selain pH lingkungan, kurkumin memiliki stabilitas yang rendah terhadap cahaya. Bila kurkumin terkena cahaya, akan terjadi dekomposisi struktur berupa degradasi fotokimia senyawa tersebut. Prinsipnya, kurkumin tidak stabil terhadap cahaya terutama dalam bentuk larutan. Produk fotodegradasi kurkumin
aseton vanilin
asam ferulat produk kondensasi
misalnya adalah asam vanilat, vanilin dan asam ferulat (Sasaki, Sat, Abe, Sugimoto, Maitani, 1998).
Gambar 6. Poduk fotodegradasi kurkumin (Tonnesen and Greenhill, 1992)
D. Kapsul
Menurut Keputusan Menteri Kesehatan Republik Indonesia Nomor 661/MENKES/SK/VII/1994 tentang persyaratan obat tradisional definisi kapsul adalah sediaan obat tradisional yang terbungkus cangkang keras atau lunak; bahan bakunya terbuat dari sediaan galenik dengan atau tanpa bahan tambahan.
terhadap 9 kapsul dan hitung bobot isi rata-rata 10 kapsul (Kementrian Kesehatan Republik Indonesia, 1994).
Kapsul lunak adalah bentuk sediaan padat dosis tunggal yang terdiri dari cairan atau semi padat yang tertutup rapat dengan bagian luar bersifat elastis (Podczeck dan Jones, 2004).
Kapsul cangkang lunak yang dibuat dari gelatin (kadang-kadang disebut gel lunak) atau bahan lain yang sesuai membutuhkan metode produksi skala besar. Cangkang gelatin lunak sedikit lebih tebal dibanding kapsul cangkang keras dan dapat diplastisasi dengan penambahan senyawa poliol, seperti sorbitol atau gliserin. Komposisi cangkang dapat mengandung pigmen atau pewarna yang diizinkan, bahan opak seperti titanium dioksida, dan pengawet.
Cangkang gelatin lunak umumnya mengandung 6% - 13% air. Umumnya kapsul cangkang lunak diisi dengan cairan. Khususnya bahan aktif dilarutkan atau disuspensikan dalam bahan pembawa cair. Dahulu digunakan bahan pembawa minyak seperti minyak nabati. Keunggulan kapsul cangkang lunak adalah keseragaman kandungan dan disolusi obatnya lebih baik daripada kapsul berisi serbuk kering. Namun, kontak antara cangkang lunak atau keras dengan isi zat cair lebih besar dibandingkan kapsul berisi serbuk kering (Direktorat Jenderal POM RI, 1995).
untuk mencegah pengendapan padatan dan menjaga homogenitas dalam kapsul. Agen pensuspensi yang banyak digunakan dengan basis minyak adalah wax, contohnya adalah beeswax, sedangkan polietilen glikol untuk basis tidak berminyak (Naguib, 2000).
E. Obat Herbal Terstandar
Obat tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan galenik atau campuran dan bahan-bahan tersebut yang secara tradisional telah digunakan untuk pengobatan berdasarkan pengalaman (Kementerian Kesehatan Republik Indonesia, 1990).
Obat tradisional merupakan produk yang dibuat dari bahan alam yang jenis dan sifat kandungannya sangat beragam sehingga untuk menjamin mutu obat tradisional diperlukan cara pembuatan yang baik dengan lebih memperhatikan proses produksi dan penanganan bahan baku. Mutu produk tergantung dari bahan awal, proses produksi dan pengawasan mutu, bangunan, peralatan dan personalia yang menangani (Kementerian Kesehatan Republik Indonesia, 1990).
Gambar 7. Logo obat herbal terstandar
F. Rheumakur
Rheumakur merupakan obat herbal terstandar yang dikeluarkan oleh PT Phytochemindo dengan bentuk sediaan kapsul lunak. Tiap kapsul mengandung ekstrak terstandarisasi kurkuminoid sebanyak 10 mg dan minyak atsiri kunyit dan temulawak 100 mg. Berdasarkan hasil penelitian farmakologi dan kimia membuktikan bahwa:
1. Minyak atsiri Curcuma xanthorrhiza (Temulawak) mengandung komponen utama xanthorrizol dan curcumene yang memiliki aktivitas anti inflamasi. 2. Minyak atsiri Curcuma domesticae (kunyit) juga terbukti mengandung
komponen utama tumeron dan tumerol yang juga memiliki aktivitas kerja antiinflamasi yang lebih cepat.
3. Dengan adanya kurkuminoid daya anti inflamasi minyak atsiri curcuma xanthorrhiza dan curcuma domesticae, akan diperkuat dan diperpanjang. 4. Selain itu kombinasi kurkuminoid dan minyak atsiri kunyit, temulawak juga
membantu melarutkan lemak sehingga dapat mencegah peradangan yang disebabkan oleh peroksidasi lemak (Anonim, 2011).
Rheumakur digunakan satu kapsul lunak 3 kali sehari sesudah makan untuk pengobatan dan satu kapsul lunak satu kali sehari untuk pencegahan serangan ulang rheumatik (Anonim, 2011).
sebagai kholagoga sehingga Rheumakur dapat mencegah terjadinya peradangan yang disebabkan oleh peroksidasi lemak (Anonim, 2010).
G. Standarisasi Ekstrak
Ekstrak adalah sediaan kental yang diperoleh dengan mengekstraksi senyawa aktif dari simplisia nabati atau simplisia hewani dengan menggunakan pelarut yang sesuai. Ekstrak tumbuhan obat yang dibuat dari simplisia nabati dapat digunakan sebagai bahan awal, bahan antara, atau bahan produk jadi (Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
Terpenuhinya standar mutu produk atau bahan ekstrak tidak terlepas dari pengendalian proses, artinya bahwa proses yang terstandar dapat menjamin produk yang terstandar tanpa penerapan pengujian atau pemeriksaan. Untuk menjaga kualitas bahan baku obat alam perlu dilakukan usaha budidaya dan standarisasi terhadap bahan baku tersebut, baik yang berupa simplisia maupun yang berbentuk ekstrak atau sediaan galenik (Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
Persyaratan mutu ekstrak terdiri dari berbagai parameter standar umum dan parameter standar spesifik. Pengertian standardisasi juga berarti proses menjamin bahwa produk akhir mempunyai nilai parameter tertentu yang konstan dan ditetapkan terlebih dahulu (Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
H. Cara Pembuatan Obat Tradisional yang Baik
Cara Pembuatan Obat Tradisional yang Baik (CPOTB) meliputi seluruh aspek yang menyangkut pembuatan obat tradisional, yang bertujuan untuk menjamin agar produk yang dihasilkan senantiasa memenuhi persyaratan yang berlaku. Landasan umum dari CPOTB ini yaitu obat tradisional diperlukan masyarakat untuk memelihara kesehatan, untuk mengobati gangguan kesehatan dan untuk memulihkan kesehatan; dilakukan langkah-langkah agar obat tradisional yang dihasilkan aman, bermanfaat, dan bermutu; keamanan dan mutu obat tradisional tergantung pada bahan baku, bangunan, prosedur dan pelaksanaan proses pembuatan, peralatan yang digunakan, pengemas termasuk bahannya serta personalia yang terlibat dalam pembuatan obat tradisional; dan CPOTB merupakan cara pembuatan obat tradisional yang diikuti dengan pengawasan menyeluruh, dan bertujuan untuk menyediakan obat tradisional yang memenuhi persyaratan berlaku (Kementrian Kesehatan Republik Indonesia, 1994).
Penerapan CPOTB merupakan persyaratan kelayakan dasar untuk menerapkan sistem jaminan mutu yang diakui dunia internasional. Untuk itu sistem mutu hendaklah dibangun, dimantapkan, dan diterapkan sehingga kebijakan yang ditetapkan dan tujuan yang diinginkan dapat dicapai (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
1. Personalia
menangani tugas yang dibebankan kepadanya (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
Semua personil yang langsung terlibat dalam kegiatan pembuatan hendaklah dilatih dalam pelaksanaan pembuatan sesuai dengan prinsip-prinsip CPOTB. Pelatihan CPOTB hendaklah dilakukan secara berkelanjutan. Catatan hasil pelatihan hendaklah dipelihara, dan keefektifannya hendaklah dievaluasi secara periodik (Kepala BPOM Republik Indonesia, 2005).
2. Bangunan
Bangunan industri obat tradisional hendaklah menjamin aktifitas industri agar dapat berlangsung aman (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
3. Peralatan
Peralatan yang digunakan dalam pembuatan produk hendaklah memiliki rancang bangun konstruksi yang tepat, ukuran yang memadai serta ditempatkan dengan tepat, sehingga mutu yang dirancang bagi tiap produk terjamin secara seragam dari bets ke bets, serta untuk memudahkan pembersihan dan perawatannya.
4. Sanitasi dan higiene
Dalam pembuatan produk hendaklah diterapkan tindakan sanitasi dan higiene yang meliputi bangunan, peralatan dan perlengkapan, personalia, bahan dan wadah serta faktor lain sebagai pencemaran produk (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
5. Pengolahan dan pengemasan
Pengolahan dan pengemasan hendaklah dilaksanakan dengan mengikuti cara yang telah ditetapkan oleh industri sehingga dapat menjamin produk yang dihasilkan senantiasa memenuhi persyaratan yang berlaku.
Hal-hal yang termasuk dalam pengolahan dan pengemasan yaitu verifikasi, pencemaran, sistem penomoran kode produksi, penimbangan dan penyerahan, pengolahan, pengemasan, dan penyimpanan (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
6. Pengawasan mutu
Pengawasan mutu merupakan bagian yang essensial dari CPOTB. Rasa ketertarikan dan tanggung jawab semua unsur dalam semua rangkaian pembuatan adalah mutlak untuk menghasilkan produk yang bermutu mulai dari bahan awal sampai pada produk jadi. Untuk keperluan tersebut bagian pengawasan mutu hendaklah merupakan bagian yang tersendiri (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
7. Inspeksi diri
Program inspeksi diri hendaklah dirancang untuk mengevaluasi pelaksanaan CPOTB dan untuk menetapkan tindak lanjut. Inspeksi diri ini hendaklah dilakukan secara teratur. Tindakan perbaikan yang disarankan hendaklah dilaksanakan. Untuk pelaksanaan inspeksi diri hendaklah ditunjuk tim inspeksi yang mampu menilai secara obyektif pelaksanaan CPOTB. Hendaklah dibuat prosedur dan catatan mengenai inspeksi diri (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
8. Dokumentasi
Dokumentasi pembuatan produk merupakan bagian dari sistem informasi manajemen yang meliputi spesifikasi, label/etiket, prosedur, metoda dan instruksi, catatan dan laporan serta jenis dokumentasi lain yang diperlukan dalam perencanaan, pelaksanaan, pengendalian serta evaluasi seluruh rangkaian kegiatan pembuatan produk. Dokumentasi sangat penting untuk memastikan bahwa setidap petugas mendapat instruksi secara rinci dan jelas mengenai bidang tugas yang harus dilaksanakannya, sehingga memperkecil risiko terjadinya salah tafsir dan kekeliruan yang biasanya timbul karena hanya mengandalkan komunikasi lisan (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
9. Penanganan terhadap hasil pengamatan produk diperedaran
Penarikan kembali produk yang berupa penarikan kembali satu atau beberapa bets atau seluruh produk tertentu dari semua mata rantai distribusi. Penarikan kembali dilakukan apabila ditemukan adanya produk yang tidak memenuhi persyaratan atau atas dasar pertimbangan adanya efek yang tidak diperhitungkan yang merugikan kesehatan. Penarikan kembali seluruh produk tertentu dapat merupakan tindak lanjut penghentian pembuatan satu jenis produk yang bersangkutan (Kepala Badan Pengawas Obat dan Makanan Republik Indonesia, 2005).
I. Kromatografi Lapis Tipis (KLT)
Kromatografi digunakan untuk memisahkan substansi campuran menjadi komponen-komponennya. Seluruh bentuk kromatografi bekerja berdasarkan prinsip ini.
Semua kromatografi memiliki fase diam dan fase gerak. Fase gerak mengalir melalui fase diam dan membawa komponen-komponen yang terdapat dalam campuran. Komponen-komponen yang berbeda bergerak pada laju yang berbeda (Clark, 2007).
Kromatografi lapis tipis adalah pemisahan fisikokimi. Di berbagai jenis teknik kromatografi, kromatografi lapis tipis adalah yang paling cocok untuk analisis obat di laboratorium farmasi, karena metodenya sederhana, cepat dalam pemisahan, sensitif, kecepatan pemisahan tinggi dan mudah untuk memperoleh kembali senyawa-senyawa yang dipisahkan dan memerlukan jumlah cuplikan yang sangat sedikit (Khopkar, 1990).
Dalam pemisahan suatu senyawa harus dipilih fase diam, fase gerak, dan cara kerja yang sesuai. Pemisahan yang lebih baik dapat diperoleh dengan mengadakan perubahan-perubahan pada fase diam, fase gerak, dan cara kerja yang antara lain meliputi kejenuhan, temperatur dalam bejana kromatografi, cara pengembangan dan keadaan permukaan (Stahl, 1969).
Fase diam yang umum dan banyak digunakan adalah silika gel yang dicampur dengan CaSO4 untuk menambah daya lengket partikel silika gel pada pendukung (pelat kaca, logam, atau plastik) dengan ketebalan 0,25 mm. Adsorban lain yang banyak dipakai adalah alumina, kieselguhr, celite, serbuk sellulose, serbuk poliamida, kanji dan sephadex. Beberapa hal yang perlu diperhatikan pada pembuatan fase diam yaitu bahwa ukuran partikel dibuat pada rentang kehalusan 1- 25 mikro dalam keadaan seragam. Keadaan seragam fase diam ini bertujuan untuk didapatnya pemisahan yang baik, laju aliran pelarut pengembangan yang cepat dan merata. Lapisan tipis silika gel atau adsorban yang lainnya dapat dibuat sendiri atau sudah dalam bentuk jadi yang dikenal sebagai pre coated plate
Fase gerak adalah suatu medium angkat yang terdiri atas satu atau beberapa pelarut. Yang digunakan adalah pelarut bertingkat mutu analitik dan bila diperlukan sistem pelarut multikomponen, maka harus berupa suatu campuran sesederhana mungkin terdiri atas maksimum tiga komponen. Pada kromatografi serap, pelarut pengembang ke dalam deret elutropik berdasar efek elusinya. Efek elusi naik dengan kenaikan kepolaran pelarut. Sedangkan laju rambat bergantung pada viskositas pelarut dan struktur lapisan (Stahl, 1985). Disamping kelarutan relatif zat terlarut dalam fase gerak, perlu dipertimbangkan pula persaingan antara zat terlarut dengan pelarut terhadap bidang adsorbsi pada permukaan fase diam. Pelarut yang mengelusi terlalu cepat tidak akan dapat memisahkan dengan baik, sebaliknya pelarut yang bergerak terlalu lambat akan memberikan waktu elusi yang terlalu panjang.
Pemilihan fase gerak untuk KLT tergantung pada polaritas pelarut tersebut. Pelarut yang memiliki polaritas tinggi akan mengubah kromatografi menjadi kromatografi pembagian, disamping itu pelarut tersebut dapat mempermudah lepas atau rusaknya lapisan tipis (Stahl, 1969).
Kromatogram pada pelat KLT akan tampak setelah visualisasi secara fisika atau kimia. Noda kromatogram tiap-tiap komponen yang terpisah setelah visualisasi akan tampak sebagai noda yang bulat apabila terjadi pemisahan yang baik. Jika pemisahan kurang sempurna maka terjadi pengekoran noda kromatogram yang digambarkan dengan noda yang tidak bulat (berekor).
pada chamber KLT sehingga fase gerak yang mengelusi pelat KLT segera menguap dalam chamber KLT, dan ketidaktepatan pemilihan fase gerak terhadap jenis fase diam dan macam sampel yang dianalisis.
Oleh sebab itu, pada pelaksanaannya ada beberapa hal yang perlu diperhatikan seperti aktivitas fase diam pada pelat dimana pelat KLT yang akan digunakan dipanaskan terlebih dahulu pada suhu 105 – 110o C selama 60 menit. Penjenuhan chamber yang digunakan dengan melapisi sekeliling dinding chamber
dengan kertas saring. Chamber yang telah jenuh ditandai dengan basahnya kertas saring pelapis dinding chamber oleh fase gerak. Selain itu, penotolan larutan sampel pada pelat KLT dilakukan dengan pipet mikro atau jarum mikro pada tempat lebih kurang 2,5 cm dari dasar, dengan diameter penotolan seminimal mungkin. Selama proses elusi temperatur ruangan juga harus dijaga sebab kenaikan temperatur ruangan akan sangat berpengaruh pada nilai Rf (Mulja, 1995).
Identifikasi senyawa-senyawa yang terpisah pada lapisan tipis lebih baik dikerjakan dengan pereaksi warna, tetapi lazimnya untuk identifikasi menggunakan harga Rf (Hardjono, 1985). Harga Rf merupakan parameter karakteristik KLT. Harga Rf didefinisikan sebagai perbandingan antara jarak senyawa dari titik awal dan jarak tepi muka pelarut dari titik awal (Roth, 1994). Angka Rf berjangka antara 0,00 sampai 1,00 dan hanya dapat ditentukan dua desimal (Stahl, 1985).
HRf = Rf x 100 (Mulja, 1995). Harga Rf ini adalah tetapan fisika yang dipengaruhi oleh beberapa faktor, seperti : tebal lapisan, kejenuhan bejana, kelembaban udara, fase gerak, bahan penjerap, dan suhu (Sastroamidjojo, 1985).
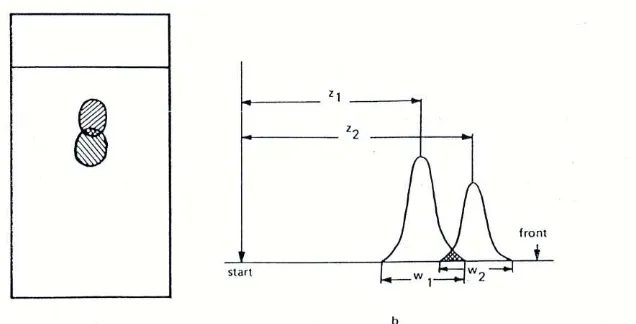
Resolusi didefinisikan sebagai perbedaan antara waktu retensi 2 puncak yang saling berdekatan (Δz = z2 – z1) dibagi dengan rata-rata lebar puncak (W1 + W2)/2 sebagaimana dalam ilustrasi dan persamaan berikut ini:
Gambar 8. Ilustrasi resolusi pada KLT: (a) kromatogram; (b) profil kromatografi masing-masing bercak
(Sherma dan Fried, 1996). Nilai Rs harus mendekati atau lebih dari 1,5 karena akan memberikan pemisahan puncak yang baik (base line resolution).
Aplikasi KLT sangat luas, yaitu untuk senyawa yang tidak mudah menguap serta terlalu kecil untuk kromatografi cair dapat dianalisis dengan KLT,
dapat pula untuk pemeriksaan kemurnian (adanya zat pengotor dalam pelarut). Pemakaiannya juga meluas untuk pemisahan anorganik (Khopkar, 1990).
J. Densitometri
Densitometri adalah metode analisis instrumental yang berdasarkan interaksi radiasi elektromagnetik dengan analit yang merupakan noda pada KLT. Densitometri lebih dititikberatkan untuk analisis kuantitatif analit-analit dengan kadar yang sangat kecil yang perlu dilakukan pemisahan terlebih dahulu dengan KLT (Mulja, 1995).
Penetapan kadar suatu senyawa dengan metode ini dilakukan dengan mengukur kerapatan bercak senyawa yang dipisahkan dengan cara KLT. Pada umumnya pengukuran kerapatan bercak tersebut dibandingkan dengan kerapatan bercak senyawa standar yang dielusi bersama-sama (Hardjono, 1985).
Metode densitometri mempunyai cara kerja yang sederhana dan cepat. Pada metode densitometri diperlukan adsorbens dan fase gerak yang murni (Gritter, 1991).
Penentuan kadar analit yang dilakukan dengan area noda pada KLT akan lebih terjamin kesasihannya dibanding metode KCKT atau KGC, sebab area noda kromatogram diukur pada posisi diam atau zig-zag menyeluruh. Korelasi kadar analit pada noda kromatogram yang dirajah terhadap area tidak menunjukkan garis lurus akan tetapi garis lengkung mendekati parabola (Mulja, 1995).
Teknik pengukuran dapat didasarkan atas pengukuran intensitas sinar yang diserap (absorbansi), intensitas sinar yang dipantulkan (reflaktansi), atau intensitas sinar yang difluorosensikan (fluorosensi). Teknik pengukuran berdasarkan refleksi dimana sinar datang sebagian diserap dan sebagian lagi dipantulkan. Sifat pemantulan ini akan menjadi sensitif dan selektif bila sinar yang datang adalah monokromatis. Disini biasanya dipilih sinar pada panjang gelombang yang diserap atau dipantulkan paling banyak oleh noda yang diteliti. Banyaknya sinar yang direfleksikan akan ditangkap oleh suatu alat yang disebut
reflection photomultiplier yang akan diteruskan ke pencatat atau rekorder untuk diubah menjadi suatu puncak atau kromatogram. Luas puncak atau tinggi puncak sesuai dengan konsentrasi senyawa pada noda yang diukur kerapatannya (Mintarsih, 1990).
Penelusuran bercak akan mendapatkan hasil yang baik apabila dilakukan pada panjang gelombang maksimum, karena perubahan konsentrasi pada bercak sedikit saja sudah terdeteksi. Pengukuran dilakukan dengan menulusuri bercak yang akan ditetapkan kadarnya pada kisaran panjang gelombang zat tersebut.
Pelat yang digunakan untuk KLT pada densitometri sebaiknya digunakan pelat buatan pabrik, karena pada pelat buatan sendiri fase diamnya kurang rata, sehingga akan mempengaruhi hasil penulusuran dengan densitometri, yaitu berupa puncak yang lebar karena kurang kompaknya fase diam dan puncak yang kasar karena permukaan pelat yang kurang rata (Mintarsih, 1990).
K. Teknik Statistik Analisis Komparatif
Analisis komparatif adalah bentuk analisis variabel (data) untuk mengetahui perbedaan di antara dua kelompok data (variabel) atau lebih. Teknik statistik yang digunakan dalam analisis komparatif ini adalah uji statistik, yaitu pengujian hipotesis komparatif (Hasan, 2004).
Uji hipotesis komparatif variabel numerik berdistribusi normal dua kelompok digunakan uji post hoc (Dahlan, 2009).
Untuk data interval atau data rasio berkorelasi yang terdiri dari k sampel (lebih dari dua sampel), analisis komparatifnya menggunakan uji one way Anova
dan two way Anova (Hasan, 2004).
1. Memeriksa syarat Anova untuk > 2 kelompok tidak berpasangan yaitu data harus normal (wajib) dan varians data harus sama (wajib).
2. Jika memenuhi syarat maka dipilih uji one way Anova.
3. Jika tidak maka dilakukan transformasi supaya distribusi data normal dan varians sama.
4. Jika varibel hasil transformasi tidak berdistribusi normal atau varians tidak sama maka dipilih uji Kruskal Wallis.
5. Jika pada uji anova atau uji Kruskal Wallis menghasilkan nilai p < 0,05, maka dilanjutkan dengan analisis post hoc (Dahlan, 2009).
Two way Anova merupakan pengujian hipotesis komparatif untuk k sampel (lebih dari dua sampel) yang berpengaruh dengan dua factor yang berpengaruh (Hasan, 2004).
L. Landasan Teori
Kurkumin merupakan senyawa aktif yang terdapat dalam kunyit yang berfungsi sebagai anti inflamasi, antioksidan, dan analgesik. Kurkumin memiliki stabilitas yang rendah terhadap pengaruh pH dan cahaya.
Obat herbal terstandar merupakan obat tradisional yang disajikan dari ekstrak atau penyarian bahan alam yang telah distandarisasi bahan bakunya dan telah diuji praklinik. Rheumakur merupakan salah satu OHT yang pembuatannya mengikuti panduan CPOTB sehingga ada penjaminan mutu selama proses produksi. Dan produk yang dihasilkan memiliki reprodusibilitas yang baik.
dalam pemisahan, sensitif, kecepatan pemisahan tinggi, dan memerlukan jumlah cuplikan yang sangat sedikit. Densitometri merupakan metode analisis KLT kuantitatif dengan mengukur kerapatan bercak senyawa yang sudah dipisahkan terlebih dahulu dengan KLT.
Teknik statistik analisis komparatif merupakan uji statistik untuk menguji hipotesis dari analisis komparatif. Analisis komparatif merupakan bentuk analisis variabel untuk mengetahui perbedaan di antara dua kelompok variabel atau lebih.
M. Hipotesis
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian non eksperimental deskriptif karena tidak dilakukan intervensi terhadap subyek uji.
B. Variabel Penelitian 1. Variabel bebas
Variabel bebas dalam penelitian ini adalah tempat pengambilan sampel sediaan padat OHT merk Rheumakur® dan metode ekstraksi sampel.
2. Varibel tergantung
Variabel tergantung pada penelitian ini adalah kadar dan reprodusibilitas kadar dalam sediaan padat OHT merk Rheumakur®.
3. Variabel pengacau terkendali
Variabel pengacau terkendali pada penelitian ini adalah, paparan cahaya, suhu dan kelembaban lingkungan.
C. Definisi Operasional 1. Obat herbal terstandar
Obat herbal terstandar (OHT) yang digunakan yaitu Rheumakur® dalam sediaan kapsul lunak.
2. Kadar kurkumin
Kadar kurkumin dalam kapsul lunak OHT merk Rheumakur® dinyatakan dalam % b/b.
3. Kromatografi lapis tipis
Kromatografi lapis tipis (KLT) yang digunakan yaitu fase normal dengan fase diam silika gel G 60 (E. Merck) dan fase gerak kloroform : asam asetat glasial : heksana (8,5 : 1,0 : 0,5) v/v.
D. Bahan
ekstraksi, magnetik stirer (Hotplate stirer Lab Tech Model LMS-1003, VOHS=220 V 50 Hz, Waats=500 W 3 A, Serial No. 08210004), ultrasonikator
Retsch tipe T460 (Schwing.1 PXE, FTZ-Nr. C-066/83 HF-Frequ. : 35 kHz),
sentrifuge, dan bejana kromatografi.
F. Tata Cara Penelitian 1. Pemilihan dan pengambilan sampel
Sampel yang dipilih adalah kapsul obat herbal terstandar merk perbandingan 9:1 untuk setiap pembuatan larutan.
3. Pembuatan fase gerak
4. Penetapan panjang gelombang serapan maksimum
Lebih kurang 10,0 mg baku kurkumin ditimbang seksama, dilarutkan dalam metanol pH 4 , kemudian dimasukkan ke dalam labu takar dan diencerkan dengan metanol pH 4 hingga 10,0 mL (larutan induk 1000 ppm). Larutan induk diencerkan dengan metanol pH 4 hingga diperoleh seri larutan baku yang mengandung kurkumin 100; 300; dan 500 ppm. Pembuatan larutan baku direplikasi 3 kali. Semua larutan baku harus terlindung dari cahaya.
Seri larutan baku ditotolkan sebanyak 1,0 mL pada lempeng silika gel G
60 kemudian segera dikembangkan dalam bejana kromatografi yang telah dijenuhkan dengan campuran kloroform:asam asetat glasial:heksana (8,5:1,0:0,5) v/v. Pengembangan dilakukan setinggi 10 cm. Lempeng silika gel G 60 segera dikeluarkan dan dikeringkan setelah pengembangan selesai.
Bercak seri larutan baku yang mengandung kurkumin 100; 300; dan 500 ppm diukur dengan densitometer pada panjang gelombang 400-500 nm. Panjang gelombang maksimum ditentukan berdasarkan serapan maksimum yang dihasilkan oleh bercak tersebut.
5. Pembuatan kurva baku kurkumin
Seri Larutan baku kurkumin dengan kadar 100; 180; 260; 340; 420; dan
500 ppm ditotolkan sebanyak 1,0 mL pada lempeng silika gel G 60 yang sebelumnya sudah dipanaskan, kemudian segera dikembangkan dalam bejana kromatografi yang telah dijenuhi dengan fase gerak. Pengembangan dilakukan setinggi 10 cm. Lempeng silika gel G 60 segera dikeluarkan dan dikeringkan setelah pengembangan selesai.
Bercak seri larutan baku kurkumin diukur AUC-nya dengan densitometer pada panjang gelombang maksimum yang telah diperoleh. Puncak kromatogram dan nilai AUC yang muncul diamati. Dengan metode regresi linear, nilai konsentrasi (ppm) diplotkan terhadap nilai AUC masing-masing seri larutan baku sehingga diperoleh persamaan y = bx + a dimana y merupakan nilai respon (AUC), x merupakan konsentrasi senyawa baku (ppm), a adalah intersept, dan b adalah slope. Pembuatan kurva baku direplikasi sebanyak 3 kali.
6. Optimasi metode ekstraksi kurkumin dalam sampel Rheumakur®
b.Menggunakan ultrasonikator. Satu kapsul lunak diambil isinya kemudian ditimbang secara seksama lebih kurang 65,0 mg Rheumakur® sebanyak 4 kali dan tambahkan metanol pH 4 4,5 mL. Setiap larutan disari menggunakan ultrasonikator masing-masing selama 10; 15; 20; dan 25 menit. Kemudian tambahkan metanol pH 4 hingga 5,0 mL. Semua larutan harus terlindung dari cahaya. Filtrat yang dihasilkan dikembangkan pada hasil sistem optimasi sesuai dengan proses kerja pada nomor 5.
7. Penetapan kadar
Masing-masing kapsul lunak dari setiap apotek diambil sebanyak 20, dikeluarkan isinya dan kemudian dihomogenkan ditimbang dengan seksama lebih kurang 65,0 mg. Larutkan dengan menambahkan 4,5 mL metanol pH 4 dan disari menggunakan ultrasonikator selama 15 menit. Kemudian diencerkan dengan methanol pH 4 hingga 5,0 mL. Sampel setiap apotek direplikasi lima kali dan semua larutan harus terlindung dari cahaya.
Sebanyak 1,0 mL larutan sampel ditotolkan pada lempeng silika gel G 60,
kemudian segera dikembangkan dalam bejana kromatografi yang telah dijenuhkan dengan fase gerak hasil optimasi. Pengembangan dilakukan setinggi 10 cm. Segera keluarkan lempeng silika gel, dikeringkan dan secepatnya discanning
G. Analisis Hasil
Hasil dari penetapan kadar kurkumin dalam kapsul lunak obat herbal terstandar merk Rheumakur® dapat dihitung berdasarkan kromatogram yang memiliki nilai Rf yang sama dengan Rf kurkumin standar menggunakan persamaan regresi linear dari kurkumin standar sehingga didapat kadar kurkumin dalam % (b/b).
Parameter yang digunakan untuk melihat reprodusibilitas kadar dalam sediaan padat OHT merk Rheumakur® yaitu dari nilai CV. Nilai CV yang baik
jika £ 2 dan dapat dihitung dengan cara sebagai berikut:
CV = 100%
x SD
Untuk mendukung analisis reprodusibilitas dilakukan uji statistik terhadap kadar yang didapat dari setiap apotek untuk melihat apakah kadar dalam kapsul lunak OHT merk Rheumakur® berbeda bermakna atau tidak. Rumusan hipotesis sementara adalah sebagai berikut:
a. Tidak terdapat perbedaan kadar kurkumin antara apotek 1 dan apotek 2. b. Tidak terdapat perbedaan kadar kurkumin antara apotek 2 dan apotek 3. c. Tidak terdapat perbedaan kadar kurkumin antara apotek 1 dan apotek 3. d. Tidak terdapat perbedaan kadar kurkumin antara apotek 1, apotek 2, dan
apotek 3.
BAB IV
HASIL DAN PEMBAHASAN
Penetapan kadar kurkumin dalam sediaan kapsul lunak Rheumakur® dapat dianalisis menggunakan metode kromatografi lapis tipis (KLT) – densitometri karena metode yang digunakan telah dioptimasi dan validasi pada awal penelitian.
Pada tahap optimasi metode diperoleh komposisi fase gerak yang optimum agar dapat memisahkan sampel Rheumakur® dengan baik. Fase gerak yang digunakan yaitu kloroform : heksan : asam asetat glasial (8,5:0,5:1,0) dengan nilai indeks polaritas 4,11, nilai As baku dan sampel 0,95-1,10, nilai Rf berada dalam range 0,2-0,8, nilai resolusi yang didapat 2,45. Selain itu, telah dilakukan penentuan pH optimum agar kurkumin tetap stabil yaitu pada pH 4. Penentuan pH ini dilakukan dengan mengukur panjang gelombang serapan maksimum baku kurkumin dengan metode spektrofotometri visibel (Kosasih, 2011).
Pada tahap validasi metode diperoleh bahwa metode KLT - densitometri memenuhi persyaratan validitas yaitu akurasi yang baik pada konsentrasi 260-500 ppm, presisi yang baik pada konsentrasi 260-500 ppm, linearitas dan spesifisitas yang baik, serta range antara 260-500 ppm (Suseno, 2011).
A. Pemilihan Sampel
Tujuan penelitian ini adalah untuk mengetahui stabilitas dari zat aktif sampel yang digunakan yaitu kurkumin selama distribusi dan penyimpanan.
Sampel yang digunakan diambil dari tiga apotek berbeda dengan nomor batch yang sama.
Sampel yang digunakan adalah sediaan kapsul lunak obat herbal terstandar (OHT) merk Rheumakur®. Rheumakur® merupakan salah satu produk OHT yang pembuatannya berdasarkan CPOTB. Komposisi pada sampel Rheumakur® ini yaitu berupa kurkuminoid (yang merupakan komponen aktif dari
Curcuma domestica dan minyak atsiri Curcuma domestica dan Curcuma xanthorriza).
Teknik pengambilan sampel yang digunakan adalah probability sample
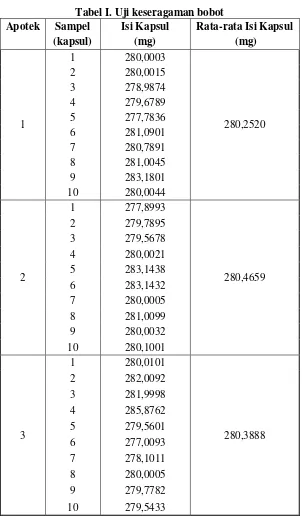
TabelI. Uji keseragaman bobot
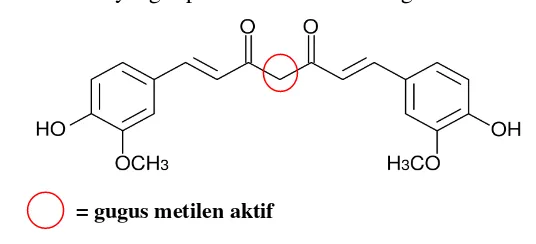
menyimpang dari bobot isi rata-rata lebih besar dari 7,5 % dan tidak satu kapsulpun yang bobot isinya menyimpang dari bobot isi rata-rata lebih besar dari 15 %. Dan tabel di atas menunjukkan Rheumakur® sudah memenuhi syarat Berdasarkan hasil orientasi, kurkumin stabil pada pH 4 dan tidak stabil pada pH basa, karena dapat terdegradasi pada gugus metilen aktifnya. Apabila kurkumin terdegradasi, maka kadar yang diperoleh akan berkurang.
= gugus metilen aktif
Gambar 9. Gugus metilen aktif kurkumin
Metanol pH 4 dengan penambahan asam asetat glasial p.a. dengan perbandingan (90:10). Metanol memiliki pH 5 sedangkan asam asetat glasial p.a.
memiliki pH 2 sehingga asam asetat glasial p.a dapat menurunkan pH metanol.
C. Penetapan Panjang Gelombang Serapan Maksimum
bercak di scan dengan alat densitometer. Hal ini bertujuan agar dapat memberikan respon yang lebih sensitif dan stabil, sehingga kesalahan yang terjadi pada pengukuran relatif lebih kecil.
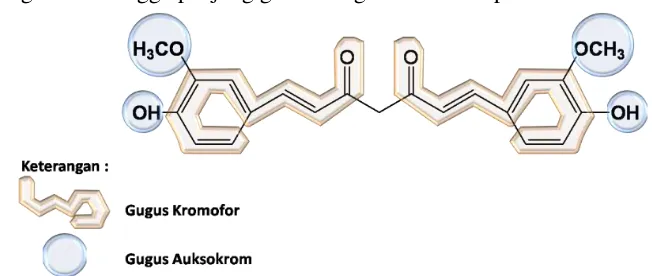
Senyawa kurkumin dapat dianalisis panjang gelombang karena memiliki gugus kromofor dan auksokrom. Gugus ini akan menyerap sinar radiasi elektromagnetik sehingga panjang gelombang kurkumin dapat diukur.
Gambar 10. Gugus kromofor dan auksokrom pada struktur kurkumin
Tabel II. Data pengukuran panjang gelombang serapan maksimum kurkumin Replikasi Baku 100 ppm Baku 300 ppm Baku 600 ppm
I 425 nm 425 nm 425 nm
II 425 nm 425 nm 425 nm
III 425 nm 425 nm 425 nm
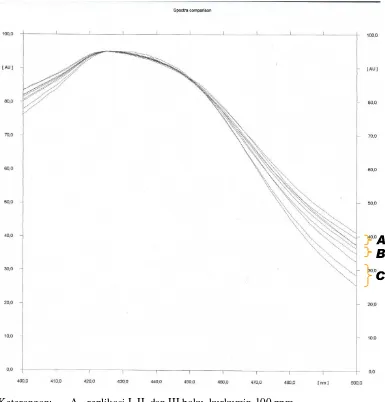
Keterangan: A= replikasi I, II, dan III baku kurkumin 100 ppm B= replikasi I, II, dan III baku kurkumin 300 ppm C= replikasi I, II, dan III baku kurkumin 500 ppm
Gambar 11. Kromatogram panjang gelombang maksimum baku kurkumin
D. Pembuatan Kurva Baku Kurkumin
dan direplikasi sebanyak 3 kali. Persamaan regresi linear disebut baik jika
memiliki koefisien korelasi 0,999.
Tabel III. Data kurva baku kurkumin
Replikasi Kadar kurkumin
Persamaan kurva baku yang digunakan untuk perhitungan kadar yaitu data replikasi I. Data di atas menunjukkan untuk replikasi I persamaan kurva baku yaitu y = 0,9753x + 8,9901 dengan nilai r sebesar 0,99963 dan kemiringan garis sebesar 44,28 º.
E. Optimasi Metode Ekstraksi Kurkumin dalam Rheumakur®
Sampel yang digunakan yaitu kapsul lunak OHT merk Rheumakur® dengan bentuk sediaan semi solid. Karena itu dilakukan optimasi metode ekstraksi untuk menyari kurkumin dalam sampel Rheumakur®. Metode yang digunakan yaitu menggunakan magnetic stirrer dan ultrasonikator.
1. Menggunakan magnetic stirrer
Prinsip metode ini yaitu pengadukan menggunakan stirer (magnet) sehingga kecepatan bisa dibuat konstan, yang dapat menghomogenkan larutan. Optimasi ini dilakukan dengan mengoptimasi pada lamanya proses menggunakan
magnetic stirrer yaitu 10; 15; 20; 25; dan 30 menit. Waktu yang digunakan dibatasi 10-30 menit, hal ini bertujuan agar kurkumin tidak terdegradasi karena preparasi sampel terlalu lama.
Keterangan:
A: Baku kurkumin, B: 10 menit, C: 15 menit, D: 20 menit, E: 25 menit, F: 30 menit Gambar 13. Perbandingan kromatogram baku dan kromatogram ekstraksi sampel
menggunakan magnetic stirrer selama 10; 15; 20; 25; dan 30 menit
Kromatogram pada menit ke-30 menunjukkan hanya terdapat 2 peak dengan nilai Rs yaitu sebesar 3,18.
Tabel IV. Hasil pengukuran AUC sampel pada variasi waktu menggunakan magnetic stirer
Data di atas menunjukkan bahwa penyarian menggunakan magnetic stirrer belum memberikan hasil yang baik, dimana respon AUC yang dihasilkan belum masuk dalam rentang hasil validasi yaitu 260-500 ppm. Kecilnya respon dan kadar yang didapat karena sampel yang telah dipreparasi belum terekstraksi seluruhnya karena sampel yang digunakan menempel pada stirrer yang digunakan. Sehingga metode ini belum tepat untuk mengekstraksi kurkumin dalam sediaan kapsul lunak Rheumakur®.
2. Menggunakan ultrasonikator
Keterangan:
A: baku kurkumin, B: 10 menit, C: 15 menit, D: 20 menit, E: 25 menit
Gambar 14. Perbandingan kromatogram baku dan kromatogram ekstraksi sampel menggunakan ultrasonikator selama 10; 15; 20; dan 25 menit
selama 20 menit, peak kurkumin ditunjukkan oleh nomor 3 dengan Rf 0,83. Hasil kromatogram terdapat 3 peak dengan nilai Rs 1,79. Kromatogram menit ke-25 menunjukkan bahwa peak kurkumin ditunjukkan oleh nomor 3 dengan Rf 0,83. Selain itu, terdapat 3 peak dengan nilai resolusi pemisahan 1,93 yang artinya pemisahan kurkumin sudah baik untuk waktu ekstraksi selama 25 menit.
Tabel V. Hasil pengukuran AUC sampel pada variasi waktu menggunakan ultrasonikator
Dari tabel di atas menunjukkan bahwa penyarian menggunakan ultrasonikator selama 15 menit sudah memberikan respon dan profil kromatogram yang baik. Respon yang dihasilkan masuk dalam rentang hasil validasi yaitu 260-500 ppm.
Berdasarkan data hasil optimasi ekstraksi sampel dengan variasi waktu penyarian diperoleh bahwa ekstraksi sampel untuk Rheumakur® yang paling baik yaitu menggunakan ultrasonikator selama 15 menit. Pada waktu yang optimal ini dilakukan replikasi sebanyak 5 replikasi untuk melihat reprodusibilitas kadar.
Tabel VI. Replikasi pengukuran AUC sampel kurkumin dengan waktu penyarian 15 menit menggunakan ultrasonikator
Dari data di atas dapat dilihat bahwa kadar yang didapat masuk dalam rentang kandungan kurkumin yang tertera dalam label yaitu 1,785-2,142 % (b/b) dengan nilai CV yang didapatkan 1,6 %, dimana CV yang baik adalah < 2 %. Sehingga dapat disimpulkan bahwa waktu penyarian selama 15 menit dapat digunakan dalam tahap penetapan kadar kurkumin dalam Rheumakur® karena memiliki keterulangan yang baik.
F. Penetapan Kadar Kurkumin dalam Sampel
Penetapan kadar kurkumin dalam sampel Rheumakur® dilakukan setelah sampel dipreparasi. Kadar kurkumin dalam kapsul lunak OHT Rheumakur® dapat dihitung berdasarkan kromatogram yang memiliki nilai Rf yang sama dengan nilai Rf kurkumin standar menggunakan persamaan kurva baku yang telah diperoleh.
Tabel VII. Kadar kurkumin pada sampel kurkumin di dalam setiap batch
Apotek Replikasi AUC Kadar Kurkumin
(% b/b) Keterangan Rheumakur® untuk masing-masing apotek yaitu 2,11316, 2,06497, dan 2,00917 % (b/b). Kadar setiap sampel masuk dalam rentang kadar kurkumin yang tertera pada label yaitu 1,785-2,142 % (b/b).
Hasil penetapan kadar pada apotek 1, 2, dan 3 memiliki nilai CV yang baik yaitu < 2 %, dengan masing-masing nilai CV 1,10498 %; 1,18888 %; dan 1,78083%. Hal ini menunjukkan bahwa preparasi sampel yang dilakukan memiliki presisi yang baik yaitu keterulangan pengambilan sampel dari setiap apotek baik sehingga memberikan kedekatan hasil pengukuran dan dapat dikatakan sampel sudah tercampur homogen pada saat dilakukan preparasi.
analisis statistik. Metode analisis statistik yang digunakan yaitu analisis komparatif. Untuk membandingkan kadar pada 2 apotek digunakan uji t tidak berpasangan. Sedangkan untuk membandingkan data kadar kurkumin diantara ketiga apotek digunakan uji one way Anova untuk k sampel berkolerasi. Untuk uji statistik tingkat kepercayaan yang digunakan 95 %.
Untuk analisis statistik apotek 1, apotek 2, dan apotek 3 digunakan uji statistik one way Anova. Hipotesis sementara untuk analisis statistik ketiga apotek yaitu tidak ada perbedaan kadar kurkumin dalam sampel diantara ketiga apotek.
Uji statistik menggunakan one way Anova setelah didapat data normalitas data dan varians. Syarat utama untuk uji one way Anova adalah data berdistribusi normal dan memiliki varian yang sama. Jika pada uji one way Anova terdapat perbedaan maka dilanjutkan dengan uji Post Hoc. Pada uji Post Hoc ini akan diketahui apakah kadar kurkumin antar 3 apotek ini berbeda bermakna atau tidak.
Tabel VIII. Nilai normalitas data apotek 1, 2, dan 3 Tests of Normality
Apotek Kolmogorov-Smirnova Shapiro-Wilk Statistic df Sig, Statistic df Sig,
*, This is a lower bound of the true significance,
Tabel IX. Nilai varian apotek 1, 2, dan 3 atas didapat nilai varian sama karena nilai p > 0,05, yaitu 0,957. Sehingga dapat dilanjutkan dengan uji one way Anova.
Tabel X. Nilai uji statistik one way Anova apotek 1, 2, dan 3
Hasil dari uji one way Anova menyatakan bahwa adanya perbedaan pada kadar kurkumin antara apotek 1, 2, dan 3. Hal ini ditunjukkan dengan nilai p < 0,05 sehingga dilanjutkan dengan uji post hoc.
Tabel XIV. Nilai uji statistik Post Hoc apotek 1, 2, dan 3
apotek 1 apotek 2 0,04819400* 0,01509481 0,008 0,0153052 0,0810828
apotek 3 0,10399000* 0,01509481 0,000 0,0711012 0,1368788
apotek 2 apotek 1 -0,04819400* 0,01509481 0,008 -0,0810828 -0,0153052
apotek 3 0,05579600* 0,01509481 0,003 0,0229072 0,0886848
apotek 3 apotek 1 -0,10399000* 0,01509481 0,000 -0,1368788 -0,0711012
apotek 2 -0,05579600* 0,01509481 0,003 -0,0886848 -0,0229072
Hasil dari uji post hoc menunjukkan:
a. Nilai p untuk apotek 1 dan apotek 2 yaitu 0,008 b. Nilai p untuk apotek 2 dan apotek 3 yaitu 0,003 c. Nilai p untuk apotek 1 dan apotek 3 yaitu 0,000
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Dari hasil penelitian yang telah diperoleh, dapat disimpulkan bahwa kadar rata-rata kurkumin yang terdapat dalam sediaan padat OHT merk Rheumakur® yang beredar dipasaran dengan fase gerak heksan : kloroform : asam asetat glasial (0,5 : 8,5 : 1,0) dan persamaan kurva baku y = 0,9753x + 8,9901, untuk setiap apoteknya masing-masing 2,11316; 2,06497; dan 2,00917% (b/b) dengan nilai CV masing-masing 1,10498 %; 1,18888%; dan 1,78083%. Kadar kurkumin dalam sediaan kapsul lunak Rheumakur® secara statistik antara 3 apotek berbeda.
B. Saran
Perlu dilakukan analisis terhadap sampel obat tradisional lain yang mengandung kurkumin dengan menggunakan metode penelitian ini.
DAFTAR PUSTAKA
Anonim, 2010, Rheumakur, http://phytochemindo.indonetwork.web.id/1167963/ rheumakur-kombinasi-minyak-kunyit-dan-temulawak.htm, diakses tanggal 6 Januari, 2011.
Aggarwal, B.B., 1995, Curcumin, Analogues, of Curcumin and Novel Uses Thereof, http://www.thepowerhour.com/curcumin/Turmeric.pdf, diakses tanggal 20 Juli 2010.
Badan Pengawas Obat dan Makanan Republik Indonesia, 2004, Monografi ekstrak Tumbuhan Obat Indonesia, Vol 1, Badan Pengawas Obat dan Makanan Republik Indonesia, Jakarta, 51.
Badan Pengawas Obat dan Makanan Republik Indonesia, 2005, Standarisasi Ekstrak Tumbuhan Obat Indonesia, Salah Satu Tahapan Penting dalam Pengembangan Obat Asli Indonesia, InfoPOM, 6(4), 1-5.
Badan Pengawas Obat Dan Makanan RI, 2005, Lampiran Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor HK 00.05.4.1380 tentang Pedoman Cara Pembuatan Obat Tradisional Yang Baik, Badan Pengawas Obat dan Makanan Republik Indonesia, Jakarta. Clark, J., 2007, Kromatografi Lapis Tipis,
http://www.chem-is-try.org/materi_kimia/instrumen_analisis/kromatografi/kromatografi_lapi s_tipis, diakses tanggal 30 Oktober 2010.
Dahlan, M. Sopiyudin, 2009, Statistik untuk Kedokteran dan Kesehatan Edisi 4, Penerbit Salemba Medika, Jakarta.
Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995, Farmakope Indonesia, Jilid IV, Departemen Kesehatan Republik Indonesia, 2-4. Gritter, J.R., Bobbit, J.M., dan Scharting, A.E., 1991, Pengantar Kromatografi,
diterjemahkan oleh Kosasih Padmawinata, Edisi II, hal.109-112, 140-147, ITB, Bandung.
Hardjono, S., 1985, Kromatografi, 32-34, Laboratorium Analisa Kimia Fisika Pusat, UGM, Yogyakarta
Harmita, 2004, Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya,
Majalah Ilmu Kefarmasian, Vol. I, No. 3, 122.
Kementrian Kesehatan Republik Indonesia, 1990, Permenkes RI No.246/MENKES/PER/V/1990 tentang izin usaha industri obat tradisional dan pendaftaran obat tradisional, Departemen Kesehatan RI, Jakarta.
Kementerian Kesehatan Republik Indonesia, 1994, Lampiran Kepmenkes Nomor 659/Menkes/SK/X/1991 Cara Pembuatan Obat Tradisional yang Baik, Departemen Kesehatan RI, Jakarta.
Kementerian Kesehatan Republik Indonesia, 1994, Lampiran Kepmenkes Nomor 661/Menkes/SK/VII/1994 Tentang Persyaratan Obat Tradisional, Departemen Kesehatan RI, Jakarta, hal.9.
Khopkar, 1990, Concepts of Analytical Chemistry, diterjemahkan oleh Sapto Rahardjo, hal.155-156, Universitas Indonesia Press, Jakarta.
Kohli, K., Ali, J., Ansar, M.J., Raheman, Z., 2005, Curcumin: A Natural Anti-Inflamatory Agent, In Indian Journal of Pharmacology, 141-142.
Kosasih, T., 2011, Optimasi Metode Analisis Kurkumin dalam Sediaan Kapsul Lunak Merk Rheumakur Menggunakan Metode Kromatografi Lapis Tipis – Densitometri, Skripsi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Kurnia, R., 2010, Kurkumin Kunyit, http://lordbroken.wordpress.com/2010/05/31/ kurkumin-kunyit/, diakses tanggal 5 November 2010.
Martono, 1996, Penentuan Kadar Kurkumin secara Kromatografi Lapis Tipis-Densitometri, Buletin ISFI Yogyakarta, Vol. 2, No. 4, 11-21.
Mintarsih, E.R.R., 1990, Penetapan Kadar Alkaloid Kinina dalam Akar, Batang, dan Daun Chinchona Succirubra Pavon et Klotzch dari Daerah Kaliurang secara Spektrodensitometri (TLC-Scanner), Skripsi, Fakultas Farmasi, Universitas Gadjah Muda, Yogyakarta.
Mulja, M. dan Suharman, 1995, Analisis Instrumental, Universitas Airlangga Press, Surabaya, hal.223-228, 231-234.
Nagappan, K.V., Meyyanathan, Raja, R.B., and Kannan, E., 2009, A Liquid Chromatography Method for the Simultaneous Detemination of Curcumin and Piperine in Food Products Using Diode Array Detection,
Asian J. V. Research Chem, 2(2), 115-118.
Naguib, Y., 1998, Softgel Capsul: An Elegant & Versatile Dosage Form, diakses dari info@vitaminretailer.com, diakses tanggal 14 November 2010. Paramasivam, M., Aktar, W., Poi, R., Banerjee, H., Bandyopahyay, A., 2008,
Occurrence of curcuminoids in Curcuma longa : A quality
standardization by HPTLC,
http://www.banglajol.info/index.php/BJP/article/viewFile/833/913, diakses tanggal 10 Februari 2010.
Podczeck, F., and Jones, B.F., 2004, Pharmaceutical capsules, second edition, Pharmaceutical Press, USA, pp.201.
Roth, Hermann, J., 1994, Pharmaceutical Analysis, diterjemahkan oleh Sarjono Kisman, Slamet Ibrahim, cetakan 2, UGM Press, Yogyakarta.
Rukmana, R., 1994, Kunyit, Penerbit Kanisius, Yogyakarta, 2.
Sastrohamidjojo, H., 1985, Kromatografi, Edisi I, Liberty, Yogyakarta, hal.32-34. Shafwatunnida, Lili, 2009, Kunyit (Curcuma Domistica Val.),
http://www.ubb.ac.id/menulengkap.php?judul=KUNYIT%20%28CURC UMA%20DOMESTICA%29&&nomorurut_artikel=45, diakses tanggal 18 Desember 2010.
Sherma, J., Fried, B., 1996, Handbook of Thin Layer Chromatography, Marcell Dekker Inc., New York, pp. 56-57.
Stahl, E., 1969, Thin Layer Chromatography : A laboratory Handbook, 2th Ed., Springer Verlag, Berlin, pp.97-101.
Stahl, E., 1985, Drug Analysis by Chromatography and Microscopy, diterjemahkan oleh Kosasih Padmawinata, Iwang Soediro, hal.7-12, ITB Press, Bandung.
Stankovic, 2004, Curcumin : Chemical and Technical Assessment (CTA), JECFA
61st edition, FAO,
ftp://ftp.fao.org/es/esn/jecfa/cta/CTA_61_Curcumin.pdf, diakses tanggal 1 Desember 2010.
Sugiono, 2008, Statistika untuk Penelitian, Alfabeta, Bandung, hal 100.
Sumiati, T., 2010, Keunggulan dan Manfaat Kunyit, http://id.shvoong.com/lifestyl e/2005091-keunggulan-dan-manfaat-kunyit/, diakses tanggal 30 Oktober 2010.
Suseno, A., 2011, Validasi Metode Analisis Kurkumin dalam Sediaan Kapsul Lunak Merk Rheumakur Menggunakan Metode Kromatografi Lapis Tipis – Densitometri, Skripsi, Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Tonnesen, H.H., Karlsen, 1983, Curcuminoid and It’s Compounds, Journal Chromatography, Vol.4, 259.
Tonnesen, H.H. & Karlsen, J., 1985, Studies of curcumin and curcuminoids: V. Alkaline degradation of curcumin, Z. Lebensm. Unters. Forsch. 180: 132-134.
Tonnesenn H.H., dan Karlsen, J., 1985a, Studies on curcumin and curcuminoids, VI: Kinetics of Curcumin Degradation in Aqueous Solution, Original Paper, Z. Lebensm. Unters. Fosch., pp. 402-404.