Laporan Praktikum Kimia Instrumen
PENENTUAN KADAR TEMBAGA (II) DALAM SAMPEL AIR SAWAH DENGAN METODE SPEKTROMETRI SERAPAN ATOM (SSA)
2 April 2012
Dosen Pembimbing Dr. Hernani, M.Si
Disusun oleh Kelompok 9
Muhamad Prisla K. (0900598) Dewi Fuji Astuti (0902212)
Siti Supriyanti (0905861)
JURUSAN PENDIDIKAN KIMIA
FAKULTAS PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS PENDIDIKAN INDONESIA
BANDUNG
A.Tanggal Praktikum : tembaganya dengan alat spektrometri serapan atom
2. Dapat menyiapkan larutan kerja dari larutan “stock” yang tersedia.
3. Dapat memahami prinsip penentuan kadar logam dalam suatu sampel dengan alat spectrometer serapan atom.
D.Tinjauan Pustaka :
Metode spekstroskopi atom dapat digunakan untuk analisis lebih dari 2 unsur baik kualitatif maupun kuantitatif. Penentuan spesi atom hanya dapat dilakukan dalam medium gas di mana setiap atom atau ion unsur terpisah secara sempurna satu sama lain.
Metode AAS adalah metode spektrometri yang didasari oleh adanya serapan atau absorbsi cahaya ultraviolet (UV) atau visible (Vis) oleh atom-atom suatu unsur dalam keadaan dasar atom-atom menyerap cahaya tersebut pada panjang gelombang tertentu, tergantung pada sifat unsurnya cahaya UV atau Visible yang diserap berasal dari energi yang diemisikan oleh sumber energi tertentu.
Hukum Lambert : bila suatu sumber sianr monokromatis melewati medium transparan, maka intensitas sinar yang diteruskan berkurang dengan bertambahnya ketebalan medium yang mengabsorbsi
Hukum Beer : intensitas sinar yang diteruskan berkurang secara eksponensial dengan bertambahnya konsentrasi spesi yang menyerap sinar tersebut
Hukum Lambert-Beer dirumuskan sebagai berikut : A = a.b.c
Keterangan :
A = absorbansi atau daya serap a = absortivitas molar
b = ketebalan medium c = konsentrasi
Fitur dasar dari spektrometer serapan atom
Komponen dasar dari sebuah spektrometer serapan atom ditunjukkan pada Gambar.40. Fungsi dari alat AAS adalah sebagai berikut :
1. Sumber radiasi (katoda berongga atau EDL) memancarkan garis tajam spektrum yang menunjukkan karakteristik dari elemen analit
2. Sianr emisi dari sumber radiasi dimodulasi
3. Sinyal termodulasi melewati flame menjadi uap, dan diatomisasi dimana atom-atom analot lalu menyerap radiasi dari sumber radiasi
4. Radiasi yang diharapkan adalah garis spektral (biasanya resonansi line) dimana dipilih oleh monokromator
5. Dimana hasil radiasi yang diteruskan ke detektir (photomultiplier) dimana sinyal cahaya diubah menjadi sinyal listrik
7. sinyal akhirnya dicatat oleh perangkat pembacaan (meter, perekam grafik, atau melalui pengolahan data untuk unit layar digital atau printer)
Atomic Absorption Spectrometry
Instrumen Spektroskopi Serapan Atom
Komponen utama
Untuk lebih jelasnya diperlihatkan oleh gambar berikut ini
1. Sumber cahaya
Atom menyerap cahaya pada panjang gelombang yang diskrit. Atom menyerap emisi cahaya yang dihasilkan oleh cathode lamp. Dimana cahaya ini mempunyai sensitivitas dan spesipik untuk atom yang menyerapnya.
a. Hallow cathode lamp
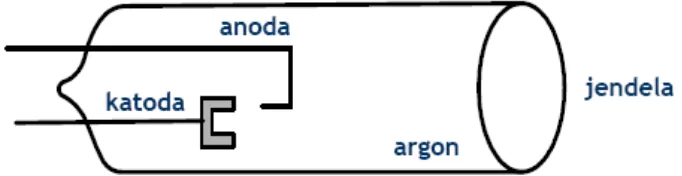
Jenis katoda pada hallow cathode ini diesesuaikan dengan panjang gelombang yang dipancarkan/diemisikan, contohnyajika analit yang digunakan mengandung Cu maka katoda yang digunakan di hallow cathode adalah logam Cu. Anoda dan katoda berada dalam sebuah silinder tertutup. Dalam silinder ini juga terdapat gas inert yaitu argon atau neon dengan tekanan rendah. Di silinder ini akan dihasilkan cahaya yang nantinya diserap oleh atom pada ruang pengkabutan. Terjadi ionisasi dari beberapa atom dari gas tersebut yang bermuatan positif akibat pemberian perbedaan potensial sekitar 300-400 volt antara anoda dan katoda, kation gas tersebut akan menabrak atom-atom logam pada katoda. Bebrapa atom-atom akan terlempar kepermukaan dan terjadieksitasi dari keadaan dasar kekeadaan tereksitasi dan mengemisikan cahaya atau radiasi tertentu ketika kembali ke keadaan dasar. Misalnya Pb* Pb + hv ( gambar 2)
Gambar 2 b. Elektrodeless Discharge Lamps (EDLs)
tetapi terenergi oleh penangkap intens frekuensi radio atau radiasi mikrowave.
2. Coper, merupakan alat untuk menyeleksi cahaya yang diemisikan oleh elemen dari hallow cathode lamp, dimana coper ini akan memilih sumber cahaya yang sesuai dengan analit yang diuji.
3. Cell sampel
Pada bagian ini merupakan tempat terjadinya proses atomisasi. Berikut penjelasan mengenai proses atomisasi:
Solution of analyte
Spray
Gaseous molecules
Atoms
Exicited molecules
Exicited atoms
Exicited ions Atomic ions
Solid/gas aerosol
hv molecules
hv atomic
Pada proses pengabutan, sampel berupa larutan dosemprotkan kedalam nyala yang bersumber dari udara dan bahan bakar, larutan ini akan berubah menjadi aerosol, pelarut akan menguap aehingga tersisa analit yang ter[adatkan. Kemudian analit ini berubah menjadi cair (mengalami pelelehan) lalu menguap menjadi gas, setelah analit menjadi gas, analit ini mengalami proses atomisasi, hasil atomisasi ini adalah terbentuknya atom Cu. Atom Cu ini mengalami eksitasi karena menyerap cahaya.
4. Kromator
Merupakan alat untuk menengkap chaya spesifik yang diteruskan oleh atom. Kromator mempunyai kemampuan untuk menyeleksi berbgai cahaya baik berupa emisi atau chaya yang diteruskan dalam jumlah yang banyak.
5. Detektor
Merupakan alat untuk mendeteksi cahaya yang diserap oleh kromator,
6. Elektronika dan read out
Merupakan alat untuk menerjemahkan cahaya yang diteruskan yang nantinya akan tergambar dalam bnetuk absorban.
Spektrofotometer
Pada umumnya, alat ini harus dapat menyediakan lebar pita dengan cukup sempit untuk mengisolasi garis terpilih untuk pengukuran dari garis lainnya yang mungkin mencampuri atau mengurangisensitifitas analisis.
- Single-Beam Instruments
- Double-Beam Instruments
Alat ini terbuat dari hallow cathode yang terpisah oleh cermin tembaga, setenga mengelilingi nyala api dan setengahnya lagi mengelilingi kedua lapisan tersebut di kombinasi ulang dengan setengan kaca perak dan ke dalam kzerney. Turner monotransformator, sebuah tabung foto multifier berperan sebagai transmitter.
Penyiapan sampel
kebanyakan sampel hal ini, biasanya tidak dilakukan bila atomisasi dilakukan menggunakan batang grafit secara elektrotermal karena matrik dari sampel dihilangkan melalui proses pengarangan sebelum atomisasi. Pada proses atomisasi dengan nyala kebanyakan sampel cair dapat disemprotkan langsung kedalam nyala setelah diencerkan dengan pelarut yang cocok.
Sampel padat biasanya dilarutkan dalam asam tetapi ada kalanya didahului dengan peleburan alkil. Asam klorida, asam nitrat dan asam sulfat biasanya digunakan untuk melarutkan logam-logam atau logam campuran. Asam nitrat biasanya membentuk senyawa yang mudah terurai tetapi sukar menguap sehingga ia lebih disukai dari pada asam klorida untuk proses pengarangan.
Intereferensi dalam Spektroskopi Serapan Atom Interferensi spektral
Interferensi ini terjadi ketika serapan atu emisi dari spesi berinterferensi mengalami overlap dengan serapan atau emisi analit. Selain itu, interferensi ini adalah hasil dari adanbya pembakaran produk yang menyebabkan serapan atau pertikulat produk yang menebarkan reaksi. Salah satu analisis interferensi adalah dengan koreksi latar belakang dengan berdasarkan efek zeeman.
Gangguan 1. Matrik
penyemprotandalam nebulizer, sehingga efisiensi nebulizerantara sampel dan larutan standar akan berbeda. Jika terdapat perbedaan kecepatan/laju maka absorban yang dihasilkan tidak berkorelasi. Untuk menggurangi atau meniadakan kesalahan matrik ini, yaitu dengan mematcingkan matrik sampel dengan matrik larutan standar. Hal ini, dilakukan dengan menambahkan beberapa asam dan regen yang lain, sehingga keduanya memiliki konsentrasi yang sama.
2. Ionisasi
Pada nyala terjadi proses ionisasi, yaitu terionnya atom-atom sehingga mengakibatkan menurunnya sensitivitas. Oleh karena spektra ion berada dengan spektra atom, maka perlu dijaga agar derajat ionisasi ini pada level yang konstan atau bila mungkin ditiadakan. Hal ini dapat dilakukan dengan menurunkan suhu dari nyala atau dengan menambahkan metal yang mudah terionisasi misalnya logam alkali. Penambahan deionizer akan mempertinggi konsentrasi elektron pada nyala sehingga akan menggeser keseimbangan berikut kesebelah kiri.
M* → M+ + e- 3. Kimia
Bentuk padat
bahan bkaar untuk memperoleh nyala reduksi sehingga memperkecil pembentukan oksida yang stabil.
Analisis logam tembaga dengan AAS
Salah satu aplikasi dari spektroskopi serapan atom adalah penentuan kadar tembaga dari suatu limbah. Limbah yang mengandung tembaga ini kebanyakan dihasilkan oleh industri persenjataan, industri paduan logam, industri kertas dan lain-lain.
Tembaga termasuk logam berat yaitu logam dengan bobot jenis lebih besar dari 5 gr/cm3. Logam – logam berat berbahaya baik secara langsung terhadap kehidupan organisme, maupun efeknya secara tidak langsung terhadap kesehatan manusia.
Hal ini berkaitan dengan sifat-sifat logam berat tersebut ( PPLH-IPB, 1997; Sutamihardja dkk, 1982) yaitu :
1. Sulit didegradasi, sehingga mudah terakumulasi dalam lingkungan perairan dan keberadaannya secara alami sulit terurai (dihilangkan)
2. Dapat terakumulasi dalam organisme termasuk kerang dan ikan, dan akan membahayakan kesehatan manusia yang mengkomsumsi organisme tersebut
3. Mudah terakumulasi di sedimen, sehingga konsentrasinya selalu lebih tinggi dari konsentrasi logam dalam air. Disamping itu sedimen mudah tersuspensi karena pergerakan masa air yang akan melarutkan kembali logam yang dikandungnya ke dalam air, sehingga sedimen menjadi sumber pencemar potensial dalam skala waktu tertentu
protein, sebagian dieksresikan melalui empedu ke dalam usus dan dibuang kefeses, sebagian lagi menumpuk dalam hati dan ginjal, sehingga menyebabkan penyakit anemia dan tuberkulosis.
Jika kadar Cu sampel belum melebihi batas (ambang batas) yang ditetapkan pemerintah yaitu 20 ppm untuk Cu, maka sesuai Keputusan Dirjen POM No. 03725/B/SK/VII/89[7] sampel air tersebut aman untuk dikonsumsi.
1. 50 mL sampel air sawah dimasukan ke dalam gelas kimia 100 mL. 2. Ditambahkan 2.5 mL HNO3 pekat, diaduk.
5. Ditutup dengan kaca arloji. 6. Dipanaskan hingga jernih. 7. Didinginkan
8. Ditambahkan sedikit aquades.
9. Dituangkan ke dalam labu ukur 50 mL. 10.Ditanda bataskan
11.Saring jika terdapat yang tidak larut. 2. Pembuatan blanko
1. Larutan HNO3 pekat ditambahkan aquades hingga pH = 2 3. Pembuatan larutan standar Cu (II)
1. Larutan induk Cu (II) 1000 ppm dipipet 1.25 mL 2. Dimasukkan ke labu seukuran 50 mL.
3. Dilarutkan dengan blanko hingga tanda batas. 4. Pembuatan larutan uji
1. Sampel hasil preparasi dipipet 5 mL
2. Dimasukkan ke dalam 4 labu seukuran 25 mL dan satu labu seukuran 50 mL
3. Ditambahkan larutan standar berturut-turut 2,4,6,8 mL untuk labu seukuran 25 mL dan 10 mL untuk labu seukuran 50 mL.
4. Ditandabataskan dengan blanko 5. Pembuatan kurva adisi standar
1. Larutan uji diukur absorbansi dengan SSA. 2. Dibuat grafik
G.Hasil dan Analisis Data
6 Blanko 0.000 0.0007 7.77
7 Sampel 0.407 0.0032 0.80
Kadar Cu(II) dalam sampel 1.9706 ppm
Analisis Data dan pembahasan
Pengambilan sampel harus mengikuti dua prinsip utama, yakni representatif dan homogen. Representatif (mewakili) berarti sampel yang diambil harus mewakili keseluruhan populasi. Pengambilan sampel yang representatif dilakukan dengan dua cara. Pertama, jika sumber pengambilang sama maka waktu pengambilan yang dibuat berbeda, tetapi jika waktu pengambilan sama maka tempat pengambilan yang berbeda. Sampel harus tetap homogen artinya diukur beberapa kali dengan volume yang sama akan memberikan kadar yang sama.
Sampel harus dijaga kondisinya dengan cara disimpan di lemari es dengan tujuan mencegah reaksi apapun yang mungkin terjadi pada sampel terutama yang mungkin akan melibatkan � 2+. Karena pada suhu dingin reaksi relatif tidak berlangsung karena pada dasarnya reaksi baik endoterm maupun eksoterm memerlukan energy terlebih untuk memulai reaksi.
Penambahan HNO3 berguna untuk mendekstruksi ikatan organologam antara � 2+dengan senyawa organik dengan bantuan pemanasan. Selain itu untuk memastikan bahwa semua Cu berada da. lam biloks +2. HNO3 pekat memiliki sifat pengoksidasi. Tidak menutup kemungkinan selama proses penyimpanan sampel terjadi proses reduksi � 2+ menjadi � +. Hal ini dicegah dengan penambahan HNO3. � + ini harus dihindari terbentuk karena akan menebabkan kenaikan energi dengan jumlah serapan yang berbeda dibandingkan � 2+pada jumlah yang samadan hal tersebut yang akan menyebabkan kesalahan analisis.
Penggunaan blanko HNO3 pH 2 pada pembuatan standar induk bertujuan untuk mencegah terhidrolisisnya � 2+. Larutan baku dibuat dalam beberapa variansi konsentrasi untuk membuat kurva kalibrasi. Menurut hukum lambert-beer maka jika repeatabilitasnya bagus maka hubungan antara absorban dengan konsentrasi adalah y = mx dimana y adalah absorbansi dan x adalah konsentrasi. Metode yang digunakan adalah adisi standar, karena kadar � 2+ dalam sampel akan memberikan signal yang lemah dan tidak masuk dalam range percobaan dengan demikian perlu ditambahkan � 2+ terukur dan kuantitatif sehingga nantinya kadar � 2+ sampel dapat diketahui.
Sebelum analisa, dilakukan terlebih dahulu dilakukan optimasi panjang gelombang yang bertujuan untuk menentukan serapan maksimum. Lamp yang digunakan adalah HCL dengan demikian selektif mendeteksi � 2+dalam sampel. Pengukuran dilakuan 3 kali (triplo) kemudian diambil reratanya untuk melihat reapeatabilitas analisa.
H.Kesimpulan
Prinsip analisa SSA adalah setiap ion logam ketika dibakar akan memberikan nyala yang khas, yang dapat diukur intensitas dengan melewatkan sinar UV sehingga dapat ditentukan absorbansi yang akhirnya sebanding dengan konsentrasi. Kadar � 2+dari air sawah Kp. Cikundul-Soreang dengan menggunakan AAS adalah sebesar 1.9706 ppm.
I. Daftar Pustaka
Budiasih, Endang, dkk. (1999). Analisis Instrumen. Malang: Universitas Negeri Malang.
Hendayana, Sumar. (1994). Kimia Analitik Instrumen. Semarang: IKIP Semarang Press
Khopkar, S.M. (1990). Konsep Dasar Kimia Analitik. Jakarta: UI Press
L.H.J Lajunen and P.Peramakiuniversity. (2004). Spectrochemical Analysis by Atomic Absorption and Emission 2nd Edition. Oulu, Finland : the royal
society of chemistry
R.A. Day, Jr. dan A.L. Underwood. (2002). Analisis Kimia Kuantitatif. Jakarta: Erlangga
Skoog, A. Douglas ,F. James Holler, dan Stanley R. (2004). Fundamental af Analytical Chemistry English Edition. Ontario : Brodis/Cole-Thomson
J. Lampiran Lampiran 1
DATA PENGAMATAN
Tabel Pengamatan : Data Spesifikasi sampel
No Parameter yang diamati Pengamatan
1 Asal Air sawah
No Parameter yang diamati Pengamatan
1 Bahan bakar Asetilen-udara
2 Lamp HCL
Hasil pengukuran Larutan sampel dan blanko
= 500 � 10
−2
15 = 0.33
2. Pembuatan larutan standar Cu (II)
� 2+ = 5 �� � 2+ = 20 ��
Lampiran 3
Dokumentasi Praktikum
bahan bakar/oksidan
hallow cathode read out set alat AAS
flame pengatur gas/oksidan penyaringan sampel
pengukuran AAS