UNIVERSITAS INDONESIA
Penilaian Ekspresi Mucin-6 (MUC6) pada Serrated Adenoma dan
Adenoma Konvensional Displasia Keras sebagai Lesi Prekursor
Kanker Kolorektal
TESIS
PILLIPUS RESAR ANDREANO
0906647860
FAKULTAS KEDOKTERAN UNIVERSITAS INDONESIA
PROGRAM STUDI PENDIDIKAN DOKTER SPESIALIS
PATOLOGI ANATOMIK
JAKARTA
UNIVERSITAS INDONESIA
Penilaian Ekspresi Mucin-6 (MUC6) pada Serrated Adenoma dan
Adenoma Konvensional Displasia Keras sebagai Lesi Prekursor
Kanker Kolorektal
TESIS
Diajukan sebagai salah satu syarat untuk meperoleh gelar Spesialis
PILLIPUS RESAR ANDREANO
0906647860
FAKULTAS KEDOKTERAN UNIVERSITAS INDONESIA
PROGRAM STUDI PENDIDIKAN DOKTER SPESIALIS
PATOLOGI ANATOMIK
JAKARTA
ABSTRAK
Nama : Pillipus Resar Andreano
Program Studi : Program Pendidikan Dokter Spesialis I Patologi Anatomik
Judul : Penilaian ekspresi Mucin-6 (MUC6) aberrant pada serrated
adenoma dan adenoma konvensional displasia keras sebagai lesi
prekursor kanker kolorektal
Latar belakang. Berdasarkan WHO, lesi-lesi prekursor dapat berkembang menjadi karsinoma kolorektal melalui 2 jalur yaitu adenoma - carcinoma
sequence dan serrated pathways. Adenoma carcinoma sequence diawali sel atipik
- adenoma displasia ringan - adenoma displasia keras -karsinoma kolorektal, sedangkan serrated pathways dimulai dari aberrant crypt foci (ACF) - polip hiperplastik - serrated adenoma (SA) - karsinoma kolorektal. Salah satu komponen penting pada lesi tersebut adalah musin yang berfungsi untuk melindungi lapisan mukosa saluran pencernaan. Musin dapat mengalami perubahan pada tumor ganas yang berperan dalam proses diferensiasi, proliferasi dan invasi sel tumor. Kepustakaan mengatakan bahwa pulasan IHK Mucin-6 (MUC6) dapat digunakan sebagai penanda bagi serrated adenoma dan adenoma konvensional displasia keras.
Tujuan. Untuk mengetahui ekspresi MUC6 aberrant di sitoplasma sel epitel kripta mukosa kolorektal pada serrated adenoma (SA) dan adenoma konvensional displasia keras.
Bahan dan cara. Penelitian ini dilakukan secara retrospektif, menggunakan studi analitik deskriptif potong lintang, dengan mengumpulkan kasus serrated adenoma (SA) dan pembanding menggunakan kasus adenoma konvensional displasia keras masing-masing 20 kasus. Dilakukan pulasan immunohistokimia (IHK) Mucin-6 (MUC6) terhadap semua kasus.
Hasil. Indeks ekspresi MUC6 aberrant kelompok serrated adenoma menunjukkan hasil sedang-kuat pada sebagian besar kasus, sedangkan kelompok adenoma konvensional displasia keras menunjukkan hasil negatif dan positif lemah pada sebagian besar kasus. Maka dapat disimpulkan terdapat hubungan bermakna antara ekspresi MUC6 aberrant pada kelompok serrated adenoma (SA) dan adenoma konvensional displasia keras, dengan nilai p=0,005.
Kesimpulan. Terdapat hubungan bermakna antara ekspresi MUC6 aberrant kelompok kasus serrated adenoma (SA) dan adenoma konvensional displasia keras.
Kata kunci : serrated adenoma, adenoma konvensional displasia keras, serrated
ABSTRACT
Name : Pillipus Resar Andreano
Study Program: Program Pendidikan Dokter Spesialis I Patologi Anatomik
Title : Expression aberrant of Mucin-6 (MUC6) assessment in serrated adenoma and conventional adenoma with severe dysplasia as precursor lesions of colorectal cancer.
Background. Based on WHO, precursor lesions can develop into colorectal carcinoma through two pathways, namely adenoma - carcinoma sequence pathways and serrated pathways. Adenoma carcinoma sequence begins atypical cells - adenoma with mild dysplasia - adenoma with severe dysplasia - colorectal carcinoma, whereas serrated pathways begins aberrant crypt foci (ACF) - hyperplastic polyps - serrated adenoma (SA) - colorectal carcinoma. One of the important components of the lesion is the mucin layer which serves to protect the gastrointestinal mucosa. Mucin may experience changes in malignant tumors which play a role in the differentiation, proliferation and invasion of tumor cells. The literature says that the outward appearance of IHC Mucin-6 (MUC6) can be used as a marker for serrated adenoma and conventional adenoma with severe dysplasia.
Objective: To find expression aberrant of MUC6 in the cytoplasm of epithelial cells in the colorectal mucosal crypts serrated adenoma (SA) and conventional adenoma with severe dysplasia.
Materials and method. This study was conducted retrospectively, using a cross-sectional descriptive analytic study, by collecting case serrated adenoma (SA) and a comparison using conventional adenoma with severe dysplasia case each of the 20 cases. Do outward MUC6 immunohistochemistry staining in all cases.
Results. Index aberrant expression of Mucin-6 (MUC6) serrated adenoma group showed moderate to strong results in most cases, while the conventional adenoma with severe dysplasia was negative and weakly positive in most cases. So we can conclude there is a relationship between the aberrant expression of Mucin-6 (MUC6) in the serrated adenoma (SA) group and conventional adenoma with severe dysplasia, with p= 0.005.
Conclusion. There is a relationship between the aberrant expression of Mucin-6 (MUC6) serrated adenoma (SA) group and conventional adenoma with severe dysplasia.
Keywords: serrated adenoma, conventional adenoma with severe dysplasia, serrated pathways, adenoma carcinoma sequence, the aberrant expression of Mucin-6 (MUC6).
DAFTAR ISI
HALAMAN JUDUL……… LEMBAR PERNYATAAN ORISINALITAS……….
LEMBAR PENGESAHAN……….. KATA PENGANTAR……….. LEMBAR PERSETUJUAN PUBLIKASI KARYA ILMIAH…
i ii iv vi ABSTRAK……… ABSTRACT………. vii viii DAFTAR ISI………. ix
DAFTAR TABEL………. xii
DAFTAR GAMBAR……… xiii
I. PENDAHULUAN……… 1
I.1. Latar Belakang……… 1
I.2. Identifikasi Masalah……… 4
I.3. Pertanyaan Penelitian……….. 4
I.4. Rumusan Hipotesis………. 4
I.5. Tujuan Penelitian……… 4
I.6. Manfaat Penelitian……….. 5
I.7. Kerangka Teori... 6
I.8. Kerangka Konsep... 7
II. TINJAUAN PUSTAKA………. 8
II.1. Usus Besar Normal……… II.1.1. Anatomi dan fisiologi……….. 8 8 II.1.2. Histologik………. 10
II.1.3. Musin sebagai komponen penting pada epitel kolorektal ………... 11
II.2. Polip Hiperplastik………..……….. II.2.1. Definisi……….. II.2.2. Etiologi……….. II.2.3. Masalah klinik……….. II.2.3.1. Epidemologi………... II.2.3.2. Lokasi………. II.2.3.3. Pemeriksaan endoskopik……… II.2.3.4. Perjalanan penyakit………...………. II.2.3.5. Terapi………. II.2.3.6. Prognosis……… II.2.4. Gambaran mikroskopik………. II.2.4.1. Gamabaran histopatologik………. II.2.4.2. Komponen Musin………. II.2.4.3. Ekspresi pulasan MUC6 aberrant pada polip hiperplastik………. 12 12 12 12 13 13 13 13 14 14 14 14 14 15
II.3 Serrated Adenoma (SA)……….
II.3.1. Definisi……… II.3.2. Etiologi……… II.3.3. Masalah klinik ……….... II.3.3.1. Epidemologi………. II.3.3.2. Lokasi………... II.3.3.3. Pemeriksaan endoskopik………. II.2.3.4. Perjalanan penyakit……….. II.3.3.5. Terapi……… II.3.3.6. Prognosis……….. II.3.4. Gambaran mikroskopik………... II.3.4.1. Gambaran histopatologik………. II.3.4.2. Ekspresi pulasan MUC6 aberrant pada
serrated adenoma……….. 16 16 16 16 17 17 17 17 18 18 18 18 20 II.4. II.5.
Adenoma Konvensional Kolorektal……….. II.4.1. Definisi………. II.4.2. Etiologi………. II.4.3. Masalah klinik……….. II.4.3.1. Epidemiologi……….………. II.4.3.2. Lokasi……….………… II.4.3.3.Gambaran klinik………..……… II.4.3.4. Pemeriksaan endoskopik……… II.4.3.5. Perjalanan penyakit……… II.4.3.6. Terapi……….. II.4.3.7. Prognosis………. II.4.4. Gambaran mikroskopik………. II.4.4.1. Gambaran histopatologik………... II.4.4.2. Komponen villosum………... II.4.4.3. Derajat displasia……….. II.4.4.4. Ekspresi pulasan MUC6 aberrant pada adenoma konvensional……… Karsinogenesis Kolorektal………... 20 20 21 21 21 21 21 22 22 23 23 24 24 24 25 26 27 III. METODOLOGI PENELITIAN…... 31
III.1. III.2. III.3. III.4. III.5. III.6. III.7. III.8. III.9. III.10 III.11 Tempat Penelitian……….………. Waktu Penelitian……….………….. Desain Penelitian….……….. Kriteria Penerimaan….……….. Kriteria Penolakan………... Populasi dan Sampel………….………. Pemilihan Sampel... Definisi Operasional……….……….. Variabel Penelitian……….. Tahapan Kerja Penelitian……… Bahan dan Tahapan Kerja……… III.11.1. Pemeriksaan histopatologik dengan pulasan haematoksilin-eosin………..…………... 31 31 31 31 31 32 32 33 34 35 36 36
III.12
III.11.2. Teknik pulasan Immunohistokimia Mucin-6 (MUC6)……… III.11.3. Interpretasi pewarnaan Immunohistokimia. Analisis Data………... 36 38 39 IV HASIL PENELITIAN... 40 IV.1. IV.2. IV.3. IV.4. IV.5.
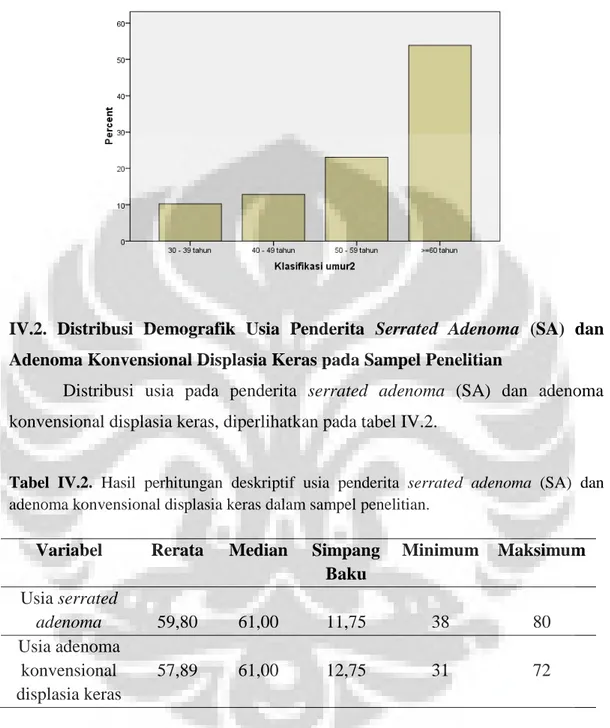
Data Patologik Sampel Penelitian………... Distribusi Demografik Penderita Serrated Adenoma (SA) dan Adenoma Konvensional Displasia Keras pada Sampel Penelitian……… Distribusi Indeks Ekspresi MUC6 Aberrant di Sitoplasma Kripta Bagian Basal/basolateral pada
Serrated Adenoma………..……….……
Distribusi Indeks Ekspresi MUC6 Aberrant di Sitoplasma di Kripta Bagian Basal/basolateral pada Adenoma Konvensional Displasia Keras….…..……. Gambar-gambar Sediaan Mikroskopik………
40 42 43 43 45 V. PEMBAHASAN………... 48
VI KESIMPULAN DAN SARAN……... 53 VI.1. VI.2. Kesimpulan………..……. Saran………. 53 53 DAFTAR PUSTAKA………... 54
SURAT IJIN PELAKSANAAN PENELITIAN (SIPP)... SURAT PERSETUJUAN IJIN PENELITIAN RSCM... KETERANGAN LULUS KAJI ETIK... DAFTAR RIWAYAT HIDUP...
DAFTAR TABEL
Tabel IV.1 Data klinikopatologik kasus serrated adenoma (SA) dan adenoma konvensional displasia keras yang dipilih sebagai sampel penelitian.
41
Tabel IV.2 Hasil perhitungan deskriptif usia penderita serrated
adenoma (SA) dan adenoma konvensional displasia
keras.
42
Tabel IV.3 Hasil analisis Chi-Square pada uji ekspresi MUC6 di sitoplasma pada 2 proporsi kasus yang berbeda yaitu
serrated adenoma (SA) dengan adenoma konvensional
displasia keras.
DAFTAR GAMBAR
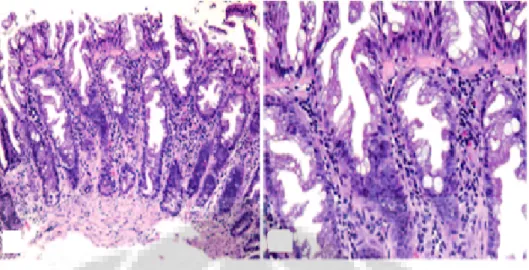
Gambar II.1 Polip hiperplastik (PH). A dan B. Kripta pada mukosa usus besar dengan inti sel kecil dan padat di bagian bawah lamina propria, dengan pelebaran kripta dibagian permukaan (pembesaran 100x).
15
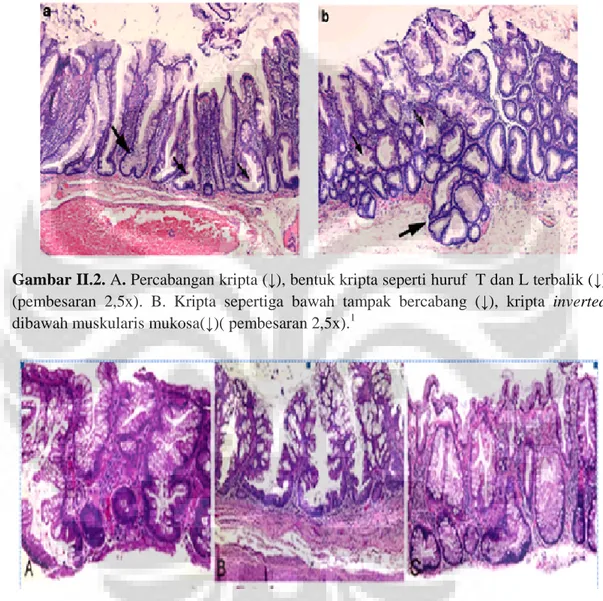
Gambar II.2 Serrated Adenoma
A. Percabangan kripta (↓), bentuk kripta seperti huruf T dan L terbalik (↓)( pembesaran 2,5x).
B. Kripta sepertiga bawah tampak bercabang (↓), kripta
inverted dibawah muskularis mukosa(↓)(pembesaran 2,5x).
19
Gambar II.3 Sessile serrated adenoma.
A. Serrated adenoma kripta basal melebar, bercabang. (pembesaran 200x).
B. SSA terdiri dari mukosa datar dengan kripta berbentuk labu atau pir, dengan gambaran displasia yang tidak nyata.(pembesaran 100x).
C. Percabangan di kripta bagian basal. (pembesaran 100x). 20
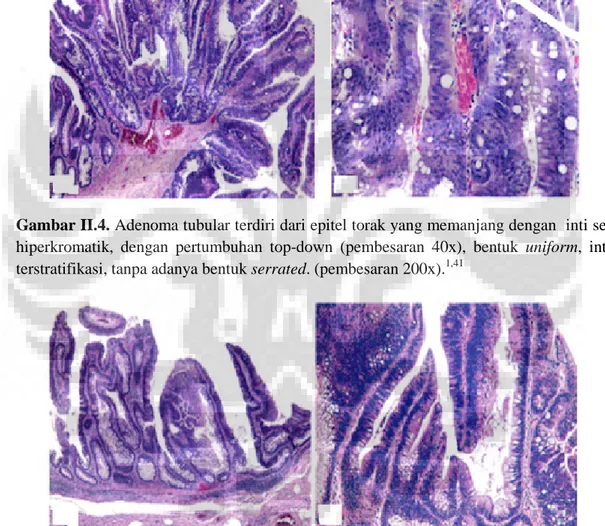
Gambar II.4 Adenoma tubular terdiri dari epitel torak yang memanjang dengan inti sel hiperkromatik, dengan pertumbuhan top-down (pembesaran 40x), bentuk uniform, inti terstratifikasi, tanpa adanya bentuk serrated. (pembesaran 200x).
26
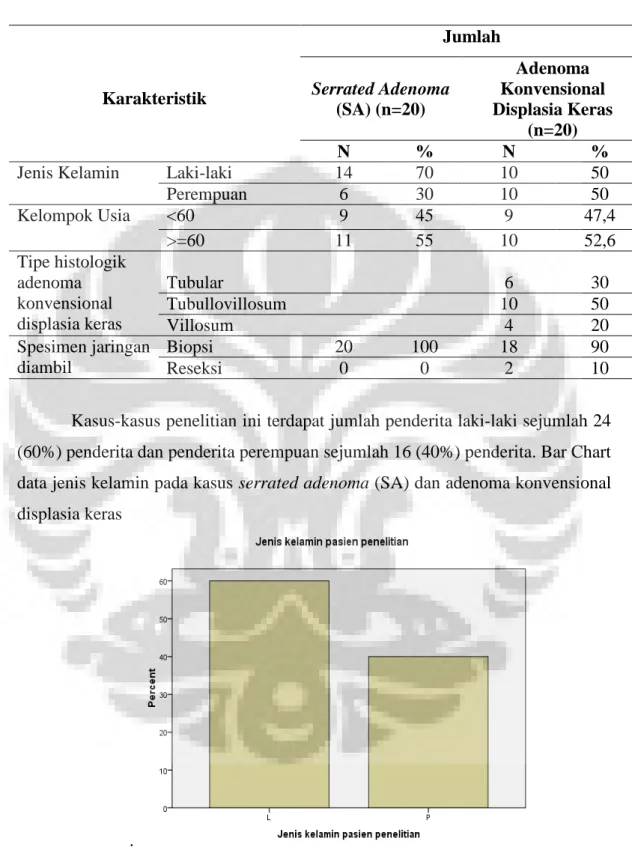
Gambar II.5 Adenoma villosum, dengan inti sel displastik, uniform, hiperkromatik (pembesaran 40x), dengan gambaran selular dan tidak terdapat gambaran serrated. (pembesaran 200x).
26
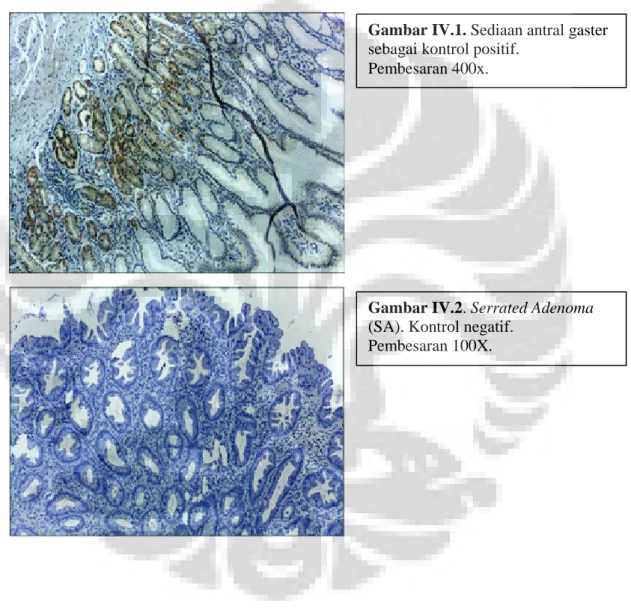
Gambar II.6 Tumorigenesis kolorektal melalui Serrated pathway. 30 Gambar IV.1 Sediaan antral gaster, sebagai kontrol positif.
(pembesaran 100x)
45
Gambar IV.2 Serrated Adenoma (SA). Kontrol negatif.
(pembesaran 100X).
45
Gambar IV.3.A Serrated Adenoma (SA). Ekspresi MUC6: positif
Indeks pulasan: lemah.(pembesaran 100X).
46
Gambar IV.3.B Serrated Adenoma (SA). Ekspresi MUC6: positif.
Indeks pulasan: sedang. (pembesaran 400X).
46
Gambar IV.3.C Serrated Adenoma (SA). Ekspresi MUC6: positif.
Indeks pulasan: kuat. (pembesaran 100X).
Gambar IV Adenoma tubular displasia keras. Ekspresi MUC6: kontrol negatif.(pembesaran 100X).
47
Gambar V.5.A Adenoma Tubullovillosum displasia keras. Ekspresi MUC6: positif . Indeks pulasan: lemah.
(pembesaran 400X).
47
Gambar V. 5 B Lokasi: kolon desendens. Diagnosis PA: adenoma tubullovillosum displasia keras. Ekspresi MUC6: positif. Indeks pulasan: rendah .
(pembesaran 400X).
BAB I
PENDAHULUAN
I.1. Latar Belakang
Karsinoma kolorektal merupakan salah satu karsinoma tersering di dunia, terutama pada negara – negara industri seperti Eropa, Australia, dan lebih rendah di negara-negara Asia dan Afrika.1-3
Di Indonesia belum tersedia angka yang pasti berapa insidens karsinoma kolorektal, namun menurut Badan Registrasi Karsinoma Indonesia pada tahun 2009 jumlah keganasan pada kolorektal menduduki peringkat ketiga yaitu mencapai 9,92% dari seluruh karsinoma di Indonesia.4
Sebelum tahun 1990 dikenal adanya jalur karsinogenesis karsinoma kolorektal, yang diperkenalkan oleh Fearon-Vogelstein. Jalur tersebut dinamakan jalur adenoma-carsinoma sequence yang diawali oleh adanya sel atipik - adenoma displasia ringan - adenoma displasia keras - karsinoma kolorektal, yang melibatkan mutasi APC (adenomatous polyposis coli).5,6,7 Sepuluh tahun terakhir,
ditemukan jalur karsinogenesis baru oleh Longacre dan Fenoglio-Preiser yaitu
serrated pathways diawali oleh mutasi BRAF atau KRAS, dengan gambaran
morfologik aberrant crypt foci (ACF) - polip hiperplastik - serrated adenoma (SA) - karsinoma kolorektal. Proses karsinogenesis tersebut meliputi penurunan jumlah apoptosis dan peningkatan jumlah sel epitel, yang akan memberikan gambaran serrated dan dysmaturation crypt.8,9 Beberapa kepustakaan dikatakan serrated pathways dapat berkembang menjadi karsinoma kolorektal lebih cepat
dibandingkan dengan jalur adenoma-carsinoma sequence.9,10
Menurut klasifikasi WHO, dikenal beberapa lesi prekursor untuk karsinoma kolorektal, antara lain aberrant crypt foci (ACF), adenoma, dan
serrated lesions. ACF adalah adanya kelompokan kripta yang abnormal dan
menyerupai polip hiperplastik (PH). Polip hiperplastik (PH) sendiri merupakan polip dengan gambaran mikroskopik menunjukan sel epitel torak dengan inti dapat normal/atipik, sitoplasma mengandung musin, tetapi tidak terdapat displasia. Beberapa penelitian, membagi PH menjadi tiga subklasifikasi
berdasarkan komponen musinnya yaitu: jenis microvesicular ( paling sering ),
goblet cell rich type, dan mucin-poor type (jarang).5-7 Adenoma didefinisikan sebagai polip neoplastik dengan proliferasi kelenjar disertai gambaran histopatologik sel epitel bertumpuk/displasia dalam berbagai tingkatan dengan inti sel hiperkromatik dan membesar. Serrated lesions adalah lesi dengan gambaran
serrated (sawtooth or stellate) pada komponen epitelnya.11
Salah satu komponen penting pada lesi prekursor karsinoma kolorektal adalah adanya musin. Musin merupakan glikoprotein dengan berat molekul tinggi yang disintesis, disimpan dan disekresikan oleh sel epitel mukosa, khususnya sel goblet.12 Susunan molekul musin merupakan proses glikosilasi yang terbentuk
oleh ikatan tinggi rantai glukosa dengan asam amino serin dan treonin melalui ikatan oksigen. Ikatan tersebut mencegah kerusakan musin oleh enzim protease, dan dapat menjaga densitas dan viskositas molekul musin, sehingga musin sangat efektif melindungi lapisan mukosa saluran pencernaan.12 Sampai saat ini dikenal
20 gen musin serotipe pada lapisan epitel yang berbeda dan dapat diklasifikasikan menjadi dua kelompok yaitu secreted mucins dan membrane bound mucins. Serotipe gen musin yang berbeda-beda tergantung dari banyak sedikitnya kandungan serin dan treonin dengan ikatan glukosa.13
Musin yang tergolong dalam membrane bound mucins, salah satunya adalah Mucin-1 (MUC1) yang tersusun atas glikoprotein yang ekspresinya khas pada sel epitel torak mukosa lambung bagian apikal.14-18 Musin yang
dikelompokan dalam secreted mucins antara lain Mucin-2 (MUC2), Mucin-5AC (MUC5AC), Mucin-5B (MUC5B), dan Mucin-6 (MUC6) yang ditemukan pada kromosom 11p15.5. Ekspresi spesifik musin tersebut terdapat pada organ yang berbeda-beda, seperti Mucin-2 (MUC2) merupakan musin yang khas pada sel goblet usus besar, Musin-5AC (MUC5AC) pada mukosa trakeobronkhial dan lambung,19sedangkan Mucin-6 (MUC6) merupakan gen musin yang spesifik pada
mukosa sel epitel kelenjar lambung bagian antral/pilorus.18,19
Dekade terakhir ditemukan bahwa musin dapat mengalami perubahan pada tumor ganas.14,20,21 Musin berperan dalam proses diferensiasi dan proliferasi
sel tumor melalui interaksi ligan dan reseptor. Selain itu, musin juga berperan dalam transduksi sinyal dan proses invasi tumor yang menyebabkan rusaknya
ikatan antar sel/adhesi sel. Salah satu musin yang berperan dalam proses karsinogenesis kolorektal adalah Mucin-6 (MUC6) aberrant. Mucin-6 (MUC6) secara khusus akan terekspresikan pada epitel kelenjar lambung bagian antral/pilorus, oleh sebab itu MUC6 disebut juga sebagai musin tipe gastrik.22,23
Selain itu pula, ekspresi MUC6 aberrant yang tinggi dapat ditemukan pada ACF/serrated adenoma (SA) dan karsinoma kolorektal. Hal tersebut berbeda dengan ekspresi MUC6 aberrant pada lesi prekursor karsinoma lainnya seperti pada polip hiperplastik dan adenoma konvensional. Polip hiperplastik dan adenoma konvensional didapatkan ekspresi MUC6 aberrant yang lemah, atau bahkan tidak mengekspresikan MUC6 aberrant, disebabkan tidak terdapatnya gangguan mikrosatelit pada lesi ini.23,24 Ekspresi MUC6 aberrant pada lesi
prekursor karsinoma kolorektal khususnya serrated adenoma (SA), menggambarkan adanya gangguan mikrosatelit yang tinggi, yang menyebabkan perkembangan lesi prekursor tersebut menjadi karsinoma lebih cepat yaitu sekitar 8 bulan. Ekspresi MUC6 aberrant dilihat pada sitoplasma epitel kripta mukosa kolorektal terutama pada bagian basal/basolateral.24
Penelitian lainnya melaporkan tidak semua serrated adenoma (SA) mengekspresikan MUC6 aberrant pada sel epitel kripta mukosa kolorektal, dan dikatakan pula bahwa adenoma konvensional memiliki ekspresi MUC6 aberrant lebih lemah dibandingkan serrated adenoma (SA).25 Ditemukannya adanya
kontroversi tentang ekspresi MUC6 aberrant pada prekursor karsinoma kolorektal maka diperlukan penelitian lebih lanjut.23,25 Secara histopatologik polip dengan
gambaran serrated adenoma (SA) pada sediaan biopsi dan reseksi sering kali menyerupai polip hiperplastik yang bukan merupakan lesi prekursor. Beberapa penelitian mengatakan serrated adenoma (SA) mempunyai ekspresi MUC6
aberrant yang lebih tinggi dibandingkan dengan adenoma konvensional displasia
keras.23,25-29 Sampai saat ini di Indonesia, belum pernah dilakukan penelitian
tentang ekspresi Mucin-6 (MUC6) aberrant baik pada serrated adenoma (SA) dan adenoma konvensional displasia keras sebagai lesi prekursor karsinoma kolorektal. Penelitian yang dilakukan akan membandingkan ekspresi MUC6
aberrant pada serrated adenoma (SA) dan adenoma konvensional displasia keras,
adenoma konvensional displasia keras dapat membantu dalam menegakkan diagnosis polip tersebut.
I.2. Identifikasi Masalah
Hingga saat ini belum ada penanda yang dapat membedakan antara
serrated adenoma (SA) dan adenoma konvensional displasia keras yang telah
didiagnosis secara histopatologik sebagai lesi prekursor karsinoma kolorektal. Seiring dengan adanya ekspresi MUC6 aberrant sebagai penanda adanya gangguan mikrosatelit, yang terdapat pada serrated adenoma (SA), diharapkan ekspresi MUC6 aberrant dapat dijadikan penanda dalam membantu diagnosis
serrated adenoma (SA) dan adenoma konvensional displasia keras.
I.3. Pertanyaan Penelitian
Apakah ekspresi MUC6 aberrant pada serrated adenoma (SA) dan adenoma konvensional displasia keras berbeda?
I.4. Rumusan Hipotesis
Ekspresi MUC6 aberrant pada serrated adenoma (SA) lebih tinggi dibandingkan adenoma konvensional displasia keras.
I.5. Tujuan Penelitian
Mengetahui ekspresi MUC6 aberrant pada sitoplasma sel epitel kripta mukosa kolorektal terutama bagian basal pada serrated adenoma (SA) dan adenoma konvensional displasia keras.
I.6. Manfaat Penelitian
I.6.1. Manfaat di bidang akademis
Hasil penelitian ini diharapkan dapat menjadi tambahan pengetahuan dalam menegakkan diagnosis serrated adenoma (SA) dan adenoma konvensional displasia keras sebagai lesi prekursor karsinoma kolorektal, yang dihubungkan dengan ekspresi MUC6 aberrant.
I.6.2. Manfaat bidang profesi
Hasil penelitian ini diharapkan dapat membantu patolog dalam menegakkan diagnosis lesi serrated adenoma (SA) dan adenoma konvensional displasia keras sebagai lesi prekursor karsinoma kolorektal.
I.6.3. Manfaat di bidang pengabdian masyarakat
Dengan dibuktikan adanya ekspresi MUC6 aberrant yang lebih tinggi pada serrated adenoma (SA) dibandingkan dengan adenoma konvensional displasia keras, dapat membantu dalam penatalaksanaan awal pada kasus tersebut.
I.7. Kerangka Teori
Mukosa kolon normal
MUC6 aberrant (+)/↓ MUC6 aberrant (+)/↑ MSS,CIMP-L MSI –H,CIMP-H
Keterangan : APC (adenomatous polyposis coli), ACF (aberrant crypt foci), MVHP (microvesicular hyperplastic polyp), GCHP (goblet cell rich hyperplastic polyp), MPHP (mucin poor hyperplastic polyp), MSS (microsatellite stable), MSI-H (microsatellite instability –high), CIMP-L (CpG island methylator phenotype – low), CIMP-H (CpG island methylator phenotype – high)
APC KRAS Adenoma konvensional displasia ringan GCHP BRAF MVHP
Serrated adenoma (SA)
Adenoma konvensional displasia keras Karsinoma kolorektal Karsinoma kolorektal ACF MPHP ??
I.8. Kerangka Konsep
Kolon Normal
Serrated adenoma (SA) Adenoma konvensional
displasia keras
Mucin-6 (MUC6) aberrant di sitoplasma sel epitel kripta mukosa kolorektal
Ekspresi positif sedang-kuat
Ekspresi negatif-positif lemah
BAB II
TINJAUAN PUSTAKA
II.1. Usus Besar Normal II.1.1. Anatomi dan fisiologi
Usus besar merupakan saluran pencernaan yang terbagi dalam beberapa bagian yaitu appendiks, sekum, kolon asendens, transversum, desendens, sigmoid dan rektum.30 Makalah ini akan dibahas kolon dan rektum. Perkembangan masa
embriologik berbeda antara kolon sisi kanan dan kolon sisi kiri, yaitu midgut yang membentuk kolon kanan yang tersusun atas sekum, kolon desendens dan kolon transversum, sedangkan hindgut membentuk kolon sisi kiri yang tersusun atas kolon desendens, sigmoid dan rektum.29 Usus besar berperan sebagai organ
reservoir dan eliminasi materi yang tidak dicerna, serta mempunyai fungsi imunitas oleh folikel limfoid dan endokrin.29,30
Usus besar secara makroskopik merupakan organ berongga yang dimulai dari valvula ileosekal sampai anus dengan ukuran lebih kurang 140-150cm. Bagian awal kolon asendens adalah sekum, dengan appendiks/umbai cacing menempel pada bagian bawah sekum. Kolon asendens terletak retroperitoneal di sisi kanan sampai ke fleksura hepatika. Fleksura tersebut dihubungkan oleh kolon transversum sampai dengan fleksura lienalis.29
Kolon sisi kiri yang tersusun atas kolon desendens, sigmoid dan rektum mempunyai letak yang berbeda-beda. Kolon desendens terletak retroperitoneal, yang dimulai dari fleksura lienalis sampai ke kolon sigmoid, di abdomen sisi kiri, yang kemudian dilanjutkan dengan kolon sigmoid yang terletak intraperitoneal dengan jaringan mesokolon sigmoid. Area peralihan antara kolon dan rektum dinamakan rectosigmoid junction.
Lokasi organ rektum terbagi menjadi beberapa bagian yaitu sepertiga atas terletak intraperitoneal, sepertiga tengah terletak retroperitoneal, sedangkan sepertiga bawah terletak pada subperitoneal. Jaringan pengantung rektum dinamakan mesorektum yang mengelilingi rektum, dan mengandung banyak kelenjar getah bening, terutama pada bagian retroperitoneal dan subperitoneal. Bagian inilah yang digunakan dalam menentukan batas sayatan melingkar pada
operasi mesorektal total baik pada karsinoma kolorektal maupun pada lesi prekursor karsinoma kolorektal yang berukuran besar.29
Usus besar bagian luar terdapat pita otot eksternal yang berjalan longitudinal sepanjang penampang usus besar yang dinamakan taenia coli dan menyebabkan organ usus besar terbagi-bagi (haustra). Seluruh bagian usus besar terdapat taenia coli kecuali appendiks dan rektum. Lipatan mesenterik yang dibentuk oleh lapisan mukosa dan submukosa memanjang kearah lumen, yang berada diantara haustra dinamakan plika semilunaris, selain itu terdapat
appendices apiploicae yang merupakan lemak subserosa, terletak pada permukaan
luar usus.29
Aliran darah pada kolon kanan dan kolon kiri berbeda, kolon kanan diperdarahi oleh arteri mesenterika superior melalui arteri ileokolika, arteri kolika kanan dan kiri, sedangkan kolon kiri mendapatkan aliran darah berasal dari arteri mesenterika inferior melalui arteri kolika inferior dan arteri rektal inferior. Aliran pembuluh darah vena pada kolon sisi kanan melalui vena mesenterika superior dan kolon sisi kiri melalui vena mesenterika inferior, yang keduanya merupakan bagian sistem portal dengan aliran darah langsung menuju ke hepar. Usus besar mempunyai aliran limfatik yang berasal dari kelenjar getah bening parakolika dan kelenjar getah bening pararektal yang terletak pada dinding usus besar, dan alirannya mengikuti aliran darah.29
Persarafan usus besar dibagi menjadi 2 yaitu sistem saraf simpatis dan parasimpatis. Bagian kolon yang dipersarafi oleh saraf simpatis terbagi menjadi 2 bagian yaitu dua pertiga kolon sisi kanan dipersarafi oleh ganglion mesenterika superior, sedangkan sepertiga kolon sisi kiri dipersarafi oleh ganglion mesenterika inferior. Peran sistem saraf simpatis adalah menghambat motilitas dan mengurangi aliran darah ke lapisan mukosa usus besar, sedangkan sistem saraf parasimpatis mempunyai peran menstimulasi akitivitas motorik. Secara garis besar kolon dibagi menjadi 3 bagian yaitu kolon kanan, kolon kiri dan rektum serta anus. Saraf yang mempersarafi kolon kanan adalah nervus vagus, kolon kiri oleh nervus postganglionik pelvika, sedangkan pada rektum dan anus, persarafan simpatis oleh ganglion hipogastrika.29
II.1.2. Histologik
Secara garis besar, organ kolon mempunyai 4 lapisan yang tersusun dari lapisan luar sampai dalam yaitu lapisan mukosa, submukosa, muskularis propria dan serosa. Lapisan mukosa terdiri atas tiga komponen, yaitu epitel permukaan, lamina propria dan muskularis mukosa, yang berfungsi mengabsorbsi air dan lubrikasi materi fekalit. Lapisan mukosa tersusun atas dua jenis sel yaitu sel absorbtif dan sel goblet. Sel-sel tersebut tersusun berdekatan dengan struktur tubular, yang kemudian disebut sebagai kripta (Lieberkuhn). Kripta kolon kanan dan transversum didominasi oleh sel absorbtif sedangkan kolon kiri lebih didominasi oleh sel goblet.29,30
Sel absorbtif berfungsi sebagai penyerapan air dan elektrolit, dengan gambaran mikroskopik inti oval, dengan ukuran relatif monoton, terletak dibagian basal, yang sebagian mempunyai anak inti, dengan sitoplasma eosinofilik. Sedangkan sel goblet berfungsi untuk sintesis, penyimpanan dan mensekresi mukus. Gambaran mikroskopik sel goblet serupa dengan sel absortif yaitu berinti dibasal dengan sitoplasma bergranul.29
Sel epitel yang melapisi kripta adalah sel epitel torak selapis yang tersusun atas sel absortif, sel goblet, sel prekursor imatur, disertai dengan sel endokrin dan sel paneth. Sel epitel kripta berfungsi dalam perbaikan epitel permukaan, yang membutuhkan waktu 3-8 hari.Stroma mukosa kolon dibentuk oleh lamina propria dan muskularis mukosa. Sel-sel yang ditemukan pada lamina prorpia antara lain sel plasma, limfosit, fibroblast dan makrofag. Lapisan lamina propria pada kolon sisi kanan lebih seluler, dengan banyak mengandung sel plasma dan eosinofil, dibandingkan dengan kolon sisi kiri dan rektum.29
Lapisan otot yang memisahkan mukosa dan submukosa dinamakan muskularis mukosa, dan pada lapisan ini ditemukan adanya pleksus saraf mukosa (meissner) dengan struktur pembuluh darah yang tersusun atas arteriol, venula dan sistem limfatik.Lapisan muskularis propria merupakan lapisan otot polos dengan serabut otot yang berjalan sirkuler disebelah dalam, dan berjalan longitudinal disebelah luar. Lapisan muskularis propria ditemukan pleksus saraf mienterikus (Auerbach).Lapisan serosa dilapisi mesotel dengan jaringan ikat di sekitarnya.29,30
II.1.3. Musin sebagai komponen penting pada epitel kolorektal
Musin merupakan glikoprotein dengan berat molekul tinggi yang disintesis, disimpan dan disekresikan oleh sel epitel mukosa, khususnya sel goblet. Susunan molekul musin merupakan proses glikosilasi yang terbentuk oleh ikatan tinggi rantai glukosa dengan asam amino serin dan treonin melalui ikatan oksigen. Ikatan tersebut mencegah kerusakan musin oleh enzim protease, dan dapat menjaga densitas dan viskositas molekul musin, sehingga musin sangat efektif melindungi lapisan mukosa saluran pencernaan.12-18
Sampai saat ini dikenal 20 gen musin serotipe pada lapisan epitel yang berbeda yang kemudian diklasifikasikan menjadi dua kelompok yaitu secreted
mucins dan membrane bound mucins. Serotipe gen musin yang berbeda-beda
tergantung dari banyak sedikitnya kandungan serin dan treonin dengan ikatan glukosa. Musin yang tergolong dalam membrane bound mucins, salah satunya adalah Mucin-1 (MUC1) yang tersusun atas glikoprotein yang ekspresinya khas pada sel epitel torak mukosa lambung bagian apikal.19,21,24 Musin yang
dikelompokan dalam secreted mucins antara lain Mucin-2 (MUC2), Mucin-5AC (MUC5AC), Mucin-5B (MUC5B), dan Mucin-6 (MUC6) yang ditemukan pada kromosom 11p15.5. Ekspresi spesifik musin tersebut terdapat pada organ yang berbeda-beda, seperti Mucin-2 (MUC2) merupakan musin yang khas pada sel goblet usus besar, Musin-5AC (MUC5AC) pada mukosa trakeobronkhial dan lambung,19,21,24 sedangkan Mucin-6 (MUC6) merupakan gen musin yang spesifik
pada mukosa sel epitel kelenjar lambung bagian antral/pilorus.21,23,24,26,29
Beberapa penelitian menunjukan adanya ekspresi MUC6 aberrant yang diregulasi oleh NFkB, yang merupakan faktor transkripsi inti dalam keadaan inflamasi seperti pada proses peradangan, regeneratif dan penyakit inflamatorik saluran gastrointestinalis. Mukosa kolon normal, tidak akan mengekspresikan MUC6, namun bila terdapat proses karsinogenesis melalui serrated pathways, maka MUC6 dapat terekspresikan (ekspresi MUC6 yang aberrant).23,24
Beberapa penelitian, menunjukkan bahwa ekspresi MUC6 yang aberrant terdapat pada sitoplasma sel epitel kelenjar di bagian basal/basolateral lapisan mukosa kolorektal pada serrated adenoma (SA), yang berbeda ekspresinya pada adenoma konvensional displasia keras.
II.2. Polip Hiperplastik (PH) II.2.1. Definisi
Polip hiperplastik (PH) secara umum berbentuk pedunculated dengan gambaran mikroskopik menunjukan proliferasi kelenjar yang dilapisi epitel torak dengan inti normal/atipik, sitoplasma mengandung musin, tetapi tidak ditemukan adanya displasia. Sebelum tahun 1990 lesi tersebut dikenal sebagai lesi non maligna, namun kemudian PH dapat mengalami gangguan mikrosatelit yang rendah, sehingga memungkinkan untuk berkembang menjadi lesi neoplastik.9,11,
II.2.2. Etiologi
Penyebab polip hiperplastik belum diketahui, namun dipengaruhi oleh beberapa faktor seperti diet, gaya hidup dan adanya peradangan pada saluran pencernaan. Polip hiperplastik juga bisa disebabkan adanya mutasi BRAF/KRAS, dan gangguan mikrosatelit yang menurut WHO terbaru, polip hiperplastik saat ini dibagi menjadi microvesicular hyperplastic polyp (MVHP), goblet cell rich
hyperplastic polyp (GCHP), dan mucin poor hyperplastic polyp (MPHP).9,10,11
II.2.3. Masalah klinik
Polip hiperplastik secara umum tidak menimbulkan gejala klinik, namun dapat pula menimbulkan gejala diare, dan bila polip berukuran besar dapat menimbulkan perdarahan saluran pencernaan.8,9
II.2.3.1. Epidemiologi
Jumlah lesi polip hiperplastik non neoplastik lebih kurang 75% dari keseluruhan polip, sedangkan 15-20% diantaranya merupakan polip hiperplastik yang neoplastik.8,9
II.2.3.2. Lokasi
Lokasi polip hiperplastik biasanya pada kolon sisi kiri yaitu kolon desendens, kolon sigmoid dan rektum. Polip hiperplastik dapat berlokasi pada kolon kanan yaitu kolon asendens dan kolon transversum namun dalam jumlah yang lebih sedikit dan berukuran lebih besar.9
II.2.3.3. Pemeriksaan endoskopik
Makroskopik umumnya berbentuk pedunculated, dengan tiga perempat kasus memiliki ukuran diameter 0,5cm sedangkan pada seperempat dari kasus tersebut memiliki ukuran diameter >1,5cm.11
II.2.3.4. Perjalanan penyakit
Polip hiperplastik kolorektal secara umum merupakan lesi non neoplastik, yang dapat diawali oleh peradangan, namun demikian polip hiperplastik dapat pula berubah menjadi lesi neoplastik bila terdapat mutasi BRAF/KRAS. Perkembangannya menjadi karsinoma kolorektal dapat melalui jalur serrated
pathways. Selain itu juga ditemukan adanya polip hamartoma yaitu juvenile polyp
dan Peutz-Jeghers polyp yang disebabkan oleh adanya mutasi pada gen SMAD4/DPC4 pada kromosom 18q21 dan serin threonin kinase tumor
suppressor gene pada kromosom 19p13.3. Polip hamartoma tersebut dapat pula
berkembang menjadi karsinoma kolorektal melalui jalur
hamartomatous-adenoma-carsinoma sequence.1,9-11
II.2.3.5. Terapi
Penatalaksaan secara umum, dilakukan kolonoskopi setiap 1-3 tahun, dan dapat disertai dengan polipektomi tergantung dari jumlah dan ukuran polip. Polip dengan ukuran kurang dari 3-4 mm, dapat diobservasi, namun untuk polip dengan ukuran yang lebih besar, sebaiknya dilakukan polipektomi.1
II.2.3.6. Prognosis
Prognosis baik, bila lesi diketahui sedini mungkin dan dilakukan penatalaksanaan yang tepat. Batts et al. lesi polip hiperplastik dengan ukuran < 1cm, dapat dilakukan observasi, dengan polipektomi, sedangkan lesi dengan ukuran > 1 cm dapat dilakukan reseksi.1
II.2.4. Gambaran mikroskopik II.2.4.1. Gambaran histopatologik
Polip hiperplastik (PH) menunjukkan gambaran mikroskopik sepertiga kripta bagian bawah menyempit yang dilapisi sel epitel torak dengan sebagian dapat mengalami proliferasi atipik/normal, dan sebagian kripta berbentuk memanjang secara teratur ke bagian permukaan. Mitosis biasanya terdapat pada bagian basal. Tampak pula arsitektur kelenjar yang tersusun atas epitel berinti kecil dibagian basal, monoton, dengan sitoplasma mengandung musin, terdapat sel goblet tetapi tidak terdapat gambaran sitologi displasia. (gambar 1)9
II.2.4.2. Komponen musin
Polip hiperplastik (PH) berdasarkan komponen musinnya dibagi menjadi 3 tipe yaitu microvesicular hyperplastic polyps (MVHP), goblet cell rich
hyperplastic polyps (GCHP) dan mucin poor types hyperplastic polyp (MPHP).
Perbedaan subtipe didasarkan pada perbedaan demografik dan molekulernya. Polip hiperplastik yang tersering adalah polip hiperplastik subtipe mikrovesikular. Gambaran histopatologik secara umum yaitu kripta memanjang dengan proliferasi epitel pada sepertiga bawah dan bervariasi, disertai gambaran bergerigi.
Microvesicular hyperplastic polyp (MVHP) mempunyai gambaran histopatologik
sel epitel permukaan mikrovesikular yang berisi musin, dengan atau tanpa sel goblet. Goblet cell hyperplastic polyp (GCHP) menunjukan jumlah sel goblet yang banyak. Pada kedua tipe tersebut tidak menunjukan gambaran atipia yang nyata. Sedangkan pada mucin poor hyperplastic polyp (MPHP) menunjukan musin yang sedikit, dan dapat ditemukan adanya inti sel atipik. Mucin poor
Gambar II.1. Polip hiperplastik (PH). A dan B. Kripta pada mukosa usus besar dengan inti sel kecil dan padat di bagian bawah lamina propria, dengan pelebaran kripta dibagian permukaan (pembesaran 100x).1
II.2.4.3 Ekspresi pulasan MUC6 aberrant pada polip hiperplastik
Polip hiperplastik disebut juga sebagai polip metaplastik, dikarenakan terdapat metaplasia gastrik. Ekspresi MUC6 aberrant sering ditemukan pada penyakit gastrointestinal yang berhubungan dengan proses regeneratif yang kemudian menjadi ulkus dan peradangan. Salah satu penelitian menemukan adanya mucin-6 (MUC6) diregulasi oleh NFkB, yang merupakan faktor transkripsi. Pada suatu penelitian ditemukan ekspresi MUC6 aberrant yang positif pada serrated adenoma (SA) dengan ukuran yang lebih besar maupun pada lesi
serrated adenoma (SA) dengan ukuran 3-4 mm, yang serupa dengan ukuran polip
hiperplastik, sedangkan pada polip hiperplastik tidak mengekspresikan MUC6. Pada penelitian lainnya ditemukan ekspresi MUC6 positif pada 16 kasus dari 92 kasus polip hiperplastik. Owens et al. melaporkan spesifisitas 100% pada ekspresi mucin-6 (MUC6) yang dapat membedakan antara sessile serrated adenoma (SSA) dibandingkan pada polip hiperplastik. Persinel et al. mengatakan bahwa tidak ditemukannya ekspresi Mucin-6 (MUC6) pada polip hiperplastik dan mukosa kolon normal.23 Namun kenyataannya, tidak semua kripta bagian basal pada serrated adenoma (SA) yang mengekspresikan MUC6 yang positif. Hal tersebut
yang menyebabkan diagnosis morfologik kripta bagian basal tidak menggambarkan sel punca yang dapat berkembang menjadi serrated adenoma (SA). Batts et al. menemukan adanya pertumbuhan ke dalam dari epitel
permukaan yang dapat dilihat pada serrated adenoma (SA), yang kemungkinan dapat menjelaskan ekspresi MUC6 yang kurang pada sejumlah kripta dibagian basal.23
II.3. Serrated adenoma (SA) II.3.1. Definisi
Serrated Adenoma (SA) didefinisikan sebagai polip yang menunjukkan
pola pertumbuhan serrated (saw-tooth architecture) yang mencolok, dengan gambaran displasia pada inti sel epitel yang tidak nyata.10,11
II.3.2. Etiologi
Serrated adenoma (SA) diawali adanya mutasi gen BRAF atau KRAS,
yang kemudian dapat mengalami gangguan mikrosatelit yang tinggi/microsatellite
instability-high (MSI-H) dan berkembang menjadi karsinoma kolorektal melalui serrated pathways.10,11,31
II.3.3. Masalah klinik
Jarang menimbulkan gejala klinik, disebabkan polip yang berukuran kecil biasanya 5 mm, namun pada sekitar 20% serrated adenoma (SA) ditemukan dengan ukuran 1 mm3 dan berbentuk sessile, flat/carpet-like.1,10,11
II.3.3.1. Epidemiologi
Jumlah kasus serrated adenoma sekitar 15-25% kasus dari keseluruhan kasus polip, dan pada salah satu penelitian prospektif, ditemukan 9% kasus
serrated adenoma (SA) yang ditemukan secara tidak sengaja pada pemeriksaan
kolonoskopi.32
II.3.3.2. Lokasi
Serrated adenoma (SA) lebih banyak terdapat pada kolon sisi kanan
(kolon asendens dan kolon transversum) dibandingkan dengan kolon sisi kiri (kolon desendens, kolon sigmoid dan rektum).10,11
II.3.3.3. Pemeriksaan endoskopik
Gambaran serrated adenoma (SA) secara endoskopik sangat beragam, pada umumnya dengan ukuran 0,5cm. Serrated adenoma (SA) dapat ditemukan dalam bentuk pedunculated disebut traditional serrated adenoma (TSA) sekitar 63%, sessile disebut sessile serrated adenoma (SSA) 29% dan flat atau carpet-like disebut flat adenoma sejumlah 8%.11,32
II.3.3.4. Perjalanan penyakit
Patogenesis pada serrated adenoma (SA) belum diketahui dengan pasti, namun diduga perkembangannya berasal dari polip hiperplastik/serrated polyp (SP) melalui serrated pathways. Serrated pathways diawali adanya mutasi BRAF/KRAS dengan gambaran morfologik awalnya aberrant crypt foci –
serrated polyp/polip hiperplastik - serrated adenoma (SA) yang dapat langsung
berkembang menjadi karsinoma kolorektal. Proses SP menjadi SA memiliki tingkat metilasi sebesar 65%, sedangkan pada proses SP menjadi adenoma konvensional tingkat metilasinya hanya sebesar 18%. Yang et al. mengatakan bahwa mutasi BRAF dapat ditemukan pada microvesicular hyperplastic polyp (MVHP) dan SA. Sementara itu pada adenoma konvensional hanya sepertiga kasus yang mengalami mutasi BRAF.11 Higuchi et al dan Oh et al. telah
menunjukkan bahwa hilangnya ekspresi gen MGMT sebesar 17-26%, dianggap sebagai hasil dari metilasi DNA yang tinggi pada SA bila dibandingkan dengan polip hiperplastik.11
II.3.3.5. Terapi
Penatalaksanaan pada serrated polyp menurut Batts et al. sebagai berikut:
• Lesi serrated polyp dengan ukuran <1cm, dilakukan eksisi secara endoskopik/polipektomi secara lengkap, dan dapat dilakukan follow up berkala bila terdapat indikasi bahwa polip ditemukan dalam jumlah banyak dan berhubungan dengan resiko karsinoma kolorektal.
• Lesi serrated polyp dengan ukuran yang lebih besar, dapat dilakukan polipektomi, dengan memperhatikan batas sayatan bila lesi tersebut memiliki batas yang tidak nyata, dan dapat pula dilakukan reseksi
segmental, jika pada endoskopik menggambarkan kecurigaan keganasan.32-35
II.3.3.6. Prognosis
Prognosis SA baik, bila dilakukan penatalaksaan yang tepat. Serrated
adenoma dapat berkembang menjadi karsinoma kolorektal dengan interval waktu
yang berbeda-beda, sebagian besar serrated adenoma (SA) akan berkembang menjadi karsinoma kolorektal dalam interval waktu 5 tahun sekitar 90% kasus, bahkan dibeberapa kasus perkembangannya menjadi karsinoma kolorektal bisa sangat singkat yaitu sekitar 8 bulan.10
II.3.4. Gambaran mikroskopik II.3.4.1. Gambaran histopatologik
Mikroskopis serrated adenoma (SA) dengan pembesaran kecil, tampak kelompokan kripta yang berbentuk seperti buah pir, kripta berbentuk horizontal, berdilatasi, konfigurasi kuboid, dan dapat ditemukan kripta yang bercabang dibagian basal. Kelompokan kripta tersebut dapat menyerupai huruf T terbalik atau huruf L diatas lapisan muskularis mukosa, (gambar 2)9,10 dan kripta tersebut
cenderung menyempit di bagian tengah dan melebar di bagian permukaan. Pola
serrated/saw tooth appearance dapat terlihat baik pada lapisan permukaan atau
basal kripta, dengan sel-sel yang berinti seperti displasia. (gambar 3A,B)9 Seluruh
kripta dilapisi oleh epitel torak selapis, dengan terdapat sel goblet yang distrofik terutama pada bagian basal kripta. Seluruh sel pada kripta tersebut mempunyai fenotif menyerupai sel foveolar lambung yang berbentuk bergerigi pada seluruh lapisan kripta.9
Serrated adenoma (SA) dengan inti sel epitel torak hiperkromatik
dengan sebagian terdapat anak inti, serta terstatifikasi pada seluruh bagiannya (gambar 3C). Mitosis pada serrated adenoma (SA) jarang ditemukan walaupun mitosis dari kripta pertengahan ke bagian atas sering terlihat.9,10
Gambaran sitologi “displasia” tidak diperlukan untuk mendiagnosis SA, karena SA mempunyai arsitektur “displasia yang unik” dengan proliferasi epitel yang abnormal (gambar 3). Cara termudah mengenali SA melalui reseksi atau spesimen polipektomi, sedangkan sediaan yang berasal dari biopsi jaringan agak sulit dikenali
dikarenakan adanya artefak, dan bila biopsinya tidak tepat, sehingga banyak ditemukan lapisan mukosa kolon normal. Goldstein et al. pada tahun 2003 melaporkan lokasi untuk SA yaitu pada kolon asenden 70%, sekum 23%, kolon transversum 6%.8
Gambar II.2. A. Percabangan kripta (↓), bentuk kripta seperti huruf T dan L terbalik (↓)
(pembesaran 2,5x). B. Kripta sepertiga bawah tampak bercabang (↓), kripta inverted
dibawah muskularis mukosa(↓)( pembesaran 2,5x).1
Gambar II.3. Sessile serrated adenoma (SSA). A. Serrated adenoma (SA) kripta basal
melebar, bercabang. (pembesaran 200x) B. SSA terdiri dari mukosa datar dengan kripta berbentuk labu atau pir, dengan gambaran displasia yang tidak nyata. (pembesaran 100x) C. Percabangan di kripta bagian basal. (pembesaran 100x)1
II.3.4.2. Ekspresi pulasan MUC6 aberrant pada serrated adenoma (SA)
Beberapa kepustakaan mengatakan bahwa ekspresi MUC6 aberrant dapat merupakan penanda serrated adenoma (SA) dengan mutasi BRAF, gangguan mikrosatelit yang tinggi dan CIMP-H. Penelitian Owens et al. melaporkan MUC6
aberrant dapat digunakan sebagai penanda, untuk membedakan antara sessile serrated adenoma dengan polip hiperplastik dengan spesifisitas 100%, sedangkan
pada penelitian mochizuka et al. ditemukan ekspresi MUC6 sebesar 27% kasus polip hiperplastik dan 76% pada kasus sessile serrated adenoma. Penelitian lainnya ditemukan ekspresi MUC6 aberrant pada 23 kasus dari 43 kasus sessile
serrated adenoma (53%), dan pada 2 kasus dari 11 kasus traditional serrated adenoma (18%).19,23-26
II.4. Adenoma Konvensional Kolorektal II.4.1. Definisi
Adenoma konvensional merupakan lesi neoplasma intraepithelial yang dilapisi oleh epitel torak yang bertumpuk/displasia dengan inti sel hiperkromatik dan membesar, yang merupakan lesi prekursor karsinoma kolorektal.11
II.4.2. Etiologi
Adenoma konvensional disebabkan oleh berbagai faktor seperti faktor genetik, atau adanya mutasi gen APC. Adenoma konvensional dapat berkembang menjadi karsinoma kolorektal melalui jalur karsinogenesis adenoma-carsinoma
sequence.10,11 Jalur tersebut ditemukan oleh Fearon-Vogelstein yang diawali oleh
sel atipik – adenoma displasia ringan- adenoma displasia keras – karsinoma kolorektal. Selain itu, adanya mutasi gen supresor tumor APC dapat ditemukan pula pada 80% kasus karsinoma kolorektal sporadik, adenoma dan familial
adenomatous polyposis (FAP).11
II.4.3. Masalah klinik II.4.3.1. Epidemiologi
Lesi adenoma ditemukan sekitar 70% kelainan kolorektal, dengan 6 % kasus diantaranya dapat berkembang menjadi karsinoma kolorektal. Adenoma lebih banyak diderita oleh laki-laki, dibandingkan perempuan (2:1).11,36,37
Prevalensi adenoma konvensional dibeberapa negara berbeda-beda, seperti di negara barat prevalensinya mencapai 50%, namun prevalensi adenoma konvensional di Indonesia masih belum diketahui dengan pasti.11,37 Prevalensi lesi
adenoma konvensional akan meningkat dengan bertambahnya usia, pada usia 50 tahun prevalensinya sekitar 20-30%, sedangkan pada usia 60 tahun prevalensinya mencapai 50%.11
II.4.3.2. Lokasi
Lokasi adenoma konvensional secara umum merata diseluruh kolon dan rektum, namun secara khusus ditemukan lebih banyak didaerah rektosigmoid/kolon sisi kiri, yaitu kolon desendens dan sigmoid, sekitar 60-70%.11
II.4.3.3. Gambaran klinik
Umumnya adenoma konvensional tidak memberikan gejala klinik, khususnya pada lesi dengan ukuran kecil, yaitu <1cm, namun pada lesi adenoma konvensional dengan ukuran >1cm, dan berbentuk pedunculated sering menimbulkan gejala konstipasi, bahkan menimbulkan perdarahan per rektum. Resiko perdarahan per rektum akan meningkat dengan bertambahnya ukuran adenoma.11
Adenoma konvensional dengan ukuran besar, dapat pula menimbulkan gejala konstipasi, defisiensi besi, invaginasi, prolaps intususepsi, bahkan sampai terjadi obstruksi usus sebagian/parsial. Beberapa kepustakaan menuliskan bahwa adenoma yang terbanyak adalah adenoma konvensional dengan struktur villosum, berukuran besar, dan terletak pada kolon sisi kiri. Adenoma konvensional tersebut dapat pula menimbulkan gejala klinik diare dan hipokalemia.11
II.4.3.4. Pemeriksaan endoskopik
Pemeriksaan yang baik untuk mendeteksi adanya polip/ adenoma adalah pemeriksaan endoskopik. Pemeriksaan ini dapat mengetahui ukuran dan bentuk dari polip/adenoma. Makroskopik adenoma konvensional secara umum adalah
pedunculated, sekitar 60% berukuran kurang dari 1 cm, dan 30% berukuran >1.5
cm, dengan mukosa pada adenoma lebih merah, bahkan dapat ulserasi dibandingkan dengan jaringan sekitarnya. Berdasarkan morfologinya adenoma tubular berbentuk pedunculated/bertangkai, sedangkan adenoma villosum berbentuk flat atau carpet-like tanpa adanya tangkai.17 Sebagian kecil kasus
adenoma konvensional (sekitar 25%) berukuran <5cm, dan berlokasi di kolon sisi kanan, yang sering ditemukan pada endoskopik secara tidak sengaja.32,34
Pemeriksaan endoskopik dapat digunakan sebagai skrining dan follow-up pada adenoma konvensional, sehingga dapat dilakukan penatalaksanaan yang tepat, dan dapat menurunkan insidens karsinoma kolorektal sebesar 70-90%.32,34
II.4.3.5. Perjalanan penyakit
Adenoma konvensional merupakan lesi prekursor karsinoma kolorektal, dan dapat mengalami pertambahan ukuran dengan berjalannya waktu, dan sekitar 5-10% kasus adenoma yang akan berlanjut menjadi karsinoma kolorektal.11
Adenoma konvensional dapat bertransformasi menjadi karsinoma kolorektal, dan membutuhkan waktu lebih kurang sepuluh tahun. Faktor-faktor yang menyebabkan adenoma konvensional merupakan lesi prekursor karsinoma kolorektal adalah memiliki distribusi lokasi yang sama dan sering terjadi secara bersamaan, adanya korelasi epidemiologik dan faktor resiko, terdapat area transisi, serta ditemukannya defek molekuler.11
II.4.3.6. Terapi
Penatalaksanaan adenoma dengan polipektomi, tanpa memperhatikan ukuran, derajat displasia dan ada tidaknya komponen villosum, selain itu bila didapatkan batas lesi/adenoma yang tidak nyata, dapat dilakukan reseksi segmental/parsial.11,37,38
II.4.3.7. Prognosis
Prognosis pada adenoma konvensional ditentukan oleh beberapa faktor, yaitu usia penderita, ukuran lesi/tumor, bentuk adenoma, derajat displasia. Kasus adenoma konvensional dengan karakteristik lesi multiple, berukuran lebih dari 1cm, dengan jumlah komponen villosum >75%, derajat displasia keras dan penderita berusia diatas 60 tahun akan meningkatkan resiko keganasan menjadi 27% dalam waktu 15 tahun, sedangkan adenoma konvensional dengan karakteristik lesi tunggal, usia dibawah 60 tahun, dengan ukuran kurang dari 1
mm, dengan derajat displasia ringan, mempunyai resiko keganasan sebesar 5% dalam waktu 15 tahun.38
Perkembangan adenoma konvensional displasia ringan menjadi displasia keras, juga dipengaruhi oleh ukuran lesi, dimana bila ukuran lesi < 5mm, maka kemungkinan perkembangannya menjadi displasia keras sebesar 1%.19 Beberapa kasus adenoma konvensional dapat pula ditemukan bersamaan dengan karsinoma kolorektal pada saat diagnosis. Ukuran adenoma dapat digunakan memperkirakan kemungkinan berkembangnya adenoma menjadi karsinoma kolorektal, yaitu bila ukuran adenoma > 2 cm, maka resikonya sebesar 10-20%, ukuran 1-2 cm resiko 5%, dan bila ukuran adenoma < 1 cm maka resikonya sebesar 1%.10,11,38-40
Sekitar 30 % kasus adenoma konvensional ditemukan dalam bentuk lesi
multiple (lebih dari 3). Prevalensi pada adenoma multiple juga meningkat sesuai
dengan bertambahnya usia, yaitu 9% pada usia < 60 tahun, 17% pada usia 60-73 tahun, dan 28% pada usia diatas 75 tahun.11
II.4.4. Gambaran mikroskopik II.4.4.1. Gambaran histopatologik
Adenoma konvensional didiagnosis berdasarkan perubahan gambaran sitologik dan arsitektur. Perubahan sitologik meliputi peningkatan rasio inti dan sitoplasma, hiperkromatik (adanya peningkatan aktivitas DNA), pleomorfisme inti (variasi bentuk dan ukuran inti), peningkatan jumlah mitosis, dan adanya mitosis atipik.9-11 Perubahan arsitektur kelenjar meliputi inti bertumpuk dengan bentuk
kelenjar yang kompleks.11
Gambaran mikrokopisnya dapat berbentuk tubuler atau villosum, dengan pembesaran kecil memiliki kripta adenomatosa, yang ditandai inti membesar dan bertumpuk pada bagian mukosa permukaan dengan pola pertumbuhan top-down.11
Gambaran morfologik pada adenoma konvensional tidak terdapat adanya epitel dengan pola serrated/ bergerigi. Kripta adenoma konvensional akan mengalami perubahan dari kripta pada mukosa kolon normal menjadi kripta adenomatosa yang menebal, dengan bentuk sel goblet yang bervariasi baik di basal maupun di permukaan.(gambar 4) Sitoplasma adenoma konvensional adalah basofilik. Mitosis dan apoptosis inti dari adenoma konvensional juga sering
terdistribusi merata dari basal ke permukaan. Terminologi patologis yang digunakan untuk subklasifikasi adenoma konvensional berdasarkan arsitektur dari sepertiga sampai setengah bagian kripta adenomatosa, bisa berbentuk villi, tubuler atau kedua-duanya. (gambar 4,5)10,11
II.4.4.2. Komponen villosum
Berdasarkan persentase struktur morfologi villosum, adenoma dibedakan menjadi 3 tipe histologik, yaitu tubuler, villosum, tubullovillosum. Adenoma tubuler (70-90% kasus) memiliki komponen villosum kurang dari 25%. Arsitektur tubuler pada lapisan mukosa tetap dipertahankan. Makroskopik adenoma tubular pada umumnya pedunculated, dan memiliki resiko keganasan sebesar 2-3%.10,11
Adenoma tubulovillosum (10-25% kasus) memiliki komponen villosum antara 25-75%, dan memiliki resiko keganasan menengah, sedangkan pada adenoma villosum (5%) kasus yang tersusun atas 75% komponen villosum ( epitel displastik yang memanjang seperti jari-jari, panjangnya dua kali ketebalan mukosa kolon normal ). Makroskopik adenoma villosum umumnya sessile, dan 30% kasus adenoma villosum ditemukan dalan derajat displasia keras, yang dapat didiagnosis bersamaan dengan karsinoma kolorektal.(gambar 4,5)10,11
II.4.4.3. Derajat displasia
Adenoma konvensional berdasarkan derajat displasianya dibagi menjadi 2 yaitu displasia ringan (displasia ringan dan sedang) dan displasia keras, berdasarkan kombinasi komponen sitologik dan arsitektur kelenjarnya. Adenoma konvensional displasia ringan ditemukan kelompokan kripta dengan epitel torak dengan inti yang bertumpuk/displasia kurang dari setengah ketebalan epitel permukaan, dan sebagian tersusun parallel, dengan kelenjar yang ditemukan back
to back, atau berbentuk kribriformis. Mitosis dapat ditemukan, dengan
pleomorfisme minimal.11
Adenoma konvensional displasia keras ditemukan kelompokan kripta dilapisi epitel torak selapis dengan inti yang displastik/bertumpuk sampai melebihi setengah epitel permukaan. Tampak pula inti bulat yang pleomorfik, kromatin kasar dan anak inti nyata, dengan peningkatan rasio inti terhadap
sitoplasma, sitoplasma eosinofilik. Gambaran mitosis pada adenoma konvensional merupakan mitosis atipik. Tampak pula adanya perubahan arsitektur kelenjar dapat berupa back to back maupun berupa sarang-sarang solid, namun tidak ditemukannya invasi membran basalis.11
Sistem klasifikasi displasia ini yang digunakan oleh WHO karena dapat digunakan untuk mengurangi variasi antar pengamat dalam interpretasi displasia oleh ahli patologi dan meningkatkan relevansi dan menghindari interpretasi berlebihan secara klinik dalam pilihan terapi.34
Gambar II.4. Adenoma tubular terdiri dari epitel torak yang memanjang dengan inti sel
hiperkromatik, dengan pertumbuhan top-down (pembesaran 40x), bentuk uniform, inti terstratifikasi, tanpa adanya bentuk serrated. (pembesaran 200x).1,41
Gambar II.5. Adenoma villosum, dengan inti sel displastik, uniform, hiperkromatik
(pembesaran 40x), dengan gambaran selular dan tidak terdapat gambaran serrated (pembesaran 200x).1,41
II.4.4.4. Ekspresi pulasan MUC6 aberrant pada adenoma konvensional.
Mucin-6 (MUC6) secara normal tidak terekspresikan pada mukosa kolon yang normal, namun pada adenoma konvensional dapat ditemukan adanya ekspresi MUC6 aberrant de novo yang merupakan penanda transformasi keganasan pada epitel kolorektal. Beberapa penelitian mengatakan ekspresi MUC6 aberrant pada adenoma konvensional belum diketahui dengan jelas mekanisme molekulernya, namun diduga dapat disebabkan oleh perubahan metilasi dan regulasi transkripsi. Bartley et al. menuliskan ditemukannya ekspresi MUC6 aberrant pada seluruh serrated lesion pada kolorektal termasuk sessile
serrated adenoma, traditional serrated adenoma, dan polip hiperplastik, tetapi
tidak ditemukan pada adenoma konvesional tipe tubular. Penelitian lainnya oleh Hirono et al. mengatakan ditemukan ekspresi MUC6 pada polip hiperplastik 68%,
sessile serrated adenoma 71%, dan pada adenoma tubular 9,5%.23-26
II.5. Karsinogenesis Karsinoma Kolorektal
Karsinoma kolorektal (KKR) merupakan salah satu jenis karsinoma yang paling banyak diteliti. Karsinogenesis kolorektal dapat dibagi menjadi 3 jalur yaitu instabilitas kromosom (chromosomal instability=CIN), jalur instabilitas mikrosatelit (microsatellite instability=MSI), dan jalur metilasi (CIMP=CpG
island methylator phenotype).39-41 Pada makalah ini akan dilihat perbedaan
perkembangan lesi prekursor menjadi karsinoma kolorektal melalui jalur serrated
pathway dan jalur adenoma-carsinoma sequence, yang melibatkan gangguan
mikrosatelit dan metilasi DNA dikaitkan dengan ekspresi MUC6.24
Jalur CIN merupakan jalur karsinogenesis kolorektal yang dikenal pertama kali, dan terjadi pada karsinoma kolorektal sporadik sekitar 85% dan herediter sekitar 10%. Jalur tersebut dikenal juga sebagai adenoma-carsinoma sequence, ditemukan oleh Fearon - Vogelstein pada tahun 1990.9 jalur tersebut diawali oleh sel atipk, atau dapat berupa fokus kripta yang aberrant, dengan gambaran mikroskopik berupa lesi mukosa yang mendahului perkembangan polip.39-44
Karsinoma kolorektal melalui beberapa tahapan, yang sekurang-kurangnya terdapat 4 kali mutasi gen dalam urutan tertentu. Tahap awal adalah mutasi APC (terletak pada kromosom 5q) sehingga sel kehilangan kontrol pertumbuhannya, dilanjutkan dengan aktivasi onkogen KRAS yang menyebabkan sel kehilangan
fungsi proliferasi, dan diikuti oleh inaktivasi gen DCC/SMAD4 (terletak pada kromosom 18q) yang menyebabkan delesi p53 (pada kromosom 17q) dan akhirnya terjadi karsinoma kolorektal.39,40
Mutasi APC ditemukan pada 60% karsinoma kolon dan 82% karsinoma rektal serta 80% adenoma.9 KRAS(12p12) merupakan gen yang terdapat pada jalur CIN namun berperan lebih penting pada jalur CIMP. Banyak gen yang berperan dalam karsinogenesis antara lain DCC, SMAD2 dan SMAD4 yang berlokasi pada kromosom 18q21.1. Walaupun beberapa onkogen dan onkosupresor telah diketahui terlibat pada karsinogenesis kolorektal, namun mutasi gen APC dianggap sebagai gen yang penting dalam mengawali proses ini.39,40
Pada tahun 2003 Torlakovic et al. melakukan review pada sejumlah pasien dengan poliposis hiperplastik yang berpotensi tinggi untuk menjadi karsinoma. Ia juga menemukan gambaran morfologi pada polip di poliposis yang berbeda dengan PH pada umumnya. Hal ini dikarenakan polip pada poliposis mempunyai gambaran serrated seperti yang dijelaskan oleh Longacre dan Fenoglio Preiser. Polip tersebut tetap mempertahankan konfigurasi sessile sehingga disebut serrated
polyp with abnormal proliferation, yang sekarang dikenal sebagai sessile serrated adenoma (SSA), dan dihubungkan dengan ekspresi DNA Mismacth Repair
protein pada hMLH1 yang menurun.10 Konfigurasi sessile pada SSA
diperkenalkan untuk membedakan lesi ini dengan lesi berbentuk pedunculated pada mayoritas adenoma, yang disebut traditional serrated adenoma (TSA). Sekitar 40% karsinoma kolorektal dengan gambaran SSA ini mempunyai defek
Mismatch Repair genes (MMR). Contohnya adalah MSI-H pada karsinoma
kolorektal yang timbul pada pasien herediter non-poliposis colorectal cancer (HNPCC) yang disebabkan mutasi germline pada DNA Mismacth Repair genes. 41-45
Saat ini dikenal pula adanya konsep baru mengenai jalur karsinogenesis kolorektal, yaitu pada serrated adenoma (SA). Konsep ini secara resmi diperkenalkan oleh Longacre dan Fenoglio-Preiser setelah tahun 1990, setelah melakukan analisis terhadap sekelompok polip yang mempunyai gambaran campuran antara PH dan adenomatosa (yaitu gambaran sitologi hiperplastik
dengan displasia dan serrated). Serrated adenoma selama hampir satu dekade juga dianggap sebagai varian dari VA atau TVA, oleh karena itu penatalaksanaan pasca operasi pada umumnya mengikuti penanganan pada adenoma konvensional.41-47
Serrated Adenoma (SA) berdasarkan bentuk makroskopik dan jalur
karsinogenesis dibagi menjadi dua yaitu traditional serrated adenoma (TSA) dan
sessile serrated adenoma (SSA).11 Traditional serrated adenoma (TSA) dapat
berkembang menjadi karsinoma kolorektal melalui alternate pathway pada karsinogenesis yang memperlihatkan microsatelite stability (MSS) dengan gambaran genetik yang unik.10,11 Termasuk adanya gen Mismatch Repair (MMR),
dan CIMP-L serta mutasi KRAS.40 Sedangkan sessile serrated adenoma (SSA)
berkembang menjadi karsinoma kolorektal melalui serrated pathways yang memperlihatkan gangguan mikrosatelit yang tinggi/microsatellite instability-high (MSI-H). Langkah pada jalur ini meliputi penurunan jumlah apoptosis, dimana kehidupan sel menjadi semakin panjang dan peningkatan jumlah sel epitel akan membentuk gambaran fenotip serrated dan dysmaturation crypt.38-40
Sessile serrated adenoma (SSA) menunjukkan adanya gangguan Mismatch Repair (MMR), dan mempengaruhi metilasi DNA pada regio promoter
yang mengandung nukleotida (sitosin dan guanin) di beberapa gen supresor tumor. Area metilasi ini disebut sebagai CpG island methylator phenotype (CIMP). Gangguan/defek pada jalur repair DNA ini bisa menyebabkan terjadinya ketidakstabilan genetik sehingga terbentuklah tumor.44,46-48 Gambaran fenotip
CIMP bisa tinggi (CIMP-H) atau rendah (CIMP-L) tergantung dengan jumlah gen yang mengalami metilasi tersebut. Adanya gangguan mikrosatelit yang tinggi dan CIMP-H akan ditunjukkan dengan ekspresi MUC6 aberrant yang positif.44
Perubahan molekuler tersebut dapat terlihat pada subkelompok dari
serrated polyp, sehingga CIMP/Serrated-Pathways saat ini dikatakan merupakan
jalur baru pada karsinogenesis kolorektal sporadik. Jalur ini dikatakan lebih cepat untuk menjadi karsinoma kolorektal dibandingkan dengan jalur
adenoma-carsinoma sequence yaitu sekitar 8 bulan.43 Estimasi rata-rata pertumbuhan SA
3.76mm/tahun bila dibandingkan dengan pertumbuhan rata–rata adenoma konvensional yaitu 2.79mm/tahun, sedangkan polip hiperplastik yaitu
1.36mm/tahun. Pasien SA, sekitar 5.3% diantaranya dapat berkembang menjadi karsinoma kolorektal. Bila dibandingkan pada kasus adenoma konvensional untuk berkembang menjadi karsinoma yaitu 2.2% , sedangkan pada polip hiperplastik yaitu 0%.(gambar 6)41
BAB III
METODE PENELITIAN
III.1. Tempat Penelitian
Penelitian dilakukan di Departermen Patologi Anatomik Fakultas Kedokteran Universitas Indonesia/Rumah Sakit Cipto Mangunkusumo, Jakarta.
III.2. Waktu Penelitian
Penelitian ini dilakukan bulan September-November 2013.
III.3. Desain Penelitian
Penelitian ini dilakukan secara retrospektif, menggunakan studi potong lintang deskriptif analitik.
III.4. Kriteria Penerimaan
• Diagnosis histopatologik adalah serrated adenoma (SA) dan adenoma konvensional displasia keras.
• Jumlah sel tumor 300 sel atau seluruh ketebalan lapisan mukosa terlihat jelas untuk dilakukan perhitungan positivitas pulasan imunohistokimia.
• Blok paraffin tersedia dan dalam kondisi baik untuk dilakukan pemotongan dalam.
III.5 Kriteria Penolakan
• Kasus yang didiagnosis sebagai serrated adenoma (SA) dengan fokus invasif.
• Kasus yang didiagnosis sebagai adenoma konvensional displasia keras dengan fokus invasif.
• Kasus yang didiagnosis sebagai polip hiperplastik dengan fokus-fokus
serrated lesion dan/atau fokus adenoma konvensional displasia
III.6 Populasi dan Sampel
• Populasi penelitian adalah semua kasus biopsi dan reseksi yang didiagnosis secara histopatologik sebagai serrated adenoma (SA) dan adenoma konvensional displasia keras sesuai dengan International
Classification of Disease-10 (ICD-10), topografi C18.6, C18.7, C18.9
(kolon), C19 (rektum) dan M8140/0 (adenoma,NOS), M8261/1 (adenoma villosum), M8263/0 (adenoma tubullovillosum) dari tahun 2007 hingga Agustus 2013.
III.7 Pemilihan Sampel
Perhitungan besar sampel untuk uji hipotesis terhadap dua proporsi/rumus besar sampel kategorik tidak berpasangan/independen :
n1=n2 = (Zα√2PQ+Zβ√P1Q1 +√P2Q2)2 ____________________________ (P1-P2)2 Zα = 1.96 Zβ= 0.842 P = P1 + P2 = 0,9 + 0,5 = 0,7 2 2 Q = 1 – P ( 0,3)
P1 = proporsi penyakit adenoma konvensional displasia keras dari kepustakaan (0,5).
P2 = proporsi penyakit serrated adenoma (SA) yang diharapkan oleh peneliti (0,9). Q1= 1-P1 = 0,5. Q2= 1-P2 = 0,1. n1=n2= [1,96√2x(0,7x0,3) + 0,842√(0,5x0,5)+(0,9x0,1)]2 _____________________________________________________________ (0,9-0,5)2