PENETAPAN KADAR HIDROKORTISON ASETAT DALAM
SEDIAAN KRIM SECARA KROMATOGRAFI CAIR
KINERJA TINGGI (KCKT)
TUGAS AKHIR
OLEH:
Beby Fitria
NIM 122410083
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
iii
KATA PENGANTAR
Assalamu’alaikum Wr. Wb.
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karunia-Nya yang telah memberikan pengetahuan, kekuatan,
kesehatan dan kesempatan kepada penulis sehingga penulis dapat menyelesaikan
tugas akhir ini, serta sholawat beriring salam untuk Rasulullah Nabi Muhammad
SAW sebagai contoh tauladan dalam kehidupan. Tugas Akhir ini berjudul
“PENETAPAN KADAR HIDROKORTISON ASETAT DALAM SEDIAAN
KRIM SECARA KROMATOGRAFI CAIR KINERJA TINGGI (KCKT)”. Tugas
Akhir ini merupakan salah satu syarat untuk memperoleh gelar Ahli Madya pada
program Diploma III Analis Farmasi Dan Makanan Fakultas Farmasi Universitas
Sumatera Utara Medan.
Penulis menyadari sepenuhnya bahwa tanpa bantuan dari berbagai pihak,
penulis tidak akan dapat menyelesaikan tugas akhir ini sebagaimana mestinya.
Untuk itu penulis mengucapkan terima kasih yang sebesar-besarnya kepada
berbagai pihak antara lain:
1. Ibu Prof. Dr. Julia Reveny, M.Si., Apt., selaku Pembantu Dekan I Fakultas
Farmasi Universitas Sumatera Utara.
2. Dra. Fat Aminah, M.Sc.,Apt., selaku dosen pembimbing yang telah
banyak memberikan arahan dan bimbingan dengan penuh perhatian hingga
iv
3. Bapak Yogi Sugianto, S.Farm., Apt., selaku Supervisor Pengawasan Mutu
PT. Kimia Farma (Persero) Tbk. Plant Medan, yang telah mengawasi
penulis selama melakukan kegiatan Praktik Kerja Lapangan (PKL).
4. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., sebagai koordinator
program Diploma III Analis Farmasi Dan Makanan.
5. Bapak Popi Patilaya,S.Si., M.Sc., Apt., sebagai Dosen Penasehat
Akademis yang telah memberikan nasehat dan pengarahan kepada penulis
dalam hal akademis setiap semester.
6. Bapak dan Ibu dosen staf Pengajar Fakultas Farmasi Program Diploma III
Analis Farmasi Dan Makanan yang berupaya mendukung kemajuan
mahasiswa Analis Farmasi Dan Makanan.
7. Seluruh staf dan pegawai PT. KIMIA FARMA (PERSERO) TBK.
PLANT MEDAN yang telah meluangkan waktu, tenaga dan pikiran
kepada penulis dalam melaksanakan Praktek Kerja Lapangan (PKL)
8. Adikku tersayang,Dinda dan Romi yang telah memberikan semangat dan
motivasi serta dukungan serta doa kepada penulis.
9. Seluruh sahabat-sahabatku Nurul, Dwi, Ezy, Adel, Sela, Yulita, Yuni,
serta teman-teman satu PKL yang saling mendukung danbahu mambahu
selama PKL hingga tugas akhir ini selesai.
10.Teman-teman Analis Farmasi dan Makanan stambuk 2012 semuanya
tanpa terkecuali, yang tidak dapat disebutkan namanya satu persatu, terima
kasih buat kebersamaan dan semangatnya selama ini, serta masukkan
v
Terima kasih yang setulus-tulusnya untuk yang teristimewa Ayahanda
Ponidi dan Ibunda Herlina serta juga untuk seluruh keluarga besar yang telah
mencurahkan perhatian serta memberikan dukungan baik moril maupun materil
dan segenap doa kepada penulis sehingga penulis dapat menyelesaikan tugas akhir
ini.
Penulis menyadari sepenuhnya dalam penyusunan tugas akhir ini, masih
banyak terdapat kekurangan dan kelemahan yang dimiliki penulis baik itu
sistematika penulisan maupun penggunaan bahasa. Untuk itu penulis
mengharapkan kritik dan saran dari berbagai pihak yang bersifat membangun
demi penyempurnaan tugas akhir ini. Semoga tugas akhir ini berguna bagi
pembaca secara umum dan penulis secara khusus. Akhir kata penulis
mengucapkan banyak terima kasih.
Medan, Mei 2015
Penulis,
vi
PENETAPAN KADAR HIDROKORTISON ASETAT DALAM SEDIAAN KRIM SECARA KROMATOGRAFI CAIR KINERJA TINGGI (KCKT)
Abstrak
Krim topikal hidrokortison asetat berfungsi sebagai antiinflamasi. Zat aktif ini memiliki kecenderungan untuk mengalami degradasi selama penyimpanan sehingga penetapan kadar zat aktif tersebut menjadi suatu pertimbangan. Oleh sebab itu, dibutuhkan penetapan kadar hidrokortison asetat dalam krimt opikal yang ditetapkan melalui suatu metode yang tervalidasi sesuai dengan standar analisis, yaitu metode Kromatograpi Cair Kinerja Tinggi (KCKT) fase terbalik dengan tujuan untuk mengetahui kadar hidrokortison asetat.
Sistem KCKT yang digunakan adalah kolom Bondapack C18 300 x 3.9
mm, fase gerak campuran asetonitril-aquabidest dengan menggunakan detektor UV 254 nm. Parameter yang dioptimasi adalah komposisi fase gerak yaitu asetonitril-aquabidest dan flow rate. Hasil analisa menunjukkan kondisi pemisahan yang baik dicapai pada fasegerak asetonitril-aquabidest (60 : 40 v/v) dengan flow rate 1.2 mL/menit. Semua komponen terpisah baik dalam waktu analisis kurangd ari 10 menit.
Berdasarkan analisa yang dilakukan, didapatkan hasil bahwa sampel krim yang digunakan pada analisa ini mengandung hidrokortison asetat dengan kadar rata-rata 102.0381 %, sesuai dengan batas yang ditetapkan dalam Farmakope Indonesia, dimana kadar hidrokortison asetat dalam sediaan krim memenuhi persyaratan yang ditetapkan, yaitu kadar tidak kurang dari 90% dan tidak lebih dari 110.0%.
vii
ASSAY OF HYDROCORTISONE ACETATE IN CREAM AVAILABLE IN HIGH PERFORMANCE OF LIQUID CHROMATOGRAPHY (HPLC)
Abstract
Topical hydrocortisone acetate cream function as anti-inflammatory. The active substance has a tendency to degrade during storage so that the assay of the active substance into a consideration. Therefore, it takes assay hydrocortisone acetate in a topical cream that is determined by a validated method in accordance with the standard analysis, the method of High Performance Liquid Chromatography (HPLC) reversed phase in order to determine the levels of hydrocortisone acetate.
HPLC system used was Bondapak C18 column 300 x 3,9 mm, mobile phase mixture of acetonitrile-aquabidest at 254 nm using a UV detector. The parameters are optimized composition mobile phase is acetonitrile-aquabidest and flow rate. The analysis shows good separation condition is achieved in the mobile phase acetonitrile-aquabidest (60: 40 v / v) with a flow rate of 1,2 mL/min. All the separate components both within the analysis is less than 10 minutes.
Based on the analysis, showed that the cream samples used in this analysis contains hydrocortisone acetate with an average level of 102,0381%, according to the limit specified in the Pharmacopoeia of Indonesia, where the levels of hydrocortisone acetate in cream meets the requirements set forth, namely content of not less than 90,0% and not more than 110,0%.
viii
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRAK ... vi
ABSTRACK ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR LAMPIRAN ... xii
DAFTAR GAMBAR ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 2
1.3 Tujuan ... 2
1.4 Manfaat ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Krim ... 4
2.2 Kulit ... 6
2.3 Obat Kulit ... 9
2.3.1 Penggunaan Klinis ... 10
2.3.2 Mekanisme Kerja ... 11
ix
2.4 Hidrokortison ... 11
2.4.1 Sifat Fisika Kimia ... 12
2.4.2Uji Kualitatif ... 12
2.4.3 Uji Kuantitatif ... 13
2.5 Kromatografi Cair Kinerja Tinggi ... 15
2.5.1 Prinsip ... 15
2.5.2Ciri-ciri KCKT ... 15
2.6 Cara Kerja KCKT ... 16
BAB III METODE PERCOBAAN ... 20
3.1 Tempat Pelaksanaan ... 20
3.2 Alat ... 20
3.3 Bahan ... 20
3.4Prosedur ... 20
3.4.1 Pengambilan Sampel Uji ... 20
3.4.2 Pembuatan pelarut ... 21
3.4.3 Pembuatan Larutan Standar ... 21
3.4.4 Pembuatan Larutan Uji ... 21
3.4.5 Perhiungan Kadar ... 22
3.4.6 Persyaratan ... 22
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1 Hasil ... 23
4.2 Pembahasan ... 23
x
5.1 Kesimpulan ... 25
5.2 Saran ... 25
DAFTAR PUSTAKA ... 26
xi
DAFTAR TABEL
Halaman
Tabel 1. Hasil penetapan kadar krim Hidrokortison secara KCKT ... 23
Tabel 2. Data Luas Area Sampel ... 30
xii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. ... 28
a. Perhitungan Kadar Krim Hidrokortison secara Kromatografi Cair
Kinerja Tinggi ... 28
b. Perhitungan Standar Deviasi (SD) dan Standar Deviasi Relatif (RSD) Krim Hidrokortison Secara Kromatografi Cair Kinerja Tinggi ... 29
Lampiran 2. Hasil Kromatogram Kadar Krim Hidrokortison ... 32
xiii
DAFTAR GAMBAR
Halaman
Gambar 1. Digital Semi Micro Balance ... 34
vi
PENETAPAN KADAR HIDROKORTISON ASETAT DALAM SEDIAAN KRIM SECARA KROMATOGRAFI CAIR KINERJA TINGGI (KCKT)
Abstrak
Krim topikal hidrokortison asetat berfungsi sebagai antiinflamasi. Zat aktif ini memiliki kecenderungan untuk mengalami degradasi selama penyimpanan sehingga penetapan kadar zat aktif tersebut menjadi suatu pertimbangan. Oleh sebab itu, dibutuhkan penetapan kadar hidrokortison asetat dalam krimt opikal yang ditetapkan melalui suatu metode yang tervalidasi sesuai dengan standar analisis, yaitu metode Kromatograpi Cair Kinerja Tinggi (KCKT) fase terbalik dengan tujuan untuk mengetahui kadar hidrokortison asetat.
Sistem KCKT yang digunakan adalah kolom Bondapack C18 300 x 3.9
mm, fase gerak campuran asetonitril-aquabidest dengan menggunakan detektor UV 254 nm. Parameter yang dioptimasi adalah komposisi fase gerak yaitu asetonitril-aquabidest dan flow rate. Hasil analisa menunjukkan kondisi pemisahan yang baik dicapai pada fasegerak asetonitril-aquabidest (60 : 40 v/v) dengan flow rate 1.2 mL/menit. Semua komponen terpisah baik dalam waktu analisis kurangd ari 10 menit.
Berdasarkan analisa yang dilakukan, didapatkan hasil bahwa sampel krim yang digunakan pada analisa ini mengandung hidrokortison asetat dengan kadar rata-rata 102.0381 %, sesuai dengan batas yang ditetapkan dalam Farmakope Indonesia, dimana kadar hidrokortison asetat dalam sediaan krim memenuhi persyaratan yang ditetapkan, yaitu kadar tidak kurang dari 90% dan tidak lebih dari 110.0%.
vii
ASSAY OF HYDROCORTISONE ACETATE IN CREAM AVAILABLE IN HIGH PERFORMANCE OF LIQUID CHROMATOGRAPHY (HPLC)
Abstract
Topical hydrocortisone acetate cream function as anti-inflammatory. The active substance has a tendency to degrade during storage so that the assay of the active substance into a consideration. Therefore, it takes assay hydrocortisone acetate in a topical cream that is determined by a validated method in accordance with the standard analysis, the method of High Performance Liquid Chromatography (HPLC) reversed phase in order to determine the levels of hydrocortisone acetate.
HPLC system used was Bondapak C18 column 300 x 3,9 mm, mobile phase mixture of acetonitrile-aquabidest at 254 nm using a UV detector. The parameters are optimized composition mobile phase is acetonitrile-aquabidest and flow rate. The analysis shows good separation condition is achieved in the mobile phase acetonitrile-aquabidest (60: 40 v / v) with a flow rate of 1,2 mL/min. All the separate components both within the analysis is less than 10 minutes.
Based on the analysis, showed that the cream samples used in this analysis contains hydrocortisone acetate with an average level of 102,0381%, according to the limit specified in the Pharmacopoeia of Indonesia, where the levels of hydrocortisone acetate in cream meets the requirements set forth, namely content of not less than 90,0% and not more than 110,0%.
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Bentuk sediaan ialah sediaan yang mengandung satu atau beberapa zat
berkhasiat, umumnya dimasukkan dalam suatu vehikulum yang diperlukan untuk
formulasi, hingga didapat suatu produk (dengan dosis-unit, volume, serta sediaan
yang diinginkan) yang siap diminum atau dipakai oleh penderita (Joenoes, 1990).
Sediaan topikal adalah sediaan yang penggunaannya pada kulit dengan
tujuan untuk menghasilkan efek local, contoh : lotio, salep, dan krim. Krim adalah
bentuk sediaaan setengah padat mengandung satu atau lebih bahan obat terlarut
atau terdispersi dalam bahan dasar yang sesuai. Istilah ini secara tradisional telah
digunakan untuk sediaan setengah padat yang mempunyai konsistensi relatif cair
diformulasi sebagai emulsi air dalam minyak atau minyak dalam air. Sekarang ini
batasan tersebut lebih disarankan untuk produk yang terdiri dari emulsi minyak
dalam air atau dispersi mikrokristal asam-asam lemak atau alkohol berantai
panjang dalam air, yang dapat dicuci dengan air dan lebih ditujukan untuk
penggunaan kosmetika dan estetika. Krim dapat digunakan untuk pemberian obat
melalui vaginal (Ansel, 1989).
Hidrokortison merupakan suatu senyawa turunan dari kortisteroid.
Hidrokortison dalam bentuk krim biasanya dikombinasikan dengan suatu asam,
misalnya bila dikombinasikan dengan suatu asam asetat maka nama dari sediaan
tersebut adalah hidrokortison asetat. Krim hidrokortison ini sebelum dipasarkan
2
kualitas krim dari awal produksi sampai pada obat jadi sehingga menjamin hasil
akhir yang berkhasiat dan menghasilkan efek terapi pada setiap penggunaan.
Kromatografi cair kinerja tinggi (HPLC, High Performance Liquid
Chromatography) merupakan suatu teknis analisis obat yang paling cepat
berkembang. Cara ini ideal untuk analisis beragam obat dalam sediaan dan cairan
biologis, karena sederhana, dan kepekaannya tinggi. Cepatnya perkembangan
HPLC didukung oleh perkembangan peralatan yang handal, harganya mahal, dan
kolom yang mangkus (Munson, 1991).
Berdasarkan hasil diatas maka penulis tertarik untuk melakukan pengujian
krim hidrokortison produksi PT. Kimia Farma (Persero) Tbk. Plant Medan secara
Kromatografi Cair Kinerja Tinggi (KCKT).
1.2 Rumusan Masalah
Apakah kadar hidrokortison asetat di dalam sediaan krim yang diproduksi
PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi persyaratan yang
ditetapkan.
1.3 Tujuan
1. Untuk mengetahui metode yang digunakan dalam pegujian kadar
hidrokortison asetat dalam sediaan krim yang diproduksi PT. Kimia Farma
(Persero) Tbk. Plant Medan.
2. Untuk mengetahui apakah kadar hidrokortison asetat dalam sediaan krim
yang diproduksi PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi
3
1.4 Manfaat
Untuk memberi informasi kepada masyarakat bahwa krim hidrokortison
yang diproduksi PT. Kimia Farma (Persero) Tbk. Plant Medan memenuhi
4
BAB II
TINJAUAN PUSTAKA
2.1 Krim
Krim adalah sediaan setengah padat berupa emulsi kental mengandung
tidak kurang dari 60% air, dimaksudkan untuk pemakaian luar. Tipe krim ada
yaitu: tipe krim air minyak (A/M) dan krim minyak air (M/A). Untuk membuat
krim digunakan zat pengemulsi, umumnya berupa surfaktan-surfaktan anionik,
kationik, dan nonionik.Untuk penstabilan krim ditambahkan zat antioksidan dan
zat pengawet. Zat pengawet yang sering digunakan ialah Nipagin 0,12-0,18%,
Nipasol 0,02-0,05% (Anief, 1999).
Krim adalah bentuk sediaan setengah padat mengandung satu atau lebih
bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai. Istilah ini
secara tradisional telah digunakan untuk sediaan setengah padat yang mempunyai
konsistensi relatif cair diformulasi sebagai emulsi air dalam minyak atau minyak
dalam air. Sekarang ini batasan tersebut lebih diarahkan untuk produk yang terdiri
dari emulsi minyak dalam air atau disperse mikrokristal asam-asam lemak atau
alkohol berantai panjang dalam air, yang dapat dicuci dengan air dan lebih
ditujukan untuk penggunaan kosmetika dan estetika. Krim dapat digunakan untuk
pemberian obat melalui vaginal (Dirjen POM, 1995).
Krim merupakan sistem emulsi sediaan semi padat dengan penampilan
tidak jernih, berbeda dengan salep yang tembus cahaya. Konsistensi dan sifat
5
minyak dalam air, dan juga pada sifat zat padat dalam fase internal (Lachman,
1994).
Cream, adalah sediaan lunak, setengah padat atau tebal, sediaan cair untuk
dipakai pada kulit. Basis cream digunakan sebagai pelumas atau sebagai
pelindung, tetapi biasanya ditambah obat didalamnya (Anief, 1984).
Krim minyak dalam air mempunyai air sebagai fase kontinu, dengan
tetesan minyak sebagai fase disperse. Untuk krim air dalam minyak, berlaku
sebaliknya. Bagian realtif lemak dan cairan mempengaruhi sifat reologi atau aliran
suatu krim. Lebih cair konsistensinya maka lebih mudah mengoleskannya
sehingga lebih mudah memakai krim ini (Polano, 1987).
Terdapat patokan klasik dermatoterapi bahwa pada kelainan yang dinamai
dermatosis yang mudah terangsang (dermatitis akut dan eksudatif), maka terapi
harus dimulai dengan obat yang lembut seperti kompres basah atau pasta
penyejuk. Patokan ini tidak menjadi kuno dengan ditemukannya steroid, yang
dapat diterima oleh masyarakat karena umumnya dijual dalam bentuk salep atau
lebih praktis seperti krim, walaupun kortikosteroid bisa juga digabung dalam
pasta penyejuk atau tanpa kortikosteroid tetap sangat diperlukan pada keadaan
vesikula atau basah akut dan parah. Pada kasus kurang parah, mungkin cukup
krim kortikosteroid saja. Krim menjadi semakin penting dalam dermatologi
karena kemajuannya cepat dalam teknologi emulsi serta ditemukannya
kortikosteroid. Krim biasanya digunakan siang hari dan salep digunakan pada
6
Dalam pembuatan krim diperlukan suatu bahan dasar. Bahan dasar yang
digunakan harus memenuhi kriteria-kriteria tertentu. Kualitas dasar krim yang
diharapkan adalah sebagai berikut :
a. Stabil
b. Lunak
c. Mudah dipakai
d. Dasar krim yang cocok
e. Terdistribusi merata
Fungsi krim adalah:
a. Sebagai bahan pembawa substansi obat untuk pengobatan kulit
b. Sebagai bahan pelumas bagi kulit
c. Sebagai pelindung untuk kulit yaitu mencegah kontak langsung dengan zat-zat
berbahaya (Anief, 1999).
2.2 Kulit
Kulit merupakan suatu organ besar yang berlapis-lapis, di mana pada
orang dewasa beratnya kira-kira delapan pon, tidak termasuk lemak.Kulit
menutupi permukaan lebih dari 20.000 cm2 dan mempunyai bermacam-macam fungsi dan kegunaan.Sediaan semipadat digunakan pada kulit, di mana umumnya
sediaan tersebut berfungsi sebagai pembawa obat topikal, sebagai pelunak kulit,
atau sebagai pembalut pelindung atau pembalut penyumbat (oklusif). Kulit
berfungsi sebagai pembatas terhadap serangan fisika dan kimia. Beberapa bahan
seperti ion nikel, gas mostar, serta minyak dammar dari Rhus toksikodendron,
7
sedangkan umumnya zat-zat lain tidak dapat. Kulit berfungsi sebagai termostat
dalam mempertahankan suhu tubuh, melindungi tubuh dari serangan
mikroorganisme, sinar ultraviolet, dan berperan pula dalam mengatur tekanan
darah (Lachman, 1994).
Obat kulit digunakan untuk mengatasi gangguan fungsi dan struktur kulit.
Gangguan fungsi struktur kulit dapat dibagi ke dalam tiga golongan, yaitu :
1. Kerusakan Kulit Akut : kerusakan yang masih baru dengan tanda bengkak,
berdarah, melepuh, dan gatal.
2. Kerusakan Kulit Sub Akut : gangguan fungsi dan struktur kulit, yang telah
terjadi antara 7-30 hari, dengan tanda-tanda antara lain bengkak yang makin
parah dan sudah mempengaruhi daerah sekelilingnya.
3. Kerusakan Kulit Kronik : kerusakan yang telah lama terjadi dan hilang serta
timbul kembali, dari beberapa bulan sampai bertahun-tahun. Biasanya kulit
menjadi tebal, keras dan retak-retak (Sartono, 1996).
Kulit terdiri bermacam-macam jarigan, termasuk pembuluh darah, kelenjar
lemak, kelenjar keringat, organ pembuluh perasa dan urat syaraf, jaringan
pengikat otot polos dan lemak. Kulit manusia terdiri dari lapisan yang berbeda :
a. Epidermis.
b. Dermis.
c. Jaringan subkutan yang berlemak.
a. Epidermis, merupakan lapisan kulit luar, tebal 0.16 mm pada pelupuk
mata sampai 0.8 mm pada telapak tangan dan telapak kaki. Epidermis
8 1. Stratum corneum (lapisan tanduk)
2. Stratum lucidum (lapisan rintangan)
3. Stratum granulosum (lapisan berbutir)
4. Stratum spinosum (lapisan sel duri)
5. Stratum germinavitum (lapisan sel basah)
Fungsi epidermis adalah untuk pelindung terhadap bakteri, iritasi kimia,
alergi dan lain-lain. Meliputi stratum corneum ada lapisan film lipid
teremulsi pH 4,5-6,5 disebut mantel asam dan merupakan film pelindung.
Bila pH-nya berubah drastis pemasukan oleh bakteri dan macam-macam
penyakit kulit akan meningkat. Stratum corneum merupakan perintang
terhadap kehilangan air, beberapa lapis dari sel mati berkeratin sangat
hidrofil, bila tercelupdalam air akan mengambang, hal ini menjaga
permukaan kulit tetap halus dan lentur (Anief, 1984).
b. Dermis, terdiri anyaman kolagen dan elastin, mengandung pembuluh
darah, pembuluh limphe, gelembung rambut, kelenjar lemak, kelenjar
keringat, otot, serabut syaraf, dan korpus pacin
c. Jaringan subkutan berlemak, bekerja sebagai isolator panas. Absorpsi obat
melalui kulit dapat:
a. Langsung menembus epidermis kulit
b. Di antara atau menembus sel stratum corneum
c. Menembus kelenjar keringat, kelenjar lemak, dan gelembung rambut
9
2.3 Obat Kulit
Efikasi kortikosteroid (corticosteroid) topikal terbukti luar biasa pada
pengobatan termatosis inflamasi setelah dikenalkannya hydrocortisone pada tahun
1952.Setelah itu, perkembangan sejumlah besar analog menawarkan potensi
pilihan, konsentrasi, serta vehikulum yang ekstensif. Efektivitas teraupetik dari
koetikosteroid topikal ada dasarnya tergantung pada aktivitas antiinflamasi-nya.
Efek-efek kortikosteroid antimitotik pada epidermis manusia menyebabkan
timbulnya mekanisme kerja tambahan pada psoriasis dan penyakit kulit lainnya
yang dihubungkan dengan meningkatnya pergantian sel (Katzung, 2004).
Kortikosteroid krim atau salep penting dalam penanganan berbagai
penyakit kulit primer, namun dalam mengatasi perasaan gatal pada kebanyakan
penyakit sistemik, obat ini hanya kecil artinya. Agaknya kerja obat ini tidak hanya
pada inhibisi protease (Walsh, 1997).
Penyakit alergi. Gejala penyakit yang dasarnya karena reaksi alergi, dapat
diatasi dengan glukokortikoid sebagai obat tambahan di samping obat-obat
primernya. Keadaan alergi tersebut antara lain: hay-fever, penyakit serum,
urtikaria, dermatitis kontak, reaksi obat, edema angioneurotik, dan anafilaksis.
Kadang-kadang pada reaksi yang gawat, misalnya anafilaksis dan edema,
angioneurotik glotis, diperlukan pemberian adrenalin dengan segera (Tanu, 1980).
Pada penggunaan topikal prednisolon dan metilprednisolon sama aktifnya
dengan hydrocortisone. Turunan 9α-fluoro hidrokortison aktif topikal, tetapi
10
pemakaian topikal. Steroid 9α-fluorinasi deksametason dan betametason yang
kemudian dikembangkan tidak mempunyai keuntungan apapun atas hidrokortison.
Tetapi triamsinolon dan fluosinolon, turunan asetonid steroid fluorinasi,
mempunyai keuntungan jelas dalam terapi topikal. Juga beta metason tidak sangat
aktif topikal, tetapi melekat rantai 5-karbon valerat ke posisi 17-hidroksil
menghasilkan senyawa lebih dari 300 kali keaktifan hidrokortison untuk
pemakaian topikal. Fluosinonid merupakan turunan 21-asetat fluosinolon
asetonid, tambahan 21-asetat meningkat aktivitas topikal sekitar 5 kali lipat.
Fluorinasi steroid tidak diperlukan untuk kekuatan tinggi, hidrokortison valerat
dan butirat mempunyai aktivitas yang serupa dengan triamsinolon asetonid
(Katzung, 2004).
2.3.1 Penggunaan Klinis
Kortikosteroid hanya diabsorpsi sedikit setelah digunakan pada kulit
normal. Misalnya kira-kira 1% dari dosis larutan hydrocortisone yang digunakan
pada ventral lengan bawah akan diabsorpsi. Oklusi jangka panjang dengan film
anti tembus seperti pembungkus plastik adalah suatu metode yang efektif untuk
meningkatkan absorpsi. Ada suatu perbedaan anatomis regional yang dapat dilihat
pada penetrasi kortikosteroid. Dibandingkan dengan absorpsi yang diperoleh dari
bawah lengan, hydrocortisone juga diabsorpsi 0,14 kali melalui plantar lengkung
telapak kaki, 0,83 kali juga diabsorpsi melalui telapak tangan, 3,5 kali melalui
kulit kepala, serta 6 kali melalui kening, 9 kali melalui kulit vulva dan 42 kali
kulit skrotum. Penetrasi meningkat beberapa kali lipat pada kulit yang mengalami
11
(eksfoliativa) kulit yang parah, seperti psoriasis eritrodermis, yang tampaknya
hambatan penetrasinya berkurang (Katzung, 2004).
2.3.2 Mekanisme Kerja
Mekanisme kerja, glukokortikoid alamiah dan sintetik serta steroid
antiinflamasi terikat pada reseptor intrasel yang spesifik setelah memasuki
jaringan sasaran. Jadi kompleks makromolekul yang terbentuk ini diangkut ke
dalam inti, tempat ia berinteraksi dengan unsur kromosom untuk mengubah
ekspresi gen. Hormon ini mengubah pengaturan banyak proses sel, termasuk
sintesis dan aktivitas enzim, permeabilitas membran, proses trasnpor dan struktur.
(Katzung, 1989).
2.3.5 Efek Samping
Efek samping lokal kortikosteroid topikal meliputi berikut: atropi, yang
mungkin tampil sebagai kulit yang tampak cekung, mengkilat, sering seperti
kertas rokok yang keriput (Katzung, 1989).
2.4 Hidrokortison
Hidrokortison asetat (C23H32O6) digolongkan ke dalam obat
antiinflamantori analgesic yaitu obat untuk penyakit yang ditandai dengan adanya
rasa nyeri, bengkak, kekakuan, dan gangguan alat fungsi penggerak (Anief, 1996).
Hidrokortison adalah golongan kortikosteroid yang mempunyai daya kerja
antialergi dan antiradang. Kortikosteroid bekerja dengan cara mencegah reaksi
alergi, mengurangi peradangan, dan menghambat sel epidermis. Kortikosteroid
12
sel epidermis. Kortikosteriod secara topikal dapat mengganggu pertahanan kulit
alami terhadap infeksi sehingga dikombinasikan dengan obat antibiotika (Sartono,
1996).
2.4.1 Sifat Fisika Kimia
Rumus molekul : C21H30O5
Berat molekul : 362,47
Nama kimia : 11β, 17α, 21 – trihydroxypregn – 4 - ena – 3,20 – dion
Nama lain : Cortisol
Pemerian : Serbuk hablur/kristal putih, tidak berbau, dan rasa pahit
Kelarutan : Sangat sukar larut dalam air, dalam eter, agak sukar larut
dalam aseton dan dalam etanol, sukar larut dalam
kloroform (Dirjen POM,1995).
2.4.2 Uji Kualitatif Hidrokortison
a. Menggunakan metoda spektrofotometri
Hidrokortison dapat diidentifikasi dengan mengukur serapannya pada
panjang gelombang tertentu dengan alat spektrofotometri. Dalam pelarut metanol
hidrokortison akan memberikan serapan pada panjang gelombang maksimum ±
13
b. Menggunakan metode Kromatografi Lapis Tipis (KLT)
Kromatografi merupakan teknik pemisahan senyawa-senyawa yang
berwarna. Cara ini pertama sekali dipaparkan pada tahun 1903 oleh Michael
Tswett. Dalam kromatografi, menggunakan dua fase yaitu fase tetap (fase diam
atau stationary phase) dan fase gerak (mobile phase), pemisahan senyawa
tergantung daripada gerakan dari dua fase ini. Menurut farmakope Indonesia Ed.
IV, lempeng yang dilapisi dapat dianggap sebagai kolom kromatografi terbuka
dan pemisahan yang tercapai dapat didasarkan pada adsorbsi, partisi, atau
kombinasi dari keduanya, tergantung dari jenis zat penyangga, cara pembuatan
dan jenis pelarut yang digunakan. Larutan uji ditotolkan pada plat KLT diikuti
dengan penotolan larutan baku. Maka noda larutan uji akan menunjukkan warna
dan harga Rf yang sama dengan noda larutan baku.
2.4.3 Uji Kuantitatif Hidrokortison
Pengujian hidrokortison dapat dilakukan dengan secara Kromatografi Cair
Kinerja Tinggi (KCKT). Kromatografi Cair Kinerja Tinggi (KCKT) atau High
Performance Liquid Chromatography (HPLC) merupakan suatu teknis analisis
obat yang paling cepat berkembang. Cara ini ideal untuk analisis beragam obat
dalam sediaan dan cairan biologi karena sederhana dan kepekaannya tinggi.
KCKT biasanya dilakukan pada suhu kamar, jadi senyawa yang tidak tahan panas
dapat ditangani dengan mudah. Peralatan KCKT memiliki kepekaan yang sangat
tinggi sehingga menghasilkan data yang lebih akurat dan membutuhkan waktu
yang tidak lama. Kepekaan dari peralatan KCKT sangat tinggi sehingga
14
Cepatnya perkembangan KCKT didukung oleh perkembangan peralatan yang
handal dan kolom yang efisien.
Kegunaan umum KCKT adalah untuk pemisahan sejumlah senyawa
organik, anorganik, maupun senyawa biologis, analisis ketidakmurnian
(impurities), analisis senyawa-senyawa tidak menguap (non-volatil), penentuan
molekul-molekul netral, ionik, isolasi dan pemurnian senyawa, pemisahan
senyawa-senyawa yang strukturnya hampir sama, pemisahan senyawa-senyawa
dalam sejumlah sekelumit (trace elements), dalam jumlah banyak, dan dalam
skala proses industri (Rohman, 2007).
KCKT merupakan salah satu metode yang mempunyai banyak
keuntungan, diantaranya adalah sebagai berikut:
1. Cepat : untuk analisis yang tidak rumit, dapat dicapai waktu analisis kurang
dari 5 menit.
2. Daya pisahnya baik : kemampuan pelarut berinteraksi dengan fase diam dan
fase gerak memberikan parameter pencapaian pemisahan yang dikehendaki.
3. Peka / detektor unik : detektor yang dipakai adalah UV 254 nm yang dapat
mendeteksi berbagai jenis senyawa dalam jumlah nanogram.
4. Kolom dapat dipakai kembali tetapi mutunya turun. Laju penurunan mutunya
bergantung pada jenis cuplikan yang disuntikkan, kemurnian pelarut, dan jenis
pelarut yang dipakai.
5. Ideal untuk molekul besar dan ion. Mudah memperoleh kembali cuplikan :
karena detector tidak merusak cuplikan. Pelarut dapat dihilangkan dengan
15
2.5 Kromatografi Cair Kinerja Tinggi (KCKT) 2.5.1 Prinsip
Suatu fase gerak cair dipompa di bawah tekanan melalui kolom baja yang
mengandung partikel-partikel fase diam dengan diameter 3-10 um. Analit tersebut
dimasukkan ke dalam bagian atas kolom melalui katup lengkung dan pemisahan
suatu campuran berlansung sesuai dengan lamanya waktu relatif yang dibutuhkan
oleh komponennya di dalam fase diam. Perlu diperhatikan bahwa semua
komponen di dalam campuran membutuhkan waktu yang kurang lebih sama
dalam fase gerak agar dapat keluar dari kolom. Pemantauan eluen kolom dapat
dilakukan dengan berbagai detektor (Watson, 2009).
Fase diam menggunakan silika gel, yang dalam molekulnya terdapat rantai
oktadesil yang terikat secara kimia, ikatannya stabil terhadap hidrolisis dan
mempunyai gabungan sifat hidrofilik dan hidrofobik, karena pada ujung rantai
terdapat gugus eter silil dan alkil pada bagian tengah. Fase gerak merupakan
campuran antara metanol atau asetonitril dengan air atau larutan dapar. Pada
penggunaan fase gerak yang mengandung air, ikatan kimia fase diam mempunyai
sifat seperti sistem terbalik (Sardjoko, 1993).
2.5.2 Ciri-ciri KCKT
Ciri-ciri KCKT sangat cocok untuk menetapkan koefisien partisi.
Keuntungan metode KCKT untuk menetapkan nilai lipofilisitas terutama bagi
senyawa lipofilik tinggi, mempunyai jarak pengukuran yang sangat luas, dan tidak
memerlukan proses pemurnian. Kerugiannya hanya dapat dipakai bagi seri
senyawa homolog, senyawa yang bersifat basa memerlukan penambahan senyawa
16
fase diam supaya menghasilkan log k’ yang tinggi, dan juga jarak pH yang
terbatas yaitu (2.0-8.0) (Sardjoko, 1993).
KCKT paling sering digunakan untuk menetapkan kadar
senyawa-senyawa tertentu seperti asam-asam amino, asam-asam nukleat, dan
protein-protein dalam cairan fisiologis, menentukan kadar senyawa-senyawa aktif obat,
produk hasil samping proses sintetis, atau produk-produk degradasi dalam sediaan
farmasi, memonitor sampel-sampel yang berasal dari lingkungan, memurnikan
senyawa dalam suatu campuran, memisahkan polimer dan menentukan distribusi
berat molekulnya dalam suatu campuran, kontrol kualitas, dan mengikuti jalannya
reaksi sintetis (Rohman, 2007).
2.6 Cara Kerja KCKT
Kromatografi merupakan teknik yang mana solut atau zat-zat terlarut
terpisah oleh perbedaan kecepatan elusi, dikarenakan solut-solut ini melewati
suatu kolom kromatografi. Penggunaan kromatografi cair secara sukses terhadap
suatu masalah yang dihadapi membutuhkan penggabungan secara tepat dari
berbagai macam kondisi operasional seperti jenis kolom, fase gerak, panjang dan
diameter kolom, kecepatan alir fase gerak, suhu kolom, dan ukuran sampel.
Ukuran tujuan memilih kombinasi kondisi kromatografi yang terbaik, maka
dibutuhkan pemahaman yang mendasar tentang berbagai macam faktor yang
mempengaruhi pemisahan pada kromatografi cair (Rohman, 2007).
Instrument KCKT pada dasarnya terdiri atas beberapa komponen pokok
17 1. Tandon pelarut
Bahan tandon harus lembab terhadap fase gerak berair dan tidak berair.
Sehingga baja anti karat dan gelas menjadi pilihan. Baja anti karat jangan dipakai
pada pelarut yang mengandung ion halida dan jika tandon harus bertekanan,
hindari penggunaan gelas. Daya tampung tandon harus lebih besar dari 500 ml di
gunakan selama 4 jam untuk kecepatan alir 1 – 2 ml / menit (Munson, 1991).
2. Pipa
Sifat pipa merupakan penyambung dari seluruh bagian sistem. Garis
tengah dalam pipa sebelum penyuntik tidak berpengaruh, hanya saja harus
lembab, tahan tekanan dan mampu dilewati pelarut dengan volume yang memadai
(Munson, 1991).
3. Pompa
Pompa yang cocok digunakan untuk KCKT adalah pompa yag mempunyai
syarat sebagaimana syarat wadah pelarut yakni: pompa harus inert terhadap fase
gerak. Bahan yang umum dipakai untuk pompa adala gelas, baja tahan karat,
teflon, dan batu nilam. Pompa yang digunakan sebaiknya mampu memberikan
tekanan sampai 5000 psi dan mampu mengalirkan fase gerak dengan kecepatan
alir 3 mL/menit. Untuk tujuan preparatif, pompa yang digunakan harus mampu
mengalirkan fase gerak dengan kecepatan 20 mL/menit (Munson, 1991).
4. Penyuntik / Sistem penyuntik Cuplikan
Teknik penyuntikan harus dilakukan dengan cepat untuk mencapai
ketelitian maksimum pada analisis kuantitatif, yang terpenting adalah sistem harus
18
Pada saat pengisian terokan, terokan dialirkan melewati keluk dan kelebihannya
dikeluarkan ke pembuang. Pada saat penyuntikan, katup diputar sehingga fase
gerak mengalir melewati keluk kolom. Presisi suntikan terokan dengan suntik
keluk ini dapat mencapai RSD 0.1% (Munson, 1991).
5. Kolom
Kolom merupakan jantung kromatograf, kebersihan atau kegagalan
analisis tergantung pada pilihan kolom dan kondisi kerja yang tepat. Dianjurkan
untuk mamasang penyaring 2 μm dijalur antar penyuntik dan kolom, untuk
menahan partikel yang dibawa fase gerak atau terokan, hal ini dapat
memperpanjang umur kolom. KCKT biasanya adalah UV 254 nm. Bila tanggapan
detektor lebih lambat dari elusi sampel timbullah pelebaran pita yang
memperburuk pemisahan. Pemilihan detektor KCKT tergantung pada sifat
sampel, fase gerak dan kepekaan yang tinggi dicapai (Munson, 1991).
Kolom dapat dibagi menjadi 2 kelompok, yaitu :
a. Kolom analitik :
garis tengah dalam 2-6 mm. untuk kemasan makropartikel panjang kolom 50 -
100 cm, untuk kemasan mikropartikel biasanya panjang kolomnya 10-30 cm.
b. Kolom preparatif :
garis tengah 6 mm atau lebih besar dan panjang 25-100 cm (Johnson,1991).
6. Detektor
Detektor harus memberikan cuplikan, tanggapan yang dapat diramalkan,
peka, hasil yang efisien dan tidak terpengaruh oleh perubahan suhu atau
19
nm. Bila tanggapan detektor lebih lambat dari elusi sampel timbullah pelebaran
pita yang memperburuk pemisahan. Pemilihan detektor KCKT tergantung pada
sifat sampel, fase gerak dan kepekaan yang tinggi dicapai (Munson, 1991).
6. Penguat Sinyal
Pada umumnya sinyal yang berasal dari detektor diperkuat terlebih dahulu
sebelum disampaikan pada alat perekam otomatik yang sesuai, biasanya berupa
suatu perekam potensiometrik. Dapat pula sinyal dikirimkan kepada suatu
integrator digital elektronik untuk mengukur luas puncak kromatogram secara
otomatik ( Munson, 1991).
7. Perekam
Perekam yang berfungsi merekam atau menunjukkan hasil pemeriksaan
suatu senyawa berupa peak (puncak). Dari daftar tersebut, secara kualitatif kita
20
BAB III
METODE PERCOBAAN
3.1 Tempat Pelaksanaan
Pengujian penetapan kadar Hidrokortison Asetat dalam sediaan krim
secara Kromatografi Cair Kinerja Tinggi dilakukan di Laboratorium PT. Kimia
Farma (Persero) Tbk. Plant Medan di Jalan Sisingamangaraja Km. 9 No. 59,
Medan.
3.2 Alat
Alat- alat yang digunakan pada analisa pengujian ini adalah timbangan
analitik elektrik, labu tentukur 50 mL dan 25 mL, beaker glass, gelas ukur, pipet
tetes, pipet volum 5 mL, spuit 10 mL, vial, batang pengaduk, filter phenomenex
0.45 μm, Ultrasonic digital, seperangkat alat Kromatografi Cair Kinerja Tinggi
(KCKT).
3.3 Bahan
Bahan-bahan yang digunakan pada analisa pengujian ini adalah
hidrokortison asetat standar, hidrokortison 2.5% krim, aquabidest, metanol, asam
asetat glasial, dan asetonitril.
3.4 Prosedur
3.4.1 Cara Pengambilan Sampel
Diambil produk ruahan (sampel) yang berada dalam 1 batch biasanya
berisi 20 gr, untuk sampel yang akan diuji ditimbang dengan menggunakan
21
3.4.2 Pembuatan Pelarut
Untuk pelarut yaitu campuran metanol dan asam asetat glasial dengan
perbandingan 1000 : 1 mL, dan untuk fase geraknya yaitu campuran asetonitril
dan aquabidest dengan perbandingan 600 : 400 dalam 1 L.
3.4.3 Pembuatan Larutan Standar
Ditimbang 25 mg hydrocortisone acetate standar, dimasukkan ke dalam
labu ukur 50 mL. Ditambahkan pelarut metanol dan asam asetat glasial (1000 : 1)
dalam labu ukur 50 mL dengan metanol 49,95 mL dan asam asetat glasial: 0,050
mL, diaddkan. Lalu dipipet 5 mL, masukkan ke dalam labu ukur 25 mL.
Diaddkan lagi dengan menggunakan pelarut sampai garis tanda, setelah itu
disaring menggunakan penyaring 0,45 μm. Larutan siap dianalisa.
3.4.4 Pembuatan Larutan Uji
Ditimbang seksama sebanyak 1 g krim, masukkan ke dalam beaker glass
100 mL. Ditambahkan (methanol : asam asetat glacial = 1000 : 1 mL) metanol
49,95 mL dan asam asetat glasial: 0,050 mL, kemudian masukkan ke dalam labu
ukur 50 mL dan larutkan dengan ultrasonic bath selama 15 menit, kemudian
tambahkan pelarut hingga volume 50 mL, kocok hingga homogen. Diultrasonik
selama 15 menit, lalu ditambah larutan methanol : asam asetat glacial sampai garis
tanda, homogenkan. Dipipet 5 mL, masukkan ke dalam labu ukur 25 mL.
Ditambahkan pelarut add 25 mL, kocok. Setelah itu disaring menggunakan
22
3.4.5 Perhitungan Kadar
Perhitungan kadar krim hidrokortison asetat dengan menggunakan rumus:
Kadar = Asp Abp ×
Bbp Bsp ×
50 x (25
5)
50 x (25
5) × 1000
25 × Kbp
Keterangan :
- Asp : Luas Area Sampel
- Abp : Luas Area Baku Pembanding
- Bbp : Bobot Baku Pembanding Hidrokortison yang ditimbang
(mg)
- Bsp : Bobot Sampel yang ditimbang (mg)
- 50 x (25/5) : Faktor Pengenceran Larutan Uji
- 50 x (25/5) : Faktor Pengenceran Larutan Standar
- Kbp : Kadar Baku Pembanding Hydrocortisone (%)
3.4.6 Persyaratan
Persyaratan Krim Hidrokortison menurut Farmakope Indonesia Edisi IV
ialah krim Hidrokortison mengandung Hidrokortison Asetat yaitu tidak kurang
23
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Telah dilakukan pengujian penetapan kadar Hidrokortison Asetat dalam
sediaan krim secara kromatografi cair kinerja tinggi (KCKT). Hasil pemeriksaan
[image:38.595.111.516.305.512.2]yang diperoleh dapat dilihat pada tabel berikut:
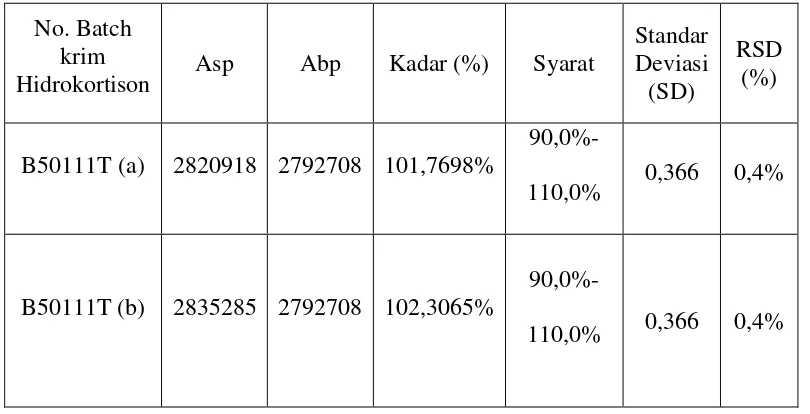
Tabel 1. Hasil penetapan kadar krim Hidrokortison secara KCKT
No. Batch krim
Hidrokortison Asp Abp Kadar (%) Syarat
Standar Deviasi (SD)
RSD (%)
B50111T (a) 2820918 2792708 101,7698%
90,0%-110,0% 0,366 0,4%
B50111T (b) 2835285 2792708 102,3065%
90,0%-110,0% 0,366 0,4%
4.2. Pembahasan
Dari tabel diatas, dapat dilihat adanya perbedaan kadar dari sampel duplo
yang diperiksa dalam satu batch, diantaranya kadar yang didapat adalah :
101,7698 % (No. Batch : B50111 T (a)), 102,3065% (No. Batch : B50111 T (b)),
dengan kadar rata-rata yaitu 102,0381 %. Standar deviasi yang didapat dari
sampel duplo adalah 0,366, sedangkan standar deviasi relatifnya (RSD) dari
sampel duplo adalah 0,4 %, Dimana syarat RSD yaitu 2%. Hasil ini diperoleh dari
24
Perhitungan kadar yang didapat secara manual berbeda dengan hasil yang
didapatkan di kromatogram. Hal ini disebabkan karena bobot hidrokortison asetat
sebagai baku pembanding ditimbang sebanyak 25,02 mg, sedangkan bobot baku
pembanding yang ditetapkan atau yang tertera pada etiket 25 mg. Penimbangan
bobot sampel dilakukan secara duplo yaitu 1000,63 mg dan 1000,45 mg yang
ditetapkan dalam 1 gram massa krim yaitu 1000 mg. Sehingga didapatkan hasil
kadar rata-ratanya tidak jauh berbeda, karena sampel yang diuji hanya satu batch
saja. Dari satu batch krim Hidrokortison produksi PT. Kimia Farma (Persero)
Tbk. Plant Medan yang dilakukan secara KCKT dinyatakan bahwa krim tersebut
memenuhi persyaratan kadar sesuai dengan yang tercantum pada persyaratan
Farmakope Indonesia Ed. IV. krim Hidrokortison mengandung Hidrokortison
Asetat yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0 % (Dirjen POM,
1995).
Penetapan kadar secara kromatografi cair kinerja tinggi merupakan salah
satu prosedur tetap yang digunakan sebagai penetapan kadar untuk produk krim
Hidrokortison pada industri farmasi PT. Kimia Farma (Persero) Tbk. Plant
Medan. Sediaan krim Hidrokortison yang diproduksi PT Kimia Farma (Persero)
Tbk. Plant Medan perlu diperiksa kadarnya, karena merupakan salah satu bentuk
pengujian dalam rangka pemastian mutu produk krim yang dikonsumsi oleh
25
BAB V
KESIMPULAN DAN SARAN
5.2 Kesimpulan
1. Metode yang digunakan untuk penetapan Kadar Hidrokortison Asetat
dalam sediaan krim yang diproduksi PT. Kimia Farma (Persero) Tbk.
Plant Medan adalah Kromatografi Cair Kinerja Tinggi.
2. Kadar Hidrokortison Asetat di dalam sediaan krim yang diproduksi PT.
Kimia Farma (Persero) Tbk. Plant Medan dengan kadar rata-rata yaitu
sebesar 102,0381 %. Maka kadar yang diperoleh tersebut memenuhi
persyaratan sesuai Farmakope Indonesia Edisi IV yaitu tidak kurang dari
90,0 % dan tidak lebih dari 110,0 % dari jumlah yang tertera pada etiket.
5.2 Saran
1. Sebaiknya digunakan juga metode lain untuk melakukan penetapatan
kadar Hidrokortison Asetat dalam sediaaan krim, sehingga dapat
dibandingkan hasilnya.
2. Sebaiknya dalam melakukan penetapan kadar Hidrokortison Asetat dalam
sediaan krim di uji sebanyak 3 batch, agar dapat dibandingkan kadar
26
DAFTAR PUSTAKA
Anief, M. (1984). Ilmu Farmasi. Jakarta: Ghalia Indonesia. Hal.48, 77.
Anief, M. (1991). Apa yang Perlu Diketahui tentang Obat Cetakan kedua. Yogyakarta: Gadjah Mada University Press. Hal.17-18, 39.
Anief, M. (1996).Penggolongan Obat Cetakan ke - 5. Yogyakarta: Gadjah Mada University Press. Hal. 21.
Anief, M. (1999). Ilmu Meracik Obat Teori dan Praktik. Yogyakarta: Gadjah Mada University Press. Hal. 71.
Ansel, H.C. (1989). Pengantar Bentuk Sediaan Farmasi Edisi Ke - 4. Jakarta: Universitas Indonesia Press. Hal.489, 513.
Dirjen, POM. (1995). Farmakope Indonesia Edisi ke – IV. Jakarta. Hal. 6, 435 – 437.
Joenoes, N.Z. (1990). Ars Prescribendi Resep Yang Rasional. Surabaya: Airlangga University Press. Hal. 73.
Johnson, E.L., dan Stevenson, R. (1991). Dasar Kromatografi Cair Kinerja
Tinggi. Bandung: ITB. Hal. 6, 9-10.
Katzung, B.G. (1989). Farmakologi Dasar dan Klinik. Jakarta: EGC. Hal.537-538.
Katzung, B.G. (2004). Farmakologi Dasar dan Klinik Buku 3. Jakarta: Salemba Empat. Hal.524-525.
Lachman, L. (1994). Teori dan Praktek Farmasi Industri. Jakarta: Universitas Indonesia. Hal.1092-1093.
Munson, J.W. (1991). Analis Farmasi Metode Moderen Parwa B. Surabaya: Airlangga University Press. Hal.14, 26-27, 30, 32, 43.
Polano, M.K. (1987). Terapi Kulit Topikal (Topical Skin Herapeutis). Jakarta: EGC. Hal. 26.
Rohman, A. (2007). Kimia Farmasi Analis. Yogyakarta: Pustaka Pelajar. Hal.378-379, 382.
27
Sartono.(1996). Apa Yang Sebaiknya Anda Ketahui Tentang Obat Wajib Apotek
Edisi ke – 2. Jakarta: PT. Gramedia Pustaka Utama. Hal. 81, 88 – 89.
Tanu, I. (1980). Farmakologi dan Terapi. Jakarta: FKUI Universitas Indonesia. Hal. 373.
Walsh, T.D. (1997). Kapita Selekta Penyakit dan Terapi. Jakarta: EGC. Hal. 287.
Watson, D.G. (2009).Analisis Farmasi Buku Ajar Untuk Mahasiswa Farmasi dan
28
LAMPIRAN
Lampiran 1.
a. Perhitungan Kadar Hidrokortison Asetat dalam Sediaan Krim secara
Kromatografi Cair Kinerja Tinggi.
Kadar hidrokortison dihitung dengan rumus sebagai berikut:
Kadar = Asp Abp ×
Bbp Bsp ×
50 x (25
5)
50 x (25
5) × 1000
25 × Kbp
Keterangan :
- Asp : Luas Area Sampel
- Abp : Luas Area Baku Pembanding
- Bbp : Bobot Baku Pembanding Hidrokortison yang ditimbang
(mg)
- Bsp : Bobot Sampel yang ditimbang (mg)
- 50 x (25/5) : Faktor Pengenceran Larutan Uji
- 50 x (25/5) : Faktor Pengenceran Larutan Standar
- Kbp : Kadar Baku Pembanding Hydrocortisone (%)
Dimana diketahui:
- Batch B50111 T (a) Batch B50111 T (b)
- Asp1 : 2820918 Asp2 : 2835285
- Abp : 2792708 Abp : 2792708
- Bbp : 25,02 Bbp : 25,02
- Kbp : 100,735 Kbp : 100,735
29 Kadar Batch B50111 T1
Kadar = Asp Abp ×
Bbp Bsp ×
50 x (25
5)
50 x (25
5) × 1000
25 × Kbp
Kadar1 =
2820918 2792708 ×
25,02 1000 ,63 ×
50 x (25
5)
50 x (25
5) × 1000
25 × 100,735% = 101,7698%
Kadar Batch B50111 T2
Kadar = Asp Abp ×
Bbp Bsp ×
50 x (25
5)
50 x (25
5) × 1000
25 × Kbp
Kadar2 =
2835285 2792708 ×
25,02 1000 ,45 ×
50 x (25
5)
50 x (25
5) × 1000
25 × 100,735% = 102,3065%
Kadar rata-rata batch B50111 T yang diperoleh:
Kadar rata-rata = (Kadar T1+Kadar T2) 2
Kadar rata-rata =101,7698% + 102,3065 %
2 = 102,0381%
b. Perhitungan standar deviasi (SD) dan standar deviasi relatif (RSD)
Hidrokortison Asetat dalam sediaan Krim secara Kromatografi Cair
Kinerja Tinggi.
Standar deviasi (SD) hidrokortison dihitung dengan rumus sebagai berikut:
SD = �∑(�−��)² (�−1)
Ket : X = nilai dari masing–masing pengukuran
X = rata-rata (mean) dari pengukuran
N = frekuensi penetapan
30 Tabel 2. Data luas area sampel
NO. Luas Area Sampel (�) (� − ��) ∑(� − ��)2
1. 2820918 -7184 51609856
2. 2835285 7184 51609856
�� 2828102
SD =
�
∑(�−��)2(�−1)
SD =
�
∑(�−��)² (�−1)
SD =
�
∑(−7184 )²(2−1)
SD =
�
∑(7184 )² (2−1)
SD =
√
51609856
SD =
√
51609856
SD =
√
51609856 + 51609856
SD =
√
103219712
SD = 10160
Standar deviasi relatif (RSD) luas area sampel dihitung dengan rumus sebagai berikut:
RSD =
����
x 100%
=
101602828102
x 100%
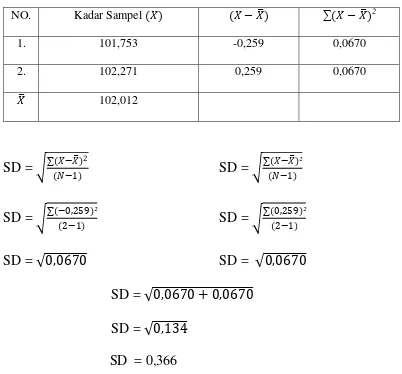
31 Tabel 3. Data kadar sampel
NO. Kadar Sampel (�) (� − ��) ∑(� − ��)2
1. 101,753 -0,259 0,0670
2. 102,271 0,259 0,0670
�� 102,012
SD =
�
∑(�−��)2(�−1)
SD =
�
∑(�−��)² (�−1)
SD =
�
∑(−0,259)²(2−1)
SD =
�
∑(0,259)² (2−1)
SD =
√
0,0670
SD =
√
0,0670
SD =
√
0,0670 + 0,0670
SD =
√
0,134
SD = 0,366
Standar deviasi relatif (RSD) kadar krim hidrokortison dihitung dengan rumus sebagai berikut:
RSD =
����
x 100%
=
0,366102,012
x 100%
32
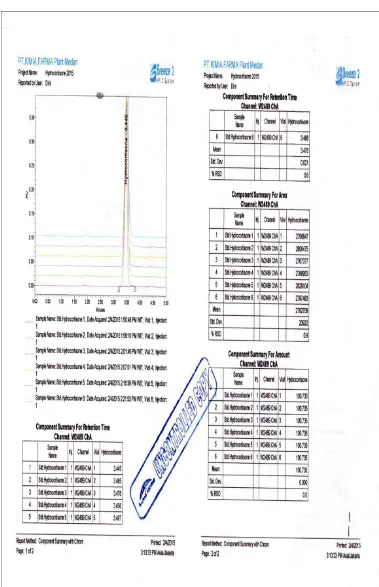
[image:47.595.114.493.154.741.2]Lampiran 2
34
[image:49.595.114.382.164.340.2]Lampiran 3
Gambar 1. Digital Semi Micro Balance
[image:49.595.114.390.404.590.2]