KARAKTERISASI DAN SKRINING FITOKIMIA SERTA
UJI EFEK ANTIDIARE EKSTRAK ETANOL
UMBI SARANG SEMUT (Myrmecodia tuberosa Jack.)
PADA TIKUS PUTIH JANTAN
SKRIPSI
OLEH: FALNA YATI NIM 111524084
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI DAN SKRINING FITOKIMIA SERTA
UJI EFEK ANTIDIARE EKSTRAK ETANOL
UMBI SARANG SEMUT (Myrmecodia tuberosa Jack.)
PADA TIKUS PUTIH JANTAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara
OLEH: FALNA YATI NIM 111524084
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KARAKTERISASI DAN SKRINING FITOKIMIA SERTA
UJI EFEK ANTIDIARE EKSTRAK ETANOL
UMBI SARANG SEMUT (Myrmecodia tuberosa Jack.)
PADA TIKUS PUTIH JANTAN
OLEH: FALNA YATI NIM 111524084
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 6 Juni 2014
Pembimbing I, Panitia Penguji,
Drs. Rasmadin Mukhtar, M.S., Apt. Dr. Marline Nainggolan, M.S., Apt. NIP 194909101980031002 NIP 195709091985112001
Pembimbing II, Drs. Rasmadin Mukhtar, M.S., Apt. NIP 194909101980031002
Dra. Suwarti Aris, M.Si., Apt. Marianne, S.Si., M.Si., Apt. NIP 195107231982032001 NIP 198005202005012006
Drs. Saiful Bahri, M.S., Apt. NIP 195208241983031001
Medan, Juli 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT, yang telah melimpahkan rahmat
dan karuaniaNya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi dengan judul “Karakterisasi dan Skrining Fitokimia serta
Uji Efek Antidiare Ekstrak Etanol Umbi Sarang Semut (Myrmecodia tuberosa
Jack.) Pada Tikus Putih Jantan’’ untuk memenuhi syarat dalam memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis menyampaikan ucapan terima kasih
kepada Dekan Fakultas Farmasi Universitas Sumatera Utara, Bapak Prof. Dr.
Sumadio Hadisahputra, Apt., yang telah memberikan bantuan dan fasilitas
selama masa pendidikan. Bapak Drs. Rasmadin Mukhtar M.S., Apt., dan Ibu
Dra. Suwarti Aris, M.Si., Apt., yang telah membimbing dengan penuh
kesabaran, tulus, ikhlas selama penelitian dan penulisan skripsi ini
berlangsung. Ibu Sri Yuliasmi, S.Farm., M.Si., Apt., selaku Penasehat
Akademik yang memberikan bimbingan kepada penulis selama masa
pendidikan. Gubernur Propinsi Papua yang telah memberikan kesempatan
kepada penulis untuk melanjutkan pendidikan di Fakultas Farmasi Universitas
Sumatera Utara.
Penulis juga ingin mempersembahkan rasa terima kasih yang tak
terhingga kepada suami dan anakku tercinta, Samsul Bahri dan Ananda
Maharani, ibundaku Surifa, ayahandaku Faisu (alm.) serta adik - adikku
tersayang, dan teman - teman ekstensi tahun 2011 yang selalu memberikan
Semoga Allah SWT memberikan balasan yang berlipat ganda dan
pahala yang sebesar - besarnya kepada semua pihak yang telah membantu
penyelesaian skripsi ini dan semoga kita tetap dalam lindunganNya.
Penulis menyadari bahwa skripsi ini masih memiliki banyak
kekurangan, oleh karena itu diharapkan kritik dan saran yang bersifat
membangun dari semua pihak guna perbaikan skripsi ini. Akhir kata penulis
berharap semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan
khususnya dibidang farmasi.
Medan, 1 Juli 2014 Penulis,
KARAKTERISASI DAN SKRINING FITOKIMIA SERTA UJI EFEK ANTIDIARE EKSTRAK ETANOL UMBI SARANG SEMUT (Myrmecodia tuberosa Jack.)
PADA TIKUS PUTIH JANTAN ABSTRAK
Diare merupakan masalah kesehatan masyarakat dan salah satu penyebab kematian di Indonesia. Tumbuhan sarang semut (Myrmecodia
tuberosa Jack.) telah digunakan secara empiris untuk mengobati diare.
Tumbuhan sarang semut mengandung tanin yang berpotensi mengurangi intensitas diare. Tujuan penelitian ini untuk mengetahui karakteristik simplisia, golongan senyawa kimia simplisia dan ekstrak etanol umbi sarang semut serta efek ekstrak etanol umbi sarang semut sebagai antidiare.
Simplisia umbi sarang semut dikarakterisasi dan diskrining fitokimia. Ekstraksi dilakukan secara maserasi menggunakan pelarut etanol 70%. Maserat yang diperoleh diuapkan dengan rotary evaporator selanjutnya difreeze dryer. Ekstrak yang diperoleh diskrining fitokimia dan diuji efek antidiare ekstrak etanol umbi sarang semut terhadap tikus putih jantan yang diinduksi oleum ricini menggunakan metode intestinal transit/metode lintasan usus halus yaitu menghitung persen lintas yang dilewati norit sebagai marker dan loperamid HCl sebagai pembanding.
Hasil makroskopik simplisia umbi sarang semut berupa potongan-potongan yang berlubang atau berongga, berwarna coklat kehitaman, berbau menyengat, berasa pahit dan agak sepat. Hasil mikroskopik serbuk simplisia terlihat adanya butir pati, parenkim, dan pembuluh kayu. Hasil penetapan kadar air simplisia umbi sarang semut diperoleh 7,98%, kadar sari larut air 6,95%, kadar sari larut etanol 5,75%, kadar abu total 2,80%, dan kadar abu tidak larut asam 0,25%. Hasil skrining fitokimia simplisia dan ekstrak etanol umbi sarang semut diperoleh senyawa flavonoid, glikosida, saponin, tanin, steroid/ triterpenoid. Ekstrak etanol umbi sarang semut mempunyai efek sebagai antidiare. Hasil uji efek antidiare kelompok norit diperoleh persen lintas marker norit (74,63 ± 0,23), oleum ricini dan norit (87,54 ± 0,78), ekstrak etanol umbi sarang semut dosis 2,5 mg/kg bb (66,46 ± 0,82), dosis 5 mg/kg bb (62,56 ± 0,45), dosis 7,5 mg/kg bb (55,37 ± 1,23), dosis 10 mg/kg bb (35,41 ± 0,98), dan loperamid HCl dosis 0,4 mg/kg bb (44,97 ± 1,20). Ekstrak etanol umbi sarang semut dosis 10 mg/kg bb mempunyai efek antidiare yang lebih baik dibandingkan loperamid HCl dosis 0,4 mg/kg bb, dan dosis 2,5, 5, 7,5 mg/kg bb (p < 0,05).
CHARACTERIZATION AND PHYTOCHEMICAL SCREENING AND ANTIDIARRHEAL TEST EFFECT OF ETHANOL EXTRACT
OF ANT PLANT (Myrmecodia tuberosa Jack.) ON WHITE MALE RATS
ABSTRACT
Diarrhea is a public health problem and one causes of death in Indonesia. Ant plant (Myrmecodia tuberosa Jack.) have been used empirically to treat diarrhea. Ant plant contain tannins have been potentially reduce the intensity of diarrhea. The purpose of this study are to understand about the characteristics of simplicia, chemical compounds of simplicia and ethanol extracts of ant plant and its antidiarrheal effect.
The simplicia ant plant characterization and phytochemical screening. Extraction is done by maserating using ethanol solvent 70%. Maserat that gained is evaporated by rotary evaporator then extract by freeze dryer. The extract that gained from previous process phytochemical screening and the antidiarrheal activity test of ethanol extract of ant plant on white male rats induced oleum ricini used intestinal transit method which by calculating the percentage of traffic that passed norit as a marker and loperamid HCl as control.
Macroscopic results of ant plant simplicia was small pieces perforated or hollow, brown to blackish, it was odor, taste bitter and a bit acidic. Microscopic results of simplicia powder showed starches, parenchyma, and xylem. The simplicia ant plant has the water content value was 7.98%, the water soluble extract of simplicia value was 6.95%, the ethanol soluble extract of simplicia value was 5.75%, the total ash value was 2.80%, and the acid insoluble ash was 0.25%. The result of phytochemical screening showed that simplicia and ethanol extract ant plant contained flavonoids, glycosides, saponins, tannins, steroids/triterpenoids. The ethanol extract of ant plant have antidiarrheal effects. The results antidiarrheal effect of norit group of cross marker norit percent (74.63 ± 0.23), oleum ricini and norit (87.54 ± 0.78), the ethanol extract ant plant a dose of 2.5 mg/kg bw (66.46 ± 0.82), a dose of 5 mg/kg bw (62.56 ± 0.45), a dose of 7.5 mg/kg bw (55.37 ± 1.23), a dose of 10 mg/kg bw (35.41 ± 0.98), and loperamide HCl dose of 0.4 mg/kg bw (44.97 ± 1.20). The ethanol extract of ant plant dose of 10 mg/kg bw have antidiarrheal effects better than loperamide HCl dose of 0.4 mg/kg bw, and dose of 2.5, 5, 7.5 mg/kg bw (p < 0.05).
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 5
1.6 Kerangka Konsep Penelitian ... 6
BAB II TINJAUAN PUSTAKA ... 7
2.1 Uraian Tumbuhan ... 7
2.1.1 Morfologi tumbuhan ... 7
2.1.2 Sistematika tumbuhan ... 9
2.1.4 Kandungan kimia tumbuhan ... 9
2.1.5 Manfaat tumbuhan ... 9
2.2 Simplisia dan Ekstrak ... 10
2.2.1 Simplisia ... 10
2.2.2 Ekstrak ... 10
2.2.3 Metode - metode ekstraksi ... 11
2.3 Uraian Farmakologi ... 12
2.3.1 Mulut ... 12
2.3.2 Faring ... 13
2.3.3 Esofagus ... 13
2.3.4 Lambung ... 13
2.3.5 Usus halus ... 13
2.3.6 Usus besar ... 14
2.4 Definisi Diare ... 14
2.4.1 Klasifikasi diare ... 15
2.4.2 Pengobatan diare ... 16
2.4.3 Obat - obat diare ... 16
2.5 Loperamid Hidrokloridum ... 17
2.6 Metode - Metode Pengujian Antidiare ... 18
BAB III METODE PENELITIAN... 20
3.1 Alat dan Bahan ... 20
3.1.1 Alat - alat ... 20
3.2 Pembuatan Larutan Pereaksi ... 21
3.2.1 Pereaksi Mayer ... 21
3.2.2 Pereaksi Dragendorff ... 21
3.2.3 Pereaksi Bouchardat ... 21
3.2.4 Pereaksi besi (III) klorida 1% ... 21
3.2.5 Pereaksi timbal (II) asetat 0,4 M ... 22
3.2.6 Pereaksi Molish ... 22
3.2.7 Pereaksi natrium hidroksida 2 N ... 22
3.2.8 Pereaksi asam klorida 2 N ... 22
3.2.9 Pereaksi Liebermann - Burchard ... 22
3.2.10 Pereaksi asam sulfat 2 N ... 22
3.3 Penyiapan Tumbuhan ... 22
3.3.1 Pengambilan bahan tumbuhan ... 22
3.3.2 Identifikasi bahan tumbuhan ... 23
3.3.3 Pengolahan bahan tumbuhan ... 23
3.4 Pemeriksaan Karakteristik Simplisia ... 23
3.4.1 Pemeriksaan makroskopik ... 24
3.4.2 Pemeriksaan mikroskopik ... 24
3.4.3 Penetapan kadar air ... 24
3.4.4 Penetapan kadar sari larut dalam air ... 25
3.4.5 Penetapan kadar sari larut dalam etanol ... 25
3.4.6 Penetapan kadar abu total ... 26
3.5 Skrining Fitokimia ... 27
3.5.1 Pemeriksaan alkaloid ... 27
3.5.2 Pemeriksaan flavonoid ... 27
3.5.3 Pemeriksaan glikosida ... 28
3.5.4 Pemeriksaan saponin ... 28
3.5.5 Pemeriksaan tanin ... 29
3.5.6 Pemeriksaan steroid/triterpenoid ... 29
3.6 Pembuatan Ekstrak Etanol Umbi Sarang Semut (EEUSS) 29 3.7 Uji Efek Antidiare ... 30
3.7.1 Penyiapan hewan percobaan ... 30
3.7.2 Pembuatan suspensi CMC 1% ... 30
3.7.3 Pembuatan suspensi loperamid HCl dari tablet Imodium® ... 30
3.7.4 Pembuatan suspensi ekstrak etanol umbi sarang semut ... 31
3.7.5 Pengujian efek antidiare ... 31
3.8 Pengumpulan Data ... 32
3.9 Analisis Data ... 32
BAB IV HASIL DAN PEMBAHASAN ... 33
4.1 Hasil Identifikasi Tumbuhan ... 33
4.2 Hasil Karakteristik Simplisia ... 33
4.3 Hasil Skrining Fitokimia ... 35
4.4 Pengujian Efek Antidiare ... 35
5.1 Kesimpulan ... 41
5.2 Saran ... 41
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Tabel Halaman
4.1 Hasil karakteristik simplisia umbi sarang semut ... 34
4.2 Hasil skrining fitokimia simplisia dan ekstrak etanol umbi
sarang semut ... 35
4.3 Efek ekstrak etanol umbi sarang semut pada tikus yang
DAFTAR GAMBAR
Gambar Halaman
1.1 Kerangka konsep penelitian ... 6
4.1 Grafik hubungan antara dosis dan persen rata - rata lintasan
DAFTAR LAMPIRAN
Lampiran Halaman
1 Hasil identifikasi tumbuhan ... 47
2 Gambar tumbuhan dan umbi sarang semut (Myrmecodia tuberosa Jack.) ... 48
3 Gambar potongan umbi sarang semut segar, simplisia dan serbuk umbi sarang semut ... 49
4 Hasil mikroskopik serbuk simplisia umbi sarang semut ... 50
5 Bagan kerja penelitian ... 51
6 Perhitungan karakteristik simplisia umbi sarang semut ... 52
7 Gambar tempat pemeliharaan tikus ... 55
8 Gambar tikus sebelum dan setelah dibedah ... 56
9 Gambar usus halus yang dilintasi marker norit ... 57
10 Tabel konversi perhitungan dosis untuk berbagai jenis hewan dengan manusia dan volume maksimum larutan sediaan uji yang dapat diberikan pada hewan uji ... 60
11 Perhitungan volume pemberian ekstrak etanol umbi sarang semut (EEUSS) dosis 2,5, 5, 7,5, 10 mg/kg bb ... 61
12 Perhitungan dosis loperamid HCl ... 63
13 Tabel dan grafik hasil orientasi dosis ekstrak etanol umbi sarang semut ... 64
14 Tabel analisis SPSS ... 66
15 Tabel hasil uji beda rata - rata antar kelompok (uji ANAVA) dan hasil uji Duncan ... 68
KARAKTERISASI DAN SKRINING FITOKIMIA SERTA UJI EFEK ANTIDIARE EKSTRAK ETANOL UMBI SARANG SEMUT (Myrmecodia tuberosa Jack.)
PADA TIKUS PUTIH JANTAN ABSTRAK
Diare merupakan masalah kesehatan masyarakat dan salah satu penyebab kematian di Indonesia. Tumbuhan sarang semut (Myrmecodia
tuberosa Jack.) telah digunakan secara empiris untuk mengobati diare.
Tumbuhan sarang semut mengandung tanin yang berpotensi mengurangi intensitas diare. Tujuan penelitian ini untuk mengetahui karakteristik simplisia, golongan senyawa kimia simplisia dan ekstrak etanol umbi sarang semut serta efek ekstrak etanol umbi sarang semut sebagai antidiare.
Simplisia umbi sarang semut dikarakterisasi dan diskrining fitokimia. Ekstraksi dilakukan secara maserasi menggunakan pelarut etanol 70%. Maserat yang diperoleh diuapkan dengan rotary evaporator selanjutnya difreeze dryer. Ekstrak yang diperoleh diskrining fitokimia dan diuji efek antidiare ekstrak etanol umbi sarang semut terhadap tikus putih jantan yang diinduksi oleum ricini menggunakan metode intestinal transit/metode lintasan usus halus yaitu menghitung persen lintas yang dilewati norit sebagai marker dan loperamid HCl sebagai pembanding.
Hasil makroskopik simplisia umbi sarang semut berupa potongan-potongan yang berlubang atau berongga, berwarna coklat kehitaman, berbau menyengat, berasa pahit dan agak sepat. Hasil mikroskopik serbuk simplisia terlihat adanya butir pati, parenkim, dan pembuluh kayu. Hasil penetapan kadar air simplisia umbi sarang semut diperoleh 7,98%, kadar sari larut air 6,95%, kadar sari larut etanol 5,75%, kadar abu total 2,80%, dan kadar abu tidak larut asam 0,25%. Hasil skrining fitokimia simplisia dan ekstrak etanol umbi sarang semut diperoleh senyawa flavonoid, glikosida, saponin, tanin, steroid/ triterpenoid. Ekstrak etanol umbi sarang semut mempunyai efek sebagai antidiare. Hasil uji efek antidiare kelompok norit diperoleh persen lintas marker norit (74,63 ± 0,23), oleum ricini dan norit (87,54 ± 0,78), ekstrak etanol umbi sarang semut dosis 2,5 mg/kg bb (66,46 ± 0,82), dosis 5 mg/kg bb (62,56 ± 0,45), dosis 7,5 mg/kg bb (55,37 ± 1,23), dosis 10 mg/kg bb (35,41 ± 0,98), dan loperamid HCl dosis 0,4 mg/kg bb (44,97 ± 1,20). Ekstrak etanol umbi sarang semut dosis 10 mg/kg bb mempunyai efek antidiare yang lebih baik dibandingkan loperamid HCl dosis 0,4 mg/kg bb, dan dosis 2,5, 5, 7,5 mg/kg bb (p < 0,05).
CHARACTERIZATION AND PHYTOCHEMICAL SCREENING AND ANTIDIARRHEAL TEST EFFECT OF ETHANOL EXTRACT
OF ANT PLANT (Myrmecodia tuberosa Jack.) ON WHITE MALE RATS
ABSTRACT
Diarrhea is a public health problem and one causes of death in Indonesia. Ant plant (Myrmecodia tuberosa Jack.) have been used empirically to treat diarrhea. Ant plant contain tannins have been potentially reduce the intensity of diarrhea. The purpose of this study are to understand about the characteristics of simplicia, chemical compounds of simplicia and ethanol extracts of ant plant and its antidiarrheal effect.
The simplicia ant plant characterization and phytochemical screening. Extraction is done by maserating using ethanol solvent 70%. Maserat that gained is evaporated by rotary evaporator then extract by freeze dryer. The extract that gained from previous process phytochemical screening and the antidiarrheal activity test of ethanol extract of ant plant on white male rats induced oleum ricini used intestinal transit method which by calculating the percentage of traffic that passed norit as a marker and loperamid HCl as control.
Macroscopic results of ant plant simplicia was small pieces perforated or hollow, brown to blackish, it was odor, taste bitter and a bit acidic. Microscopic results of simplicia powder showed starches, parenchyma, and xylem. The simplicia ant plant has the water content value was 7.98%, the water soluble extract of simplicia value was 6.95%, the ethanol soluble extract of simplicia value was 5.75%, the total ash value was 2.80%, and the acid insoluble ash was 0.25%. The result of phytochemical screening showed that simplicia and ethanol extract ant plant contained flavonoids, glycosides, saponins, tannins, steroids/triterpenoids. The ethanol extract of ant plant have antidiarrheal effects. The results antidiarrheal effect of norit group of cross marker norit percent (74.63 ± 0.23), oleum ricini and norit (87.54 ± 0.78), the ethanol extract ant plant a dose of 2.5 mg/kg bw (66.46 ± 0.82), a dose of 5 mg/kg bw (62.56 ± 0.45), a dose of 7.5 mg/kg bw (55.37 ± 1.23), a dose of 10 mg/kg bw (35.41 ± 0.98), and loperamide HCl dose of 0.4 mg/kg bw (44.97 ± 1.20). The ethanol extract of ant plant dose of 10 mg/kg bw have antidiarrheal effects better than loperamide HCl dose of 0.4 mg/kg bw, and dose of 2.5, 5, 7.5 mg/kg bw (p < 0.05).
BAB I PENDAHULUAN
1.1 Latar Belakang
Sampai saat ini diare masih menjadi masalah kesehatan dunia terutama
di negara berkembang termasuk Indonesia. Besarnya masalah tersebut terlihat
dari tingginya angka kesakitan dan kematian akibat diare (Adisasmito, 2007).
Hasil Riset Kesehatan Dasar (Rikesdas) tahun 2010 menunjukkan presentase
yang cukup tinggi, dalam sehari ada sekitar 460 balita meninggal karena
terjangkit diare, dan diare pun merenggut nyawa hampir 31,4% bayi usia 29
hari sampai 11 bulan. Angka kejadian diare disebagian wilayah Indonesia
hingga saat ini masih sangat tinggi. Indonesia menjadi salah satu negara
dengan tingkat kejadian diare yang cukup tinggi. Hasil survei kesehatan
Rumah Tangga (SKRT), diare menempati urutan kedua pada balita dan ketiga
pada bayi, serta nomor lima untuk semua umur, sebagai penyebab kematian di
Indonesia. Angka kematian akibat diare 23 per 100 ribu penduduk dan pada
balita 75 per 100 ribu balita (Kementrian Kesehatan Republik Indonesia,
2010).
Meningkatnya angka kejadian diare dan efek samping obat antidiare
yang ada saat ini, mendorong para peneliti untuk terus berusaha dalam
menemukan obat sebagai antidiare baru, terutama yang berasal dari tanaman
(Anas, dkk., 2000). Ada 88 jenis tumbuhan obat yang dinyatakan berkhasiat
sebagai obat diare. Tetapi sampai sekarang pengetahuan maupun pemakaian
sedangkan informasi ilmiah belum banyak diperoleh salah satu diantaranya
adalah sarang semut (Pudjarwoto, 1992).
Sarang semut yang telah dikenal oleh masyarakat luas adalah sarang
semut berupa lubang - lubang di tanah, bangunan, atau daun - daun di pohon
yang dibuat sendiri oleh koloni semut tertentu, bisa semut merah, rangkang,
semut hitam atau semut putih. Namun yang dimaksud disini adalah bukan
sarang semut seperti itu, melainkan tumbuhan epifit yang menempel di pohon
besar yang batang bagian bawahnya menggelembung berisi rongga - rongga
yang disediakan sebagai sarang semut jenis tertentu. Tumbuhan ini memang
seperti itu, sejak dari biji berkecambah batang bagian bawahnya secara
progresif menggelembung dengan sendirinya. Dalam waktu beberapa bulan,
batang bagian bawahnya terbentuk rongga - rongga yang cukup kompleks
mirip sarang semut. Rongga - rongga itu pada akhirnya akan menarik perhatian
semut - semut jenis tertentu untuk datang dan akhirnya membentuk koloni
didalamnya (Subroto, dkk., 2008).
Hasil uji penapisan kimia yang dilakukan terungkap bahwa tumbuhan
sarang semut mengandung senyawa - senyawa kimia dari golongan flavonoid,
tanin, polifenol, tokoferol, dan mineral - mineral lainnya seperti: kalsium, besi,
fosfor, natrium, kalium, seng (Subroto, dkk., 2008). Beberapa penelitian yang
telah dilakukan terhadap umbi tumbuhan sarang semut antara lain: efek
antiinflamasi ekstrak etanol umbi sarang semut (Kristina, 2008), uji aktivitas
antikanker ekstrak sarang semut terhadap terhadap sel hela dan MCM – B2
potensi antimikroba ekstrak etanol umbi sarang semut terhadap Candida
albicans, Escherichia coli, dan Staphylococcus aureus (Efendi, dkk., 2013),
dan uji efek ekstrak etanol sarang semut terhadap perubahan bobot badan
mencit (Khairuddin, dkk., 2012). Terkait potensinya dalam mengatasi keluhan
penyakit diare, telah dibuktikan adanya efek antidiare ekstrak air umbi sarang
semut jenis Myrmecodia pendens (Defrin, dkk., 2010) dan uji efek antidiare
infus sarang semut dari jenis Hydnophytum sp (Soares, 2010). Tumbuhan
sarang semut merupakan tumbuhan yang termasuk dalam suku Rubiaceae dan
terdiri dari 5 kelompok genus. Namun, hanya genus Myrmecodia dan
Hydnophytum yang paling dekat berasosiasi dengan semut (Florentinus, 2013).
Tumbuhan sarang semut yang banyak dimanfaatkan sebagai bagian dari
pengobatan adalah Myrmecodia tuberosa, Myrmecodia pendens dan
Hydnophytum formicarum (Rubiaceae) (Soeksmanto, dkk., 2010).
Berdasarkan uraian di atas, maka peneliti melakukan penelitian
terhadap umbi sarang semut (Myrmecodia tuberosa Jack.) sebagai antidiare.
Penelitian meliputi karakteristik simplisia, skrining fitokimia simplisia dan
ekstrak serta uji efek antidiare ekstrak etanol umbi sarang semut (Myrmecodia
tuberosa Jack.) terhadap tikus putih jantan dengan menggunakan metode
intestinal transit/metode lintasan usus halus, sebagai penginduksi diare
diberikan oleum ricini, sebagai marker diberikan norit, dan sebagai
1.2 Perumusan Masalah
Berdasarkan latar belakang di atas, maka perumusan masalah penelitian
adalah:
a. data karakteristik simplisia umbi sarang semut belum ada.
b. apa kandungan golongan senyawa kimia simplisia dan ekstrak etanol
umbi sarang semut?
c. apakah ekstrak etanol umbi sarang semut memiliki efek antidiare yang
diinduksi dengan oleum ricini?
1.3 Hipotesis
Berdasarkan perumusan masalah di atas, maka hipotesis penelitian ini
adalah:
a. memperoleh karakteristik simplisia umbi sarang semut sehingga dapat
dijadikan sebagai acuan karakteristik simplisia.
b. simplisia dan ekstrak etanol umbi sarang semut mengandung senyawa
flavonoid, glikosida, saponin, tanin, steroid/triterpenoid.
c. ekstrak etanol umbi sarang semut memiliki efek antidiare.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
a. untuk mengetahui karakteristik simplisia umbi sarang semut.
b. untuk mengetahui golongan senyawa kimia yang terkandung dalam
simplisia dan ekstrak etanol umbi sarang semut.
antidiare pada tikus putih jantan yang diinduksi oleum ricini.
1.5 Manfaat Penelitian
Manfaat yang diperoleh dari penelitian ini adalah:
a. dapat menambah inventaris tanaman obat yang berkhasiat sebagai
antidiare.
b. dapat mengembangkan umbi sarang semut menjadi suatu sediaan herbal
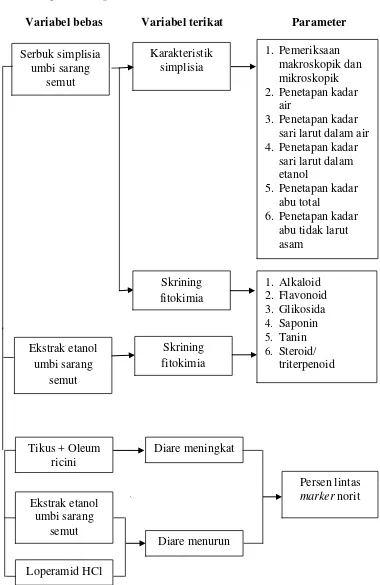
1.6 Kerangka Konsep Penelitian
Variabel bebas Variabel terikat Parameter
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan 2.1.1 Morfologi tumbuhan
Sarang semut merupakan tumbuhan yang berasal dari Papua. Walaupun
sarang semut ini tidak hanya terdapat di Papua, namun keragaman sarang
semut di pulau tersebut paling tinggi, sampai 10 varietas. Sebaran Myrmecodia
tuberosa, juga terdapat juga di Ambon, Sumatera Barat, Sulawesi Utara, dan
Kalimantan. Sarang semut tersebar dari hutan bakau dan pohon - pohon di
pinggir pantai hingga ketinggian 2.400 m. Sarang semut paling banyak
ditemukan di padang rumput, di hutan dan daerah pertanian terbuka dengan
ketinggian sekitar 600 m dan jarang ditemukan di hutan tropis dataran rendah.
Sarang semut banyak ditemukan menempel pada beberapa pohon, umumnya di
pohon kayu putih, cemara gunung, kaha, dan pohon beech, tetapi jarang pada
pohon - pohon dengan batang halus dan rapuh. Adapun secara morfologi,
sarang semut mempunyai ciri - ciri sebagai berikut:
a. Umbi
Umbi pada tumbuhan sarang semut umumnya berbentuk bulat saat muda,
kemudian menjadi lonjong memendek atau memanjang setelah tua.
Umbinya hampir selalu berduri. Dalam umbi sarang semut terdapat labirin
yang dihuni oleh semut atau cendawan. Keunikan tumbuhan ini terletak
pada koloni semut yang bersarang pada umbi sehingga terbentuk lubang
semut. Pusat Penelitian dan Pengembangan Zoologi mengidentifikasi
semut di dalam labirin adalah jenis Ochetellus sp. Simbiosis mutualisme
terjadi diantara semut dan Myrmecodia. Semut akan melindungi
Myrmecodia dari herbivora dan predator lain dan Myrmecodia menjadi
rumah yang nyaman sekaligus menyediakan sumber pakan untuk
kelangsungan hidup koloni semut (Muhammad, 2011).
b. Batang
Tumbuhan sarang semut memiliki satu cabang, jarang bercabang.
Batangnya tebal dan ruasnya pendek, berwarna coklat muda hingga abu
-abu.
c. Daun
Daun sarang semut tunggal, bertangkai, tersusun menyebar namun lebih
banyak terkumpul diujung batang, dan berwarna hijau. Berbentuk jorong,
panjang 20 - 40 cm, lebar 5 - 7 cm. Helaian agak tebal, lunak dengan ujung
tumpul dan pangkal meruncing. Bagian tepi rata, permukaan halus, dan
tulang daun berwarna merah (Florentinus, 2013).
d. Bunga
Pembungaan dimulai sejak terbentuknya beberapa ruas (internodal) pada
batangnya dan ada pada tiap nodus (buku), bunga berwarna putih. Sarang
semut adalah tumbuhan yang melakukan penyerbukan sendiri
2.1.2 Sistematika tumbuhan
Menurut Tjitrosoepomo (2005) sistematika tumbuhan sarang semut
adalah sebagai berikut:
Divisi : Spermatophyta
Sub Divisi : Angiospermae
Kelas : Dicotyledoneae
Ordo : Rubiales
Family : Rubiaceae
Genus : Myrmecodia
Species : Myrmecodia tuberosa Jack.
2.1.3 Nama daerah
Di Indonesia, namanya berbeda - beda. Di Papua, sarang semut disebut
sebagai nongon. Di Jawa dikenal sebagai urek - urek polo. Sedangkan di
Sumatera disebut kepala beruk dan rumah semut.
2.1.4 Kandungan kimia tumbuhan
Kandungan kimia dari sarang semut antara lain flavonoid, tanin,
polifenol, tokoferol, mineral - mineral lainnya seperti kalsium, besi, fosfor,
natrium, kalium, seng, magnesium (Muhammad, 2011).
2.1.5 Manfaat tumbuhan
Sarang semut selain mampu mencegah dan mengobati kanker juga
efektif membantu penyembuhan penyakit gangguan jantung, ambien (wasir),
rematik, stroke, maag, gangguan fungsi, prostat, pegal linu, melancarkan ASI,
mampu menghambat enzim xantin oksidan yang memicu asam urat dan radikal
bebas (florentinus, 2013).
2.2 Simplisia dan Ekstrak 2.2.1 Simplisia
Simplisia adalah bahan alamiah yang dipergunakan sebagai obat yang
belum mengalami pengolahan apapun juga kecuali dikatakan lain, berupa
bahan yang telah dikeringkan. Simplisia dibedakan simplisia nabati, simplisia
hewani dan simplisia pelikan (mineral). Simplisia nabati adalah simplisia yang
berupa tumbuhan utuh, bagian tumbuhan atau eksudat tumbuhan (Ditjen POM,
2000).
2.2.2 Ekstrak
Ekstrak adalah sediaan kental yang diperoleh dengan mengekstraksi
senyawa aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut
yang sesuai (Ditjen POM, 2000).
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan suatu
pelarut cair. Senyawa aktif yang terdapat dalam simplisia dapat digolongkan ke
dalam golongan minyak atsiri, alkaloid, flavonoid dan lain - lain. Diketahui
senyawa aktif yang dikandung simplisia akan mempermudah pemilihan pelarut
2.2.3 Metode - metode ekstraksi
Menurut Ditjen POM (2000) metode ekstraksi dengan menggunakan
pelarut dapat dibagi ke dalam dua cara yaitu:
a. Cara dingin, yaitu:
1. Maserasi, adalah proses pengektraksian simplisia dengan menggunakan
pelarut dengan beberapa kali pengocokan atau pengadukan pada
temperatur ruangan (kamar). Secara teknologi termasuk ekstraksi dengan
prinsip metode pencapaian konsentrasi pada keseimbangan. Maserasi
kinetik berarti dilakukan pengadukan yang kontinu (terus - menerus).
Remaserasi berarti dilakukan pengulangan penambahan pelarut setelah
dilakukan penyaringan maserat pertama dan seterusnya.
2. Perkolasi, adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna (exhaustive extraction) yang umumnya dilakukan pada
temperatur ruangan. Proses terdiri dari tahapan pengembangan bahan,
tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/
penampungan ekstrak) terus - menerus sampai diperoleh ekstrak (perkolat)
yang jumlahnya 1 - 5 kali bahan.
b. Cara panas
1. Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya,
selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan
dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses
pada residu pertama sampai 3 - 5 kali sehingga dapat termasuk proses
2. Soxhlet, adalah ekstraksi menggunakan pelarut yang selalu baru yang
umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu
dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
3. Digesti, adalah maserasi kinetik (dengan pengadukan kontinu) pada
temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu secara
umum dilakukan pada temperatur 40 - 50°C.
4. Infus, adalah ekstraksi dengan pelarut air pada temperatur penangas air
(bejana infus tercelup dalam penangas air mendidih, temperatur terukur 96
- 98°C) selama waktu tertentu (15 - 20 menit).
5. Dekok, adalah infus pada waktu yang lebih lama (≥ 30 menit) dan
temperatur sampai titik didih air.
2.3 Uraian Farmakologi
Saluran pencernaan makanan merupakan saluran yang menerima
makanan dari luar dan dipersiapkan untuk diserap oleh tubuh melalui proses
pencernaan (pengunyahan, penelanan dan pencampuran) dengan enzim dan zat
cair mulai dari mulut (oris) sampai anus (Syaifuddin, 2006). Saluran
pencernaan terdiri dari:
2.3.1 Mulut
Mulut merupakan jalan masuk yang dilalui makanan pertama kali pada
sistem pencernaan. Rongga mulut dilengkapi dengan alat pencernaan (gigi dan
lidah) serta kelenjar pencernaan untuk membantu pencernaan makanan
2.3.2 Faring
Faring merupakan organ yang menghubungkan rongga mulut dengan
kerongkongan (esofagus). Di dalam lengkung faring terdapat tonsil (amandel)
yaitu kumpulan kelenjar limfe yang banyak mengandung limfosit yang
merupakan pertahanan tubuh terhadap infeksi (Tarwoto dkk., 2009).
2.3.3 Esofagus
Esofagus merupakan bagian saluran pencernaan sepanjang ± 25 cm dan
berdiameter 2 cm. Esofagus berbentuk seperti tabung berotot yang
menghubungkan rongga mulut dengan lambung. Fungsi esofagus adalah
menyalurkan makanan ke lambung. Agar makanan dapat berjalan sepanjang
esofagus, terdapat gerakan peristaltik sehingga makanan dapat berjalan menuju
lambung (Tarwoto dkk., 2009).
2.3.4 Lambung
Lambung adalah bagian dari saluran pencernaan yang dapat mekar
paling banyak. Fungsi lambung adalah menerima makanan dari esofagus dan
bekerja sebagai penimbun sementara, sedangkan kontraksi otot mencampur
makanan dengan getah lambung (Handoyo, 2008).
2.3.5 Usus halus
Usus halus adalah bagian dari sistem pencernaan makanan yang
berpangkal pada pilorus dan berakhir pada sekum panjangnya sekitar 3 m
dengan lebar 2,5 cm, walaupun tiap orang memiliki ukuran yang berbeda -
beda, dan merupakan saluran paling panjang tempat proses pencernaan
Usus halus sering disebut dengan usus kecil karena ukuran diameternya
lebih kecil jika dibandingkan dengan usus besar. Usus halus ini terbagi menjadi
3 bagian yaitu duodenum disebut usus 12 jari panjangnya ± 25 cm, jejunum
panjangnya ± 2,5 m, serta ileum panjangnya ± 3,6 m (Tarwoto dkk., 2009).
Fungsi dari usus halus adalah menerima zat - zat makanan yang sudah
dicerna untuk diserap melalui kapiler - kapiler darah dan saluran - saluran
limfe, menyerap protein dalam bentuk asam amino, serta karbohidrat diserap
dalam bentuk monosakarida (Syaifuddin, 2006).
2.3.6 Usus besar
Panjang usus besar ± 180 cm dan terdiri atas sekum, apendiks, kolon,
rektum, dan anus. Bahan makanan masuk dalam sekum masih setengah cair,
kemudian dalam kolon menjadi setengah padat. Fungsi usus besar adalah
absorpsi cairan, mensekresi mukus (lendir), dan berfungsi sebagai pelumas.
Pelumasan ini penting karena cairan diabsorpsi dan feses menjadi lebih keras
sehingga kemungkinan merusak mukosa menjadi lebih besar (Tambayong,
2001).
2.4 Definisi Diare
Diare adalah defekasi yang sering dalam sehari dengan feses yang
lembek atau cair, terjadi karena chymus yang melewati usus kecil dengan
cepat, kemudian feses melewati usus besar dengan cepat sehingga tidak cukup
waktu untuk absorpsi, hal ini menyebabkan dehidrasi dan ketidakseimbangan
elektrolit.
(chymus), kemudian diteruskan ke usus halus untuk diuraikan lebih lanjut oleh
enzim - enzim. Setelah terjadi proses resorpsi, sisa chymus yang terdiri atas
90% air dan sisa - sisa makanan yang sulit dicernakan didorong masuk ke usus
besar. Dengan bantuan bakteri pengurai yang terdapat diusus besar sebagian
besar sisa makanan masih dapat diserap dan air diresorpsi kembali. Dengan
demikian, lambat laun isi usus menjadi suatu massa yang lebih padat (Endang
dan Puspadewi, 2012).
2.4.1 Klasifikasi diare
Berdasarkan lama waktu diare menurut Sudoyo, dkk (2009) diare
dibagi menjadi dua kelompok yaitu:
a. Diare akut
Adalah diare yang berlangsung kurang dari 15 hari. Diare akut disebabkan
oleh banyak penyebab antara lain infeksi (bakteri, parasit, virus),
keracunan makanan, efek obat - obatan dan lain - lain.
b. Diare kronis
Adalah diare yang berlangsung lebih dari 15 hari. Diare kronis terjadi pada
tumor dan penyakit - penyakit usus beradang kronis.
Berdasarkan penyebab terjadinya diare menurut Sundari, dkk (2001)
diare dibagi menjadi dua kelompok yaitu:
a. Diare tidak bersifat langsung
Disebabkan karena higiene perorangan dan sanitasi lingkungan yang
kurang baik, lingkungan hidup yang tidak memenuhi syarat kesehatan. Hal
b. Diare yang bersifat langsung
Dapat dibagi atas:
1. Infeksi mikroorganisme seperti bakteri, virus, parasit.
2. Rangsangan zat atau makanan yang masuk ke dalam saluran
pencernaan seperti keracunan makanan, alergi makanan tertentu.
3. Melabsorpsi atau gangguan absorpsi makanan (Sundari, dkk., 2001).
2.4.2 Pengobatan diare
Pengobatan diare secara garis besar dibagi menjadi 2 yaitu:
a. Pengobatan simtomatik
Dimana daya kerja obat mengurangi peristaltik usus atau memproteksi
usus, menciutkan lapisan permukaan usus (adstringensia) dan zat - zat
yang dapat menyerap racun yang dihasilkan oleh bakteri (adsorben)
(Sundari, dkk., 2001).
b. Pengobatan kausatif
Dimana bakteri yang menjadi penyebab diare dimatikan dengan zat
antibakteri.
2.4.3 Obat - obat diare
Kelompok obat yang sering digunakan pada diare adalah:
a. Kemoterapeutika
Untuk terapi kausal, yakni memberantas bakteri penyebab diare, seperti
antibiotika, sulfonamida, kinolon, dan furazolidon.
b. Obstipansia
cara yakni:
1. Zat - zat penekan peristaltik sehingga memberikan banyak waktu untuk
resorpsi air dan elektrolit oleh mukosa usus: candu dan alkaloidnya,
derivat - derivat petidin (difenoksilat dan loperamid), dan antikolinergika
(atropin, ekstrak belladona).
2. Adstringensia, yang menciutkan selaput lendir usus, misalnya asam samak
(tanin dan tanalbumin, garam - garam bismut dan aluminium).
3. Adsorbensia, misalnya carbo adsorbens yang permukaannya dapat
menyerap (adsorpsi) zat - zat beracun (toksin) yang dihasilkan oleh bakteri
atau yang berasal dari makanan (udang, ikan).
4. Spasmolitika, yakni zat - zat yang dapat melepaskan kejang - kejang otot
yang mengakibatkan nyeri perut pada diare, antara lain papaverin, dan
oksifenonium (Tan dan Rahadja, 2007).
2.5 Loperamid Hidrokloridum
Loperamid merupakan derivat difenoksilat dengan khasiat obstipasi
yang 2 - 3 kali lebih kuat tetapi tanpa khasiat terhadap SSP, sehingga tidak
mengakibatkan ketergantungan. Zat ini mampu menormalkan keseimbangan
resorpsi - sekresi dari sel - sel mukosa, yaitu memulihkan sel - sel yang berada
dalam keadaan hipersekresi ke keadaan resorpsi normal kembali (Tan dan
Rahardja, 2007).
Loperamid memperlambat motilitas saluran cerna melalui efek pada
otot sirkular dan longitudinal usus. Efek samping yang paling umum
hariannya tidak boleh melebihi 16 mg (Goodman dan Gilman’s, 2012).
2.6 Metode - Metode Pengujian Antidiare
Aktivitas antidiare ditujukan terbatas pada aktivitas obat yang dapat
memperlambat peristaltik usus, sehingga mengurangi frekuensi defekasi dan
memperbaiki konsistensi feses. Ada dua metode uji yang bisa digunakan, yaitu
metode intestinal transit dan metode proteksi terhadap diare yang disebabkan
oleh oleum ricini.
a. Metode intestinal transit
Metode intestinal transit dapat digunakan untuk mengevaluasi aktivitas
obat antidiare, laksansia, antispasmodik, berdasarkan pengaruhnya pada rasio
jarak usus yang ditempuh oleh suatu marker dalam waktu tertentu terhadap
panjang usus keseluruhan pada hewan percobaan mencit dan tikus. Obat
antidiare akan memperkecil rasio, sedangkan obat laksansia dan obat
antispasmodik akan memperbesar rasio ini dibandingkan rasio hewan tanpa
perlakuan. Sampel, penginduksi diare dan norit diberikan pada hewan uji.
Kemudian dalam rentang waktu tertentu hewan dikorbankan, diukur panjang
usus keseluruhan. Hitung persen lintasan norit dengan cara membandingkan
panjang lintasan norit dengan panjang usus. Jika persen yang didapat lebih
kecil dari kontrol bahwa dapat disimpulkan sampel uji memiliki efek antidiare
(KKIPM, 1993).
b. Metode proteksi terhadap diare oleh oleum ricini
Kandungan utama dari oleum ricini, yakni trigliserida dari asam
menjadi gliserida dan asam risinoleat. Sehingga surfaktan anionik, zat ini
bekerja mengurangi absorpsi cairan dan elektrolit serta menstimulasi peristaltik
usus, sehingga berkhasiat sebagai laksansia berdasarkan kerja ini. Obat yang
berkhasiat antidiare akan melindungi hewan percobaan mencit terhadap diare
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah penelitian eksperimental.
Penelitian meliputi pengambilan dan pengolahan bahan tumbuhan, identifikasi
tumbuhan, karakteristik simplisia, skrining fitokimia simplisia, pembuatan
ekstrak dengan cara maserasi, skrining fitokimia ekstrak, penyiapan hewan
percobaan dan pengujian efek antidiare ekstrak etanol umbi sarang semut
diberikan secara oral pada hewan percobaan. Data hasil penelitian dianalisis
secara ANAVA (analisis variansi) dan dilanjutkan dengan uji beda rata - rata
Duncan menggunakan program SPSS (Statistical Product and Service
Solution) versi 17.
3.1 Alat dan Bahan 3.1.1 Alat - alat
Alat - alat yang digunakan terdiri dari: alat - alat gelas laboratorium,
pisau, talenan, lemari pengering, blender (Philip), oven (Memmert), neraca
listrik (Mettler Toledo), mikroskop (Olympus), ayakan, kaca objek, pipet tetes,
neraca hewan (Presica Geniweigher GW - 1500), rotary evaporator (Heidolph
WB 2000), krus porselin, spuit, oral sonde, lumpang dan stamfer, waterbath,
freeze dryer (Edward), aluminium foil, kertas saring, spatula, seperangkat alat
bedah hewan, meja bedah, kandang tikus.
3.1.2 Bahan - bahan
sarang semut. Bahan kimia yang digunakan adalah etanol 70%, etanol 96%
(teknis), n - heksan (teknis), pereaksi Bouchardat, Dragendorff, Mayer, besi
(III) klorida 4,5% b/v, Molish, timbal (II) asetat 0,4 M, asam sulfat 6 N, asam
klorida 2 N, Lieberman - Burchard, toluen, kloroform, asam klorida, akuades
(teknis), karboksi metil selulosa (CMC), norit, loperamid HCl (tablet
Imodium®), oleum ricini.
3.2 Pembuatan Larutan Pereaksi 3.2.1 Pereaksi Mayer
Sebanyak 5 g kalium iodida dalam 10 ml air suling kemudian
ditambahkan larutan 1,36 g merkuri (II) klorida dalam 60 ml air suling. Larutan
dikocok dan ditambahkan air suling hingga 100 ml (Ditjen POM, 1995).
3.2.2 Pereaksi Dragendorff
Sebanyak 0,8 g bismut nitrat dilarutkan dalam asam nitrat pekat 20 ml
kemudian dicampur dengan larutan kalium iodida sebanyak 27,2 g dalam 50 ml
air suling. Campuran didiamkan sampai memisah sempurna. Larutan jernih
diambil dan diencerkan dengan air suling hingga 100 ml (Ditjen POM, 1995).
3.2.3 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida dilarutkan dalam 20 ml air suling kemudian
ditambah 2 g iodium sambil diaduk sampai larut, lalu ditambah air suling
hingga 100 ml (Ditjen POM, 1995).
3.2.4 Pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling hingga 100
3.2.5 Pereaksi timbal (II) asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat ditimbang, kemudian dilarutkan
dalam air suling hingga 100 ml (Ditjen POM, 1995).
3.2.6 Pereaksi Molish
Sebanyak 3 g α - naftol dilarutkan dalam asam nitrat 0,5 N hingga 100
ml larutan (Harborne, 1987).
3.2.7 Pereaksi natrium hidroksida 2 N
Sebanyak 8 g kristal natrium hidroksida dilarutkan dalam air suling
hingga diperoleh larutan 100 ml (Depkes, 1979).
3.2.8 Pereaksi asam klorida 2 N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling
sampai 100 ml (Depkes, 1979).
3.2.9 Pereaksi Liebermann - Burchard
Sebanyak 2 bagian asam asetat anhidrat dicampurkan dengan 1 bagian
asam sulfat pekat (Harborne, 1987).
3.2.10 Pereaksi asam sulfat 2 N
Sebanyak 10 ml asam sulfat pekat diencerkan dengan air suling hingga
diperoleh 100 ml larutan (Depkes, 1979).
3.3 Penyiapan Tumbuhan
3.3.1 Pengambilan bahan tumbuhan
Pengambilan bahan dilakukan secara purposif yaitu tanpa
membandingkan dengan tumbuhan yang sama dari daerah lain. Bahan
Kelurahan Jika, Distrik Mimika Timur, Kabupaten Mimika, Provinsi Papua
tanggal 5 Juli 2013.
3.3.2 Identifikasi bahan tumbuhan
Identifikasi tumbuhan dilakukan di Lembaga Ilmu Pengetahuan
Indonesia (LIPI), Pusat Penelitian Biologi, Bidang Botani Pusat Penelitian
Biologi - LIPI Bogor. Hasil identifikasi tumbuhan dapat dilihat pada Lampiran
1, halaman 47 dan gambar tumbuhan dan umbi sarang semut dapat dilihat pada
Lampiran 2, halaman 48.
3.3.3 Pengolahan bahan tumbuhan
Umbi dari sarang semut yang masih segar dikupas kulitnya, dicuci,
kemudian ditiriskan. Belah umbi tersebut menjadi beberapa bagian. Bersihkan
semut - semut yang terdapat didalamnya. Dipotong - potong dengan ukuran
panjang 4 - 5 cm, lebar 4 - 5 cm, dan tebal 0,3 - 0,4 cm, lalu ditimbang sebagai
berat basah adalah 3200 g, dikeringkan didalam lemari pengering. Umbi
dianggap kering jika dipatahkan hancur dan ditimbang sebagai berat kering
adalah 450 g. Kemudian simplisia diblender hingga menjadi serbuk. Gambar
potongan umbi sarang semut segar, simplisia dan serbuk umbi sarang semut
dapat dlilihat pada Lampiran 3, halaman 49 dan bagan kerja penelitian dapat
dilihat pada Lampiran 5, halaman 51.
3.4 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik
dan mikroskopik, penetapan kadar air, penetapan kadar sari larut dalam air,
kadar abu tidak larut dalam asam. Hasil karakteristik simplisia umbi sarang
semut dapat dilihat pada Tabel 4.1, halaman 34.
3.4.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk, warna,
bau dan rasa dari simplisia umbi sarang semut.
3.4.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia umbi
sarang semut. Serbuk simplisia ditaburkan di atas kaca objek yang telah ditetesi
dengan larutan kloralhidrat dan ditutup dengan kaca penutup, selanjutnya
diamati di bawah mikroskop. Gambar mikroskopik serbuk simplisia umbi
sarang semut dapat dilihat pada Lampiran 4, halaman 50.
3.4.3 Penetapan kadar air
Penetapan kadar air dilakukan menurut metode Azeotropi (destilasi
toluena). Alat terdiri dari labu alas bulat 500 ml, pendingin, tabung
penyambung, tabung penerima 5 ml berskala 0,05 ml, alat penampung dan
pemanas listrik.
a. Penjenuhan toluen
Sebanyak 200 ml toluen dan 2 ml air suling dimasukan ke dalam labu
alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi
selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit,
kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,05 ml.
b. Penetapan kadar air
seksama, labu dipanaskan hati - hati selama 15 menit. Setelah toluen mendidih,
kecepatan tetesan diatur lebih kurang 2 tetes tiap detik sampai sebagian besar
air terdestilasi, kemudian kecepatan tetesan dinaikkan hingga 4 tetes tiap detik.
Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan toluen.
Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan
mendingin pada suhu kamar. Setelah air dan toluen memisah sempurna,
volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air yang
dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa.
(WHO, 1998). Hasil perhitungan kadar air dapat dilihat pada Lampiran 6,
halaman 52.
3.4.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml
air - kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu
bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan
selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai
kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan
ditara. Sisa dipanaskan pada suhu 105°C sampai bobot tetap. Kadar sari yang
larut dalam air dihitung dalam persen terhadap bahan yang telah dikeringkan
(Ditjen POM, 1995). Hasil perhitungan kadar sari larut dalam air dapat dilihat
pada Lampiran 6, halaman 52.
3.4.5 Penetapan kadar sari larut dalam etanol
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml
pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring cepat untuk
menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering
dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara.
Sisa dipanaskan pada suhu 105°C sampai bobot tetap. Kadar sari yang larut
dalam etanol dihitung dalam persen terhadap bahan yang telah dikeringkan
(Ditjen POM, 1995). Hasil perhitungan kadar sari larut dalam etanol dapat
dilihat pada Lampiran 6, halaman 53.
3.4.6 Penetapan kadar abu total
Sebanyak 2 g serbuk yang telah digerus dan ditimbang seksama
dimasukkan dalam krus porselin yang telah dipijar dan ditara, kemudian
diratakan. Krus dipijar perlahan - lahan sampai arang habis, pijaran dilakukan
pada suhu 600°C sampai arang habis, kemudian didinginkan dan ditimbang
sampai diperoleh bobot tetap. Kadar abu dihitung terhadap bahan yang telah
dikeringkan (Ditjen POM, 1995). Hasil perhitungan kadar abu total dapat
dilihat pada Lampiran 6, halaman 53.
3.4.7 Penetapan kadar abu tidak larut dalam asam
Abu yang diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml
asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
dikumpulkan, disaring melalui kertas saring bebas abu, cuci dengan air panas,
dipijarkan. Residu dan kertas saring dipijar pada suhu 600°C sampai bobot
tetap kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam
asam dihitung terhadap bahan yang telah dikeringkan (Ditjen POM, 1995).
Lampiran 6, halaman 54.
3.5 Skrining Fitokimia
Skrining fitokimia serbuk simplisia meliputi pemeriksaan senyawa
golongan alkaloid, flavonoid, glikosida, saponin, tanin, dan steroid/
triterpenoid.
3.5.1 Pemeriksaan alkaloid
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml
asam klorida 2 N dan 9 ml air suling, dipanaskan di atas penangas air selama 2
menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk tes
alkaloid. Diambil 3 tabung reaksi, lalu ke dalamnya dimasukkan 0,5 ml filtrat.
Pada masing-masing tabung reaksi:
a. Ditambahkan 2 tetes pereaksi Mayer akan terbentuk endapan menggumpal
berwarna putih atau kuning
b. Ditambahkan 2 tetes pereaksi Bouchardat akan terbentuk endapan
berwarna coklat sampai hitam
c. Ditambahkan 2 tetes pereaksi Dragendorff akan terbentuk endapan
berwarna merah atau jingga
Alkaloid positif jika terjadi endapan atau kekeruhan pada dua atau tiga dari
percobaan diatas (Ditjen POM, 1995).
3.5.2 Pemeriksaan flavonoid
Serbuk simplisia ditimbang 10 g, lalu ditambahkan 10 ml air panas,
didihkan selama 5 menit, disaring dalam keadaan panas. Filtrat yang diperoleh
amil alkohol, dikocok dan dibiarkan memisah. Flavonoid positif jika terjadi
warna merah, kuning, atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.5.3 Pemeriksaan glikosida
Serbuk simplisia ditimbang sebanyak 3 g, lalu disari dengan 30 ml
campuran etanol 95% dengan air (7:3) dan 10 ml asam klorida 2 N, direfluks
selama 2 jam, didinginkan dan disaring. Diambil 20 ml filtrat, ditambahkan 25
ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan selama 5
menit, lalu disaring. Filtrat disari dengan 20 ml campuran isopropanol dan
kloroform (2:3) dilakukan berulang sebanyak 3 kali. Kumpulan sari air
diuapkan pada temperatur tidak lebih dari 50°C. Sisanya dilarutkan dalam 2 ml
metanol. Larutan sisa digunakan untuk percobaan berikut: 0,1 ml larutan
percobaan dimasukkan dalam tabung reaksi dan diuapkan diatas penangas air.
Pada sisa ditambahkan 2 ml air dan 5 tetes pereaksi Molish, kemudian secara
perlahan - lahan ditambahkan 2 ml asam sulfat pekat melalui dinding tabung,
terbentuk cincin berwarna ungu pada batas cairan, menunjukkan adanya
glikosida (Ditjen POM, 1995).
3.5.4 Pemeriksaan saponin
Serbuk simplisia ditimbang sebanyak 0,5 g dan dimasukkan ke dalam
tabung reaksi, lalu ditambahkan 10 ml air panas, didinginkan, kemudian
dikocok kuat - kuat selama 10 detik. Jika terbentuk busa setinggi 1 - 10 cm
yang stabil tidak kurang dari 10 menit dan buih tidak hilang dengan
POM, 1995).
3.5.5 Pemeriksaan tanin
Sebanyak 0,5 g serbuk simplisia disari dengan 10 ml air suling lalu
disaring, filtratnya diencerkan dengan air suling sampai tidak berwarna.
Diambil 2 ml larutan dan ditambahkan 1 - 2 tetes pereaksi besi (III) klorida 1%.
Jika terjadi warna biru kehitaman atau hijau kehitaman menunjukkan adanya
tanin (Harborne, 1987).
3.5.6 Pemeriksaan steroid/triterpenoid
Serbuk simplisia ditimbang sebanyak 1 g, dimaserasi dengan 20 ml n
-heksan selama 2 jam, disaring. Filtrat diuapkan dalam cawan penguap dan pada
sisanya ditambahkan pereaksi Liebermann - Burchard melalui dinding cawan.
Apabila terbentuk warna ungu atau merah yang berubah menjadi biru ungu
atau biru hijau menunjukkan adanya steroid/triterpenoid (Ditjen POM, 1995).
Hasil skrining fitokimia simplisia dan ekstrak etanol umbi sarang semut dapat
dilihat pada Tabel 4.2, halaman 35.
3.6 Pembuatan Ekstrak Etanol Umbi Sarang Semut (EEUSS)
Pembuatan ekstrak dilakukan secara maserasi menggunakan pelarut
etanol 70%. Dimasukkan 10 bagian simplisia ke dalam wadah berwarna gelap,
dituangi dengan 75 bagian cairan penyari, tutup, dibiarkan selama 5 hari
terlindung dari cahaya sambil sering diaduk, diserkai, diperas, dicuci ampas
dengan cairan penyari secukupnya hingga diperoleh 100 bagian. Dipindahkan
ke dalam bejana tertutup, dibiarkan ditempat sejuk, terlindung dari cahaya,
diuapkan menggunakan rotary evaporator pada temperatur ± 40°C, kemudian
difreeze dyrer pada suhu -40°C.
3.7 Uji Efek Antidiare
Pengujian efek antidiare meliputi penyiapan hewan percobaan,
pembutan suspensi CMC 1%, pembuatan suspensi loperamid HCl dari tablet
Imodium®, pembuatan suspensi ekstrak etanol umbi sarang semut, dan
pengujian efek antidiare.
3.7.1 Penyiapan hewan percobaan
Hewan yang digunakan pada penelitian ini adalah tikus putih jantan
galur Wistar dengan berat badan 150 - 200 g. Dua minggu sebelum pengujian
dilakukan hewan percobaan harus dipelihara dan dirawat dengan sebaik
-baiknya dalam kandang yang mempunyai ventilasi baik, tempat minum dan
lingkungan sekitarnya dijaga kebersihannya setiap hari. Tikus diberi makan
pelet dan minum. Hewan yang sehat ditandai dengan pertumbuhan normal dan
suhu badan normal (Depkes, 1979). Kandang atau tempat pemeliharaan tikus
dapat dilihat pada Lampiran 7, halaman 55.
3.7.2 Pembuatan suspensi CMC 1%
Sebanyak 1 g CMC ditaburkan ke dalam lumpang yang berisi air suling
panas sebanyak 20 ml, ditutup dan dibiarkan selama 30 menit hingga diperoleh
massa yang transparan, digerus lalu diencerkan dengan air suling hingga 100
ml (Anief, 1998).
3.7.3 Pembuatan suspensi loperamid HCl dari tablet Imodium®
tablet Imodium® digerus dalam lumpang, kemudian ditambahkan suspensi
CMC 1% sedikit demi sedikit sambil digerus homogen lalu diencerkan dengan
suspensi CMC 1% hingga 10 ml. Perhitungan dosis loperamid HCl dapat
dilihat pada Lampiran 12, halaman 63.
3.7.4 Pembuatan suspensi ekstrak etanol umbi sarang semut
Ekstrak etanol umbi sarang semut dibuat pada satu konsentrasi, yaitu
ditimbang sebanyak 100 mg ekstrak etanol umbi sarang semut, kemudian
digerus dalam lumpang, lalu ditambahkan suspensi CMC 1% sedikit demi
sedikit sambil digerus homogen, lalu diencerkan dengan suspensi CMC 1%
hingga 100 ml. Disetiap melakukan penelitian suspensi ekstrak etanol umbi
sarang semut dibuat baru dengan konsentrasi yang sama. Perhitungan volume
pemberian ekstrak etanol umbi sarang semut dapat dilihat pada Lampiran 11,
halaman 61 - 62.
3.7.5 Pengujian efek antidiare
Hewan percobaan terdiri dari 35 ekor, dibagi dalam 7 kelompok, setiap
kelompok terdiri dari 5 ekor tikus. Semua kelompok diberi perlakuan secara
per oral. Pada t = 0 menit kelompok I (kontrol negatif) diberi suspensi norit 5%
sebanyak 1 ml. Kelompok II diberi oleum ricini sebanyak 2 ml dan suspensi
norit 5% sebanyak 1 ml dan kelompok III, IV, V dan VI diberi suspensi ekstrak
etanol umbi sarang semut 0,1% masing - masing dosis 2,5, 5, 7,5 dan 10 mg/kg
bb. Kelompok VII sebagai pembanding diberikan suspensi loperamid HCl
dosis 0,4 mg/kg bb. Ekstrak etanol umbi sarang semut dan suspensi loperamid
hewan diberi oleum ricini sebanyak 2 ml. Pada t = 120 menit semua hewan
diberikan suspensi norit 5% sebanyak 1 ml kemudian pada saat t = 180 menit
semua hewan dikorbankan secara dislokasi leher. Usus dikeluarkan secara hati
- hati. Diukur panjang usus yang dilalui marker norit mulai dari pilorus sampai
ujung akhir (berwarna hitam) dan panjang seluruh usus dari pilorus sampai
katup ileosekal dari masing - masing hewan. Kemudian dari masing - masing
tikus dihitung persen lintas yang dilalui oleh marker norit terhadap panjang
usus seluruhnya (Chitme, dkk., 2004). Gambar tikus sebelum dan setelah
dibedah dapat dilihat pada Lampiran 8, halaman 56, dan Gambar usus halus
yang dilintasi marker norit dapat dilihat pada Lampiran 9, halaman 57 - 59.
3.8 Pengumpulan Data
Nilai rasio kemudian dirata - rata untuk masing - masing kelompok, dan
nilai dari masing - masing kelompok tersebut dibandingkan.
3.9 Analisis Data
Data hasil pengamatan persen lintas marker norit dianalisis secara
statistik dengan metode ANAVA (analisis variansi) pada tingkat kepercayaan
95% dilanjutkan dengan uji Duncan untuk melihat perbedaan nyata antar
kelompok perlakuan. Analisis statistik ini menggunakan program SPSS
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan dilakukan di Lembaga Ilmu Pengetahuan
Indonesia, Bidang Botani Pusat Penelitian Biologi - LIPI Bogor menunjukkan
bahwa sampel adalah tumbuhan sarang semut jenis Myrmecodia tuberosa Jack.
sinonimnya Myrmecodia armata DC, suku Rubiaceae.
4.2 Hasil Karakteristik Simplisia
Hasil karakteristik simplisia umbi sarang semut secara makroskopik
berupa potongan - potongan yang berlubang atau berongga, berwarna coklat
kehitaman, berbau menyengat, berasa pahit dan agak sepat. Hasil pemeriksaan
mikroskopik serbuk simplisia umbi sarang semut terlihat adanya parenkim,
butir pati dan pembuluh kayu.
Menurut Ditjen POM (2000), standarisasi suatu simplisia merupakan
pemenuhan terhadap persyaratan sebagai bahan obat dan penetapan nilai untuk
berbagai parameter produk. Simplisia yang akan digunakan sebagai bahan obat
harus memenuhi persyaratan yang tercantum dalam monografi terbitan resmi
Departemen Kesehatan (Materia Medika Indonesia). Hasil karakteristik
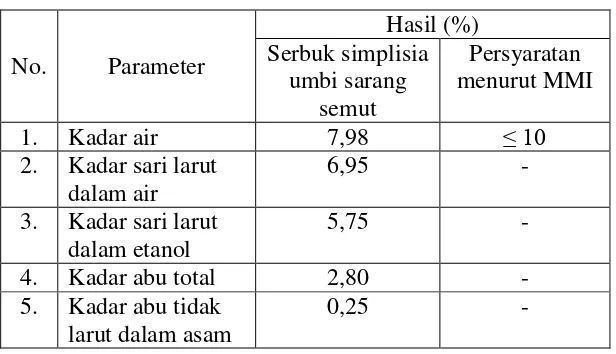
Tabel 4.1 Hasil karakteristik simplisia umbi sarang semut
Berdasarkan Tabel 4.1 ditunjukkan bahwa kadar air simplisia umbi
sarang semut diperoleh 7,98%, berarti simplisia sudah memenuhi persyaratan
(≤ 10%). Penetapan kadar air dilakukan berhubungan dengan mutu simplisia
agar tidak mudah ditumbuhi mikroorganisme. Hasil penetapan kadar sari larut
air simplisia umbi sarang semut adalah 6,95%, sedangkan hasil penetapan
kadar sari larut etanol adalah 5,75%. Penetapan kadar sari menyatakan jumlah
zat yang tersari dalam air atau dalam etanol (Ditjen POM, 1995).
Hasil penetapan kadar abu total simplisia umbi sarang semut adalah
2,80%, sedangkan hasil penetapan kadar abu tidak larut asam adalah 0,25%.
Penetapan kadar abu total dilakukan untuk mengetahui kandungan mineral dan
senyawa anorganik dalam simplisia misalnya logam K, Ca, Na, Pb. Sedang
penetapan kadar abu tidak larut asam dilakukan untuk mengetahui kadar
senyawa yang tidak larut dalam asam misalnya silikat. Persyaratan untuk
penetapan kadar sari larut air, kadar sari larut etanol, kadar abu total, kadar abu
terbitan resmi Departemen Kesehatan (Materia Medika Indonesia).
4.3 Hasil Skrining Fitokimia
Skrining fitokimia bertujuan untuk mengetahui golongan senyawa
kimia yang terkandung dalam simplisia maupun ekstrak. Hasil pemeriksaan
skrining fitokimia baik terhadap simplisia maupun ekstrak etanol umbi sarang
semut menunjukkan bahwa keduanya mengandung senyawa kimia golongan
flavonoid, glikosida, saponin, tanin, steroid/triterpenoid. Beberapa hasil
penelitian melaporkan bahwa kandungan senyawa aktif golongan tanin,
flavonoid, saponin, steroid/triterpenoid bertanggung jawab atas khasiat
antidiare dari beberapa tanaman obat (Longanga, dkk., 2000). Hasil skrining
fitokimia dapat dilihat pada Tabel 4.2.
Tabel 4.2 Hasil skrining fitokimia simplisia dan ekstrak etanol umbi sarang semut
No. Pemeriksaan Serbuk simplisia umbi sarang semut
(+) positif: mengandung golongan senyawa (-) negatif: tidak mengandung golongan senyawa
4.4 Pengujian Efek Antidiare
Pada penelitian ini, pengujian efek antidiare ekstrak umbi sarang semut
norit sebagai marker. Metode intestinal transit/metode lintasan usus halus ini
bertujuan untuk mengevaluasi aktivitas obat antidiare, laksansia, ataupun
antispasmodik, berdasarkan pengaruhnya pada rasio jarak usus yang ditempuh
oleh suatu norit dalam jangka waktu tertentu terhadap panjang usus
keseluruhan pada hewan percobaan. Dengan ketentuan persen rasio sebagai
antidiare adalah lebih kecil sedangkan laksansia atau antispasmodik nilainya
lebih besar dibandingkan dengan kelompok pemberian norit (KKIPM, 1993).
Oleum ricini digunakan dalam menginduksi diare. Trigliserida dari
asam risinoleat yang terdapat dalam oleum ricini akan mengalami hidrolisis
dalam usus halus oleh lipase pankreas menjadi gliserida dan asam risinoleat
(Katzung, 2007). Asam risinoleat yang merupakan metabolit aktif dari oleum
ricini memiliki kemampuan dalam menginduksi terjadinya diare dengan cara
menstimulasi aktivitas peristaltik dimukosa intestinal (Anas, dkk., 2000).
Loperamid HCl sebagai pembanding merupakan obat opoid yang paling
tepat untuk efek lokal pada usus karena tidak mudah menembus ke dalam otak.
Oleh karena itu, loperamid HCl hanya mempunyai sedikit efek sentral dan
tidak mungkin menyebabkan ketergantungan (Neal, 2006).
Penentuan dosis ekstrak etanol umbi sarang semut pada penelitian
didasarkan pada orientasi. Hasil orientasi yang dilakukan pada dosis 2,5, 5, 7,5,
10 mg/kg bb ternyata semua dosis memberikan peningkatan efek antidiare
seperti pada terlihat pada Lampiran 13, halaman 64 - 65. Oleh karena itu dosis
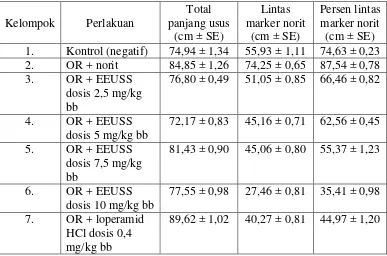
Tabel 4.3 Efek ekstrak etanol umbi sarang semut pada tikus yang diinduksi
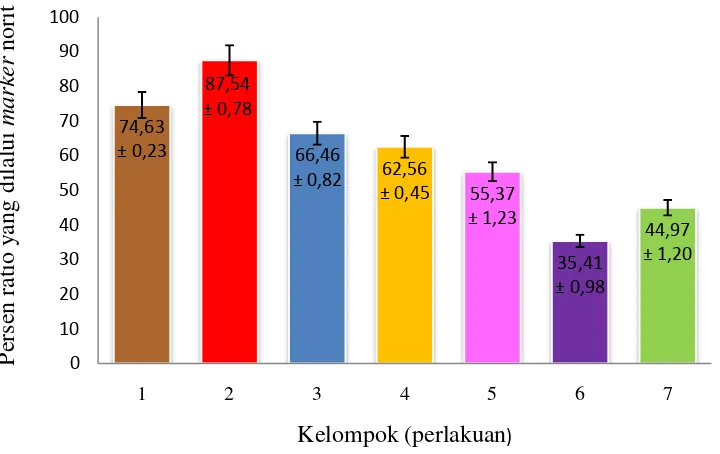
Gambar 4.1 Grafik hubungan antara dosis dan persen rata - rata lintasan norit Keterangan gambar: OR: oleum ricini, EEUSS: ekstrak etanol umbi sarang
semut. 1. Kontrol (norit), 2. OR + norit, 3. OR + EEUSS dosis 2,5 mg/kg bb, 4. OR + EEUSS + dosis 5 mg/kg bb, 5. OR + EEUSS 7,5 mg/kg bb, 6. OR + EEUSS 10 mg/kg bb, 7. Loperamid HCl dosis 0,4 mg/kg bb.
Pada Tabel 4.3 dan Gambar 4.1 terlihat pada pemberian norit diperoleh
persen lintas marker norit 74,63 ± 0,23 yang menggambarkan usus tanpa
diinduksi oleum ricini sedangkan pemberian oleum ricini dan norit terjadi
peningkatan persen lintas marker norit yaitu 87,54 ± 0,78 namun setelah
pemberian EEUSS dengan dosis yang bervariasi terlihat adanya penurunan
persen lintas marker norit yaitu dosis 2,5 mg/kg bb (66,46 ± 0,82), 5 mg/kg bb
(62,56 ± 0,45), 7,5 mg/kg bb (55,37 ± 1,23), 10 mg/kg bb (35,41 ± 0,98). Dosis
EEUSS 10 mg/kg bb (35,41 ± 0,98) memiliki persen lintas marker norit
tertinggi dibandingkan dengan EEUSS dosis 2,5 mg/kg bb (66,46 ± 0,82), 5
mg/kg bb memiliki efek antidiare yang lebih baik dibandingkan dengan dosis
2,5, 5 dan 7,5 mg/kg bb.
Pada pemberian loperamid HCl dengan dosis 0,4 mg/kg bb terjadi
penurunan persen lintas marker norit yang berarti yaitu 44,97 ± 1,20. Ini
menunjukkan bahwa pada loperamid HCl dosis 0,4 mg/kg bb lebih baik
menghambat gerakan peristaltik usus yang diinduksi oleum ricini dibandingkan
dengan EEUSS dosis 2,5, 5, 7,5 mg/kg bb tetapi jika dibandingkan dengan
EEUSS dosis 10 mg/kg bb lebih baik daripada loperamid HCl dosis 0,4 mg/kg
bb.
Uji analisis variansi (ANAVA) dilakukan untuk melihat ada tidaknya
perbedaan dari setiap perlakuan pada tiap kelompok hewan percobaan, dengan
menggunakan program SPSS versi 17 terhadap persen lintas marker norit
dimana hasil analisis variansi dapat dilihat pada Lampiran 14, halaman 66 - 67.
Hasil analisis variansi diperoleh harga F hitung (270,462) ˃ F tabel (F tabel
2,44) dapat dilihat pada Lampiran 16, halaman 69. Hal ini menunjukkan
adanya perbedaan yang signifikan antar kelompok perlakuan terhadap persen
ratio lintas marker norit dengan nilai signifikansi p ˂ 0,05, d an untuk
mengetahui kelompok perlakuan mana yang memiliki efek yang sama atau
berbeda antara satu perlakuan dengan perlakuan yang lain dilakukan uji
Duncan untuk semua perlakuan, hasil uji tersebut dapat dilihat pada Lampiran
15, halaman 68.
Hasil uji Duncan menunjukkan bahwa ada perbedaan yang signifikan
2,5, 5, 7,5, dan 10 mg/kg bb dengan loperamid 0,4 mg/kg bb. Keempat dosis
EEUSS juga memperlihatkan adanya perbedaan yang signifikan antara persen
lintas marker norit dengan kelompok yang diberikan oleum ricini dan
kelompok kontrol (norit). Dari hasil penelitian ini terlihat bahwa EEUSS
mempunyai efek antidiare. Dari keempat dosis EEUSS menunjukkan adanya
hubungan antara dosis dan efek. Semakin besar dosis yang diberikan makin
besar efek antidiarenya.
Efek antidiare ini terkait dengan adanya senyawa tanin dan flavonoid
yang terkandung dalam ekstrak etanol umbi sarang semut. Tanin dapat
mengurangi intensitas diare dengan cara menciutkan selaput lendir usus dan
mengecilkan pori sehingga akan menghambat sekresi cairan dan elektrolit (Tan
dan Rahardja, 2007). Selain itu, sifat adstringens tanin akan membuat usus
halus lebih tahan (resisten) terhadap rangsangan senyawa kimia yang
mengakibatkan diare, toksin bakteri dan induksi diare oleh oleum ricini
(Kumar, 1983).
Beberapa penelitian juga telah melaporkan mengenai flavonoid sebagai
antidiare. Mekanisme flavonoid dalam menghentikan diare yang diinduksi
oleum ricini adalah dengan menghambat motilitas usus sehingga mengurangi