TESIS
UJI AKTIVITAS ANTIKANKER PAYUDARA
KOMBINASI EKSTRAK n-HEKSANA DAN ETILASETAT
BUAH ANDALIMAN (Zanthoxylum acanthopodium DC.) DENGAN
DOKSORUBISIN TERHADAP SEL KANKER T47D
SECARA IN VITRO
Oleh:
RATIH ANGGRAENI
NIM 127014005
PROGRAM STUDI MAGISTER FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI AKTIVITAS ANTIKANKER PAYUDARA
KOMBINASI EKSTRAK n-HEKSANA DAN ETILASETAT
BUAH ANDALIMAN (Zanthoxylum acanthopodium DC.) DENGAN
DOKSORUBISIN TERHADAP SEL KANKER T47D
SECARA IN VITRO
TESIS
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh:
RATIH ANGGRAENI
NIM 127014005
PROGRAM STUDI MAGISTER FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
LEMBAR PENGESAHAN TESIS
UJI AKTIVITAS ANTIKANKER PAYUDARA
KOMBINASI EKSTRAK n-HEKSANA DAN ETILASETAT BUAH ANDALIMAN (Zanthoxylum acanthopodium DC.) DENGAN DOKSORUBISIN
TERHADAP SEL KANKER T47D SECARA IN VITRO
Oleh:
RATIH ANGGRAENI NIM 127014005
Medan, Oktober 2014 Menyetujui:
Komisi Pembimbing, Komisi Penguji,
Prof. Dr. Sumadio Hadisahputra, Apt. Prof. Dr. Urip Harahap, Apt.
NIP 195311281983031002 NIP 195301011983031004
Prof. Dr. Jansen Silalahi, M.App.Sc., Apt. Prof. Dr. Rosidah, M.Si., Apt.
NIP 195006071979031001 NIP 195103261978022001
Prof. Dr. Sumadio Hadisahputra, Apt. NIP 195311281983031002
Prof. Dr. Jansen Silalahi, M.App.Sc., Apt. NIP 195006071979031001
Mengetahui: Disahkan Oleh:
Ketua Program Studi, Dekan,
Prof. Dr. Karsono, Apt. Prof. Dr. Sumadio Hadisahputra, Apt.
PENGESAHAN TESIS
Nama Mahasiswa : Ratih Anggraeni Nomor Induk Mahasiswa : 127014005
Program Studi : Magister Farmasi
Judul Tesis : Uji Aktivitas Antikanker Payudara Kombinasi Ekstrak n-Heksana dan Etilasetat Buah Andaliman (Zanthoxylum acanthopodium DC.) dengan Doksorubisin terhadap Sel Kanker T47D secara InVitro
Telah diuji dan dinyatakan LULUS di depan Tim Penguji pada hari Selasa tanggal
dua puluh satu bulan Oktober tahun dua ribu empat belas.
Mengesahkan:
Tim Penguji Tesis
Ketua Tim Penguji Tesis : Prof. Dr. Sumadio Hadisahputra, Apt.
Anggota Tim Penguji Tesis : Prof. Dr. Jansen Silalahi, M.App.Sc., Apt.
Prof. Dr. Urip Harahap, Apt.
Prof. Dr. Rosidah, M.Si., Apt.
SURAT PERNYATAAN
Saya yang bertanda tangan di bawah ini:
Nama Mahasiswa : Ratih Anggraeni
Nomor Induk Mahasiswa : 127014005
Program Studi : Magister Farmasi
Judul Tesis : Uji Aktivitas Antikanker Payudara Kombinasi Ekstrak
n-Heksana dan Etilasetat Buah Andaliman
(Zanthoxylum acanthopodium DC.) dengan
Doksorubisin terhadap Sel Kanker T47D secara In
Vitro
Dengan ini menyatakan bahwa tesis yang saya buat adalah hasil karya saya sendiri,
bukan plagiat, dan apabila dikemudian hari diketahui tesis saya tersebut plagiat
karena kesalahan saya sendiri, maka saya bersedia diberi sanksi apapun oleh
Program Studi Magister Farmasi Fakultas Farmasi USU. Saya tidak akan menuntut
pihak manapun atas perbuatan saya tersebut.
Demikianlah surat pernyataan ini saya perbuat dengan sebenarnya dalam keadaan
sehat.
Medan, Oktober 2014 Yang membuat pernyataan,
Ratih Anggraeni
KATA PENGANTAR
Puji dan syukur kehadirat Allah swt. yang telah memberikan nikmat dan
karunia yang berlimpah sehingga penulis dapat menyelesaikan perkuliahan dan
penelitian hingga tersusunnya tesis yang berjudul Uji Aktivitas Antikanker Payudara
Kombinasi Ekstrak n-Heksana dan Etilasetat Buah Andaliman (Zanthoxylum
acanthopodium DC.) dengan Doksorubisin terhadap Sel Kanker T47D secara In
Vitro. Tesis ini diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar
Magister Farmasi di Fakultas Farmasi Universitas Sumatera Utara. Pada kesempatan
ini, dengan segala kerendahan hati penulis mengucapkan terima kasih kepada:
1. Prof. Dr. dr. Syahril Pasaribu, DTMH&H., M.Sc., (CTM)., Sp.A(K)., selaku
Rektor Universitas Sumatera Utara.
2. Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara.
3. Prof. Dr. Karsono, Apt., selaku Ketua Program Studi Magister Farmasi Fakultas
Farmasi Universitas Sumatera Utara.
4. Prof. Dr. Sumadio Hadisahputra, Apt., dan Prof. Jansen Silalahi, M.App.Sc.,
Apt., selaku pembimbing yang telah membimbing dan memberikan petunjuk
serta arahan selama penelitian hingga penulis dapat menyelesaikan tesis ini.
5. Prof. Dr. Urip Harahap, Apt., dan Prof. Dr. Rosidah, M.Si., Apt., selaku penguji
yang telah memberikan saran untuk menyempurnakan tesis ini.
6. Dra. Suwarti, M.Si., Apt., selaku Kepala Laboratorium Farmakognosi beserta
7. Prof. dr. Supargiyono, DTM&H., SU., Ph.D., SpParK., selaku Direktur Pusat
Kedokteran Tropis Fakultas Kedokteran Universitas Gadjah Mada beserta staf.
Penulis juga mengucapkan terima kasih dan penghargaan yang
setinggi-tingginya kepada Ayahanda (alm.) Suroso dan Ibunda Agusrina, serta kakak dan
abang ipar, dan teristimewa kepada M. Taufik Alfyan yang tiada henti mendoakan
dan memberikan semangat dan kasih sayang yang tak ternilai dengan apapun.
Penulis mengucapkan terima kasih kepada Cut Masyithah, Denny Satria, Fitri Yanti,
Puji Lestari, Vonna Aulianshah, Mainal Furqan, dan semua pihak yang tidak dapat
disebutkan satu per satu yang telah banyak membantu hingga selesainya tesis ini.
Semoga Allah swt. membalas dengan balasan yang berlipat ganda atas kebaikan dan
bantuan yang telah diberikan kepada penulis.
Penulis menyadari bahwa tesis ini masih jauh dari kesempurnaan. Oleh
karena itu, dengan segala kerendahan hati penulis mengharapkan kritik dan saran
yang bersifat membangun demi kesempurnaan tesis ini. Akhir kata penulis berharap
semoga tesis ini dapat menjadi kontribusi yang bermanfaat bagi ilmu pengetahuan
khususnya di bidang farmasi.
Medan, Oktober 2014 Penulis,
UJI AKTIVITAS ANTIKANKER PAYUDARA
KOMBINASI EKSTRAK n-HEKSANA DAN ETILASETAT BUAH ANDALIMAN (Zanthoxylum acanthopodium DC.) DENGAN DOKSORUBISIN TERHADAP SEL KANKER T47D SECARA IN VITRO
Abstrak
Kanker payudara merupakan salah satu jenis kanker yang menjadi penyebab kematian terbesar di Indonesia pada wanita. Penggunaan agen kemoterapi doksorubisin merupakan salah satu pengobatan kanker payudara. Doksorubisin dapat menyebabkan resistensi
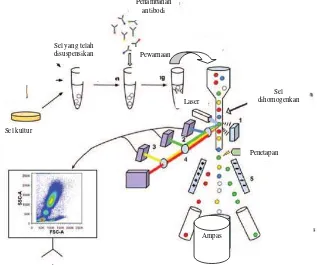
Buah andaliman yang digunakan diperoleh dari Kecamatan Onan Runggu, Kabupaten Samosir, Sumatera Utara. Lalu buah andaliman dibuat menjadi ekstrak melalui maserasi bertingkat menggunakan pelarut n-heksana, etilasetat, dan etanol. Pengujian sitotoksik ENBA dan EEABA secara in vitro (nilai IC50) terhadap sel T47D dan sel Vero menggunakan metode MTT yang kemudian dianalisis menggunakan SPSS 19 lalu dihitung indeks selektivitasnya. Selanjutnya ENBA dan EEABA dikombinasikan dengan doksorubisin. Kombinasi yang paling aktif dilanjutkan untuk uji penghambatan siklus sel dan apoptosis dengan metode flow cytometry serta efek penekanan ekspresi protein Bcl-2 dan cox-2 dengan metode imunositokimia terhadap sel T47D.
sehingga potensi sitotoksik akan berkurang. Terapi kombinasi dengan obat herbal dapat meningkatkan sensitivitas sel kanker payudara dan meminimalkan efek samping doksorubisin. Penelitian sebelumnya telah melakukan uji tentang efek sitotoksik ekstrak etilasetat buah andaliman terhadap sel MCF-7. Tujuan penelitian ini untuk mengetahui aktivitas antikanker yang dikandung ekstrak n-heksana (ENBA) dan ekstrak etilasetat (EEABA) buah andaliman serta kombinasi ENBA dan EEABA dengan doksorubisin terhadap sel T47D.
Hasil penelitian menunjukkan bahwa nilai IC50 ENBA dan EEABA sebesar 30,908 µg/mL dan 24,476 µg/mL. Pengujian dengan sel Vero menunjukkan ENBA dan EEABA selektif terhadap sel T47D. Kombinasi optimum ENBA-doksorubisin dan EEABA-doksorubisin sebesar 20 µg/mL – 25 nM (½ IC50 – 1/16 IC50) dan 7,5 µg/mL – 25 nM (2/8 IC50 – 1/16 IC50). Kombinasi ENBA dan EEABA dengan doksorubisin memiliki aktivitas antikanker terhadap sel T47D melalui penghambatan siklus sel pada fase G0-G1, yaitu sebesar 84,37% dan 80,83% dan apoptosis pada tahap apoptosis akhir dan nekrosis awal sebesar 69,51% dan 62,94% dikarenakan terjadi penghambatan ekspresi protein Bcl-2 dan cox-2.
ANTICANCER ACTIVITIES OF
n-HEXANE EXTRACT AND ETHYLACETATE EXTRACT OF ANDALIMAN FRUIT (Zanthoxylum acanthopodium DC.)
IN COMBINATION WITH DOXORUBICIN ON T47D CANCER CELLS IN VITRO
Abstract
Breast cancer is one of cancer variety of the Indonesia's leading cause of death in women. The use of chemotherapeutic agent doxorubicin is one of the breast cancer treatment. Doxorubicin can cause resistance so that the cytotoxic potency will be reduced. Combination therapy with herbal medicines can increase the sensitivity of breast cancer cells and minimize the side effects of doxorubicin. Previous research has tested ethylacetate extract of andaliman fruit’s cytotoxic effect on MCF-7 cells. The purpose of this study to was to determine the anticancer activity of n-hexane extract (ENBA) and ethylacetate extract (EEABA) of andaliman fruit and their combination with doxorubicin on T47D cells.
This study used andaliman fruit from Kecamatan Onan Runggu, Kabupaten Samosir, Sumatera Utara. Extract was made by multilevel maceration with n-hexane, ethylacetate, and ethanol. Cytotoxic effect of EEABA and ENBA was tested in vitro (IC50 values) on the T47D cells and Vero cells used MTT using SPSS 19 and calculated selectivity index. Then ENBA and EEABA were combined with doxorubicin. The most active combination was eventually tested on the inhibition of cell cycle and apoptosis by flowcytometry method and suppressive effects of Bcl-2 and cox-2 protein expression by immunocytochemistry method on T47D cells.
The result of this study showed that IC50 values ENBA and EEABA at 30.908 µg/mL and 24.476 µg/mL. Selectivity test on Vero cells showed that ENBA and EEABA were selective to ward T47D cells. Optimal combination of ENBA-doxorubicin was 20 µg/mL - 25 nM (½ IC50 – 1/16 IC50) and combination of EEABA-doxorubicin was 7.5 µg/mL - 25 nM (2/8 IC50 – 1/16 IC50). Combination of ENBA and EEABA with doxorubicin had anticancer activity to ward T47D cells due to inhibition of cell cycle at G0-G1 phase, amounting to 84.37% and 80.83% and apoptosis in the late stage of apoptosis and early necrosis of 69.51% and 62.94% caused by inhibition of Bcl-2 and cox-2 protein expression.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN TESIS ... iii
PENGESAHAN TESIS ... iv
SURAT PERNYATAAN ... v
KATA PENGANTAR ... vi
ABSTRAK ... viii
ABSTRACT ... ix
DAFTAR ISI ... x
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ... xviii
BAB I PENDAHULUAN ... ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 5
1.3 Hipotesis ... 5
1.4 Tujuan Penelitian ... 6
1.5 Manfaat Penelitian ... 6
1.6 Kerangka Pikir Penelitian ... 7
BAB II TINJAUAN PUSTAKA ... 8
2.1 Siklus Sel ... 8
2.2 Kanker ... 12
2.2.1 Karsinogenesis ... 15
2.2.2 Kanker payudara ... 17
2.2.2.1 Sel T47D ... 20
2.2.3 Sel Vero ... 21
2.2.4 P-glycoprotein ... 21
2.3 Penanganan Kanker ... 24
2.3.1 Penanganan kanker payudara ... 25
2.3.1.1 Doksorubisin ... 26
2.3.1.2 Terapi kombinasi ... 28
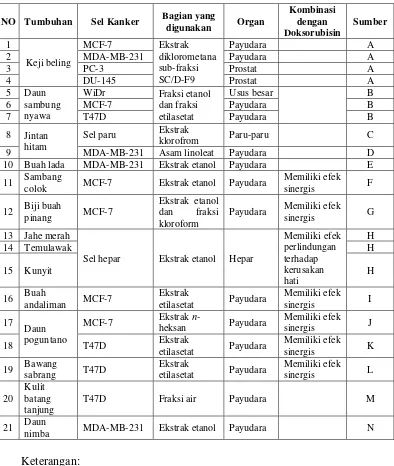
2.4 Tanaman yang Bersifat Antikanker ... 29
2.4.1 Andaliman ... 29
2.4.2 Pengujian sifat antikanker dari berbagai tanaman obat ... 32
2.4.2.1 Metode pemisahan ekstraksi ... 33
2.4.2.2 Metode pengujian aktivitas antikanker ... 34
BAB III METODE PENELITIAN ... 40
3.1 Alat ... 40
3.2 Bahan ... 41
3.3 Penyiapan Bahan Uji ... 42
3.4 Pembuatan Pereaksi ... 43
3.5 Pemeriksaan Karateristik Simplisia dan Ekstrak ... 44
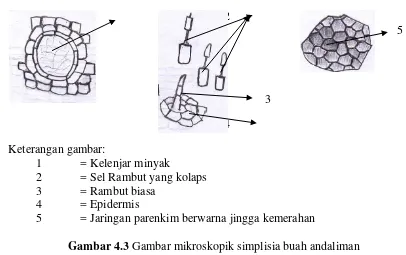
3.5.1 Pemeriksaan makroskopik dan mikroskopik ... 44
3.5.2 Penetapan kadar air ... 44
3.5.4 Penetapan kadar sari yang larut dalam etanol ... 46
3.5.5 Penetapan kadar abu total ... 46
3.5.6 Penetapan kadar abu yang tidak larut dalam asam ... 47
3.6 Skrining Fitokimia Simplisia dan Ekstrak ... 47
3.6.1 Pemeriksaan alkaloid ... 47
3.6.2 Pemeriksaan flavonoid ... 48
3.6.3 Pemeriksaan glikosida ... 48
3.6.4 Pemeriksaan saponin ... 49
3.6.5 Pemeriksaan tanin ... 49
3.6.6 Pemeriksaan steroid/triterpenoid ... 49
3.6.7 Pemeriksaan antrakuinon ... 49
3.7 Sterilisasi Alat dan Bahan ... 50
3.8 Pembuatan Media ... 50
3.8.1 Pembuatan media Roswell Park Memorial Institute (RPMI) ... 50
3.8.2 Pembuatan media kultur lengkap (MK-RPMI) ... 50
3.8.3 Pembuatan media M199 ... 51
3.8.4 Pembuatan media MK-M199 ... 52
3.9 Penumbuhan Sel ... 52
3.9.1 Penumbuhan sel kanker payudara (T47D) ... 52
3.9.2 Subkultur sel kanker payudara (T47D) ... 52
3.9.3 Panen sel kanker payudara (T47D) ... 53
3.9.4 Penumbuhan sel Vero ... 53
3.9.5 Subkultur sel Vero ... 54
3.9.7 Penghitungan sel T47D dan sel Vero ... 54
3.10 Pembuatan Larutan Uji ... 55
3.11 Pengujian Sitotoksik ... 56
3.11.1 Pengujian sitotoksik terhadap sel Vero ... 56
3.11.2 Pengujian sitotoksik terhadap sel T47D ... 57
3.11.3 Analisis Hasil ... 57
3.11.4 Indeks Selektivitas ... 58
3.12 Uji Kombinasi Ekstrak Buah Andaliman dengan Doksorubisin terhadap Sel T47D ... 58
3.13 Pengujian Kombinasi Ekstrak Buah Andaliman dengan Doksorubisin terhadap Apoptosis dan Siklus Sel Sel T47D ... ... 60
3.14 Pengujian Kombinasi Ekstrak Buah Andaliman dengan Doksorubisin dalam Penghambatan Ekspresi Protein Bcl-2 dan Cox-2 terhadap Sel T47D ... 61
BAB IV HASIL DAN PEMBAHASAN ... 63
4.1 Identifikasi Tumbuhan ... 63
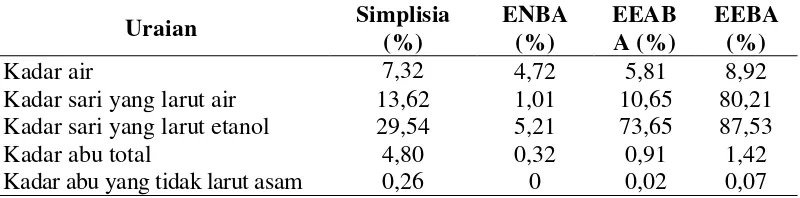
4.2 Karakteristik Simplisia dan Ekstrak ... 63
4.3 Hasil Skrining Fitokimia Simplisia dan Ekstrak ... 67
4.4 Efek Sitotoksik ENBA dan EEABA terhadap Sel Vero dan Sel T47D ... 69
4.4.1 Efek sitotoksik terhadap sel Vero ... 69
4.4.2 Efek sitotoksik terhadap sel T47D ... 69
4.4.3 Pengaruh Selektivitas ENBA dan EEABA terhadap Sel Vero dan Sel T47D ... 70
4.5 Hasil Pengujian Kombinasi ENBA dan EEABA dengan Doksorubisin terhadap Sel T47D ... 71
4.7 Pengaruh Kombinasi ENBA dan EEABA dengan
Doksorubisin terhadap Siklus Sel T47D ... 78
4.8 Pengaruh Kombinasi ENBA dan EEABA dengan Doksorubisin dalam Penghambatan Ekspresi Protein Bcl-2 dan Cox-2 terhadap Sel T47D ... 81
BAB V KESIMPULAN DAN SARAN ... 87
5.1 Kesimpulan ... 87
5.2 Saran ... 88
DAFTAR PUSTAKA ... 89
DAFTAR TABEL
Halaman
Tabel 2.1 Beberapa tumbuhan yang berpotensi sebagai antikanker ... 30
Tabel 2.2 Interpretasi nilai CI (Combination Index) ... 36
Tabel 4.1 Hasil karakteristik simplisia dan ekstrak buah andaliman .... 66
Tabel 4.2 Hasil skrining fitokimia simplisia dan ekstrak buah
andaliman ... 68
Tabel 4.3 Nilai indeks selektivitas (IS) ENBA dan EEABA ... 71
Tabel 4.4 Nilai indeks kombinasi ENBA-doksorubisin dan
EEABA-doksorubisin ... 72
Tabel 4.5 Pengaruh tunggal ENBA, tunggal EEABA, tunggal doksorubisin, kombinasi ENBA-doksorubisin dan
EEABA-doksorubisin terhadap apoptosis sel T47D ... 76
Tabel 4.6 Pengaruh kombinasi ENBA-doksorubisin dan
EEABA-doksorubisin terhadap siklus sel T47D ... 79
Tabel 4.7 Hasil pengujian penghambatan ekspresi protein Bcl-2 ... 81
DAFTAR GAMBAR
Halaman
Gambar 1.1 Diagram kerangka pikir penelitian ... 7
Gambar 2.1 Mekanisme pemompaan oleh Pgp ... 23
Gambar 2.2 Struktur kimia doksorubisin ... 27
Gambar 2.3 Reduksi MTT menjadi formazan ... 35
Gambar 2.4 Skema alat flow cytometer ... 37
Gambar 3.1 Hemositometer ... 55
Gambar 4.1 Buah andaliman segar ... 63
Gambar 4.2 Simplisia buah andaliman ... 64
Gambar 4.3 Gambar mikroskopik simplisia buah andaliman ... 65
Gambar 4.4 Korelasi antara konsentrasi larutan uji dengan efek toksik yang ditimbulkan terhadap sel T47D ... 69
Gambar 4.5 Apoptosis sel T47D kontrol ... 74
Gambar 4.6 Apoptosis sel T47D tunggal ENBA ... 74
Gambar 4.7 Apoptosis sel T47D tunggal EEABA ... 74
Gambar 4.8 Apoptosis sel T47D tunggal doksorubisin ... 75
Gambar 4.9 Apoptosis sel T47D kombinasi ENBA-doksorubisin ... 75
Gambar 4.10 Apoptosis sel T47D kombinasi EEABA-doksorubisin ... 75
Gambar 4.11 Persentase jumlah sel yang diberi perlakuan tunggal ENBA, tunggal EEABA, tunggal doksorubisin, kombinasi ENBA-doksorubisin dan EEABA-doksorubisin terhadap apoptosis sel T47D ... 76
Gambar 4.12 Siklus sel T47D kontrol ... 78
Gambar 4.14 Siklus sel T47D kombinasi EEABA-doksorubisin ... 79
Gambar 4.15 Ekspresi protein Bcl-2 dengan berbagai perlakuan ... 82
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Surat hasil identifikasi tumbuhan andaliman
(Zanthoxylum acanthopodium DC.) ... 101
Lampiran 2. Perhitungan karakterisasi simplisia, ekstrak n-heksana (ENBA), ekstrak etilasetat (EEABA), dan ekstrak
etanol (EEBA) buah andaliman ... 102
Lampiran 3. Perhitungan persen sel hidup sel T47D ... 105
Lampiran 4. Gambar alat ... 106
Lampiran 5. Hasil penentuan IC50 ENBA pada sel Vero dengan
analisa probit SPSS 19 ... 107
Lampiran 6. Hasil penentuan IC50 EEABA pada sel Vero dengan
analisa probit SPSS 19 ... 108
Lampiran 7. Hasil penentuan IC50 ENBA pada sel T47D dengan
analisa probit SPSS 19 ... 109
Lampiran 8. Hasil penentuan IC50 EEABA pada sel T47D dengan
analisa probit SPSS 19 ... 110
Lampiran 9. Indeks Kombinasi (IK) ENBA-doksorubisin pada
sel T47D ... 111
Lampiran 10. Indeks Kombinasi (IK) EEABA-doksorubisin pada
UJI AKTIVITAS ANTIKANKER PAYUDARA
KOMBINASI EKSTRAK n-HEKSANA DAN ETILASETAT BUAH ANDALIMAN (Zanthoxylum acanthopodium DC.) DENGAN DOKSORUBISIN TERHADAP SEL KANKER T47D SECARA IN VITRO
Abstrak
Kanker payudara merupakan salah satu jenis kanker yang menjadi penyebab kematian terbesar di Indonesia pada wanita. Penggunaan agen kemoterapi doksorubisin merupakan salah satu pengobatan kanker payudara. Doksorubisin dapat menyebabkan resistensi
Buah andaliman yang digunakan diperoleh dari Kecamatan Onan Runggu, Kabupaten Samosir, Sumatera Utara. Lalu buah andaliman dibuat menjadi ekstrak melalui maserasi bertingkat menggunakan pelarut n-heksana, etilasetat, dan etanol. Pengujian sitotoksik ENBA dan EEABA secara in vitro (nilai IC50) terhadap sel T47D dan sel Vero menggunakan metode MTT yang kemudian dianalisis menggunakan SPSS 19 lalu dihitung indeks selektivitasnya. Selanjutnya ENBA dan EEABA dikombinasikan dengan doksorubisin. Kombinasi yang paling aktif dilanjutkan untuk uji penghambatan siklus sel dan apoptosis dengan metode flow cytometry serta efek penekanan ekspresi protein Bcl-2 dan cox-2 dengan metode imunositokimia terhadap sel T47D.
sehingga potensi sitotoksik akan berkurang. Terapi kombinasi dengan obat herbal dapat meningkatkan sensitivitas sel kanker payudara dan meminimalkan efek samping doksorubisin. Penelitian sebelumnya telah melakukan uji tentang efek sitotoksik ekstrak etilasetat buah andaliman terhadap sel MCF-7. Tujuan penelitian ini untuk mengetahui aktivitas antikanker yang dikandung ekstrak n-heksana (ENBA) dan ekstrak etilasetat (EEABA) buah andaliman serta kombinasi ENBA dan EEABA dengan doksorubisin terhadap sel T47D.
Hasil penelitian menunjukkan bahwa nilai IC50 ENBA dan EEABA sebesar 30,908 µg/mL dan 24,476 µg/mL. Pengujian dengan sel Vero menunjukkan ENBA dan EEABA selektif terhadap sel T47D. Kombinasi optimum ENBA-doksorubisin dan EEABA-doksorubisin sebesar 20 µg/mL – 25 nM (½ IC50 – 1/16 IC50) dan 7,5 µg/mL – 25 nM (2/8 IC50 – 1/16 IC50). Kombinasi ENBA dan EEABA dengan doksorubisin memiliki aktivitas antikanker terhadap sel T47D melalui penghambatan siklus sel pada fase G0-G1, yaitu sebesar 84,37% dan 80,83% dan apoptosis pada tahap apoptosis akhir dan nekrosis awal sebesar 69,51% dan 62,94% dikarenakan terjadi penghambatan ekspresi protein Bcl-2 dan cox-2.
ANTICANCER ACTIVITIES OF
n-HEXANE EXTRACT AND ETHYLACETATE EXTRACT OF ANDALIMAN FRUIT (Zanthoxylum acanthopodium DC.)
IN COMBINATION WITH DOXORUBICIN ON T47D CANCER CELLS IN VITRO
Abstract
Breast cancer is one of cancer variety of the Indonesia's leading cause of death in women. The use of chemotherapeutic agent doxorubicin is one of the breast cancer treatment. Doxorubicin can cause resistance so that the cytotoxic potency will be reduced. Combination therapy with herbal medicines can increase the sensitivity of breast cancer cells and minimize the side effects of doxorubicin. Previous research has tested ethylacetate extract of andaliman fruit’s cytotoxic effect on MCF-7 cells. The purpose of this study to was to determine the anticancer activity of n-hexane extract (ENBA) and ethylacetate extract (EEABA) of andaliman fruit and their combination with doxorubicin on T47D cells.
This study used andaliman fruit from Kecamatan Onan Runggu, Kabupaten Samosir, Sumatera Utara. Extract was made by multilevel maceration with n-hexane, ethylacetate, and ethanol. Cytotoxic effect of EEABA and ENBA was tested in vitro (IC50 values) on the T47D cells and Vero cells used MTT using SPSS 19 and calculated selectivity index. Then ENBA and EEABA were combined with doxorubicin. The most active combination was eventually tested on the inhibition of cell cycle and apoptosis by flowcytometry method and suppressive effects of Bcl-2 and cox-2 protein expression by immunocytochemistry method on T47D cells.
The result of this study showed that IC50 values ENBA and EEABA at 30.908 µg/mL and 24.476 µg/mL. Selectivity test on Vero cells showed that ENBA and EEABA were selective to ward T47D cells. Optimal combination of ENBA-doxorubicin was 20 µg/mL - 25 nM (½ IC50 – 1/16 IC50) and combination of EEABA-doxorubicin was 7.5 µg/mL - 25 nM (2/8 IC50 – 1/16 IC50). Combination of ENBA and EEABA with doxorubicin had anticancer activity to ward T47D cells due to inhibition of cell cycle at G0-G1 phase, amounting to 84.37% and 80.83% and apoptosis in the late stage of apoptosis and early necrosis of 69.51% and 62.94% caused by inhibition of Bcl-2 and cox-2 protein expression.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Kanker merupakan suatu penyakit yang mengalami pertumbuhan tidak
normal dan cepat, yang ditandai dengan pembelahan sel yang tidak terkendali dan
memiliki kemampuan untuk menyerang jaringan biologis lainnya. Kanker bukanlah
penyakit yang menular, namun menjadi masalah kesehatan yang serius di belahan
dunia manapun termasuk di Indonesia (Diandana, 2009; Hawari, 2004).
Kanker merupakan suatu penyakit yang kompleks yang diakibatkan oleh
banyak faktor. Secara fisiologis, sistem pertumbuhan sel dalam individu diatur oleh
suatu sistem keseimbangan, yaitu apoptosis dan proliferasi. Apabila terjadi apoptosis
yang berlebih, maka akan mengalami kemunduran fungsi dari suatu sistem organ
yang dapat menimbulkan penyakit. Sebaliknya, apabila terjadi proliferasi yang
berlebih, maka akan membentuk suatu massa tumor (malignancy) yang akan
mengarah pada kanker (Sudiana, 2011).
Kanker termasuk penyakit mematikan di dunia, baik pria maupun wanita. 5
jenis kanker penyebab kematian terbesar di dunia pada wanita adalah kanker
payudara, leher rahim, kolon, paru-paru, dan lambung (Yaacob, et al., 2010). Kanker
payudara merupakan penyakit kanker jenis sarkoma yang sering ditemui pada
wanita. National Cancer Institute (NCI) memperkirakan akan ada kasus baru kanker
payudara pada wanita sebanyak 232.340 kasus dengan jumlah kematian 39.620
kematian dan sebanyak 22.240 kasus pada laki-laki dengan jumlah kematian 410
seluruh dunia termasuk di Indonesia. Insidensi kanker payudara di Indonesia terdapat
26 per 100.000 wanita yang disusul kanker serviks sebanyak 16 per 100.000 wanita.
Berdasarkan data tahun 2007 Sistem Informasi Rumah Sakit (SIRS), kanker
payudara menempati urutan pertama pada pasien rawat inap di seluruh rumah sakit di
Indonesia (Depkes RI, 2013). Kanker payudara merupakan penyebab utama
kematian pada wanita yang disebabkan metastasis kanker tersebut (Walker, et al.,
1997; Klauber-DeMore, et al., 2001).
Penggunaan agen kemoterapi merupakan salah satu pengobatan kanker
payudara selain pembedahan, radioterapi, dan terapi hormonal (Jong, 2005). Salah
satu agen kemoterapi yang efektif digunakan adalah doksorubisin. Doksorubisin
merupakan agen kemoterapi golongan antrasiklin yang memiliki aktivitas antitumor
spektrum luas (Wattanapitayakul, et al., 2005). Doksorubisin memiliki efek samping
hepatotoksik (Ekowati, et al., 2013) dan kardiotoksik (Arafa, et al., 2005).
Penggunaan jangka panjang doksorubisin dapat menyebabkan resistensi karena
ekspresi berlebih dari P-glikoprotein (Pgp), yakni protein yang berperan pada
pengeluaran obat dari sel, sehingga potensi sitotoksik doksorubisin pada sel kanker
akan berkurang (Sarmoko, 2012; Imai, et al., 2005; Wong, et al., 2006). Berdasarkan
data National Cancer Institute, efek samping yang dapat terjadi akibat kemoterapi
berbasis antrasiklin (doksorubisin) dikelompokkan menjadi mual, muntah, diare,
stomatitis, alopesia, rentan terinfeksi, trombositopenia, neuropati, dan myalgia
(Partridge, et al., 2001). Timbulnya resistensi ini menjadi kendala utama dalam
kemoterapi karena dapat menurunkan sensitivitas sel kanker terhadap agen
Oleh karena itu, perlu dilakukan terapi kombinasi dengan menggunakan agen
kemopreventif untuk meningkatkan sensitivitas sel kanker payudara terhadap agen
kemoterapi doksorubisin dan meminimalkan efek samping doksorubisin. Akan
tetapi, masih langkanya pembuktian penggunaan bahan alami secara ilmiah
menimbulkan kekhawatiran apakah alternatif pengobatan tersebut mempunyai
dampak positif ataukah justru berdampak negatif. Bahan alami yang ideal digunakan
sebagai ko-kemoterapi adalah bahan alami yang berefek sinergis dengan agen
kemoterapi, sehingga dosis agen kemoterapi yang dipakai dapat diturunkan sebagai
upaya menghindari efek samping serta membantu percepatan penyembuhan kanker
(Untung, et al., 2008).
Berbagai kendala dan efek samping yang ditimbulkan oleh berbagai
pengobatan kanker memotivasi kita sebagai farmasis untuk menciptakan suatu ide
pengobatan kanker, khususnya kanker payudara yang memiliki efektifitas tinggi
dengan efek samping minimal. Salah satu upaya mengatasi penyakit kanker ini
adalah mengembangkan obat dari tumbuh-tumbuhan yang mengandung senyawa
antikanker. Pengembangan obat kanker dari tanaman ini dipandang memiliki
beberapa keuntungan, seperti biaya yang lebih murah, mudah didapat, dan efek
samping relatif sedikit (Depkes RI, 2008).
Tumbuhan bermarga Zanthoxylum tidak menunjukkan adanya efek sitotoksik
terhadap sel normal (sel Vero) sehingga berpotensi sebagai obat antikanker yang
aman (Da Silva, et al., 2007). Buah andaliman (Zanthoxylum acanthopodium DC.)
merupakan tanaman khas Sumatera Utara yang termasuk marga dari Zanthoxylum,
suku Rutaceae (Suryanto, et al., 2004). Buah andaliman mengandung banyak
uji aktivitas antioksidan dari ekstrak etanol andaliman (Marwoto, et al., 2004;
Tensiska, et al., 2003), ekstrak heksan andaliman (Tensiska, et al., 2003), ekstrak
metanol andaliman (Gultom, 2011), ekstrak etilasetat andaliman (Gultom, 2012),
minyak atsiri andaliman (Cahyana, 2003), dan senyawa terpenoid andaliman
(Wijaya, 1999) terbukti dapat meredam radikal bebas. Uji sitotoksik buah andaliman
telah diteliti pada sel MCF-7 dan sel T47D oleh Thaib (2013). Pada sel MCF-7,
ekstrak n-heksana buah andaliman (ENBA) memberikan hasil 159,747 µg/mL,
ekstrak etilasetat buah andaliman (EEABA) memberikan hasil 136,490 µg/mL, dan
ekstrak etanol memberikan hasil 957,499 µg/mL. Pada sel T47D, ENBA
memberikan hasil 57,013 µg/mL, EEABA memberikan hasil 52,031 µg/mL, dan
ekstrak etanol memberikan hasil 463,231 µg/mL. Ekstrak dinyatakan aktif apabila
memberikan nilai IC50 10 – 100 µg/mL dan cukup aktif apabila memberikan nilai
IC50 100 – 500 µg/mL (Weerapreeyakul, et al., 2012).
Sel kanker payudara memiliki beberapa jenis untuk diteliti. Banyaknya jenis
sel kanker payudara akan memberikan hasil yang berbeda. Salah satu sel kanker
payudara yang sering digunakan dalam penelitian adalah sel T47D (human ductal
breast epithelial tumor cell line). Sel T47D merupakan continous cell lines yang
dikultur dari jaringan epitel duktus payudara seorang wanita berusia 54 tahun. Sel
ini dapat ditumbuhkan pada suhu 37ºC secara kontinu, menempel pada dasar flask.
Sel T47D sering digunakan dalam penelitian kanker secara in vitro karena mudah
penanganannya, memiliki kemampuan replikasi yang tidak terbatas atau cepat
pertumbuhannya, memiliki homogenitas yang tinggi dan mudah diganti sel baru yang
telah dibekukan jika terjadi kontaminasi (Abcam, 2007). Sel T47D merupakan sel
termutasi sehingga resisten terhadap mekanisme apoptosis, yaitu suatu mekanisme
fisiologis pengurangan sel untuk perbaikan jaringan dan pelepasan sel yang rusak
yang dapat membahayakan tubuh (Ruddon, 2007; Junedi, et al., 2010).
Berdasarkan uraian di atas, tujuan penelitian ini untuk melakukan uji aktivitas
antikanker yang terkandung dalam ENBA dan EEABA terhadap sel T47D melalui
uji sitotoksik, indeks selektivitas, indeks kombinasi dengan doksorubisin, apoptosis,
siklus sel, dan pengujian ekspresi protein.
1.2 Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini adalah:
a. apakah ENBA dan EEABA memiliki aktivitas antikanker terhadap sel T47D
melalui efek sitotoksik dan nilai indeks selektivitas?
b. apakah dapat diketahui konsentrasi optimum kombinasi ENBA dan EEABA
dengan agen kemoterapi doksorubisin pada sel T47D?
c. apakah kombinasi ENBA dan EEABA dengan agen kemoterapi doksorubisin
memiliki aktivitas antikanker terhadap sel T47D melalui penghambatan
apoptosis dan siklus sel serta menekan ekspresi protein Bcl-2 dan cox-2?
1.3 Hipotesis
Berdasarkan rumusan masalah penelitian di atas, maka hipotesis penelitian ini
adalah:
a. ENBA dan EEABA memiliki aktivitas antikanker terhadap sel T47D melalui
b. konsentrasi optimum kombinasi ENBA dan EEABA dengan agen kemoterapi
doksorubisin pada sel T47D dapat diketahui.
c. kombinasi ENBA dan EEABA dengan agen kemoterapi doksorubisin memiliki
aktivitas antikanker terhadap sel T47D melalui penghambatan apoptosis dan
siklus sel serta menekan ekspresi protein Bcl-2 dan cox-2.
1.4 Tujuan Penelitian
Adapun tujuan penelitian ini untuk mengetahui aktivitas antikanker yang
dikandung ENBA dan EEABA serta kombinasi ENBA dan EEABA dengan
doksorubisin terhadap sel T47D.
1.5 Manfaat Penelitian
Manfaat dari penelitian ini adalah memberikan informasi ilmiah kepada
tenaga kesehatan, khususnya farmasis, bahwa buah andaliman berfungsi sebagai
agen ko-kemoterapi antikanker, khususnya kanker payudara yang selektif dan dapat
dimanfaatkan sebagai salah satu obat tradisional yang bersifat antikanker.
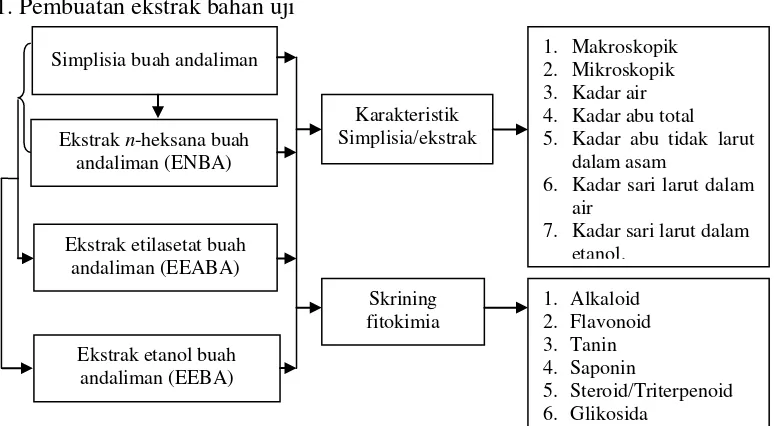
1.6 Kerangka Pikir Penelitian
Simplisia buah andaliman 1. Pembuatan ekstrak bahan uji
2. Pengujian sitotoksik dan indeks selektivitas
3. Pengujian aktivitas antikanker
Gambar 1.1 Diagram kerangka pikir penelitian Sel T47D Efek sitotoksik Persentase sel hidup
Sel Vero Ekstrak n-heksana buah
andaliman (ENBA) 5. Kadar abu tidak larut
dalam asam
6. Kadar sari larut dalam air
7. Kadar sari larut dalam etanol.
ENBA/EEABA
Persentase sel hidup
BAB II
TINJAUAN PUSTAKA
2.1 Siklus Sel
Siklus sel merupakan proses perkembangbiakan sel yang memperantarai
pertumbuhan dan perkembangan makhluk hidup. Setiap sel baik normal maupun
kanker mengalami siklus sel. Siklus sel memiliki dua fase utama, yakni fase S
(sintesis) dan fase M (mitosis). Fase S merupakan fase terjadinya replikasi DNA
kromosom dalam sel, sedangkan pada fase M terjadi pemisahan 2 set DNA
kromosom tersebut menjadi 2 sel (Nurse, 2000). Fase yang membatasi kedua fase
utama tersebut yang dinamakan Gap. G1 (Gap-1) terdapat sebelum fase S dan setelah
fase S dinamakan G2 (Gap-2). Pada fase G1, sel melakukan persiapan untuk sintesis
DNA yang merupakan fase awal siklus sel. Penanda fase ini adalah adanya ekspresi
dan sintesis protein sebagai persiapan memasuki fase S. Pada fase G2, sel melakukan
sintesis lebih lanjut untuk proses pembelahan pada fase M (Ruddon, 2007).
Siklus sel dikontrol oleh beberapa protein yang bertindak sebagai regulator
positif dan negatif. Kelompok cyclin, khususnya cyclin D, E, A, dan B merupakan
protein yang levelnya fluktuatif selama proses siklus sel. Cyclin bersama dengan
kelompok cyclin dependent kinase (CDK), khususnya CDK 4, 6, dan 2, bertindak
sebagai regulator positif yang memacu terjadinya siklus sel. Pada mamalia ekspresi
kinase (CDK4, CDK2, dan CDC2/CDK1) terjadi bersamaan dengan ekspresi cyclin
(D, E, A, dan B) secara berurutan seiring dengan jalannya siklus sel (G1-S-G2-M)
(Nurse, 2000). Aktivasi CDK dihambat oleh regulator negatif siklus sel, yakni CDK
keluarga INK4 (meliputi p16, p18, p19). Selain itu, tumor suppressor protein (p53
dan pRb) juga bertindak sebagai protein regulator negatif (Foster, et al., 2001).
Checkpoint pada fase G2 terjadi ketika ada kerusakan DNA yang akan
mengaktivasi beberapa kinase termasuk ataxia telangiectasia mutated (ATM) kinase.
Hal tersebut menginisiasi dua kaskade untuk menginaktivasi Cdc2-CycB baik
dengan jalan memutuskan kompleks Cdc2-CycB maupun mengeluarkan kompleks
Cdc-CycB dari nukleus atau aktivasi p21. Checkpoint pada fase G1 akan dapat dilalui
jika ukuran sel memadai, ketersediaan nutrien mencukupi, dan adanya faktor
pertumbuhan (sinyal dari sel yang lain). Checkpoint pada fase G2 dapat dilewati jika
ukuran sel memadai, dan replikasi kromosom terselesaikan dengan sempurna.
Checkpoint pada metaphase (M) terpenuhi bila semua kromosom dapat menempel
pada gelendong (spindle) mitosis. Checkpoint ini akan menghambat progresi siklus
sel ke fase mitosis, sedangkan checkpoint pada fase M (mitosis) terjadi jika benang
spindle tidak terbentuk atau jika semua kromosom tidak dalam posisi yang benar dan
tidak menempel dengan sempurna pada spindle. Kontrol checkpoint sangat penting
untuk menjaga stabilitas genomik. Kesalahan pada checkpoint akan meloloskan sel
untuk berkembang biak meskipun terdapat kerusakan DNA atau replikasi yang tidak
lengkap atau kromosom tidak terpisah sempurna sehingga akan menghasilkan
kerusakan genetik. Hal ini kritis bagi timbulnya kanker. Oleh karena itu, proses
regulasi siklus sel mampu berperan dalam pencegahan kanker (Ruddon, 2007).
2.1.1 Apoptosis dan proliferasi
Pertumbuhan sel dalam individu diatur oleh suatu sistem keseimbangan, yaitu
organ akan mengalami kemunduran fungsi yang dapat menimbulkan penyakit.
Sebaliknya, apabila terjadi proliferasi berlebihan, maka akan membentuk suatu
massa tumor yang akan mengarah pada kanker (Sudiana, 2011).
Apoptosis adalah kematian sel melalui mekanisme genetik dengan
kerusakan/fragmentasi kromosom atau DNA. Apoptosis dibedakan menjadi dua
kelompok, yaitu apoptosis fisiologis dan apoptosis patologis. Apoptosis fisiologis
adalah kematian sel yang diprogram (programmed cell death). Proses kematian sel
erat kaitannya dengan enzim telomerase. Pada sel embrional, enzim ini mengalami
aktivasi sedangkan pada sel somatik enzim ini tidak mengalami aktivasi, kecuali sel
bersangkutan mengalami transformasi menjadi ganas. Telomer yang terletak pada
ujung kromosom merupakan faktor yang sangat penting dalam melindungi
kromosom. Pada sel normal, telomer akan memendek pada saat pembelahan diri.
Apabila ukuran telomer mencapai ukuran tertentu (level kritis) akibat pembelahan
berulang, maka sel tersebut tidak dapat melakukan pembelahan diri lagi. Selanjutnya
sel akan mengalami apoptosis secara fisiologis. Pada sel ganas, pemendekan
telomerase sampai pada level kritis tidak terjadi karena pada sel ganas terjadi aktivasi
dari enzim ribonukleoprotein (telomerase) secara terus menerus. Enzim ini sangat
berperan pada sintetis telomer DNA, sehingga berbagai elemen yang dibutuhkan
pada pembentukan telomer dapat dibentuk secara terus menerus dan ukuran telomer
pada ujung kromosom dapat dipertahankan. Oleh karena itu, sel ganas dapat bersifat
immortal (Sudiana, 2011).
Sedangkan apoptosis patologis adalah kematian sel karena adanya proses
suatu rangsangan. Proses ini dapat melalui beberapa jalur, yaitu aktivitas p53, jalur
aktivitas p53 karena sel memiliki gen cacat yang dipicu oleh banyak faktor, antara
lain bahan kimia, radikal bebas, maupun virus (oncovirus). Gen yang cacat dapat
memicu aktivitas beberapa enzim seperti PKC dan CPK-K2 yang dapat memicu
aktivitas p53. P53 adalah faktor transkripsi terhadap pembentukan p21. Peningkatan
p21 akan menekan semua CDK (Cyclin Dependent Kinase) dengan cyclin, dimana
siklus pembelahan sel sangat tergantung pada ikatan kompleks antara CDK dengan
cyclin. Apabila terjadi pengikatan p21, maka semua CDK akan ditekan, baik pada
CDK-1 pada fase M maupun CDK-4 dan CDK-6 pada fase S, lalu siklus sel akan
berhenti sehingga p53 akan memicu aktivitas Bax. Protein Bax akan menekan
aktivitas Bcl-2 sehingga terjadi perubahan membran permeabilitas dari mitokondria
yang mengakibatkan pelepasan sitokrom c ke sitosol sehingga akan mengaktivasi
kaskade kaspase. Kaspase aktif ini akan mengaktifkan DNA-se yang akan menembus
membran inti dan merusak DNA, sehingga DNA akan terfragmentasi dan mengalami
apoptosis (Sudiana, 2011).
Apoptosis melalui jalur sitotoksik dipicu oleh adanya sel yang memiliki gen
cacat sehingga sel akan mengekspresikan protein asing. Protein asing yang
dihasilkan dapat bersifat imunogenik sehingga memicu pembentukan antibodi.
Antibodi akan menempel di permukaan sel killer dan akan memicu pelepasan enzim
yang disebut sebagai sitotoksin. Sitotoksin tersebut mengandung perforin dan
granzyme. Perforin dapat memperforasi membran sel yang memiliki gen cacat
sedangkan granzyme akan masuk ke dalam sel dan mengaktivasi kaspase kaspade.
Kaspase yang aktif ini akan mengaktivasi DNA-se sehingga sel mengalami
apoptosis. Apoptosis dengan jalur disfungsi mitokondria terjadi karena adanya
berlebih maupun protein yang diekspresikan adalah protein abnormal. Terjadinya
apoptosis melalui jalur ligan dan fas terjadi karena dipicu oleh adanya sel yang
terinfeksi virus, dimana di permukaan sel terekspresi suatu protein yang disebut fas.
Fas yang terdapat pada membran sel yang terinfeksi virus akan diikat oleh ligan yang
berada di permukaan NK-cell atau CTL. Adanya ikatan antar fas-ligan akan
mengaktifkan suatu protein yang disebut Fas Associated Protein Death Domain
(FADD) yang dapat mengaktivasi kaspase kaskade. Selanjutnya, kaspase yang aktif
akan mengaktifkan DNA-se sehingga sel akan mengalami apoptosis (Sudiana, 2011).
2.2 Kanker
Kanker adalah segolonga
tidak terkendali dan kemampuan sel menyera
pertumbuhan langsung di jaringan tetangganya (invasif) maupun migrasi sel ke
tempat yang lebih jauh (metastasis). Pertumbuhan yang tidak terkendali tersebut
disebabkan kerusaka
pembelahan sel. Sel kanker kehilangan fungsi kontrolnya terhadap regulasi daur sel
maupun fungsi homeostasis sel pada organisme multiseluler sehingga sel tidak dapat
berproliferasi secara normal. Akibatnya, sel akan berproliferasi terus-menerus
sehingga menimbulkan pertumbuhan jaringan yang abnormal (Diandana, 2009).
Sel kanker timbul dari sel normal tubuh yang mengalami transformasi atau
perubahan menjadi ganas oleh karsinogen atau karena mutasi spontan. Transformasi
sejumlah gen yang menyebabkan gen tersebut termutasi disebut neoplasma atau
tumor. Neoplasma merupakan jaringan abnormal yang terbentuk akibat aktivitas
berkembang menjadi karsinoma in situ di mana sel pada jaringan tersebut masih
terlokalisasi dan mungkin memiliki kesamaaan fungsional dengan sel normal (King,
2000). Sel neoplasma mengalami perubahan morfologi, fungsi, dan siklus
pertumbuhan yang akhirnya menimbulkan disintegrasi dan hilangnya komunikasi
antarsel. Tumor diklasifikasikan sebagai benigna, yaitu kejadian neoplasma yang
bersifat jinak dan tidak menyebar ke jaringan di sekitarnya. Sebaliknya, maligna
disinonimkan sebagai tumor yang melakukan metastasis, yaitu menyebar dan
menyerang jaringan lain sehingga maligna sering disebut sebagai kanker. Kanker
sering dikenal sebagai tumor, tetapi tidak semua tumor disebut kanker
Sel kanker memiliki perbedaan yang sangat signifikan dengan sel normal. Sel
kanker tidak mengenal apoptosis dan akan terus hidup meski seharusnya mati
(bersifat immortal) (Sofyan, 2000). Sel kanker tidak mengenal komunikasi
ekstraseluler atau asosial yang diperlukan untuk menjalin koordinasi antarsel
sehingga dapat saling menunjang fungsi masing-masing. Dengan sifatnya yang
asosial, sel kanker bertindak semaunya sendiri tanpa peduli apa yang dibutuhkan
oleh lingkungannya. Sel kanker dapat memproduksi growth factor sendiri sehingga
tidak bergantung pada rangsangan sinyal pertumbuhan dari luar untuk melakukan
proliferasi sehingga dapat tumbuh menjadi tak terkendali. Sel kanker juga tidak
sensitif terhadap sinyal yang dapat menghentikan pertumbuhan dan pembelahan sel.
Sel kanker mampu menghindar dari sinyal antipertumbuhan yang berhubungan
dengan siklus sel (Kumar, et al., 2005).
(Diandana,
2009).
Sel kanker mampu menyerang jaringan lain (invasif), merusak jaringan
jangkauan metastasis tumor, akan semakin sulit disembuhkan. Kanker pada stadium
metastasis merupakan penyebab 90% kematian penderita kanker (Pecorino, 2005).
Untuk mencukupi kebutuhan pangan dirinya sendiri, sel kanker mampu membentuk
pembuluh darah baru (neoangiogenesis) meski dapat mengganggu kestabilan
jaringan tempat ia tumbuh. Sinyal inisiasi pada proses neoangiogenesis diantaranya
adalah Vascular Endothelial Growth Factor (VEGF) dan Fibroblast Growth Factor
(FGF). Selain itu, regulator yang lain adalah angiopoietin-1, angiotropin, angiogenin,
epidermal growth factor, granulocytecolony-stimulating factor, interleukin-1 (IL-1),
IL-6, IL-8, PDGF, TNF-α, kolagen, cathepsin. Sel kanker memiliki kemampuan
yang tidak terbatas dalam memperbanyak dirinya sendiri (proliferasi) meski sudah
tidak dibutuhkan dan jumlahnya sudah melebihi kebutuhan yang seharusnya (Kumar,
et al., 2005).
Secara umum, penyebab kanker dapat dibagi dalam 3 kategori, yaitu
karsinogen fisik (radiasi sinar UV dan radiasi ionisasi), karsinogen kimiawi (asap
tembakau dan asbestos), dan karsinogen biologis (virus, bakteri, dan parasit) (PCC,
2013). Selain itu, kanker dapat timbul karena pola hidup yang tidak sehat. Hampir
separuh dari kanker yang terdiagnosis setiap tahun disebabkan oleh gaya hidup yang
tidak sehat. Pencetus kanker dapat berasal dari makanan yang kaya akan gula buatan,
karbohidrat olahan, pengawet, produk sampingan dari hasil penggorengan (minyak
jelantah), mengandung banyak lemak, asupan antioksidan yang kurang, dan
minuman yang mengandung bahan kimia (minuman beralkohol) (Mueller, et al.,
2010). Penyebab kanker juga bisa timbul karena kondisi kejiwaan yang tidak stabil
dan faktor keturunan. Orang tua yang mengidap kanker sangat mungkin menurunkan
2.2.1 Karsinogenesis
Kanker bukan termasuk penyakit yang datang begitu saja, melainkan akibat
akumulasi atau penumpukan kerusakan-kerusakan tertentu di dalam tubuh.
Serangkaian proses berkembangnya kanker disebut karsinogenesis. Karsinogenesis
adalah suatu proses terjadinya kanker melalui mekanisme multi tahap yang
menunjukkan perubahan genetik dan menyebabkan transformasi progresif sel normal
menjadi sel malignan (ganas). Perubahan ini diawali dari mutasi somatik satu sel
tunggal yang mengakibatkan perubahan dari normal menjadi hiperplastik, displastik,
dan pada akhirnya menjadi suatu keganasan atau malignansi (memiliki kemampuan
metastasis atau menginvasi jaringan di sekitarnya). Perubahan genetik ini termasuk
perubahan seluler mendasar pada sel kanker yang dipengaruhi oleh beberapa gen
seperti tumor suppresor genes (pRb, p53, PTEN, E-cadherin) dan proto-oncogenes
(ras, c-myc, Bcl-2). Karsinogenesis dapat dibagi menjadi empat tahap utama, yaitu
tahap inisiasi, promosi, progresi, dan metastasis (Tsao, et al., 2004).
Tahap inisiasi adalah tahap pertama pada karsinogenesis dan merupakan hasil
perubahan genetik yang menuntun pada proliferasi tidak terkontrol (abnormal)
sebuah sel. Tahap inisiasi dapat terjadi melalui jalur germinal dan somatik. Namun
pada kebanyakan kasus diperoleh secara somatik akibat terjadinya kesalahan acak
saat pembelahan sel atau karena paparan dari karsinogen spesifik seperti tobako dan
radiasi. Pada tahap ini, senyawa yang berpotensi sebagai senyawa karsinogen
diaktivasi terlebih dahulu di dalam tubuh terutama di hepar menjadi senyawa
metabolitnya. Senyawa metabolit ini ada yang bersifat reaktif, mutagenik, dan
mampu berikatan dengan makromolekul di dalam tubuh seperti DNA dengan ikatan
normal secara spontan, tetapi pada tingkat lebih lanjut dapat menjadi ganas
(malignan) (King, 2000).
Selanjutnya tahap promosi yang merupakan tingkat lanjutan dari tahap
inisiasi. Pada tahap ini, sel mulai mengalami hiperplastik pada inti sel. Berbeda
dengan tahap inisiasi yang dapat melewati jalur germinal dan somatik, tahap promosi
hanya diketahui terjadi melalui jalur somatik. Pada tahap promosi, sel akan
memperoleh beberapa keuntungan selektif untuk tumbuh sehingga pertumbuhannya
menjadi cepat dan berubah menjadi tumor jinak. Tahap promosi tidak melibatkan
perubahan struktural dari genom secara langsung, tetapi biasanya terjadi perubahan
ekspresi gen yang terinisiasi (Tsao, et al., 2004; King, 2000).
Pada tahap progresi, kemampuan pembelahan yang tinggi menuntun
terbentuknya koloni sel yang lebih besar melalui perubahan genetik lebih lanjut dan
munculnya keistimewaan lain seperti peningkatan mobilitas dan angiogenesis
(Kumar, 2005). Pada tahap ini, sel tumor dikatakan sebagai sel malignan. Pada fase
ini juga akan terjadi karsinoma dan metastasis melalui aktivasi onkogen dan
malfungsi dari enzim topoisomerase (Pecorino, 2005).
Tahap metastasis merupakan tahap akhir dalam karsinogenesis. Pada tahap
ini, sel kanker melakukan invasi ke jaringan lain di dalam tubuh melalui pembuluh
darah, pembuluh limpa, atau rongga tubuh. Sel malignan yang bermetastasis ini
masuk melalui basement membran menuju saluran limpoid. Sel tersebut akan
berinteraksi dengan sel limpoid yang digunakan sebagai inangnya. Selanjutnya, sel
kanker akan masuk ke jaringan lainnya membentuk tumor sekunder dengan
didukung kemampuan neoangiogenesis yang dimilikinya. Tahap metastasis dapat
terdegradasinya CAMs (Cell-cell Adhesion Molecules) dan E-cadherin sebagai
molekul yang menjaga pertautan antarsel. Molekul tersebut diketahui sudah sangat
sedikit bahkan tidak ditemukan lagi pada sel kanker, sehingga proses metastasis
dapat terus terjadi (Kumar, et al., 2005).
Kanker dapat terjadi dalam berbagai jenis sel, antara lain karsinoma (pada
kelenjar epitel), glioma (pada jaringan otak), leukemia (pada sel darah putih),
sarkoma (pada jaringan lunak dan jaringan ikat seperti tulang rawan, lemak, otot,
ataupun tulang), myeloma (pada jaringan selaput saraf/neuron), hepatoma (pada sel
hati), fibroma (pada jaringan ikat fibrosa), dan limfoma (pada kelenjar getah bening)
(Anonim1
2.2.2 Kanker payudara
, 2014).
Kanker payudara merupakan kanker yang menyerang jaringan epitelial
payudara, yaitu membran mukosa dan kelenjar sehingga kanker payudara tergolong
pada karsinoma. Kanker payudara merupakan kanker yang paling umum diderita
oleh wanita selain kanker serviks. Penyebab kanker payudara sangat beragam, antara
lain kerusakan pada DNA yang menyebabkan mutasi genetik. Kerusakan ini dapat
disebabkan oleh radiasi yang berlebihan. Selanjutnya karena kegagalan immune
surveillance dalam pencegahan proses malignan pada fase awal, faktor pertumbuhan
yang abnormal, dan malfungsi DNA repairs seperti BRCA1, BRCA2, dan p53
(Torosian, 2002).
Kanker payudara terjadi ketika sel pada payudara tumbuh tidak terkendali
dan dapat menginvasi jaringan tubuh yang lain baik yang dekat dengan organ
tersebut maupun bermetastasis ke jaringan tubuh yang letaknya berjauhan. Semua
umumnya kanker muncul baik dari saluran (ducts) maupun kelenjar (glands).
Perkembangannya memerlukan waktu berbulan-bulan atau bertahun-tahun sampai
tumor tersebut cukup besar untuk dirasakan pada payudara. Deteksi dapat dilakukan
dengan mammogram yang kadang-kadang dapat mendeteksi tumor sejak dini
(Elwood, et al., 1993).
Peningkatan insidensi kanker payudara disebabkan oleh kegagalan terapi
terhadap kanker itu sendiri. Kegagalan ini diakibatkan oleh adanya multidrug
resistance (MDR) dan terjadi hingga 71% dibandingkan dengan faktor penyebab
lainnya (Mechetner, et al., 1998). Multidrug resistance atau resistensi obat ini
diakibatkan oleh adanya breast cancer resistance protein (BCRP) yang salah satunya
adalah P-glycoprotein (Pgp) (Imai, et al., 2005). Aktivasi Pgp dan peningkatan
ekspresinya dapat menurunkan efikasi dari beberapa agen kemoterapi, seperti Taxol
dan Doxorubicin (Mechetner, et al., 1998). Penekanan aktivitas Pgp dan ekspresinya
mampu meningkatkan efektivitas agen kemoterapi (Zhou, et al., 2006).
Selain itu, paparan estrogen endogen yang berlebihan juga dapat
berkontribusi sebagai penyebab kanker payudara. Sekitar 50% kasus kanker
payudara merupakan kanker yang bergantung pada estrogen dan sekitar 30% kasus
merupakan kanker yang positif mengekspresi HER-2 berlebihan. Kedua protein
tersebut selain berperan dalam metastasis, juga berperan dalam perkembangan
kanker payudara (early cancer development) (Gibbs, 2000).
Proses metastasis kanker payudara diinisiasi oleh adanya aktivasi/ekspresi
berlebih beberapa protein, seperti Estrogen Reseptor (ER) dan c-erbB-2 (HER- 2)
yang merupakan protein predisposisi kanker payudara. Aktivasi reseptor estrogen
mengatur proliferasi sel. Estrogen dapat memacu ekspresi protein yang berperan
dalam siklus sel seperti cyclin D1, CDK4, cyclin E, dan CDK2. Selain itu, aktivasi
reseptor estrogen mampu mengaktivasi beberapa onkoprotein yang berperan dalam
sinyal pertumbuhan, misalnya Ras, Myc, dan cycD1 (Foster, et al., 2001). Aktivasi
protein ini mengakibatkan adanya pertumbuhan yang berlebihan melalui aktivasi
onkoprotein yang lain seperti P13K, AKT, Raf, ERK, dan MAP kinase (Hahn, et al.,
2002). Di lain pihak, kompleks estrogen dengan reseptornya juga akan memacu
transkripsi beberapa gen tumor suppressor, seperti BRCA1, BRCA2, dan p53.
Namun, pada penderita kanker payudara (yang umumnya telah lewat masa
menopause), gen tersebut telah mengalami perubahan (transformed) akibat dari
hiperproliferasi sel payudara selama perkembangannya sehingga tidak berperan
sebagaimana mestinya (Adelmann, et al., 2000, Clarke, 2001; Ingvarsson, et al.,
2002).
Beberapa jenis sel kanker payudara yang dapat dikultur adalah MCF-7,
Ia-270, BT-20, BT-474, BT-549, Colo-824, HBL-100, MA-CLS-2, MDA-MB-231,
MDA-MB-435S, MDA-MB-436, MB-MDA-468, MX-1, SK-BR-3, ZR-75-1, dan
T47D (Pao, et al., 1985; Anonim2
2.2.2.1 Sel T47D
, 2014). Banyaknya jenis sel kanker payudara ini
akan memberikan hasil yang berbeda pada setiap selnya. Perbedaan hasil ini akan
memberikan peluang baru untuk menyelidiki perkembangan yang terjadi pada
resistensi obat pada pasien dengan tumor payudara yang memiliki p53 termutasi
(Schafer, et al., 2000).
Sel T47D merupakan sel kanker yang mengekspresikan reseptor estrogen
sehingga resisten terhadap mekanisme apoptosis (Ruddon, 2007; Junedi, et al.,
2010). Pada sel ini, p53 mengalami missense mutation pada residu 194 (dalam
zinc-binding domain L2) sehingga p53 kehilangan fungsinya. Jika p53 tidak dapat
mengikat response element pada DNA, maka akan mengurangi atau menghilangkan
kemampuannya dalam meregulasi siklus sel dan memacu apoptosis. Sel ini dapat
kehilangan estrogen reseptor (ER) apabila kekurangan estrogen pada jangka waktu
lama selama percobaan in vitro. Oleh karena itu, sel ini digunakan pada model untuk
penelitian resistensi obat pada pasien dengan tumor payudara yang memiliki p53
termutasi (Abcam, 2007).
Sel T47D sering digunakan dalam penelitian kanker secara in vitro karena
mudah penanganannya, memiliki kemampuan replikasi yang tidak terbatas atau cepat
pertumbuhannya, memiliki homogenitas yang tinggi dan mudah diganti sel baru yang
telah dibekukan jika terjadi kontaminasi (Abcam, 2007). Sel T47D memiliki
mekanisme antiapoptosis dan karsinogenesis lebih kuat daripada sel MCF-7.
Beberapa protein yang terlibat dalam stimulasi pertumbuhan sel ini termasuk
caspase-3 subunit p12, protein nuklir Hcc-1, G1/S-specific cyclin-D3, cathepsin B,
protein CDV3 homolog, N (G), N(G)-dimethylarginine dimethylaminohydrolase 2,
dan prohibitin (Aka, et al., 2012).
2.2.3 Sel Vero
Sel Vero ATCC CCL-81 merupakan sel epitel non kanker (sel normal). Sel
ini berasal dari organ ginjal monyet hijau asal Afrika. Sel Vero merupakan sel
monolayer berbentuk poligonal dan pipih, immortal, non tumorigenic fibroblastic
cell. Sel ini melekat erat pada substrat yang berbahan polistirena dengan membentuk
diferensiasi sel, sitotoksisitas, dan transformasi sel yang diinduksi oleh berbagai
senyawa kimia (Goncalves, et al., 2006).
2.2.4 P-glycoprotein
P-glycoprotein (Pgp) merupakan protein ABC-transporter pada manusia yang
termasuk dalam subfamili MDR/TAP (Allen, et al., 2002). Pgp dikenal dalam
beberapa sebutan, yaitu ABCD1, ATP-binding cassette sub-family B member 1,
MDR1, dan PGY1 (Choi, et al., 2005). ABCD1 atau Pgp termasuk dalam
ATP-dependent efflux pump yang memiliki substrat spesifik, antara lain: obat (colchicine
dan tacrolimus), agen kemoterapi (etoposide, adriamycin, dan vinblastine), lipid,
steroid, xenobiotik, peptide, bilirubin, cardiac glycoside (digoxin), glucocorticoids
(dexamethasone), dan agen terapi HIV tipe 1 (inhibitor protease dan nonnucleoside
reverse transcriptase) (Kitagawa, 2006). Di dalam tubuh, Pgp dapat ditemukan pada
sel usus, hati, tubula ginjal dan capillary endothelial (Deng, et al., 2001).
P-glycoprotein adalah sebuah glikoprotein transmembran yang memiliki 10 -
15 kDa N-terminal glycosylation dengan bobot 170-kDa dikode oleh gen MDR1
(Kitagawa, 2006). Gen ini dicirikan dengan pompa efflux obat dan anggota dari
keluarga ATP-binding transport (Choi, et al., 2005). Dalam sistem organ, Pgp
berpengaruh terhadap absorbsi, distribusi, dan eliminasi obat (Matheny, et al., 2001).
Kemampuan Pgp sebagai effluxpump berguna dalam detoksifikasi senyawa-senyawa
yang masuk ke dalam sel. Senyawa yang termasuk substrat dari Pgp akan diikat dan
dikeluarkan dari dalam sel. Aktivitas Pgp sangat bergantung pada aktivasi Pgp oleh
ATP melalui pembentukkan kompleks Pgp-ATP (Conseil, et al., 1998). Hidrolisis
ATP oleh ATPase memberikan energi aktivasi pada Pgp (Choi, et al., 2005).
agen tersebut terhadap sel kanker. Pada kondisi ekspresi berlebihan, Pgp dapat
menyebabkan resistensi obat terutama agen kemoterapi pada jenis kanker payudara
seperti doksorubisin (Mechetner, et al., 1998). Pgp akan mengikat doksorubisin
sebagai salah satu substratnya untuk dikeluarkan dari dalam sel (Wong, et al., 2006).
Pgp atau ABCD1 pertama kali diujikan sebagai multidrug resistance dan terbukti
sebagai penyebab resistensi obat kemoterapi (Juliano, et al., 1976). Mekanisme
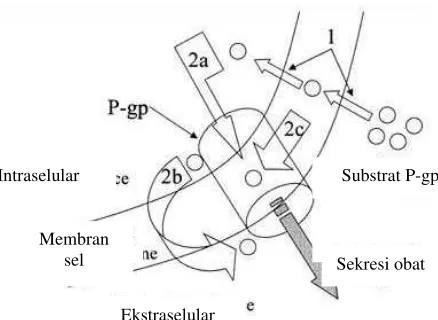
pemompaan oleh Pgp dapat dilihat pada Gambar 2.1.
Pgp memompa senyawa-senyawa (2a, 2b, 2c) yang termasuk substratnya
untuk dikeluarkan dari dalam sel. Ekspresi berlebih dari Pgp ini dapat menyebabkan
resistensi obat pada terapi kanker payudara (Matheny, et al., 2001).
Gambar 2.1 Mekanisme pemompaan oleh Pgp (Matheny, et al., 2001)
Penghambatan aktivasi dan ekspresi Pgp memegang peranan penting dalam
keberhasilan terapi kanker (Zhou, et al., 2006). Penghambatan aktivitas Pgp dapat
melalui beberapa mekanisme, antara lain penghambatan substrat Pgp secara langsung
dengan berikatan pada Pgp-binding domain dan penghambatan hidrolisis ATP oleh
ATPase melalui ikatan substrat dengan ATP. Penghambatan ini dapat dilakukan
menggunakan senyawa flavonoid dan polifenol melalui dua sisi ikatan pada
ATP-Membran
sel Sekresi obat
Ekstraselular
binding sites dan steroid interacting region dimana ATPase berikatan dengan Pgp
cytosolic domain (Kitagawa, 2006).
Deng, et al., (2001) melaporkan bahwa aktivasi NF-κB sebagai akibat
adanya stimulus dari lingkungan berupa stress, paparan agen sitotoksik, heat shock,
iradiasi, stress genotoksik, inflamasi, paparan sitokin, dan faktor pertumbuhan dapat
meningkatkan ekspresi Pgp. NF-κB yang aktif mampu berikatan dengan promoter
gen MDR1 sehingga proses ekspresi Pgp dapat berjalan. Inaktivasi NF-κB mampu
menghambat ekspresi Pgp.
2.3 Penanganan Kanker
Penanganan kanker ada dua macam, yaitu pencegahan dan penghambatan
kanker. Upaya pencegahan kanker disebut kemopreventif. Senyawa
kemopreventif dibagi menjadi dua kategori, yaitu blocking agent dan suppressing
agent. Blocking agent mencegah karsinogen mencapai target aksinya, baik melalui
penghambatan aktivasi metabolisme maupun menghambat interaksi dengan target
makromolekul seperti DNA, RNA, atau protein. Sedangkan suppressing agent
menghambat pembentukan malignan dari sel yang telah terinisiasi pada tahap
promosi atau progresi (Surh, 1999).
Kemopreventif dibagi menjadi tiga golongan, yaitu primer, sekunder, dan
tersier. Kemopreventif primer adalah mencegah terjadinya sel kanker sejak tahap
premalignan. Usaha pencegahan saat karsinogenesis pada tahap awal malignan
untuk meminimalkan resiko yang mungkin terjadi setelah terapi untuk malignan
primer. Upaya penyembuhan (kuratif) kanker, antara lain kemoterapi menggunakan
obat-obatan, seperti golongan siklofosfamid, methotreksat, dan 5-flurourasil. Pada
dasarnya kinerja obat-obatan tersebut sama, yaitu menghambat proliferasi sel
sehingga sel tidak jadi memperbanyak diri. Kemoterapi bisa diberikan secara tunggal
ataupun kombinasi dengan harapan bahwa sel-sel yang resisten terhadap obat
tertentu juga bisa merespon obat yang lain sehingga bisa diperoleh hasil yang lebih
baik. Dampaknya pada pasien biasanya rambut rontok, selera makan menurun, serta
rasa lemah dan letih (Sharma, 2000).
Terapi hormon digunakan untuk jenis kanker yang berkaitan dengan hormon,
misalnya kanker payudara (berkaitan dengan hormon estrogen) pada wanita dan
kanker prostat (berkaitan dengan hormon androgen) pada pria. Terapi hormon pada
dasarnya berusaha menghambat sintesis steroid sehingga sel tidak dapat membelah.
Terapi ini membawa dampak negatif bila diaplikasikan pada wanita yang masih
dalam usia subur karena dapat menghambat siklus menstruasi. Radioterapi
menggunakan sinar-X dengan dosis tertentu dapat merusak DNA dan memaksa sel
untuk berapoptosis. Efek negatif yang ditimbulkan hampir sama dengan kemoterapi
(Sharma, 2000; Wargasetia, 2005).
2.3.1 Penanganan kanker payudara
Upaya penyembuhan kanker payudara dapat digolongkan secara
pembedahan, kemoterapi, terapi hormon, radioterapi, dan terapi gen (Jong, 2005;
Sharma, 2000; Wargasetia, 2005).
Penentuan stadium kanker payudara sangat penting sebagai panduan
stadium 0 (tumor in situ, sel-sel kanker berada pada tempatnya di dalam jaringan
payudara yang normal), stadium 1 (tumor dengan garis tengah kurang dari 2 cm dan
belum menyebar keluar payudara), stadium 2A (tumor dengan garis tengah 2-5 cm
dan belum menyebar ke kelenjar getah bening, ketiak, atau tumor dengan garis
tengah kurang dari 2 cm tetapi sudah menyebar ke kelenjar getah bening ketiak),
stadium 2B (tumor dengan garis tengah lebih besar dari 5 cm dan belum menyebar
ke kelenjar getah bening ketiak atau tumor dengan garis tengah 2-5 cm tetapi sudah
menyebar ke kelenjar getah bening ketiak), stadium 3A (tumor dengan garis tengah
kurang dari 5 cm dan sudah menyebar ke kelenjar getah bening ketiak disertai
perlengketan satu sama lain atau perlengketan ke struktur lainnya, atau tumor dengan
garis tengah lebih dari 5 cm dan sudah menyebar ke kelenjar getah bening ketiak),
stadium 3B (tumor telah menyusup keluar payudara, yaitu ke dalam kulit payudara
atau ke dinding dada atau telah menyebar ke kelenjar getah bening di dalam dinding
dada dan tulang dada), dan terakhir stadium 4 (tumor telah menyebar keluar daerah
payudara dan dinding dada, misalnya ke hati, tulang, atau paru-paru) (American
Cancer Society, 2014).
Kemoterapi merupakan salah satu pengobatan yang bertujuan mematikan
ataupun memperlambat pertumbuhan sel kanker. Jenis agen kemoterapi yang sering
digunakan pada kanker payudara antara lain kemoterapi neoajuvan, ajuvan, dan
paliatif (Yudissanta, dkk., 2012). Obat kemoterapi yang biasanya diberikan dalam
upaya penyembuhan kanker payudara ada dalam bentuk tunggal dan kombinasi.
Beberapa bentuk tunggal yang biasanya diberikan antara lain docetaxel (Anonim,
yang biasanya diberikan antara lain antrasiklin-cyclophosphamide,
taxanes-cyclophosphamide, dan antrasiklin-cyclophosphamide-taxol (Anonim3
2.3.1.1Doksorubisin
, 2014).
Doksorubisin merupakan golongan antibiotik antrasiklin sitotoksik yang
diisolasi dari Streptomyces peucetius var. caesius. Doksorubisin telah digunakan
secara luas untuk mengobati kanker payudara. Senyawa ini menunjukkan
kemampuan yang kuat dalam melawan kanker dan telah digunakan sebagai obat
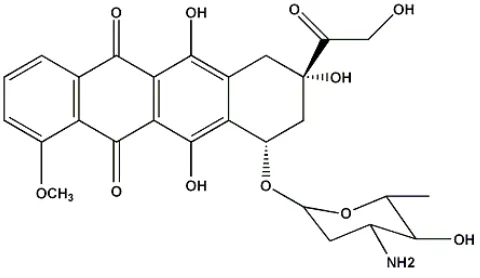
kemoterapi kanker sejak akhir tahun 1960-an (Singal, et al., 1998). Struktur kimia
doksorubisin ditunjukkan pada Gambar 2.2.
Gambar 2.2 Struktur kimia doksorubisin
Doksorubisin memiliki aktivitas antineoplastik dan spesifik untuk fase S
dalam siklus sel. Mekanisme aktivitas antineoplastiknya belum diketahui dengan
pasti. Mekanisme aksi doksorubisin kemungkinan melibatkan ikatan dengan DNA
melalui interkalasi di antara pasangan basa serta menghambat sintesis DNA dan
RNA. Kemungkinan mekanisme yang lain adalah melibatkan ikatan dengan lipid
membran sel yang akan mengubah berbagai fungsi selular dan berinteraksi dengan
topoisomerase II membentuk kompleks pemotong DNA. Doksorubisin telah
digunakan pada beberapa pengobatan jenis tumor seperti kanker payudara,
Hodgkin, dan non-Hodgkin baik dalam aplikasi tunggal maupun kombinasi dengan
beberapa agen antitumor lainnya (Tyagi, et al., 2004).
Efek samping yang timbul segera setelah pengobatan dengan doksorubisin
adalah mual, imunosupresi, dan aritmia yang sifatnya revesibel serta dapat dikontrol
dengan obat-obat lain. Efek samping yang paling serius dalam jangka waktu yang
lama adalah hepatotoksik (Ekowati, et al., 2013) dan cardiomyopathy yang diikuti
dengan gagal jantung (Tyagi, et al., 2004). Berdasarkan hasil penelitian restrospektif,
diketahui bahwa toksisitas kardiak akibat pemberian doksorubisin merupakan efek
samping yang bergantung pada dosis. Mekanisme yang memperantarai toksisitas
kardiak tersebut diduga disebabkan oleh terbentuknya spesies oksigen reaktif,
meningkatnya kadar anion superoksida dan pengurasan ATP yang kemudian
menyebabkan luka jaringan kardiak (Wattanapitayakul, et al., 2005). Permasalahan
yang sering timbul pada penggunaan doksorubisin dalam terapi kanker terutama
kanker payudara adalah resistensi obat yang menjadi penyebab kegagalan terapi.
Pengeluaran obat yang disebabkan oleh adanya pompa efflux Pgp menjadi salah satu
penyebab utama resistensi obat ini (Mechetner, et al., 1998).
Doksorubisin termasuk obat golongan antrasiklin yang merupakan substrat
Pgp. Doksorubisin akan dikenali oleh Pgp dan selanjutnya segera dikeluarkan dari
dalam sel sehingga menurunkan konsentrasi efektif doksorubisin dalam sel kanker.
Mekanisme pemompaan oleh Pgp sangat bergantung pada aktivasi protein tersebut
dan penekanan ekspresi Pgp. Oleh karena itu, inaktivasi Pgp dan penekanan
ekspresinya mampu mengatasi permasalahan resistensi sel kanker terhadap
doksorubisin (Mechetner, et al., 1998; Zhou, et al., 2006; Wong, et al., 2006).