PENETAPAN KADAR PROTEIN PADA YOGURT KEMASAN
DENGAN METODE KJELDAHL
TUGAS AKHIR
Oleh:
VENNY C S SITOMPUL
112410014
PROGRAM DIPLOMA III ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
Penetapan Kadar Protein pada Yogurt Kemasan dengan Metode Kjeldahl
Abstrak
Menurut SNI, yogurt adalah produk yang diperoleh dari susu yang telah dipasteurisasi kemudian difermentasikan dengan bakteri tertentu sampai diperoleh keasaman, bau, dan rasa yang khas, dengan atau tanpa penambahan bahan lain yang diizinkan. Tujuan penelitian ini adalah untuk menentukan kadar protein di dalam yogurt kemasan.
Sampel yang digunakan dalam pengujian adalah yogurt kemasan sebanyak tiga botol. Penetapan kadar protein dilakukan menurut metode Kjeldahl sesuai dengan prosedur Standard Nasional Indonesia (SNI) dan peralatan kerja untuk metode Kjeldahl yang digunakan di laboratorium Makanan Minuman Hasil Pertanian Balai Riset dan Standardisasi (Baristand) Industri Medan.
Hasil penelitian menunjukkan bahwa yogurt yang diperiksa mengandung kadar protein masing-masing 1,72 %, 1,75 % dan 1,78 %, dengan rata-rata kadar protein sebesar 1,75 %. Hasil ini tidak mencapai batas minimum kadar protein yang tertera di SNI 01 – 2981 – 1992, yakni minimal 3,5 %.
Kadar protein yogurt sangat ditentukan oleh kualitas bahan dasarnya, yaitu susu. Semakin tinggi kadar protein susu, semakin baik kualitas yogurt yang dihasilkannya
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yang Maha Esa karena atas berkat dan kasih-Nya, penulis dapat menyelesaikan Tugas Akhir yang berjudul “Penetapan Kadar Protein pada Yogurt Kemasan dengan Metode Kjeldahl”.
Tujuan penyusunan tugas akhir ini sebagai salah satu persyaratan untuk menyelesaikan pendidikan Program Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera Utara. Tugas Akhir ini disusun berdasarkan apa yang penulis lakukan pada Praktek Kerja Lapangan (PKL) di Balai Riset Standardisasi (Baristand) Industri Medan.
Selama menyusun Tugas Akhir ini, penulis juga mendapat bantuan dari berbagai pihak, untuk itu penulis mengucapkan terima kasih kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU.
2. Bapak Prof, Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi USU. 3. Ibu Prof. Dr. Rosidah, M.Si, Apt., selaku Dosen Pembimbing Tugas Akhir
dan Pak Alhamra, Kepala Laboratorium Makanan Minuman Hasil Pertanian selaku Pembimbing PKL di Baristand Industri Medan.
4. Bapak Drs., Ismail, M.Si., Apt., selaku Dosen Pembimbing Akademik, Ibu dan Bapak Dosen beserta seluruh staf di Fakultas Farmasi USU.
5. Bapak Ir. Maruahal Situmorang, M.Si., selaku Kepala dan seluruh staf Baristand Industri Medan.
mahasiswi Program Studi Diploma III Analis Farmasi dan Makanan angkatan 2011, yang tidak dapat penulis sebutkan satu persatu, namun tidak mengurangi arti keberadaan mereka.
Penulis mengucapkan terimakasih terutama kepada kedua orang tua, ayah H. Sitompul dan ibu, Y. Purba yang sudah memberi dukungan dalam penulisan Tugas Akhir. Juga saudara kandung penulis, Ingrid Yohanna Sitompul yang selalu memberikan semangat, Ompung Ebenhaezer beserta keluarga terkasih yang selalu mendoakan dan memberikan nasihat kepada penulis agar semangat dalam meraih cita-cita.
Penulis menyadari bahwa tulisan ini tidak luput dari kekurangan. Oleh karena itu, kritik dan saran yang bersifat membangun sangat penulis harapkan demi kesempurnaan tulisan ini. Akhir kata, penulis berharap semoga Tugas Akhir ini bermanfaat bagi pembaca.
Medan, Juni 2014 Penulis,
2.4 Akibat Kekurangan dan Kelebihan Protein ... 10
2.4.1 Akibat Kekurangan Protein ... 10
2.4.2 Akibat Kelebihan Protein ... 11
2.5 Analisis Protein ... 11
2.5.1 Analisis Kualitatif ... 11
2.5.2 Analisis Kuantitatif ... 13
BAB III METODE PENGUJIAN ... 18
3.1 Tempat Pengujian ... 18
3.2 Alat dan Bahan ... 18
3.2.1 Alat ... 18
3.2.2 Bahan ... 18
3.3 Pereaksi ... 18
3.4 Prosedur ... 18
3.5 Flowshet ... 20
BAB IV HASIL DAN PEMBAHASAN ... 21
4.1 Hasil ... 21
4.2 Pembahasan ... 21
BAB V KESIMPULAN DAN SARAN ... 24
5.1 Kesimpulan ... 23
5.2 Saran ... 23
DAFTAR TABEL
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur Primer Protein ... 6
Gambar 2. Struktur Sekunder Protein ... 7
Gambar 3. Struktur Tersier Protein ... 7
Gambar 4. Struktur Kuarterner Protein ... 7
DAFTAR LAMPIRAN
Penetapan Kadar Protein pada Yogurt Kemasan dengan Metode Kjeldahl
Abstrak
Menurut SNI, yogurt adalah produk yang diperoleh dari susu yang telah dipasteurisasi kemudian difermentasikan dengan bakteri tertentu sampai diperoleh keasaman, bau, dan rasa yang khas, dengan atau tanpa penambahan bahan lain yang diizinkan. Tujuan penelitian ini adalah untuk menentukan kadar protein di dalam yogurt kemasan.
Sampel yang digunakan dalam pengujian adalah yogurt kemasan sebanyak tiga botol. Penetapan kadar protein dilakukan menurut metode Kjeldahl sesuai dengan prosedur Standard Nasional Indonesia (SNI) dan peralatan kerja untuk metode Kjeldahl yang digunakan di laboratorium Makanan Minuman Hasil Pertanian Balai Riset dan Standardisasi (Baristand) Industri Medan.
Hasil penelitian menunjukkan bahwa yogurt yang diperiksa mengandung kadar protein masing-masing 1,72 %, 1,75 % dan 1,78 %, dengan rata-rata kadar protein sebesar 1,75 %. Hasil ini tidak mencapai batas minimum kadar protein yang tertera di SNI 01 – 2981 – 1992, yakni minimal 3,5 %.
Kadar protein yogurt sangat ditentukan oleh kualitas bahan dasarnya, yaitu susu. Semakin tinggi kadar protein susu, semakin baik kualitas yogurt yang dihasilkannya
BAB I PENDAHULUAN
1.1 Latar Belakang
Minuman ringan merupakan minuman olahan dalam bentuk bubuk atau cair yang mengandung bahan makanan atau bahan tambahan lainnya baik alami maupun sintetik yang dikemas dalam kemasan siap untuk dikonsumsi (Cahyadi, 2005).
Susu merupakan bahan pangan yang mempunyai nilai gizi tinggi karena mempunyai kandungan nutrisi yang lengkap seperti laktosa, lemak, protein, berbagai vitamin, dan mineral (Widodo, 2009). Susu sapi sebagai bahan dasar pembuatan yogurt memiliki komposisi nutrisi (untuk setiap 100 ml), antara lain: vitamin A 158 I.U, vitamin D 2,0 I.U, vitamin B6 0,036 mcg, kalori 69 kkal, protein 3,3 g, lemak 3,7 g, kaktosa 4,8 g, kalsium 125 mg, kasein 2,8 g, besi 0,10 mg, mineral 0,72 g (Sunarlim dan Usmiati, 2008).
Yogurt merupakan salah satu jenis susu fermentasi yang telah dikenal dan cukup digemari oleh masyarakat secara luas (Usmiati dan Abubakar, 2009). Yogurt sebagai penghasil protein membantu masyarakat agar terpenuhi asupan proteinnya. Hal ini dapat mengurangi terjadinya resiko terkena penyakit kwashiorkor dan marasmus (Widodo, 2009).
1.2 Tujuan Percobaan
- Untuk mengetahui kadar protein yang terdapat di dalam yogurt kemasan apakah sesuai dengan Standar Nasional Indonesia (SNI).
- Untuk mengetahui faktor yang mempengaruhi kadar protein pada yogurt kemasan.
1.3 Manfaat Percobaan
- Mengetahui kadar protein yang terdapat di dalam yogurt kemasan apakah sesuai dengan Standar Nasional Indonesia (SNI).
BAB II
TINJAUAN PUSTAKA
2.1 Susu
Susu merupakan bahan makanan yang sangat penting untuk kebutuhan manusia, karena mengandung zat yang sangat diperlukan oleh tubuh, seperti protein, karbohidrat, lemak, vitamin dan mineral. Kecuali susu merupakan bahan asal untuk produk olahan susu, seperti susu kental manis, susu bubuk, susu skim,
butter, ice cream, keju, yogurt dan lain-lain. Susu mudah rusak oleh lingkungan, baik oleh temperatur udara ataupun udara sekitarnya, sehingga perlu perhatian khusus untuk penanganan pada waktu pemerahan ataupun sesudah pemerahan agar diperoleh susu yang berkualitas baik, memenuhi standar susu yang telah ditentukan dan masih layak dikonsumsi (Soeparno, 2011).
2.2 Yogurt
Menurut SNI 01– 2981–1992, yogurt adalah produk yang diperoleh dari susu yang telah dipasteurisasi kemudian difermentasikan dengan bakteri tertentu sampai diperoleh keasaman, bau, dan rasa yang khas, dengan atau tanpa penambahan bahan lain yang diizinkan.
Yogurt secara komersial diproduksi di era tahun 1970-an. Konsumsi yogurt sejak tahun 1975 semakin meningkat dan menjadi bisnis besar. Pada tahun 1975, konsumsi yogurt di Inggris telah mencapai 23 ml/orang per minggu. Konsumsi yogurt di Amerika Serikat meningkat 4,5 kali lipat dalam kurun waktu 10 tahun, dari tahun 1970 sampai tahun 1980 (Wahyudi dan Samsundari, 2008).
hasil penelitian Carter dan Collin pada tahun 1978. Hasil penelitian ini menunjukkan bahwa dengan infeksi 10 sel Salmonella enteridis dapat membunuh marmot bebas mikroba, tetapi dibutuhkan 109 sel untuk membunuh marmot normal yang secara alami memiliki mikroba dalam saluran pencernaannya (Wahyudi dan Samsundari, 2008).
2.2.1 Sifat-Sifat Yogurt
Yogurt yang baik memiliki tekstur yang halus, lembut, konsisten dan tidak ada sineresis. Komposisi bahan baku dan formulasi yang tepat serta proses pengolahan yang benar dibutuhkan untuk menghasilkan yoghurt dengan tekstur dan konsistensi yang baik. Dewasa ini yoghurt telah mengalami perkembangan dalam proses pembuatannya sehingga menghasilkan yogurt dengan aroma dan citarasa yang semakin baik dan bervariasi. Citarasa khas pada yogurt disebabkan oleh terbentuknya asam laktat, asam asetat, karbonil, diasetil, dan asetaldehid (Widodo, 2002).
2.2.2 Komposisi Yogurt
Yogurt merupakan produk olahan susu dari hasil fermentasi dari Bakteri Asam Laktat (BAL) sebagai starter, yakni Streptococcus thermophilus dan
Lactobacillus bulgaricus yang hidup bersimbiosis. Lama proses fermantasi akan
berakibat pada turunnya pH yogurt dengan rasa asam yang khas, selain itu dihasilkan
asam asetat, asetal dehid, dan bahan lain yang mudah menguap. Komposisi yogurt secara adalah protein 4-6%, lemak 0,1-1%, laktosa 2-3%, asam laktat 0,6-1,3%, pH 3,8-4,6% (Susilorini dan Sawitri, 2007), vitamin A, vitamin B kompleks diantaranya vitamin B1 (tiamin), vitamin B2 (riboflavin), vitamin B3 (niasin),
2.2.3 Manfaat Yougrt
Yogurt bermanfaat bagi manusia sebagai makanan fungsional (probiotik), berfungsi meningkatkan gizi makanan, membantu pertumbuhan, membantu proses pencernaan, meningkatkan kekebalan tubuh, meningkatkan konsumsi vitamin B (termasuk vitamin B12), menyediakan asam lemak omega–3, enzim pencernaan, laktase dan asam laktat, serta dapat menyerang bakteri berbahaya dan sel kanker (Wahyudi dan Samsundari, 2008).
2.2.4 Syarat Mutu Yogurt
Menurut SNI 01–2981–1992, syarat mutu yogurt adalah sebagai berikut: Tabel 1. Syarat Mutu Yogurt
No. Kriteria Uji Satuan Persyaratan
1.
Bahan kering tanpa lemak, %, b/b Protein (N × 6,37), %, b/b
Abu
2.3 Protein
Protein adalah suatu polipeptida yang mempunyai bobot molekul yang sangat bervariasi, dari 5000 hingga lebih dari satu juta. Di samping berat molekul yang berbeda-beda, protein mempunyai sifat yang berbeda-beda pula. Ada protein yang mudah larut dalam air, tetapi ada juga yang sukar larut dalam air (Poedjiadi dan Supriyanti, 2006).
2.3.1 Penggolongan Protein
Protein adalah molekul yang sangat vital untuk organisme dan terdapat di semua sel. Protein merupakan polimer yang disusun oleh 20 macam asam amino standar. Rantai asam amino dihubungkan dengan ikatan kovalen yang spesifik. Struktur & fungsi ditentukan oleh kombinasi, jumlah dan urutan asam amino sedangkan sifat fisik dan kimiawi dipengaruhi oleh asam amino penyusunnya. Penggolongan protein berdasarkan strukturnya ada empat macam, yaitu struktur primer, sekunder, tersier dan kuarterner.
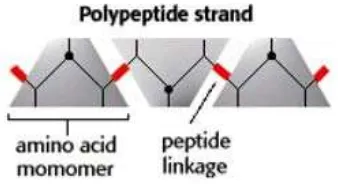
Struktur primer (struktur utama), terdiri dari asam-asam amino yang dihubungkan satu sama lain secara kovalen melalui ikatan peptida.
Gambar 1. Struktur Primer Protein
pada orientasi ikatan hidrogennya. Ada dua jenis struktur sekunder, yaitu: α-heliks dan β-sheet.
Gambar 2. Struktur Sekunder Protein α-Heliks (A) dan β-Sheet (B)
Struktur tersier, terbentuk karena adanya pelipatan membentuk struktur yang kompleks. Pelipatan distabilkan oleh ikatan hidrogen, ikatan disulfida, interaksi ionik, ikatan hidrofobik, ikatan hidrofilik.
Gambar 3. Struktur Tersier Protein
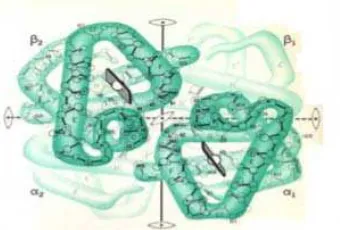
Struktur kuartener, terbentuk dari beberapa bentuk tersier, dengan kata lain multi sub unit. Interaksi intermolekul antar sub unit protein ini membentuk struktur keempat/kuartener.
2.3.2 Sifat-Sifat Protein
Berat molekul protein sangat besar, ribuan sampai jutaan, sehingga merupakan suatu makromolekul. Seperti senyawa polmer lain (misalnya: pati), protein dapat pula dihidrolisis oleh asam, basa, atau enzim tertentu dan menghasilkan campuran asam-asam amino (Yazid dan Nursanti, 2006).
Sifat fisikokimia protein berbeda satu sama lain, tergantung pada komposisi dan jenis asam amino penyusunnya. Sebagian besar protein bila dilarutkan dalam air akan membentuk dispersi koloidal dan tidak dapat berdifusi bila dilewatkan melalui membran semipermeabel. Beberapa protein mudah larut dalam air, tetapi ada pula yang sukar larut. Namun, semua protein tidak dapat larut dalam pelarut organik, seperti eter, klorofom, atau benzena (Yazid dan Nursanti, 2006).
Pada umumnya, protein sangat peka terhadap pengaruh-pengaruh fisik dan zat kimia, sehingga mudah mengalami perubahan bentuk. Perubahan atau modifikasi pada struktur molekul protein disebut denaturasi. Hal-hal yang dapat menyebabkan terjadinya denaturasi adalah panas, pH, tekanan, aliran listrik, dan adanya bahan kimia seperti urea, alkohol, atau sabun. Proses denaturasi terkadang berlangsung secara reversible, tetapi ada pula yang irreversible, tergantung pada penyebabnya. Protein yang mengalami denaturasi akan menurunkan aktivitas biologinya dan berkurang kelarutannya, sehingga mudah mengendap (Yazid dan Nursanti, 2006).
protein akan bereaksi dengan ion H+, sehingga protein bermuatan positif. Sebaliknya, dalam larutan basa, gugus karboksilat bereaksi dengan ion OH–, sehingga protein bermuatan negatif. Adanya muatan pada molekul protein menyebabkan protein bergerak di bawah pengaruh medan listrik (Yazid dan Nursanti, 2006).
Setiap jenis protein dalam larutan mempunyai pH tertentu yang disebut titik isoelektrik (TI). Pada pH isoelektrik (pI), molekul protein mempunyai muatan positif dan negatif yang sama, sehingga saling menetralkan atau bermuatan nol. Akibatnya, protein tidak bergerak di bawah pengaruh medan listrik. Pada titik isoelektris, protein akan mengalami pengendapan atau pemurnian suatu protein (Yazid dan Nursanti, 2006).
2.3.3 Manfaat Protein
Menurut (Priyani dan Mizawarti, 2006), protein berfungsi sebagai berikut: 1. Sebagai enzim yang mengkatalisis semua reaksi kimia dalam metabolisme 2. Sebagai regulator untuk aktivitas enzim (merupakan komponen dari enzim)
ataupun sebagai messanger kimia dalam hormon maupun reseptor untuk hormon tersebut
3. Berperan dalam transpor berbagai senyawa penting, seperti ion logam, O2, glukosa, lipid dan lain-lain
4. Berperan dalam gerak, seperti kontraksi serabut otot ataupun gerakan mekanis dalam pemisahan kromosom selama proses pembelahan sel
5. Dibutuhkan untuk fungsi sensor, rhodopsin, protein dalam retina, diperlukan dalam proses sel saraf
7. Bagian struktural yang memberikan sifat karakteristik kuat, keras seperti kolagen yang merupakan penyusun tulang, tendon, maupun ligamen.
2.4 Akibat Kekurangan dan Kelebihan Protein 2.4.1 Akibat Kekurangan Protein
1. Kwashiorkor
Istilah “kwashiorkor” pertama kali diperkenalkan oleh Dr. Cecily Wiliams pada tahun 1993 di Ghana, Afrika. Penyakit ini lebih banyak terdapat pada usia dua hingga tiga tahun yang komposisi gizi makanannya tidak seimbang, terutama dalam hal protein (Yuniastuti, 2008).
Menurut (Widodo, 2009 dan Ellya, 2010), gejala penyakit kwashiorkor adalah sebagai berikut:
a. Pertumbuhan terhambat b. Otot-otot berkurang dan lemah
c. Pembengkakan (edema) terutama pada perut (pembesaran hati), kaki dan tangan
d. Muka bulat seperti bulan (moonface) e. Gangguan psikomotorik
f. Nafsu makan berkurang
g. Rambut halus, jarang dan pirang kemerahan kusam
h. Kulit tampak kering (xerosis) dan memberi kesan kasar dengan garis-garis permukaan yang jelas
2. Marasmus
Marasmus berasal dari kata Yunani yang berarti wasting (merusak). Marasmus umumnya merupakan penyakit pada bayi (12 bulan pertama) karena terlambat diberi makanan tambahan. Merasmus adalah penyakit kelaparan, banyak terdapat diantara kelompok sosial ekonomi rendah di sebagian besar negara sedang berkembang dan lebih banyak dari kwashiorkor (Yuniastuti, 2008).
Menurut (Widodo, 2009), gejala penyakit kwashiorkor adalah sebagai berikut:
a. Pertumbuhan yang terhambat b. Lemak dibawah kulit berkurang c. Otot-otot berkurang dan melemah d. Muka seperti orang tua (Oldman’s face) 2.4.2 Akibat Kelebihan Protein
Jika terlalu berlebihan mengkonsumsi protein, maka dapat memberatkan ginjal dan hati yang harus memetabolisme dan mengeluarkan kelebihan nitrogen dan juga dapat menyebabkan asidosis, dehidrasi, diare, kenaikan amonia darah, kenaikan ureum darah, dan demam. Makanan yang tinggi proteinnya biasanya tinggi lemak sehingga menyebabkan obesitas, maka diet protein tinggi dianjurkan untuk menurunkan berat badan (Ellya, 2010).
2.5 Analisis Protein 2.5.1 Analisis Kualitatif
1. Reaksi Xantoprotein
Larutan asam nitrat pekat ditambahkan dengan hati-hati ke dalam larutan protein. Setelah dicampur terjadi endapan putih yang dapat berubah menjadi kuning apabila dipanaskan. Reaksi yang terjadi ialah nitrasi pada inti benzena yang terdapat pada molekul protein. Reaksi ini positif untuk protein yang mengandung tirosin, fenilalanin dan triptofan.
2. Reaksi Hopkins-Cole
Larutan protein yang mengandung triptofan dapat direaksikan dengan pereaksi Hopkins-Cole yang mengandung asam glioksilat. Pereaksi ini dibuat dari asam oksalat dengan serbuk magnesium dalam air. Setelah dicampur dengan pereaksi Hopkins-Cole, asam sulfat dituangkan perlahan-lahan sehingga membentuk lapisan di bawah larutan protein. Beberapa saat kemudian akan terjadi cincin ungu pada batas antara kedua lapisan tersebut. 3. Reaksi Millon
Pereaksi Millon adalah larutan merkuro dan merkuri nitrat dalam asam nitrat. Apabila pereaksi ini ditambahkan pada larutan protein, akan menghasilkan endapan putih yang dapat berubah menjadi merah oleh pemanasan. Pada dasarnya reaksi ini positif untuk fenol-fenol, karena terbentuknya senyawa merkuri dengan gugus hidroksifenil yang berwarna. 4. Reaksi Natriumnitroprusida
2.5.2 Analisis Kuantitatif
Menurut (Sudarmadji, dkk., 1989), metode analisis kuantitatif protein, yaitu: 1. Metode Lowry
Konsentrasi protein diukur berdasarkan Optical Density (OD) pada panjang gelombang 600 nm. Untuk mengetahui banyaknya proteindalam larutan, lebih dahulu dibuat kurva standar yang melukiskan hubungan antara konsentrasi dengan OD (absorbansi). Larutan Lowry ada dua macam, yaitu Lowry A yang terdiri dari fosfotungstat-fosfomolibdat (1:1) dan Lowry B yang terdiri dari natrium karbonat (Na2CO3) 2% dalam natrium hidroksida (NaOH) 0,1 N, cupri sulfat (CuSO4) dan natrium kalium tartrat (Na-K-tartrat) 2%. Cara penentuannya adalah 1 ml larutan protein ditambahkan 5 ml Lowry B, dikocok dan didiamkan selama 10 menit. Kemudian ditambah 0,5 ml Lowry A, dikocok dan didiamkan selama 20 menit. Selanjutnya, diamati absorbansinya pada panjang gelombang 600 nm.
2. Metode Spektrofotometer UV
Sebagian besar protein mengabsorbansi sinar ultraviolet maksimum pada panjang gelombang 280 nm. Hal ini terutama oleh adanya asam amino tiroosin, triptophan, dan fenilalanin yang ada pada protein tersebut. Pengukuran protein berdasarkan absorbansi sinar UV adalah cepat, mudah, dan tidak merusak bahan.
3. Metode Turbidimetri atau Kekeruhan
kekeruhan diukur dengan alat Turbidimeter. Cara ini hanya dipakai untuk bahan protein yang berupa larutan, tetapi biasanya hasilnya kurang tepat, sehingga jarang dipakai untuk penetapan kadar protein.
4. Metode Pengecatan
Beberapa bahan pewarna, misalnya orange G, orange 12 dan amido black dapat membentuk senyawa berwarna dengan protein dan menjadi tidak larut. Dengan mengukur sisa bahan pewarna yang tidak bereaksi dalam larutan (dengan kolorimeter), maka jumlah protein dapat ditentukan dengan cepat.
5. Titrasi Formol
Larutan protein dinetralkan dengan basa (NaOH), kemudian ditambahkan formalin akan membentuk dimenthiol. Dengan terbentuknya dimenthiol, ini berarti gugus aminonya sudah terikat dan tidak akan mempengaruhi reaksi antara asam (gugus karboksil) dengan basa (NaOH) sehingga akhir titrasi dapat diakhiri dengan tepat. Indikator yang digunakan adalah fenolftalein, akhir titrasi bila tepat terjadi perubahan warna menjadi merah muda yang tidak hilang dalam 30 menit. Titrasi formol ini hanya tepat untuk menentukan suatu proses terjadinya pemecahan protein dan kurang tepat untuk penentuan protein.
6. Metode Kjeldahl
maupun proses pengolahan lain yang biasa dilakukan pada makanan. Metode ini digunakan untuk menganalisis kadar protein kasar dalam bahan makanan secara tidak langsung karena senyawa yang dianalisisnya adalah kadar nitrogennya. Dengan mengalikan hasil analisis tersebut dengan faktor konversi 6,25, diperoleh nilai protein dalam bahan uji tersebut.
Penentuan kadar protein dengan metode ini memiliki kelemahan karena adanya senyawa lain yang bukan protein yang mengandung N akan terdeteksi sehingga kadar protein yang diperoleh langsung dengan metode Kjeldahl ini disebut dengan kadar protein kasar (Crude Proteint).
Menurut (Bintang, 2010; Yazid dan Nursanti, 2006), metode Kjeldahl dilakukan dengan beberapa tahapan kerja, yaitu:
a. Tahap Destruksi
Pada tahap ini sampel dipanaskan dengan asam sulfat (H2SO4) pekat sehingga terjadi destruksi menjadi unsur-unsur, diamana seluruh nitrogen (N) organik diubah menjadi N anorganik, yaitu elemen karbon (C) teroksidasi menjadi karbon dioksida (CO2) dan hidrogen (H) teroksidasi menjadi air (H2O), sedangkan elemen nitrogennya akan berubah menjadi amonium sulfat [(NH4)2SO4]. Asam sulfat yang dipergunakan untuk destruksi harus dalam jumlah yang cukup dan diperhitungkan untuk dapat mengurai bahan protein, lemak, dan karbohidrat di dalam sampel.
maka titik didih asam sulfat akan ditinggikan sehingga proses destruksi akan berjalan dengan cepat. Tiap satu gram kalium sulfat akan mampu meningkatkan titik didih asam sulfat 30C. Suhu destruksi berkisar antara 3700 – 4100C. Proses destruksi diakhiri jika larutan telah menjadi warna hijau jernih.
Reaksi yang terjadi proses destruksi adalah:
Protein + H2SO4 (NH4)2SO4 + CO2↑ + SO2↑ + H2O↑
b. Tahap Destilasi
Pada tahap ini, amonium sulfat [(NH4)2SO4] yang terbentuk pada setiap tahap destruksi dipecah menjadi amonia (NH3) dengan penambahan NaOH sampai alkalis dan dipanaskan. Amonia yang dibebaskan selanjutnya akan ditangkap oleh larutan baku asam. Larutan baku asam yang dipakai adalah asam sulfat. Agar kontak antara asam dan amonia berjalan sempurna, maka ujung selang pengalir destilat harus tercelup ke dalam larutan asam. Destilasi diakhiri bila semua amonia terdestilasi sempurna yang ditandai dengan destilasi tidak bereaksi basa.
Reaksi yang terjadi pada tahap destilasi:
(NH4)2SO4 + 2 NaOH Na2SO4 + 2 H2O + 2 NH3↑
c. Tahap Titrasi
Penampung destilat yang digunakan adalah asam sulfat berlebih, maka sisa asam sulfat yang tidak bereaksi dengan amonia dititrasi dengan NaOH 0,1 N menggunakan indikator Mengsel. Titik akhir
titrasi dapat ditandai dengan perubahan warna dari warna ungu menjadi hijau.
Rekasi yang terjadi pada tahap titrasi: NH3 + H2SO4 (NH4)2SO4
Kelebihan H2SO4 + 2 NaOH Na2SO4 + 2 H2O Kadar protein dihitung dengan persamaan berikut:
������������ (%) = ��������
� × 100%
Fk = Faktor konversi atau perkalian = 6,25
BAB III
METODE PENGUJIAN
3.1 Tempat Pengujian
Pengujian Penetapan Kadar Protein pada Yogurt Kemasan dengan Metode Kjeldahl dilakukan di Badan Riset Standardisasi (Baristand) Industri Medan yang berada di Jalan Sisingamangaraja No. 24 Medan.
3.2 Alat dan Bahan 3.2.1 Alat
Alat-alat yang digunakan adalah alat penyulingan dan kelengkapannya, batu didih, buret, corong, erlenmeyer 250 ml, gelas ukur, labu Kjedahl 100 ml, labu ukur 100 ml, labu destilasi, neraca analitik, pembakar, pipet tetes, dan pipet volume 25 ml.
3.2.2 Bahan
Bahan yang digunakan adalah 3 botol Yogurt Kemasan. 3.3 Pereaksi
Pereaksi yang digunakan adalah bubuk campuran selen, HCl 0,01 N, NaOH 40 %, indikator campuran (mengsel), H2SO4 pekat, larutan asam borat 2%.
3.4 Prosedur
- Ditimbang seksama 0,51 g cuplikan, dimasukkan ke dalam labu Kjeldahl 100 ml
- Ditambahkan 2 g campuran selen dan 25 ml H2SO4 pekat.
- Didinginkan, kemudian dimasukkan ke dalam labu ukur 100 ml, ditambah dengan air suling dan ditepatkan sampai tanda garis.
- Dipipet 5 ml larutan dan dimasukkan ke dalam labu destilasi, ditambahkan 5 ml NaOH 40%.
- Disuling selama lebih kurang 10 menit, sebagai penampung gunakan 10 ml larutan asam borat 2% yang telah dicampur indikator.
- Dibilas ujung pendingin dengan air suling. - Dititer dengan larutan HCl 0,01 N.
Perhitungan:
������������= ��������
� × 100%
Dimana: N = Normalitas HCl (0,1069 N)
V = Volume HCl yang digunakan untuk titrasi (ml) BE= Berat ekivalen HCl
Fp = Faktor pengencer (100/25 = 4) Fk = Faktor konversi (6,25)
3.5 Flowshet
← Dimasukkan ke dalam labu Kjeldahl 100 ml ← Ditambahkan 2 g campuran selen dan 25 ml H2SO4
pekat
← Dipanaskan di api pembakar sampai mendidih (±2 jam)
← Didiamkan hingga dingin
← Dimasukkan ke dalam labu ukur 100 ml ← Diencerkan dengan air suling
← Ditepatkan sampai tanda garis ← Dipipet 5 ml larutan
← Dimasukkan ke dalam alat penyuling ← Ditambahkan 5 ml NaOH 40%
← Disuling selama lebih kurang 10 menit, sebagai
penampung gunakan 10 ml larutan asam borat 2% yang telah dicampur indikator
← Dibilas ujung pendingin dengan air suling
← Dititer dengan larutan HCl 0,01 N ← Dihitung kadar protein (%)
0,51 g yogurt
Larutan Jernih Kehijau-hijauan
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil
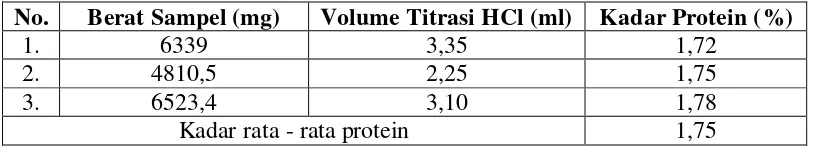
Berdasarkan penelitian yang telah dilakukan, didapatkan kadar protein dari 3 botol yogurt kemasan masing-masing adalah 1,72 %, 1,75%, dan 1,78 % seperti dalam tabel 2 dan perhitungan pada lampiran halaman 25.
4.2. Pembahasan
Dari data yang diperoleh kadar protein pada yogurt kemasan X rata-rata sebesar 1,75%. Menurut SNI 01– 2981–1992, dinyatakan kadar protein pada yogurt kemasan adalah minimal 3,5%. Ini berarti yogurt kemasan X tidak memenuhi syarat Standar Nasional Indonesia (SNI).
Kadar protein yogurt sangat ditentukan oleh kualitas bahan dasarnya, yaitu susu, semakin tinggi kadar protein susu semakin baik kualitas yogurt yang dihasilkannya. Oleh karena itu, perlu peningkatan kadar protein susu melalui pemberian pakan yang berkualitas terhadap ternak sapi perah dan sistem pengolahan yogurt itu sendiri (Askar dan Sugiarto, 2005).
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
- Hasil yang diperoleh, kadar protein yogurt kemasan satu adalah 1,72 %, kemasan kedua 1,75 %, kemasan ketiga 1,78 % dengan kadar rata-rata sebesar 1,75%. Kadar protein yang diperoleh tidak sesuai dengan SNI 01– 2981–1992, dimana persyaratan kadar protein yogurt dinyatakan minimal 3,5%
- Kadar protein yogurt sangat ditentukan oleh kualitas bahan dasarnya, yaitu susu. Semakin tinggi kadar protein susu, semakin baik kualitas yogurt yang dihasilkannya.
5.2 Saran
DAFTAR PUSTAKA
Askar, S. dan Sugiarto. (2005). Prosiding Temu Teknis Nasional Tenaga Fungsional Pertanian 2005. Uji Kimiawi dan Organoleptik Sebagai Uji Mutu Yoghurt. Hal. 108 – 110.
Bintang, M. (2010). Biokimia Teknik Penelitian. Jakarta: Erlangga. Hal. 100; 108– 110.
Budianto, A. K. (2009). Dasar-Dasar Ilmu Gizi. Cetakan Keempat. Malang: UMM Press. Hal. 55 – 63.
Cahyadi, W. (2005). Bahan Tambahan Pangan. Jakarta: PT. Bumi Aksara. Hal. 67-74.
Ellya, E. S. (2010). Gizi Dalam Kesehatan Reproduksi. Jakarta: Trans Info Media. Hal. 30 – 42.
Poedjiadi, A., dan Supriyanti, F.M. T. (2006). Dasar-Dasar Biokimia. Jakarta: UI Press. Hal. 81; 109 – 122.
Priyani. dan Mizawarti. (2006). Buku Ajar: Biokimia.Medan: Departemen Biologi USU. Halaman 72.
Soedarmadji, S., Haryono, B., dan Suhardi. (1989). Analisa Bahan Makanan dan Pertanian. Yogyakarta: Penerbit Liberty. Hal. 119 – 144.
Soeparno, Rihastuti, R.A, Indratiningsih, Triatmojo, S. (2011). Dasar Teknologi Hasil Ternak. Yogyakarta: Gadjah Mada University Press. Hal. 43 – 66. Usmiati, S dan Abubakar. (2009). Teknologi Pengolahan Susu.Balai Bogor:
Besar Penelitian dan Pengembangan Pascapanen Pertanian. Hal. 20 – 21. Sunarlim, R dan Usmiati, S. (2008).Balai Besar Penelitian dan Pengembangan
Pascapanen Pertanian. Kombinasi Beberapa Bakteri Asam Laktat Terhadap Karakteristik Yogurt. Hal. 331.
Wahyudi, A., dan Samsundari, S. (2008). Bugar Dengan Susu Fermentasi. Malang: UMM Press. Hal. 9 – 14.
Widodo, R. (2009). Pemberian Makanan Suplemen dan Obat Pada Anak. Jakarta: Buku Kedokteran EGC. Hal. 21 – 25.
Yazid, E., dan Nursanti, L. (2006). Penuntun Praktikum Biokimia untuk Mahasiswa Analis. Yogyakarta: Penerbit Andi. Hal. 66 – 68.
LAMPIRAN
Lampiran1. Identitas Sampel
Nama Sampel : Cimory Yogurt Drink Lychee Wadah/Kemasan : Botol / 250 ml
Pabrik : PT. Cisarua Mountain Dairy
Komposisi : Susu sapi segar, air, gula, sari buah leci, penstabil nabati, perisa identik alami leci, kultur Streptococcus thermophillus dan Lactobacillus delbrueckii subsp.
Bulgaricus, pewarna Karmin Cl No. 75470 Waktu daluarsa : 30 Mei 2014
Lampiran 2. Data Hasil dan Perhitungan Tabel 2. Data Hasil
No. Berat Sampel (mg) Volume Titrasi HCl (ml) Kadar Protein (%)
Lampiran 3. Gambar Proses Penetepan Kadar
Gambar 1. Penambahan campuran Gambar 2. Tahap Destruksi
selen dan H2SO4 pekat
Gambar 3. Sampel didinginkan Gambar 4. Diencerkan dengan air
suling