1
PENETAPAN KADAR OKTIL METOKSISINAMAT DALAM
LOSIO DENGAN METODE KROMATOGRAFI CAIR
KINERJA TINGGI (KCKT)
TUGAS AKHIR
Oleh:
MUHAMMAD SYAHRUM HARAHAP
NIM 122410010
PROGRAM STUDI
DIPLOMA III ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2
KATA PENGANTAR
Puji dan syukur kehadirat Allah yang Maha Kuasa yang telah
melimpahkan rahmat, karunia, dan ridhoNya, sehingga penulis dapat
menyelesaikan tugas akhir yang berjudul “Penetapan Kadar Oktil Metoksi
Sinamat Dalam Lusio Dengan Metode Kromatografi Cair Kinerja Tinggi
(KCKT)”. Tugas Akhir ini diajukan sebagai salah satu syarat untuk memperoleh
gelar ahlimadya pada program Diploma III Analis Farmasi dan Makanan pada
Fakultas Farmasi Universitas Sumatera Utara.
Selama penulisan Tugas Akhir ini, penulis banyak mendapat bimbingan
dan bantuan dari berbagai pihak, maka dalam kesempatan ini penulis
mengucapkan terima kasih yang setulus-tulusnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi USU.
2. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program
Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi USU.
3. Ibu Dra. Sudarmi, M.Si.,Apt., selaku dosen pembimbing yang telah
memberikan pengarahan dan bimbingan kepada penulis dengan penuh
perhatian hingga selesainya Tugas Akhir ini.
4. Bapak Drs. Awaluddin Saragih M.Si., Apt., selaku Dosen Pembimbing
Akademik penulis selama melaksanakan pendidikan pada Program
3
5. Ibu Lambok Okta SR, M.Kes., Apt., selaku Manager Mutu di Balai Besar
POM Medan, yang memberikan izin tempat pelaksanaan Praktek Kerja
Lapangan.
6. Kakak Fanny Annita Raprap, S.Si., Apt., selaku Penanggung jawab
Laboratorium Kosmetik di Balai Besar POM Medan yang telah membantu
penulis selama menjalani Praktek Kerja Lapangan.
7. Kakak penulis Sri Belia, yang selalu memberikan nasehat dan kasih
sayang kepada penulis.
8. Sahabat-sahabat terbaik penulis, Sahrum,Amin,Dian,Vegi,Nana yang
selalu semangat dan selalu menghibur penulis setiap saat.
Dan terkhusus ucapan terima kasih kepada orang tua penulis bapak Husni
Harahap dan ibu Nurhadiah yang tercinta yang telah memberikan do’a restu
kepada penulis dalam menyelesaikan tugas akhir ini.
Penulis menyadari dalam tugas akhir ini masih banyak kekurangan dan
ketidaksempurnaan. Dengan segala kerendahan hati penulis mengharapkan saran
dan kritik yang bersifat membangun yang pada akhirnya dapat digunakan untuk
menambah pengetahuan dan berguna bagi kita semua. Akhir kata semoga Allah
SWT melimpahkan rahmat dan karuni-Nya untuk kita semua, Amin.
Medan, Juni 2015
Penulis,
4
BAB II TINJAUAN PUSTAKA 2.1 Lotio ... 3
2.5.1 Klasifikasi Kromatografi Cair Kinerja Tinggi ... 9
5
BAB IV HASIL DAN PEMBAHASAN 4.1 Hasil ... 20
4.2 Pembahasan ... 21
BAB V KESIMPULAN DAN SARAN 5.1 Kesimpulan ... 22
5.2 Saran ... 22
6
DAFTAR LAMPIRAN
Lampiran 1. Gambar alat Kromatografi Cair Kinerja Tinggi
(KCKT) ... 25
Lampiran 2. Gambar Alat Ultrasonic Cleaner dan Sampel Herborist ... 26
Lampiran 3. Neraca Mikro, Neraca Analitik ... 27
Lampiran 4. Kromatogram Larutan Baku Oktil Metoksisinamat ... 28
Lampiran 5. Kromatogram Larutan Uji Oktil Metoksisinamat ... 29
Lampiran 6. Perhitungan Penetapan kadar oktil Metoksisinamat ... .. 30
BAB I PENDAHULUAN
1.1 Latar Belakang
Kosmetik dikenal manusia sejak berabad-abad yang lalu. Pada abad ke 19,
pemakaian kosmetik mulai mendapat perhatian, yaitu selain untuk kecantikan juga
untuk kesehatan. Perkembangan ilmu kosmetik serta industrinya baru dimulai
secara besar-besaran pada abad ke-20. Kosmetik menjadi salah satu bagian dunia
usaaha. Bahkan sekarang teknologi kosmetik begitu maju dan merupakan paduan
antara kosmetik dan obat (pharmaceutical) atau yang disebut dengan kosmetik
medik (cosmeceuticals) (Tranggono dan Latifah 2007).
Losio adalah produk kosmetik yang umumnya berupa emulsi, terdiri dari
sedikitnya dua cairan yang tidak tercampur dan mempunyai viskositas rendah
serta dapat mengalir dibawah pengaruh gravitasi. Proses pembuatan losion adalah
bahan-7
bahan yang larut dalam fase lemak, dengan cara pemanasan dan pengadukan.
Losion merupakan campuran dari air, alkohol, emolien, humektan, bahan
pengental, bahan pengawet dan bahan pewangi (Mitsui, 1997).
Kulit merupakan suatu organ besar yang berlapis-lapis, dimana pada orang
dewasa beratnya kira-kira delapan pon, tidak termasuk lemak. Kuit menutupi
permukaan lebih dari 20.000 cm² dan mempunyai bermacam-macam fungsi dan
kegunaan. Kulit berfungsi sebagai pembatas terhadap serangan fisika dan kimia,
termostat dalam mempertahankan suhu tubuh,melindungi tubuh dari serangan
mikroorganisme, sinar ultraviolet, dan berperan dalam mengatur tekanan darah
(Lachman, dkk.,1994).
Banyak produk kosmetik yang mengandung tabir surya yang beredar di
masyarakat. Ada yang berupa zat tunggal maupun campuran. Salah satu contoh
campurannya adalah Oktil metoksisinamat dan oksibenzon. Metode resmi untuk
penetapan kadar campuran kedua senyawa tersebut belum ada, padahal dalam
industri kosmetik sangat dibutuhkan metode analisa yang cepat dan memenuhi
persyaratan kesahihan yang ditetapkan. Oleh karena itu, diperlukan metode
Kromatografi Cair Kinerja Tinggi (KCKT) yang memiliki daya pisah, ketepatan
dan ketelitian yang tinggi untuk menetapkan kadar masing-masing senyawa dalam
campuran tersebut (christine P, 2005).
8
Adapun tujuan dari penetapan kadar Oktil Metoksisinamat dalam sediaan
Losio adalah untuk mengetahui apakah kadar Oktil Metoksisinamat dalam sediaan
Losio memenuhi persyaratan yang dipersyaratkan MA PPOMN 15/KO/01.
1.3 Manfaat
Manfaat yang diperoleh dari penetapan kadar Oktil Metoksisinamat dalam
sediaan Lusio adalah agar dapat mengetahui bahwa sediaan Lusio oktil
metoksisinamat yang beredar di pasaran memenuhi persyaratan yang
dipersyaratkan MA PPOMN 15/KO/01 sehingga baik untuk digunakan.
BAB II
TINJAUAN PUSTAKA
2.1 Lotio
Lotio merupakan preparat cair yang dimaksudkanuntuk pemakaian luar
pada kulit. Kebanyakan lutio mengandung bahan serbuk halus yang tidak larut
dalam media dispersi dan disuspensikan dengan menggunakan zat pensuspensi
dan zat pendispersi. Lotio lain sebagai bahan cair fase terdispersi yang tidak
bercampur dengan bahan pembawa dan biasanya menyebar dengan bantuan zat
pengemulsi atau bahan penstabil lain yang sesuai (Ansel, HC 1989).
Pada umumnya pembawa dari lotio adalah air. Lotio dimaksudkan untuk
digunakan pada kulit sebagai pelindung atau untuk obat karena sifat
9
permukaan kulit yang luas. Lotio dimaksudkan segera kering pada kulit setelah
pemakaian dan meninggalkan lapisan tipis dari komponen obat pada permukaan
kulit (Ansel, HC 1989).
2.1.1 Pembagian Lotio berdasarkan fungsinya
1. Hand and body lotion, yaitu lotion pelembab untuk melembutkan dan
menghaluskan kulit tubuh dan tangan.
2. Sun block lotion, yaitu lotion untuk mengatasi sengatan sinar matahari.
Terlalu lama terkena terik matahari, akan mengakibatkan warna kulit
berubah suram kecoklatan, kulit menjadi kering dan mempercepat penuaan
kulit. (Anonim, 2015)
2.2 Oktil Metoksisinamat
Struktur Oktil Metoksisinamat:
Titik lebur : -25˚ C (-13˚ F)
Deskripsi :Cairan Kental,jernih;berwarna kuning pucat;bau khas lemah
Kelarutan :Larut dalam etanol, Minyak mineral, minyak silikon.Tak larut
dalam Air, gliserin, propilen glikol
Stabilitas :Waktu penyimpanan minimum dua tahun dalam kemasan asli
Bersegel
Indeks bias :1,539 dan 1,550
Penyimpanan :Simpan didalam wadah bertutup rapat terlindungi dari cahaya.
10
(Anonim,1998 dan Depkes RI 1993).
Dua etilheksil 4 metoksisinamat juga dikenal sebagai Oktil
Metoksisinamat. Senyawa kimia dari golongan sinamat ini menyerap cahaya
dengan panjang gelombang 290 nm- 320 nm didalam cakupan cakupan
Ultraviolet B.Meskipun kita tidak dapat melihat sinar Ultraviolet, ia adalah bagian
dari spektrum sinar matahari, sehingga kita terpapar oleh nya setiap
hari.Ultraviolet adalah komponen cahaya yang menyebabkan keratosis
(pencoklatan), eritema (kemerahan), kulit terbakar dan melanoma.Hal ini
disebabkan panjang gelombang Ultraviolet lebih pendek dari pada panjang
gelombang sinar tampak ,sehingga memiliki energi lebih tinggi menyebabkan
dapat membakar kulit (Anonim,1998).
Sinar Ultraviolet dikategorikan kedalam tiga bagian utama panjang
gelombang sinar Ultraviolet lebih pendek dari pada spektrum sinar tampak dan
Ultravioet C adalah yang terpendek.juga yang paling berbahaya.Panjang
gelombang Ultraviolet C berada diantara 100 nm sampai 290 nm, dan untung saja
lapisan ozon menjaga permukaan bumi dari paparan Ultraviolet C,Ultraviolet B
yang bertanggung jawab terhadap kulit terbakar,memiliki kisaran panjang
gelombang 290 nm-320 nmn.para ilmuan belum menemukan efek dari sinar
Ultraviolet A terhadap kesehatan tetapi diduga bahwa Ultraviolet A mungkin
adalah agen penyebab kanker.membutuhkan ribuan kali Ultraviolet A untuk
menyebabkan kerusakan kulit setara yang disebabkan Ultraviolet B. Panjang
gelombang Ultraviolet berada dikisaran 320 nm – 400 nm (Anonim,1998).
11
2.3 Tabir surya
Tabir surya merupakan suatu senyawa yang dapat digunakan untuk
melindungi kulit dari sengatan sinar matahari terutama ultra violet (UV). Untuk
melindungi kulit dari radiasi sinar UV maka dibuat kosmetika tabir surya yang
dapat menyerap sinar ultraviolet dari cahaya matahari secara efektif
(Shaath,1986).
Suatu tabir surya mengandung senyawa yang dapat melindungi kulit dari
pengaruh buruk sinar ultraviolet (UV) dimana mekanisme kerjanya dapat dibagi
menjadi dua yaitu secara fisik yaitu memantulkan dan membiaskan sinar UV yang
mengenai kulit dan secara kimia dengan cara menyerap sinar UV yang
dipancarkan matahari. Sinar UV adalah bagian dari sinar matahari yang
merupakan suatu gelombang elektromagnetik yang secara umum terbagi kedalam
3 kategori berdasarkan panjang gelombang, yaitu: UVA (320-400 nm), UVB
(280-320 nm), dan UVC (200-280 nm) (Prasiddha,2015).
Radiasi UV dalam jumlah kecil bermanfaat untuk sintesis vitamin D dalam
tubuh, tetapi paparan yang berlebihan dapat menyebabkan kulit terbakar dan efek
berbahayanya yaitu sintesis radikal bebas yang memicu eritema dan katarak. Saat
sinar UV menerpa suatu benda terus-menerus, elektron atom benda tersebut akan
meloncat dari orbitnya yang menyebabkan terbentuknya radikal bebas. Sinar UVB
juga dapat menyebabkan kerusakan fotokimia pada DNA sel sehingga memicu
pertumbuhan kanker kulit (Prasiddha,2015).
Senyawa dalam tabir surya mampu melindungi kulit karena adanya ikatan
12
terpapar sinar UV sehingga akan menurunkan energi dan bersifat melindungi
kulit. Contoh senyawa yang biasa digunakan dalam tabir surya antara lain:
turunan salisilat, turunan sinamat, phenylbenzimidazole sulfonic acid (PBSA).
Senyawa dari turunan alkil sinamat dalam tabir surya memiliki kemampuan dalam
menyerap sinar UV dikarenakan adanya ikatan konjugasi pada gugus fungsi
benzena dan gugus fungsi karbonil (Prasiddha,2015).
2.4 Kromatografi
Kromatografi pertama kali dikembangkan oleh seorang ahli botani Rusia
Michael Tswett pada tahun 1903 untuk memisahkan pigmen berwarna dalam
tanaman dengan cara perkolasi ekstrak petroleum eter dalam kolom gelas yang
berisi kalsium karbonat (Johnson dan Stevenson, 1991).
Teknik kromatografi telah berkembang dan telah digunakan untuk
memisahkan berbagai macam komponen yang kompleks,baik komponen organic
maupun komponen anorganik. Saat ini kromatografi merupakan teknik pemisahan
yang paling umum dan paling sering digunakan dalam bidang kimia untuk
melakukan analisis, baik analisis kualitatif, kuantitatif atau preparative dalam
bidang farmasi. (Gandjar dan Rohman, 2007).
2.4.1 Pembagian Kromatografi
Kromatografi dapat dibedakan atas berbagai macam, tergantung pada
13
dibedakan menjadi: (a) kromatografi adsorbsi; (b) kromatografi partisi; (c)
kromatografi pasangan ion; (d) kromatografi penukar ion (e) kromatografi
eksklusi ukuran dan (f) kromatografi afinitas (Rohman, 2009).
Berdasarkan alat yang digunakan, kromatografi dapat dibagi atas : (a)
kromatografi kertas; (b) kromatografi lapis tipis, yang keduanya sering disebut
kromatografi planar, (c) kromatografi cair kinerja tinggi (KCKT) dan (d)
kromatografi gas (KG). Bentuk kromatografi yang paling awal adalah
kromatografi kolom yang digunakan untuk pemisahan sampel dalam jumlah yang
besar (Rohman, 2009).
2.5 Kromatografi Cair Kinerja Tinggi
Kromatografi cair kinerja tinggi (KCKT) atau biasa juga disebut dengan
HPLC (High Perpormance Liquid Chromatography) dikembangkan pada akhir
tahun 1960-an dan awal tahun 1970-an. Saat ini, KCKT merupakan teknik
pemisahan yang diterima secara luas untuk analisis bahan obat (Rohman, 2009).
Kromatografi cair kinerja tinggi (KCKT) merupakan teknik yang mana
solute atau zat terlarut terpisah oleh perbedaan kecepatan elusi, dikarenakan
solute-solute ini melewati suatu kolom kromatografi. Pemisahan solute-solute ini
diatur oleh distribusi solute dalam fase gerak dan fase diam. Penggunaan
kromatografi cair secara sukses terhadap suatu masalah yang dihadapi
membutuhkan penggabungan secara tepat dari berbagai macam kondisi
operasional seperti jenis kolom, fase gerak, panjang dan diameter kolom,
kecepatan alir fase gerak, suhu kolom, dan ukuran sampel (Gandjar dan Rohman,
14
Kromatografi cair kinerja tinggi (KCKT) merupakan sistem pemisahan
dengan kecepatan dan efisiensi yang tinggi karena didukung oleh kemajuan dalam
teknologi kolom, sistem pompa tekanan tinggi, dan detektor yang sangat sensitif
dan beragam sehingga mampu menganalisa berbagai cuplikan secara kualitatif
maupun kuantitatif, baik dalam komponen tunggal maupun campuran (Ditjen
POM, 1995).
Kromatografi Cair Kinerja Tinggi merupakan jenis yang khusus dari
kromatografi kolom. Berbeda dengan kromatografi gas, metode ini menggunakan
cairan dengan tekanan tinggi sebagai fase mobil (fase gerak) sebagai pengganti
gas. Metode ini dapat dibedakan dari kromatografi kolom klasik oleh empat sifat
yang khas yaitu:
- Menggunakan kolom pendek untuk mempersingkat waktu.
- Menggunakan kolom sempit dengan diameter antara 1 sampai 3 mm,
untuk memungkinkan pemisahan dalam jumlah mikro.
- Ukuran partikel bahan sorbsi (penyerap) terletak dibawah 50 µm, hingga
akan tercapai suatu bilangan dasar teoritik yang tinggi.
- Pelarut elusi dialirkan kedalam kolom dengan tekanan untuk
mengkompensasikan tekanan arus di dalam kolom.
(Roth, 1998).
Menurut Synder (1979), banyak kelebihan metode kromatografi cair
kinerja tinggi dibandingkan dengan metode lainnya. Beberapa kelebihan
kromatografi cair kinerja tinggi antara lain:
15
2. Mudah melaksanakannya.
3. Kecepatan analisis dan kepekaan yang tinggi.
4. Dapat dihindari terjadinya dekomposisi/kerusakan bahan yang dianalisis.
5. Resolusi yang baik.
6. Dapat digunakan bermacam-macam detektor.
7. Kolom dapat dipergunakan kembali.
2.5.1 Klasifikasi Kromatografi Cair Kinerja Tinggi (KCKT)
Klasifikasi kromatografi cair kinerja tinggi (KCKT) berdasarkan pada sifat
fase diam yaitu:
a. Kromatografi Absorbsi
Pemisahan kromatografi adsorbsi menggunakan fase diam silika gel atau
alumina, meskipun demikian sekitar 90% kromatografi ini memakai silika gel
sebagai fase diamnya. Fase geraknya berupa pelarut non polar yang ditambah
dengan pelarut polar seperti air atau alkohol rantai pendek untuk meningkatkan
kemampuan elusinya sehingga tidak timbul pengekoran puncak, seperti n-heksana
ditambah metanol. Jenis KCKT ini sesuai untuk pemisahan-pemisahan campuran
isomer struktur dan untuk pemisahan solut dengan gugus fungsional yang berbeda
(Gandjar dan Rohman, 2007).
b. Kromatografi Partisi
Kromatografi jenis ini disebut juga dengan kromatografi fase terikat.
Kebanyakan fase diamnya adalah silika yang dimodifikasi secara kimiawi atau
fase terikat. Sejauh ini yang digunakan untuk memodifikasi silika adalah
16
dengan fenil. Fase diam yang paling populer digunakan adalah oktadesilsilana
(ODS atau C18) dan kebanyakan pemisahannya adalah dengan fase terbalik.
Sedangkan fase geraknya adalah campuran asetonitril atau metanol dengan air
atau dengan larutan buffer. (Gandjar dan Rohman, 2007).
Ditinjau dari jenis fase diam dan fase geraknya, maka kromatografi partisi
dapat dibedakan atas:
1. Kromatografi Fase Normal
Kromatografi fase normal (fase diam lebih polar daripada fase gerak),
kemampuan elusi meningkat dengan meningkatnya polaritas pelarut. Fase gerak
ini biasanya tidak polar. Dietil eter, benzen, hidrokarbon lurus seperti pentana,
heksana, heptana maupun iso-oktana sering digunakan. Halida alifatis seperti
diklorometana, dikloroetana, butilklorida dan kloroform juga digunakan.
Umumnya gas terlarut tidak menimbulkan masalah pada fase normal (Gandjar dan
Rohman, 2007).
2. Kromatografi Fase Terbalik
Kromatografi fase terbalik (fase diam kurang polar daripada fase gerak),
kemampuan elusi menurun dengan meningkatnya polaritas pelarut. Kandungan
utama fase gerak fase terbalik adalah air. Pelarut yang dapat campur dengan air
seperti metanol, etanol, asetonitril, dioksan, tetrahidrofuran dan dimetilformamida
ditambahkan untuk mengatur kepolaran fase gerak. Dapat ditambahkan pula asam,
basa, dapar dan/atau surfaktan. Mutu air harus tinggi baik air destilasi maupun air
mineral (Gandjar dan Rohman, 2007).
17
KCKT penukar ion menggunakan fase diam yang dapat menukar kation
atau anion dengan suatu fase gerak. Ada banyak penukar ion yang beredar di
pasaran, meskipun demikian yang paling luas penggunaanya adalah polistiren
resin (Gandjar dan Rohman, 2007).
Tehnik ini tergantung pada penukaran (adsorpsi) ion-ion diantara fase
gerak dan tempat-tempat berion dari kemasan. Kebanyakan resin-resin berasal
dari polimer stiren divinilbenzen dimana gugus-gugus fungsinya telah ditambah.
Resin-resin tipe asam sulfonat dan amin kuarterner merupakan jenis resin pilihan
paling baik dan banyak digunakan. Keduanya, fase terikat dan resin telah
digunakan. Tehnik ini dipakai secara luas dalam life sciences dan dikenal secara
khas untuk pemisahan asam-asam amino. Tehnik ini dapat dipakai untuk
keduanya, kation-kation dan anion-anion (Johnson dan Stevenson, 1991).
d. Kromatografi Eksklusi
Kromatografi ini disebut juga dengan kromatografi permiasi gel dan dapat
digunakan untuk memisahkan atau menganalisis senyawa dengan berat molekul
lebih besar dari 2000 Dalton. Fase diam yang digunakan dapat berupa silica atau
polimer yang bersifat porus sehingga solute dapat melewati porus atau berdifusi
melewati fase diam (Gandjar dan Rohman, 2007).
Tehnik ini unik karena dalam pemisahan didasarkan pada ukuran molekul
dari solut. Kemasan adalah suatu gel dengan suatu permukaan berlubang-lubang
sangat kecil yang inert. Molekul-molekul kecil dapat masuk ke dalam jaringan
18
tidak dapat masuk ke dalam jaringan dan lewat melalui kolom tanpa ditahan
(Johnson dan Stevenson, 1991).
2.5.2 Instrumentasi Kromatogarfi Cair Kinerja Tinggi (KCKT)
Bagan instrumentasi Kromatografi Cair Kinerja Tinggi (KCKT) dapat
dilihat pada lampiran 1 hal 31. Instrumentasi Kromatografi Cair Kinerja Tinggi
(KCKT) pada dasarnya terdiri atas enam komponen pokok yaitu:
1. Wadah Fase Gerak
Wadah fase gerak yang digunakan harus bersih. Wadah pelarut kosong
ataupun labu laboratorium dapat digunakan sebagai wadah fase gerak. Wadah ini
biasanya dapat menampung fase gerak antara 1 sampai 2 liter pelarut (Gandjar
dan Rohman, 2007).
2. Pompa
Pompa yang cocok untuk KCKT mempunyai beberapa ciri yaitu : pompa
harus dibuat dari bahan yang lembam terhadap semua macam pelarut, mampu
menghasilkan tekanan sampai 5000-6000 psi pada kecepatan alir sampai 3
ml/menit, sedangkan jika untuk skala preparative perlu kecepatan alir sampai 20
ml/menit, dan menghantarkan aliran pelarut yang tetap dan terulangkan ke dalam
kolom. Ada tiga macam jenis pompa yang banyak dipakai pada KCKT antara lain:
- Reciprocating Pumps
- Displacement Pumps (Syringe Pumps)
- Pneumatic Pumps (Constant Pressure Pumps)
(Gritter, 1991).
19
Sampel-sampel cair dan larutan disuntikkan secara langsung ke dalam fase
gerak yang mengalir dibawah tekanan menuju kolom menggunakan alat penyuntik
(injektor). Ada tiga macam sistem injektor pada KCKT yaitu :
- Injektor dengan memakai diafragma (septum)
- Injektor tanpa septum
- Injektor dengan pipa dosis
(Mulja dan Suharman, 1995).
4. Kolom
Kolom merupakan komponen yang vital pada analisis kromatografi.
Keberhasilan atau kegagalan analisis bergantung pada pilihan kolom dan kondisi
kerja yang tepat. Kolom pada kromatografi cair kinerja tinggi merupakan bagian
yang sangat penting, karena proses separasi (pemisahan) komponen-komponen
sampel akan terjadi di dalam kolom. Kolom akan menjadi kunci penentu
keberhasilan pemisahan komponen-komponen sampel serta hasil akhir analisis
dengan KCKT. Dianjurkan untuk memasang penyaring 2 µm di jalur antara
penyuntik dan kolom untuk menahan partikel yang dibawa fase gerak dan
memperjang umur dari kolom (Mulja & Suharman, 1995).
5. Detektor
Detektor diperlukan untuk mengindera adanya komponen cuplikan di
dalam efluen kolom dan mengukur jumlahnya. Detektor yang baik sangat peka,
20
jenis senyawa. Kita menginginkan pula detektor yang kurang peka terhadap
perubahan aliran dan suhu, tetapi hal itu selalu tidak terpenuhi. Detektor pada
KCKT dikelompokkan menjadi dua golongan yaitu :
- Detektor universal yaitu detektor yang mampu mendeteksi zat secara
umum, tidak bersifat spesifik, dan tidak bersifat selektif seperti detektor
indeks bias dan spektrofotometri massa.
- Detektor yang spesifik yang hanya akan mendeteksi analit secara spesifik
dan selektif, seperti detektor UV-Vis, detektor fluoresensi, dan
elektrokimia. (Mulja & Suharman, 1995).
6. Komputer, Integrator, atau Rekorder
Alat pengumpul data seperti computer, integrator , atau recorder,
dihubungkan dengan detektor. Alat ini akan mengukur sinyal elektronik yang
dihasilkan oleh detektor lalu memplotkannya sebagai suatu kromatogram yang
21 BAB III METODOLOGI
3.1 Tempat Pengujian
Pengujian penetapan kadar Oktil Metoksisinamat dalam losion dengan
metode Kromatografi Cair Kinerja Tinggi (KCKT) dilakukan di Laboratorium
kosmetik, Balai Besar Pengawas Obat dan Makanan di Medan yang berada di
Jalan Willem Iskandar Pasar V Barat I No. 2 Medan.
3.2 Alat
Alat yang digunakan adalah Seperangkat alat KCKT (shimadzu) dengan
kolom baja tahan karat yang berisi Oktadesil silika(ODS atau C18), sonikator,
penyaring membrane PTFE 0,45 um; penyaring vakum, timbangan analitik
(shimadzu), dan Alat-alat gelas.
3.3 Bahan
Bahan yang digunakan adalah akuabides, metanol, baku pembanding oktil
metoksisinamat.
3.4 Sampel
• Nama contoh : HERBORIST LOTION
• Wadah/Kemasan : Botol plastik
22
• No Reg : 524301
• Komposisi :water,propylene glycol,isopropyl myristate cetyl,
Mineral oil,octyl methoxycinamate,pottasium
Hydroxide,green tea,
• Kadaluarsa : Juni 2016
• Produksi : PT. Victoria care Indonesia
3.5 Prosedur
3.5.1 Pembuatan Larutan uji
Ditimbang sampel setara ±10 mg oktil metoksisinamat secara seksama,
tambah 5 ml metanol,aduk dan tuang kedalam labu tentukur 10 ml,bilas wadah
dengan metanol dan cukupkan dengan metanol,pipet 1,0 ml kedalam labu tentukur
50 ml dan encerkan sampai tanda dengan metanol,saring dengan penyaring
membran.
3.5.2 Larutan Baku Pembanding
Ditimbang 10 mg baku oktil metoksisinamat,tambah 5 ml metanol,aduk
dan tuang kedalam labu tentukur 10 ml,bilas wadah dengan metanol dan
cukupkan dengan metanol,pipet 1,0 ml kedalam labu tentukur 50 ml dan encerkan
23
3.6 Kromatografi Cair Kinerja Tinggi
3.6.1 Pengaturan Kondisi Sistem
Sistem diperiksa dan dicek untuk meyakinkan apakah sistem pengalir
pelarut telah disambungkan dengan baik, kolom telah dipasang, tersedia cukup
pelarut di dalam botol pelarut, sistem pengawasan pelarut bekerja dengan baik
untuk menghilangkan gelembung udara, penyaring pelarut sudah dipasang, dan
detektor yang sesuai sudah terpasang dengan benar.
3.6.2 Mengaktifkan Sistem
Setelah masing-masing sistem diatur, hubungkan setiap sistem dengan
sumber arus listrik. Tekan tombol power pada pompa, detektor UV-VIS ke posisi
ON dan CBM (Communication Bus Module) ke posisi ON.
3.6.3 Penentuan Garis Alas
Bila nilai absorbansi yang ditampilkan pada detektor UV-VIS telah
menunjukkan 0,000 lalu biarkan beberapa menit sampai diperoleh garis alas yang
relatif cukup lurus yang menandakan sistem telah stabil.
3.7 Cara Penetapan
Kemudian larutan uji dan baku diinjeksikan secara terpisah kedalam
kolom kromatografi cair kinerja tinggi (KCKT) dan dilakukan elusi dengan
kondisi menggunakan kolom Oktadesil silika(ODS), detektor dengan panjang
gelombang 280 nm, dengan laju alir 1,5 ml/menit, dengan volume injeksi 20 µl,
dengan fase gerak metanol pro hplc dan aquabides dengan perbandingan 90:10
24
Hasil yang diperoleh dapat dilihat dari terbentuknya puncak yang direkam
oleh CBM (Communication Bus Module) yakni sejenis penghubung dengan
sistem komputer yang dilengkapi dengan pencetak kromatogram.
3.8 Ketentuan Hasil
Kadar oktil metoksisinamat dalam lution dengan metode Kromatografi
Cair Kinerja Tinggi (KCKT) dapat dihitung dengan rumus:
��
Bb : Bobot baku yang ditimbang dalam mg
Bu : Bobot uji yang ditimbang dalam mg
Fu : Faktor pengenceran larutan uji
Fb : Faktor pengenceran larutan baku
3.9 Persyaratan
Persyaratan Oktil metoksisinamat dalam lotion menurut MA PPOMN
15/KO/01 memenuhi persyaratan jika kadar Oktil Metoksisinamat mengandung
25 BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Pada pengujian penetapan kadar Oktil Metoksisinamat dalam sediaan
Lotio dengan kromatografi cair kinerja tinggi diperoleh kadar Oktil
Metoksisinamat sebagai berikut:
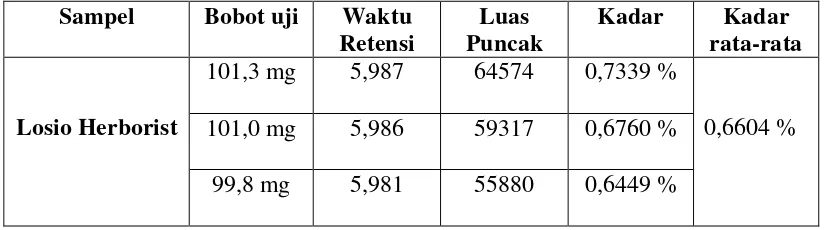
Tabel 1. Kadar Oktil Metoksisinamat dalam Losio Herborist
Berdasarkan pengujian yang dilakukan terhadap penetapan kadar Oktil
Metoksisinamat dalam Lotio Herborist dengan metode kromatografi cair kinerja
tinggi (KCKT) diperoleh kadar Oktil Metoksisinamat sebesar 0,6604%.
Kromatogram hasil pengujian dari kromatografi cair kinerja tinggi
(KCKT) dapat dilihat pada lampiran 4 dan 5 hal 28 dan 29 sedangkan perhitungan
penetapan kadar Oktil Metoksisinamat dalan lusio dengan metode KCKT dapat
26
4.2 Pembahasan
Berdasarkan hasil penetapan kadar Oktil Metoksisinamat dalam Lusio
dengan metode Kromatografi Cair Kinerja Tinggi (KCKT), diperoleh hasil
bahwasanya lusio yang mengandung Oktil Metoksisinamat yang diuji tersebut
memenuhi persyaratan yang ditetapkan oleh MA PPOMN 15/KO/01, yaitu tidak
lebih dari 10,0 %.
Oktil Metoksisinamat dalam sediaan lusio dapat ditetapkan kadarnya
dengan kromatografi cair kinerja tinggi (KCKT) karena analisis dengan KCKT
cepat, daya pisah baik, peka, penyiapan sampel yang mudah, dan dapat
dihubungkan dengan detektor yang sesuai. Panjang gelombang analisis yang
dipilih adalah 280 nm, karena pada panjang gelombang tersebut Oktil
Metoksisinamat memberikan respon puncak yang baik.
Metode KCKT yang digunakan pada penetapan kadar Oktil
Metoksisinamat dalam lusio adalah kromatografi partisi metode kolom fase
terbalik yakni fase diam bersifat non polar berupa Oktadesilsilan (C18) dan fase
gerak bersifat polar yaitu air : metanol (90 : 10). Pada saat penggunaan metode
kolom fase terbalik terjadi kompetisi antara fase gerak dengan sampel yang diuji
yang terjadi di dalam kolom
Dari hasil pengujian yang telah dilakukan, dapat dinyatakan bahwa
penetapan kadar Oktil Metoksisinamat dalam losio dengan metode Kromatografi
Cair Kinerja Tinggi (KCKT) dengan menggunakan prinsip kromatografi partisi
metode kolom fase terbalik merupakan metode yang cukup baik dalam penetapan
27 BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil percobaan penetapan kadar Oktil Metoksisinamat dalam Losio
dengan metode kromatografi cair kinerja tinggi, diketahui bahwa Oktil
Metoksisinamat sebesar 0,6604 % dimana losio Herborist yang diuji tersebut
memenuhi persyaratan yang ditetapkan oleh MA PPOMN 15/KO/01, yaitu tidak
lebih dari 10%.
5.2Saran
Penetapan kadar suatu senyawa kimia di dalam sediaan kosmetik saat ini,
hanya dilakukan pada satu merek lotion saja . Diharapkan kepada penulis
selanjutnya agar menggunakan lotion merek yang berbeda dipasaran agar
wawasan kita tentang produk kosmetik yang baik dan memenuhi persyaratan
28
DAFTAR PUSTAKA
Anonim. 1998. Cosmetic supplies usa. California warehouse. USA
Anonim. 2015. Perawatan Wajah. http://file.upi.edu/Direktori.com tanggal 10 juni 2015.
Ansel HC. 1989. Pengantar Bentuk Sediaan Farmasi, edisi IV. Jakarta : Universitas Indonesia. Hal.519,521.
Christine P. 2005. Penetapan kadar campuran Oktil Metoksisinamat dan Oksibenson dengan metode hight performance liquid chromatography dan spektrofotometri ultra violet. Index Jurnal. Yogyakarta: Universitas Negri Malang.
Depkes RI. (1993). Kodeks kosmetika Indonesia. Edisi II. Jakarta: DitJen POM RI. Hal. 351-352
DitJen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 769-771
Gandjar, I. G., dan A.Rohman. (2007). Kimia Farmasi Analisis. Yogyakarta: Penerbit Pustaka Pelajar. Hal. 378- 394, 406
Gritter, Roy J, dkk. (1991). Pengantar Kromatografi. Bandung: ITB Press. Hal 22.
Johnson, E.L., and Stevenson, R (1991). Basic Liquid Chromatography. Penerjemah Kosasih Padmawinata. Dasar Kromatografi Cair. Bandung: Penerbit ITB. Hal. 291-302
Lachman, L., Liberman, A.H., dan Kanig, J.L. (1994). Teori dan Praktek Farmasi Industri II. Penerjemah: Siti Suyatmi, Edisi Ketiga. Jakarta:Penerbit Universitas Indonesia. Hal. 1117-1118
Mitsui, T., 1997, New Cosmetic and Science, Elsevier, Amsterdam.
Mulja, Muhammad, dan Suharman. (1995). Analisis Instrumental. Surabaya: Airlangga University Press. Hal 248.
Rohman, A. (2009). Kromatografi untuk Analisis Obat. Yogyakarta: Graha Ilmu Hal. 2
29
Shaath, N.A. 1990. Sunscreen, Development, Evaluation, and Regulatory Aspects.
New York: Marcell Dekker
Tranggono, R.I., dan Latifah, F. (2007). Buku Pegangan Ilmu Pengetahuan Kosmetik. Jakarta: penerbit Penebar Swadaya. Hal 3-4.
Prasiddha, dkk. 2015. Potensi Senyawa Bioaktif Rambut Jagung Untuk Tabir Surya. Malang:FTP Universitas Brawijaya Malang Vol. 4 hal: 40-45.
30 Lampiran 1
31 Lampiran 2
Alat Ultrasonic Cleaner untuk menghomogenkan larutan
32 Lampiran 3
Neraca Mikro (4 desimal 0,0001)
35 Lampiran 6
Perhitungan
Penetapan Kadar Oktil Metoksisinamat
Faktor Pengenceran Oktil Metoksi Sinamat = 100
2 x 10 = 500 mg/ml
Kadar Baku Oktil Metoksi Sinamat = 100 %
Bobot Baku = 13,59 mg
Bobot Sampel Herborist Lotion 1 = 101,3 mg
Bobot Sampel Herborist Lotion 2 = 101 mg
Bobot Sampel Herborist Lotion 3 = 99,8 mg
Kadar Herborist Lotion 1 = ��
�� x
Kadar Herborist Lotion 2 = ��
�� x
Kadar Herborist Lotion3 = ��
�� x
Kadar Rata-rata (Kr) dan Deviasi
36
Kr 2 = �1+�3
2 =
0,7339+0,6449
2 = 0,6894
D2 = ��2−�1
��2 ×100% =
0,6894−0,7339
0,6894 × 100% = 6,45%
Kr 3 = �2+�3
2 =
0,6760 +0,6449
2 = 0,6604
D3 = ��3−�2
��3 ×100% =
0,6604−0,6760
0,6604 × 100% = 2,36%