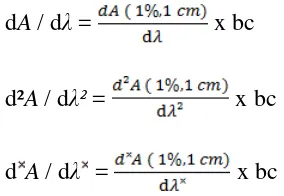UJI VALIDASI PADA ESTIMASI KANDUNGAN KAFEIN DAN
ASAM SITRAT DALAM MINUMAN BERENERGI SECARA
SPEKTROFOTOMETRI DERIVATIF
SKRIPSI
OLEH:
F. DADANG DALIMUNTHE
NIM 121524014
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI VALIDASI PADA ESTIMASI KANDUNGAN KAFEIN DAN
ASAM SITRAT DALAM MINUMAN BERENERGI SECARA
SPEKTROFOTOMETRI DERIVATIF
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh
Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
F. DADANG DALIMUNTHE
NIM 121524014
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI VALIDASI PADA ESTIMASI KANDUNGAN KAFEIN DAN
ASAM SITRAT DALAM MINUMAN ENERGI SECARA
SPEKTROFOTOMETRI DERIVATIF
OLEH:F. DADANG DALIMUNTHE NIM 121524014
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Januari 2015
Medan, Januari 2015 Fakultas Farmasi
Universitas Sumatera Utara a. n. Dekan
Wakil Dekan I,
Prof. Dr. Julia Reveny, M.Si., Apt. NIP 195807101986012001
Pembimbing I
Prof. Dr. Siti Morin Sinaga, M.Sc., Apt. NIP 195008281976032002
Pembimbing II
Dr. Muchlisyam, M.Si., Apt. NIP 195006221980021001
Panitia Penguji,
Prof. Dr. Ginda Haro, M.Sc., Apt. NIP 195108161980031002
Dra. Masria L. Tambunan, M.Si., Apt. NIP 195005081977022001
Prof. Dr. Siti Morin Sinaga, M.Sc., Apt. NIP 195008281976032002
iv
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah melimpahkan anugerah dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “Uji Validasi Pada Estimasi Kandungan Kafein dan Asam Sitrat dalam Minuman Berenergi Secara Spektrofotometri Derivatif”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi dari Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis hendak menyampaikan rasa hormat dan terima kasih yang sebesar-besarnya kepada Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas dan masukan selama masa pendidikan dan penelitian, kepada Prof. Dr. Siti Morin Sinaga, M.Sc., Apt., dan Dr. Muchlisyam, M.Si., Apt., selaku dosen pembimbing yang telah banyak memberikan bimbingan, arahan, dan bantuan selama masa penelitian dan penulisan skripsi ini, Penulis juga menyampaikan ucapan terima kasih kepada Prof. Dr. Ginda Haro, M.Sc., Apt., Dra. Tuty Roida Pardede, M.Si., Apt., dan Dra. Masria L. Tambunan, M.Si., Apt., selaku dosen penguji yang telah memberikan masukan dalam penyusunan skripsi ini.
v
Ricky Dalimunthe, kerabat kerabat, dan teman-teman semua atas motivasi dan segala bantuan dalam penyelesaian skripsi ini.
Semoga Allah SWT memberikan balasan yang berlipat ganda kepada semua pihak yang telah membantu dalam penulisan skripsi ini. Penulis menyadari bahwa skripsi ini masih banyak kekurangan, oleh karena itu sangat diharapkan kritik dan saran yang bersifat membangun dari semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang farmasi.
Medan, Januari 2015 Penulis,
vi
UJI VALIDASI PADA ESTIMASI KANDUNGAN KAFEIN DAN ASAM SITRAT DALAM MINUMAN BERENERGI SECARA
SPEKTROFOTOMETRI DERIVATIF ABSTRAK
Menurut SNI 01-6684-2002 minuman berenergi merupakan minuman yang mengandung satu atau lebih bahan yang mudah dan cepat diserap oleh tubuh untuk menghasilkan energi dengan atau tanpa bahan tambahan makanan yang diizinkan. Spektrofotometri derivatif merupakan metode transformasi dari spektrofotometri konvensional yang dikembangkan untuk analisis kuantitatif multikomponen senyawa aktif pada suatu sediaan. Tujuan penelitian ini adalah untuk menguji validasi metode spektrofotometri derivatif dalam mengestimasi kandungan kafein dan asam sitrat pada minuman berenergi.
Metode penelitian yang dilakukan adalah pengambilan sampel secara purposif terhadap minuman berenergi Kratingdaeng® dan Kratingdaeng-S® dan melakukan penetapan kadar terhadap kandungan kafein dan asam sitrat dengan spektrofotometri derivatif teknik zero crossing pada serapan derivat kedua dalam pelarut HCl 0,1 N.
Dari hasil penelitian yang dilakukan diperoleh kandungan kafein dan asam sitrat pada sampel minuman berenergi Kratingdaeng® adalah (49,4713 ± 0,5109) mg dan (1050,7729 ± 79,9639) mg/kg secara berturut-turut sedangkan kandungan kafein dan asam sitrat pada sampel Kratingdaeng-S® adalah (50,9210 ± 0,3524) mg dan (1746,9913 ± 352,1797) mg/kg secara berturut-turut. Kandungan kafein dalam sampel minuman berenergi Kratingdaeng® memenuhi persyaratan SNI 01-6684-2002, sedangkan pada sampel Kratingdaeng-S® tidak memenuhi persyaratan tersebut. Kandungan asam sitrat pada sampel Kratingdaeng® dan Kratingdaeng-S® memenuhi persyaratan berdasarkan Peraturan Kepala BPOM R.I. No. 8 Tahun 2013. Hasil uji perolehan kembali kafein dan asam sitrat masing-masing adalah 99,12% dan 100,25%, sedangkan simpangan baku relatif kafein dan asam sitrat masing-masing adalah sama yaitu sebesar 0,86%.
Berdasarkan hasil penelitian yang dilakukan maka metode spektrofotometri derivatif yang digunakan memenuhi persyaratan akurasi dan presisi dan dapat digunakan untuk menetapkan kandungan kafein dan asam sitrat dalam minuman berenergi.
vii
VALIDATION IN ESTIMATION OF CAFFEINE AND CITRIC ACID IN ENERGYDRINK BY DERIVATIVE SPECTROFOTOMETRY
ABSTRACT
According to SNI 01-6684-2002 Energy drinks are beverages that contain one or more ingredients are easily and quickly absorbed into body to produce energy with or without food additives are permitted. Derivative spectrophotometry is a transformation method from conventional spectrophotometric that developed for quantitative analysis of multicomponent active compounds in a preparation. The aim of this study was to test the validation of derivative spectrophotometry method in estimating the content of caffeine and citric acid in energy drinks.
The method of this research was done by purposive sampling to Kratingdaeng® and Kratingdaeng-S® energy drinks sample and determine the levels of caffeine and citric acid content using derivative spectrophotometry with zero crossing technique to second derivative absorption in HCl 0,1N.
The research results were obtained the caffeine and citric acid content of the sample Kratingdaeng® energy drinks were (49.4713 ± 0.5109) mg and (1050.7729 ± 79.9639) mg/kg concecutively while the caffeine and citric acid content of the sample Kratingdaeng-S® energy drinks were (50.9210 ± 0.3524) mg and (1746.9913 ± 352.1797) mg/kg concecutively. The content of caffeine in Sample Kratingdaeng® energy drinks still meet the requirements of SNI 01-6684-2002, while the sample Kratingdaeng-S® do not meet these requirements. The content of citric acid in the samples of Kratingdaeng® and Kratingdaeng-S® meet the requirements based on Regulation of BPOM RI No.8 in 2013. The result of the recovery at caffeine and citric acid were 99.12% and 100.25%, while the Relative Standard Deviation of caffeine and citric acid were same of 0.86%.
Based on the results of research that derivative spectrophotometry method fulfilled the requirements of accuracy and precision and can be used to determinate the content of caffeine and citric acid in energy drinks.
viii DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 5
1.4 Tujuan Penelitian ... 5
1.5 Manfaat Penelitian ... 6
BAB II TINJAUAN PUSTAKA ... 7
2.1 Minuman Berenergi ... 7
2.2 Uraian Bahan ... 7
2.2.1 Kafein ... 7
2.2.2 Asam sitrat... 9
ix
2.3.1 Hukum Lambert-Beer ... 12
2.3.2 Kegunaan Spektrofotometri ... 13
2.4 Spektrofotometri Derivatif ... 14
2.4.1 Komponen Spektrofotometri derivatif ... 18
2.4.2 Kegunaan Spektrofotometri derivatif ... 18
2.5 Validasi Metode Analisis ... 19
2.5.1 Akurasi ... 20
2.5.2 Presisi ... 21
2.5.3 Batas Deteksi dan Batas Kuantitasi ... 21
2.5.4 Linieritas ... 22
2.5.5 Rentang ... 22
BAB III METODE PENELITIAN ... 23
3.1 Jenis Penelitian ... 23
3.2 Tempat dan Waktu Penelitian ... 23
3.3 Alat ... 23
3.4 Bahan-Bahan ... 23
3.5 Pengambilan Sampel ... 24
3.6 Prosedur Penelitian ... 24
3.6.1 Pembuatan Pereaksi ... 24
3.6.2 Pembuatan Larutan Induk Baku ... 24
3.6.2.1 Pembuatan Larutan Induk Baku Kafein ... 24
x
3.6.3.1 Pembuatan Spektrum Serapan Maksimum
Kafein ... 25
3.6.3.2 Pembuatan Spektrum Serapan Maksimum Asam Sitrat ... 25
3.6.4 Pembuatan Spektrum Serapan Derivatif ... 25
3.6.4.1 Pembuatan Spektrum Serapan Derivatif Kafein ... 25
3.6.4.2 Pembuatan Spektrum Serapan Derivatif Asam Sitrat ... 26
3.6.5 Penentuan Zero Crossing ... 26
3.6.6 Penentuan Panjang Gelombang Analisis ... 26
3.6.7 Pembuatan dan Penentuan Linieritas Kurva Kalibrasi Kafein dan Asam Sitrat ... 27
3.6.8 Penetapan Kandungan Kafein dan Asam Sitrat dalam Minuman Berenergi ... 28
3.6.8.1 Penentuan Kandungan Kafein dalam Minuman Berenergi ... 28
3.6.8.2 Penentuan Kandungan Asam Sitrat dalam Minuman Berenergi ... 29
3.6.9 Uji Validasi ... 31
3.6.9.1 Uji Akurasi ... 31
3.6.9.2 Uji Presisi ... 32
BAB IV HASIL DAN PEMBAHASAN ... 34
4.1 Hasil Penentuan Kurva Serapan Maksimum ... 34
4.2 Hasil Penentuan Kurva Serapan Kafein pada Derivat Pertama dan Kedua ... 35
4.3 Hasil Penentuan Kurva Serapan Asam Sitrat pada Derivat Pertama dan Kedua ... 37
xi
4.4.1 ZeroCrossing Derivat Pertama Kafein dan Asam
Sitrat ... 39
4.4.2 Zero Crossing Derivat Kedua Kafein dan Asam Sitrat ... 40
4.5 Hasil Penentuan Panjang Gelombang Analisis Kafein dan Asam Sitrat ... 42
4.6 Hasil Penentuan Linieritas Kurva Kalibrasi ... 50
4.6.1 Kurva Kalibrasi ... 50
4.6.2 Batas Deteksi dan Batas Kuantitasi ... 51
4.7 Hasil Penentuan Kandungan Kafein dan Asam Sitrat dalam Sampel Minuman Berenergi ... 52
4.8 Hasil Uji Validasi ... 59
4.8.1 Hasil Uji Akurasi ... 59
4.8.2 Hasil Uji Presisi ... 60
BAB V KESIMPULAN DAN SARAN ... 61
5.1 Kesimpulan ... 61
5.2 Saran ... 62
DAFTAR PUSTAKA ... 63
xii
DAFTAR TABEL
Halaman Tabel 4.1 Panjang Gelombang Analisis dan Absorbansi pada
Derivat Kedua ... 49 Tabel 4.2 Absorbansi Kafein dan Asam Sitrat Dalam Sampel pada
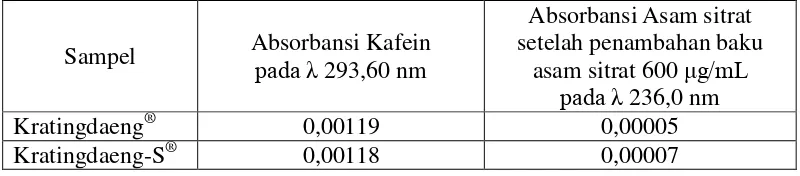
Masing-Masing Panjang Gelombang Analisis ... 52 Tabel 4.3 Absorbansi Kafein dan Asam Sitrat Setelah Penambahan
Baku Asam Sitrat Konsentrasi 500 µg/mL Pada Derivat
Kedua ... 55 Tabel 4.4 Absorbansi Kafein dan Asam Sitrat Setelah Penambahan
Baku Asam Sitrat Konsentrasi 600 µg/mL pada Derivat
Kedua ... 55 Tabel 4.5 Kandungan Kafein dan Asam Sitrat Setelah Penambahan
Baku Asam Sitrat Konsentrasi 500 µg/mL ... 58 Tabel 4.6 Perolehan Kembali Kafein dan Asam Sitrat dengan
Metode Penambahan Baku pada Minuman Berenergi
xiii
DAFTAR GAMBAR
Halaman Gambar 2.1 Kurva Serapan Derivat Pertama Sampai Derivat
Keempat ... 16 Gambar 2.2 Kurva Sederhana Aplikasi Zero Crossing ... 17 Gambar 4.1 Kurva Serapan Maksimum Kafein Konsentrasi
10 µg/mL ... 34 Gambar 4.2 Kurva Serapan Maksimum Asam Sitrat Konsentrasi
500 µg/mL ... 35 Gambar 4.3 Kurva Tumpang Tindih Serapan Kafein dalam berbagai
konsentrasi ... 36 Gambar 4.4 Kurva Tumpang Tindih Serapan Derivat Pertama
Kafein dalam berbagai konsentrasi ... 36 Gambar 4.5 Kurva Tumpang Tindih Serapan Derivat Kedua Kafein
dalam berbagai konsentrasi ... 37 Gambar 4.6 Kurva Tumpang Tindih Serapan Asam Sitrat dalam
berbagai konsentrasi ... 38 Gambar 4.7 Kurva Tumpang Tindih Serapan Derivat Pertama Asam
Sitrat dalam berbagai konsentrasi ... 38 Gambar 4.8 Kurva Tumpang Tindih Serapan Derivat Kedua Asam
Sitrat dalam berbagai konsentrasi ... 39 Gambar 4.9 Zero Crossing Kafein Derivat Pertama dengan λ =
214,20 nm; 236,0 nm; 286,0 nm; dan 308,0 nm ... 40 Gambar 4.10 Zero Crossing Asam Sitrat Derivat Pertama dengan
λ = 209,40 nm; 258,80 nm; dan 302,16 nm ... 40
Gambar 4.11 Zero Crossing Kafein Derivat Kedua dengan λ = 214,20
nm; 229,0 nm; 236,0 nm; 260,0 nm; 286,0 nm; dan 308,0 nm ... 41 Gambar 4.12 Zero Crossing Asam Sitrat Derivat Kedua dengan λ =
222,50 nm; 259,0 nm; 287,70 nm; 293,60 nm; 336,0
xiv
Gambar 4.13 Kurva Serapan Campuran Kafein Konsentrasi 10 µg/mL
dan Asam Sitrat Konsentrasi 500 µg/mL ... 43 Gambar 4.14 Kurva Tumpang Tindih Serapan Kafein Konsentrasi 10
µg/mL dan Asam Sitrat Konsentrasi 500 µg/mL ... 43 Gambar 4.15 Kurva Tumpang Tindih Serapan Kafein Konsentrasi 10
µg/mL dan Asam Sitrat Konsentrasi 500 µg/mL dan Campuran Kafein Konsentrasi 10 µg/mL dan Asam
Sitrat Konsentrasi 500 µg/mL ... 43 Gambar 4.16 Kurva Serapan Derivatif Pertama Campuran Kafein
Konsentrasi 10 µg/mL dan Asam Sitrat Konsentrasi 500
µg/mL ... 44 Gambar 4.17 Kurva Tumpang Tindih Serapan Derivatif Pertama
Kafein Konsentrasi 10 µg/mL dan Asam Sitrat
Konsentrasi 500 µg/mL ... 44 Gambar 4.18 Kurva Tumpang Tindih Serapan Derivatif Pertama
Kafein Konsentrasi 10 µg/mL dan Asam Sitrat Konsentrasi 500 µg/mL dan Campuran Kafein Konsentrasi 10 µg/mL dan Asam Sitrat Konsentrasi 500
µg/mL ... 44 Gambar 4.19 Kurva Serapan Derivatif Kedua Campuran Kafein
Konsentrasi 10 µg/mL dan Asam Sitrat Konsentrasi 500
µg/mL ... 45 Gambar 4.20 Kurva Tumpang Tindih Serapan Derivatif Kedua
Kafein Konsentrasi 10 µg/mL dan Asam Sitrat
Konsentrasi 500 µg/mL ... 45 Gambar 4.21 Kurva Tumpang Tindih Serapan Derivatif Kedua
Kafein Konsentrasi 10 µg/mL dan Asam Sitrat Konsentrasi 500 µg/mL dan Campuran Kafein Konsentrasi 10 µg/mL dan Asam Sitrat Konsentrasi 500
µg/mL ... 45 Gambar 4.22 Zero Crossing dari Kafein Konsentrasi 10 µg/mL pada
λ = 293,60 nm ... 46
Gambar 4.23 Zero Crossing dari Asam Sitrat Konsentrasi 500 µg/mL
pada λ = 236,0 nm ... 46 Gambar 4.24 Zero Crossing Campuran Kafein dan Asam Sitrat
xv
Gambar 4.25 Zero Crossing Campuran Kafein dan Asam Sitrat
dengan Asam Sitrat λ = 236,0 nm ... 47 Gambar 4.26 Kurva Kalibrasi Kafein Pada Panjang Gelombang 293,60 nm ... 51 Gambar 4.27 Kurva Kalibrasi Asam Sitrat Pada Panjang Gelombang
236,0 nm ... 51 Gambar 4.28 Kurva Tumpang Tindih Kafein Konsentrasi 10 µg/mL
dan Asam Sitrat Konsentrasi 500 µg/mL dengan
Sampel Kratingdaeng® ... 56 Gambar 4.29 Kurva Tumpang Tindih Kafein Konsentrasi 10 µg/mL
dan Asam Sitrat Konsentrasi 500 µg/mL dengan
Sampel Kratingdaeng-S® ... 56 Gambar 4.30 Kurva Tumpang Tindih Kafein Konsentrasi 10 µg/mL
dan Asam Sitrat Konsentrasi 500 µg/mL dengan Sampel Kratingdaeng® Setelah Penambahan Baku Asam
Sitrat Konsentrasi 500 µg/mL ... 57 Gambar 4.31 Kurva Tumpang Tindih Kafein Konsentrasi 10 µg/mL
dan Asam Sitrat Konsentrasi 500 µg/mL dengan Sampel Kratingdaeng-S® Setelah Penambahan Baku Asam Sitrat Konsentrasi 500 µg/mL ... 57
xvi
DAFTAR LAMPIRAN
Halaman Lampiran 1. Gambar Sampel Minuman Berenergi ... 66 Lampiran 2. Komposisis Sampel Minuman Berenergi ... 67 Lampiran 3. Gambar Alat Spektrofotometer Ultraviolet (UV) ... 68 Lampiran 4. Uji Kualitatif Asam Sitrat dengan Pereaksi Deninges .... 69 Lampiran 5. Perhitungan Pembuatan HCl 0,1N ... 70 Lampiran 6. Bagan Alir Prosedur Penelitian ... 71 Lampiran 7. Kurva Serapan Kafein Baku dan Asam Sitrat Baku ... 76 Lampiran 8. Kurva Serapan Derivat Pertama Kafein Baku dan Asam
Sitrat Baku ... 81 Lampiran 9. Kurva Serapan Derivat Kedua Kafein Baku dan Asam
Sitrat Baku ... 86 Lampiran 10. Kurva Serapan Panjang Gelombang Analisis Kafein
dan Asam Sitrat ... 91 Lampiran 11. Hasil Pengukuran Serapan Derivat Kedua Kafein,
Asam Sitrat dan Campuran Kafein dan Asam Sitrat
pada λ 200-300 nm ... 93 Lampiran 12. Data Kalibrasi Kafein BPFI, Persamaan Regresi dan
Koefisien Korelasi ... 98 Lampiran 13. Data Kalibrasi Asam Sitrat P.A, Persamaan Regresi
dan Koefisien Korelasi ... 100 Lampiran 14. Perhitungan Batas Deteksi (Limit of Detection, LOD)
dan Batas Kuantitasi (Limit of Quantitation, LOQ)
Kafein dan Asam Sitrat ... 102 Lampiran 15. Kurva Serapan Derivat Kedua Kafein dan Asam Sitrat
dalam Sampel ... 103 Lampiran 16. Hasil Analisis Kandungan Jumlah Kafein dan Asam
Sitrat dalam Sampel ... 113 Lampiran 17. Contoh Perhitungan Kadar Kafein dan Asam Sitrat
xvii
Lampiran 18. Contoh Perhitungan Kadar Kafein dan Asam Sitrat
dalam Sampel Kratingdaeng-S® ... 118
Lampiran 19. Perhitungan Statistik Kadar Kafein dan Asam Sitrat dalam Sampel Kratingdaeng® ... 121
Lampiran 20. Perhitungan Statistik Kadar Kafein dan Asam Sitrat dalam Sampel Kratingdaeng-S® ... 124
Lampiran 21. Kurva Serapan Uji Perolehan Kembali Kafein dan Asam Sitrat dalam Sampel Kratingdaeng-S® ... 127
Lampiran 22. Hasil Uji Perolehan Kembali Kafein dan Asam Sitrat Setelah Penambahan Masing-Masing Larutan Baku pada Sampel ... 130
Lampiran 23. Contoh Perhitungan Uji Perolehan Kembali Kafein Asam Sitrat dengan menggunakan Sampel Kratingdaeng® ... 131
Lampiran 24. Perhitungan Simpangan Baku Relatif (Relative Standard Deviation, RSD) Persen Perolehan Kembali Kafein ... 134
Lampiran 25. Perhitungan Simpangan Baku Relatif (Relative Standard Deviation, RSD) Persen Perolehan Kembali Asam Sitrat ... 135
Lampiran 26. Daftar Nilai Distribusi t ... 136
Lampiran 27. Sertifikat Pengujian Kafein ... 137
Lampiran 28. Label Asam Sitrat Pro Analis ... 138
Lampiran 29. SNI 01-6684-2002 Tentang Minuman Berenergi ... 139
vi
UJI VALIDASI PADA ESTIMASI KANDUNGAN KAFEIN DAN ASAM SITRAT DALAM MINUMAN BERENERGI SECARA
SPEKTROFOTOMETRI DERIVATIF ABSTRAK
Menurut SNI 01-6684-2002 minuman berenergi merupakan minuman yang mengandung satu atau lebih bahan yang mudah dan cepat diserap oleh tubuh untuk menghasilkan energi dengan atau tanpa bahan tambahan makanan yang diizinkan. Spektrofotometri derivatif merupakan metode transformasi dari spektrofotometri konvensional yang dikembangkan untuk analisis kuantitatif multikomponen senyawa aktif pada suatu sediaan. Tujuan penelitian ini adalah untuk menguji validasi metode spektrofotometri derivatif dalam mengestimasi kandungan kafein dan asam sitrat pada minuman berenergi.
Metode penelitian yang dilakukan adalah pengambilan sampel secara purposif terhadap minuman berenergi Kratingdaeng® dan Kratingdaeng-S® dan melakukan penetapan kadar terhadap kandungan kafein dan asam sitrat dengan spektrofotometri derivatif teknik zero crossing pada serapan derivat kedua dalam pelarut HCl 0,1 N.
Dari hasil penelitian yang dilakukan diperoleh kandungan kafein dan asam sitrat pada sampel minuman berenergi Kratingdaeng® adalah (49,4713 ± 0,5109) mg dan (1050,7729 ± 79,9639) mg/kg secara berturut-turut sedangkan kandungan kafein dan asam sitrat pada sampel Kratingdaeng-S® adalah (50,9210 ± 0,3524) mg dan (1746,9913 ± 352,1797) mg/kg secara berturut-turut. Kandungan kafein dalam sampel minuman berenergi Kratingdaeng® memenuhi persyaratan SNI 01-6684-2002, sedangkan pada sampel Kratingdaeng-S® tidak memenuhi persyaratan tersebut. Kandungan asam sitrat pada sampel Kratingdaeng® dan Kratingdaeng-S® memenuhi persyaratan berdasarkan Peraturan Kepala BPOM R.I. No. 8 Tahun 2013. Hasil uji perolehan kembali kafein dan asam sitrat masing-masing adalah 99,12% dan 100,25%, sedangkan simpangan baku relatif kafein dan asam sitrat masing-masing adalah sama yaitu sebesar 0,86%.
Berdasarkan hasil penelitian yang dilakukan maka metode spektrofotometri derivatif yang digunakan memenuhi persyaratan akurasi dan presisi dan dapat digunakan untuk menetapkan kandungan kafein dan asam sitrat dalam minuman berenergi.
vii
VALIDATION IN ESTIMATION OF CAFFEINE AND CITRIC ACID IN ENERGYDRINK BY DERIVATIVE SPECTROFOTOMETRY
ABSTRACT
According to SNI 01-6684-2002 Energy drinks are beverages that contain one or more ingredients are easily and quickly absorbed into body to produce energy with or without food additives are permitted. Derivative spectrophotometry is a transformation method from conventional spectrophotometric that developed for quantitative analysis of multicomponent active compounds in a preparation. The aim of this study was to test the validation of derivative spectrophotometry method in estimating the content of caffeine and citric acid in energy drinks.
The method of this research was done by purposive sampling to Kratingdaeng® and Kratingdaeng-S® energy drinks sample and determine the levels of caffeine and citric acid content using derivative spectrophotometry with zero crossing technique to second derivative absorption in HCl 0,1N.
The research results were obtained the caffeine and citric acid content of the sample Kratingdaeng® energy drinks were (49.4713 ± 0.5109) mg and (1050.7729 ± 79.9639) mg/kg concecutively while the caffeine and citric acid content of the sample Kratingdaeng-S® energy drinks were (50.9210 ± 0.3524) mg and (1746.9913 ± 352.1797) mg/kg concecutively. The content of caffeine in Sample Kratingdaeng® energy drinks still meet the requirements of SNI 01-6684-2002, while the sample Kratingdaeng-S® do not meet these requirements. The content of citric acid in the samples of Kratingdaeng® and Kratingdaeng-S® meet the requirements based on Regulation of BPOM RI No.8 in 2013. The result of the recovery at caffeine and citric acid were 99.12% and 100.25%, while the Relative Standard Deviation of caffeine and citric acid were same of 0.86%.
Based on the results of research that derivative spectrophotometry method fulfilled the requirements of accuracy and precision and can be used to determinate the content of caffeine and citric acid in energy drinks.
1 BAB I
PENDAHULUAN 1.1 LatarBelakang
Menurut SNI 01-6684-2002 minuman berenergi merupakan minuman yang mengandung satu atau lebih bahan yang mudah dan cepat diserap oleh tubuh untuk menghasilkan energi dengan atau tanpa bahan tambahan makanan yang diizinkan. Umumnya produk minuman olahan, termasuk minuman berenergi yang mengandung bahan tambahan makanan tidak mencantumkan jumlah komposisi bahan tambahan makanan yang jelas pada kemasannya.
Secara umum minuman berenergi yang beredar dipasaran adalah minuman yang mengandung kombinasi kafein dengan bahan lain seperti taurin, ginseng, vitamin B dan bahan tambahan lain seperti gula, asam sitrat serta pengawet. Asam sitrat biasanya dipakai untuk meningkatkan rasa asam (mengatur tingkat keasaman) pada berbagai pengolahan minum, produk air, susu dan selai. Penggunaan asam sitrat sebagai bahan pengatur keasaman dalam produk minuman sampai saat ini belum dibatasi kadar penggunaannya (Ditjen POM, 2013).
2
Beberapa metode analisis modern dalam industri adalah metode analisis spektrofotometri Ultraviolet-Visible (UV-Vis) dan Kromatografi Cair Kinerja Tinggi (KCKT). Metode analisis yang biasa digunakan dalam penentuan kadar kafein maupun asam sitrat antara lain metode titrasi (Ditjen POM, 1995), spektrofotometri (USP, 2007) dan kromatografi cair kinerja tinggi (USP, 2007). Menurut penelitian yang dilakukan oleh Tautua, dkk., (2014), analisis kafein dalam minuman berenergi dapat dilakukan menggunakan spektrofotometri UV dengan panjang gelombang maksimum 270 nm. Spektrofotometri derivatif ultraviolet dengan teknik zero-crossing telah dikembangkan untuk analisis simultan kadar senyawa-senyawa campuran dari kafein, vit B2, B6 dalam minuman berenergi, diperoleh kandungan kafein pada panjang gelombang 267,2 nm orde tiga sebanyak 49,3836 mg/sajian (Safitri, 2007).
Menurut penelitian yang dilakukan oleh Brima dan Abbas (2014), kadar asam sitrat dalam minuman berenergi dapat ditentukan dengan menggunakan metode titrasi asam basa sebesar (7,3 ± 0,06) g/L. Analisis multikomponen campuran asam askorbat dan asam sitrat dengan metode gabungan serapan UV derivatif diperoleh panjang gelombang analisis pada derivat pertama 194 - 196 nm, derivat kedua 195 nm dan 265 nm, derivat ketiga 264 - 266 nm dan derivat keempat pada 265 nm (Rojas, 2008).
3
spektrofotometri konvensional memiliki keterbatasan, yaitu tidak dapat digunakan secara langsung untuk analisis secara kuantitatif maupun kualitatif dari senyawa yang memiliki matriks kompleks, sehingga harus dilakukan pemisahan analit dari matriks (Owen, 2000). Pemisahan kafein dari matriks dapat menjadi sumber kesalahan analisis dan memperpanjang waktu analisis, oleh karena itu, diperlukan metode lain yang lebih cepat, murah dengan tingkat ketelitian dan ketepatan yang tinggi, serta dapat mengatasi efek matriks tanpa harus memisahkannya terlebih dahulu (Nurhidayati, 2007).
Menurut Owen (2000), spektrofotometri derivatif merupakan metode transformasi dari spektrofotometri konvensional yang dikembangkan untuk analisis kuantitatif multikomponen senyawa aktif pada suatu sediaan. Spektrofotometri derivatif dapat digunakan untuk senyawa yang memiliki matriks kompleks, sehingga penentuan baik secara kuantitatif maupun kualitatif dapat dilakukan tanpa harus melakukan pemisahan antara analit dengan matriksnya. Selain itu metode spektrofotometri derivatif relatif lebih sederhana, alat dan biaya operasionalnya relatif lebih murah dan waktu analisisnya lebih cepat.
Spektrofotometri derivatif menawarkan beberapa keuntungan dibandingkan dengan spektrofotometri konvensional antara lain gambaran struktur yang terinci dari spektrum serapan dan gambaran ini dapat lebih jelas bila spektrum derivatif ditingkatkan (Munson, 1991).
4
dan metode tersebut. Pengujian kinerja analitik diperlukan untuk menjamin keabsahan dan keakuratan data hasil analisis. Parameter parameter yang digunakan antara lain linearitas, presisi, akurasi, limit deteksi, dan limit kuantisasi (Harmita, 2004).
Berdasarkan uraian di atas maka penulis tertarik menguji validasi metode spektrofotometri derivatif dalam mengestimasi kandungan kafein dan asam sitrat dalam minuman berenergi.
1.2 PerumusanMasalah
Perumusan masalah pada penelitian ini adalah:
a. Apakah metode spektrofotometri derivatif dapat digunakan untuk menganalisa kandungan kafein dan asam sitrat dalam minuman berenergi?
b. Apakah kandungan persajian kafein dan asam sitrat dalam minuman berenergi telah memenuhi persyaratan SNI 01-6684-2002 tentang minuman berenergi dan Peraturan Kepala BPOM R.I. No. 8 Tahun 2013 tentang batas maksimum penggunaan bahan tambahan pangan pengatur keasaman?
c. Apakah hasil uji validasi terhadap metode spektrofotometri derivatif untuk menganalisa kandungan kafein dan asam sitrat dalam minuman berenergi dapat memenuhi syarat pengujian validasi?
1.3 Hipotesis
Hipotesis pada penelitian ini adalah:
5
b. Kandungan persajian kafein dan asam sitrat dalam minuman berenergi telah memenuhi persyaratan SNI 01-6684-2002 tentang minuman berenergi dan Peraturan Kepala BPOM R.I. No. 8 Tahun 2013 tentang batas maksimum penggunaan bahan tambahan pangan pengatur keasaman.
c. Hasil uji validasi terhadap metode spektrofotometri derivatif untuk menganalisa kandungan kafein dan asam sitrat dalam minuman berenergi dapat memenuhi syarat pengujian validasi.
1.4 TujuanPenelitian
Tujuan penelitian ini adalah:
a. Untuk mengetahui metode spektrofotometri derivatif dapat digunakan dalam menganalisa kandungan kafein dan asam sitrat dalam minuman berenergi. b. Untuk mengetahui kandungan persajian kafein dan asam sitrat dalam minuman
berenergi telah memenuhi persyaratan SNI 01-6684-2002 tentang minuman berenergi dan Peraturan Kepala BPOM R.I. No. 8 Tahun 2013 tentang batas maksimum penggunaan bahan tambahan pangan pengatur keasaman.
6 1.5 Manfaat Penelitian
7 BAB II
TINJAUAN PUSTAKA
2.1 Minuman Berenergi
Minuman berenergi adalah minuman yang mengandung satu atau lebih bahan yang mudah dan cepat diserap oleh tubuh untuk menghasilkan energi dengan atau tanpa bahan tambahan makanan yang diizinkan (Badan Standarisasi Nasional, 2002). Minuman berenergi bertujuan memberi peningkatan energi melalui kombinasi zat stimulan seperti kafein, ginseng, vitamin B, asam amino dan gula. Asupan makanan antara lain berfungsi untuk menggantikan energi tubuh yang hilang akibat beraktivitas. Jika energi tersebut tidak segera diganti maka orang tersebut akan kekurangan energi sehingga tubuhnya akan menjadi lemas dan kurang bersemangat (Tautua, dkk., 2013).
Menurut Badan Standarisasi Nasional (2002), persyaratan minuman berenergi dengan jenis uji total energi minimal 100 kkal per sajian, taurin 1000 mg per sajian, kafein 50 mg per sajian dan uji lainnya dapat dilihat pada Lampiran 29 Halaman 139.
2.2 Uraian Bahan 2.2.1 Kafein
8
oral, dengan kecepatan bioavaibilitas 100 % (Gunawan dan Wilmana, 2007). Meurut Ditjen POM (1995), kafein memiliki: ,
Rumus struktur :
Rumus Molekul : C8H10N4O2 Berat Molekul : 194,19 Nama Kimia : Coffein
Kandungan : Tidak kurang dari 98,5% dan tidak lebih dari 101,0% C8H10N4O2, dihitung terhadap zat anhidrat. Pemerian : Serbuk putih atau bentuk jarum mengkilat putih; biasanya menggumpal; tidak berbau; rasa pahit.
Larutan ini bersifat netral pada kertas lakmus. Bentuk hidratnya mekar di udara.
9
cangkir sehari) dapat bekerja adiktif. Minum kopi lebih dari 4 - 5 cangkir sehari meningkatkan kadar homosistein dalam darah dan dapat menimbulkan resiko penyakit jantung namun bila dihentikan sekaligus dapat mengakibatkan sakit kepala (Gunawan dan Wilmana, 2007).
Minum lebih dari 10 cangkir kopi sehari dapat menimbulkan debar jantung, gangguan lambung, tangan gemetaran, gelisah dan ingatan berkurang serta sukar tidur, sebaiknya jangan minum lebih dari 3 cangkir kopi dalam sehari (Tjay dan Rahardja, 2007). Berdasarkan SNI 01-6684-2002, batas maksimum kandungan kafein dalam minuman berenergi adalah 50 mg persaji.
2.2.2 Asam Sitrat
Asam sitrat pertama kali diekstraksi dan dikristalisasi dari buah jeruk, sehingga asam sitrat hasil ektraksi dari buah-buahan ini dikenal sebagai asam sitrat alami. Asam sitrat (C6H8O7) banyak digunakan dalam industri terutama industri makanan, minuman, dan obat-obatan. Kurang lebih 60% dari total produksi asam sitrat digunakan dalam industri makanan, dan 30% digunakan dalam industri farmasi, sedangkan sisanya digunakan dalam industri pemacu rasa, pengawet, pencegah rusaknya rasa dan aroma, sebagai antioksidan, pengatur pH dan sebagai pemberi kesan rasa dingin. Asam ini biasanya dipakai untuk meningkatkan rasa asam (mengatur tingkat keasaman) pada berbagai pengolahan minum, produk air susu, selai, jeli, dan lain-lain (Bizri dan Wahem, 1994).
10 Rumus Molekul : C6H8O7 Berat Molekul : 192,12 Nama Kimia : Asam sitrat
Kandungan :Tidak kurang dari 99,5% dan tidak lebih dari 100,5% C6H8O7, dihitung terhadap zat anhidrat. Pemerian : Hablur bening; tidak berwarna atau serbuk hablur
granul sampai halus, putih; tidak berbau atau praktis tidak berbau; rasa sangat asam.
Kelarutan : Sangat mudah larut dalam air; mudah larut dalam etanol, agak sukar larut dalam eter.
Asam sitrat termasuk dalam kelompok pengasaman jika ditinjau dari fungsi pengatur keasaman. Pengatur keasaman (asidulan) merupakan senyawa kimia yang bersifat asam dan merupakan salah satu dari bahan tambahan pangan yang sengaja ditambahkan ke dalam pangan dengan berbagai tujuan. Penggunaan pengatur keasaman di dalam pangan, yaitu untuk memperoleh rasa asam yang tajam, sebagai pengontrol pH atau sebagai bahan pengawet (Cahyadi, 2012). Penambahan asam sitrat akan menurunkan pH larutan menjadi pH asam sehingga dapat meningkatkan proporsi asam yang tidak terdisosiasi yang berperan dalam pengawetan (Afrianti, 2010).
11 2.3 Spektofotometri
Spektrofotometer adalah alat untuk mengukur transmitan atau serapan suatu sampel sebagai fungsi panjang gelombang. Spektrofotometer merupakan penggabungan dari dua fungsi alat yang terdiri dari spektrometer yang menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer sebagai alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi. Jika suatu molekul sederhana dikenakan radiasi elektromagnetik maka molekul tersebut akan menyerap radiasi elektromagnetik. Interaksi antara molekul dengan radiasi elektromagnetik ini akan meningkatkan energi dari tingkat dasar ke tingkat tereksitasi (Rohman dan Gandjar, 2007).
Teknik analisis spektrofotometri berdasarkan interaksi radiasi elektromagnet dengan komponen atom atau molekul yang menghasilkan fenomena bermakna sebagai parameter analisis (Satiadarma, dkk., 2004).
Bagian molekul yang bertanggung jawab terhadap penyerapan cahaya disebut kromofor dan terdiri atas ikatan rangkap dua atau rangkap tiga, terutama jika ikatan rangkap tersebut terkonjugasi. Semakin panjang ikatan rangkap dua atau rangkap tiga terkonjugasi di dalam molekul, molekul tersebut akan lebih mudah menyerap cahaya (Cairns, 2008).
12
Radiasi ultraviolet diabsorpsi oleh molekul organik aromatik, molekul yang mengandung elektron-π terkonjugasi atau atom yang mengandung elektron -n, menyebabkan transisi elektron di orbit terluarnya dari tingkat energi elektron dasar ke tingkat energi tereksitasi lebih tinggi. Besarnya absorbansi radiasi tersebut berbanding dengan banyaknya molekul analit yang mengabsorpsi dan dapat digunakan untuk analisis kuantitatif (Satiadarma, dkk., 2004).
2.3.1 Hukum Lambert-Beer
Menurut Hukum Lambert, serapan berbanding lurus terhadap ketebalan sel yang disinari. Sedangkan menurut Beer, serapan berbanding lurus dengan konsentrasi. Kedua pernyataan ini dapat dijadikan satu dalam Hukum Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus terhadap konsentrasi dan ketebalan sel, hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan (Rohman dan Gandjar, 2007).
Hukum Lambert-Beer umumnya dikenal dengan persamaan sebagai berikut:
A = abc
Dimana: A = absorbansi a = absorptivitas b = tebal kuvet (cm) c = konsentrasi
13 gelombang radiasi (Rohman dan Gandjar, 2007). 2.3.2 Kegunaan Spektofotometri
Kegunaan spektrofotometri ultraviolet dalam analisis kualitatif sangat terbatas karena rentang daerah radiasi yang relatif sempit hanya dapat mengakomodasi sedikit sekali puncak absorpsi maksimum dan minimum, karena itu identifikasi senyawa yang tidak diketahui tidak memungkinkan untuk dilakukan (Satiadarma, dkk., 2004). Akan tetapi, jika digabung dengan cara lain seperti spektroskopi inframerah, resonansi magnet inti dan spektroskopi massa, maka dapat digunakan untuk identifikasi atau analisis kualitatif senyawa tersebut (Rohman dan Gandjar, 2007).
Metode spektrofotometri memiliki beberapa keuntungan antara lain kepekaan yang tinggi, ketelitian yang baik, mudah dilakukan, cepat pengerjaannya dan dapat digunakan untuk menentukan senyawa campuran (Munson, 1991).
Pada analisis kuantitatif dengan cara penetapan kadar, larutan standar obat yang akan dianalisis disiapkan, serapan sampel dan standar dapat ditentukan (Cairns, 2008), dimana konsentrasi zat dalam sampel dihitung dengan rumus sebagai berikut:
Ct
Cs At As =
14
Penentuan kadar senyawa organik yang mempunyai struktur kromofor atau mengandung gugus kromofor, serta mengabsorpsi radiasi ultraviolet penggunaanya cukup luas (Satiadarma, dkk., 2004).
2.4 Spektrofotometri Derivatif
Spektrofotometri deivatif berkaitan dengan transformasi spektrum serapan menjadi spektrum derivatif pertama, kedua atau spektrum derivatif dengan order
yang lebih tinggi. Spektrum derivat pertama dibuat dengan memplotkan dA / dλ
dengan panjang gelombang, derivat kedua dibuat dengan memplotkan d2A / dλ2 dengan panjang gelombang dan seterusnya (Ditjen POM, 1995).
Konsep derivatif telah diperkenalkan pertama kali pada tahun 1950, dimana terlihat memberikan banyak keuntungan. Aplikasi utama spektrofotometri derivatif ultraviolet – visibel adalah untuk identifikasi kualitatif dan analisis senyawa dalam sampel. Metode spektrofotometri derivatif sangat cocok untuk analisis pita absorpsi yang overlapping atau tumpang tindih (Owen, 1995).
15
sehingga berguna jika analit adalah dua komponen yang mengabsorpsi radiasi pada sisi pita absorpsi dari komponen yang mengganggu (Satiadarma, dkk., 2004).
Pada spektrofotometri konvensional, spektrum serapan merupakan plot serapan (A) terhadap panjang gelombang (λ). Pada spektrofotometri derivatif, plot serapan terhadap panjang gelombang dimana:
A = f (λ), order nol
dA / dλ = f ′ (λ), order pertama d2A / dλ2 = f ″ (λ), order kedua dan seterusnya ( Owen, 1995).
Menurut Talsky (1994) sesuai dengan hukum Lambert-Beer, maka ada hubungan linier antara konsentrasi dengan absorbansi untuk semua orde pada spektrofotometri derivatif adalah:
dA / dλ = x bc d²A / dλ² = x bc d A / dλ = x bc
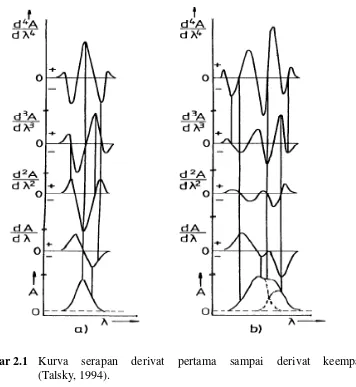
[image:34.595.111.253.442.540.2]16
Gambar 2.1 Kurva serapan derivat pertama sampai derivat keempat (Talsky, 1994).
Ada tiga aplikasi spektrofotometri derivatif yang sering digunakan dalam anlisa kuantitatif antara lain metode zero crossing, metode peak to peak dan metode multivariate spectrophotometric calibration (Talsky, 1994).
17
Panjang gelombang serapan maksimum suatu senyawa pada spektrum normal akan menjadi λ zero crossing pada spektrum derivatif pertama, panjang gelombang tersebut tidak mempunyai serapan atau dA / dλ = 0 (Munson, 1991).
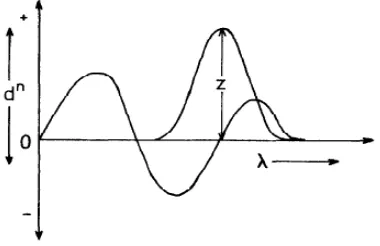
[image:36.595.213.403.394.517.2]Bila campuran analit memiliki panjang gelombang zero-crossing lebih dari satu, maka yang dipilih untuk dijadikan panjang gelombang analisis adalah panjang gelombang zero crossing yang serapan pasangannya dan campurannya persis sama, karena pada panjang gelombang tersebut dapat secara selektif mengukur serapan senyawa pasangannya dan memiliki serapan yang paling besar. Pada serapan yang paling besar, serapannya lebih stabil sehingga kesalahan analisis dapat diperkecil (Nurhidayati, 2007). Kurva sederhana aplikasi zero crossing dapat dilihat pada Gambar 2.2.
Gambar 2.2 Kurva sederhana aplikasi zero crossing (Talsky, 1994).
18 2.4.1 Komponen Spektrofotometer Derivatif
Komponen-komponen pada spektrofotometer UV-Visibel biasa sama dengan komponen pada spektrofotometer derivatif. Alat spektrofotometer harus dilengkapi dengan peralatan sedemikian rupa untuk dapat menghasilkan spektrum derivatif (Ditjen POM, 1995).
Biasanya spektrofotometer telah mempunyai software untuk mengolah data yang dapat dioperasikan malalui komputer yang telah terhubung dengan spektrofotometer. Spektrofotometri derivatif merupakan metode manipulatif terhadap spektra pada spektrofotometri UV-Visibel (Moffat, dkk., 2005).
2.4.2 Kegunaan Spektrofotometri Derivatif
Teknik spektrofotometri derivatif menawarkan beberapa keuntungan dibandingkan dengan spektrofotometri konvensional seperti Spektrum derivatif yang diukur dapat digunakan untuk meningkatkan perbedaan antara spektrum yang dianalisis, untuk menyelesaikan pita serapan analit yang tumpang tindih dalam analisis kualitatif dan yang paling penting untuk mengurangi efek interferensi dari hamburan sinar, matriks , atau senyawa menyerap lainnya dalam analisis kuantitatif (Owen, 2000).
Spektrofotometri derivatif banyak digunakan untuk zat-zat dalam suatu campuran yang spektrumnya saling mengganggu dan saling tumpang tindih atau
overlapping dimana zat-zat tersebut dapat larut dalam pelarut yang sama serta memiliki serapan maksimum pada panjang gelombang yang berdekatan (Watson, 2005).
19
informasi dari teknis lain seperti IR, NMR, MS dan digunakan untuk analisis multikomponen (Skujins and Varian, 1986).
Beberapa keuntungan dari spektrofotometri derivatif antara lain yaitu spektrum serivatif memberikan gambaran struktur yang terinci dari spektrum serapan dan gambaran ini makin jelas dari spektum derivatif pertama ke derivatif keempat (Munson, 1991).
Selain itu dapat dilakukan analisis kuantitatif suatu komponen dalam campuran dengan panjang gelombangnya saling berdekatan. Bila dibandingkan dengan kromatografi cair kinerja tinggi (KCKT), metode spektrofotometri derivatif relatif lebih sederhana, alat dan biaya operasionalnya lebih murah dan waktu analisisnya lebih cepat (Nurhidayati, 2007).
2.5 Validasi Metode Analisis
Tujuan utama yang harus dicapai dari suatu kegiatan analisis kimia adalah dihasilkannya data hasil uji yang absah (valid). Secara sederhana hasil uji yang absah dapat digambarkan sebagai hasil uji yang mempunyai akurasi (accuracy) dan presisi (precission) yang baik. Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
20
validasi adalah akurasi, presisi, limit deteksi, limit kuantitasi, kelinieran dan rentang (Rohman dan Gandjar, 2007).
2.5.1 Akurasi
Akurasi (kecermatan) adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit sebenarnya. Akurasi dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan dan dapat ditentukan melalui dua cara yaitu metode simulasi (spiked placebo recovery) dan metode penambahan bahan baku atau standard addition method (Harmita, 2004).
Dalam metode simulasi, sejumlah analit bahan murni (senyawa pembanding kimia) ditambahkan kedalam campuran bahan sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar standar yang ditambahkan atau kadar sebenarnya. Jika plasebo tidak memungkinkan untuk disiapkan, maka sejumlah analit yang telah diketahui konsentrasinya dapat ditambahkan langsung ke dalam sediaan farmasi. Ini dinamakan metode penambahan baku standar (Harmita, 2004).
21
Keterangan: CF = Kadar zat dalam sampel setelah penambahan larutan baku CA = Kadar zat dalam sampel sebelum penambahan larutan baku C A * = Kadar larutan baku zat yang ditambahkan
2.5.2 Presisi
Presisi adalah derajat kesesuaian di antara masing-masing hasil uji, jika prosedur analisis ditetapkan berulang kali pada sejumlah cuplikan yang diambil dari satu sampel homogen. Presisi dinyatakan sebagai deviasi standar atau deviasi standar relatif (Satiadarma, dkk., 2004).
Parameter-parameter seperti simpangan baku (SB), simpangan baku relatif (Relative Standard Deviation) dan derajat kepercayaan haruslah dikalkulasi untuk mendapatkan tingkat presisi tertentu (Ermer dan Miller, 2005). Nilai simpangan baku relatif dinyatakan memenuhi persyaratan jika < 10 - 20% (Ermer dan Miller, 2005).
Simpangan baku relatif = ×100%
X SB
2.5.3 Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah nilai parameter, yaitu konsentrasi analit terendah yang dapat dideteksi yang masih memberikan respon signifikan dibandingkan dengan blanko (Harmita, 2004).
Batas deteksi merupakan batas uji yang secara spesifik menyatakan apakah analit yang dianalisis berada di atas atau di bawah nilai tertentu (Rohman, 2007). Batas deteksi dapat dihitung dengan rumus sebagai berikut (Harmita, 2004):
Batas deteksi (LOD) =
slope SB x
22
Menurut Harmita (2004), batas kuantitasi adalah jumlah analit terkecil dalam sampel yang masih dapat diukur dalam kondisi percobaan yang sama dan memenuhi kriteria cermat dan seksama.
Batas kuantitasi (LOQ) =
slope SB x
10
2.5.4 Linearitas
Linieritas menunjukkan kemampuan suatu metode analisis untuk memperoleh hasil pengujian yang sesuai dengan kisaran konsentrasi analit tertentu. Hal ini dapat dilakukan dengan cara membuat kurva kalibrasi dari beberapa set larutan baku yang telah diketahui konsentrasinya. Persamaan garis yang digunakan pada kurva kalibrasi diperoleh dari persamaan y = ax + b. Persaman ini akan menghasilkan koefisien korelasi (r). Koefisien korelasi inilah yang digunakan untuk mengetahui linieritas suatu metode analisis. Kelinieran suatu metode analisis adalah kemampuan untuk menunjukkan bahwa nilai hasil uji langsung atau setelah diolah secara matematika, proporsional dengan konsentrasi analit dalam sampel dalam batas rentang konsentrasi tertentu (Satiadarma, dkk., 2004).
2.5.5 Rentang
23 BAB III
METODOLOGI PENELITIAN
3.1 Jenis Penelitian
Penelitian ini adalah penelitian deskriptif dengan metode spektrofotometri derivatif terhadap analisa 2 zat yang terkandung dalam 2 merek sampel minuman berenergi.
3.2 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara, dimulai dari April - Juli 2014.
3.3 Alat
Alat–alat yang digunakan dalam penelitian ini adalah spektrofotometer ultraviolet,
Personal Computer (PC) yang dilengkapi software UV Probe 2.3 (UV-1800
Shimadzu), neraca analitik (Mettler Toledo), kuvet, kertas saring, bola karet, spatula, alat-alat gelas dan alat-alat lainnya yang diperlukan dalam penyiapan sampel.
3.4 Bahan-bahan
24 3.5 Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif yaitu pengambilan sampel ditentukan atas dasar pertimbangan bahwa sampel yang diambil mempunyai karakteristik yang sama dengan sampel yang diteliti (Sudjana, 2005). Sampel yang digunakan pada penelitian ini adalah 2 merek minuman berenergi yaitu merek Kratingdaeng® dan Kratingdaeng-S® yang dibeli di pasar swalayan sekitar Universitas Sumatera Utara, Medan. Gambar dan komposisi sampel minuman berenergi dapat dilihat pada Lampiran 1 dan 2 halaman 66 dan 67.
3.6 Prosedur Penelitian 3.6.1 Pembuatan Pereaksi
Diencerkan 8,3 mL HCl 37% dengan 1 liter akuades (Ditjen POM, 1979). Perhitungan pembuatan pereaksi dapat dilihat pada Lampiran 5 halaman 70. 3.6.2 Pembuatan Larutan Induk Baku
3.6.2.1 Pembuatan Larutan Induk Baku Kafein
Ditimbang dengan seksama 25 mg baku pembanding kafein BPFI kemudian dimasukkan ke dalam labu tentukur 25 mL, dilarutkan dengan HCl 0,1 N hingga larut, dicukupkan volume dengan HCl 0,1 N sampai garis tanda sehingga didapatkan larutan dengan konsentrasi 1000 μg/mL (LIB I). Dari larutan LIB I dipipet 2,5 mL dimasukkan ke dalam labu tentukur 25 mL, dicukupkan dengan HCl 0,1 N sampai garis tanda sehingga didapatkan larutan dengan
25
3.6.2.2 Pembuatan Larutan Induk Baku Asam Sitrat
Ditimbang dengan seksama 250 mg baku pembanding asam sitrat kemudian dimasukkan ke dalam labu tentukur 25 mL, dilarutkan dengan HCl 0,1 N hingga larut, dicukupkan volume dengan HCl 0,1 N sampai garis tanda sehingga didapatkan larutan dengan konsentrasi 10000 μg/mL.
3.6.3 Pembuatan Spektrum Serapan Maksimum
3.6.3.1 Pembuatan Spektrum Serapan Maksimum Kafein
Dipipet 1mL Larutan Induk Baku II (LIB II) kafein (konsentrasi 100 μg/mL),
dimasukkan ke dalam labu tentukur 10 mL, diencerkan dengan HCl 0,1 N hingga garis tanda, lalu dikocok sampai homogen sehingga diperoleh larutan dengan
konsentrasi 10 μg/mL, kemudian diukur serapan pada panjang gelombang 200
-400 nm.
3.6.3.2 Pembuatan Spektrum Serapan Maksimum Asam Sitrat
Dipipet 0,5 mL Larutan Induk Baku asam sitrat (konsentrasi 10000
μg/mL), dimasukkan ke dalam labu tentukur 10 mL, diencerkan dengan HCl
0,1 N hingga garis tanda, lalu dikocok sampai homogen sehingga diperoleh
larutan dengan konsentrasi 500 μg/mL, kemudian diukur serapan pada panjang
gelombang 200-400 nm.
3.6.4 Pembuatan Spektrum Serapan Derivatif
3.6.4.1 Pembuatan Spektrum Serapan Derivatif Kafein
26
μg/mL, 6 μg/mL, 8 μg/mL, 10 μg/mL dan 12 μg/mL. Kemudian dibuat spektrum
serapan, kemudian spektrum ditransformasikan menjadi spektrum serapan derivat pertama dan derivat kedua pada panjang gelombang 200-400 nm dengan ∆λ = 4nm.
3.6.4.2 Pembuatan Spektrum Serapan Derivatif Asam Sitrat
Dipipet Larutan Induk Baku asam sitrat (konsentrasi 10000 μg/mL) sebanyak 0,2 mL; 0,3 mL; 0,4 mL; 0,5 mL dan 0,6 mL. Masing-masing dimasukkan kedalam labu tentukur 10 mL, diencerkan dengan HCl 0,1 N hingga garis tanda. Lalu dikocok sampai homogen sehingga diperoleh larutan dengan konsentrasi 200
μg/mL, 300 μg/mL, 400 μg/mL, 500 μg/mL dan 600 μg/mL. Kemudian dibuat
spektrum serapan, kemudian spektrum ditransformasikan menjadi spektrum serapan derivat pertama dan derivat kedua pada panjang gelombang 200-400 nm dengan ∆λ = 4nm.
3.6.5 Penentuan Zero Crossing
Penentuan zero crossing diperoleh dengan menumpangtindihkan spektrum serapan kafein dan asam sitrat dari berbagai konsentrasi larutan. Zero Crossing setiap spektrum serapan kafein dan asam sitrat ditunjukkan oleh panjang gelombang yang memiliki serapan nol pada berbagai konsentrasi.
3.6.6 Penentuan Panjang Gelombang Analisis
Dibuat larutan kafein dengan konsentrasi 10 μg/mL dan larutan asam
sitrat dengan konsentrasi 500 μg/mL, serta larutan campuran kafein (konsentrasi
27
Spektrum serapan kafein dan asam sitrat serta campuran kafein dan asam sitrat ditumpangtindihkan. Panjang gelombang analisis yang dipilih adalah pada saat serapan senyawa pasangannya nol dan serapan maksimum kafein dan asam sitrat serta dan campuran kafein dan asam sitrat hampir sama atau persis sama, karena pada panjang gelombang tersebut dapat secara selektif mengukur serapan kafein dan asam sitrat.
3.6.7 Pembuatan dan Penentuan Linearitas Kurva Kalibrasi Kafein dan Asam Sitrat
Dibuat larutan baku kafein dengan konsentrasi 4 μg/mL, 6 μg/mL, 8 μg/mL,
10 μg/mL dan 12 μg/mL. Kemudian diukur serapan derivat kedua kafein pada
panjang gelombang analisis kafein. Prosedur yang sama dilakukan juga pada asam sitrat. Dibuat larutan baku asam sitrat dengan konsentrasi 200 μg/mL, 300
μg/mL, 400 μg/mL, 500 μg/mL dan 600 μg/mL. Kemudian diukur serapan derivat
kedua asam sitrat pada panjang gelombang analisisnya. Ditentukan persamaan regresi linier kafein dan asam sitrat y = ax + b. Berdasarkan nilai serapan pada masing-masing panjang gelombang analisis kafein dan asam sitrat, dilakukan perhitungan limit deteksi (limit of detection, LOD) dan limit kuantitasi (limit of quantitation, LOQ). Untuk menentukan (LOD) dan (LOQ) dapat digunakan rumus (Harmita, 2004).
28 Keterangan : SB = Simpangan baku
LOD = Limit Of Detection, Batas deteksi
LOQ = Limit Of Quantitation, Batas kuantitasi
3.6.8 Penentuan Kandungan Kafein dan Asam Sitrat dalam Minuman Berenergi
Untuk penentuan kadar kandungan kafein dan asam sitrat digunakan dua merek minuman berenergi masing-masing sebanyak 6 botol dengan volume 150 mL/botol. Sebanyak 25 mL larutan diambil dari masing-masing botol kemudian disaring, lebih kurang 10 mL filtrat pertama dibuang, dan filtrat selanjutnya ditampung (larutan sampel).
3.6.8.1Penentuan Kandungan Kafein dalam Minuman Berenergi
Dipipet sebanyak 0,3 mL larutan sampel ke dalam labu tentukur 25 mL dan dicukupkan dengan larutan HCl 0,1 N lalu dikocok sampai homogen. Larutan kemudian diukur absorbansinya pada serapan derivat kedua dengan panjang gelombang analisis kafein 293,60 nm. Berdasarkan hasil pengukuran absorbansi kafein pada panjang gelombang analisisnya, ditentukan konsentrasi kafein dengan menggunakan persamaan garis regresinya. Selanjutnya Kadar kafein dalam sampel dapat dihitung dengan rumus:
Kadar (µg/mL) =
29 thitung =
Data diterima jika t hitung< t tabel.Tabel distribusi t dapat dilihat pada Lampiran 26
di halaman 136.
Untuk menghitung simpangan baku (SB) digunakan rumus (Sudjana, 2005): SB =
Keterangan : X = Kadar kandungan zat dalam sampel
= Kadar kandungan zat rata-rata sampel n = jumlah pengulangan
Untuk menentukan kadar kandungan kafein sebenarnya dalam sampel dengan
interval kepercayaan 99%, α = 1%, dk = n-1, dapat digunakan rumus (Sudjana,
2005):
Kadar kandungan zat : µ = (α/2, dk) x SB/ )
Keterangan : µ : Kadar kandungan sebenarnya
: Kadar kandungan zat rata-rata sampel SB : Simpangan baku
dk : derajat kebebasan (dk = n-1)
t : harga t tabel sesuai dengan dk = n-1
α : tingkat kepercayaan n : jumlah pengulangan
3.6.8.2Penentuan Kandungan Asam Sitrat dalam Minuman Berenergi
30
absorbansi asam sitrat pada panjang gelombang analisnya, ditentukan konsentrasi asam sitrat dengan menggunakan persamaan garis regresi. Karena absorbansi asam sitrat dalam sampel yang didapat negatif, maka dilanjutkan dengan teknik penambahan baku asam sitrat dalam sampel. Disediakan 12 buah labu ukur 25 ml kemudian dipipet 0,3 mL masing-masing sampel kedalam labu ukur lalu ditambahkan 1,25 mL larutan Induk Baku asam sitrat (10000 μg/mL) yang setara dengan konsentrasi 500 μg/mL. Dicukupkan volume dengan larutan HCl 0,1 N lalu dikocok sampai homogen. Sebagai pembanding hasil serapan asam sitrat dalam sampel setelah penambahan baku asam sitrat, dilakukan juga penambahan baku dengan konsentrasi yang berbeda dengan cara yang sama ditambahkan 1,5 mL larutan induk baku asam sitrat (10000 μg/mL) yang setara dengan konsentrasi 600 μg/mL ke dalam labu ukur 25 mL. Dicukupkan volume dengan larutan HCl 0,1 N lalu dikocok sampai homogen. Kemudian diukur absorbansi asam sitrat pada serapan derivat kedua dengan panjang gelombang 236,0 nm.
Berdasarkan hasil pengukuran absorbansi asam sitrat pada panjang gelombang analisisnya, ditentukan konsentrasi asam sitrat menggunakan persamaan garis regresi. Kadar asam sitrat dapat dihitung dengan rumus:
Kadar (µg/ml) =
Kandungan asam sitrat yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis untuk mengetahui data ditolak atau diterima menggunakan uji distribusi t dengan rumus:
thitung =
31 di halaman 136.
Untuk menghitung simpangan baku (SB) digunakan rumus (Sudjana, 2005):
SB =
Keterangan : X = Kadar kandungan zat dalam sampel
= Kadar kandungan zat rata-rata dalam sampel n = jumlah pengulangan
Untuk menentukan kadar kandungan asam sitrat sebenarnya dalam sampel dengan
interval kepercayaan 99%, α = 1%, dk = n-1, dapat digunakan rumus (Sudjana,
2005):
Kadar kandungan zat : µ = (α/2, dk) x SB/ )
Keterangan : µ : Kadar kandungan zat sebenarnya : Kadar kandungan zat rata-rata dalam sampel SB : Simpangan baku
dk : derajat kebebasan (dk = n-1) t : harga t tabel sesuai dengan dk = n-1
α : tingkat kepercayaan n : jumlah pengulangan
3.6.9 Uji Validasi
Uji validasi yang dilakukan pada penelitian ini menggunakan uji akurasi dengan parameter persen (%) perolehan kembali menggunakan metode penambahan baku (standard addition method) dan uji presisi dengan parameter simpangan baku relatif (Relative Standard Deviation, RSD).
32
Sebanyak 25 mg serbuk kafein dilarutkan dengan HCL 0,1 N dalam labu ukur 25 mL (konsentrasi 1000 μg/mL). Sebanyak 250 mg serbuk asam sitrat dilarutkan dengan HCL 0,1 N dalam labu ukur 25 mL (konsentrasi 10000 μg/mL). Dipipet sebanyak 0,3 mL masing-masing sampel, ditambahkan dengan 1,25 mL larutan baku asam sitrat yang setara dengan konsentrasi 500 μg/mL ke dalam labu ukur 25 mL.
Untuk uji akurasi, ditambahkan larutan baku kafein dan asam sitrat masing-masing sebanyak 1 mL dan 0,5 mL ke dalam sampel. Selanjutnya volume dicukupkan dengan HCL 0,1 N sampai garis tanda. Serapan diukur dengan menggunakan spektrofotometer UV. Hasil spektrum ditransformasikan menjadi
derivat kedua dengan Δλ = 4 nm, kemudian dihitung persen perolehan kembali
berdasarkan nilai absorbansi kafein dan asam sitrat pada masing-masing panjang gelombang analisis.
Persen perolehan kembali dapat dihitung dengan rumus (Harmita, 2004).
% perolehan kembali = 100%
Keterangan: CF = Kadar zat dalam sampel setelah penambahan larutan baku CA = Kadar zat dalam sampel sebelum penambahan larutan baku
C*A= Kadar larutan baku zat yang ditambahkan 3.6.9.2 Uji Presisi
33
Berdasarkan hasil perolehan kembali kafein dan asam sitrat ditentukan simpangan baku kafein dan asam sitrat. Untuk menghitung simpangan baku (SB) digunakan rumus (Sudjana, 2005):
SB =
Keterangan : X = Kadar kandungan zat dalam sampel
= Kadar kandungan zat rata-rata dalam sampel n = jumlah pengulangan
Berdasarkan nilai simpangan baku yang didapat, dihitung simpangan baku relatif (Relative Standard Deviation, RSD) kafein dan asam sitrat. Simpangan baku relatif dapat dihitung dengan rumus di bawah ini :
RSD = x 100%
Keterangan : = Kadar kandungan rata-rata zat dalam sampel SB = Simpangan baku
34 BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil Penentuan Kurva Serapan Maksimum
Penentuan kurva serapan maksimum dilakukan pada panjang gelombang 200–400 nm. Pengukuran kafein dan asam sitrat dilakukan pada konsentrasi 10
μg/mL dan konsentrasi 500 μg/mL secara berturut-turut. Berdasarkan hasil
penelitian, diperoleh serapan maksimum kafein baku pada panjang gelombang 272,60 nm. Panjang gelombang tersebut mendekati panjang gelombang kafein pada serapan maksimum menurut Moffat, dkk., (2005), yaitu 273 nm. Sedangkan serapan maksimum asam sitrat didapat pada gelombang 208,20 nm tidak berbeda jika dibandingkan dengan panjang gelombang asam sitrat pada serapan maksimum yang diperoleh dari penelitian sebelumnya yaitu 208,0 nm (Sari, 2014). Kurva serapan maksimum kafein konsentrasi 10 μg/mL dan asam sitrat konsentrasi 500 μg/mL dapat dilihat pada Gambar 4.1 dan Gambar 4.2.
nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
1.55882
1.00000
0.50000
0.00000
35 nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
0.56764
0.40000
0.20000
36
[image:55.595.117.490.180.389.2]tindih serapan kafein, serapan derivat pertama kafein dan serapan derivat kedua kafein dalam berbagai konsentrasi, masing-masing dapat dilihat pada Gambar 4.3, Gambar 4.4 dan Gambar 4.5.
nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
2.50163
2.00000
1.50000
1.00000
0.50000
37
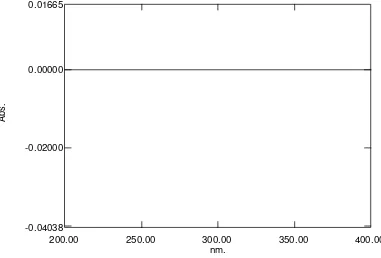
nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
0.01665
0.00000
-0.02000
38
dengan konsentrasi 200 μg/mL; 300 μg/mL; 400 μg/mL; 500 μg/mL dan 600
μg/mL dapat dilihat pada Lampiran 9 halaman 87 - 89. Kurva tumpang tindih
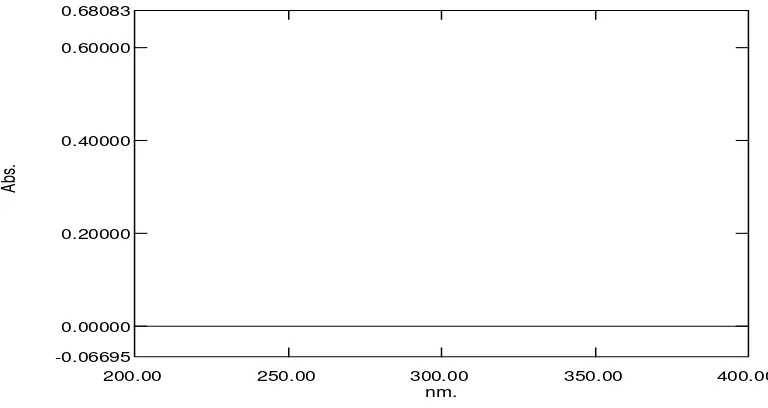
[image:57.595.115.499.222.426.2]serapan asam sitrat, serapan derivat pertama asam sitrat dan serapan derivat kedua asam sitrat dalam berbagai konsentrasi, masing-masing dapat dilihat pada Gambar 4.6, Gambar 4.7 dan Gambar 4.8.
nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
0.68083
0.60000
0.40000
0.20000
0.00000
39 nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
0.00209
0.00000
-0.00200
40 nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
0.09317
0.05000
0.00000
-0.05000
-0.10000
41 Gambar 4.11 dan Gambar 4.12.
nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
0.01665
0.00000
-0.02000
42
Berdasarkan gambar 4.9 sampai Gambar 4.12 diatas, didapatkan panjang gelombang zero crossing dari masing- masing kafein dan asam sitrat pada derivat pertama dan kedua yang selanjutnya ditumpangtindihkan untuk menentukan panjang gelombang analisis.
4.5 Hasil Penentuan Panjang Gelombang Analisis Kafein dan Asam Sitrat
Penentuan panjang gelombang analisis dilakukan berdasarkan pengamatan pada kurva serapan masing-masing derivat, kemudian dilanjutkan dengan pengukuran absorbansi pada masing-masing zero crossing. Panjang gelombang analisis ditentukan dengan cara menumpangtindihkan spektrum serapan dari kafein, asam sitrat dan campuran kafein dan asam sitrat. Selanjutnya ditentukan panjang gelombang dimana pita serapan salah satu zat berada pada serapan nol, sedangkan pita serapan zat lain memiliki nilai positif dan tumpang tindih dengan pita serapan campuran dari kedua zat.
Kurva serapan, kurva serapan derivat pertama, kurva serapan derivat kedua dari campuran kafein konsentrasi 10 μg/mL dan asam sitrat konsentrasi 500
μg/mL dapat dilihat pada Gambar 4.13, Gambar 4.15, dan Gambar 4.19. Kurva
tumpang tindih serapan, serapan derivat pertama, serapan derivat kedua dari kafein konsentrasi 10 μg/mL dan asam sitrat konsentrasi 500 μg/mL dapat dilihat pada Gambar 4.14, Gambar 4.17, dan Gambar 4.20. Kurva tumpang tindih serapan, serapan derivat pertama, serapan derivat kedua dari kafein konsentrasi 10
μg/mL, asam sitrat konsentrasi 500 μg/mL dan campuran kafein konsentrasi 10
μg/mL dan asam sitrat konsentrasi 500 μg/mL dapat dilihat pada Gambar 4.15,
43 nm.
200.00 250.00 300.00 350.00 400.00
Abs
.
1.55882
1.00000
0.50000
44 nm.
200.00 250.00 300.00 350.00 400.00
Abs
.
0.05054
0.00000
-0.05000
45 nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
0.00978
0.00000
-0.01000
46
nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
0.01126
0.00000
-0.01000
47
nm.
200.00 250.00 300.00 350.00 400.00
A
bs
.
0.01126
0.00000
-0.01000
48
Berdasarkan gambar diatas, diperoleh panjang gelombang yang dapat dipakai untuk penentuan kandungan campuran kafein dan asam sitrat adalah pada serapan derivat kedua. Hal tersebut diketahui berdasarkan pemilihan panjang gelombang analisis pada setiap derivat. Panjang gelombang analisis didapatkan dengan menentukan zero crossing untuk kafein dan asam sitrat.
Panjang gelombang analisis ditentukan dengan cara menumpangtindihkan spektrum derivat dari kafein dan asam sitrat. Selanjutnya ditentukan panjang gelombang dimana absorbansi salah satu zat berada pada nilai nol, sedangkan zat lain memiliki nilai positif. Pada serapan derivat pertama, zero crossing untuk kafein ditemukan pada panjang gelombang 205,0 nm; 245,20 nm; 272,20 nm dan 302,40 nm dan asam sitrat pada panjang gelombang 209,40 nm; 258,80 nm dan 302,16 nm. Pada serapan derivat pertama, panjang gelombang analisis untuk kafein dapat ditemukan. Namun panjang gelombang analisis untuk asam sitrat tidak ditemukan, sehingga penentuan kandungan zat dalam sampel tidak bisa dilakukan pada derivat pertama. Oleh karena itu dibuat spektrum serapan derivat kedua, kemudian dilakukan penentuan panjang gelombang analisis dengan cara yang sama seperti pada derivat pertama.
49
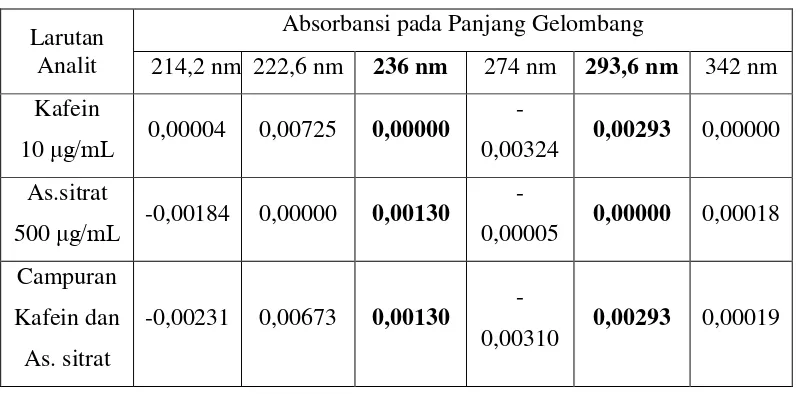
analisis dan absorbansi pada derivat kedua dapat dilihat pada Tabel 4.1. Tab el 4.1 Panjang Gelombang Analisis dan Absorbansi pada Derivat Kedua
Larutan Analit
Absorbansi pada Panjang Gelombang
214,2 nm 222,6 nm 236 nm 274 nm 293,6 nm 342 nm Kafein
10 μg/mL 0,00004 0,00725 0,00000
-0,00324 0,00293 0,00000 As.sitrat
500 μg/mL -0,00184 0,00000 0,00130
-0,00005 0,00000 0,00018 Campuran
Kafein dan As. sitrat
-0,00231 0,00673 0,00130
-0,00310 0,00293 0,00019
Berdasarkan Tabel 4.1 diperoleh panjang gelombang analisis kafein adalah 222,6 nm; 274 nm; 293,6 nm dan Panjang gelombang analisis asam sitrat adalah 214,2 nm; 236,0 nm; 342,0 nm.
[image:68.595.113.515.129.326.2]50
adalah nol, sedangkan nilai absorbansi untuk asam sitrat dan larutan campuran keduanya memiliki nilai serapan sama yaitu 0,00130, sehingga untuk asam sitrat panjang gelombang analisisnya adalah pada 236,0 nm. Panjang gelombang analisis kafein yang dipakai adalah 293,60 nm karena pada panjang gelombang tersebut, nilai serapan kafein dan campuran kafein dengan asam sitrat memiliki kedekatan yang lebih tinggi dibandingakan dengan nilai serapan pada panjang gelombang zero crossing kafein yang lain yaitu 222,6 nm dan 274 nm. Pada panjang gelombang analisis kafein 293,60 nm, nilai absorbansi dari asam sitrat adalah nol, sedangkan nilai absorbansi untuk kafein dan larutan campuran kafein dan asam sitrat memiliki nilai serapan sama yaitu 0,00293. Spektrum dan absorbansi kafein dan asam sitrat dapat dilihat pada Lampiran 10 halaman 91 - 92. Hasil pengukuran serapan derivat kedua kafein, asam sitrat dan campuran kafein dan asam sitrat pada panjang gelombang 200-300 nm dapat dilihat pada Lampiran 11 halaman 93 – 97.
4.6 Hasil Penentuan Linearitas Kurva Kalibrasi 4.6.1Kurva Kalibrasi
51
Standard Curve
Conc. (mg/l)
0.00000 5.00000 10.00000 15.00000
Ab
s
.
0.00400
0.00300
0.00200
0.00100
52
konsentrasi 10 μg/mL dan asam sitrat dengan konsentrasi 500 μg/mL dapat terdeteksi dan terukur menggunakan metode spektrofotometri derivatif.
Batas deteksi merupakan parameter uji batas yang dilakukan untuk mendeteksi jumlah terkecil analit dalam sampel yang masih memberikan respon signifikan dengan blanko sedangkan batas kuantitasi merupakan kuantitas terkecil analit yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
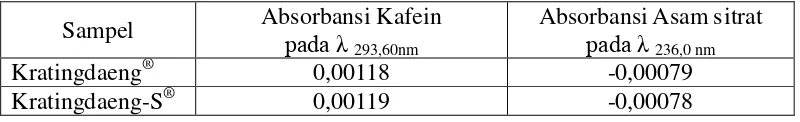
4.7 Hasil Penentuan Kandungan Kafein dan Asam Sitrat dalam Sampel Minuman Berenergi
Seperti yang tertera pada komposisi label kemasan minuman berenergi merek Kratingdaeng® dan Kratingdaeng-S® mengandung kafein dengan kadar 50 mg per sajiannya sedangkan kadar kandungan asam sitrat tidak dicantumkan pada label kemasan tersebut.
Sampel yang telah disiapkan kemudian diukur pada panjang gelombang 200 – 400 nm. Selanjutnya spektrum hasil serapan ditransformasikan menjadi spektrum
serapan derivat kedua dengan Δλ = 4 nm. Berdasarkan spektrum tersebut dapat