PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2013
PENGEMBANGAN DAN VALIDASI METODE
KROMATOGRAFI CAIR KINERJA TINGGI PADA
PENETAPAN KADAR ASPARTAM DALAM MINUMAN
RINGAN YANG BEREDAR DI KOTAMADYA MEDAN
SKRIPSI
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2013
PENGEMBANGAN DAN VALIDASI METODE
KROMATOGRAFI CAIR KINERJA TINGGI PADA
PENETAPAN KADAR ASPARTAM DALAM MINUMAN
RINGAN YANG BEREDAR DI KOTAMADYA MEDAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi Universitas
Sumatera Utara
PENGESAHAN SKRIPSI
PENGEMBANGAN DAN VALIDASI METODE
KROMATOGRAFI CAIR KINERJA TINGGI PADA
PENETAPAN KADAR ASPARTAM DALAM MINUMAN
RINGAN YANG BEREDAR DI KOTAMADYA MEDAN
OLEH:
ALFADES
NIM 091501032
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 27 Juli 2013
Pembimbing I,
Drs. Syafruddin, M.S., Apt. NIP 194811111976031003
Pembimbing II,
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195201041980031002
Panitia Penguji,
Prof. Dr. rer. nat. Effendy D.L.P., S.U., Apt. NIP 195306191983031001
Drs. Syafruddin, M.S., Apt. NIP 194811111976031003
Dra. Salbiah, M.Si., Apt. NIP 194810031987012001
Dra. Nurmadjuzita, M.Si., Apt. NIP 194809041974122001
Medan,
Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat
kasih dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini yang
berjudul ” Pengembangan dan Validasi Metode Kromatografi Cair Kinerja Tinggi
pada Penetapan Kadar Aspartam dalam Minuman Ringan yang Beredar di
Kotamadya Medan”. Skripsi ini diajukan sebagai salah satu syarat untuk
memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatera
Utara.
Pada kesempatan ini penulis menyampaikan ucapan terimakasih kepada
Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara yang telah memberikan fasilitas selama masa
pendidikan. Bapak Drs. Syafruddin, M.S., Apt., dan Drs. Fathur Rahman Harun,
M.Si., Apt., selaku pembimbing yang telah memberikan waktu, bimbingan dan
nasehat selama penelitian hingga selesainya penyusunan skripsi ini. Ibu Poppy
Anjelisa Zaitun Hasibuan, S.Si., M.Si., Apt., selaku penasehat akademik yang
memberikan bimbingan kepada penulis selama menempuh pendidikan di Fakultas
Farmasi. Bapak dan Ibu staf pengajar Fakultas Farmasi Universitas Sumatera
Utara yang telah mendidik selama perkuliahan. Bapak Kepala Laboratorium
Penelitian dan Staf-Staf Laboratorium Penelitian yang telah memberikan fasilitas,
petunjuk dan membantu selama penelitian. Bapak Prof. Dr. rer. nat. Effendy De
Lux Putra S.U., Apt., Dra. Salbiah, M.Si., Apt., Dra. Nurmadjuzita, M.Si., Apt.,
selaku dosen penguji yang memberikan masukan, kritik, arahan dan saran dalam
Penulis juga ingin mempersembahkan rasa terima kasih yang tak terhingga
kepada Ayahanda R. Tampubolon dan Ibunda M.D br Siagian atas doa dan
pengorbanannya dengan tulus dan ikhlas, untuk abang dan adik tersayang dan
teman-teman Sains dan Teknologi Farmasi 2009 yang selalu setia memberi doa,
dorongan dan semangat.
Penulis menyadari bahwa skripsi ini masih banyak kekurangannya, oleh
karena itu sangat diharapkan kritik dan saran yang bersifat membangun dari
semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga
skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang farmasi.
Medan, Penulis,
Alfades
PENGEMBANGAN DAN VALIDASI METODE KROMATOGRAFI CAIR KINERJA TINGGI PADA PENETAPAN KADAR ASPARTAM DALAM
MINUMAN RINGAN YANG BEREDAR DI KOTAMADYA MEDAN
Abstrak
Minuman ringan merupakan produk minuman yang banyak dikonsumsi masyarakat. Biasanya mengandung aspartam yang mempunyai tingkat kemanisan 200-400 kali sukrosa, sehingga sering ditambahkan dalam produk minuman ringan dengan tujuan penghematan biaya produksi. Dikeluarkannya pedoman persyaratan penggunaan pemanis buatan pada produk pangan oleh Badan POM RI memberikan konsekuensi akan perlunya suatu metode analisis yang praktis, akurat dan teliti. Peneliti sebelumnya telah melakukan penetapan kadar aspartam dalam minuman ringan secara Kromatografi Cair Kinerja Tinggi dengan perbandingan fase gerak asetonitril : dapar fosfat pH 2,6 (17,5:82,5) dengan laju alir 1,2 ml/menit menggunakan kolom Shimpac VP-ODS (150 mm x 4,6 mm) dan dektektor UV/Vis tetapi tidak disebutkan waktu retensinya; pada pH 3,5 (15:85) dengan laju alir 1,5 ml/menit menggunakan kolom Shimpac VP-ODS (150 mm x 4,6 mm) dan detektor PDA dengan waktu retensi 4,0 menit; dan pada pH 6,0 (15:85) dengan laju alir 1,4 ml/menit menggunakan kolom Shimpac XR-ODS (50 mm x 3,0 mm) dan detektor UV/Vis dengan waktu retensi 1,15 menit. Tujuan penelitian ini adalah untuk mengembangkan suatu metode alternatif pada penetapan kadar aspartam dalam minuman ringan secara Kromatografi Cair Kinerja Tinggi menggunakan kolom Shimpac VP-ODS (250 mm x 4,6 mm) dengan detektor UV/Vis.
Dalam pengembangan metode ini, dilakukan penentuan panjang gelombang, pemilihan pH fase gerak dan komposisi fase gerak untuk mendapatkan kondisi analisis yang optimum. Uji validasi dilakukan terhadap parameter akurasi, presisi, batas deteksi dan batas kuantitasi untuk menjamin kualitas dari metode analisis.
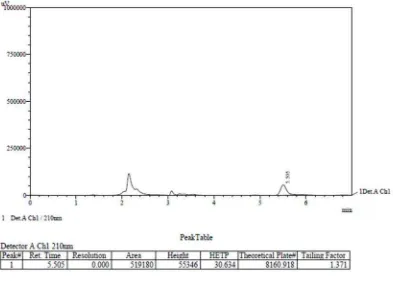
Hasil optimasi diperoleh kondisi analisis yang optimal menggunakan fase gerak asetonitril : dapar fosfat pH 4,3 dengan perbandingan 20 : 80, laju alir 1,2 ml/menit pada panjang gelombang 210 nm dengan waktu retensi 5,5 menit. Dari hasil uji validasi metode diperoleh persen recovery 102,85% dan RSD 0,28%, ini menunjukkan bahwa metode memiliki akurasi dan presisi yang baik dengan batas deteksi (LOD) 7,54 µ g/ml dan batas kuantitasi (LOQ) 25,14 µ g/ml. Dari hasil penelitian ini diperoleh kadar Aspartam dalam Nutri Sari 391,31 ± 8,48 mg/kg, Okki Koko Drink 95,97 ± 1,42 mg/kg, Ale-ale 31,39 ± 0,42 mg/kg, Jas Jus 128,86 ± 0,88 mg/kg dan Frutang 87,45 ± 1,37 mg/kg. Dapat disimpulkan bahwa kandungan aspartam dalam semua sampel minuman ringan masih memenuhi persyaratn menurut SNI 01-6993,2004, yaitu 600 mg/kg.
Kata kunci: aspartam, minuman ringan, kromatografi cair kinerja tinggi,
DEVELOPMENT AND VALIDATION OF HIGH PERFORMANCE LIQUID CHROMATOGRAPHY METHOD IN THE DETERMINATION
OF ASPARTAME IN SOFT DRINK THAT CIRCULATE IN MEDAN
Abstract
Soft drinks are a beverage product that almost consumed by the people. Commonly softdrink contain aspartame which has 200 – 400 times sweetness of sucrose, so it is usually added in soft drink products to economize the production cost. The exit of alternative sweetener guideline requirement in food product by BPOM RI gives a consequence the need of a practical, accurate and thorough analytical method. Previous researchers have done the determination of aspartame concentration in soft drink by High Performance Liquid Chromatography with mobile phase ratio of acetonitrile: phosphate buffer pH 2.6 (17.5:82.5) in flow rate 1.2 ml/min using Shimpac colomn VP-ODS (150 x 4.6 mm) with UV/Vis detector, but it wasn’t mentioned the retention time; in pH 3.5 (15:85) with flow rate 1.5 ml/min using Shimpac colomn VP-ODS (150 x 4.6 mm) with PDA detector, it was obtained retention time 4.0 min; and in pH 6.0 (15:85) with flow rate 1.4 ml/min using Shimpac XR-ODS (50 x 3.0 mm) with UV/Vis detector, it was obtained retention time 1.15 min. The purpose of this research is to develop an alternative analysis method that can be used in determination of aspartame concentration using High Performance Liquid Chromatography using Shimpac colomn VP-ODS (250 x 4.6 mm) with UV/Vis detector.
On this development method, need to be wavelength parameter, pH of mobile phase and the ratio of mobile phase to could optimum analithical method. Validation test was done against accuracy and precission parameters, limit of detection and limit of quantitation to guarantee quality of analithical method.
Optimization result obtained optimum analytical condition in mobile phase acetonitrile : phosphate buffer pH 4.3 with ratio of mobile phase 20 : 80, flow rate 1.2 ml/min in 210 nm wavelength with retention time 5.5 min. From the validation test result, it was obtained recovery 102,85% and RSD 0.28%, it was indicated that this method had a good accuracy and precission with limit of detection (LOD) 7.54 µ g/ml and limit of quantitation (LOQ) 25.14 µ g/ml. From this research result, it was obtained that aspartame concentration in Nutri Sari was 392.31 ± 8.48 mg/kg, Okki Koko Drink 95.97 ± 1.42 mg/kg, Ale-ale 31.39 ± 0.42 mg/kg, Jas Jus 128.86 ± 0.88 mg/kg dan Frutang 87.45 ± 1.37 mg/kg. It can be seen that concentration of aspartame in all of the soft drink samples were still fulfilled with Indonesian National Standard 01-6993, 2004 (600 mg/kg).
Keywords: aspartame, soft drink, high performance liquid chromatography,
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ANSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xx
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 5
1.5 Manfaat Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Bahan Tambahan Pangan ... 6
2.2 Pembagian Pemanis ... 7
2.2.1 Pemanis Alami ... 7
2.2.2 Pemanis Buatan ... 7
2.3.1 Sifat Fisika dan Kimia ... 8
2.3.2 Sinonim ... 10
2.3.3 Sintesis ... 10
2.3.4 Metabolisme ... 11
2.3.5 Toksisitas ... 11
2.3.6 Metode Analisis Lain untuk Penetapan Kadar 12
Aspartam ... 2.4 Kromatografi ... 12
2.4.1 Sejarah Kromatografi ... 12
2.4.2 Klasifikasi Kromatografi ... 13
2.5 Kromatografi Cair Kinerja Tinggi ... 15
2.5.1 Jenis KCKT ... 15
2.5.2 Proses Pemisahan dalam Kolom Kromatografi Cair 15
2.5.3 Parameter Penting dalam Kromatografi Cair ... 17
2.5.4 Instrumen Kromatografi Cair Kinerja Tinggi ... 22
2.6 Validasi Metode ... 26
2.6.1 Akurasi (Kecermatan) ... 27
2.6.2 Presisi (Keseksamaan) ... 28
2.6.3 Spesifitas (Selektifitas) ... 28
2.6.4 Batas Deteksi dan Batas Kuantitasi ... 28
2.6.5 Linearitas ... 28
2.6.6 Rentang (Kisaran) ... 28
2.6.7 Kekuatan (Ketahanan) ... 29
2.6.8 Kekasaran (Ketangguhan) ... 29
3.1 Tempat dan Waktu Penelitian ... 30
3.2 Alat-alat ... 30
3.3 Bahan-bahan ... 30
3.4 Sampling Minuman Ringan ... 31
3.5 Pembuatan Fase Gerak ... 31
3.5.1 Pembuatan Dapar Fosfat 10 mM KH2PO4 (pH 2,6) . 31 3.5.2 Pembuatan Dapar Fosfat 12,5 mM KH2PO4 (pH 3,5) 31 3.5.3 Pembuatan Dapar Fosfat 41,2 mM KH2PO4 (pH 4,3) 32 3.5.4 Pembuatan Dapar Fosfat 22 mM KH2PO4 / 3 mM K2HPO4 (pH 6,0) ... 32
3.5.5 Pembuatan Fase Gerak Asetonitril ... 32
3.6 Prosedur Analisis ... 33
3.6.1 Pembuatan Pelarut ... 33
3.6.2 Pembuatan Larutan Sampel ... 34
3.6.3 Penyiapan Alat KCKT ... 34
3.6.4 Penentuan Panjang Gelombang ... 34
3.6.5 Optimasi pH Fase Gerak ... 35
3.6.6 Optimasi Komposisi Fase Gerak ... 35
3.6.7 Analisis Kualitatif ... 35
3.6.8 Analisis Kuantitatif ... 36
3.7 Validasi Metode ... 37
3.7.1 Akurasi ... 37
3.7.2 Presisi ... 38
3.7.3 Batas Deteksi dan Batas Kuantitasi ... 38
BAB IV HASIL DAN PEMBAHASAN ... 41
4.1 Optimasi ... 41
4.1.1 Penetuan Panjang Gelombang ... 41
4.1.2 Optimasi pH Fase Gerak ... 42
4.1.3 Optimasi Komposisi Fase Gerak ... 43
4.2 Analisis Kualitatif ... 44
4.3 Analisis Kuantitatif ... 46
4.3.1 Penentuan Kurva Kalibrasi ... 46
4.3.2 Penetapan Kadar Analit pada Sampel yang Dianalisis ... 46 4.4 Hasil Uji Validasi ... 47
BAB V KESIMPULAN DAN SARAN 49 5.1 Kesimpulan ... 49
5.2 Saran ... 49
DAFTAR PUSTAKA ... 50
DAFTAR TABEL
Halaman
Tabel 1. Data optimasi Aspartam BPFI pada sistem KCKT dengan fase gerak asetonitril : dapar fosfat dengan berbagai variasi
pH ... 43
Tabel 2. Data optimasi Aspartam BPFI dan sampel pada sistem KCKT dengan fase gerak asetonitril : dapar fosfat pH 4,3
dengan perbandingan yang berbeda ... 44
Tabel 3. Hasil penetapan kadar aspartam dalam minuman ringan ... 47
Tabel 4. Hasil pengujian validasi dengan parameter akurasi, presisi, batas deteksi (LOD) dan batas kuantitasi (LOQ) aspartam pada minuman ringan Okki Koko Drink dengan
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur kimia dari aspartam ... 8
Gambar 2. Prinsip konversi produk aspartam ... 9
Gambar 3. Stabilitas aspartam dalam larutan dapar pada suhu 25 °C 9
Gambar 4. Reaksi sintesis pembentukan aspartam ... 10
Gambar 5. Diagram metabolisme aspartam ... 11
Gambar 6. Pengelompokkan kromatografi secara umum ... 14
Gambar 7. Ilustrasi proses pemisahan yang terjadi di dalam kolom KCKT ... 16
Gambar 8. Kromatogram yang diperoleh dari analisis KCKT ... 17
Gambar 9. Tiga jenis puncak ... 21
Gambar 10. Pengukuran derajat asimetris puncak ... 21
Gambar 11. Sistem KCKT secara skematik yang menunjukkan semua komponen utamanya dan gambaran grafis suatu sistem KCKT isokratik ... 22
Gambar 12. Tipe injektor katup putaran ... 24
Gambar 13. Spektrum panjang gelombang aspartam ... 41
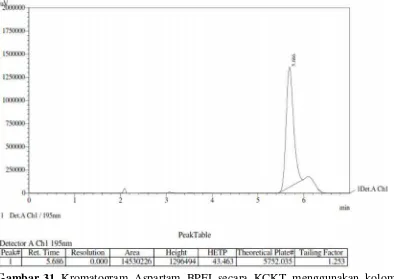
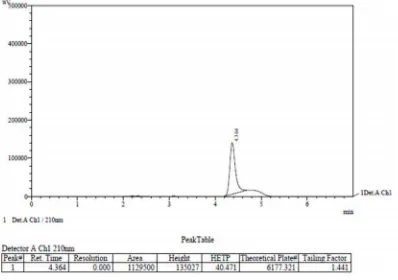
Gambar 14. Kromatogram sampel (Okki Koko Drink) sebelum penambahan baku secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 45
Gambar 16. Kurva kalibrasi Aspartam BPFI KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan
didteksi pada panjang gelombang 210 nm ... 46
Gambar 17. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 2,6 (15:85), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 54
Gambar 18. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 2,6 (17,5:82,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 54
Gambar 19. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 2,6 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 55
Gambar 20. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 2,6 (22,5:77,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 55
Gambar 21. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 3,5 (15:85), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 56
Gambar 22. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 3,5 (17,5:82,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 56
Gambar 24. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 3,5 (22,5:77,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan
dideteksi pada panjang gelombang 210 nm ... 57
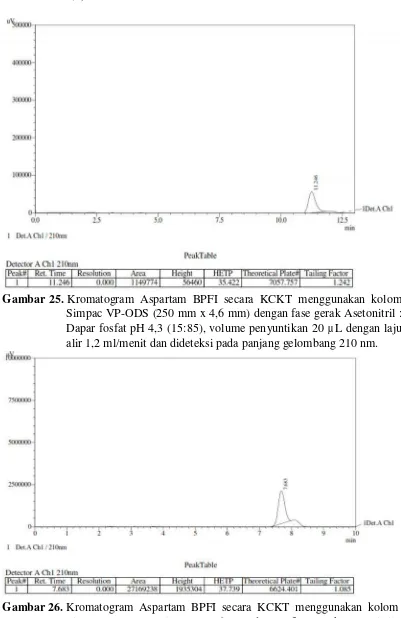
Gambar 25. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (15:85), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 58
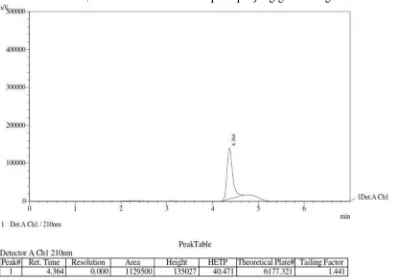
Gambar 26. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (17,5:82,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 58
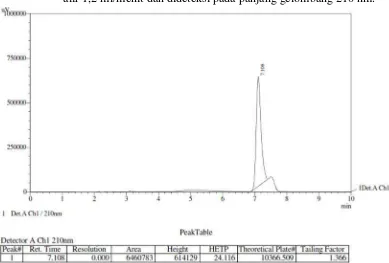
Gambar 27. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 59
Gambar 28. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (22,5:77,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 59
Gambar 29. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 6,0 (15:85), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 60
Gambar 30. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 6,0 (17,5:82,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 60
Gambar 32. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 6,0 (22,5:77,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan
dideteksi pada panjang gelombang 210 nm ... 61
Gambar 33. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (15:85), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 62
Gambar 34. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (17,5:82,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 62
Gambar 35. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 63
Gambar 36. Kromatogram Nutri Sari secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 63
Gambar 37. Kromatogram Jas Jus secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 64
Gambar 38. Kromatogram Ale-ale secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 64
Gambar 40. Kromatogram Frutang secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan
dideteksi pada panjang gelombang 210 nm ... 65
Gambar 41. Kromatogram Aspartam BPFI secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (22,5:77,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 66
Gambar 42. Kromatogram Frutang secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (22,5:77,5), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm ... 66
Gambar 43. Kromatogram Aspartam BPFI 4 ppm secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm 67
Gambar 44. Kromatogram Aspartam BPFI 10 ppm secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm 67
Gambar 45. Kromatogram Aspartam BPFI 20 ppm secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm 68
Gambar 46. Kromatogram Aspartam BPFI 40 ppm secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan dideteksi pada panjang gelombang 210 nm 68
Gambar 48. Kromatogram Aspartam BPFI 160 ppm secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2
ml/menit dan dideteksi pada panjang gelombang 210 nm 69
Gambar 49. Kromatogram Aspartam BPFI 320 ppm secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2
ml/menit dan dideteksi pada panjang gelombang 210 nm 70
Gambar 50. Kromatogram Nutri Sari injeksi 1-6 secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2
ml/menit dan dideteksi pada panjang gelombang 210 nm 74-75
Gambar 51. Kromatogram Okki Koko Drink injeksi 1-6 secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2
ml/menit dan dideteksi pada panjang gelombang 210 nm 78-79
Gambar 52. Kromatogram Ale-ale injeksi 1-6 secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2
ml/menit dan dideteksi pada panjang gelombang 210 nm 82-83
Gambar 53. Kromatogram Jas Jus injeksi 1-6 secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2
ml/menit dan dideteksi pada panjang gelombang 210 nm 86-87
Gambar 54. Kromatogram Frutang injeksi 1-6 secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2
ml/menit dan dideteksi pada panjang gelombang 210 nm 90-91
Gambar 55. Kromatogram sampel (Okki Koko Drink) sebelum penambahan baku injeksi 1-6 secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan
Gambar 56. Kromatogram sampel (Okki Koko Drink) setelah penambahan baku injeksi 1-6 secara KCKT meggunakan kolom shimpac VP-ODS (250 mm x 4,6 mm) dengan fase gerak asetonitril : dapar fosfat pH 4,3 (20:80), volume penyuntikan 20 µ L dengan laju alir 1,2 ml/menit dan
dideteksi pada panjang gelombang 210 nm ... 97-98
Gambar 57. Produk minuman ringan yang digunakan sebagai sampel 108
Gambar 58. Intrument KCKT (Shimadzu Prominence Series) ... 108
Gambar 59. Pompa vakum (Boeco) ... 108
Gambar 60. Neraca analitik (Boeco) ... 109
Gambar 61. Sonifikator (Branson 1510) ... 109
Gambar 62. Sonifikator (Kudos) ... 109
Gambar 63. Syringe ... 110
Lampiran 1.
DAFTAR LAMPIRAN
Gambar kromatogram hasil optimasi pH fase gerak
Halaman
dapar fosfat (pH 2,6) ... 54
Lampiran 2. Gambar kromatogram hasil optimasi pH fase gerak dapar fosfat (pH 3,5) ... 56
Lampiran 3. Gambar kromatogram hasil optimasi pH fase gerak dapar fosfat (pH 4,3) ... 58
Lampiran 4. Gambar kromatogram hasil optimasi pH fase gerak dapar fosfat (pH 6,0) ... 60
Lampiran 5. Gambar kromatogram hasil optimasi komposisi fase gerak asetonitril : dapar fosfat pH 4,3 ... 62
Lampiran 6. Gambar kromatogram penentuan kurva kalibrasi ... 67
Lampiran 7. Perhitungan persamaan garis regresi ... 71
Lampiran 8. Contoh perhitungan kadar aspartam dalam sampel ... 73
Lampiran 9. Kromatogram hasil penyuntikan Nutri Sari ... 74
Lampiran 10. Analisis data statistik dari hasil penyuntikan sampel Nutri Sari ... 76
Lampiran 11. Kromatogram hasil penyuntikan Okki Koko Drink ... 78
Lampiran 12. Analisis data statistik dari hasil penyuntikan sampel Okki Koko Drink ... 80 Lampiran 13. Kromatogram hasil penyuntikan Ale-ale ... 82
Lampiran 14. Analisis data statistik dari hasil penyuntikan sampel Ale-ale ... 84
Lampiran 15. Kromatogram hasil penyuntikan Jas Jus ... 86
Lampiran 16. Analisis data statistik dari hasil penyuntikan sampel Jas Jus ... 88
Lampiran 18. Analisis data statistik dari hasil penyuntikan sampel
Frutang ... 92
Lampiran 19. Data kadar aspartam dalam sampel ... 94
Lampiran 20. Gambar Kromatogram analisis perolehan kembali ... 95
Lampiran 21. Contoh perhitungan persen perolehan kembali ... 99
Lampiran 22. Data hasil perhitungan persen perolehan kembali ... 100
Lampiran 23. Data perhitungan batas deteksi (LOD) dan batas kuantitasi (LOQ) ... 102
Lampiran 24. Sertifikat aspartam BPFI ... 103
Lampiran 25. Tabel distribusi t ... 104
Lampiran 26. Standar Nasional Indonesia untuk aspartam ... 105
Lampiran 27. Sampling minuman ringan ... 106
Lampiran 28. Spesifikasi sampel ... 107
PENGEMBANGAN DAN VALIDASI METODE KROMATOGRAFI CAIR KINERJA TINGGI PADA PENETAPAN KADAR ASPARTAM DALAM
MINUMAN RINGAN YANG BEREDAR DI KOTAMADYA MEDAN
Abstrak
Minuman ringan merupakan produk minuman yang banyak dikonsumsi masyarakat. Biasanya mengandung aspartam yang mempunyai tingkat kemanisan 200-400 kali sukrosa, sehingga sering ditambahkan dalam produk minuman ringan dengan tujuan penghematan biaya produksi. Dikeluarkannya pedoman persyaratan penggunaan pemanis buatan pada produk pangan oleh Badan POM RI memberikan konsekuensi akan perlunya suatu metode analisis yang praktis, akurat dan teliti. Peneliti sebelumnya telah melakukan penetapan kadar aspartam dalam minuman ringan secara Kromatografi Cair Kinerja Tinggi dengan perbandingan fase gerak asetonitril : dapar fosfat pH 2,6 (17,5:82,5) dengan laju alir 1,2 ml/menit menggunakan kolom Shimpac VP-ODS (150 mm x 4,6 mm) dan dektektor UV/Vis tetapi tidak disebutkan waktu retensinya; pada pH 3,5 (15:85) dengan laju alir 1,5 ml/menit menggunakan kolom Shimpac VP-ODS (150 mm x 4,6 mm) dan detektor PDA dengan waktu retensi 4,0 menit; dan pada pH 6,0 (15:85) dengan laju alir 1,4 ml/menit menggunakan kolom Shimpac XR-ODS (50 mm x 3,0 mm) dan detektor UV/Vis dengan waktu retensi 1,15 menit. Tujuan penelitian ini adalah untuk mengembangkan suatu metode alternatif pada penetapan kadar aspartam dalam minuman ringan secara Kromatografi Cair Kinerja Tinggi menggunakan kolom Shimpac VP-ODS (250 mm x 4,6 mm) dengan detektor UV/Vis.
Dalam pengembangan metode ini, dilakukan penentuan panjang gelombang, pemilihan pH fase gerak dan komposisi fase gerak untuk mendapatkan kondisi analisis yang optimum. Uji validasi dilakukan terhadap parameter akurasi, presisi, batas deteksi dan batas kuantitasi untuk menjamin kualitas dari metode analisis.
Hasil optimasi diperoleh kondisi analisis yang optimal menggunakan fase gerak asetonitril : dapar fosfat pH 4,3 dengan perbandingan 20 : 80, laju alir 1,2 ml/menit pada panjang gelombang 210 nm dengan waktu retensi 5,5 menit. Dari hasil uji validasi metode diperoleh persen recovery 102,85% dan RSD 0,28%, ini menunjukkan bahwa metode memiliki akurasi dan presisi yang baik dengan batas deteksi (LOD) 7,54 µ g/ml dan batas kuantitasi (LOQ) 25,14 µ g/ml. Dari hasil penelitian ini diperoleh kadar Aspartam dalam Nutri Sari 391,31 ± 8,48 mg/kg, Okki Koko Drink 95,97 ± 1,42 mg/kg, Ale-ale 31,39 ± 0,42 mg/kg, Jas Jus 128,86 ± 0,88 mg/kg dan Frutang 87,45 ± 1,37 mg/kg. Dapat disimpulkan bahwa kandungan aspartam dalam semua sampel minuman ringan masih memenuhi persyaratn menurut SNI 01-6993,2004, yaitu 600 mg/kg.
Kata kunci: aspartam, minuman ringan, kromatografi cair kinerja tinggi,
DEVELOPMENT AND VALIDATION OF HIGH PERFORMANCE LIQUID CHROMATOGRAPHY METHOD IN THE DETERMINATION
OF ASPARTAME IN SOFT DRINK THAT CIRCULATE IN MEDAN
Abstract
Soft drinks are a beverage product that almost consumed by the people. Commonly softdrink contain aspartame which has 200 – 400 times sweetness of sucrose, so it is usually added in soft drink products to economize the production cost. The exit of alternative sweetener guideline requirement in food product by BPOM RI gives a consequence the need of a practical, accurate and thorough analytical method. Previous researchers have done the determination of aspartame concentration in soft drink by High Performance Liquid Chromatography with mobile phase ratio of acetonitrile: phosphate buffer pH 2.6 (17.5:82.5) in flow rate 1.2 ml/min using Shimpac colomn VP-ODS (150 x 4.6 mm) with UV/Vis detector, but it wasn’t mentioned the retention time; in pH 3.5 (15:85) with flow rate 1.5 ml/min using Shimpac colomn VP-ODS (150 x 4.6 mm) with PDA detector, it was obtained retention time 4.0 min; and in pH 6.0 (15:85) with flow rate 1.4 ml/min using Shimpac XR-ODS (50 x 3.0 mm) with UV/Vis detector, it was obtained retention time 1.15 min. The purpose of this research is to develop an alternative analysis method that can be used in determination of aspartame concentration using High Performance Liquid Chromatography using Shimpac colomn VP-ODS (250 x 4.6 mm) with UV/Vis detector.
On this development method, need to be wavelength parameter, pH of mobile phase and the ratio of mobile phase to could optimum analithical method. Validation test was done against accuracy and precission parameters, limit of detection and limit of quantitation to guarantee quality of analithical method.
Optimization result obtained optimum analytical condition in mobile phase acetonitrile : phosphate buffer pH 4.3 with ratio of mobile phase 20 : 80, flow rate 1.2 ml/min in 210 nm wavelength with retention time 5.5 min. From the validation test result, it was obtained recovery 102,85% and RSD 0.28%, it was indicated that this method had a good accuracy and precission with limit of detection (LOD) 7.54 µ g/ml and limit of quantitation (LOQ) 25.14 µ g/ml. From this research result, it was obtained that aspartame concentration in Nutri Sari was 392.31 ± 8.48 mg/kg, Okki Koko Drink 95.97 ± 1.42 mg/kg, Ale-ale 31.39 ± 0.42 mg/kg, Jas Jus 128.86 ± 0.88 mg/kg dan Frutang 87.45 ± 1.37 mg/kg. It can be seen that concentration of aspartame in all of the soft drink samples were still fulfilled with Indonesian National Standard 01-6993, 2004 (600 mg/kg).
Keywords: aspartame, soft drink, high performance liquid chromatography,
BAB I
PENDAHULUAN
1.1 Latar Belakang
Minuman ringan (Soft drink) berdasarkan Keputusan Kepala Badan
Pengawas Obat dan Makanan Republik Indonesia No. HK.00.05.52.4040 tentang
Kategori Pangan adalah produk minuman yang diperoleh tanpa melalui proses
fermentasi dengan atau tanpa penambahan karbondioksida, dengan atau tanpa
pengenceran sebelum diminum, tetapi tidak termasuk air, sari buah, susu atau susu
untuk persiapan produk, teh, kopi, cokelat, produk telur, produk daging, kamir atau
ekstrak sayur, sup, sari sayur dan minuman beralkohol (BPOM RI, 2006).
Pada dasarnya pemanis buatan (artificial sweeteners) termasuk ke dalam
golongan bahan tambahan kimia, yang secara substansi memiliki tingkat kemanisan
lebih tinggi, yaitu berkisar antara 30 sampai dengan ribuan kali lebih manis
dibandingkan sukrosa. Karena tingkat kemanisannya yang tinggi, penggunaan
pemanis buatan dalam produk pangan hanya dibutuhkan dalam jumlah kecil
sehingga dapat dikatakan rendah kalori atau tidak mengandung kalori. Selain itu,
penggunaan pemanis buatan untuk memproduksi makanan jauh lebih murah
dibanding penggunaan sukrosa (Ambarsari, dkk., 2007).
Penggunaan aspartam dalam industri produk minuman ringan masih sering
digunakan dan diijinkan penggunaannya, tetapi dalam batasan tertentu. Karena itu,
masyarakat Indonesia hampir setiap hari mengkonsumsi aspartam dalam jumlah
tertentu baik secara terpisah maupun gabungan dengan dua atau lebih pemanis
buatan lainnya. Kombinasi aspartam dengan pemanis lainnya dimaksudkan untuk
meningkatkan rasa manis yang lebih, tetapi masih dalam batasan yang diijinkan
Penggunaan pemanis sintetik dapat mempengaruhi kesehatan tubuh.
Penelitian telah menunjukkan bahwa pemanis seperti aspartam dapat
terdekomposisi menjadi produk yang berbahaya. Salah satu konsekuensinya dapat
menyebabkan gangguan penglihatan atau bahkan kebutaan. Dekomposisi pemanis
dalam tubuh, berarti bahwa pemanis dikonversi melalui reaksi kimia menjadi
senyawa yang berbahaya seperti metanol (Nseir, 2010).
Dalam larutan dan pada keadaan tertentu seperti pencampuran, temperatur,
dan pH, ikatan ester terhidrolisis membentuk dipeptida aspartilfenilalain dan
metanol. Pada akhirnya, aspartilfenilalanin dapat terhidrolisis menjadi dua asam
amino, yaitu asam aspartat dan fenilalanin. Kemungkinan yang lain, metanol
mungkin juga dihidrolisis dari siklisasi aspartam menjadi diketopiperazin (DKP)
(Butchko, 2001). Hal serupa terjadi juga dalam tubuh, dimana aspartam akan
dihidrolisis oleh enzim proteolitik yang ada dalam usus halus dan sel mukosa
menjadi asam aspartat (40%), fenilalanin (50%), dan metanol (10%) (O’Donnel,
2006).
Banyaknya minuman ringan yang mengandung aspartam yang beredar di
pasaran membuat peneliti tertarik untuk menetapkan kadar aspartam dalam
minuman ringan yang beredar di Kotamadya Medan. Hasil yang diperoleh
dibandingkan dengan persyaratan yang tercantum dalam SNI-01-6993-2004.
Metode penetapan kadar aspartam dapat dilakukan dengan berbagai cara
diantaranya metode secara volumetri, yaitu titrasi bebas air, secara spektrofotometri
Ultraviolet dan secara Kromatografi Cair Kinerja Tinggi.
Pada penelitian ini dilakukan analisis pemanis aspartam di dalam minuman
ringan menggunakan metode KCKT, dan untuk mendapatkan hasil analisis
pH fase gerak dan komposisi fase gerak. Kondisi analisis optimum yang
diperoleh diterapkan pada penetapan kadar aspartam dalam minuman ringan.
Adapun alasan memilih metode ini karena analisisnya cepat, daya pisah baik, peka,
kolom dapat dipakai berulang kali dan perangkatnya dapat digunakan secara
otomatis dan kuantitatif (Gandjar dan Rohman, 2007).
Penelitian sebelumnya telah dilakukan penetapan kadar aspartam dalam
minuman ringan secara Kromatografi Cair Kinerja Tinggi dengan perbandingan
fase gerak asetonitril : dapar fosfat pH 2,6 (17,5:82,5) dengan laju alir 1,2 ml/menit
mengunakan kolom Shimpac VP-ODS (150 mm x 4,6 mm) dengan detektor
UV/Vis, tetapi tidak disebutkan waktu retensinya, pada pH 3,5 (15:85) dengan laju
alir 1,5 ml/menit menggunakan kolom Shimpac VP-ODS (150 mm x 4,6 mm) dan
detektor PDA (photo diode array) dengan waktu retensi 4,0 menit, dan pada pH 6,0
(15:85) dengan laju alir 1,4 ml/menit menggunakan kolom Shimpac XR-ODS (50
mm x 30 mm) dan detektor UV/Vis dengan waktu retensi 1,15 menit.
Dikeluarkannya pedoman persyaratan penggunaan pemanis buatan pada
produk pangan dalam Surat Keputusan Kepala Badan Pengawasan Obat dan
Makanan Republik Indonesia No. HK.00.05.1.4547 tahun 2004, memberikan
konsekuensi akan perlunya suatu metode analisis yang praktis, akurat dan teliti.
Sehingga perlu adanya suatu metode alternatif untuk analisis kadar aspartam dalam
minuman ringan secara Kromatografi Cair Kinerja Tinggi
Validasi merupakan persyaratan mendasar yang diperlukan untuk menjamin
kualitas dan hasil dari semua aplikasi analitik. Untuk menguji validitas dari metode
ini dilakukan pengujian antara lain uji akurasi dengan parameter % recovery, uji
presisi dengan parameter koefisien variasi (RSD), uji sensitifitas dengan
1.2 Perumusan Masalah
Adapun yang menjadi permasalahan dalam penelitian ini adalah:s
1. Berapakah perbandingan komposisi fase gerak asetonitril : dapar fosfat
dengan berbagai variasi pH pada panjang gelombang yang sesuai, sehingga
diperoleh kondisi analisis yang optimal dan efisien pada penetapan kadar
aspartam dalam minuman ringan secara Kromatografi Cair Kinerja Tinggi.
2. Apakah komposisi fase gerak asetonitril : dapar fosfat dengan berbagai
variasi pH pada panjang gelombang yang diperoleh dapat digunakan pada
penetapan kadar aspartam dalam minuman ringan secara Kromatografi Cair
Kinerja Tinggi dengan validasi yang memenuhi persyaratan.
3. Apakah kadar aspartam dalam minuman ringan yang beredar di Kotamadya
Medan memenuhi persyaratan yang tercantum dalam SNI-01-6993-2004?
1.3 Hipotesis
Hipotesis penelitian ini adalah:
1. Perbandingan fase gerak asetonitril : dapar fosfat dengan berbagai variasi
pH merupakan kondisi analisis yang optimal dan efisien pada penetapan
kadar aspartam dalam minuman ringan secara Kromatografi Cair Kinerja
Tinggi.
2. Kondisi optimum fase gerak asetonitril : dapar fosfat dengan berbagai
variasi pH dan panjang gelombang yang sesuai dapat digunakan pada
penetapan kadar aspartam dalam minuman ringan secara Kromatografi Cair
Kinerja Tinggi.
3. Kadar aspartam dalam minuman ringan yang beredar di Kotamadya Medan
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Untuk mengetahui perbandingan asetonitril : dapar fosfat dengan berbagai
variasi pH dan panjang gelombang yang sesuai, sehingga diperoleh kondisi
analisis yang optimal dan efisien pada penetapan kadar aspartam dalam
minuman ringan secara Kromatografi Cair Kinerja Tinggi.
2. Untuk menyesuaikan kondisi optimum fase gerak asetonitril : dapar fosfat
dengan berbagai variasi pH dan panjang gelombang yang diperoleh dengan
validasi metode yang memenuhi persyaratan.
3. Untuk mengetahui kesesuaian kadar aspartam dalam minuman ringan yang
beredar di Kotamadya Medan dengan persyaratan yang tercantum dalam
SNI-01-6993-2004.
1.5 Manfaat Penelitian
Penelitian ini bermanfaat sebagai sumber informasi kepada masyarakat
mengenai kadar aspartam dalam minuman ringan yang beredar di pasaran, sehingga
masyarakat lebih berhati-hati dalam mengkonsumsi minuman ringan. Disamping
itu, dapat digunakan sebagai metode alternatif pada penetapan kadar aspartam
secara Kromatografi Cair Kinerja Tinggi untuk industri farmasi atau makanan dan
BAB II
TINJAUAN PUSTAKA
2.1 Bahan Tambahan Pangan
Bahan Tambahan Pangan (BTP) adalah bahan yang ditambahkan ke dalam
pangan untuk mempengaruhi sifat dan bentuk pangan, baik yang mempunyai atau
tidak mempunyai nilai gizi (BPOM RI, 2011 dan BPOM RI, 2004).
Menurut ketentuan yang ditetapkan, ada beberapa kategori Bahan
Tambahan Makanan. Pertama, Bahan Tambahan Makanan yang bersifat aman,
dengan dosis yang tidak dibatasi, misalnya pati. Kedua, Bahan Tambahan Makanan
yang digunakan dengan dosis tertentu, dan dengan demikian dosis maksimum
penggunaannya juga telah ditetapkan. Ketiga, bahan tambahan yang aman dan
dalam dosis yang tepat, serta telah mendapatkan izin beredar dari instansi yang
berwenang, misalnya zat pewarna yang sudah dilengkapi sertifikat aman (Yuliarti,
2007).
Menurut Yuliarti (2007), beberapa Bahan Tambahan Makanan yang telah
diizinkan oleh Badan POM, diantaranya:
1. Pengawet: natrium benzoat, kalium sorbat, nisin
2. Pewarna: tartrazin
3. Pemanis: aspartam, sakarin dan siklamat
4. Penyedap rasa: monosodium glutamat
5. Antikempal: aluminium silikat, magnesium karbonat, trikalsium fosfat
6. Antioksidan: asam askorbat, alfa tokoferol
7. Pengemulsi, pemantap dan pengental: lesitin, sodium laktat dan potassium
2.2. Pembagian Pemanis
2.2.1 Pemanis Alami
Pemanis alami yang sering digunakan untuk makanan, terutama adalah tebu
dan bit. Kedua jenis pemanis ini sering disebut gula alam atau sukrosa. Selain itu
ada berbagai pemanis lain yang dapat digunakan untuk makanan, diantaranya
laktosa, maltosa, galaktosa, glukosa, fruktosa, sorbitol, manitol (Yuliarti, 2007).
2.2.2 Pemanis Buatan
Pemanis buatan merupakan bahan tambahan yang dapat memberikan rasa
manis dalam makanan, tetapi tidak memiliki nilai gizi. Sebagai contoh adalah
sakarin, siklamat, aspartam. Sekalipun penggunaannya diizinkan, pemanis buatan
dan juga bahan kimia yang lain sesuai peraturan penggunaannya harus dibatasi.
Alasannya, meskipun pemanis buatan tersebut aman dikonsumsi dalam kadar yang
kecil, tetap saja dalam batas-batas tertentu akan menimbulkan bahaya kesehatan
bagi manusia maupun hewan yang mengonsumsinya (Yuliarti, 2007).
2.3 Aspartam
Aspartam ditemukan secara kebetulan oleh James Schulter pada tahun 1965,
ketika mensintesis obat-obat untuk bisul atau borok. Asparrtam adalah senyawa
metil ester dipeptida, yaitu L-aspartil-L-alanin-metilester dengan rumus
C14H18N2O5 memiliki daya kemanisan 100-200 kali sukrosa (Cahyadi, 2009; Tan,
2007).
Pada penggunaannya dalam minuman ringan, aspartam kurang
turunya rasa manis. Selain itu, aspartam tidak tahan panas sehingga tidak baik
digunakan dalam bahan pangan yang diolah melalui pemanasan (Cahyadi, 2009).
2.3.1 Sifat Fisika dan Kimia
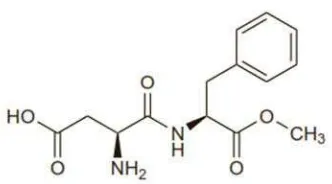
[image:31.596.215.381.200.292.2]2.3.1.1 Struktur
Gambar 1. Struktur kimia dari Aspartam (Butchko, 2001).
2.3.1.2 Rumus Molekul
C14H18N2O5 (O’Donnell, 2006).
2.3.1.3 Berat Molekul
294,30 (Glória, 2003).
2.3.1.4 Nama Kimia
(3S)-3-Amino-4-[[(2S)-1-methoxy-1-oxo-3-phenylpropan-2-yl]amino]-4-
oxobutanoic acid (The Department of Health, 2012).
2.3.1.5 Pemerian
Senyawa yang tidak berbau, putih atau hampir putih, sedikit higroskopis,
serbuk kristal (Cahyadi, 2009; Martindale, 2009; The Department of Health, 2012).
2.3.1.6 Stabilitas
Dalam larutan dan pada keadaan tertentu seperti pencampuran, temperatur,
dan pH, ikatan ester terhidrolisis membentuk dipeptida aspartilfenilalain dan
metanol. Pada akhirnya, aspartilfenilalanin dapat terhidrolisis menjadi dua asam
mungkin juga dihidrolisis dari siklisasi aspartam menjadi diketopiperazin (DKP)
(Butchko, 2001). Hal serupa terjadi juga dalam tubuh, dimana aspartam akan
dihidrolisis oleh enzim proteolitik yang ada dalam usus halus dan sel mukosa
menjadi asam aspartat (40%), fenilalanin (50%), dan metanol (10%) (O’Donnel,
2006).
O O O H2 H H H HO C
esterase
H2O
C C C NH2
N C C OH CH2 + H
3C OH
Methanol
peptidase O H O
H2 H O H H O Aspartylphenylalanine O O H2N C C HO C C C C N C C H2 H OH
NH2 CH2 OCH3
esterase O
H2 H H2O
HO C C C C OH + NH2
CH2
Aspartame
C C N O HO
O N C H H2
+ H3C OH
Aspartic acid Phenylalanine
Diketopiperazine Methanol
Gambar 2. Prinsip konversi produk aspartam (Butchko, 2001).
Pada suhu 25 °C, stabilitas maksimum aspartam ditunjukkan pada pH 4,3.
Aspartam berfungsi dengan sangat baik di atas interval pH 3-5, tetapi kebanyakan
stabil pada suasana asam lemah yang mana kebanyakan digunakan dalam industri
makanan, yaitu antara pH 3 dan 5 (Butchko, 2001; O’Donnel, 2006; Smith, 2003).
Gambar 3. Stabilitas aspartam dalam larutan dapar pada suhu 25°C (Butchko,
2.3.1.7 Kelarutan
Sedikit larut dalam air (pada suhu 20 °C, pH 4,5-6,0 sebanyak 36%) dan
dalam alkohol (pada suhu 25 °C sebanyak 0,4%) (Smith, 2003); praktis tidak larut
dalam diklorometana, n-heksan dan dalam metilen klorida (Martindale, 2009; The
Department of Health, 2012)
2.3.2 Sinonim
N-L-α-Aspartyl-L-phenylalanine-1-Methyl Ester; Aspartylphenylalanine
methyl ester; 3-Amino-N-(α-carboxyphenethyl)succinamic acid N-methyl ester; N-
L-α-aspartyl-L-phenylalaninate; APM; Aspartaam; Aspartamas; Aspartamo;
Aspartamum (Commite of Food Chemical Codex, 2004; Smith, 2003; The United
State Pharmacopoeia Convention, 2007; Martindale, 2009).
2.3.3 Sintesis
Sintesis aspartam dalam skala besar diperoleh melalui reaksi:
Gambar 4. Reaksi sintesis pembentukan aspartam (Belitz, 2009).
Bahan baku untuk produksi aspartam adalah dua asam amino, yaitu
fenilalanin dan asam aspartat. Gugus reaktif dari asam amino diproteksi pertama
asam amino kemudian digandengkan dengan yang lain secara kimia atau enzimatis
dan gugus reaktif dihilangkan. Langkah ini diikuti dengan tahap melarutkan dengan
HCl dan kristalisasi untuk menghilangkan pengotor atau zat asing (O’Donnell,
2006).
2.3.4 Metabolisme
Aspartam dapat dihidrolisis dan dimetabolisme dalam dua jalur utama, yaitu
melalui intesitnal lumen dan sel mukosa. Dalam keduanya, keadaan dosis aspartam
yang besar akan melepaskan aspartat, fenilalanin dan metanol ke dalam aliran
darah, dan senyawa ini dimetabolisme dan atau diekskresikan (Salminen dan
Hallikainen, 2002). Aspartam diabsorbsi dan dimetabolisme mengikuti laju
kinetika orde pertama. Aspartam dihidrolisis dalam usus halus oleh enzim
proteolitik dan hidrolitik menjadi aspartat, fenilalanin, dan metanol (Glória, 2003).
Gambar 5. Diagram metabolisme Aspartam (Glória, 2003)
2.3.5 Toksisitas
Efek samping yang tersering timbul pada dosis tinggi dapat berupa nyeri
kepala dan lambung, pusing, mual, muntah dan perubahan suasana jiwa, lebih
jarang reaksi alergi dan serangan epilepsi. Ada kalanya aspartam dalam Cola light
dapat mencetuskan serangan migrain. Tidak boleh diberikan pada anak-anak dan
wanita hamil dengan fenilketonuria (PKU), dimana terdapat kekurangan enzim
yang mengubah fenilalanin menjadi tirosin. Sebabnya adalah fenilalanin akan
2.3.6 Metode Analisis Lain untuk Penetapan Kadar Aspartam
2.3.6.1 Penetapan Kadar Aspartam dengan Metode Titrasi Bebas Air
Penetapan kadar Aspartam dengan metode titrasi bebas air menggunakan
asam perklorat 0,1 N sebagai pentiter. Prosedur penetapan kadar aspartam dengan
metode titrasi asam basa, yaitu dengan menimbang secara teliti 300 mg sampel
(aspartam) dan dilarutkan dengan 1,5 ml asam formiat 96% dalam erlenmeyer 150
ml. Ditambah 60 ml asam asetat glasial dan kristal violet sebagai indikator,
kemudian dititrasi dengan asam perklorat 0,1 N hingga terbentuk warna hijau.
Setiap ml asam perklorat 0,1 N setara dengan 29,43 mg C14H18N2O5 (The United
State Pharmacopoeia Convention, 2007).
2.3.6.2 Penetapan Kadar Aspartam dengan Metode Spektrofotometri Ultraviolet
Penentuan kadar aspartam secara kuantitatif dapat dilakukan dengan
spektrofotometri. Mula-mula aspartam dilarutkan dengan HCl 2 N. Kemudian
panaskan supaya terjadi hidrolisis menghasilkan fenilalanin. Analisis kuantitatif
memerlukan tahap pemisahan zat aktif dengan zat pengotor lainnya dengan cara
ekstraksi. Ekstraksi yang dilakukan adalah ekstraksi cair-cair, yaitu zat yang telah
dilarutkan diekstraksi dengan kloroform sebanyak 2 kali masing-masing 10 menit,
kemudian fase organik dipisahkan dari fase air. Fase air diekstraksi kembali dengan
petroleum eter selama 10 menit. Pengukuran dilakukan pada fase air (Cahyadi,
2009) pada panjang gelombang 200-217 nm (Glória, 2003).
2.4 Kromatografi
2.4.1 Sejarah Kromatografi
Kromatografi pertama kali dikembangkan oleh ahli botani Rusia pada tahun
tanaman dengan cara perkolasi ekstrak petroleum eter dalam kolom gelas yang
berisi CaCO3. Oleh karena itu, diberi nama kromatografi yang berasal dari bahasa
Yunani “chroma” yang berarti warna dan “grapein” yang berarti menulis
(Wonorahardjo, 2013). Saat ini kromatografi merupakan teknik pemisahan yang
paling umum dan paling sering digunakan dalam bidang kimia analisis dan dapat
dimanfaatkan untuk melalukan analisis, baik analisis kualitatif, analisis kuantitatif,
atau preparatif dalam bidang farmasi, industri dan lain sebagainya (Gandjar dan
Rohman, 2008).
Organisasi standar internasional IUPAC (International Union of Pure and
Applied Chemistry) mendefinisikan kromatografi sebagai metode pemisahan secara
fisika yang mana komponen-komponen yang akan dipisahkan terbagi diantara dua
fase, yang satu adalah fase diam sementara yang lain adalah fase gerak yang
bergerak pada arah tertentu (Gandjar dan Rohman, 2012).
2.4.2 Klasifikasi Kromatografi
Prinsip dari metode kromatografi adalah distribusi komponen sampel antara
dua fase, yakni fase diam dan fase gerak. Fase diam dalam praktiknya adalah cairan
yang terikat pada permukaan padatan sehingga tidak dapat bergerak, atau padatan
itu sendiri. Sedangkan, fase gerak adalah cairan atau gas pembawa yang tidak
bereaksi dengan senyawa-senyawa yang dipisahkan (Wonorahardjo, 2013).
Klasifikasi tipe kromatografi yang paling umum adalah berdasarkan tipe
fase gerak dan fase diam. Kromatografi gas-cair atau kromatografi cair-cair,
kromatografi gas, sering menjadi penanda suatu jenis kromatografi. Yang sering
digunakan adalah tipe fase geraknya, seperti kromatografi gas merujuk pada fase
menunjukkan fase gerak cair (dan fase diam padat atau cair, tetapi tidak disebut).
Jika kedua fase disebut ini berarti bahwa kromatografi dibuat secara spesifik untuk
tujuan tertentu (Wonorahardjo, 2013).
Berdasarkan pada mekanisme pemisahannya, kromatografi dibedakan
menjadi : (a) kromatografi adsorbsi; (b) kromatografi partisi; (c) kromatografi
pasangan ion; (d) kromatografi penukar ion (e) kromatografi eksklusi ukuran dan
(f) kromatografi afinitas (Rohman, 2009).
Berdasarkan pada alat yang digunakan, kromatografi dapat dibagi atas: (a)
kromatografi kertas; (b) kromatografi lapis tipis, yang kedua sering disebut
kromatografi planar; (c) kromatografi cair kinerja tinggi (KCKT) dan (d)
kromatografi gas (KG) (Rohman, 2009).
Gambar 6. Pengelompokkan kromatografi secara umum (Gandjar dan Rohman,
2.5 Kromatografi Cair Kinerja Tinggi
2.5.1 Jenis KCKT
Hampir semua jenis campuran solut dapat dipisahkan dengan KCKT karena
banyaknya fase diam yang tersedia dan selektifitas yang dapat ditingkatkan dengan
mengatur fase gerak. Pemisahan dapat dilakukan dengan fase normal atau fase
terbalik tergantung pada polaritas relatif fase diam dan fase gerak. Berdasarkan
pada kedua pemisahan ini, sering kali KCKT dikelompokkan menjadi KCKT fase
normal dan KCKT fase terbalik. Berdasarkan mekanisme interaksi antara analit
dengan fase diam, kromatografi cair dapat dibagi menjadi 4 metode, yakni:
kromatografi fase normal (normal phase chromatography) atau disebut juga
kromatografi adsorpsi (adsorption chromatography), kromatografi fase balik
(reversed-phase chromatography), kromatografi penukar ion (ion-exchange
chromatography) dan kromatografi eksklusi ukuran (size-exclusion
chromatography) (Gandjar dan Rohman, 2008).
Kromatografi fase balik menggunakan fase diam dari silika yang
dimodifikasi secara kimiawi. Fase diam yang paling popular digunakan adalah
oktadesilsilan (ODS atau C18) yang relatif non polar sedangkan fase geraknya relatif
lebih polar daripada fase diam. Kondisi kepolaran kedua fase ini merupakan
kebalikan dari kromatografi fase normal sehingga disebut kromatografi fase balik
(Meyer, 2010).
2.5.2 Proses Pemisahan dalam Kolom Kromatografi Cair
Pemisahan analit dalam kolom kromatografi berdasarkan pada aliran fase
analit dengan permukaan fase diam sehingga terjadi perbedaan waktu perpindahan
setiap komponen dalam campuran (Meyer, 2010).
Sebagai contoh, campuran dua komponen dimasukkan ke dalam sistem
kromatografi adsorbsi (fase normal) yang dinotasikan sebagai partikel ● (nonpolar)
dan ▲ (polar) (Gambar 7a). Masuknya eluen (fase gerak/nonpolar) ke dalam kolom
akan menimbulkan kesetimbangan baru.
Gambar 7 . Ilustrasi proses pemisahan yang terjadi di dalam kolom KCKT (Meyer,
2010).
Molekul sampel dalam fase gerak diadsorpsi sebagian oleh permukaan fase
diam berdasarkan pada koefisien distribusinya, di mana komponen ▲ cenderung
menetap di fase diam dan komponen ● lebih cenderung di dalam fase gerak
(Gambar 7b), sedangkan molekul yang sebelumnya diadsorpsi akan muncul
kembali di fase gerak (Gambar 7c). Setelah proses ini terjadi berulang kali, kedua
komponen akan terpisah. Komponen ● yang lebih suka dengan fase gerak akan
berpindah lebih cepat daripada komponen ▲ yang cenderung menetap di fase diam,
sehingga komponen ● akan muncul terlebih dahulu dalam kromatogram, kemudian
2.5.3 Parameter Penting dalam Kromatografi Cair
2.5.3.1 Tinggi dan Luas Puncak
Tinggi dan luas puncak berkaitan secara proporsional dengan kadar atau
jumlah analit tertentu yang terdapat dalam sampel (memiliki informasi kuantitatif).
Namun demikian, luas puncak lebih umum digunakan dalam perhitungan
kuantitatif karena lebih akurat/cermat daripada perhitungan menggunakan tinggi
puncak. Hal ini dikarenakan luas puncak relatif tidak banyak dipengaruhi oleh
kondisi kromatografi, kecuali laju alir. Sementara itu, tinggi puncak dipengaruhi
oleh banyak faktor seperti misalnya faktor tambat, suhu kolom serta cara injeksi
sampel (Ornaf dan Dong, 2005).
Sebuah puncak memiliki lebar puncak (Wb), tinggi (h) dan luas puncak
seperti yang dapat dilihat pada Gambar 8 berikut:
Gambar 8. Kromatogram yang diperoleh dari analisis KCKT (Ornaf dan Dong,
2005).
Lebar puncak yang diukur biasanya merupakan lebar pada 5% tinggi puncak (Ornaf
dan Dong, 2005).
2.5.3.2 Waktu tambat
Periode waktu antara penyuntikan sampel dan puncak maksimum yang
terekam oleh detektor disebut sebagai waktu tambat/retention time (tR). Waktu
sebagai waktu hampa/void time (t0). Waktu tambat merupakan fungsi dari laju alir
fase gerak dan panjang kolom. Jika fase gerak mengalir lebih lambat atau kolom
semakin panjang, waktu hampa dan waktu tambat akan semakin besar, dan
sebaliknya bila fase gerak mengalir lebih cepat atau kolom semakin pendek, maka
waktu hampa dan waktu tambat akan semakin kecil (Meyer, 2010).
2.5.3.3 Faktor Kapasitas
Waktu tambat dipengaruhi oleh laju alir, ukuran kolom dan parameter yang
lain. Oleh karena itu, diperlukan suatu ukuran derajat tambatan dari analit yang
lebih independen yaitu faktor kapasitas (k’). Faktor kapasitas dihitung dengan
membagi waktu tambat bersih (t’R) dengan waktu hampa (t0) seperti yang dapat
dilihat pada rumus berikut ini (Ornaf dan Dong, 2005).
Dalam beberapa literatur lain, faktor kapasitas juga disebut sebagai faktor
tambat (k). Idealnya, analit yang sama jika diukur pada dua instrumen yang berbeda
namun memiliki fase diam dan fase gerak yang sama, maka faktor tambat dari analit
pada kedua system KCKT tersebut secara teoritis adalah sama (Meyer, 2010).
Faktor tambat yang disukai berada diantara nilai 1 hingga 10. Jika nilai k
terlalu kecil menunjukkan bahwa analit terlalu cepat melewati kolom sehingga
tidak terjadi interaksi dengan fase diam dan oleh karena itu tidak akan muncul
dalam kromatogram. Sebaliknya nilai k yang terlalu besar mengindikasikan waktu
analisis akan panjang (Meyer, 2010).
Faktor kapasitas dipengaruhi oleh perbandingan komposisi fase gerak yang
kromatogram yang berbeda pada setiap perbandingan komposisi fase gerak
(Snyder, 2010).
2.5.3.4 Selektivitas
Kemampuan sistem kromatografi dalam memisahkan/membedakan analit
yang berbeda dikenal sebagai selektivitas (α). Selektivitas umumnya tergantung
pada sifat analit itu sendiri, interaksinya dengan permukaan fase diam serta jenis
fase gerak yang digunakan (Meyer, 2010).
Selektivitas ditentukan sebagai rasio perbandingan dua faktor kapasitas dari
analit yang berbeda. Selektivitas ditentukan dengan rumus sebagai berikut:
Nilai selektivitas yang didapatkan dalam sistem KCKT harus lebih besar dari 1
(Ornaf dan Dong, 2005).
2.5.3.5 Efisiensi Kolom
Ukuran kuantitatif dari efisiensi kolom disebut sebagai nilai lempeng/plate
number (N) (Ornaf dan Dong, 2005). Kolom yang efisien adalah kolom yang
mampu menghasilkan puncak yang sempit dan memisahkan analit dengan baik.
Nilai lempeng akan semakin tinggi jika ukuran kolom semakin panjang, hal ini
berarti proses pemisahan yang terjadi semakin baik. Hubungan proporsionalitas
antara nilai lempeng dengan panjang kolom disebut sebagai nilai HETP/High
Equivalent of a Theoritical Plate. Praktik HPLC yang baik adalah mendapatkan
nilai HETP yang kecil untuk nilai N yang maksimum dan efisiensi kolom yang
Parameter yang dapat mempengaruhi nilai lempeng antara lain waktu
tambat puncak, ukuran partikel kolom, laju alir fase gerak, suhu kolom, viskositas
fase gerak dan berat molekul analit. FDA merekomendasikan agar tiap analisis
KCKT yang valid mempunyai nilai lempeng lebih besar dari 2000 (Meyer, 2010).
2.5.3.6 Resolusi
Resolusi merupakan derajat pemisahan dari dua puncak analit yang
bersebelahan (Ornaf dan Dong, 2005).
Harga resolusi yang semakin besar memiliki arti proses pemisahan semakin bagus
dan sebaliknya resolusi yang kecil merupakan pertanda proses pemisahan yang
buruk. Dua puncak yang tidak terpisah dengan sempurna namun sudah dapat
terlihat memiliki resolusi 1. Sedangkan bila kedua puncak yang saling berdekatan
terpisah sempurna tepat pada garis alas, resolusi bernilai 1,5. Oleh karena itu pada
analisis kuantitatif, resolusi yang ditunjukkan harus lebih besar dari 1,5. Sementara
bila kedua puncak memiliki perbedaan yang signifikan, maka diperlukan nilai
resolusi yang lebih besar (Meyer, 2010).
2.5.3.7 Faktor Ikutan dan Faktor Asimetri
Puncak kromatogram dalam kondisi ideal akan memperlihatkan bentuk
Gaussian dengan derajat simetris yang sempurna (Ornaf dan Dong, 2005). Namun
kenyataannya dalam praktik kromatografi, puncak yang simetris secara sempurna
jarang dijumpai. Jika diperhatikan dengan cermat, maka hamper setiap puncak
Gambar 9. Tiga jenis puncak. (Meyer,2010)
Ada dua cara yang digunakan untuk pengukuran derajat asimetris puncak,
yakni faktor ikutan dan faktor asimetri. Faktor ikutan/tailing factor (Tf) seperti yang
diterangkan dalam Farmakope Amerika Serikat (USP) Edisi Ketigapuluh dihitung
dengan menggunakan lebar puncak pada ketinggian 5% (W0,05), rumusnya
dituliskan sebagai berikut:
Dengan nilai a dan b merupakan setengah lebar puncak pada ketinggian 5% seperti
yang ditunjukkan pada Gambar 10.
Gambar 10. Pengukuran derajat asimetris puncak (Snyder, 2010).
Sementara itu, faktor asimetri/asymmetry factor (As) dihitung dengan rumus
sebagai berikut.
Namun nilai a dan b dalam perhitungan faktor asimetri merupakan setengah lebar
a=b, maka faktor ikutan dan asimetri bernilai 1. Kondisi ini menunjukkan bentuk
puncak yang simetris sempurna (Dolan, 2003). Bila puncak berbentuk tailing, maka
kedua faktor ini akan bernilai lebih besar dari 1 dan sebaliknya bila puncak
berbentuk fronting, maka faktor ikutan dan asimetri akan bernilai lebih kecil dari 1
(Hinshaw, 2004).
2.5.4 Instrumen Kromatografi Cair Kinerja Tinggi
Instrumen KCKT tersusun atas 6 bagian dasar, yakni wadah fase gerak
(reservoir), pompa (pump), tempat injeksi sampel (injector), kolom (coloumn),
detector (detector) dan perekam (recorder) (McMaster, 2007). Ilustrasi instrument
dasar KCKT dapat dilihat pada Gambar 11.
Gambar 11. (a) Sistem KCKT secara skematik yang menunjukkan semua
komponen utamanya. (b) Gambaran grafik suatu sistem KCKT isokratik (Dong, 2006).
2.5.4.1 Wadah Fase Gerak
Wadah fase gerak harus bersih dan inert. Wadah pelarut kosong ataupun
labu laboratorium dapat digunakan sebagai wadah fase gerak. Wadah ini biasanya
digunakan harus dilakukan degassing (penghilangan gas) yang ada pada fase gerak,
sebab adanya gas akan berkumpul dengan komponen lain terutama dipompa dan
detektor sehingga akan mengacaukan analisis (Gandjar dan Rohman, 2008).
2.5.4.2 Pompa
Pompa yang cocok digunakan untuk KCKT adalah pompa yang mempunyai
syarat sebagaimana syarat wadah pelarut yakni : pompa harus inert terhadap fase
gerak. Bahan yang umum dipakai untuk pompa adalah gelas, baja tahan karat,
teflon, dan batu nilam. Pompa yang digunakan sebaiknya mampu memberikan
tekanan sampai 6000 psi dan mampu mengalirkan fase gerak dengan kecepatan alir
0,1-10 ml/menit. Aliran pelarut dari pompa harus tanpa denyut untuk menghindari
hasil yang menyimpang pada detektor (Gandjar dan Rohman, 2007).
2.5.4.3 Tempat Injeksi Sampel
Ada 3 jenis injektor, yakni syringe injector, loop valve dan automatic
injector (autosampler). Syringe injector merupakan bentuk injektor yang paling
sederhana (Meyer, 2010).
Pada waktu sampel diinjeksikan ke dalam kolom, diharapkan agar aliran
pelarut tidak mengganggu masuknya keseluruhan sampel ke dalam kolom. Sampel
dapat langsung diinjeksikan ke dalam kolom (on column injection) atau digunakan
katup injeksi (Meyer, 2010).
Katup putaran (loop valve), tipe injektor ini umumnya digunakan untuk
menginjeksi volume lebih besar daripada 10 µ l dan sekarang digunakan dengan
cara otomatis (dengan adaptor khusus, volume-volume lebih kecil dapat
diinjeksikan secara manual). Bila katup difungsikan, maka cuplikan di dalam
Automatic injector atau disebut juga autosampler memiliki prinsip yang
mirip, hanya saja sistem penyuntikannya bekerja secara otomatis (Meyer, 2010).
Gambar 12. Tipe Injektor katup putaran (Meyer, 2010).
2.5.4.4 Kolom
Kolom merupakan jantung dari instrument KCKT karena proses pemisahan
terjadi disini. Kolom umumnya terbuat dari 316- grade stainless steel yang relative
tahan karat dan dikemas dengan fase diam tertentu. Ukuran kolom untuk tujuan
analitik berkisar antara panjang 10 hingga 25 cm dan diameter dalam 3 hingga 9
cm. Sedangkan untuk tujuan preparative digunakan kolom dengan diameter 10 mm
hingga 1 inchi (25,4 mm) (Meyer, 2010).
Ada 2 jenis kolom pada KCKT, yaitu kolom konvensional dan kolom
mikrobor. Kolom merupakan bagian KCKT yang mana terdapat fase diam untuk
berlangsungnya proses pemisahan solut analit (Rohman, 2009).
Kolom mikrobor mempunyai 3 keuntungan yang utama dibanding dengan
kolom konvensional, yakni:
− Konsumsi fase gerak kolom mikrobor hanya 80% atau lebih kecil dibanding
dengan kolom konvensional karena pada kolom mikrobor kecepatan alir fase
− Adanya aliran fase gerak yang lebih lambat membuat kolom mikrobor lebih
ideal jika digabung dengan spektrometer massa
− Sensitifitas kolom mikrobor ditingkatkan karena solut lebih pekat, karenanya
jenis kolom ini sangat bermanfaat jika jumlah sampel terbatas
Meskipun demikian, dalam prakteknya, kolom mikrobor ini tidak setahan kolom
konvensional dan kurang bermanfaat untuk analisis rutin (Rohman, 2009).
2.5.4.5 Detektor
Detektor pada KCKT dikelompokkan menjadi 2 golongan, yaitu detektor
universal (yang mampu mendeteksi zat secara umum, tidak bersifat spesifik,dan
tidak selektif) seperti detektor indeks bias dan detektor spektrometri massa; dan
golongan detektor yang spesifik dan selektif, seperti detektor UV-Vis, detektor
fluoresensi dan elektrokimia (Gandjar dan Rohman, 2008).
Idealnya, suatu detektor harus mempunyai karakteristik sebagai berikut:
− Mempunyai respon terhadap solut yang cepat dan reprodusibel
− Mempunyai sensitifitas yang tinggi, yakni mampu mendeteksi solut pada kadar
yang sangat kecil
− Stabil dalam pengoperasian
− Mempunyai sel volume yang kecil sehingga mampu meminimalkan pelebaran
pita
− Signal yang dihasilkan berbanding lurus dengan konsentrasi solut pada kisaran
yang luas (kisaran dinamis linier)
− Tidak peka terhadap perubahan suhu dan kecepatan alir fase gerak (Gandjar
Suatu detektor dibutuhkan untuk mendeteksi adanya komponen cuplikan
dalam aliran yang keluar dari kolom. Detektor-detektor yang baik memiliki
sensitifitas yang tinggi, gangguan (noise) yang rendah, kisaran respons linier yang
luas, dan memberi tanggapan/respon untuk semua tipe senyawa. Suatu kepekaan
yang rendah terhadap aliran dan fluktuasi temperatur sangat diinginkan, tetapi tidak
selalu dapat diperoleh (Johnson dan Stevenson, 1991).
2.5.4.6 Perekam Data
Komponen yang terelusi mengalir ke detektor dan dicatat sebagai puncak-
puncak yan