KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN JUS BUAH
SIRSAK DAN EKSTRAK ETANOL DAUN
SIRSAK (
Annona muricata
L
.)
SKRIPSI
OLEH:
RINA RIANES
NIM 050804005
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN JUS BUAH
SIRSAK DAN EKSTRAK ETANOL DAUN
SIRSAK (
Annona muricata
L
.)
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh
Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
RINA RIANES
NIM 050804005
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA
SERTA UJI AKTIVITAS ANTIOKSIDAN JUS BUAH
SIRSAK DAN EKSTRAK ETANOL DAUN
SIRSAK (
Annona muricata
L
.)
OLEH:
RINA RIANES
NIM 050804005
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal : 06 Oktober 2012
Pembimbing I, Panitia Penguji,
Dra. Saleha Salbi, M.Si., Apt. Dra. Aswita Hafni Lubis, M.Si., Apt.
NIP 194909061980032001 NIP 195304031983032001
Pembimbing II, Dra. Saleha Salbi, M.Si., Apt.
NIP 194909061980032001
Dra. Suwarti Aris, M.Si., Apt. Drs. Muchlisyam, M.Si., Apt.
NIP 195107231982032001 NIP 195006221980021001
Marianne, S.Si., M.Si, Apt. NIP 198005202005012006
Medan, Oktober 2012 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat
kasih dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini yang
berjudul ”Karakterisasi Simplisia dan Skrining Fitokimia serta Uji Aktivitas
Antioksidan Jus Buah Sirsak dan Ekstrak Etanol Daun Sirsak”. Skripsi ini
diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana farmasi pada
Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis menyampaikan ucapan terimakasih yang
sebesar-besarnya kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku
Dekan Fakultas Farmasi Universitas Sumatera Utara yang telah memberikan
fasilitas selama masa pendidikan. Ibu Dra. Saleha Salbi, M.Si., Apt., dan Dra.
Suwarti Aris, M.Si., Apt., selaku pembimbing yang telah memberikan waktu,
bimbingan, dan nasehat selama penelitian hingga selesainya penyusunan skripsi
ini. Bapak Drs. Awaluddin Saragih, M.Si., Apt., selaku penasehat akademis yang
memberikan bimbingan kepada penulis selama ini. Bapak dan Ibu staf pengajar
Fakultas Farmasi Universitas Sumatera Utara yang telah mendidik selama
perkuliahan. Bapak dan Ibu Kepala Laboratorium Penelitian dan Farmakognosi
yang telah memberikan fasilitas, petunjuk dan membantu selama penelitian. Ibu
Dra. Aswita Hafni Lubis, M.Si., Apt., Drs. Syahrial Yoenoes, S.U., Apt., dan
Marianne, S.Si., M.Si, Apt., selaku dosen penguji yang memberikan masukan,
kritik, arahan dan saran dalam penyusunan skripsi ini.
Penulis juga ingin mempersembahkan rasa terima kasih yang tak terhingga
dengan tulus dan ikhlas, untuk adik tersayang, dan teman-teman yang selalu setia
memberi doa, dorongan dan semangat.
Penulis menyadari bahwa skripsi ini masih banyak kekurangannya, oleh
karena itu sangat diharapkan kritik dan saran yang bersifat membangun dari
semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga
skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang farmasi.
Medan, Oktober 2012
Penulis,
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA UJI AKTIVITAS ANTIOKSIDAN JUS BUAH SIRSAK DAN EKSTRAK
ETANOL DAUN SIRSAK (Annona muricata L.)
ABSTRAK
Tanaman sirsak (Annona muricata L.) suku Annonaceae banyak terdapat di Indonesia, masyarakat banyak memanfaatkan buah ini untuk jus, daunnya digunakan masyarakat sebagai obat penyakit kanker. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia dan skrining fitokimia serta aktivitas dari jus buah sirsak dan ekstrak etanol daun sirsak sebagai antioksidan dengan metode penangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazyl).
Simplisia daun sirsak diekstraksi secara maserasi dengan pelarut etanol 96%, selanjutnya ekstrak dipekatkan menggunakan alat rotary evaporator
dan dikeringkan menggunakan freeze dryer. Jus buah sirsak dan ekstrak etanol daun sirsak di uji aktivitas antioksidannya terhadap radikal bebas dengan mengukur absorbansi DPPH pada panjang gelombang 516 nm setelah didiamkan 60 menit suhu kamar. Aktivitas antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil karakteristik simplisia daun sirsak diperoleh kadar air 8,32%, kadar sari larut air 19,09%, kadar sari larut etanol 12,59%, kadar abu total 7,48%, kadar abu tidak larut asam 0,12% dan hasil karakteristik dari jus buah sirsak diperoleh kadar sari larut air 57,06%, kadar sari larut etanol 58,94%, kadar abu total 2,94%, kadar abu tidak larut asam 0,00%. Hasil skrining fitokimia diperoleh bahwa ekstrak etanol daun sirsak mengandung senyawa alkaloid, flavonoida, glikosida, saponin, tanin, steroida dan jus buah sirsak mengandung glikosida. Hasil pengujian aktivitas antioksidan dengan metode penangkapan radikal bebas DPPH menunjukkan bahwa ekstrak etanol daun sirsak memiliki IC50 sebesar 60,74 ppm, sedangkan jus buah sirsak memiliki IC50 sebesar 760,55 ppm dan IC50 dari vitamin C sebesar 4 ppm.
SIMPLEX CHARACTERIZATION AND PHYTOCHEMICAL SCREENING AND TESTS ANTIOXIDANT ACTIVITY
SOURSOP JUICE AND ETHANOL EXTRACT LEAF OF SOURSOP (Annona muricata L.)
ABSTRACT
Soursop (Annona muricata L.) of the family Annonaceae much found in Indonesia, many people use this fruit for juice, that leaves discussed the public as a cure for cancer. The purpose of this study was to investigate the characteristics of simplicia and phytochemical screening and the activity of soursop juice and ethanol extracts of leaves the soursop as an antioxidant with DPPH radical scavenging method of capture (1,1-diphenyl-2-picrylhydrazyl).
Simplex soursop leaf was extracted with maceratelly by using 96% ethanol, then the extract was concentrated using a rotary evaporator and dried using a freeze dryer. Juice of soursop and ethanol extracts leaves of the soursop tested activity of antioxidant against free radical by measuring DPPH absorbance at 516 nm of wavelength after 60 minutes left to stand at room temperature. The antioxidant’s activity was measured as a decrease in absorbance of DPPH liquid after addition of extract.
The moisture content of soursop leaf simplex is 8.32%, content water-soluble extract is 19.09%, the levels of ethanol-water-soluble extract 12.59%, 7.48% total ash, acid insoluble ash content of 0.12% and the results characterization from soursop fruit juice content of 57.06% water-soluble extract, ethanol-soluble extract content 58.94%, 2.94% total ash, acid insoluble ash content of 0.00%. Phytochemical screening results obtained that the ethanol extract leaves of the soursop contains alkaloid compounds, flavonoids, glycosides, saponins, tannins, steroida and soursop juice-containing glycosides. The test results of antioxidant activity by DPPH radical scavenging method showed that the ethanol extract leaves of the soursop has IC50 of 60.74 ppm, while the soursop juice has the IC50 of 760.55 ppm and IC50 of vitamin C at 4 ppm.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Perumusan Masalah ... 3
1.3Hipotesis ... 3
1.4Tujuan ... 4
1.5Manfaat ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1Uraian Tumbuhan ... 5
2.1.1 Morfologi tanaman sirsak ... 5
2.1.2 Daerah tumbuh ... 6
2.1.4 Uraian kandungan tumbuhan ... 7
2.2Radikal Bebas ... 8
2.2.1 Kerusakan jaringan akibat radikal bebas ... 9
2.2.2 Pertahanan jaringan terhadap radikal bebas ... 9
2.3Antioksidan ... 10
2.3.1 Vitamin C ... 10
2.3.2 Flavonoid ... 11
2.4Ekstraksi ... 12
2.5Spektrofotometer Ultraviolet dan Visibel (UV/Vis) ... 13
2.6Metode perangkap radikal 1,1-diphenyl-2-picrylhydrazyl (DPPH) ... 14
2.6.1Pelarut ... 15
2.6.2Pengukuran absorbansi – panjang gelombang ... 15
2.6.3Waktu pengukuran ... 15
BAB III METODE PENELITIAN ... 16
3.1Alat ... 16
3.2Bahan ... 16
3.3Penyiapan Bahan Tumbuhan ... 17
3.3.1Pengambilan bahan tumbuhan ... 17
3.3.2 Identifikasi tumbuhan ... 17
3.3.3 Pembuatan simplisia daun sirsak ... 17
3.4Pembuatan Pereaksi ... 17
3.4.1 Besi (III) klorida 1% ... 17
3.4.3Timbal (II) asetat 0,4 M ... 18
3.4.4Pereaksi Mayer ... 18
3.4.5Pereaksi Molisch ... 18
3.4.6Pereaksi Dragendorff ... 18
3.4.7Larutan kloralhidrat 70% ... 19
3.4.8Larutan asam sulfat 2 N ... 19
3.4.9Pereaksi Bouchardat ... 19
3.4.10 Pereaksi Liebermann-Burchard ... 19
3.4.11 Larutan pereaksi DPPH 0,5 mM ... 19
3.5Pemeriksaan Karakteristik Simplisia ... 19
3.5.1 Pemeriksaan makroskopik ... 19
3.5.2Pemeriksaan mikroskopik ... 20
3.5.3Penetapan kadar air ... 20
3.5.4Penetapan kadar sari yang larut dalam air ... 21
3.5.5Penetapan kadar sari yang larut dalam etanol ... 21
3.5.6Penetapan kadar abu total ... 21
3.5.7Penetapan kadar abu yang tidak larut dalam asam ... 22
3.6 Skrining Fitokimia ... 22
3.6.1 Pemeriksaan alkaloid ... 22
3.6.2 Pemeriksaan flavonoida ... 23
3.6.3 Pemeriksaan glikosida ... 23
3.6.3.1Pemeriksaan glikosida antrakinon ... 24
3.6.4Pemeriksaan saponin ... 24
3.6.6 Pemeriksaan steroida/triterpenoida ... 24
3.7 Pembuatan Jus Sirsak ... 25
3.8 Pembuatan Ekstrak Etanol Daun Sirsak ... 25
3.9 Pengujian Kemampuan Antioksidan dengan Spektrofotometer Visibel ... 26
3.9.1Prinsip metode penangkapan radikal bebas DPPH ... 26
3.9.2Pembuatan larutan blanko ... 26
3.9.3Penentuan panjang gelombang serapan maksimum ... 26
3.9.4Pembuatan larutan induk ... 26
3.9.5Pembuatan larutan uji ... 26
3.9.6Penentuan persen peredaman ... 27
3.9.7Penentuan nilai IC50 ... 27
BAB IV HASIL DAN PEMBAHASAN ... 29
4.1 Hasil Identifikasi Tumbuhan ... 29
4.2Karakteristik Simplisia ... 29
4.2.1 Identifikasi makroskopik ... 29
4.2.2 Identifikasi mikroskopik ... 29
4.2.3 Hasil karakteristik serbuk simplisia daun sirsak dan jus buah sirsak ... 30
4.3 Hasil Skrining Fitokimia ... 30
4.4 Hasil Analisis Aktivitas Antioksidan Sampel Uji ... 32
4.5 Hasil Analisis Peredaman Radikal Bebas DPPH oleh Sampel Uji ... 39
BAB V KESIMPULAN DAN SARAN ... 41
5.1 Kesimpulan ... 41
5.2 Saran ... 42
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Tabel Halaman
1. Hasil pemeriksaan skrining fitokimia dari serbuk simplisia daun sirsak,
ekstrak etanol daun sirsak dan jus buah sirsak ... 31
2. Hasil analisis peredaman radikal bebas oleh ekstrak etanol daun sirsak
dan jus buah sirsak ... 40
3. Karakteristik serbuk simplisia daun sirsak ... 51
DAFTAR GAMBAR
Gambar Halaman
1. Struktur kimia vitamin C ... 11
2. Kerangka flavonoid ... 11
3. Struktur dasar flavonoid ... 12
4. Kurva serapan maksimum larutan DPPH 40 ppm dalam metanol secara spektrofotometri visible ... 32
5. Hasil uji aktivitas antioksidan jus buah sirsak dengan DPPH ... 33
6. Hasil uji aktivitas antioksidan jus buah sirsak dengan DPPH ... 34
7. Hasil uji aktivitas antioksidan jus buah sirsak dengan DPPH ... 35
8. Hasil uji aktivitas antioksidan ekstrak etanol daun sirsak dengan DPPH ... 36
9. Hasil uji aktivitas antioksidan ekstrak etanol daun sirsak dengan DPPH ... 37
10.Hasil uji aktivitas antioksidan ekstrak etanol daun sirsak dengan DPPH ... 38
11.Hasil analisis aktivitas antioksidan ekstrak etanol daun sirsak dan jus buah sirsak ... 39
12.Tumbuhan sirsak (Annona muricata L.) ... 46
13.Daun sirsak ... 46
14.Simplisia daun sirsak ... 46
15.Mikroskopik serbuk simplisia daun sirsak ... 47
17.Pembuatan simplisia daun sirsak ... 49
DAFTAR LAMPIRAN
Lampiran Halaman
1. Surat hasil identifikasi tumbuhan ... 45
2. Gambar tumbuhan sirsak (Annona muricata L.), daun sirsak ... 46
3. Gambar mikroskopik ... 47
4. Gambar alat spektrofotometerUV/Vis (Shimadzu 1800) ... 48
5. Bagan kerja ... 49
6. Hasil Pemeriksaan karakteristik ... 51
7. Perhitungan Pemeriksaan karakteristik serbuk simplisia ... 52
8. Perhitungan pemeriksaan karakteristik jus buah sirsak ... 57
9. Hasil Uji Antioksidan pada jus buah sirsak ... 61
10.Hasil Uji Antioksidan pada ekstrak etanol daun sirsak ... 71
KARAKTERISASI SIMPLISIA DAN SKRINING FITOKIMIA SERTA UJI AKTIVITAS ANTIOKSIDAN JUS BUAH SIRSAK DAN EKSTRAK
ETANOL DAUN SIRSAK (Annona muricata L.)
ABSTRAK
Tanaman sirsak (Annona muricata L.) suku Annonaceae banyak terdapat di Indonesia, masyarakat banyak memanfaatkan buah ini untuk jus, daunnya digunakan masyarakat sebagai obat penyakit kanker. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia dan skrining fitokimia serta aktivitas dari jus buah sirsak dan ekstrak etanol daun sirsak sebagai antioksidan dengan metode penangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazyl).
Simplisia daun sirsak diekstraksi secara maserasi dengan pelarut etanol 96%, selanjutnya ekstrak dipekatkan menggunakan alat rotary evaporator
dan dikeringkan menggunakan freeze dryer. Jus buah sirsak dan ekstrak etanol daun sirsak di uji aktivitas antioksidannya terhadap radikal bebas dengan mengukur absorbansi DPPH pada panjang gelombang 516 nm setelah didiamkan 60 menit suhu kamar. Aktivitas antioksidan diukur sebagai penurunan absorbansi larutan DPPH setelah penambahan ekstrak.
Hasil karakteristik simplisia daun sirsak diperoleh kadar air 8,32%, kadar sari larut air 19,09%, kadar sari larut etanol 12,59%, kadar abu total 7,48%, kadar abu tidak larut asam 0,12% dan hasil karakteristik dari jus buah sirsak diperoleh kadar sari larut air 57,06%, kadar sari larut etanol 58,94%, kadar abu total 2,94%, kadar abu tidak larut asam 0,00%. Hasil skrining fitokimia diperoleh bahwa ekstrak etanol daun sirsak mengandung senyawa alkaloid, flavonoida, glikosida, saponin, tanin, steroida dan jus buah sirsak mengandung glikosida. Hasil pengujian aktivitas antioksidan dengan metode penangkapan radikal bebas DPPH menunjukkan bahwa ekstrak etanol daun sirsak memiliki IC50 sebesar 60,74 ppm, sedangkan jus buah sirsak memiliki IC50 sebesar 760,55 ppm dan IC50 dari vitamin C sebesar 4 ppm.
SIMPLEX CHARACTERIZATION AND PHYTOCHEMICAL SCREENING AND TESTS ANTIOXIDANT ACTIVITY
SOURSOP JUICE AND ETHANOL EXTRACT LEAF OF SOURSOP (Annona muricata L.)
ABSTRACT
Soursop (Annona muricata L.) of the family Annonaceae much found in Indonesia, many people use this fruit for juice, that leaves discussed the public as a cure for cancer. The purpose of this study was to investigate the characteristics of simplicia and phytochemical screening and the activity of soursop juice and ethanol extracts of leaves the soursop as an antioxidant with DPPH radical scavenging method of capture (1,1-diphenyl-2-picrylhydrazyl).
Simplex soursop leaf was extracted with maceratelly by using 96% ethanol, then the extract was concentrated using a rotary evaporator and dried using a freeze dryer. Juice of soursop and ethanol extracts leaves of the soursop tested activity of antioxidant against free radical by measuring DPPH absorbance at 516 nm of wavelength after 60 minutes left to stand at room temperature. The antioxidant’s activity was measured as a decrease in absorbance of DPPH liquid after addition of extract.
The moisture content of soursop leaf simplex is 8.32%, content water-soluble extract is 19.09%, the levels of ethanol-water-soluble extract 12.59%, 7.48% total ash, acid insoluble ash content of 0.12% and the results characterization from soursop fruit juice content of 57.06% water-soluble extract, ethanol-soluble extract content 58.94%, 2.94% total ash, acid insoluble ash content of 0.00%. Phytochemical screening results obtained that the ethanol extract leaves of the soursop contains alkaloid compounds, flavonoids, glycosides, saponins, tannins, steroida and soursop juice-containing glycosides. The test results of antioxidant activity by DPPH radical scavenging method showed that the ethanol extract leaves of the soursop has IC50 of 60.74 ppm, while the soursop juice has the IC50 of 760.55 ppm and IC50 of vitamin C at 4 ppm.
BAB I PENDAHULUAN
1.1Latar belakang
Tanaman obat sebenarnya sudah ada sejak jaman dahulu kala, bahkan
sebelum ditemukannya obat kimia. Tanaman obat bersifat aman dan bahkan tidak
menimbulkan efek samping bila dikonsumsi (Herliana dan Rifai, 2011).
Buah sirsak mengandung serat dan vitamin. Kandungan zat gizi terbanyak
dalam buah sirsak adalah karbohidrat. Salah satu jenis karbohidrat yang
terkandung dalam buah sirsak adalah gula pereduksi (glukosa dan fruktosa)
dengan kadar 81,9 -93,6% dari kandungan gula total. Sementara kandungan gula
lainnya berupa sukrosa, dekstrosa, dan levulosa. Sirsak juga mengandung
berbagai vitamin, antara lain vitamin A, B, dan C. Vitamin utama yang
terkandung dalam buah sirsak adalah vitamin C, yaitu sekitar 20 mg/100g daging
buah. Buah sirsak juga kaya vitamin B. Adapun mineral yang terkandung dalam
buah sirsak adalah fosfor, kalsium, zat besi, natrium dan kalium (Suranto, 2011).
Vitamin C berbentuk krisrtal putih, merupakan suatu asam organik dan terasa
asam, tetapi tidak berbau. Dalam larutan, vitamin C mudah rusak karena oksidasi
oleh oksigen dari udara, tetapi lebih stabil bila terdapat dalam bentuk kristal
kering (Sediaoetama, 2008).
Daun sirsak mengandung senyawa asetogenin, tanin, fitosterol, kalsium
oksalat, alkaloid murisin, flavonoida dan steroida (Suranto, 2011).
Antioksidan adalah zat yang dapat menetralisir radikal bebas sehingga
sehingga tidak liar lagi (Kosasih, dkk., 2004). Antioksidan alami dari tumbuhan
umumnya adalah senyawa fenol atau polifenol yang dapat berupa golongan
flavanoid (salah satu golongan fenol alami terbesar), turunan asam sinamat,
kumarin, tokoferol, dan asam-asam organik polifungsional. Antioksidan golongan
flavonoid antara lain adalah flavon, flavonol, isoflavon, katekin, dan kalkon
(Suranto, A., 2011). Radikal bebas merupakan atom atau molekul yang sifatnya
sangat tidak stabil. Ketidakstabilan ini disebabkan karena atom tersebut memiliki
satu atau lebih elektron yang tidak berpasangan (Kosasih, dkk., 2004).
Metode perangkap radikal 1,1-diphenyl-2-picrylhydrazyl (DPPH) adalah suatu metode sederhana, cepat dan murah yang dapat digunakan untuk menguji
kemampuan antioksidan yang terkandung dalam makanan. Metode ini dapat
digunakan untuk sampel yang padat dan bentuk larutan. Prinsipnya adalah
elektron ganjil pada molekul DPPH memberikan serapan maksimum pada
panjang gelombang 516 nm, berwarna ungu. Warna akan berubah dari ungu
menjadi kuning lemah apabila elektron ganjil tersebut berpasangan dengan atom
hidrogen yang disumbangkan senyawa antioksidan. Perubahan warna ini
berdasarkan reaksi kesetimbangan kimia (Prakash, 2001).
Pada metode DPPH sebaiknya digunakan standar atau kontrol positif.
Standard yang umum digunakan adalah asam askorbat (vitamin C). Standard ini
digunakan untuk memastikan bahwa prosedur yang dilakukan telah sesuai
(Molyneux, 2004).
Berdasarkan hal di atas, penulis tertarik untuk mengetahui karakterisasi
simplisia dan skrining fitokimia serta aktivitas antioksidan jus buah sirsak dan
1.2Perumusan Masalah
Perumusan masalah terdiri dari:
a. apakah karakterisasi simplisia daun sirsak yang diteliti sesuai dengan
Materia Medika Indonesia?
b. apakah golongan senyawa kimia yang terkandung didalam simplisia daun,
ekstrak etanol daun dan jus buah sirsak?
c. apakah jus buah dan ekstrak etanol daun sirsak memiliki aktivitas
antioksidan?
d. bagaimana kekuatanaktivitas antioksidan dari jus buah dan ekstrak etanol
daun sirsak dibandingkan dengan vitamin C?
1.3Hipotesis
Hipotesis penelitian terdiri dari:
a. karakteristik simplisia daun sirsak sesuai dengan Materia Medika
Indonesia
b. golongan senyawa kimia yang terkandung didalam simplisia daun dan
ekstrak etanol daun sirsak adalah alkaloida, flavonoida, glikosida, saponin,
tanin, steroida sedangkan pada buah golongan senyawa kimia yang
terkandung didalamnya adalah glikosida
c. jus buah dan ekstrak etanol daun sirsak memiliki aktivitas antioksidan
d. jus buah sirsak dan ekstrak etanol daun sirsak memiliki aktivitas
antioksidan yang lemah dibandingkan dengan aktivitas antioksidan
vitamin C
1.4Tujuan
1. Untuk menentukan karakteristik simplisia daun sirsak dan jus buah sirsak.
2. Untuk mengetahui golongan senyawa kimia yang terkandung dalam
simplisia daun sirsak, ekstrak etanol daun sirsak dan jus buah sirsak.
3. Untuk mengetahui aktivitas antioksidan dari jus buah sirsak dan ekstrak
etanol daun sirsak.
4. Untuk mengetahui perbandingan kekuatan antioksidan dari jus buah sirsak
dengan ekastrak etanol daun sirsak dibandingkan dengan vitamin C sebagai control.
1.5Manfaat
Manfaat dari penelitian ini adalah sebagai informasi tentang jus buah dan
ekstrak etanol daun sirsak yang memiliki aktivitas antioksidan dan dapat
BAB II
TINJAUAN PUSTAKA
2.1Uraian Tumbuhan
2.1.1Morfologi tanaman sirsak a. Daun
Daun sirsak berbentuk bulat panjang dengan ujung lancip pendek. Daun
tuanya berwarna hijau tua sedangkan daun mudanya berwarna hijau kekuningan.
Daun sirsak tebal dan agak kaku dengan urat daun menyirip atau tegak pada urat
daun utama. Daun sirsak terkadang menimbulkan bau yang tidak enak dicium
(Herliana dan Rifai, 2011).
b. Bunga
Bunga sirsak berukuran besar, bermahkota tebal dan warnanya hijau.
Bunga ini tersusun dari berlapis-lapis mahkota, 3 helai lapisan dalam dan 3 helai
lapisan luarnya. Bunga sirsak keluar pada tunas yang pendek di sepanjang cabang
atau ranting. Umumnya bunga sirsak berbunga sempurna, tetapi sering juga
ditemukan bunga betina saja. Sifat penyerbukannya adalah penyerbukan silang
dengan bantuan serangga (Suranto, 2011).
c. Buah
Buah sirsak termasuk buah semu, daging buah lunak atau lembek,
berwarna putih, berserat dan berbiji pipih berwarna hitam. Rasa daging buah
sirsak yaitu manis, manis asam, segar serta beraroma khas. Apabila sudah matang,
warna kulit buahnya agak terang, hijau kekuningan dan mengkilap. Bagian
d. Batang
Pohon sirsak tingginya bias mencapai 10 m, dengan diameter batang 10-30
cm. Batang sirsak dapat digunakan untuk perbanyakan tanaman secara vegetatif
dengan cara okulasi maupun sambung pucuk. Batang tanaman sirsak mempunyai
banyak cabang dan cabangnya mempunyai banyak ranting sehingga
menjadikannya rimbun. Kulit batang sirsak mudah dikupas sehingga
memudahkan untuk diokulasi (Suranto, 2011).
2.1.2Daerah tumbuh
Sirsak merupakan jenis tanaman yang paling mudah tumbuh diantara
jenis-jenis Annona lainnya dan memerlukan iklim tropik yang hangat dan lembab.
Tanaman ini dapat tumbuh pada ketinggian sampai 1200 m dari permukaan laut.
Tanaman sirsak akan tumbuh sangat baik pada keadaan iklim bersuhu 22-28oC,
dengan kelembaban dan curah hujan berkisar antara 1500-2500 mm per tahun.
Keadaan yang terlalu panas dan terlalu dingin akan mempengaruhi
pertumbuhan tanaman sirsak. Pertumbuhan dan pembungaannya sangat terhambat
oleh cuaca yang dingin. Sedangkan musim kemarau, tanaman sirsak akan
menyesuaikan diri terhadap lingkungannya dengan merontokkan daunnya untuk
2.1.3Sistematika tumbuhan
Tanaman sirsak (Annona muricata Linn.) termasuk tanaman tahunan dengan sistematika sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyldonae
Famili : Annonaceae
Genus : Annona
Species : Annona muricata L. (Herliana dan Rifai N, 2011). 2.1.4Uraian kandungan tumbuhan
a. Buah
Buah sirsak mengandung serat dan vitamin. Komposisi rata-rata satu buah
sirsak adalah 67,5% daging buah, 20% kulit buah, 8,5% biji, dan 4% poros tegah
buah (empulur). Pada daging buahnya mengandung 80% air, 3% asam yang dapat
dititrasi, dan 24% gula nonpereduksi (Suranto, 2011).
Kandungan zat gizi terbanyak dalam buah sirsak adalah karbohidrat, yaitu
sekitar 685 dari seluruh bagian padat daging buahnya. Salah satu jenis karbohidrat
yang terkandung dalam buah sirsak adalah gula pereduksi (glukosa dan fruktosa)
dengan kadar 81,9 -93,6% dari kandungan gula total. Sementara kandungan gula
lainnya berupa sukrosa 2,54%, dekstrosa5,05%, dan levulosa 0,04%. Sirsak juga
mengandung berbagai vitamin, antara lain vitamin A,B, dan C. Vitamin utama
yang terkandung dalam buah sirsak adalah vitamin C, yaitu sekitar 20 mg/100g
daging buah. Adapun mineral yang terkandung dalam buah sirsak adalah fosfor,
kalsium, zat besi, natrium dan kalium (Suranto, 2011).
b. Daun
Daun sirsak mengandung senyawa monotetrahidrofuran asetogenin,
seperti anomurisin A dan B, gigantetrosin A, annonasin-10-one, murikatosin A
dan B, annonasin, dan goniotalamisin. Khasiat senyawa-senyawa ini untuk
pengobatan berbagai penyakit. Daun dan batang sirsak juga mengandung senyawa
tanin, fitosterol, kalsium oksalat, serta alkaloid murisin (Suranto, 2011).
c. Biji
Di Indonesia, biji sirsak terkenal sebagai pestisida alami yang mampu
membunuh larva hama dan penyakit tanaman. Biji sirsak mengandung 8% air, 2%
protein, 13% abu, 8% serat, 20% lemak, dan 47% karbohidrat. Selain itu, biji
sirsak mengandung 0,2% mineral/abu yang larut dalam air, 0,8% asam yang dapat
dititrasi, dan 17 mg kalsium/100 g. Biji sirsak juga mengandung 17% minyak
kuning (yellow oil) (Suranto, 2011). 2. 2 Radikal Bebas
Radikal bebas merupakan atom atau molekul yang sifatnya sangat tidak
stabil. Ketidakstabilan ini disebabkan karena atom tersebut memiliki satu atau
lebih elektron yang tidak berpasangan. Atom tersebut berusaha untuk memiliki
pasangan elektron, sehingga sifatnya sangat reaktif. Atom ini cenderung mencuri
partikel dari molekul lain dan kemudian membuat senyawa baru yang tidak
Sel persenyawaan terjadi, mulailah reaksi berantai yang dapat merusak
sel-sel penting dalam tubuh. Kerusakan itu antara lain menyebabkan terjadinya
mutasi DNA, sehingga berubah menjadi ganas dan menimbulkan berbagai
penyakit (Kosasih, dkk, 2004).
Pembentukan radikal bebas dan reaksi oksidasi pada biomolekul akan
berlangsung sepanjang hidup. Radikal bebas yang sangat berbahaya dalam
makhluk hidup antara lain adalah golongan hidroksil (OH*), superoksida (O-2),
nitrogen monooksida (NO), peroksidal (RO-2), peroksinitrit (ONOO-), asam
hipoklorit (HOCl), hydrogen peroksida (H2O2) (Silalahi, 2006).
2. 2. 1. Kerusakan jaringan akibat radikal bebas
Sifat radikal bebas yang tidak stabil ini menyebabkan reaksi menerima
atau memberikan elektron dengan molekul sekitarnya. Kebanyakan molekul ini
bukan radikal bebas melainkan makromolekul biologi seperti lipid, protein, asam
nukleat dan karbohidrat. Dengan reaksi ini timbullah reaksi radikal bebas
beruntun yaitu terbentuknya radikal bebas baru yang bereaksi lagi dengan
makromolekul lain (Kosasih, dkk, 2004).
2.2.2 Pertahanan jaringan terhadap radikal bebas
Tubuh telah menyiapkan pertahanan berupa antioksidan terhadap serangan
radikal bebas ini di tingkat sel, membran dan ekstrasel. Antioksidan adalah
senyawa yang dalam kadar rendah dibanding bahan yang dapat dioksidasi, sangat
memperlambat atau menghambat oksidasi bahan tersebut. Antioksidan
melumpuhkan radikal bebas dengan memberikan elektron kepadanya sehingga
2. 3. Antioksidan
Antioksidan berfungsi mengatasi atau menetralisir radikal bebas dan
melindungi tubuh dari beragam penyakit. Antioksidan adalah zat yang dapat
menetralisir radikal bebas sehingga atom dengan elektron yang tidak berpasangan
mendapat pasangan elektron sehingga tidak liar lagi (Kosasih, dkk, 2004).
Diketahui bahwa masuknya antioksidan berasal dari makanan, seperti
sayur mayur dan suplemen makanan termasuk vitamin A, vitamin E, vitamin C
dan betakaroten, ginseng dan ginko biloba (Kosasih, dkk, 2004). Antioksidan
alami dari tumbuhan umumnya adalah senyawa fenol atau polifenol yang dapat
berupa golongan flavanoid (salah satu golongan fenol alami terbesar), turunan
asam sinamat, kumarin, tokoferol, dan asam-asam organik polifungsional.
Antioksidan golongan flavonoid antara lain adalah flavon, flavonol, isoflavon,
katekin, dan kalkon (Suranto, 2011).
2.3.1 Vitamin C
Vitamin C atau asam askorbat mempunyai berat molekul 178,13, rumus
molekul C6H8O6, titik lebur lebih kurang 190°C, berbentuk serbuk atau hablur,
warnanya putih atau agak kuning, apabila kena cahaya lambat laun menjadi gelap.
Stabil di udara dalam keadaan kering dan mudah teroksidasi dalam larutan, mudah
larut dalam air, agak sukar larut dalam etanol, tidak larut dalam kloroform, eter
dan benzen. Penyimpanannya dalam wadah tertutup rapat dan tidak tembus
cahaya (Ditjen POM, 1995). Struktur kimia vitamin C dapat dilihat pada Gambar
Gambar 1. Struktur kimia vitamin C
Vitamin C merupakan salah satu senyawa kimia yang mempunyai potensi
sebagai antioksidan dengan mendonorkan hidrogen dari gugus hidroksilnya
kepada radikal bebas. Vitamin C juga dapat meningkatkan kekebalan tubuh
terhadap infeksi dan virus. Aktivitas sistem kekebalan yang optium memerlukan
keseimbangan antara pembentukan radikal bebas dan proteksi antioksidan
(Silalahi, 2006).
2.3.2 Flavonoid
Senyawa flavonoid merupakan salah satu senyawa polifenol yang
mengandung 15 atom karbon dalam inti dasarnya, yang tersusun dalam
konfigurasi C6 – C3 – C6, yaitu dua cincin aromatik yang dihubungkan oleh satuan
3 karbon yang dapat atau tidak dapat membentuk cincin ketiga (Markham, 1988).
Kerangka flavonoid dapat dilihat pada Gambar 2 berikut:
Gambar 2. Kerangka flavonoid
Flavonoid terdapat dalam tumbuhan sebagai campuran dari flavonoid yang
pada tumbuhan terdapat dalam berbagai bentuk struktur molekul dengan beberapa
bentuk kombinasi glikosida. Untuk menganalisis flavonoid lebih baik memeriksa
aglikon yang telah terhidrolisis daripada dalam bentuk glikosida dengan
strukturnya yang rumit dan kompleks. Flavonoid dapat berkhasiat sebagai
antioksidan, antibakteri dan antiinflamasi (Harborne, 1984). Struktur dasar dan sistem penomoran untuk turunan flavonoid dapat dilihat pada Gambar 3 berikut:
[image:30.595.234.400.261.365.2]
Gambar 3. Struktur dasar flavonoid
2.4 Ekstraksi
Ekstraksi adalah suatu proses pemisahan kandungan senyawa kimia dari
jaringan tumbuhan maupun hewan. Sebelum ekstraksi dilakukan biasanya
bahan-bahan dikeringkan terlebih dahulu kemudian dihaluskan pada derajat kehalusan
tertentu (Harborne, 1984).
Metode ekstraksi yang sering digunakan dalam berbagai penelitian
menurut (Ditjen POM, 2000) adalah sebagai berikut:
a. Cara dingin
1. Maserasi adalah proses penyarian simplisia dengan cara perendaman
menggunakan pelarut dengan sesekali diaduk, pada temperatur kamar.
Maserasi dengan pengadukan secara terus-menerus disebut maserasi kinetik
dan yang dilakukan pengulangan panambahan pelarut setelah dilakukan
2. Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru
sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur
kamar. Proses perkolasi terdiri dari tahap pelembaban bahan, tahap
perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan
ekstrak) terus-menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali
bahan.
b. Cara panas
1. Refluks adalah proses penyarian simplisia dengan menggunakan pelarut pada
temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas
yang relatif konstan dengan adanya pendingin balik.
2. Digesti adalah proses penyarian dengan pengadukan secara terus-menerus pada
temperatur lebih tinggi daripada temperatur ruangan, yaitu secara umum
dilakukan pada temperatur 40-50°C.
3. Sokhletasi adalah proses penyarian dengan menggunakan pelarut yang selalu
baru, dilakukan dengan menggunakan alat soklet sehingga menjadi ekstraksi
kontinu dengan pelarut relatif konstan dengan adanya pendingin balik.
4. Infundasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 15 menit.
5. Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 30 menit.
2.5Spektrofotometer Ultraviolet dan Visibel (UV/Vis)
Spektrofotometer UV/Vis adalah pengukuran panjang gelombang dan
ultraviolet dan cahaya tampak memiliki energi yang cukup untuk mempromosikan
elektron pada kulit terluar ke tingkat energi yang lebih tinggi. Spektroskopi
UV/Vis biasanya digunakan untuk molekul dan ion anorganik atau kompleks di
dalam larutan. Spektrum UV/Vis mempunyai bentuk yang lebar dan hanya sedikit
informasi tentang struktur yang bisa didapatkan dari spektrum ini. Tetapi
spektrum ini sangat berguna untuk pengukuran secara kuantitatif. Sinar ultraviolet
berada pada panjang gelombang 200-400 nm sedangkan sinar tampak berada pada
panjang gelombang 400-800 nm (Dachriyanus, 2004).
2.6 Metode perangkap radikal 1,1-diphenyl-2-picrylhydrazyl (DPPH)
DPPH pertama kali ditemukan pada tahun 1922 oleh Goldschmidt dan
Renn. DPPH berwarna ungu pekat seperti KMnO4, bersifat tidak larut dalam air
(Ionita, 2005).
DPPH merupakan singkatan untuk senyawa kimia 1,1-diphenyl-2 -picrylhydrazil. DPPH berupa serbuk berwarna ungu gelap yang terdiri dari molekul radikal bebas yang stabil. DPPH mempunyai berat molekul 394.32
dengan rumus bangun C18H12N5O6. Penyimpanannya dalam wadah tertutup baik
pada suhu -20°C (Molyneux, 2004).
Metode perangkap radikal 1,1-diphenyl-2-picrylhydrazyl (DPPH) adalah suatu metode sederhana, cepat dan murah yang dapat digunakan untuk menguji
kemampuan antioksidan yang terkandung dalam makanan. Metode ini dapat
digunakan untuk sampel yang padat dan bentuk larutan. Prinsipnya adalah
elektron ganjil pada molekul DPPH memberikan serapan maksimum pada
menjadi kuning lemah apabila elektron ganjil tersebut berpasangan dengan atom
hidrogen yang disumbangkan senyawa antioksidan. Perubahan warna ini
berdasarkan reaksi kesetimbangan kimia (Prakash, 2001).
2.6.1 Pelarut
Metode perangkap radikal 1,1-diphenyl-2-picrylhydrazyl (DPPH) akan memberi hasil yang baik dengan menggunakan pelarut metanol atau etanol dan
kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel uji sebagai
antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004).
2.6.2 Pengukuran absorbansi – panjang gelombang
Panjang gelombang maksimum (λmaks) yang digunakan dalam pengukuran
sampel uji sangat bervariasi. Menurut beberapa literatur panjang gelombang
maksimum untuk DPPH antara lain 515 nm, 516 nm, 517 nm, 518 nm, 519 nm
dan 520 nm. Apabila pengukuran menghasilkan tinggi puncak maksimum, maka
itulah panjang gelombangnya yaitu sekitar panjang gelombang yang disebutkan di
atas (Molyneux, 2004).
2.6.3 Waktu pengukuran
Lamanya pengukuran menurut literatur yang direkomendasikan adalah
selama 60 menit, tetapi dalam beberapa penelitian waktu yang digunakan sangat
bervariasi yaitu 5 menit, 10 menit, 20 menit, 30 menit dan 60 menit. Waktu reaksi
yang tepat adalah ketika reaksi sudah mencapai kesetimbangan. Kecepatan reaksi
dipengaruhi oleh sifat dari aktivitas antioksidan yang terdapat di dalam sampel
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah metode eksperimental. Penelitian
meliputi pengumpulan dan penyiapan bahan tumbuhan, karakterisasi simplisia,
pembuatan jus buah, pembuatan ekstrak etanol, skrining fitokimia, dan uji
aktivitas antioksidan dengan metode peredaman radikal bebas DPPH
menggunakan alat spektrofotometer visibel dibandingkan dengan Vitamin C.
3.1 Alat
Alat-alat yang digunakan terdiri dari alat gelas laboratorium,
spektrofotometer UV/Vis (Shimadzu 1800), penguap vacum putar (Stuart),
Freeze dryer (Virtis), mikroskop, neraca analitis (Vibra), penangas air (Yenaco), desikator, timbangan, object glass, gelas penutup, lemari pengering, pisau, dan
krus tang.
3.2 Bahan
Bahan yang digunakan pada penelitian adalah buah sirsak yang sudah
matang, daun sirsak (Annona muricata L). Bahan-bahan kimia lainnya adalah berkualitas pro analisis produksi Sigma: 1,1-diphenyl-2-picrylhydrazyl (DPPH); produksi E-Merck: metanol, toluen, raksa(II) klorida, kalium iodida, bismuth (III)
nitrat, asam nitrat pekat, besi (III) klorida, asam klorida pekat, asam sulfat pekat,
timbal (II) asetat, kloralhidrat, kloroform, isopropanol, benzene, asam asetat
anhidrida, natrium hidroksida, amil alcohol. Bahan kimia berkualitas teknis:
etanol 96%. Kertas saring, dan air suling.
3.3 Penyiapan bahan tumbuhan
Penyiapan bahan tumbuhan meliputi pengambilan bahan tumbuhan,
identifikasi tumbuhan, dan pembuatan simplisia daun sirsak.
3.3.1 Pengambilan bahan tumbuhan
Pengambilan bahan tumbuhan dilakukan secara purposive yaitu tanpa
membandingkan dengan daerah lain. Sampel yang digunakan adalah buah sirsak
yang masak dan daun sirsak dari daun ketiga sampai kelima dari batang yang
diambil dari Desa Keramat Kecamatan Naga Timbul Kabupaten Tanjung
Morawa.
3.3.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang Botani Pusat Penelitian Biologi-LIPI Bogor.
3.3.3 Pembuatan simplisia daun sirsak
Daun sirsak dipisahkan dari batangnya, dikumpulkan, dicuci, lalu
ditiriskan. Kemudian daun ditimbang sebagai berat basah. Bahan ini kemudian
dikeringkan di lemari pengering hingga kering, yaitu ketika simplisia tersebut
diremas akan hancur, kemudian ditimbang sebagai berat kering. Simplisia
kemudian disimpan pada wadah yang terlindung dari sinar matahari.
3.4Pembuatan Pereaksi
3.4.1 Besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida di larutkan dalam air suling sampai 100 ml
3.4.2Larutan HCl 2N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling sampai
100 ml (Depkes RI, 1978).
3.4.3Timbal (II) asetat 0,4 M
Timbal (II) asetat sebanyak 15,17g dilarutkan dalam air suling bebas CO2
hingga 100 ml (Depkes RI, 1978).
3.4.4Pereaksi Mayer
Sebanyak 1,4 g raksa (II) klorida, kemudian dilarutkan dalam air suling
hingga 60 ml. pada wadah lain ditimbang sebanyak 5 g kalium iodide lalu
dilarutkan dalam 10 ml air suling. Kedua larutan dicampurkan dan ditambahkan
air suling hingga diperoleh larutan 100 ml (Depkes RI, 1978).
3.4.5Pereaksi Molisch
Sebanyak 3 g α-naftol dilarutkan dalam asam nitrat 0,5 N hingga 100 ml
(Depkes RI, 1978).
3.4.6Pereaksi Dragendorff
Sebanyak 0,8 g bismuth nitrat dilarutkan dalam asam nitrat pekat 20 ml
kemudian dicampurkan dengan larutan kalium iodida sebanyak 27,2 g dalam 50
ml air suling. Campuran didiamkan sampai memisah sempurna. Larutan jernih
diambil dan diencerkan dengan air suling secukupnya hingga 100 ml
3.4.7Larutan kloralhidrat 70%
Sebanyak 50 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 20 ml
air suling (Depkes RI, 1978).
3.4.8Larutan asam sulfat 2 N
Sebanyak 5,5 ml asam sulfat pekat diencerkan dengan air suling hingga
diperoleh 100 ml (Depkes RI, 1978).
3.4.9Pereaksi Bouchardat
Sebanyak 4 g kalium iodida dilarutkan dalam air suling secukupnya
kemudian ditambahkan 2 g iodida sedikit demi sedikit cukupkan dengan air suling
(Depkes RI, 1978).
3.4.10 Pereaksi Liebermann-Burchard
Campur secara perlahan 5 ml asam asetat anhidrida dengan 5 ml asam
sulfat pekat tambahkan etanol hingga 50 mL (Merck, 1978).
3.4.11 Larutan pereaksi DPPH 0,5 mM
Sebanyak 19,7 mg DPPH ditimbang, kemudian dilarutkan dalam metanol
hingga volume 100 ml.
3.5Pemeriksaan Karakteristik Simplisia
3.5.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk, warna,
3.5.2Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia daun sirsak.
Serbuk simplisia ditaburkan diatas kaca objek yang telah di tetesi dengan larutan
kloralhidrat dan tutup dengan kaca penutup, kemudian diamati dibawah
mikroskop.
3.5.3Penetapan kadar air
Penetapan kadar air dilakukan menurut metode Azeotropi (destilasi
toluena). Alat terdiri dari labu alas bulat 500 ml, pendingin, tabung penyambung,
tabung penerima 5 ml berskala 0,05 ml, alat penampung dan pemanas listrik.
Cara kerja :
Dimasukkan 200 ml toluena dan 2 ml air suling ke dalam labu alas bulat,
lalu didestilasi selama 2 jam. Setelah itu, toluena dibiarkan mendingin selama 30
menit, dan dibaca volume air pada tabung penerima dengan ketelitian 0,05 ml.
Kemudian ke dalam labu tersebut dimasukkan 5 g serbuk simplisia yang telah
ditimbang seksama, labu dipanaskan hati-hati selama 15 menit. Setelah toluena
mendidih, kecepatan tetesan diatur lebih kurang 2 tetes tiap detik sampai sebagian
besar air terdestilasi, kemudian kecepatan tetesan dinaikkan hingga 4 tetes tiap
detik. Setelah semua air terdestilasi, bagian dalam pendingin dibilas dengan
toluena. Destilasi dilanjutkan selama 5 menit, kemudian tabung penerima
dibiarkan mendingin pada suhu kamar. Setelah air dan toluena memisah
sempurna, volume air dibaca dengan ketelitian 0,05 ml. Selisih kedua volume air
yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang
3.5.4 Penetapan kadar sari yang larut dalam air
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml
air-kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu
bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan
selama 18 jam, lalu disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai
kering dalam cawan penguap yang berdasar rata yang telah ditara dan sisa
dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang
larut dalam air dihitung terhadap bahan yang telah dikeringkan (WHO, 1992;
Ditjen POM, 1995).
3.5.5 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 g serbuk simplisia, dimaserasi selama 24 jam dalam 100 ml
etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama,
kemudian dibiarkan selama 18 jam. Kemudian disaring cepat untuk menghindari
penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan
penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan
pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam
etanol 96% dihitung terhadap bahan yang telah dikeringkan (WHO, 1992; Ditjen
POM, 1995).
3.5.6Penetapan kadar abu total
Sebanyak 2 g serbuk simplisia dimasukkan dalam krus porselin yang telah
dipijar dan ditara, kemudian diratakan. Krus dipijar perlahan-lahan sampai arang
habis, jika arang masih tidak dapat dihilangkan, ditambahkan air panas, saring
melalui kertas saring bebas abu. Pijarkan sisa dan kertas saring dalam krus yang
timbang. Kadar abu dihitung terhadap bahan yang telah dikeringkan (WHO, 1992;
Ditjen POM, 1995).
3.5.7Penetapan kadar abu yang tidak larut dalam asam
Abu yang diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml
asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam
dikumpulkan, disaring melalui kertas saring bebas abu, cuci dengan air panas,
dipijarkan, kemudian didinginkan dan ditimbang sampai bobot tetap. Kadar abu
yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan
(WHO, 1992; Ditjen POM, 1995).
3.6Skrining Fitokimia
Skirining fitokimia dilakukan untuk mengetahui golongan senyawa
alkaloida, flavonoida, glikosida, glikosida antrakinon, saponin, tanin, dan
steroida/triterpenoida.
3.6.1Pemeriksaan alkaloid
Serbuk simplisia ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml
asam klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2
menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk uji
alkaloida: diambil tabung reaksi, lalu kedalamnya dimasukkan 0,5 ml filtrat.
Pada masing-masing tabung reaksi:
1. Ditambahkan 2 tetes pereaksi Meyer
2. Ditambahkan 2 tetes pereaksi Bouchardat
Alkaloida positif jika terjadi endapan atau kekeruhan pada paling sedikit
dua dari tiga percobaan diatas (Depkes, (1978).
3.6.2Pemeriksaan flavonoida
Sebanyak 10 g serbuk simplisia ditambahkan 10 ml air panas, dididihkan
selama 5 menit dan disaring dalam keadaan panas, kedalam 5 ml filtrat
ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil
alcohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna
merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.3Pemeriksaan glikosida
Serbuk simplesia ditimbang sebanyak 3 g, lalu disari dengan 30 ml
campuran etanol 95% dengan air (7:3) dan 10 ml asam klorida 2 N, direfluks
selama 2 jam, didinginkan dan disaring. Diambil 20 ml filtrat ditambahkan 25 ml
air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu
disaring. Filtrat disari dengan 20 ml campuran isopropanol dan kloroform (2:3),
dilakukan berulang kali sebanyak 3 kali. Sari air dikumpulkan dan diuapkan pada
temperatur tidak lebih dari 50oC. Sisanya dilarutkan dalam 2 ml metanol. Larutan
sisa digunakan untuk percobaan berikut: 0,1 ml larutan percobaan dimasukkan
dalam tabung reaksi dan diuapkan diatas penangas air. Pada sisa ditambahkan 2
ml air dan 5 tetes peraksi Mollish. Kemudian secara perlahan-lahan ditambahkan
2 ml asam sulfat pekat melalui dinding tabung, terbentuknya cincin berwarna
3.6.3.1Pemeriksaan glikosida antrakinon
Serbuk simplisia ditimbang sebanyak 0,2 g, kemudian ditambahkan 5 ml
asam sulfat pekat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml
benzene, dikocok dan didiamkan. Lapisan benzene dipisahkan dan disaring, kocok
lapisan benzene dengan 2 ml NaOH 2 N, didiamkan. Lapisan air berwarna merah
dan lapisan benzene tidak berwarna menunjukkan adanya antrakinon (Depkes,
1978).
3.6.4Pemeriksaan saponin
Serbuk simplisia ditimbang sebanyak 0,5 g dan dimasukkan kedalam
tabung reaksi, lalu ditambahkan 10 ml air panas, didinginkan kemudian dikocok
kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1-10 cm yang stabil tidak
kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida
2N menunjukkan adanya saponin (Depkes, 1978).
3.6.5Pemeriksaan tanin
Serbuk simplisia ditimbang sebanyak 1 g, dididihkan selama 3 menit
dalam 100 ml air suling lalu didinginkan dan disaring. Pada filtrat ditambahkan
1-2 tetes pereaksi besi (III) klorida 1%. Jika terjadi warna biru kehitaman atau
hijau kehitaman menunjukkan adanya tanin (Depkes, 1978).
3.6.6Pemeriksaan steroida/triterpenoida
Sebanyak 1 g serbuk simplisia dimaserasi dengan 20 ml n-heksan selama 2
jam, lalu disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan
hijau menunjukkan adanya steroida, sedangkan warna merah, merah muda atau
ungu menunjukkan adanya triterpenoida (Harbone, 1987).
3.7 Pembuatan Jus Sirsak
Sebanyak 200 g daging buah sirsak segar dihaluskan menggunakan
blender, lalu diperas melalui kain kasa, hasil perasan ditampung dalam beker
gelas, disaring, kemudian diukur volumenya. Sari buah dibekukan di freezer, selanjutnya dipekatkan di freeze dryer sampai diperoleh sari buah sirsak yang kental.
3.8 Pembuatan Ekstrak Etanol Daun Sirsak
Pembuatan ekstrak dilakukan secara maserasi menggunakan pelarut etanol
(DepkesRI, 1979).
Caranya:
Sebanyak 200 g simplisia yang telah dihaluskan dimasukkan ke dalam
sebuah wadah, dituangi dengan 2000 ml etanol 96%, ditutup, dibiarkan selama 3
hari terlindung dari cahaya sambil sesekali diaduk, disekai. Ampas dicuci dengan
etanol dengan etanol 96% yaitu dengan menambahkan sebanyak 1500 ml kedalam
wadah tertutup, dibiarkan ditempat sejuk terlindung dari cahaya, selama 2 hari.
Saring. Filtrat yang diperoleh digabung dengan filtrat yang diperoleh sebelumnya.
3.9 Pengujian Kemampuan Antioksidan dengan Spektrofotometer Visibel 3.9.1Prinsip metode penangkapan radikal bebas DPPH
Kemampuan sampel uji dalam meredam proses oksidasi DPPH ( 1.1-diphenyl-2picryl-hidrazyl) sebagai radikal bebas dalam larutan metanol (sehingga terjadi peredaman warna ungu DPPH) dengan nilai IC50 (sebagai konsentrasi
sampel uji yang mampu menurunkan radikal bebas sebesar 50%) digunakan
sebagai parameter untuk menentukan aktivitas antioksidan sampel uji tersebut.
3.9.2Pembuatan larutan blanko
Larutan DPPH 0,5 mM dipipet sebanyak 5 ml, kemudian dimasukkan ke
dalam labu tentukur 25 ml, dicukupkan volumenya dengan metanol sampai garis
tanda (konsentrasi 40 ppm)
3.9.3Penentuan panjang gelombang serapan maksimum
Larutan DPPH konsentrasi 40 ppm dihomogenkan dan diukur serapannya
pada panjang gelombang 400-800 nm (Graham, 1976).
3.9.4Pembuatan larutan induk
Sebanyak 25 mg sampel uji ditimbang kemudian dilarutkan dalam labu
tentukur 25 ml dengan metanol lalu volumenya dicukupkan dengan metanol
sampai garis tanda (konsentrasi 1000 ppm).
3.9.5Pembuatan larutan uji
Larutan induk dipipet sebanyak 0,5 ml; 1 ml; 1,5 ml; 2 ml; kemudian
ppm, 40 ppm, 60 ppm, 80 ppm), kemudian dalam masing-masing labu tentukur
ditambahkan 5 ml larutan DPPH (konsentrasi 40 ppm) lalu volume dicukupkan
dengan metanol sampai garis tanda.
3.9.6Penentuan persen peredaman
Kemampuan antioksidan diukur sebagai penurunan serapan larutan DPPH
(peredaman warna ungu DPPH) akibat adanya penambahan larutan uji. Nilai
serapan larutan DPPH sebelum dan sesudah penambahan larutan uji tersebut
dihitung sebagai persen peredaman.
% ��������� = Α������� −Α������
Α������� × 100
Keterangan : A control = Absorbansi tidak mengandung sampel
A sampel = Absorbansi sampel
3.9.7Penentuan nilai IC50
Nilai IC50 merupakan bilangan yang menunjukkan konsentrasi sampel uji
(µg/ml) yang memberikan peredaman DPPH sebesar 50%). Nilai 0% berarti tidak
mempunyai aktivitas antioksidan, sedangkan nilai 100% berarti peredaman total
dan pengujian perlu dilanjutkkan dengan pengenceran larutan uji untuk melihat
batas konsentrasi aktivitasnya. Hasil perhitungan dimasukkan kedalam persamaan
regresi dengan konsentrasi ekstrak (µg/ml) sebagai absis (sumbu X) dan nilai %
peredaman (antioksidan) sebagai ordinatnya (sumbu Y).
Secara spesifik, suatu senyawa dikatakan sebagai antioksidan sangat kuat
sedang jika IC50 bernilai 100-150 µg/ml, dan lemah jika IC50 bernilai 151-200
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense, Bidang Botani Pusat Penelitian Biologi – LIPI Bogor menunjukkan bahwa sampel
termasuk spesies Annona muricata L., suku Annonaceae. Hasil identifikasi dapat dilihat pada Lampiran 1, halaman 45.
4.2 Karakteristik Simplisia 4.2.1 Identifikasi makroskopik
Pemeriksaan karakteristik simplisia secara makroskopik yaitu daun
tunggal, rapuh, warna kuning kecoklatan, bentuk bundar panjang, lanset atau
bundar telur terbalik, ujung dan pangkal daun runcing, tepi rata. Gambar daun
sirsak ditunjukkan pada Lampiran 2, halaman 46.
Pemeriksaan karakteristik pada buah sirsak, kulit buah berwarna hijau
kekuningan, memiliki duri yang tidak tajam dan agak lunak. Daging buah
berwarna putih, berserat dan berbiji pipih berwarna hitam. Rasa daging buah
sirsak yaitu manis asam, beraroma khas.
4.2.2 Identifikasi mikroskopik
Pemeriksaan mikroskopik serbuk simplisia daun sirsak dijumpai adanya
epidermis atas, epidermis bawah dengan stomata tipe anomositik, rambut penutup,
pembuluh kayu, sel batu dan berkas pengangkut. Hasil pemeriksaan mikroskopik
4.2.3 Hasil karakteristik serbuk simplisia daun sirsak dan jus buah sirsak Hasil karakteristik serbuk simplisia daun sirsak dapat dilihat pada
Lampiran 6, Tabel 3, halaman 51. Hasil karakteristik jus sirsak dapat dilihat pada
Lampiran 6, Tabel 4, halaman 51.
Hasil penetapan kadar air simplisia daun sirsak yang dikeringkan
memenuhi persyaratan Materia Medika Indonesia yaitu tidak melebihi 10%.
Kadar air yang melebihi persyaratan memungkinkan terjadinya pertumbuhan
jamur. Kadar abu total 7,48% tidak memenuhi peryaratan, yang menurut Materia
Medika Indonesia tidak lebih dari 6%. Mutu ekstrak dipengaruhi oleh bahan asal
yaitu tumbuhan obatnya dan khusus dipandang dari segi biologi, meliputi lokasi
tumbuhan asal (Ditjen POM, 2000). Monografi dari buah sirsak tidak ditemukan
di buku Materia Medika Indonesia.
4.3 Hasil Skrining Fitokimia
Hasil skrining fitokimia terhadap serbuk simplisia daun, ekstrak etanol
daun dan jus buah sirsak, diketahui bahwa mengandung golongan
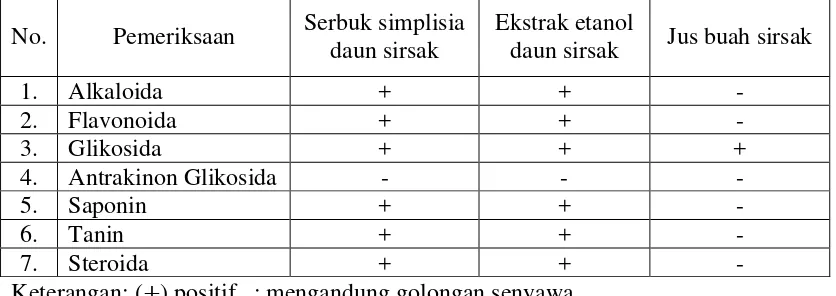
Tabel 1. Hasil pemeriksaan skrining fitokimia dari serbuk simplisia daun sirsak, ekstrak etanol daun sirsak dan jus buah sirsak
No. Pemeriksaan Serbuk simplisia
daun sirsak
Ekstrak etanol
daun sirsak Jus buah sirsak
1. Alkaloida + + -
2. Flavonoida + + -
3. Glikosida + + +
4. Antrakinon Glikosida - - -
5. Saponin + + -
6. Tanin + + -
7. Steroida + + -
Keterangan: (+) positif : mengandung golongan senyawa (−) negatif : tidak mengandung golongan senyawa
Hasil di atas menunjukkan bahwa daun sirsak memiliki potensi sebagai
antioksidan, yaitu dengan adanya senyawa-senyawa yang mempunyai potensi
sebagai antioksidan umumnya merupakan senyawa flavonoida dan karatenoid
(betakaroten) (Prakash, 2001;Kumalaningsih, 2006). Senyawa-senyawa tersebut
bertindak sebagai penangkap radikal bebas karena gugus hidroksil yang
dikandungnya dalam hal ini disebut reduktor sehingga dapat mendonorkan
hidrogen kepada radikal bebas (Silalahi, 2006).
Hasil skrining fitokimia terhadap serbuk simplisia daun sirsak, ekstrak
etanol daun sirsak menunjukkan bahwa daun sirsak berpotensi memiliki aktivitas
antioksidan, karena mengandung golongan senyawa kimia seperti flavonoid,
steroid dan tanin. Antioksidan alami dari tumbuhan umumnya adalah senyawa
fenol atau polifenol. Antioksidan yang terkandung dalam buah sirsak antara lain
adalah vitamin C (Suranto, 2011). Dalam larutan, vitamin C mudah rusak karena
oksidasi oleh oksigen dari udara, tetapi lebih stabil bila terdapat dalam bentuk
4.4 Hasil Analisis Aktivitas Antioksidan Sampel Uji
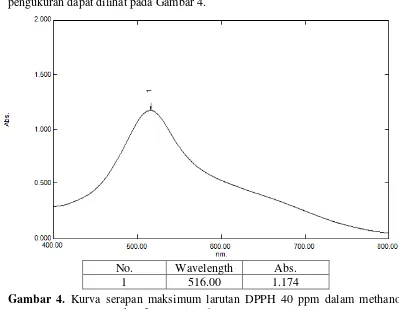
Penentuan panjang gelombang serapan maksimum larutan DPPH 40 ppm
dalam metanol diukur dengan menggunakan spektrofotometer visibel UV/Vis.
Hasil pengukuran menunjukkan bahwa larutan DPPH dalam metanol
menghasilkan serapan maksimum pada panjang gelombang 516 nm dan termasuk
dalam kisaran panjang gelombang sinar tampak (400 nm – 750 nm). Data hasil
[image:50.595.106.505.255.564.2]pengukuran dapat dilihat pada Gambar 4.
Gambar 4. Kurva serapan maksimum larutan DPPH 40 ppm dalam methanol secara spektrofotometri visible
Aktivitas antioksidan dari jus buah sirsak diperoleh dari hasil pengukuran
absorbansi DPPH dengan adanya penambahan larutan uji jus buah sirsak dengan
konsentrasi 200 ppm, 400 ppm, 600 ppm dan 800 ppm yang dibandingkan dengan
larutan kontrol DPPH (tanpa penambahan larutan uji). Data hasil pengukuran
dapat dilihat pada Gambar 5, 6, 7 dimana dari data hasil pengukuran absorbansi
DPPH digunakan sebagai parameter aktivitas antioksidan dan berdasarkan
No. Wavelength Abs.
perhitungan persamaan regresi linier diperoleh nilai IC50 untuk larutan uji jus
buah sirsak.
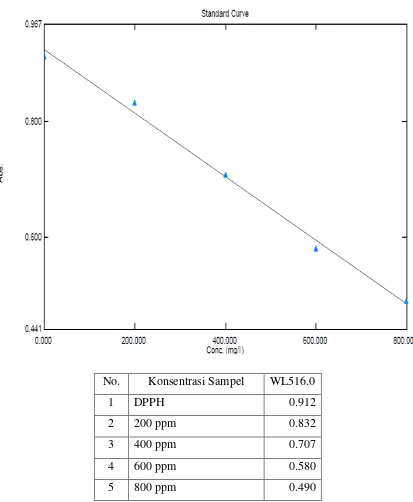
No. Konsentrasi Sampel WL516.0
1 DPPH 0.912
2 200 ppm 0.832
3 400 ppm 0.707
4 600 ppm 0.580
[image:51.595.104.517.146.648.2]5 800 ppm 0.490
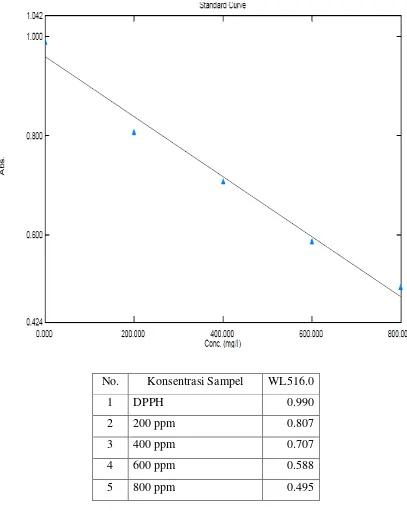
No. Konsentrasi Sampel WL516.0
1 DPPH 0.990
2 200 ppm 0.807
3 400 ppm 0.707
4 600 ppm 0.588
[image:52.595.108.515.84.595.2]5 800 ppm 0.495
Gambar 7. Hasil uji aktivitas antioksidan jus buah sirsak dengan DPPH Aktivitas antioksidan dari ekstrak etanol daun sirsak diperoleh dari hasil
pengukuran absorbansi DPPH dengan adanya penambahan larutan uji ekstrak
daun sirsak dengan konsentrasi 20 ppm, 40 ppm, 60 ppm dan 80 ppm yang
dibandingkan dengan larutan kontrol DPPH (tanpa penambahan larutan uji). Data
hasil pengukuran dapat dilihat pada Gambar 8, 9, 10 dimana dari data hasil
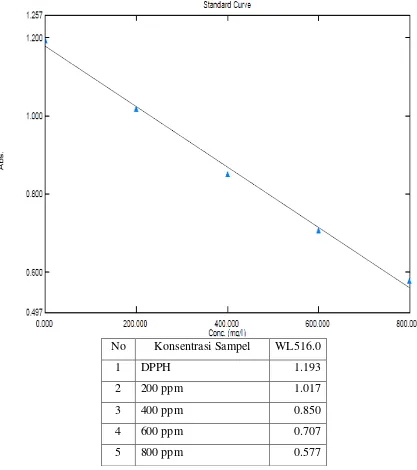
No Konsentrasi Sampel WL516.0
1 DPPH 1.193
2 200 ppm 1.017
3 400 ppm 0.850
4 600 ppm 0.707
pengukuran absorbansi DPPH digunakan sebagai parameter aktivitas antioksidan
dan berdasarkan perhitungan persamaan regresi linier diperoleh nilai IC50 untuk
[image:54.595.95.515.180.668.2]larutan uji ekstrak etanol daun sirsak.
Gambar 8. Hasil uji aktivitas antioksidan ekstrak etanol daun sirsak dengan DPPH
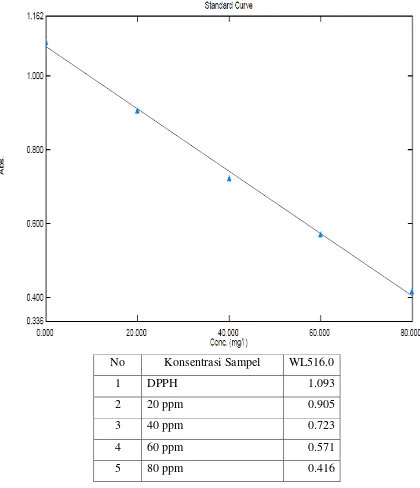
No Konsentrasi Sampel WL516.0
1 DPPH 1.093
2 20 ppm 0.905
3 40 ppm 0.723
4 60 ppm 0.571
Gambar 9. Hasil uji aktivitas antioksidan ekstrak etanol daun sirsak dengan DPPH
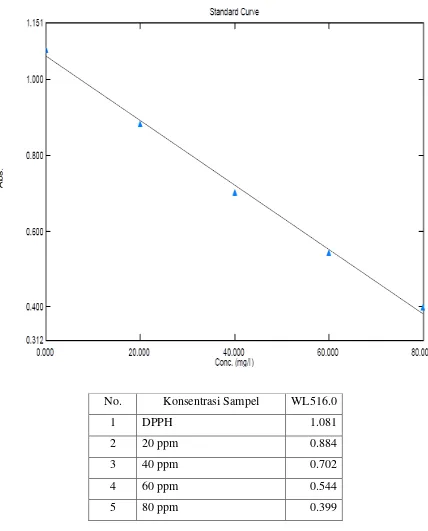
No. Konsentrasi Sampel WL516.0
1 DPPH 1.081
2 20 ppm 0.884
3 40 ppm 0.702
4 60 ppm 0.544
Gambar 10. Hasil uji aktivitas antioksidan ekstrak etanol daun sirsak dengan DPPH
Pada hasil analisis aktivitas antioksidan ekstrak etanol daun sirsak dan jus
buah sirsak dapat dilihat adanya penurunan nilai absorbansi DPPH yang diberi
larutan uji terhadap kontrol pada setiap kenaikan konsentrasi.
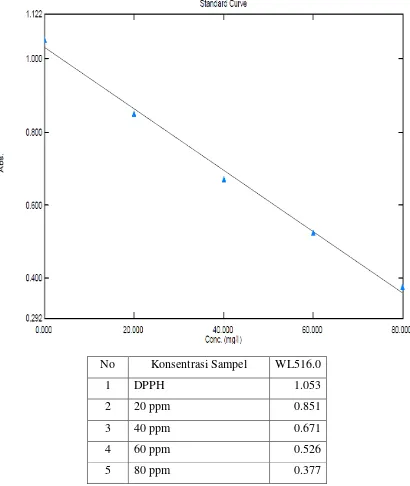
No Konsentrasi Sampel WL516.0
1 DPPH 1.053
2 20 ppm 0.851
3 40 ppm 0.671
4 60 ppm 0.526
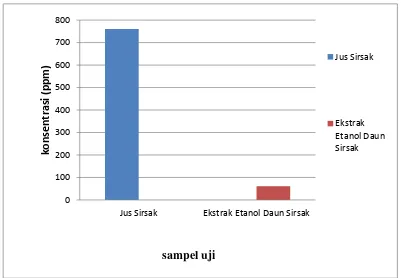
0 100 200 300 400 500 600 700 800
Jus Sirsak Ekstrak Etanol Daun Sirsak
k o ns e n tr a si (ppm ) sampel uji Jus Sirsak Ekstrak Etanol Daun Sirsak
Hubungan absorbansi DPPH terhadap penambahan konsentrasi larutan uji
dalam menganalisis aktivitas antioksidannya dapat dilihat pada gambar-gambar
[image:57.595.116.517.167.445.2]berikut ini:
Gambar 11. Hasil analisis aktivitas antioksidan ekstrak etanol daun sirsak dan jus buah sirsak
4.5 Hasil Analisis Peredaman Radikal Bebas DPPH oleh Sampel Uji
Kemampuan antioksidan diukur sebagai penurunan serapan larutan DPPH
(peredaman warna ungu DPPH) akibat adanya penambahan larutan uji. Nilai
serapan larutan DPPH sebelum dan sesudah penambahan larutan uji tersebut
dihitung sebagai persen peredaman. Hasil analisis yang telah dilakukan
menunjukkan nilai persen peredaman pada setiap kenaikan konsentrasi sampel uji
Tabel 2. Hasil analisis peredaman radikal bebas oleh ekstrak etanol daun sirsak dan jus buah sirsak
Jenis Konsentrasi Larutan Uji
(ppm) Absorbansi % Peredaman
Ekstrak Etanol Daun Sirsak
0 (blanko) 1,075 -
20 0,880 18,13
40 0,698 35,06
60 0,547 49,11
80 0,397 63,06
Jus Buah Sirsak
0 (blanko) 1,031 -
200 0,885 14,16
400 0,754 26,86
600 0,625 39,37
800 0,520 49,56
4.6 Analisis Nilai IC50 (Inhibitory Concentration) Sampel Uji
Nilai IC50 diperoleh berdasarkan persamaan regresi linier yang didapatkan
dengan cara memplot konsentrasi larutan uji dan persen peredaman DPPH sebagai
parameter aktivitas antioksidan, dimana konsentrasi larutan uji (ppm) sebagai
absis (sumbu X) dan nilai % peredaman sebagai ordinat (sumbu Y). IC50 hasil dari
persamaan regresi linier yang diperoleh untuk ekstrak etanol daun sirsak adalah
60,74 ppm, IC50 hasil dari persamaan regresi linier yang diperoleh untuk jus buah
sisak adalah 760,64 ppm dan IC50 hasil dari persamaan regresi linier yang
diperoleh untuk vitamin C adalah 4 ppm.
Suatu senyawa dikatakan sebagai antioksidan sangat kuat jika nilai IC50
kurang dari 50 µg/ml, kuat untuk IC50 bernilai 50-100 µg/ml, sedang jika IC50
bernilai 100-150 µg/ml, dan lemah jika IC50 bernilai 151-200 µg/ml (Mardawati,
2008). Nilai IC50 yang diperoleh dari ekstrak etanol daun sirsak dapat dikatakan
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
1. Hasil karakteristik serbuk simplisia daun sirsak diperoleh kadar air sebesar
8,32%, kadar sari larut air sebesar 19,09%, kadar sari larut etanol sebesar
12,59%, kadar abu total sebesar 7,48%, kadar abu tidak larut asam sebesar
0,12%. Dan hasil pemeriksaan karakteristik jus sirsak diperoleh kadar sari
larut air sebesar 57,06%, kadar sari larut etanol sebesar 58,94%, kadar abu
total sebesar 2,94%, kadar abu tidak larut asam sebesar 0,00%.
2. Hasil skrining fitokimia dari serbuk simplisia daun sirsak mengandung
golongan senyawa alkaloida, flavonoida, glikosida, saponin, tanin,
steroida. Pada ekstrak etanol daun sirsak mengandung golongan senyawa
alkaloida, flavonoida, glikosida, saponin, tanin, steroida. Sedangkan pada
jus buah sirsak mengandung glikosida.
3. Jus buah sirsak dan ekstrak etanol daun sirsak memiliki aktivitas
antioksidan.
4. Terdapat perbedaan aktivitas antioksidan antara jus buah sirsak dan ekstrak etanol daun sirsak. Aktivitas antioksidan baik jus buah sirsak
maupun ekstrak etanol daun sirsak masih di bawah aktivitas antioksidan
5.2 Saran
Disarankan kepada peneliti selanjutnya agar dapat melanjutkan penelitian
ini untuk menguji efektivitas terhadap anti kanker dari ekstrak etanol daun sirsak.
DAFTAR PUSTAKA
Cahyadi. W. (2009). Analisis & Aspek Kesehatan Bahan Tambahan Pangan. Edisi Kedua. Jakarta: Bumi Aksara. Halaman 134.
Dachriyanus. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi. Padang: Andalas University Press. Halaman 1
Ditjen POM. (1978). Materia Medika Indonesia. Jilid II, Jakarta: Departemen Kesehatan RI. Halaman 150-156.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Halaman 29-31.
Ditjen POM. (1995). Farmakope Indonesia. Edisi Keempat. Jakarta: Departemen Kesehatan RI. Halaman 39, 119, 796.
Ditjen POM. (1995). Materia Medika Indonesia, Jilid VI. Jakarta: Departemen Kesehatan RI. Halaman 321-326, 333-337.
Ditjen POM. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Cetakan Pertama. Jakarta: Departemen Kesehatan. Halaman. 9-11.
Farnsworth, N.R. (1966). Biological and Phytochemical Screening of Plants.
Journal of Pharmaceutical Sciences. 55(3): 263.
Harborne, J.B. (1984). Metode Fitokimia Penuntun Cara Modern Menganalisa Tumbuhan. Penerjemah: Kosasih Padmawinata dan Iwang Soediro. Terbitan Kedua. Bandung: Penerbit ITB. Halaman 47-102, 152-153.
Herliana, E., Rifai N. (2011). Khasiat & Manfaat Daun Sirsak Menumpas Kanker. Jakarta: Mata Elang Media. Halaman 12-16
Ionita, P. (2005). Is DPPH Stable Free Radical a Good Scavenger for Oxygen Active Species?. Bucharest. Chemical Paper. 59(1): 11-16.
Kumalaningsih, S. (2006). Antioksidan Alami. Surabaya: Trubus Agrisarana. Halaman 16-17, 24-25.
Kosasih, E.N., Tony, S., dan Hendro H. (2004). Peran Antioksidan pada Lanjut Usia. Jakarta: Pusat Kajian Nasional Masalah Lanjut Usia. Halaman 17-18, 57.
Mardawati, E., Filianty, F., dan Harta, H. (2008). Kajian Aktivitas Antioksidan Ekstrak Kulit Manggis (Garcinia mangostana L) dalam Rangka Pemanfaatan Limbah Kulit Manggis di Kecamatan Puspahiang Kabupaten Tasikmalaya. Halaman 4.
Molyneux, P. (2004). The Use of The Stable Free Radical Diphenylpicrylhydrazyl (DPPH) for Estimating Antioxidant Activity. Songklanakarin. J. Sci. Technol. 26(2): 214-215.
Prakash, A. (2001). Antioxidant Activity. Analytical Progress. 19(2): 1-4.
Rosidah, Yam, M.F., Sadikun, A., dan Asmawi, M.Z. (2008). Antioxidant Potential of Gynura procumbens. Pharmaceutical Biology 46(9): 616-625.
Sediaoetama, A.D. (2008). Ilmu Gizi untuk Mahasiswa dan Profesi. Jilid I. Jakarta: Penerbit Dian Rakyat. Halaman 131.
Silalahi, J. (2006). Makanan Fungsional. Yogyakarta: Penerbit Kanisius. Halaman 40, 47-48.
Suranto, A. (2011). Dahsyatnya Sirsak Tumpas Penyakit. Jakarta: Pustaka Bunda. Halaman 4-15.
Lampiran 2.
Gambar 12. Tumbuhan sirsak (Annona muricata L.)
Lampiran 3.
Gambar 15. Mikroskopik serbuk simplisia daun sirsak Keterangan:
1. Epidermis 2. Palisade
Lampiran 4. .
Lampiran 5.
dibersihkan dari