Rina Afriyana Sirait : Penerapan Metode Spektrofotometri Ultraviolet Pada Penetapan Kadar Nifedipin Dalam Sediaan Tablet, 2009.
PENERAPAN METODE SPEKTROFOTOMETRI ULTRAVIOLET PADA PENETAPAN KADAR NIFEDIPIN
DALAM SEDIAAN TABLET
SKRIPSI
Oleh:
RINA AFRIYANA SIRAIT NIM 050804018
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Rina Afriyana Sirait : Penerapan Metode Spektrofotometri Ultraviolet Pada Penetapan Kadar Nifedipin Dalam Sediaan Tablet, 2009.
PENERAPAN METODE SPEKTROFOTOMETRI ULTRAVIOLET PADA PENETAPAN KADAR NIFEDIPIN
DALAM SEDIAAN TABLET
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
Oleh:
RINA AFRIYANA SIRAIT NIM 050804018
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
Rina Afriyana Sirait : Penerapan Metode Spektrofotometri Ultraviolet Pada Penetapan Kadar Nifedipin Dalam Sediaan Tablet, 2009.
PENGESAHAN SKRIPSI
PENERAPAN METODE SPEKTROFOTOMETRI ULTRAVIOLET PADA PENETAPAN KADAR NIFEDIPIN
DALAM SEDIAAN TABLET
Oleh:
RINA AFRIYANA SIRAIT NIM 050804018
Dipertahankan di hadapan Panitia Penguji Fakultas Farmasi
Universitas Sumatera Utara Pada tanggal: Agustus 2009 Pembimbing I,
(Dra. Nurmadjuzita, M.Si., Apt.) NIP 194809041974122001
Pembimbing II,
(Drs. Fathur Rahman Harun, M.Si.,Apt.) NIP 19520041980031002
Panitia Penguji,
(Drs. Chairul Azhar Dalimunthe, M.Sc., Apt.) NIP 194907061980021001
(Dra. Nurmadjuzita, M.Si., Apt.) NIP 194809041974122001
(Drs. Syafruddin, MS., Apt.) NIP 194811111976031003
(Dra. Salbiah, M.Si., Apt.) NIP 194810031987012001
Dekan,
iv
KATA PENGANTAR Assalamu’alaikum Wr.Wb.
Segala puji dan syukur kehadirat Allah SWT yang telah melimpahkan nikmat, rahmat, hidayah dan karunia-Nya, sehingga penulis dapat mengerjakan penelitian dan menyelesaikan penulisan skripsi ini dengan baik, juga shalawat beserta salam kepada junjungan Nabi Muhammad SAW.
Penulis mempersembahkan rasa terima kasih yang tak terhingga dan penghargaan yang sebesar-besarnya kepada Ayahanda Pachry Sirait dan Ibunda Nuraisyah Sinaga, serta saudaraku Rini Apryani Sirait dan Pebriansyah Sirait atas segala do’a, kasih sayang, dorongan moril maupun materil kepada penulis selama ini. Semoga Allah SWT selalu melindungi kalian semua.
Dengan segala ketulusan hati penulis juga menyampaikan terimakasih yang sebesar-besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., sebagai Dekan Fakultas Farmasi, beserta seluruh staf, yang telah memberikan fasilitas dan membantu kelancaran pendidikan penulis selama perkuliahan hingga selesai.
2. Ibu Dra. Nurmadjuzita, M.Si., Apt., dan Bapak Drs. Fathur Rahman Harun, M.Si., Apt. selaku pembimbing yang telah meluangkan waktu dan kesabaran yang begitu besar dalam membimbing penulis selama penelitian hingga selesainya penulisan skripsi ini.
v
Ibu Dra. Lely Sari Lubis M.Si., Apt. selaku penasehat akademik yang telah memberikan arahan dan bimbingan kepada penulis selama ini.
4. Bapak Drs. Chairul Azhar Dalimunthe, M.Sc., Apt., Bapak Drs. Syafruddin, MS., Apt., dan Ibu Dra. Salbiah, M.Si., Apt., selaku dosen penguji yang telah memberikan kritikan, saran dan arahan kepada penulis dalam menyelesaikan skripsi ini.
5. Bapak dan Ibu Staf Laboratorium Kimia Farmasi Kualitatif yang telah memberikan petunjuk dan saran serta fasilitas laboratorium selama penulis melakukan penelitian.
6. Rekan-rekan mahasiswa Fakultas Farmasi khususnya Stambuk 2005 dan buat sahabat-sahabatku Gema, Devi, Syabrina, Inayah, atas dukungan, semangat, bantuan dan persahabatan selama ini serta seluruh pihak yang tidak mungkin penulis sebutkan satu persatu yang telah banyak memberikan bantuan, motivasi dan inspirasi bagi penulis selama masa perkuliahan sampai penyusunan skripsi ini.
Penulis menyadari bahwa tulisan ini jauh dari sempurna. Untuk itu saran dan kritik diharapkan demi perbaikan dan kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini dapat memberikan kontribusi yang bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Wassalamu’alaikum Wr.Wb
Medan, Agustus 2009 Penulis
vi
Penetapan Kadar Nifedipin Dalam Sediaan Tablet Secara Spektrofotometri Ultraviolet
Abstrak
Tablet Nifedipin merupakan salah satu sediaan obat yang sering digunakan dalam pengobatan hipertensi. Tujuan penelitian ini adalah untuk menetapkan kadar nifedipin dalam sediaan tablet yang beredar di pasaran apakah memenuhi persyaratan mutu obat. Sehingga dengan kadar yang tepat obat dapat memberikan efek terapi yang dikehendaki.
Penetapan kadar nifedipin dalam sediaan tablet dilakukan secara spektrofotometri ultraviolet dengan pelarut metanol pada panjang gelombang 235 nm dan diuji validitasnya berdasarkan parameter akurasi (kecermatan) dengan metode penambahan baku (standard addition method), presisi (keseksamaan), batas deteksi (limit of detection), dan batas kuantitasi (limit of quantitation).
Diperoleh kadar untuk tablet Nifedipin generik (Kimia Farma) sebesar 107,75 % ± 1,970 tablet Nifedipin (Dexa Medica) sebesar 106,69% ± 1,095 dan tablet nama dagang; tablet Adalat (Bayer) sebesar 100,02% ± 3,066, tablet Cordalat (Kimia Farma) sebesar 100,26% ± 1,183, tablet Nifedin (Sanbe Farma) sebesar 105,75% ± 0,101, tablet Farmalat (Pratapa Nirmala)sebesar 100,76% ± 2,041.
Hasil penelitian menunjukkan bahwa kadar nifedipin dalam sediaan tablet generik dan tablet dengan nama dagang memenuhi standar persyaratan tablet menurut Farmakope Indonesia Edisi IV (1995) yaitu tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
vii
Determination of Nifedipine in the Tablet Using by Ultraviolet Spectrophotometry
Abstract
Nifedipine tablet is one of the drugs, which was used in medication, and therapy of hypertension. The purpose of this research was used to determination Nifedipine in the tablet, which circulates in the general whether it fulfilled requirement of drug quality, or not so that it will give the therapeutic effect.
The determining of nifedipin in tablet was done by ultraviolet spectrophotometry using methanol as a solvent at wavelength 235 nm and tested it validity based on parameter accuracy using standard addition method, precision, limit of detection and limit of quatitation.
Based on quantitative determination of nifedipine in generic tablet; Kimia Farma was 107.75% ± 1.970, Dexa Medica was 106.69% ± 1.095 and branded name; Adalat (Bayer) was 100.02% ± 3.066, Cordalat (Kimia Farma) was 100.26% ± 1.183, Nifedin (Sanbe Farma) was 105,75% ± 0.101 and Farmalat (Pratapa Nirmala) was 100.76% ± 2.041.
The result of research indicate that determining nifedipine in the generic tablet and branded name was fullfilled requirement of The Farmakope Indonesia Edisi IV (1995), not less than 90.0% and not more than 110.0% of the labelled amount.
Key word : nifedipine, determination, ultraviolet spectorphotometry
viii
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I. PENDAHULUAN ... 1
1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 2
1.3. Hipotesis ... 3
1.4. Tujuan ... 3
BAB II. TINJAUAN PUSTAKA ... 4
2.1. Uraian Bahan ... 4
2.1.1. Sifat Fisika dan Kimia Nifedipin ... 4
2.1.2. Farmakologi ... 5
2.1.3. Efek Samping ... 5
2.1.4. Dosis ... 6
2.1.5. Sediaan ... 6
ix
2.2.1. Teori Spektrofotometri ... 7
2.2.2. Hukum Lambert Beer...9
2.2.3. Penggunaan Spektrofotometri Ultraviolet ...10
2.2.4. Peralatan Untuk Spektrofotometri ………..13
2.3. Validasi ... 14
BAB III. METODOLOGI PENELITIAN ... 16
3.1. Alat-alat ... 16
3.2. Bahan-bahan ... 16
3.3. Pengambilan Sampel ... 16
3.4. Prosedur Penelitian ... 17
3.4.1. Pembuatan Larutan Induk Baku BPFI ... ... 17
3.4.2. Penetapan Panjang Gelombang Serapan Maximum ... 17
3.4.3. Pembuatan Kurva Kallibrasi ... 17
3.4.4. Penetapan Kadar Nifedipin dalam Sediaan Tablet ... 18
3.4.5.Uji Validasi dengan Parameter Akurasi, Presisi, Batas Deteksi dan Batas Kuantitasi...18
3.4.5.1 Uji Akurasi dengan Persen Perolehan Kembali (%Recovery)………..18
3.4.5.2 Uji Presisi………..19
3.4.5.3 Penentuan Batas Deteksi (LOD) dan Batas Kuantitasi LOQ)….………...19
3.4.6 Analisis Data secara Statistik ...20
.BAB IV. HASIL DAN PEMBAHASAN...22
x
4.2. Pembuatan Kurva Kalibrasi...24
4.3. Penentuan Kadar Nifedipin dalam sediaan tablet...26
4.4. Uji Validasi Metode Spektrofotometri Ultraviolet...26.
BAB V. KESIMPULAN DAN SARAN...28
5.1. Kesimpulan...28
5.2. Saran...28
DAFTAR PUSTAKA...29
xi
DAFTAR TABEL
Halaman Tabel 1.Data Absorbansi dari Kurva Serapan Maksimum...24 Tabel 2.Data Kurva Kalibrasi BPFI ... 25 Tabel 3.Kadar rata-rata nifedipin pada sediaan tablet ... ... 26 Tabel 4. Data hasil pengujian perolehan kembali nifedipin dengan metode
xii
DAFTAR GAMBAR
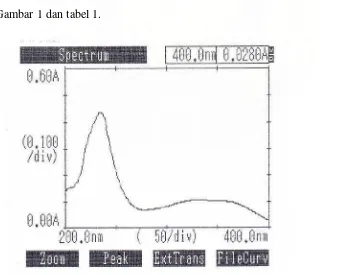
Halaman Gambar 1. Kurva Serapan Nifedipin BPFI (konsentrasi 7 mcg/ml)
dalam pelarut metanol…..………...23 Gambar 2. Kurva Kalibrasi Nifedipin BPFI dalam pelaruut metanol pada
xiii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan Persamaan Regresi. ... 31
Lampiran 2. Data kadar nifedipin sediaan tablet ... 32
Lampiran 3. Perhitungan Statistik Kadar Nifedipin pada Generik Kimia Farma ... 33
Lampiran 4. Perhitungan Statistik Kadar Nifedipin pada Tablet Nifedipin Generik Dexa Medica...35
Lampiran 5. Perhitungan Statistik Kadar Nifedipin pada Tablet Adalat (Bayer) ... 37
Lampiran 6. Perhitungan Statistik Kadar Nifedipin pada Tablet Nifedin (Sanbe) ... 39
Lampiran 7. Perhitungan Statistik Kadar Nifedipin pada Tablet Farmalat (Pratapa Nirmala) ... 41
Lampiran 8. Perhitungan Statistik Kadar Nifedipin pada Tablet Cordalat (Kimia Farma) ... 43
Lampiran 9. Perhitungan Konsentrasi Pengukuran ... 45
Lampiran 10.Contoh Perhitungan Penimbangan Sampel ... 46
Lampiran 11.Contoh Perhitungan Persentase (%) Perolehan Kembali ... 47
Lampiran 12.Data hasil persen perolehan kembali Nifedipin pada tablet (PT. Kimia Farma) dengan Metode Penambahan Baku (standard addition method) ... 49
Lampiran 13. Contoh perhitungan batas deteksi (LOD) dan batas kuantitasi (LOQ ... 50
Lampiran 14. Data Persen Perolehan Kembali (% Recovery)Perhitingan Statistik ... 51
Lampiran 15. Nilai Distribusi t ...52
xiv
BAB I PENDAHULUAN
1.1 Latar Belakang
Nifedipin termasuk derivat dihidropiridin, yang merupakan kelompok dari antagonis kalsium (Calcium Entry Blockers). Berkhasiat dalam pencegahan dan pengobatan angina pektoris dan pengobatan hipertensi. Obat ini bekerja dengan menghambat masuknya kalsium ke dalam sel-sel otot jantung dan sel-sel otot polos dinding arteri. Nifedipin diabsobsi dengan cepat dan hampir sempurna (90%) dalam lambung, +95% terikat oleh protein plasma (Siswandono, 1995).
Nifedipin memiliki sifat yang tidak stabil di bawah pengaruh cahaya akan mengalami tata ulang fotokimia menjadi turunan 4-(2-nitrofenil)-piridin (Schunack, W., 1990).
Pada pembuatan obat, pemeriksaan kadar zat aktif merupakan persyaratan yang harus dipenuhi untuk menjamin kualitas sediaan obat. Sediaan obat yang berkualitas baik akan menunjang tercapainya efek terapeutik yang diharapkan. Salah satu persyaratan mutu adalah kadar yang dikandung harus memenuhi persyaratan kadar seperti yang tercantum dalam Farmakope Indonesia.
xv
Dilihat dari struktur nifedipin yang mempunyai gugus kromofor (ikatan rangkap terkonjugasi) dan gugus ausokrom (gugus nitro dan gugus karboksil), maka senyawa ini dapat menyerap radiasi pada panjang gelombang di daerah ultraviolet. Dalam The Merck Indeks, nifedipin memiliki serapan maksimum dalam larutan metanol pada panjang gelombang 235 dan 340 nm ( 21590, 5010 ), dalam larutan asam panjang gelombang 238 dan 338 nm ( 20600, 5740) dan dalam larutan basa 238 dan 340 nm ( 20510, 5740). Sedangkan dalam Clark, nifedipin hanya memiliki serapan maksimum dalam larutan asam pada panjang gelombang 238 nm (A11 =595 b) dan 338 nm (A11 = 195 b).
Berdasarkan hal tersebut di atas, peneliti memilih metode spektrofotometri ultraviolet sebagai metode yang digunakan pada penetapan kadar nifedipin dalam sediaan tablet. Karena metode ini memiliki banyak keuntungan antara lain dapat digunakan untuk analisis suatu zat dalam jumlah kecil, pengerjaannya mudah, sederhana, cukup sensitif dan selektif, biayanya relatif murah dan mempunyai kepekaan analisis cukup tinggi (Munson, 1991). Untuk menguji keabsahan dari metode ini dilakukan uji validasi dengan parameter akurasi, presisi, limit deteksi dan limit kuantitasi. Selanjutnya metode ini digunakan untuk menentukan apakah sediaan tablet nifedipin yang beredar di pasaran tersebut memenuhi persyaratan Farmakope Indonesia Edisi IV (1995).
1.2 Perumusan Masalah
xvi
2. Apakah kadar nifedipin dalam sediaan tablet yang beredar di pasaran telah sesuai dengan ketentuan Farmakope Indonesia Edisi IV tahun 1995 ?
1.3 Hipotesis
1. Metode spektrofotometri ultraviolet dapat digunakan pada penentuan kadar nifedipin dalam sediaan tablet serta memenuhi uji validasi.
2. Kadar nifedipin dalam sediaan tablet yang beredar di pasaran sesuai dengan ketentuan Farmakope Indonesia Edisi IV tahun 1995.
1.4 Tujuan
1. Untuk mengetahui metode spektrofotometri ultraviolet dapat digunakan dalam penetapan kadar nifedipin pada tablet serta memenuhi uji validasi.
xvii
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Bahan 2.1.1 Sifat Fisikokimia
Rumus Struktur :
Rumus Molekul : C17H18N2O6
Nama Kimia : Dimetil 1,4 – dihidro 2,6 –dimetil 4 ( o nitrofenil ) -3,5 –piridina dikarboksilat ( 21829 -25 -4 )
Berat Molekul : 346,34
Suhu lebur : antara 171º sampai 175º
Pemerian : Serbuk kuning; terurai oleh cahaya langsung.
Kelarutan : Praktis tidak larut dalam air; mudah larut dalam aseton dan kloroform; kurang larut dalam etanol ( Ditjen POM, 1995;
Moffat, 2004)
xviii
2.1.2 Farmakologi
Nifedipin adalah zat pertama (1975) dari kelompok dihidropiridin dengan gugusan fenil pada posisi-para. Khasiat utamanya adalah vasodilatasi, maka terutama digunakan pada hipertensi esensil (ringan/ sedang), juga pada angina variant berdasarkan efeknya terhadap jantung yang relatif ringan: tak berkhasiat ionotrop negatif. Pada angina stabil hanya digunakan bila beta-blockers dikontra-indikasi atau kurang efektif. Khususnya dianjurkan tablet long-acting Oros (=system osmotis yang melepaskan obat secara teratur untuk waktu lama).
Agar efeknya pesat, tablet dapat dikunyah dan diletakkan di bawah lidah (pada krisis hipertensi). Selanjutnya obat ini juga berguna pada Penyakit Raynaud dan serangan sedu (hiccup) (Tjay dan Kirana, 2002).
2.1.3 Efek Samping
Efek samping yang sering terjadi adalah udema pergelangan kaki(10%). Dosis awal yang terlalu tinggi dapat memprovokasi serangan angina akibat hipotensi kuat mendadak, sporadis, malah ischemia dan infark akibat refleks tachycardia, terutama pada lansia. Beberapa penelitian memberikan indikasi mengenai peningkatan resiko jantung dan kanker (Mycek et all, 2001).
xix
2.1.4 Dosis
• Dosis dewasa :
Dosis angina dan fenomena Raynaud, sediaan konvensional, dosis awal 10 mg (usia lanjut dan gangguan hati 5 mg) 3 kali sehari dengan atau setelah makan; dosis pemeliharaan 5-20 mg 3 kali sehari; untuk efek yang segera pada angina: gigit kapsul dan telan dengan cairan. Hipertensi ringan sampai sedang dan profilaksis angina: sediaan lepas lambat, 30 mg sekali sehari (tingkatkan bila perlu, maksimum 90 mg sekali sehari) atau 20 mg 2 kali sehari dengan atau setelah makan (awalnya 10 mg 2 kali sehari, dosis pemeliharaan lazim 10-40 mg 2 kali sehari).
• Dosis anak-anak: Hipertrofi kardiopati 0,6-0,9 mg/kg/24 jam dalam 3-4 dosis terbagi.
• Dosis pasien hemodialisis: tidak diperlukan dosis tambahan.
• Dosis pasien dengan gangguan hepar: diperlukan penurunan dosis 50-60% pada pasien yang menderita sirosis hepatik.
(Anonim, 2008; Tjay dan Kirana, 2002)
2.1.5 Sediaan
xx
2.2 Spektrofotometri Ultraviolet
2.2.1 Teori Spektrofotometri Ultraviolet
Spektrofotometri serapan merupakan pengukuran suatu interaksi antara radiasi elektromagnetik dan molekul atau atom dari suatu zat kimia. Teknik yang sering digunakan dalam analisis farmasi meliputi spektrofotometri ultraviolet, cahaya tampak, infra merah dan serapan atom. Jangkauan panjang gelombang untuk daerah ultraviolet adalah 190-380 nm, daerah cahaya tampak 380-780 nm, daerah infra merah dekat 780-3000 nm, dan daerah infra merah 2,5-40 µm atau 4000-250 cm-1 ( Ditjen POM, 1995).
Radiasi ultraviolet dan sinar tampak diabsorpsi oleh molekul organik aromatik, molekul yang mengandung elektron-π terkonyugasi dan atau atom yang mengandung elektron-n, menyebabkan transisi elektron di orbital terluarnya dari tingkat energi elektron dasar ke tingkat energi elektron tereksitasi lebih tinggi. Besarnya serapan radiasi tersebut sebanding dengan banyaknya molekul analit yang mengabsorpsi sehingga dapat digunakan untuk analisis kuantitatif (Satiadarma, 2004).
Gugus fungsi yang menyerap radiasi di daerah ultraviolet dekat dan daerah tampak disebut khromofor dan hampir semua khromofor mempunyai ikatan tak jenuh. Pada khromofor jenis ini transisi terjadi dari π →π*, yang menyerap pada
λmax kecil dari 200 nm (tidak terkonyugasi), misalnya pada >C=C< dan -C≡C-.
xxi
perbedaan energi antara keadaan dasar dan keadaan tereksitasi menjadi lebih kecil sehingga penyerapan terjadi pada panjang gelombang yang lebih besar.
Gugus fungsi seperti –OH, -NH2 dan –Cl yang mempunyai elektron-elektron
valensi bukan ikatan disebut auksokhrom yang tidak menyerap radiasi pada panjang gelombang lebih besar dari 200 nm, tetapi menyerap kuat pada daerah ultraviolet jauh. Bila suatu auksokhrom terikat pada suatu khromofor, maka pita serapan khromofor bergeser ke panjang gelombang yang lebih panjang (efek batokhrom) dengan intensitas yang lebih kuat. Efek hipsokhrom adalah suatu pergeseran pita serapan ke panjang gelombang lebih pendek, yang sering kali terjadi bila muatan positif dimasukkan ke dalam molekul dan bila pelarut berubah dari non polar ke pelarut polar (Dachriyanus, 2004).
Secara eksperimental, sangat mudah untuk mengukur banyaknya radiasi yang diserap oleh suatu molekul sebagai fungsi frekuensi radiasi. Suatu grafik yang menghubungkan antara banyaknya sinar yang diserap dengan frekuensi (atau panjang gelombang) sinar merupakan spectrum absorpsi. Transisi yang dibolehkan (allowed transition) untuk suatu molekul dengan struktur kimia yang berbeda adalah tidak sama ssehingga spectra absorpsinya juga berbeda. Dengan demikian, spectra dapat digunkan sebagai bahan informasi yang bermanfaat untuk analisis kualitatif. Banyaknya sinar yang diabsorpsi pada panjang gelombang tertentu sebanding dengan banyaknya molekul yang menyerap radiasi, sehingga spectra absorpsi juga dapat digunakan untuk analisis kuantitatif (Gandjar dan Rohman,2007).
xxii
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang dimana terjadi serapan maksimum. Untuk memperoleh panjang gelombang serapan maksimum, dilakukan dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu larutan baku pada konsentrasi tertentu.
b. Pembuatan Kurva Kalibrasi
Dibuat seri larutan baku dari zat yang akan dianalisis dengan berbagai konsentrasi. Masing – masing absorbansi larutan dengan berbagai konsentrasi diukur, kemudian dibuat kurva yang merupakan hubungan antara absorbansi dengan konsentrasi. Bila hukum Lambert-Beer terpenuhi maka kurva kalibrasi berupa garis lurus.
c. Pembacaan absorbansi sampel atau cuplikan
Absorbansi yang terbaca pada spektrofotometer hendaknya antara 0,2 sampai 0,6. Anjuran ini berdasarkan anggapan bahwa pada kisaran nilai absorbansi tersebut kesalahan fotometrik yang terjadi adalah paling minimal (Gandjar dan Rohman, 2007).
2.2.2 Hukum Lambert Beer
Menurut Hukum Lambert, serapan berbanding lurus terhadap ketebalan sel yang disinari. Menurut Hukum Beer, yang hanya berlaku untuk cahaya monokromatik dan larutan yang sangat encer, serapan berbanding lurus dengan konsentrasi (banyak molekul zat). Kedua pernyataan ini dapat dijadikan satu dalam Hukum Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus terhadap konsentrasi dan ketebalan sel, yang dapat ditulis dalam persamaan:
xxiii
Dimana: A = serapan (tanpa dimensi) a = absorptivitas ( g-1 cm-1) b = ketebalan sel (cm) C = konsentrasi(g. l-1)
= absorptivitas molar ( M-1cm-1)
Jadi dengan Hukum Lambert-Beer konsentrasi dapat dihitung dari ketebalan sel dan serapan. Absorptivitas merupakan suatu tetapan dan spesifik untuk setiap molekul pada panjang gelombang dan pelarut tertentu.
Menurut Roth dan Blaschke (1981), absorptivitas spesifik juga sering digunakan sebagai ganti absorptivitas. Harga ini memberikan serapan larutan 1% (b/v) dengan ketebalan sel 1 cm, sehingga dapat diperoleh persamaan:
A = A11 . b . C
Dimana: A11 = absorptivitas spesifik (ml g-1 cm-1) b = ketebalan sel (cm)
C = konsentrasi senyawa terlarut (g/100 ml larutan)
2.2.3 Penggunaan Spektrofotometri Ultraviolet
Pada umumnya spektrofotometri ultraviolet dalam analisis senyawa organik digunakan untuk:
xxiv
2. Menjelaskan informasi dari struktur berdasarkan panjang gelombang serapan maksimum suatu senyawa
3. Mampu menganalisis senyawa organik secara kuantitatif dengan menggunakan hukum Lambert-Beer (Dachriyanus, 2004).
Analisis kualitatif
Kegunaan spektrofotometri ultraviolet dalam analisis kualitatif sangat terbatas, karena rentang daerah radiasi yang relatif sempit hanya dapat mengakomodasi sedikit sekali puncak absorpsi maksimum dan minimum, karena itu identifikasi senyawa yang tidak diketahui, tidak memungkinkan.
Penggunaannya terbatas pada konfirmasi identitas dengan menggunakan parameter panjang gelombang puncak absorpsi maksimum, λmax, nilai
absorptivitas, a, nilai absorptivitas molar, ε, atau nilai ekstingsi, A1%, 1 cm, yang
spesifik untuk suatu senyawa yang dilarutkan dalam suatu pelarut dan pH tertentu (Satiadarma, 2002).
Analisis Kuantitatif
xxv
cukup luas. Konsentrasi kerja larutan analit umumnya 10 sampai 20 µg/ml, tetapi untuk senyawa yang nilai absorptivitasnya besar dapat diukur pada konsentrasi yang lebih rendah. Senyawa yang tidak mengabsorpsi radiasi ultraviolet-sinar tampak dapat juga ditentukan dengan spektrofotometri ultraviolet-sinar tampak, apabila ada reaksi kimia yang dapat mengubahnya menjadi khromofor atau dapat disambungkan dengan suatu pereaksi khromofor (Satiadarma, 2004).
Analisis kuantitatif secara spektrofotometri dapat dilakukan dengan metode regresi dan pendekatan.
1. Metode Regresi
Analisis kuantitatif dengan metode regresi yaitu dengan menggunakan persamaan garis regresi yang didasarkan pada harga serapan dan konsentrasi standar yang dibuat dalam beberapa konsentrasi, paling sedikit menggunakan 5 rentang konsentrasi yang meningkat yang dapat memberikan serapan yang linier, kemudian diplot menghasilkan suatu kurva yang disebut dengan kurva kalibrasi. Konsentrasi suatu sampel dapat dihitung berdasarkan kurva tersebut.
2. Metode Pendekatan
Analisis kuantitatif dengan cara ini dilakukan dengan membandingkan serapan standar yang konsentrasinya diketahui dengan serapan sampel. Konsentrasi sampel dapat dihitung melalui rumus perbandingan C= As.Cb/Ab dimana As=
serapan sampel, Ab= serapan standar, Cb= konsentrasi standar, dan C=
xxvi
2.2.4 Peralatan Untuk Spektrofotometri
Spektrofotometer adalah alat untuk mengukur transmitans atau serapan suatu sampel sebagai fungsi panjang gelombang. Alat ini terdiri dari spektrometer yang menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer sebagai alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi (Khopkar, 1990; Day and Underwood, 1981).
Unsur-unsur terpenting suatu spektrofotometer ditunjukkan secara skematik dalam gambar berikut:
Berikut ini adalah uraian bagian-bagian spektrofotometer:
1. Sumber-sumber lampu; lampu deutrium digunakan untuk daerah UV pada panjang gelombang dari 190-350 nm, sementara lampu halogen kuarsa atau lampu tungsten digunakan untuk daerah visibel (pada panjang gelombang antara 350-900 nm).
Sumber Monokromator Kuvet Detektor
Penguat
Pembacaan, pengamatan Bagian optik
Bagian listrik
1 2 3
4
5
xxvii
2. Monokromator: digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya dapat berupa prisma ataupun grating. Untuk mengarahkan sinar monokromatis yang diinginkan dari hasil penguraian. 3. Kuvet: Pada pengukuran didaerah tampak, kuvet kaca atau kuvet kaca corex
dapat digunakan, tetapi untuk pengukuran pada daerah UV kita harus menggunakan sel kuarsa karena gelas tidak tembus cahaya pada daerah ini. Umumnya tebal kuvet adalah 10 mm, tetapi yang lebih kecil ataupun yang lebih besar dapat digunakan. Sel yang biasa digunakan berbentuk persegi, tetapi bentuk silinder dapat juga digunakan. Kuvet yang bertutup digunakan untuk pelarut organik. Sel yang baik adalah kuarsa atau gelas hasil leburan yang homogen.
4. Detektor: Peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang.
5. Suatu amplifier (penguat) dan rangkaian yang berkaitan yang membuat isyarat listrik dapat untuk diamati.
6. Sistem pembacaan yang memperlihatkan besarnya isyarat listrik (Khopkar, 1990; Rohman, 2007; Day and Underwood, 1981).
2.3. Validasi
Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
xxviii
analisis adalah kedekatan nilai hasil uji yang diperoleh dengan prosedur tersebut dari harga sebenarnya, sering kali dinyatakan dalam persen perolehan kembali analit pada penentuan kadar sampel yang mengandung analit dalam jumlah diketahui. Akurasi merupakan ukuran ketepatan prosedur analisis.
Akurasi prosedur analisis ditentukan dengan menerapkan prosedur tersebut pada sampel atau campuran komponen matriks yang telah dibubuhi analit dalam jumlah diketahui.
Presisi dari suatu metode analisis adalah derajat kesesuaian diantara masing-masing hasil uji, jika prosedur analisis diterapkan berulang kali pada sejumlah cuplikan yang diambil dari satu sampel homogen. Presisi dinyatakan sebagai deviasi standar atau deviasi standar relatif (koefisien variasi). Presisi dapat diartikan pula sebagai derajat reprodusibilitas atau keterulangan dari prosedur analisis.
Kespesifikan dari suatu metode analisis adalah kemampuannya untuk mengukur kadar analit secara khusus dengan akurat, disamping komponen lain yang terdapat dalam matriks sampel.
Limit deteksi adalah nilai parameter uji batas, yaitu konsentrasi analit terendah yang dapat dideteksi.
Kelinieran suatu metode analisis adalah kemampuan untuk menunjukkan bahwa nilai hasil uji langsung atau setelah diolah secara matematika, proporsional dengan konsentrasi analit dalam sampel dalam batas rentang konsentrasi tertentu.
xxix
BAB III
METODOLOGI PENELITIAN
Metode penelitian yang dilakukan adalah metode eksperimental. Penelitian ini dilaksanakan di Laboratorium Kimia Farmasi Kualitatif Fakultas Farmasi Universitas Sumatera Utara.
3.1 Alat – alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas, spektrofotometer ultra violet (UV mini 1240 Shimadzu) dan neraca analitik (Vibra AJ)
3.2 Bahan-bahan
Bahan- bahan yang digunakan dalam penelitian ini adalah : metanol (pro analisis dari E.Merck), akuades (Laboratorium Kimia Farmasi Kuantitatif), nifedipin baku (BPFI); tablet nifedipin generik dan nama dagang.
3.3 Pengambilan Sampel
xxx
3.4 Prosedur Penelitian
3.4.1 Pembuatan Larutan Induk Baku Nifedipin BPFI
Sejumlah lebih kurang 25 mg nifedipin BPFI ditimbang seksama, dimasukkan ke dalam labu tentukur 50 ml, dilarutkan dengan metanol lalu dicukupkan sampai garis tanda dengan metanol dan dikocok homogen, sehingga diperoleh larutan dengan konsentrasi 500 mcg/ml, larutan ini disebut larutan induk baku (LIB I). Dari larutan ini dipipet 5 ml masukkan ke dalam labu tentukur 50 ml, encerkan dengan metanol sampai garis tanda sehingga diperoleh konsentrasi 50 mcg/ml (LIB II)
3.4.2 Penentuan Panjang Gelombang Serapan Maksimum
Dipipet 3,5 ml dari larutan induk baku (LIB) II (50 mcg/ml) masukkan ke dalam labu tentukur 25 ml, encerkan dengan metanol sampai garis tanda (7 mcg/ml). Lalu dikocok sampai homogen sehingga diperoleh larutan dengan konsentrasi 7 mcg/ml. Kemudian ukur serapan pada panjang gelombang 200-400 nm (hasil dapat dilihat pada halaman 11).
3.4.3 Pembuatan Kurva Kalibrasi
xxxi
3.4.4 Penentuan Kadar Nifedipin dalam Sediaan Tablet
Timbang dan serbukkan tidak kurang dari 20 tablet. Timbang seksama sejumlah serbuk setara dengan 20 mg nifedipin (Penimbangan serbuk sebanyak 6 kali perlakuan), masukkan ke dalam labu tentukur 25 ml. Lalu ditambahkan 5 ml metanol, kocok dan encerkan dengan metanol sampai garis tanda. Kemudian disaring, 5 ml filtrat pertama dibuang.. Dipipet 2 ml filtrat, masukkan ke dalam labu tentukur 25 ml, dicukupkan dengan metanol sampai garis tanda dan kocok homogen. Kemudian dipipet 3,5 ml larutan, masukkan ke dalam labu tentukur 25 ml. Lalu dicukupkan dengan metanol sampai garis tanda, kocok homogen dan diukur serapannya pada panjang gelombang maksimum yang diperoleh (hasil dapat dilihat pada Tabel 3, halaman 14)
3.4.5 Uji Validasi dengan Parameter Akurasi, Presisi, Batas Deteksi dan Batas Kuantitasi
3.4.5.1 Uji Akurasi dengan Persen Perolehan Kembali (%Recovery)
Uji akurasi dilakukan dengan metode penambahan baku (Standard Addition Method) yaitu dengan membuat 3 konsentrasi analit sampel dengan rentang spesifik 80, 100 dan 120%, dimana masing-masing dilakukan sebanyak 3 kali replikasi. Setiap rentang spesifik mengandung 70% analit sampel dan 30% baku pembanding, kemudian dianalisa dengan perlakuan yang sama seperti pada penetapan kadar sampel (hasil dapat dilihat pada Tabel 4, halaman 15).
Persen perolehan kembali (% recovery) dapat dihitung dengan rumus sebagai berikut :
%Recovery =
C B A−
xxxii
Keterangan :
A = konsentrasi sampel yang diperoleh setelah penambahan baku B = konsentrasi sampel sebelum penambahan baku
C = konsentrasi baku yang ditambahkan 3.4.5.2 Uji Presisi
Uji presisi (keseksamaan) ditentukan dengan parameter RSD (Relative Standard Deviasi) dengan rumus :
RSD = x100% (WHO, 1992; Indrayanto dan Yuwono, 2003).
3.4.5.3 Penentuan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
xxxiii
Keterangan :
SB = Simpangan Baku LOD = Batas Deteksi LOQ = Batas Kuantitasi
3.4.6 Analisis Data secara Statistik
untuk menghing Standar deviasi (SD) digunakan rumus :
(
)
1 2
− −
=
∑
n Xi X SD
Untuk mengetahui apakah data diterima atau ditolak digunakan rumus seperti dibawah ini :
t =
n SD
X X−
=
Dasar penolakan data jika thitung ≥ ttabel dan bila thitung mempunyai nilai
negatif, ditolak jika thitung ≤ - ttabel.
Untuk mencari kadar sebenarnya dengan taraf kepercayaan 99 persen, dengan derajat kebebasan dk = n – 1, digunakan rumus:
xxxiv
Keterangan:
µ = interval kepercayaan X = kadar rata – rata sampel X = kadar sampel
t = harga t tabel sesuai dengan dk = n-1 = tingkat kepercayaan
xxxv
BAB IV
HASIL DAN PEMBAHASAN
Menurut Moffat (2004), nifedipin mempunyai spektrum serapan maksimum pada daerah ultraviolet dalam larutan asam pada panjang gelombang 235 nm (A1
1 = 595 b) dan 338 nm (A 1
1 = 195 b). Menurut Merck Indeks (2001) , dalam larutan asam memberikan spektrum serapan maksimum pada panjang gelombang 235 nm ( = 20600) dan 338 nm ( = 5740), dalam larutan basa pada panjang gelombang 238 nm ( = 20600) dan 340 nm ( = 5740) dan dalam metanol pada panjang gelombang 235 nm ( = 21590) dan 340 nm ( = 5010). Dari data kedua literatur diatas kemungkinan nifedipin dapat ditetapkan kadarnya secara spektrofotometri ultraviolet. Dalam penelitian ini digunakan pelarut metanol, karena dari hasil orientasi dalam larutan asam diperoleh larutan yang kurang jernih.
Adapun alasan peneliti memilih panjang gelombang 235 nm untuk pengukuran karena panjang gelombang tersebut nifedipin memiliki nilai absorptivitas molar ( ) yang lebih besar daripada panjang gelombang 334 nm. Holme dan Peck (1983) menyatakan bahwa dengan nilai absorptivitas yang besar maka pengukuran dapat dilakukan pada konsentrasi yang rendah, sehingga sensitivitas maksimum dari metode ini dapat tercapai.
xxxvi
gelombang maksimum, meskipun panjang gelombang tersebut sudah diketahui dalam literatur. Hal ini dikarenakan panjang gelombang suatu senyawa dapat berbeda bila ditentukan pada kondisi dan alat yang berbeda.
Penentuan panjang gelombang ini dilakukan pada konsentrasi yang memberikan serapan dengan kesalahan fotometrik terkecil (+ 0,4343). Untuk mendapatkan konsentrasi tersebut dapat dihitung menggunakan nilai absorptivitas molar ( ) dari literatur, dalam metanol pada panjang gelombang 235 nm dengan
absorptivitas molarnya 21590 (The Merck Indeks, 2001). Contoh perhitungan dapat dilihat pada Lampiran 9, halaman 33.
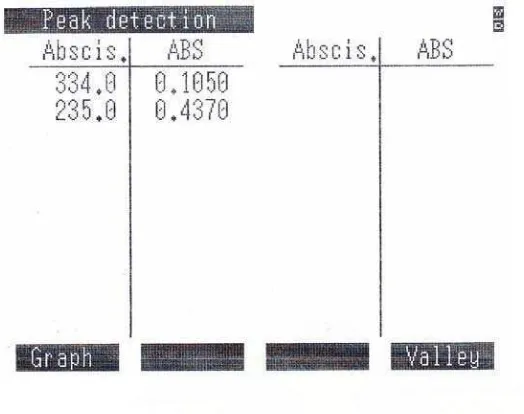
Dari perhitungan didapatkan konsentrasi pengukuran adalah 7 mcg/ml dan dari hasil pengukuran diperoleh panjang gelombang maksimum, pada 235 nm dan 334 nm dengan serapan masing-masing 0,4370 dan 0,1050 seperti terlihat pada Gambar 1 dan tabel 1.
xxxvii
Tabel 1. Data Absorbansi dari Kurva Serapan Maksimum
Selanjutnya, untuk penetapan kadar nifedipin dalam sediaan tablet yang beredar di pasaran dilakukan pada panjang gelombang maksimum nifedipin BPFI dengan absorptivitas terbesar yaitu pada panjang gelombang 235 nm. Menurut Satiadarma (2004), penentuan kadar dilakukan dengan mengukur serapan pada panjang gelombang maksimum (puncak kurva), agar dapat memberikan serapan tertinggi untuk setiap konsentrasi. Bila suatu senyawa mempunyai lebih dari satu puncak absorpsi maksimum, lebih diutamakan panjang gelombang absorpsi maksimum yang absorptivitasnya terbesar dan memberikan kurva kalibrasi linier dalam rentang konsentrasi yang relatif lebar.
4.2 Pembuatan Kurva Kalibrasi
xxxviii
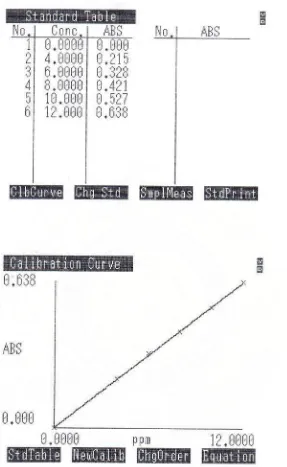
Tabel 2. Data Kurva Kalibrasi dari Nifedipin BPFI
Gambar 2. Kurva kalibrasi nifedipin BPFI dalam pelarut metanol pada panjang gelombang 235 nm.
xxxix
4.3 Penentuan Kadar Nifedipin dalam sediaan tablet
Hasil penentuan kadar nifedipin dalam sediaan tablet dapat dilihat pada tabel dibawah ini.
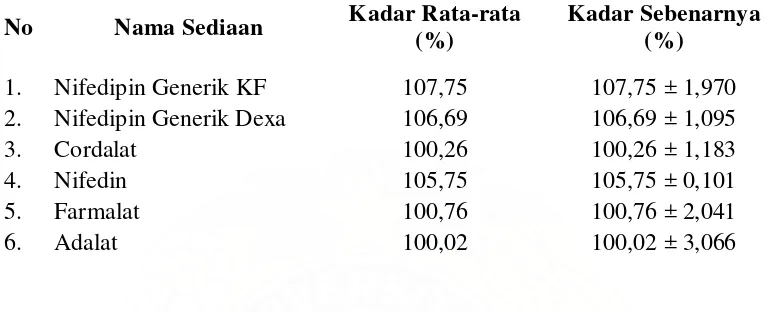
Tabel 3. Kadar rata-rata nifedipin pada sediaan tablet
No Nama Sediaan Kadar Rata-rata (%)
Kadar Sebenarnya (%)
1. Nifedipin Generik KF 107,75 107,75 ± 1,970 2. Nifedipin Generik Dexa 106,69 106,69 ± 1,095
3. Cordalat 100,26 100,26 ± 1,183
4. Nifedin 105,75 105,75 ± 0,101
5. Farmalat 100,76 100,76 ± 2,041
6. Adalat 100,02 100,02 ± 3,066
Dari data diatas menunjukkan, kadar nifedipin dalam sediaan tablet generik maupun nama dagang, memenuhi persyaratan kadar yang tertera dalam Farmakope Indonesia Edisi IV tahun 1995 yaitu tidak kurang dari 90,0 % dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket.
4.4 Uji validasi metode Spektrofotometri Ultraviolet
Pada penelitian ini dilakukan uji validasi dengan metode penambahan bahan baku (standard addition method) terhadap sampel tablet nifedipin (PT. Kimia Farma) yang meliputi uji akurasi dengan parameter persen perolehan kembali (% recovery), uji presisi dengan parameter RSD (Relatif Standar Deviasi), batas deteksi (LOD) dan batas kuantitasi (LOQ) (WHO, 1992; Indriyanto dan Yuwono, 2003).
masing-xl
masing dengan 3 replikasi dan setiap rentang spesifik mengandung 70% analit dan 30% baku pembanding. Contoh perhitungan dapat dilihat pada Lampiran 14, halaman 39.
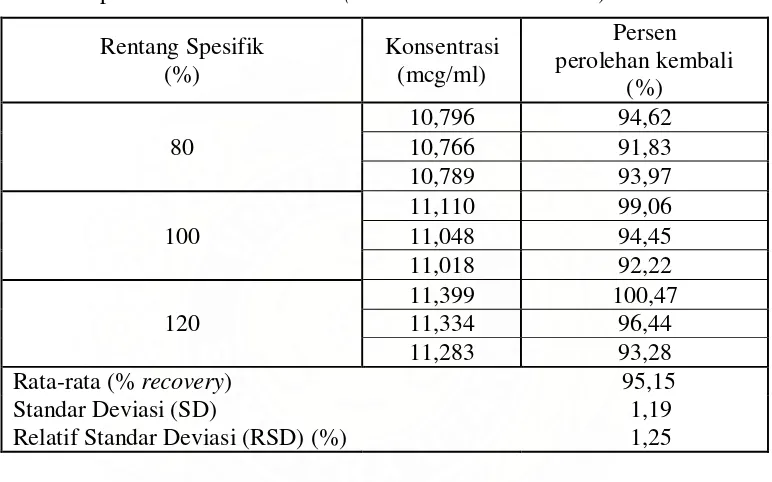
Data hasil pengujian perolehan kembali nifedipin dengan metode penambahan bahan baku (standard addition method) dapat dilihat pada tabel 4. Tabel 4. Data hasil pengujian perolehan kembali nifedipin dengan metode
penambahan bahan baku (standard addition method) Rentang Spesifik
xli
BAB V
KESIMPULAN DAN SARAN 5.1. Kesimpulan
Metode spektrofotometri ultraviolet dapat digunakan untuk penetapan kadar nifedipin dalam sediaan tablet karena dari hasil uji validasi, metode ini menunjukkan akurasi dan presisi yang baik dengan batas deteksi (LOD) 0,2927 mcg/ml dan batas kuantitasi (LOQ) 0,9758 mcg/ml.
Dari hasil penelitian menunjukkan bahwa semua tablet yang diperiksa baik yang generik maupun nama dagang memenuhi standar persyaratan tablet menurut Farmakope Indonesia Edisi IV Tahun 1995 yaitu tidak kurang dari 90,0 % dan tidak lebih dari 110,0 % dari jumlah yang tertera pada etiket.
5.2. Saran
xlii
DAFTAR PUSTAKA
Budavari, (2001). The Merck Index. Encyclopedia of Chemicals, Drugs, and Biologicals. Thirteenth Edition. Whitehouse: Merck & Co., Inc. Page 1170.
Day, R.A & Underwood, A.L. (1999). Analisis Kimia Kuantitatif. Penerjemah: Pudjaatmaka, A.H. Edisi kelima, Jakarta: Penerbit Erlangga. Halaman: 393.
Dachriyanus (2004). Analisis Struktur Senyawa Organik Secara Spektrofotometri. Padang : Andalas University Press. Hal 1.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen kesehatan Republik Indonesia. Jakarta. Halaman 611-613.
Gandjar, I. G. dan Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan II. Yogyakarta: Pustaka pelajar. Halaman 246.
Harmita, (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Majalah Ilmu Kefarmasian. Vol. I, No.3. Halaman 117-128.
Holme, D. J., and Peck, H. (1983). Analytical Biochemistry. London: Longman Inc. Page 40.
Indriyanto, G. dan Yuwono M., (2003). In Gazales, J.Ed. Encyclopedia of Chromatography (Marcel Dekker). Suplement.
Katzung, B.G., (2001). Farmakologi Dasar dan Klinik. Penerjemah dan Editor Bagian Farmakologi Fakultas Kedokteran Universitas Airlangga. Edisi Pertama. Jakarta: Penerbit Salemba Medika. Halaman 332-340.
Khopkar, S.M., (1990). Konsep Dasar Kimia Analitik. Penerjemah A. Saptoraharjo. Cetakan Pertama. Jakarta: Penerbit Universitas Indonesia. Halaman Kesehatan Republik Indonesia. Jakarta. Halaman 26-217. Moffat, A.C., (2004). Clarke’s Isolation and Identification of Drugs. Third
Edition. London: The Pharmaceutics Press. Page 1337.
xliii
Mycek, M.J., Harvey, R.A., Champe C.C. ( 2001 ). Farmakologi Ulasan Bergambar. Lippincott’s illustrated reviews: Farmacology. Penerjemah Azwar Agoes. Edisi Kedua. Jakarta: Penerbit Widya Medika. Halaman 189-190.
Roth, J.H., and Blaschke, G., (1998). Analisis Farmasi. Penerjemah: Kisman, dkk. Cetakan Ketiga. Yogyakarta. UGM Press. Hal 355-357.
Satiadarma, K., (2004). Azas Pengembangan Prosedur Analisis. Edisi Pertama. Cetakan Pertama. Surabaya : Airlangga University Press. Halaman 378-388.
Setiawati, A., dan Bustami, Z.S., (1995). Antihipertensi, dalam Farmakologi dan Terapi. Editor : Ganiswara, S.G., Edisi IV. Jakarta: UI-Press. Halaman 329.
Siswandono dan Soekardjo, B. (1995). Kimia Medisinal. Surabaya : Airlangga University Press. Hal 364, 367.
Shargel, L. (1985). Biofarmasetika Dan Farmakokinetika Terapan. Penerjemah Fasich. Edisi Kedua. Surabaya: Penerbit Unversitas Airlangga. Halaman 16.
Tjay, T.H dan Raharjo, K. (2002). Obat-obat Penting. Jakarta: Penerbit PT Elek Media Komputindo. Halaman 503, 527.
USP Pharmacopeia, (2008). The National Formulary. 31st Edition. The United State Pharmacopeia Convention. Page 1247
xliv
Lampiran 1. Perhitungan Persamaan Regresi Nifedipin BPFI
No X Y XY X² Y²
Maka persamaan garis regresinya adalah Y = 0,052807X – 0,002789
xlv
Lampiran 2. Data kadar nifedipin sediaan tablet
xlvi
Lampiran 3. Perhitungan Statistik Kadar Nifedipin pada Generik Kimia Farma
(
)
distribusi t diperoleh nilai ttabel = 4,0321
xlvii
Lampiran 3, sambungan...
karena thitung ≤ ttabel maka data diterima
maka kadar sebenarnya terletak antara: µ = X± t (1-1/2 )dk x SD/ n
= 107,745 ±
6 1967 , 1 0321 ,
4 x
= 107,745 ± 1,970
xlviii
Lampiran 4. Perhitungan Statistik Kadar Nifedipin pada Tablet Generik Dexa Medica)
distribusi t diperoleh nilai ttabel = 4,0321
Data ditolak jika thitung ≥ ttabel atau thitung ≤ - ttabel
xlix
distribusi t diperoleh nilai ttabel = 4,6040
Data ditolak jika thitung ≥ ttabel atau thitung ≤ - ttabel
karena thitung ≤ttabel maka data diterima
l
Lampiran 5. Perhitungan Statistik Kadar Nifedipin pada Tablet Adalat (Bayer)
distribusi t diperoleh nilai ttabel = 4,0321
li
karena thitung ≤ttabel maka data diterima
maka kadar sebenarnya terletak antara: µ = X± t (1-1/2 )dk x SD/ n
= 102,41 ±
6 8628 , 1 0321 ,
4 x
= 102,41 ± 3,066
lii
distribusi t diperoleh nilai ttabel = 4,0321
Data ditolak jika thitung ≥ ttabel atau thitung ≤ - ttabel
selanjutnya terhadap data yang dianggap tidak menyimpang
liii
distribusi t diperoleh nilai ttabel = 4,6040
Data ditolak jika thitung ≥ ttabel atau thitung ≤ - ttabel
karena thitung ≤ttabel maka data diterima
maka kadar sebenarnya terletak antara: µ = X± t (1-1/2 )dk x SD/ n
liv
distribusi t diperoleh nilai ttabel = 4,0321
lv
Lampiran 7. sambungan... karena thitung ≤ttabel maka data diterima
maka kadar sebenarnya terletak antara: µ = X± t (1-1/2 )dk x SD/ n
= 100,76 ±
6 2398 , 1 0321 ,
4 x
lvi
Lampiran 8. Perhitungan Statistik Kadar Nifedipin pada Tablet Cordalat (Kimia Farma)
distribusi t diperoleh nilai ttabel = 4,0321
Data ditolak jika thitung ≥ ttabel atau thitung ≤ - ttabel
lvii
distribusi t diperoleh nilai ttabel = 4,6040
Data ditolak jika thitung ≥ ttabel atau thitung ≤ - ttabel
karena thitung ≤ttabel maka data diterima
lviii
Lampiran 9. Perhitungan Konsentrasi Pengukuran
Diketahui : nilai absorptivitas ( ) 21590 M-1cm-1 ( Merck Indeks, 2001) BM nifedipin adalah 346,34
A = .b.c (mol/liter)
0,4343 = 21590 M-1cm-1 x 1 cm x c
c =
1 21590
4343 , 0
x M
c = 2,0115 x 10-5 M c = 2,0115 x 10-5 mol/ liter
c = 2,0115 x 10-5 x 346,34 x 103 mcg/ml c = 6,966 mcg/ ml
lix
Lampiran 10. Contoh Perhitungan Penimbangan Sampel
Berat 20 tablet = 5, 497 g Kandungan nifedipin pada etiket = 10 mg
Dibuat larutan uji dengan kadar lebih kurang 8 mcg/ml.
Ditimbang serbuk setara dengan 20 mg nifedipin, maka berat sampel yang ditimbang adalah:
Berat penimbangan sampel =
mg
Sampel yang telah ditimbang dimasukkan dalam labu ukur 25 ml, lalu dilarutkan dalam pelarut metanol dan cukupkan sampai garis tanda dengan air.
Kadar larutan uji =
ml mg
25 20
X 1000 mcg/ml = 800 mcg/ml
Kemudian dipipet 2,0 ml larutan uji, lalu dimasukkan ke dalam labu ukur 25 ml dan dicukupkan dengan metanol sampai garis tanda.
Kadar larutan uji =
ml
Lalu dipipet lagi 3,5 ml larutan uji, dan dimasukkan ke dalam labu tentukur 25 ml kemudian dicukupkan sampai garis tanda.
Kadar larutan uji =
lx
Lampiran 11. Contoh Perhitungan Persentase (%) Perolehan Kembali Berat 20 tablet = 5497 mg
Berat 1 tablet = 274,85 mg Kandungan zat berkhasiat = 10 mg Perolehan 80 %
Sampel yang ditimbang = mg
lxi
Baku 30 % =
100 30
x 10 mg = 3 mg
Perolehan 120 %
=
100 120
x 10 mg = 12 mg
Analit 70 % =
100 70
x 12 mg = 8,4 mg
Sampel yang ditimbang = mg
mg 10
4 , 8
x 274,85 mg
= 230,874 mg Baku 30 %
=
100 30
lxii
lxiii
Lampiran 13. Contoh perhitungan batas deteksi (LOD) dan batas kuantitasi (LOQ)
Persamaan garis regresi: Y = 0,052807X + 0,002789
lxiv
Lampiran 14. Data Persen Perolehan Kembali (% Recovery) a. Perolehan 80%
b. Perolehan 100%
lxv
Lampiran 15. Nilai Distribusi t
lxvi