Tumbuhan ketepeng
(L.) Roxb.)
Simplisia daun ketepeng
Serbuk simplisia
Dicuci di air mengalir Ditiriskan
Karakterisasi Skrining fitokimia Pembuatan ekstrak
•Makroskopik •Mikroskopik •Penetapan kadar air •Penetapan kadar sari
yang larut air
•Penetapan kadar sari yang larut etanol •Penetapan kadar abu
total
Dimasukkan ke dalam bejana
Dimasukkan etanol 80% sampai simplisia terendam sempurna
Dibiarkan selama 5 hari terlindung dari cahaya, sambil sesekali diaduk
Disaring
Diuapkan dengan penguap rotary evaporator Maserat
Ekstrak kental (72,5 g)
500 g serbuk simplisia
Ampas
Ampas Maserat
Ditambahkan etanol dan akuades Dihomogenkan
Dimasukkan dalam corong pisah Diekstraksi dengan n-heksana sampai tidak memberikan hasil positif dengan pereaksi Liebermann-Burchard
Dikocok dan didiamkan sampai terbentuk dua lapisan dan dipisahkan
Diekstraksi dengan etilasetat Dikumpulkan
Dipekatkan dengan rotary evaporator Dikocok dan didiamkan
sampai terbentuk dua lapisan dan dipisahkan
Dikumpulkan Dikumpulkan
Dipekatkan dengan Dipekatkan dengan
waterbath rotary evaporator
Ekstrak etanol daun ketepeng (30 g)
Fraksi n-heksana
Fraksi etilasetat pekat (2,41 g) Fraksi air
1. Penetapan kadar air
a. Berat sampel = 5,046 g Volume I = 3,5 ml Volume II = 3,8 ml
Kadar air = 3,8-3,5
5,046 x 100 % = 5,9453%
b. Berat sampel = 5,064 g Volume I = 3,8 ml Volume II = 4,2 ml
Kadar air = 4,2-3,8
5,064 x 100% = 7,9776%
c. Berat sampel = 5,045 g Volume I = 0,7 ml Volume II = 1,0 ml
Kadar air = 1,0-0,7
5,045 x 100% = 5,9464%
Kadar air rata-rata = (5,9453+7,9776+5,9464)%
3
=
6,6231%2. Penetapan kadar sari larut dalam etanol Kadar air
=
volume II-volume Iberat sampel
x 100%
Kadar sari= Berat sari Berat sampel x
100
Berat sari = 0,1565 g
Kadar sari rata-rata = 15,0536+15,0536+15,6271%
3 = 15,4087%
3. Penetapan kadar sari larut dalam air
c. Berat sampel = 5,0013 g Berat sari = 0,1988 g
Kadar sari
=
0,19885,0013 x 100
20 x 100% = 19,8748%
Kadar sari rata-rata = (20,0995+21,4228+19,8748)%
3 = 20,4657%
4. Penetapan kadar abu total
a. Berat sampel = 2,0160 g Berat abu = 0,0898 g
Kadar abu = 0,0898
2,0160
x 100 % = 4,4543 %
b. Berat sampel = 2,0850 g Berat abu = 0,0786 g
Kadar abu = 0,0786
2,0850 x 100% = 3,7697%
c. Berat sampel = 2,0900 g Berat abu = 0,0880 g
Kadar abu = 0,0880
2,0900 x 100% = 4,2105%
Kadar abu total rata-rata = (4,4543+3,7697+4,2105)%
3 = 4,1448%
Kadar abu total= Berat abu
a. Berat sampel = 2,0160 g Berat abu = 0,0060 g
Kadar abu = 0,0060
2,0160 x 100% = 0,2976 %
b. Berat sampel = 2,0850 g Berat abu = 0,0080 g
Kadar abu = 0,0080
2,0850 x 100% = 0,3836%
c. Berat sampel = 2,0900 g Berat abu = 0,0090 g
Kadar abu = 0,0090
2,0900 x 100% = 0,4306 %
Kadar abu yang tidak larut asam rata-rata = 0,2976%+0,3836%+0,4306%
3 = 0,3706%
Kadar abu yang tidak larut dalam asam
=
Berat abu(EEDK)
Fase gerak n-heksana:etilasetat
(50:50) (60:40) (70:30) (80:20) (90:10)
Gambar hasil kromatogram dengan fase gerak n-heksana:etilasetat Keterangan:
berbagai fase gerak
Fase gerak
Asam asetat 5% HCl 1% BAW (4:1:5)
Keterangan:
Fase diam = kertas saring Whatmann, A = asam asetat 5%, B = HCl 1%, C = BAW (4:1:5) dilihat di bawah sinar UV 366 nm
AlCl3 NH3 FeCl3
Keterangan:
Fase diam = kertas saring Whatmann, fase gerak = asam asetat 5%, A = disemprot dengan AlCl3, B = disemprot dengan NH3, C = disemprot dengan FeCl3, b.k= biru kehitaman, k= kuning, k.m= kuning muda
k k k
k.m k.m
b.k b.k
Penampak bercak
AlCl3 NH3 FeCl3
Keterangan:
Fase diam = kertas saring Whatmann, fase gerak = HCl 1%, A = disemprot dengan AlCl3, B = disemprot dengan NH3, C = disemprot dengan FeCl3, b.k= biru kehitaman, k= kuning
k k b.k
AlCl3 NH3 FeCl3
Keterangan:
Fase diam = kertas saring Whatmann, fase gerak = BAW (4:1:5), A = disemprot dengan AlCl3, B = disemprot dengan NH3, C = disemprot dengan FeCl3, b.k= biru kehitaman, k= kuning
k
k
k
k
k
b.k b.k
b.k b.k
b.k b.k k
1. Hasil penentuan waktu kerja ekstrak etanol daun ketepeng Menit ke- Absorbansi
40 0.5931 Menit ke- Absorbansi
1 0.7001
3. Hasil penentuan waktu kerja fraksi etilasetat daun ketepeng Menit ke- Absorbansi
38 0.2509 Menit ke- Absorbansi
1 0.4812
1. Ekstrak etanol daun ketepeng
Data absorbansi menit ke-60 pengukuran pertama
Konsentrasi larutan uji
(µg/ml) Absorbansi % peredaman
0 1,12995 -
40 0,64645 42,79
60 0,51094 54,78
80 0,41066 63,65
100 0,29915 73,52
% peredaman = Akontrol-Asampel
Akontrol × 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Perhitungan % peredaman ekstrak etanol daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,12995-0,64645
1,12995
× 100% = 42,79%
- Konsentrasi 60 µ g/ml
% peredaman = 1,12995-0,51094
1,12995 × 100% = 54,78%
- Konsentrasi 80 µ g/ml
% peredaman = 1,12995-0,41066
1,12995 × 100% = 63,65%
- Konsentrasi 100 µ g/ml
% peredaman = 1,12995-0,29915
Konsentrasi larutan uji
(µg/ml) Absorbansi % peredaman
0 1,12887 -
40 0,64674 42,71
60 0,51088 54,74
80 0,41064 63,64
100 0,29639 73,74
% peredaman = Akontrol-Asampel
Akontrol × 100%
Keterangan:
A
kontrol = Absorbansi tidak mengandung sampelA
sampel = Absorbansi sampelPerhitungan % peredaman ekstrak etanol daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,12887-0,64674
1,12887 × 100% = 42,71%
- Konsentrasi 60 µ g/ml
% peredaman = 1,12887-0,51088
1,12887
× 100% = 54,74%
- Konsentrasi 80 µ g/ml
% peredaman = 1,12887-0,41064
1,12887 × 100% = 63,64%
- Konsentrasi 100 µ g/ml
% peredaman = 1,12887-0,29639
Data absorbansi menit ke-60 pengukuran ketiga
Konsentrasi larutan uji
(µg/ml) Absorbansi % peredaman
0 1,12907 -
40 0,63835 43,46
60 0,51337 54,53
80 0,40311 64,29
100 0,29706 73,69
% peredaman = Akontrol-Asampel
Akontrol × 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel
Asampel = Absorbansi sampel
Perhitungan % peredaman ekstrak etanol daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,12907-0,63835
1,12907 × 100% = 42,98%
- Konsentrasi 60 µ g/ml
% peredaman = 1,12907-0,51337
1,12907 × 100% = 54,68%
- Konsentrasi 80 µ g/ml
% peredaman = 1,12907-0,40311
1,12907
× 100% = 64,29%
- Konsentrasi 100 µ g/ml
% peredaman = 1,12907-0,29706
Konsentrasi
2. Fraksi n-heksana daun ketepeng
Data absorbansi menit ke-60 pengukuran pertama
Konsentrasi larutan uji (µg/ml) Absorbansi % peredaman
0 1,13287 -
40 0,92514 18,33
60 0,86003 24,08
80 0,79924 29,45
100 0,67717 40,22
% peredaman = Akontrol-Asampel
Akontrol × 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Perhitungan % peredaman fraksi n-heksana daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,13287-0,92514
1,13287 × 100% = 18,33%
- Konsentrasi 60 µ g/ml
% peredaman = 1,13287-0,86003
- Konsentrasi 80 µ g/ml
% peredaman = 1,13287-0,79924
1,13287 × 100% = 29,45%
- Konsentrasi 100 µ g/ml
% peredaman = 1,13287-0,67717
1,13287 × 100% = 40,22%
Data absorbansi menit ke-60 pengukuran kedua
Konsentrasi larutan uji (µg/ml) Absorbansi % peredaman
0 1,13487 -
40 0,92406 18,57
60 0,86166 24,07
80 0,79854 29,63
100 0,67680 40,36
% peredaman = Akontrol-Asampel
Akontrol × 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Perhitungan % peredaman fraksi n-heksana daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,13487-0,92406
1,13487 × 100% = 18,57%
- Konsentrasi 60 µ g/ml
% peredaman = 1,13487-0,86166
1,13487 × 100% = 24,07%
- Konsentrasi 80 µ g/ml
% peredaman = 1,13487-0,79854
% peredaman = 1,13487-0,67680
1,13487 × 100% = 40,36%
Data absorbansi menit ke-60 pengukuran ketiga
Konsentrasi larutan uji (µg/ml) Absorbansi % peredaman
0 1,13669 -
40 0,92526 18,6
60 0,86562 23,84
80 0,79521 30,04
100 0,67790 40,36
% peredaman = Akontrol-Asampel
Akontrol
× 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Perhitungan % peredaman fraksi n-heksana daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,13669-0,92526
1,13669 × 100% = 18,60%
- Konsentrasi 60 µ g/ml
% peredaman = 1,13669-0,86562
1,13669 × 100% = 23,84%
- Konsentrasi 80 µ g/ml
% peredaman = 1,13669-0,79521
1,13669 × 100% = 30,04%
- Konsentrasi 100 µ g/ml
% peredaman = 1,13669-0,67790
Data nilai rata-rata % peredaman fraksi n-heksana
3. Fraksi etilasetat daun ketepeng
Data absorbansi menit ke-60 pengukuran pertama
Konsentrasi larutan uji (µg/ml) Absorbansi % peredaman
0 1,13545 -
40 0,25447 77,59
60 0,10541 90,99
80 0,09438 91,68
100 0,07930 93,01
% peredaman = Akontrol-Asampel
Akontrol × 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Perhitungan % peredaman fraksi etilasetat daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,13545-0,25447
1,13545 × 100% = 77,59%
- Konsentrasi 60 µ g/ml
% peredaman = 1,13545-0,10541
% peredaman = 1,13545-0,09438
1,13545 × 100% = 91,68%
- Konsentrasi 100 µ g/ml
% peredaman = 1,13545-0,07930
1,13545 × 100% = 93,01%
Data absorbansi menit ke-60 pengukuran kedua
Konsentrasi larutan uji (µg/ml) Absorbansi % peredaman
0 1,13203 -
40 0,25627 77,36
60 0,10551 90,68
80 0,09514 91,59
100 0,07974 92,95
% peredaman = Akontrol-Asampel
Akontrol × 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Perhitungan % peredaman fraksi etilasetat daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,13203-0,25627
1,13203 × 100% = 77,36%
- Konsentrasi 60 µ g/ml
% peredaman = 1,13203-0,10551
1,13203 × 100% = 90,68%
- Konsentrasi 80 µ g/ml
% peredaman = 1,13203-0,09514
- Konsentrasi 100 µ g/ml
% peredaman = 1,13487-0,07974
1,13487 × 100% = 92,95%
Data absorbansi menit ke-60 pengukuran ketiga
Konsentrasi larutan uji
(µg/ml) Absorbansi % peredaman
0 1,13792 -
40 0,25432 77,65
60 0,10072 91,15
80 0,09047 92,05
100 0,0807 92,91
% peredaman = Akontrol-Asampel
Akontrol
× 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel
Asampel = Absorbansi sampel
Perhitungan % peredaman fraksi etilasetat daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,13792-0,25432
1,13792 × 100% = 77,65%
- Konsentrasi 60 µ g/ml
% peredaman = 1,13792-0,10072
1,13792 × 100% = 91,15%
- Konsentrasi 80 µ g/ml
% peredaman = 1,13792-0,09047
% peredaman = 1,13792-0,08070
1,13792 × 100% = 92,91%
Data nilai rata-rata % peredaman fraksi etilasetat Konsentrasi
4. Fraksi air daun ketepeng
Data absorbansi menit ke-60 pengukuran pertama
Konsentrasi larutan uji
(µg/ml) Absorbansi % peredaman
0 1,13939 -
40 0,73331 35,64
60 0,58847 48,35
80 0,44942 60,55
100 0,35907 68,48
% peredaman = Akontrol-Asampel
Akontrol
× 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Perhitungan % peredaman fraksi air daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,13939-0,73331
- Konsentrasi 60 µ g/ml
% peredaman = 1,13939-0,58847
1,13939 × 100% = 48,35%
- Konsentrasi 80 µ g/ml
% peredaman = 1,13939-0,44942
1,13939 × 100% = 60,55%
- Konsentrasi 100 µ g/ml
% peredaman = 1,13939-0,35907
1,13939 × 100% = 68,48%
Data absorbansi menit ke-60 pengukuran kedua
Konsentrasi larutan uji (µg/ml) Absorbansi % peredaman
0 1,13618 -
40 0,73335 35,44
60 0,58855 48,20
80 0,44981 60,41
100 0,35658 68,61
% peredaman = Akontrol-Asampel
Akontrol
× 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Perhitungan % peredaman fraksi air daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,13618-0,73335
1,13618 × 100% = 35,44%
- Konsentrasi 60 µ g/ml
% peredaman = 1,13618-0,58855
% peredaman = 1,13618-0,44981
1,13618 × 100% = 60,41%
- Konsentrasi 100 µ g/ml
% peredaman = 1,13487-0,35658
1,13487 × 100% = 68,61%
Data absorbansi menit ke-60 pengukuran ketiga
Konsentrasi larutan uji (µg/ml) Absorbansi % peredaman
0 1,13725 -
40 0,73325 35,52
60 0,58887 48,22
80 0,44276 61,06
100 0,35922 68,41
% peredaman = Akontrol-Asampel
Akontrol × 100%
Keterangan:
Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Perhitungan % peredaman fraksi air daun ketepeng - Konsentrasi 40 µ g/ml
% peredaman = 1,13725-0,73325
1,13725 × 100% = 35,52%
- Konsentrasi 60 µ g/ml
% peredaman = 1,13725-0,58887
1,13725 × 100% = 48,22%
- Konsentrasi 80 µ g/ml
% peredaman = 1,13725-0,44276
- Konsentrasi 100 µ g/ml
% peredaman = 1,13725-0,35922
1,13725 × 100% = 68,41%
Data nilai rata-rata % peredaman fraksi air Konsentrasi
larutan uji (µg/ml)
% peredaman
I II III Rata-rata
0 - - - -
40 35,64 35,44 35,52 35,53
60 48,35 48,20 48,22 48,25
80 60,55 60,41 61,06 60,67
X Y XY X2
0 0 0 0
40 42,98 1719,2 1600
60 54,68 3280,8 3600
80 63,86 5108,8 6400
100 73,65 7365 10000
∑x=280 ∑y= 235,17 ∑xy=17473,8 ∑x2==21600
x
�=56 y�=47,034
X = Konsentrasi (µg/ml) Y = % Peredaman
a= (∑xy)-(∑x)(∑y)/n
(∑x2)-(∑x)2/n
a= (17473,8)-(280)(73,65)/5
(21600)-(280)2/5
a= 4304,28
5920
a= 0,727 b= y� - ax�
b= 47,034 – (0,727)(56) b= 6,32
Jadi, persamaan garis regresi Y = 0,727X + 6,32 Nilai IC50 : Y = 0,727X + 6,32
2. Fraksi n-heksana daun ketepeng
X Y XY X2
0 0 0 0
40 18,50 740 1600
60 24,00 1440 3600
80 29,70 2376 6400
100 40,31 4031 10000
∑x=280 ∑y=112,51 ∑xy=8587 ∑x2==21600
x
�=56 y�=22,502
X = Konsentrasi (µg/ml) Y = % Peredaman
a= (∑xy)-(∑x)(∑y)/n
(∑x2)-(∑x)2/n
a= (8587)-(280)(112,51)/5
(21600)-(280)2/5
a= 2286,44
5920
a= 0,386 b= y� - ax�
b= 22,502 – (0,386)(56) b= 0,87
Jadi, persamaan garis regresi Y = 0,386X + 0,87 Nilai IC50 : Y = 0,386X + 0,87
X Y XY X2
0 0 0 0
40 77,53 3101,2 1600
60 90,94 5456,4 3600
80 91,77 7341,6 6400
100 92,96 9296 10000
∑x=280 ∑y=353,2 ∑xy=25195,2 ∑x2==21600
x�=56 y�=70,64
X = Konsentrasi (µg/ml) Y = % Peredaman
a= (∑xy)-(∑x)(∑y)/n
(∑x2)-(∑x)2/n
a= (25195,2)-(280)(353,2)/5
(21600)-(280)2/5
a= 5416
5920
a= 0,915 b= y� - ax�
b= 70,64 – (0,915)(56) b= 19,407
Jadi, persamaan garis regresi Y = 0,915X + 19,407 Nilai IC50 : Y = 0,915X + 19,407
4. Fraksi air daun ketepeng
X Y XY X2
0 0 0 0
40 35,53 1421,2 1600
60 48,25 2895 3600
80 60,67 4853,6 6400
100 68,50 6850 10000
∑x=280 ∑y=212,95 ∑xy=16019,8 ∑x2==21600
x�=56 y�=42,59
X = Konsentrasi (µg/ml) Y = % Peredaman
a= (∑ ��)−(∑ �)(∑ �)/�
(∑ �2)−(∑ �)2/�
a= (16019,8)-(280)(212,95)/5
(21600)-(280)2/5
a= 4094,6
5920
a= 0,69 b= y� - ax�
b= 42,59 – (0,69)(56) b= 3,85
Jadi, persamaan garis regresi Y = 0,69X + 3,85 Nilai IC50 : Y = 0,69X + 3,85
Ambarsari, I., Qanytah., dan Sarjana. (2013). Perubahan Aktivitas Antioksidan pada Bawang Putih Selama Proses Pengolahan dan Penyimpanan. Buletin
Teknologi Pascapanen Pertanian. 9(2): 64-73.
Antolovich, M., Paul, D.P., Emilios, P., Suzanne, M., dan Kevin, R. (2002). Methods for Testing Antioxidant Activity. The Analyst. 127: 183, 185, 190-198.
Arista, M. (2013). Aktivitas Antioksidan Ekstrak Etanol 80% dan 96% Daun Katuk (Sauropus androgynus (L) Merr.). Jurnal Ilmiah Fakultas Farmasi
Universitas Surabaya. 2(2): 1-6.
Chatterjee, S., Sabyasachi, C., Dey, K., dan Sikha, D. (2013). Study of Antioxidant Activity and Immune Stimulating Potency of the Ethnomedicinal Plant, Cassia alata (L.) Roxb. Medicinal & Aromatic
Plant. 2: 4.
Djauhariya, E., dan Hernani. (2004). Gulma Berkhasiat Obat. Jakarta: Seri Agrisehat. Halaman 24.
Departemen Kesehatan RI. (1989). Materia Medika Indonesia. Jilid Kelima. Jakarta: Depkes RI. Halaman 124-128.
Departemen Kesehatan RI. (1995). Materia Medika Indonesia. Jilid Keenam. Jakarta: Depkes RI. Halaman 299-306, 321, 325-326, 333-336.
Ditjen POM RI. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan RI. Halaman 100, 649-653, 659, 696, 733, 772.
Ditjen POM RI. (1995). Farmakope Indonesia. Edisi Keempat. Jakarta: Departemen Kesehatan RI. Halaman 889,999.
Ditjen POM RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halaman 1, 9-12, 17.
Farnsworth, N.R. (1966). Biological and Phytochemical Screening of Plants.
Journal of Pharmaceutical Sciences. 55(3): 241-269.
Gandjar, I.G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Halaman 222.
Handa, S.S., Khanuja, S.P.S., Longo, G., dan Rakesh, D.D. (2008). Extractions
Tecnologies for Medicinal and Aromatic Plants. Trieste: ICS-UNIDO.
Hariana, H.A. (2005). Tumbuhan Obat dan Khasiatnya. Edisi Kedua. Jakarta: Penebar Swadaya. Halaman 45.
Huliselan, Y., dan Defny S.W. (2015). Aktivitas Antioksidan Ekstrak Etanol, Etilasetat, dan n-Heksan dari Daun Sesewanua (Clerodendron Squamatum Vahl.). Pharmacon Jurnal Ilmiah Farmasi. 4(3): 155-163.
Ionita, P. (2003). Is DPPH Stable Free Radical a Good Scavenger for Oxygen Active Species? Bucharest Chem. 59(1): 11-16.
Julyasih, K.S., Wirawan, I.G.P., Wiwik, S.H., dan Wiludjeng, W. (2009). Aktivitas Antioksidan Beberapa Jenis Rumput Laut (Seaweeds) Komersial di Bali. Seminar Nasional. Surabaya: Fakultas Pertanian UPN Veteran. Kosasih, E.N., Setiabudhi, T., dan Heryanto, H. (2004). Peranan Antioksidan
Pada Lanjut Usia. Jakarta: Pusat Kajian Nasional Masalah Lanjut Usia.
Halaman 48-49, 56-59.
Kumalaningsih, S. (2006). Antioksidan Alami. Surabaya: Trubus Agrisarana. Halaman 24.
Mardawati, E., Achyar, C.S., dan Marta, H. (2008). Kajian Aktivitas Antioksidan Ekstrak Kulit Manggis (Garcinia mangostana L.) dalam Rangka Pemanfaatan Limbah Kulit Manggis di Kecamatan Puspahiang Kabupaten Tasikmalaya. Laporan Akhir Penelitian. Bandung: Fakultas Teknologi Industri Pertanian Universitas Padjadjaran. Halaman 17.
Marinova, G., dan Batchvarov, V. (2011). Evaluation of the Methods for Determination of the Free Radical Scavenging Activity by DPPH. Bulgaria: Bulgarian Journal of Agricultural Science. 17(1): 11-24.
Markham, K.R. (1988). Cara Mengidentifikasi Flavonoid. Terjemahan Kosasih Padmawinata. Bandung: ITB. Halaman 8-9.
Molyneux, P. (2004). The Use of The Stable Free Radical DPPH For Estimating Antioxidant Activity. Songklanakarin J. Sci. Technol. 26(2): 211-219. Panichayupakaranant, P., dan Songsri, K. (2004). Bioassay-Guided Isolation of
The Antioxidant Constituent from Cassia alata L. Leaves. Songklanakarin
mirifica, Stevia rebaudiana Bertoni, Curcuma longa Linn., Andrographis paniculata (Burm.f.) Nees. and Cassia alata Linn. for the Development of Dietary Supplement. Kasetsart J. Nat. Sci. 41: 548-554.
Prakash, A., Fred, R., dan Eugene, M. (2001). Antioxidant Activity. Medallion Laboratories Analytical Progress. 45(2): 59-63.
Raaman, N. (2006). Phytochemical Techniques. New Delhi: New India Publishing Agency. Halaman 28-31.
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Edisi Keenam. Terjemahan Kosasih Padmawinata. Bandung: FMIPA ITB. Halaman 100-150.
Rohman, A. (2009). Kromatografi untuk Analisis Obat. Yogyakarta: Graha Ilmu. Halaman 51.
Saifudin, A. (2014). Senyawa Alam Metabolit Sekunder. Yogyakarta: Deepublish. Halaman 52-55.
Sannigrahi, S., Upal, K.M., Dilip, K.P., Sambit, P., dan Sourabh, J. (2010). Antioxidant Potential of Crude Extract and Different Fractions of Enhydra
fluctuans Lour. Iranian Journal of Pharmaceutical Research. 9(1): 75-82.
Santoso, D., dan Didik, G. (2000). Ramuan Tradisional untuk Penyakit Kulit. Jakarta: Penebar Swadaya. Halaman 65.
Sarkar, B., Suraj, K., Praveen, P., dan Mayank, M. (2014). HPLC Analysis And Antioxidant Potential Of Plant Extract of Cassia alata. Asian Journal of
Pharmaceutical Science & Technology. 4(1): 4-7.
Sarker, S. D dan Nahar, L. (2007). Chemistry for Pharmacy Student. United Kingdom: John Wiley and Son, Ltd. Halaman 322-323.
Shah, B.N., dan Seth, A.K. (2010). Textbook of Pharmacognosy and
Phytochemistry. India: Elsevier. Halaman 407-408, 410-411.
Silalahi, J. (2006). Makanan Fungsional. Yogyakarta: Kanisius. Halaman 38-55. Trease, G.E., dan Evans, W.C. (1983). Pharmacognosy. Edisi Keduabelas.
London: Bailliere Tindall. Halaman 220-221.
METODE PENELITIAN
Penelitian yang dilakukan adalah penelitian eksperimental. Penelitian meliputi pengambilan tumbuhan, identifikasi tumbuhan, karakterisasi simplisia, skrining fitokimia, pembuatan ekstrak etanol, fraksi n-heksana, fraksi etilasetat, fraksi air, analisis kandungan secara kromatografi lapis tipis dan kromatografi kertas, serta uji aktivitas antioksidan dengan metode pemerangkapan DPPH.
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan pada bulan September 2015 sampai dengan Januari 2016 di Laboratorium Fitokimia dan Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara.
3.2 Alat
Alat-alat yang digunakan terdiri dari alat-alat gelas laboratorium, cawan penguap berdasar rata, chamber, desikator, krus porselin, lemari pengering, mikroskop, neraca analitis (Vibra), neraca kasar (O’haus), oven listrik (Memmert), penangas air, rotary evaporator (Stuart), spektrofotometer UV/Vis (Shimadzu UV-1800) dan tanur (Gallenkamp).
3.3 Bahan
1,1-pekat, benzena, besi (III) klorida, bismut (III) nitrat, etanol, eter, etilasetat, iodium, isopropanol, kalium iodida, kloralhidrat, kloroform, metanol, n-heksana, natrium hidroksida, timbal (II) asetat, silika gel F254, toluen, vanilin. Bahan kimia berkualitas teknis: etanol 96%, etilasetat dan n-heksana.
3.4 Penyiapan Tumbuhan 3.4.1 Pengambilan tumbuhan
Pengambilan tumbuhan dilakukan secara purposif yaitu tanpa membandingkan dengan tumbuhan yang sama dari daerah lain. Tumbuhan yang digunakan adalah daun ketepeng (Senna alata (L.) Roxb.) yang diperoleh dari Kelurahan Padang Bulan Selayang II, Kecamatan Medan Selayang, Kota Medan, Provinsi Sumatera Utara.
3.4.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Bogoriense, Bidang Botani, Pusat Penelitian dan Pengembangan Biologi, LIPI Bogor.
3.4.3 Pengolahan tumbuhan
Pemeriksaan karakteristik simplisia seperti penetapan kadar air dilakukan menurut prosedur World Health Organization (1992); pemeriksaan makroskopik, pemeriksaan mikroskopik, penetapan kadar sari larut air, penetapan kadar sari larut etanol, penetapan kadar abu total dan penetapan kadar abu tidak larut asam dilakukan menurut prosedur yang terdapat dalam buku Materia Medika Indonesia (1995).
3.4.4.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan terhadap simplisia daun ketepeng dengan mengamati bentuk, warna, bau, rasa dan ukuran daun dan juga dilakukan pemeriksaan makroskopik terhadap daun ketepeng segar.
3.4.4.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia daun ketepeng. Sedikit serbuk simplisia ditaburkan di atas kaca objek yang telah ditetesi dengan larutan kloralhidrat dan ditutup dengan kaca penutup, kemudian diamati di bawah mikroskop.
3.4.4.3 Penetapan kadar air
dilanjutkan selama 5 menit kemudian tabung penerima dibiarkan mendingin pada suhu kamar. Volume air dibaca dengan ketelitian 0,05 ml setelah air dan toluen memisah sempurna. Selisih kedua volume air yang dibaca sesuai dengan kandungan air yang terdapat dalam bahan yang diperiksa. Kadar air dihitung dalam persen.
3.4.4.4 Penetapan kadar sari larut dalam air
Sebanyak 5 g serbuk yang telah dikeringkan di udara, dimaserasi selama 24 jam dalam 100 ml air-kloroform (2,5 ml kloroform dalam air suling sampai 1 liter) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama kemudian dibiarkan selama 18 jam, kemudian disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa penguapan dipanaskan pada suhu 105oC sampai diperoleh bobot tetap. Kadar persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan di udara.
3.4.4.5 Penetapan kadar sari larut dalam etanol
Sebanyak 2 g serbuk yang telah digerus dan ditimbang dengan seksama dimasukkan dalam krus porselin yang telah dipijar dan ditara kemudian diratakan. Krus dipijar perlahan-lahan sampai arang habis, pemijaran dilakukan pada suhu 600oC selama 3 jam kemudian didinginkan dan ditimbang sampai diperoleh bobot tetap. Kadar abu total dihitung terhadap bahan yang telah dikeringkan di udara. 3.4.4.7 Penetapan kadar abu tidak larut dalam asam
Abu yang telah diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml asam klorida encer selama 5 menit, lalu bagian yang tidak larut dalam asam dikumpulkan dan disaring dengan kertas saring yang dipijarkan sampai bobot tetap kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang dikeringkan di udara.
3.5 Pembuatan Larutan Pereaksi
Pembuatan larutan pereaksi asam klorida 2 N, larutan asam sulfat 2 N, larutan asam nitrat 0,5 N, larutan natrium hidroksida 2 N, pereaksi Bouchardat, kloralhidrat, pereaksi Mayer, pereaksi Dragendorff, pereaksi Molisch, larutan timbal (II) asetat 0,4 M menurut Depkes RI (1995).
3.5.1 Larutan pereaksi Bouchardat
20 ml asam nitrat pekat. Pada wadah lain ditimbang sebanyak 27,2 g kalium iodida lalu dilarutkan dalam 50 ml air suling. Kedua larutan dicampurkan dan didiamkan sampai memisah sempurna. Larutan yang jernih diambil dan diencerkan dengan air suling hingga 100 ml.
3.5.3 Larutan pereaksi Mayer
Sebanyak 2,266 g raksa (II) klorida ditimbang, kemudian dilarutkan dalam air suling hingga 100 ml. Pada wadah lain ditimbang sebanyak 50 g kalium iodida lalu dilarutkan dalam 100 ml air suling. 60 ml larutan I dicampurkan dengan 10 ml larutan II dan ditambahkan air suling hingga diperoleh larutan pereaksi Mayer sebanyak 100 ml.
3.5.4 Larutan pereaksi Molisch
Sebanyak 3 g alfa naftol ditimbang, kemudian dilarutkan dalam asam nitrat 0,5 N hingga volume 100 ml.
3.5.5 Larutan pereaksi asam klorida 2 N
Sebanyak 17 ml asam klorida pekat dilarutkan dalam air suling hingga volume 100 ml.
3.5.6 Larutan pereaksi asam sulfat 2 N
Sebanyak 5,5 ml asam sulfat pekat dilarutkan dalam air suling hingga volume 100 ml.
3.5.7 Larutan pereaksi asam nitrat 0,5 N
Sebanyak 15,17 g timbal (II) asetat ditimbang, kemudian dilarutkan dalam air suling bebas karbondioksida hingga diperoleh volume pereaksi sebanyak 100 ml.
3.5.9 Larutan pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dalam air suling hingga volume 100 ml.
3.5.10 Larutan pereaksi kloralhidrat 70% b/b
Sebanyak 70 g kristal kloralhidrat ditimbang, kemudian dilarutkan dalam 30 ml air suling.
3.5.11 Larutan pereaksi natrium hidroksida 2 N
Sebanyak 8,001 gram kristal natrium hidroksida ditimbang, dilarutkan dalam air suling sehingga diperoleh larutan 100 ml.
3.6 Skrining Fitokimia
Skrining fitokimia serbuk simplisia daun ketepeng meliputi pemeriksaan senyawa alkaloida, glikosida, saponin, flavonoida, antrakinon, tanin dan triterpenoid/ steroid.
3.6.1 Pemeriksaan alkaloida
c. Ditambahkan 2 tetes pereaksi Mayer
Alkaloida disebut positif jika terjadi endapan atau kekeruhan pada paling sedikit 2 tabung reaksi dari percobaan di atas (Depkes, RI., 1995).
3.6.2 Pemeriksaan glikosida
Serbuk simplisia ditimbang sebanyak 3 g kemudian disari dengan 30 ml campuran 7 bagian volume etanol 96% dan 3 bagian volum air suling ditambah dengan 10 ml asam klorida 2 N. Direfluks selama 30 menit, didinginkan dan disaring. Diambil 20 ml filtrat, ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M lalu dikocok selama 5 menit dan disaring. Filtrat disari dengan 20 ml campuran 3 bagian kloroform dan 2 isopropanol dilakukan berulang sebanyak tiga kali. Kumpulan sari air diuapkan pada temperatur tidak lebih dari 500C. Sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan berikut, yaitu 0,1 ml larutan percobaan dimasukkan ke dalam tabung reaksi, diuapkan di penangas air. Sisa dilarutkan dalam 2 ml air suling dan 5 tetes pereaksi Molisch kemudian secara perlahan ditambahkan 2 ml asam sulfat pekat. Glikosida pada tumbuhan dikatakan positif jika terbentuk cincin ungu (Depkes, RI., 1995). 3.6.3 Pemeriksaan saponin
Sebanyak 10 g serbuk simplisia kemudian ditambahkan 100 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, filtrat yang diperoleh kemudian diambil 5 ml lalu di tambahkan 0,1 g serbuk Mg dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah, kuning, jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.5 Pemeriksaan antrakinon
Sebanyak 0,2 g serbuk simplisia ditambahkan 5 ml asam sulfat 2 N, dididihkan 5 menit, didinginkan, ditambahkan 10 ml benzen, dikocok lalu didiamkan. Lapisan benzen dipisahkan dengan cara disaring, filtrat yang berwarna kuning menunjukkan adanya antrakinon. Lapisan benzen dikocok dengan 1-2 ml natrium hidroksida 2 N lalu didiamkan. Lapisan air berwarna merah dan lapisan benzen tidak berwarna menunjukkan adanya antrakinon (Depkes, RI., 1995). 3.6.6 Pemeriksaan tanin
Sebanyak 0,5 g sampel disari dengan 10 ml air suling, disaring lalu filtratnya diencerkan dengan air suling sampai tidak berwarna. Dua ml larutan ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida. Terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin (Depkes, RI., 1995).
3.6.7 Pemeriksaan triterpenoid/steroid
3.7 Pembuatan Ekstrak dan Fraksi 3.7.1 Pembuatan ekstrak etanol
Pembuatan ekstrak dilakukan secara maserasi menggunakan pelarut etanol 80%. Masukkan 10 bagian simplisia ke dalam wadah berwarna gelap, tuang 75 bagian cairan penyari, tutup, biarkan selama 5 hari terlindung dari cahaya sambil sering diaduk, serkai, peras, cuci ampas dengan cairan penyari secukupnya hingga diperoleh 100 bagian. Pindahkan ke dalam bejana tertutup, biarkan di tempat sejuk, terlindung dari cahaya, selama 2 hari. Enap tuangkan atau saring (Depkes RI., 1979). Maserat diuapkan dengan rotary evaporator pada temperatur ±40oC sampai diperoleh ekstrak kental.
3.7.2 Pembuatan fraksi
3.8.1 Pembuatan profil KLT
Pembuatan profil KLT dari ekstrak etanol daun ketepeng dilakukan menggunakan fase gerak n-heksana-etilasetat dengan berbagai perbandingan, fase diam plat lapis silika gel 60 F254 dan sebagai penampak bercak digunakan pereaksi Liebermann-Burchard. Cara kerja: larutan ekstrak ditotolkan pada plat lapis silika gel 60 F254 yang sebelumnya telah diaktifkan, kemudian dimasukkan ke dalam
chamber yang telah jenuh dengan uap pengembang dan ditutup rapat, setelah elusi
selesai plat dikeluarkan dari chamber dan dikeringkan di udara, kemudian plat disemprot dengan larutan penampak bercak. Warna bercak yang terjadi diamati dan dihitung harga Rf-nya.
3.8.2 Pembuatan profil KKt
Pembuatan profil KKt dari ekstrak daun ketepeng dilakukan dengan menggunakan fase gerak asam asetat 5%, HCl 1% dan BAW (4:1:5) dengan fase diam kertas saring Whatmann dan sebagai penampak bercak digunakan pereaksi AlCl3, NH3 dan FeCl3. Cara kerja: larutan ekstrak ditotolkan pada kertas Whatmann, kemudian dimasukkan ke dalam chamber yang telah jenuh dengan uap pengembang dan ditutup rapat, setelah elusi selesai plat dikeluarkan dari
chamber dan dikeringkan di udara, kemudian disemprot dengan pereaksi AlCl3, NH3 dan FeCl3. Warna bercak yang terbentuk pada kertas Whatmann diamati dan dihitung harga Rf-nya.
terjadi perubahan warna DPPH dari ungu menjadi kuning) dengan nilai IC50 (konsentrasi sampel uji yang mampu meredam radikal bebas 50%) digunakan sebagai salah satu parameter untuk menentukan aktivitas antioksidan pada sampel uji.
3.9.2 Pembuatan larutan blanko DPPH
Sebanyak 19,7 mg DPPH dilarutkan dalam metanol hingga volume 100 ml untuk mendapatkan larutan DPPH 0,5 mM (konsentrasi 200 µg/ml). Dipipet sebanyak 5 ml kemudian dimasukkan ke dalam labu tentukur 25 ml, dicukupkan dengan metanol sampai garis tanda (konsentrasi 40 µg/ml).
3.9.3 Pengukuran panjang gelombang serapan maksimum DPPH
Larutan DPPH konsentrasi 40 μg/ml dihomogenkan dan diukur
serapannya pada panjang gelombang 400-750 nm yang merupakan panjang gelombang sinar tampak.
3.9.4 Pembuatan larutan induk ekstrak dan fraksi
Sebanyak 25 mg ekstrak etanol, fraksi n-heksana, fraksi etilasetat daun ketepeng ditimbang, dimasukkan ke dalam labu tentukur 25 ml, dilarutkan dengan metanol lalu volumenya dicukupkan dengan metanol sampai garis tanda (konsentrasi 1000 µg/ml).
3.9.5 Penentuan waktu reaksi
setiap menit selama 80 menit.
3.9.6 Pengukuran aktivitas antioksidan sampel uji
Larutan induk dipipet sebanyak 1 ml; 1,5 ml; 2 ml; dan 2,5 ml ke dalam labu tentukur 25 ml untuk mendapatkan konsentrasi larutan uji 40 µg/ml, 60 µg/ml, 80 µg/ml, dan 100 µg/ml. Ditambahkan 5 ml larutan DPPH 0,5 mM (200 µg/ml) ke dalam masing-masing labu tentukur lalu volumenya dicukupkan dengan metanol sampai garis tanda. Pengukuran dilakukan pada panjang gelombang 516 nm setelah didiamkan di tempat gelap.
3.9.7 Penentuan persen peredaman
Kemampuan antioksidan diukur sebagai penurunan serapan DPPH akibat adanya penambahan larutan uji. Nilai serapan DPPH sebelum dan sesudah penambahan larutan uji tersebut dihitung sebagai persen peredaman.
% peredaman = Akontrol- Asampel
Akontrol x 100%
Keterangan:
Akontrol
= Absorbansi tidak mengandung sampel
Asampel = Absorbansi sampelSelanjutnya hasil perhitungan dimasukkan ke dalam persamaan regresi dengan konsentrasi ekstrak (µg/ml) sebagai absis (sumbu X) dan nilai % peredaman (antioksidan) sebagai ordinatnya (sumbu Y).
3.9.8 Penentuan nilai IC50
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Herbarium Bogoriense, Bidang Botani Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI), Bogor, menunjukkan bahwa tumbuhan yang diteliti adalah Senna alata (L.) Roxb, suku Leguminosae.
4.2 Hasil Karakterisasi Simplisia
Hasil pemeriksaan makroskopik simplisia daun ketepeng yaitu simplisia berbau khas lemah (bau langu), mula-mula tidak berasa, lama-lama agak kelat. Daun majemuk, helaian anak daun berwarna hijau muda sampai hijau tua, bentuk jorong sampai bundar telur sungsang, panjang 3-15 cm, lebar 2,5-9 cm, ujung daun tumpul, pangkal daun miring dan pinggir daun rata. Tangkai anak daun lebih kurang 2 cm. Tulang daun menyirip dan tulang cabang daun kadang-kadang agak sejajar, ibu tulang daun dan tulang cabang jelas menonjol di permukaan bawah. Hasil pemeriksaan makroskopik simplisia yang diperoleh sesuai dengan yang terdapat pada Materia Medika Indonesia (1989) dan dapat dilihat pada Lampiran 3, halaman 52.
Tabel 4.1 Hasil pemeriksaan karakteristik serbuk simplisia daun ketepeng
No. Parameter Hasil Pemeriksaan
(%)
Syarat MMI (%)
1. Kadar air 6,62 -
2. Kadar sari larut air 20,46 > 20
3. Kadar sari larut etanol 15,40 > 15
4. Kadar abu total 4,14 < 6
5. Kadar abu tidak larut asam 0,37 < 1
Kadar air simplisia daun ketepeng diperoleh lebih kecil dari 10% yaitu 6,62%. Kadar air yang melebihi 10% dapat menjadi media yang baik untuk pertumbuhan mikroba, keberadaan jamur atau serangga, serta mendorong kerusakan mutu simplisia (WHO, 1992).
Hasil karakterisasi simplisia daun ketepeng menunjukkan kadar sari yang larut dalam air sebesar 20,46% sedangkan kadar sari yang larut dalam etanol sebesar 15,40%. Hasil penetapan kadar sari menunjukkan bahwa sari yang larut dalam air lebih besar daripada dalam etanol, hal ini menunjukkan bahwa senyawa yang terlarut dalam air lebih banyak seperti glikosida, gula, gom, protein, enzim, zat warna, dan asam organik sedangkan senyawa yang larut dalam etanol adalah glikosida, antrakinon, steroid terikat, dan dalam jumlah sedikit yang larut yaitu lemak dan saponin (Depkes, RI., 1989).
kadar abu pada simplisia daun ketepeng menunjukkan kadar abu total sebesar 4,14% dan kadar abu tidak larut dalam asam sebesar 0,37%. Hasil pemeriksaan karakterisasi simplisia yang meliputi kadar sari larut air, kadar sari larut etanol, kadar abu dan kadar abu tidak larut asam memenuhi persyaratan yang telah ditetapkan dalam Materia Medika Indonesia. Hasil perhitungan karakterisasi simplisia daun ketepeng dapat dilihat pada Lampiran 8, halaman 57.
4.3 Hasil Skrining Fitokimia Serbuk Simplisia
Hasil skrining fitokimia terhadap serbuk simplisia diketahui bahwa serbuk simplisia daun ketepeng mengandung golongan senyawa-senyawa kimia seperti yang terlihat pada Tabel 4.2 berikut ini.
Tabel 4.2 Hasil skrining fitokimia serbuk simplisia
No. Pemeriksaan Hasil
1. Alkaloid -
2. Flavonoid +
3. Tanin +
4. Saponin +
5. Glikosida +
6. Triterpenoid/ steroid +
7. Antrakinon +
Keterangan:
(+) positif : mengandung golongan senyawa (-) negatif : tidak mengandung golongan senyawa
4.4. Hasil Ekstraksi dan Fraksinasi
Hasil ekstraksi 500 g simplisia daun ketepeng dengan cara maserasi menggunakan pelarut etanol 80% sebanyak 5 liter, simplisia : pelarut (1 gram : 10 ml) diperoleh ekstrak etanol daun ketepeng sebanyak 72,5 g. Ekstrak etanol difraksinasi menggunakan pelarut n-heksana dan air, dari 30 g ekstrak diperoleh fraksi n-heksana 3,51 g, selanjutnya fraksi air difraksinasi dengan etilasetat sehingga diperoleh fraksi etilasetat 2,41 g. Ekstrak dan fraksi yang diperoleh diuji aktivitas antioksidan dengan metode peredaman radikal bebas DPPH.
4.5Profil Kromatografi Lapis Tipis Ekstrak Etanol Daun Ketepeng
Hasil analisis KLT ekstrak etanol daun ketepeng mengggunakan fase gerak n-heksana:etilasetat (90:10) dengan penampak bercak Liebermann-Burchard diperoleh 11 noda dengan 4 senyawa triterpenoid/steroid (Rf 0,31; 0,76; 0,80 dan 0,84). Gambar kromatogram dan tabel data hasil analisis secara KLT dapat dilihat padaLampiran 9, halaman 61.
4.6 Profil Kromatografi Kertas Ekstrak Etanol Daun Ketepeng
flavonoid. Hasil pemisahan ekstrak etanol daun ketepeng secara kromatografi kertas dapat dilihat pada Tabel 4.3.
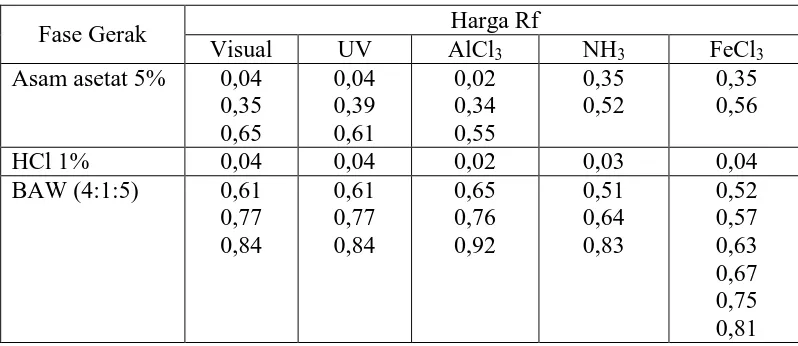
Tabel 4.3 Data hasil analisis KKt ekstrak etanol daun ketepeng
Fase Gerak Harga Rf
Pada tabel di atas terlihat bahwa hasil kromatografi ekstrak etanol daun ketepeng dengan KKt menunjukkan fase gerak terbaik adalah BAW (4:1:5), diperoleh 6 noda senyawa tanin yang berwarna biru kehitaman dan 3 noda senyawa flavonoid yang berwarna kuning dengan NH3 maupun AlCl3. Fase gerak asam asetat 5% dan HCl 1% memberikan jumlah noda lebih sedikit dibanding fase gerak BAW (4:1:5). Gambar kromatogram dapat dilihat pada Lampiran 10, halaman 63.
4.7 Hasil Analisis Aktivitas Antioksidan Ekstrak dan Fraksi
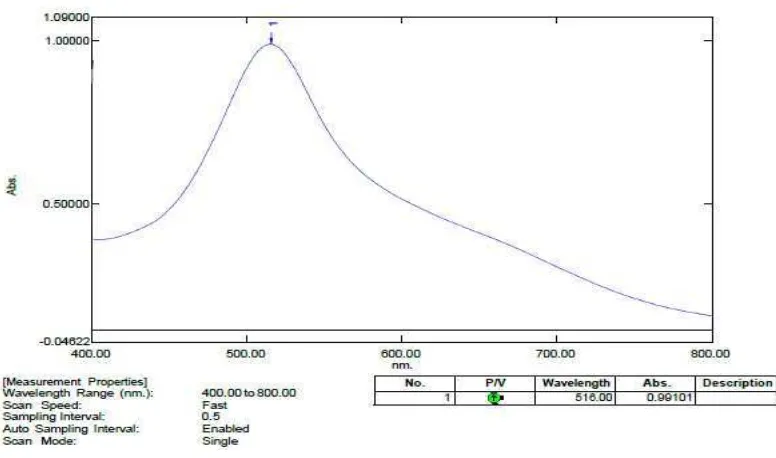
4.7.1 Hasil penentuan panjang gelombang serapan maksimum
Hasil pengukuran serapan maksimum larutan DPPH 40 µg/ml dalam metanol dengan menggunakan spektrofotometer UV-Visibel. Hasil pengukuran menunjukkan bahwa larutan DPPH dalam metanol menghasilkan serapan maksimum sebesar 0,99101 pada panjang gelombang 516 nm. Data hasil pengukuran panjang gelombang serapan maksimum larutan DPPH 40 µg/ml dalam metanol dapat dilihat pada Gambar 4.1.
Gambar 4.1 Kurva panjang gelombang DPPH dalam metanol 4.7.2 Hasil analisis peredaman radikal bebas DPPH oleh sampel uji
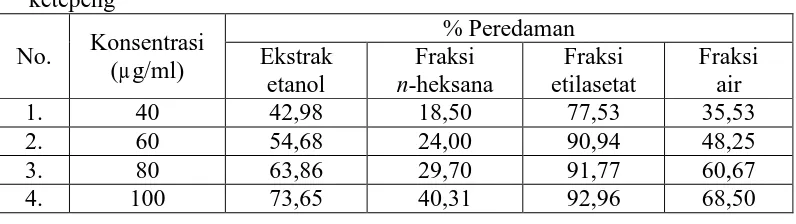
ketepeng
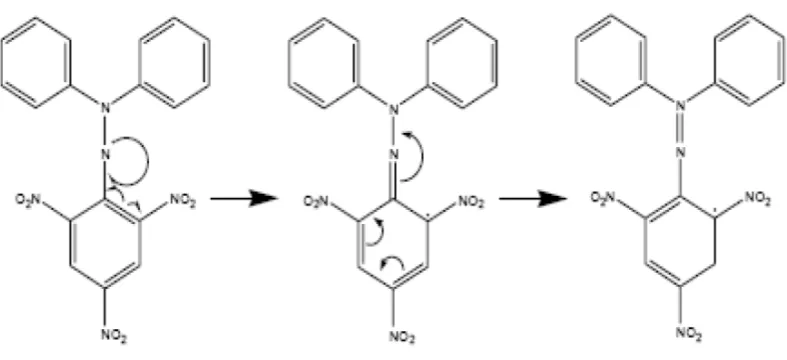
Hasil analisis peredaman radikal bebas oleh ekstrak dan fraksi daun ketepeng menunjukkan bahwa semakin meningkat konsentrasi ekstrak atau fraksi maka semakin meningkat aktivitas peredaman DPPH karena semakin banyak atom hidrogen dari ekstrak atau fraksi daun ketepeng yang berpasangan dengan elektron pada radikal bebas DPPH sehingga serapan semakin menurun yang ditandai dengan berubahnya warna larutan menjadi kuning (Molyneux, 2004). 4.7.3 Hasil analisis aktivitas antioksidan
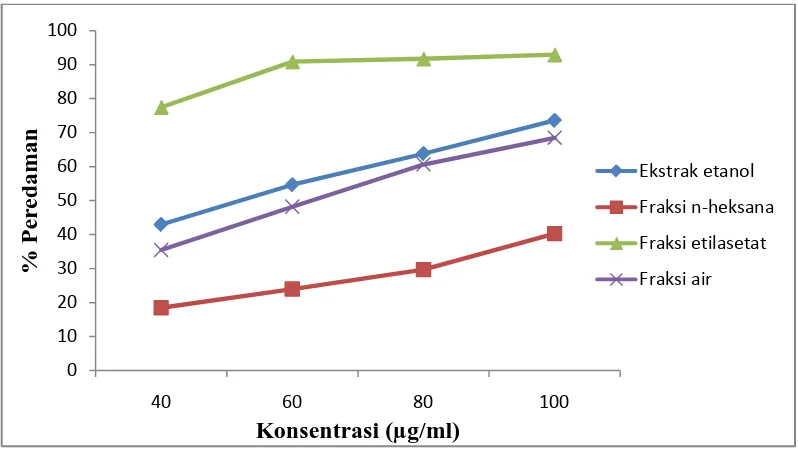
Gambar 4.2 Grafik hasil analisis aktivitas antioksidan ekstrak etanol, fraksi
n-heksana, fraksi etilasetat dan fraksi air dari daun ketepeng
Pada Gambar 4.2 dapat dilihat adanya peningkatan persen peredaman radikal bebas DPPH pada setiap kenaikan konsentrasi. Peningkatan persen peredaman DPPH ini menunjukkan adanya aktivitas antioksidan dari ekstrak atau pun fraksi. Interaksi antioksidan dengan DPPH baik secara transfer elektron atau donor hidrogen kepada DPPH, akan menetralkan radikal bebas DPPH. Jika semua elektron pada radikal bebas DPPH menjadi berpasangan, maka warna larutan berubah dari ungu tua menjadi kuning terang. Perubahan ini dapat diukur secara stoikiometri sesuai dengan jumlah elektron atau atom hidrogen yang ditangkap oleh molekul DPPH akibat adanya zat antioksidan (Molyneux, 2004).
4.7.4 Hasil analisis nilai IC50 (Inhibitory Concentration) sampel uji
Nilai IC50 diperoleh berdasarkan persamaan regresi linier yang didapatkan dengan memplot konsentrasi larutan uji dan persen peredaman DPPH, dengan konsentrasi larutan uji (µg/ml) sebagai absis dan nilai persen peredaman sebagai ordinat. Hasilnya dapat dilihat pada Tabel 4.5 berikut ini.
daun ketepeng
No. Larutan uji Persamaan regresi IC50 (µg/ml) 1. Ekstrak etanol Y= 0,727x + 6,322 60,08 2. Fraksi n-heksana Y= 0,386x + 0,874 127,27 3. Fraksi etilasetat Y= 0,915x + 19,40 33,43
4. Fraksi air Y= 0,691x + 3,857 66,78
Hasil pada Tabel 4.5 menunjukkan bahwa ekstrak etanol, fraksi n-heksana, fraksi etilasetat dan fraksi air dari daun ketepeng memiliki aktivitas antioksidan yang berbeda satu dengan yang lain. Ekstrak etanol daun ketepeng memiliki aktivitas antioksidan yang kuat dengan nilai IC50 sebesar 60,08 µ g/ml, fraksi
n-heksana memiliki aktivitas antioksidan yang lemah dengan nilai IC50 sebesar 127,27 µg/ml, fraksi etilasetat memiliki aktivitas antioksidan yang sangat kuat dengan nilai IC50 sebesar 33,43 µg/ml dan fraksi air memiliki aktivitas antioksidan yang kuat dengan nilai IC50 sebesar 66,78 µ g/ml. Perbedaan nilai IC50 pada masing-masing fraksi disebabkan oleh adanya distribusi jenis dan jumlah golongan senyawa metabolit sekunder yang bersifat sebagai antioksidan berdasarkan kepolaran pelarut yang digunakan (Huliselan dan Defny, 2015).
Fraksi etilasetat dengan nilai IC50 terendah yaitu 33,43 µg/ml memiliki aktivitas antioksidan terkuat karena adanya senyawa polifenol seperti flavonoid, tanin dan antrakinon. Keefektifan antioksidan pada ekstrak etilasetat dalam menetralkan radikal bebas berkaitan dengan sifat etilasetat yang semi polar sehingga banyak komponen bioaktif yang larut di dalamnya seperti senyawa polifenol (Huliselan dan Defny, 2015).
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Hasil karakterisasi simplisia diperoleh kadar air 6,62%, kadar sari yang larut dalam etanol 15,40%, kadar sari yang larut dalam air 20,46%, kadar abu total 4,14% dan kadar abu yang tidak larut dalam asam 0,37%. Karakteristik tersebut memenuhi persyaratan yang telah tertera dalam Materia Medika Indonesia.
2. Hasil skrining fitokimia pada simplisia diperoleh bahwa simplisia daun ketepeng mengandung senyawa glikosida, tanin, flavonoid, antrakinon, saponin dan triterpenoid/steroid sedangkan ekstrak etanol daun ketepeng yang dianalisis secara KLT dan KKt mengandung 6 senyawa tanin, 3 senyawa flavonoid, dan 4 senyawa triterpenoid/steroid.
3. Hasil pengujian aktivitas antioksidan dengan menggunakan metode pemerangkapan radikal bebas 1,1-diphenyl-2-picrylhydrazyl (DPPH) diperoleh fraksi etilasetat memiliki aktivitas antoksidan paling kuat dengan nilai IC50 dari masing-masing ekstrak etanol, fraksi n-heksana, fraksi etilasetat dan fraksi air sebesar 60,08, 127,27, 33,43 dan 66,78 µg/ml.
5.2 Saran
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi morfologi tumbuhan, daerah tumbuh (habitat), sistematika tumbuhan, nama daerah dan nama asing, kegunaan tumbuhan dan kandungan kimia.
2.1.1 Morfologi tumbuhan
Ketepeng merupakan perdu tegak, berumur 1-2 tahun, cabang banyak, batang muda berwarna hijau. Tinggi mencapai 3 meter. Daun majemuk menyirip genap, tangkai daun panjang, terdiri dari 5-12 pasang anak daun. Anak daun bulat panjang ada pula yang bulat telur. Panjang daun 3-15 cm, lebar 2,5-9 cm. Tangkai pendek 1-2 cm, warna hijau, pangkal dan ujung daun tumpul, tepi daun rata, bau langu. Bunga tersusun dalam tandan yang panjang, tumbuh dari ujung cabang, mahkota bunga berwarna kuning, jumlah tandan bunga 3-8 buah. Buah polong, panjang 10-20 cm, lebar 12-15 mm, segi empat, bersayap. Buah muda warna hijau, buah matang hitam dan pecah. Biji terdapat dalam buah, berjumlah 50-70, warna coklat muda, bentuk bulat telur pipih, meruncing di bagian pangkal. Tumbuhan ini berkembangbiak dengan biji (Djauhariya dan Hernani, 2004).
2.1.2 Habitat
kelapa, dan kelapa sawit (Djauhariya dan Hernani, 2004). 2.1.3 Sistematika tumbuhan
Menurut Santoso dan Didik (2000), klasifikasi tumbuhan ketepeng adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledoneae Ordo : Fabales
Familia : Leguminosae Genus : Senna
Spesies : Senna alata (L.) Roxb.
Sinonim : Cassia alata L. 2.1.4 Nama daerah dan nama asing
Tumbuhan ketepeng di Indonesia memiliki berbagai macam nama daerah,
seperti daun kupang (Melayu), daun kurap, ura’kap (Sumatera), gelenggang
(Tapanuli), ki manila, ketepeng gede, katepeng (Sunda), ketepeng cina, ketepeng
kebo, ketepeng badak (Jawa Tengah), acong-acong (Madura), tabakum (Tidore),
dan kupang-kupang (Ternate). Nama asing tumbuhan ketepeng adalah seven
golden candlestick (Inggris), chum-het-thet (Thailand), dan dui ye dou (Cina)
menghilangkan rasa gatal di kulit (sebagai obat luar), obat sariawan dan obat malaria (diminum). Berdasarkan aktivitas biologis yang telah diteliti, kulit kayu tumbuhan ini berpotensi sebagai pencahar (Santoso dan Didik, 2000).
2.1.6 Kandungan kimia
Kandungan aktif tumbuhan ketepeng yang telah diketahui antara lain glikosida, flavonoid, tanin, triterpenoid/steroid, saponin dan turunan antrakinon seperti krisarobin glukosida, krisofanol, asam krisofanat rein serta aloe-emodina (Hariana, 2005).
2.2Uraian Golongan Senyawa Kimia Daun Ketepeng
Senyawa kimia yang terdapat pada daun ketepeng meliputi glikosida, flavonoid, tanin, triterpenoid/steroid dan saponin.
2.2.1 Glikosida
Glikosida adalah suatu senyawa yang jika dihidrolisis akan menghasilkan bagian gula yang disebut glikon dan bagian bukan gula disebut aglikon. Gula yang dihasilkan biasanya adalah glukosa, ramnosa, dan lain sebagainya. Jika bagian gulanya adalah glukosa maka disebut glukosida, sedangkan jika bagian gulanya selain glukosa disebut glikosida (Robinson, 1995).
Berdasarkan hubungan ikatan antara glikon dan aglikonnya, glikosida dibagi (Robinson, 1995):
dihubungkan oleh atom S. Contoh: Sinigrin.
c. N-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya dihubungkan oleh atom N. Contoh: Adenosine.
d. C-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya dihubungkan oleh atom C. Contoh: Barbaloin.
2.2.2 Flavonoid
Flavonoid mengandung lima belas atom karbon dalam inti dasarnya mempunyai struktur C6-C3-C6 yaitu dua cincin aromatik yang dihubungkan oleh tiga atom karbon yang merupakan rantai alifatik. Menurut perkiraan, kira-kira 2% dari seluruh karbon yang difotosintesis oleh tumbuhan diubah menjadi flavonoid atau senyawa yang berkaitan erat dengannya. Sebagian besar tanin berasal dari flavonoid sehingga merupakan salah satu golongan fenol alam yang terbesar (Markham, 1988).
Flavonoid mencakup banyak pigmen dan terdapat pada seluruh dunia tumbuhan mulai dari fungus sampai angiospermae. Flavonoid mempunyai banyak fungsi dalam tubuh tumbuhan. Beberapa fungsi utamanya adalah untuk tumbuhan yaitu pengaturan tumbuh, pengaturan fotosintesis, kerja antimikroba dan antivirus dan anti serangga (Robinson, 1995).
2.2.3 Tanin
kompleks (Trease dan Evans, 1983). a. Tanin terhidrolisis (hydrosable tannin)
Tanin jenis ini biasanya berikatan pada karbohidrat dengan membentuk jembatan oksigen dan dapat dihidrolisis menggunakan asam sulfat atau asam klorida ataupun dengan enzim. Prekursor pembentukan tanin ini adalah asam fenolit (asam galat, asam elagit), residu glukosa, serta antara asam fenolit dan glukosa ada ikatan ester.
b. Tanin terkondensasi (condesed tannins)
Tanin terkondensasi biasanya tidak dapat dihidrolisis, tetapi terkondensasi menghasilkan asam klorida. Tanin jenis ini kebanyakan terdiri dari polimer flavanoida yang merupakan senyawa fenol. Nama lain dari tanin ini adalah
Proanthocyanidin yang merupakan polimer dari flavanoida yang dihubungkan
melalui C8 dengan C4. Prekursor pembentukan tanin ini adalah flavanoida, katekin, flavonol-3-4-diol.
c. Tanin kompleks (complex tannin)
Tanin kompleks merupakan campuran antara tanin terhidrolisis dan tanin terkondensasi. Contoh tumbuhan yang mengandung tanin kompleks adalah teh, kuercus, dan castanea. Ada dua tipe dari tanin kompleks, yaitu true tannin (berat molekul 1000-5000) dan pseudo tannin (berat molekul kurang dari 1000).
2.2.4 Triterpenoid/steroid
kebanyakan merupakan suatu alkohol, aldehid atau karboksilat (Harbone, 1987). Triterpenoid merupakan senyawa tanpa warna, berbentuk kristal, sering kali bertitik leleh tinggi dan optis aktif, yang dibagi atas empat kelompok senyawa yaitu triterpen sebenarnya, steroid, saponin, dan glikosida jantung. Sebagian senyawa triterpenoid juga merupakan komponen aktif dalam tumbuhan obat, yang berkhasiat sebagai anti diabetes, gangguan menstruasi, gangguan kulit kerusakan hati dan malaria (Robinson, 1995).
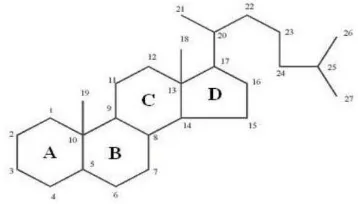
Steroid adalah triterpen yang kerangka dasarnya sistem cincin siklopentana perhidrofenantren. Dahulu steroid dianggap sebagai senyawa satwa (digunakan sebagai hormon kelamin, asam empedu), tetapi pada tahun-tahun terakhir ini makin banyak senyawa steroid yang ditemukan dalam jaringan tumbuhan (Harborne, 1987).
Gambar 2.1. Struktur dasar steroida dan sistem penomorannya Menurut asalnya senyawa steroid dibagi atas:
a. Zoosterol, yaitu steroid yang berasal dari hewan, misalnya kolesterol.
b. Fitosterol, yaitu steroid yang berasal dari tumbuhan, misalnya sitosterol dan stigmasterol.
2.2.5 Saponin
Saponin adalah glikosida triterpenoida dan sterol. Senyawa golongan ini banyak terdapat pada tumbuhan tinggi, merupakan senyawa dengan rasa yang pahit dan mampu membentuk larutan koloidal dalam air serta menghasilkan busa jika dikocok dalam air. Aglikon dari saponin sering disebut sebagai sapogenin. Saponin merupakan senyawa aktif permukaan, bersifat seperti sabun dan dapat diuji berdasarkan kemampuannya membentuk busa. Pembentukan busa yang mantap sewaktu mengekstraksi tumbuhan atau pada waktu memekatkan ekstrak tumbuhan merupakan bukti terpercaya akan adanya saponin pada tumbuhan tersebut (Harbone, 1987).
2.2.6 Antrakinon
Penicillium dan Aspergillus (Sarker dan Nahar, 2007).
2.3 Ekstraksi
Ekstraksi adalah proses penarikan zat aktif yang terdapat dalam tumbuhan dengan pelarut yang sesuai, sedangkan ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa yang tersisa diperlakukan sedemikian hingga memenuhi baku yang ditetapkan (Ditjen POM RI, 1995).
Metode ekstraksi menurut Handa, dkk (2008) ada beberapa cara, yaitu: 1. Maserasi
Maserasi adalah suatu proses penarikan zat aktif dari simplisia dengan cara merendam simplisia dalam sejumlah besar pelarut dalam suatu wadah tertutup dan didiamkan minimal 3 hari pada temperatur kamar dengan beberapa kali pengadukan, lalu disaring atau pun didekantasi.
2. Infusi
Infusi adalah proses penyarian zat aktif dari simplisia dengan menggunakan air dingin atau pun air mendidih dalam waktu yang relatif singkat. 3. Digesti
Digesti adalah proses penyarian secara maserasi dengan pengadukan pada temperatur yang lebih tinggi dari temperatur kamar.
digunakan untuk senyawa-senyawa yang larut dalam air dan tahan pemanasan. 5. Perkolasi
Perkolasi adalah suatu cara penyarian simplisia menggunakan perkolator. Simplisia dibasahi dengan cairan penyari lalu didiamkan selama 4 jam, kemudian ditambahkan lagi cairan penyari dan didiamkan selama 24 jam. Outler perkolator dibuka sehingga cairan yang terkandung di dalamnya dapat menetes perlahan secara terus-menerus sampai diperoleh ekstrak (perkolat).
6. Sokletasi
Sokletasi adalah proses penyarian kontinu menggunakan alat soklet, dimana pelarut akan terkondensasi dari labu menuju pendingin, kemudian jatuh membasahi sampel dan mengisi bagian tengah alat soklet. Tabung sifon juga terisi dengan larutan ekstraksi dan ketika mencapai bagian atas tabung sifon, larutan tersebut akan kembali ke dalam labu.
2.4 Radikal Bebas
Radikal bebas merupakan suatu spesies kimia yang memiliki satu atau lebih elektron yang tidak berpasangan pada orbital terluarnya. Adanya elektron yang tidak berpasangan menyebabkan spesies tersebut menjadi sangat reaktif untuk mencari pasangannya dengan menarik atau menyerang elekron dari senyawa lain sehingga menyebabkan senyawa tersebut akan menjadi radikal juga. Salah satu contoh radikal bebas adalah spesies oksigen reaktif atau Reactive
keadaan dasar (ground state) menyebabkan oksigen tereduksi, membentuk radikal bebas. Contoh senyawa oksigen reaktif adalah anion superoksida, oksigen triplet, radikal perhidroksil, radikal hidroksil, dan sebagainya (Kosasih, dkk., 2004).
Reaksi oksidasi yang melibatkan spesies oksigen reaktif tidak hanya berkaitan dengan kerusakan mutu produk pangan, namun reaksi oksidasi yang terjadi pada berbagai organ dan cairan tubuh juga berkaitan dengan munculnya penyakit-penyakit degeneratif seperti aterosklerosis, kanker dan liver. Target utama radikal bebas didalam tubuh adalah protein, asam lemak tidak jenuh dan lipoprotein, serta unsur DNA termasuk karbohidrat, terutama membran lipid
bilayer karena muatan asam lemaknya yang tinggi menyebabkan membran sangat
rentan terhadap radikal bebas. Berbagai kemungkinan dapat terjadi sebagai akibat kerja radikal bebas, misalnya gangguan fungsi sel, kerusakan struktur sel, molekul termodifikasi yang tidak dapat dikenali oleh sistem imun, dan bahkan mutasi. Semua gangguan tersebut dapat memicu munculnya berbagai penyakit (Kosasih, dkk., 2004).
2.5 Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya kepada molekul radikal bebas tanpa terganggu sama sekali dan dapat memutus reaksi berantai dari radikal bebas (Kumalaningsih, 2006).
enzimatis merupkan pertahanan utama (primer) terhadap kondisi stres oksidatif pada sel (Winarsi, 2007). Penggunaan senyawa antioksidan semakin berkembang, baik untuk makanan maupun untuk pengobatan seiring dengan bertambahnya pengetahuan tentang aktivitas radikal bebas yang dapat membahayakan kesehatan manusia (Julyasih, dkk., 2009).
Berdasarkan fungsinya, menurut Kumalaningsih (2006) antioksidan dapat dibedakan menjadi 5, yaitu:
a. Antioksidan primer
Antioksidan ini berfungsi untuk mencegah terbentuknya radikal bebas baru karena ia dapat merubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, yaitu sebelum sempat bereaksi. Antioksidan primer yang ada dalam tubuh yang sangat terkenal adalah enzim superoksida dismutase (SOD). b. Antioksidan sekunder
Antioksidan sekunder merupakan senyawa yang berfungsi menangkap radikal bebas serta mencegah terjadinya reaksi berantai sehingga tidak terjadi kerusakan yang lebih besar. Contoh yang populer dari antioksidan sekunder adalah vitamin E, vitamin C dan beta karoten.
c. Antioksidan tersier
Antioksidan yang termasuk oxygen scavenger mengikat oksigen sehingga tidak mendukung reaksi oksidasi, misalnya: vitamin C.
e. Chelators atau sequesstrants
Antioksidan ini mengikat logam yang mampu mengkatalisis reaksi oksidasi misalnya asam sitrat dan asam amino.
Mekanisme kerja antioksidan secara umum adalah menghambat oksidasi lemak. Oksidasi lemak menurut Antolovich, dkk., (2002) terdiri dari beberapa tahap, yaitu:
a. Inisiasi: LH + R* → L* + RH
Dimana LH merupakan molekul substrat, contohnya lipid, dan R* merupakan radikal pengoksidasi. Oksidasi lipid menghasilkan radikal asam lemak yang sangat reaktif (L*) yang dapat dengan cepat bereaksi dengan oksigen membentuk radikal peroksil lipid (LOO*) yang memiliki efek sangat berbahaya bagi tubuh. b. Propagasi: L* + O2→ LOO*
LOO* + LH → L* + LOOH
Radikal peroksil adalah pembawa rantai yang dapat mengoksidasi lipid lebih jauh, menghasilkan hidroperoksid lipid (LOOH).
c. Branching: LOOH → LO* + HO* 2LOOH → LOO* + LO* + H2O
Pemecahan dari hidroperoksid lipid melibatkan katalis ion logam transisi. Tahap ini akan menghasilkan peroksil lipid dan alkoksi lipid radikal.
non radikal.
Antioksidan yang ada di dalam tubuh yang sangat terkenal adalah enzim superoksida dismustase. Enzim ini sangat penting sekali karena dapat melindungi hancurnya sel-sel dalam tubuh akibat serangan radikal bebas. Bekerjanya enzim ini sangat dipengaruhi oleh mineral-mineral seperti mangan, seng, tembaga dan selenium. Berdasarkan jenisnya antioksidan dapat dibedakan menjadi dua yaitu antioksidan alami dan antioksidan sintetik (Kumalaningsih, 2006).
2.5.1 Antioksidan alami
Sayur-sayuran dan buah-buahan kaya akan zat gizi (vitamin, mineral, serat pangan) serta berbagai kelompok zat bioaktif lain yang disebut zat fitokimia. Zat bioaktif ini bekerja secara sinergis meliputi mekanisme enzim detoksifikasi, peningkatan sistem kekebalan, pengurangan agregasi platelet, pengaturan sintesis kolesterol dan metabolisme hormon, penurunan tekanan darah, antioksidan, antibakteri serta efek antivirus (Silalahi, 2006).
Salah satu antioksidan alami yang berperan sebagai antioksidan adalah flavonoid. Senyawa ini berperan sebagai penangkap radikal bebas karena mengandung gugus hidroksil yang dapat bertindak sebagai donor hidrogen terhadap radikal bebas (Silalahi, 2006).
2.5.2 Antioksidan sintetik
efektif untuk lemak hewan, sedangkan PG selain untuk lemak hewan juga baik untuk minyak nabati walaupun senyawa ini menimbulkan perubahan warna jika terdapat besi dan air. Senyawa ini mempunyai kelarutan yang lebih baik serta stabil pada suhu tinggi dan sedikit menguap dibandingkan dengan BHA dan BHT. Saat ini banyak negara yang tidak mengizinkan penggunaan BHA dan BHT, karena pada percobaan, pemberian dalam dosis tinggi BHA dan BHT menimbulkan efek teratogenik pada tikus (Julyasih, dkk., 2009).
2.6 Kromatografi
Kromatografi adalah suatu metode yang digunakan untuk pemisahan komponen cuplikan yang komponen-komponennya terdistribusi antara dua fase, salah satunya diam dan yang lainnya bergerak. Fase diam dapat berupa bahan padat atau porus dalam bentuk molekul kecil atau dalam bentuk cairan yang dilapiskan pada pendukung padat atau dilapiskan pada dinding kolom. Fase gerak dapat berupa gas atau cairan yang dapat dengan mudah mengalir pada fase diam (Rohman, 2009).
Schraiber pada tahun 1938. Pada kromatografi lapis tipis, fase diamnya berupa lapisan yang seragam pada permukaan bidang datar yang didukung oleh lempeng kaca, plat aluminium atau plat plastik (Rohman, 2009).
Fase diam dapat berupa serbuk halus yang berfungsi sebagai permukaan penjerap (kromatografi cair-padat) atau berfungsi sebagai penyangga untuk lapisan zat cair (kromatografi cair-cair). Fase diam yang umum dipakai adalah silika gel (asam silikat), alumina (aluminium oksida), kieselgur (tanah diatom) dan selulosa (Saifudin, 2014).
Eluen pengembang dapat berupa pelarut tunggal ataupun campuran pelarut dengan susunan tertentu Pelarut-pelarut pengembang harus mempunyai kemurnian yang tinggi. Terdapatnya sejumlah kecil air atau zat pengotor lainnya dalam pengembang dapat menghasilkan kromatogram yang tidak diharapkan (Hahn-Deinstrop, 2007).
Menurut Hahn-Deinstrop (2007), cara mengamati bercak pada KLT dapat digolongkan menjadi dua:
366 nm untuk melihat fluoresensi.
Mengidentifikasi noda-noda dalam kromatografi lapis tipis sangat lazim menggunakan harga Rf (Retordation Factor).
Rf= Jarak titik pusat bercak dari titik awal Jarak garis depan pelarut dari titik awal
Angka Rf memiliki interval antara 0,00 hingga 1,00 dan hanya dapat ditentukan dua desimal. hRf adalah angka Rf dikalikan faktor 100 (h), menghasilkan nilai antara 0 - 100. Jika keadaan luar misalnya sifat penjerap yang agak menyimpang maka profil kromatogram juga akan menyimpang, yang secara umum ditunjukkan dengan angka Rf lebih rendah atau lebih tinggi, maka sistem pelarut harus diganti dengan yang lebih sesuai. Jika angka hRf lebih tinggi dari hRf yang dinyatakan, kepolaran pelarut harus dikurangi, jika hRf lebih rendah maka komponen polar pelarut harus dinaikkan (Hahn-Deinstrop, 2007).
2.6.2 Kromatografi kertas
Kromatografi kertas (KKt) adalah teknik kromatografi tertua yang digunakan untuk memisahkan senyawa-senyawa dalam analit. Perbedaan utama KKt dengan teknik kromatografi yang lain yaitu penggunaan sehelai kertas sebagai penjerap atau fase diam. Campuran yang akan dipisahkan, ditotolkan pada bagian bawah kertas, kemudian ditaruh di dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak), pemisahan terjadi selama proses elusi (Raaman, 2006).