PENETAPAN KADAR VITAMIN C DARI JUS BUAH APEL
(Malus domestica Borkh.) YANG BERWARNA MERAH DAN
HIJAU SECARA TITRASI DENGAN 2,6-DIKLOROFENOL
INDOFENOL PADA BEBERAPA INTERVAL WAKTU
SKRIPSI
OLEH:
NOVARIA SARI DEWI P
NIM 111501063
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR VITAMIN C DARI JUS BUAH APEL
(Malus domestica Borkh.) YANG BERWARNA MERAH DAN
HIJAU SECARA TITRASI DENGAN 2,6-DIKLOROFENOL
INDOFENOL PADA BEBERAPA INTERVAL WAKTU
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
NOVARIA SARI DEWI P
NIM 111501063
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR VITAMIN C DARI JUS BUAH APEL
(Malus domestica Borkh.) YANG BERWARNA MERAH DAN
HIJAU SECARA TITRASI DENGAN 2,6-DIKLOROFENOL
INDOFENOL PADA BEBERAPA INTERVAL WAKTU
OLEH:
NOVARIA SARI DEWI P NIM 111501063
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 28 Juli 2015
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Dra. Siti Nurbaya, M.Si., Apt. Dr. Masfria, M.S., Apt.
NIP 195008261974122001 NIP 195707231986012001
Pembimbing II, Dra. Siti Nurbaya, M.Si., Apt.
NIP 195008261974122001
Dra. Tuty Roida Pardede, M.Si., Apt. Dra. Sudarmi, M.Si., Apt.
NIP 195401101980032001 NIP 195409101983032001
Drs. Maralaut Batubara, M.Phill., Apt. NIP 105101311976031003
Medan, Agustus 2015 Fakultas Farmasi
Universitas Sumatera Utara Wakil Dekan I,
KATA PENGANTAR
Salam kasih dan damai sejahtera,
Puji syukur penulis ucapkan kepada Tuhan Yang Maha Kuasa atas segala
limpahan kasih, rahmat, dan anugerahNya, sehingga bersamaNya penulis dapat
menyelesaikan penelitian dan penyusunan skripsi ini.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul
“Penetapan Kadar Vitamin C dari Jus Buah Apel (Malus domestica Borkh.) yang
Berwarna Merah dan Hijau secara Titrasi dengan 2,6-Diklorofenol Indofenol pada
Beberapa Interval Waktu”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada Bapak Prof. Dr. Sumadio
Hadisahputra, Apt., selaku Dekan dan Prof. Dr. Julia Reveny, M.Si., Apt., selaku
Wakil Dekan I Fakultas Farmasi Universitas Sumatera Utara beserta seluruh staf
pengajar dan staf administrasi Fakultas Farmasi yang telah mendidik penulis
selama masa perkuliahan dan membantu kemudahan administrasi hingga selesai.
Ibu Dra. Siti Nurbaya, M.Si., Apt., selaku Pembimbing I dan Ibu Dra. Tuty Roida
Pardede, M.Si., Apt., selaku Pembimbing II, yang telah membimbing dan
memberi petunjuk serta saran-saran selama penelitian hingga selesainya skripsi
ini. Ibu Dr. Masfria, M.S., Apt., Ibu Dra. Sudarmi, M.Si., Apt., dan Bapak Drs.
Maralaut, M.Phill., Apt., selaku tim Penguji yang telah memberikan petunjuk
serta saran-saran dalam menyempurnakan skripsi ini. Ibu Dra. Erly Sitompul,
selaku Kepala Laboratorium Kimia Organik, dan Bapak Drs. Nahitma Ginting,
M.Si., Apt., selaku Kepala Laboratorium Sintesa Obat yang telah membimbing
penulis, khususnya selama menjadi asisten di kedua Laboratorium tersebut.
Penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada
Alm. Ayahanda B. Panjaitan dan Ibunda G. Saragih, S.Pd yang telah memberikan
kasih sayang, perhatian, dan semangat yang tak terhingga kepada penulis,
Adik-adik ku terkasih Bella, Jonni, dan Raja, serta seluruh keluarga yang selalu
mendoakan dan memberikan semangat, sahabat-sahabat ku Vanny, Merna dan
Asrika, rekan asisten laboratorium Sandhy, Lisah, Daud dan seluruh teman-teman
Farmasi, terima kasih untuk perhatian, semangat, doa, dan kebersamaannya
selama ini, serta seluruh pihak yang telah ikut membantu penulis namun tidak
tercantum namanya, yang telah memberikan cinta dan kasih sayang yang tidak
ternilai dengan apapun, doa yang tulus serta pengorbanan baik materi maupun
non-materi.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari sempurna, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis
berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Juli 2015
Penulis,
PENETAPAN KADAR VITAMIN C DARI JUS BUAH APEL
(Malus domestica Borkh.) YANG BERWARNA MERAH DAN
HIJAU SECARA TITRASI DENGAN 2,6-DIKLOROFENOL
INDOFENOL PADA BEBERAPA INTERVAL WAKTU
ABSTRAK
Buah apel (Malus domestica Borkh.) merupakan salah satu buah yang sangat populer dan banyak dikonsumsi oleh masyarakat dalam bentuk minuman dengan cara diblender atau dibuat jus. Disamping warnanya yang menarik, buah apel bermanfaat untuk kesehatan karena memiliki kadar zat gizi yang tinggi. Penelitian ini bertujuan untuk mengetahui kadar vitamin C yang terkandung dalam jus buah apel merah dan hijau dan penurunan kadar vitamin C dalam jus apel merah dan jus apel hijau pada beberapa interval waktu yaitu 0 hingga 5 jam.
Sampel buah apel merah dan hijau yang digunakan, diperoleh dari Supermarket buah Palangkaraya. Penetapan kadar vitamin C yang terdapat dalam jus buah apel merah dan hijau dilakukan dengan metode volumetri dengan 2,6-diklorofenol indofenol, metode ini merupakan cara yang paling banyak digunakan untuk menentukan kadar vitamin C dalam bahan pangan karena larutan 2,6 -diklorofenol indofenol selektif terhadap vitamin C.
Hasil penelitian menunjukkan bahwa kadar vitamin C pada jus buah apel merah pada titik waktu 0 hingga 5 jam adalah 12,76 mg/100 g menjadi 1,35 mg/100 g. Sedangkan kadar vitamin C pada jus buah apel hijau pada titik waktu 0 hingga 5 jam adalah 16,49 mg/100 g menjadi 2,97 mg/100 g.
Hasil uji statistik SPSS (statistical package for the social science) menunjukkan adanya perbedaan kadar vitamin C pada jus buah apel merah dan hijau. Diperoleh perbedaan yang signifikan rata-rata penurunan kadar vitamin C dari jus buah apel dan hijau pada titik waktu 0 hingga 5 jam. Pada uji validasi metode diperoleh persen recovery pada jus buah apel merah sebesar 98,36% dengan simpangan baku relatif sebesar 0,80%, sedangkan persen recovery pada jus buah apel hijau sebesar 97,35% dengan simpangan baku relatif sebesar 0,01%.
DETERMINATION OF VITAMIN C FROM JUICE OF RED
AND GREEN APPLE (Malus domestica Borkh.) BY
VOLUMETRIC METHOD USING 2,6-DICLOROPHENOL
INDOPHENOL ON SEVERAL TIME INTERVALS
ABSTRACT
Apple (Malus domestica Borkh.) is one of the most popular fruit and most consumed by the society for drinking by blended or juiced. Beside of its interesting colour, apple also has good function for health because it contents high levels of nutrition. This research was intended to find out about the content of vitamin C in red and green apple juice and to find out about the decreasing of vitamin C level in red and green apple juice on several time intervals, which is 0 to 5 hours.
Red and greed apple samples were used, obtained from Palagkaraya Fruit Supermarket, Medan. The vitamin C content determination in juice of red and green apple (Malus domestica Borkh.) was done with volumetri method with 2,6-dichlorophenol indophenols. This method is the most used method in determining vitamin C content in food because the 2,6-dichlorophenol indophenols solution is selective to vitamin C.
The result of the research shows that the vitamin C content in red apple juice on 0 to 5 hours are 12.76 mg/100 g to 1.35 mg/100 g. Whereas the vitamin C content in green apple juice on 0 to 5 hours are 16.49 mg/100 g to 2.97 mg/100 g.
The results of statistical tests SPSS (statistical package for the social sciences) shows the differences in the levels of vitamin C in red and green apple juice. It is obtained the significant difference on average decreasing the levels of vitamin C in red and green apple juice on 0 to 5 hours. In the validation test method, the percent recovery of red apple juice was obtained 98.36% and relative standard deviation of 0.80%, whereas the percent recovery of green apple juice was obtained 97.35% and relative standard deviation of 0.01%.
DAFTAR ISI
Halaman
JUDUL ... i
PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Apel ... 4
2.2 Ekologi dan Syarat Tumbuh Apel ... 5
2.3 Vitamin ... 7
2.3.1 Vitamin C ... 8
2.5 Analisis Kembali Kadar Vitamin C yang Ditambahkan pada
Sampel (Analisis Recovery) ... 16
2.6 Analisis Data Secara Statistik ... 17
2.6.1 Penolakan Hasil Pengamatan (Rejection of Measure ment) ... 17
2.6.2 Uji Ketelitian (Presisi) Metode Analisis ... 17
2.6.3 Pengujian Beda Nilai Rata-rata ... 18
BAB III METODE PENELITIAN ... 19
3.1 Tempat dan Waktu Penelitian ... 19
3.2 Alat dan Bahan ... 19
3.2.1 Alat-alat ... 19
3.2.2 Bahan-bahan ... 19
3.3 Pengambilan Sampel ... 20
3.4 Prosedur Penelitian ... 20
3.4.1 Pembuatan Pereaksi ... 20
3.4.1.1 Larutan 2,6-diklorofenol indofenol 0,025% b/v 20
3.4.1.2 Larutan asam metafostfat 3% b/v ... 20
3.4.1.3 Larutan NaHCO3 0,084% b/v ... 20
3.4.2 Perhitungan Kesetaraan Larutan Pentiter 2,6-Dikloro fenol Indofenol ... 21
3.4.3 Penyiapan Larutan Sampel ... 21
3.4.4 Penetapan Kadar Vitamin C dari Larutan Sampel ... 22
3.4.5 Validasi ... 23
3.4.5.1 Uji Perolehan Kembali (Recovery) ... 23
3.4.5.2 Uji Ketelitian (Presisi) Metode Analisis ... 24
3.4.6.1 Penolakan Hasil Pengamatan ... 24
3.4.6.2 Pengujian Beda Nilai Rata-rata ... 26
BAB IV HASIL DAN PEMBAHASAN ... 27
4.1 Hasil Identifikasi Tumbuhan ... 27
4.2 Hasil Penetapan Kadar Vitamin C dari Jus Buah Apel Merah dan Jus Buah Apel Hijau pada Beberapa Interval Waktu ... 27
4.3 Profil Penurunan Kadar Vitamin C pada Jus Buah Apel yang Berwarna Merah dan Hijau pada Berberapa Interval Waktu (0 hingga 5 jam) ... 30
4.4 Hasil Uji Statistik ... 33
4.5 Hasil Uji Perolehan Kembali (Recovery) ... 35
BAB V KESIMPULAN DAN SARAN ... 36
5.1 Kesimpulan ... 36
5.2 Saran ... 36
DAFTAR PUSTAKA ... 38
DAFTAR TABEL
Tabel Halaman
4.1 Hasil penetapan kadar vitamin C dari jus buah apel merah dan jus buah apel hijau pada interval waktu 0 hingga 5 jam ... 28
4.2 Hasil uji F kadar vitamin C jus buah apel (Malus domestica
(Borkh.) yang berwarna merah dan hijau ... 29
4.3 Hasil uji analisis Duncan terhadap kadar vitamin C dari jus buah apel merah dan jus buah apel hijau pada interval waktu 0 hingga 5 jam ... 33
4.4 Hasil uji perolehan kembali (recovery) vitamin C dari jus buah
apel merah ... 34
4.5 Hasil uji perolehan kembali (recovery) vitamin C dari jus buah
DAFTAR GAMBAR
Gambar Halaman
2.1 Rumus bangun vitamin C ... 9
2.2 Reaksi perubahan vitamin C ... 10
2.3 Reaksi antara vitamin C dan iodin ... 14
2.4 Reaksi antara asam askorbat dengan 2,6-diklorofenol indofenol 15
4.1 Profil penurunan kadar vitamin C dari jus buah apel merah dan
jus buah apel hijau pada interval waktu 0 hingga 5 jam ... 30
4.2 Grafik regresi penurunan kadar vitamin C pada jus apel merah . 31
DAFTAR LAMPIRAN
Lampiran Halaman
1. Sertifikat identifikasi tumbuhan ... 41
2. Sertifikat baku pembanding ... 42
3. Gambar buah apel merah dan apel hijau (Malus domestica
Borkh.) ... 43
4. Gambar jus buah apel merah dan jus buah apel hijau ... 44
5. Bagan alir penetapan kadar dari jus buah apel merah ... 45
6. Bagan alir penetapan kadar dari jus buah apel hijau ... 46
7. Data perhitungan kesetaraan larutan 2,6- diklorofenol indo
fenol ... 47
8. Perhitungan kadar vitamin C dari jus buah apel merah ... 48
9. Data hasil penetapan kadar vitamin C dari jus buah apel merah 51
10. Perhitungan statistik kadar vitamin C dari jus buah apel merah 53
11. Contoh perhitungan analisis perolehan kembali (recovery)
vitamin C dari jus buah apel merah (Malus domestica Borkh.) 61
12. Data hasil analisis perolehan kembali (recovery) vitamin C dari
jus buah apel merah (Malus domestica Borkh.) ... 63
13. Perhitungan kadar vitamin C dari jus buah apel hijau ... 65
14. Data hasil penetapan kadar vitamin C dari jus buah apel hijau 66
15. Perhitungan statistik kadar vitamin C dari jus buah apel hijau . 68
16. Contoh perhitungan analisis perolehan kembali (recovery)
vitamin C dari jus buah apel hijau ... 76
17. Data hasil analisis perolehan kembali (recovery) vitamin C dari
jus buah apel merah (Malus domestica Borkh.)... 78
PENETAPAN KADAR VITAMIN C DARI JUS BUAH APEL
(Malus domestica Borkh.) YANG BERWARNA MERAH DAN
HIJAU SECARA TITRASI DENGAN 2,6-DIKLOROFENOL
INDOFENOL PADA BEBERAPA INTERVAL WAKTU
ABSTRAK
Buah apel (Malus domestica Borkh.) merupakan salah satu buah yang sangat populer dan banyak dikonsumsi oleh masyarakat dalam bentuk minuman dengan cara diblender atau dibuat jus. Disamping warnanya yang menarik, buah apel bermanfaat untuk kesehatan karena memiliki kadar zat gizi yang tinggi. Penelitian ini bertujuan untuk mengetahui kadar vitamin C yang terkandung dalam jus buah apel merah dan hijau dan penurunan kadar vitamin C dalam jus apel merah dan jus apel hijau pada beberapa interval waktu yaitu 0 hingga 5 jam.
Sampel buah apel merah dan hijau yang digunakan, diperoleh dari Supermarket buah Palangkaraya. Penetapan kadar vitamin C yang terdapat dalam jus buah apel merah dan hijau dilakukan dengan metode volumetri dengan 2,6-diklorofenol indofenol, metode ini merupakan cara yang paling banyak digunakan untuk menentukan kadar vitamin C dalam bahan pangan karena larutan 2,6 -diklorofenol indofenol selektif terhadap vitamin C.
Hasil penelitian menunjukkan bahwa kadar vitamin C pada jus buah apel merah pada titik waktu 0 hingga 5 jam adalah 12,76 mg/100 g menjadi 1,35 mg/100 g. Sedangkan kadar vitamin C pada jus buah apel hijau pada titik waktu 0 hingga 5 jam adalah 16,49 mg/100 g menjadi 2,97 mg/100 g.
Hasil uji statistik SPSS (statistical package for the social science) menunjukkan adanya perbedaan kadar vitamin C pada jus buah apel merah dan hijau. Diperoleh perbedaan yang signifikan rata-rata penurunan kadar vitamin C dari jus buah apel dan hijau pada titik waktu 0 hingga 5 jam. Pada uji validasi metode diperoleh persen recovery pada jus buah apel merah sebesar 98,36% dengan simpangan baku relatif sebesar 0,80%, sedangkan persen recovery pada jus buah apel hijau sebesar 97,35% dengan simpangan baku relatif sebesar 0,01%.
DETERMINATION OF VITAMIN C FROM JUICE OF RED
AND GREEN APPLE (Malus domestica Borkh.) BY
VOLUMETRIC METHOD USING 2,6-DICLOROPHENOL
INDOPHENOL ON SEVERAL TIME INTERVALS
ABSTRACT
Apple (Malus domestica Borkh.) is one of the most popular fruit and most consumed by the society for drinking by blended or juiced. Beside of its interesting colour, apple also has good function for health because it contents high levels of nutrition. This research was intended to find out about the content of vitamin C in red and green apple juice and to find out about the decreasing of vitamin C level in red and green apple juice on several time intervals, which is 0 to 5 hours.
Red and greed apple samples were used, obtained from Palagkaraya Fruit Supermarket, Medan. The vitamin C content determination in juice of red and green apple (Malus domestica Borkh.) was done with volumetri method with 2,6-dichlorophenol indophenols. This method is the most used method in determining vitamin C content in food because the 2,6-dichlorophenol indophenols solution is selective to vitamin C.
The result of the research shows that the vitamin C content in red apple juice on 0 to 5 hours are 12.76 mg/100 g to 1.35 mg/100 g. Whereas the vitamin C content in green apple juice on 0 to 5 hours are 16.49 mg/100 g to 2.97 mg/100 g.
The results of statistical tests SPSS (statistical package for the social sciences) shows the differences in the levels of vitamin C in red and green apple juice. It is obtained the significant difference on average decreasing the levels of vitamin C in red and green apple juice on 0 to 5 hours. In the validation test method, the percent recovery of red apple juice was obtained 98.36% and relative standard deviation of 0.80%, whereas the percent recovery of green apple juice was obtained 97.35% and relative standard deviation of 0.01%.
BAB I PENDAHULUAN
1.1 Latar Belakang
Buah apel (Malus domestica Borkh.) merupakan salah satu buah yang
sangat populer dan banyak dikonsumsi oleh masyarakat dalam bentuk minuman
dengan cara diblender dan dibuat jus. Secara umum telah diketahui bahwa buah
apel bermanfaat untuk kesehatan karena memiliki kadar zat gizi yang tinggi
(Untung, 1996).
Berbagai jenis warna buah apel yang beredar di pasaran kota Medan antara
lain warna merah tua, merah jambu, dan hijau. Buah apel yang berwarna merah
memiliki rasa manis, sedangkan buah apel yang berwarna hijau memiliki rasa
yang lebih asam.
Kandungan gizi yang terdapat dalam 100 gram buah apel adalah
hidrat arang 14,9 gram, lemak 0,4 gram, protein 0,3 gram, kalsium 6 mg, fosfor
10 mg, besi 0,3 mg, vitamin A 90 SI, vitamin B1 0,04 mg, vitamin C 5 mg dan
kandungan airnya 84% (Arisandi dan Andriani, 2008).
Vitamin C bersifat mereduksi dan mudah terurai. Vitamin C mudah
teroksidasi menjadi asam dehidroaskorbat sehingga kadar vitamin C menjadi
berkurang (Andarwulan dan Koswara, 1992).
Masyarakat umumnya gemar meminum jus buah apel dan jus buah apel
banyak dijual dalam bentuk siap saji, sehingga masyarakat meminum jus buah
waktu tersebut, ada kemungkinan vitamin C yang terkandung dalam jus apel
mengalami perubahan terutama karena oksidasi.
Kadar vitamin C dapat ditentukan dengan beberapa metode seperti titrasi
iodimetri, titrasi 2,6-diklorofenol indofenol (Andarwulan dan Koswara, 1992;
Horwitz, 2002; Ditjen POM, 1995; Kumar, et. al., 2013) dan secara
spektrofotometri ultraviolet (Andarwulan dan Koswara, 1992).
Menurut Andarwulan dan Koswara (1992), metode iodimetri tidak efektif
untuk mengukur kandungan vitamin C dalam bahan pangan, karena adanya
komponen lain selain vitamin C yang juga bersifat pereduksi. Senyawa-senyawa
tersebut mempunyai warna titik akhir yang sama dengan warna titik akhir titrasi
vitamin C dengan iodin. Penelitian ini tidak dapat dilakukan dengan metode
spektrofotometri UV karena vitamin C tidak terdapat sebagai senyawa tunggal
dalam jus buah apel.
Berdasarkan uraian di atas, peneliti ingin mengetahui profil perubahan
kadar vitamin C setelah beberapa interval waktu pada pembuatan jus buah apel
merah dan jus buah apel hijau. Dalam penelitian ini digunakan metode volumetri
yaitu titrasi dengan larutan diklorofenol indofenol karena selain larutan
2,6-diklorofenol indofenol lebih selektif terhadap vitamin C, metode ini merupakan
cara yang paling banyak digunakan untuk menentukan kadar vitamin C dalam
bahan pangan (Andarwulan dan Koswara, 1992).
1.2 Perumusan Masalah
a. Berapakah kadar vitamin C yang terdapat pada jus buah apel (Malus
b. Apakah terdapat penurunan kadar vitamin C pada jus buah apel merah dan
pada jus buah apel hijau pada beberapa interval waktu.
c. Apakah ada perbedaan penurunan kadar vitamin C pada jus buah apel
merah dibanding pada jus buah apel hijau pada beberapa interval waktu.
1.3 Hipotesis
a. Terdapat kadar vitamin C dalam jumlah tertentu pada jus buah apel(Malus
domestica Borkh.) yang berwarna merah dan hijau.
b. Terdapat penurunan kadar vitamin C pada jus buah apel merah dan pada
jus buah apel hijau pada beberapa interval waktu.
c. Ada perbedaan penurunan kadar vitamin C pada jus buah apel merah
dibanding pada jus buah apel hijau pada beberapa interval waktu.
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah:
a. Untuk mengetahui kadar vitamin C jus buah apel (Malus domestica
Borkh.) yang berwarna merah dan hijau.
b. Untuk mengetahui adanya penurunan kadar vitamin C pada jus buah apel
merah dan pada jus buah apel hijau pada beberapa interval waktu.
c. Untuk mengetahui perbedaan penurunan kadar vitamin C pada jus buah
apel merah dibanding pada jus buah apel hijau pada beberapa interval
waktu.
1.5.1 Manfaat Penelitian
Manfaat penelitian ini dapat dijadikan sebagai sumber informasi tentang
penurunan kadar vitamin C dari jus buah apel merah dan jus buah apel hijau pada
BAB II
TINJAUAN PUSTAKA
2.1 Apel
Apel (Malus domestica Borkh.) termasuk rajanya buah komersial karena
konsumennya luar biasa banyaknya. Di Indonesia, apel diperkenalkan oleh orang
Belanda dan dikembangkan oleh orang Indonesia. Sayangnya daerah di Indonesia
yang cocok ditanami apel masih sangat terbatas. Daerah Batu, Malang, merupakan
sentra apel di Indonesia karena tanaman ini banyak diusahakan sebagai suatu
usaha tani. Oleh penduduk di Malang tanaman ini ditanam di pekarangan maupun
di kebun (Untung, 1996).
Menurut Untung (1996), dalam tatanama atau sistemik (taksonomi)
tumbuhan buah apel, diklasifikasikan sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Sub-divisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Rosales
Family : Rosaceae
Genus : Malus
Spesies : Malus domestica
Apel diketahui mengandung beberapa vitamin dan mineral yang
bermanfaat bagi manusia. Sebutir apel berdiameter 5-7 cm mengandung vitamin
protein 3 g, energi 58 kalori, lemak 4 g, karbohidrat 14,9 g, kalsium 6 mg, besi 3
mg, fosfor 10 mg, dan kalium 130 mg (Untung, 1996).
Dengan kandungan seperti itu ada orang berpendapat bahwa tingkat
keasaman yang rendah pada apel meningkatkan produksi air liur yang baik untuk
kesehatan gigi. Penelitian menunjukkan bahwa memakan apel sebutir sehari
memperkecil risiko terkena asma, arthritis, dan penyakit kulit (Untung, 1996).
Selain dimakan segar, apel bisa diolah menjadi jam (selai), jeli, dan sari
buah. Meski namanya olahan, tetapi bukan berarti yang dipakai apel busuk atau
cacat. Biasanya yang diolah apel berukuran kecil atau buah apel hasil
penjarangan. Kandungan pektin pada apel sekitar 24%. Pektin yang dapat
membentuk gel bila ditambah gula pada pH tertentu, memegang peranan penting
dalam industri jeli, sari buah, dan selai (Untung, 1996).
2.2 Ekologi dan Syarat Tumbuh Apel
Apel termasuk tanaman yang selalu berganti daun dan tumbuh di daerah
dingin. Kendati demikian, karena sudah lama dibudidayakan ada kultivar-kultivar
apel yang mampu tumbuh dan beradaptasi dengan baik di daerah bersuhu sedang
dan panas. Oleh karena kemampuannya beradaptasi di berbagai kondisi iklim,
apel tumbuh di berbagai penjuru dunia. Di Eropa, Amerika Utara dan Selatan,
New Zealand, Australia, dan Asia, tanaman ini dapat dijumpai (Untung, 1996).
Meskipun variasi kultivar apel membuat tanaman buah ini bisa ditanam di
berbagai penjuru dunia, tapi tempat tumbuh yang paling baik ialah di daerah yang
mempunyai dua musim, yakni musim dingin dan musim panas. Temperatur yang
buah akan membantu pembentukan pigmen antosianin. Pigmen antosianin adalah
pigmen yang membuat apel berwarna merah (Untung, 1996).
Di Indonesia apel tumbuh di dataran tinggi yang kering dan curah hujan
yang tidak terlalu tinggi. Curah hujan yang terlalu tinggi dapat menimbulkan
berbagai macam problem, terutama serangan jamur. Tanah, suhu, dan kelembaban
pun perlu mendapat perhatian agar apel dapat tumbuh dengan baik (Untung,
1996).
Kriteria tempat tumbuh pohon apel yang baik, antara lain:
1. Ketinggian tempat
Pada ketinggian 700 - 1.200 meter di atas permukaan laut memang tidak
banyak jenis tanaman buah yang dapat tumbuh dengan baik. Lebih-lebih jika
dataran tinggi itu tipe iklimnya kering. Namun, di daerah seperti itulah apel dapat
tumbuh dengan baik (Untung, 1996).
2. Suhu
Suhu maksimum yang dikehendaki apel ialah 270C dan suhu minimum
sekitar 160C. Kelembaban udara yang dikehendaki tanaman ini berkisar antara 75
- 85%. Selain suhu dan kelembaban, tempat tumbuh apel pun harus terbuka agar
sekitar 50 - 80% sinar matahari dapat menyinari pohon buah ini. Sinar matahari
sangat berperan dalam pertumbuhan apel. Tanpa sinar matahari yang cukup kulit
buah apel tidak akan berwarna merah sehingga daya tarik penampilannya
berkurang (Untung, 1996).
3. Curah hujan
Curah hujan yang diperlukan bagi pertumbuhan apel berkisar antara 1.000
kering ialah bulan-bulan yang curah hujannya kurang dari 60 mm per bulan
(Untung, 1996).
4. Tanah
Tanah ber-pH 7 dan berpengairan bagus merupakan tempat tumbuh paling
ideal bagi tanaman apel. Kendatipun demikian apel bisa beradaptasi di
tempat-tempat yang agak menyimpang dari persyaratan ideal tersebut. Pertumbuhan apel
akan baik sekali pada tanah dengan struktur bagus. Perbaikan struktur tanah dapat
dilakukan dengan pemberian bahan organik seperti kompos/pupuk kandang.
Semakin baik struktur tanah semakin bagus pula aerasi udara di antara rongga
partikel tanah sehingga semakin subur pula pertumbuhan tanaman. Pada aerasi
tanah yang jelek pengambilan unsur hara akan terhambat. Bahkan lebih fatal lagi,
akar-akar rambut bisa berhenti berkembang (Untung, 1996).
2.3 Vitamin
Vitamin merupakan suatu senyawa organik yang sangat diperlukan tubuh
untuk proses metabolisme dan pertumbuhan yang normal. Vitamin-vitamin tidak
dapat dibuat oleh tubuh manusia dalam jumlah yang cukup, oleh karena itu harus
diperoleh dari bahan pangan yang dikonsumsi. Sebagai perkecualian adalah
vitamin D, yang dapat dibuat dalam kulit asalkan kulit mendapat cukup
kesempatan kena sinar matahari (Winarno, 1980; Andarwulan dan Koswara,
1992).
Vitamin adalah senyawa-senyawa organik yang dibutuhkan untuk
pertumbuhan normal dan mempertahankan hidup hewan, termasuk manusia yang
proses anabolisme. Senyawa-senyawa tersebut diperlukan dan efektif dalam
jumlah sedikit, tidak menghasilkan energi dan tidak digunakan sebagai unit
pembangun struktur tubuh organisme, tetapi sangat penting untuk tranformasi
energi dan pengaturan metabolisme tubuh (Andarwulan dan Koswara, 1992).
Vitamin dapat dibedakan menjadi dua golongan yaitu vitamin yang dapat
larut dalam air dan vitamin yang dapat larut dalam lemak. Jenis vitamin yang larut
dalam air adalah vitamin B kompleks dan vitamin C. Vitamin yang dapat larut
dalam lemak adalah vitamin A, D, E, dan K, serta provitamin A yaitu ß-karoten.
Bahan makanan yang kaya akan vitamin adalah sayur-sayuran dan buah-buahan
(Sudarmadji., dkk, 1989).
2.3.1 Vitamin C
Vitamin C atau asam askorbat mempunyai berat molekul 176,13 dengan
rumus molekul C6H8O6. Vitamin C dalam bentuk murni merupakan kristal putih,
tidak berwarna, tidak berbau dan mencair pada suhu 190 - 192°C. Senyawa ini
bersifat reduktor kuat dan mempunyai rasa asam. Sifat-sifat tersebut terutama
disebabkan adanya struktur enediol yang berkonyugasi dengan gugus karbonil
dalam cincin lakton. Bentuk vitamin C yang ada di alam terutama adalah L-asam
askorbat. Biasanya D-asam askorbat ditambah ke dalam bahan pangan sebagai
antioksidan, bukan sebagai sumber vitamin C (Andarwulan dan Koswara, 1992;
Tjokonegoro, 1985).
Vitamin C mudah larut dalam air (1g dapat larut sempurna dalam 3 ml
air), sedikit larut dalam alkohol (1 g larut dalam 50 ml alkohol absolut atau 100
ml gliserin) dan tidak larut dalam benzena, eter, kloroform, minyak dan
udara, logam-logam seperti Cu, Fe, dan cahaya (Andarwulan dan Koswara, 1992;
Tjokonegoro, 1985).
Rumus bangun vitamin C dapat dilihat pada gambar di bawah ini (Ditjen
POM, 1995):
Gambar 2.1 Rumus bangun vitamin C
Vitamin C, suatu zat gizi yang luar biasa, telah dikenal sebagai suatu
senyawa utama tubuh yang dibutuhkan dalam berbagai proses penting, mulai dari
pembuatan kolagen, karnitin pengangkut lemak, hormon adrenalin dan kortison,
pengangkut elektron dalam berbagai reaksi enzimatik, pelindung integritas
pembuluh darah, pemacu gusi yang sehat, pelindung radiasi, pengatur tingkat
kolesterol, pendetoksifikasi radikal bebas, senyawa antibakteria dan antivirus,
serta pemacu imunitas (Goodman, 2000; Khomsan, 2002).
Vitamin C juga dikenal sebagai senyawa ampuh untuk menangkal radikal
bebas. Beberapa di antara radikal bebas itu bersifat toksik dan sangat reaktif.
Untuk mengganti elektron yang hilang, radikal bebas melakukan serangkaian
reaksi kimia yang menyebabkan kerusakan pada membran sel, mutasi DNA,
mempercepat penuaan, dan penyebab penumpukan lemak. Pemakaian vitamin C
sebagai salah satu antioksidan alami secara luas dianjurkan dalam mengobati dan
Vitamin C (asam askorbat) bersifat sangat sensitif terhadap pengaruh-
pengaruh luar yang menyebabkan kerusakan seperti suhu, oksigen, enzim, kadar
air, dan katalisator logam. Asam askorbat sangat mudah teroksidasi menjadi asam
dehidroaskorbat yang masih mempunyai keaktifan sebagai vitamin C. Asam
dehidroaskorbat secara kimia sangat labil dan dapat mengalami perubahan lebih
lanjut menjadi asam diketogulonat yang tidak memiliki keaktifan vitamin C lagi
(Andarwulan dan Koswara, 1992).
Asam askorbat Asam dehidro Asam diketogulonat Asam
askorbat oksalat
Gambar 2.2 Reaksi Perubahan Vitamin C (Silalahi, 1985).
Asam askorbat bersifat sangat larut dalam air, akibatnya sangat mudah
hilang akibat luka di permukaan atau pada waktu pemotongan bahan pangan.
Dalam processed food, kehilangan terbanyak terjadi akibat degredasi kimiawi.
Dalam bahan pangan yang kaya akan vitamin C seperti produk buah-buahan,
kehilangan vitamin C ada kaitannya dengan reaksi kecokelatan non-enzimatik
(Andarwulan dan Koswara, 1992).
Stabilitas asam askorbat biasanya meningkat dengan penurunan suhu
penyimpanan akan tetapi selama pembekuan terjadi kerusakan yang cukup besar.
penyimpanan dibawah -180C dapat menyebabkan kerusakan yang cukup berarti
(Andarwulan dan Koswara, 1992).
Vitamin C dapat ditemukan di alam hampir pada semua tumbuhan
terutama sayuran dan buah-buahan, terutama buah-buahan segar. Karena itu
sering disebut Fresh Food Vitamin (Budiyanto, 2004; Goodman, 2000).
Jumlah vitamin C yang terkandung dalam tanaman tergantung pada
varietas dari tanaman, pengolahan, suhu, masa pemanenan dan tempat tumbuh
(Counsell dan Hornig, 1981).
2.3.2 Fungsi Vitamin C
Fungsi vitamin C di dalam tubuh bersangkutan dengan dengan sifat
alamiahnya sebagai antioksidan yang berperan serta di dalam banyak proses
metabolisme yang berlangsung di dalam jaringan tubuh, antioksidan adalah
senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya
dengan cuma-cuma kepada molekul radikal bebas tanpa terganggu sama sekali
dan dapat memutus reaksi berantai dan radikal bebas (Sediaoetama, 2008).
Salah satu fungsi utama vitamin C berkaitan dengan sintesis kolagen.
Kolagen adalah sejenis protein yang merupakan salah satu komponen utama dari
jaringan ikat, tulang, gigi, pembuluh darah dan mempercepat proses penyembuhan
(Sediaoetama, 2008).
Kekurangan asupan vitamin C dapat menyebabkan penyakit sariawan atau
skorbut. Bila terjadi pada anak (6 - 12 bulan), gejala-gejala penyakit skorbut ialah
terjadinya pelembekan tenunan kolagen, infeksi, dan demam. Pada anak yang
giginya telah keluar, gusi membengkak, empuk dan terjadi pendarahan. Pada
vitamin C dalam makanannya. Gejalanya ialah pembengkakan dan perdarahan
pada gusi, luka lambat sembuh sehingga mudah berdarah dan mengalami infeksi
berulang. Akibat yang parah dari keadaan ini ialah gigi menjadi goyah dan dapat
lepas (Winarno, 2002).
Vitamin C dapat terserap sangat cepat dari alat pencernaan masuk ke
dalam saluran darah dan dibagikan ke seluruh jaringan tubuh. Pada umumnya
tubuh menahan vitamin C sangat sedikit. Kelebihan vitamin C dibuang melalui air
kemih. Karena itu bila seseorang mengkonsumsi vitamin C dalam jumlah besar
(megadose), sebagian besar akan dibuang keluar, terutama bila orang tersebut
biasa mengkonsumsi makanan yang bergizi tinggi (Winarno, 2002).
Menurut Silalahi (2006), apabila akan mengkonsumsi suplemen vitamin C
maka tidak boleh lebih dari 2000 mg per hari, meskipun vitamin C akan dibuang
melalui urin, vitamin C dalam dosis tinggi dapat menyebabkan sakit kepala,
peningkatan jumlah urin, diare dan mual. Bagi seseorang dengan kecenderungan
pembetukan batu ginjal, diharapkan untuk tidak mengkonsumsi vitamin C dalam
dosis tinggi.
Kebutuhan harian vitamin C bagi orang dewasa adalah sekitar 60 mg,
untuk wanita hamil 95 mg, anak-anak 45 mg, dan bayi 35 mg, namun karena
banyaknya polusi di lingkungan antara lain oleh adanya asap-asap kendaraan
bermotor dan asap rokok maka penggunaan vitamin C perlu ditingkatkan hingga
2.4 Metode Penetapan Kadar Vitamin C
Ada beberapa metode dalam penentuan kadar vitamin C yaitu:
a. Metode titrasi iodimetri
Iodium akan mengoksidasi senyawa-senyawa yang mempunyai potensial
reduksi yang lebih kecil dibandingkan iodium, dimana dalam hal ini potesial
reduksi iodum +0,535 volt, karena vitamin C mempunyai potensial reduksi yang
lebih kecil (+0,116 volt) dibandingkan iodium sehingga dapat dilakukan titrasi
langsung dengan iodium (Andarwulan dan Koswara, 1992; Sudjadi dan Rohman,
2008).
Deteksi titik akhir titrasi pada iodimetri ini dilakukan dengan
menggunakan indikator amilum yang akan memberikan warna biru kehitaman
pada saat tercapainya titik akhir titrasi (Sudjadi dan Rohman, 2008).
Metode ini dapat juga digunakan untuk pemeriksaan harian terhadap
sediaan vitamin C yang tidak mengandung senyawa mereduksi lainnya (Watson,
2010). Larutan baku lain yang dapat digunakan berdasarkan sifat mereduksi asam
askorbat adalah serium (IV) ammonium sulfat atau kalium iodat (Sudjadi dan
Rohman, 2008).
Kandungan vitamin C dalam larutan murni dapat ditentukan secara titrasi
menggunakan larutan 0,01 N iodin. Menurut Andarwulan dan Koswara (1992),
metode iodimetri tidak efektif untuk mengukur kandungan vitamin C dalam bahan
pangan, karena adanya komponen lain selain vitamin C yang juga bersifat
pereduksi. Senyawa-senyawa tersebut mempunyai titik akhir yang sama dengan
Gambar 2.3 Reaksi antara vitamin C dan iodin (Sudjadi dan Rohman, 2008). b. Metode titrasi 2,6-diklorofenol indofenol
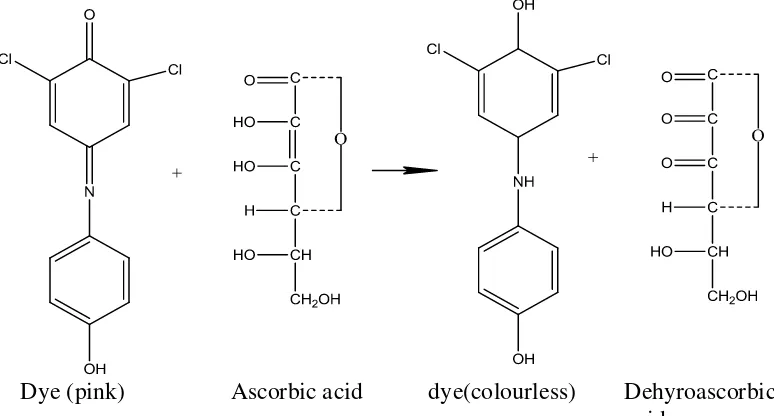
Metode 2,6-diklorofenol indofenol (DCIP) ini berdasarkan atas sifat
mereduksi asam askorbat terhadap zat warna 2,6-diklorofenol indofenol. Asam
askorbat akan mereduksi indikator warna 2,6-diklorofenol indofenol membentuk
larutan yang tidak berwarna. Pada titik akhir titrasi, kelebihan zat warna yang
tidak tereduksi akan berwarna merah muda dalam larutan asam (Sudjadi dan
Rohman, 2008).
Larutan 2,6-diklorofenol indofenol dalam suasana netral atau basa akan
berwarna biru sedangkan dalam suasana asam akan berwarna merah muda.
Apabila 2,6-diklorofenol indofenol direduksi oleh asam askorbat maka akan
menjadi tidak berwarna, dan bila semua asam askorbat sudah mereduksi 2,6
-diklorofenol indofenol maka kelebihan larutan 2,6--diklorofenol indofenol sedikit
saja sudah akan terlihat terjadinya warna merah muda (Sudarmadji., dkk, 1989).
Titrasi vitamin C harus dilakukan dengan cepat karena banyak faktor yang
menyebabkan oksidasi vitamin C misalnya pada saat penyiapan sampel atau
penggilingan. Oksidasi ini dapat dicegah dengan menggunakan asam metafosfat,
asam asetat, asam trikloroasetat, dan asam oksalat. Penggunaan asam-asam di atas
yang terdapat dalam jaringan tanaman. Selain itu, larutan asam metafosfat–asetat
juga berguna untuk pangan yang mengandung protein karena asam metafosfat
dapat memisahkan vitamin C yang terikat dengan protein. Suasana larutan yang
asam akan memberikan hasil yang lebih akurat dibandingkan dalam suasana netral
atau basa (Andarwulan dan Koswara, 1992; Counsell dan Hornig, 1981).
Metode ini pada saat sekarang merupakan cara yang paling banyak
digunakan untuk menentukan kadar vitamin C dalam bahan pangan. Metode ini
lebih baik dibandingkan metode iodimetri karena zat pereduksi lain tidak
mengganggu penetapan kadar vitamin C. Reaksinya berjalan kuantitatif dan
praktis spesifik untuk larutan asam askorbat pada pH 1 - 3,5. Untuk perhitungan
maka perlu dilakukan standarisasi larutan 2,6-diklorofenol indofenol dengan
vitamin C standar (Andarwulan dan Koswara, 1992; Sudarmadji., dkk, 1989).
[image:31.595.121.508.418.626.2]Dye (pink) Ascorbic acid dye(colourless) Dehyroascorbic acid
Gambar 2.4 Reaksi asam askorbat dengan 2,6-diklorofenol indofenol c. Metode Spektrofotometri Ultraviolet
` Metode ini berdasarkan kemampuan vitamin C yang terlarut dalam air
265 nm dan A11= 556a. Oleh karena vitamin C dalam larutan mudah sekali
mengalami kerusakan, maka pengukuran dengan cara ini harus dilakukan secepat
mungkin. Untuk memperbaiki hasil pengukuran, sebaiknya ditambahkan senyawa
pereduksi yang lebih kuat daripada vitamin C. Hasil terbaik diperoleh dengan
menambahkan larutan KCN (sebagai stabilisator) ke dalam larutan vitamin
(Andarwulan dan Koswara, 1992).
2.5 Analisis Kembali Kadar Vitamin C yang Ditambahkan pada Sampel (Analisis Recovery)
Akurasi adalah ukuran yang menunjukkan kedekatan hasil analisis dengan
kadar analit yang sebenarnya. Akurasi dinyatakan sebagai persen perolehan
kembali (% recovery) analit yang ditambahkan (Harmita, 2004).
Kecermatan (recovery) ditentukan dengan dua cara yaitu metode simulasi
(Spiked – placebo recovery) dan metode penambahan baku (Standard addition
method). Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke
dalam campuran bahan pembawa sediaan farmasi (plasebo) lalu campuran
tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang
ditambahkan (kadar analit sebenarnya). Dalam metode penambahan baku
dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada
sampel yang diperiksa, lalu dianalisis dengan metode tersebut. Persen perolehan
kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan
tadi dapat ditemukan (Harmita, 2004).
Menurut Harmita 92004), rumus perhitungan persen recovery:
% Recovery =
C B A
Keterangan: A = Kadar vitamin C sebelum penambahan baku vitamin C B = Kadar vitamin C setelah penambahan baku vitamin C C = Kadar vitamin C baku yang ditambahkan
2.6 Analisis Data Secara Statistik
2.6.1 Penolakan Hasil Pengamatan (Rejection of Measurement)
Di antara hasil yang diperoleh dari satu seri penetapan kadar terhadap satu
macam sampel, adakalanya terdapat hasil yang sangat menyimpang bila
dibandingkan dengan yang lain tanpa diketahui kesalahannya secara pasti
sehingga timbul kecenderungan untuk menolak hasil yang sangat menyimpang
(Sudjadi dan Rohman, 2008).
Untuk memastikan hasil yang sangat menyimpang ditolak atau diterima,
perlu dilakukan analisis data secara statistika. Pada taraf kepercayaan 95% (α =
0,05), hasil analisis ditolak jika Qhitung > Qtabel (Sudjadi dan Rohman, 2008).
2.6.2 Uji Ketelitian (Presisi) Metode Analisis
Uji presisi (keseksamaan) adalah ukuran yang menunjukkan derajat
kesesuaian antara hasil uji individual yang diterapkan secara berulang pada
sampel. Keseksamaan diukur sebagai simpangan baku relatif (Relative Standard
Deviation) atau koefisien variasi (Harmita, 2004).
Menurut Harmita (2004), rumus perhitungan persen RSD:
% RSD =
X SD
x 100%
Keterangan: SD = standar deviasi
X = kadar rata-rata sampel
Data hasil perhitungan koefisien variasi (%RSD) dapat dilihat pada
2.6.3 Pengujian Beda Nilai Rata-Rata
Untuk mengetahui apakah kadar vitamin C berbeda pada tiap sampel,
maka dilakukan uji beda rata-rata kadar sampel yang diuji dengan uji F
menggunakan software SPSS. Data berbeda secara signifikan jika Fhitung > Ftabel
dan data tidak berbeda secara signifikan jika Fhitung < Ftabel. Jika data yang
BAB III
METODE PENELITIAN
Penelitian ini merupakan penelitian deskriptif. Penelitian ini bertujuan
untuk mengetahui penurunan kadar vitamin C dari jus buah apel merah dan jus
buah apel hijau secara volumetric dengan 2,6-diklorofenol indofenol pada
beberapa interval waktu.
3.1 Waktu dan tempat penelitian
Penelitian dilakukan di Laboratorium Kimia Farmasi Kualitatif Fakultas
Farmasi Universitas Sumatera Utara pada bulan November 2014 – Januari 2015.
3.2 Bahan dan Alat 3.2.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah mikroburet 10 mL,
neraca analitik, pisau (Stainless), juicer, kertas saring, statif dan klem, eksikator,
maat pipet 10 mL, pipet volum 1 mL, pipet volum 2 mL, pipet volum 5 mL, botol
timbang, dan alat-alat gelas laboratorium.
3.2.2 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini jika tidak dinyatakan
lain adalah bahan yang berkualitas pro analisis dari E.Merck yaitu
2,6-diklorofenol indofenol, asam metafosfat, asam asetat glasial, natrium bikarbonat,
akuades (PT. Rudang) dan asam askorbat Baku Pembanding Farmakope Indonesia
3.3 Pengambilan Sampel
Metode pengambilan sampel yang digunakan adalah sampling purposif
yaitu sampel dipilih dengan pertimbangan sesuai dengan tujuan (purpose)
penelitian, dimana sampel yang terambil dianggap dapat mewakili sampel yang
tidak terambil. Sampel yang digunakan dalam penelitian ini adalah buah apel
merah dan buah apel hijau yang diperoleh dari Supermarket Buah Palangkaraya
(Palangkaraya Fruit) Medan, Sumatera Utara. Gambar sampel yang digunakan
dapat dilihat pada Lampiran 1, halaman 41.
3.4 Prosedur Penelitian 3.4.1 Pembuatan Pereaksi
Pembuatan pereaksi berdasarkan Farmakope Indonesia Edisi IV:
3.4.1.1 Larutan 2,6-diklorofenol indofenol 0,025% b/v
Ditimbang seksama 50 mg natrium 2,6-diklorofenol indofenol P yang
telah disimpan dalam eksikator, ditambahkan 50 mL larutan NaHCO3, dikocok
kuat, dan jika sudah terlarut, ditambahkan air hingga 200 mL. Disaring ke dalam
botol bersumbat kaca berwarna coklat (Ditjen POM, 1995).
3.4.1.2Larutan asam metafosfat-asetat LP
Dilarutkan 15 g asam metafosfat P dalam 40 mL asam asetat glasial P dan
diencerkan dengan air secukupnya hingga 500 mL. Disimpan di tempat dingin,
hanya boleh digunakan dalam jangka waktu 2 hari (Ditjen POM, 1995).
3.4.1.3Larutan NaHCO3 0,084% b/v
3.4.2 Perhitungan Kesetaraan Larutan Pentiter 2,6-Diklorofenol Indofenol
Ditimbang seksama 50 mg asam askorbat BPFI, dipindahkan ke dalam
labu tentukur 100 mL, kemudian dilarutkan dengan larutan asam metafosfat-asetat
LP, dicukupkan sampai garis tanda. Dipipet 1 mL, dimasukkan kedalam
erlenmeyer dan ditambahkan larutan asam metafosfat-asetat 6 mL. Dititrasi segera
dengan larutan 2,6-diklorofenol indofenol hingga warna merah muda mantap
tidak kurang dari 5 detik. Dilakukan titrasi blanko menggunakan 7 mL asam
metafosfat-asetat dan dititrasi dengan larutan 2,6-diklorofenol indofenol hingga
warna merah muda mantap. Kadar larutan baku 2,6-diklorofenol indofenol
dinyatakan dengan kesetaraan dalam mg asam askorbat (Ditjen POM, 1995;
Sudjadi dan Rohman, 2008).
Menurut Ditjen POM (1995), perhitungan kesetaraan dilakukan dengan
rumus :
Kesetaraan (mg) = %
−
Keterangan:
Va = Volume aliquot (mL)
W = Berat vitamin C (mg)
Vt = Volume titrasi (mL)
Vb = Volume blanko (mL)
Vc = Volume labu tentukur (mL)
Contoh perhitungan dan hasil perhitungan dapat dilihat pada Lampiran 7, halaman
47.
3.4.3 Penyiapan Larutan Sampel
Sampel dicuci dan dibersihkan, ditimbang sekitar 500 g lalu dipotong
menjadi beberapa potongan dan dimasukkan ke dalam juicer, jus yang diperoleh
100 mL, pada titik 0 jam, 1 jam, 2 jam, 3 jam, 4 jam, 5 jam masing-masing segera
ditambahkan asam metafosfat-asetat sampai garis tanda, dihomogenkan,
kemudian disaring, filtrat pertama dibuang ± 20 mL.
3.4.4 Penetapan Kadar Vitamin C dari Larutan Sampel
Dipipet 2 mL larutan sampel lalu dimasukkan ke dalam erlenmeyer
kemudian ditambah 5 mL asam metafosfat-asetat. Dititrasi dengan larutan
2,6-diklorofenol indofenol sampai terbentuk warna merah muda yang mantap sebagai
titik akhir titrasi. Dilakukan penetapan blanko (Ditjen POM, 1995; Sudjadi dan
Rohman, 2008).
Dilakukan penetapan kadar vitamin C dalam jus buah apel merah dan jus
buah apel hijau pada beberapa interval waktu setelah jus diproses, antara lain pada
0 jam, 1 jam, 2 jam, 3 jam, 4 jam, 5 jam, hingga diperoleh profil penurunan kadar
vitamin C dari jus buah apel merah dan jus buah apel hijau. Kemudian
dibandingkan profil penurunan kadar vitamin C pada jus buah apel merah dan jus
buah apel hijau.
Menurut Horwitz (2002), kadar vitamin C dapat dihitung dengan rumus :
Kadar vitamin C (mg/g) = − K n
p
Keterangan:
Vt = Volume titrasi (mL)
Vb = Volume blanko (mL)
Vl = Volume labu tentukur (mL)
Vp = Volume pemipetan (mL)
Bs = Berat sampel (g)
Contoh perhitungan dapat dilihat pada Lampiran 8, halaman 50 (untuk sampel jus
3.4.5 Validasi
3.4.5.1 Uji Perolehan Kembali (Recovery)
Akurasi adalah ukuran yang menunjukkan kedekatan hasil analisis dengan
kadar analit yang sebenarnya. Akurasi dinyatakan sebagai persen perolehan
kembali (% recovery) analit yang ditambahkan (Harmita, 2004).
Dalam hal ini digunakan metode standar adisi. Metode adisi dapat
dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada
sampel yang diperiksa, lalu dianalisis dengan metode tersebut. Persen perolehan
kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan
tadi dapat ditemukan (Harmita, 2004).
Prosedur uji perolehan kembali (recovery) dengan metode adisi dilakukan
sebagai berikut: Dikerjakan dengan prosedur yang sama seperti penetapan kadar
vitamin C dalam sampel dengan penambahan vitamin C baku yaitu 2,0 mg dengan
cara sebanyak 20 mg vitamin C baku dimasukkan kedalam labu tentukur 100 mL
(konsentrasi 0,20 mg/mL), lalu dipipet sebanyak 10 mL yang ditambahkan pada
sampel yang ditimbang seksama dan dilakukan enam kali perulangan.
Menurut Harmita (2004), rumus perhitungan persen recovery:
% Recovery = −
x 100%
Keterangan :
A = Kadar vitamin C sebelum penambahan baku vitamin C B = Kadar vitamin C setelah penambahan baku vitamin C C = Kadar vitamin C baku yang ditambahkan
Data hasil analisis perolehan kembali (persen recovery) dapat dilihat pada
Lampiran 11, halaman 61 (untuk sampel jus apel merah) dan Lampiran 16,
3.4.5.2 Uji Ketelitian (Presisi) Metode Analisis
Uji presisi adalah ukuran yang menunjukkan derajat kesesuaian antara
hasil uji individual yang diterapkan secara berulang pada sampel. Ketelitian
diukur sebagai simpangan baku relatif (Relative Standard Deviation) atau
koefisien variasi (Harmita, 2004).
Rumus perhitungan persen simpangan baku relatif (RSD):
% RSD =
X SD
x 100%
Keterangan:
SD = standar deviasi
X = kadar rata-rata sampel
Sementara itu, nilai simpangan baku dihitung dengan menggunakan rumus:
SD =
1 -n
X
-Xi 2
Data hasil perhitungan koefisien variasi (%RSD) dapat dilihat pada
Lampiran 12, halaman 63 (untuk sampel jus apel merah) dan Lampiran 17,
halaman 78 (untuk sampel jus apel hijau).
3.4.6 Analisis Data Secara Statistik 3.4.6.1 Penolakan Hasil Pengamatan
Di antara hasil yang diperoleh dari satu seri penetapan kadar terhadap satu
macam sampel, ada kalanya terdapat hasil yang sangat menyimpang bila
dibandingkan dengan yang lain tanpa diketahui kesalahannya secara pasti
sehingga timbul kecenderungan untuk menolak hasil yang sangat menyimpang
Untuk memastikan hasil yang sangat menyimpang ditolak atau diterima,
perlu dilakukan analisis data secara statistika. Pada taraf kepercayaan 95%
(α=0,05), hasil analisis ditolak jika Qhitung > Qtabel (Sudjadi dan Rohman, 2008).
Untuk menghitung nilai Q digunakan rumus:
Qhitung =
N n −N n
N n −N n
Hasil pengujian atau nilai Q yang diperoleh ditinjau terhadap daftar harga Q
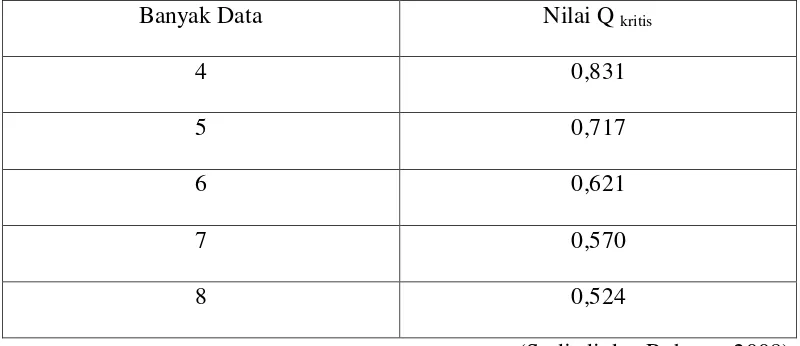
[image:41.595.112.512.339.512.2]pada Tabel 1, apabila Q hitung > Q kritis maka data tersebut ditolak.
Tabel 1. Nilai Qkritis pada taraf kepercayaan 95%
Banyak Data Nilai Q kritis
4 0,831
5 0,717
6 0,621
7 0,570
8 0,524
(Sudjadi dan Rohman,2008).
Wibisono (2005), untuk menentukan kadar vitamin C di dalam sampel
dengan taraf kepercayaan 95%, α = 0.05, dk = n-1, dapat digunakan rumus:
Keterangan:
µ = Interval kepercayaan
X = Kadar rata-rata sampel
t = Harga t tabel sesuai dengan dk = n-1
α = Tingkat kepercayaan
SD = Standar deviasi
n = Jumlah pengulangan
n
SD
x
t
3.4.6.2 Pengujian Beda Nilai Rata-rata
Untuk mengetahui apakah kadar vitamin C berbeda pada tiap sampel,
maka dilakukan uji beda rata-rata sampel yang diuji dengan uji F menggunakan
software SPSS. Data berbeda secara signifikan jika Fhitung > Ftabel dan data tidak
berbeda secara signifikan jika Fhitung < Ftabel. Jika data yang diperoleh berbeda
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan oleh Lembaga Ilmu
Pengetahuan Indonesia Pusat Penelitian Biologi Bogor adalah buah apel merah
(Malus domestica Borkh.) dan buah apel hijau (Malus domestica Borkh.). Hasil
identifikasi tumbuhan dapat dilihat pada Lampiran 1, halaman 41.
4.2 Hasil Penetapan Kadar Vitamin C dari Jus Buah Apel Merah dan Jus Buah Apel Hijau pada Beberapa Interval Waktu
Pengerjaan sampel dilakukan dengan cara penyimpanan pada suhu ruang
(270C) pada interval waktu 0 hingga 5 jam. Penetapan kadar vitamin C dilakukan
secara titrasi volumetri dengan 2,6-diklorofenol indofenol.
Data volume titrasi pada penetapan kadar vitamin C dari jus buah apel
merah pada interval waktu 0 hingga 5 jam dapat dilihat pada Lampiran 9, halaman
51. Sedangkan data volume titrasi pada penetapan kadar vitamin C dari jus buah
apel hijau pada interval waktu 0 hingga 5 jam dapat dilihat pada Lampiran 15,
halaman 66. Contoh perhitungan kadar vitamin C dari jus buah apel hijau dapat
dilihat pada Lampiran 13, halaman 65.
Hasil penetapan kadar vitamin C dari jus buah apel merah dan jus buah
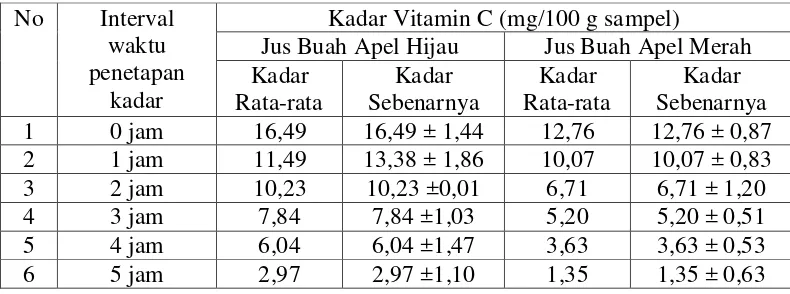
Tabel 4.1 Hasil penetapan kadar vitamin C dari jus buah apel merah dan jus buah apel hijau pada interval waktu 0 hingga 5 jam.
No Interval
waktu penetapan
kadar
Kadar Vitamin C (mg/100 g sampel)
Jus Buah Apel Hijau Jus Buah Apel Merah
Kadar Rata-rata
Kadar Sebenarnya
Kadar Rata-rata
Kadar Sebenarnya
1 0 jam 16,49 16,49 ± 1,44 12,76 12,76 ± 0,87
2 1 jam 11,49 13,38 ± 1,86 10,07 10,07 ± 0,83
3 2 jam 10,23 10,23 ±0,01 6,71 6,71 ± 1,20
4 3 jam 7,84 7,84 ±1,03 5,20 5,20 ± 0,51
5 4 jam 6,04 6,04 ±1,47 3,63 3,63 ± 0,53
6 5 jam 2,97 2,97 ±1,10 1,35 1,35 ± 0,63
Hasil penetapan kadar vitamin C dari jus buah apel merah dan jus buah
apel hijau pada interval waktu 0 hingga 5 jam menunjukkan penurunan kadar
kandungan vitamin C dari kedua jenis sampel yang dianalisis. Kandungan vitamin
C terbesar terdapat pada jus buah apel hijau pada 0 jam yaitu 16,49 ± 1,44 mg/100
g. Dimana kadar kandungan vitamin C-nya mengalami penurunan signifikan
hingga 2,97 ± 1,10 mg/100 g pada 5 jam. Sedangkan kadar kandungan vitamin C
pada jus buah apel merah lebih sedikit dibandingkan pada jus buah apel hijau,
yaitu 12,76 ± 0,87 mg/100 g pada 0 jam, dan juga mengalami penurunan yang
signifikan hingga 1,35 ± 0,63 mg/100 g pada 5 jam.
Menurut Safaryani, dkk., (2007), kerusakan jaringan tersebut
menyebabkan jaringan-jaringan mudah terpengaruh oleh udara, sehingga
memungkinkan vitamin C rusak karena teroksidasi menjadi asam dehidroaskorbat.
Umumnya kehilangan vitamin C terjadi bila jaringan rusak dan terkena udara.
Dari data yang diperoleh terlihat bahwa bertambahnya selang waktu dari
pembuatan jus maka bertambah juga penurunan kadar vitamin C, karena semakin
sehingga dapat dikatakan faktor lamanya jus terpapar dengan udara akan
mempengaruhi penurunan kadar vitamin C.
Hasil analisis kemudian dilanjutkan dengan pengujian beda nilai rata-rata
antar jus buah apel merah dan jus buah apel hijau, yaitu uji F dengan taraf
kepercayaan 95% untuk mengetahui apakah variasi antar populasi sama atau
berbeda menggunakan software SPSS.
Tabel 4.2 Hasil uji F kadar vitamin C jus buah apel (Malus domestica Borkh.) yang berwarna merah dan hijau
Jumlah Kuadrat
df Rata-rata
Kuadrat
F Sig.
Jus Buah apel Merah Antar Kelompok Dalam Kelompok Total 530.035 19.241 549.275 5 30 35 106.007 .641
165.287 .000
Jus Buah apel Hijau Antar Kelompok Dalam Kelompok Total 731.197 49.983 781.180 5 30 35 146.239 1.666
87.773 .000
Uji F yaitu uji untuk melihat bagaimana pengaruh semua variabel secara
bersama-sama terhadap variabel berikutnya, atau untuk menguji apakah regresi
yang diperoleh signifikan atau non signifikan. Uji F dapat dilakukan dengan
membandingkan Fhitung dengan Ftabel, jika Fhitung > Ftabel, maka signifikan, jika
Fhitung < Ftabel maka non signifikan.
Dari Tabel 4.2 diperoleh Fhitung untuk jus buah apel merah sebesar
165,287 dan Fhitung untuk jus buah apel hijau sebesar 146,239, sedangkan Ftabel
sebesar 2,53 dimana Fhitung > Ftabel. Hal ini menunjukkan bahwa kadar vitamin C
antara jus buah apel merah dan hijau berbeda secara statistik, maka dilanjutkan
4.3 Profil Penurunan Kadar Vitamin C pada Jus Buah Apel yang Berwarna Merah dan Hijau pada Berberapa Interval Waktu (0 hingga 5 jam)
Semua bahan pangan yang diolah akan mengalami derajat kehilangan
vitamin tertentu (tergantung cara pengolahannya). Pengolahan pangan yang baik
adalah pengolahan pangan yang dapat meminimumkan kehilangan zat gizi dan
menghasilkan produk yang yang aman dikonsumsi. Disamping proses
pengolahan, kondisi-kondisi sebelum pengolahan juga dapat mempengaruhi
kandungan zat-zat gizi (Andarwulan dan Koswara, 1992). Pada penetapan kadar
vitamin C dari jus buah apel merah dan jus buah apel hijau ini, penyiapan larutan
sampel melewati beberapa tahap pengolahan seperti pemotongan dan proses pada
juicer yang memakan waktu kurang lebih 10 menit sehingga hal ini
[image:46.595.113.487.408.628.2]memungkinkan terjadinya penurunan kadar vitamin C dari sampel.
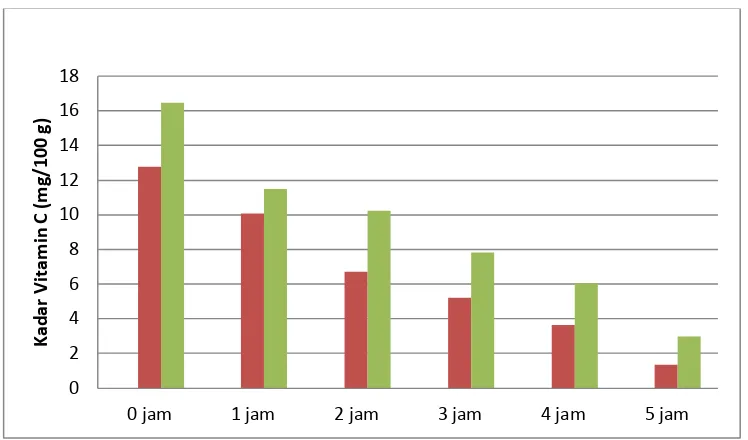
Gambar 4.1 Perbandingan penurunan kadar vitamin C dari jus buah apel merah dan hijau pada interval watu 0 hingga 5 jam
Keterangan:
: Jus buah apel merah : Jus buah apel hijau
0 2 4 6 8 10 12 14 16 18
0 jam 1 jam 2 jam 3 jam 4 jam 5 jam
Grafik regresi untuk hasil penurunan kadar vitamin C dari jus apel merah dan
[image:47.595.114.477.137.322.2]jus apel hijau dapat dilihat pada gambar di bawah ini:
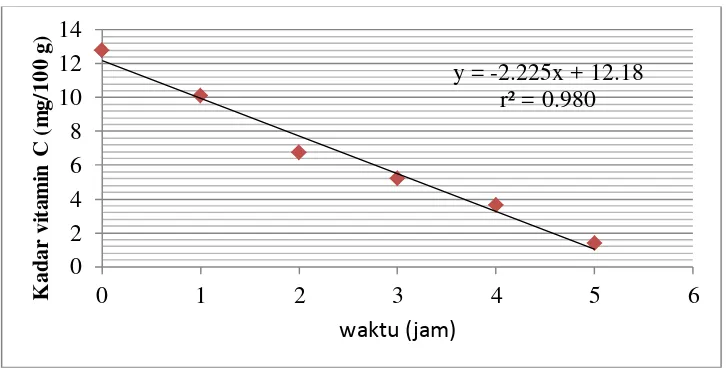
[image:47.595.113.478.360.544.2]Gambar 4.2 Grafik regresi penurunan kadar vitamin C pada jus apel merah
Gambar 4.3 Grafik regresi penurunan kadar vitamin C pada jus apel hijau
Dari Gambar 4.1 dapat dilihat bahwa profil penurunan kadar vitamin C
pada kedua sampel cukup cepat. Hal ini dikarenakan pada penelitian ini,
penetapan kadar vitamin C dari jus buah apel merah dan jus buah apel hijau
dilakukan dengan penyimpanan pada suhu ruang. Menurut Mahlizar (2014) dan
Oyetade, et. al (2012), kadar vitamin C pada sampel yang disimpan pada suhu
ruang semakin cepat menurun seiring dengan semakin lamanya penyimpanan, hal y = -2.225x + 12.18
r² = 0.980
0 2 4 6 8 10 12 14
0 1 2 3 4 5 6
K a d a r v it a m in C ( m g /1 0 0 g ) waktu (jam)
y = -2.466x + 15.34 r² = 0.967
0 5 10 15 20
0 1 2 3 4 5 6
ini berbeda pada sampel yang disimpan pada suhu dingin, yang mana kadar
vitamin C pada sampel tidak mengalami penurunan yang cepat.
Hal ini didukung oleh Juniasih (1997) dan Winarno (1980), penyimpanan
buah pada suhu dingin (50C) dapat menghambat aktivitas enzim, reaksi-reaksi
kimia dan menghambat atau menghentikan pertumbuhan mikroba sebagai
penyebab busuk dan rusah pada buah. Proses pendinginan juga dapat
memperlambat kecepatan reaksi-reaksi metabolisme. Oleh karena itu, dengan
penyimpanan pada suhu dingin dapat memperpanjang masa hidup dari
jaringan-jaringan di dalam bahan pangan tersebut. Hal ini membuktikkan bahwa suhu
mempengaruhi penurunan kadar vitamin C pada sampel.
Dalam penelitian lain yang dilakukan oleh Rachmawati (2009), terhadap
kandungan vitamin C pada cabai rawit putih (Capsicum frustescens) juga terdapat
penurunan kadar vitamin C pada cabai rawit putih yang dipengaruhi oleh suhu dan
lama penyimpanan. Cabai rawit putih yang diberi perlakuan penyimpanan pada
suhu 100C dan 200C selama 15 hari, kandungan vitamin C mengalami penurunan
masing-masing yaitu: dari 43,6 mg/100mL menjadi 35,2 mg/100mL dan dari 40,9
mg/100 mL menjadi 31,6 mg/100 mL.
Menurut Gaman dan Sherington (1992), faktor penyimpanan juga
mempengaruhi kandungan vitamin C. Penyimpanan buah pada ruangan terbuka
dan pada suhu ruang dapat menyebabkan teroksidasinya vitamin C oleh faktor
udara, sinar matahari, dan suhu yang tinggi.
Kondisi penyimpanan juga mempengaruhi aktivitas reaksi enzimatik
dalam jaringan buah. Pada sel yang tidak mengalami kerusakan, enzim askorbat
mengoksidasi vitamin C. Akan tetapi apabila sel mengalami kerusakan enzim
askorbat oksidase akan dibebaskan dengan cara kontak langsung dengan asam
askorbat sehingga vitamin C mengalami kerusakan. Pernyataan ini juga didukung
oleh Noor, dkk., (1990), yang menyatakan penyimpanan buah-buahan pada
kondisi pada suhu ruang akan menurunkan kandungan vitamin C dengan cepat
karena adanya proses respirasi dan oksidasi.
[image:49.595.114.506.350.519.2]4.4 Hasil Uji Statistik
Tabel 4.3 Hasil uji analisis Duncan terhadap kadar vitamin C dari jus buah apel merah dan jus buah apel hijau pada interval waktu 0 hingga 5 jam
Analisis Duncan bertujuan untuk mencari atau menguji kelompok mana
yang memiliki perbedaan atau tidak memiliki perbedaan yang signifikan dengan
kelompok lainnya. Dari Tabel 4.3 dapat dilihat bahwa hasil analisis Duncan
terhadap semua kelompok, nilai rata-rata kadar vitamin C dari jus buah apel
terdapat perbedaan yang signifikan antara kadar vitamin C pada jus buah apel
merah dan hijau pada interval waktu 0 hingga 5 jam.
4.5 Hasil Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (recovery) vitamin C dari jus buah apel merah
dan hijau dapat dilihat pada Tabel 4.4 dan Tabel 4.5.
Tabel 4.4 Hasil uji perolehan kembali (recovery) vitamin C dari jus buah apel merah
No Penambahan
Vitamin C (mg)
Kadar Vitamin C Setelah Penambahan Baku
Rata-rata Perolehan Kembali
(%)
1 2,01 39,41
96,70
2 2,01 39,48
3 2,01 39,41
4 2,01 39,26
5 2,01 39,43
6 2,01 39,64
Rata-rata (% recovery)
Standard Deviation (SD)
Relative Standard Deviation (RSD) (%)
96,70 0,0967 0,24
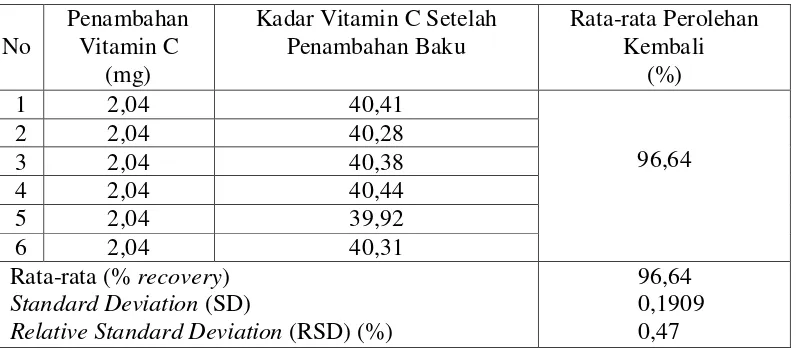
Tabel 4.5 Hasil uji perolehan kembali (recovery) vitamin C dari jus buah apel hijau
No
Penambahan Vitamin C
(mg)
Kadar Vitamin C Setelah Penambahan Baku
Rata-rata Perolehan Kembali
(%)
1 2,04 40,41
96,64
2 2,04 40,28
3 2,04 40,38
4 2,04 40,44
5 2,04 39,92
6 2,04 40,31
Rata-rata (% recovery)
Standard Deviation (SD)
Relative Standard Deviation (RSD) (%)
[image:50.595.115.513.290.466.2] [image:50.595.114.512.531.706.2]Dari Tabel 4.4 di atas, diperoleh persen perolehan kembali rata-rata untuk
jus buah apel merah adalah 96,70% dan dari Tabel 4.5 di atas, diperoleh persen
perolehan kembali rata-rata untuk jus buah apel hijau adalah 96,64%, yang
keduanya masih memenuhi persyaratan akurasi yang diizinkan yaitu: 90%-107%.
Hasil persen RSD rata-rata dari pengujian pada jus buah apel merah dan hijau
berturut-turut adalah 0,24% dan 0,47% dengan nilai rata-rata hasil uji perolehan
kembali yang diizinkan adalah 2% (Harmita, 2004). Dari hasil yang diperoleh
tersebut maka dapat disimpulkan bahwa akurasi dan presisi metode analisis yang
dilakukan cukup tinggi, contoh perhitungan dan hasil perhitungan dapat dilihat
pada Lampiran 11, halaman 61 (untuk sampel jus apel merah) dan Lampiran 16,
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat disimpulkan bahwa:
a. Kadar vitamin C jus buah apel merah yaitu 12,76 mg/100 g, sedangkan kadar
vitamin C jus buah apel hijau yaitu 16,49 mg/100 g.
b. Terdapat penurunan kadar vitamin C pada jus buah apel merah, yaitu pada 0
jam: 12,76 mg/100 g, pada 1 jam: 10,07 mg/100 g, pada 2 jam: 6,71 mg/100 g,
pada 3 jam: 5,20 mg/100 g, pada 4 jam: 3,63 mg/100 g, pada 5 jam: 1,35
mg/100 g. Sedangkan kadar vitamin C jus buah apel hijau, pada 0 jam: 16,49
mg/100 g, pada 1 jam: 11,49 mg/100 g, pada 2 jam: 10,23 mg/100 g, pada 3
jam: 7,84 mg/100 g, pada 4 jam: 6,04 mg/100 g, dan pada 5 jam: 2,97 mg/100
g .
c. Berdasarkan hasil pengujian beda nilai rata-rata secara statistik dengan metode
ANOVA dilanjutkan dengan uji DUNCAN dengan taraf kepercayaan 95%
diperoleh perbedaan yang signifikan rata-rata penurunan kadar vitamin C
antara kadar vitamin C pada jus buah apel merah dengan kadar vitamin C pada
jus buah apel hijau.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk menetapkan kadar dan
membandingkan penurunan kadar vitamin dan mineral lainnya pada jus buah apel
Disarankan juga kepada masyarakat untuk segera meminum jus apel yang
telah dibuat agar mencegah rusaknya vitamin C dalam jus dan memaksimalkan
DAFTAR PUSTAKA
Andarwulan, N., dan Koswara, S. (1992). Kimia Vitamin. Jakarta: Rajawali Press. Hal. 23-44.
Arisandi,