LAPORAN PRAKTEK KERJA PROFESI
FARMASI INDUSTRI
di
PT. Mutiara Mukti Farma (MUTIFA)
Medan
Disusun oleh :
Janti Kosman, S. Farm NIM 073202044
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Kuasa
karena atas berkat dan karunia-Nya sehingga penulis dapat menyelesaikan Latihan
Kerja Profesi Apoteker di PT Mutiara Mukti Farma (PT MUTIFA) Medan dan
penyusunan laporan ini. Adapun Latihan Kerja Profesi ini merupakan salah satu
syarat dalam mengikuti Program Pendidikan Profesi Apoteker di Fakultas Farmasi
Universitas Sumatera Utara.
Selama Latihan Kerja Profesi ini penulis telah banyak menerima bantuan
dari berbagai pihak berupa bimbingan dan arahan. Pada kesempatan ini dengan
segala kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya
kepada:
1. Bapak Jacob, selaku Direktur Utama PT MUTIFA yang telah berkenan
memberikan fasilitas kepada penulis melakukan Latihan Kerja Profesi.
2. Bapak Drs. D. R. Nainggolan, Apt., yang telah memberikan bimbingan
dan fasilitas kepada penulis selama melakukan Latihan Kerja Profesi.
3. Bapak Prof. Sumadio Hadisahputra, Apt. selaku Dekan Fakultas Farmasi
USU.
4. Bapak Drs. Wiryanto, M.S., Apt selaku Koordinator Program Pendidikan
Apoteker Fakultas Farmasi USU.
5. Seluruh staf dan karyawan PT MUTIFA yang telah memberikan fasilitas
Penulis menyadari sepenuhnya bahwa laporan ini masih jauh dari
sempurna, untuk itu penulis mengharapkan saran dan kritik yang membangun.
Penulis juga berharap semoga laporan ini dapat memberi manfaat bagi ilmu
pengetahuan, khususnya di bidang farmasi.
Medan, Mei 2008
RINGKASAN
Telah dilakukan Praktek Kerja Profesi (PKP) di Industri Farmasi PT.
Mutiara Mukti Farma (MUTIFA) Medan yang merupakan salah satu program
dalam pendidikan profesi apoteker, yang bertujuan agar mahasiswa/mahasisiwi
mengetahui dan memahami tugas dan fungsi apoteker dalam industri farmasi,
yang diharapkan dapat sebagai bekal untuk menghadapi dunia kerja yang
sesungguhnya. Memperoleh wawasan dan pengetahuan yang lebih luas, serta
memahami penerapan CPOB di PT. Mutiara Mukti Farma (MUTIFA) dan
mengetahui gambaran tentang situasi dan kondisi kerja di PT. Mutiara Mukti
Farma (MUTIFA).
Praktek kerja profesi di Industri Farmasi PT. Mutiara Mukti Farma
(MUTIFA) Medan dilaksanakan pada tanggal 7 April 2008 sampai dengan 25
April 2008 dengan jumlah jam efektif 300 jam.
Kegiatan yang dilakukan selama Praktek Kerja Profesi (PKP) di Industri
antara lain membuat catatan kegiatan harian yang berisi absensi dan materi
kegiatan yang ditandatangani oleh pembimbing, melihat kegiatan di Ruang
Produksi, Laboratorium Quality Control (QC), Gudang Bahan Baku, Ruang β laktam, sistem pengolahan air minum dan untuk produksi, sistem pengaturan
udara (AHU) dan sistem pengolahan air limbah. Tugas khusus yang diberikan
berupa metoda analisa penetapan kadar untuk tablet dan sirup dari beberapa
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
DAFTAR ISI... v
DAFTAR GAMBAR ... vii
DAFTAR TABEL... viii
DAFTAR LAMPIRAN... ix
RINGKASAN ... x
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang ... 2
1.2. Tujuan ... 2
BAB II TINJAUAN UMUM PT. MUTIARA MUKTI FARMA (MUTIFA) MEDAN ... 3
2.1. Sejarah... 3
2.3. Lokasi dan Sarana Produksi ... 5
2.3.1. Lokasi... 5
2.3.2. Sarana Produksi... 7
2.4. Penerapan CPOB di PT. Mutiara Mukti Farma (MUTIFA) ... 11
BAB III KEGIATAN DI PT. MUTIARA MUKTI FARMA (MUTIFA) MEDAN ... 17
3.1. Keterlibatan dalam Produksi ... 17
3.2. Tinjauan ke bagian-bagian lain ... 21
3.2.1. Research and Development (R&D) ... 21
3.2.2. Quality Control (QC) ... 21
3.2.3. Quality Assurance (QA)... 30
3.2.4. Gudang ... 32
3.2.5. Limbah ... 35
BAB IV PEMBAHASAN... 40
4.1 Personalia ... 41
4.2 Bangunan dan Fasilitas ... 42
4.3 Peralatan... 42
4.5 Produksi ... 43
4.6 Pengawasan Mutu ... 44
4.7 Inspeksi Diri ... 44
4.8 Penanganan Keluhan, Penarikan Obat yang Beredar, dan produk kembalian ... 44
4.9Dokumentasi ... 45
4.10 Pengamatan Pengolahan Limbah ... 45
BAB V KESIMPULAN DAN SARAN... 46
5.1. Kesimpulan ... 46
5.2. Saran... 46
DAFTAR PUSTAKA ... 48
LAMPIRAN
DAFTAR GAMBAR
Gambar 1. Denah lokasi PT. MUTIFA Medan... 5
Gambar 2. Struktur Organisasi R & D di PT. MUTIFA... 21
Gambar 3. Struktur Pemastian Mutu di PT. MUTIFA... 32
Gambar 4. Diagram Sistem Pengolahan Limbah Cair di PT. MUTIFA... 35
DAFTAR TABEL
Tabel 1. Ukuran Ruangan masing-masing Bagian di PT. MUTIFA Medan ... 6
Tabel 2. Jumlah Personil pada PT. MUTIFA Medan ... 9
Tabel 3. Personalia PT. MUTIFA Medan Beradasarkan Jenjang Pendidikan... 10
Tabel 4. Tolak Ukur yang dipakai untuk Pemantauan Limbah Cair... 36
DAFTAR LAMPIRAN
Lampiran 1. Struktur Organisasi PT. MUTIFA Medan... 49
Lampiran 2. Bagan Proses Pembuatan Tablet/Kaplet... 50
Lampiran 3. Bagan Proses Pembuatan Kapsul ... 51
Lampiran 4. Bagan Proses Pembuatan Serbuk Oral ... 52
Lampiran 5. Bagan Proses Pembuatan Liquida ... 53
BAB I
PENDAHULUAN
1.1 Latar Belakang
Obat adalah bahan atau paduan bahan-bahan yang digunakan untuk
mempengaruhi atau menyelidiki sistem fisiologi atau keadaan patologi dalam
rangka penetapan diagnosa, pencegahan, penyembuhan, pemulihan dan
peningkatan kesehatan. Oleh karena itu, proses produksi obat memerlukan
pengawasan yang ketat untuk menjamin kualitas obat yang dihasilkan.
Salah satu upaya yang dilakukan pemerintah untuk menjamin tersedianya obat
yang bermutu, aman dan berkhasiat yaitu dengan mengharuskan setiap industri
farmasi untuk menerapkan Cara Pembuatan Obat yang Baik (CPOB) sesuai
keputusan Menteri Kesehatan RI Nomor 43/MENKES/SK/II/1988 pada tanggal 2
Februari 1988. CPOB adalah pedoman pembuatan obat bagi industri farmasi di
Indonesia yang bertujuan untuk memastikan agar sifat dan mutu obat yang
dihasilkan senantiasa memenuhi persyaratan mutu yang telah ditentukan dan
sesuai dengan tujuan penggunaannya. Mutu suatu obat tidak dapat ditentukan
berdasarkan pemeriksaan produk akhir saja, melainkan harus dibentuk ke dalam
produk selama keseluruhan proses pembuatan.
Apoteker merupakan salah satu tenaga inti dalam industri farmasi karena turut
berperan dalam menghasilkan obat yang bermutu, aman dan berkhasiat.
Kedudukan apoteker juga diatur dalam CPOB, yaitu sebagai penanggung jawab
memiliki wawasan, pengetahuan, keterampilan dan kemampuan dalam
mengaplikasikan dan mengembangkan ilmunya secara profesional, terutama
dalam memahami kenyataan di lapangan industri. Dengan demikian, Praktek
Kerja Profesi di industri farmasi menjadi salah satu kebutuhan mahasiswa calon
apoteker.
Program Pendidikan Profesi Apoteker Fakultas Farmasi Universitas Sumatera
Utara (USU) telah bekerja sama dengan PT. Mutiara Mukti Farma (MUTIFA)
untuk menyelenggarakan Praktek Kerja Profesi. Praktek Kerja Profesi ini
dilaksanakan pada tanggal 10 April 2008 hingga 25 April 2008. Praktek Kerja
Profesi di industri farmasi ini diharapkan dapat memberikan pengetahuan praktis
kepada mahasiswa calon apoteker tentang pekerjaan kefarmasian di industri
dengan penerapan CPOB.
1.2 Tujuan
Adapun tujuan Praktek Kerja Profesi Apoteker Fakultas Farmasi USU di
industri PT. Mutiara Mukti Farma (MUTIFA) adalah :
a. Mengetahui dan memahami tugas dan fungsi apoteker dalam industri farmasi,
yang diharapkan dapat sebagai bekal untuk menghadapi dunia kerja yang
sesungguhnya.
b. Memperoleh wawasan dan pengetahuan yang lebih luas, serta memahami
penerapan CPOB di PT. Mutiara Mukti Farma (MUTIFA).
c. Mengetahui gambaran tentang situasi dan kondisi kerja di PT. Mutiara Mukti
BAB II
TINJAUAN UMUM PT. MUTIARA MUKTI FARMA (MUTIFA) MEDAN
2.1 Sejarah
Pada tahun 1975 didirikan Industri Farmasi di kota Medan dengan nama
“Sejati Pharmaceutical Industries”, yang memproduksi obar merek “SIAGOGO”.
Setelah beberapa tahun berproduksi, perusahaan ini kemudian dialihkan
pemiliknya kepada Bapak Drs. W. H. Siahaan dan memindahnamakan perusahaan
tersebut dalam suatu akte notaris tertanggal 31 Januari 1980 dengan nama PT.
Mutiara Mukti Farma (MUTIFA) yang berlokasi di Jl. Brigjen Katamso No. 220
Medan.
Berdasarkan Surat Keputusan Menteri Kesehatan RI tahun 1981 No.
0098/SK/PAB/81 memutuskan memberikan izin untuk mendirikan pabrik Farmasi
kepada PT. Mutiara Mukti Farma (MUTIFA) dengan nama “MUTIFA
INDUSTRI FARMASI” untuk memproduksi obat-obatan. Dengan
dikeluarkannya surat izin produksi oleh Departemen Kesehatan RI c/q Badan
Pengawasan Obat dan Makanan No. 213/AA/III/81, mulailah PT Mutiara Mukti
Farma memproduksi obat-obatan.
Pada tahun 1983, perusahaan ini menjalankan dan melaksanakan operasinya
dalam menghasilkan berbagai jenis dan bentuk sediaan obat untuk memenuhi
kebutuhan masyarakat Indonesia wilayah barat umumnya dan daerah Sumatera
Pada Tanggal 29 November 1988, dengan akte notaris No. 35 diadakanlah
perubahan akte atas pemegang saham serta manajemen perusahaan, yang
ditetapkan melalui keputusan Menteri Kehakiman RI No. C2-1134.HT.01.04 th
89 tanggal 31 Januari 1989. Dalam akte tersebut, berdasarkan keputusan rapat
Dewan Komisaris serta pemegang saham, ditetapkan bahwa yang menjadi
penanggung jawab dengan jabatan Direktur Utama adalah Bapak Jacob.
3
Sesuai dengan Keputusan Menteri Kesehatan RI No. 43/Menkes/SK/II/1988
tentang Pedoman Cara Pembuatan Obat yang Baik (CPOB), bahwa setiap industri
farmasi harus mengacu pada pedoman tersebut, maka untuk memenuhi ketentuan
tersebut PT. MUTIFA telah membangun pabrik yang baru di Jl. Karya Jaya No.
68 Km 8,5 Namorambe. Pada Mei 1994 produksi telah dilaksanakan di pabrik
yang baru dan pada saat ini kegiatan administrasi juga telah dilakukan dilokasi
tersebut. Pada tanggal 27 Juli 1994 PT. MUTIFA diberikan sertifikat sebagai
industri farmasi yang telah memenuhi CPOB.
Bentuk sediaan yang telah diproduksi sampai saat ini terdiri dari 8 jenis
sediaan yaitu : tablet, sirup, salep, serbuk oral, serbuk obat luar dan cairan obat
luar sebanyak 114 item. Pendistribusian sediaan yang diproduksi PT. MUTIFA
Medan meliputi wilayah : Provinsi Sumatera Utara, Riau, Sumatera Selatan, DKI
Jakarta, Jawa Barat, Jawa Tengah, Jawa Timur, Sulawesi Utara dan Sulawesi
Selatan. Untuk wilayah Sumatera obat didistribusikan melalui PBF Mekada
Untuk memproduksi obat-obatan dilakukan dengan sistem skala prioritas,
yang mengutamakan obat yang lebih cepat laku di pasaran. Hal ini tidak berlaku
untuk obat Inpres dan Askes.
Bahan baku, yaitu bahan berkhasiat dan bahan tambahan yang diperlukan
oleh perusahaan untuk pembuatan sediaan obat diperoleh dari RRC, Amerika
Serikat, Jerman, Belanda, India, Taiwan, dan Switzerland melalui distributor
masing-masing.
2.2 Visi dan Misi
Visi dan Misi PT. Mutifa adalah “Anda sehat kami bangga”.
2.3 Lokasi dan Sarana Produksi 2.3.1 Lokasi
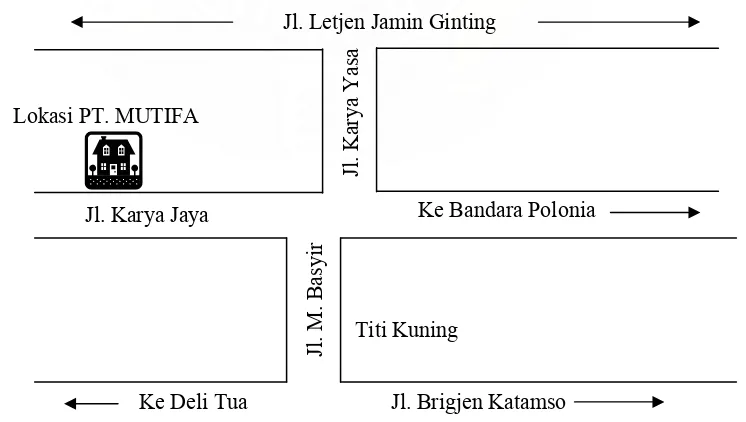
PT. MUTIFA Medan berada di Jl. Karya Jaya No. 68 Km 8,5 Namorambe
Medan. Denah lokasi PT. MUTIFA ditunjukkan pada Gambar 1 berikut ini :
Jl. Letjen Jamin Ginting
Jl
Ke Deli Tua Jl. Brigjen Katamso
Luas areal PT. MUTIFA Medan mempunyai luas areal 9600 m2 dan luas
bangunan 6259 m2.
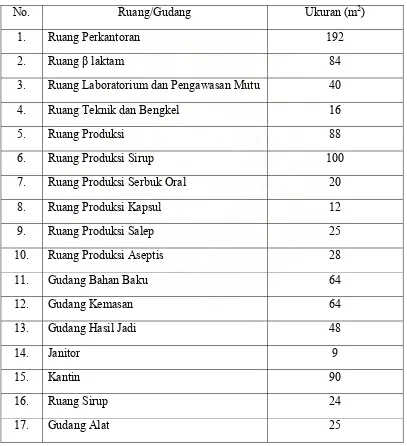
Luas masing-masing ruangan adalah sebagai berikut :
Tabel 1. Ukuran Ruangan masing-masing Bagian di PT. MUTIFA Medan.
No. Ruang/Gudang Ukuran (m2)
1. Ruang Perkantoran 192
2. Ruang laktam 84
3. Ruang Laboratorium dan Pengawasan Mutu 40
4. Ruang Teknik dan Bengkel 16
5. Ruang Produksi 88
6. Ruang Produksi Sirup 100
7. Ruang Produksi Serbuk Oral 20
8. Ruang Produksi Kapsul 12
9. Ruang Produksi Salep 25
10. Ruang Produksi Aseptis 28
11. Gudang Bahan Baku 64
12. Gudang Kemasan 64
13. Gudang Hasil Jadi 48
14. Janitor 9
15. Kantin 90
16. Ruang Sirup 24
Sumber arus listrik berasal dari Perusahaan Listrik Negara (PLN) dan
apabila arus listrik dari PLN terputus digunakan generator.
Sumber air berasal dari sumur pompa dan air PAM. Untuk keperluan
produksi digunakan air PAM yang telah diolah menjadi air demineral, aquadest
dan aquabidest. Air sumur digunakan untuk pencucian alat, mandi, dan bila aliran
PAM mengalami kerusakan digunakan untuk menggantikan air PAM dimana air
sumur ini telah mengalami tiga kali penyaringan. Bangunan penunjang lainnya
terdiri dari musholla, kamar mandi dan pos jaga.
2.3.2 Sarana Produksi
Ruangan produksi dengan gudang bahan baku, gudang kemasan dan obat
jadi dibuat sedemikian rupa sehingga waktu yang dibutuhkan untuk mengangkut
bahan baku ke ruang produksi, bahan kemasan ke ruang pengemasan, obat jadi
dari ruang karantina ke gudang obat jadi relatif singkat dan tidak melalui ruang
produksi lainnya sehingga kemungkinan terjadinya pencemaran silang dapat
dihindari.
Keadaan ruang produksi adalah sebagai berikut :
Lantai
Lantai ruang produksi beta laktam, kapsul, puyer, salep, dan sirup, terbuat
dari beton yang dilapisi traso dan bata diantaranya diisi dengan semen putih.
Lantai mempunyai permukaan yang rata, mudah dibersihkan, tidak menahan
partikel, tahan terhadap deterjen dan desinfektan tetapi tidak tahan terhadap bahan
Dinding
Dinding ruang terbuat dari beton, yang dilapisi epoksi sehingga permukaan
dinding menjadi licin dan rata, kedap air, mudah dibersihkan, tahan terhadap
deterjen, desinfektan, tidak menahan partikel dan tidak menjadi tempat
bersarangnya binatang kecil.
Langit-langit
Langit-langit ruang terbuat dari beton, yang dilapisi epoksi sehingga
permukaan langit-langit menjadi licin dan rata, kedap air, mudah dibersihkan,
tahan terhadap detergent, desinfektan, tidak menahan partikel tetapi tidak tahan
terhadap goresan logam.
Pengaturan Udara
Aliran udara yang digunakan dalam ruangan produksi beta laktam, kapsul,
puyer, salep, dan sirup adalah sirkulasi sistem filter, berarti udara masuk ke dalam
ruangan melalui proses penyaringan. Udara masuk dari luar disalurkan ke dalam
ruangan produksi, lalu udara kotor dihisap dan dialirkan keluar. Dengan adanya
sirkulasi sistem filter dengan proses penyaringan maka dapat menghasilkan
efisiensi penyaringan 80% terhadap partikel yang berukuran 10µ.
Kecepatan pertukaran udara dalam ruangan produksi cairan 25 kali per jam
dan untuk koridor 20 kali per jam. Sedangkan untuk produksi beta laktam dan
non beta laktam (kapsul, puyer, tablet, dan salep), kecepatan pertukaran udara
dalam ruangan produksi 20 kali per jam dan untuk koridor 25 kali per jam.
Pengaturan temperatur, kelembaban udara agar kondisi ruangan baik dan nyaman
Sistem pengaturan udara ruang laktam dibuat tersendiri yaitu udara yang
masuk dari luar disaring dan dialirkan keruang laktam. Lalu udara kotor yang
berada di ruangan laktam dihisap dan dikeluarkan dengan menggunakan alat
Wet Scrubbs, merupakan serangkaian alat yang bekerja dengan cara menghisap dan mengalirkan udara yang berada di ruang laktam melalui suatu corong yang
dilengkapi dengan suatu alat pemercik air. Percikan air yang sudah bercampur
dengan udara kotor ditampung didalam bak, diklorinasi, diencerkan dan dialirkan
ke penampungan limbah.
Personalia
Untuk mendukung kegiatan operasionalnya, PT. MUTIFA memerlukan
personil yang cakap, terampil dan terlatih yang saat ini berjumlah 127 orang.
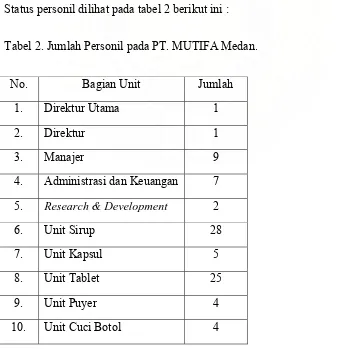
Status personil dilihat pada tabel 2 berikut ini :
Tabel 2. Jumlah Personil pada PT. MUTIFA Medan.
No. Bagian Unit Jumlah
1. Direktur Utama 1
2. Direktur 1
3. Manajer 9
4. Administrasi dan Keuangan 7
5. Research & Development 2
6. Unit Sirup 28
7. Unit Kapsul 5
8. Unit Tablet 25
9. Unit Puyer 4
11. Gudang Kemasan 4
12. Gudang Bahan Baku 8
13. Gudang Barang Jadi 3
14. Teknisi 5
15. Laboratorium 9
16. Kolektor 1
17. Akuntansi 3
18. Penjualan/Pemasaran 2
19. Supir 3
20. Pembelian 1
21. Cleaning Service 5
22. Satpam 5
Jumlah seluruhnya 135
Dalam rangka memenuhi persyaratan CPOB, langkah-langkah yang diambil
PT. MUTIFA Medan dibidang personalia adalah dengan cara mengirim pimpinan
atau staf untuk mengikuti penataran mengenai CPOB. Selanjutnya diharapkan
pimpinan atau staf tersebut dapat memberikan bimbingan dan pelatihan tentang
CPOB kepada karyawan sehingga kegiatan perusahaan akan memenuhi ketentuan
CPOB. Berdasarkan jenjang pendidikan, maka personil PT. MUTIFA Medan
dapat diuraikan sebagai berikut :
Tabel 3. Personalia PT. MUTIFA Medan Beradasarkan Jenjang Pendidikan.
No. Jenjang Pendidikan Jumlah (Orang)
1. Sarjana 11
3. SLTA/sederajat 102
4. SLTP 15
5. SD 2
Struktur Organisasi
Struktur organisasi pada PT. MUTIFA merupakan struktur organisasi yang
memperlihatkan wewenang dan tanggung jawab vertikal, yang berarti bahwa
tiap-tiap orang dalam organisasi kecuali buruh mempunyai beberapa orang bawahan.
Kekuasaan tertinggi berada pada rapat umum pemegang saham yang
pelaksanaannya harus dipertanggungjawabkan oleh Direktur Utama. Untuk
menjalankan aktifitas perusahaan, Direktur Utama melimpahkan wewenang, tugas
dan tanggungjawab kepada Direktur. Direktur membawahi 9 bagian, dan
masing-masing bawahan dipimpin oleh manajer yang langsung bertanggungjawab penuh
kepada Direktur. Masing-masing bagian membawahi sub bagian yang
bertanggungjawab penuh kepada Kepala bagiannya dalam melaksanakan tugas
yang telah dibebankan kepadanya. Struktur Organisasi PT. MUTIFA Medan dapat
dilihat pada lampiran 1 halaman 49.
2.4 Penerapan CPOB di PT. Mutiara Mukti Farma (MUTIFA)
CPOB adalah bagian dari Pemastian Mutu yang memastikan bahwa obat
dibuat dan dikendalikan secara konsisten untuk mencapai standar mutu yang
spesifikasi produk. CPOB mencakup seluruh aspek produksi dan pengendalian
mutu.
Pada pembuatan obat, pengendalian menyeluruh adalah sangat esensial
untuk menjamin bahwa konsumen menerima obat yang bermutu tinggi.
Pembuatan secara sembarangan tidak dibenarkan bagi produk yang digunakan
untuk menyelamatkan jiwa, atau memulihkan atau memelihara kesehatan.
Tidaklah cukup bila produk jadi hanya sekedar lulus dari serangkaian
pengujian, tetapi yang lebih penting adalah bahwa mutu harus dibentuk ke dalam
produk tersebut. Mutu obat tergantung pada bahan awal, bahan pengemas, proses
produksi dan pengendalian mutu, bangunan, peralatan yang dipakai dan personil
yang terlibat.
Persyaratan dasar dari CPOB adalah:
a) Semua proses pembuatan obat dijabarkan dengan jelas, dikaji secara
sistematis berdasarkan pengalaman dan terbukti mampu secara konsisten
menghasilkan obat yang memenuhi persyaratan mutu dan spesifikasi yang
telah ditetapkan.
b) Tahap proses yang kritis dalam pembuatan, pengawasan proses dan sarana
penunjang serta perubahannya yang signifikan divalidasi.
c) Tersedia semua sarana yang diperlukan dalam CPOB termasuk :
• personil yang terkualifikasi dan terlatih
• bangunan dan sarana dengan luas yang memadai
• peralatan dan sarana penunjang yang sesuai
• prosedur dan instruksi yang disetujui
• tempat penyimpanan dan transportasi yang memadai.
d) Prosedur dan instruksi ditulis dalam bentuk instruksi dengan bahasa yang
jelas, tidak bermakna ganda, dapat diterapkan secara spesifik pada sarana
yang tersedia.
e) Operator memperoleh pelatihan untuk menjalankan prosedur secara benar
f) Pencatatan dilakukan secara manual atau dengan alat pencatat selama
pembuatan yang menunjukkan bahwa semua langkah yang dipersyaratkan
dalam prosedur dan instruksi yang ditetapkan benar-benar dilaksanakan
dan jumlah serta mutu produk yang dihasilkan sesuai dengan yang
diharapkan. Tiap penyimpangan dicatat secara lengkap dan diinvestigasi.
g) Catatan pembuatan termasuk distribusi yang memungkinkan penelusuran
riwayat bets secara lengkap, disimpan secara komprehensif dan dalam
bentuk yang mudah diakses.
h) Penyimpanan dan distribusi obat yang dapat memperkecil risiko terhadap
mutu obat.
i) Tersedia sistem penarikan kembali bets obat manapun dari peredaran.
j) Keluhan terhadap produk yang beredar dikaji, penyebab cacat mutu
diinvestigasi serta dilakukan tindakan perbaikan yang tepat dan
pencegahan pengulangan kembali keluhan.
Sumber daya manusia sangat penting dalam pembentukan dan penerapan
sistem pemastian mutu yang memuaskan dan pembuatan obat yang benar. Oleh
sebab itu industri farmasi bertanggung jawab untuk menyediakan personil yang
personil hendaklah memahami tanggung jawab masing-masing dan dicatat.
Seluruh personil hendaklah memahami prinsip CPOB dan memperoleh pelatihan
awal dan berkesinambungan, termasuk instruksi mengenai higiene yang berkaitan
dengan pekerjaan.
Bangunan dan fasilitas untuk pembuatan obat hendaklah memiliki desain,
konstruksi dan letak yang memadai, serta disesuaikan kondisinya dan dirawat
dengan baik untuk memudahkan pelaksanaan operasi yang benar. Tata letak dan
desain ruangan harus dibuat sedemikian rupa untuk memperkecil risiko terjadinya
kekeliruan, pencemaran silang dan kesalahan lain, dan memudahkan pembersihan,
sanitasi dan perawatan yang efektif untuk menghindari pencemaran-silang,
penumpukan debu atau kotoran, dan dampak lain yang dapat menurunkan mutu
obat.
Peralatan untuk pembuatan obat hendaklah memiliki desain dan konstruksi
yang tepat, ukuran yang memadai serta ditempatkan dan dikualifikasi dengan
tepat, agar mutu obat terjamin sesuai desain serta seragam dari bets ke bets dan
untuk memudahkan pembersihan serta perawatan.
Tingkat sanitasi dan higiene yang tinggi hendaklah diterapkan pada setiap
aspek pembuatan obat. Ruang lingkup sanitasi dan higiene meliputi personil,
bangunan, peralatan dan perlengkapan, bahan produksi serta wadahnya, dan
segala sesuatu yang dapat merupakan sumber pencemaran produk. Sumber
pencemaran potensial hendaklah dihilangkan melalui suatu program sanitasi dan
Tujuan inspeksi diri adalah untuk mengevaluasi apakah semua aspek
produksi dan pengawasan mutu industri farmasi memenuhi ketentuan CPOB.
Program inspeksi diri hendaklah dirancang untuk mendeteksi kelemahan dalam
pelaksanaan CPOB dan untuk menetapkan tindakan perbaikan yang diperlukan.
Inspeksi diri hendaklah dilakukan secara independen dan rinci oleh petugas yang
kompeten dari perusahaan. Ada manfaatnya bila juga menggunakan auditor luar
yang independen. Inspeksi diri hendaklah dilakukan secara rutin dan, di samping
itu, pada situasi khusus, misalnya dalam hal terjadi penarikan kembali obat jadi
atau terjadi penolakan yang berulang. Semua saran untuk tindakan perbaikan
supaya dilaksanakan. Prosedur dan catatan inspeksi diri hendaklah
didokumentasikan dan dibuat program tindak lanjut yang efektif.
Semua keluhan dan informasi lain yang berkaitan dengan kemungkinan
terjadi kerusakan obat hendaklah dikaji dengan teliti sesuai dengan prosedur
tertulis. Untuk menangani semua kasus yang mendesak, hendaklah disusun suatu
sistem, bila perlu mencakup penarikan kembali produk yang diketahui atau diduga
cacat dari peredaran secara cepat dan efektif. Penarikan kembali produk adalah
suatu proses penarikan kembali dari satu atau beberapa bets atau seluruh bets
produk tertentu dari peredaran.
Penarikan kembali produk dilakukan apabila ditemukan produk yang cacat
mutu atau bila ada laporan mengenai reaksi yang merugikan yang serius serta
berisiko terhadap kesehatan. Penarikan kembali produk dari peredaran dapat
Produk kembalian adalah obat jadi yang telah beredar, yang kemudian
dikembalikan ke industri farmasi karena keluhan mengenai kerusakan, daluwarsa,
atau alasan lain misalnya kondisi wadah atau kemasan yang dapat menimbulkan
keraguan akan identitas, mutu, jumlah dan keamanan obat yang bersangkutan.
Dokumentasi adalah bagian dari sistem informasi manajemen dan
dokumentasi yang baik merupakan bagian yang esensial dari pemastian mutu.
Dokumentasi yang jelas adalah fundamental untuk memastikan bahwa tiap
personil menerima uraian tugas yang relevan secara jelas dan rinci sehingga
memperkecil risiko terjadi salah tafsir dan kekeliruan yang biasanya timbul karena
hanya mengandalkan komunikasi lisan. Spesifikasi, Dokumen Produksi
Induk/Formula Pembuatan, prosedur, metode dan instruksi, laporan dan catatan
harus bebas dari kekeliruan dan tersedia secara tertulis. Keterbacaan dokumen
BAB III
KEGIATAN DI PT. MUTIARA MUKTI FARMA (MUTIFA) MEDAN
3.1 Keterlibatan dalam Produksi
Yang dimaksud dengan produksi adalah semua kegiatan mulai dari
penerimaan bahan awal, pengolahan sampai dengan pengemasan untuk
menghasilkan obat jadi.
Tugas dan fungsi bagian produksi PT. MUTIFA antara lain :
1. Melaksanakan pembuatan obat mulai dari permintaan bahan baku ke
gudang, pengolahan, pengemasan, sampai pengiriman obat ke gudang obat
jadi.
2. Melaksanakan secara teknis dan administrasi semua tugas selama
pengolahan dan pengemasan dengan berpedoman kepada prosedur tetap
(protap) yang telah ditetapkan.
Sasaran utama yang harus dicapai oleh bagian produksi antara lain adalah sebagai
berikut :
1. Memenuhi dan menyerahkan permintaan sesuai jumlah yang diharapkan
dan waktu penyerahan yang diminta.
2. Menghasilkan produk yang diminta sesuai dengan jumlah yang ditetapkan
secara efektif dan efisien.
Sebelum proses berlangsung, ada beberapa hal yang perlu dipersiapkan agar
produksi dapat berjalan lancar dan menghasilkan suatu produk sesuai dengan yang
Tahapan yang perlu diperhatikan sebelum produksi adalah sebagai berikut :
1. Ruang produksi harus tetap dijaga kebersihannya, menggunakan
desinfektan untuk memperkecil terjadinya kontaminasi oleh
mikroorganisme.
2. Temperatur dan kelembaban ruangan harus diatur sedemikian rupa
sesuai dengan sifat bahan yang akan digunakan. Bila perlu dapat
digunakan Air Conditioner (AC) sebagai alat pendingin ruangan dan
dehumidifier sebagai alat pengatur kelembaban.
3. Ruangan produksi harus mendapat penerangan dan pertukaran udara
yang cukup, karena dapat memperlancar kegiatan.
4. Alat-alat yang digunakan harus selalu dalam keadaan bersih dan dalam
kondisi yang baik.
Sebelum proses produksi berlangsung, dibuat laporan proses produksi yang
bertujuan untuk dokumentasi, sehingga jika terjadi kekeliruan atau kesalahan pada
proses produksi, dapat segera diketahui pada proses mana kesalahan tersebut
terjadi dan dilakukan langkah-langkah yang diambil untuk mengatasi
permasalahan tersebut.
Laporan proses produksi, berguna untuk menghitung jam kerja yang
diperlukan dalam mengerjakan suatu batch sediaan. Laporan ini dibuat dan ditandatangani oleh petugas yang melaksanakan tahapan proses produksi.
Selama proses produksi berlangsung dilakukan pengawasan dalam proses
melaksanakan IPC setelah seksi bagian produksi membuat permohonan periksa.
Produk antara maupun produk ruahan yang sedang diperiksa (berstatus karantina)
diberi label kuning dan jika lulus pemeriksaan diberi label hijau dan dapat
diteruskan ke proses selanjutnya. Produk yang tidak memenuhi persyaratan akan
diberi label merah dan tidak boleh diteruskan sebelum persyaratan yang telah
ditentukan dipenuhi, atau bahan tersebut akan dimusnahkan jika tidak
memungkinkan untuk proses ulang.
Setelah tahap pengemasan selesai, obat jadi dikarantina, kemudian dibuat
permohonan periksa ke bagian pengawasan mutu untuk dilakukan Finished Pack Analysis. Obat jadi yang lulus pemeriksaan selanjutnya diserahkan ke gudang obat jadi.
Bagian produksi pada PT. MUTIFA terdiri atas bagian sebagai berikut :
Unit tablet
Unit ini dilengkapi dengan mesin pencampuran bahan, granulator dan mesin
pencetak tablet. Dalam memproduksi sediaan bentuk tablet perlu diperhatikan
kondisi bahan baku, komposisi dan pencampuran bahan pengikat, karena hal
tersebut berpengaruh dalam proses pencetakan tablet. Hal-hal yang diperiksa
selama produksi adalah keseragaman bobot, waktu hancur, diameter dan tebal,
kekerasan, kadar zat berkhasiat dan disolusi. Bagan proses pembuatan tablet dapat
dilihat pada lampiran 2 halaman 50.
Unit kapsul
Mesin-mesin yang digunakan pada produksi kapsul adalah mesin
diperhatikan kondisi ruangan yaitu temperatur dan kelembaban. Pengaturan
temperatur dengan memakai alat pendingin (AC) untuk mendapatkan temperatur
25°C. Hal-hal yang diperiksa selama produksi adalah keseragaman bobot, kadar
zat berkhasiat dan waktu hancur. Bagan proses pembuatan kapsul dapat dilihat
pada lampiran 3 halaman 51.
Unit sebuk oral
Alat-alat yang digunakan pada produksi ini antara lain mesin pencampuran
bahan, alat pengisi serbuk dan oven. Hal-hal yang diperiksa selama produksi
adalah keseragaman bobot dan kadar zat berkhasiat. Bagan proses pembuatan
serbuk oral dapat dilihat pada lampiran 4 halaman 52.
Unit Liquida
Unit liquida memproduksi sediaan bentuk cairan seperti suspensi, sirup dan
cairan obat luar. Unit ini dilengkapi dengan mesin pencampuran dan mesin
pengisi sediaan. Hal-hal yang diperiksa selama produksi adalah pH larutan, BJ
larutan, keseragaman volume, viskositas larutan, kadar zat berkhasiat dan
kebocoran wadah. Bagan proses pembuatan liquida dapat dilihat pada lampiran 5
halaman 53.
Unit salep
Mesin-mesin yang digunakan pada produksi salep antara lain mesin
pencampur bahan (mixer) dan mesin pengisi. Hal-hal yang diperiksa selama produksi adalah keseragaman bobot, kadar zat berkhasiat dan homogenitas. Bagan
3.2 Tinjauan ke bagian-bagian lain
3.2.1 Research and Development (R&D)
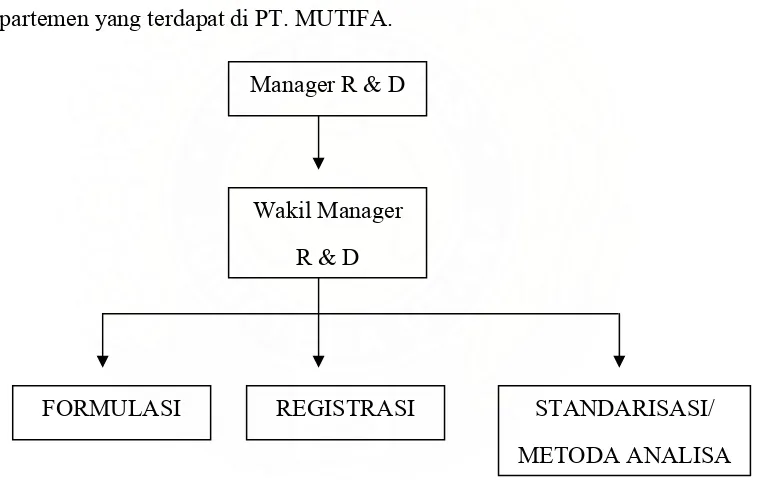
Research and Development (R&D) di PT. MUTIFA baru dibentuk pada
tahun 2008. R & D bertanggung jawab untuk menghasilkan produk-produk baru
di PT. MUTIFA. Kegiatan-kegiatan yang terlibat dalam menghasilkan
produk-produk baru tersebut adalah formulasi, registrasi dan standarisasi/metoda analisa.
Disamping itu, bagian R & D juga bertanggung jawab untuk menyusun semua
protap, protokol, validasi maupun program yang diperlukan untuk semua
departemen yang terdapat di PT. MUTIFA.
Manager R & D
Wakil Manager
R & D
FORMULASI REGISTRASI STANDARISASI/
METODA ANALISA
Gambar 2. Struktur Organisasi R & D di PT. MUTIFA
3.2.2 Quality Control (QC)
Bagian pengawasan mutu bertanggung jawab dalam melaksanakan mutu
suatu produk yang dihasilkan oleh industri farmasi agar senantiasa memiliki
Sistem pengawasan mutu harus dirancang dengan tepat untuk menjamin bahwa
tiap obat mengandung bahan dengan mutu yang benar dan jumlah yang tepat
sesuai dengan prosedur sehingga obat tersebut senantiasa memenuhi spesifikasi
yang telah ditetapkan.
Manajer pengawasan mutu PT. MUTIFA adalah seorang apoteker yang
cakap, terlatih, yang dapat bekerja secara professional. Ruang lingkup tugas,
wewenang dan tanggung jawab dari manajer pengawasan mutu adalah :
1. Manajer pengawasan mutu diberi wewenang dan tanggung jawab penuh atas
penyusunan, verifikasi, dan pelaksanaan seluruh proses pengawasan mutu.
2. Manajer pengawasan mutu sebagai satu-satunya yang memiliki wewenang
untuk meluluskan bahan awal, produk antara, produk ruahan dan obat jadi.
Bila produk tersebut tidak sesuai dengan speseifikasinya, atau bahan yang
dibuat tidak sesuai dengan prosedur yang disetujui dan kondisi yang
ditentukan maka manajer produksi langsung menolaknya.
3. Memberikan pengarahan dalam melaksanakan tugas di laboratorium kimia,
mikrobiologi, pelaksanaan pengawasan dalam proses (In Process
Control/IPC) maupun pelaksanaan CPOB.
4. Bertanggung jawab untuk menjamin bahwa semua pengujian dilaksanakan
dengan metode yang benar dan telah disetujui.
5. Bertanggung jawab atas pelaksanaan inspeksi bahan baku, bahan pengemas,
maupun proses produksi.
7. Jika ada kegagalan dalam produksi, mendiskusikan hal tersebut dengan
manajer produksi dan ikut serta mencari penyebab dan jalan keluarnya.
8. Bertanggung jawab atas pengadaan, pemakaian dan pembuatan pereaksi (baku
pembanding primer dan baku pembanding sekunder).
9. Bertanggung jawab agar alat-alat untuk analisa dipakai serta dijaga dengan
benar, dikalibrasi dan senantiasa tersedia suku cadangnya.
10.Bertanggung jawab moral yang tinggi, kemampuan, pengembangan dan
pelatihan serta melakukan evaluasi tahunan atas semua karyawan yang
dibawahinya.
11.Bertanggung jawab atas pelaksanaan inspeksi CPOB dan menjamin
pelaksanaan CPOB secara ketat.
12.Membuat laporan bulanan dan anggaran tahunan bagian pengawasan mutu.
13.Memastikan bahwa semua prosedur analisa disimpan secara baik dan benar.
14.Mengusahakan perbaikan biaya pengawasan mutu.
Laboratorium pengawasan mutu di PT. MUTIFA dibagi atas laboratorium
kimia dan mikrobiologi. Kedua laboratorium tersebut dalam ruangan yang
terpisah dan memiliki alat pengujian masing-masing. Selain itu, ruang
penimbangan, ruang penyimpanan bahan dan ruangan instrumen dipisahkan
secara tersendiri.
Area ruangan produksi berada pada satu area dengan kegiatan produksi
dan pengemasan. Terdapat ruangan khusus untuk instrumen spektrofotometer dan
ruang instrumen HPLC. Pada laboratorium kimia terdapat lemari asam yang
memiliki sistem penghisap udara tersendiri. Untuk instalasi pipa diberi penandaan
Sampah dan sisa bahan laboratorium QC dibuang pada tempat yang telah
disediakan. Bahan beracun dan bahan yang mudah terbakar disimpan pada tempat
khusus dan terpisah, zat-zat tersebut berupa asam atau basa. limbah yang
dihasilkan dari bagian QC dibuang ke Instalasi Pengolahan Air Limbah di
PT. MUTIFA.
Personil bagian QC terdiri dari apoteker dan analis yang terdidik dan
terlatih serta berpengalaman dibidangnya. Tugas dan wewenang personil
diterangkan dalam protap yang disimpan oleh yang bersangkutan. Tiap personil
menggunakan pakaian jas laboratorium, masker dan sarung tangan tahan asam dan
basa yang diperlukan untuk tugasnya.
Peralatan serta instrumen laboratorium uji disesuaikan dengan prosedur
pengujian. Dibuat protap-protap untuk pengoperasian instrumen dan peralatan
serta dilekatkan pada dinding yang berdekatan dengan peralatan yang
bersangkutan. Perawatan dan kalibrasi instrumen dilakukan secara rutin dan
didokumentasikan, sedangkan verifikasi tetap dilakukan setiap hari sebelum
digunakan. Terdapat penandaan yang jelas tentang keadaan instrumen, apakah
berfungsi baik atau tidak. Tanggal dan waktu kalibrasi selanjutnya tertera pada
instrumen dengan jelas.
Penerimaan dan pembuatan pereaksi serta media biakan dicatat dalam buku
khusus. Pembuatan pereaksi dilakukan di laboratorium berdasarkan petunjuk
pembuatan yang tertulis dan setiap pereaksi diberi label yang sesuai seperti
konsentrasi, faktor standarisasi, batas waktu penggunaan, tanggal standarisasi
pembuat. Media biakan selalu dilakukan kontrol positif dan kontrol negatif untuk
membuktikan tidak adanya kesalahan terhadap interpretasi hasil pengujian.
Baku pembanding berada dalam tanggung jawab seseorang yang ditunjuk.
Baku pembanding disimpan ditempat dingin dan kering, serta digunakan secara
tepat, terdapat penandaan yang jelas berupa kode untuk menghindari kekeliruan.
Baku pembanding primer hanya digunakan untuk tujuan yang diuraikan
dalam monograf. Sedangkan baku sekunder atau baku pembanding kerja,
diturunkan dari baku pembanding primer secara periodik dan teratur untuk
mengkoreksi adanya penyimpangan selama penyimpanan.
Prosedur pengujian yang akan digunakan terlebih dahulu divalidasi dengan
memperhatikan fasilitas dan peralatan yang ada. Spesifikasi dan prosedur
pengujian untuk setiap bahan awal, produk antara, produk ruahan dan obat jadi
memuat ketentuan dan cara pemeriksaan serta pengujian identitas, kemurnian,
kualitas dan kadar atau potensi.
Prosedur pengujian memuat :
Jumlah contoh yang diperlukan
Banyaknya pereaksi yang digunakan untuk pengujian
Alat atau instrument yang digunakan
Rumus perhitungan yang digunakan
Pengujian dilakukan mengikuti instruksi pada prosedur pengujian untuk
masing-masing bahan atau produk dan diperiksa oleh supervisor. Catatan analisa
meliputi :
Nama dan nomor batch.
Nama petugas yang mengambil contoh.
Metoda analisa yang digunakan.
Perhitungan dalam unit ukuran, rumus yang digunakan dan range yang
diperbolehkan.
Kesimpulan (diterima atau ditolak).
Perhitungan dalam unit ukuran, rumus yang digunakan dan range yang
diperbolehkan.
Tanggal dan tanda tangan petugas yang melakukan pengujian.
Nama pemasok, jumlah keseluruhan dan jumlah bahan awal yang diterima.
Jumlah keseluruhan, wadah, bahan baku, bahan pengemas, produk antara,
produk ruahan dan obat jadi dari batch yang dianalisa.
Rujukan pustaka dari mana prosedur pengujian diambil.
Contoh pertinggal diberi identitas yang jelas, mewakili tiap batch bahan baku yang diterima, dan obat jadi dalam kemasan lengkap, disimpan dalam jangka
dengan label penandaan. Jumlah contoh pertinggal adalah minimal 3 kali jumlah
untuk pengujian lengkap.
Validasi yang dilakukan oleh PT. MUTIFA antara lain :
Prosedur penetapan kadar, untuk mengetahui ketelitian dan ketepatan
metode yang digunakan dalam memenuhi spesifikasi yang telah
ditetapkan.
Kalibrasi instrumen yang dipakai dalam pengujian, dilakukan secara
berkala untuk menjamin bahwa instrumen tersebut memberikan hasil
pengukuran dengan presisi dan akurasi yang tinggi.
Validasi proses. Validasi proses terdiri dari komposisi/formula, spesifikasi
bahan baku, bagan alur proses, perlengkapan dan peralatan terkait, sistem
penunjang, kondisi ruangan, proses pembuatan dan parameter kritis,
dokumentasi, stabilitas dan pengemasan.
Spesifikasi ditetapkan sendiri oleh pabrik yang telah memenuhi persyaratan
yang ada dalam farmakope dan senantiasa direvisi secara rutin. Spesifikasi dibuat
dalam bentuk dokumen dan disimpan tersendiri, yang meliputi :
Spesifikasi bahan baku
Spesifikasi produk antara
Spesifikasi produk ruahan
Pengambilan contoh dilakukan terhadap sebagian kecil dari batch yang ada. Contoh yang diambil hendaklah mewakili batch yang ada dan berdasarkan prosedur tetap yang telah dibuat. Untuk zat aktif yang harus diukur potensinya,
contoh diambil dari tiap wadah, sedangkan untuk bahan lain umumnya mengikuti
rumus n+1.
Pengambilan sampel dilakukan terhadap sebagian kecil dari batch yang ada. Sampel yang diambil hendaklah mewakili batch yang ada dan berdasarkan prosedur tetap yang telah dibuat. Jumlah sampel yang diambil mengikuti rumus
n+1.
Sampel bahan awal dan produk antara, diambil secara acak mewakili tiap
wadah menggunakan peralatan yang sesuai. Sedangkan untuk obat jadi diambil
pada proses awal, tengah, dan akhir. Pengambilan sampel dilakukan dengan tepat
untuk mencegah kontaminasi silang. Wadah untuk bahan yang sampel, diberi
label yang menunjukkan isi wadah, nomor batch, tanggal pengambilan dan tanda bahwa sampel telah diambil dari wadah tersebut. Pengambilan sampel bahan baku
dilakukan pada tempat yang bersih dan dilakukan pemeriksaan awal terlebih
dahulu sebelum pengambilan sampel.
Bahan baku yang akan diuji telah dilengkapi dengan sertifikat analisis dari
produsen atau supplier, bahan pengemas dilihat dari segi fisiknya. Pengawasan pada kemasan diperiksa oleh IPC sebelum kegiatan pengemasan berjalan, selama
proses berlangsung dan pada produk akhir yang sudah dikemas.
Untuk menjamin keseragaman batch, sampel diambil mewakili setiap batch
kualitasnya. Produk antara dan produk ruahan yang ditolak diberi penandaan dan
diawasi dengan sistem karantina.
Setiap batch obat jadi dilakukan pengujian terhadap spesifikasi yang ditetapkan. Sampel diambil pada awal, tengah dan akhir dengan jumlah tertentu
(sesuai prosedur yang ada) untuk diuji dan sebagai sampel pertinggal. Batch yang tidak memenuhi syarat, diselidiki kesalahannya dan dilakukan pengujian ulang
bersama bagian penelitian dan pengembangan. Bila dilakukan pengolahan ulang,
maka prosedur tersebut harus diperiksa dan disetujui oleh bagian QC.
Setiap bawan awal, produk antara, produk ruahan dan produk jadi yang telah
diuji dan memenuhi persyaratan yang ditetapkan diberi label ”DILULUSKAN”
Setiap bahan awal, produk antara, produk ruahan dan obat jadi telah
ditetapkan batas waktu penyimpanannya. Jika obat telah melewati batas waktu
penyimpanan, maka bagian QC akan melakukan untuk pengujian ulang
berdasarkan tanggal pengujian ulang. Jika masih memenuhi syarat maka bahan
diberi label ” DILULUSKAN”. Selain itu, jika suatu bahan disimpan pada lokasi
yang tidak tepat, maka bagian QC juga melakukan pengujian ulang untuk
memastikan mutu sediaan apakah masih memenuhi spesifikasi yang ditetapkan.
Bagian QC ikut berperan serta dalam pembuatan prosedur pengolahan induk
dan proses pengemasan. Setiap perubahan dan penyesuaian pada prosedur tersebut
harus disetujui oleh bagian QC sebelum ditetapkan. Selain itu, juga memberikan
Bagian QC memeriksa semua catatan produksi tiap batch obat untuk menentukan apakah proses pengolahan telah memenuhi semua prosedur yang
telah ditetapkan.
Untuk mengetahui stabilitas obat jadi, kondisi penyimpanan yang cocok dan
tanggal kadaluarsa maka QC menyusun protap untuk pengujian stabilitas obat.
Pengujian stabilitas obat meliputi:
• Jumlah contoh dan jadwal pengujian berdasarkan sifat zat yang diuji
• Kondisi penyimpanan
• Metode pengujian yang spesifik, bermakna, dan handal
• Pengujian produk dalam kemasan yang sama dengan kemasan produk
yang dipasarkan
• Pada obat jadi untuk rekonstursi, pengujian stabilitas dilakukan sebelum
dan sesudah rekonstusi.
Bagian QC bersama litbang bertanggung jawab dalam memilih pemasok
yang mampu dan dapat dipercaya dalam penyediaan bahan awal. Semua calon
pemasok dievaluasi secara berkala sebelum diberi pesanan. Inspeksi selalu
dilakukan terhadap kredibilitas pemasok. Inspeksi tersebut dilakukan bersama
litbang, bagian produksi, dan bagian pembelian. Selain itu mereka juga menilai
kualifikasi pemasok.
3.2.3 Quality Assurance (QA)
Pemastian Mutu adalah suatu konsep luas yang mencakup semua hal baik
secara tersendiri maupun secara kolektif, yang akan mempengaruhi mutu dari obat
dengan tujuan untuk memastikan bahwa obat yang dihasilkan dengan mutu yang
sesuai dengan tujuan pemakaiannya.
Tugas-tugas Bagian Pemastian Mutu mencakup :
a. Pengawasan terhadap bahan awal, termasuk di dalamnya bahan baku dan
bahan pengemas.
b. Pengawasan terhadap produk antara dan pengawasan selama proses (in process controls) serta validasi yang diperlukan dilakukan.
c. Pengkajian terhadap semua dokumen yang terkait dengan proses,
pengemasan dan pengujian bets, dilakukan sebelum memberikan
pengesahan pelulusan untuk distribusi.
d. Melakukan kualifikasi terhadap meliputi semua faktor yang relevan
termasuk kondisi pembuatan, hasil pengujian dan/atau pengawasan selama
proses, pengkajian dokumen produksi termasuk pengemasan, pengkajian
penyimpangan dari prosedur yg telah ditetapkan, pemenuhan dan
persyaratan dari spesifikasi produk jadi dan pemeriksaan produk dalam
kemasan akhir.
e. Menyediakan prosedur inspeksi diri dan/atau audit mutu yang secara
berkala mengevaluasi efektivitas dan penerapan sistem Pemastian Mutu.
f. Melaporkan, menyelidiki, dan mencatat apabila terjadi penyimpangan.
g. Mengevaluasi dan menyetujui pemasok bahan awal dan pengemas untuk
memenuhi spesifikasi mutu yang telah ditentukan oleh perusahaan.
h. Mengevaluasi dan menyetujui prosedur pengolahan ulang.
j. Mengevaluasi perubahan yang akan dilakukan yang dianggap berdampak
pada mutu produk.
k. Mengatur dan memastikan bahwa sedapat mungkin, produk disimpan,
didistribusikan dan selanjutnya ditangani sedemikian rupa agar mutu tetap
dijaga selama masa edar/simpan obat.
l. Meluluskan produk untuk didistribusikan dengan dasar tiap bets produksi
dibuat dan dikendalikan sesuai dengan persyaratan yang tercantum dalam
izin edar dan peraturan lain yang berkaitan dengan aspek produksi,
pengawasan mutu dan pelulusan produk.
m. Sarana penunjang, mesin-mesin dan personalia.
3.2.4 Gudang
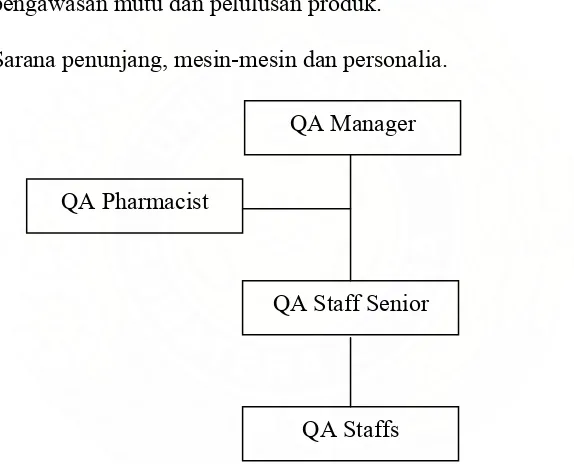
Gambar 3. Struktur Pemastian Mutu di PT. MUTIFA QA Manager
QA Pharmacist
QA Staff Senior
QA Staffs
Gudang bertugas melaksanakan penerimaan, penyimpanan, pemeliharaan
bahan baku, kemasan dan sediaan jadi. Gudang melaksanakan penyimpanan dan
pengeluaran bahan baku, sediaan jadi dan kemasan dengan memakai prinsip FIFO
sistem satu pintu. Pelaksanaan kegiatan di gudang adalahmenerima, menyimpan,
memelihara, menyalurkan bahan baku, bahan sediaan dan kemasan serta
melaksanakan administrasi penerimaan, penyimpanan, penyaluran sesuai
peraturan dan ketentuan yang berlaku.
Proses masuknya bahan baku ke gudang adalah :
Bahan dipesan dengan menggunakan Surat Pesanan (SP).
1. Barang yang masuk ke gudang disertai dengan sertifikat analisis (CA) dan
disesuaikan dengan SP.
2. Memeriksa kondisi fisik dari bahan tersebut.
3. Bon faktur ditandatangani oleh Kepala gudang, lalu diserahkan ke kasir
industri.
4. Bahan baku yang masuk tersebut langsung dibuat Bukti Barang Masuk
(BBM).
Selanjutnya bahan ini disimpan di karantina untuk dianalisis lebih lanjut.
Barang yang belum diperiksa atau dalam tahap pemeriksaan diberi label karantina.
Label karantina ini berwarna kuning berisi nama barang, jumlah, nomor batch
atau nomor order, tanggal diterima, unit penerimaan, tanda tangan. Barang yang
diluluskan diberi label “diluluskan” berwarna hijau dan berisi nama barang,
tanggal diterima, jumlah, pembuat/penyalur, nomor batch asal dan data yang diisi oleh Unit Quality Assurance (QA) (tanggal tes, nomor lot, tanda tangan dan tanggal kadaluarsa), sedangkan barang yang ditolak diberi label “ditolak” yang
Bahan baku atau kemasan dianalisis oleh Unit Quality Control (QC) setelah menerima Surat Pengiriman contoh bahan baku atau kemasan. Unit ini bertugas
memberikan persetujuan atau penolakan terhadap bahan baku atau kemasan
berdasarkan hasil analisis. Bahan baku atau kemasan yang diluluskan oleh Unit
Quality Assurance (QA) akan merobek label “karantina”, menempelkan label “diluluskan” yang berwarna hijau dan ditempatkan di daerah yang diluluskan.
Bahan baku atau kemasan yang ditolak oleh Unit Quality Assurance (QA) akan merobek label “karantina” dan menempelkan label “ditolak” yang berwarna
merah serta menempatkan di daerah ditolak. Khusus bahan baku dan kemasan
yang ditolak, Unit Quality Assurance (QA) harus membuat surat penolakan kepada pemasok dengan menyebutkan alasan penolakan. Barang yang sesuai
dengan spesifikasi atau persyaratan selanjutnya disimpan di gudang obat
jadi/bahan baku dan dibuat berita acara penerimaan barang.
Bahan baku, sediaan jadi maupun kemasan yang disimpan di gudang
memiliki kartu stok yang berfungsi sebagai kontrol dan memudahkan pemeriksaan
jika ada kekeliruan. Untuk penyimpanan bahan baku disusun berdasarkan jenis
bahan baku, sedang untuk bahan baku cair dan beta laktam disimpan terpisah.
Untuk penyimpanan kemasan disusun berdasarkan jenis dan bentuknya, sehingga
mudah dalam pengambilan maupun penyusunannya.
Masuknya obat jadi/sediaan jadi di gudang obat jadi berasal dari hasil
produksi diserahkan oleh kepala unit produksi kepada kepala gudang obat jadi.
Kemudian kepala gudang obat jadi membuat surat Bukti Penyerahan Hasil
Produksi (BPHP) yang menerangkan nama obat jadi, kemasan, jumlah, nomor
jadi berdasarkan fungsi farmakologis obat, alfabetis dan bentuk sediaan guna memudahkan dalam pencarian. Jadi untuk proses administrasi, masing-masing
kepala gudang tersebut membuat laporan masuk atau keluarnya bahan baku, obat
jadi dan kemasan secara komputerisasi maupun manual.
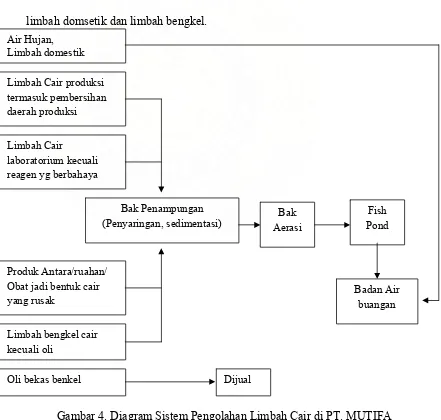
3.2.5 Limbah
Limbah Non Beta Laktam
Jenis limbah di PT. MUTIFA ada 3 jenis yaitu :
1. Limbah cair, limbah ini berasal dari limbah produksi, limbah laboratorium,
limbah domsetik dan limbah bengkel.
Air Hujan, Obat jadi bentuk cair yang rusak
Badan Air buangan
Limbah bengkel cair kecuali oli
Oli bekas benkel Dijual
Limbah laboratorium yang mengandung sisa bahan berbahaya ditampung
dalam wadah tertutup rapat dan diberi tanda yang jelas menyatakan jenis dan
penggolongan resiko limbah tersebut.
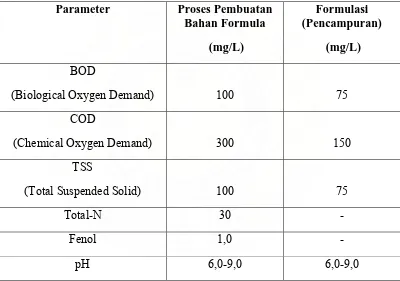
Tolak ukur yang dipakai untuk pemantauan limbah cair adalah
berdasarkan baku mutu air limbah yang disyaratkan dalam Surat Keputusan
Menteri Negara Kependudukan dan Lingkungan Hidup No. 03/Men KLH/II/1991
seperti yang terdapat dalam tabel berikut :
Parameter Proses Pembuatan
Bahan Formula
(Biological Oxygen Demand) 100 75
COD
(Chemical Oxygen Demand) 300 150
TSS
(Total Suspended Solid) 100 75
Total-N 30 -
Fenol 1,0 -
pH 6,0-9,0 6,0-9,0
Tabel 4. Tolak Ukur yang dipakai untuk Pemantauan Limbah Cair
2. Limbah Padat, berasal dari kemasan bahan awal (bahan baku/bahan
kemasan), buangan proses produksi, bahan awal yang rusak, produk obat
Dust Collector Debu Produksi
Vacum Cleaner
3. Limbah Udara, berasal dari gas, uap dan asap dari bahan kimia, bahan
baku dan proses produksi, pembakaran zat padat, debu produksi,
suara/getaran mesin. Limbah ini sebagian berbahaya, sebagian tidak
berbahaya.
Sistem penanggulan limbah udara antara lain pada tabel berikut :
Jenis Cara Pengendalian
1. Suara/getaran mesin produksi
2. Suara/blowdown steam boiler
3. Gas/asam laboratorium
4. Asap pembakaran sampah
5. Uap solven/uap sair
1. Pemasangan partieal enclosure dan pemakaian inert oleh pekerja
2. Pemasangan bak penangakap uap
3. Lemari Asam
4. Incenerator cerobong tinggi
5. Exhaust fan dengan sistem penangkap uap
Debu Lantai
Limbah Domestik
Bahan baku, produk antara, ruahan dan produk jadi yang rusak
Incenerator
Tong/Vat karton
Pembuangan terakhir milik PEMDA Aluoil, botol, pot plastic, yang rusak
atau sisa cetakan lama
Kertas karton&plastic yang tidak penandaan nama pabrik, botol kada rusak
Dijual Kemasan bahan awal
Limbah Beta Laktam
Jenis limbah beta laktam dapat berupa limbah cair, padat dan udara. Limbah
cair berasal dari gedung produksi beta laktam berupa pencucian alat/mesin,
pembersihan ruangan, meja dan kursi serta loundry. Limbah padat berupa wadah
bekas bahan baku antibiotik beta laktam, bahan baku beta laktam yang rusak,
buangan proses produksi dan produk jadi antibiotika beta laktam yang rusak.
Limbah udara berupa debu produksi antibiotika beta laktam. Kesemua limbah ini
memiliki sifat yang berbahaya.
Pengelolaan Limbah Beta Laktam:
1. Limbah Cair
Limbah cair yang berasal dari gedung beta laktam dialirkan ke
bak/kolam perusakan cincin beta laktam dengan menggunakan larutan
NaOH, setelah itu dialirkan/digabung dengan limbah cair non beta laktam di
bak penampungan, dan seterusnya diolah bersama.
2. Limbah Padat
Limbah padat yang berupa wadah yang mengandung bahan antibiotika
beta laktam dicuci dan dibilas bersih dengan air bersih diruang pencucian di
dalam gedung beta laktam. Air pencucian tersebut merupakan limbah cair
dari gedung beta laktam yang dialirkan ke bak perusak cincin beta laktam,
sedangkan wadah yang telah dicuci dan dibilas bersih tersebut dikeluarkan
dari gedung beta laktam dan ditangani limbahnya seperti pada pengelolaan
3. Limbah Udara
Limbah udara berupa debu produksi disedot dan dikumpulkan oleh dust collector. Cara pembuangan limbah debu produksi yang dikumpulkan oleh
dust collector pada gedung beta laktam adalah sebagai berikut :
Catridge atau filter dust collector dilepas, kemudian dimasukkan ke
dalam kantong dan diikat.
Filter yang sudah terbungkus dan terisolasi kemudian dibawa ke ruang
khusus yang dipersiapkan untuk melebur/melarutkan limbah debu dari
filter dust collector.
Kantong yang terisi filter dust collector tersebut dibuka kemudian
dilarutkan kedalam air yang kemudian air tersebut dialirkan ke kolam
pengolahan limbah gedung beta laktam untuk dinetralisir. Kemudian
filter yang sudah bersih dibakar bersama limbah padat non beta laktam
BAB IV
PEMBAHASAN
Industri farmasi sebagai produsen obat-obatan harus dapat menjamin bahwa
produk yang dihasilkan memenuhi persyaratan mutu dan terus menjaga
konsistensi mutunya dalam setiap pembuatan. Salah satu pedoman yang
digunakan industri farmasi untuk menghasilkan produk yang bermutu adalah Cara
Pembuatan Obat yang Baik (CPOB).
PT. MUTIFA Medan sebagai salah satu PMDN yang memproduksi obat
telah menerapkan CPOB sejak bulan April tahun 1994. Penerapan CPOB dan
seluruh aspek rangkaian produksi merupakan suatu langkah untuk menjamin mutu
obat jadi, sehingga memenuhi persyaratan yang ditentukan sesuai dengan tujuan
penggunaannya.
Dalam prosesnya, mutu dalam produk harus dibentuk di dalam produk
tersebut, tidak cukup hanya lulus dari pemeriksaan mutu. Sehingga dalam
pelaksanaannya diperlukan kondisi yang dikendalikan dengan pengawasan yang
menyeluruh untuk menjamin bahwa konsumen menerima obat yang bermutu.
Aspek-aspek yang mempengaruhi proses pembentukan mutu terhadap
produk tertuang dalam aspek-aspek yang harus diperhatikan dalam CPOB. Selama
Praktek Kerja Profesi (PKP) Apoteker dilakukan pengamatan terhadap proses
4.1 Personalia
Struktur organisasi perusahaan pada bagian produksi dan pada bagian
pengawasan mutu dipimpin oleh orang yang berbeda, dimana masing-masing
diberi wewenang dan tanggung jawab untuk dapat melaksanakan tugasnya secara
efektif, serta tidak mempunyai kepentingan lain di luar pabrik yang dapat
membatasi tanggung jawabnya.
Untuk membantu tenaga di atas, ditunjuk tenaga yang terampil yang sesuai
untuk melaksanakan pengawasan langsung di bagian produksi dan pengawasan
mutu.
Pada saat perekrutan karyawan, dilakukan pemeriksaan kesehatan fisik
maupun mental untuk menjamin karyawan mampu mengikuti peraturan CPOB
dan perkembangan yang ada. Selain itu, untuk terus meningkatkan pemahaman
karyawan tentang pentingnya penerapan CPOB, maka dilakukan pelatihan setahun
sekali.
Berdasarkan pengamatan selama melakukan Praktek Kerja Profesi di PT.
MUTIFA Medan, dijumpai beberapa permasalahan terkait personalia antara lain
tingkat kesadaran dan kedisiplinan karyawan masih kurang untuk melaksanakan
CPOB. Hal ini dapat dilihat dimana karyawan masih kurang menyadari
pentingnya penggunaan perlengkapan kerja seperti pakaian kerja, sarung tangan,
penutup kepala dan masker dalam proses produksi untuk mencegah kontaminasi
4.2 Bangunan dan Fasilitas
Lokasi PT. MUTIFA Medan dibangun di kawasan yang jauh dari pusat kota
dan keramaian. Sumber cemaran yang tidak dapat dihindari adalah pencemaran
udara. Pencemaran udara dapat diminimalkan dengan sistem HVAC, dimana
udara yang masuk di-filter terlebih dahulu.
Desain, konstruksi, dan tata letak ruangan PT. MUTIFA Medan disesuaikan
dengan persyaratan CPOB sehingga memudahkan pelaksanaan produksi dan
perawatan. Bangunan produksi antibiotik beta laktam terpisah dengan bangunan
produksi non beta laktam. Serta tata letak ruangnya mengikuti alur produksi
sehingga mencegah terjadinya kontaminasi silang.
Bagian gudang masih perlu dibenahi, yaitu dari segi kapasitas gudang dan
jumlah bahan yang disimpan. Misalnya pada gudang kemasan yang luasnya masih
kurang memadai dibanding dengan jumlah bahan pengemas yang disimpan,
sehingga ada beberapa bahan pengemas yang ditumpuk dengan jumlah tumpukan
yang tidak sesuai.
4.3 Peralatan
PT. MUTIFA Medan seiring dengan peningkatan kapasitas produksi pabrik
baik dari segi jumlah maupun jenis produknya berupaya menambah dan
memperbaiki peralatan yang ada sehingga dapat menghasilkan produk yang sesuai
dengan persyaratan dan tujuan penggunaanya.
Menurut pengamatan kami, peralatan yang ada telah dikalibrasi sesuai
produk yang dihasilkan tetap baik, namun ada beberapa mesin yang kemampuan
produksinya tidak maksimal, seperti mesin-mesin pengemas sehingga
menyebabkan waktu kerja karyawan menjadi tidak efektif dan efisien.
4.4 Sanitasi dan Higiene
PT. MUTIFA Medan berupaya menerapkan sanitasi dan higiene meliputi
personalia, bangunan, dan peralatan. Semua karyawan menjalankan pemeriksaan
kesehatan sebelum dan selama bekerja. Setiap personil harus menerapkan higiene
perorangan, seperti memakai pakaian pelindung sesuai dengan kelas
kebersihannya dan mencuci tangan sebelum masuk ruang produksi.
Sanitasi bangunan dilakukan dengan jadwal yang rutin dan teratur. Tersedia
locker untuk setiap karyawan dan tersedia kantin yang terpisah dari ruang produksi.
Peralatan yang telah selesai digunakan dibersihkan baik bagian dalam
maupun luar sesuai prosedur yang ditetapkan. Prosedur pembersihan dan sanitasi
peralatan telah dibuat secara rinci dan ditaati.
4.5 Produksi
Proses produksi dilakukan sesuai dengan catatan pengolahan batch dan catatan pengemasan batch. Pada setiap tahapan dilakukan dengan memperhatikan kesiapan jalur dan dilaksanakan sesuai prosedur yang ditetapkan. Selama proses
produksi maupun pengemasan, selalu dilakukan In Process Control (IPC) sebagai suatu bentuk pengawasan mutu produk. IPC yang dilakukan adalah evaluasi
Untuk mencegah kesalahan dan mix up produk, dilakukan penandaan identitas yang jelas beserta tahapan produksinya pada setiap wadah, alat, dan
ruangan yang sedang dipakai dalam proses produksi.
Penanganan penimbangan, penghitungan dan penyerahan bahan baku, bahan
pengemas, produk antara dan produk ruahan dan produk jadi harus
didokumentasikan.
4.6 Pengawasan Mutu
Bagian QC adalah bagian yang independen dan bertanggung jawab langsung
kepada direktur pabrik. Letak laboratorium bersebelahan dengan ruang produksi
yang dipisahkan oleh dinding dan kaca. QC memiliki laboratorium kimia dan
biologi yang memiliki ruangan yang terpisah dengan fasilitasnya masing-masing.
4.7 Inspeksi Diri
PT. MUTIFA Medan melakukan inspeksi diri dan audit mutu yang meliputi
seluruh aspek-aspek CPOB. Inspeksi diri dilakukan oleh tim inspeksi yang
dibentuk perusahaan dari masing-masing bagian. Audit mutu dilakukan minimal
satu kali setahun dengan panitia audit. Hasil dari audit ini akan dievaluasi dan
dibuat laporannya untuk kemudian dilakukan perbaikan.
4.8 Penanganan Keluhan, Penarikan Obat yang Beredar, dan produk kembalian
Dalam proses pembentukan mutu, memerlukan alur pemberian informasi
sehingga tidak menimbulkan kerugian bagi semua pihak baik konsumen maupun
perusahaan. Penanganan terhadap keluhan ditangani oleh bagian QA.
4.9 Dokumentasi
Seluruh proses yang dijalankan harus sesuai dengan instruksi yang rinci dan
jelas (prosedur tetap) kemudian mendokumentasikannya pada catatan pengolahan
dan pengemasan batch. Dokumen ini akan diperiksa oleh bagian QC untuk meluluskan produk jadi dan kemudian disimpan sebagai riwayat lengkap dari
setiap batch produk sehingga memudahkan dalam penyelidikan dan penelusuran terhadap batch yang bersangkutan.
4.10 Pengamatan Pengolahan Limbah
PT. MUTIFA Medan memiliki instalasi pengolahan limbah. Hasil
pengamatan kami pada bak VI (Fish Pond) yang seharusnya sebagai bak
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Setelah melaksanakan Praktek Kerja Profesi (PKP) Apoteker di PT. Mutiara
Mukti Farma (MUTIFA) dapat diambil kesimpulan sebagai berikut :
a. Praktek Kerja Profesi sangat membantu mahasiswa apoteker untuk lebih
memahami penerapan CPOB dan menambah wawasan yang lebih luas
mengenai semua kegiatan di industri farmasi.
b. PT. MUTIFA Medan telah menerapkan ketentuan Cara Pembuatan Obat
yang Baik (CPOB) sesuai dengan Keputusan Menteri Kesehatan RI No.
43/Menkes/SK/II/1988 tentang CPOB.
c. PT. MUTIFA memiliki komitmen yang kuat dalam menerapkan CPOB
secara konsisten dan kontinu dalam semua aspek kegiatan guna
mengutamakan mutu dari produk yang dihasilkan. Mutu obat telah
dibentuk mulai dari awal proses produksi dengan memenuhi persyaratan
CPOB, sehingga tidak hanya ditentukan dengan pengujian produk jadi
saja.
5.2 Saran
a. PT. MUTIFA hendaknya mengirim tenaga/staf untuk mengikuti pelatihan
CPOB dan diharapkan dapat memberikan pengarahan dan pelatihan
kepada karyawan di setiap unit produksi secara berkesinambungan.
b. PT. MUTIFA hendaknya menindak tegas para karyawan yang melanggar
c. Untuk menjaga kelancaran proses produksi sebaiknya PT. MUTIFA
menyediakan suku cadang dan mesin serta melaksanakan latihan terhadap
teknisi untuk meningkatkan keterampilan dan pengetahuan tentang
peralatan dan mesin.
d. Hendaknya PT. MUTIFA meningkatkan inspeksi diri dengan cara menilai
apakah seluruh aspek produksi dan pengendalian mutu telah selalu
memenuhi CPOB.
e. Untuk meningkatkan kualitas obat dan mengantisipasi perkembangan di
masa yang akan datang terutama di bidang tekhnologi formulasi dan
mikrobiologi, sebaiknya PT. MUTIFA meningkatkan sumber daya
manusianya dengan mengirimkan tenaga-tenaga ahlinya (profesional)
DAFTAR PUSTAKA
Badan POM (2006). Pedoman Cara Pembuatan Obat yang Baik, Jakarta.
Badan POM (2001). Petunjuk Operasional Penerapan Cara Pembuatan Obat yang Baik, Jakarta.
Depkes RI (1992). Undang-undang Kesehatan no. 23
Depkes RI (1990). Permenkes RI No. 57/Menkes/Per/III/1990 tentang Analisa Mengenai Dampak Lingkungan, Jakarta.
Depkes RI (1990). Surat Keputusan Menteri Kesehatan RI No. 245/Menkes/
SK/V/1990 tentang Ketentuan dan Tata Cara Pelaksanaan Pemberian Izin Usaha Industri Farmasi, Jakarta.
Depkes RI (1990). Permenkes RI No. 286/Menkes/Per/III/1990 tentang Kegiatan di Bidang Kesehatan yang Wajib Membuat AMDAL, Jakarta.
Depkes RI (1979). Farmakope Indonesia, Edisi III, Jakarta.
Depkes RI (1995). Farmakope Indonesia, Edisi IV, Jakarta.
Lampiran 1. Struktur Organisasi PT. MUTIFA Medan
ASS. MANAGER PRODUKSI PENGAWAS PRODUKSI