LAPORAN PRAKTEK KERJA PROFESI FARMASI INDUSTRI
di
PT. Mutiara Mukti Farma (MUTIFA) Medan
Disusun oleh:
Deddy R. Hutagalung, S. Farm. NIM 083202110
PROGRAM PENDIDIKAN PROFESI APOTEKER FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2010
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa atas limpahan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan Praktek Kerja Profesi (PKP) di Industri Farmasi PT. Mutiara Mukti Farma (MUTIFA) Medan dan penyusunan laporan ini.
Pada kesempatan ini, penulis menyampaikan terima kasih yang
sebesar-besarnya kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara.
2. Bapak Drs. Wiryanto, M.S.,Apt., selaku Koordinator Program Studi Pendidikan Profesi Apoteker Fakultas Farmasi Universitas Sumatera Utara 3. Bapak Jacob selaku Direktur Utama PT. MUTIFA Medan yang telah
berkenan memberikan fasilitas kepada penulis untuk melaksanakan Praktek Kerja Profesi (PKP).
4. Ibu Betty, S.Si., Apt., selaku Manager Quality Assurance (QA) yang telah membimbing dan mengarahkan penulis selama melaksanakan Praktek Kerja Profesi (PKP).
5. Bapak Donald Situmeang, S.Si., Apt., selaku Manager Produksi Solid Non Beta Laktam dan sebagai pembimbing dan memberikan fasilitas serta mengarahkan penulis selama melaksanakan Praktek Kerja Profesi (PKP) di PT. MUTIFA.
telah membimbing dan mengarahkan penulis selama melaksanakan Praktek Kerja Profesi (PKP).
7. Ibu Dra. Nuranti Sirait selaku Manager Quality Control (QC) yang telah membimbing dan mengarahkan penulis selama melaksanakan Praktek Kerja Profesi (PKP).
8. Bapak Amiruddin, S.H, Selaku manager personalia yang telah membantu kami melaksanakan praktek kerja profesi.
9. Ibu Erika Hutajulu, S. Farm., Apt., selaku Supervisor Research and Development (R & D) PT. MUTIFA Medan yang telah membimbing dan mengarahkan penulis selama melaksanakan Praktek Kerja Profesi (PKP). 10. Saudara Edi Jones, Amd, selaku Kabag PPIC dan Saudari Melya Utami,
S.Farm., Apt., selaku Supervisor QC, Saudari Herawati, SH, selaku Kabag GBK (Gudang Bahan Kemasan) yang telah membantu dan mengarahkan penulis selama melaksanakan Praktek Kerja Profesi (PKP).
11. Seluruh staf dan karyawan PT. MUTIFA Medan atas perhatian dan bantuan yang diberikan kepada penulis selama melaksanakan Praktek Kerja Profesi (PKP).
Penulis menyadari atas kekurangan dalam penulisan laporan ini, untuk itu diharapkan kritik dan saran yang membangun demi kesempurnaan laporan ini..
Medan, Januari 2010 Penulis
(Deddy R. Hutagalung, S.Farm)
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
LEMBAR PENGESAHAN... ii
KATA PENGANTAR... iii
DAFTAR ISI... v
DAFTAR GAMBAR... viii
DAFTAR TABEL... ix
DAFTAR LAMPIRAN... x
RINGKASAN... xi
BAB I PENDAHULUAN... 1
1.1 Latar Belakang ... 1
1.2 Tujuan ... 1
1.3 Manfaat ... 2
1.4 Tempat dan Waktu ... 2
BAB II TINJAUAN UMUM ... 3
A. Industri Farmasi ... 3
B. Cara pembuatan Obat yang Baik (CPOB) ………. 3
1. Manajemen Mutu ……… 4
3. Bangunan dan Fasilitas ………... 7
4. Peralatan ………... 9
5. Sanitasi dan Higiene ... 9
6. Produksi ... 10
7. Pengawasan Mutu ……… 14
8. Inspeksi Diri dan Audit Mutu …... 15
9. Penanganan Keluhan terhadap Produk Penarikan Kembali Produk dan Produk Kembalian ... 15
10. Dokumentasi ... 17
11. Pembuatan dan Analisa Berdasarkan Kontrak ... 18
12. Kualifikasi dan Validasi ... 19
BAB III TINJAUAN KHUSUS PT. MUTIFA ... 22
A. Sejarah ... 22
B. Lokasi dan Sarana Produksi ... 23
1. Lokasi ... 23
2. Sarana Produksi ... 25
C. Struktur Organisasi ... 26
1. Departemen Produksi... 26
2. Departemen Pemastian Mutu/Quality Assurance (QA) .. 28
3. Departemen Pengawasan Mutu/Quality Control (QC) ... 29
4. Departemen Research and Development (R&D)………. 30
5. Departemen Personalia ……... 30
6. Departemen Keuangan …... 31
8. Departemen Production Planning and Inventory
Control (PPIC)………. 31
D. Limbah ... 33
BAB IV PEMBAHASAN ………. 38
BAB V KESIMPULAN DAN SARAN... 47
A. Kesimpulan ... 47
B. Saran ... 47
DAFTAR PUSTAKA ... 48
LAMPIRAN... 49
DAFTAR GAMBAR
Halaman
Gambar 1. Bagan Aspek yang Saling Berkaitan Membangun
Manajemen Mutu ... 6
Gambar 2. Denah Lokasi PT. MUTIFA ……….... 23
Gambar 3. Struktur Organisasi Departemen R & D di PT. MUTIFA... 30
Gambar 4. Diagram Sistem Pengolahan Limbah Cair di PT.MUTIFA... 33
DAFTAR TABEL
Halaman
Tabel 1. Ukuran Ruangan Masing-Masing Bagian di PT. MUTIFA…….. 24
Tabel 2. Tolak Ukur Pemantauan Limbah Cair di PT. MUTIFA………… 34
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Struktur Organisasi PT. MUTIFA ... 49
Lampiran 2. Status dan Jumlah Personil di PT.MUTIFA ……….... 50
Lampiran 3. Personalia PT Mutifa Medan Berdasarkan Jenjang Pendidikan. ... 51
Lampiran 4. Bagan Proses Pembuatan Tablet/Kaplet... 52
Lampiran 5. Bagan Proses Pembuatan Liquida ... 53
Lampiran 6. Bagan Proses Pembuatan Kapsul ... 54
RINGKASAN
Telah dilakukan Praktek Kerja Profesi (PKP) di Industri Farmasi PT.Mutiara Mukti Farma (MUTIFA) Medan yang merupakan salah satu program dalam pendidikan profesi apoteker, yang bertujuan agar mahasiswa/mahasisiwi mengetahui dan memahami tugas dan fungsi apoteker dalam industri farmasi, yang diharapkan dapat sebagai bekal untuk menghadapi dunia kerja yang sesungguhnya. Mahasiswa juga diharuskan dapat memperoleh wawasan dan pengetahuan yang lebih luas, memahami penerapan CPOB di PT. MUTIFA Medan, serta mengetahui gambaran tentang situasi dan kondisi kerja di PT. MUTIFA Medan.
PKP di Industri Farmasi PT. MUTIFA Medan dilaksanakan pada tanggal 16 November 2009 hingga 30 November 2009 dengan jumlah jam efektif 300 jam. Kegiatan yang dilakukan selama PKP di Industri antara lain membuat catatan kegiatan harian yang berisi absensi, dan materi kegiatan yang ditandatangani oleh pembimbing, pengamatan kegiatan produksi di bagian Beta Laktam dan Non Beta laktam (NBL), Laboratorium Quality Control (QC), Gudang Bahan Baku, Gudang Bahan Kemasan, dan Gudang Obat Jadi, sistem pengolahan air untuk produksi, sistem pengaturan udara (AHS), sistem pengolahan limbah, dan Laboratorium Research and Develepment (R & D).
RINGKASAN
Telah dilakukan Praktek Kerja Profesi (PKP) di Industri Farmasi PT.Mutiara Mukti Farma (MUTIFA) Medan yang merupakan salah satu program dalam pendidikan profesi apoteker, yang bertujuan agar mahasiswa/mahasisiwi mengetahui dan memahami tugas dan fungsi apoteker dalam industri farmasi, yang diharapkan dapat sebagai bekal untuk menghadapi dunia kerja yang sesungguhnya. Mahasiswa juga diharuskan dapat memperoleh wawasan dan pengetahuan yang lebih luas, memahami penerapan CPOB di PT. MUTIFA Medan, serta mengetahui gambaran tentang situasi dan kondisi kerja di PT. MUTIFA Medan.
PKP di Industri Farmasi PT. MUTIFA Medan dilaksanakan pada tanggal 16 November 2009 hingga 30 November 2009 dengan jumlah jam efektif 300 jam. Kegiatan yang dilakukan selama PKP di Industri antara lain membuat catatan kegiatan harian yang berisi absensi, dan materi kegiatan yang ditandatangani oleh pembimbing, pengamatan kegiatan produksi di bagian Beta Laktam dan Non Beta laktam (NBL), Laboratorium Quality Control (QC), Gudang Bahan Baku, Gudang Bahan Kemasan, dan Gudang Obat Jadi, sistem pengolahan air untuk produksi, sistem pengaturan udara (AHS), sistem pengolahan limbah, dan Laboratorium Research and Develepment (R & D).
PENDAHULUAN
1.1 Latar Belakang
Industri farmasi merupakan salah satu tempat bagi profesi apoteker untuk
melakukan pekerjaan kefarmasian terutama menyangkut pengadaan, pengendalian
mutu sediaan farmasi, penyimpanan, pendistribusian dan pengembangan obat.
Kemampuan seorang apoteker dalam mengelola industri farmasi merupakan
faktor yang sangat penting untuk keberhasilan industri.
Kedudukan apoteker diatur oleh peraturan pemerintah yang dituangkan
dalam Pedoman Cara Pembuatan Obat yang Baik (CPOB), yaitu apoteker
berperan sebagai penanggung jawab produksi dan pengendalian mutu. Untuk
menghasilkan sediaan obat jadi yang memenuhi persyaratan yang telah ditetapkan
sesuai dengan tujuan penggunaannya, maka setiap industri farmasi wajib
menerapkan Cara Pembuatan Obat yang Baik (CPOB) dalam seluruh aspek dan
rangkaian kegiatan produksi. Dalam hal ini sangat diperlukan Apoteker
profesional, yaitu Apoteker yang mempunyai Ilmu pengetahuan dan keahlian
tinggi serta mempunyai wawasan luas.
Dalam pelaksanaan Praktek Kerja Profesi di industri farmasi, Fakultas
Farmasi USU menjalin kerjasama dengan PT. Mutiara Mukti Farma (MUTIFA).
1.2 Tujuan
Adapun tujuan Praktek Kerja Profesi Apoteker Fakultas Farmasi
Universitas Sumatera Utara di Industri Farmasi Medan adalah :
1. Mengetahui dan memahami tugas, fungsi dan tanggung jawab apoteker di
Industri Farmasi.
2. Membekali calon apoteker agar memiliki wawasan, pengetahuan,
keterampilan dan pengalaman praktis untuk melakukan pekerjaan
kefarmasian, serta memahami penerapan CPOB di Industri Farmasi.
3. Mengetahui gambaran tentang situasi dan kondisi kerja di Industri Farmasi
4. Memberi kesempatan kepada calon apoteker untuk melihat dan mempelajari
5. Mempersiapkan calon apoteker dalam memasuki dunia kerja
1.3 Manfaat
Adapun manfaan Praktek Kerja Profesi Apoteker di Industri Farmasi
Medan adalah:
1. Mengetahui, memahami tugas dan tanggung jawab apoteker dalam
menjalankan pekerjaan kefarmasian di industri farmasi.
2. mendapatkan pengalaman praktis mengenai pekerjaan kefarmasian di
industri farmasi.
3. meningkatkan rasa percaya diri untuk menjadi apoteker yang profesional
di industri.
1.4 Tempat dan Waktu
Praktek Kerja Profesi industri farmasi dilaksanakan di PT. Mutiara Mukti
Farma (MUTIFA) Jalan Karya Jaya No. 68 Km 8,5 Namorambe Medan, pada
tanggal 16 November 2009 sampai 30 November 2009.
RINGKASAN
Telah dilakukan Praktek Kerja Profesi (PKP) di Industri Farmasi
PT.Mutiara Mukti Farma (MUTIFA) Medan yang merupakan salah satu program
dalam pendidikan profesi apoteker, yang bertujuan agar mahasiswa/mahasisiwi
mengetahui dan memahami tugas dan fungsi apoteker dalam industri farmasi,
yang diharapkan dapat sebagai bekal untuk menghadapi dunia kerja yang
sesungguhnya. Mahasiswa juga diharuskan dapat memperoleh wawasan dan
pengetahuan yang lebih luas, memahami penerapan CPOB di PT. MUTIFA
Medan, serta mengetahui gambaran tentang situasi dan kondisi kerja di PT.
MUTIFA Medan.
PKP di Industri Farmasi PT. MUTIFA Medan dilaksanakan pada tanggal
16 November 2009 hingga 30 November 2009 dengan jumlah jam efektif 300
jam. Kegiatan yang dilakukan selama PKP di Industri antara lain membuat
catatan kegiatan harian yang berisi absensi, dan materi kegiatan yang
ditandatangani oleh pembimbing, pengamatan kegiatan produksi di bagian Beta
Laktam dan Non Beta laktam (NBL), Laboratorium Quality Control (QC),
Gudang Bahan Baku, Gudang Bahan Kemasan, dan Gudang Obat Jadi, sistem
pengolahan air untuk produksi, sistem pengaturan udara (AHS), sistem
pengolahan limbah, dan Laboratorium Research and Develepment (R & D).
BAB III
TINJAUAN KHUSUS
PT. MUTIFA (MUTIARA MUKTI FARMA) MEDAN
A. Sejarah
Pada tahun 1975 didirikan Industri Farmasi di kota Medan dengan nama
“Sejati Pharmaceutical Industries”, yang memproduksi obar merek “SIAGOGO”.
Setelah beberapa tahun berproduksi, perusahaan ini kemudian dialihkan
pemiliknya kepada Bapak Drs. W. H. Siahaan dan memindahnamakan perusahaan
tersebut dalam suatu akte notaris tertanggal 31 Januari 1980 dengan nama PT.
Mutiara Mukti Farma (MUTIFA) yang berlokasi di Jl. Brigjen Katamso No. 220
Medan.
Berdasarkan Surat Keputusan Menteri Kesehatan RI tahun 1981 No.
0098/SK/PAB/81 memutuskan memberikan izin untuk mendirikan pabrik farmasi
kepada PT. Mutiara Mukti Farma (MUTIFA) dengan nama “MUTIFA
INDUSTRI FARMASI” untuk memproduksi obat-obatan. Dengan dikeluarkannya
surat izin produksi oleh Departemen Kesehatan RI c/q Badan Pengawasan Obat
dan Makanan No. 213/AA/III/81, mulailah PT Mutiara Mukti Farma
memproduksi obat-obatan.
Pada tahun 1983, perusahaan ini menjalankan dan melaksanakan
operasinya dalam menghasilkan berbagai jenis maupun bentuk sediaan obat untuk
memenuhi kebutuhan masyarakat Indonesia wilayah barat umumnya dan daerah
Sumatera Utara pada khususnya.
Pada tanggal 29 November 1988, dengan akte notaris No. 35 diadakanlah
perubahan akte atas pemegang saham serta manajemen perusahaan, yang
ditetapkan melalui keputusan Menteri Kehakiman RI No. C2-1134.HT.01.04 th 89
tanggal 31 Januari 1989. Dalam akte tersebut, berdasarkan keputusan rapat Dewan
Komisaris serta pemegang saham, ditetapkan bahwa yang menjadi penanggung
jawab dengan jabatan Direktur Utama adalah Bapak Jacob.
Sesuai dengan Keputusan Menteri Kesehatan RI No.
43/Menkes/SK/II/1988 tentang Pedoman Cara Pembuatan Obat yang Baik
maka untuk memenuhi ketentuan tersebut PT. MUTIFA telah membangun pabrik
yang baru di Jl. Karya Jaya No. 68 Km 8,5 Namorambe. Pada bulan Mei 1994
produksi telah dilaksanakan di pabrik yang baru dan pada saat ini kegiatan
administrasi juga telah dilakukan di lokasi tersebut. Pada tanggal 27 Juli 1994 PT.
MUTIFA diberikan sertifikat sebagai industri farmasi yang telah memenuhi
CPOB.
Bentuk sediaan yang telah diproduksi sampai saat ini adalah tablet, sirup,
salep, bedak dan kapsul sebanyak 114 item. Pendistribusian sediaan yang
diproduksi PT. MUTIFA Medan meliputi wilayah : Provinsi Sumatera Utara,
Riau, Sumatera Selatan, Daerah Khusus Ibukota (DKI) Jakarta, Jawa Barat, Jawa
Tengah, Jawa Timur, Sulawesi Utara, dan Sulawesi Selatan. Untuk wilayah
Sumatera, obat didistribusikan melalui Pedagang Besar Farmasi (PBF) Mekada
Abadi. Obat-obatan diproduksi berdasarkan sistem skala prioritas, yang
mengutamakan obat yang lebih cepat laku di pasaran. Hal ini tidak berlaku untuk
obat Inpres dan Askes.
B. Lokasi dan Sarana Produksi 1. Lokasi
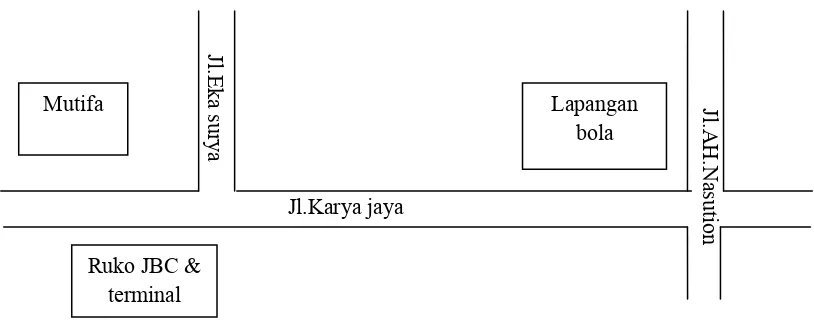
PT. MUTIFA Medan berada di Jl. Karya Jaya No. 68 Km 8,5 Namorambe
Medan. Denah lokasi PT. MUTIFA ditunjukkan pada Gambar 2 berikut ini :
Mutifa
Ruko JBC & terminal
Jl
.E
ka
s
urya
Jl.Karya jaya
Jl
.A
H
.N
as
ut
ion
Lapangan bola
Luas areal PT. MUTIFA Medan mempunyai luas areal 9600 m2 dan luas
bangunan 6259 m2. Luas masing-masing ruangan adalah sebagai berikut :
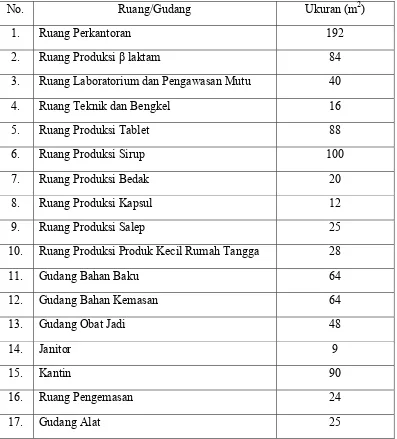
Tabel 1. Ukuran Ruangan Masing-Masing Bagian di PT. MUTIFA
No. Ruang/Gudang Ukuran (m2)
1. Ruang Perkantoran 192
2. Ruang Produksi β laktam 84
3. Ruang Laboratorium dan Pengawasan Mutu 40
4. Ruang Teknik dan Bengkel 16
5. Ruang Produksi Tablet 88
6. Ruang Produksi Sirup 100
7. Ruang Produksi Bedak 20
8. Ruang Produksi Kapsul 12
9. Ruang Produksi Salep 25
10. Ruang Produksi Produk Kecil Rumah Tangga 28
11. Gudang Bahan Baku 64
12. Gudang Bahan Kemasan 64
13. Gudang Obat Jadi 48
14. Janitor 9
15. Kantin 90
16. Ruang Pengemasan 24
17. Gudang Alat 25
Sumber arus listrik berasal dari Perusahaan Listrik Negara (PLN), dan
apabila arus listrik dari PLN terputus digunakan generator. Sumber air berasal dari
sumur pompa dan air PAM. Untuk keperluan produksi digunakan air sumur yang
telah mengalami proses pengolahan. Air PAM digunakan untuk pencucian alat,
mandi, dan bila aliran PAM mengalami masalah, untuk menggantikan air PAM
digunakan air sumur yang telah mengalami tiga kali penyaringan. Bangunan
2. Sarana Produksi
Ruangan produksi, gudang bahan baku, gudang bahan kemasan, dan obat
jadi dirancang sedemikian rupa sehingga waktu yang dibutuhkan untuk
mengangkut bahan baku ke ruang produksi, bahan kemasan ke ruang pengemasan,
obat jadi dari ruang karantina ke gudang obat jadi relatif singkat.
Produk beta laktam diproduksi dalam bangunan tersendiri dan terpisah
dengan produk non beta laktam. Ruang produksi dirancang sedemikian rupa
sehingga diharapkan dapat mencegah terjadinya kontaminasi silang terhadap
proses produksi obat serta terlewatnya salah satu langkah dalam proses produksi.
Keadaan ruang produksi adalah sebagai berikut :
a. Lantai
Lantai ruang produksi beta laktam dan non beta laktam terbuat dari
beton yang dilapisi granit di antaranya diisi dengan semen putih. Sudut
ruangan berbentuk lengkung dengan lantai. Lantai mempunyai permukaan
yang rata, mudah dibersihkan, tidak menahan partikel, tahan terhadap gesekan,
deterjen, desinfektan, dan bahan kimia.
b. Dinding
Dinding ruang terbuat dari beton, yang dilapisi dengan sebagian epoksi
dan sebagian acrylic, sehingga permukaan dinding menjadi licin, rata, kedap
air, mudah dibersihkan, tahan terhadap bahan kimia, deterjen, desinfektan,
tidak menahan partikel, serta tidak menjadi tempat bersarangnya binatang
kecil.
c. Langit-langit
Langit-langit ruang terbuat dari beton, yang dilapisi epoksi sehingga
permukaan langit-langit menjadi licin dan rata, kedap air, mudah dibersihkan,
tahan terhadap bahan kimia, deterjen, desinfektan, dan tidak menahan partikel.
d. Pengaturan Udara
Aliran udara yang digunakan dalam ruangan produksi beta laktam dan
non beta laktam adalah Air Handling System (AHS). Supply udara yang akan
disalurkan ke dalam ruang produksi berasal dari 2 sumber, yaitu berasal dari
(sebanyak 20%). Supply udara tersebut kemudian melewati filter yang
terdapat di dalam filter house yang terdiri dari prefilter yang memiliki efisiensi
penyaringan sebesar 35% dan medium filter yang memiliki efisiensi
penyaringan sebesar 95%. Selanjutnya, supply udara ini melewati cooling coil
(evaporator) yang akan menurunkan suhu (T) dan kelembaban relatif (RH)
udara. Kemudian udara dipompa dengan menggunakan static pressure fan
(blower) ke dalam ruang produksi melalui ducting (saluran udara). Jumlah
udara yang masuk ke dalam ruang produksi diatur dengan menggunakan
volume dumper. Selanjutnya udara disirkulasi kembali ke AHS. Kecepatan pertukaran udara dalam ruangan produksi beta laktam maupun non beta
laktam 20 kali per jam dan untuk koridor 25 kali per jam.
C. Struktur Organisasi
Struktur organisasi PT. MUTIFA merupakan struktur organisasi vertikal.
Kekuasaan tertinggi dipegang oleh direktur utama. Direktur utama membawahi
delapan departemen. Masing-masing departemen dipimpin oleh seorang manager
yang langsung bertanggung jawab penuh kepada direktur utama.
1. Departemen Produksi
Departemen produksi di PT. MUTIFA terdiri atas tiga bagian, yaitu:
a. Departemen produksi beta laktam
b. Departemen produksi solid non beta laktam
c. Departemen produksi cair non beta laktam
Ada pun tugas dan tanggung jawab departemen produksi , yaitu :
• Melaksanakan pembuatan obat mulai dari pengolahan, pengemasan primer dan sekunder, sampai karantina produk jadi.
• Melaksanakan secara teknis dan administrasi semua tugas selama pengelolahan dan pengemasan dengan berpedoman pada prosedur tetap
(protap) yang ditetapkan.
• Jika ada kegagalan dalam produksi, mendiskusikannya dengan manager QC dan mencari penyebab serta jalan keluar.
• Turut membantu pelaksanaan inspeksi CPOB dan menjaga pelaksanaan serta pematuhan terhadap peraturan CPOB.
• Memelihara kebersihan daerah produksi.
Bagian-bagian produksi PT. MUTIFA terdiri atas:
a. Unit tablet
Unit ini dilengkapi dengan timbangan, mesin mixer, granulator, oven,
FBD (Fluid Bed Dryer), lubrikator, mesin pencetak tablet, mesin penghitung
tablet, mesin penyalut, mesin strip, dan mesin blister. Hal-hal yang diperiksa
selama produksi adalah keseragaman bobot, waktu hancur, ketebalan, kekerasan,
kadar zat berkhasiat, friability, LOD (Loss On Drying), dan disolusi.
b. Unit kapsul
Mesin-mesin yang digunakan pada produksi kapsul adalah mesin mixer,
FBD, mesin pengisi kapsul, mesin kilap kapsul, mesin strip dan mesin blister.
Pada produksi kapsul perlu diperhatikan kondisi ruangan yaitu temperatur dan
kelembaban. Hal-hal yang diperiksa selama produksi adalah keseragaman bobot,
kadar zat berkhasiat, waktu hancur, disolusi, dan LOD.
c. Unit liquida
Unit liquida memproduksi sediaan bentuk cair seperti suspensi, emulsi dan
sirup. Unit ini dilengkapi dengan mesin mixer dan mesin pengisi obat ke dalam
wadah (automatic), dan mesin alucap manual. Hal-hal yang diperiksa selama
produksi adalah pH larutan, berat jenis (BJ) larutan, keseragaman volume,
viskositas larutan, kadar zat berkhasiat, dan kebocoran wadah.
d. Unit salep
Mesin-mesin yang digunakan pada produksi salep antara lain mesin mixer
dan mesin pengisi salep ke dalam wadah. Hal-hal yang diperiksa selama produksi
2. Departemen Pemastian Mutu/Quality Assurance (QA)
Departemen QA bertanggung jawab dalam menjamin mutu suatu produk
mulai dari pemesanan bahan baku dan kemasan obat sampai obat siap dikonsumsi
konsumen, termasuk di dalamnya pemilihan pemasok. Sistem mutu ditetapkan
berdasarkan CPOB.
Tugas-tugas bagian pemastian mutu mencakup:
a. Desain dan pengembangan obat dilakukan dengan cara yang
memperhatikan persyaratan CPOB.
b. Semua langkah produksi dan pengendalian diuraikan secara jelas dan
CPOB diterapkan.
c. Tanggung jawab manajerial diuraikan dengan jelas dalam uraian jabatan.
d. Pengaturan disiapkan untuk pembuatan pasokan dan penggunaan bahan
awal dan pengemas yang benar.
e. Validasi yang perlu dilakukan.
f. Pengkajian terhadap semua dokumen yang terkait dengan proses
pengemasan dan pengujian batch, dilakukan sebelum memberikan
pengesahan pelulusan untuk distribusi. Penilaian hendaklah meliputi
semua faktor yang relevan termasuk kondisi pembuatan, hasil pengujian
atau pengawasan selama proses, pengkajian dokumen produksi termasuk
pengemasan, pengkajian penyimpangan dari prosedur yang telah
ditetapkan, pemenuhan persyaratan dari spesifikasi produk jadi dan
pemeriksaan produk dalam kemasan akhir.
g. Obat tidak dijual atau dipasok sebelum manager pemastian mutu
menyatakan bahwa tiap batch produksi dibuat dan dikendalikan sesuai
dengan persyaratan yang tercantum dalam izin edar serta peraturan lain
yang berkaitan dengan aspek produksi, pengawasan mutu dan pelulusan
produk.
h. Tersedia pengaturan yang memadai untuk memastikan bahwa sedapat
mungkin produk disimpan, didistribusikan dan selanjutnya ditangani
sedemikian rupa agar mutu tetap dijaga selama masa edar /simpan obat.
i. Tersedia prosedur inspeksi diri atau audit mutu yang secara berkala
j. Pemasok bahan awal dan pengemas dievaluasi dan disetujui untuk
memenuhi spesifikasi mutu yang telah ditentukan oleh perusahaan.
k. Penyimpangan dilaporkan, diselidiki dan dicatat.
l. Tersedia sistem persetujuan terhadap perubahan yang berdampak pada
mutu produksi.
m. Prosedur pengolahan ulang dievaluasi dan disetujui.
n. Evaluasi mutu produk berkala dilakukan untuk verifikasi konsistensi
proses dan memastikan perbaikan proses yang berkesinambungan.
3. Departemen Pengawasan Mutu/Quality Control (QC)
Departemen QC di PT. MUTIFA terdiri dari tiga bagian, yaitu:
a. Unit QC
b. Bagian Registrasi
c. Bagian Standarisasi
Unit QC di PT. MUTIFA bertanggung jawab untuk memastikan bahwa: • Bahan awal untuk produksi obat memenuhi spesifikasi identitas,
kemurnian, kualitas dan keamanan yang telah ditetapkan.
• Semua pengawasan selama proses (in process controls) dan pemeriksaan laboratorium terhadap suatu batch obat telah dilaksanakan dan batch
tersebut memenuhi spesifikasi.
• Suatu batch obat memenuhi persyaratan mutunya selama waktu peredaran yang telah ditetapkan.
Bagian standarisasi bekerja sama dengan departemen R&D dalam
melakukan analisis dan evaluasi terhadap produk mulai dari pembelian bahan
baku sampai produk jadi. Tujuannnya adalah untuk menentukan kualitas produk
yang dihasilkan.
Bagian registrasi juga bekerja sama dengan departemen R&D. Dalam
waktu bersamaan dengan trial formulasi skala produksi yang dilakukan oleh
departemen R&D, bagian registrasi ini melakukan pendaftaran produk ke Balai
POM. Bagian registrasi ini dibantu oleh seorang administrasi desain yang bertugas
4. Departemen Research and Development (R&D)
Adapun tugas dan kegiatan departemen R&D adalah : • Mengembangkan dan merencanakan formula baru.
• Mengevaluasi dan memperbaiki formula yang sudah beredar kemudian diinformasikan ke departemen QC dan produksi.
• Bekerja sama dengan unit QC dalam menentukan standarisasi bahan baku, kemasan dan obat jadi.
• Mengelola perpustakaan.
Kegiatan R&D PT. MUTIFA difokuskan pada bidang formulasi.
Departemen R&D melakukan penelitian untuk mendapatkan formula baru
berdasarkan permintaan dari bagian pemasaran. Bagian pemasaran juga
memberikan ide-ide atau usulan kepada bagian formulasi untuk membuat suatu
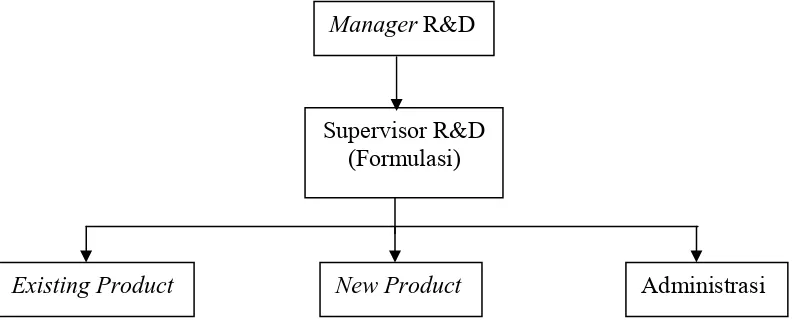
produk baru yang dianggap dapat laku di pasaran. Struktur organisasi departemen
R&D dapat dilihat pada gambar 3 berikut :
Manager R&D
Supervisor R&D (Formulasi)
Administrasi Existing Product New Product
Gambar 3. Struktur Organisasi Departemen R&D di PT. MUTIFA 5. Departemen Personalia
Departemen personalia di PT. MUTIFA menangani keperluan yang
berkaitan dengan ketenagakerjaan dan karyawan, mulai dari perekrutan karyawan,
6. Departemen Keuangan (Finance)
Departemen keuangan di PT. MUTIFA merencanakan anggaran dan
kontrol biaya setelah ramalan penjualan (forecasting) dibuat oleh bagian
pemasaran, membayar biaya operasional industri dan mengurus penggajian
karyawan.
7. Departemen Teknik
Adapun tanggung jawab departemen teknik di PT. MUTIFA, yaitu: • Pemeliharaan alat-alat dan mesin produksi.
• Pemeliharaan fasilitas penunjang di pabrik farmasi, yaitu listrik, AHU dan water system.
• Pemeliharaan instrumen laboratorium. • Pemeliharaan instalasi pengelolahan limbah.
Untuk menunjang jalannya proses produksi, departemen teknik dituntut
untuk dapat melaksanakan tugasnya dengan baik dalam hal pemeliharaan
mesin-mesin produksi, alat-alat laboratorium dan alat-alat lainnya agar berada dalam
kondisi baik sehingga selalu siap digunakan. Departemen teknik bertugas
memonitoring sistem AHU. AHU didesain untuk mencegah kontaminasi silang
dari udara antara ruang produksi dengan koridor di mana tekanan koridor lebih
positif dibandingkan ruang produksi.
8. Departemen Production Planning and Inventory Control (PPIC)
Departemen PPIC merupakan jembatan komunikasi antara pemasaran,
produksi, pengadaan, penyimpanan dan pengembangan produk. Perencanaan
produksi harus dilakukan sebaik mungkin dengan mempertimbangkan
variabel-variabel yang mempengaruhi sehingga tidak terjadi penimbunan dan kekurangan
stok barang. PPIC menyusun rencana dengan menyesuaikan permintaan
marketing dengan mempertimbangkan anggaran, persediaan bahan baku, jadwal,
kapasitas produksi dan peralatan yang tersedia. Departemen PPIC di PT.
a. Production Planning
Setelah ramalan penjualan (forecasting) dibuat oleh bagian pemasaran
(marketing), selanjutnya disusun perencanaan produksi (production planning) dan
Rencana Anggaran Belanja Perusahaan (RABP) sebagai acuan untuk memenuhi
permintaan bagian pemasaran tersebut. Perencanaan produksi terdiri dari rencana
produksi tahunan, yang kemudian dipilah menjadi rencana produksi periodik (
semester dan triwulan). Selanjutnya rencana produksi periodik dipilah lagi
menjadi rencana produksi bulanan, mingguan dan harian.
Sasaran pokok dari perencanaan produksi antara lain:
• Ketepatan waktu penyelesaian pesanan (permintaan) pelanggan • Berkurangnya biaya produksi
• New product launching dan menjaga produk-produk lama berjalan teratur dan lancar
b. Inventory Control
Alasan perlunya persediaan bagi industri, yaitu: • Antisipasi adanya unsur ketidakpastian permintaan • Adanya unsur ketidakpastian pasokan dari supplier
• Adanya unsur ketidakpastian tenggang waktu (lead time) waktu pemesanan
Inventory (persediaan) di industri farmasi, terdiri dari raw material (bahan
baku), packaging material (bahan pengemas), finished product (obat jadi), dan work in process (barang setengah jadi). Tujuan diadakannya persediaan antara lain:
• Untuk memberikan layanan terbaik bagi pelanggan. • Untuk memperlancar proses produksi.
• Untuk mengantisipasi kemungkinan terjadinya kekurangan persediaan (stockout).
D. Limbah
Departemen teknik dan QC bekerja sama menangani limbah di PT.
MUTIFA. Departemen teknik memusatkan perhatian pada pemeliharaan instalasi
pengelolahan limbah sedangkan departemen QC memantau proses pengolahan
limbah dan tolak ukurnya agar memenuhi persyaratan baku mutu lingkungan.
Limbah di PT. MUTIFA dibagi dua yaitu limbah non beta laktam dan limbah beta
laktam.
a sama menangani limbah di PT.
MUTIFA. Departemen teknik memusatkan perhatian pada pemeliharaan instalasi
pengelolahan limbah sedangkan departemen QC memantau proses pengolahan
limbah dan tolak ukurnya agar memenuhi persyaratan baku mutu lingkungan.
Limbah di PT. MUTIFA dibagi dua yaitu limbah non beta laktam dan limbah beta
laktam.
a. Limbah Non Beta Laktam a. Limbah Non Beta Laktam
Jenis limbah non beta laktam di PT. MUTIFA ada 3 jenis yaitu: Jenis limbah non beta laktam di PT. MUTIFA ada 3 jenis yaitu:
1. Limbah cair . 1. Limbah cair .
Limbah cair ini berasal dari limbah produksi, limbah laboratorium, limbah
domestik, dan limbah bengkel
Limbah cair ini berasal dari limbah produksi, limbah laboratorium, limbah
domestik, dan limbah bengkel
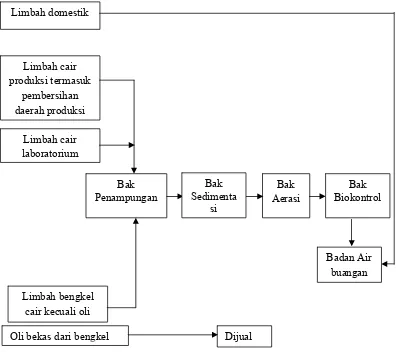
Diagram sistem pengolahan limbah cair dapat dilihat pada gambar 4 berikut ini: Diagram sistem pengolahan limbah cair dapat dilihat pada gambar 4 berikut ini:
. .
Gambar 4 . Diagram Sistem Pengolahan Limbah Cair di PT.MUTIFA Oli bekas dari bengkel Dijual
Limbah domestik Limbah cair produksi termasuk pembersihan daerah produksi Limbah cair laboratorium Badan Air buangan Bak Aerasi Bak Biokontrol Limbah bengkel cair kecuali oli
Bak Sedimenta
si Bak
Tolak ukur yang dipakai untuk pemantauan limbah cair adalah
berdasarkan baku mutu air limbah yang diisyaratkan dalam Surat Keputusan
Menteri Negara Lingkungan Hidup No.51/MENLH/10/1995* tentang Baku Mutu
Limbah Cair Industri seperti yang terdapat dalam tabel 2.
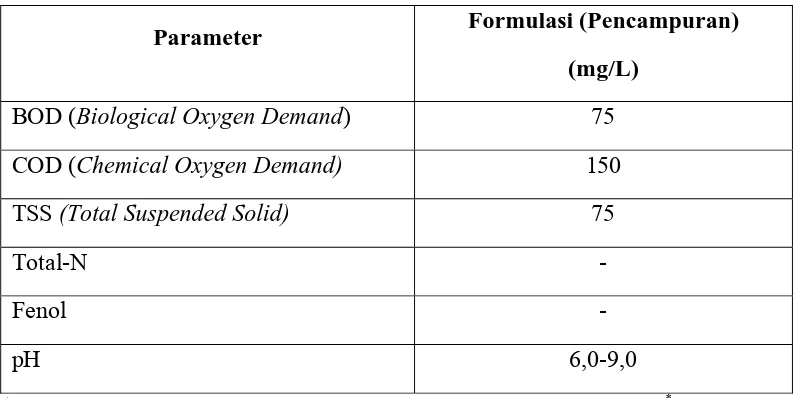
Tabel 2. Tolak Ukur Pemantauan Limbah Cair di PT. MUTIFA
Parameter Formulasi (Pencampuran)
(mg/L)
BOD (Biological Oxygen Demand) 75
COD (Chemical Oxygen Demand) 150
TSS (Total Suspended Solid) 75
Total-N -
Fenol -
pH 6,0-9,0
* Surat Keputusan Menteri Negara Lingkungan Hidup No.51/MENLH/10/1995* tentang Baku
Mutu Limbah Cair Industri
2. Limbah Padat.
Limbah padat ini berasal dari:
a. Bekas kemasan bahan awal (bahan baku/bahan kemasan) seperti kertas,
kotak karton, wadah kayu/plastik/kaca, drum, kaleng.
b. Buangan proses produksi seperti tepung sisa proses, produk antara/ruahan
yang rusak atau kotor, kemasan (aluminium foil, botol, dus)
c. Buangan bahan hasil pengujian laboratorium seperti tablet bekas pengujian
kekerasan, waktu hancur, dan lain-lain.
d. Bahan awal dan produk jadi yang rusak
e. Wadah bekas bahan produksi (plastik, tong rusak, dan lain-lain).
f. Limbah padat domestik.
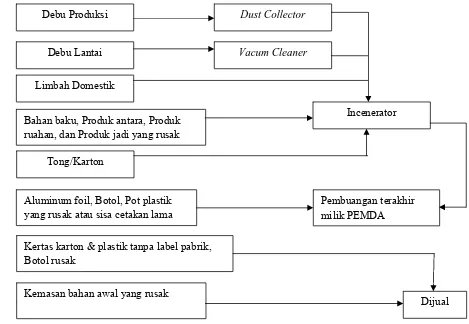
Tolak ukur yang dipakai untuk pemantauan limbah padat adalah kualitas
limbah padat yang berserakan di pabrik. Diagram sistem pengolahan limbah padat
di PT. MUTIFA adalah sebagai berikut:
3.
3. Limbah Udara .
Limbah udara ini berasal dari:
a. Gas, uap dan asap
- Bahan kimia / reagensia.
- Bahan baku seperti ammonia liquida, alkohol, dan lain-lain.
- Proses produksi seperti metilen klorida dari proses coating.
- Pembakaran zat padat.
- Asap pembakaran sampah Kemasan bahan awal yang rusak
Dust Collector Debu Produksi
Vacum Cleaner Debu Lantai
Limbah Domestik
Incenerator Bahan baku, Produk antara, Produk
ruahan, dan Produk jadi yang rusak
Tong/Karton
Aluminum foil, Botol, Pot plastik yang rusak atau sisa cetakan lama
Pembuangan terakhir milik PEMDA
Kertas karton & plastik tanpa label pabrik, Botol rusak
Dijual
Tabel 3. Sistem Penanggulangan Limbah Udara di PT. MUTIFA b. Debu produksi.
Tolak ukur yang dipakai untuk pamantauan limbah udara adalah kualitas
udara di dalam dan di luar lingkungan pabrik, meliputi kadar H2S, NH2, SO2, CO,
NO2, TSP. Sistem penanggulangan limbah udara antara lain tertera pada tabel 3.
Jenis Cara Pengendalian
1.Bahan kimia/reagensia
laboratorium
2. Asap pembakaran sampah
3. Uap solven
4. Debu Produksi
1. Lemari Asam
2. Incenerator cerobong tinggi
3. Exhaust fan
4. Pemasangan dust collector
4. Limbah Suara.
Limbah suara ini berasal dari mesin produksi, genset, mesin sistem
penunjang (AHU, mesin boiler). Cara pengendalian limbah suara ini dapat diatasi
dengan menggunakan ear insert oleh pekerja.
Tolak ukur yang digunakan untuk pemantauan limbah suara adalah angka
kebisingan dan getaran di dalam dan di luar area pabrik yang diukur sesuai dengan
angka kebisingan maksimum 65 dB dan getaran maksimum 7,5 Hz.
b. Limbah Beta Laktam
Jenis limbah beta laktam dapat berupa limbah cair, padat, udara, dan suara. Limbah cair berasal dari gedung produksi beta laktam berupa pencucian
alat/mesin. Limbah padat berupa wadah bekas bahan baku antibiotik beta laktam,
bahan baku beta laktam yang rusak, tong plastik, buangan proses produksi, dan
produk jadi antibiotik beta laktam yang rusak. Limbah udara berupa debu
produksi antibiotika beta laktam. Limbah suara berasal dari mesin produksi,
Pengelolaan Limbah Beta Laktam adalah sebagai berikut:
1. Limbah Cair.
Limbah cair yang berasal dari gedung beta laktam dialirkan ke bak/kolam
perusakan cincin beta laktam dengan menggunakan larutan NaOH, setelah itu
dialirkan/digabung dengan limbah cair non beta laktam di bak penampungan, dan
seterusnya diolah bersama.
2. Limbah Padat.
Limbah padat yang berupa wadah yang mengandung bahan antibiotik beta
laktam dicuci dan dibilas bersih dengan air bersih di ruang pencucian di dalam
gedung beta laktam. Air pencucian tersebut merupakan limbah cair dari gedung
beta laktam yang dialirkan ke bak perusak cincin beta laktam, sedangkan wadah
yang telah dicuci dan dibilas bersih tersebut dikeluarkan dari gedung beta laktam
dan ditangani limbahnya seperti pada pengelolaan limbah padat non beta laktam.
3. Limbah Udara.
Limbah udara berupa debu produksi disedot dan dikumpulkan oleh dust
collector.
4. Limbah Suara.
Limbah suara sistem penanganannya sama dengan penanganan limbah
suara di non beta laktam.
BAB IV PEMBAHASAN
Industri farmasi sebagai produsen obat-obatan harus dapat menjamin
bahwa produk yang dihasilkan memenuhi persyaratan mutu dan terus menjaga
konsistensi mutunya dalam setiap pembuatan. Salah satu pedoman yang
digunakan industri farmasi untuk menghasilkan produk yang bermutu adalah Cara
Pembuatan Obat yang Baik (CPOB).
PT. MUTIFA Medan sebagai salah satu PMDN yang memproduksi obat
telah menerapkan CPOB sejak bulan April tahun 1994. Penerapan CPOB dan
seluruh aspek rangkaian produksi merupakan suatu langkah untuk menjamin mutu
obat jadi, sehingga memenuhi persyaratan yang ditentukan sesuai dengan tujuan
penggunaannya. Dalam prosesnya, mutu dalam produk harus dibentuk di dalam
produk tersebut, tidak cukup hanya lulus dari pemeriksaan mutu. Aspek-aspek
yang mempengaruhi proses pembentukan mutu terhadap produk tertuang dalam
aspek-aspek yang harus diperhatikan dalam CPOB. Selama Praktek Kerja Profesi
(PKP), penulis melakukan pengamatan terhadap proses pembentukan mutu
melalui penerapan CPOB.
A. Manajemen Mutu
Untuk menjamin khasiat, keamanan dan mutu produknya, PT. MUTIFA
memiliki manajemen mutu sesuai dengan CPOB 2006. Hal ini dapat dilihat dari
adanya pemisahan kewenangan dan tanggung jawab departemen QA dan QC.
Departemen QA bertanggung jawab dalam menjamin mutu produk mulai
dari pemesanan bahan baku dan kemasan obat sampai obat siap dikonsumsi
konsumen, termasuk di dalamnya pemilihan pemasok. Sistem mutu ditetapkan
berdasarkan CPOB. Beberapa hal yang ditangani departemen QA antara lain: • Penyelenggaran pelatihan CPOB kepada karyawan yang bekerja di area
produksi dan pengawasan mutu.
• Penanganan dan pengendalian sistem dokumentasi. • Menyusun dan mengendalikan protap.
• Mengadakan audit terhadap pemasok. • Melaksanakan inspeksi diri.
• Penolakan dan pelulusan obat jadi. • Penyelidikan terhadap kegagalan. • Penanganan hasil uji di luar spesifikasi.
• Penanganan keluhan, penarikan kembali obat jadi dan penanganan obat kembalian.
Departemen QC memiliki kewenangan dan tanggung jawab melaksanakan
pengawasan dan pengujian seluruh bahan awal yang akan digunakan dalam
produksi, melakukan pengawasan selama proses produksi dan pengujian obat jadi.
Sedangkan departemen QA memiliki kewenangan dan tanggung jawab untuk
menyusun kebijakan mutu perusahaan berdasarkan CPOB yang dapat menjamin
mutu obat yang dihasilkan agar sesuai dengan persyaratan mutu obat yang telah
ditetapkan dan memastikan seluruh kegiatan yang terlibat dalam proses
pembuatan obat, melaksanakan kebijakan tersebut. Departemen QA menjadi
polisi yang mandiri untuk memantau keseluruhan proses pembuatan obat mulai
dari rencana design industri (R&D), pembelian bahan, proses produksi hingga
distribusi obat jadi.
B. Personalia
PT. MUTIFA memiliki struktur organisasi di mana departemen produksi,
QA dan QC dipimpin oleh manager yang berbeda serta tidak saling bertanggung
jawab satu dengan yang lain. Manager produksi dan QA merupakan seorang
apoteker yang terdaftar dan memiliki pengalaman praktis yang memadai pada
bidang masing-masing sehingga memiliki keterampilan manajerial untuk
melaksanakan tugas secara profesional. Sedangkan manager QC adalah seorang
sarjana kimia yang berpengalaman dalam bidangnya.
Untuk mendukung kegiatan operasionalnya, PT. MUTIFA memerlukan
personil yang terampil dan terlatih. Status dan jumlah personil dilihat pada tabel 4.
Dalam rangka memenuhi persyaratan CPOB, langkah-langkah yang diambil PT.
MUTIFA Medan di bidang personalia adalah dengan cara mengirim pimpinan
pimpinan atau staf tersebut dapat memberikan bimbingan dan pelatihan tentang
CPOB kepada karyawan sehingga kegiatan perusahaan akan memenuhi ketentuan
CPOB. Berdasarkan jenjang pendidikan, maka personil PT. MUTIFA Medan
dapat dilihat pada lampiran 2 dan 3.
C. Bangunan dan Fasilitas
Lokasi PT. MUTIFA Medan dibangun di kawasan yang jauh dari pusat
kota dan keramaian. Bangunan produksi antibiotik beta laktam terpisah dengan
bangunan produksi non beta laktam. Area penimbangan bahan awal dilakukan di
area penimbangan yang terpisah dan didesain khusus untuk kegiatan tersebut.
Area ini merupakan bagian dari area produksi.
Ruang produksi dirancang mengikuti alur proses produksi sehingga
memperkecil resiko terjadinya kekeliruan antara produk obat atau komponen obat
yang berbeda, mencegah pencemaran silang dan memperkecil resiko terlewatnya
atau salah melaksanakan tahapan proses produksi. Di dalam area produksi
terdapat ruang pengawasan selama proses (in process control).
Area produksi diventilasi menggunakan AHU termasuk filter udara
dengan tingkat efisiensi yang dapat mencegah pencemaran dan pencemaran silang
serta mengendalikan suhu dan kelembaban. Area di mana dilakukan kegiatan
yang menimbulkan debu seperti penimbangan bahan, pencampuran dan
pencetakan tablet memiliki dust collector. Tetapi dust collector belum berfungsi
dengan baik. Hal ini dapat dilihat pada saat kegiatan tersebut berlangsung,
ruangan terdapat debu di lantai dan di sela-sela peralatan. Debu tersebut hanya
dibersihkan pada saat selesai kegiatan produksi dengan vacum cleaner.
Area penyimpanan PT. MUTIFA terdiri dari gudang bahan baku, gudang
bahan kemasan, dan obat jadi. Gudang bahan baku terdiri dari ruang administrasi,
karantina, penolakan, penyimpanan bahan baku psikotropik yang terkunci,
pengambilan sampel, penyimpanan bahan baku setelah diluluskan. Gudang bahan
kemasan terdiri dari ruang administrasi, karantina, produk kembalian, produk
ditolak, penyimpanan aluminium foil, penyimpanan brosur dan label,
penyimpanan kemasan sekunder seperti master dus, kotak karton dan botol.
Gudang bahan jadi terdiri dari ruang karantina, penolakan, penyimpanan produk
di gudang masing-masing, menggunakan palet yang terbuat dari kayu, berfungsi
agar tidak berkontak langsung dengan lantai, tidak tercemar debu, kotoran dan
terhindar dari rembesan air.
Area pengawasan mutu memiliki ruangan terpisah untuk memberi
perlindungan terhadap instrumen seperti spektrofotometri UV-Visibel. Ruang
istirahat, kantin, toilet dan bengkel tidak berhubungan langsung dengan area
produksi, laboratorium pengawasan mutu dan area penyimpanan.
D. Peralatan
Alat timbang dan alat ukur untuk proses produksi dan pengawasan
dikalibrasi secara berkala. Dalam tiap ruang produksi hanya terdapat satu
peralatan yaitu :
• Ruang pencampuran hanya terdapat satu alat drum mixer. • Ruang granulasi hanya terdapat satu alat granulator.
• Ruang pengeringan hanya terdapat satu alat fluid bed dryer. • Ruang lubrikasi hanya terdapat satu alat lubrikator.
Hal ini bertujuan untuk menghindari resiko kekeliruan dan pencemaran silang.
E. Sanitasi dan Higine
Setiap personil yang masuk ke dalam area produksi (grey area) harus
mengenakan pakaian pelindung, masker, sarung tangan dan penutup kepala. Hal
ini dilakukan untuk menjamin perlindungan produk dari pencemaran dan untuk
keamanan personil. Personil mencuci tangan sebelum memasuki area produksi.
Sarana toilet dan tempat cuci tangan mudah diakses dari area produksi.
Pembersihan ruangan dan peralatan produksi dilakukan setiap hari setelah
kegiatan produksi berakhir dengan vacum cleaner dan kuas. Penyimpanan
peralatan dan bahan pembersih pada ruangan terpisah dengan ruang pengolahan.
F. Produksi
Produksi adalah semua kegiatan dari penerimaan bahan awal, pengolahan
sampai pengemasan untuk menghasilkan obat jadi. Proses produksi dilaksanakan
berdasarkan rencana produksi mingguan. Manager produksi akan menurunkan
pengemasan batch. Bersama dengan dikeluarnya SPP, manager produksi juga mengeluarkan Surat Perintah Pengeluaran Barang (SPPB) kepada kepala gudang.
Seluruh bahan awal dan bahan pengemas yang diterima diperiksa
kesesuiannya dengan pemesanan kemudian dikarantina. Apabila memenuhi
persyaratan spesifikasi maka diluluskan dan bahan awal serta bahan pengemas
tersebut dapat dipakai. Apabila bahan awal dan bahan pengemas tersebut berlebih
maka dikembalikan ke gudang penyimpanan.
Bahan awal tersebut kemudian diserahkan ke ruang penimbangan. Untuk
tiap penimbangan dilakukan pembuktian kebenaran identitas, jumlah bahan yang
ditimbang oleh dua petugas penimbangan dan pembuktian tersebut dicatat.
Sebelum dilakukan pengolahan, peralatan diperiksa kebersihannya dan
dinyatakan bersih secara tertulis sebelum digunakan. Semua kegiatan pengolahan
dilaksanakan mengikusi prosedur pengolahan induk. Pengawasan selama proses
produksi dilakukan pada produk antara dan produk ruahan.
Kegiatan pengemasan dilakukan pada produk ruahan agar dihasilkan
produk jadi. Produk jadi dikarantina pada area produksi. Bagian pengawasan
mutu melakukan finished pack analysis dan pengambilan sampel pertinggal.
Setelah produk jadi memenuhi persyaratan spesifikasi, departemen pemastian
mutu meluluskannya. Produk jadi kemudian diserahkan ke gudang obat jadi dan
siap didistribusikan.
G. Pengawasan Mutu
Departemen pengawasan mutu di PT. MUTIFA bertanggung jawab atas: • Pelaksanaan pengambilan contoh.
• Pemeriksaan contoh bahan baku, produk ruahan dan produk jadi. • Menyusun dan merevisi prosedur tetap (protap).
• Menjaga kebersihan ruangan dan peralatan yang digunakan .
Mula-mula bahan baku yang baru datang akan masuk ke gudang dengan
status karantina. Gudang akan mengirimkan slip penerimaan barang ke
departemen QC. Berdasarkan slip yang diterima, QC melakukan pengambilan
contoh untuk semua bahan aktif dan bahan penolong. Setiap bahan baku yang
acuan pemeriksaan bahan. Setelah diperiksa, bahan baku yang diluluskan
ditempelkan label released (warna hijau) kemudian bahan baku disimpan di
gudang. Apabila bahan baku ditolak ditempelkan label rejected (warna merah)
dan ditempatkan pada area ditolak yang ada di gudang. Kemudian dikembalikan
kepada pemasok.
Produk ruahan adalah produk yang telah selesai diolah dan siap untuk
dikemas. Pengambilan contoh dilakukan pada saat pembuatan berlangsung yaitu
pada awal, tengah dan akhir proses. Produk ruahan harus segera diperiksa sesuai
dengan spesifikasinya.
Produk jadi adalah produk yang telah melewati seluruh tahapan produksi,
termasuk pengemasan dan siap untuk didistribusikan. Pengambilan contoh
dilakukan pada proses pengemasan yaitu pada awal, tengah dan akhir
pengemasan. Setelah diperiksa sesuai dengan spesifikasinya, penerbitan label
released/rejected harus diparaf oleh manager QA.
H. Inspeksi Diri dan Audit Mutu
Inspeksi diri PT. MUTIFA diadakan satu tahun sekali. Inspeksi diri
dilakukan oleh tim inspeksi diri yang diketuai oleh manager QA. Inspeksi diri
dilakukan terhadap departemen produksi, R&D, QC, QA, dan teknik. Laporan
dibuat setelah inspeksi diri selesai dilaksanakan. Inspeksi yang dilakukan pada
tiap-tiap departemen mencakup antara lain: • Personalia
• Bangunan
• Perawatan bangunan dan peralatan
• Penyimpanan bahan awal, bahan pengemas dan obat jadi • Peralatan
• Pengolahan dan pengawasan selama proses • Pengawasan mutu
• Dokumentasi • Sanitasi dan higiene
• Prosedur penarikan kembali obat jadi • Penanganan keluhan
• Pengawasan label
• Hasil inspeksi diri sebelumnya dan tindakan perbaikan
Laporan tersebut mencakup hasil inspeksi diri, evaluasi serta kesimpulan,
saran tindakan perbaikan. Audit mutu dilakukan oleh badan POM. Audit ini
mencakup aspek CPOB. Badan POM didampingi manager QA melaksanakan
audit langsung di lapangan.
. I. Penanganan Keluhan terhadap Produk, Penarikan Kembali Produk dan Produk Kembalian
Keluhan dapat berupa keluhan menyangkut efek samping obat dan
menyangkut teknis kualitas obat. Keluhan tersebut dilaporkan ke departemen QA.
Keluhan yang menyangkut teknis kualitas obat dapat dibagi atas: • Kategori A
Misalnya kesalahan pada cetakan bahan pengemas yang mengandung
resiko bagi pasien, laporan negatif dari media massa yang berkaitan
dengan keamanan obat dan pemalsuan.
• Kategori B
Misalnya kesalahan dalam bahan pengemas tercetak yang tidak
mengandung resiko terhadap pasien (nomor kode tidak ada) dan cacat
estetik.
Tindak lanjutnya dapat berupa penggantian produk atau penarikan produk
(recall). Penarikan obat jadi dapat dilakukan karena keinginan produsen (misalnya
mau mengganti kemasan) atau keinginan badan POM. Produk kembalian yang
ditarik akan disimpan di gudang. Penanganan selanjutnya bisa dihancurkan,
J. Dokumentasi
Sistem dokumentasi PT. MUTIFA meliputi: • Prosedur tetap (protap)
• Spesifikasi (bahan baku, pengemas, produk jadi)
• Catatan pengolahan batch dan catatan pengemasan batch
• Penandaan (status ruangan, mesin, label karantina, released, rejected) • Protokol dan laporan validasi
• Dokumen registrasi • Catatan kalibrasi
Sistem dokumentasi merupakan hal yang penting dalam industri farmasi
untuk memastikan bahwa setiap karyawan mendapat instruksi yang jelas dan rinci
mengenai bidang tugas yang harus dilaksanakannya sehingga memperkecil resiko
terjadinya salah tafsir dan kekeliruan yang biasanya timbul apabila hanya
mengandalkan instruksi lisan. Sistem dokumentasi produk (catatan pengolahan
dan pengemasan batch) harus menggambarkan riwayat lengkap dari setiap batch
suatu produk sehingga memungkinkan penyelidikan serta penelusuran kembali
terhadap batch yang bersangkutan apabila terdapat kesalahan selama produk tersebut dipasarkan.
K. Kualifikasi dan Validasi
Manager QA membentuk tim validasi dan menyusun protokol validasi
untuk produk yang akan divalidasi. Kegiatan validasi akan dilakukan oleh
departemen yang bersangkutan, dimonitor dan didokumentasikan oleh tim
validasi. Setiap akhir validasi harus dibuat suatu laporan validasi sebagai
pertanggungjawaban.
Kualifikasi di PT. MUTIFA merupakan tanggung jawab departemen
teknik. Kualifikasi adalah pembuktian secara tertulis berdasarkan data yang
menunjukan bahwa suatau peralatan, fasilitas, sistem penunjang dan proses
Kualifikasi mencakup:
• Design Qualification (DQ)
Dokumen awal yang harus disiapkan mencakup desain alat dan
spesifikasi konstruksi. DQ hanya dilakukan untuk alat/sistem baru dan
harus disiapkan sebelum instalation qualification.
• Instalation Qualification (IQ)
Pembuktian secara tertulis bahwa peralatan terpasang dengan benar
dan memenuhi desain yang telah ditentukan
• Operational Qualification (OQ)
Pembuktian secara tertulis bahwa peralatan dapat dioperasikan
sesuai dengan desain yang telah ditentukan dan memenuhi kriteria
penerimaan. Protap pengoperasian alat harus dibuat segera setelah
melakukan OQ.
• Performance Qualification (PQ)
Pembuktian secara tertulis bahwa peralatan dapat secara konsisten
memberikan kinerja yang baik atau berfungsi menghasilkan produk sesuai
standar mutu yang telah ditetapkan. PQ untuk peralatan dapat juga
mengambil data dari validasi proses.
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Setelah melaksanakan Praktek Kerja Profesi (PKP) Apoteker di PT.
Mutiara Mukti Farma (MUTIFA) dapat diambil kesimpulan sebagai berikut :
1. Profesi apoteker di industri farmasi memiliki tugas dan ruang lingkup yang
cukup luas mulai dari bagian pengembangan produk, produksi sampai
bagian jaminan dan pengawasan mutu (QA/QC).
2. PT. MUTIFA Medan telah menerapkan ketentuan Cara Pembuatan Obat
yang Baik (CPOB) .
3. PT. MUTIFA memiliki komitmen yang kuat dalam menerapkan CPOB
secara konsisten dan kontiniu dalam semua aspek kegiatan guna
mengutamakan mutu dari produk yang dihasilkan. Mutu obat telah
dibentuk mulai dari awal proses produksi dengan memenuhi persyaratan
CPOB, sehingga tidak hanya ditentukan dengan pengujian produk jadi
saja.
4. Seluruh kegiatan di PT. MUTIFA telah menggunakan dokumen produksi
berupa protap-protap yang tertulis atau dokumen-dokumen lain, seperti
catatan pengolahan batch, catatan pengemasan batch, prosedur analisa
bahan baku dan obat jadi, dll
B. Saran
1. Sebaiknya pada penyimpanan bahan baku digudang diberi pembatas antara
bahan baku cairan dan padatan (serbuk)
2. Sebaiknya pada penyimpanan bahan kemasan di gudang ditata lebih rapi
sehingga mudah mengambil dan mengetahui posisi dari bahan kemasan.
3. Sebaiknya ruangan karantina obat jadi diperbesar supaya tidak terlalu
DAFTAR PUSTAKA
Ansel, C. H (1989). Pengantar Bentuk Sediaan Farmasi. Edisi keempat. UI.Press.
Badan POM (2006). Pedoman Cara Pembuatan Obat yang Baik. Jakarta.
Badan POM (2001). Petunjuk Operasional Penerapan Cara Pembuatan Obat yang Baik. Jakarta.
Depkes RI (1992). Undang-undang Kesehatan no. 23
Depkes RI (1990). Permenkes RI No. 57/Menkes/Per/III/1990 tentang Analisa Mengenai Dampak Lingkungan. Jakarta.
Depkes RI (1990). Surat Keputusan Menteri Kesehatan RI No. 245/Menkes/ SK/V/1990 tentang Ketentuan dan Tata Cara Pelaksanaan Pemberian Izin Usaha Industri Farmasi. Jakarta.
Depkes RI (1990). Permenkes RI No. 286/Menkes/Per/III/1990 tentang Kegiatan di Bidang Kesehatan yang Wajib Membuat AMDAL. Jakarta.
Depkes RI (1979). Farmakope Indonesia. Edisi III. Jakarta.
Depkes RI (1995). Farmakope Indonesia. Edisi IV. Jakarta.
Lachman, L., Liebermann, H.A., and Kanig, J.L. (1989). Teori dan Praktek Farmasi Industri. Judul asli: The Theory and Practice of Industrial Pharmacy. (Penerjemah: Suyatmi, S.). Edisi Ketiga. Jakarta: UI Press. Priyambodo, B (2007). Manajemen Farmasi Industri. Edisi I. Yogyakarta: Global
Pustaka Utama.
Lampiran 1. Status dan Jumlah Personil di PT. MUTIFA
No. Bagian Unit Jumlah
1. Direktur Utama 1
2. Manajer 10
3. Administrasi dan Keuangan 7
4. Research & Development 3
5. Unit Sirup 28
6. Unit Kapsul 5
7. Unit Tablet 25
8. Unit Puyer 4
9. Unit Bedak 4
10. Gudang Kemasan 4
11. Gudang Bahan Baku 8
12. Gudang Obat Jadi 3
13. Teknisi 5
14. Laboratorium 9
15. Kolektor 1
16. Akuntansi 3
17. Penjualan/Pemasaran 2
18. Supir 3
19. Pembelian 1
21. Satpam 5
Lampiran 2. Personalia PT. MUTIFA Medan Berdasarkan Jenjang Pendidikan
No. Jenjang Pendidikan Jumlah (Orang)
1. Apoteker 7
2. Sarjana 11
3. Sarjana Muda 5
4. SLTA/sederajat 102
5. SLTP 15
6. SD 2
Lampiran 3 . Daftar Produk PT. MUTIFA
No. Nama Obat Kemasan Komposisi
TABLET
1. Omecal-D Tab/10 x 10 strip CaCO3, Vit D
2. Omecold Tab/10 x 10 strip Paracetamol, phenylpropanolamin HCl,
Chlorpheniramine maleat
3. Omedeson 0,5 mg Pot/1000’s Dexamethason
4. Omedeson 0,5 mg Box/10 x 20 strip Dexamethason
5. Omedom 10 mg Tab/10 x 10 strip Domperidon
6. Omegastri Sugar Coated Box/10 x 10
strip
Klordiazopoksida, klidinium bromida
7. Omegdiar (kaolin+pectin) Box/10 x 10 strip Kaolin, pectin
8. Omegdiar (kaolin+pectin) Pot/1000’s Kaolin, pectin
9. Omegesic F.C 500 mg Box/10 x 10 strip Metampiron, Vit B1, Vit B6, Vit B12
10. Omegfantrin 125 mg Box/4 x 25 blister Pyrantel pamoat
11. Omegfantrin 250 mg Box/2 x 25 blister Pyrantel pamoat
12. Omegrip 500 mg Box/10 x 10 strip Paracetamol
13. Omegtamine Box/10 x 30 strip Dexamethason, Dexchlorfeniramine
maleat
14. Omegtrim adult 480 mg Box/10 x 10 strip Trimethoprim, Sulphametoxazole
15. Omegzole 200 mg Tab/10 x 10 strip Ketokonazole
16. Omemox 250 mg Box/10 x 10 kaplet Amoxyciline
17. Omemox 500 mg Box/10 x 10 strip Amoxyciline
18. Omenacort 4 mg Tab/10 x 10 strip Triamcinolone
19. Omeneuron Box/10 x 10 strip Vit B1, Vit B6, Vit B12
20. Omeproksil 500 mg Box/10 x 10 strip Cyprofloxacine HCl monohidrat
21. Omeric 100 mg Box/10 x 10 strip Allopurinol
22. Omeric 300 mg Box/10 x 10 strip Allopurinol
23. Omeroxol 30 mg Tab/10 x 10 strip Ambroxol HCl
24. Omesip 4 mg sugar coated Tab/10 x 10 strip Siproheptadine HCl
25. Omestan F.C 500 mg Box/10 x 10 blister Asam mefenamat
26. Ometilson 4 mg Kapl/10 x 10 strip Metilprednisolon
27. Omevomid 10 mg Tab/10 x 10 strip Metoclopramide
28. Panviton kapl. Ekstrak
Ginseng
Box/10 x 5 kaplet Curcumae, Ekstrak ginseng, Vit C, Vit B1, Vit B6, Vit B12, Nikotinamid, Ca-pantothenat, Mn (II), Cu, Co, Ca, Mg, Zink
29. Stomach tablet Box/10 x 10 tablet Aluminium hidroksida2, Magnesium
hidroksida2, simetikon
30. Omedrinat Box/10 x 10 tablet Dimenhidrinat
31. Omegluphage Dus/10 x 10 strip Metformin HCl
32. Omekur Dus/10 x 10 strip Cimetidine
33. Omenizol Dus/10 x 10 strip Metronidazol
34. Omeramine F.C 150 mg Dus/10 x 10 strip Ranitidin HCl
35. Omeretic tab Dus/10 x 10 strip Piroksikam
36. Omesolvon Box 10 strip x 10
tablet
Bromheksin HCl
37. Omezyrteks Box 5 strip x 10
tablet
Setirizine HCl
38. Panvit-C kaplet Dus/10 x 10 strip Vit C, Vit B1, Vit B2, Vit B3
panthotenat), Vit B6, Vit B12
39. Vilergi Dus/10 x 10 strip Dexchlorfeniramine maleat
40. Vitalamin Gold kaplet Dus/10 x 10 strip Vit A, Vit B1, Vit B2, Vit B6, Vit B12, Vit C, Vit D, Kalsium pantotenat, Nikotinamid, Asam folat, Fe(II) Fumarat, ZnSO4, CuSO4, MnSO4
41. Vitalamin Gold kaplet Botol 500 kaplet Vit A, Vit B1, Vit B2, Vit B6, Vit B12, Vit C,Vit D, Kalsium pantotenat, nikotinamid, asam folat, Fe(II) Fumarat, ZnSO4, CuSO4, MnSO4
42. Vitalamin kaplet Botol 500 kaplet Vit A, Vit B1, Vit B2, Vit B6, Vit B12,
Vit C, Vit D, Kalsium pantotenat, Nikotinamid, Asam folat, Fe(II) Fumarat
43. Vitalamin kaplet Dus/10 x 10 strip Vit A, Vit B1, Vit B2, Vit B6, Vit B12,
Vit C, Vit D, Kalsium pantotenat, nikotinamid, asam folat, Fe(II) Fumarat
44. Vitamin A 5.000 IU Kaleng 1000 tablet Vitamin A 5.000 IU
45. Antacida (magcumalu) Pot/1000’s Aluminium hidroksida, Magnesium
hidroksida
46. Ampicillin 250 mg Box/10 x 10 kaplet Ampicillin tririhidrat
47. Ampicillin 500 mg Box/10 x 10 kaplet Ampicillin tririhidrat
48. Antalgin 500 mg Box/10 x 20 strip Antalgin
49. Antalgin 500 mg Pot /1000’s Antalgin
50. CTM 4 mg Pot /1000’s Chlorpheniramin maleat
51. Chloroquin Pot /1000’s Chloroquin difosfat
52. Gliseril Guaikolat 100 mg Pot /1000’s Gliseril guaikolat
53. INH 100 mg Pot /1000’s Isoniazida
54. Metronidazol 250 mg Box/10 x 10 strip Metronidazol
55. Metronidazol 500 mg Box/10 x 10 strip Metronidazol
56. Papaverin HCl 40 mg Pot /1000’s Papaverin HC
57. Paracetamol 500 mg Pot /1000’s Paracetamol
58. Paracetamol 500 mg Box/10 x 20 strip Paracetamol
59. Prednison Pot /1000’s Prednison
60. Trisulfa Pot /1000’s Sulfadiazina,Sulfametazin,
sulfasomidina
61. Vitamin B komplex Pot /1000’s Vit B1, Vit B2, Vit B5, Vit B6
62. Vitamin B1-50 mg Pot /1000’s Vit B1
63. Vitamin B6-10 mg Pot /1000’s Vit B6
SYRUP
1. Anak Mas Botol 60 ml Asetaminofen, Koffein, CTM
2. Chloramfenikol suspensi Botol 60 ml Kloramfenikol palmitat
3. Curbion Botol 60 ml Betakaroten, Curcumae, Biotin, Lysin
HCl, Vit B1, Vit B2, Vit B3, Vit B5, Vit B6, Vit B12
4. Curbion cod liver oil kids E Botol 60 ml Vit A, Vit D, DHA, EPA, Curcumae
extract, Vit B1, Vit B2, Vit B3, Vit B5, Vit B6, Biotin, Lysin HCl, Betakaroten
5. Curbion cod liver oil kids E Botol 100 ml Vit A, Vit D, DHA, EPA, Curcumae
extract, Vit B1, Vit B2, Vit B3, Vit B5, Vit B6, Biotin, Lysin HCl, Betakaroten, Kalsium, Asam folat, Asam L glutamat
6. Curbion cod liver oil kids E Botol 200 ml Vit A, Vit D, DHA, EPA, Curcumae
Betakaroten, Kalsium, Asam folat, Asam L glutamat
7. Curbion Fit Botol 100 ml Echianaceae, Zink, Pikolinat,
Selenium, Vit C, Curcumae extract, Vit B1, Vit B2, Vit B3, Vit B5, Vit B6, Vit B12, DHA, EPA, Royal Jelly, Minyak ikan cod
8. Curbion Fit Botol 60 ml Echianaceae, Zink, Pikolinat,
Selenium, Vit C, Curcumae extract, Vit B1, Vit B2, Vit B3, Vit B5, Vit B6, Vit B12, DHA, EPA, Royal Jelly, Minyak ikan cod
9. Curbion Fit Botol 200 ml Echianaceae, Zink, Pikolinat,
Selenium, Vit C, Curcumae ext, Vit B1, Vit B2, Vit B3, Vit B5, Vit B6, Vit B12, DHA, EPA, Royal Jelly, Minyak ikan cod
10. Curbion Hi- DHA syrup Botol 60 ml Vit A, Vit D, DHA, EPA, Curcumae
ext, Vit B1, Vit B2, Vit B3, Vit B5, Vit B6, Vit B12, Biotin, Lysin HCl, Betakaroten, Kalsium, Asam folat, Asam L glutamat
11. Curbion Hi- DHA syrup Botol 100 ml Vit A, Vit D, DHA, EPA, Curcumae
extract, Vit B1, Vit B2, Vit B3, Vit B5, Vit B6, Vit B12, Biotin, Lysin HCl, Betakaroten, Kalsium, Asam folat, Asam L glutamat
12. Curbion Supra Botol 60 ml Fe, Curcumae extract, Vit B1, Vit B2,
Vit B3, Vit B6, Asam folat, Biotin, Royal Jelly, Minyak ikan cod
13. Curbion Supra Botol 100 ml Fe, Curcumae extract, Vit B1, Vit B2,
Vit B3, Vit B6, Asam folat, Biotin, Royal Jelly, Minyak ikan cod
14. Curbion Supra Botol 200 ml Fe, Curcumae extract, Vit B1, Vit B2,
Vit B3, Vit B6, Asam folat, Biotin, Royal Jelly, Minyak ikan cod
15. Dextrometorfan HBr syrup
kaca
Botol 100 ml Dextrometorfan HBr
16. Dextrometorfan HBr syrup OGB plastik
Botol 60 ml Dextrometorfan HBr
17. Obat batuk hitam Botol 100 ml Glycirhizae succus, Ammonium
chlorida, Olium anisi, Antimon liquida
18. Omecough Botol 60 ml Dextrometorfan HBr, Paracetamol,
Gliseril guaikolat, Chlorpheniramin maleat
19. Omedom Botol 60 ml Domperidon
20. Omegdiar suspensi Botol 60 ml Kaolin, pectin
21. Omegrif Botol 60 ml Asetaminofen
22. Omelysta Botol 100 ml Vit A, Vit D, Vit B1, Vit B2, Vit, Vit
B6, Vit B12, Vit C, Niacinamide, Ca-panthothenate, L-Lysin HCl, Ca- glycerolfosfat
23. Omemox dry syrup Botol 60 ml Amosisilin trihidrat
24. Omeroxol Botol 60 ml Ambroxol HCl
25. Omesolvon Botol 60 ml Bromheksin HCl, Gliseril guaikolat,
Etanol 3,72% v/v
chlorida, Menthol, Na sitrat, Dextrometorfan HBr
27. Omevita syrup Botol 60 ml Vit A, Vit D, Vit B1, Vit B2, Vit B6,
Vit B12, Vit C, Niacinamide, Ca-panthothenate, L-Lysin HCl
28. Omevita syrup Botol 100 ml Vit A, Vit D, Vit B1, Vit B2, Vit B6,
Vit B12, Vit C, Niacinamide, Ca-panthothenate, L-Lysin HCl
29. Omevomid Botol 60 ml Metoklopramide HCl
30. Pantonik syrup ginseng extra Botol 300 ml Ginseng extract, Vit B1, Vit B2, Vit B6, Vit B12, Vit C, Niacinamide, Ca-panthothenate, Liver extract, Mn(II), Fe(II)
31. Paracetamol 60 ml kaca Botol 60 ml Paracetamol
32. Paracetamol OGB plastik Botol 60 ml Paracetamol
33. Tusselix Botol 100 ml Ephedrin HCl, CTM, Glycirhizae
succus, Ammonium chlorida KAPSUL
1. Chloramphenicol 250 mg Pot/1000’s Chloramphenicol
2. Omegavit Box/10 x 10 strip Ferros glukonas, Magnesium sulfat,
Copper sulphate, Vit C, Vit B12, As folat
3. Omeretik 20 mg Box/10 x 10 strip Piroksikam
4. Omestan 250 mg Box/10 x 10 strip Asam mefenamat
5. Tetracycline 250 mg Pot/1000’s Tetracycline HCl
6. Turtensi Botol/30’s Alii sativi bulbus, Apium graveolus
folium ext, Phylanthi herba ext, Cantella herba ext, Ortosiphonis folium ext, curcumae rhyzoma ext, Imperatae radix ext
7. Vidabion Cal Box/10 x 10 strip Ferrous fumarate, As folat, CaCO3, Vit
B12, Cholecalciferol, ascorbic acid