Lampiran 1. Tabel specific gravities 20o/20oC of alcohol-water mixtures
Lampiran 1. Tabel specific gravities 20o/20oC of alcohol-water mixtures
Lampiran 1. Tabel specific gravities 20o/20oC of alcohol-water mixtures
Lampiran 1. Tabel specific gravities 20o/20oC of alcohol-water mixtures
Lampiran 1. Tabel specific gravities 20o/20oC of alcohol-water mixtures
Lampiran 2
Data pengamatan kadar total padatan terlarut
Daftar Sidik ragam Total padatan terlarut
SK db JK KT F Hit F 0.05 F 0.01
Kombinasi Ulangan Total Rataan
Lampiran 3
Data pengamatan pH
Kombinasi Ulangan Total
Daftar Sidik Ragam pH
Lampiran 4
Data pengamatan kadar alkohol
Kombinasi Ulangan Total Rataan
Lampiran 5
Data pengamatan organoleptik warna Kombinasi
Daftar Sidik Ragam Organoleptik Warna
Lampiran 6
Data pengamatan organoleptik aroma
Kombinasi Ulangan Total Rataan
1 2
Daftar Sidik Ragam Organoleptik Aroma
Lampiran 7
Data pengamatan uji organoleptik rasa Kombinasi
Daftar Sidik Ragam Uji Orgnoleptik Rasa
Lampiran 8.
Gambar produk minuman ferbeet
P1L1 P2L1 P3L1 P4L1 P1L2 P2L2
P3L2 P4L2 P1L3 P2L3 P3L3 P4L3
P1L4 P2L4 P3L4 P4L4
Keterangan:
P1 = Penambahan gula pasir 10% w/v
P2 = Penambahan gula pasir 15% w/v
P3 = Penambahan gula pasir 20% w/v
P4 = Penambahan gula pasir 25% w/v
L1 = Fermentasi selama 2 hari
L2 = Fermentasi selama 4 hari
L3 = Fermentasi selama 6 hari
Agam, C. F. S. 2012. Pengaruh derajat keasaman dan konsentrasi starter ragi terhadap mutu minuman beralkohol dari sirsak. Skripsi. Fakultas Pertanian Universitas Sumatera Utara, Medan.
Amerine, M. A. dan C. S. Ough. 1980. Method for Analysis of Musts and Wine. John Wiley and Sons, Inc., New York.
Anam, C., Kawiji dan Setiawan, R. D. 2013. Kajian karakteristik fisik dan sensori serta aktivitas antioksidan dari granul effervescent buah beet (Beta
vulgaris) dengan perbedaan metode granulasi dan kombinasi sumber
asam. Jurnal Teknosains Pangan. 2(2): 21-28.
Ananda, L. 2008. Karakteristik fisikokimia serbuk bit merah (Beta vulgaris L.). Skripsi. Fakultas Teknologi Pertanian Universitas Katolik Soegijapranata,Semarang.
Apriyantono A., F., D.Puspitasari, N. L., Sedarnawati, danBudiyanto S. 1989. Analisis Pangan. PAU Pangan dan Gizi, Bogor.
Badan Standarisasi Nasional, 1996. SNI 01-4019-1996. Anggur Buah. http/bsn.go.id.
Bangun, M. K. 1991. Perancangan Percobaan. USU-Press, Medan.
Bernard, H., Anastasia, S., Maria, S., Gerard S., dan Sophie, V. S. 2012. Alcohol Consumption, Beverage Preference, and Diet in Middle-Aged Men from the Stanislas Study. Journal of Nutrition and Metabolism. 2(10):1-6.
Briggs, D. E., J. S. Hough, R. Stevens dan T. W. Young. 1981. Malting and Brewing Science. Chapman and Hall, London.
Coles, L. T. dan Clifton, P. M. 2012.Effect of beetroot juice on lowering blood pressure in free-living, disease-free adults : a randomized, placebo-controlled trial. Nutrition Journal. 11(1): 106-115.
Departemen perindustrian. 1973. Mutu dan Cara Pengujian Minuman Beralkohol, Jakarta.
Desrosier, N. W. 1988. Teknologi Pengawet Pangan, Terjemamahan Muchji Mulohardjo, UI-Press, Jakarta.
Dwidjoseputro, D. 1978. Dasar-dasar Mikrobiologi. Djambatan, Jakarta. Frazier, W. C. dan Westhoff, D. C., 1979. Food Microbiologi. Tata Mc Graw Hill
Publishing Company Ltd, New York.
Hamidah, H. 2003. Produksi Alkohol. USU- Press, Medan. Hidayat, N. 2007. Mikrobiologi Industri. Fakultas Pertanian Universitas
Brawijaya, Malang.
International Comission of Micobiological Specifications for Foods (ICMSF). 1980. Microbial Ecology of Foods Volume 1. Factors Affecting Life and Death of Microorganisms. Academic Press, New York.
International Comission of Micobiological Specifications for Foods (ICMSF). 1980. Microbial Ecology of Foods Volume 2. Food Commodities. Academic Press, New York.
Isnan, M. 2009.Saccharomyces cereviseae. http://www.food-industry.co.id. [21september 2015].
Judoamidjojo, M., A. A. Darwisdan E. G. Said. 1992. Teknologi Fermentasi. Rajawali-press, Jakarta.
Latorre, M. E., Bonelli,P. R.,Rojas, A. M.,dan Gerschenson, L. N. 2012. Microwave inactivation of red beet (Beta vulgaris L. var. conditiva) peroxidase and polyphenoloxidase and the effect of radiation on vegetable tissue quality. Journal of Food Engineering. 109 (1): 676-684.
Mangunwidjaja, D. dan A. Suryani. 1994. Teknologi Bioproses. Penebar Swadaya, Jakarta.
Maurice, M. L. 2011. Factors effecting ethanol fermentation via simultaneous saccharification and fermentation. Skripsi. Shanghai Jiao Tong University, Shanghai.
Nikon. 2004. Saccharomyces yeast cells: nikon microscopy. Phase contrast image galery.http//www.microscopy.com/galleries/pliasecontrast/
saccharomycessmall. Html (15 oktober 2009).
Nisa, A., Saeed, K., Hina, S., Zahra, N., Mazhar, S., Kalim, L., dan Syed, Q. 2015. Nutritional, Antioxidant, Microbiological and Toxicological Studies on Red Dye Extracted from Red Beet Roots (Beta vulgaris). Research Journal of Chemical Science. 5(4):1-6.
Nurdiyastuti, I. 2008. Prospek Pengembangan Pangan Fungsional. http://www.sinarharapan.com. [21 September 2015].
Palczar, M. Z., Reid dan Chen. 1983. Microbiology. 4th edition, Tata Mc. Graw-hill Book Company, New York.
Prentis, S. 1990. Bioteknologi; Suatu Revolusi Industri yang baru.Penerjemah Maggy Thenawidjaja. Erlangga, Jakarta.
Ocloo F. C. K. dan Ayernor G. S. 2008. Physical, chemical and microbiological changes in alcoholic fermentation of sugar syrup from cassava flour. African Journal of Biotechnology, 7 (2) : 164-168.
Prescott, S. Dan C. G. Dunn. 1981. Industrial Microbiology. Mc. Graw-Hill Book. Co. New York.
Rizani, K. Z. 2000. Pengaruh Konsentrasi Gula Reduksi dan Inokulum (Saccharomyces cereviseae) Pada proses fermentasi produksi etanol. Skripsi. Jurusan Biologi. Fakultas Matematika dan Ilmu Pengetahuan Alam. Universitas Brawijaya, Malang.
Rupesh S., B. K. Mishra, K. B. Shukla, N. K. Jain, K. C. Sharma, K. Sunil, K. Krishna, dan J. K. Ranjan. 2013. Fermentation Process for Alcoholic Beverage Production From Mahua (Madhuca indica J. F. Mel.) Flowers. African Journal of Biotechnology. 2(39): 5771-5777.
Sa`id, E. G. 1987. Bio Industri Penerapan teknologi Fermentasi. P.T Medyatama Sarana Perkasa, Jakarta.
SCI. 2015. Where Science Meets Business Siahaan, Andri S. 2010. Pengaruh Konsentrasi Ragi dan Lama Fermentasi
Terhadap Mutu Minuman Beralkohol Dari Nenas. [Skripsi]. Fakultas Pertanian Universitas Sumatera Utara, Medan.
Slavov, A., Karagyozov,V.,Denev,P., Kratchanova, M., dan Kratchanov, C. 2013. Antioxidant activity of red beet juices obtained after microwave and thermal pretreatments. Czech Journal of Food Science. 2(31): 139-147.
Soekarto, S. T. 1985. Penilaian Uji Organoleptik Untuk Industri Pangandan Hasil Pertanian. IPB-press, Bogor.
Sudarmadji, S., B. Haryona, dan Suhardi. 1989. Prosedur Analisa Untuk Bahan Makanan dan Pertanian. Liberty, Yogyakarta.
Tahir A., Madiha A., dan Tasnim F. 2010. Effect of Cultural Conditions on Ethanol Production by Locally Isolated Saccharomyces cerevisiae BIO-07. Journal of Applied Pharmacy. 3(2): 72-78.
Tom, C., Glyn, H., Daniel, J. W., dan Emma J. S. 2015. The Potential Benefits of Red Beetroot Supplementation in Health and Disease. Journal of Nutrients. 10(7):2801-2822.
USDA. 2013. Nutrition Fact Raw Beet Widyaningrum, M. L. dan Suhartiningsih. 2014. Pengaruh penambahan bit (Beta
vulgaris) terhadap sifat organoleptik kerupuk. E-Journal Boga. 3(1):
233-238.
Tempat dan Waktu Penelitian
Penelitian dilaksanakan pada bulan Februari sampai Maret 2016 di Laboratorium Teknologi Pangan Program Studi Ilmu dan Teknologi Pangan Fakultas Pertanian Universitas Sumatera Utara Medan.
Bahan Penelitian
Akar bit merah, gula pasir, ragi roti merek saf-Instant.
Bahan Kimia
Asam sitrat 0,1N, NaOH 0,1 N, NaOH 40% Phenolftalein dan akuades.
Alat Penelitian
Media fermentasi, blender, beaker glass, pipet skala, hand refraktometer, labu suling, biuret, erlenmeyer, pH meter, kain saring, piknometer, pancistainless
steel, botol kaca, tutup botol, aluminium foil, pisau stainless steel, timbangan,
spatula, kertal label, sendok stainless steel, dan termometer.
Metode Penelitian
Penelitian ini dilakukan dengan menggunakan rancangan acak lengkap (RAL) (Bangun, 1991), yang terdiri dari dua faktor, yaitu:
Faktor I : Konsentrasi gula pasir (P) : P1 = 10 %
P2 = 15%
P3 = 20%
Faktor II : Lama fermentasi (L): L1 = 2 hari
L2 = 4 hari
L3 = 6 hari
L4 = 8 hari
Banyaknya kombinasi perlakuan atau Treatment Combination (Tc) adalah4 x 4 = 16, maka jumlah ulangan (n) minimum adalah sebagai berikut:
Tc (n-1) ≥ 15 16 (n-1) ≥ 15 16 n -16 ≥ 15 n ≥ 1,93
Jadi, untuk ketelitian dalam penelitian ini dilakukan ulangan sebanyak 2 kali.
Model Rancangan
Penelitian ini dilakukan dengan model rancangan acak lengkap (RAL) dua faktorial (Bangun, 1991),dengan model sebagai berikut:
Ŷijk = µ + αi + βj + (αβ)ij + εijk
dimana:
Ŷijk : Hasil pengamatan dari faktor P pada taraf ke-i dan faktor L pada taraf ke-j dalam ulangan ke-k
µ : Efek nilai tengah
αi : Efek faktor P pada taraf ke-i βj : Efek faktor L pada taraf ke-j
(αβ)ij : Efek interaksi faktor P pada taraf ke-i dan faktor L pada taraf ke-j
Apabila diperoleh hasil yang berbeda nyata dan sangat nyata maka uji dilanjutkan dengan uji beda rataan, menggunakan uji Least Significant Range (LSR).
Pelaksanaan Penelitian
Pembuatan starter
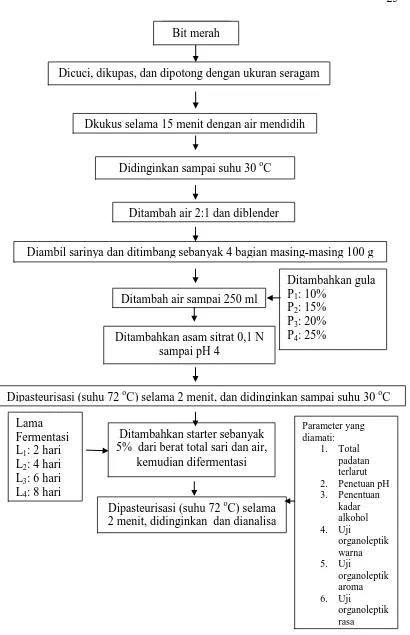
Dipanaskan air sampai mendidih dan ditambahkan gula sebanyak 20% w/v, kemudian diaduk hingga larut dan didinginkan sampai suhu 30 oC. Setelah dingin ditambahkan ragi roti sebanyak 3 gram tiap 100 ml larutan, kemudian diinkubasi selama 24 jam. Skema pembuatan starter dapat dilihat pada Gambar 2. Pembuatan minuman ferbeet
Pengamatan dan Pengukuran Data
Pengamatan dan pengukuran data dilakukan dengan cara analisis terhadap parameter sebagai berikut:
- Total padatan terlarut - pH
- Kadar alkohol
- Nilai uji organoleptik warna - Nilai uji organoleptik aroma - Nilai uji organoleptik rasa
Penentuan total padatan terlarut
Total padatan terlarut ditentukan dengan metode Sudarmadji, dkk. (1986). Sampel ferbeetditimbang sebanyak 5 g, dimasukkan ke dalam gelas ukur,kemudian diberi penambahan akuades sebanyak 20 ml dan diaduk hingga homogen. Diambil satu tetes larutan dan diteteskan pada prisma
handrefractometer lalu dibaca angka di titik terang dan gelap pada skala
refraktometer. Nilai total padatan terlarut (TSS) dihitung dengan mengalikan skala refraktometer dengan faktor pengenceran (FP).
TSS (ºBrix) = skala refraktometer x FP FP = Faktor Pengencer
Penentuan pH
(15 - 30 menit). Elektroda pada pH meter dibilas dengan akuades dan dikeringkan elektroda dengan kertas tisu. Setelah itu elektroda dicelupkan ke dalam larutan sampel dan di-set pengukur pH – nya.Elektroda dibiarkan tercelup di dalam larutan selama beberapa saat sampai diperoleh pembacaan yang stabil, lalu nilai pH sampel dicatat.
Penentuan kadar alkohol
Kadar alkohol dihitung menurut SNI 01-4019-1996 sebagai etil alkohol. Diambil contoh sebanyak 100 ml dalam labu suling dan ditambahkan akudes 50 ml kemudian didestilasi. Hasil destilasi ditampung dengan piknometer sampai tanda garis (50 ml). Piknometer didinginkan pada suhu 20oC selama 15 menit kemudian ditimbang. Sebagai pembanding dihitung berat piknometer kosong dan berat air pada suhu 20oC. Dari tabel spesifik gravity of ethanol at 20oC (lampiran 1) pada suhu menunjukkan kadar etil alkohol pada sampel.
BJ Etil Alkohol = berat etil alkohol sulingan pada 20oC Berat air pada 20oC
Penentuan nilai uji organoleptik warna
Tabel 5. Skala nilai skor warna
Skala numerik Keterangan
4 ungu kemerahan
3 merah kecokelatan
2 kecokelatan
1 cokelat kehitaman
Penentuan nilai uji organoleptik aroma
Uji organoleptik aroma dilakukan dengan metode Soekarto(1985). Uji kesukaan atau uji hedonik dilakukan terhadap aroma minuman dengan 17 orang panelis. Caranya dengan memberikan sampel yang telah diberi kode kepada 17 orang panelis yang melakukan penilaian. Penilaian dilakukan dengan skala 1-4 berdasarkan Tabel 6:
Tabel 6. Skala nilai hedonik aroma
Skala hedonik Keterangan
4 sangat suka
3 suka
2 agak suka
1 tidak suka
Penentuan nilaiuji organoleptik rasa
Tabel 7. Skala nilai hedonik rasa
Skala numerik Keterangan
4 sangat suka
3 suka
2 agak suka
Gambar 2. Skema pembuatan starter Dipanaskan air
sampai mendidih
Ditambahkan gula 20% w/v
Didinginkan sampai suhu 30 oC
Ditambahkan ragi roti 3 g/100 ml
Diinkubasi selama 24 jam
Bit merah Bit merah
Dkukus selama 15 menit dengan air mendidih
Didinginkan sampai suhu 30 oC
Diambil sarinya dan ditimbang sebanyak 4 bagian masing-masing 100 g Ditambah air 2:1 dan diblender
Ditambahkan gula P1: 10%
P2: 15%
P3: 20%
P4: 25%
Dicuci, dikupas, dan dipotong dengan ukuran seragam
Ditambah air sampai 250 ml
Dipasteurisasi (suhu 72 oC) selama 2 menit, dan didinginkan sampai suhu 30 oC
Dipasteurisasi (suhu 72 oC) selama 2 menit, didinginkan dan dianalisa Lama
Ditambahkan asam sitrat 0,1 N sampai pH 4
Ditambahkan starter sebanyak 5% dari berat total sari dan air,
Berdasarkan hasil penelitian yang telah dilakukan, penambahan gula pasir memberikan pengaruh terhadap total padatan terlarut, pH, kadar alkohol, dan uji organoleptik. Pengaruh penambahan gula pasir dan lama fermentasi dijelaskan sebagai berikut;
Pengaruh Penambahan Gula Pasir Terhadap Parameter yang Diamati
Hasil penelitian menunjukkan bahwa penambahan gula pasir memberikan pengaruh terhadap parameter yang diamati. Pengaruh penambahan gula pasir terhadap parameter dapat dilihat pada Tabel 8.
Tabel 8. Pengaruh penambahan gula pasir terhadap parameter yang diamati Parameter yang diuji Konsentrasi gula pasir
P1=10% P2=15% P3=20% P4=25%
Keterangan: Notasi huruf yang berbeda menunjukan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
Tabel 8 menunjukkan bahwa total padatan terlarut tertinggi terdapat pada perlakuan P4 yaitu sebesar 13,544oBrix sedangkan total padatan terlarut paling
rendah terdapat pada perlakuan P1 sebesar 5,0895 oBrix. Nilai pH tertinggi
terdapat pada perlakuan P4 sebesar 3,3163, sedangkan pH terendah pada
perlakuan P1 sebesar3,1538. Kadar alkohol tertinggi sebesar 8,1275 %w/w berada
pada perlakuan P3 dan kadar alkohol terendah pada perlakuan P1sebesar
Uji organoleptik warna tertinggi terdapat pada perlakuan P1 sebesar 3,2916
(merah keunguan) dan organoleptik paling rendah terdapat pada perlakuan P3
sebesar 3,2250 dengan warna merah cerah. Uji organoleptik aroma paling tinggi terdapat pada perlakuan P3 sebesar 3,0417 (paling disukai panelis) dan nilai
aroma paling rendah yaitu perlakuan P4 sebesar 2,8583. Sedangkan organoleptik
rasa tertinggi ada pada perlakuan P4sebesar 3,2833 dan terendah pada perlakuan
sebesar 2,9917.
Tabel 8 juga menunjukkan bahwa semakin tinggi penambahan konsentrasi gula pasir maka semakin tinggi nilai total padatan terlarut dan pH yang dihasilkan, sedangkan kadar alkohol semakin meningkat hingga perlakuan P3(penambahan
gula 20%w/v), namun menurun kembali pada konsentrasi gula 25% w/v. Uji organoleptik warna dipengaruhi oleh warna merah dari bit (merah keunguan), dimana warna bit alami memberi nilai yang paling tinggi, sedangkan nilai hedonik rasa dipengaruhi oleh rasa manis dari gula pasir yang ditambahkan, dimana semakin tinggi konsentrasi gula pasir yang ditambahkan maka nilai organoleptik rasa semakin tinggi.
Pengaruh Lama Fermentasi Terhadap Parameter yang Diamati
Tabel 9. Pengaruh lama fermentasi terhadap parameter yang diamati
Parameter yang diuji Lama fermentasi
L1 L2 L3 L4
Keterangan: Notasi huruf yang berbeda menunjukan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar).
L1= 2 hari L2= 4 hari L3= 6 hari L4= 8 hari
Tabel 9 menunjukkan bahwalama fermentasi berpengaruh terhadap total padatan terlarut, dimana semakin lama lama fermentasi derajat total padatan terlarut yang terdapat pada minuman semakin rendah. Total padatan terlarut paling tinggi terdapat pada perlakuan lama fermentasi paling singkat (L1) sebesar
13,4621oBrixdan total padatan terlarut yang paling rendah terdapat pada perlakuan L4 sebesar 5,9378oBrix. Lama fermentasi juga mempengaruhi nilai pH minuman,
dimana pH paling tinggi terdapat pada perlakuan P1 sebesar 3,4113 dan paling
rendah pada perlakuan P4 sebesar 3,0163.Kadar alkohol paling tinggi terdapat
pada perlakuan L4 sebesar 10,3438 %w/w dan paling rendah pada perlakuan P1
-sebesar 3,4325 %w/w. Nilai uji organoleptik warna minuman paling tinggi terdapat pada perlakuan L1sebesar 3,3250 dan paling rendah pada perlakuan L3
sebesar 3,1750. Nilai uji organoleptik aroma tertinggi terdapat pada perlakuan L4
-sebesar 3,1083dan nilai yang paling rendah terdapat pada perlakuan L1sebesar
2,7917. Nilai organoleptik rasa tertinggi terdapat pada perlakuan
Total Padatan Terlarut
Pengaruh penambahan gula pasir terhadap total padatan terlarut
Berdasarkan daftar analisis sidik ragam (lampiran 2) menunjukkan bahwa penambahan gula pasir memberi pengaruh berbeda sangat nyata (P<0,01) terhadap kadar total padatan terlarut minuman. Hasil uji LSR (Least Significant
Range) pengaruh penambahan gula pasir terhadap total padatan terlarut dapat
dilihat pada Tabel 10.
Tabel 10. Uji LSR pengaruh penambahan gula pasir terhadap total padatan terlarut
Jarak LSR Konsentrasi gula Rataan Notasi
0,05 0,01 (%w/v) 0,05 0,01
- - - P1=10% 5,0895 d D
2 0,7653 1,0699 P2=15% 7,1651 c C
3 0,8143 1,1158 P3=20% 9,9215 b B
4 0,8379 1,1461 P4=25% 13,5450 a A
Keterangan: Notasi huruf yang berbeda menunjukan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
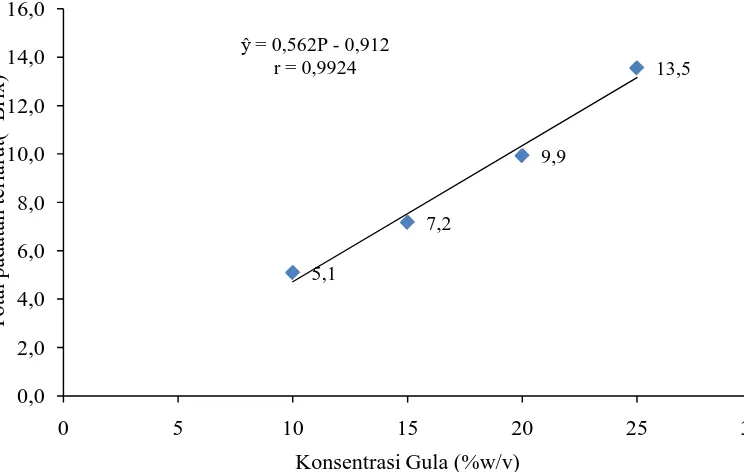
Tabel 10menunjukkan bahwa perlakuan P4 (penambahan gula pasir
sebayak 25%w/v) menghasilkan nilai total padatan terlarut paling tinggi sebesar 13,5450 obrix, sedangkan perlakuan P1 (penambahan gula pasir sebanyak
Gambar 4. Hubungan penambahan gula pasir dengantotal padatan terlarut
Tabel 10 dan Gambar 4 dapat dilihat bahwa penambahan gula pasir menghasilkan nilai total padatan terlarut yang semakin tinggi. Hal ini disebabkan karena gula (sukrosa) tersusun atas glukosa dan fruktosa dan sangat mudah larut di dalam air, sesuai dengan skripsi Nova (2009) yang menjelaskan bahwa penambahan gula pasir pada minuman campuran sari buah sebesar 185%, 200%, 215%, 230%, dan 245% menunjukkan peningkatan kadar total padatan terlarut dari 79,6 oBrix sampai 94,6 oBrix dan semakin banyak konsentrasi dalam produk maka kandungan karbohidrat yang larut akan semakin tinggi.
Pengaruh lama fermentasi terhadap total padatan terlarut
Daftar analisis sidik ragam total padatan terlarut (Lampiran 2) menunjukkan bahwa lama fermentasi memberi pengaruh berbeda sangat nyata (P<0,01) terhadap nilai total padatan terlarut yang dihasilkan. Hasil uji Least
Significant Range (LSR) terhadap total padatan terlarut dapat dilihat pada
Tabel 11. Uji LSR pengaruh lama fermentasi terhadap total padatan terlarut
Jarak LSR Lama fermentasi Rataan Notasi
0,05 0,01 (hari) 0,05 0,01
- - - L1=2hari 13,4621 a A
2 0,7653 1,0699 L2=4hari 8,6816 b B
3 0,8143 1,1158 L3=6hari 7,6396 c B
4 0,8379 1,1461 L4=8hari 5,9378 d C
Keterangan: Notasi huruf yang berbeda menunjukan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
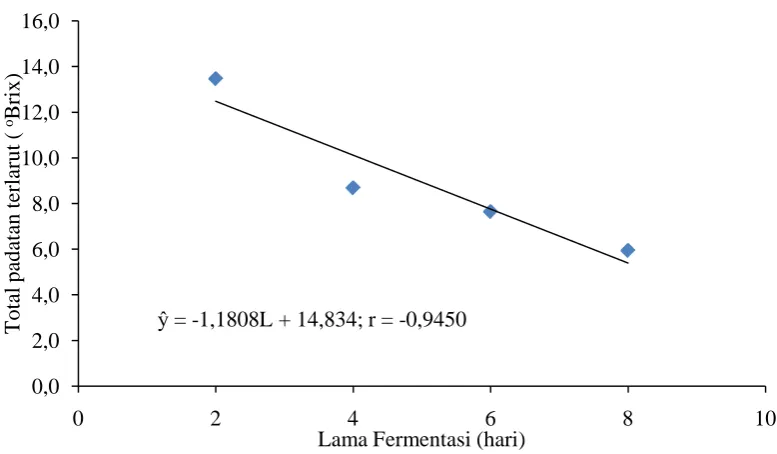
Tabel 11 menunjukkan bahwa perlakuan L1 (lama fermentasi 2 hari)
menghasilkan nilai total padatan terlarut yang paling tinggi,hal ini sesuai dengan literatur Winarno,dkk (1990) yang menyatakan bahwa total padatan terlarut merupakan jumlah gula pereduksi yang terdapat pada bahan dan menurut Judoamidjojo, dkk (1992) yang menyatakan bahwa salah satu jenis mikrorganisme yang memiliki daya konversi gula paling tinggi adalah
Saccharomycescerevisiae. Perlakuan L1 merupakan perlakuan dengan lama fermentasi paling singkat, sehingga gula yang dikonversi oleh
Saccharomycescerevisiae akan lebih sedikit dibandingkan perlakuan lainnya.
Semakin lama waktu fermentasi maka jumlah gula yang dikonversi juga semakin banyak, sehingga perlakuan L1 menjadi perlakuan dengan nilai total padatan
Gambar 5. Hubungan lama fermentasidengan total padatan terlarut
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap total padatan terlarut
Data analisis sidik ragam (lampiran 2)menunjukkan bahwa interaksi antara lama fermentasi dan penambahan gula pasir berbeda sangat nyata (P<0,01) terhadap nilai total padatan terlarut minuman ferbeet yang dihasilkan. Uji LSR (Least Significant Range)interaksi antara penambahan gulapasir dan lama fermentasi terhadap total padatan terlarut minuman ferbeet dapat dilihat pada Tabel 12.
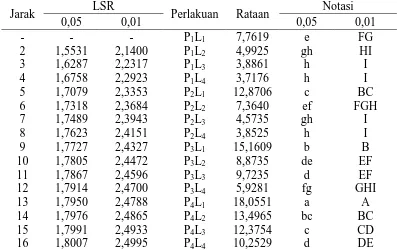
Tabel 12 menunjukkan bahwa perlakuan P4L1 (penambahan gula pasir
sebanyak 25% w/v dan lama fermentasi 2 hari) menghasilkan nilai total padatan terlarut paling tinggi yaitu sebesar 18,0551 oBrix, dan perlakuan P1L4
(penambahan gula pasir sebanyak 10% w/v dan lama fermentasi 8 hari) menghasilkan nilai total padatan terlarut paling rendah yaitu sebesar 3,7176 oBrix. Hubungan interaksi antara penambahan gula pasir dan lama fermentasi dengan total padatan terlarut dapat dilihat pada Gambar 6.
Tabel 12. Uji LSR pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap total padatan terlarut
Jarak LSR Perlakuan Rataan Notasi
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Gambar 6. Hubungan interaksi antara penambahan gula pasir dan lama fermentasi dengan total padatan terlarut
Gambar 6 menunjukkan bahwa semakin tinggi konsentrasi gula yang ditambahkan ke dalam minuman dan lama fermentasi yang paling singkat menunjukkan nilai total padatan terlarut yang paling tinggi (perlakuan P4L1)
sebesar 18,0551obrix. Hal ini disebabkan oleh karena penambahan gula pasir ke dalam minuman akan meningkatkan jumlah gula pereduksi, dimana jumlah gula pereduksi yang akan diukur dalam derajat total padatan terlarut (Winarno, 1984), lama fermentasi yang semakin lama akan menurunkan nilai total padatan terlarut minuman, hal ini disebabkan karena dalam proses fermentasi terjadi perombakan karbohidrat dan gula menjadi senyawa yang lebih sederhana oleh khamir
Sacccharomycess cereviseae. Hal ini sesuai dengan literatur Hidayat, dkk (2006)
yang menyatakan bahwa fermentasi dapat diartikan sebagai perubahan gradual karbohidrat yang dilakukan oleh bakteri, khamir, ataupun jamur, sehingga kadar karbohidrat/gula akan menurun atau berkurang.
Penentuan Nilai pH
Pengaruh penambahan gula pasir terhadap pH
Daftar sidik ragam (lampiran 3) menunjukkan bahwa penambahan gula pasir memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap nilai pH minuman ferbeet, sehingga uji LSR tidak dilanjutkan.
Pengaruh lama fermentasi terhadap pH
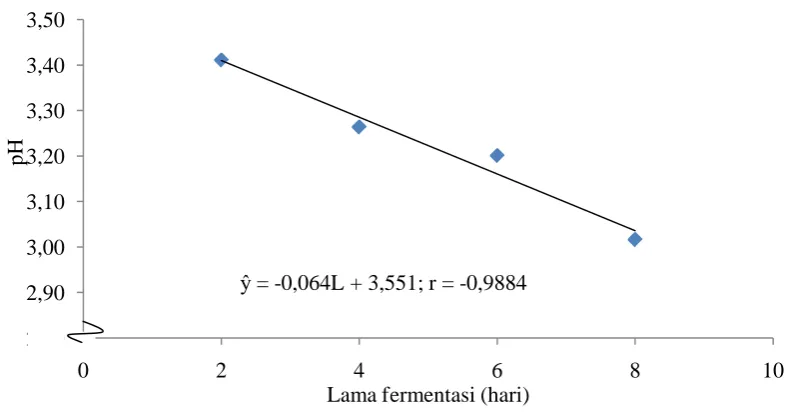
Tabel 13. Uji LSR pengaruh lama fermentasi terhadap pH minuman ferbeet
Jarak LSR Lama fermentasi Rataan Notasi
0,05 0,01 (hari) 0,05 0,01
- - - L1= 2 hari 3,411 a A
2 0,178 0,245 L2= 4 hari 3,264 ab AB
3 0,186 0,255 L3= 6 hari 3,201 b AB
4 0,192 0,262 L4= 8 hari 3,016 c B
Keterangan: Notasi huruf yang berbeda menunjukkan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Tabel 13 menunjukkan bahwa lama fermentasi selama 2 hari (L1)
merupakan perlakuan dengan pH paling tinggi yaitu sebesar 3,411, dan perlakuan dengan pH paling rendah adalah L4 (fermentasi selama 8 hari).
Adapun hubungan antara lama fermentasi (L) dengan pH minuman dapat dilihat pada Gambar 7.
Gambar 7. Hubungan lama fermentasi dengan pH
Tabel 13 dan Gambar 7 menunjukkan bahwa semakin lama waktu fermentasi nilai pH minuman juga semakin menurun, hal ini disebabkan karena dalam proses fermentasi akan dihasilkan senyawa asam yang akan menyesuaikan
literatur Amerine, dkk (1980) yang menyatakan bahwa semakin lama waktu fermentasi makan akan semakin banyak asam-asam mudah menguap yang dihasilkan, dan menurut Desrosier (1988) yang menyatakan bahwa semakin lama proses fermentasi maka akan semakin banyak asam mudah menguap (asam laktat, asam asetat, asam butirat, dan asam propionat), dimana asam yang dihasilkan berasal dari perombakan glukosa menjadi alkohol.
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap pH
Data analisis sidik ragam (Lampiran 3) menunjukkan bahwa interaksi lama fermentasi dan penambahan gula pasir memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap pH minuman ferbeet, sehingga uji LSR tidak dilanjutkan.
Kadar Alkohol
Pengaruh penambahan gula pasir terhadap kadar alkohol
Penambahan gula pasir pada proses fermentasi minuman ferbeet memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap kadar alkohol minuman ferbeet. Uji LSR (Least Significant Range) pengaruh penambahan gula pasir dengan kadar alkohol minuman dapat dilihat pada Tabel 14.
Tabel 14. Uji LSR pengaruh penambahan gula pasir terhadap kadar alkohol Jarak LSR Konsentrasi gula Rataan Notasi
0,05 0,01 (%w/v) 0,05 0,01
- - - P1 = 10% 6,7763 bc BC
2 0,21099 0,29073 P2= 15% 7,3012 bc BC
3 0,22127 0,30319 P3= 20% 8,1275 a A
4 0,22767 0,31142 P4= 25% 7,3862 b B
Keterangan: Notasi huruf yang berbeda menunjukan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
penurunan pada perlakuan P4 (penambahan gula sebesar 25% w/v). Adapun
hubungan penambahan gula pasir dengan kadar alkohol (%w/w) dapat dilihat pada Gambar 8.
Gambar 8. Hubungan penambahan gula pasir dengan kadar alkohol
Pengaruh lama fermentasi terhadap kadar alkohol
Data analisis sidik ragam (Lampiran 4) menunjukkan bahwa lama fermentasi memberi pengaruh sangat nyata (P<0,01) terhadap kadar alkohol minuman ferbeet. Uji LSR (Least Significant Range) pengaruh lama fermentasi terhadap kadar alkohol minuman dapat dilihat pada Tabel 15.
Tabel 15. Uji LSR pengaruh lama fermentasi terhadap kadar alkohol (%w/w)
Jarak LSR Lama fermentasi Rataan Notasi
0,05 0,01 (hari) 0,05 0,01
- - - L1 = 2 hari 3,4325 d D
2 0,21099 0,29073 L2= 4 hari 6,5238 c C
3 0,22127 0,30319 L3= 6 hari 9,2913 b B
4 0,22767 0,31142 L4= 8 hari 10,3438 a A
Keterangan: Notasi huruf yang berbeda menunjukan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Dilihat dari tabel di atas, kadar alkohol paling tinggi dihasilkan dengan perlakuan L4 (fermentasi selama 8 hari) yaitu sebesar 10,343%w/w. Kadar alkohol
paling rendah dihasilkan dengan perlakuan fermentasi paling singkat (L1selama 2 hari) yaitu sebesar 3,4325%w/w. Hubungan antara lama fermentasi
dengan kadar alkohol minuman ferbeet juga dapat dilihat pada Gambar 9.
Tabel 15 dan Gambar 9menunjukkan bahwa lama fermentasi (L) memberi pengaruh terhadap kadar alkohol pada minuman. Semakin lama proses fermentasi maka kadar alkohol minuman akan semakin tinggi pula. Hal ini sesuai dengan literatur Tahir, dkk (2010), yang menyatakan bahwa proses fermentasi dengan suhu 30oC, pH, waktu inkubasi 48 jam, dan konsentrasi gula 15% menunjukkan peningkatan produksi alkohol hingga 94% gula terfermentasi. Hal ini juga didukung literatur Rupesh, dkk (2013), dimana pada proses fermentasi bunga
Mahua dengan menggunakan Saccharomyces cerevisiae selama 21 hari
menunjukkan proses peningkatan produksi alkohol hingga proses fermentasi selesai. Proses fermentasi juga dipengaruhi oleh pH substrat, dimana pH optimum adalah 4.
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap kadar alkohol
Lama fermentasi dan penambahan gula pasir memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap kadar alkohol minuman ferbeet (lampiran 1). Uji LSR (Least Significant Range) pengaruhinteraksi penambahan gula pasir dan lama fermentasi terhadap kadar alkoholminuman dapat dilihat pada Tabel 16.
Tabel 16 menunjukkan bahwa kadar alkohol paling dihasilkan pada perlakuan P3L4(lama fermentasi 8 hari dan penambahan gula 20% w/v) yaitu
sebesar 11,405% w/w, sedangkan perlakuan fermentasi selama 2 hari dan penambahan gula 10% w/v (P1L1) menghasilkan alkohol paling rendah sebesar
Tabel 16. Uji LSR pengaruh interaksipenambahan gula dan lama fermentasi terhadap kadar alkohol minuman ferbeet
Jarak LSR Perlakuan Rataan Notasi
Keterangan: Notasi huruf yang berbeda menunjukan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Gambar 10. Hubungan interaksi lama fermentasi dan penambahan gula dengan kadar alkohol minuman ferbeet
Tabel 16 dan Gambar 10 menunjukkan bahwa interaksi perlakuan P3L4 menghasilkan alkohol paling tinggi, hal ini terjadi karena waktu fermentasi
paling lama (L4) akan menghasilkan alkohol yang semakin tinggi, dan
penambahan gula pasir sebanyak 20%w/v (P3) menunjukkan konsentrasi optimum
produksi alkohol. Hal ini sesuai dengan literatur Sa`id (1987), konsentrasi gula optimum pada proses fermentasi adalah 28% dan konsentrasi gula yang berlebih dapat menghambat aktivitas khamir, dan menurut USDA (2013) kandungan karbohidrat bit merah sebesar 9,96%w/w. Berdasarkan literatur tersebut perlakuan P3 (penambahan gula sebesar 20%) menjadi perlakuan dengan produksi alkohol
paling tinggi karena kekurangan substrat (karbohidrat atau gula) pada perlakuan P3 dapat diperoleh dari bit merah itu sendiri. Adapun Perlakuan L4 (fermentasi
selama 8 hari) menghasilkan alkohol paling tinggi karena semakin lama waktu fermentasi maka alkohol yang dihasilkan semakin tinggi(Sa`id, 1987).
Uji Organoleptik Warna
Pengaruh penambahan gula pasir terhadap uji organoleptik warna
Daftar analisis sidik ragam (Lampiran 5) menunjukkan bahwa penambahan gula pasir memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap nilai uji organoleptik warna minuman ferbeet, sehingga uji LSR tidak dilanjutkan.
Pengaruh lama fermentasi terhadap uji organoleptik warna
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap uji organoleptik warna
Daftar analisis sidik ragam (Lampiran 5) menunjukkan bahwa Interaksi lama fermentasi dan penambahan gula pasir memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap nilai uji organoleptik warna minuman ferbeet, sehingga uji LSR tidak dilanjutkan.
Uji Organoleptik Aroma
Pengaruh penambahan gula pasir terhadap nilai uji organoleptik aroma
Daftar sidik ragam uji organoleptik aroma (Lampiran 6) menunjukkan bahwa penambahan gula pasir memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap nilai organoleptik aroma minuman ferbeet, sehingga uji LSR tidak dilanjutkan.
Pengaruh lama fermentasi terhadap uji organoleptik aroma
Daftaranalisis sidik ragam (Lampiran 6) menunjukkan bahwa lama fermentasi memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap aroma minuman ferbeet. Uji LSRpengaruh lama fermentasi terhadap uji organoleptik aroma dapat dilihat pada Tabel 17.
Tabel 17. Uji LSR pengaruh lama fermentasi terhadap nilai uji organoleptik aroma minuman ferbeet
Tabel 17 menunjukkan bahwa nilai uji organoleptik aroma semakin meningkat seiring dengan lama fermentasi yang semakin lama. Adapun hubungan lama fermentasi dengan nilai uji organoleptik aroma minuman ferbeet dapat dilihat pada Gambar 11.
Gambar 11. Hubungan lama fermentasi dengan nilai uji organoleptik aroma Gambar 11 menunjukkan bahwa nilai organoleptik aroma minuman
ferbeet meningkat secara linear seiring dengan lama fermentasi yang semakin
lama. Adapun nilai organoleptik aroma paling tinggi adalah perlakuan L4 dengan
lama fermentasi selama 8 hari. Nilai organoleptik aroma semakin meningkat seiring pertambahan lama fermentasi diakibatkan karena dalam proses fermentasi dihasilkan asam-asam organik mudah menguap dan alkohol yang semakin tinggi seiring penambahan lama fermentasi, hal ini sesuai dengan literatur Amerine, dkk (1980) yang menyatakan hal serupa. Asam-asam organik mudah menguap dan alkohol menghasilkan aroma yang khas, sehingga semakin lama fermentasi aroma khas minuman akan semakin kuat dan disukai panelis.
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap nilai uji organoleptik aroma
Daftar analisis sidik ragam organoleptik aroma (Lampiran 6) menunjukkan bahwa interaksi lama fermentasi dan penambahan gula pasir memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap nilai organoleptik aroma minuman ferbeet, sehingga uji LSR tidak dilanjutkan.
Uji Organoleptik Rasa
Pengaruh penambahan gula pasir terhadap nilai organoleptik rasa
Daftar analisis sidik ragam organoleptik rasa (Lampiran 7) menunjukkan bahwa penambahan gula pasir memberikan pengaruh berbeda nyata (P<0,05) terhadap nilai organoleptik rasa minuman febeet. Uji LSR pengaruh penambahan gula pasir terhadap nilai organoleptik rasa dapat dilihat pada Tabel 18.
Tabel 18. Uji LSR pengaruh penambahan gula pasir terhadap nilai organoleptik rasa
Jarak LSR penambahan
gula(%w/v) Rataan
Keterangan: Notasi huruf yang berbeda menunjukan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Gambar 12. Hubungan penambahan gula pasir dengan nilai organoleptik rasa
Gambar 13 menunjukkan bahwa penambahan gula pasir meningkatkan nilai organoleptik rasa minuman (disukai panelis), hal ini disebabkan gula pasir yang ditambahkan memiliki rasa manis yang disukai panelis. Hal ini sesuai dengan jurnal Drewnowski, dkk (2012), yang menyebutkan bahwa rasa manis pada makanan memberi kepuasan yang lebih tinggi karena reseptor rasa manis tidak hanya diekspresikan di dalam mulut, namun juga di daerah kerongkongan dan pankreas.
Pengaruh lama fermentasi terhadap uji organoleptik rasa
Daftar analisis sidik ragam organoleptik rasa (Lampiran 7) menunjukkan bahwa lama fermentasi memberikan pengaruh berbeda sangat nyata (P<0,01) terhadap nilai uji organolpetik rasa minuman ferbeet sehingga uji LSR dilanjutkan.Uji LSR pengaruh lama fermentasi terhadap uji organoleptik rasa dapat dilihat pada Tabel 19.
Tabel 19. Uji LSR pengaruh lama fermentasi terhadap nilai uji organoleptik rasa
Keterangan: Notasi huruf yang berbeda menunjukan pengaruh yang berbeda nyata pada taraf 5% (huruf kecil) dan berbeda sangat nyata pada taraf 1% (huruf besar)
Tabel 19 menunjukkan bahwa semakin lama waktu fermentasi, nilai organoleptik rasa minuman semakin menurun. Hubungan lama fermentasi dengan nilai organoleptik rasa juga dapat dilihat pada Gambar 13.
Gambar 13. Hubungan lama fermentasi dengan nilai organoleptik rasa
Gambar 12 menunjukkan nilai organoleptik rasa minuman menurun secara linear seiring dengan semakin lamanya waktu fermentasi, hal ini disebabkan karena pada proses fermentasi nilai pH minuman akan semakin rendah. Penurunan pH akan meningkatkan rasa asam yang tidak disukai panelis, hal ini sesuai dengan literatur Ocloo dan Ayernor (2008) yang menyatakan penurunan pH seiring dengan waktu fermentasi yang semakin lama dan menurut Desrosier
(1988) menyebutkan bahwa asam-asam organik yang dihasilkan semakin banyak seiring peningkatanwaktu fermentasi.
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap uji organoleptik rasa
Daftar analisis sidik ragam organoleptik rasa (Lampiran 7) menunjukkan bahwa interaksi penambahan gula pasir dan lama fermentasi memberikan pengaruh berbeda tidak nyata (P>0,05) terhadap nilai organoleptik rasa minuman
Kesimpulan
Dari hasil penelitian pengaruh penambahan gula pasir dan lama fermentasi terhadap mutu minuman ferbeet dapat diambil beberapa kesimpulan sebagai berikut:
1. Penambahan gula pasir memberikan pengaruh berbeda sangat nyata terhadap kadar total padatan terlarut, kadar alkohol, dan uji organoleptik rasa. Semakin tinggi penambahan gula pasir maka akan semakin besar gula pereduksi yang terlarut dalam minuman yang akan meningkatkan nilai total padatan terlarut dan organoleptik rasa, Penambahan gula pasir 20%w/v juga memberikan hasil optimum terhadap kadar alkohol minuman dibandingkan dengan konsentrasi 10%w/v, 15%w/v, dan 25%w/v.
2. Lama fermentasi memberikan pengaruh berbeda sangat nyata terhadap kadar total padatan terlarut, kadar alkohol, pH, uji organoleptik aroma, dan uji organoleptik rasa. Semakin lama waktu fermentasi maka kadar total padatan terlarut minuman akan semakin menurun, kadar alkohol semakin meningkat, nilai organoleptik aroma semakin meningkat, dan nilai organoleptik rasa semakin menurun.
Saran
1. Untuk memperoleh mutu minuman ferbeet yang baik disarankan untuk menetapkan penambahan gula pasir sebanyak 20%w/v dan lama fermentasi 8 hari (P3L4) karena kombinasi perlakuan tersebut
menghasilkan alkohol yang paling tinggi (11,405 w/w), sertanilai organoleptik aroma dan rasa yang disukai panelis.
Bit Merah
Bit merah (Beta vulgaris) merupakan tanaman berbunga dari famili
Chenopodiaceae, dengan ciri-ciri morfologis seperti umbi yang pada umumnya
dijadikan sebagai sayuran. Bit memiliki aroma yang khas seperti bau tanah (earthy taste), warna akar yang memiliki warna merah pekat, serta rasa yang manis seperti gula (Widyaningrum dan Suhartiningsih, 2014).
Tanaman bit memiliki ciri-ciri akar yang menggembung mirip dengan umbi-umbian sering disebut dengan buah bit. Warna merah yang terdapat pada buah bit disebabkan oleh adanya senyawa yang mengandung nitrogen dan juga merupakan senyawa antioksidan tinggi dan larut air, namun dapat mengalami kerusakan akibat perubahan pH, cahaya, udara, dan stabil pada suhu dibawah 14 oC, kondisi tanpa cahaya serta pH sekitar 5,6 (Anam, dkk., 2013).
bit dengan suhu yang tinggi. Betanin merupakan pigmen yang mudah terdegradasi oleh cahaya, oksigen, dan panas. Betalain sangat sensitif terhadap suhu, dimana betalain akan terdegradasi secara spontan seiring peningkatan suhu. Suhu optimum proses ekstraksi betalain dari bit merah yaitu sekitar 40oC (Nisa, dkk., 2015).
Bit sebagai salah satu pangan sumber nitrat merupakan faktor yang mempengaruhi semakin tingginya penelitian terhadap umbi bit, dimana nitrat merupakan komponen yang penting dalam menjaga kesehatan kardiovaskular. Disamping itu, bit juga mengandung komponen bioaktif yang baik untuk kesehatan, khususnya untuk mencegah penyakit yang ditimbulkan oleh inflamasi kronis. Konsumsi bit secara teratur juga akan meningkatkan pertahanan antioksidan tubuh, membantu melindungi komponen sel dari kerusakan oksidasi (Tom, dkk., 2015).
Pigmen Bit Merah
Gambar 1. Struktur kimia senyawa betalain (SCI, 2015)
Pigmen bit merah lebih stabil pada pH asam yaitu 4,5. Warna pigmen akan berubah menjadi ungu apabila terjadi penurunan pH dan akan berubah menjadi kuning kecokelatan apabila pH meningkat. Kandungan antioksidan bit merah merupakan yang tertinggi dibandingkan sayuran lain. Antioksidan pada bit merah terdiri dari flavonoid (350-2760 mg/kg), betasianin (840-900 mg/kg), betanin (300-600 mg/kg), asam askorbat (50-868 mg/kg), dan karotenoid (0,44 mg/kg) (Ananda, 2008).
Kandungan Bit Merah
Umbi bit mengandung 250 mg senyawa NO3- setiap 100 g umbi bit
merah, dimana senyawa NO3- akan dipecah di dalam tubuh menjadi bentuk NO2-,
Tabel 1. Komposisi gizi pada bit merah per 100 g bahan
Karbohidrat (g) 9,96
Serat pangan (g) 2,00
Gula (g) 7,96
Kalsium (mg) 16,00
Besi (mg) 0,79
Magnesium (mg) 23,00
Fosfor (mg) 38,00
Asam Pantotenat (mg) 0,15
Vitamin B-6 (mg) 0,07
Mutu Minuman Beralkohol
Mutu minuman beralkohol umumnya bergantung pada proses fermentasi itu sendiri. Kondisi fermentasi yang higenis serta kondisi substrat yang sesuai akan memudahkan dalam menerapkan standar mutu minuman beralkohol. Minuman beralkohol (wine, bir, spirits) apabila dikonsumsi dengan kadar yang rendah atau sedang akan menurunkan penyakit kardiovaskular. Namun sebaliknya, konsumsi yang berlebihan akan memberikan efek yang buruk pada sistem kardiovaskular. Selain itu, konsumsi minuman beralkohol yang tinggi menunjukkan buruknya pola diet pada masyarakat (Bernard, dkk., 2012).
Berdasarkan SNI 01-4019-1996, mutu minuman beralkohol dari buah dapat dilihat pada Tabel 2 berikut:
Tabel 2. Syarat minuman beralkohol dari buah
No Kriteria Uji Satuan Persyaratan
1 keadaan: - bau & rasa normal/khas
2 Etil alkohol % v/v 5-15
3 Metil alkohol % v/v alkohol maks 0,1
4 Asam mudah menguap
(dihitung sebagai asam asetat) g/100ml maksimal 0,2 5 Bahan tambahan makanan
- Zat warna negatif
- Pengawet (SO2) negatif
- Pemanis Buatan negatif
6 Cemaran logam
8 Cemaran Mikroorganisme
- angka lempeng total koloni/ml maks 2,0x102
- Coliform APM/ml maks 20
- E. Coli APM/ml <3
- Staphylococcus aureus koloni/ml 0
- kapang koloni/ml maks 50
- khamir koloni/ml maks 50
Fermentasi Karbohidrat
Umumnya mikroorganisme Saccharomyces dapat hidup dalam lingkungan dengan kadar oksigen cukup ataupun pada lingkungan dengan kadar oksigen yang rendah. Mikroorganisme jenis ini sering disebut aerob fakultatif, dimana pada kondisi lingkungan dengan kadar oksigen yang tinggi akan menggunakan oksigen untuk respirasi. Namun, pada kondisi lingkungan dengankadar oksigen yang rendah mikroba ini akan melakukan perombakan karbohidrat menjadi alkohol. Tahap awal fermentasi yaitu glikolisis yang akan menghasilkan asam piruvat, kemudian diikuti dengan proses perombakan asam piruvat menjadi asam asetat dan CO2 serta diubah menjadi alkohol pada tahap
akhir (Isnan Mulia, 2009).
Proses fermentasi dilakukan dengan melibatkan mikroba untuk memperoleh produk pangan yang diinginkan. Jenis mikroba yang digunakan adalah bakteri, khamir, dan kapang. Mikroba yang banyak digunakan dalam proses fermentasi alkohol adalah Saccharomycescereviseae. Fermentasi dapat dilakukan dengan menggunakan kultur alami maupun dengan kultur tunggal ataupun campuran. Salah satu fermentasi dengan menggunakan kultur alami adalah fermentasi tradisional dimana mikroba yang digunakan berasal dari alam (Hidayat, 2007).
Suhu yang baik untuk proses fermentasi yaitu sekitar 25 oC - 30 oC. Sel khamir yang digunakan untuk fermentasi alkohol dari pati dan gula adalah
Saccharomycescereviseae, sedangkan derajat keasaman yang cocok untuk proses
metabolisme mikroba tergantung karakteristik mikroba yang digunakan. Untuk mikroba Saccharomycescereviseaedan beberapa golongan khamir lainnya melalui tahap EMP (Embden Meyernof Parnas) (Rizani, 2000).
Kemampuan ragidalam merombak karbohidrat menjadi alkohol berbeda-beda. Ragi belum tentu hanya menggunakan satu jenis khamir dengan sifat khamir tidak sama pula sehingga proses fermentasi terkadang sulit dikontrol. Pada kondisi tertentu, waktu fermentasi yang dibutuhkan cukup lama karena kondisi yang tidak sesuai untuk memproduksi alkohol,sehingga pemilihan ragi dalam proses fermentasi sangat penting. Selain itu, proses persiapan juga merupakan faktor yang berpengaruh dimanaproses persiapan meliputi sterilisasi media pertumbuhan ragi yang sering terkontaminasi selama proses persiapan maupun proses fermentasi (Briggs, dkk., 1981).
Proses fermentasi dapat terjadi melalui reaksi yang berbeda-beda karena perbedaan kandungan karbohidrat atau gula yang terdapat pada bahan yang difermentasi. Gula yang paling sederhana akan dirombak paling cepat dengan proses perombakan menjadi etanol (2C2H5OH). Persamaan reaksinya secara
umum adalah:
C6H12O6 2C2H5OH + 2CO2 + 2 ATP (energi yang dilepas: 118 kj per
mol) (Nurdiyastuti, 2008).
Hasil proses fermentasi dengan substrat karbohidrat (gula, pati, selulosa) adalah etanol. Etanol merupakan nama IUPAC dari etil alkohol, alkohol ini merupakan cairan yang tidak berwarna serta memiliki aroma yang khas. Etanol mudah menguap dengan berat jenis pada suhu 15oC adalah 0,7937 g/ml serta titik didihnya 78,32oC pada tekanan 76 mmHg. Alkohol ini juga larut dalam air dan eter dan panas pembakaran sekitar 328 Kkal (Judoamidjojo, dkk, 1992).
Khamir-khamir yang mampu melakukan proses fermentasi aerob umumnya memiliki keterbatasan kapasitas respirasi. Ketika kadar glukosa dalam keadaan tinggi, glikolisis akan berjalan cepat sehingga menghasilkan piruvat dalam jumlah yang tinggi. Namun, akibat terbatasnya kapasitas respirasi khamir tersebut untuk menggunakan piruvat, maka piruvat yang tersisa akan diubah menjadi etanol. Sebaliknya, khamir anaerob memiliki kapasitas respirasi yang tidak terbatas sehingga mampu memanfaatkan piruvat yang dihasilkan melalui proses glikolisis (Prentis, 1990).
Penambahan Gula
Menurut Departemen Perindustrian (1975), pada proses fermentasi untuk menghasilkan alkohol biasanya ditambahkan gula. Namun pada umumnya proses fermentasi dapat berlangsung tanpa penambahan gula. Tujuan penambahan gula sebenarnya adalah untuk menambah kadar alkohol yang dihasilkan pada akhir proses fermentasi.
adalah 28% dan konsentrasi pada awal proses fermentasi yaitu 16%, Hal ini bertujuan untuk mempercepat proses fermentasi. Kadar gula minimum untuk pertumbuhan khamir adalah 10%.
Sumber Mikroba
Mikroba yang digunakan untuk proses fermentasi (S. Cereviseae) merupakan khamir sejati tergolong eukariot yang secara morfologi hanya membentuk blastospora berbentuk bulat lonjong silidris, oval atau bulat telur yang dipengaruhi oleh strainnya dan dapat berkembang biak dengan membelah diri atau pertunasan. Pertumbuhan mikroba ini dipengaruhi oleh lingkungan dan nutrisi yang tersedia bagi pertumbuhan selnya. Penampilan makroskopik mempunyai koloni berbentuk bulat, warna kuning muda, permukaan berkilau, licin, tekstur lunak dan memiliki sel bulat dengan askospora 1-8 buah (Nikon, 2004).
Taksonomi khamir Saccharomyces cereviseae adalah sebagai berikut : Class : Ascomycetes
Sub Class : Hemiascomycetidae Ordo : Endomycetales Famili : Saccharomycoideae Genus : Saccharomyces
Spesies : Saccharomyces cereviseae (Palczar, dkk, 1983).
Tabel 3. Komposisi sel khamir Saccharomyces cereviseae
Faktor yang Mempengaruhi Fermentasi
a. Spesies Sel Khamir
Pemilihan mikroba yang digunakan umumnya didasarkan pada jenis karbohidrat yang digunakan sebagai substrat, contohnya untuk menghasilkan alkohol dari pati dan gula digunakan mikroba Saccharomycescereviseae sedangkan laktosa dari whey menggunakan Candida pseudotropicalis. Pemilihan tersebut bertujuan untuk mendapatkan mikroba yang dapat tumbuh optimal dalam konsentrasi bahan yang tinggi, dan dapat menghasilkan alkohol yang tinggi (Mangunwidjaja dan Suryani, 1994).
b. Suhu
Khamir memiliki suhu toleransi untuk pertumbuhan sel yang optimum yaitu sekitar 25 – 30oC namun khamir dapat tumbuh secara efisien pada suhu 28-35oC. Peningkatan suhu sampai suhu 40oC dapat meningkatkan produksi awal alkohol, namun proses fermentasi akan menurun karena pertumbuhan sel khamir akan menurun yang diakibatkan kadar alkohol yang tinggi (Dwidjoseputro, 1978).
c. Jumlah sel khamir
d. Oksigen
Selama proses fermentasi berlangsung, khamir membutuhkan oksigen dalam jumlah yang kecil sekitar 0,05-0,1 mmHg, oksigen diperlukan khamir untuk proses pertumbuhan selnya pada tahap awal fermentasi. Namun kadar oksigen berbanding terbalik dengan kadar etanol yang dihasilkan, hal ini sesuai dengan International Commission of Microbiologial Specifications for Foods (1980) yang menyatakan bahwa persediaan oksigen yang tinggi penting untuk pertumbuhan awal mikroba namun produksi alkohol terbaik pada kondisi anaerob.
Jenis-jenis Alkohol dan Reaksi Alkohol
Tahapan perubahan pati menjadi alkohol pada proses fermentasi adalah sebagai berikut:
1. Hidratasi pati : merupakan proses pengurangan ukuran umbi dan penambahan air untuk memudahkan pati keluar.
2. Gelatinisasi pati : tergantung dari karakteristik pati yang terdapat pada bahan, suhu, waktu, ukuran partikel.
3. Hidrolisis pati : konversi pati menjadi maltosa dan dekstrin yang tidak terfermentasi, melalui proses hidrolisis enzimatis. Pati yang terdiri dari amilosa dan amilopektin, dimana amilosa dapat dihidrolisis menjadi maltosa sedangkan amilopektin akan terhidrolisis sebagian saja.
5. Proses pembuatan alkohol dapat dilakukan dengan proses fermentasi, sedangkan untuk proses pemurnian atau pemisahan alkohol dilakukan melalui proses destilasi. Menurut Hamidah (2003), proses pembuatan alkohol dari proses fermentasi dapat dilakukan dengan menggunakan tiga jenis karbohidrat yaitu:
1. Bahan-bahan yang mengandung gula 2. Bahan yang mengandung pati 3. Bahan yang mengandung selulosa
Adapun sifat fisik etanol dapat dilihat pada Tabel 4 berikut: Tabel 4. Sifat fisik etanol
Sifat fisik Nilai
Massa molekul relatif 46,07 g/mol
Titik beku -114,1oC
Titik didih normal 78,32oC
Densitas pada suhu 20oC 0,7893 g/ml
Kelarutan dalam air suhu 20oC sangat larut
Viskositas pada suhu 20oC 1,17 cP
Kalor spesifik, 20oC 0,579 kal/g oC
Kalor pembakaran, 25 oC 7092,1 kal/g
Kalor penguapan 78,32oC 200,6 kal/g
Sumber: Rizani (2000).
Starter Fermentasi
Menurut Frazier dan Westhoff (1979), inokulum ataupun kultur mikroba
Penelitian Sebelumnya
Penelitian sebelumnya dari Maurice (2011), derajat keasaman atau pH
yang cocok untuk menghasilkan alkohol paling tinggi adalah 4,5. Konsentrasi starter sebanyak 3 g/l menunjukkan kadar etanol dan waktu fermentasi yang efisien dan suhu maksimum fermentasi adalah 35oC. Konsentrasi glukosa juga merupakan faktor yang penting, dimana konsentrasi glukosa 40 g/l menunjukkan hasil etanol yang maksimum dengan waktu sekitar 20 jam dibandingkan dengan konsentrasi glukosa 100 g/l.
Latar Belakang
Variasi pengolahan minuman di Indonesia dengan menggunakan mikroba masih rendah. Padahal jenis tanaman yang dapat dimanfaatkan untuk membuat minuman sangat banyak dijumpai di Indonesia.Minuman hasil fermentasi merupakan minuman yang telah lama dikenal oleh masyarakat luas sebagai minuman hasil olahan dengan memanfaatkan peran bakteri atau khamir.Minuman hasil fermentasi diproduksi dengan tujuan untuk membentuk cita rasa, pengawetan, dan untuk menghasilkan nutrisi tertentu. Minuman hasil fermentasi ini bisa dijumpai dalam berbagai rasa dan kondisi yang berbeda-beda tergantung jenis mikroba yang digunakan, misalnya bakteri asam laktat akan menghasilkan rasa asam pada produk olahan. Pengolahan minuman yang mengandung alkohol menggunakan jenis khamir tertentu dan bahan pangan yang akan diolah biasanya mengandung kadar gula atau karbohidrat yang relatif tinggi.
memabukkan. Untuk mencegah kadar alkohol yang berlebihan di dalam darah maka dibutuhkan kombinasi yang tepat antara konsentrasi alkohol dalam minuman dan daya tampung cairan dalam tubuh, sehingga diharapkan kadar alkohol yang rendah akan mencegah kelebihan alkohol dalam darah. Untuk itu diperlukan bahan dengan kandungan gula dan lama fermentasi yang tepat.
Kandungan gula sebagai substrat sangat berpengaruh terhadap pertumbuhan khamir pada proses fermentasi. Kadar gula yang terlalu tinggi akan menghasilkan kadar alkohol yang terlalu tinggi sehingga menghambat pertumbuhan khamir dan akan meninggalkan residu gula yang belum terfermentasi.
karbohidrat sebagai bahan bahan baku fermetasi serta kandungan nutrisi yang relatif tinggi sehingga cocok digunakan sebagai bahan pembuat minuman ferbeet. Berdasarkan penjelasan tersebut, maka penulis tertarik untuk melakukan penelitian tentang “Pengaruh Penambahan Gula Pasir dan Lama Fermentasi Terhadap Mutu Minuman Ferbeet”.
Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui pengaruh penambahan gula pasir dan lama proses fermentasi terhadap kadar alkohol dan mutu minuman
Ferbeet (Fermented betroot).
Kegunaan Penelitian
Penelitian ini berguna untuk mendapatkan data yang tepat dalam penyusunan skripsi sebagai salah satu syarat untuk mendapatkan gelar sarjana Teknologi Pangan di program studi Ilmu dan Teknologi Pangan, Fakultas Pertanian, Universitas Sumatera Utara, Medan. Sebagai sumber informasi mengenai pengaruh gula terhadap minuman hasil fermentasi.
Hipotesis Penelitian
MICHAEL SIMANJUNTAK: Pengaruh Penambahan Gula Pasir dan Lama Fermentasi Terhadap Mutu Minuman Ferbeet (Fermented Beetroot). Dibimbing oleh TERIP KARO-KARO dan SENTOSA GINTING.
Penelitian ini bertujuan untuk mengetahui pengaruh penambahan gula pasir dan lama fermentasi terhadap mutu minuman Ferbeet. Penelitian ini menggunakan rancangan acak lengkap (RAL) dengan dua faktor: yaitu lama fermentasi (L): (2 hari, 4 hari, 6 hari, dan 8 hari) dan konsentrasi gula pasir (P): (10%, 15%, 20%, dan 25%). Parameter yang diamati adalah total padatan terlarut (TSS), pH, kadar alkohol, uji organoleptik warna, uji organoleptik aroma dan rasa.
Hasil penelitian menunjukkan bahwa penambahan gula pasir memberikan pengaruh berbeda sangat nyata terhadap total padatan terlarut dan kadar alkohol, berbeda nyata terhadap nilai uji organoleptik rasa, berbeda tidak nyata terhadap pH, nilai uji organoleptik warna dan aroma. Lama fermentasi memberikan pengaruh berbeda sangat nyata terhadap total padatan terlarut, pH, kadar alkohol, nilai uji organoleptik aroma dan rasa, dan berbeda tidak nyata terhadap nilai uji organoleptik warna. Interaksi penambahan gula pasir dan lama fermentasi memberikan pengaruh berbeda nyata terhadap total padatan terlarut dan kadar alkohol, berbeda tidak nyata terhadap pH dan nilai organoleptik warna, aroma, dan rasa.
Kata kunci: penambahan gula pasir, lama fermentasi, minuman Ferbeet
ABSTRACT
MICHAEL SIMANJUNTAK: The Effect of The Addition of Sugar and Fermentation
Time on The Quality of Ferbeet Beverage (fermented betroot). Supervised by TERIPKARO KARO and SENTOSA GINTING.
This research was aim to determine the effect of the addition of sugar and fermentation time on the quality of the Ferbeet beverage. This study used a completely randomized design (CRD) with two factors: fermentation time (L): (2 days, 4 days, 6 days, and 8 days) and sugar concentration (P): (10%, 15%, 20 %, and 25%). Parameters measured were total soluble solid (TSS), pH, alcohol content, organoleptic of color, flavor and taste.
The results showed that the addition of sugar had highly significant effect on total soluble solids and alcohol concentration, had significant effect from organoleptic taste, had no significant effect on pH, color and aroma. The fermentation time had highly significant effect on total soluble solids, pH, alcohol content, the value of organoleptic aroma and flavor, and had no significant effect on color. Interaction of sugar addition and fermentation time had significant effect on total dissolved solids and alcohol concentration, had no significant effect on pH and organoleptic of color, aroma, and taste.
FERBEET (Fermented Beetroot)
SKRIPSI
Oleh :
MICHAEL SIMANJUNTAK
110305026/ILMU DAN TEKNOLOGI PANGAN
PROGRAM STUDI ILMU DAN TEKNOLOGI PANGAN
FAKULTAS PERTANIAN
FERBEET (Fermented Beetroot)
SKRIPSI
Oleh :
MICHAEL SIMANJUNTAK
110305026/ILMU DAN TEKNOLOGI PANGAN
Skripsi sebagai salah satu syarat untuk memperoleh Gelar sarjana di Fakultas Pertanian
Universitas Sumatera Utara
PROGRAM STUDI ILMU DAN TEKNOLOGI PANGAN
FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA
MEDAN
Nama : Michael Simanjuntak
NIM : 110305026
Program Studi : Ilmu dan Teknologi Pangan
Disetujui oleh: Komisi Pembimbing
Ir. Terip Karo-Karo M.S
Ketua Anggota
Ir. Sentosa Ginting, MP
Mengetahui :
MICHAEL SIMANJUNTAK: Pengaruh Penambahan Gula Pasir dan Lama Fermentasi Terhadap Mutu Minuman Ferbeet (Fermented Beetroot). Dibimbing oleh TERIP KARO-KARO dan SENTOSA GINTING.
Penelitian ini bertujuan untuk mengetahui pengaruh penambahan gula pasir dan lama fermentasi terhadap mutu minuman Ferbeet. Penelitian ini menggunakan rancangan acak lengkap (RAL) dengan dua faktor: yaitu lama fermentasi (L): (2 hari, 4 hari, 6 hari, dan 8 hari) dan konsentrasi gula pasir (P): (10%, 15%, 20%, dan 25%). Parameter yang diamati adalah total padatan terlarut (TSS), pH, kadar alkohol, uji organoleptik warna, uji organoleptik aroma dan rasa.
Hasil penelitian menunjukkan bahwa penambahan gula pasir memberikan pengaruh berbeda sangat nyata terhadap total padatan terlarut dan kadar alkohol, berbeda nyata terhadap nilai uji organoleptik rasa, berbeda tidak nyata terhadap pH, nilai uji organoleptik warna dan aroma. Lama fermentasi memberikan pengaruh berbeda sangat nyata terhadap total padatan terlarut, pH, kadar alkohol, nilai uji organoleptik aroma dan rasa, dan berbeda tidak nyata terhadap nilai uji organoleptik warna. Interaksi penambahan gula pasir dan lama fermentasi memberikan pengaruh berbeda nyata terhadap total padatan terlarut dan kadar alkohol, berbeda tidak nyata terhadap pH dan nilai organoleptik warna, aroma, dan rasa.
Kata kunci: penambahan gula pasir, lama fermentasi, minuman Ferbeet
ABSTRACT
MICHAEL SIMANJUNTAK: The Effect of The Addition of Sugar and Fermentation
Time on The Quality of Ferbeet Beverage (fermented betroot). Supervised by TERIPKARO KARO and SENTOSA GINTING.
This research was aim to determine the effect of the addition of sugar and fermentation time on the quality of the Ferbeet beverage. This study used a completely randomized design (CRD) with two factors: fermentation time (L): (2 days, 4 days, 6 days, and 8 days) and sugar concentration (P): (10%, 15%, 20 %, and 25%). Parameters measured were total soluble solid (TSS), pH, alcohol content, organoleptic of color, flavor and taste.
The results showed that the addition of sugar had highly significant effect on total soluble solids and alcohol concentration, had significant effect from organoleptic taste, had no significant effect on pH, color and aroma. The fermentation time had highly significant effect on total soluble solids, pH, alcohol content, the value of organoleptic aroma and flavor, and had no significant effect on color. Interaction of sugar addition and fermentation time had significant effect on total dissolved solids and alcohol concentration, had no significant effect on pH and organoleptic of color, aroma, and taste.
MICHAEL SIMANJUNTAK, dilahirkan di Lumban Pea, Sumatera
Utara pada tanggal 25 juli 1993. Anak ketiga dari 6 bersaudara dari ayahanda Polman Simanjuntak dan Ibunda Nesma Nababan.
Lulus dari SD N1 Lumbanrang Kecamatan Lumbanjulu pada tahun 2005, pada tahun 2008 lulus dari SLTP N1 Lumbanjulu dan pada tahun 2011 lulus dari SMA N1 Lumbanjulu. Kemudian pada tahun 2011, penulis diterima di program studi Ilmu dan Teknologi Pangan Fakultas pertanian Universitas Sumatera Utara melalui jalur SNMPTN.
Selama perkuliahan, penulis juga mengikuti dan berpartisipasi dalam kegiatan organisasi IMITP (Ikatan Mahasiswa Ilmu dan Teknologi Pangan).
Segala puji, hormat dan juga syukur penulis ucapkan kepada Tuhan Yang Maha Kuasa atas berkat dan kasihnya yang melimpah sehingga penulis dapat menyelesaikan skripsi ini yang berjudul “Pengaruh Penambahan Gula Pasir dan Lama Fermentasi Terhadap Mutu Minuman Ferbeet (Fermented Beetroot)”
Pada kesempatan ini penulis juga menyampaikan terima kasih yang sebesar – besarnya kepada kedua orang tua penulis yang telah membesarkan, memberi nasehat, serta mendidik penulis. Penulis juga menyampaikan terima kasih kepada Ir. Terip Karo-Karo, MS dan Ir. Sentosa Ginting, MP selaku ketua dan anggota komisi pembimbing yang telah membimbing serta memberi saran serta ilmu kepada penulis.
Penulis juga menyampaikan terima kasih kepada staf pengajar dan pegawai di program studi Ilmu Teknologi Pangan Fakultas Pertanian, kepada teman-teman dan adik satu program studi, dan juga semua yang telah membantu dalam menyelesaikan skripsi ini.
Akhir kata semoga skripsi ini bermanfaat bagi semua pihak yang membutuhkan.
Medan, Juni 2016
Hal
Kegunaan Penelitian... 3
Hipotesis Penelitian ... 3
Fermentasi Karbohidrat ... 9
Penambahan Gula ... 11
Sumber Mikroba ... 12
Faktor yang Mempengaruhi Fermentasi ... 13
Jenis-jenis Alkohol dan Reaksi Alkohol... 14
Starter Fermentasi ... 15
Penelitian Sebelumnya... 16
BAHAN DAN METODE ... 17
Tempat dan Waktu Penelitian ... 17
Bahan Penelitian... 17
Bahan Kimia... 17
Alat Penelitian ... 17
Metode Penelitian... 17
Penentuan total padatan terlarut ... 20
Penentuan pH ... 20
Penentuan kadar alkohol ... 21
Penentuan nilai uji organoleptik warna ... 21
Penentuan nilai uji organoleptik aroma ... 22
Penentuan nilai uji organoleptik rasa ... ... 22
HASIL DAN PEMBAHASAN ... 26
Pengaruh Penambahan Gula Pasir Terhadap Parameter yang Diamati ... 26
Pengaruh Lama Fermentasi Terhadap Parameter yang Diamati ... 27
Total Padatan Terlarut ………29
Pengaruh penambahan gula pasir terhadap total padatan terlarut ... 29
Pengaruh lama fermentasi terhadap total padatan terlarut ... 30
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap total padatan terlarut ... 32
Penentuan Nilai pH ………34
Pengaruh penambahan gula pasir terhadap pH ... 34
Pengaruh lama fermentasi terhadap pH ... 34
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap pH ... 36
Kadar Alkohol ………36
Pengaruh penambahan gula pasir terhadap kadar alkohol ... 36
Pengaruh lama fermentasi terhadap kadar alkohol ... 38
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap kadar alkohol ... 39
Uji Organoleptik Warna ………...41
Pengaruh penambahan gula pasir terhadap uji organoleptik warna ... 41
Pengaruh lama fermentasi terhadap uji organoleptik warna ... 41
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap uji organoleptik warna ... 42
Uji Organoleptik Aroma ………42
Pengaruh penambahan gula pasir terhadap uji organoleptik roma ... 42
Pengaruh lama fermentasi terhadap uji organoleptik aroma ... 44
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap nilai uji organoleptik aroma ... 44
Uji Organoleptik Rasa ……….44
Pengaruh penambahan gula pasir terhadap uji organoleptik rasa ... 44
Pengaruh lama fermentasi terhadap uji organoleptik rasa... 45
Pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap uji organoleptik rasa ... 47
KESIMPULAN DAN SARAN ... 48
Kesimpulan ... 48
Saran ... 49
No Hal
1. Komposisi gizi pada bit merah per 100 g bahan... 7
2. Syarat minuman beralkohol dari buah ... 8
3. Komposisi sel khamir Saccharomyces cerevisiae ... 12
4. Sifat fisik etanol ... 15
5. Skala nilai skor warna ... 22
6. Skala nilai hedonik aroma ... 22
7. Skala nilai hedonik rasa ... 23
8. Pengaruh penambahan gula pasir terhadap parameter yang diamati ... 26
9. Pengaruh lama fermentasi terhadap parameter yang diamati ... 28
10. Uji LSR pengaruh lama fermentasi terhadap total padatan terlarut... ... 29
11. Uji LSR pengaruh penambahan gula pasir terhadap total padatan terlarut ... 31
12. Uji LSR pengaruh interaksi penambahan gula pasir dan lama fermentasi terhadap total padatan terlarut ... 33
13. Uji LSR pengaruh lama fermentasi terhadap pH minuman ferbeet ... 35
14. Uji LSR pengaruh penambahan gula pasir terhadap kadar alkohol ... 36
15. Uji LSR pengaruh lama fermentasi terhadap kadar alkohol ... 38
16. Uji LSR pengaruh interaksi penambahan gula dan lama fermentasi terhadap kadar alkohol minuman ferbeet ... 40
No Hal
1. Struktur kimia senyawa betalain ... 6
2. Skema pembuatan starter ... 24
3. Skema pembuatan minuman beralkohol ferbeet dari bit merah ... 25
4. Hubungan penambahan gula pasir dengan total padatan terlarut... 30
5. Hubungan lama fermentasi dengan total padatan terlarut ... 32
6. Hubungan interaksi lama fermentasi dan penambahan gula pasir dengan total padatan terlarut... ... 33
7. Hubungan lama fermentasi dengan pH ... 35
8. Hubungan penambahan gula pasir dengan kadar alkohol …………... 37
9. Hubungan lama fermentasi dengan kadar alkohol minuman ferbeet ….. 38
10. Hubungan interaksi lama fermentasi dan penambahan gula dengan kadar alkohol minuman ferbeet ……… 40
11. Hubungan lama fermentasi dengan nilai uji organoleptik aroma …....… 43
12. Hubungan penambahan gula pasir dengan nilai organoleptik rasa ... 45
No Hal
1.Tabel specific gravities 20o/20oC of alcohol-water mixtures ... 54
2.Data pengamatan total padatan terlarut... 60
3.Data pengamatan pH ... 61
4.Data pengamatan kadar alkohol ... 62
5.Data pengamatan organoleptik warna ... 63
6.Data pengamatan organoleptik aroma ... 64
7.Data pengamatan organoleptik rasa ... 65