STUDI PROSES MEKANISME PENGADUKAN DENGAN
METODE STATIC -MIXER UNTUK MENINGKATKAN
EFISIENSI TRANSESTERIFIKASI MINYAK SAWIT MENJADI
BIODIESEL
RIZAL ALAMSYAH
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN
PERNYATAAN MENGENAI DISERTASI DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa disertasi
“Studi Proses Mekanisme
Pengadukan Dengan Metode Static-Mixer Untuk Meningkatkan Efisiensi
Transesterifikasi Minyak Sawit Menjadi Biodiesel”
adalah karya saya dengan
arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada
Perguruan Tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya
yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam
teks dan dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
ABSTRACT
RIZAL ALAMSYAH.
Study on Mixing Process Using Static-mixer Method to
Increase Transesterification Efficiency of Refined Palm Oil into Biodiesel.
SUPERVISORS: ARMANSYAH H. TAMBUNAN, Y. ARIS PURWANTO, and
DADAN KUSDIANA
One of the difficulties faced in the current technology for biodiesel production
is the requirement for rigorous mixing of methanol with the feedstock oil in the
reactor. Utilization of blade mixer has limitation due to the immiscible state of those
substances. This research was devoted to assess of static-mixer utilization in a
transesterification reactor for biodiesel production in terms of kinetics reaction
(reaction rate coefficient k, activation energy Ea, and collision factor or coefficient
factor A).
The experiments were conducted by reacting refined bleached deodorized palm
olein (triglyceride or TG) with methanol (MeOH) at 50, 55, 60, 65, and 70
oC, using
potassium hydroxide (KOH) as a catalyst at atmospheric pressure. Molar ratio of TG
and MeOH was 1 : 11.5 and KOH used was 1% of palm oil weight.
Transesterification process using blade agitator with the same reaction condition was
performed as base of comparison to those of static-mixer. Energy consumption was
measured for heater during oil heating, transesterification, boiling water and biodiesel
drying by kWh meter. It was also conducted for pump for distribution, reactant
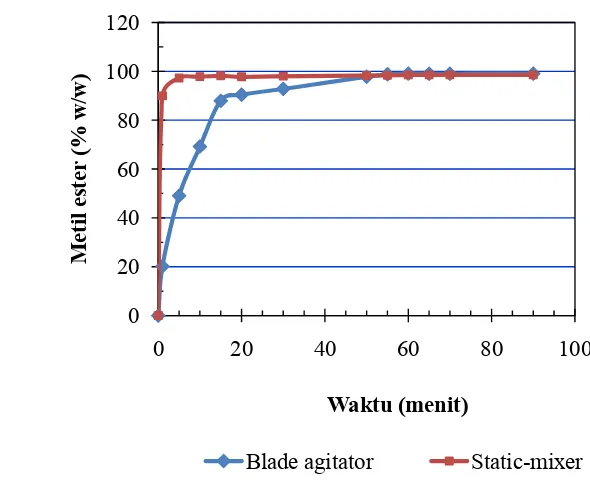
mixing, and impeller of blade agitator. The experiments showed that static-mixer has
significant effect in reducing reaction time to reach required fatty acid methyl ester
content (FAME) i.e. 96.5% than those of blade agitator. Transesterification reaction
time with static-mixer were shorter than with blade agitator for all temperature levels.
Reaction temperature of 65
oC with 5 minutes of reaction time demonstrated the best
condition for running the static-mixer reactor.
The kinetics satudy was conducted based on the decrease of bounded glicerol
or
unmethyl esterified compound
(uME) which consists of triglyceride TG,
digliceryde DG, and monoglyceride MG during transesterification reaction. Since the
bounded glycerol decreased rapidly in the first stage reaction so the reation rate was
evaluated into two stages reaction of transesterification that gived the initial and the
final reaction rate coefficient (k
1and k
2), the initial and final activation energy (Ea
1and Ea
2) and the initial and final collision factor (A
1and A
2). The value of Ea
1, Ea
2,
A
1, and A
2for static-mixer experiments were 1.33 J/mol, 16.71 J/mol, 6.48, minute
-1and 8.89 minute
-1,
respectively.
static-mixer improved the energy ratio of blade agitator. The static-mixer experiment
at reaction temperature 65
oC demonstrated the lowest energy consumption (Q
in) e.g
1804.35 kJ/kg, meanwhile Q
infor 50, 55, 60 and 70
oC were 1810.45 kJ/kg, 1807.77
kJ/kg, 1801.79 kJ/kg, and 1838.66 kJ/kg respectively. Based on the heat transfer
analysis, the overall heat transfer from the reactor wall was 260.62 kJ, meanwhile the
highest of heat transfer was released from pipe for circulating the reactants.
RINGKASAN
RIZAL ALAMSYAH.
Studi Proses Mekanisme Pengadukan Dengan Metode
Static -Mixer Untuk Meningkatkan Efisiensi Transesterifikasi Minyak Sawit
Menjadi Biodiesel.
Dibimbing oleh ARMANSYAH H. TAMBUNAN, Y. ARIS
PURWANTO, dan DADAN KUSDIANA
Biodiesel merupakan monoalkil ester (misal:
fatty acid methyl ester
atau
FAME) yang diproses dengan metode transesterifikasi antara trigliserida yang berasal
dari minyak nabati atau lemak hewani dengan alkohol rantai pendek terutama
metanol untuk digunakan sebagai bahan bakar mesin diesel. Proses esterifikasi atau
transesterifikasi dapat dilangsungkan dengan menggunakan katalis atau tanpa katalis.
Sejauh ini dalam produksi biodiesel umumnya dilakukan dengan proses
transesterifikasi menggunakan katalis basa. Kekurangan dari proses katalis basa
adalah: 1) terdapat dua fase campuran minyak nabati-metanol (MeOH) yang
memerlukan mekanisme pengadukan yang kuat agar proses transesterifikasi bisa
efektif dan reaksi mengarah ke sebelah kanan, 2) dalam purifikasi biodiesel kasar
(crude biodiesel)
diperlukan proses yang panjang karena di dalam produk masih
terkandung
impurities
yang terdiri dari residu katalis, metanol yang tidak bereaksi,
dan sabun yang harus dipisahkan. Waktu reaksi transesterifikasi dengan sistem
pengadukan ini berkisar antara 60 – 90 menit.
Tujuan penelitian yang dilakukan adalah untuk: 1) menentukan kinetika reaksi
transesterifikasi (laju reaksi, konstanta laju reaksi k, energi aktivasi Ea, dan frekuensi
tumbukan A) menggunakan reaktor
static-mixer
pada beberapa tingkat suhu yaitu 50,
55, 60, 65, dan 70
oC pada tekanan atmosfir. Sebagai pembanding proses
transesterifikasi dengan menggunakan
blade agitator
dilakukan pada tingkat suhu
yang sama, dan 2) mengkaji kebutuhan energi transesterifikasi, kebutuhan energi
pemanasan awal, purifikasi (pencucian dan pengeringan) dan rasio energi biodiesel
dari minyak curah sawit
(refined bleached deodorized palm olein
- RBDPO
).
Pembuatan biodiesel dilakukan dengan proses transesterifikasi RBDPO
dengan metanol (MeOH) menggunakan reaktor
static-mixer
. Rasio molar antara
RBDPO dan MeOH adalah 1 : 11,5. Jumlah KOH yang digunakan sebanyak 1% dari
RBDPO. Proses pembuatan biodiesel adalah diawali dengan pemanasan awal
RBDPO dalam reaktor sesuai suhu yang ditentukan (50, 55, 60, 65, dan 70
oC) dan
pada saat yang sama juga MeOH dipanaskan. Saat suhu yang diinginkan tercapai,
campuran MeOH-KOH dimasukkan ke dalam reaktor, kemudian pengadukan dimulai
dengan menghidupkan pompa
static-mixer
sehingga campuran melewati
static-mixer
.
Sampling
dilakukan pada biodiesel dengan mengambil contoh di keran bagian atas
pada selang waktu menit ke 1, 5, 10, 15, 20, 30, 40, 50, 55, 60, 65, 70, 80, dan 90
untuk dianalisis mutunya sesuai dengan Sandard SNI 04-7128-2006.
SNI 04-7128-2006 untuk biodiesel. Pengujian dilakukan untuk beberapa parameter
mutu utama antara lain untuk: gliserol bebas dan total gliserol dengan metoda uji
(AOCS: Ca 14-56), kandungan metil ester (biodiesel), angka asam (AOCS: Cd 3-63),
angka penyabunan (AOCS: Cd 3-25), viskositas, densitas, dan kadar air. Biodiesel
yang dihasilkan secara visual memiliki warna kuning jernih dan terlihat encer. Hasil
samping reaksi transesterifikasi adalah gliserol yang berwarna coklat gelap dan lebih
kental dibanding metil ester, yang berada pada lapisan bagian bawah.
Reaksi transesterifikasi menunjukkan bahwa laju reaksi metil ester
menggunakan
static-mixer
lebih cepat dibanding dengan
blade agitator
pada periode
awal proses. Hasil percobaan menunjukkan bahwa penggunaan
static-mixer
mempunyai pengaruh yang signifikan terhadap pengurangan waktu reaksi untuk
mencapai kandungan metil ester minimum yaitu 96,5% dibanding menggunakan
blade agitator
, untuk seluruh perlakuan suhu yang diberikan. Waktu reaksi
transesterifikasi dengan
static-mixer
lebih pendek dibanding dengan
blade agitator
unrtuk semua perlakuan suhu. Suhu reaksi 65
oC dan waktu reaksi 5 menit
memperlihatkan kondisi terbaik untuk mengoperasikan reactor
static-mixer
. Hasil
yang sama juga ditunjukkan dengan hasil penurunan, gliserol terikat (triglierida TG,
digliserida DG, dan monogliserida MG) yang tidak bereaksi, viskositas dan angka
asam dari biodiesel untuk penggunaan kedua metode pengadukan tersebut.
Perhitungan kinetika didasarkan atas penurunan jumlah gliserol terikat atau
unmethyl esterified compound
(uME) yang tidak bereaksi dan terdiri dari TG, DG,
dan MG). Karena penurunan jumlah gliserol terikat dengan
static-mixer
lebih cepat
pada tahap awal proses, maka laju reaksi dievaluasi ke dalam 2 tahap proses
transesterifikasi sehingga memberikan konstanta laju reaksi awal (k
1) dan laju raksi
akhir (k
2). Perubahan dari laju reaksi awal menuju laju reaksi akhir terlihat naik
turun, akan tetapi hasil masih menunjukkan kecenderungan penurunan. Perubahan
jumlah gliserol terikat dengan
blade agitator
menunjukkan penurunan yang stabil
sehingga laju reaksi dievaluasi dalam satu tahap reaksi transesterifikasi. Dari hasil
yang diperoleh laju reaksi awal (k
1) dengan
static-mixer
pada tahap awal lebih tinggi
dibandingkan dengan menggunakan
blade agitator
.
Waktu reaksi transesterifikasi dengan
static-mixer
lebih pendek dibanding
dengan blade agitator untuk semua perlakuan suhu. Suhu reaksi 65
oC dan waktu
reaksi 5 menit memperlihatkan kondisi terbaik untuk mengoperasikan reaktor
static-mixer. Energi aktifasi (Ea) dan frekuensi tumbukan (A) dihitung berdasarkan
persamaan Arhenius untuk tahap awal dan akhir reaksi untuk
static-mixer
, serta untuk
satu tahap pada
blade agitator.
Dengan
demikian muntuk static-mixer dihasilkan
energi aktivasi awal dan akhir (Ea
1and Ea
2) serta frekuensi tumbukan awal dan akhir
(A
1and A
2) yang masing-masing nilainya adalah : 1,33 J/mol, 16,71 J/mol, 6,48,
menit
-1dan 8,89 menit
-1. Nilai Ea dan A
untuk percobaan
blade agitator
adalah 10,49
J/mol, dan 2,9 menit
-1.
Kebutuhan energi rata-rata untuk produksi biodiesel (Q
in) menggunakan
static-mixer
© Hak Cipta milik
Institut Pertanian Bogor
, tahun 2010
Hak Cipta dilindungi Undang-undang
1.
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebut sumber
a.
Pengutipan hanya untuk kepentingan pendidikan, penelitian,
penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau
tinjauan suatu masalah
b.
Penulisan tidak merugikan kepentingan yang wajar IPB
2.
Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya
tulis dalam bentuk apapun tanpa izin IPB
STUDI PROSES PENGADUKAN DENGAN METODE STATIC
-MIXER UNTUK MENINGKATKAN EFISIENSI
TRANSESTERIFIKASI MINYAK SAWIT MENJADI
BIODIESEL
RIZAL ALAMSYAH
Disertasi
Sebagai salah satu syarat memperoleh gelar
Doktor pada
Program Studi Ilmu Keteknikan Pertanian
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN
Penguji pada Ujian Tertutup: Dr. Ir. Kohar Irwanto, MSi. Dr. Ir. Leopold E. Nelwan, MSi.
Judul Disertasi : STUDI PROSES PENGADUKAN DENGAN METODE STATIC -MIXER UNTUK MENINGKATKAN EFISIENSI TRANSESTERIFIKASI MINYAK SAWIT MENJADI BIODIESEL
Nama : Rizal Alamsyah
NIM : F 161060042
Disetujui Komisi Pembimbing
Prof. Dr. Ir. Armansyah H. Tambunan Ketua
Dr. Ir. Y. Aris Purwanto, MSc. Anggota
Dr. Ir. Dadan Kusdiana, MSc. Anggota
Diketahui
Ketua Program Studi Ilmu Keteknikan Pertanian
Dekan Sekolah Pascasarjana
Dr. Ir. Wawan Hermawan, MS. Prof. Dr. Ir. Khairil A. Notodiputro, MS.
KATA PENGANTAR
Puji syukur saya panjatkan ke hadirat Allah SWT, atas segala izin, ridha dan
karuniaNya sehingga disertasi berjudul
Studi Proses Mekanisme Pengadukan
Dengan Metode Static-Mixer Untuk Meningkatkan Efisiensi Transesterifikasi
Minyak Sawit Menjadi Biodiesel
dapat dirancang dan diselesaikan. Kegiatan
penelitian ini dilaksanakan mulai dari bulan Maret 2008 hingga September 2009.
Disertasi ini dibuat dalam rangka penelitian untuk penyelesaian studi program
Doktor (S3) di bidang Ilmu Keteknikan Pertanian pada Sekolah Pasca Sarjana Institut
Pertanian Bogor. Penelitian ini dirancang sedemikian rupa yang diharapkan dapat
memberikan kontribusi dalam khazanah teknologi energi terbarukan
(renewable
energy).
Dalam penyelesaian disertasi ini penulis banyak mendapatkan bimbingan,
arahan, serta koreksi konstruktif dari komisi pembimbing. Oleh karena itu ucapan
terima kasih disampaikan kepada Prof. Dr. Ir. Armansyah H. Tambunan (ketua), Dr.
Ir. Y. Aris Purwanto, M.Sc. (anggota) dan Dr. Ir. Dadan Kusdiana, MSc. (anggota).
Penulis juga menyampaikan terima kasih yang sebesar-besarnya kepada Dr. Ir. Kohar
Irwanto, MSi. dan Dr. Ir. Leopold E. Nelwan, MSi. selaku dosen penguji pada ujian
tertutup. Penulis juga menyampaikan terima kasih yang sebesar-besarnya kepada Dr.
Ir. Joelianingsih, MT. dan Dr. Ir. Desrial, M.Eng. selaku dosen penguji pada Ujian
Terbuka.
Ucapan terima kasih disampaikan pula kepada:
1.
Rektor IPB, Dekan Sekolah Pascasarjana IPB, Dekan Fakultas Teknologi
Pertanian IPB, Ketua Program Studi Ilmu Keteknikan Pertanian Sekolah Pasca
Sarjana IPB atas penerimaan yang diberikan kepada penulis untuk mengikuti
pendidikan program DOKTOR (S3) di IPB melalui jalur penelitian
(by research)
.
Tak lupa staf pengajar dan pegawai yang ada di lingkup Sekolah Pasaca Sarjana
IPB, atas segala ilmu pengetahuan dan pelayanan yang telah diberikan selama
menempuh pendidikan di IPB.
2.
Dr. Sony Solistia Wirawan (BPPT), Prof. Hiroshi Nabetani
(Food National
Research, Japan)
, Dr. Milan Martinov (CIGR), Dr. Zazueta Ranahan (CIGR), Ir.
Ari Rahmadi, MSc. dan Ir. Maharani (BPPT) atas masukan dan arahan teknis
penulisan karya ilmiah yang telah disusun,
3.
Prof. Dr. Kamaruddin Abdullah (Universitas Persada), Prof. Dr. Ir. Irawadi
Djamaran (TIN, IPB), dan Dr. Ir. Setyo Pertiwi, MSc. (TEP, IPB) atas arahan
teknisnya
4.
Ayahanda (H. Abdul Moeis Abdullah) dan Ibunda (Hj. Nelly Sadiah) atas
asuhan, didikan, perhatian, doa yang tulus, serta dorongan morilnya.
5.
Istri (Dra. Ariyanti) dan anak-anak penulis tercinta
(Arizia Tamara dan Amira
Mayariza Ghina) atas segala dorongan semangat motivasi dan yang telah
bersabar menanti selama pendidikan.
6.
Staf Laboratorium Energi dan Elektrifikasi Pertanian, Pak Harto, Firman, dan
Darma atas segala bantuan teknis.
7.
Bengkel Tanggerang (Kota Tanggerang) atas pembuatan dan pengujian awal
static-mixer
dan Ir. Asadi, MSi (UPN Jakarta) atas masukan teknis selama
konstruksi reaktor.
Supriatna, MSi., Ramlan Ruvendi, SE, MM., dan teman-teman di Bidang Sarana
Riset dan Standardisasi BBIA serta Ir. Wawan Kartiwa, MSi (BPK, Bandung)
yang sering memberikan dorongan moril selama studi.
9.
Saudara/i Ade Wahyuni SP, Atika SP, Retno STP, Ismail STP, dan Didin N, STP
atas bantuan teknis pengujian laboratorium, dan
10.
Rasa terimakasih juga disampaikan kepada sdr. Mulyawatulloh, Firman, Darma,
Rusmawati, dan Harto (TEP) atas kelancaran teknis dan administrasi penelitian.
Penulis menyadari tulisan ini masih mempunyai kekurangan, untuk itu saran,
masukan, maupun kritik yang konstruktif sangat diharapkan. Penulis turut berdoa
semoga Allah SWT memberikan limpahan rahmat dan karuniaNya kepada semuanya.
Akhir kata semoga dari disertasi ini dapat memberikan manfaat bagi yang
memerlukannya. Aaamiin ya rabbal a’lamin.
RIWAYAT HIDUP
Penulis dilahirkan di Bogor, Jawa Barat pada tanggal 10 Juli 1959 sebagai
anak keempat dari H. Abdul Muis Abdullah dan Hj. Nely Sadiah. Pada tanggal 10
Desember 1990 penulis menikah dengan Hj. Dra. Ariyanti dan dikaruniai dua anak
yaitu Arizia Tamara dan Amira Mayariza Ghina.
Penulis menyelesaikan pendidikan SD, SMP sampai SMA di Bogor
masing-masing tahun 1971, 1974 dan 1977. Pendidikan Sarjana (S1) ditempuh pada Jurusan
Mekanisasi Pertanian Fateta IPB dan diselesaikan pada tahun 1983. Selanjutnya
penulis mendapat kesempatan melanjutkan Pendidikan Pasca Sarjana (S2) di
School
Applied Science
jurusan
Food Engineering
,
The University of New South Wales
(UNSW)
, Sydney-Australia dan diselesaikan pada tahun 1990. Penulis juga pernah
mengikuti program pendidikan training for trainer di
Cornell University USA
dalam
bidang
Food Technology
pada tahun 1993 serta pernah mengikuti
Training Course on
Biomass Integrated Utilization Technologies,
di
China Agricultural Unive
r
sity
(CAU) Beijing China pada tahin 2008. Selanjutnya, sejak Agustus 2006 penulis
diterima sebagai mahasiswa S3 di Program Studi Ilmu Keteknikan Pertanian (TEP)
Sekolah Pasca Sarjana Institut Pertanian Bogor (IPB) melalui jalur penelitian
(by
research)
. Penulis bekerja sebagai peneliti sejak tahun 1986 hingga sekarang dan
menjabat sebagai Kepala Bidang Sarana Riset dan Standardisasi di Balai Besar
Industri Agro (BBIA) Kementerian Perindustrian, Bogor dari tahun 2009 hingga
sekarang.
Biodiesel Production Process from Palm Oil Olein by Utilizing Static-Mixer
Reactor”. Sebuah
review
berjudul “The Current Status Of Biodiesel Production
Technology:
A Review
, dipublikasikan pada Jurnal Keteknikan Pertanian. Vol. 21 No.
4 (Desember) Tahun. 2007.
Karya ilmiah berjudul “Rekayasa Mekanisme Pengadukan Dengan Metode
Static-mixer Untuk Meningkatkan Efisiensi Proses Transesterifikasi Minyak Nabati
Menjadi Biodiesel” dipresentasikan dan dipublikasikan pada Prosiding Seminar
Nasional Perteta, Yogyakarta 18 November 2008. Karya ilmiah tersebut juga
merupakan bagian dari hasil penelitian Disertasi S3 penulis.
Disertasi yang berjudul “Rekayasa Mekanisme Pengadukan Dengan Metode
Static Mixer Untuk Meningkatkan Efisiensi Proses Transesterifikasi Minyak Nabati
Menjadi Biodiesel” ini juga telah mendapat anugerah
(award)
yang dilombakan
dalam momen DISSERTATION SCHOLAR DISSERTATION AWARD, yang
disponsori FORD FOUNDATION dan dilaksanakan oleh The Indonesian
International Education Foundation (IIEF) pada bulan Mei 2010.
i
DAFTAR ISI
Halaman
DAFTAR TABEL ……….
iv
DAFTAR GAMBAR ………...
v
DAFTAR LAMPIRAN………....
viii
DAFTAR SIMBOL ………....
x
I. PENDAHULUAN
………..……….
1
1.1 Latar Belakang ………...…
1
1.2 Rumusan Masalah ………..
5
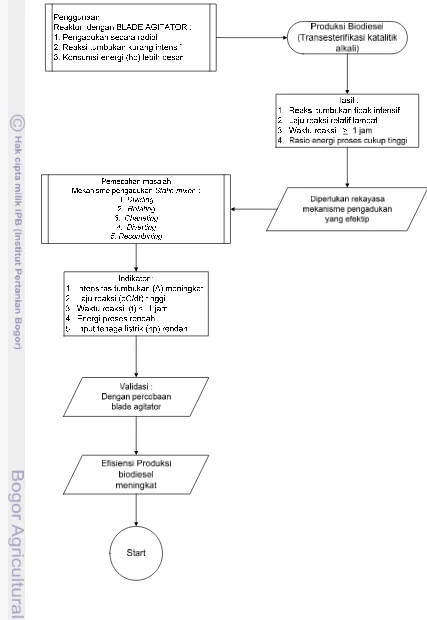
1.3 Kerangka Pemikiran ………..…….
6
1.4 Hipotesis ……….
8
1.5 Tujuan Penelitian ………....
8
1.6 Manfaat Penelitian ………...
9
1.7 Ruang Lingkup dan
Outline
Disertasi ………
9
II. TINJAUAN PUSTAKA
……….…………
11
2.1 Biodiesel ………..…...
11
2.2 Proses Transesterifikasi ……….……
12
2.2.1 Faktor-faktor yang Mempengaruhi Proses Transesterifikasi
13
2.2.2 Penggunaan Katalis………..……….
16
2.2.3 Kinetika Reaksi ………
25
2.3
Static-mixer
……….……...
30
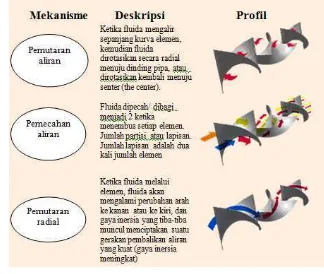
2.3.1 Profil Turbulensi Fluida dalam
Static-mixer
...
30
2.3.2 Jenis
Static-mixer
……….. 31
2.3.3 Aplikasi
Static-mixer
……….. 33
2.4
Blade agitator
………
34
III.
METODE PENELITIAN
……… 37
3.1 Tempat dan Waktu Penelitian ……….……..
37
3.2 Bahan ……….………....
37
3.3 Reaktor
Static-mixer
……….……….
37
3.4 Kondisi Percobaan ………... 39
3.5 Prosedur Percobaan ……….……….
41
3.5.1 Uji Performansi ………...
41
3.5.2 Analisis Parameter Uji ………...……….
42
3.5.3 Kinetika Reaksi ...
423.5.4 Analisis Kehilangan Panas ………...…
44
ii
IV. HASIL DAN PEMBAHASAN
…….………
47
4.1 Karakteristik Teknik Reaktor ……….………
47
4.1.1 Uji Performansi………..………..
47
4.1.2 Analisis Parameter Uji ……..………..……….
51
4.2 Kinetika Reaksi …….………
56
4.2.1 Laju Reaksi ………
56
4.2.2 Perbandingan Reaksi menggunakan
Static-mixer
dan
Blade
agitator
………
61
4.2.3 Konstanta Laju Reaksi (k) ...
63
4.2.4 Energi Aktifasi (Ea) dan Frekuensi Tumbukan (A) ………....
68
4.3 Analisis Energi ……….. ………
72
4.3.1 Analisis Kehilangan Panas ………..………
72
4.3.2 Kebutuhan Energi untuk Proses Transesterifikasi ………..….
78
4.3.3 Kebutuhan Energi untuk Pemanasan awal dan Purifikasi………
79
4.3.4 Rasio Energi ……….………...
81
V. KESIMPULAN
……….………..
86
5.1 Kesimpulan ……...………
86
5.2 Saran ………...
87
DAFTAR PUSTAKA
……….………..
88
iii
DAFTAR TABEL
Halaman
1 Data konsumsi BBM Indonesia tahun 2009 ...
2
2 Karakteristik
katalis asam homogen ...
22
3 Karakteristik katalis asam heterogen ...
22
4 Perbandingan metode katalis lipase dan alkali dalam pengolahan
biodiesel………
24
5 Komparasi metode katalis dan non-katalis...
24
6 Petunjuk
penggunaan
static mixer...
33
7 Hasil uji coba reaktor
static-mixer
... 50
8 Keseimbangan masa pengolahan biodiesel dengan
static-mixer…..
50
9 Konstanta laju reaksi transesterifikasi dengan
static-mixer
dan
blade
agitator
...
65
10 Perbandingan energi aktivasi (Ea) dan frekuensi tumbukan (A)
70
11 Konsumsi energi untuk setiap tahap produksi biodiesel ……...
79
iv
DAFTAR GAMBAR
Halaman
1
Bauran energi Indonesia tahun 2006 dan proyeksinya tahun 2025
1
2
Opsi proses transesterifikasi ………..……
4
3
Kerangka pemikiran penelitian ………
7
4
Reaksi alkoholisis trigliserida dengan metanol ...
12
5
Diagram proses transesterifikasi (untuk FFA minyak < 0,5 %)
19
6
Diagram proses Es-trans (esterifikasi-transesterifikasi) untuk
FFA minyak > 0,5 %) ...
20
7
Mekanisme reaksi katalis asam ...
21
8
Reaksi transesterifikasi TG dan MeOH ...
25
9
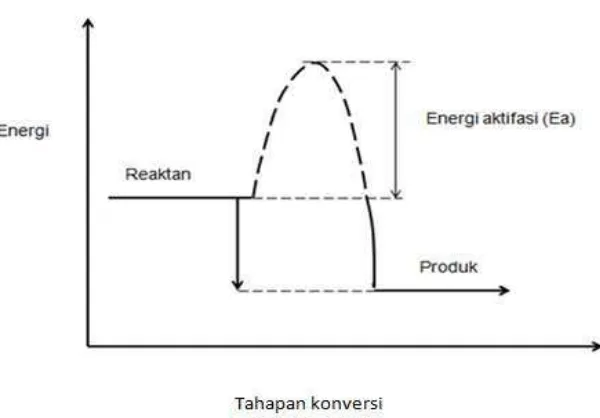
Hubungan energi dan reaksi bahan kimia ……….
27
10
Jenis elemen dan
housing
dari
static-mixer
tipe
helical ………..
32
11
Profil zona reaksi reaktan A dan B dalam reaktor
blade agitator
35
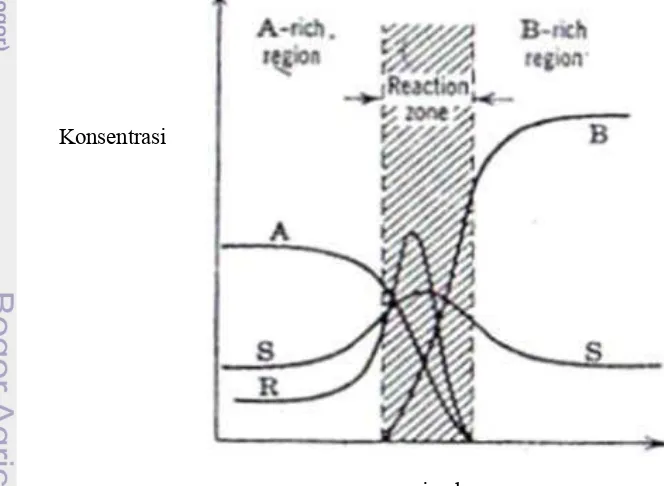
12
Profil zona reaksi reaktan, produk, serta reaktan yang tidak
bereaksi ...
35
13
Diagram reaktor dan setting percobaan
...……….. 49
14
Diagram rancangan (a) elemen
static-mixer
, (b)
balde agitator
41
15
Diagram posisi pengukuran kondisi proses ...
42
16
Diagram alir percobaan penelitian………
45
17
Sampel produk biodiesel selama proses transesterifikasi
…...… 47
18
Produk hasil pengendapan ...………...…...……
48
19
Proses pencucian biodiesel ..………..
48
20
Perbandingan biodiesel pada tahap transesterifikasi, pencucian,
dan pengeringan ………..………...
49
21
FAME yang dihasilkan dengan
static-mixer
pada suhu 50, 60
dan 70
oC ………..………...
52
v
23
Gliserol total FAME yang dihasilkan dengan
static-mixer
pada
suhu 50, 60 dan 70
oC ...
54
24
Viskositas AME yang dihasilkan dengan
static-mixer
pada
suhu 50, 60 dan 70
oC ...
55
25
Densitas FAME yang dihasilkan dengan
static-mixer
pada suhu
50, 60 dan 70
oC ...
56
26
Pengaruh suhu terhadap pembentukan FAME menggunakan
static-mixer ...
57
27
Pengaruh suhu terhadap pembentukan FAME menggunakan
blade agitator ...
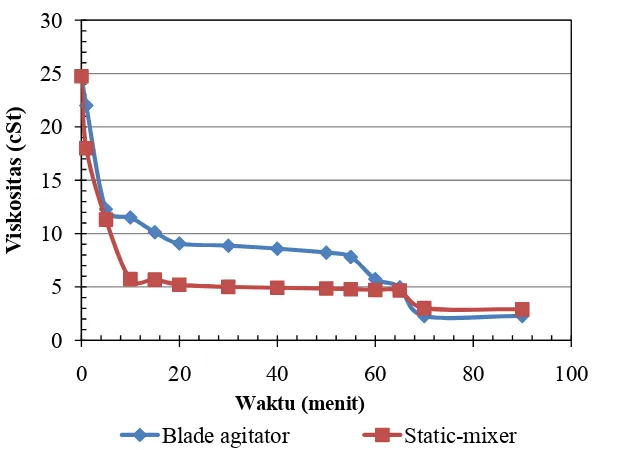
57
28
Viskositas FAME yang dihasilkan dengan
static-mixer
dan
blade
agitator
pada suhu 65
oC ...
58
29
Angka asam FAME yang dihasilkan dengan
static-mixer
dan
blade agitator
pada suhu 65
oC ...
58
30
Pembentukan
FAME
menggunakan
static-mixer
dan
blade
agitator
pada suhu 50
oC ...
60
31
Pembentukan
FAME
menggunakan
static-mixer
dan
blade
agitator
pada suhu 70
oC ………….……….
60
32
Hubungan konsentrasi ME selama reaksi transesterifikasi
menggunakan
static-mixer
dan
blade agitator
pada suhu 50
oC
65
33
Hubungan konsentrasi ME selama reaksi transesterifikasi
menggunakan
static-mixer
dan
blade agitator
pada suhu 55
oC
66
34
Hubungan konsentrasi ME selama reaksi transesterifikasi
menggunakan
static-mixer
dan
blade agitator
pada suhu 60
oC
66
35
Hubungan konsentrasi ME selama reaksi transesterifikasi
menggunakan
static-mixer
dan
blade agitator
pada suhu 65
oC
67
36
Hubungan Konsentrasi ME selama reaksi transesterifikasi
menggunakan
static-mixer
dan
blade agitator
pada suhu 70
oC
67
37
Plot Arhenius antara konstanta laju reaksi (ln k) tahap awal
vi
38
Plot Arhenius antara konstanta laju reaksi (ln k) tahap akhir
dengan kebalikan suhu mutlak menggunakan
static-mixer
………
69
39
Plot Arhenius antara konstanta laju reaksi (ln k) dengan
kebalikan suhu mutlak menggunakan
blade agitator
……
………
69
40
Posisi pengukuran suhu pada reaktor,
static-mixer ...
72
41
Sebaran suhu pada tutup atas, uap keluar, heater,dan kran atas
73
42
Sebaran suhu pada pipa sirkulasi, dinding luar,
static-mixer,
dan
kran bawah ……….………..
73
43
Sebaran suhu pada tutup bawah, dinding dalam, glas wool, dan
kran tengah ………...
74
44
Sebaran suhu rata-rata pada reaktor………
76
45
Kehilangan panas pada reaktor ………..
77
46
Kebutuhan
energi
transesterifikasi yang dibutuhkan untuk
static-mixer
dan
blade agitator
………….………..
79
47
Distribusi energi produksi biodiesel dengan reaktor
static-mixer
80
48
Distribusi energi produksi biodiesel dengan reaktor
blade
agitator
……….
81
49
Rasio energi produksi biodiesel dengan tanpa melibatkan energi
purifikasi ………...……
82
50
Rasio energi produksi biodiesel dengan melibatkan energi
vii
DAFTAR LAMPIRAN
Halaman
1 Gambar piktorial reaktor
static-mixer ...
95
2 Gambar irisan reaktor
static-mixer
... 96
3 Tampak atas reaktor
static-mixer
...
.
97
4 Spesifikasi
Reaktor
Static-Mixer ...
98
5 Rancangan Fungsional Reaktor
Static-mixer ……….……
…... 100
6 Perhitungan rancangan tangki reaktor
static-mixer
………..… 105
7 Perhitungan
rancangan
settling tank
dan pencucian.
...
106
8 Perhitungan tenaga pompa …...….
107
9 Perhitungan tenaga pemanas (
Heater)
... 110
10 Perhitungan
rancangan
kondensor...
112
11 Perhitungan komposisi bahan baku sesuai dengan rasio yang
viii
27 Perhitungan Er suhu 60
oC
………...
... 140
28 Perhitungan Er suhu 65
oC
………...………
…… 141
29 Perhitungan Er suhu 70
oC
………...……
….. 142
30
Roadmap
biodiesel Indonesia ...
143
ix
DAFTAR SINGKATAN
A : Frekuensi tumbukkan atau faktor pre-eksponensial (tidak berdimensi)
As : Angka penyabunan (mg KOH/g biodiesel)
Aa : Angka asam (mg KOH/g biodiesel)
Ad luas / penampang dinding tangki reaktor (m2)
CN: : Bilangan setana (tidak berdimensi)
CP : Cloud Point atau titik kabut (oC)
CR : Residu karbon (% w/w),
Dd : Diameter dinding tangki reaktor (m)
DG : Digliserida
Ef : Rasio energi
Ea : Energi aktivasi (kj/mol)
f : Koefisien gesekan
FFA : Free fatty acyd atau kadar asam lemak bebas (% )
FP : Flash point atau titik nyala (oC)
g : percepatan gravitasi (m/det2)
GL : Gliserol
Gb : Gliserol bebas (% massa)
Gttl : Gliserol total (% massa)
hp : Tenaga motor (Watt)
h : koefisien pindah panas konveksi (W/m2°K),
hf : Kehilangan tekanan akibat gesekan (m)
hb : Kehilangan tekanan akibat belokan (m)
hl : Kehilangan tekanan akibat kran (m)
hsm : Kehilangan tekanan akibat static-mixer (m)
ht : Kehilangan total (m)
k : Konstanta laju reaksi transesterifikasi keseluruhan (menit -1)
k1 : Konstanta laju reaksi transesterifikasi tahap awal (menit -1)
k2 : Konstanta laju reaksi transesterifikasi tahap akhir (menit -1)
x
kr : Konstanta laju reaksi konversi TG menjadi ME (menit -1)
kl : Konstanta laju reaksi konversi Me menjadi TG (menit -1)
k’ : Pseudo konstanta laju reaksi transesterifikasi (menit -1)
Kt : Parameter pressure drop aliran turbulen
MeOH : Metanol
ME : Kandungan metil ester (% w/w)
MG : Monogliserida
NNu : bilangan Nusselt (tidak berdimensi)
n : Jumlah elemen static-mixer
n : Jumlah mol
PP : Pour point atau titik tuang (oC)
NGr : bilangan Grashoff (tidak berdimensi)
Npr : bilangan Prandtl (tidak berdimensi)
p : Panjang pipa (m)
Q : Laju volumetrik (m3/menit)
qn : kehilangan panas (kJ),
R : Tetapan gas (8,31 jK-1mol-1)
Rn : Asam lemak, n :1,2,3....dst
RBDPO : Refined bleached deodorized palm olein
Re : Bilangan Reynolds (tidak berdimensi)
T : Suhu biodiesel (oC)
TG : Trigliserida
[ TG ] : Kadar trigliserida (%,w/w)
t : Waktu (jam)
td : temperatur dinding luar (°K)
tu : suhu udara luar (°K)
μ ME : unmethyl esterfied compounds
[μ ME] : Kadar unmethyl esterfied compounds (% w/w)
w : Lebar elemen
v : kecepatan alir (m/det)
xi
DAFTAR SIMBOL
ß
:
koefisien muai volume (1/K)
ρ
:
Densitas (kg/L)
μ
:
Viskositas kinematik (cSt)
μ
d
:
Viskositas dinamik (Pa.s)
1
I. PENDAHULUAN
1.1 Latar Belakang
Bahan bakar minyak berbasis fosil seperti solar, premium (bensin), premix dan minyak tanah sangat memegang peranan penting dalam memenuhi kebutuhan energi nasional antara lain untuk transportasi, industri, mesin pertanian, dan keperluan rumah tangga. Dilihat dari kebutuhan energi nasional, sekitar lima puluh persen bahan bakar tersebut dipasok dari bahan bakar yang berasal dari minyak bumi, sedangkan sebagian lagi dipenuhi dari sumber energi lain seperti batu bara, gas bumi, panas bumi dan tenaga air. Sumber energi terbarukan (renewable energy) seperti biomassa sejauh ini belum banyak dimanfaatkan
sehingga menyebabkan bauran energi (energy mix) dirasakan masih timpang.
Bauran energi di Indonesia dalam memenuhi kebutuhan energi nasional adalah: minyak bumi 52 %, gas bumi 29 %, batu bara 15 %, PLTA 3 %, panas bumi 1 % dan energi terbarukan 0,2 %. Ketimpangan ini dimungkinkan karena penguasaan teknologi yang belum maksimal dan sistem pengelolaan energi yang kurang baik (Komara, 2007). Pada tahun 2025 direncanakan target bauran energi berubah dengan penurunan penggunaan minyak bumi dan peningkatan penggunaan sumber energi gas, batu bara, dan energi baru terbarukan seperti terlihat dalam Gambar 1.
Gambar 1. Bauran energi Indonesia tahun 2006 dan proyeksinya tahun 2025 (Perpres No. 5 Tahun 2006)
2 Kebutuhan energi bersifat primer dan selalu beriringan dengan pertumbuhan ekonomi. Dengan pertumbuhan industri dan produksi kendaraan transportasi yang terus meningkat mengakibatkan kenaikan permintaan bahan bakar dari minyak bumi. Dengan tingkat pertumbuhan ekonomi nasional yang terus dipacu dan membaik, bisa dipastikan konsumsi energi juga akan meningkat. Data terakhir konsumsi BBM (bensin, solar, dan minyak tanah) pada tahun 2009 disajikan dalam Tabel 1. Dalam tabel tersebut disajikan data konsumsi bahan bakar menurut sektor (industri, rumah tangga, dan transportasi) dan terlihat bahwa jenis BBM solar merupakan jumlah terbanyak dikonsumsi dengan jumlah 122,25 kL, sedangkan dilihat dari sektor maka sektor transportasi mengkonsumsi BBM kedua terbanyak yaitu 35,05 % setelah sektor industri.
Tabel 1. Data Konsumsi BBM Indonesia Tahun 2008
Konsumsi Menurut Jenis (Juta kL)
Jenis BBM bersubsidi Bensin Solar Minyak tanah Jumlah Jumlah 114,79 122,25 46,83 283,87
Konsumsi Menurut Sektor (%) Sektor Industri Transportasi Rumah
tangga
komersial Lain-lain Jumlah
Jumlah 39,84 35,05 15,50 5,06 4,55 100 Sumber : Pusdatin KESDM (2009).
Sebagian dari kebutuhan BBM dalam negeri dipenuhi oleh minyak impor dan saat ini impor BBM mencapai 30 persen dari kebutuhan dalam negeri (Ariati, 2007). Angka tersebut relatif tinggi karena Indonesia merupakan negara penghasil minyak mentah. Di sisi lain laju peningkatan konsumsi bahan bakar minyak di dalam negeri yang semakin tinggi menyebabkan jumlah impor bahan bakar minyak (BBM) pada tahun 2010 diperkirakan akan meningkat 40 persen dari kebutuhan dalam negeri. Oleh sebab itu, ketergantungan impor Indonesia terhadap komoditas BBM dan minyak mentah akan terus meningkat. Di sisi lain cadangan minyak bumi Indonesia terbatas.
3 PERPRES No. 5 tahun 2006 tentang kebijakan energi nasional yang menjelaskan target pemerintah di bidang konversi energi melalui pemanfaatan sumber energi alternatif. Biodiesel berpotensi menggantikan solar dan bisa menjadi solusi permasalahan bahan bakar minyak (BBM) di masa mendatang.
Informasi yang menyatakan FAME (biodiesel) dengan stabilitas oksidasi dan termal yang lebih rendah dibanding petroleum diesel telah mendorong beberapa fihak untuk melakukan hydrogenated vegetable oil (HVO) agar stabilitas oksidasi dan oksidasi termal lebih baik dari peroleum diesel. dengan pertimbangan bila tidak dilakukan akan membuat FAME (biodiesel) akan tidak kompetitif dengan HVO. Sebenarnya reaksi oksidasi ini terjadi karena pengaruh oksigen atmosfir dalam biodiesel (autoxidation). Proses ini berlangsung selama transportasi dan penyimpanan biodiesel dan dalam tangki bahan bakar di kendaraan.
Biodiesel termasuk golongan alkil ester dengan nama kimia alkil ester mempunyai kemiripan sifat dengan solar. Biodiesel merupakan salah satu jenis bahan bakar pengganti solar yang yang berasal dari minyak nabati yang bahan bakunya bisa diperbaharui dengan cara budidaya. Beberapa sumber minyak nabati yang bisa digunakan sebagai sumber bahan biodiesel adalah biji sawit, biji jarak, biji nyamplung, kelapa, kedelai dan lainnya. Penggunaan biodiesel sebagai bahan bakar untuk mesin diesel mempunyai beberapa keuntungan antara lain bisa mengurangi ketergantungan terhadap pasar minyak dunia, menjadikan substitusi bahan bakar solar (biosolar) dan bisa mengurangi emisi gas buang kendaraan (Wirawan, et al., 2008; Carraretto, et. al., 2004). Biodiesel merupakan metil ester (fatty acid methyl ester) yang diproses dengan cara transesterifikasi antara
trigliserida yang berasal dari minyak nabati atau lemak hewan dengan alkohol rantai pendek terutama metanol untuk digunakan sebagai bahan bakar mesin diesel (Mettelbach dan Remschmidt, 2004; Knothe, 2005).
4 yang lebih maju sejalan dengan waktu (Ariyati, 2007). Proses transesterifikasi tersebut bisa dilakukan dengan menggunakan katalis atau tanpa katalis. Katalis yang digunakan dalam proses transesterifikasi (catalytic transesterification) bisa terdiri dari katalis asam, basa, dan biokatalis (enzim), sedangkan untuk untuk proses transesterifikasi tanpa katalis (non-catalytic transesterification) bisa diproses pada tekanan atmosfir dan kondisi tekanan tinggi (supercritical). Secara skematis metode-metode transesterifikasi dapat dilihat dalam Gambar 2.
Sejauh ini teknik produksi biodiesel komersil umumnya dilakukan dengan proses transesterifikasi menggunakan katalis basa. Salah satu masalah yang dihadapi dalam menghasilkan biodiesel dengan metode ini adalah laju reaksi atau efektifitas proses transesterifikasi yang masih relatif lambat sehingga berimplikasi terhadap jumlah energi yang dibutuhkan dalam proses relatif besar (Carraretto et al., 2004; Mootabadi et al., 2008; Ajav dan Akingbehin, 2002). Untuk lebih
mendapatkan proses yang lebih efisien dari proses katalis basa ini, maka perlu dikembangkan suatu rekayasa proses yang lebih efisien diilihat dari pemakaian energi, laju reaksi, waktu reaksi.
Masalah dalam proses transesterifikasi katalis basa tersebut adalah sukar bercampurnya trigliserida dan metanol. Dengan mekanisme pencampuran biasa menggunakan blade agitator, frekuensi tumbukan kurang optimal bila dilakukan
5 pada putaran (rpm) yang rendah. Bahan-bahan tersebut bisa bereaksi atau proses reaksi bisa mengarah ke kanan bila diterapkan mekanisme pengadukan yang amat kuat (vigorous stirring) dan suhu yang relatif tinggi (Darnoko dan Cheryan, 2000a). Dengan kata lain dibutuhkan putaran (rpm) yang amat tinggi, di mana sebagai konsekuensinya memerlukan daya (horse power / hp) yang cukup besar.
Untuk memperbaiki rekayasa proses ini maka perlu dikembangkan suatu proses pengolahan biodiesel dengan katalis basa yang mempunyai sistem pengadukan (stirring) yang lebih intensif sehingga laju reaksi lebih tinggi dari yang sudah dicapai, konstanta reaksi (k) lebih tinggi, dan energi aktivasi (Ea) yang lebih rendah. Untuk pengembangan rekayasa proses ini diperlukan suatu pendekatan rancangan peralatan yang baru. Salah satu pendekatannya adalah pemanfatan sistem pengadukan static-mixer pada reaktor biodiesel.
Rasio energi (perbandingan energi output – input) di dalam suatu proses pengolahan biodiesel dapat dijadikan suatu ukuran nilai efisiensi ekonomis dan teknis selama proses berlangsung sehingga dapat dijadikan cara untuk menentukan metode yang terbaik dalam pengolahan biodiesel (Costa, 2006; Mootabadi, et al., 2008; Spath dan Mann, 2000 ). Semakin tinggi nilai rasio energi maka akan semakin efisien energi yang digunakan untuk poduksi biodiesel. Penelitian yang membahas analisis rasio energi dari pengolahan biodiesel masih belum banyak dilakukan. Sejauh ini penelitian rasio energi biodesel dilakukan dengan menggunakan reaktor konvensional (blade agitator). Dalam penelitian ini akan dilakukan proses transesterifikasi dengan menggunakan reaktor static-mixer di samping itu juga dihitung energi input untuk pemanasan awal minyak dan purifikasi (pencucian dan pengeringan).
1.2 Rumusan Masalah
Sistematika perumusan masalah yang akan dikaji dalam penelitian ini adalah sebagai berikut:
6 Metode pengadukan yang banyak diterapkan masih menggunakan metode pengadukan (mixing) konvensional dalam proses produksi biodisel (blade agitator); akibatnya bila pengadukan kurang kuat mengakibatkan efektifitas reaksi
(frekuensi) tumbukan berkurang serta menghasilkan nilai konstanta reaksi (k) yang relatif kecil,
Konversi biodiesel (metil ester) dari minyak nabati (triglserida) dengan katalis basa dipengaruhi pengadukan (vigorous stiring), semakin tinggi rpm produksi semakin tinggi produksi/laju pembentukan metil ester. Pengadukan yang efektif diperkirakan dapat meningkatkan reaksi tumbukan, laju reaksi, dan meningkatkan konstanta reaksi pada proses produksi biodiesel.
1.3 Kerangka Pemikiran
Waktu reaksi yang relatif lama dan konsumsi energi yang tinggi merupakan kendala dalam pengolahan biodiesel dari minyak nabati dengan metode katalitik basa. Lamanya reaksi disebabkan laju reaksi pembentukan metil ester (biodiesel) masih lambat. Lambatnya pembentukan metil ester ini erat kaitannya dengan mekanisme pengadukan yang selama ini digunakan. Umumnya pengolahan biodiesel menggunakan reaktor yang dilengkapi dengan blade agitator untuk melangsungkan reaksi transesterifikasi. Persoalan dengan sistem
pengadukan bahan seperti ini adalah dua fase bahan dalam reaksi sulit bercampur. Bila putaran blade agitator tidak tinggi akan memberikan efek pencampuran yang tidak maksimal (laju reaksi yang lambat), sehingga sulit untuk mendapatkan waktu reaksi yang singkat.
8 Sejauh ini penelitian pengolahan biodiesel dengan menggunakan static-mixer masih terbatas. Thompson (2007) melakukan penelitian pengolahan
biodiesel (canola metil ester) dari minyak canola menggunakan static-mixer skala 30 ml dengan melihat pengaruh berbagai konsentrasi katalis. Reaktor static-mixer merupakan reaktor skala laboratorium dengan lebar elemen 4,9 mm dan panjang 300 mm. Hasil penelitian menunjukkan waktu pengolahan metil ester yang terbaik (total gliserol terendah) dicapai pada suhu 60 oC, konsentrasi katalis 1,5 % dengan waktu proses 30 menit.
Untuk memperbaiki rekayasa proses ini diperlukan suatu rancangan peralatan yang baru yaitu reaktor static mixer yang mampu memberikan konstanta reaksi yang lebih tinggi dan memberikan efisiensi energi (rasio energi output-input) yang tinggi.
1.4 Hipotesis
Tiga hipotesis yang dikemukakan dalam penelitian ini terdiri dari:
1. Konstanta laju reaksi (k) dan frekuensi tumbukan (A) dapat meningkat dengan sistem pengadukan static-mixer
2. Waktu reaksi pembentukan biodiesel (fatty acid methyl ester atau FAME) dengan static-mixer akan lebih singkat dibandingkan waktu reaksi menggunakan blade agitator
3. Konsumsi energi dapat berkurang dengan penerapan static-mixer dalam reaktor pengolahan biodiesel
1.5 Tujuan Penelitian
Tujuan penelitian adalah untuk mengkaji reaksi pengolahan biodiesel dari minyak sawit dengan reaktor static-mixer sehingga diperoleh waktu transesterifikasi lebih singkat dan kebutuhan energi pengolahan relatif lebih kecil dibandingkan reaktor blade agitator. Secara spesifik tujuan penelitian adalah untuk:
9
static-mixer pada beberapa tingkat suhu yaitu 50, 55, 60, 65, dan 70oC pada
tingkat suhu yang sama pada tekanan atmosfir. Sebagai pembanding proses transesterifikasi dengan menggunakan blade agitator dilakukan.
2. Mengkaji kebutuhan energi transesterifikasi, kebutuhan energi pemanasan awal dan purifikasi (pencucian dan pengeringan) dan rasio energi biodiesel dari minyak curah sawit (refined bleached deodorized palm olein RBDPO).
1.6 Manfaat Penelitian
Manfaat yang diharapkan dari hasil penelitian ini adalah untuk 1) memberikan informasi karakteristik transesterifikasi biodiesel dengan reaktor static-mixer, 2) memberikan informasi rancangan sebagai bahan scale up reaktor,
dan 3) memberikan alternatif rancangan pengolahan biodiesel dengan waktu yang lebih singkat dan energi pengolahan biodiesel lebih kecil.
1.7 Ruang Lingkup dan Outline Disertasi
Penelitian ini mengkaji pembuatan biodiesel dengan menggunakan sistem pengadukan static-mixer. Dalam proses pembuatan biodiesel tersebut digunakan bahan baku (feedstock) trigliserida (TG) dari minyak goreng sawit (RBDPO), methanol (MeOH) dengan bantuan katalis KOH. Percobaan dilakukan dengan mengunakan reaktor static-mixer dengan mereaksikan reaktan (TG, MeOH, dan katalis sebanyak 16,5 liter (kapasitas maksimum reaktor 23 liter). Secara garis besar pembuatan biodiesel terdiri dari tahap proses pemanasan awal minyak, proses transesterifikasi, dan proses purifikasi (pencucian dan pengeringan). Untuk memvalidasi hasil proses transesterifikasi dengan static-mixer maka dilakukan juga percobaan yang sama dengan menggunakan reaktor blade agitator. Secara garis besar pembahasan dalam penelitian ini terdiri dari 3 pembahasan, yaitu:
10 Kedua, pembahasan mengenai kajian tentang menentukan kinetika reaksi transesterifikasi (laju reaksi, konstanta laju reaksi k, energi aktivasi Ea, dan frekuensi tumbukan A) menggunakan reaktor static-mixer pada beberapa tingkat suhu yaitu 50, 55, 60, 65, and 70oC pada tekanan atmosfir. Hasilnya dibandingkan dengan hasil yang dicoba dengan menggunakan reaktor blade agitator pada kondisi percobaan yang sama.
11
II. TINJAUAN PUSTAKA
2.1 Biodiesel
Biodiesel merupakan sejenis bahan bakar diesel yang diproses dari bahan hayati terutama minyak nabati dan lemak hewan dan secara kimiawi dinyatakan sebagai monoalkil ester dari asam lemak rantai panjang yang bersumber dari golongan lipida (Darnoko, et al., 2001; Tapasvi, et al., 2005; Ma dan Hanna, 1999). Biodiesel didefinisikan sebagai monoalkil ester rantai panjang dari asam lemak yang diderivasi dari bahan yang dapat diperbaharui (renewable feedstocks), seperti minyak nabati dan lemak hewan, untuk penggunaan penyundutan kompresi (compression-ignition) dari mesin diesel (Krawczyk, 1996). Biodiesel dianggap sebagai bahan bakar pengganti (alternatif) dari bahan bakar konvensional diesel solar yang tersusun dari metil ester asam lemak (FAME).
Terminologi biodiesel berasal dari persetujuan Department of Energy (DOE), The Environmental Protection Agency (EPA) dan The American Society of
Testing Materials (ASTM) sebagai salah satu energi alternatif untuk mesin diesel
(ASTM, 2002; DOE, 2009; EPA 2009 ). Istilah bio merujuk kepada bahan terbarukan dan bahan hayati yang berbeda dari solar yang berbahan baku minyak bumi. Dalam kenyataannya, biodiesel bisa digunakan murni (100 % metil ester) atau sebagai campuran dengan perbandingan tertentu dengan bahan bakar solar. Dalam istilah perdagangan campuran biodiesel dengan solar dinamakan dengan notasi BXX. Misalnya bila campuran biosolar mengandung 5 % atau 10 % solar maka notasi masing-masing biosolar dinyatakan sebagai B5 dan B10.
Biodiesel merupakan monoalkil ester (misal: fatty acid methyl ester/FAME) yang diproses dengan metode transesterifikasi antara trigliserida
12 2.2 Proses Transesterifikasi
Reaksi transesterifikasi memegang peranan penting dalam pengolahan biodiesel dari minyak nabati (trigliserida atau TG). Reaksi transesterifikasi disebut juga reaksi alkoholisis dan proses ini sering dikaitkan dengan proses untuk mengurangi viskositas trigliserida (TG) (Otera, 1993). Reaksi transesterifikasi secara umum dinyatakan sebagi berikut (persamaan 1):
Bila methanol (MeOH) digunakan dalam reaksi di atas maka reaksinya disebut metanolisis dan reaksinya bisa dilihat seperti pada Gambar 4. Untuk menjadikan biodiesel, minyak nabati diproses secara kimia dengan cara transesterifikasi dengan keberadaan alkohol (metanol atau etanol) dan katalis (basa atau asam) untuk menghasilkan alkil ester (biodiesel) dan gliserol sebagai hasil samping.
H2C O C O
R1
HC O C
O
R2
H2C O C O
R3
3CH3OH
MeOH
H3C O C O
R1
H3C O C O
R2
H3C O C O
R3
H2C OH
HC OH
H2C OH
TG FAME GL
... [2]
Gambar 4. Reaksi alkoholisis TG dengan MeOH reaksi keseluruhan pers. [2]; tiga reaksi berurutan dan reversibel pers. [3] (R1,2,3 = asam lemak)
Trigliserida (TG) sebagai komponen utama dari minyak nabati bila direaksikan dengan dengan alkohol (misal methanol), maka ketiga rantai asam lemak akan dibebaskan dari skeleton gliserol dan bergabung dengan methanol untuk menghasilkan asam lemak alkil ester (misal asam lemak metil ester atau
TG + CH3OH DG + CH3COOR1
DG + CH3OH MG + CH3COOR2 ……...[3]
MG + CH3OH GL + CH3COOR3.
RCOOR1 + R2OH RCOOR2 + R1OH ……….…..…..[1]
13 FAME). Reaksi transesterifikasi merupakan reaksi tiga tahap dan reaksi balik (reversible) yang membentuk tiga molar FAME dan satu molar gliserol (GL) dari
satu molar trigliserida (TG) dan tiga molar methanol. Digliserida (DG) dan monogliserida (MG) merupakan hasil reaksi antara (intermediate). Terdapat dua jenis proses transesterifikasi yaitu transesterifikasi dengan katalis dan transesterifikasi tanpa katalis. Katalis diharapkan dapat mempengaruhi laju reaksi dalam memproduksi biodiesel secara katalitik pada skala komersial.
2.2.1 Faktor-Faktor Yang Mempengaruhi Proses Transesterifikasi
Transesterifikasi minyak nabati menjadi biodesel merupakan suatu proses bertahap dan reversible. Proses ini dipengaruhi oleh beberapa parameter antara lain: 1) Homogenisasi reaksi (keseragaman pencampuran), 2) molar rasio antara methanol and minyak nabati, 3) suhu reaksi, 4) tekanan dalam reaksi, 5) waktu reaksi, dan 6) jenis katalis (Mettelbach dan Reshmidt, 2004).
2.2.1.1 Homogenisasi Reaksi (Pencampuran)
Homogenisasi campuran dalam reaksi merupakan salah satu parameter penting yang mempengaruhi efektifitas reaksi karena dari kondisi ini maka reaksi tumbukan akan terjadi yang pada akhirnya akan mempengaruhi laju reaksi, konstanta reaksi, energi aktivasi dan lama reaksi. Transesterifikasi tidak akan berlangsung baik bila campuran bahan tidak dihomogenisasi terutama selama tahap awal proses. Pengadukan yang kuat (vigorous stirring) merupakan salah satu metode homogenisasi yang cukup berhasil untuk proses yang dilakukan secara batch dan kontinyu (darnoko dan Cheryan, 2000)..
2.2.1.2 Rasio Molar
14 jumlah alkohol terlalu berlebih maka akan berakibat menganggu pemisahan gliserol (Srivasta dan Prasad, 2000). Rasio molar untuk proses transesterifikasi dengan katalis asam perbandingannya direkomendasikan bisa mencapai 30 : 1 (Mittelbach dan Reshmidt, 2004).
2.2.1.3 Suhu Reaksi
Transesterifikasi dapat dilakukan pada berbagai tingkatan suhu tergantung dari jenis minyak nabati yang digunakan. Dalam proses metanolisis kastor oil menjadi metil risinoleat, reaksi akan berlangsung memuaskan bila dioperasikan pada suhu 20 – 35oC dengan rasio molar 6 :1 and 12 : 1 menggunakan NaOH sebagai katalis (Fredman et al., 1984). Untuk transesterifikasi minyak kedelai dengan metanol molar ratio yang digunakan adalah 6 : 1 dengan 1 % NaOH, untuk berbagai suhu transesterifikasi (Fredman et al., 1986). Setelah satu jam proses ester yang terbentuk adalah 94,87 % dan 64 % untuk suhu 45 dan 32 oC. Suhu reaksi mempengaruhi laju reaksi dan ester yang terbentuk. Yamazaki et al., (2007) menjelaskan flowrate produksi FAME meningkat dari 0,1 g/menit mulai pada suhu 250 oC menjadi 1,0 g/menit pada suhu 330 oC.
2.2.1.4 Waktu Reaksi
15 penghitungan waktu reaksi dimulai saat suhu bahan secara keseluruhan telah mencapai 70 oC
2.2.1.5 Tekanan Reaksi
Metil ester dapat direaksikan dalam kondisi tekanan rendah dan tinggi. Secara komersil produksi biodiesel dari minyak nabati dilangsungkan pada tekanan rendah guna mengurangi biaya pengolahan dan keamanan dan umumnya dilakukan pada tekanan atmosfir. Proses produksi biodiesel dengan tekanan tinggi dapat dilangsungkan di atas tekanan 100 bar pada suhu 250 oC dengan kelipatan 7 hingga 8 molar ekses dalam keberadaan katalis basa (Gerpen dan Knothe, 2005). Tekanan reaksi yang tinggi ini juga bisa dilakukan pada transesterifikasi tanpa katalis yang dilakukan pada tekanan 8,09 MPa dan suhu optimal 350 oC (Kusdiana dan Saka, 2000). Keuntungan penggunaan tekanan tinggi dalam proses transesterifikasi adalah bahan baku yang mengandung lebih 20 % FFA dapat diolah tanpa perlakuan pendahuluan serta dapat menghasilkan gliserol kandungan tinggi dapat dihasilkan sebagai hasil samping (Kusdiana dan Saka, 2000 Kusdiana dan Saka, 2000). Pendekatan yang diusulkan Mittelbach dan Junek (1986) yaitu penggunaan tekanan rendah merupakan rekomendasi yang sudah banyak diterapkan dan berhasil dilakukan dalam mengolah biodiesel.
2.2.1.6 Jenis Katalis
16 yang tinggi (Aksoy et al., 1988). Contoh katalis asam yang sering digunakan adalah H2SO4 (disajikan lebih lanjut dalam sub Bab 2.2.2).
2.2.2 Penggunaan Katalis
Katalis dalam proses produksi biofuel (misal esterifikasi atau transesterifikasi) merupakan suatu bahan (misal basa, asam atau enzim) yang berfungsi untuk mempercepat reaksi dengan jalan menurunkan energi aktivasi (actifation energy, Ea) dan tidak mengubah kesetimbangan reaksi, serta bersifat
sangat spesifik. Sebenarnya proses produksi bisa berlangsung tanpa katalis akan tetapi reaksi akan berlangsung sangat lambat, membutuhkan suhu yang tinggi dan tekanan yang tinggi pula. Umumnya untuk mencapai hasil (yields) ester yang memuaskan dalam kondisi reaksi yang sedang, produksi biodiesel dilakukan dengan keberadaan katalis yang meliputi katalis basa (alkali), asam termasuk katalis bahan transisi logam, dan katalis enzim.
Menurut perbedaan fase dengan reaktan, katalis dapat dibagi menjadi katalis homogen yang memiliki fase yang sama dengan reaktannya dan katalis heterogen yang berbeda fase dengan reaktannya (contohnya, katalis padat pada campuran reaktan cair). Katalis heterogen menyediakan permukaan luas untuk tempat reaksi kimia terjadi. Agar reaksi terjadi, satu atau lebih reaktan harus tersebar pada permukaan katalis dan teradsorb ke dalamnya. Setelah reaksi selesai, produk menjauh dari permukaan katalis padat. Seringkali, perpindahan reaktan dan produk dari satu fase ke fase lainnya ini berperan dalam menurunkan energi aktivasi (Mittelbach dan Remschmidt, 2004).
2.2.2.1 Katalis Basa
17 penggunaan katalis basa adalah memerlukan pengadukan yang cukup kuat sehingga merata untuk memperoleh hasil yang maksimal. Di samping itu dalam proses purifikasi biodiesel dari katalis dan bahan lainnya memerlukan waktu yang cukup lama seperti dalam proses decanting, netralisasi, washing, dan drying. (Friedman et al., 1984; Friedman et al., 1986; Noureddini and Zhu, 1997; Darnoko dan Cheryan, 2000).
Saat ini hampir seluruh reaksi pengolahan biodiesel skala komersial menggunakan katalis basa homogen. Katalis yang bersifat basa lebih umum digunakan pada reaksi transesterifikasi karena menghasilkan metil ester yang tinggi dan waktu yang cepat. Konsentrasi katalis yang umum digunakan adalah 0.5-4% dari berat minyak (Mittelbach dan Reschmidt, 2004; Zhang et al., 2003,). Namun pemakaian katalis basa hanya berlangsung sempurna bila minyak dalam kondisi netral dan tanpa keberadaan air. Secara garis besar reaksi yang berlangsung disajikan dalam persamaan [4] dan reaksi pembentukan sabun disajikan dalam persamaan [5].
Katalis homogen selama ini telah digunakan secara luas pada produksi biodiesel, karena harganya yang murah. Walaupun begitu, untuk aplikasi industri katalis heterogen yang berwujud padat menawarkan keuntungan dibandingkan katalis homogen, yaitu mudahnya pemisahan katalis dari produk dengan cara penyaringan dan tidak perlu proses netralisasi untuk menghilangkan sisa katalis. Beberapa katalis heterogen pada proses pembuatan biodiesel menggambarkan bahwa katalis yang mengandung campuran unsur Ca dan Mg, serta katalis yang mengandung K menghasilkan rendemen metil ester yang tinggi.
Katalis bersifat basa yang umum digunakan adalah basa Brönsted sederhana seperti NaOH dan KOH. Freedman et al. (1984) membandingkan penggunaan katalis basa NaOH dan NaOCH3 pada saat memproduksi biodiesel
RONa RO- + Na+
Na + ROH RO- + Na+ + ½ H2 (g)
NaOH + ROH RO- + Na+ + H2O
R1COOR2 + NaOH R1COONa + R2OH ………...[5]
18 dari minyak kedelai. Hasil penelitian mereka adalah bahwa jumlah katalis optimal adalah 1% NaOH atau 0,5% NaOCH3.
Noureddini dan Zhu (1997) menghasilkan rendemen metil ester 80% dari minyak kedelai pada rasio molar metanol-asam lemak 6:1, suhu 60°C, laju pengadukan 300 rpm selama dua jam, dan katalis NaOH 2-4%. Freedman et al. (1984) menyebutkan metil ester dari minyak jelantah dengan kondisi terbaik pada rasio molar metanol terhadap minyak 6:1, katalis KOH 1% dan suhu 65°C.
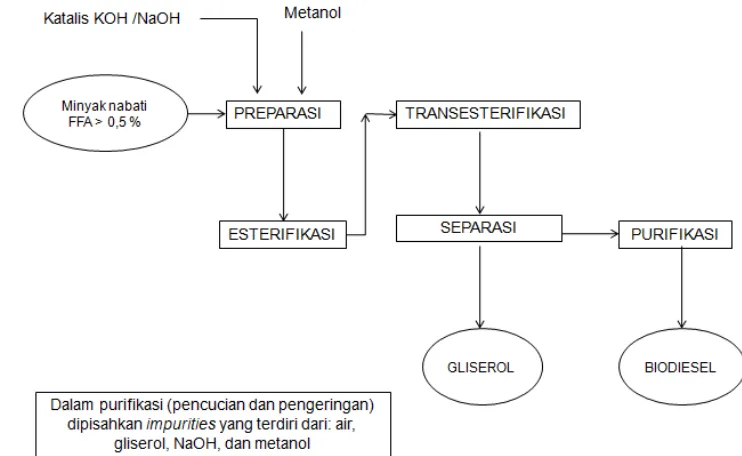
Secara komersial biodiesel banyak diproduksi dengan transesterifikasi alkali (basa) di bawah tekanan atmosfir, diproses secara batch, dioperasikan pada suhu 60 – 70 oC dengan methanol berlebih serta menggunakan katalis NaOH. Dalam proses ini metil ester akan terbentuk secara maksimal dalam waktu 60 menit. Dengan kondisi proses tersebut hasil atau kandungan metil ester yang terbentuk sekitar 97 - 99% (Freedman et al.,1984,) dan proses yang dipilih bergantung dari mutu bahan baku (minyak nabati) awal. Bila minyak mempunyai nilai FFA < 0,5 % maka bisa langsung diproses dengan transesterifikasi dengan katalis basa eperti tersaji dalam diagram proses pada Gambar 5. Bila kandungan FFA > 5 % maka proses harus dilakukan dengan Es-trans (esterifikasi-transesterifikasi). Tahap awal dilakukan netralisasi dengan mereaksikan minyak dengan metanol dan asam misal H2SO4 (proses ini disebut esterifikasi) sehingga nilai FFA minyak
akan turun atau < 0,5 dan selanjutnya dilanjutkan dengan proses transesterifikasi. Proses esterifikasi dan esterifikasi-transesterifikasi (estrans) disajikan dalam Gambar 6.
Setelah reaksi selesai akan terbentuk 2 lapisan, lapisan atas berupa metil ester atau biodiesel serta bagian bawah adalah gliserol. Pada metil ester yang terbentuk ditambahkan asam untuk menetralisir katalis basa dan didiamkan (settling). Untuk purifikasi lebih lanjut biodiesel yang terbentuk dicuci dengan air
19 (Freedman et al., 1984; Noureddini dan Zhu, 1997; Darnoko dan Cheryan, (2000). Untuk lebih meningkatkan mutu biodiesel hasil purifikasi difilter kembali sehingga grade biodiesel akan lebih baik.
20 2.2.2.2 Katalis Asam
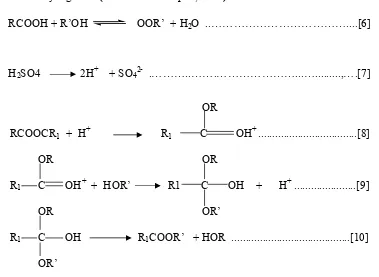
Katalis asam memberikan keuntungan antara lain cocok untuk proses pengolahan biodiesel dengan bahan baku (feedstock) dengan tingkat keasaman yang tinggi atau untuk proses / transesterifikasi (dengan asam lemak bebas yang tinggi). Oleh karena itu cocok untuk proses transesterifikasi minyak sawit atau minyak jelantah (waste edible oil), pada reaksi [6] proses esterifikasi dari asam lemak bebas, sedangkan pada persamaan [7] disajikan mekanisme reaksi transesterifikasi dengan katalis asam. Keunggulan lain dari katalis asam adalah mampu menjadikan produk ester dengan rantai cabang yang panjang, dan katalis asam dapat digunakan dalam tahap pra-esterifikasi. Mekanisme reaksi katalis asam disajikan dalam Gambar 7.
Kekurangan penggunaan katalis asam adalah: 1) memberikan reaksi yang sangat lambat (pada T 65oC, rasio molar metanol terhadap minyak 30, memerlukan waktu 50 jam), 2) menghasilkan produk yang tidak diinginkan (dialkil eter atau gliserol eter bila suhu reaksi dinaikan), dan 3) konversi ester menurun dengan adanya kandungan air. Transesterifikasi berkatalis asam lebih Gambar 6. Diagram proses Es-trans (esterifikasi-transesterifikasi) untuk FFA
[image:47.612.125.496.87.315.2]21 toleran terhadap asam lemak bebas tinggi, tetapi membutuhkan pemanasan tinggi dan waktu yang lama (Canakci dan Gerpen, 1999).
Secara garis besar katalis asam terdiri dari katalis asam homogen dan katalis asam heterogen. Katalis asam homogen terdiri dari beberapa jenis yang masing-masing memberikan kinerja yang berbeda seperti terlihat dalam Tabel 2. Demikian juga dengan katalis asam heterogen mempunyai fungsi dan karakteristik yang spesifik tergantung dari jenisnya seperti dapat dilihat dalam Tabel 3. Transesterifikasi katalis asam dilakukan dalam rangka mensintesis minyak yang mempunyai nilai FFA tinggi. Katalis asam seperti asam sulfat, asam phospat, asam klorida cocok untuk reaksi yang minyak mempunyai bilangan asam lemak bebas yang tinggi. Menyerupai sistem katalis enzimatis, reaksi katalis asam memerlukan waktu reaksi jauh lebih panjang dibanding reaksi katalis basa (Nelson et al., 1996; Watanabe et al., 2001, Canakci, M dan Gerpen, 2001; Linko et al., 1998). Proses transesterifikasi tidak banyak diterapkan dalam skala
produksi karena dianggap tidak ekonomis dan dianggap time consuming. Gambar 7. Mekanisme reaksi katalis asam (Schuchardt et al., 1998)
RCOOH + R’OH OOR’ + H2O ..………....[6]
H2SO4 2H+ + SO42- .………..…….………...…...,….[7]
OR
RCOOCR1 + H+ R1 C OH+ ...[8]
OR OR
R1 C OH+ + HOR’ R1 C OH + H+ ...[9]
OR OR’
R1 C OH R1COOR’ + HOR ...[10]
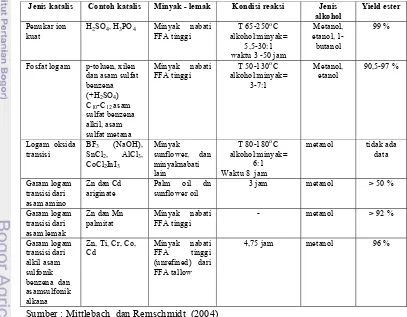
[image:48.612.133.512.110.387.2]22 Tabel 2. Karakteristik katalis asam homogen
Jenis katalis Contoh katalis
Minyak - lemak
Kondisi reaksi Jenis alkohol
Yield ester Asam
mineral
H2SO4, H3PO4 Minyak nabati
FFA tinggi
T 65-250o C alkohol:minyak=
5,5-30:1 waktu 3 -50 jam
Metanol, etanol, 1-butanol 99 % Asam alfatik dan sulfonik p-toluen, xilen dan asam sulfat benzena (+H2SO4)
C10-C12 asam
sulfat benzena alkil, asam sulfat metana
Minyak nabati FFA tinggi
T 50-130o C alkohol:minyak= 3-7:1 Metanol, aqu etanol 90,5-97 % Asam Lewis dan halogenida BF3 (NaOH), SnCl2, AlCl3, CoCl2InI3 Minyak sunflower, & minyak lain
T 80-180o C alkohol:minyak= 6:1, Waktu 8 jam
metanol tidak ada data
Sumber : Mittlebach dan Remschmidt (2004)
Tabel 3. Karakteristik katalis asam heterogen
Jenis katalis Contoh katalis Minyak - lemak Kondisi reaksi Jenis alkohol
Yield ester
Penukar ion kuat
H2SO4, H3PO4 Minyak nabati FFA tinggi
T 65-250o C alkohol:minyak=
5,5-30:1 waktu 3 -50 jam
Metanol, etanol, 1-butanol
99 %
Fosfat logam p-toluen, xilen dan asam sulfat benzena (+H2SO4) C10-C12 asam sulfat benzena alkil, asam sulfat metana Minyak nabati FFA tinggi
T 50-130o C alkohol:minyak= 3-7:1 Metanol, etanol 90,5-97 % Logam oksida transisi BF3 (NaOH), SnCl2, AlCl3, CoCl2InI3 Minyak sunflower, dan minyaknabati lain
T 80-180o C alkohol:minyak=
6:1 Waktu 8 jam
metanol tidak ada data
Garam logam transisi dari asam amino
Zn dan Cd ariginate
Palm oil dn sunflower oil
3 jam metanol > 50 %
Garam logam transisi dari asam lemak
Zn dan Mn palmitat
Minyak nabati FFA tinggi
- metanol > 92 %
Garam logam transisi dari alkil asam sulfonik benzena dan asamsulfonik alkana
Zn, Ti, Cr, Co, Cd
Minyak nabati FFA tinggi (unrefined) dari FFA tallow
4,75 jam metanol 96 %
23 2.2.2.3 Katalis Enzim
Katalis enzim memberikan kemampuan untuk : 1) penggunaan berulang-ulang hingga 50 kali tanpa kehilangan potensi katalitiknya, 2) penggunaan metanol yang sedikit. 3) katalis enzim bisa mengkonversi metil ester pada suhu, tekanan, dan pH sedang, 4) hasil reaksi memberikan proses purifikasi lebih mudah, 5) mutu gliserol yang tinggi sebagai by product, 6) menunjang pencegahan kerusakan lingkungan (mengurangi limbah cair), 7) dilakukan dalam satu tahap proses, dan 8) bisa mengolah feedstock dengan keasaman yang tinggi tanpa perlakuan awal (Choo dan Ong, 1986; Mittelbach, 1990; Nelson et al.,1996; Wu et al.,1999; Fukuda et al., 2001; Ban et al.,2001)
Kekurangannya terkait dengan waktu transesterifikasi yang lama, berlangsung pada pH tertentu, cocok dengan pelarut tertentu, dan kandungan air tertentu, harga katalis yang mahal, efisiensi reaksi rendah, enzim membutuhkan imobilisasi dan membutuhkan penambahan air (10 wt %) sehingga yield ester turun drastis, serta enzim mudah untuk non aktif dalam minyak (phospolipid), sehingga minyak nabati harus dilakukan degumming (Choo and Ong, 1986; Nelson et al.,1996; Wu et al.,1999; Fukuda et al., 2001; Ban et al.,2001)
24 Tabel 4. Perbandingan Metode katalis lipase dan alkali dalam pengolahan
biodiesel
Parameter Katalis basa Katalis lipase
Suhu reaksi 60 – 70 oC 30 – 40 oC
FFA dalam bahan saponified products metil ester
Air dalam bahan bereaksi tidak ada pengaruh
Hasil metil ester normal lebih tinggi
Recovery glyserol sulit mudah
Purifikasi metil ester berulang tidak ada
Biaya produksi murah relatif mahal
*)Sumber : (Fukuda et al., 2001)
2.2.2.4 Transesterifikasi non-Katalis
Transesterifikasi non-katalis merupakan salah satu metode pengolahan biodiesel dengan tujuan pengurangan waktu reaksi, peniadaan penggunaan katalis, purifikiasi yang lebih baik, dan meningkatkan mutu hasil proses biodiesel. Pada Tabel 5 disajikan perbandingan karakteristik pengolahan biodiesel dengan bantuan katalis dan non-katalis.
Tabel 5. Komparasi metode katalis dan non-katalis *)
Parameter Katalis Superkritik MeOH
Waktu reaksi 1 – 8 jam 120 – 240 detik
Kondisi reaksi tekanan 0,1 MPa, suhu 30 – 65 oC
Tekanan > 8.09 MPa suhu > 239.4 oC
Katalis basa atau asam tidak ada
FFA saponified products metil ester
Hasil (yield) normal lebih tinggi
Hasil purifikasi metanol, katalis dan saponified products
metanol
Proses bertahap sederhana
Konsumsi energi rendah tinggi
25 2.2.3 Kinetika Reaksi
2.2.3.1 Tumbukan (collisions)
Reaksi yang hanya melibatkan satu partikel mekanisme tumbukan berlangsung secara sederhana akan tetapi bila reaksi yang melibatkan tumbukan antara dua atau lebih partikel mekanisme reaksi menjadi lebih rumit. Reaksi yang melibatkan tumbukan antara dua partikel dapat bereaksi jika partikel-partikel melakukan kontak satu dengan yang lain. Partikel-partikel harus bertumbukan sehingga terjadi reaksi. Reaksi terjadi karena kedua partikel tersebut harus bertumbukan dengan mekanisme yang tepat, dan partikel-partikel harus bertumbukan dengan energi yang cukup untuk memutuskan ikatan-ikatan. Bila dikaitkan mekanisme tumbukan dalam proses transesterifikasi (biodiesel) antara trigliserida (TG) dan methanol (MeOH) maka dapat dijelaskan seperti dalam Gambar 8 di bawah ini.
Tumbukan terjadi antara tiga molekul CH3OH atau (3A) dan satu molekul
trigliserida (TG). Keduanya bereaksi untuk menghasilkan 3 molekul fatty acid methyl ester (FAME) dan 1 molekul gliserol (G). Sebagai hasil dari tumbukan
antara satu molekul TG dan tiga molekul methanol (MeOH) berubah menjadi tiga moleklul FAME dan satu molekul GL. Di dalam reaksi transesterifikasi, sebenarnya antara TG dan MeOH sukar sekali untuk bersatu (bereaksi) karena
26 kedua bahan tersebut mempunyai phase yang berbeda, di samping itu TG dan MeOH mempunyai sifat elektronegatifitas yang berbeda dan menyebabkan ikatan keduanya menimbulkan tolakan karena keduanya memiliki elektronegatifitas yang tinggi (Atkins, 1986)
Untuk menjadikan reaksi berlangsung dan mengarah ke sebelah kanan sehingga terbentuk 3 BE (biodiesel) maka diperlukan efek pengadukan yang sangat tinggi (vigorous stirring) yang salah satunya dipu