ANALISIS KANDUNGAN NATRIUM BENZOAT DAN KAFEIN
PADA MINUMAN ENERGI SECARA SIMULTAN DENGAN
METODE SPEKTROFOTOMETRI ULTRAVIOLET
SKRIPSI
OLEH:
FLORENCIA
NIM 101501020
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
ANALISIS KANDUNGAN NATRIUM BENZOAT DAN KAFEIN
PADA MINUMAN ENERGI SECARA SIMULTAN DENGAN
METODE SPEKTROFOTOMETRI ULTRAVIOLET
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
FLORENCIA
NIM 101501020
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
ANALISIS KANDUNGAN NATRIUM BENZOAT DAN KAFEIN
PADA MINUMAN ENERGI SECARA SIMULTAN DENGAN
METODE SPEKTROFOTOMETRI ULTRAVIOLET
OLEH:
FLORENCIA
NIM 101501020
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 14 Juli 2014
Pembimbing I, Panitia Penguji,
Prof. Dr. Siti Morin Sinaga, M.Sc., Apt. Prof. Dr. rer. nat. E. D. L. Putra, S.U., Apt.
NIP 195008281976032002 NIP 195306191983031001
Pembimbing II, Prof. Dr. Siti Morin Sinaga, M.Sc., Apt.
NIP 195008281976032002
Dr. Muchlisyam, M.Si., Apt. Drs. Maralaut Batubara, M.Phill., Apt.
NIP 195006221980021001 NIP 195101311976031003
Dra. Tuty Roida Pardede, M.Si., Apt. NIP 195401101980032001
Medan,
Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan
karunia yang berlimpah sehingga penulis dapat menyelesaikan penyusunan skripsi
yang berjudul Analisis Kandungan Natrium Benzoat dan Kafein pada Minuman
Energi Secara Simultan dengan Metode Spektrofotometri Ultraviolet. Skripsi ini
diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di
Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada Bapak Prof. Dr. Sumadio
Hadisahputra, Apt., selaku Dekan Fakultas Farmasi yang telah menyediakan
fasilitas kepada penulis selama perkuliahan di Fakultas Farmasi. Penulis juga
mengucapkan terima kasih kepada Ibu Prof. Dr. Siti Morin Sinaga, M.Sc., Apt.,
dan Bapak Dr. Muchlisyam, M.Si., Apt., yang telah meluangkan waktu dan tenaga
dalam membimbing penulis dengan penuh kesabaran dan tanggung jawab,
memberikan petunjuk dan saran-saran selama penelitian hingga selesainya skripsi
ini. Ucapan terima kasih juga penulis hanturkan kepada Bapak Prof. Dr. rer. nat.
Effendy De Lux Putra, S.U., Apt., selaku ketua penguji, Bapak Drs. Maralaut
Batubara, M.Phill., Apt., dan Ibu Dra. Tuty Roida Pardede, M.Si., Apt., selaku
anggota penguji yang telah memberikan saran untuk menyempurnakan skripsi ini,
dan juga kepada Bapak Dr. Kasmirul Ramlan Sinaga, M.S., Apt., selaku dosen
penasehat akademik yang tidak pernah lelah untuk memberikan arahan dan
semangat kepada penulis dari awal perkuliahan hingga selesai serta Bapak dan Ibu
staf pengajar Fakultas Farmasi USU yang telah banyak membimbing penulis
Penulis juga mempersembahkan rasa terima kasih yang tak terhingga
kepada keluarga tercinta, Papa Herman Hanitio dan Mama Ani, Adikku Kevin,
Jessica, Edward dan Felicia atas limpahan kasih sayang, doa, dan dukungan yang
tak ternilai dengan apapun. Penulis juga mengucapkan terima kasih kepada
sahabat terdekat, Anddora Michi, Felicia Christine, Hendrik, Jimmy Angga
Winata, Maya Octavia, Mita Joselin, Novita Sari yang telah banyak membantu
penulis selama masa perkuliahan dan memberikan masukan hingga selesainya
skripsi ini serta teman-teman mahasiswa/i Farmasi Stambuk 2010 yang selalu
mendoakan dan memberi dukungan serta semangat yang tiada henti.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum
sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang
membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga
skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, Juli 2014
Penulis,
Florencia
ANALISIS KANDUNGAN NATRIUM BENZOAT DAN KAFEIN
PADA MINUMAN ENERGI SECARA SIMULTAN DENGAN
METODE SPEKTROFOTOMETRI ULTRAVIOLET
ABSTRAK
Minuman energi adalah minuman yang mengandung satu atau lebih bahan yang mudah dan cepat diserap oleh tubuh untuk menghasilkan energi, salah satu zat yang ditambahkan adalah kafein, dan pengawet yang sering digunakan yaitu asam benzoat biasanya terdapat dalam bentuk natrium benzoat. Tujuan dari penelitian ini adalah untuk uji validasi metode spektrofotometri ultraviolet pada penetapan kadar natrium benzoat dan kafein secara simultan dengan metode perhitungan persamaan regresi.
Metode penelitian ini dilakukan dengan metode spektrofotometri ultraviolet menggunakan perhitungan persamaan regresi yang diukur absorbansinya pada panjang gelombang asam benzoat 229 nm dan kafein 272 nm. Penelitian ini terlebih dahulu dilakukan dengan penetapan kadar baku asam benzoat dan kafein, selanjutnya dilakukan analisis kandungan natrium benzoat dan kafein secara simultan pada minuman energi.
Hasil penelitian menunjukkan bahwa kandungan natrium benzoat pada minuman energi yaitu sebesar (494,6513 ± 17,1173); (266,8128 ± 6,6828); (242,6389 ± 4,0538); (223,8319 ± 2,3345); (374,1924 ± 5,7813); (266,1196 ±
8,8433) mg/kg untuk sampel A, B, C, D, E, F dan kandungan kafein yaitu sebesar (48,7618 ± 0,5964); (46,6278 ± 0,3529); (45,5494 ± 1,1778); (47,9144
± 0,6550); (45,9813 ± 1,4295); (47,9624 ± 0,8852) mg/sajian untuk sampel A, B, C, D, E, F. Hal ini menunjukkan bahwa kandungan natrium benzoat dan kafein dalam minuman energi yang dianalisis memenuhi persyaratan kandungan yang tercantum dalam SNI 01-6684-2002 tentang minuman energi (natrium benzoat tidak lebih dari 600 mg/kg dan kafein tidak lebih dari 50 mg/sajian). Namun hasil ini bukan merupakan kandungan natrium benzoat dan kafein yang sebenarnya tetapi kandungan total beserta bahan-bahan lain dalam sampel yang memberikan serapan pada panjang gelombang maksimum yang digunakan misalnya vitamin B5, sakarin, vitamin B1, nikotinamid, vitamin B2, vitamin B12 dan vitamin B6.
ANALYSIS OF SODIUM BENZOATE AND CAFFEINE IN
ENERGY DRINK SIMULTANEOUSLY WITH
SPECTROPHOTOMETRY ULTRAVIOLET
ABSTRACT
Energy drinks are beverages that contain one or more materials that are easily and quickly absorbed by the body to produce energy, one of the added substance is caffeine, and preservative that is often used is benzoic acid which usually found in the form of sodium benzoate. The purpose of this study was to test the spectrophotometry ultraviolet method validation in the determination of sodium benzoate and caffeine simultaneously with regression equation as the calculation method.
This study method is doned by ultraviolet spectrophotometry using calculation of regression equation that measured at a wavelength of benzoic acid 229 nm and caffeine 272 nm. Firstly, this study conducted by assay of benzoic acid and caffeine, then we do content analysis of sodium benzoate and caffeine simultaneously in energy drinks.
The content of sodium benzoate in energy drinks that were analyzed are (494.6513 ± 17.1173); (266.8128 ± 6.6828); (242.6389 ± 4.0538); (223.8319 ±
2.3345); (374.1924 ± 5.7813); (266.1196 ± 8.8433) mg/kg for sample A, B, C, D, E, F and the content of caffeine are (48.7618 ± 0.5964); (46.6278 ± 0.3529); (45.5494 ± 1.1778); (47.9144 ± 0.6550); (45.9813 ± 1.4295); (47.9624
± 0.8852) mg/serving for sample A, B, C, D, E, F. This result indicate that the content of sodium benzoate and caffeine meet the requirements listed in the SNI 01-6684-2002 on energy drinks (sodium benzoate not more than 600 mg/kg and caffeine not more than 50 mg/serving). However, these results are not the actual content of sodium benzoate and caffeine but the total content along with other substances in the sample that gives absorption at the maximum wavelength used for example vitamin B5, saccharine, vitamin B1, nicotinamide, vitamin B2, vitamin B12 and vitamin B6.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Minuman Energi ... 5
2.2 Bahan Tambahan Pangan ... 6
2.2.1 Bahan pengawet ... 6
2.3 Natrium Benzoat ... 7
2.5 Spektrofotometri Ultraviolet ... 9
2.5.1 Hukum Lambert-Beer ... 10
2.5.2 Kegunaan spektrofotometri ultraviolet ... 11
2.6 Validasi Metode ... 15
BAB III METODE PENELITIAN ... 18
3.1 Tempat dan Waktu Penelitian ... 18
3.2 Bahan-bahan ... 18
3.2.1 Pereaksi ... 18
3.3 Alat-alat ... 18
3.4 Pembuatan Pereaksi ... 18
3.4.1 Larutan HCl 0,1 N ... 18
3.5 Pengambilan Sampel ... 19
3.6 Pembuatan Larutan Induk Baku ... 19
3.6.1 Pembuatan larutan induk baku asam benzoat ... 19
3.6.2 Pembuatan larutan induk baku kafein ... 20
3.7 Penentuan Panjang Gelombang Maksimum ... 20
3.7.1 Penentuan panjang gelombang maksimum asam benzoat ... 20
3.7.2 Penentuan panjang gelombang maksimum kafein ... 20
3.8 Pembuatan Kurva Serapan Tumpang Tindih Asam Benzoat dan Kafein (1 : 1) ... 21
3.9 Pembuatan Kurva Kalibrasi ... 21
3.9.1 Pembuatan kurva kalibrasi asam benzoat ... 21
3.9.2 Pembuatan kurva kalibrasi kafein ... 21
3.11 Penetapan Kadar Natrium Benzoat dan Kafein dalam
Sampel ... 22
3.11.1 Penetapan kadar natrium benzoat dan kafein dalam sampel A ... 22
3.11.2 Penetapan kadar natrium benzoat dan kafein dalam sampel B ... 23
3.11.3 Penetapan kadar natrium benzoat dan kafein dalam sampel C ... 23
3.11.4 Penetapan kadar natrium benzoat dan kafein dalam sampel D ... 23
3.11.5 Penetapan kadar natrium benzoat dan kafein dalam sampel E ... 23
3.11.6 Penetapan kadar natrium benzoat dan kafein dalam sampel F ... 24
3.12 Analisis Data Secara Statistik ... 24
3.13 Validasi Metode ... 25
3.13.1 Uji perolehan kembali (recovery) ... 25
3.13.2 Simpangan baku relatif ... 26
3.13.3 Penentuan batas deteksi (Limit of Detection) dan batas kuantitasi (Limit of Quantitation) ... 27
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Penentuan Panjang Gelombang Maksimum ... 28
4.2 Pembuatan Kurva Serapan Tumpang tindih Asam Benzoat dan Kafein (1 : 1) ... 29
4.3 Kurva Kalibrasi ... 30
4.3.1 Kurva kalibrasi asam benzoat ... 30
4.3.2 Kurva kalibrasi kafein
... 31
4.5 Penetapan Kadar Natrium Benzoat dan Kafein dalam
Sampel ... 33
4.6 Validasi Metode Analisis ... 35
4.6.1 Uji perolehan kembali (recovery) ... 35
4.6.2 Simpangan baku relatif ... 36
4.6.3 Batas deteksi dan batas kuantitasi ... 36
BAB V KESIMPULAN DAN SARAN ... 38
5.1 Kesimpulan ... 38
5.2 Saran ... 39
DAFTAR PUSTAKA ... 40
DAFTAR TABEL
Halaman
Tabel 1. Kandungan Natrium Benzoat dan Kafein pada Minuman
Energi ... 33
Tabel 2. Persen Perolehan Kembali (recovery) Asam Benzoat dan
DAFTAR GAMBAR
Halaman
Gambar 1. Spektrum Absorpsi Senyawa X dan Y (Tidak terjadi tumpang tindih pada kedua panjang gelombang yang
digunakan) ... 13
Gambar 2. Spektrum Absorpsi Senyawa X dan Y (Tumpang tindih satu arah; X dapat diukur tanpa gangguan Y, tetapi X
mengganggu pada pengukuran langsung Y) 14
Gambar 3. Spektrum Absorpsi Senyawa X dan Y (Tumpang tindih dua arah. Tidak ada panjang gelombang dimana masing-masing senyawa dapat diukur tanpa mengalami gangguan oleh yang lainnya) ... 14
Gambar 4. Kurva Serapan Baku Pembanding Asam Benzoat, Konsentrasi 5 µg/ml dalam Larutan HCl 0,1 N. Panjang
Gelombang Maksimum 229 nm ... 28
Gambar 5. Kurva Serapan Baku Pembanding Kafein, Konsentrasi 9 µg/ml dalam Larutan HCl 0,1 N. Panjang Gelombang
Maksimum 272 nm ... 29
Gambar 6. Kurva Serapan Tumpang Tindih Baku Pembanding
Asam Benzoat dan Kafein (1 : 1) ... 30
Gambar 7. Kurva Kalibrasi Asam Benzoat pada Panjang Gelombang 229 nm dan 272
nm ...
31 Gambar 8. Kurva Kalibrasi Kafeinpada
Panjang Gelombang 229nm dan 272 nm
...
32DAFTAR LAMPIRAN
Halaman
Lampiran 1. Komposisi Sampel Minuman Energi ... 43
Lampiran 2. Panjang Gelombang Maksimum Bahan-bahan dalam
Sampel Minuman Energi ... 44
Lampiran 3. Perhitungan Konsentrasi Pengukuran Asam Benzoat ... 45
Lampiran 4. Perhitungan Konsentrasi Pengukuran Kafein ... 46
Lampiran 5. Data Kalibrasi Asam Benzoat pada Panjang
Gelombang 229 nm dengan Spektrofotometri
Ultraviolet, Perhitungan Persamaan Garis Regresi dan
Koefisien Korelasi (r) ... 47
Lampiran 6. Data Kalibrasi Asam Benzoat pada Panjang Gelombang 272 nm dengan Spektrofotometri Ultraviolet, Perhitungan Persamaan Garis Regresi dan
Koefisien Korelasi (r) ... 49
Lampiran 7. Data Kalibrasi Kafein pada Panjang Gelombang 229 nm dengan Spektrofotometri Ultraviolet, Perhitungan
Persamaan Garis Regresi dan Koefisien Korelasi (r) .... 51
Lampiran 8. Data Kalibrasi Kafein pada Panjang Gelombang 272 nm dengan Spektrofotometri Ultraviolet, Perhitungan
Persamaan Garis Regresi dan Koefisien Korelasi (r) .... 53
Lampiran 9. Hasil Analisis Kadar Baku Asam Benzoat dan Kafein
Secara Simultan ... 55
Lampiran 10. Contoh Perhitungan Kadar Baku Asam Benzoat dan
Kafein ... 56
Lampiran 11. Hasil Analisis Kadar Natrium Benzoat dan Kafein
dalam Sampel ... 58
Lampiran 12. Contoh Perhitungan Kadar Natrium Benzoat dan
Kafein dalam Sampel A ... 60
Lampiran 13. Contoh Perhitungan Kadar Natrium Benzoat dan
Kafein dalam Sampel B ... 63
Lampiran 14. Contoh Perhitungan Kadar Natrium Benzoat dan
Lampiran 15. Contoh Perhitungan Kadar Natrium Benzoat dan
Kafein dalam Sampel D ... 69
Lampiran 16. Contoh Perhitungan Kadar Natrium Benzoat dan Kafein dalam Sampel E ... 72
Lampiran 17. Contoh Perhitungan Kadar Natrium Benzoat dan Kafein dalam Sampel F ... 75
Lampiran 18. Perhitungan Statistik Kadar Natrium Benzoat dan Kafein dalam Sampel A ... 78
Lampiran 19. Perhitungan Statistik Kadar Natrium Benzoat dan Kafein dalam Sampel B ... 82
Lampiran 20. Perhitungan Statistik Kadar Natrium Benzoat dan Kafein dalam Sampel C ... 86
Lampiran 21. Perhitungan Statistik Kadar Natrium Benzoat dan Kafein dalam Sampel D ... 90
Lampiran 22. Perhitungan Statistik Kadar Natrium Benzoat dan Kafein dalam Sampel E ... 94
Lampiran 23. Perhitungan Statistik Kadar Natrium Benzoat dan Kafein dalam Sampel F ... 98
Lampiran 24. Hasil Uji Perolehan Kembali Asam Benzoat dan Kafein Setelah Penambahan Masing-masing Larutan Standar pada Sampel ... 102
Lampiran 25. Contoh Perhitungan Uji Perolehan Kembali Asam Benzoat dan Kafein pada Sampel ... 103
Lampiran 26. Perhitungan Simpangan Baku Relatif (RSD) Kadar Asam Benzoat dan Kafein pada Sampel ... 107
Lampiran 27. Perhitungan Batas Deteksi dan Batas Kuantitasi ... 109
Lampiran 28. Daftar Nilai Distribusi t ... 113
Lampiran 29. Sertifikat Baku Natrium Benzoat ... 114
Lampiran 30. Sertifikat Baku Kafein ... 115
ANALISIS KANDUNGAN NATRIUM BENZOAT DAN KAFEIN
PADA MINUMAN ENERGI SECARA SIMULTAN DENGAN
METODE SPEKTROFOTOMETRI ULTRAVIOLET
ABSTRAK
Minuman energi adalah minuman yang mengandung satu atau lebih bahan yang mudah dan cepat diserap oleh tubuh untuk menghasilkan energi, salah satu zat yang ditambahkan adalah kafein, dan pengawet yang sering digunakan yaitu asam benzoat biasanya terdapat dalam bentuk natrium benzoat. Tujuan dari penelitian ini adalah untuk uji validasi metode spektrofotometri ultraviolet pada penetapan kadar natrium benzoat dan kafein secara simultan dengan metode perhitungan persamaan regresi.
Metode penelitian ini dilakukan dengan metode spektrofotometri ultraviolet menggunakan perhitungan persamaan regresi yang diukur absorbansinya pada panjang gelombang asam benzoat 229 nm dan kafein 272 nm. Penelitian ini terlebih dahulu dilakukan dengan penetapan kadar baku asam benzoat dan kafein, selanjutnya dilakukan analisis kandungan natrium benzoat dan kafein secara simultan pada minuman energi.
Hasil penelitian menunjukkan bahwa kandungan natrium benzoat pada minuman energi yaitu sebesar (494,6513 ± 17,1173); (266,8128 ± 6,6828); (242,6389 ± 4,0538); (223,8319 ± 2,3345); (374,1924 ± 5,7813); (266,1196 ±
8,8433) mg/kg untuk sampel A, B, C, D, E, F dan kandungan kafein yaitu sebesar (48,7618 ± 0,5964); (46,6278 ± 0,3529); (45,5494 ± 1,1778); (47,9144
± 0,6550); (45,9813 ± 1,4295); (47,9624 ± 0,8852) mg/sajian untuk sampel A, B, C, D, E, F. Hal ini menunjukkan bahwa kandungan natrium benzoat dan kafein dalam minuman energi yang dianalisis memenuhi persyaratan kandungan yang tercantum dalam SNI 01-6684-2002 tentang minuman energi (natrium benzoat tidak lebih dari 600 mg/kg dan kafein tidak lebih dari 50 mg/sajian). Namun hasil ini bukan merupakan kandungan natrium benzoat dan kafein yang sebenarnya tetapi kandungan total beserta bahan-bahan lain dalam sampel yang memberikan serapan pada panjang gelombang maksimum yang digunakan misalnya vitamin B5, sakarin, vitamin B1, nikotinamid, vitamin B2, vitamin B12 dan vitamin B6.
ANALYSIS OF SODIUM BENZOATE AND CAFFEINE IN
ENERGY DRINK SIMULTANEOUSLY WITH
SPECTROPHOTOMETRY ULTRAVIOLET
ABSTRACT
Energy drinks are beverages that contain one or more materials that are easily and quickly absorbed by the body to produce energy, one of the added substance is caffeine, and preservative that is often used is benzoic acid which usually found in the form of sodium benzoate. The purpose of this study was to test the spectrophotometry ultraviolet method validation in the determination of sodium benzoate and caffeine simultaneously with regression equation as the calculation method.
This study method is doned by ultraviolet spectrophotometry using calculation of regression equation that measured at a wavelength of benzoic acid 229 nm and caffeine 272 nm. Firstly, this study conducted by assay of benzoic acid and caffeine, then we do content analysis of sodium benzoate and caffeine simultaneously in energy drinks.
The content of sodium benzoate in energy drinks that were analyzed are (494.6513 ± 17.1173); (266.8128 ± 6.6828); (242.6389 ± 4.0538); (223.8319 ±
2.3345); (374.1924 ± 5.7813); (266.1196 ± 8.8433) mg/kg for sample A, B, C, D, E, F and the content of caffeine are (48.7618 ± 0.5964); (46.6278 ± 0.3529); (45.5494 ± 1.1778); (47.9144 ± 0.6550); (45.9813 ± 1.4295); (47.9624
± 0.8852) mg/serving for sample A, B, C, D, E, F. This result indicate that the content of sodium benzoate and caffeine meet the requirements listed in the SNI 01-6684-2002 on energy drinks (sodium benzoate not more than 600 mg/kg and caffeine not more than 50 mg/serving). However, these results are not the actual content of sodium benzoate and caffeine but the total content along with other substances in the sample that gives absorption at the maximum wavelength used for example vitamin B5, saccharine, vitamin B1, nicotinamide, vitamin B2, vitamin B12 and vitamin B6.
BAB I
PENDAHULUAN
1.1Latar Belakang
Minuman energi adalah minuman yang mengandung satu atau lebih bahan
yang mudah dan cepat diserap oleh tubuh untuk menghasilkan energi dengan atau
tanpa bahan tambahan makanan yang diizinkan (BSN, 2002). Minuman energi
sering digunakan oleh para remaja, dewasa, dan populasi yang aktif secara fisik.
Minuman ini dipasarkan sebagai alternatif alami yang meningkatkan kinerja fisik
dan kognitif seperti konsentrasi, perhatian, dan kewaspadaan. Bahan aktif utama
dalam minuman energi adalah kafein, meskipun juga terdapat zat lain seperti
taurin, karbohidrat, riboflavin, piridoksin, dan berbagai herbal seperti ginseng
(Mubarak, 2012).
Pengawet adalah bahan tambahan makanan yang mencegah atau
menghambat fermentasi, pengasaman atau peruraian lain terhadap makanan yang
disebabkan oleh mikroorganisme (BSN, 1995). Dengan penambahan pengawet
tersebut, produk minuman diharapkan dapat terpelihara kesegarannya. Asam
benzoat merupakan pengawet yang sering digunakan salah satunya pada minuman
energi, yang umumnya terdapat dalam bentuk garamnya yaitu natrium benzoat
yang bersifat lebih mudah larut (Cahyadi, 2008).
Berdasarkan SNI 01-6684-2002 tentang minuman energi, batas
penggunaan kafein pada minuman energi yaitu 50 mg/sajian (BSN, 2002) dan
batas penggunaan natrium benzoat pada minuman energi yaitu 600 mg/kg (BSN,
Penetapan kadar natrium benzoat dan kafein masing-masing dapat
dilakukan secara titrasi dan spektrofotometri ultraviolet. Pada penetapan kadar
secara spektrofotometri ultraviolet, kadar baku natrium benzoat dan kafein
mempunyai profil kurva serapan tumpang tindih sehingga serapan yang diperoleh
merupakan jumlah serapan dari kedua komponen tersebut. Salah satu upaya untuk
memperoleh kadar masing-masing zat tersebut adalah dengan metode
spektrofotometri ultraviolet secara simultan, tetapi pada penetapan kadar natrium
benzoat dan kafein pada minuman energi dengan metode spektrofotometri
ultraviolet secara simultan, metode perhitungan persamaan multikomponen dan
matriks tidak dapat dilakukan karena tidak diketahui komposisi natrium benzoat
dan kafein tersebut sehingga digunakan metode perhitungan persamaan regresi
(Sari, dkk., 2013).
Metode Spektrofotometri memiliki beberapa keuntungan antara lain
kepekaan yang tinggi, ketelitian yang baik, mudah dilakukan, cepat pengerjaannya
dan dapat digunakan untuk menentukan senyawa campuran (Munson, 1991).
Untuk menguji validasi metode, dilakukan uji akurasi (ketepatan) dengan
parameter persen perolehan kembali dengan metode penambahan baku (standard
addition method) dan uji presisi (ketelitian) dengan parameter Relative Standard
Deviation (RSD) (Harmita, 2004).
Berdasarkan uraian di atas maka penulis tertarik untuk menetapkan kadar
natrium benzoat dan kafein secara simultan pada minuman energi dengan metode
1.2Perumusan Masalah
1. Apakah campuran natrium benzoat dan kafein dapat dianalisis dengan
metode spektrofotometri ultraviolet secara simultan menggunakan metode
perhitungan persamaan regresi?
2. Apakah kandungan natrium benzoat dan kafein dalam minuman energi
sesuai dengan standar yang ditetapkan oleh SNI 01-6684-2002 tentang
minuman energi?
1.3Hipotesis
1. Dapat dilakukan analisis campuran natrium benzoat dan kafein dengan
metode spektrofotometri ultraviolet secara simultan menggunakan metode
perhitungan persamaan regresi.
2. Kandungan natrium benzoat dan kafein dalam minuman energi sesuai
dengan standar yang ditetapkan oleh SNI 01-6684-2002 tentang minuman
energi.
1.4Tujuan Penelitian
1. Untuk menetapkan kadar campuran natrium benzoat dan kafein dengan
metode spektrofotometri ultraviolet secara simultan menggunakan metode
perhitungan persamaan regresi.
2. Untuk mengetahui kesesuaian kandungan natrium benzoat dan kafein
dalam minuman energi dengan standar yang ditetapkan oleh SNI
1.5Manfaat Penelitian
Untuk mengetahui kadar natrium benzoat dan kafein pada minuman energi
agar dapat dimanfaatkan sebagai salah satu informasi bagi masyarakat dalam
BAB II
TINJAUAN PUSTAKA
2.1 Minuman Energi
Minuman energi adalah minuman ringan non-alkohol yang dirancang
untuk memberikan konsumen energi. Minuman energi lebih populer dari
sebelumnya dan tampaknya akan semakin besar setiap tahun. Minuman energi
sering digunakan oleh para remaja, dewasa, dan populasi yang aktif secara fisik.
Minuman ini dipasarkan sebagai alternatif alami yang meningkatkan kinerja fisik
dan kognitif seperti konsentrasi, perhatian, dan kewaspadaan (Mubarak, 2012).
Bahan utama dalam kebanyakan minuman energi adalah kafein, yang dilengkapi
dengan berbagai macam asam amino, vitamin B, dan suplemen herbal (Babu,
dkk., 2008).
Pada dasarnya setiap orang memerlukan suplai energi yang cukup untuk
dapat melakukan aktivitas sehari-hari. Energi ini dapat diperoleh dari makanan
atau suplemen. Suplemen mempunyai batasan istilah yaitu produk yang
digunakan untuk melengkapi kebutuhan zat gizi makanan. Beberapa suplemen
makanan berperan dalam menyuplai energi dan menjadi salah satu alternatif
apabila dari konsumsi pangan tidak mencukupi. Hal ini dapat dilihat dengan
banyaknya orang yang lebih suka mengambil cara cepat untuk memperoleh energi
dengan minuman energi (energy drink). Bahkan, banyak yang mengkonsumsi
minuman energi setiap hari karena beranggapan minuman energi sebagai sumber
tenaga tambahan yang siap untuk digunakan tubuh untuk melakukan aktivitas
2.2 Bahan Tambahan Pangan
2.2.1 Bahan pengawet
Pengawet adalah bahan tambahan makanan yang mencegah atau
menghambat fermentasi, pengasaman atau peruraian lain terhadap makanan yang
disebabkan oleh mikroorganisme (BSN, 1995). Pemakaian bahan pengawet
menguntungkan karena dengan bahan pengawet, bahan pangan dapat dibebaskan
dari kehidupan mikroba, baik yang bersifat patogen yang dapat menyebabkan
keracunan atau gangguan kesehatan lainnya maupun mikrobial yang nonpatogen
yang dapat menyebabkan kerusakan bahan pangan, misalnya pembusukan. Zat
pengawet terdiri dari senyawa organik dan anorganik dalam bentuk asam dan
garamnya (Cahyadi, 2008).
Zat pengawet organik lebih banyak dipakai daripada yang anorganik
karena bahan ini lebih mudah larut. Bahan organik digunakan baik dalam bentuk
asam maupun dalam bentuk garamnya. Zat kimia yang sering digunakan sebagai
bahan pengawet adalah asam sorbat, asam propionat, asam benzoat, asam asetat
dan epoksida (Cahyadi, 2008).
Zat pengawet anorganik yang masih sering dipakai adalah sulfit, hidrogen
peroksida, nitrat dan nitrit. Sulfit digunakan dalam bentuk gas SO2, garam Na atau
K sulfit, bisulfit dan metabisulfit. Garam nitrat dan nitrit umumnya digunakan
pada proses curing daging untuk memperoleh warna yang baik dan mencegah
pertumbuhan mikroba. Selain digunakan pada produk daging, nitrat dan nitrit juga
2.3 Natrium Benzoat
Menurut Ditjen POM (1995), sifat fisikokimia natrium benzoat adalah
sebgai berikut:
Rumus struktur :
Rumus Molekul : C7H5NaO2
Berat Molekul : 144,11
Nama Kimia : Natrium benzoat
Kandungan : Tidak kurang dari 99,0% dan tidak lebih dari
100,50% C7H5NaO2, dihitung terhadap zat anhidrat.
Pemerian : Granul atau serbuk hablur, putih; tidak berbau atau
praktis tidak berbau; stabil di udara.
Kelarutan : Mudah larut dalam air, agak sukar larut dalam
etanol dan lebih mudah larut dalam etanol 90%.
Aktivitas asam benzoat dan garamnya sebagai anti mikroorganisme
tergantung pada pH, karena pH sangat menentukan jumlah asam yang terdisosiasi.
Pada pH 2,19 asam yang tidak terdisosiasi adalah 99%, pada pH 4,2 asam yang
tidak terdisosiasi adalah 50%. Natrium benzoat sebagai antimikroorganisme
berperan dalam menganggu permeabilitas membran sel (Afrianti, 2010), yaitu
dengan menganggu atau menghalangi jalannya nutrien masuk ke dalam sel dan
kebutuhan sel tidak dapat terpenuhi dengan baik. Asam benzoat dan garamnya
relatif kurang efektif sebagai bahan pengawet pada pH lebih besar, tetapi kerjanya
sebagai pengawet akan naik dengan turunnya pH sampai di bawah pH 5 (Cahyadi,
2008).
2.4 Kafein
Menurut Ditjen POM (1995), sifat fisikokimia kafein adalah sebagai
berikut:
Rumus struktur :
Rumus Molekul : C8H10N4O2
Berat Molekul : 194,19
Nama Kimia : 1,3,7-Trimetil xantin
Kandungan : Tidak kurang dari 98,5% dan tidak lebih dari
101,0% C8H10N4O2, dihitung terhadap zat anhidrat.
Pemerian : Serbuk putih atau bentuk jarum mengkilat putih;
biasanya menggumpal; tidak berbau; rasa pahit.
Kelarutan : Agak sukar larut dalam air, dalam etanol; mudah
larut dalam kloroform; sukar larut dalam eter.
Kafein merupakan perangsang sistem saraf pusat yang kuat. Orang yang
pikirnya lebih cepat dan lebih jernih (Louisa dan Dewoto, 2009). Kafein
merupakan antagonis kompetitif reseptor adenosin di otak. Telah diketahui bahwa
adenosin jika terikat ke reseptor sel saraf akan menurunkan aktivitas sel saraf.
Akibat kemiripan struktur molekul kafein dengan struktur adenosin maka kafein
dapat terikat pada reseptor tersebut tetapi tidak memberi efek penurunan aktivitas
sel saraf justru sebaliknya, aktivitas sel saraf ditingkatkan. Jika kondisi ini terus
berlangsung, akan terjadi beberapa efek, seperti denyut jantung, tekanan darah,
dan aliran darah ke otot ningkat, sementara itu aliran darah kekulit dan organ
dalaman akan menurun, tetapi pelepasan glukosa oleh hati meningkat
(Dalimunthe, 2009).
2.5 Spektrofotometri Ultraviolet
Spektrofotometer ultraviolet adalah alat yang digunakan dalam
pengukuran panjang gelombang dan intensitas sinar ultraviolet yang diabsorpsi
oleh sampel. Sinar ultraviolet memiliki energi yang cukup untuk mempromosikan
elektron pada kulit terluar ke tingkat energi yang lebih tinggi (Dachriyanus, 2004).
Radiasi ultraviolet diabsorpsi oleh molekul organik, molekul yang mengandung
elektron-π terkonjugasi dan/ atau atom yang mengandung elektron-n,
menyebabkan transisi elektron di orbit terluarnya dan tingkat energi elektron dasar
ke tingkat energi tereksitasi lebih tinggi (Satiadarma, dkk., 2004).
Bagian molekul yang bertanggung jawab terhadap penyerapan cahaya
disebut kromofor dan terdiri atas ikatan rangkap dua atau rangkap tiga, terutama
jika ikatan rangkap tersebut terkonjugasi. Semakin panjang ikatan rangkap dua
mudah menyerap cahaya (Cairns, 2009). Pada molekul organik dikenal pula
istilah auksokrom yang merupakan gugus fungsional yang mempunyai elektron
bebas, seperti: –OH, –O, –NH2 dan –OCH3, yang memberikan transisi n→ π*.
Terikatnya gugus auksokrom pada gugus kromofor akan mengakibatkan
pergeseran pita absorpsi menuju ke panjang gelombang yang lebih besar
(pergeseran merah atau pergeseran batokromik) disertai dengan peningkatan
intensitas (efek hiperkromik) (Gandjar dan Rohman, 2008).
2.5.1 Hukum Lambert-Beer
Hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh
larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan
(Gandjar dan Rohman, 2008). Menurut Denney dan Sinclair (1991), dalam hukum
Lambert-Beer terdapat beberapa pembatasan, yaitu:
1. Larutan yang menyerap cahaya adalah campuran yang homogen
2. Menggunakan sinar monokromatis
3. Rendahnya konsentrasi dari senyawa yang menyerap cahaya.
Menurt Gandjar dan Rohman (2008), hukum Lambert-Beer umumnya
dikenal dengan persamaan sebagai berikut:
A = abc
Dimana: A = absorbansi
a = absorptivitas
b = tebal kuvet (cm)
c = konsentrasi
Absorptivitas (a) merupakan satu konstanta yang tidak tergantung pada tebal
tergantung pada suhu, pelarut, struktur molekul dan panjang gelombang radiasi.
Satuan a ditentukan oleh satuan b dan c.
2.5.2 Kegunaan spektrofotometri ultraviolet
Menurut Dachriyanus (2004),pada umumnya spektrofotometri ultraviolet
dalam analisis senyawa organik digunakan untuk:
1. Menjelaskan struktur berdasarkan panjang gelombang maksimum suatu
senyawa
2. Mampu menganalisis senyawa organik secara kuantitatif dengan
menggunakan hukum Lambert-Beer.
Kegunaan spektrofotometri ultraviolet dalam analisis kualitatif sangat
terbatas karena rentang daerah radiasi yang relatif sempit hanya dapat
mengakomodasi sedikit sekali puncak absorpsi maksimum dan minimum, karena
itu identifikasi senyawa yang tidak diketahui tidak memungkinkan untuk
dilakukan (Satiadarma, dkk., 2004). Akan tetapi, jika digabung dengan cara lain
seperti spektroskopi inframerah, resonansi magnet inti dan spektroskopi massa,
maka dapat digunakan untuk identifikasi atau analisis kualitatif senyawa tersebut
(Gandjar dan Rohman, 2008).
Penggunaan utama spektrofotometri ultraviolet adalah dalam analisis
kuantitatif. Apabila dalam alur radiasi spektrofotometer terdapat senyawa yang
mengabsorpsi radiasi, maka akan terjadi pengurangan kekuatan radiasi yang
mencapai detektor. Parameter kekuatan energi radiasi khas yang diabsorpsi oleh
molekul adalah absorbansi (A) yang dalam batas konsentrasi rendah nilainya
sebanding dengan banyaknya molekul yang mengabsorbapsi radiasi dan
mempunyai struktur kromofor atau mengandung gugus kromofor, serta
mengabsorpsi radiasi ultraviolet, penggunaannya cukup luas (Satiadarma, dkk.,
2004).
Analisis kuantitatif dengan metode spektrofotometri ultraviolet dapat
digolongkan menjadi analisis zat tunggal atau analisis satu komponen dan analisis
kuantitatif dua macam zat atau lebih (analisis multikomponen):
1. Analisis kuantitatif zat tunggal (analisis satu komponen)
Terdapat dua metode penggunaan pengukuran spektrofotometri dalam
analisis senyawa, yaitu metode penetapan kadar absolut dan komparatif.
Metode penetapan kadar komparatif lebih disukai. Pada jenis penetapan kadar
ini, larutan standar obat yang akan dianalisis disiapkan, serapan sampel dan
standar ditentukan pada kondisi yang sama (Cairns, 2009). Menurut Holme
dan Peck (1983), konsentrasi sampel dihitung dengan rumus sebagai berikut:
As At =
Cs Ct
Keterangan: As = Absorbansi baku pembanding
At = Absorbansi sampel
Cs = Konsentrasi baku pembanding
Ct = Konsentrasi sampel
2. Analisis kuantitatif dua macam zat atau lebih (analisis multikomponen)
Analisis kuantitatif dua macam zat atau lebih bahkan kadang-kadang
ditentukan secara simultan dalam sekali pengamatan tanpa dipisahkan. Hal ini
didasarkan pada asumsi bahwa absorbansi total dari campuran komponen
merupakan jumlah serapan masing-masing komponen tersebut (Day dan
Menurut Day dan Underwood (2002), ada tiga kemungkinan analisis
campuran dua komponen atau lebih, yaitu:
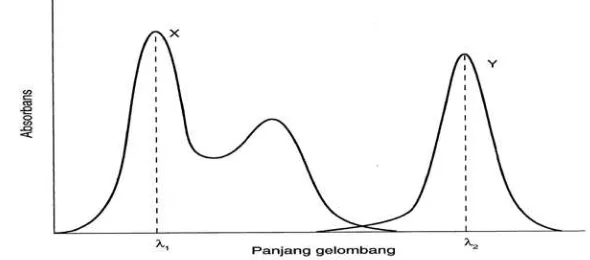
a. Spektrum tanpa tumpang tindih
Spektrum tidak saling tumpang tindih memungkinkan untuk menemukan
suatu panjang gelombang dimana X menyerap dan Y tidak menyerap, serta
panjang gelombang serapan maksimum dimana Y menerap dan X tidak
menyerap. Komponen X dan Y masing-masing diukur pada λ1 dan λ2.
Spektrum tanpa tumpang tindih dapat dilihat pada Gambar 1 dibawah ini.
[image:30.595.160.455.315.445.2]
Gambar 1. Spektrum Absorpsi Senyawa X dan Y (Tidak terjadi tumpang tindih pada kedua panjang gelombang yang digunakan)
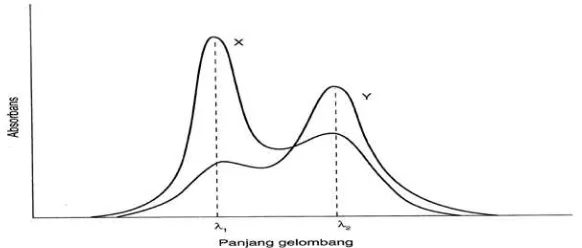
b. Spektrum tumpang tindih satu arah
Spektrum dari X dan Y tumpang tindih satu arah. Y tidak mengganggu
pengukuran X pada λ1 tetapi X menyerap cukup banyak bersama-sama
denganY pada λ2. Pemecahan masalah ini pada prinsipnya cukup sederhana.
Konsentrasi X ditetapkan langsung dari serapan larutan pada λ1. Kemudian
serapan yang diberikan oleh konsentrasi X pada λ2 dihitung dari absorptivitas
molar X pada λ2 yang telah diketahui sebelumnya. Serapan ini dikurangkan
dari serapan terukur larutan pada λ2 sehingga akan diperoleh serapan yang
biasa. Spektrum tumpang tindih satu arah dapat dilihat pada Gambar 2 di
bawah ini.
[image:31.595.156.463.139.270.2]
Gambar 2. Spektrum Absorpsi Senyawa X dan Y (Tumpang tindih satu arah; X dapat diukur tanpa gangguan Y, tetapi X mengganggu pada pengukuran langsung Y)
c. Spektrum tumpang tindih dua arah
Spektrum dari X dan Y saling tumpang tindih dua arah, pada keadaan ini
tidak ada panjang gelombang serapan maksimum dimana X dan Y menyerap
[image:31.595.168.459.478.602.2]tanpa gangguan. Spektrum tumpang tindih dua arah dapat dilihat pada
Gambar 3 di bawah ini.
Gambar 3. Spektrum Absorpsi Senyawa X dan Y (Tumpang tindih dua
arah. Tidak ada panjang gelombang dimana masing-masing
senyawa dapat diukur tanpa mengalami gangguan oleh yang
Maka perlu penyelesaian dua persamaan dengan dua variabel yang tidak
diketahui. Hal ini karena serapan total dari campuran beberapa komponen
merupakan jumlah serapan masing-masing komponen tersebut. Sehingga,
konsentrasi X dan Y yang belum diketahui dalam kedua persamaan dapat
diukur dengan mudah.
2.6 Validasi Metode
Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada
prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut
memenuhi persyaratan untuk penggunaannya (Harmita, 2004). Suatu metode
analisis harus divalidasi untuk melakukan verifikasi bahwa parameter-parameter
kerjanya cukup mampu untuk mengatasi masalah analisis (Gandjar dan Rohman,
2008).
Validasi metode analisis dilakukan dengan uji labratorium, dengan
demikian dapat ditunjukkan bahwa karakteristik kinerjanya telah memenuhi
persyaratan untuk diterapkan dalam analisis senyawa atau sediaan yang
bersangkutan (Satiadarma, dkk., 2004). Parameter analisis yang ditentukan pada
validasi adalah akurasi, presisi, spesifitas, batas deteksi, batas kuantitasi, linieritas
dan rentang (Gandjar dan Rohman, 2008).
Akurasi (kecermatan) adalah ukuran yang menunjukkan derajat kedekatan
hasil analisis dengan kadar analit sebenarnya. Akurasi dinyatakan sebagai persen
perolehan kembali (recovery) analit yang ditambahkan dan dapat ditentukan
melalui dua cara yaitu metode simulasi (spiked placebo recovery) dan metode
sejumlah analit bahan murni (senyawa pembanding kimia) ditambahkan kedalam
campuran bahan sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan
hasilnya dibandingkan dengan kadar standar yang ditambahkan (kadar
sebenarnya). Dalam metode adisi (penambahan bahan baku), sejumlah sampel
yang dianalisis ditambah analit dengan konsentrasi tertentu, dicampur dan
dianalisis kembali. Selisih kedua hasil dibandingkan dengan kadar yang
sebenarnya (hasil yang diharapkan). Dalam kedua metode, persen perolehan
kembali dinyatakan sebagai rasio antara hasil yang diperoleh dengan hasil yang
sebenarnya (Harmita, 2004).
Menurut Harmita (2004), persen perolehan kembali dapat ditentukan
dengan rumus sebagai berikut:
% perolehan kembali = CF − CA
CA∗
×
100 %Keterangan: CF = Kadar sampel setelah penambahan larutan baku
CA = Kadar sampel sebelum penambahan larutan baku
C*A = Kadar larutan baku yang ditambahkan
Presisi adalah derajat kesesuaian di antara masing-masing hasil uji, jika
prosedur analisis ditetapkan berulang kali pada sejumlah cuplikan yang diambil
dari satu sampel homogen. Presisi dinyatakan sebagai deviasi standar atau deviasi
standar relatif. Presisi dapat diartikan pula sebagai reprodusibilitas
(reproducibility) atau keterulangan (repeatability) dari prosedur analisis pada
kondisi kerja normal (Satiadarma, dkk., 2004). Parameter-parameter seperti
standar deviasi, simpangan baku relatif dan derajat kepercayaan haruslah
dikalkulasi untuk mendapatkan tingkat presisi tertentu. Nilai simpangan baku
relatif dinyatakan memenuhi persyaratan jika lebih kecil dari 10 – 20% (Ermer
Menurut Harmita (2004), simpangan baku relatif dapat ditentukan dengan
rumus sebagai berikut:
Simpangan baku relatif = SD X
� x 100%
Batas deteksi adalah parameter, yaitu konsentrasi analit terendah yang
dapat dideteksi yang masih memberikan respon signifikan dibandingkan dengan
blanko (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dapat dihitung dengan rumus
sebagai berikut:
Simpangan baku (����) =
�
∑(Y – Yi ) 2n−2
Batas deteksi = 3 × SY X�
�����
Batas
kuantitasi adalah jumlah analit terkecil dalam sampel yang masih dapat diukur dalam kondisi percobaan yang sama dan memenuhi kriteria cermatdan seksama (Harmita, 2004).
Menurut Harmita (2004), batas kuantitasi dapat dihitung dengan rumus
sebagai berikut:
Batas kuantitasi = 10 × SY X� �����
Kelinieran suatu metode analisis adalah kemampuan untuk menunjukkan
bahwa nilai hasil uji langsung atau setelah diolah secara matematika, proporsional
dengan konsentrasi analit dalam sampel dalam rentang konsentrasi tertentu
(Satiadarma, dkk., 2004). Linieritas dapat diukur dengan melakukan pengukuran
selanjutnya dapat ditentukan nilai kemiringan (slope), intersep dan koefisien
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakuka n di Laboratorium Kimia Farmasi Kuantitatif
Fakultas Farmasi Universitas Sumatera Utara dan di Laboratorium Kimia Farmasi
Kualitatif Fakultas Farmasi Universitas Sumatera Utara, dimulai dari Januari 2014
sampai April 2014.
3.2 Bahan-bahan
3.2.1 Pereaksi
Bahan-bahan yang digunakan dalam penelitian ini kecuali dinyatakan lain
adalah bahan yang berkualitas pro analisis dari E. Merck yaitu asam klorida,
aquadest (CV. Rudang Jaya), kafein (BPFI) dan natrium benzoat (BPFI).
3.3 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah Spektrofotometri
UV-Visible (Hitachi U-2900), neraca analitik (Mettler Teledo), spatula, indikator
universal dan alat-alat gelas.
3.4 Pembuatan Pereaksi
3.4.1 Larutan HCl 0,1 N
3.5 Pengambilan Sampel
Sampel yang digunakan adalah minuman energi yang diperoleh dari pusat
perbelanjaan Maximart, Yang Lim Plaza, Jalan Emas, Medan. Metode
pengambilan sampel dilakukan secara purposif, yaitu metode pengambilan sampel
ditentukan atas dasar pertimbangan bahwa sampel yang tidak terambil mempunyai
karakteristik yang sama dengan sampel yang diteliti (Sudjana, 2005).
Pengambilan sampel didasarkan atas pertimbangan dimana produk yang
beredar di pasaran yang mengandung kafein dan natrium benzoat pada
komposisinya. Diperoleh 6 (enam) sampel minuman energi dan diberi penanda
sebagai sampel A, sampel B, sampel C, sampel D, sampel E dan sampel F.
3.6 Pembuatan Larutan Induk Baku
3.6.1 Pembuatan larutan induk baku asam benzoat
Ditimbang 59 mg baku pembanding natrium benzoat (mengandung asam
benzoat 50 mg) kemudian dimasukkan ke dalam labu tentukur 100 ml, dilarutkan
dengan HCl 0,1 N hingga larut, dicukupkan volume dengan HCl 0,1 N sampai
garis tanda (LIB I).
Konsentrasi LIB I : 50 mg
100 ml × 1000 µg/mg = 500 µg/ml
Dari larutan LIB I dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml,
diencerkan dengan HCl 0,1 N sampai garis tanda (LIB II).
Konsentrasi LIB II : 5 ml
3.6.2 Pembuatan larutan induk baku kafein
Ditimbang 50 mg baku pembanding kafein kemudian dimasukkan ke
dalam labu tentukur 100 ml, dilarutkan dengan HCl 0,1 N hingga larut,
dicukupkan volume dengan HCl 0,1 Nsampai garis tanda (LIB I).
Konsentrasi LIB I : 50 mg
100 ml × 1000 µg/mg = 500 µg/ml
Dari larutan LIB I dipipet 5 ml dimasukkan ke dalam labu tentukur 50 ml,
diencerkan dengan HCl 0,1 N sampai garis tanda (LIB II).
Konsentrasi LIB II : 5 ml
50 ml× 500 µg/ml = 50 µg/ml
3.7 Penentuan Panjang Gelombang Maksimum
3.7.1 Penentuan panjang gelombang maksimum asam benzoat
Dipipet sebanyak 2,5 ml dari LIB II asam benzoat (50 µg/ml), dimasukkan
ke dalam labu tentukur 25 ml dan dicukupkan volume dengan HCl 0,1 N sampai
garis tanda. Diperoleh konsentrasi 5 µg/ml. Kemudian diukur serapannya pada
panjang gelommbang 200 – 400 nm sehingga diperoleh panjang gelombang
maksimum (hasil pengukuran dapat dilihat pada Gambar 4, halaman 28).
3.7.2 Penentuan panjang gelombang maksimum kafein
Dipipet sebanyak 4,5 ml dari LIB II asam benzoat (50 µg/ml), dimasukkan
ke dalam labu tentukur 25 ml dan dicukupkan volume dengan HCl 0,1 N sampai
garis tanda. Diperoleh konsentrasi 9 µg/ml. Kemudian diukur serapannya pada
panjang gelommbang 200 – 400 nm sehingga diperoleh panjang gelombang
3.8 Pembuatan Kurva Serapan Tumpang Tindih Asam Benzoat dan Kafein (1 : 1)
Larutan baku pembanding asam benzoat dan kafein dibuat dengan
konsentrasi masing-masing 4 µg/ml dan 4 µg/ml (1 : 1) dengan cara dipipet
sebanyak 2 ml dari LIB II asam benzoat (50 µg/ml), dimasukkan ke dalam labu
tentukur 25 ml dan dicukupkan volume dengan HCl 0,1 N sampai garis tanda dan
diperoleh konsentrasi 4 µg/ml. Selanjutnya, dipipet 2 ml dari LIB II kafein (50
µg/ml), dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan volume dengan
HCl 0,1 N sampai garis tanda dan diperoleh konsentrasi 4 µg/ml. Kemudian
diukur serapan masing-masing pada rentang panjang gelombang 200 - 400 nm.
Kurva serapan masing-masing yang diperoleh dibuat tumpang tindih pada
kerangka yang sama (hasil pengukuran dapat dilihat pada Gambar 6, Halaman
30).
3.9 Pembuatan Kurva Kalibrasi
3.9.1 Pembuatan kurva kalibrasi asam benzoat
Dari LIB II dipipet 1,5 ml; 2 ml; 2,5 ml; 3 ml; dan 3,5 ml, masing-masing
dimasukkan ke dalam labu tentukur 25 ml, kemudian dicukupkan dengan HCl 0,1
N hingga garis tanda sehingga konsentrasi asam benzoat yang diperoleh adalah 3
µg/ml, 4 µg/ml, 5 µg/ml, 6 µg/ml dan 7 µg/ml. Diukur serapannya pada panjang
gelombang maksimum asam benzoat yang telah diperoleh.
3.9.2 Pembuatan kurva kalibrasi kafein
Dari LIB II dipipet 2,5 ml; 3 ml; 3,5 ml; 4 ml; dan 4,5 ml, masing-masing
dimasukkan ke dalam labu tentukur 25 ml, kemudian dicukupkan dengan HCl 0,1
µg/ml, 6 µg/ml, 7 µg/ml, 8 µg/ml dan 9 µg/ml. Diukur serapannya pada panjang
gelombang maksimum kafein yang telah diperoleh.
3.10 Penetapan Kadar Baku Asam Benzoat dan Kafein Secara Simultan
Untuk larutan baku asam benzoat dipipet sebanyak 10 ml dari LIB II asam
benzoat (50 µg/ml), dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan
volume dengan HCl 0,1 N sampai garis tanda. Diperoleh konsentrasi 5 µg/ml.
Sedangkan untuk larutan baku kafein dipipet sebanyak 18 ml dari LIB II kafein
(50 µg/ml), dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan volume
dengan HCl 0,1 N sampai garis tanda. Diperoleh konsentrasi 9 µg/ml.
Masing-masing larutan baku diukur serapannya pada panjang gelombang 229 nm untuk
asam benzoat dan 272 nm untuk kafein. Kemudian masing- masing larutan dipipet
sebanyak 10 ml dan dicampur dalam labu tentukur. Diukur serapannya pada
panjang gelombang 229 nm dan 272 nm. Perlakuan diulang sebanyak 6 kali.
3.11 Penetapan Kadar Natrium Benzoat dan Kafein dalam Sampel
3.11.1 Penetapan kadar natrium benzoat dan kafein dalam sampel A
Dipipet 0,3 ml larutan sampel, dimasukkan dalam labu tentukur 25 ml.
Ditambahkan 1 ml HCl 0,1 N hingga suasana asam kemudian pH diperiksa
dengan menggunakan indikator universal (pH = 2). Volume dicukupkan dengan
aquadest hingga garis tanda. Diukur serapannya pada panjang gelombang
maksimum asam benzoat dan kafein yang telah diperoleh. Perlakuan diulang
3.11.2 Penetapan kadar natrium benzoat dan kafein dalam sampel B
Dipipet 0,3 ml larutan sampel, dimasukkan dalam labu tentukur 25 ml.
Ditambahkan 1 ml HCl 0,1 N hingga suasana asam kemudian pH diperiksa
dengan menggunakan indikator universal (pH = 2). Volume dicukupkan dengan
aquadest hingga garis tanda. Diukur serapannya pada panjang gelombang
maksimum asam benzoat dan kafein yang telah diperoleh. Perlakuan diulang
sebanyak 6 kali.
3.11.3 Penetapan kadar natrium benzoat dan kafein dalam sampel C
Dipipet 0,3 ml larutan sampel, dimasukkan dalam labu tentukur 25 ml.
Ditambahkan 1 ml HCl 0,1 N hingga suasana asam kemudian pH diperiksa
dengan menggunakan indikator universal (pH = 2). Volume dicukupkan dengan
aquadest hingga garis tanda. Diukur serapannya pada panjang gelombang
maksimum asam benzoat dan kafein yang telah diperoleh. Perlakuan diulang
sebanyak 6 kali.
3.11.4 Penetapan kadar natrium benzoat dan kafein dalam sampel D
Dipipet 0,3 ml larutan sampel, dimasukkan dalam labu tentukur 25 ml.
Ditambahkan 1 ml HCl 0,1 N hingga suasana asam kemudian pH diperiksa
dengan menggunakan indikator universal (pH = 2). Volume dicukupkan dengan
aquadest hingga garis tanda. Diukur serapannya pada panjang gelombang
maksimum asam benzoat dan kafein yang telah diperoleh. Perlakuan diulang
sebanyak 6 kali.
3.11.5 Penetapan kadar natrium benzoat dan kafein dalam sampel E
Dipipet 0,4 ml larutan sampel, dimasukkan dalam labu tentukur 25 ml.
dengan menggunakan indikator universal (pH = 2). Volume dicukupkan dengan
aquadest hingga garis tanda. Diukur serapannya pada panjang gelombang
maksimum asam benzoat dan kafein yang telah diperoleh. Perlakuan dilang
sebanyak 6 kali.
3.11.6 Penetapan kadar natrium benzoat dan kafein dalam sampel F
Dipipet 0,5 ml larutan sampel, dimasukkan dalam labu tentukur 25 ml.
Ditambahkan 1 ml HCl 0,1 N hingga suasana asam kemudian pH diperiksa
dengan menggunakan indikator universal (pH = 2). Volume dicukupkan dengan
aquadest hingga garis tanda. Diukur serapannya pada panjang gelombang
maksimum asam benzoat dan kafein yang telah diperoleh. Perlakuan diulang
sebanyak 6 kali.
Nilai serapan yang diperoleh harus berada dalam rentang nilai kurva
kalibrasi larutan baku, dengan demikian konsentrasi natrium benzoat dan kafein
dapat dihitung berdasarkan persamaan garis regresi linier dari kurva kalibrasi.
Konsentrasi asam benzoat dan kafein dapat dihitung dengan rumus:
Konsentrasi (µg/ml) = Konsentrasi awal (µg/ml )×volume (ml )×F. Pengenceran Volume Sampel (ml )
Kadar natrium benzoat dapat ditentukan dari berat molekulnya (BM).
Kadar natrium benzoat (mg/kg) = kadar asam benzoat x BM natrium benzoat BM asam benzoat
3.12 Analisis Data Secara Statistik
Kadar natrium benzoat dan kafein yang diperoleh dari hasil pengukuran
diterima menggunakan uji distribusi t. Menurut Sudjana (2005), uji distribusi t
dapat ditentukan dengan rumus sebagai berikut:
t hitung =
�
X− X�
SD /√n
�
Data diterima jika t hitung < t tabel. Tabel distribusi t dapat dilihat pada Lampiran
28, halaman 113.
Menurut Sudjana (2005), untuk mencari standar deviasi (SD) digunakan
rumus sebagai berikut:
SD =
�
∑(X− X�) 2n−1
Keterangan : X = kadar sampel
X
�
= kadar rata-rata sampel n = jumlah pengulangan
dan untuk menentukan kadar natrium benzoat dan kafein sebenarnya dalam
sampel dengan interval kepercayaan 99%, α = 1%, dk = n-1, dapat digunakan
rumus (Sudjana, 2005):
Kadar : µ = X� ± (t (α/2, dk) x SD/√n )
Keterangan : µ : kadar sebenarnya X� : kadar rata-rata sampel SD : standar deviasi
dk : derajat kebebasan (dk = n-1)
t : harga t tabel sesuai dengan dk = n-1 α : tingkat kepercayaan
3.13 Validasi Metode
3.13.1 Uji perolehan kembali (recovery)
Uji perolehan kembali dilakukan dengan metode penambahan larutan baku
(standard addition method). Dalam metode ini, kadar asam benzoat dan kafein
dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar
asam benzoat dan kafein dalam sampel setelah penambahan larutan standar
dengan konsentrasi tertentu (Harmita, 2004).
Uji perolehan kembali dilakukan dengan menambahkan larutan baku asam
benzoat berkonsentrasi 50 µg/ml sebanyak 0,6 ml dan larutan baku kafein
berkonsentrasi 50 µg/ml sebanyak 0,9 ml ke dalam sampel dan dianalisis dengan
perlakuan yang sama pada sampel (prosedur 3.11.2).
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan
rumus sebagai berikut:
% perolehan kembali = CF − CA
CA∗
×
100 %Keterangan: CF =Kadar sampel setelah penambahan larutan baku
CA = Kadar sampel sebelum penambahan larutan baku
C*A = Kadar larutan baku yang ditambahkan
3.13.2 Simpangan baku relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif.
Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat
kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang
memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan
Menurut Harmita (2004), simpangan baku relatif dapat dihitung dengan
rumus sebagai berikut:
RSD = SD
X
� x 100%
Keterangan : X� = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation
3.13.3 Penentuan batas deteksi (Limit of Detection) dan batas kuantitasi (Limit of Quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat
dihitung dengan rumus sebagai berikut:
Simpangan baku (����) =
�
∑(Y – Yi ) 2n−2
Batas deteksi (LOD) = 3 × SY X� �����
BAB IV
HASIL DAN PEMBAHASAN
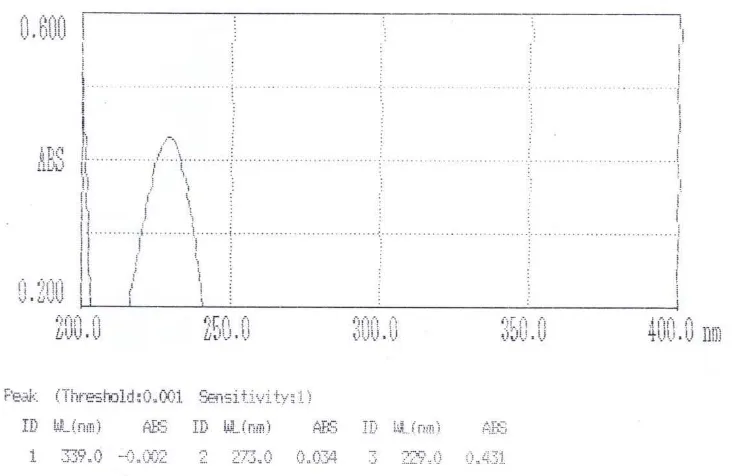
4.1 Penentuan Panjang Gelombang Maksimum
Penentuan panjang gelombang maksimum asam benzoat dilakukan dengan
mengukur absorbansi masing-masing komponen dari larutan baku dengan
konsentrasi asam benzoat 5 µg/ml dan kafein 9 µg/ml pada rentang panjang
gelombang 200 – 400 nm dengan menggunakan spektrofotometer ultraviolet. Dari
pengukuran yang dilakukan, didapat absorbansi maksimum asam benzoat pada
panjang gelombang 229 nm dan absorbansi maksimum kafein pada panjang
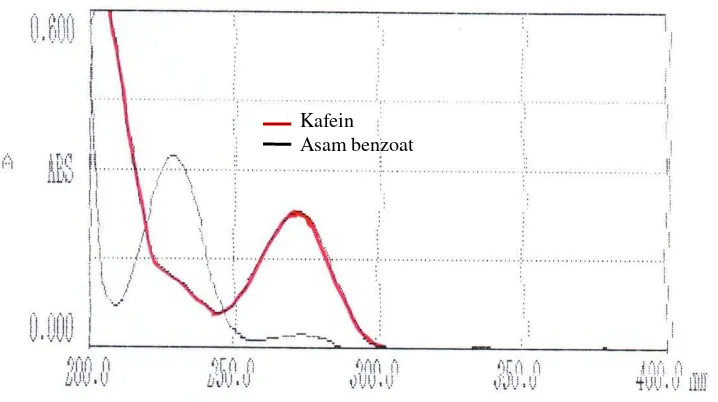
gelombang 272 nm. Kurva serapan dari baku pembanding asam benzoat dan
[image:46.595.121.488.428.666.2]kafein dapat dilihat pada Gambar 4 dan Gambar 5 di bawah ini.
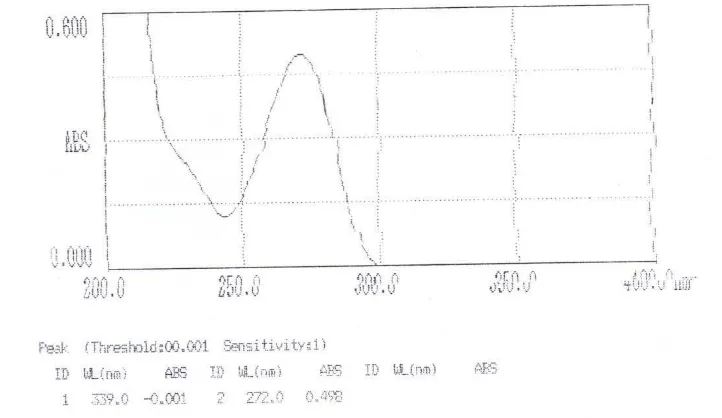
Gambar 5. Kurva Serapan Baku Pembanding Kafein, Konsentrasi 9 µg/ml dalam Larutan HCl 0,1 N. Panjang Gelombang Maksimum 272 nm
4.2 Pembuatan Kurva Serapan Tumpang Tindih Asam Benzoat dan Kafein (1 : 1)
Larutan baku pembanding asam benzoat dan kafein dibuat dengan
konsentrasi masing-masing 4 µg/ml dan 4 µg/ml. Perbandingan konsentrasi yang
dibuat sesuai dengan perbandingan rata-rata zat berkhasiat yang terdapat dalam
sampel. Kemudian diukur serapan masing-masing pada rentang panjang
gelombang 200 - 400 nm. Kurva serapan masing-masing dibuat tumpang tindih
pada kerangka yang sama. Diperoleh spektrum asam benzoat dan kafein saling
tumpang tindih dimana spektrum absorpsi asam benzoat mempengaruhi spektrum
absorpsi kafein dan spektrum absorpsi kafein juga mempengaruhi spektrum
absorpsi asam benzoat sehingga serapan yang terukur pada panjang gelombang
maksimum asam benzoat merupakan serapan asam benzoat dan kafein. Begitu
juga sebaliknya serapan yang terukur panjang gelombang maksimum kafein
Pada kurva serapan dapat dilihat terjadi tumpang tindih antara serapan
kedua senyawa. Maka, perhitungan dilakukan dengan metode persamaan regresi
[image:48.595.121.480.208.409.2]untuk kedua senyawa tersebut. Kurva serapan tumpang tindih dapat dilihat pada
Gambar 6 di bawah ini.
Gambar 6. Kurva Serapan Tumpang Tindih Baku Pembanding Asam Benzoat dan Kafein (1 : 1)
4.3 Kurva Kalibrasi
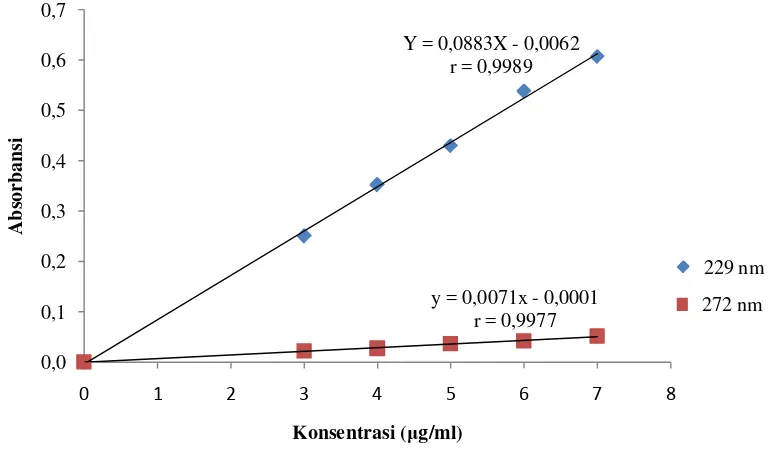
4.3.1 Kurva kalibrasi asam benzoat
Kurva kalibrasi asam benzoat diperoleh dengan cara mengukur absorbansi
larutan baku dengan konsentrasi 3; 4; 5; 6; dan 7 µg/ml pada panjang gelombang
229 nm dan 272 nm. Dari pengukuran ini didapat persamaan regresi pada panjang
gelombang 229 nm yaitu Y = 0,0883X – 0,0062 dengan koefisien korelasi (r)
0,9989 dan persamaan regresi pada panjang gelombang 272 nm yaitu Y =
0,0071X – 0,0001 dengan koefisien korelasi (r) 0,9977. Kurva kalibrasi asam
benzoat pada panjang gelombang 229 nm dan 272 nm dapat dilihat pada Gambar
7 berikut ini.
Gambar 7. Kurva Kalibrasi Asam Benzoat pada Panjang Gelombang 229 nm dan 272 nm
Berdasarkan kurva di atas diperoleh hubungan yang linier antara
konsentrasi dengan absorbansi. Nilai r > 0,99 menunjukkan adanya korelasi linier
hubungan antara X dan Y (Watson, 2010). Data dan hasil perhitungan dapat
dilihat pada Lampiran 5 dan Lampiran 6, halaman 47 dan halaman 49.
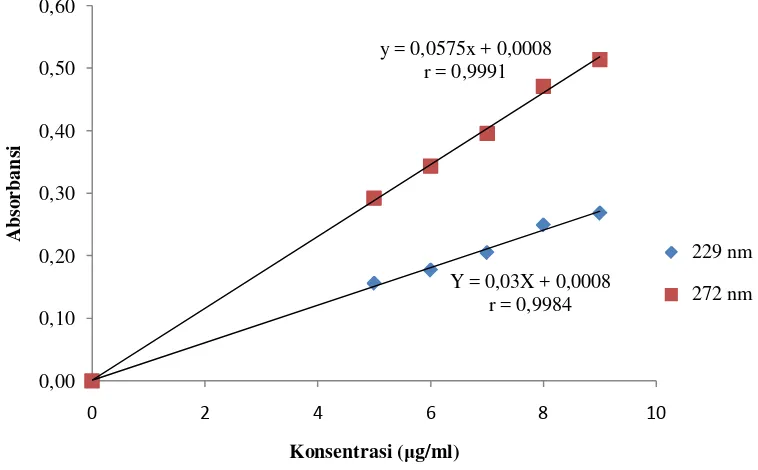
4.3.2 Kurva kalibrasi kafein
Kurva kalibrasi kafein diperoleh dengan cara mengukur absorbansi larutan
baku dengan konsentrasi 5; 6; 7; 8; dan 9 µg/ml pada panjang gelombang 229 nm
dan 272 nm. Dari pengukuran ini didapat persamaan regresi pada panjang
gelombang 229 nm yaitu Y = 0,0300X + 0,0008 dengan koefisien korelasi (r)
0,9984 dan persamaan regresi pada panjang gelombang 272 nm yaitu Y =
0,0575X + 0,0008 dengan koefisien korelasi (r) 0,9991. Kurva kalibrasi kafein
pada panjang gelombang 229 nm dan 272 nm dapat dilihat pada Gambar 8 berikut
ini.
Y = 0,0883X - 0,0062 r = 0,9989
y = 0,0071x - 0,0001 r = 0,9977 0,0
0,1 0,2 0,3 0,4 0,5 0,6 0,7
0 1 2 3 4 5 6 7 8
Abso
r
ban
si
Konsentrasi (μg/ml)
Gambar 8. Kurva Kalibrasi Kafein pada Panjang Gelombang 229 nm dan 272 nm
Berdasarkan kurva di atas diperoleh hubungan yang linier antara
konsentrasi dengan absorbansi. Nilai r > 0,99 menunjukkan adanya korelasi linier
hubungan antara X dan Y (Watson, 2010). Data dan hasil perhitungan dapat
dilihat pada Lampiran 7 dan Lampiran 8, halaman 51 dan halaman 53.
4.4 Penetapan Kadar Baku Asam Benzoat dan Kafein Secara Simultan
Hasil pengukuranuntuk masing-masing larutan baku diperoleh konsentrasi
sebesar 5,0350 µg/ml untuk asam benzoat dan 9,0430 µg/ml untuk kafein.
Kemudian setelah pencampuran larutan baku, konsentrasi rata-rata asam benzoat
dan kafein yang diperoleh dengan metode persamaan regresi yaitu sebesar 5,0251
µg/ml dan 9,2918 µg/ml. Hasil perhitungan menunjukkan bahwa persen kadar
yaitu 99,80% untuk asam benzoat dan 102,75% untuk kafein dan kadar ini masih
di dalam batas kadar yang diizinkan dalam Farmakope Indonesia yaitu 90-110 %
(Ditjen POM, 1979). Berdasarkan hal tersebut dapat dinyatakan bahwa metode Y = 0,03X + 0,0008
r = 0,9984 y = 0,0575x + 0,0008
r = 0,9991
0,00 0,10 0,20 0,30 0,40 0,50 0,60
0 2 4 6 8 10
Abso
r
ban
si
Konsentrasi (μg/ml)
Series1
perhitungan persamaan regresi dapat digunakan untuk penetapan kadar natrium
benzoat dan kafein. Contoh perhitungan dapat dilihat pada Lampiran 10, halaman
56.
4.5 Penetapan Kadar Natrium Benzoat dan Kafein dalam Sampel
Pada penetapan kadar natrium benzoat dan kafein pada sampel dilakukan
pemipetan larutan sampel dengan volume yang berbeda-beda. Hal ini disebabkan
setelah dilakukan orientasi dengan volume yang sama, hasil yang diperoleh diluar
dari nilai kurva kalibrasi.
Penetapan kadar natrium benzoat dan kafein dilakukan secara
spektrofotometri ultraviolet. Natrium benzoat dalam sampel akan bereaksi dengan
asam klorida membentuk asam benzoat dalam suasana asam. Dengan
menggunakan dua panjang gelombang yaitu masing-masing 229 nm untuk asam
benzoat dan 272 nm untuk kafein dilakukan perhitungan kadar untuk kedua
senyawa secara persamaan regresi. Sampel diukur pada kedua panjang gelombang
tersebut. Analisis kemudian dilanjutkan dengan perhitungan statistik dengan
distribusi t pada tingkat kepercayaan 99% (perhitungan statistik dapat dilihat pada
Lampiran 18-23, halaman 78-98). Kandungan natrium benzoat dan kafein pada
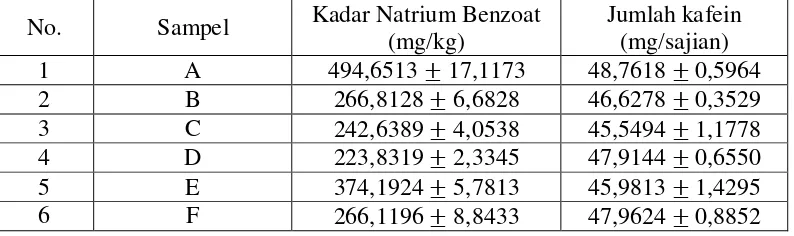
[image:51.595.116.513.637.755.2]sampel minuman energi dapat dilihat pada Tabel 1 di bawah ini.
Tabel 1. Kandungan Natrium Benzoat dan Kafein pada Minuman Energi
No. Sampel Kadar Natrium Benzoat
(mg/kg)
Jumlah kafein (mg/sajian)
1 A 494,6513 ± 17,1173 48,7618 ± 0,5964
2 B 266,8128 ± 6,6828 46,6278 ± 0,3529
3 C 242,6389 ± 4,0538 45,5494 ± 1,1778
4 D 223,8319 ± 2,3345 47,9144 ± 0,6550
5 E 374,1924 ± 5,7813 45,9813 ± 1,4295
Berdasarkan Tabel 1, semua sampel minuman energi yang dianalisis
mengandung natrium benzoat antara 223 - 494 mg/kg, semua sampel minuman
energi tersebut tidak mencantumkan jumlah natrium benzoat pada label namun
hasil yang diperoleh memenuhi persyaratan kadar natrium benzoat yang tercantum
dalam SNI 01-0222-1995 tentang bahan tambahan pangan yaitu tidak lebih dari
600 mg/kg. Dan semua sampel minuman energi tersebut juga mengandung kafein
antara 45 - 48 mg/sajian, hasil yang diperoleh berbeda dengan yang tertera pada
label yaitu 50 mg/sajian namun masih memenuhi persyaratan kandungan kafein
dalam minuman energi yang tercantum dalam SNI 01-6684-2002 tentang
minuman energi yaitu tidak lebih dari 50 mg/sajian. Contoh perhitungan dapat
dilihat pada Lampiran 12-17, halaman 60-75.
Kandungan kafein dan natrium benzoat dalam sampel minuman energi
yang diperoleh pada panjang gelombang maksimum 229 nm dan 272 nm bukan
merupakan kandungan natrium benzoat dan kafein yang sebenarnya tetapi
merupakan kandungan total beserta bahan-bahan lain dalam sampel yang
memberikan serapan pada panjang gelombang maksimum yang digunakan
misalnya vitamin B5 (λmaks = 200 nm), sakarin (λmaks = 235 nm), vitamin B1
(λmaks = 246 nm), nikotinamid (λmaks = 261 nm), vitamin B2 (λmaks = 267 nm),
vitamin B12 (λmaks = 278 nm) dan vitamin B6 (λmaks = 290 nm). Sedangkan
bahan – bahan yang mempunyai panjang gelombang maksimum pada daerah
visible (400 - 800 nm) tidak mempengaruhi hasil penelitian. Panjang gelombang
maksimum bahan-bahan yang terdapat dalam sampel minuman energi dapat
dilihat pada Lampiran 2, halaman 44. Pada analisis sampel minuman energi yang
tidak mempertimbangkan bahan-bahan lain dalam sampel yang memberikan
serapan pada panjang gelombang maksimum yang digunakan. Pada penelitian ini
seharusnya menggunakan metode Kromatografi Cair Kinerja Tinggi (KCKT)
yang dapat memisahkan bahan - bahan dalam sampel.
4.6 Validasi Metode Analisis
4.6.1 Uji perolehan kembali (recovery)
Hasil uji perolehan kembali kadar asam benzoat dan kafein setelah
penambahan masing-masing larutan baku asam benzoat dan kafein dalam sampel
dapat dilihat pada Lampiran 24, halaman 102. Perhitungan persen perolehan
kembali asam benzoat dan kafein dalam sampel dapat dilihat pada Lampiran 25,
halaman 103. Persen perolehan kembali asam benzoat dan kafein dapat dilihat
[image:53.595.112.513.471.530.2]pada Tabel 2 di bawah ini.
Tabel 2. Persen Perolehan Kembali (recovery) Asam Benzoat dan Kafein
No. Persen Perolehan
kembali
Syarat rentang persen perolehan kembali
1 Asam benzoat 109,41
80 - 120%
2 Kafein 105,79
Berdasarkan Tabel 2, dapat dilihat bahwa rata-rata hasil uji perolehan
kembali untuk asam benzoat 109,41% dan kafein 105,79%. Persen perolehan
kembali tersebut menunjukkan kecermatan atau akurasi yang baik berdasarkan
syarat persen perolehan kembali yaitu berada pada rentang 80 – 120% (Ermer dan
Miller, 2005). Hasil yang diperoleh masih dipengaruhi oleh bahan – bahan lain
dalam sampel minuman energi yang panjang gelombang maksimumnya berada
4.6.2 Simpangan baku relatif
Untuk menetapkan presisi dari metode yang digunakan maka dilakukan
perhitungan simpangan baku relatif (Relative Standard Deviation). Berdasarkan
data hasil pengukuran asam benzoat dan kafein dalam minuman energi, diperoleh
nilai simpangan baku relatif (RSD) sebesar 2,33% untuk asam benzoat dan 2,57%
untuk kafein. RSD yang diperoleh memenuhi persyaratan yaitu lebih kecil dari 10
- 20%. Parameter-parameter seperti standar deviasi, simpangan baku relatif dan
derajat kepercayaan haruslah dikalkulasi untuk mendapatkan tingkat presisi
tertentu (Ermer dan Miller, 2005). Dari hasil yang diperoleh menunjukkan bahwa
metode yang dilakukan memiliki presisi yang baik. Perhitungan simpangan baku
relatif (RSD) kadar asam benzoat dan kafein dapat dilihat pada Lampiran 26,
halaman 107.
4.6.3 Batas deteksi dan batas kuantitasi
Batas deteksi dan batas kuantitasi untuk asam benzoat dan kafein
ditentukan berdasarkan data kurva kalibrasi kedua komponen tersebut. Dari hasil
perhitungan diperoleh batas deteksi asam benzoat dan kafein pada panjang
gelombang 229 nm masing-masing sebesar 0,4043 µg/ml dan 0,6100 µg/ml.
Sedangkan, batas kuantitasinya sebesar 1,3477 µg/ml untuk asam benzoat dan
2,0333 µg/ml untuk kafein. Dan batas deteksi asam benzoat dan kafein pada
panjang gelombang 272 nm masing-masing sebesar 0,5493 µg/ml dan 0,3652
µg/ml. Sedangkan, batas kuantitasinya sebesar 1,8310 µg/ml untuk asam benzoat
Batas deteksi merupakan parameter uji batas yang dilakukan untuk
mendeteksi jumlah terkecil analit dalam sampel yang masih memberikan respon
signifikan dibandingkan dengan blanko. Sedangkan, batas kuantitasi merupakan
kuantitas terkecil analit yang masih dapat memenuhi kriteria cermat dan seksama
(Harmita, 2004). Perhitungan batas deteksi dan batas kuantitasi asam benzoat dan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang dilakukan, maka dapat diambil kesimpulan:
1. Hasil pengujian terhadap bahan baku menunjukkan bahwa terdapat
perbedaan konsentrasi sebelum dan sesudah pencampuran yaitu
konsentrasi asam benzoat dan kafein sebelum pencampuran adalah 5,0350
µg/ml dan 9,0430 µg/ml, sedangkan konsentrasi asam benzoat dan kafein
setelah pencampuran adalah 5,0251 µg/ml dan 9,2918 µg/ml dan ini masih
dalam batas kadar yang diizinkan dalam Farmakope Indonesia (Ditjen
POM, 1979), sehingga analisis dengan metode spektrofotometri ultraviolet
secara simultan menggunakan metode perhitungan persamaan regresi
dapat digunakan untuk menganalisis campuran kafein dan natrium
benzoat.
2. Kandungan natrium benzoat dan kafein pada minum