BAB I
PENDAHULUAN
A. Latar Belakang
Dalam analisis kimia suatu bahan, maka akan sering dihadapkan pada pekerjaan-pekerjaan seperti menghilangkan konstituen pengganggu atau mengisolasikannya maupun memekatkan konstituen yang dikehendaki sebelum dilakukuan identifikasi maupun pengukuran jumlahnya. Untuk melakukan analisis kimia tersebut maka kita harus menggunakan suatu metode agar dapat menentukan hasil yang tepat, kromatografi salah satunya, dan dapat pula digunakan sebagai analisa secara kuantitatif.
Kromatografi Lapis Tipis merupakan teknik pemisahan cara lama yang digunakan secara luas, terutama dalam analisis campuran yang rumit dari sumber alam. Tetapi dalam kuantisasi belakangan ini kromatografi lapis tipis digantikan oleh “HPLC” (High Performance Thin-layer Chromatography) atau Kromatografi Lapis Tipis Kinerja Tinggi.
Salah satu metode pemisahan yang memerlukan biaya paling murah dan memakai peralatan sangat sederhana ialah kromatografi lapis tipis preparatif (KLTP). Walaupun KLTP dapat memisahkan dalam jumlah gram,sebagian besar pemakaian hanya dalam jumlah miligram. KLT preparatif dilakukan dengan menggunakan lapisan tebal
Kromatografi Lapis Tipis Preparatif merupakan metode isolasi yang sudah lama popular karena metode ini telah digunakan secara universal oleh mahasiswa dan peneliti-peeliti bahan alam. Selain itu metode ini tidak memerlukan biaya pengerjaan yang mahal. Ini menjadi nilai tambah dari metode kromatografi lapis tipis preparative.
Prinsip kerja dari metode kromatografi lapis tipis preparatif, adalah dimana proses isolasi berdasarkan perbedaan daya serap dengan kecepatan yang berbeda sehingga terjadi pemisahan.
B. Rumusan Masalah
1. Apa defenisi umum dan bagaimana prinsip kerja dari Kromatografi Lapis Tipis Preparatif ?
2. Apa hasil yang dapat diperoleh dari metode Kromatografi Lapis Tipis Preparatif ?
C. Maksud dan Tujuan Praktikum 1. Maksud
Adapun maksud dari praktikum ini yaitu Untuk mengisolasi komponen kimia dengan menggunakan metode Kromatografi Lapis Tipis Preparatif pada daun bagore (Caesalpinia crista L.)
2. Tujuan
Adapun tujuan percobaan ini yaitu untuk memisahkan senyawa kimia fraksinasi kasar daun bagore (Caesalpinia crista L.) menggunakan Kromatografi Lapis Tipis Preparatif berdasarkan warna dan tingkat kepolaran.
D. Manfaat Praktikum
Preparatif dalam memisahkan senyawa dengan berbagai perbandingan eluen dari kepolaran rendah hingga kepolaran yang tinggi.
BAB II
TINJAUAN PUSTAKA A. Uraian Tanaman
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh) Super Divisi : Spermatophyta (Menghasilkan biji) Divisi : Magnoliophyta (Tumbuhan berbunga) Kelas : Magnoliopsida (berkeping dua / dikotil) Sub Kelas : Rosidae
Ordo : Fabales
Famili : Caesalpiniaceae Genus : Caesalpinia
Spesies : Caesalpinia crista L. Nama simplisia : Daun Bagore
Kandungan kimia : Alkaloid, karbohidrat, glikosida, tannin, flavonoid, dan kumarin
B. Metode Isolasi
Isolasi adalah proses pemisahan komponen kimia yang terdapat dalam suatu ekstrak. Hal ini dilakukan ketika ingin mengambil bahan aktif dari ekstrak kasar (crude extract) (Skalika-Wozniak et al, 2008).
Kromatografi merupakan suatu proses pemisahan yang mana analit-analit dalam sampel terdistribusi antara dua fase, yaitu fase diam dan fase gerak. Fase diam dapat berupa bahan padat atau porus dalam bentuk molekul kecil atau dalam bentuk cairan yang dilapiskan pada pendukung padat atau dilapiskan pada
dinding kolom. Fase gerak dapat berupa gas atau cairan. Jika gas digunakan sebagai fase gerak, maka prosesnya dikenal sebagai kromatografi gas. Dalam kromatografi cair dan juga kromatografi lapis tipis, fase gerak yang di gunakan selalu cair (Rohman,2009).
Kromatografi dapat dibedakan atas berbagai macam, tergantung pada pengelompokannya. Berdasarkan pada mekanisme pemisahannya, kromatografi dibedakan menjadi (Rohman, 2009):
a. Kromatografi adsorbsi b. Kromatografi partisi
c. Kromatografi pasangan ion d. Kromatografi penukar ion e. Kromatografi ekslusi ukuran f. Kromatografi afinitas
Kromatografi melibatkan pemisahan terhadap campuran berdasarkan perbedaan-perbedaan tertentu yang dimiliki oleh senyawanya. Perbedaan yang dapat dimanfaatkan meliputi kelarutan dalam berbagai pelarut serta sifat polar. Fase gerak membawa komponen suatu campuran melalui fase diam, dan fase diam akan berikatan dengan komponen tersebut dengan afinitas yang berbeda-beda. Jenis kromatografi yang berlainan bergantung pada perbedaan jenis fase, namun semua jenis kromatografi tersebut berdasar pada asas yang sama (Bresnick, 2012).
Kromatografi lapis tipis digunakan untuk pemisahan senyawa secara cepat, dengan menggunakan zat penjerap berupa serbuk halus yang dipaliskan serta rata pada lempeng kaca. Lempeng yang dilapis, dapat dianggap sebagai “kolom kromatografi terbuka” dan pemisahan dapat didasarkan pada penyerapan, pembagian atau gabungannya, tergantung dari jenis zat penyerap dan cara pembuatan lapisan zat penyerap dan jenis pelarut. Kromatografi lapis tipis dengan penyerap penukar ion dapat digunakan untuk pemisahan senyawa polar. Harga Rf yang diperoleh pada kromatografi lapis tipis tidak tetap, jika dibandingkan dengan yang diperoleh pada kromatografi kertas. Oleh karena itu pada lempeng yang sama di samping kromatogram zat yang di uji perlu dibuat kromatogram zat pembanding kimia, lebih baik dengan kadar yang berbeda-beda (Dirjen POM, 1979).
Kromatografi Lapis Tipis merupakan teknik pemisahan cara lama yang digunakan secara luas, terutama dalam analisis campuran yang rumit dari sumber alam. Tetapi dalam kuantisasi belakangan ini kromatografi lapis tipis digantikan oleh “HPLC” (High Performance Thin-layer Chromatography) atau Kromatografi Lapis Tipis Kinerja Tinggi (Munson, 2010).
Perbandingan jarak perambatan suatu zat dengan jarak perambatan fase bergerak di hitung dari titik penotolan larutan zat, dinyatakan dengan Rf (Retondary factor) zat tersebut. Perbandingan
perambatan suatu zat dengan jarak perambatan zat pembanding dinyatakan dengan Rr (Anonim, 2012).
Jarak perambatan noda Rf = Jarak perambatan eluen
Teknik kromatografi lapis tipis (KLT) dikembangkan oleh Egon Stahl dengan menghamparkan penyerap pada lempeng gelas, sehingga merupakan lapis tipis. KLT merupakan kromatografi serapan, tetapi dapat juga merupakan kromatografi partisi karena bahan penyerap telah dilapisi air dari udara (Sudjadi, 1986).
Ada beberapa macam silika gel yang beredar, diantaranya (Sudjadi, 1986) :
1. Silika gel dengan pengikat.
2. Silika gel dengan pengikat dan indikator fluoresensi. 3. Silika gel tanpa pengikat.
4. Silika gel tanpa pengikat tapi dengan indikatorberfluoresensi. 5. Silika gel untuk keperluan pemisahan preparatif.
Metode identifikasi. Untuk melihat senyawa tak berwarna pada lempeng, biasanya digunakan metode berikut (Sudjadi, 1986) :
1. Metode kromatogram di bawah sinar ultraviolet (254 atau 366 nm). a. Pada lapisan berflouresensi,misalnya Silica Gel GF254,
bercak muncul sebagai noda hitam.
b. Untuk senyawa berflouresensi digunakan lapisan biasa, bercak terlihat berflouresensi.
2. Menyemprot dengan pereaksi yang menghasilkan warna dan atau berflouresensi.
Kromatografi lapis tipis preparatif (KLTP) adalah salah satu metode yang memerlukan pembiayaan paling murah dan memakai peralatan paling dasar. Walaupun KLTP dapat memisahkan bahan dalam jumlah gram, sebagian besar pemakainya hanya dalam jumlah miligram.KLTP bersama-sama dengan kromatografi kolom terbuka, masih dijumpai dalam sebagian besar publikasi mengenai isolasi bahan alam (Hostettmann, 2006).
Ketebalan penjerap (adsorben) yang paling sering dipakai pada KLTP adalah sekitar 0,5-2 mm. Ukuran pelat kromatografi biasanya 20 x 20 cm atau 20 x 40 cm. Pembatasan ketebalan lapisan dan ukuran pelat sudah tentu mengurangi jumlah bahan yang dapat dipisahkan dengan KLTP. Penjerap yang paling umum digunakan ialah silika gel dan dipakai untuk pemisahan campuran senyawa lipofil maupun campuran senyawa hdrofil (Hostettmann, 2006).
Cuplikan pada KLTP dilarutkan dalam sedikit pelarut sebelum ditotolkan pada pelat KLTP. Pelarut yang baik adalah pelarut atsiri ( heksana, diklorometana, etil asetat), karena jika pelarut kurang atsiri akan terjadi pelebaran pita. Konsentrasi cuplikan harus sekitar 5% -10%. Cuplikan ditotolkan berupa pita yang harus sesempit mungkin karena pemisahan tergantung pada lebar pita (Szekely 1983).
KLTP klasik mempunyai beberapa kekurangan, kekurangan yang utama adalah pengambilan senyawa dari pelat yang dilanjutkan dengan pengekstrasian dari penjerap. Jika senyawa beracun harus dikerok dari pelat, dapat menimbulkan masalah yang serius (misalnya Adolf dkk. 1982). Kekurangan yang lainya ialah jangka waktu yang diperlukn untuk pemisahan dan adanya pencemar dan sisa dari pelat sendiri setelah pengekstrasian pita yang mengandung senyawa yang dipisahkan dengan pelarut (Szekely 1983).
Untuk mengatasi beberapa masalah tersebut, beberapa pendekatan yang melibatkan kromatografi sentrifugal telah dicoba. Pada prinsipnya kromatografi sentrifugal adalah kromatografi klasik dengan aliran fase gerak yang dipercepat oleh gaya sentrifugal (Szekely 1983).
BAB III
PROSEDUR KERJA
A. Alat dan Bahan 1. Alat
Alat yang digunakan adalah batang pengaduk panjang, botol UC Bekas, cawan porselin, chamber KLTP, corong kaca, gelas
kimia, gelas ukur, kertas saring, lempeng 7 x 0,5 cm, lampu UV 254 dan 366 nm, lempeng KLTP, pipa kapiler, pipet tetes, statif, timbangan analitik, vial.mistar, dan sendok tanduk besi.
2. Bahan
Bahan yang digunakan adalah aluminium foil, fraksi methanol daun bagore (Caesalpinia crista L.), etil-Asetat, kapas, kertas saring, methanol, n-Hexan, silica gel kasar dan halus, tisu. B. Prosedur Kerja
Disiapkan alat dan bahan. Dipilih hasil fraksi yang terelusi dengan baik pada kromatografi kolom konvensional dan kromatografi kolom cair vakum. Kemudian masing-masing fraksi yang telah dipilih dilarutkan dengan eluen dan ditotolkan pada lempeng KLTP menggunakan pipa kapiler. Selanjutnya dielusi dalam chamber yang berisi eluen n-heksan:etil (8:2) yang telah jenuh. Kemudian dibiarkan terelusi, selanjutnya diamati penampakan bercak noda pada lampu UV 254 dan 366 nm. Dan dilakukan uji antioksidan dengan pereaksi DPPH.
BAB IV
HASIL PENGAMATAN A. Tabel Pengamatan
N
O Fraksi Jumlah Pita Warna
1 Kromatografi Kolom
Konvensional (KKK) 2
Kuning dengan Latar Ungu 2 Kromatografi Cair Vakum 2 Kuning dengan
(KCV) Latar Ungu B. Gambar Hasil Pengamatan
Hasil Praktikum
Gambar Hasil Pengamatan
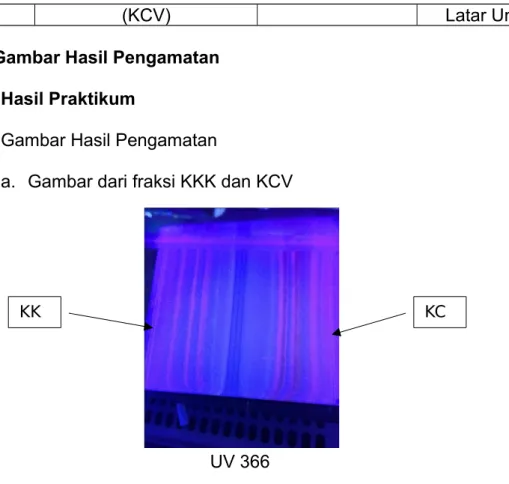
a. Gambar dari fraksi KKK dan KCV
UV 366
Dari gambar pengamatan tersebut diperoleh 2 pita untuk fraksi KKK dan 2 pita juga dari Fraksi KCV yang bersifat antioksidan dimana ditandai dengan pita warna kuning dengan latar belakang ungu setelah disemprotkan DPPH.
C. PEMBAHASAN
Kromatografi Lapis Tipis merupakan teknik pemisahan cara lama yang digunakan secara luas, terutama dalam analisis campuran yang rumit dari sumber alam. Tetapi dalam kuantisasi belakangan ini kromatografi lapis tipis digantikan oleh “HPLC” (High Performance Thin-layer Chromatography) atau Kromatografi Lapis Tipis Kinerja Tinggi.
KC V KK
Pada percobaan ini dilakukan identifikasi sampel ektrak Daun bagore menggunakan metode kromatografi lapis tipis preparatif. Dimana metode ini KLTP klasik mempunyai beberapa kekurangan, kekurangan yang utama adalah pengambilan senyawa dari pelat yang dilanjutkan dengan pengekstrasian dari penjerap. Jika senyawa beracun harus dikerok dari pelat, dapat menimbulkan masalah yang serius.
Pada pengerjaan pertama, alat dan bahan yang akan digunakan siapkan agar dapat meminimalisir dan memperlancar proses pengerjaan. selanjutnya penyiapan pelarut dari n-heksan: etil (8:2). Hal ini dilakukan agar dapat mengetahui apakah sampel dapat membentuk fraksi yang baik atau terelusi dengan baik.
Pada metode Kromatogrfi kolom konvensional dipilih fraksi pada vial nomor 22 sebagai fraksi yang akan ditotolkan di Lempeng KLTP. Dan pada metode kromatografi cair vakum dipilih fraksi pada perbandingan 6:4 sebagai fraksi yang akan ditotolkan di Lempeng KLTP.
Selanjutnya disiapkan serangkaian alat kromatografi kromatografi lapis tipis preparative. Dimana terdapat chamber berukuran besar untuk menampung eluen dengan panjang 20x20 cm untuk membentuk pita noda, yang akan diambil atau dikeruk sebagai isolate.
Pada percobaan ini, merupakan percobaan berkelanjutan, dimana hasil penetolan eluen yang cocok berdasarkan data hasil pengamatan pada percobaan kromatogrfai cair vakum yaitu pada fraksi ke 4 dengan menggunakan eluen n-heksan: etil (1:1). Selanjutnya digunakan lempeng
kltp untuk mendeteksi pembentukan pita yang sebelumnya telah ditotolkan hasil campuran fraksi dan eluen n-heksan: etil (8:2). Setelah itu dielusi pada chamber dan menghasilkan pita noda.
Kemudian diamati pada lampu UV. Dari hasil pengamatan noda atau pita dapat terlihat pada lampu UV 254 dan juga UV 366. Terdapat 2 pita yang terbentuk pada lempeng KLTP untuk metode KKK dan KCV setelah disemprotkan dengan DPPH. Kemudian pada metode KKK dan KCV dikeruK lurus pita panjang berwarna kuning pada bagian yang tidak di semprotkan dengan DPPH.
Hasil pengerukan kemudian disimpan kedalam vial dan hasil pengamatan pada percobaan KLTP akan dilanjutkan pada percobaan selanjutnya dengan cara sentrifuge untuk mengetahui dengan pasti senyawa yang terbentuk pada lempeng.
BAB V
KESIMPULAN
A. Kesimpulan
Dari hasil percobaan dapat disimpulkan bahwa dengan menggunakan metode kromatografi lapis tipis preparatif 2 noda atau
pita yang terbentuk dengan optimal yaitu dengan menggunakan eluen n-heksan: etil perbandingan (8:2) pada sampel ekstrak daun bagore. B. Saran
Sebaiknya alat-alat di laboratorium harus ditambah agar dapat meminimalkan dan mengefisienkan waktu praktikum. Terutama alat yang berhubungan dengan praktikum ini.
DAFTAR PUSTAKA
Anonim., 2012, ”Penuntun dan Buku Kerja Praktikum Fitokimia 2”, Fakultas Farmasi, Universitas Muslim Indonesia, Makassar. Anonim., 2015, ”Penuntun dan Buku Kerja Praktikum Fitokimia 2”,
Fakultas Farmasi, Universitas Muslim Indonesia, Makassar. Bresnick, Stephen., 2002. Intisari Fisika.Hipokrates.Jakarta
Munson, James,W., 2010. Analisis Farmasi. Airlangga University Press: Surabaya
Sudjadi, Drs., 1986, “Metode Pemisahan”, UGM Press, Yogyakarta.
Hostettmann. M, Hostettmann. K, Marston. A., cara kromatografi preparatif, 1995. ITB Bandung
Rohman, Abdul., 2007. Kimia Farmasi Analisis. Pustaka Pelajar. : Jakarta Skalicka-Woźniak, 200, Isolation of the new minor constituents
dihydropyranochromone and furanocoumarin from fruits of Peucedanum alsaticum L. by high-speed counter-current chromatography, Journal of Chromatography A 1216 (30) : 5669- 5675
Http :// www.itis.com
(diakses Makassar, 26/04/2015 20:00)
Gambar 1. Metode Kromatografi cair vakum