PERBANDINGAN EFIKASI TERAPI KOMBINASI
ARTESUNAT + SULFADOKSIN-PIRIMETAMIN DENGAN
ARTESUNAT + DOKSISIKLIN PADA PENDERITA
MALARIA FALCIPARUM TANPA KOMPLIKASI
TESIS
Oleh
INDIRA JULIA
047027003/KT
PERBANDINGAN EFIKASI TERAPI KOMBINASI
ARTESUNAT + SULFADOKSIN-PIRIMETAMIN DENGAN
ARTESUNAT + DOKSISIKLIN PADA PENDERITA
MALARIA FALCIPARUM TANPA KOMPLIKASI
TESIS
Untuk memperoleh gelar Magister Kedokteran Tropis dalam Program Studi Ilmu Kedokteran Tropis pada
Sekolah Pascasarjana Universitas Sumatera Utara
Oleh
INDIRA JULIA
047027003/KT
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
Judul Tesis : PERBANDINGAN EFIKASI TERAPI KOMBINASI ARTESUNAT + SULFADOKSIN-PIRIMETAMIN DENGAN ARTESUNAT + DOKSISIKLIN PADA
PENDERITA MALARIA FALCIPARUM TANPA
KOMPLIKASI
Nama Mahasiswa : INDIRA JULIA
Nomor Pokok : 047027003
Program Studi : Ilmu Kedokteran Tropis
Menyetujui
Komisi Pembimbing
(dr. Yosia Ginting, SpPD-KPTI) Ketua
(dr. Umar Zein, DTM&H, SpPD-KPTI) (Drs. Saib Suwilo, MSc., PhD) Anggota Anggota
Ketua Program Studi, Direktur,
Telah diuji pada
Tanggal : 18 Juni 2007
PANITIA PENGUJI TESIS
KETUA : dr. Yosia Ginting, SpPD-KPTI
ANGGOTA : 1. dr. Umar Zein, DTM&H, SpPD-KPTI
2. Drs. Saib Suwilo, MSc.,PhD.
3. dr. Datten Bangun, MSc.
KATA PENGANTAR
Puji dan syukur kehadirat Allah Subhanahu Wata’ala atas rahmat, karunia dan
hidayahNya, sehingga penulis dapat menyelesaikan tesis ini sebagai salah satu tugas
akhir dalam menyelesaikan pendidikan pada Program Pascasarjana Magister Ilmu
Kedokteran Tropis Universitas Sumatera Utara.
Berkat dukungan dan bimbingan dari berbagai pihak, akhirnya tesis ini dapat
diselesaikan. Untuk itu perkenankanlah penulis menyampaikan ucapan terima kasih dan
penghargaan yang setinggi-tingginya kepada :
1. dr. Yosia Ginting, SpPD-KPTI, dr. Umar Zein, DTM&H, SpPD-KPTI, dan
Drs. Saib Suwilo, MSc., PhD selaku pembimbing yang telah memberikan
bimbingan, masukan dan dorongan mulai dari perencanaan pembuatan tesis
sampai penyelesaiannya.
2. dr. Datten Bangun, MSc dan dr. Endang Haryanti Gani, DTM&H, SpParK
sebagai komisi pembanding yang telah memberikan bimbingan dan berbagai
masukan dalam penyelesaian tesis ini.
3. Prof. Dr. dr. Syahril Pasaribu, DTM&H, MSc (CTM),SpAK, selaku Ketua
Program Studi Ilmu Kedokteran Tropis, dr. R. Lia Kusumawati, MS, SpMK
selaku sekretaris Program Studi Ilmu Kedokteran Tropis atas kesempatan,
bimbingan dan arahan sejak penulis dalam masa pendidikan sampai
penyelesaian tesis.
Program Studi Ilmu Kedokteran Tropis yang telah memberikan ilmu dan
berbagai bantuan selama penulis dalam masa pendidikan.
5. dr. Margan R.P.Sibarani, selaku Kepala Dinas Kesehatan Tingkat II Kabupaten
Nias Selatan yang telah memberi izin, menyediakan fasilitas, sarana dan
bantuan tenaga dalam pelaksanaan penelitian.
6. dr. Leonardo, Mathius, Yusnidar, dan Tina yang telah bekerja dengan
sungguh-sungguh membantu penulis selama di lapangan.
7. Pemda Kota Sabang dan dr. H. Ikhsan, Mkes selaku Kepala Dinas Kesehatan
dan Kesejahteraan Sosial Kota Sabang yang telah memberikan fasilitas dan
bantuan obat-obatan kepada penulis.
8. dr. Titik Yuniarti, dr. Philip Darmawan, dr. Lambok Siahaan, dan rekan-rekan
peserta Program Pascasarjana Magister Ilmu Kedokteran Tropis atas
persahabatan dan kerjasama yang terjalin selama mengikuti pendidikan.
9. Kedua orang tua tercinta, ibunda Roswati Arifin dan ayahanda Julius, serta
saudara-saudaraku yang telah melimpahkan kasih sayang dan tak
henti-hentinya memberikan dorongan serta doa kepada penulis.
10. Kepada suamiku dr. Rifi Rio Odias serta ayah dan ibu mertua, dr. Rusdi Zain,
SpTHT dan drg. Asnimar atas kasih sayang, pengertian dan kesabarannya
kepada penulis.
11. Kepada semua pihak yang tidak dapat disebutkan satu persatu yang telah
memberikan bantuan moril dan materil kepada penulis selama menyelesaikan
Semoga segala bantuan dan bimbingan yang diberikan kepada penulis menjadi amal
ibadah. Akhirnya penulis berharap semoga tulisan ini dapat bermanfaat bagi semua
pihak, dan semoga Allah Subhanahu Wata’ala selalu melimpahkan rahmat dan
hidayahNya kepada kita semua.
Medan, Juni 2007
RIWAYAT HIDUP
Nama Lengkap : dr. Indira Julia
Tanggal Lahir : 01 Nopember 1978
Tempat Lahir : Medan
Alamat : Jl. Rawacangkuk IV No.1 Medan
Riwayat Pendidikan
1. Sekolah Dasar di SD Tamansiswa Medan, tamat tahun 1991
2. Sekolah Menengah Pertama di SMP Negeri XI Medan, tamat tahun 1994
3. Sekolah Menengah Atas di SMA Al-Ulum Medan, tamat tahun 1997
RINGKASAN
Malaria merupakan suatu infeksi parasit yang sangat penting dan menjadi salah satu masalah utama kesehatan di dunia, terutama di negara-negara beriklim tropis termasuk Indonesia. WHO melaporkan ada sebanyak 300 juta sampai 500 juta penderita yang menunjukkan gejala klinis malaria setiap tahunnya, dan menimbulkan 0,5 juta sampai 2,5 juta kematian.
Cepatnya penyebaran resistensi terhadap obat antimalaria yang digunakan selama ini merupakan tantangan yang serius dalam strategi pengendalian penyakit malaria, karena hal ini mengakibatkan terjadinya penyebaran malaria ke daerah baru dan munculnya kembali malaria. Salah satu upaya untuk mengurangi cepatnya perkembangan resistensi adalah dengan penggunaan obat secara kombinasi.
Penelitian ini dilakukan untuk mengetahui efikasi kombinasi artesunat-sulfadoksin pirimetamin dan artesunat-doksisiklin dalam pengobatan malaria falciparum. Penelitian ini merupakan uji klinis terbuka secara random, yang dilakukan di kecamatan Teluk Dalam, Lahusa, dan Amandraya, kabupatan Nias Selatan pada bulan September sampai dengan Desember 2006. Sampel penelitian adalah semua penderita malaria falciparum yang diketahui dari pemeriksaan darah tepi dan memenuhi kriteria inklusi. Secara acak sampel dibagi ke dalam dua kelompok penelitian, satu kelompok mendapat artesunat-sulfadoksin-pirimetamin dan kelompok lainnya mendapat artesunat-doksisiklin. Pada hari ke 0, 1, 2, 3, 7, 14, dan 28, dilakukan pemeriksaan darah tepi untuk melihat kepadatan parasit. Pemeriksaan darah rutin untuk hemoglobin, leukosit, eosinofil, trombosit, eritrosit, dan KGD dilakukan pada hari ke 0 dan 14. Kepadatan parasit menurun secara bermakna pada kedua kelompok pengobatan, dimulai sejak H1 dan menghilang pada H3 sampai H28. Pada penelitian ini tidak dijumpai adanya Early Treatment Failure (ETF) dan Late Treatment Failure (LTF), dengan demikian semua subjek penelitian mengalami kesembuhan (100%). Pada pemeriksaan darah rutin, terdapat perbedaan kadar hemoglobin, lekosit, eritrosit, dan trombosit, sebelum dan sesudah pengobatan pada kelompok artesunat-sulfadoksin-pirimetamin. Pada kelompok artesunat-doksisiklin terdapat perbedaan bermakna (p=0,000) kadar eritrosit dan trombosit sebelum dan sesudah pengobatan. Efek samping pemberian artesunat-sulfadoksin-pirimetamin yang terbanyak adalah sakit kepala (44,74%) dan lemas (36,84%). Pada kelompok artesunat-doksisiklin efek samping yang terbanyak adalah gangguan pencernaan (55,56%). Dapat diambil kesimpulan bahwa kombinasi artesunat-sulfadoksin-pirimetamin dan kombinasi artesunat-doksisiklin mempunyai efikasi yang sama terhadap pengobatan malaria falciparum tanpa komplikasi.
SUMMARY
Malaria is an important parasitic infection that become a major health problem in the world, especially in tropical countries, includes Indonesia. WHO reported that there are 300-500 million people that show clinical features of malaria, and caused 0,5 – 2,5 million death annually.
The rapid spread of resistance to anti malaria drugs that had been used these days is a serius challenge in dealing with malaria disease, because this can trigger the spread of malaria into new area and re-arise malaria. One of the ways to decreased the speed of resistance is to use anti malaria drug in combination.
This research is to study the efficacy between artesunate - sulfadoxine-pyrimethamine in combination with artesunate-doxycycline in combination for therapy falciparum malaria. This research is a randomized opened clinical trial, took place in Kecamatan Teluk Dalam, Lahusa and Amandraya, Kabupaten Southern Nias from September to December 2006. The samples were gathered from all patients with falciparum malaria and were done by detecting the peripheral blood swab and match the inclusion criteria. Randomized, the samples were splitted into two study groups, one study group was given combination of artesunate - sulfadoxine-pyrimethamine and another group was given artesunate-doxycycline. Peripheral blood count was done at day 0, 1, 2, 3, 7, 14 and 28 to check parasitic density. Blood routine to check haemoglobin, leukocyte, eosinophil, thrombocyte, erythrocyte and blood sugar level was done at day 0 and 14. Parasitic density decreased significantly in both study groups since day 1 and diminished at day 3 until day 28. In this research, there was no Early Treatment Failure (ETF) and Late Treatment Failure (LTF), and that so all of the samples cured (100%). Blood routine, there was a difference for haemoglobin, erythrocyte and thrombocyte before and after treatment in artesunate - sulfadoxine-pyrimethamine group. In artesunate-doxycycline group, there was a significant difference (p=0,000) for erythrocyte and thrombocyte before and after treatment. Side effect for artesunate - sulfadoxine-pyrimethamine group were headache (44,74%) and malaise (36,84%). In artesunate-doxycycline the of mostly found side effects was enteric discomfort (55,56%). Thus, we can conclude that the combination of artesunate - sulfadoxine-pyrimethamine and combination of artesunate-doxycycline have the same efficacy in treatment for uncomplicated falciparum malaria.
DAFTAR ISI
DAFTAR SINGKATAN ... xii
BAB 1: PENDAHULUAN... 1
2.3.1. Sulfadoksin-pirimetamin... 16
2.3.2. Artesunat... ... 17
2.3.3. Doksisiklin ... 19
2.4. Resistensi Obat Malaria ... 20
2.5. Pengobatan Malaria dengan Kombinasi Obat... 22
3.2.1. Peralatan Pemeriksaan Fiik... 24
3.2.2. Peralatan dan Bahan Laboratorium... 24
3.2.3. Obat-Obatan... 25
3.3. Disain Penelitian ... 25
3.4. Populasi Penelitian... 26
3.4.1 Populasi Terjangkau... 26
3.4.2 Kriteria Inklusi... ... 26
3.4.3 Kriteria Eksklusi ... ... 26
3.4.4 Perkiraan Besar Sampel... .. 27
3.5. Cara Kerja... ... ... 28
3.6. Kerangka Kerja... ... 31
3.7. Kelompok Perlakuan ... 32
3.8. Variabel Yang Diamati... 32
3.8.1 Variabel Tergantung... 32
3.8.2 Variabel Bebas ... 32
3.9. Analisa Data... 32
3.10 Definisi Operasional ... 33
BAB 4 : HASIL DAN PEMBAHASAN ... 36
4.1. Hasil... 36
4.2. Pembahasan... 44
BAB 5 : KESIMPULAN DAN SARAN ... 47
5.1. Kesimpulan... 47
5.2. Saran... 48
DAFTAR PUSTAKA... 49
DAFTAR TABEL
Halaman
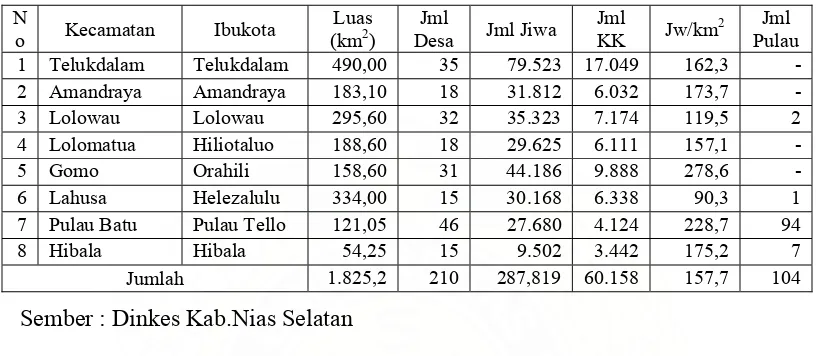
Tabel 1. Kondisi Umum Kabupaten Nias Selatan... 12
Tabel 2. Karakteristik Dasar Sampel Penelitian... 38
Tabel 3. Karakteristik Dasar Sampel Penelitian Berdasarkan
Gejala Klinis dan Tanda Klinis... 39
Tabel 4. Rata-rata Kepadatan Parasit Sebelum dan Sesudah
Pengobatan... 40
Tabel 5. Respon Pengobatan... 41
Tabel 6. Karakteristik Hematologi Sebelum dan Sesudah
Pengobatan... 42
Tabel 7. Distribusi Efek Samping Obat... 43
DAFTAR GAMBAR
Halaman
Gambar 1. Kerangka Konsep Penelitian ... 9
Gambar 2. Peta Kabupaten Nias Selatan... 11
Gambar 3. Sepuluh Besar Data Kesakitan Kabupaten Nias Selatan... 13
Gambar 4. Skema Siklus Hidup Plasmodium Malaria... 15
Gambar 5. Struktur Kimia Sulfadoksin-pirimetamin... 17
Gambar 6. Struktur Kimia Artesunat... 18
Gambar 7. Struktur Kimia Doksisiklin... 20
Gambar 8. Kerangka Kerja Penelitian... 31
Gambar 9. Alur Pemeriksaan Sampel... 37
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Persetujuan Komite Etik Peneltian Bidang Kesehatan... 53
Lampiran 2 Naskah Penjelasan Untuk Mendapatkan Persetujuan Subjek Penelitian ... 54
Lampiran 3 Surat Pernyataan Kesediaan... 56
Lampiran 4 Formulir Anamnesa... 57
Lampiran 5 Formulir Pemeriksaan Fisik Diagnostik... 58
Lampiran 6 Formulir Catatan Medis ... 59
Lampiran 7 Hasil Pemeriksaan Kepadatan Plasmodium... 63
Lampiran 8 Hasil Pemeriksaan Laboratorium Darah Rutin H0 dan H14... 67
DAFTAR SINGKATAN
ACPR : Adequate Clinical and Parasitological Response
AMI : Annual Malaria Incidence
API : Annual Parasite Incidence
AR : Artesunat
BB : Berat Badan
Depkes RI : Departemen Kesehatan Republik Indonesia
Dinkes : Dinas Kesehatan
Dx : Doksisiklin
dkk : dan kawan-kawan
Et al : et alliance
ETF : Early Treatment Failure
FCT : Fever Clearance Time
Hb : Hemoglobin
HIA : High Incidence Area
kg : kilogram
KGD : Kadar Gula Darah
LCF : Late Clinical Failure
LPF : Late Parasitological Failure
LTF : Late Treatment Failure
mg : milligram
PABA : Para Amino Benzoic Acid
PAPDI : Perhimpunan Dokter Spesialis Penyakit Dalam Indonesia
PCD : Passive Case Detection
PCT : Parasite Clearance Time
R I : Resisten tingkat I
R II : Resisten tingkat II
R III : Resisten tingkat III
SP : Sulfadoksin-pirimetamin
SPR : Slide Positivity Rate
SPSS : Statistical Programme for Social Science
USU : Universitas Sumatera Utara
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Malaria merupakan suatu infeksi parasit yang sangat penting dan menjadi salah satu
masalah utama kesehatan di dunia, terutama di negara-negara beriklim tropis termasuk
Indonesia. Ada sekitar 91 negara di dunia merupakan endemik malaria, yang menyerang
hampir 40% dari seluruh populasi dunia, dari jumlah tersebut WHO melaporkan ada
sebanyak 300 juta sampai 500 juta penderita yang menunjukkan gejala klinis malaria
setiap tahunnya, dan menimbulkan 0,5 juta sampai 2,5 juta kematian (Guerin, 2001).
Walaupun upaya penanggulangan malaria sejak lama dilaksanakan, namun dalam
beberapa tahun terakhir daerah endemis malaria bertambah luas dan bahkan di beberapa
dacrah terjadi peningkatan kasus. Di Indonesia, menurut hasil Survei Kesehatan Rumah
Tangga (SKRT) tahun 2001, 70 juta penduduk tinggal di daerah endemik malaria dan
56,3 juta penduduk diantaranya tinggal pada daerah endemik malaria sedang sampai
tinggi. Pada tahun 2003 malaria sudah tersebar di 6053 desa pada 226 kabupaten di 30
propinsi (Depkes, 2004 a).
Angka kejadian malaria masih sangat tinggi, yaitu terdapat 15 juta kasus malaria
dengan 38 ribu kematian setiap tahunnya. Di Jawa dan Bali misalnya, terjadi peningkatan
dari 0,12 per seribu penduduk pada tahun 1997 menjadi 0,81 per seribu penduduk pada
tahun 2003. Sedangkan di luar Jawa-Bali pada tahun 1997, kasus yang malaria meningkat
dari 16,06 per seribu penduduk menjadi 31,09 per seribu penduduk pada tahun 2003
Kabupaten Nias Selatan merupakan pemekaran dari Kabupaten Nias yang terletak
di bagian barat Provinsi Sumatera Utara. Daerah ini merupakan salah satu daerah dengan
angka kejadian malaria yang masih tinggi. Angka ini semakin meningkat akibat
terjadinya bencana tsunami pada akhir tahun 2004 lalu, hal ini disebabkan banyaknya
payau-payau, kolam, dan parit yang tercampur dengan air laut, yang berpotensi sebagai
tempat berkembangbiaknya nyamuk Anopheles. Pada tahun 2005 didapati Annual
Malaria Incidence (AMI) sekitar 124,24 ‰, sehingga Nias Selatan dikategorikan sebagai
High Incidence Area (HIA). Kasus malaria klinis yang diperiksa darahnya selama tahun
2005 sebesar 7,36 % dengan angka Slide Positive Rate (SPR) sebesar 11,46 % dan
spesies yang dominan dijumpai adalah Plasmodium falciparum (Hakim, 2006).
Banyak usaha-usaha yang telah dan tengah dilakukan untuk penanggulangan
penyakit malaria ini. Diantaranya adalah penemuan obat anti malaria. Obat anti malaria
telah banyak dikembangkan dan dijual di pasaran, namun kebanyakan tidak efektif. Hal
ini disebabkan karena parasit menunjukan resistensi yang cepat terhadap obat-obat
tersebut. Cepatnya penyebaran resistensi terhadap obat antimalaria yang digunakan
selama ini merupakan tantangan yang serius dalam strategi pengendalian penyakit
malaria, karena hal ini mengakibatkan terjadinya penyebaran malaria ke daerah baru dan
munculnya kembali malaria (WHO, 2001; Tjitra, 2004).
Klorokuin merupakan salah satu obat anti malaria yang banyak dilaporkan telah
resisten. Kasus resistensi obat anti malaria di Indonesia, terutama klorokuin
penyebarannya tidak merata dan tidak saja terdapat di daerah tertentu, namun semua
Penelitian yang dilakukan pada tahun 2001 terhadap malaria falciparum,
ditemukan resistensi terhadap klorokuin dengan derajat RI (resisten tingkat I), RII
(resisten tingkat II), dan RIII (resisten tingkat III) di Irian Jaya (Taylor dkk, 2001). Pada
tahun 2002 juga dilakukan penelitian di Nusa Tenggara Timur, dan ditemukan kegagalan
pengobatan kasep (late treatment failure) sebesar 69,1% (Sutanto dkk, 2004).
Berdasarkan penelitian yang dilakukan secara in vivo pada tahun 2001, kasus
resistensi terhadap klorokuin juga ditemukan di Sumatera Utara tepatnya di Siabu
Kabupaten Mandailing Natal sebesar 47,5% dan sulfadoksin-pirimetamin sebesar 50%
(Ginting dkk, 2001).
Dari penelitian yang dilakukan di Kampala, Uganda dari tahun 1998-1999
didapatkan kegagalan pengobatan klorokuin terhadap malaria falciparum, dengan clinical
failure sebesar 47% dan parasitological resistance (RI-RIII) sebesar 70% (Dorsey dkk ,
2000).
Selain klorokuin, resistensi terhadap sulfadoksin-pirimetamin juga telah menyebar
luas. Pada tahun 2000 dilakukan penelitian di Kenya, didapatkan bahwa telah terjadi
resistensi sulfadoksin-pirimetamin dengan dengan derajat RI, RII, dan RIII pada
pengobatan malaria falciparum (Vreugdenhil dkk, 2004).
Kebanyakan masalah resistensi ini dikarenakan penggunaan obat dengan half life
yang panjang pada daerah dengan transmisi malaria yang tinggi. Pada daerah tersebut,
akan menguntungkan bila menggunakan obat dengan half life yang pendek, seperti
doksisiklin dan derivat artemisinin (Sponer dkk, 2002).
Salah satu upaya untuk mengurangi cepatnya perkembangan resistensi adalah
obat-obat anti malaria ini juga untuk meningkatkan efek obat-obat-obat-obat bersangkutan secara
sinergis dan aditif, meningkatkan angka kesembuhan, dan mempercepat respon
pengobatan. Untuk wilayah yang resisten klorokuin WHO menganjurkan untuk
melakukan pengobatan dengan kombinasi derivat artemisinin (Bloland, 2001; RBM,
2003; Sutisna, 2004).
Keuntungan penggunaan kombinasi derivat artemisinin ini selain memperlambat
terjadinya resistensi juga karena efikasinya yang tinggi. Efikasi dapat dinilai dari
kemampuan obat untuk membersihkan parasit dalam darah dan menghilangkan gejala
malaria. Efek terhadap gametosit dapat menghambat penyebaran penularan malaria di
daerah dengan tingkat transmisi rendah dan sedang (WHO, 2001).
Penggunaan obat anti malaria berbasis artemisinin di Nias Selatan juga sedang
dikembangkan. Obat-obat tersebut disediakan oleh WHO dan organisasi kesehatan dunia
lainnya, namun penggunaan obat tersebut belum berjalan dengan baik.
Dalam penelitian ini, digunakan kombinasi obat artesunat –
sulfadoksin-pirimetamin sebagai alternatif pengobatan malaria falciparum tanpa komplikasi yang
berbasis artemisinin. Pada suatu penelitian yang dilakukan di Papua, kombinasi artesunat
dengan selfadoksin-pirimetamin pada malaria falciparum menunjukkan adanya
peningkatan efikasi pirimetamin bila dibandingkan dengan
sulfadoksin-pirimetamin sendiri (Tjitra, 2001). Keadaan ini diperkuat dengan dilakukannya suatu
penelitian yang di Afrika pada tahun 1992, dengan membandingkan kombinasi
sulfadoksin-pirimetamin dengan artesunat dan sulfadoksin-pirimetamin sendiri, hasil
artesunat mempunyai efikasi yang tinggi yaitu sebesar 99% dibanding dengan
sulfadoksin-pirimetamin sendiri yaitu sebesar 82% (Dorsey dkk, 2002).
Van den broek dkk, juga melakukan penelitian di Sudan dengan menggunakan
kombinasi obat artesunat dengan sulfadoksin-pirimetamin, hasil yang diperoleh
menunjukkan bahwa efikasi kombinasi obat tersebut mencapai 97-98% ( Van Den Broek
dkk, 2005).
Sejak dahulu antibiotika sudah digunakan sebagai obat anti malaria yang dapat
mengendalikan resistensi, salah satunya adalah doksisiklin. Oleh karena kerja obat ini
lambat maka dalam penggunaannya harus bersama obat anti malaria lain yang kerjanya
cepat (Tjitra, 1993; Pradines dkk, 2001).
Pada penelitian tahun 2001 yang dilakukan di Irian Jaya menunjukkan bahwa
penggunaan kombinasi klorokuin dengan doksisiklin selama 7 hari memberikan angka
kesembuhan yang tinggi (90,9%) terhadap malaria falciparum tanpa komplikasi
dibanding dengan doksisiklin atau klorokuin sendiri (Taylor dkk, 2001).
Doksisiklin juga dapat dikombinasikan dengan kina, kombinasi obat tersebut
pernah diteliti di Brazil dan menunjukkan bahwa terjadi parasite clearance time sebesar
80,2% pada hari kedua, 48,8% pada hari ketiga, dan 7,5% pada hari keempat (Alecrim
dkk, 2006).
Seperti yang direkomendasikan oleh WHO sebagai second line treatment,
doksisiklin juga dikombinasikan dengan artesunat. Kombinasi kedua obat ini pernah
diteliti pada tahun 1994 di Thailand, bahwa kombinasi doksisiklin dengan artesunat
memberikan angka kesembuhan sebesar 80% terhadap malaria falciparum tanpa
Mengingat ketersediaannya yang mudah diperoleh dan harga yang relatif murah di
Indonesia, perlu dilakukan penelitian lebih lanjut untuk melihat keefektifannya.
1.2. Perumusan Masalah
Berdasarkan uraian pada latar belakang, maka dapat dirumuskan permasalahan
sebagai berikut :
Apakah kombinasi artesunat - sulfadoksin-pirimetamin mempunyai efikasi yang
lebih baik dibandingkan dengan kombinasi artesunat-doksisiklin.
1.3. Landasan Teori
Resistensi plasmodium terhadap obat anti malaria merupakan tantangan besar yang
dihadapi dalam upaya pemberantasan malaria. Untuk mencegah resistensi sebaiknya
dimulai dengan memperbaiki protokol pengobatan yang berguna dalam tata laksana dan
pemberian pengobatan yang rasional. Saat ini pengobatan malaria dengan menggunakan
kombinasi obat merupakan pengobatan yang sudah baku (Tjitra, 2000).
Untuk wilayah yang resisten terhadap klorokuin, WHO merekomendasikan untuk
melakukan pengobatan dengan kombinasi derivat artemisinin. Obat kombinasi
artemisinin umumnya merupakan regimen tiga hari. Kombinasi artesunat dengan
sulfadoksin-pirimetamin pada pengobatan malaria falciparum menunjukkan adanya
peningkatan efikasi pirimetamin bila dibandingkan dengan
sulfadoksin-pirimetamin tunggal. WHO juga merekomendasikan kombinasi artesunat dengan
dari dalam darah, hilangnya gejala klinis, dan sedikit efek samping yang ditimbulkan
(WHO, 2006; Looareesuwan dkk, 1994).
Mengingat pemberian sulfadoksin-pirimetamin yang praktis, dan ketersediaan
doksisiklin yang mudah diperoleh dengan harga relatif murah dan belum mengalami
resistensi, untuk itu perlu dilakukan penelitian untuk melihat kombinasi obat artesunat
dengan sulfadoksin-pirimetamin dan doksisiklin.
1.4. Tujuan Penelitian
1.4.1. Tujuan Umum
Untuk mengetahui kombinasi obat yang paling efektif pada pengobatan
malaria falciparum tanpa komplikasi di Nias Selatan.
1.4.2. Tujuan Khusus
- Untuk mengetahui apakah kombinasi artesunat-doksisiklin dapat
digunakan dalam upaya meningkatkan keberhasilan pengobatan malaria
falciparum tanpa komplikasi di Nias Selatan.
- Untuk mengetahui efikasi masing-masing kombinasi obat anti malaria
terhadap malaria falciparum tanpa komplikasi.
1.5. Hipotesis
Kombinasi artesunat - sulfadoksin-pirimetamin lebih efektif dibandingkan dengan
1.6. Manfaat Penelitian
- Untuk mendapatkan terapi alternatif pada pengobatan penderita malaria falciparum
tanpa komplikasi.
- Sebagai masukan ke kalangan praktisi untuk menentukan obat anti malaria yang
lebih efektif pada pengobatan malaria falciparum tanpa komplikasi.
- Sebagai acuan dalam perencanaan penyediaan obat-obat anti malaria alternatif oleh
sarana-sarana kesehatan.
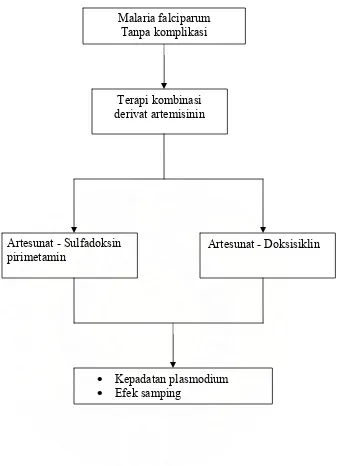
1.7. Kerangka Konsep
Dari landasan teori yang telah diuraikan, maka dapat disusun kerangka konsep
Artesunat - Sulfadoksin pirimetamin
Artesunat - Doksisiklin Terapi kombinasi
derivat artemisinin Malaria falciparum
Tanpa komplikasi
• Kepadatan plasmodium
• Efek samping
BAB 2
TINJAUAN PUSTAKA
Malaria merupakan masalah kesehatan dibanyak negara diseluruh dunia, terutama
di negara sedang berkembang yang beriklim tropis, termasuk Indonesia. Walaupun
program pelaksanaan dan pemberantasan penyakit malaria sejak lama telah dilakukan,
namun hingga saat ini angka kesakitan dan kematiannya masih cukup tinggi (Gunawan,
2000).
Malaria adalah penyakit infeksi sistemik yang disebabkan oleh parasit jenis
protozoa dari genus Plasmodium, yang ditularkan melalui gigitan nyamuk Anopheles
betina. Malaria juga dapat ditularkan secara langsung melalui transfusi darah, jarum
suntik, serta dari ibu hamil kepada bayinya. Penduduk yang paling beresiko terkena
malaria adalah anak balita, wanita hamil, dan penduduk yang mengunjungi daerah
endemik malaria (Gunawan, 2000).
Plasmodium yang dapat mengenai manusia adalah Plasmodium falciparum
(P.falciparum), Plasmodium malariae (P.malariae), Plasmodium vivax (P.vivax), dan
Plasmodium ovale (P.ovale). P. falciparum merupakan jenis plasmodium yang paling
2.1. Data Umum Kabupaten Nias Selatan
Kabupaten Nias Selatan adalah salah satu kabupaten di Sumatera Utara yang
terletak di Pulau Nias. Ibukota Nias Selatan adalah Teluk Dalam, terletak 0012’-103 LU
dan 970-980 BT dengan luas wilayah 1.825,2 km2. Kabupaten ini terdiri dari 104 gugusan
pulau besar dan kecil. Letak pulau-pulau tersebut memanjang sejajar Pulau Sumatera,
dengan panjang lebih kurang 60 km dan lebar 40 km. Dari seluruh gugusan pulau
tersebut, ada empat pulau besar, yaitu Pulau Tanah Bala (39,67 km2), Pulau Tanah Masa
(32,16 km2), Pulau Tello (18 km2), dan Pulau Pini (24,36 km2). Masyarakat Nias Selatan
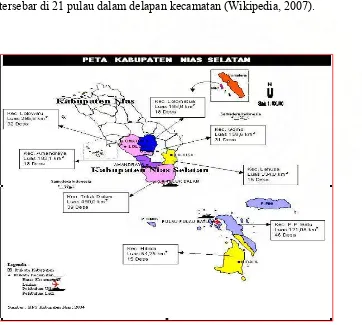
tersebar di 21 pulau dalam delapan kecamatan (Wikipedia, 2007).
Gambar 2. Peta Kabupaten Nias Selatan
Berdasarkan data dari Dinas Kesehatan Kabupaten Nias Selatan, jumlah penduduk
terhadap perempuan adalah 0,91 serta jumlah keluarga adalah 60.158 KK, dengan
demikian maka kepadatan penduduknya adalah 157,7 jiwa per km2. Kelompok umur
yang dominan adalah usia 15-44 tahun (Dinkes Kab.Nias Selatan).
Tabel 1. Kondisi Umum Kabupaten Nias Selatan
N
Sember : Dinkes Kab.Nias Selatan
Pada Maret 2005, gempa melanda kepulauan Nias yang mengakibatkan terjadinya
perubahan jumlah serta sosial ekonomi masyarakat serta lingkungan yang pada akhirnya
akan meningkatkan risiko terjadinya penularan penyakit infeksi. Salah satu penyakit
menular yang diperkirakan akan mengalami peningkatan pasca bencana adalah malaria.
Pada tahun 2005 terjadi peningkatan nilai AMI melebihi tahun sebelumnya yaitu dari
105‰ menjadi 124,24‰ (Hakim, 2006).
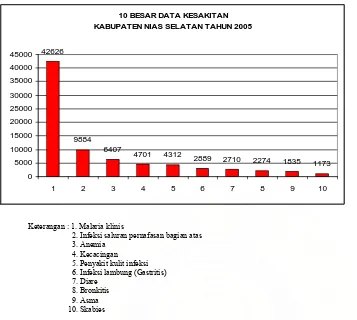
Pada tahun 2005, berdasarkan data sepuluh besar penyakit di Kabupaten Nias
Selatan, penyakit yang paling banyak dijumpai adalah malaria klinis yakni sebayak
10 BESAR DATA KESAKITAN
Keterangan : 1. Malaria klinis
2. Infeksi saluran pernafasan bagian atas
Gambar 3. Sepuluh Besar Data Kesakitan Kabupaten Nias Selatan Tahun 2005
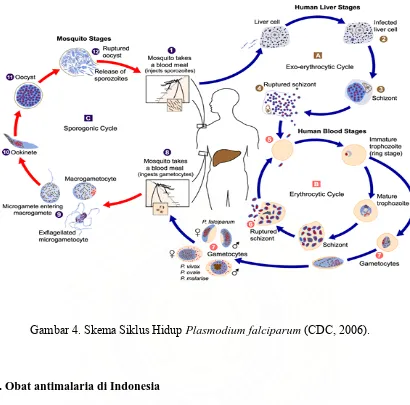
2.2. Siklus Hidup Plasmodium Malaria
Plasmodium mempunyai dua hospes dalam siklus hidupnya yaitu pada manusia dan
nyamuk. Siklus yang berlangsung pada tubuh manusia disebut siklus aseksual atau
skizogoni, dan siklus yang berlangsung pada nyamuk disebut siklus seksual atau
sporogoni.
2.2.1. Siklus aseksual
Proses penyebarannya adalah dimulai nyamuk Anopheles yang mengandung
membentuk skizon jaringan dalam sel hati (eksoeritrositer). Setelah sel hati pecah keluar
merozoit, masuk ke eritrosit, parasit tampak sebagai kromatin kecil, dikelilingi
sitoplasma yang membesar, bentuk tidak teratur dan membentuk tropozoit. Tropozoit
berkembang menjadi skizon muda, kemudian berkembang menjadi skizon matang dan
membelah banyak menjadi merozoit dalam eritrosit (eritrositer). Eritrosit pecah kemudian
merozoit, pigmen dan sisa sel keluar, sebagian besar merozoit masuk kembali ke eritrosit
dan sebagian membentuk gametosit jantan dan betina (bentuk seksual) yang siap dihisap
oleh nyamuk (Nugroho, 2000; CDC, 2006).
2.2.2. Siklus seksual
Di dalam tubuh nyamuk terjadi perkawinan antara sel gamet jantan dan betina yang
kemudian membentuk zigot. Zigot berubah menjadi ookinet, yang kemudian masuk
menembus lapisan epitel dan membran basal lambung nyamuk. Di dalam lambung
nyamuk ini ookinet berubah menjadi ookista. Di dalam ookista dibentuk ribuan sporozoit
yang kemudian matang dan pecah, keluar sporozoit dan masuk ke kelenjar liur nyamuk
Gambar 4. Skema Siklus Hidup Plasmodium falciparum (CDC, 2006).
2.3. Obat antimalaria di Indonesia
Saat ini obat-obatan anti malaria yang ada dan telah dipakai di Indonesia adalah
klorokuin, sulfadoksin-pirimetamin, kina, dan primakuin. Di samping itu terdapat
beberapa obat yang terdaftar sebagai antibiotika di Indonesia tetapi dapat juga bekerja
sebagai anti malaria seperti derivat tetrasiklin, doksisiklin, klindamisin, eritromisin,
kloramfenikol, azitromisin, sulfametoksasol-trimetoprim dan kuinolon. Obat ini
umumnya bersifat skizontosida darah untuk P.falciparum, kerjanya sangat lambat. Oleh
sebab itu, obat ini digunakan bersama obat anti malaria lain yang kerjanya cepat dan
2.3.1. Sulfadoksin-pirimetamin
Sulfadoksin-pirimetamin merupakan obat anti malaria kombinasi antara
sulfonamida/sulfon dengan diaminopirimidin yang bersifat skizontosida jaringan
P.falciparum, skizontosida darah dan sporontosida untuk keempat jenis Plasmodium
manusia (Tjitra, 2000).
Sulfadoksin bekerja berkompetisi dengan paraamino benzoic acid (PABA), dengan
menghambat enzim dihydropteroate synthase sehingga pembentukan asam folat
terganggu. Asam folat dibutuhkan oleh parasit untuk pembentukan asam nukleat yang
berguna untuk pembentukan inti parasit. Pirimetamin bekerja dengan menghambat enzim
dihydrofolate reductase dari plasmodium sehingga secara tidak langsung akan
menghalangi pembentukan asam nukleat pada parasit malaria (Tjitra, 2000; WHO, 2006).
Obat ini dengan cepat diabsorbsi dari saluran pencernaan, berikatan dengan plasma
protein kemudian dimetabolisme di hati dan diekskresikan melalui urin. Konsentrasi
puncak dalam darah dicapai dalam 2 – 4 jam, dengan waktu paruh sulfonamida adalah
180 jam dan pirimetamin adalah 90 jam. Obat ini dapat melalui plasenta dan dapat
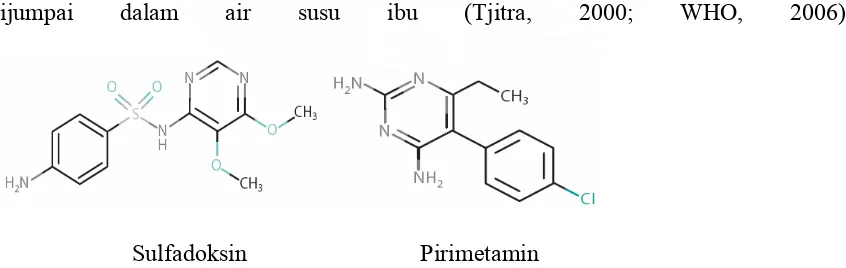
dijumpai dalam air susu ibu (Tjitra, 2000; WHO, 2006).
Sulfadoksin Pirimetamin
Sulfadoksin-pirimetamin dikemas dalam bentuk tablet untuk pemberian per-oral
dan setiap tabletnya mengandung 500 mg sulfadoksin atau sulfalen dan 25 mg
pirimetamin. Dosis yang diberikan untuk pengobatan malaria falciparum tanpa
komplikasi adalah sulfadoksin 25 mg/kgBB dan pirimetamin 1,25 mg/kgBB dosis
tunggal (Tjitra, 1993; WHO, 2006).
Obat ini sangat praktis karena dapat diberi dalam dosis tunggal, namun obat ini
mempunyai kelemahan karena mudah mengalami resisten. Oleh karena itu, kombinasi
obat ini digunakan secara selektif untuk pengobatan radikal malaria falciparum di daerah
yang resisten terhadap klorokuin. Efek samping yang pernah dilaporkan adalah kulit
kemerahan dengan gatal dan sindroma Steven Johnson (Tjitra, 1993; Tjitra, 2000).
2.3.2. Artesunat
Artesunat merupakan obat anti malaria yang bersifat skizontosidal dan gametosidal.
Obat ini bekerja dengan cara menghambat enzim calcium adenosine triphosphatase,
yaitu dengan melepaskan gugus peroksida yang dipicu adanya Fe2+. Fe2+ merupakan hasil
pemecahan hemoglobin yag dilakukan oleh Plasmodium. Gugus peroksida yang terlepas
bekerja untuk menghancurkan Plasmodium. Obat ini tersedia dalam bentuk tablet untuk
pemberian peroral, bentuk serbuk kering dalam ampul dengan pelarut 5% NaHCO3 untuk
pemberian secara parenteral (intravena atau intramuskular), dan bentuk kapsul rektal
(suppositories) untuk pemberian per-rektal. Satu tablet mengandung 50 mg artesunat,
satu ampul mengandung 60 mg artesunat yang dilengkapi dengan 0,6 ml larutan 5%
NaHCO3, dan satu kapsul rektal mengandung 100 mg atau 400 mg artesunat (Krisna,
Artesunat cepat diabsorbsi, dengan konsentrasi plasma puncak 1,5 jam pada
pemberian oral, 2 jam pada pemberian per-rektal, dan 0,5 jam pada pemberian intra
muskular. Waktu paruh artesunat peroral adalah 4-8 jam, sedangkan parenteral
diperkirakan hanya 48 menit (Tjitra, 2000; WHO, 2006).
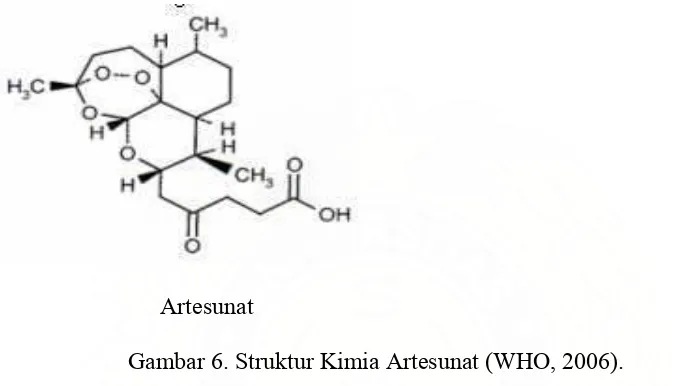
Artesunat
Gambar 6. Struktur Kimia Artesunat (WHO, 2006).
Dosis untuk pengobatan tunggal malaria falciparum tanpa komplikasi yang resisten
multidrug, peroral adalah 2 mg/kgBB/dosis, 2 kali sehari pada hari pertama, kemudian
dilanjutkan 2 mg/kg BB dosis tunggal pada 4 hari selanjutnya. Sedangkan dosis untuk
pengobatan kombinasi adalah 4 mg/kg BB dosis tunggal selama 3 hari (WHO, 1997).
Efek samping yang pernah dilaporkan adalah gangguan saluran pencernaan berupa
mual dan muntah, bercak merah di kulit, gatal-gatal, rambut rontok dan demam obat
(Tjitra, 2000; WHO, 1997).
2.3.3. Doksisiklin
atau kapsul mengandung 100 mg doksisiklin hiklat atau doksisiklin hidroklorida. Selain
digunakan untuk pengobatan malaria di daerah resisten multidrug dalam kombinasi
dengan obat antimalaria lainnya, seperti kina, meflokuin, atau artesunat. Doksisiklin
dapat juga digunakan untuk profilaksis malaria di daerah yang resisten terhadap
meflokuin (Tjitra, 2000).
Doksisiklin bekerja dengan menghambat pembentukan sintesa protein, yaitu dengan cara mengikat tRNA yang berfungsi sebagai pengangkut asam amino. Hampir secara keseluruhan doksisiklin diabsorbsi di saluran pencernaan. Konsentrasi plasma puncak dicapai sekitar 2 jam setelah pemberian. Sekitar 80-95% berikatan protein dengan waktu paruh 10-24 jam. Umumnya diekresikan melalui feses, pada penderita dengan fungsi ginjal yang baik 40% diekresikan melalui urin (WHO, 2006).
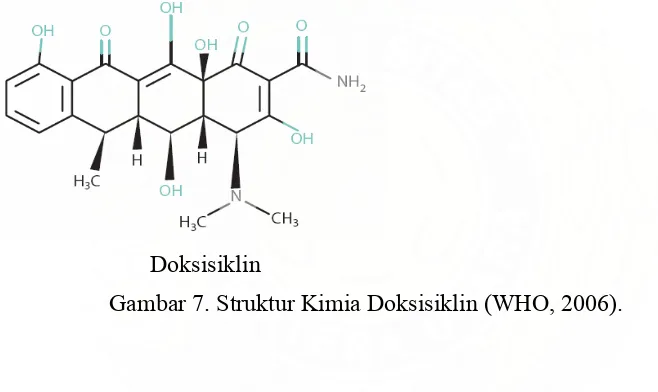
Doksisiklin
Gambar 7. Struktur Kimia Doksisiklin (WHO, 2006).
Dosis doksisiklin untuk profilaksis malaria 1,5 mg/kgBB/hari, dosis tunggal.
Sedangkan dosis pengobatan untuk orang dewasa adalah 2 mg/kgBB/dosis, diberikan 2
kali sehari selama 7 hari. Doksisiklin tidak diberikan pada wanita hamil dan menyusui,
serta anak-anak dibawah 8 tahun.
Efek samping yang pernah dilaporkan adalah gangguan saluran pencernaan dan
2.4. Resistensi Obat Malaria
Resistensi obat anti malaria adalah kemampuan parasit untuk terus hidup dalam
tubuh manusia, berkembang biak dan menimbulkan gejala penyakit walaupun telah
diberikan pengobatan secara teratur baik dengan dosis standar maupun dosis yang lebih
yang lebih tinggi, yang masih bisa ditolerir oleh pemakai obat. Pada saat ini resistensi
Plasmodium terhadap obat anti malaria merupakan tantangan besar yang dihadapi dalam
upaya pemberantasan malaria (Tjitra, 2000; Bloland, 2001).
Secara umum resistensi terjadi karena mutasi spontan yang dapat mengurangi
sensitivitas obat. Mutasi ini sendiri tidak menyebabkan kemampuan hidup atau
perkembangbiakan parasit menjadi meningkat, tetapi menekan pengaruh obat terhadap
parasit. Untuk beberapa obat, hanya perlu satu tempat mutasi untuk membuat resisten,
sementara untuk obat-obat lain diperlukan beberapa tempat mutasi. Pemberian obat akan
menghilangkan parasit yang lemah, sementara parasit yang resisten akan tetap hidup.
(Bloland, 2001; Tjitra, 2004).
Resistensi P.falciparum terhadap klorokuin pertam kali dilaporkan pada tahun 1961
oleh Moore dan Lanier di Kolombia, Amerika Selatan. Sejak itu dilaporkan pula
kasus-kasus dari Brazil, Guyana, Suriname,Venezuela, Bolivia dan Panama. Di Asia Tenggara
resistensi dilaporkan untuk pertama kali di Muangthai pada tahun 1961, kemudian
berturut-turut di Malaysia tahun 1962, Kamboja tahun 1964, Laos tahun 1964, Vietnam
tahun 1967, Filipina tahun 1970, Birma tahun 1971 dan Sabah tahun 1972 (Pribadi,
1980).
malaria yang penderitanya resisten terhadap obat anti malaria semakin meluas. Hingga
tahun 1996 telah ditemukan resistensi P.falciparum terhadap klorokuin dengan derajat
yang berbeda di semua propinsi. P.falciparum yang resistensi terhadap
sulfadoksin-pirimetamin secara in vivo dan in vitro juga telah ditemukan antara lain di 11 propinsi di
Sumatera, Jawa, Kalimantan, Sulawesi, dan Irian Jaya (Depkes RI, 2003 ; Tjitra, 2000).
Kecepatan penyebaran resistensi Plasmodium terhadap obat anti malaria berbeda
pada masing-masing daerah atau negara. Beberapa faktor yang dapat menimbulkan
resistensi adalah penggunaan dosis obat yang tidak tepat pada pengobatan malaria.
Minum obat yang tidak benar, seperti kurangnya kepatuhan penderita, kualitas obat yang
jelek, intensitas transmisi malaria, dan imunitas yang rendah juga memudahkan
terjadinya resistensi (Bloland, 2001).
2.5. Pengobatan Malaria dengan Kombinasi Obat
Pengobatan kombinasi adalah pengobatan dua atau lebih obat anti malaria secara
simultan dimana masing-masing obat mempunyai cara kerja yang independen dan
mempunyai target biokimia yang berbeda pada parasit. Obat-obat kombinasi ini harus
mempunyai cara kerja yang berbeda dan mekanisme terjadinya resistensi juga harus
berbeda. Selain itu masing-masing obat yang dikombinasi harus mempunyai batas efikasi
minimal 75% (PAPDI, 2003; Tjitra, 2004).
Obat anti malaria kombinasi di Indonesia yang ideal harus aman dan toleran untuk
semua kelompok umur, efektif dan cepat, respon pengobatannya baik untuk semua jenis
Plasmodium, singkat waktu pengobatannya, belum mengalami resistensi, dan terjangkau.
masing-masing obat tersebut, meningkatkan angka kesembuhan, mempercepat respon
pengobatan, dan mencegah berkembangnya resistensi (Tjitra, 2004).
Secara umum kombinasi obat anti malaria dikelompokkan menjadi kombinasi obat
anti malaria artemisinin dan non artemisinin. Mulai tahun 2004 untuk daerah yang
resisten klorokuin, WHO menganjurkan untuk melakukan pengobatan dengan kombinasi
derivat artemisinin. Pada saat ini penggunaan kombinasi derivat arrtemisinin telah
terbukti efektif dalam mengurangi morbiditas dan mortalitas akibat penyakit malaria
BAB 3
METODOLOGI PENELITIAN
3.1. Tempat dan Waktu Penelitian
Penelitian dilakukan di Kecamatan Teluk Dalam, Lahusa, dan Amandraya,
Kabupatan Nias Selatan pada bulan September sampai dengan Desember 2006.
3.2. Alat dan Bahan
3.2.1. Peralatan Pemeriksaan Fisik dan Klinis
Pada subjek penelitian dilakukan pemeriksaan fisik dan klinis dengan menggunakan
peralatan : termometer suhu tubuh, timbangan badan, stetoskop.
3.2.2. Peralatan dan Bahan Laboratorium
Peralatan dan bahan laboratorium yang dibutuhkan adalah : mikroskop object glass,
cover glass, slide box, hemolet, rak pewarnaan, kapas, kertas tissue, pipet tetes, pipet 10
ml, gelas ukur (10 ml dan 100 ml), aquadest, baker glass (100 ml dan 500 ml),
tabung reaksi, hair dryer, minyak imersi, larutan Giemsa, metanol, alkohol dan larutan
buffer.
3.2.3. Obat-obatan
1. Artesunat 50 mg, merupakan produksi dari Beijing Wanhui Double Crane
Pharmaceutical yang diimpor oleh PT. Trimitra Sehati, Indonesia dengan nomor
Batch 050406, tanggal produksi 08042006, dan tanggal kadaluarsa 04/2009.
2. Sulfadoksin-pirimetamin, yang merupakan kombinasi antara sulfonamida/
sulfalen dengan diaminopirimidin, mengandung 500 mg sulfadoksin dan 25 mg
pirimetamin. Sediaan ini merupakan sediaan generik buatan PT. Indofarma,
nomor Batch 0505005, dan tanggal kadaluarsa 06/2009.
3. Doksisiklin 100 mg, merupakan sediaan generik buatan PT. Indofarma, nomor
Batch C0305 LJ, tanggal kadaluarsa 06/2010.
4. Parasetamol 500 mg buatan PT. Indofarma, diberikan sebagai pengobatan
simptomatis bila suhu aksila >38,50C.
3.3 Desain Penelitian
Penelitian dilakukan dengan uji klinis terbuka (open trial) secara random.
3.4. Populasi Penelitian
3.4.1. Populasi Terjangkau
Penderita dengan gejala demam dan atau riwayat demam dalam satu minggu terakhir
dan dijumpai P.falciparum pada sediaan darah tepi selama periode penelitian.
3.4.2. Kriteria Inklusi
1. Umur > 14 tahun, laki-laki dan perempuan.
3. Suhu aksila ≥ 37,50C atau dengan riwayat demam dalam 1 minggu terakhir.
4. Tidak mengkonsumsi obat antimalaria dalam 2 minggu terakhir, diketahui dari
anamnesa.
5. Bersedia ikut dalam penelitian dan mengikuti prosedur yang telah ditetapkan
(informed consent).
3.4.3. Kriteria Eksklusi
1. Dijumpai Plasmodium jenis lain selain falciparum pada pemeriksaan darah tepi.
2. Hamil dan menyusui.
3. Ada gangguan fungsi hati, ginjal, dan jantung yang berat yang diketahui dari
anamnesa, pemeriksaan fisik diagnostik dan laboratorium.
4. Ada riwayat alergi terhadap obat antimalaria yang digunakan dan muncul reaksi
alergi terhadap obat yang digunakan sewaktu penelitian berlangsung.
5. Terdapat gejala dan tanda malaria berat.
6. Mengundurkan diri dari penelitian sewaktu penelitian berlangsung.
3.4.4. Perkiraan Besar Sampel (Sudigdo, 2002)
Jumlah sampel minimal untuk penelitian dihitung menurut rumus di bawah ini
n1 = n2 =
(
)
P1 : Proporsi kesembuhan penderita malaria falciparum tanpa komplikasi dengan
P2 : Proporsi kesembuhan penderita malaria falciparum tanpa komplikasi dengan
artesunat dan doksisiklin = 80% (Looareesuwan, dkk, 1994).
Q1 = 1 - P1 = 0,01 Q2 = 1 – P2 = 0,20
P = ½ ( P1 + P2 ) = 0,895 Q = 1 – P = 0,105
= 0,05 Z = 1,645
= 0,20 Z = 0,842
Dari perhitungan di atas didapatkan besarnya sampel pada masing-masing
kelompok yaitu minimal 31 orang. Untuk mengantisipasi angka drop out, direncanakan
jumlah sampel sebesar 38 orang untuk tiap kelompok pengobatan, yang dipilih dengan
cara random sederhana.
3.5. Cara kerja
Penderita yang ditemukan di lapangan dengan keluhan demam atau riwayat demam
dalam satu minggu terakhir dengan atau tanpa gejala klinis malaria, dilakukan
pemeriksaan yang meliputi anamnesa, pemeriksaan fisik dan pemeriksaan darah tepi
malaria sediaan tebal dan tipis, untuk menghitung kepadatan parasitnya. Sebelumnya
penderita diminta untuk mengisi formulir persetujuan ikut dalam penelitian dan
ditandatangani oleh penderita atau orang tua penderita.
Pada pemeriksaan sediaan tebal darah diambil dari jari tangan penderita yang
sebelumnya dibersihkan dengan alkohol 70%, kemudian diletakkan di atas gelas objek
dan dikeringkan, diwarnai dengan pewarnaan Giemsa 10% dalam larutan buffer pH 7,1
Pada sediaan darah tipis, cara pengecatannya sama dengan pemeriksaan darah tebal tetapi
sebelum dilakukan pengecatan sediaan darah difiksasi dengan metanol (Harijanto, 2000).
Penderita yang memenuhi kriteria inklusi akan diambil sebagai subjek penelitian.
Kemudian secara random dibagi menjadi dua kelompok, satu kelompok diberi kombinasi
artesunat – sulfadoksin-pirimetamin dan kelompok lainnya diberi kombinasi
artesunat-doksisiklin. Obat diminum pada hari pertama pengobatan, sesuai dengan kelompok
pengobatan dan diawasi pemberiannya. Apabila setengah jam setelah pemberian obat
penderita muntah, maka obat akan diberikan kembali dengan dosis yang sama. Penderita
malaria yang tidak memenuhi kriteria inklusi tetap diberikan pengobatan malaria sesuai
dengan standar pengobatan, dan bila bukan menderita malaria maka akan diobati sesuai
dengan penyakit yang dideritanya. Penderita dengan suhu >38,50C diberikan tablet
parasetamol 500 mg dengan dosis 3 x 1 tablet. Sebelum dilakukan pengobatan, maka
terlebih dahulu diberikan penjelasan kepada penderita tentang kegunaan obat dan efek
samping yang dapat terjadi. Penderita yang menjadi subjek penelitian akan diberikan
catatan mengenai jadwal pemeriksaan berikutnya.
Setiap penderita dari masing-masing kelompok pengobatan akan dinilai respon
klinisnya, yaitu ETF, LTF, dan ACPR.
Kepadatan parasit diperiksa pada hari ke 0, 1, 2, 3, 7, 14, dan 28, penderita diminta
datang kembali untuk dilakukan pemeriksaan darah tepi. Apabila penderita tidak datang
sesuai dengan hari yang ditentukan maka akan dikunjungi kekediamannya. Semua
sediaan darah tepi penderita yang diteliti, dikonfirmasi ke bagian Parasitologi FK-USU
untuk didiagnosa spesies Plasmodium dan dihitung kepadatan parasitnya. Kepadatan
Pemeriksaan fisik dilakukan pada hari ke 0, 1, 2, 3, 7, 14, dan 28, dengan mengukur
suhu tubuh, serta mengukur besar limpa dengan metode Hackett
Pemeriksaan darah rutin untuk hemoglobin, leukosit, eosinofil, trombosit, eritrosit,
dan KGD pada hari ke 0 dan 14.
Selama masa pengobatan penderita di pantau terhadap kepatuhan minum obat, efek
samping yang terjadi akibat obat yang diberikan, maupun komplikasi malaria. Apabila
selama pemantauan terjadi efek samping akibat pemakaian obat, maka penderita akan
diberikan obat simptomatis untuk menghilangkan gejala akibat efek samping tersebut.
Apabila penderita menunjukkan tanda malaria berat atau terjadi komplikasi malaria,
maka penderita dikeluarkan dari penelitian dan dirawat di puskesmas atau rumah sakit
serta diberikan pengobatan malaria dengan menggunakan kina HCl perinfus, dengan cara
loading dose 20 mg/kgBB dalam dekstrosa 5% atau NaCl fisiologis diberikan dalam 4
jam. Dilanjutkan dengan 10 mg/kgBB dalam 4 jam setiap 8 jam berikutnya sampai
3.6.Kerangka Kerja .6.Kerangka Kerja
Gambar 8. Kerangka Kerja Penelitian Gambar 8. Kerangka Kerja Penelitian
pemeriksaan fisik hari ke
3.7. Kelompok Perlakuan
Penelitian ini terdiri dari 2 kelompok perlakuan sebagai berikut :
1. Kelompok I : diberikan kombinasi artesunat dengan sulfadoksin pirimetamin,
dosis artesunat 1x 4 tablet selama 3 hari , dosis sulfadoksin-pirimetamin 1x3
tablet pada hari pertama.
2. Kelompok II : diberikan kombinasi artesunat dengan doksisiklin, dosis
artesunat 1x 4 tablet selama 3 hari, dosis doksisiklin 2x 1 kapsul selama 7
hari.
3.8. Variabel yang diamati
3.8.1. Variabel Tergantung
Variabel tergantung adalah Plasmodium falciparum.
3.8.2. Variabel Bebas
Variabel bebas adalah kelompok perlakuan / pengobatan.
3.9. Analisa Data
Analisa statistik dilakukan dengan menggunakan program SPSS versi 10.0.
- Untuk melihat perbedaan kepadatan parasit dan komponen hematologi sebelum
dan sesudah pengobatan antar kelompok, digunakan uji t tidak berpasangan bila
data berdistribusi normal, tetapi bila data tidak berdistribusi normal maka
digunakan uji Mann-Whitney.
digunakan adalah uji t berpasangan bila data berdistribusi normal. Sementara itu
bila data tidak berdistribusi normal maka digunakan uji Wilcoxon.
- Untuk melihat efek samping pengobatan pada kedua kelompok dilakukan
dengan menggunakan uji Chi-square.
3.10. Definisi Operasional
1. Penderita malaria falciparum tanpa komplikasi adalah penderita dengan gejala klinis
malaria dan pada pemeriksaan darah tepi dengan metode standar ditemukan bentuk
P.falciparum aseksual dan penderita tidak menunjukkan tanda dan gejala malaria
berat sejak awal pemeriksaan sampai selesai pengobatan.
2. Malaria berat adalah suatu kondisi malaria dengan faktor pemberat seperti :
penurunan kesadaran, anemia berat (Hb < 5 gr % atau hematokrit < 15%), gagal
ginjal akut (urine < 400 ml/24 jam atau < 12 ml/kgBB atau kreatinin > 3 mg %),
edema paru, hipoglikemia ( KGD < 40 mg%), syok, perdarahan spontan, kejang,
hemoglobinuria, hiperparasitemia > 5% pada daerah hipoendemik, ikterus (bilirubin >
3 mg% dan hiperpireksia (temperatur rektal > 400C).
3. Pemeriksaan apusan darah tepi adalah tehnik pemeriksaan standar untuk menegakkan
diagnosa malaria, yaitu dengan menentukan Plasmodium dalam darah penderita.
4. Kepadatan parasit adalah jumlah Plasmodium per-200 lekosit atau per-1000 eritrosit
yang ditemukan pada pemeriksaan apusan darah tepi.
5. H0 adalah hari pertama pengamatan dan didiagnosa sebagai penderita malaria.
6. H1,H2,H3,H7,H14,H28 adalah hari ke-n pemberian obat dan pengamatan lanjutan
7. Parasite Clearance Time (PCT) adalah lamanya waktu yang diperlukan sampai tidak
ditemukannya lagi plasmodium dalam bentuk aseksual dalam darah penderita.
8. Demam adalah suatu kenaikan suhu tubuh >37,50C yang diukur dengan termometer
pada aksila.
9. Anemia adalah suatu penurunan kadar Hb darah di bawah nilai standar normal yang
diukur dengan menggunakan metode cyan.
10.Komponen hematologi pasien diperoleh dengan melakukan pemeriksaan darah rutin
untuk melihat kadar leukosit, trombosit, eosinofil, eritrosit dan beberapa komponen
darah lainnya.
11.Hipoglikemi adalah suatu keadaan penurunan kadar gula darah < 40 mg%.
12.Ukuran limpa adalah hasil pengukuran limpa secara palpasi dengan metode Hackett:
- Hackett 0 (H.0) : tidak teraba pada inspirasi maksimal.
- Hackett 1 (H.1) : limpa teraba pada inspirasi maksimal.
- Hackett 2 (H.2) : limpa teraba dari garis datar bawah arcus kosta sampai setengah
antara arkus kosta dan umbilikus pada garis mammilaris kiri.
- Hackett 3 (H.3) : limpa teraba antara garis setengah kosta-umbilikus sampai garis
datar umbilikus.
- Hackett 4 (H.4) : limpa teraba dari garis datar umbilikus sampai setengah
umbilikus dan simfisis pubis.
- Hackett 5 (H.5) : limpa teraba di bawah garis H.4
13.Early Treatment Failure (ETF), bila terjadi salah satu kriteria di bawah ini :
a. Ditemukan tanda-tanda bahaya / malaria berat pada HI, H2, dan H3 serta dijumpai
b. Kepadatan parasit (parasitemia) pada H2 > H0.
c. Kepadatan parasit (parasitemia) pada H3 ≥ 25% H0.
14. Late Treatment Failure (LTF), dibagi atas dua golongan, yaitu :
a. Late Clinical and Parasitological Failure (LCPF)
Bila terjadi salah satu kriteria di bawah ini pada hari ke 4 sampai ke 28 :
Terjadi gejala malaria berat
Masih terdapat gametosit disertai demam (>37,50C)
b. Late Parasitological Failure (LPF)
Bila masih terdapat parasit bentuk aseksual pada hari ke 7, 14, 21 dan 28
walaupun tidak disertai dengan demam.
15. Adequate Clinical and Parasitological Response (ACPR)
Penderita yang pada kunjungan ulangan/kontrol (H3, H7, dan H28) tidak ada keluhan
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil
Pada penelitian ini dilakukan pemeriksaan pada 826 orang penduduk. Dari jumlah
penduduk yang diperiksa, hanya 723 orang yang menderita demam atau riwayat demam
satu minggu terakhir yang bersedia untuk dilakukan pemeriksaan darah. Dari jumlah
tersebut 412 orang penduduk tidak menderita malaria, 311 orang menderita malaria
dimana 238 orang terinfeksi P.falciparum, 7 orang terinfeksi P.vivax, dan 66 orang
terinfeksi P.falciparum dan P. vivax.
Dari 238 orang menderita malaria falciparum yang memenuhi kriteria inklusi
sebanyak 83 orang, kemudian dengan random sederhana dibagi menjadi dua kelompok.
Kelompok artesunat - sulfadoksin-pirimetamin (Ar-SP) sebanyak 46 orang, dan
kelompok artesunat - doksisiklin (Ar-Dx) sebanyak 37 orang.
Sampai akhir penelitian 4 orang dikeluarkan dari penelitian pada kelompok Ar-SP,
dan 6 orang dari kelompok Ar-Dx karena tidak minum obat dan tidak bersedia
memeriksa darah ulangan pada hari yang telah ditentukan. Jumlah sampel sampai akhir
penelitian sebanyak 73 orang, yaitu 42 orang pada kelompok Ar-SP dan 31 orang pada
Pasien yang diperiksa
Pasien pada awal pemeriksaan 46 orang
Kombinasi Artesunat+Doksisiklin 37 orang
Pasien pada awal pemeriksaan 37 orang
Pasien pada akhir pemeriksaan 42 orang
Pasien pada akhir pemeriksaan 31 orang
Eksklusi 6 orang Eksklusi 4 orang
Tabel 2. Karakteristik Dasar Sampel Penelitian
Keterangan : Ar : Artesunat SP : Sulfadoksin-pirimetamin Dx : Doksisiklin a)
Berdasarkan tabel 2 di atas, distribusi sampel penelitian menurut umur dibagi
menjadi lima kelompok, didapati bahwa sampel penelitian terbanyak pada kelompok
umur ≥ 55 tahun (28,57%) pada kelompok Ar-SP dan 29,03% pada kelompok Ar-Dx.
Jumlah sampel penelitian berdasarkan jenis kelamin didapati bahwa pada kelompok
Ar-SP didominasi oleh wanita (69,05%), sedangkan pada kelompok Ar-Dx jumlah
sampel pria dan wanita hampir tersebar merata, pria (51,61%) dan wanita (48,39%).
Dengan menggunakan uji statistik untuk melihat perbandingan antar kedua kelompok,
tidak dijumpai perbedaan bermakna karakteristik dasar sampel penelitian pada kedua
Tabel 3. Karakteristik Dasar Sampel Penelitian Berdasarkan Gejala Klinis dan
Keterangan : Ar : Artesunat SP : Sulfadoksin-pirimetamin Dx : Doksisiklin
b)
Uji Chi-square
* Signifikan
Berdasarkan gejala klinis awal, keluhan yang paling banyak dijumpai berupa
demam, menggigil, pusing, badan pegal, lemas, dan gangguan pencernaan. Pada kedua
kelompok keluhan terbanyak berupa demam yaitu 45,24% pada kelompok Ar-SP, dan
45,16% pada kelompok Ar-Dx. Sedangkan gejala klinis awal yang paling sedikit
dijumpai adalah gangguan pencernaan (9,25%) pada kelompok Ar-SP dan pusing serta
menggigil pada kelompok Ar-Dx (16,13%). Berdasarkan suhu tubuh awal, yang paling
banyak dijumpai adalah <37,50C baik pada kelompok SP maupun pada kelompol
Ar-Dx dengan persentase masing-masing 54,76% dan 54,84%. Dari pemeriksaan fisik yang
dilakukan pada subjek penelitian, tidak dijumpai adanya pembesaran limpa. Secara
keseluruhan pada kedua kelompok tidak dijumpai perbedaan bermakna gejala klinis awal
Tabel 4. Rata-rata Kepadatan Parasit Sebelum dan Sesudah Pengobatan
Karakteristik Ar-SP Ar-Dx pc))
Mean ± SD pa) Mean ± SD pa)
Kepadatan Parasit (/µl)
a. H0 344,76 ± 350,38 0,000 378,06 ± 355,05 0,000 0,308 b. H1 47,62 ± 106,10 0,000 43,87 ± 121,48 0,000 0,175 c. H2 11,43 ± 28,33 0,000 12,90 ± 34,85 0,000 0,955
d. H3 0 0
e. H7, H14 dan H28 0 0
Keterangan : Ar : Artesunat SP : Sulfadoksin-pirimetamin Dx : Doksisiklin SD = Standard Deviation
a) Uji Normalitas Kolmogorov-Smirnov
c)
Uji Mann-Whitney
Dari tabel di atas, dapat dilihat bahwa kepadatan parasit sebelum pengobatan (H0)
pada kelompok Ar-SP rata-rata 344,76 parasit/µl dan pada kelompok Ar-Dx rata-rata
378,06 parasit/µl. Pada masing-masing kelompok pengobatan terjadi penurunan
kepadatan parasit yang bermakna dari H0 sampai dengan H2, dan mulai H3 sampai H28
sudah tidak ditemukan lagi parasit dalam darah. Dari uji statistik dengan Mann-Whitney
yang membandingkan penurunan kepadatan parasit pada kelompok Ar-SP dan Ar-Dx
diperoleh p>0,05 artinya tidak terdapat perbedaan bermakna penurunan kepadatan parasit
0
Gambar 10. Perbandingan Nilai Mean Kepadatan Parasit
Tabel 5. Respon Pengobatan
Keterangan : Ar : Artesunat SP : Sulfadoksin-pirimetamin Dx : Doksisiklin ETF = Early Treatment Failure
LTF = Late Treatment Failure
ACPR = Adequate Clinical and Parasitological Response
Respon pengobatan sampai hari ke-28 pada kedua kelompok, tidak terjadi
kegagalan pengobatan baik Early Treatment Failure (ETF) maupun Late Treatment
Failure (LTF), semua subjek penelitian mengalami kesembuhan (Adequate Clinical and
Tabel 6. Karakteristik Hematologi Sebelum dan Sesudah Pengobatan
Keterangan : Ar : Artesunat SP : Sulfadoksin-pirimetamin Dx : Doksisiklin
a)
Uji normalitas Kolmogorov-Smirnov
c)
Uji Mann-Whitney
d)
Uji t tidak berpasangan e) Uji t berpasangan
* Signifikan
Dari tabel di atas, terlihat bahwa terjadi perubahan yang bermakna dari komponen
hematologi hemoglobin, lekosit, eritrosit, dan trombosit (p<0,05) sebelum dan sesudah
pengobatan pada kelompok Ar-SP. Pada kelompok Ar-Dx perubahan yang bermakna
hanya pada komponen hematologi eritrosit dan trombosit saja. Berdasarkan uji statistik
dengan membandingkan kelompok pengobatan Ar-SP dengan Ar-Dx terhadap perubahan
Tabel 7. Distribusi Efek Samping Obat
Keterangan : Ar : Artesunat SP : Sulfadoksin-pirimetamin Dx : Doksisiklin
b)
Uji Chi-square
*
Signifikan
Efek samping yang terjadi setelah pemberian obat berupa lemas, sakit kepala, dan
gangguan pencernaan. Pada penggunaan Ar-SP, efek samping yang paling banyak adalah
sakit kepala (44,74%), kemudian lemas (36,84%) dan yang paling sedikit adalah
gangguan pencernaan (18,42%). Pada penggunaan Ar-Dx, efek samping yang paling
banyak adalah gangguan pencernaan (55,56%), sakit kepala (27,78%), dan yang paling
sedikit adalah lemas (16,67%). Pada penelitian ini, efek samping berupa reaksi alergi
akibat pemakaian obat tidak dijumpai. Dari uji Chi-square diperoleh nilai p>0,05 pada
efek samping gangguan pencernaan, artinya tidak terdapat perbedaan bermakna pada
kedua kelompok pengobatan. Dijumpai nilai p<0,05 pada lemas dan sakit kepala, yang
berarti ada perbedaan bermakna antar kedua kelompok pengobatan, dimana lemas dan
sakit kepala lebih banyak dijumpai pada kelompok Ar-SP.
4.2. Pembahasan
Penelitian ini dilakukan di tiga kecamatan Kabupaten Nias Selatan dengan
menggunakan metode uji klinis terbuka (open trial). Obat yang digunakan pada
Berdasarkan karakteristik dasar sampel penelitian berdasarkan kelompok umur,
didapati bahwa kelompok umur terbanyak adalah kelompok umur ≥55 tahun, baik pada
kelompok pengobatan Ar-SP maupun Ar-Dx. Berdasarkan jenis kelamin, jumlah wanita
lebih banyak dijumpai daripada pria pada kelompok pengobatan Ar-SP, tetapi pada
kelompok Ar-Dx jumlah sampel wanita hampir sama dengan pria.
Pada penelitian ini kepadatan parasit yang dijumpai rendah dan pada pemeriksaan
mikroskopis tidak dijumpainya bentuk gametosit, serta pada pemeriksaan fisik tidak
dijumpai adanya pembesaran limpa, dengan demikian dearah penelitian ini termasuk
kategori Low Transmission Area. Jenis Plasmodium yang dijumpai adalah P.falciparum,
P.vivax, dan Mix (P.falciparum dan P.vivax), dan jenis yang terbanyak adalah
P.falciparum (76,5%). Kepadatan parasit menurun secara bermakna pada kedua
kelompok pengobatan dimulai sejak H1 dan menghilang pada H3 sampai H28. Pada
kelompok Ar-SP terjadi penurunan sebesar 86,19% pada H1, pada H2 terjadi penurunan
sebesar 75,99% dan pada H3 sebesar 8,75%. Pada kelompok Ar-Dx terjadi penurunan
sebesar 88,40% pada H1, terjadi penurunan sebesar 70,60% pada H2, dan 7,75% pada
H3. Pada penelitian ini tidak dijumpai adanya Early Treatment Failure (ETF) dan Late
Treatment Failure (LTF), dengan demikian semua subjek penelitian mengalami
kesembuhan (100%). Dari hasil uji statistik tidak dijumpai perbedaan yang bermakna
penurunan kepadatan parait pada kedua kelompok pengobatan, dengan demikian
kombinasi Ar-SP dan kombinasi Ar-Dx mempunyai efikasi yang baik untuk membunuh
parasit bentuk aseksual.
yang diderita sebelumnya, cara pengukuran hemoglobin dengan metode Sahli yang
sangat subjektif, serta faktor lain yang dapat mempengaruhi kadar hemoglobin yang
belum dapat disingkirkan.
Perubahan komponen hematologi, seperti peningkatan kadar hemoglobin sesudah
pengobatan dapat terjadi karena hilangnya parasit Plasmodium dalam darah. Peningkatan
eritrosit juga terjadi seiring dengan meningkatnya kadar hemoglobin dan menghilangnya
Plasmodium dari darah. Kadar trombosit yang meningkat sebelum dan sesudah
pengobatan berbeda secara bermakna pada kedua kelompok pengobatan, hal ini
menunjukkan bahwa penurunan kepadatan Plasmodium akan meningkatan kadar
trombosit. Namun pada penelitian yang dilakukan oleh Erhart dkk pada tahun 2001, tidak
terjadi perubahan trombosit sebelum dan sesudah pengobatan. Secera keseluruhan
berdasarkan uji statistik yang membandingkan perubahan hematologi sesudah
pengobatan pada kedua kelompok pengobatan tidak berbeda bermakna.
Efek samping obat yang terjadi berupa lemas dan sakit kepala paling banyak
muncul pada kelompok pengobatan Ar-SP, yaitu 44,74% dan 36,84%, sedangkan pada
kelompok Ar-Dx efek samping yang paling banyak adalah gangguan pencernaan
(55,56%).
Walaupun dalam hal menghilangkan parasit dalam darah kedua obat ini sama-sama
mempunyai efikasi yang baik, tetapi dari segi efek samping obat yang dilaporkan secara
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian dan pembahasan, dapat diambil kesimpulan sebagai berikut :
1. Terjadi penurunan kepadatan parasit dalam darah dimulai dari H1, dan
menghilang pada H3 sampai H28 pada kedua kelompok pengobatan, dengan
demikian artesunat – sulfadoksin-pirimetamin dan artesunat-doksisiklin
mempunyai efikasi yang sama baiknya. Semua subjek penelitian mengalami
kesembuhan (100%).
2. Efek samping obat lebih banyak terjadi pada kelompok pengobatan
artesunat-sulfadoksin-pirimetamin, yaitu berupa lemas (44,74%) dan sakit kepala
(36,84%) yang muncul sejak hari kedua pengobatan dan mulai menghilang
setelah selesai waktu pengobatan. Oleh karena efek samping yang ditimbulkan
akibat penggunaan artesunat – sulfadoksin-pirimetamin, maka dianjurkan untuk
menggunakan artesunat-doksisiklin.
3. Pada penelitian ini tidak dijumpai parasitemia yang tinggi (> 1000/µl) serta tidak
dijumpai gametosit dalam darah.
5.2. Saran
1. Perlu dilakukan penelitian lebih lanjut dengan kepadatan parasit yang lebih besar
2. Oleh karena penggunakan kombinasi artesunat dan doksisiklin yang diberikan
sampai 7 hari, maka untuk mengurangi ketidakpatuhan dan efek samping yang
ditimbulkan perlu dilakukan penelitian dengan menggunakan kombinasi artesunat
DAFTAR PUSTAKA
Alecrim M.G, Lacerda M.V, Mourao M.P, Alecrim W.D, Padilha A, Cardoso B.S, Boulos M : Successful Treatment of Plasmodium falciparum Mlaria with a Six-Dose Regimen of Artemether-Lumefantrine versus Quinine-Doxycycline in the Western Amazon Region of Brazil. Am.J.Trop. Med. Hyg. 74(1), 2006, pp.20-5.
Bloland PB, 2001: Drug Resistance in Malaria, World Health Organization. 2-8.
CDC, 2006 : Schema of the Life Cycle Malaria. Available from URL : http://www.cdc.gov/malaria/biology/life_cycle.htm
Departemen Kesehatan Republik Indonesia, 2005: Gebrak Malaria, Pedoman Tatalaksana Kasus Malaria di Indonesia, Ditjen Pemberantasan Penyakit Menular dan Penyehatan Lingkungan, Edisi Kedua.
Departemen Kesehatan Republik Indonesia,2004a : Penggunaan Artemisinin Untuk Atasi Malaria di Daerah yang Resisten Klorokuin.. Available from URL : http://www.depkes.go.id/index.php?option=viewarticle&sid=437&Itemid=2
Departemen Kesehatan Republik Indonesia, 2004b. Malaria Akan Diturunkan 50 Persen
di 12 Provinsi. Available from URL : http://www.depkes.go.id/index.php?option=news&task=viewarticle&sid=644
Departemen Kesehatan Republik Indonesia,2003 : 70 Juta Penduduk Terancam Wabah Malaria. 23 Februari 2006 : Suara Karya Online.htm.
Dinas Kesehatan Kabupaten Nias Selatan, 2006.
Departemen Kesehatan Republik Indonesia, 2002: Profil Kesehatan Indonesia 2001, Menuju Indonesia Sehat 2010.
Dorsey G, Njama D, Kamya M.R, Cattamanchi A, Kyabayinze D, Staedke S.G, Gasasira A, Rosenthal P.J: Sulfadoxine/Pyrimethamine Alone or with Amodiaquine or Artesunate for Treatment of Uncomplicated Malaria : a Longitudinal Randomised Trial, The Lancet; Dec 21-Dec 28, 2002; 360, 9350, pp.2031-37.
Erhart L.M, Yingyuen K, Chuanak N, Buathong N, Laoboonchai A, Miller R.S, Meshnick S.R, Gasser R.A, Wongsrichanalai C, : Hematologic and Clinical of Malaria in a Semi-Immune Population of Western Thailand. Am.J.Trop. Med. Hyg, 70(1), 2004. pp.8-14.