TESIS
Oleh
ALI AKBARI
127006017/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
PENGGUNAAN KITOSAN MOLEKUL TINGGI DARI CANGKANG
BELANGKAS (
Tachypleus gigas
) DAN GELATIN SEBAGAI
MEMBRAN UNTUK MENURUNKAN KADAR LOGAM
TIMBAL (Pb) DENGAN METODE
SOLID
TESIS
Diajukan Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Magister Sains dalam Program Studi Ilmu Kimia Pada Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Sumatera Utara
Oleh
ALI AKBARI
127006017/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
PENGGUNAAN KITOSAN MOLEKUL TINGGI DARI CANGKANG
BELANGKAS (
Tachypleus gigas
) DAN GELATIN SEBAGAI
MEMBRAN UNTUK MENURUNKAN KADAR LOGAM
TIMBAL (Pb) DENGAN METODE
SOLID
KATA PENGANTAR
Puji syukur penulis haturkan kehadirat Allah SWT yang telah banyak memberikan anugerah-Nya, sehingga tesis dapat diselesaikan dengan baik.
Tesis ini berjudul “ PENGGUNAAN KITOSAN MOLEKUL TINGGI DARI CANGKANG BELANGKAS (TACHYPLEUS GIGAS) DAN GELATIN SEBAGAI MEMBRAN UNTUK MENURUNKAN KADAR LOGAM TIMBAL (Pb) DENGAN METODE SOLID PHASE EXTRACTION ( SPE )
“
tesis ini merupakan salah satu syarat untuk memperoleh gelar Magister Sains (M.Si) Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara Medan.Keberhasilan dari penelitian dan penulisan tesis ini tidak terlepas dari bantuan berbagai pihak yang terlibat secara langsung maupun tidak langsung dan telah memberikan dukungan secara moril maupun materil, dalam kesempatan ini penulis ingin menyampaikan terimakasih yang tidak terhingga kepada:
Orangtua penulis, buat ibunda Nur Hasni yang selalu sabar mendoakan, memberikan perhatian, dan menjadi inspirasi di setiap langkah hidup kami.
Bapak Prof. Dr. dr. Syafril Pasaribu, DMT&H, M.Sc, (CTM), Sp.A(K) dan Dr. Sutarman, M.Sc selakuk Rektor Universitas Sumatera Utara dan Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Bapak Prof. Dr. Harry Agusnar, M.Sc.M.Phill selaku dosen pembimbing I dan Bapak Prof. Dr. Zul Alfian, M.Sc selaku dosen pembimbing II yang telah banyak memberikan arahan dan masukan kepada penulis, sehingga penulis dapat menyelesaikan tesis ini dengan baik
Kak Lely selaku tata usaha Pascasarjana Ilmu Kimia dan bang Edi selaku teknisi Laboratorium Kimia Polimer FMIPA-USU.
Rekan – rekan penulis di program Pascasarjana Ilmu Kimia angkatan 2013 yang telah banyak berbagi Ilmu yang bermanfaat, Raja, Robi, Tika, Jane, Cornel, Kiki, elisa. Penghargaan yang sebesar – besarnya kepada Bapak Kepala Balai KIPM Kelas I Medan I, Bapak Ir. Anwar, M.Si yang telah memberikan kesempatan kepada penulis untuk mengikuti Pendidikan Sekolah Pascasarjana Fakultas MIPA Jurusan Kimia Universitas Sumatera Utara.
Terimakasih penulis ucapkan kepada seluruh keluarga yang telah memberikan motivasi dan semangat kepada penulis, terutama kepada istriku Julia Rahmadani Lubis, S.Si.,Apt, anak – anak ku Putri Ratifa Zahra dan Putra Raziq Fawwas.
Semua saudara dan teman – teman di Balai KIPM Kelas I Medan I walaupun tidak disebutkan satu persatu, yang selalu mendoakan penulis, dan dengan sabar mendengarkan keluh kesah serta memberikan masukannya kepada penulis.
Hanya Allah SWT yang dapat membalas segala kebaikan yang telah diberikan kepada penulis, penulis berharap semoga Allah SWT memberikan berkah-Nya berlipat ganda.
Penulis menyadari bahwa tesis ini masih banyak kekurangan. Oleh karena itu, masukan dan saran membangun dari pihak pembaca sangat diharapkan penulis demi kesempurnaan tesis ini. Akhir kata semoga tesis ini bermanfaat bagi penelitian dan kemajuan ilmu pengetahuan untuk masa yang akan datang.
Medan, Pebruari 2015 Penulis
RIWAYAT HIDUP
DATA PRIBADI
Nama Lengkap berikut gelar : Ali Akbari, S.Si
Tempat dan Tanggal Lahir : Pasaman Barat, Sumatera Barat, 09 November 1979 Alamat Rumah : Jl. Bilal Ujung Gg Karya No 296 c
Kelurahan Pulo Brayan Darat I Kecamatan Medan Timur Propinsi Sumatera Utara
Telepon/HP : 0812-1022-5856
Email : akbarifish@yahoo.com
Nama Ayah : (Alm) Mas’ud
Nama Ibu : Nur Hasni
DATA PENDIDIKAN
SD
: SD Inpres Negeri Parit, Pasaman Barat
Tamat : 1992 SMP : SMP Negeri I Parit, Pasaman Barat Tamat : 1995 SMU : SMU Negeri I Lembah Melintang Tamat : 1998Diploma : D3 Kimia Industri USU Tamat : 2002
Strata-1 : Kimia USU Tamat : 2004
Abstrak
Kitosan dan gelatin dapat digunakan sebagai bahan dasar dalam pembuatan membran untuk menurunkan kadar logam berat timbal (Pb) dengan metode Solid Phase Extraction (SPE), yaitu dengan cara melarutkan kitosan dalam larutan asam asetat 1 % dan gelatin dilarutkan dalam aquades pada suhu 60 oC, perlakuan pertama dilakukan dengan pencampuran larutan kitosan dan larutan gelatin dengan perbandingan K25 : G75, K50 : G50 dan K75 : G25, kemudian pada perlakukan kedua larutan kitosan 2 % ditambah serbuk gelatin dengan variasi 0,1 g, 0,2 g, 0,3 g, 0,4 g dan 0,5 g, selanjutnya membran dicetak pada plat kaca kemudian dikeringkan dalam oven pada suhu 60 oC selama 18 jam, selanjutnya membran digunakan untuk menurunkan kadar logam timbal (Pb). Analisa dan uji tarik masing – masing dilakukan dengan menggunakan alat Spektrofotometer Serapan Atom (AAS) dan alat Universal Testing Machine, dari hasil penelitian diperoleh penurunan kadar logam Pb yang optimum terdapat pada membran campuran kitosan dan gelatin 75 % : 25% yaitu 83,696 % dan pada membran campuran kitosan 2 % dengan penambahan serbuk gelatin 0,5 g yaitu sebesar 69,316 %.
Kata kunci : Adsorpsi, Ekstraksi Fase Padat, Timbal (Pb), Membran Kitosan-Gelatin
PENGGUNAAN KITOSAN MOLEKUL TINGGI DARI CANGKANG
BELANGKAS (
Tachypleus gigas
) DAN GELATIN SEBAGAI
MEMBRAN UNTUK MENURUNKAN KADAR LOGAM
TIMBAL (Pb) DENGAN METODE
SOLID
Abstract
Chitosan and gelatine can be used as raw materials in manufacturing of membrane for heavy metals adsorption using method Solid Phase Extraction (SPE), chitosan by dissolved it in 1 % acetid acid and gelatin by dissolved with aquadest temperature at 60 oC. Which the manufacturing conducted thorough frist procedure mixer chitosan and gelatin, the rasio concentration of chitosan : gelatin membrane varied at K25 % : G75 %, K50 % : G50 %, K75 % : G25 %, than the second procedure weight gelatine varied at 0.1 g, 0,2 g, 0,3 g, 0,4 g and 0,5 g, resvectively membrane is formed on glass plat, than dried at temperature 60 oC for 18 hours. Than chitosan - gelatin membrane used to reduce lead (Pb) , Analysis and tensile test were carried out by using Atomic Adsorption Spectrofotometer (AAS) and Universal Testing Machine , from experiment result obtained the best condition to Pb metal adsorption were chitosan : gelatin membrane K75 % : G25 % was 83,696 % and chitosan added 0,5 g gelatin membrane was 69,316 %
Keyword : Adsorption, Solid Phase Extraction (SPE), Lead (Pb), Kitosan-Gelatin Membrane
THE USE OF HIGH MOLECULAR CHITOSAN SHELL HORSESHOE
CRAB (Tachypleus gigas) AND GELATIN AS METAL MEMBRANES
DAFTAR TABEL
Nomor Judul Halaman
Tabel
2.1 Karakteristik Kitosan... 8
2.2. Aplikasi dan Kegunaan Kitosan di Berbagai Bidang ………... 9
2.3. Komposisi Asam Amino Gelatin Beberapa Jenis Hewan…..……… 13
2.4. Karakterisasi Kitin dan Kitosan dari Cangkang Belangkas………… 16
4.1. Hasil Analisis FTIR Kitosan………..… 43
4.2. Hasil Analisis FTIR Gelatin………. 44 4.3. Hasil Analisis FTIR Kitosan-Gelatin……… 45
4.4. Data Sensitivity Instrumen AAS……….. 47 4.5. Absorbansi Uji Linearity……….. 48
4.6. Absorbansi Blanko Sampel……….. 51
4.7. Hasil Pengukuran Bahan Acuan……….. 52
4.8. Hasil Uji Reapetability Minggu ke-1……… 53
4.9. Hasil Uji Reapetability Minggu ke-2……… 54
4.10. Hasil Pengukuran Sampel dengan AAS……….. 55
4.11. Hasil Penurunan Logam Pb Setelah dilewatkan melalui Membran Kitosan – Gelatin (v/v)………. 56
4.12. Hasil Penurunan Logam Pb Setelah dilewatkan melalui Membran Kitosan- Gelatin (w/v)………. 57
4.13. Data Hasil Perbandingan SPE Modifikasi dengan SPE Komersil… 58
4.14. Data Hasil Uji Kekuatan Tarik Membran Kitosan – Gelatin……. 59
DAFTAR ISI Halaman KATA PENGANTAR i RIWAYAN HIDUP iii
ABSTRAK iv ABSTRACT v
DAFTAR ISI vi DAFTAR TABEL ix DAFTAR GAMBAR x DAFTAR LAMPIRAN xii DAFTAR SINGKATAN xiii BAB 1. PENDAHULUAN 1.1. Latar Belakang 1 1.2. Perumusan Masalah 4 1.3. Pebatasan Masalah 4 1.4. Tujuan Penelitian 4
1.5. Manfaat Penelitian 4 1.6. Ruang Lingkup Penelitian 5 BAB 2. TINJAUAN PUSTAKA 2.1 Khitin dan Kitosan 6 2.1.1. Isolasi Kitin dan Kitosan 7
2.1.2. Struktur Molekul Kitosan 7 2.1.3. Sifat dan Karakterisasi Kitosan 8
2.2. Gelatin 11
2.3. Belangkas 15
2.4. Logam Berat Beracun 17
2.5. Ekstraksi Fase Padat (SPE) 18
2.6. Adsorpsi 19
2.7. Membran 20
2.7.1 Klasifikasi Membran 21
2.7.2 Membran Polimer 22
2.7.3 Karakterisasi Membran 22
2.8. Validasi Metode 23
2.9. Spektrofotometri Serapan Atom (AAS) 24
2.10. Bahan Acuan 25
BAB 3. METODOLOGI PENELITIAN
3.1. Alat dan Bahan 27
3.1.1. Alat – alat 27
3.1.2. Bahan – bahan Penelitian 28
3.2. Prosedur Penelitian 28
3.2.1. Penyedian Membran Kitosan – Gelatin 29 3.2.1.1 Penyediaan Membran Kitosan - Gelatin
dengan Perbandingan Volume (v/v) 29
3.2.1.2 Penyediaan Membran Kitosan - Gelatin
dengan Memvariasikan Serbuk Gelatin (w/v) 29
3.2.2. Preparasi Bahan Acuan 30
3.2.3. Uji SEM 30
3.2.4. Perlakukan Ekstraksi Metode SPE dengan Membran
Kitosan – Gelatin 31
3.2.6. Analisis dengan AAS 33
3.2.7. Perhitungan 34
3.3. Bagan Penelitian 35
3.3.1. Pembuatan Membran Kitosan-Gelatin (v/v) 35
3.3.2. Pembuatan Membran Kitosan-Gelatin (w/v) 36
3.3.3. Penggunaan Membran Kitosan-Gelatin sebagai penurun
Konsentrasi Ion Logam 37
BAB 4. HASIL DAN PEMBAHASAN
4.1. Pengaruh Persentase kitosan dan Gelatin terhadap morfologi membran
Kitosan-Gelatin 38
4.2. Analisa Membran Kitosan-Gelatin dengan FTIR 42
4.3. Penentuan Sensitivity AAS 46
4.4. Uji Linearity 47
4.5. Penentuan Batas Deteksi ( LOD dan LOQ ) 50
4.6. Penentuan Akurasi dan Presisi 51
4.7. Uji Repeatability 52
4.8. Analisa Sampel 54
4.9. Uji Kekuatan Tarik 58
BAB 5. KESIMPULAN
5.1. Kesimpulan 60
5.2. Saran 60
DAFTAR PUSTAKA
DAFTAR TABEL
Nomor Judul Halaman
2.1 Karakterisasi Kitosan 9
2.2 Aplikasi dan Kegunaan Kitosan di Berbagai Bidang 10
2.3 Komposisi Asam Amino Gelatin Berbagai Jenis Hewan 14
2.4 Karakterisasi Kitin dan Kitosan dari Cangkang Belangkas 17
4.1 Hasil Analisa FTIR Kitosan 43
4.2 Hasil Analisa FTIR Gelatin 44
4.3 Hasil Analisa FTIR Kitosan dan Gelatin 45
4.4 Data Sensitivity Instrumen AAS 47
4.5 Absorbansi Uji Linerity 48
4.6 Absorbansi Blanko Sampel 50
4.7 Hasil Pengukuran Bahan Acuan 51
4.8 Hasil Uji Repeatability Minggu ke – 1 53
4.9 Hasil Uji Repeatability Minggu ke – 2 54
4.10 Hasil Pengukuran Sampel dengan AAS 55
4.11 Hasil Penurunan Logam Pb Setelah dilewatkan Melalui Membran
Kitosan – Gelatin(v/v) 56
4.12 Hasil Penurunan Logam Pb Setelah dilewatkan Melalui Membran
Kitosan – Gelatin(w/v) 57
4.13 Perbandingan Hasil Penelitian Menggunakan SPE Komersil dengan
SPE Modifikasi 58
DAFTAR GAMBAR
Nomor Judul Halaman
2.1 Struktur Molekul Kitosan 8
2.2 Struktur Kimia Gelatin 13
2.3 Bagian Depan Belangkas 15
2.4 Bagian Belakang Belangkas 16
2.5 Ketertelusuran Pengujian Kimia 26
3.1 Foto Membran Kitosan Masih Dalam Cetakan 31
3.2 Foto Membran Kitosan Yang Sudah dicelupkan kedalam NaOH 32 3.3 Mekanisme Penyerapan Logam Pb dengan Membran Kitosan – Gelatin 32 3.4 Bagan Penelitian Pembuatan Membran Kitosan – Gelatin (v/v) 35 3.5 Bagan Penelitian Pembuatan Membran Kitosan – Gelatin (w/v) 36 3.6 Bagan Penelitian Penggunaan Membran Kitosan – Gelatin 37
4.1 Hasil SEM Membran Kitosan 39
4.2 Hasil SEM Membran Gelatin 40
4.3 Hasil SEM Membran Kitosan – Gelatin 41
4.4 Spektrum Transformasi Infra Merah (FTIR) Membran Kitosan 42 4.5 Spektrum Transformasi Infra Merah (FTIR) Membran Gelatin 43 4.6 Spektrum Transformasi Infra Merah (FTIR) Membran Kitosan – Gelatin 44 4.7 Spektrum Transformasi Infra Merah (FTIR) gabungan Membran Kitosan,
Membran Gelatin dan Membran Kitosan – Gelatin 45
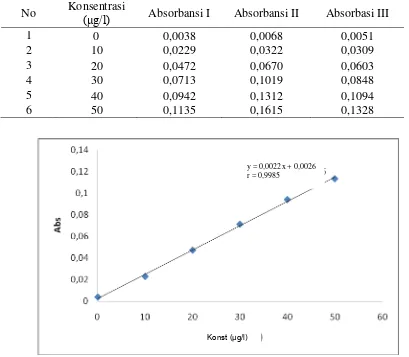
4.8 Kurva Kalibrasi Uji Linearity ke-I 48
4.9 Kurva Kalibrasi Uji Linearity ke-II 49
4.10 Kurva Kalibrasi Uji Linearity ke-III 49
4.12 Kurva Uji Repeatability ke – I 53
4.13 Kurva Uji Repeatability ke – II 54
4.14 Kurva Kalibrasi Pengukuran Sampel 55
4.15 Grafik Hasil Penurunan Logam Pb Setelah dilewatkan melalui Membran
Kitosan – Gelatin (v/v) 56
4.16 Grafik Hasil Penurunan Logam Pb Setelah dilewatkan melalui Membran
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Ukuran Ketebalan Membran 65
2. Perhitungan Persentase Daya Serap , Konsentrasi Bahan Acuan, Perhitungan Nilai
Rata – Rata dan Standar Deviasi 66
3. Hasil Analisa Logam Pb Setelah Dilewatkan Dengan Membran Kitosan – Gelatin 68
4. Data Hasil Pengukuran logam Pb dengan AAS 69
5. Kurva Kalibrasi Pengukuran Larutan standar Pb 70
6. Hasil SEM Membran Kitosan 71
7. Hasil SEM Membran Gelatin 72
8. Hasil SEM Membran Kitosan-Gelatin 73
9. Hasil FTIR Membran Kitosan 74
10. Hasil FTIR Membran Gelatin 75
11. Hasil FTIR Membran Kitosan-Gelatin 76
12. Sertifikat Bahan Acuan 77
13. Membran Hasil Cetakan 78
DAFTAR SINGKATAN
FTIR : Fourier Transform Infrared Spectroscopy
SEM : Scanning Electron Microscopy
AAS : Atomic Absorption Spectrofotometer
CRM : Certificate References Materials
Abstrak
Kitosan dan gelatin dapat digunakan sebagai bahan dasar dalam pembuatan membran untuk menurunkan kadar logam berat timbal (Pb) dengan metode Solid Phase Extraction (SPE), yaitu dengan cara melarutkan kitosan dalam larutan asam asetat 1 % dan gelatin dilarutkan dalam aquades pada suhu 60 oC, perlakuan pertama dilakukan dengan pencampuran larutan kitosan dan larutan gelatin dengan perbandingan K25 : G75, K50 : G50 dan K75 : G25, kemudian pada perlakukan kedua larutan kitosan 2 % ditambah serbuk gelatin dengan variasi 0,1 g, 0,2 g, 0,3 g, 0,4 g dan 0,5 g, selanjutnya membran dicetak pada plat kaca kemudian dikeringkan dalam oven pada suhu 60 oC selama 18 jam, selanjutnya membran digunakan untuk menurunkan kadar logam timbal (Pb). Analisa dan uji tarik masing – masing dilakukan dengan menggunakan alat Spektrofotometer Serapan Atom (AAS) dan alat Universal Testing Machine, dari hasil penelitian diperoleh penurunan kadar logam Pb yang optimum terdapat pada membran campuran kitosan dan gelatin 75 % : 25% yaitu 83,696 % dan pada membran campuran kitosan 2 % dengan penambahan serbuk gelatin 0,5 g yaitu sebesar 69,316 %.
Kata kunci : Adsorpsi, Ekstraksi Fase Padat, Timbal (Pb), Membran Kitosan-Gelatin
PENGGUNAAN KITOSAN MOLEKUL TINGGI DARI CANGKANG
BELANGKAS (
Tachypleus gigas
) DAN GELATIN SEBAGAI
MEMBRAN UNTUK MENURUNKAN KADAR LOGAM
TIMBAL (Pb) DENGAN METODE
SOLID
Abstract
Chitosan and gelatine can be used as raw materials in manufacturing of membrane for heavy metals adsorption using method Solid Phase Extraction (SPE), chitosan by dissolved it in 1 % acetid acid and gelatin by dissolved with aquadest temperature at 60 oC. Which the manufacturing conducted thorough frist procedure mixer chitosan and gelatin, the rasio concentration of chitosan : gelatin membrane varied at K25 % : G75 %, K50 % : G50 %, K75 % : G25 %, than the second procedure weight gelatine varied at 0.1 g, 0,2 g, 0,3 g, 0,4 g and 0,5 g, resvectively membrane is formed on glass plat, than dried at temperature 60 oC for 18 hours. Than chitosan - gelatin membrane used to reduce lead (Pb) , Analysis and tensile test were carried out by using Atomic Adsorption Spectrofotometer (AAS) and Universal Testing Machine , from experiment result obtained the best condition to Pb metal adsorption were chitosan : gelatin membrane K75 % : G25 % was 83,696 % and chitosan added 0,5 g gelatin membrane was 69,316 %
Keyword : Adsorption, Solid Phase Extraction (SPE), Lead (Pb), Kitosan-Gelatin Membrane
THE USE OF HIGH MOLECULAR CHITOSAN SHELL HORSESHOE
CRAB (Tachypleus gigas) AND GELATIN AS METAL MEMBRANES
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Pencemaran lingkungan perairan yang disebabkan oleh logam-logam berat seperti kadmium, timbal dan tembaga yang berasal dari limbah industri sudah lama diketahui. Untuk menghilangkan bahan pencemar perairan tersebut hingga kini masih terus dikembangkan. Penggunaan biomaterial merupakan salah satu teknologi yang dapat dipertimbangkan, mengingat meterialnya mudah didapatkan dan membutuhkan biaya yang relatif murah sebagai bahan penyerap senyawa beracun dalam lingkungan perairan. Kontaminan logam berat di perairan masih merupakan permasalahan lingkungan yang penting dan belum terpecahkan (Sudha, 2003).
Selama ini, sebagaimana yang kita ketahui limbah dari hewan crustaceae seperti udang, kepiting dan belangkas di Indonesia hanya dimanfaatkan untuk pakan ternak, hidrolisat protein, silase, bahan baku terasi, petis dan lain – lain, sementara itu, limbah seperti ini di negara – negara maju seperti Jepang dan Amerika Serikat telah diisolasi kitinnya. kitin juga dapat diubah menjadi kitosan setelah lebih dari 70 % gugus asetilnya dihilangkan.
(Harry Noviary, 2010) telah melakukan karakterisasi cangkang belangkas, dalam penelitiannya mengemukakan bahwa cangkang belangkas mempunyai kandungan kitin sebesar 86,2 % dan mempunyai viskositas tinggi yaitu 800-2000 serta mempunyai berat molekul 106
Pemanfaatan kitosan sebagai bahan penjerap (adsorben) dalam berbagai bidang telah banyak dilakukan oleh peneliti – peneliti sebelumya, misalnya dibidang lingkungan perairan tentang adsorpsi kandungan logam Cr (III) dan Fe (II) yang dilakukan oleh (Endang Widjajanti, 2008), adsorpsi logam Cr (III) dan Ni (II) pada limbah cair pelapisan logam (Meriatna, 2008), adsorpsi logam Pb (II), Cd (II) dan (Cu) (Marganof, 2003) dan lain lain, tetapi pada umumnya penelitian yang dilakukan masih mengunakan metode sederhana dan tingkat konsentrasi logam yang besar.
78,9 mg Pb/g kitosan (Endang W Laksono, dkk, 2006), 815 mg Hg(II)/g kitosan (Amit B, 2006).
Meskipun demikian kemampuan adsorpsi kitosan terhadap logam atau ion logam masih perlu ditingkatkan misalnya dengan memperluas permukaan kitosan atau memperbanyak gugus aktif misalnya memodifikasi dengan senyawa lain. Penelitian Kurita dkk (1986) menyatakan bahwa peningkatan sifat hidrofilitas kitosan dapat meningkatkan kemampuan adsorpsi kitosan terhadap ion logam.
Gelatin mempunyai sifat hidrofilitas yang tinggi ini dapat dilihat dari fungsinya, dalam produk pangan gelatin berfungsi sebagai penstabil, pembentuk gel, pengikat, pengental, pengemulsi, pelapis dan lain sebagainya.
.Lebih jauh (Gomes, 2011). Mengatakan berdasarkan sifat gelatin dan kitosan, perlu dilakukan suatu penelitian yang lebih intensif dalam membahas sifat fisik dan kimia dari kombinasi kedua senyawa tersebut. Kombinasi kedua biopolimer ini akan saling memperbaiki kelemahan serta meningkatkan sifat fisiko-kimia dari gelatin murni maupun kitosan murni.
Menurut (Mulder (1996), membran merupakan batas atau penghalang selektif antara dua fase. Selektif menunjukkan keselektifan membran atau proses yang menggunakan membran terebut. Membran polimer merupakan semua pembatas atau penghalang polimer yang bersifat semipermeabel (Kesting , 1971)
Sehingga berdasarkan hal – hal yang diuraikan diatas dan berpedoman kepada penelitian – penelitian sebelumnya, maka dilakukan penelitian penggunaaan membran kitosan-gelatin dengan metode SPE (Solid Phase Extraction) dalam suatu kolom untuk menurun kadar logam Pb.
Dalam penelitian ini, pengamatan dan analisa lebih di tekankan pada pengaruh konsentrasi kitosan dan gelatin yang digunakan sebagai bahan untuk menurunan kadar logam timbal (Pb). Film dibuat dengan mengkompositkan kitosan dan gelatin. Keduanya akan dicampur dengan variasi konsentrasi masing-masing K25% : G75%, K50% : G50% dan K75% : G25%,
Sedangkan metode yang digunakan dalam penelitian ini adalah metode SPE serta analisis logam Pb dilakukan menggunakan alat AAS-Grafite Furnace A Analyst 800.
1.2 Perumusan Masalah
Berdasarkan hal – hal yang telah diuraikan diatas maka permasalahan dalam penelitian ini adalah bagaimana pengaruh penggunaan membran kitosan-gelatin untuk menurunkan kadar logam timbal (Pb)
1.3 Pembatasan Masalah
Penelitian ini hanya dibatasi pada penggunaan kitosan molekul tinggi dan gelatin sebagai membran untuk menurunkan kadar logam timbal (Pb) dengan metode SPE
(Solid Phase Extraction)
1.4 Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui penurunan kadar logam Pb dengan metode SPE menggunakan membran campuran larutan kitosan dengan larutan gelatin dan larutan kitosan dengan serbuk gelatin.
1.5 Manfaat Penelitian
Hasil penelitian ini diharapkan bermanfaat sebagai informasi teknologi untuk menurunkan kadar logam Pb dengan biaya relatif murah dan ramah lingkungan, selain itu juga sebagai informasi bagi pelaksanaan penelitian yang berkaitan dengan pemanfaatan membran kitosan
1.6 Ruang Lingkup Penelitian
BAB 2
TINJAUAN PUSTAKA
2.1 Kitin dan Kitosan
Kitin berasal dari kata “Chiton” yang berarti mantel atau lapisan luar dan pertama kali ditemukan oleh Braconot pada tahun 1811 dalam residu ekstrak jamur yang dinamakan
fungiue. Pada tahun 1823 Odins mengisolasi suatu senyawa kutikula serangga jenis ekstra yang disebut dengan nama kitin (Neely dan William, 1969). Kitin merupakan konstituen organik yang sangat penting pada hewan golongan orthopoda, annelid, molusca, corlengterfa dan nematoda. Kitin biasanya berkonyugasi dengan protein dan tidak hanya terdapat pada kulit dan kerangkanya saja, tetapi terdapat pada trachea, insang, dinding usus, dan pada bagian dalam kulit pada cumi – cumi (Neely dan William, 1969). Kitin mempunyai rumus molekul C18H26N2O10 (Hirano, 1976), merupakan zat padat yang tidak berbentuk (amorphous) tak larut dalam air, asam organik encer, alkali encer dan pekat, alkohol, dan pelarut organik lainnya tetapi larut dalam asam – asam mineral yang pekat. Kitin kurang larut dibandingkan dengan selulosa dan merupakan N-glukosamin yang terdeatilasi sedikit, sedangkan kitosan adalah kitin yang terdeasetilasi sebanyak mungkin. Kitosan yang disebut juga dengan β-1, 4-2 amino-2-dioksi-D-glukosa, merupakan turunan dari kitin melalui proses deasetilase. Kitosan juga merupakan suatu polimer multifungsi karena mengandung tiga jenis gugus fungsi yaitu asam amino, gugus hidroksil primer dan sekunder. Adanya gugus fungsi ini menyebabkan kitosan mempunyai kreatifitas kimia yang tinggi. (Tokura, 1995).
2.1.1. Isolasi Kitin dan Kitosan
Isolasi kitin dari limbah kulit belangkas dilakukan secara bertahap yaitu tahap pemisahan protein (deproteinasi) dengan larutan basa, demineralisasi, tahap pemutihan (bleancing) dengan aseton dan natrium hipoklorit, sedangkan transformasi kitin menjadi kitosan dilakukan tahap deasetilasi dengan basa berkonsentrasi tinggi (Arreneus, 1996 dan Fahmi, 1997)
Derajat deasetilasi pada pembuatan kitosan bervariasi dengan jumlah larutan alkali yang digunakan, tergantung waktu reaksi dan suhu reaksi. Biasanya kualitas produk kitosan dinyatakan dengan besarnya nilai derajat deasetilasi. Semakin besar derajat deasetilasi kitosan berarti semakin besar jumlah gugus amina dalam rantai polimernya, dan semakin besar pula rantai polimer tersebut untuk bereaksi dengan agen ikat silang (Santoso, 2010).
Hasil penelitian menunjukkan bahwa kemampuan adsorpsi kitosan terhadap logam berat sangat dipengaruhi oleh sifat fisika dan kimia kitosan. Kitosan tak berikat silang mempunyai kapasitas adsorpsi lebih besar dari pada kitosan berikat silang, tetapi kitosan berikat silang mempunyai ketahanan fisik, serbuk kitosan dengan ukuran partikel yang lebih kecil mempunyai kapasitas absorpsi yang lebih besar dari pada serbuk dengan ukuran partikel yang lebih besar (Karthikeyan dkk., 2004)
2.1.2. Struktur Molekul Kitosan
Kitosan adalah padatan amorf putih kekuningan, tidak beracun dan baik sebagai flokulan dan koagulan serta mudah membentuk membran atau film (Meiratna, 2008), merupakan polimer rantai panjang yang disusun oleh monomer-monomer glukosamin (2-amino-2-deoksi-D-glikosa). Biopolimer ini disusun oleh 2 jenis amino yaitu glukosamin (2-amino-2-deoksi-D-glukosa, 70-80%) dan N-asetilglukosamin (2- asetamino-2-deoksi-D-glukosa, 20-30%). Berat molekul kitosan adalah 1,036 x 106 Dalton. Berat molekul tergantung dari degradasi yang terjadi pada saat proses pembuatannya (Astuti, 2008).
(1,4)-2-Amino-2-Deoksi-beta-D-Glukosa. Struktur kitosan dapat dilihat pada gambar 2.1
Gambar 2.1 Struktur Molekul Kitosan (Kumar, 2000)
2.1.3. Sifat dan Karakteristik Kitosan
Sifat dari kitosan adalah tidak larut dalam air, memiliki ketahanan kimia cukup baik, larut dalam larutan asam tetapi tidak larut dalam basa dan ikatan silang kitosan memiliki sifat tidak larut dalam media campuran asam dan basa, memiliki reaktivitas kimia yang tinggi karena mengandung gugus -OH dan gugus -NH2 (Muzzarelli, 1997). Tetapi menurut (Kumar et al., 2000) kitosan mempunyai sifat yang lebih spesifik yaitu dengan adanya sifat bioaktif, biokomposit, pengkelat, antibakteria dan dapat terdegradasi.
Sandford dan Hutchins menyatakan sifat kationik, biologi, dan sifat kimia kitosan sebagaimana dikutip Meriatna (2008) adalah sebagai berikut :
1. Sifat kationik
Jumlah muatan positif tinggi: suatu muatan per unit gugus glukosamin, jika banyak material bermuatan negatif (seperti protein) maka muatan positif kitosan berinteraksi kuat dengan muatan negatif lain (polimer), flokulan yang baik:gugus NH3+ berinteraksi dengan muatan negatif dari polimer lain.
2. Sifat biologi
Dapat terdegradasi secara alami, polimer alami, non toksik. 3. Sifat kimia
disebabkan oleh adanya gugus amina dan gugus hidroksil dari rantai kitosan yang dapat dijadikan sebagai tempat untuk berkoordinasi dan bereaksi (Lee, dkk., 2009). Atom nitrogen pada gugus amina menyediakan pasangan elektron bebas yang dapat bereaksi dengan kation logam. Pada pH asam, gugus amina terprotonasi sehingga meningkatkan kelarutan kitosan yang bersifat tidak larut dalam pelarut alkali dan pada pH netral (Bernkop, dkk., 2004).
Adapun karakteristik kitosan ditunjukkan pada Tabel 2.1 sebagai berikut:
Tabel 2.1 Karakteristik Kitosan
No Karakteristik Ukuran
1. 2. 3. 4. 5. 6. 7. Bentuk partikel Massa air Massa abu Persen deasetilasi Warna larutan Viskositas: Rendah Medium Tinggi Ekstra tinggi Berat molekul Serpihan bubuk < 10% < 2% > 70% Jernih < 200 200-799 800-2000 >2000 <106 Sumber: (Robert dalam Meiratna, 2008)
2.1.4. Kegunaan Kitosan
atau film. Kitosan merupakan suatu biopolymer alam yang reaktif yang dapat melakukan perubahan-perubahan kimia.
Menurut Robert (1992) kitosan digunakan dalam berbagai bidang, misalnya (1) dalam industri kertas, kaca, kain, pewarna (2) dalam industri kosmetik (3) dalam bidang pertanian dan makanan (4) dalam industri semen (5) dalam bidang kesehatan (6) untuk penyerapan ion logam. Kitosan juga memiliki kegunaan yang beragam seperti: bahan perekat, adiktif untuk kertas dan tekstil, penjernihan air minum, serta untuk mempercepat penyembuhan luka, memperbaiki sifat pengikatan warna.
Beberapa aplikasi dan kegunaan kitosan di berbagai bidang ditunjukkan pada tabel 2.2 sebagai berikut:
Tabel 2.2 Aplikasi dan Kegunaan Kitosan di Berbagai Bidang
No. Bidang Aplikasi Kegunaan
1. 2. 3. 4. Pengelohan limbah Pertanian Industri Kecil Bioteknologi
- Bahan Koagolasi/Flokulasi untuk limbah cair
- Penghilangan ion-ion metal dari limbah cair
- Dapat menurunkan kadar asam sayur, buah dan ekstrak kopi
- Sebagai pupuk - Bahan antimikrobial - Serat tekstil
- Meningkatkan ketahanan warna - Bahan-bahan immobilisasi enzim
- Koagulasi/flokulasi,Flokulan pektin/protein
- Koagulasi ,Flokulan mikroba - Pembentuk komplek
5. 6. 7. 8. Klarifikasi/Penjernihan - Limbah industri pangan,-
Limbah sari buah
- Penjernihan air minum, kolam renang ,zat warna, tanin
Kosmetik
Biomedis
Fotografi
- Mempercepat penyembuhan luka, menurunkan kolesterol
- Melindungi film dari kerusakan
Sumber: Robert (1992)
2.1.5. Kemampuan Kitosan Untuk Menyerap Logam
Kemampuan kitosan untuk mengikat logam dengan cara pengkhelat adalah dihubungan dengan kadar nitrogen yang tinggi pada rantai polimernya. Kitosan mempunyai satu kumpulan amino linier bagi setiap unit glukosa. Kumpulan amino ini mempunyai satu kumpulan amino linier bagi setiap unit glukosa. Kumpulan amino ini mempunyai sepasang electron yang dapat berkoordinat atau membentuk ikatan-ikatan aktif dengan kation-kation logam. Unsur nitrogen pada setiap monomer kitosan dikatakan sebagai gugus yang aktif berkoordinat dengan kation logam (Hutahahean, 2001).
berlangsung. Ketiga proses tersebut tergantung dari ion logam masing-masing seperti penukaran ion logam Ca. Kitosan menunjukkan afinitas yang tinggi pada logam transisi golongan 3, begitu pula pada logam yang bukan golongan alkali dengan konsentrasi rendah (Muzzarelli, 1973).
Menurut Mc Kay (1987), kitosan mempunyai kemampuan untuk mengikat logam dan membentuk kompleks kitosan dengan logam. Contoh mekanismenya adalah sebagai berikut:
2R-NH3+ + Cu2+ + 2 Cl- (RNH2)CuCl2
2.2 Gelatin
Gelatin merupakan bahan alami yang diperoleh dari hidrolisis parsial kolagen. Gelatin bisa bersifat sebagai gelling agent (bahan pembuat gel) atau sebagai non gelling agent. Gelatin merupakan protein konversi bersifat larut air yang diperoleh dari hidrolisis kolagen yang bersifat tidak larut air. Tulang sapi, kulit sapi, dan kulit babi adalah bahan yang biasa digunakan untuk memperoleh gelatin (Sobral, 2001). Gelatin adalah protein dengan berbagai sifat fungsional dan aplikasi, termasuk kemampuannya membentuk film. Sumber bahan baku gelatin dapat berasal dari sapi dan babi, namun ditemukan sumber lain yang lebih relevan untuk mendapatkan gelatin, yaitu gelatin dari tulang dan kulit ikan (Gomez, 2002).
Dalam produk pangan, gelatin dimanfaatkan sebagai bahan penstabil, pembentuk gel, pengikat, pengental, pengemulsi dan lain sebagainya. Selain itu, gelatin digunakan sebagai bahan baku pembuatan kapsul. Permintaan akan gelatin telah meningkat selama bertahun-tahun. Laporan terkini mengindikasikan produksi gelatin dunia mendekati angka 326.000 ton per tahun, dimana gelatin dari kulit babi sebesar 46%, dari kulit sapi sebesar 29,4%, dari tulang sapi sebesar 23,1%, dan dari sumber lain sebesar 1,5% (Karim, 2009).
sedangkan untuk produk permen dan sejenisnya berfungsi konsistensi produk, daya gigit dan kekerasan serta tekstur, kelembapan, daya lengket dimulut. Dalam bidang farmasi digunakan sebagai cangkang kapsul dan di Indonesia beredar jenis kapsul keras yang terbuat dari gelatin yang diberi pewarna dan pelentur Dengan demikian gelatin merupakan interaksi dari jaringan kulit hewan mempunyai banyak fungsi diantaranya sebagai bahan pengemulsi, pengikat dan mempunyai gizi. Berdasarkan sifat bahan dasarnya pembuatan gelatin dapat dilakukan dengan cara 2 prinsip dasar yaitu cara alkali dan cara asam.
Cara alkali atau basa dilakukan untuk memperoleh gelatin tipe B, yaitu bahan dasarnya berasal dari kulit tua (keras,liat) maupun tulang. Mula-mula bahan diperlakukan dengan proses perendaman ,melalui perendaman beberapa minggu dalam larutan kalsium hidroksida, sehingga jaringan kolagen akan mengembang dan terpisah. Kemudian bahan dinetralkan dengan asam, selanjutnya dicuci dengan air dilanjutkan dengan ekstraksi melalui pemanasan.
Cara pengasaman dilakukan untuk menghasilkan gelatin tipe A (asam). Tipe A umumnya diperoleh dari kulit babi, dimana tidak memerlukan perendaman yang lama dengan asam, karena jaringan belum kuat terikat sehingga cukup dengan asam yang encer selama beberapa hari, dinetralkan dan dicuci berulang-ulang, untuk menghilangkan asam dan garamnya. Proses utama pembuatan gelatin dibagi menjadi tiga tahap. Tahap pertama adalah tahap persiapan bahan baku, yaitu penghilangan komponen non kolagen dari bahan baku dengan atau tanpa pengurangan ikatan antara komponen kolagen. Tahap kedua merupakan konversi kolagen menjadi gelatin. Tahap ketiga adalah pemurnian dan perolehan gelatin dalam bentuk kering (Ward dan Courts, 1977).
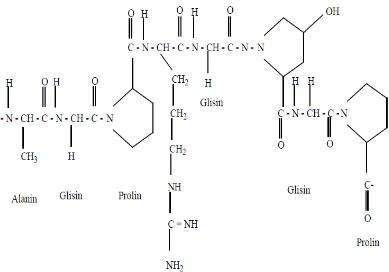
(hampir 1 dalam 3 residu asam amino, menyusun setiap 3 residu), proline dan 4-hydroxyproline residu (Gambar 2.2). Tipe strukturnya adalah -Ala-Gly-Pro-Arg-Gly-Glu-4Hyp-Gly-Pro- (Chaplin,2006).
Gambar 2.2 Struktur Kimia Gelatin (Chaplin,2006)
Gelatin dari sumber dan proses yang berbeda menunjukkan perbedaan komposisi asam amino (Glicksman,1969). Sumber bahan yang berbeda menunjukkan perbedaan komposisi asam amino gelatin tertera pada tabel 2.3.
Tabel 2.3 Komposisi Asam Amino Gelatin Beberapa Jenis Hewan
Asam Amino Anjing laut Ikan Paus Babi Sapi Ikan cod
Asam asparat 4.5 4.8 4.4 4.3 5.2
Hidroksiprolin 10.1 8.5 10.9 9.6 6.6
Sarin 3.8 4.0 3.3 3.2 6.3
Asam glutamate 7.6 8.0 7.8 7.4 8.0
Prolin 12.0 12.6 12.7 12.4 10.8
Glisin 31.6 30.2 30.8 33.3 31.5
Alanin 10.8 10.4 11.1 11.5 10.2
Valin 2.3 2.2 2.3 2.0 1.8
Sistein 0.0 0.0 0.0 0.0 0.0
Metionin 0.5 0.6 0.5 0.5 1.5
Isoleusin 1.0 1.2 1.1 1.2 1.3
Leusin 2.5 2.8 2.6 2.4 2.2
Tirosin 0.4 0.5 0.2 0.1 0.5
Phenilalanin 1.4 1.5 1.5 1.3 1.3
Hidroksilisine 0.7 0.9 0.7 0.7 0.7
Omitin 0.0 0.0 0.2 0.6 0.0
Lisin 2.6 3.0 2.7 2.6 2.9
Histidin 0.6 0.6 0.4 0.5 0.9
Arginin 5.2 5.3 5.1 4.6 5.6
Sumber: Armesen, 2002
protein. Dalam industri pangan gelatin digunakan sebagai pembentuk gel, penstabil, pengemulsi, pengental, pembentuk busa, pembentuk Kristal, pelapis, perekat, pengikat air, dan penjernih (Jones Ward and Courts,1977).
[image:33.612.243.458.201.330.2]2.3 Belangkas
Gambar 2.3 Belangkas Bagian Depan
Klasifikasi
Kingdom : Animalia
Filum : Arthropoda
Kelas : Merostomata
Ordo : Xiphosura
Famili : Limulidae
penggolongan tersebut adalah karena belangkas memiliki 6 pasang kaki dan tubuh yang beruas-ruas. Ada 4 spesies belangkas yang diketahui oleh manusia dan masih hidup di masa kini di mana keempat spesies tersebut digolongkan ke dalam famili Limulidae. Adapun tempat-tempat yang menjadi habitat asli belangkas adalah pesisir Asia Pasifik (termasuk Indonesia), Asia Selatan, & Amerika Utara bagian tenggara.
Anatomi dan Morfologi
Sudah disinggung di bagian awal kalau belangkas memiliki bentuk yang mirip dengan ikan pari. Tubuh dari belangkas seluruhnya diselubungi oleh cangkang yang keras dan berwarna kecoklatan. Dilihat dari segi anatomis, tubuh dari belangkas terbagi menjadi 3 bagian utama yang masing-masingnya dipisahkan oleh sambungan tipis atau segmen : kepala (prosoma), perut (opisthosoma), dan ekor (telson). Di bagian kepala belangkas terdapat 9 mata yang letaknya terpecar-pencar 1 di masing-masing sisi kepala, 5 di bagian depan, dan 2 di bagian bawah kepala.
Gambar 2.4 Bagian Belakang Belangkas
Jika tubuh belangkas dibalik, akan terlihat kaki-kaki dari belangkas yang bentuknya mirip kaki kepiting atau laba-laba. Total, belangkas memiliki 6 pasang kaki yang memiliki fungsinya masing-masing. Pasangan kaki pertama berguna untuk memegang makanan dan memasukannya ke mulut. Pasangan kaki kedua digunakan untuk berjalan di dasar laut, sementara 4 pasang sisanya digunakan untuk memberikan daya dorong tambahan saat belangkas bergerak. Walaupun belangkas bisa berenang dan melayang di air dengan memakai ekor dan kaki- kakinya, belangkas lebih banyak bergerak dengan cara berjalan dan merayap di dasar laut. (Heard, Willie. 2001).
Harry Noviary (2010) mengemukakan tentang studi karakterisasi pembuatan kitin dan kitosan dari cangkang belangkas, ditunjukkan pada tabel dibawah ini :
Tabel 2.4 Karakterisasi Kitin dan Kitosan dari Cangkang Belangkas
Karakterisasi
Derajat Deasetilasi 82,9 %
Kitosan 83,5 %
Berat molekul kitin 1311000 g/mol Berat molekul kitosan 1048000 g/mol (Sumber : Harry Noviary, 2010)
2.4 Logam Berat Beracun di Perairan
1. Sulit didegradasi, sehingga mudah terakumulasi dalam lingkungan perairairan dan keberadaannya secara alami sulit terurai (dihilangkan)
2. Dapat terakumulasi dalam terakumulasi dalam organism termasuk kerang dan ikan dan akan membahayakan kesehatan manusia yang mengkonsumsi organism tersebut.
3. Mudah terakumulasi di sedimen, sehingga konsentrasinya selalu lebih tinggi dari konsentrasi logam didalam air.
Efek keracunan yang dapat ditimbulkannya berupa penyakit paru – paru, hati, tekanan darah tinggi, gangguan pada sistim ginjal dan kelenjer pencernaan serta mengakibatkan kerapuhan pada tulang ( Clarkson, 1988 dan Saeni, 1997).
Logam timbal (Pb) berasal dari buangan industri metalurgi, yang bersifat racun dalam bentuk Pb-arsenat. Dapat juga berasal dari proses korosi lead bearing alloys.
Kadang – kadang terdapat dalam bentuk kompleks dengan zat organik seperti hexaetil timbal, dan tetra akil lead (TAL) ( Iqbal dan Qodir, 1990). Pada hewan dan manusia timbal dapat masuk kedalam tubuh melalui makanan dan minuman yang dikonsumsi serta melalui pernafasan dan penetrasi pada kulit. Didalam tubuh manusia timbal dapat menghambat aktifitas enzim yang terlibat dalam pembentukan Hemoglobin yang dapat menyebabkan penyakit anemia. Gejala yang diakibatkan oleh keracunan logam timbal adalah kurangnya nafsu makan, kejang, kolik khusus, muntah dan pusing – pusing, timbal juga dapat menyerang susunan saraf dan mengganggu sistim reproduksi, kelainan ginjal dan kelainan jiwa (Iqbal dkk 1990 ; Pallar, 1994)
2.5 Ekstraksi Fase Padat (SPE)
singkat, hasil ektraksi tidak membentuk emulsi serta cukup selektif (Botsoglou dan Fletouris, 2001)
Ekstraksi fase padat dapat dibagi menjadi 4 berdasarkan jenis fase diam atau penjerap yang dikemas dalam cartridge, yakni fase normal (normal phase), fase terbalik (reversed phase), adsorpsi (adsorption) dan pertukaran ion (ion exchange)
(Anonim, 1998). Pemilihan penjerap didasarkan pada kemampuannya berikatan dengan analit, dimana ikatan antara analit dengan penjerap harus lebih kuat dibandingkan ikatan antara analit dengan matriks sampel. Sehingga analit akan tertahan pada penjerap. Selanjutnya dipilih pelarut yang mampu melepaskan ikatan antara analit dengan penjerap pada tahap elusi (Botsoglou dan Fletouris, 2001).
Adapun 4 langkah utama dalam penggunaan ekstraksi fase padat adalah Tahap pertama yaitu pengkondisian (conditioning), merupakan tahapan yang dilakukan dengan penambahan pelarut yang mampu mengaktifkan penjerap serta mampu membasahi permukaan penjerap sehingga analit yang terdapat dalam larutan sampel dapat berinteraksi dengan penjerap. Tahap kedua yaitu retensi (retention/loading) merupakan proses pemasukan larutan sampel, dimana pada proses ini analit yang diinginkan akan tertahan pada penjerap sementara komponen lain dari matriks yang tidak diinginkan akan keluar dari cartridge. Tahap ketiga dilanjutkan dengan pembilasan (washing) yang dilakukan dengan penambahan larutan yang mampu menghilangkan sisa matriks yang tertinggal tetapi tidak mempengaruhi interaksi analit dengan penjerap. Tahap terakhir yaitu pengelusian (elutioning) yang dilakukan dengan penambahan larutan yang mampu memutuskan ikatan analit dengan penjerap (Anonim, 1988)
2.6 Adsorpsi
adsorbat antara lain : aluminium, karbon aktif, silica gel dan lain – lain (Mc. Cabe, 1999)
Adsorpsi yang terjadi karena adanya daya tarik dari permukaan adsorben dan energi kinetik molekul adsorben, dapat berupa adsorpsi fisika, adsorpsi kimia dan adsorpsi isotherm. Pada adsorpsi fisika terjadi gaya van der waals antara molekul adsorbat dan adsorban untuk berikatan. Hal ini terjadi akibat perbedaan energi gaya tarik elektrostatik, oleh karena itu adsorpsi fisika merupakan reaksi reversible, sedangkan reaksi kimia adalah merupakan reaksi antara elektron – elektron pada permukaan adsorben dengan molekul – molekul adsorbat membentuk ikatan yang lebih kuat dibandingkan dengan adsorpsi fisika dan proses ini merupakan irreversible (Besnasconi, 1995).
Proses adsorpsi berlangsung 3 tahap yaitu : pergerakan molekul – molekul adsorbat menuju permukaan adsoben, penyebaran molekul – molekul adsorbat kedalam rongga – rongga adsorben dan penarikan molekul – molekul adsorbat oleh permukaan aktif membentuk ikatan yang berlangsung sangat cepat (sorpsi) (Metcalf and Eddy, 1979)
2.7 Membran
Membran banyak digunakan dalam proses pemisah, pemurnian, dan pemekatan suatu larutan, keunggulan pemisahan dengan menggunakan membran antara lain hemat energi, serta mampu memisahkan larutan – larutan yang peka terhadap suhu.
Membran kitosan lebih mudah diperoleh dibandingkan dengan membran kitin, karena kelarutannya yang tinggi terhadap asam asetat 1 % sehingga mudah untuk mendapatkan membrannya setelah pelarutnya diuapkan, namun ketahanan sobeknya rendah untuk kegunaan tertentu sering ditambahkan polimer penguat seperti polivinil klorida (PVC), PVA, poliester dan N-metilon nilon.
Membran kitosan adalah membran pengkompleks pertama dari polimer alam dan telah digunakan untuk menarik unsur – unsur logam transisi dalam jumlah renik dari larutan garamnya.
2.7.1 Klasifikasi Membran
Banyak jenis membran yang kita kenal sehingga dapat diklasifikasikan menjadi beberapa golongan, misalnya ada membran berukuran tipis atau tebal, strukturnya bisa homogen dan heteragen, membran alami atau buatan dan lain sebagainya, secara makro membran merupakan pembatas antara dua fase yang berjalan secara selektif sedangkan proses pemisahaannya merupakan skala mikro yang meliputi difusi, pelarutan, osmosis, ultrafiltrasi, pertukaran ion dan elektrodialisa (Stephenson, 2000).
Membran dapat dibagi berdasarkan beberapa hal (Mulder, 1991) yaitu : 1. Jenis membran berdasarkan bahan dasar pembuatannya
a. Membran biologis, yaitu membran yang terdapat dalam sel makhluk hidup
b. Membran sintetis, dapat dibedakan memjadi membran organik (bahan penyusun utamanya adalah polimer atau cairan), membran anorganik (bahan penyusun utamanya logam atau non logam, kaca) atau campuran keduanya (keramik)
2. Jenis membran bedasarkan fungsinya
partikel ukuran 0,1 µm dari larutannya, membran mikrofiltrasi dapat dibedakan dari membran reverse osmosis (RO) dan ultrafiltrasi (UL) berdasarkan ukuran partikel yang dapat dipisahkan. Membran ultrafiltrasi ukuran porinya berkisar antara 0,05 – 1 µm terutama untuk pemisahan partikel ukuran 0,001 µm dari larutannya. Sedangkan
proses reverse osmosis menggunakan membran dengan ukuran pori 0,0001 – 0,001 µm, membran reverse osmosis digunakan untuk memisahkan zat terlarut yang
memiliki berat molekul rendah seperti garam anorganik atau molekul orgnik kecil seperti glukosa dan sukrosa dari larutannya.
3. Jenis membran berdasarkan prinsip pemisahan akibat ukuran pori
Berdasarkan ukuran porinya untuk proses pemisahan, membran dapat diklasifikasikan sebagai berikut :
a. Membran berpori, prinsip pemisahannya berdasarkan ukuran partikel zat yang akan dipisahkan dengan ukuran pori – pori membran, membran jenis ini biasa digunakan dalam proses pemisahan mikrofiltrasi dan ultrafiltrasi
b. Membran tak berpori, prinsip pemisahannya berdasarkan perbedaan kelarutan dan kemampuan berdifusi suatu zat terhadap membran tersebut. Membran ini digunakan untuk pemisahan gas dan pervaporasi.
c. Membran cair (berbentuk emulsi), dimana di dalam membran terdapat zat pembawa yang menentukan selektivitas terhadap komponen tertentu yang akan dipisahkan. Pemisahan menggunakan membran cair sering dilakukan dengan teknik difusi berfasilitas dengan memilih jenis emulsi dan zat pembawa yang spesifik untuk zat tertentu.
2.7.2 Membran Polimer
Bahan dasar dari selulosa asetat adalah selulosa. Selulosa adalah merupakan polimer alam yang mempunyai struktur rantai yang linie seperti batang dan molekul infleksibel, bersifat hidrofilik namun tidak larut dalam air, hal ini disebabkan karena sifat kristalin dari ikatan hydrogen antara gugus hidroksilnya (Mulder, 1991)
2.7.3 Karakterisasi Membran
Agar diperoleh membran yang baik perlu dilakukan karakterisasi yang meliputi pengukuran terhadap fungsi dan efesiensi membran yaitu permiabilitas dan permselektivitas membran. Selain daripada itu karakterisasi sifat mekanik juga diperlukan untuk mengetahui kekuatan membran, seperti uji kekuatan tarik dan daya jebol. Morfologi mikrostruktur membran dapat dilihat dengan alat Scanning Electron Microscopy (SEM).
1. Permeabilitas
Permeabilitas merupakan ukuran kecepatan dari suatu spasi untuk menembus membran. Sifat ini dipengaruhi oleh jumlah dan ukuran pori, tekanan yang diberikan, serta ketebalan membran. Permeabilitas dinyatakan sebagai suatu besaran fluks yang didefenisikan sebagai jumlah volume permeat yang melewati satu satuan luas membran dalam suatu waktu tertentu dengan adanya gaya penggerak berupa tekanan (Mulder, 1991).
2. Permeselektivitas
Permeselektivitas dapat digunakan untuk mengetahui daya membran dalam menahan dan melewati suatu partikel. Sifat ini tergantungpada interaksi antara membran dengan partikel tersebut, ukuran pori membran dan ukuran partikel yang akan melewati pori membran. Permselektivitas dinyatakan sebagai koefisien rejeksi, dilambangkan dengan R, yaitu fraksi konsentrasi zat yang tertahan oleh membran. Semakin besar R berarti semakin selektif membran tersebut dalam melewatkan partikel-partikel dalam larutan umpan (Mulder, 1991)
3. Sifat Mekanik
struktur membran, berarti jarak molekul dalam membran semakin rapat sehingga kekuatan tarik dan jebol yang kuat.
2.8 Validasi Metode
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaanya (Harmita, 2004). Menurut USP (United States Pharmacopeia), ada 8 langkah dalam validasi metode analisis yakni akurasi, presisi, batas deteksi, batas kuantifikasi, spesifisitas, linieritas dan rentang, kekasaran (Ruggedness) dan ketahanan (Robutness) (Gandjar dan Rohman, 2007). Akurasi dari suatu metode analisis adalah kedekatan nilai yang terukur dengan nilai sebenarnya, sering kali dinyatakan dalam persen perolehan kembali analit pada penentuan kadar sampel yang mengandung analit dalam jumlah diketahui. Akurasi merupakan ukuran ketepatan prosedur analisis. Akurasi prosedur analisis ditentukan dengan menerapkan prosedur tersebut pada sampel atau campuran komponen matriks yang telah dibubuhi analit dalam jumlah diketahui.
Presisi dari suatu metode analisis adalah derajat kesesuaian di antara masing-masing hasil uji, jika prosedur analisis ditetapkan berulang kali pada sejumlah cuplikan yang diambil dari satu sampel homogen. Presisi dinyatakan sebagai simpangan baku atau simpangan baku relatif (Relative Standard Deviation).
Batas deteksi adalah nilai parameter uji batas, yaitu konsentrasi analit terendah yang masih dapat dideteksi, meskipun tidak selalu dapat dikuantifikasi pada kondisi percobaan yang dilakukan. Limit deteksi dinyatakan dalam konsentrasi analit dalam sampel.
Spesifisitas adalah kemampuan untuk mengukur analit yang dituju secara tepat dan spesifik dengan adanya komponen-komponen lain dalam matriks sampel seperti ketidakmurnian, produk degradasi, dan komponen matriks.
Linieritas merupakan kemampuan suatu metode untuk memperoleh hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran yang diberikan. Rentang didefenisikan sebagai konsentrasi terendah dan tertinggi yang mana suatu metode analisis menunjukkan akurasi, presisi, dan linieritas yang mencukupi. ( Ole Bjorn Jensen, 2005)
Kekasaran merupakan tingkat reprodusibilitas hasil yang diperoleh di bawah kondisi yang bermacam-macam yang diekspresikan sebagai persen standar deviasi relatif (%RSD).
Ketahanan merupakan kapasitas metode untuk tetap tidak terpengaruh oleh adanya variasi parameter metode yang kecil (Gandjar dan Rohman, 2007; Satiadarma, 2004).
2.9 Spektrometri Serapan Atom (SSA)
Larutan sampel dilewatkan ke suatu nyala dan unsur-unsur di dalam sampel diubah menjadi uap atom sehingga nyala rnengandung atom unsur-unsur yang dianalisis. Beberapa diantara atom akan tereksitasi secara termal oleh ayala, tetapi kebanyakan atom tetap tinggal sebagai atom netral dalam keadaan dasar (ground state). Atom-atom ground state ini kemudian menyerap radiasi yang diberikan oleh sumber radiasi yang terbuat dari unsur-unsur yang bersangkutan. Panjang gelombang yang dihasilkan oleh sumber radiasi adalah sama dengan panjang gelombang yang diabsorpsi oleh atom dalam nyala. Absorpsi ini mengikuti hukum Lambert-Beer. yakni absorbansi berbanding lurus dengan panjang uyala yang dilalui sinar dan konsentrasi uap atom dalam nyala. Kedua variabel ini sulit untuk ditentukan tetapi panjang nyala dapat dibuat konstan sehingga absorbansi hanya berbanding langsung dengan konsentrasi analit dalam larutan sampel. Teknik-teknik analisisnya sama seperti pada spektrofotometri UV-Vis yaitu standar tunggal, kurva kalibrasi dan kurva adisi standar. (Perkin elmer, 2007)
2.10 Bahan Acuan
Bahan acuan merupakan suatu bahan yang mempunyai satu atau lebih sifat bahan yang homogen dan cukup stabil untuk dapat digunakan dalam mengkalibrasi peralatan, menguji metode dan jaminan mutu dari hasil suatu pengujian terutama dilaboratorium pangan sehingga dapat menambah tingkat kepercayaan customers terhadap hasil yang dikeluarkan oleh suatu laboratorium. (ISO/IEC 17025:2005), seluruh pengujian kimia harus tertelusur ke satuan SI untuk pengujian kimia ketertelusuran pengujian kimia digambarkan seperti dibawah ini.
Satuan SI
(1 mol = 0.012 kg atom 12C) Standard Internasional (misalnya standard massa)
Bahan Acuan Murni (misalnya KIO3, Ag murni)
Metode Primer
Bahan Acuan Bermatriks Primer (misalnya CRM dari NIST, IRRM) Metode dan Bahan Acuan Sekunder
(misalnya AAS, Na2S2O3)
Gambar 2.5 Ketertelusuran Pengujian Kimia
Berbeda dengan ketertelusuran kimia fisika ke SI yang lebih transparan dan langsung, ketertelusuran kimia ke SI adalah lebih sulit. Satuan SI untuk pengukuran kimia (amount of substance) adalah mol, yaitu jumlah atom atau molekul yang setara dengan 0.012 kilogram atom karbon-12. Penerapan dari satuan mol ini untuk menggambarkan ketertelusuran kimia masih membingungkan, karena itu masalah ketertelusuran pengukuran kimia dipecahkan dengan perantaraan metode primer dan bahan acuan
BAB 3
METODOLOGI PENELITIAN
3.1 Alat dan Bahan
3.1.1 Alat – alat Penelitian
Alat – alat yang digunakan dalam penelitian ini adalah : - Alat – Alat gelas yang biasa digunakan dilaboratorium
- Timbangan analitik dengan ketelitian 0,0001 g, Scaltec - Desikator
- Oven Memmert - Microwave Digestion CEM - Hot plate
- Micrometer Screw
- Seperangkan alat Spectrofotometer Serapan Atom (Atomic Absorption Spectrophotometer), Perkin Elmer Grafite Furnace A-Analyst 800
- Scanning Electron Microscopy (SEM) – EDX Bruker – Carl Zeiss Evo MA - Fourier Transform Infared Microscopy (FTIR) Shimadzu
Pengukuran Spektrofotometer Serapan Atom (AAS) dilakukan di Laboratorium Balai Pembinaan dan Pegujian Mutu Hasil Perikanan Medan dan analisa SEM (Scanning Electron Microscopy) dilakukan di Laboratorium Pusat Laboratorium Forensik POLRI Jakarta, serta pengukuran pergeseran bilangan gelombang digunakan Spektroskopis FT-IR di Laboratorium Kimia Organik Universitas Gajah Mada – Jogjakarta, sedangkan uji tarik dilakukan di Laboratorium Teknik Kimia Universitas Sumatera Utara.
Bahan utama yang digunakan dalam penelitian ini adalah kitosan dari cangkang belangkas dan gelatin komersil. Sedangkan bahan analisis dan pembantu yang digunakan dalam penelitian ini adalah :
- Tepung ikan
Tepung ikan yang digunakan dalam penelitian ini adalah merupakan suatu bahan
Standart References Material (SRM) yang sudah memiliki nilai sertifikat kandungan logam timbal (Pb) dan mempunyai merek dagang DOM-3 - Canada - Air deionisasi
- Larutan Standart Pb Merck
- NaOH
- V2O5 Merck
- CH3COOH glasial p.a (Merck)
- HNO3 p.a (Merck
- HCl p.a (Merck)
3.2 Prosedur Penelitian
Penelitian ini terdiri dari delapan tahap yaitu : 1. Penyedian membran kitosan – gelatin 2. Preparasi bahan acuan
3. Uji SEM 4. Uji FTIR
5. Ekstraksi dengan vacum SPE 6. Validasi metode
7. Analisis dengan AAS 8. Uji kekuatan tarik
3.2.1 Penyediaan Membran Kitosan – Gelatin
Sebanyak 2 g gelatin dilarutkan kedalam 100 ml air deionisasi. Kelarutan gelatin dalam air sangat dipengaruhi oleh suhu lingkungan, biasanya gelatin akan larut sempurna didalam air pada suhu 60 oC selama 3 jam. Sebaiknya larutan yang terbentuk segera digunakan, apabila larutan yang terbentuk tidak segera digunakan, disimpan dalam kulkas dan panaskan terlebih dahulu jika akan digunakan. (Jeanette, 2009) - Pembuatan Larutan Kitosan 2 %
Sebanyak 2 g kitosan dilarutkan kedalam 100 ml larutan asam asetat 1 %. Sebaiknya larutan yang terbentuk segera digunakan.
3.2.1.1 Penyediaan Membran Kitosan – Gelatin dengan Perbandingan Volume
-
larutan kitosan dan gelatin yang tersedia di tuangkan ke petridish dengan perbandingan volume kitosan dan gelatin yaitu 25% : 75%, 50% : 50% dan 75% : 25%-
Kemudian dikeringkan di dalam oven pada suhu 60 0C selama 18 jam- Film kitosan - gelatin yang terbentuk dilepaskan dari petri dish, kemudian dicelupkan kedalam larutan NaOH 1 % dan dilanjutkan dengan pencucian berulang – ulang dengan air deionisasi untuk menghilangkan kadar NaOH dan dikeringkan pada suhu kamar
- ulangi prosedur 1 sampai 3 untuk perbandingan kitosan – gelatin 50% : 50 % dan 75% : 25%
3.2.1.2 Penyediaan Membran Kitosan – Gelatin dengan Memvariasikan
Kadar Serbuk Gelatin
- Sebanyak 10 ml larutan kitosan di tuangkan ke petridish, kemudian ditaburi dengan serbuk gelatin dengan kadar 0.1 g, 0.2 g, 0.3 g, 0.4 g, dan 0.5 g
- Film kitosan - gelatin yang terbentuk dilepaskan dari petri dish, kemudian dicelupkan kedalam larutan NaOH 1 % dan dilanjutkan dengan pencucian berulang – ulang dengan air deionisasi dan dikeringkan pada suhu kamar
- ulangi prosedur 1 sampai 3 untuk kadar kitosan 0.2 g – 0.5 g
3.2.2 Preparasi Bahan Acuan
- Tepung ikan ditimbang sebanyak 0,5 g dan dimasukkan kedalam vessel
Microwave Digestion
- Kemudian tambahkan V2O5 sebanyak 0,02 g
- Selanjutnya tambahkan HNO3 (pekat) sebanyak 10 ml melalui dinding vessel - Dengan segera tutup vessel sekuat mungkin agar tidak ada uap yang keluar - Masukkan vessel kedalam rak microwave digestion secara berurutan
- Kemudian rak yang sudah berisi vessel dimasukkan kedalam alat microwave digestion
- Operasikan microwave digestion dengan method yang sudah tersedia (Power = 100, T = 200 oC, t = 15 menit)
- Matikan temperatur Microwave digestion setelah 15 menit
- Selanjutnya tunggu temperatur turun, kemudian vessel dikeluarkan dari alat
Microwave digestion
- Sediakan labu takar 50 ml dan diberi label masing – masing labu takar
- Kemudian larutan yang terbentuk dipindahkan kedalam labu takar 50 ml seterusnya diencerkan dengan aqudes sampai garis tanda
(Sumber SNI 01-2354.5-2011)
3.2.3 Uji SEM
Sebelum dilakukan pengujian dengan SEM terlebih dahulu membran diukur ketebalannya, uji SEM ini dilakukan untuk mengetahui morfologi membran yang dihasilkan antara membran kitosan, membran gelatin dan membran kitosan - gelatin
Pada tahapan ini membran kitosan – gelatin digunakan untuk menurunkan kadar logam timbal (Pb) yang ada dalam larutan tepung ikan, adapun tahap pengoperasiannya adalah sebagai berikut :
- Membran kitosan – gelatin dimasukkan kedalam kolom SPE
- Kolom SPE yang telah diisi membran diletakkan diatas alat vacuum SPE - larutan tepung ikan hasil destruksi dipipet sebanyak 10 ml, kemudian
dimasukkan kedalam kolom
- Selanjutnya larutan tepung ikan dilewatkan pada kolom SPE dengan bantu pompa dan ditampung untuk dianalisis menggunakan Spektrofotometer Serapan Atom (AAS).
Gambar 3.1 dan 3.2 menunjukkan membran yang masih dalam cetakan dan membran yang sudah dicelupkan kedalam NaOH setelah beberapa kali pencucian dengan aquades.
[image:50.612.219.408.367.549.2]
Gambar 3.2 Foto Membran Kitosan setelah dicelupkan kedalam NaOH
Gambar 3.3 Menunjukkan Mekanisme Penyerapan Logam Pb dengan Membran Kitosan – Gelatin
Keterangan gambar : 1. Pompa Vacum
1
2 3
4
[image:51.612.219.406.77.260.2]2. Kolom
3. Vacum Chember 4. Kolom SPE
5. Tabung penampung
3.2.5 Validasi Metode
Validasi metode adalah suatu konfirmasi bahwa metode yang bersangkutan memenuhi persyaratan yang ditentukan (sesuai tujuan tertentu) dengan cara menguji metode dan melengkapi bukti-bukti yang objektif. (SNI 19-17025-2000).
Karakteristik validasi yang dilakukan dalam penelitian ini adalah uji sensitivity alat, uji linerity, uji batas deteksi (LoD dan LoQ), uji repeatability, uji presisi dan uji akurasi.
3.2.6 Analisis dengan AAS
- penurunan larutan stock standar logam Pb 1000 ppm
Larutan stock standar logam Pb 1000 ppm diturunkan menjadi 100 ppm, dari 100 ppm kemudian diturunkan lagi menjadi 10 ppm sampai 1 ppm.
- Pembuatan titik kurva kalibrasi
Kurva kalibrasi dibuat sebanyak lima titik konsentrasi yaitu 2 ppb, 4 ppb, 6 ppb dan 8 ppb
- Kondisi operasi alat
Element Timbal (Pb)
Lampu / Current Hallow cathode lamp / 12 mA Panjang gelombang Pb =283,3
Slit 0,7 nm (low)
Atomisation site Pyro / platform Tipe pengukuran Area grafik
Tipe signal Atomic absorption – Background absorption Waktu integrasi 4 menit
Volume sampel 20 µl Temperatur inject 20 0C
Tekanan gas Argon 3.6 bar atau 52 psig atau 360 kPa Kecepatan alir gas Argon 300 ml/min
Sensitivity check Pb 50 µg/l Absorbansi 0.15 ± 20 % (Perkin Elmer, 2007)
3.2.7 Perhitungan
3.3 Bagan Penelitian
3.3.1. Pembuatan Membran Kitosan - Gelatin ( Kitosan dan Gelatin sama – sama dilarutkan )
Gambar 3.4 Bagan Penelitian Pembuatan Membran Kitosan –Gelatin (v/v)
3.3.2. Pembuatan Membran Kitosan - Gelatin ( Larutan Kitosan dengan serbuk Gelatin )
2 g serbuk Gelatin
Larutan Gelatin 2 g serbuk Kitosan
Larutan Kitosan
dilarutkan dalam 100 ml CH COOH
dilarutkan dalam 100 ml aquades
Campuran larutan Kitosan + Gelatin
Masing – masing larutan dituang ke dalam cetakan dengan perbandingan Kitosan : Gelatin (25% : 75%, 50% : 50%, 75% : 25%) dihomogenkan
dikeringkan pada suhu 60 0C selama 18 Jam
Film Kitosan + Gelatin
dicelupkan kedalam NaOH didiamkan pada suhu kamar
dicuci berulang – ulang dengan aquades didiamkan pada suhu kamar
Membran Kitosan + Gelatin
Analisa SEM
2 g serbuk Kitosan
dilarutkan dalam 100 ml CH3COOH 1 % Larutan Kitosan 2 %
dituang ke cetakan
ditaburi serbuk gelatin (0.1%, 0.2%, 0.3%, dan 0.4%) dihomogenkan
dikeringkan pada suhu 60 oC selama 18 jam Film Kitosan - Gelatin
Analisa FTIR
Gambar 3.5 Bagan Penelitian Pembuatan Membran Kitosan – Gelatin (w/v)
3.3.3 Penggunaan Membran Kitosan - Gelatin Sebagai Penurun Konsentrasi Ion Logam
Gambar 3.6 Bagan Penelitian Penggunaan Membran Kitosan - Gelatin
Larutan hasil
Analisis logam Pb dengan AAS 10 ml larutan bahan
dilewatkan melalui membran kitosan – gelatin dengan variasi campuran larutan Kitosan : larutan Gelatin ( 25% :75%, 50% : 50% dan 75% :25%) dan campuran larutan kitosan 2% dengan
dicelupkan kedalam NaOH didiamkan pada suhu kamar
dicuci berulang – ulang dengan aquades didiamkan pada suhu kamar
BAB 4
HASIL DAN PEMBAHASAN
4.1 Pengaruh Persentase Kitosan dan Gelatin terhadap Morfologi
Membran Kitosan – Gelatin
a. Hasil SEM Kitosan
b. Hasil SEM Gelatin
Gambar 4.2 Hasil SEM Membran Gelatin dan Unsur Gelatin
4.2. Analisa Membran Kitosan Gelatin dengan FTIR
FTIR dapat memperlihatkan informasi dalam memprediksi dan mengidentifikasi gugus fungsi yang ada dalam suatu senyawa. FTIR merupakan cara yang paling mudah dan cepat untuk melihat senyawa senyawa kimia pada permukaan membran. Analisa menggunakan FTIR (Fourier Tansfom infrared spectra), ini dilakukan untuk mengetahui ada tidaknya gugus fungsi kitosan dan gelatin di dalam membran yang terbentuk.
Gambar 4.4 Spektrum Transformasi Infra Merah (FTIR) Membran Kitosan
Tabel 4.1 Hasil Analisis FTIR Kitosan Gugus Fungsi Bilangan
Gelombang (cm-1) Yang diperoleh
Bilangan Gelombang (cm-1)
Literatur O-H
N-H (Amina) C-H C=O (Amida)
C-N C-O
3749.62 3425.58 2924.09 1635.64 1342.46 1080.14
3600-3800 3500-3100 3000-2800 1670-1600 1350-1000 1080 – 1300 Sumber Fesseden J.R 1999
[image:61.612.149.470.106.275.2]Sedangkan untuk identifikasi gugus fungsi pada gelatin ditunjukkan pada gambar 4.5 sebagai berikut :
[image:61.612.127.524.351.613.2]Berdasarkan hasil FTIR pada gambar 16 menunjukkan puncak serapan khas muncul pada gugus amina NH(3425.58 cm-1), gugus karbonil C=O (1635.64 cm-1), gugus O-H bebas (3749.62 cm-1), dan gugus amina C-N (1342.46 cm-1).
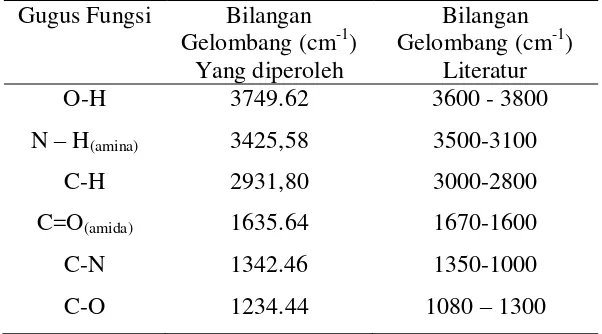
Tabel 4.2 Hasil Analisis FTIR Gelatin Gugus Fungsi Bilangan
Gelombang (cm-1) Yang diperoleh
Bilangan Gelombang (cm-1)
Literatur O-H
N – H(amina) C-H C=O(amida)
C-N C-O
3749.62 3425,58 2931,80 1635.64 1342.46 1234.44
3600 - 3800 3500-3100 3000-2800 1670-1600 1350-1000 1080 – 1300
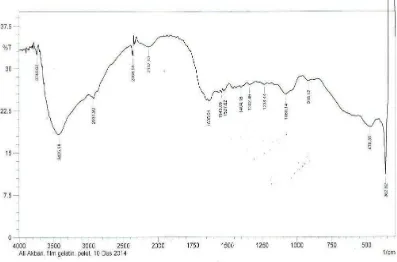
Gambar 4.6 Spektrum Transformasi Infra Merah (FTIR) Membran Kitosan – Gelatin Berdasarkan hasil FTIR pada gambar 4.. menunjukkan puncak serapan khas muncul pada gugus amina NH(2924.09 cm-1), gugus karbonil C=O (1635.64cm-1), gugus amina C-N (1080.14cm-1) gugus OH bebas (3749.62 cm-1) dan gugus asetil C-O (1156 cm-1) hal ini menunjukkan bahwa terjadi interaksi kimia antara kitosan dengan gelatin.
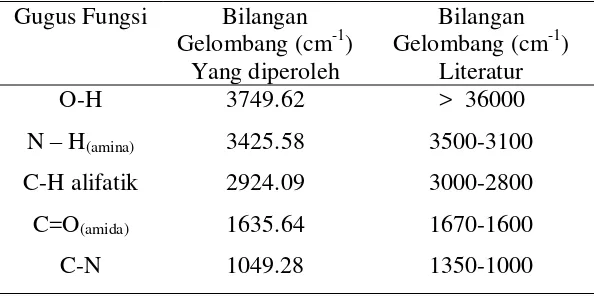
Tabel 4.3 Hasil analisis FTIR membran kitosan – gelatin Gugus Fungsi Bilangan
Gelombang (cm-1) Yang diperoleh
Bilangan Gelombang (cm-1)
Literatur O-H
N – H(amina) C-H alifatik
C=O(amida) C-N
3749.62 3425.58 2924.09 1635.64 1049.28
[image:63.612.172.469.519.668.2]Secara keseluruhan hasil analisis FTIR dalam penelitian ini dapat dilihat pada hasil spektrum dibawah ini :
4000 3500 3000 2500 2000 1500 1000 500 0
0.0 7.5 15.0 22.5 30.0 37.5
%T
cm-1
Film gelatin-kitosan mempunyai perbedaan daerah serapan pada 1580-1490 cm-1 dan 1700-1630 cm-1 dengan film gelatin dan film kitosan. Cara yang mudah untuk melihat interaksi yang terjadi pada campuran gelatin dan kitosan adalah dengan cara membandingkannya dengan spektra gelatin dan kitosan itu sendiri. Apabila pada spektra film gelatin-kitosan tidak ada perubahan, hal ini menandakan tidak adanya interaksi antara kedua senyawa tersebut. Peningkatan intensitas beberapa pita serapan pada daerah 1700-1500 cm-1. Hal ini berkaitan dengan adanya interaksi elektrostatik antara gugus amino dan karbonil melalui pembentukkan kompleks polielektrolit (PEC). Spektra infra merah film gelatin-kitosan pada daerah 1700-1500 cm-1 tidak mengalami perubahan posisi puncak yang signifikan, sehingg