OPTIMASI SINTESIS MONOGLISERIDA
DARI MINYAK INTI SAWIT MENGGUNAKAN KATALIS NATRIUM HIDROKSIDA DAN PELARUT TER-BUTANOL
TESIS
Oleh
SRI KUNCOROWATI 097006036/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA MEDAN
2012
OPTIMASI SINTESIS MONOGLISERIDA DARI MINYAK INTI SAWIT MENGGUNAKAN KATALIS NATRIUM HIDROKSIDA
DAN PELARUT TER-BUTANOL
TESIS
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Sains dalam Program Studi Ilmu Kimia Pascasarjana FMIPA
Universitas Sumatera Utara
Oleh
SRI KUNCOROWATI 097006036/KIM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA MEDAN
2012
Universitas Sumatera Utara
PENGESAHAN THESIS
Judul Tesis : OPTIMASI SISNTESIS MONOGLISERIDA DARI MINYAK INTI SAWIT MENGGUNAKAN KATALIS NATRIUM HIDROKSIDA DAN PELARUT TER- BUTANOL
Nama Mahasiswa : Sri Kuncorowati Nomor Pokok : 097006036
Program Studi : Magister Ilmu Kimia
Menyetujui Komisi Pembimbing
(Dr. Mimpin Ginting, MS) (Dr. Donald Siahaan Ketua Anggota
)
Ketua Program Studi Dekan
(Prof. Basuki Wirjosentono, MS, Ph.D) (Dr.Sutarman, MSc)
Tanggal Lulus: 4 Mei 2012
PERNYATAAN ORISINALITAS
OPTIMASI SINTESIS MONOGLISERIDA DARI MINYAK INTI SAWIT MENGGUNAKAN KATALIS NATRIUM HIDROKSIDA
DAN PELARUT TER-BUTANOL
TESIS
Dengan ini saya menyatakan bahwa saya mengakui semua karya Tesis ini adalah hasil kerja saya sendiri kecuali kutipan dan ringkasan yang tiap satunya telah dijelaskan sumbernya dengan benar.
Medan, 4 Mei 2012
Sri Kuncorowati NIM. 097006036
Universitas Sumatera Utara
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Sebagai Sivitas Akademika Universitas Sumatera Utara, saya yang bertanda tangan di bawah ini:
Nama : Sri Kuncorowati Nomor Pokok : 097006036
Program Studi : Magister Ilmu Kimia Jenis Karya Ilmiah : Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non-Eksklusif (Non-Exclusif Royalty Free Right) atas Tesis saya yang berjudul:
OPTIMASI SINTESIS MONOGLISERIDA DARI MINYAK INTI SAWIT MENGGUNAKAN KATALIS NATRIUM HIDROKSIDA DAN PELARUT
TER-BUTANOL
beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti Non- Eksklusif ini, Universitas Sumatera Utara berhak menyimpan, mengalih media, memformat, mengelola dalam bentuk data-base, merawat dan mempublikasikan Tesis saya tanpa meminta izin dari saya selama tetap mencantumkan nama saya sebagai penulis dan sebagai pemegang dan atau sebagai pemilik hak cipta.
Demikian pernyataan ini dibuat dengan sebenarnya.
Medan, 4 Mei 2012
Sri Kuncorowati NIM. 097006036
Telah diuji pada Tanggal : 4 Mei 2012
PANITIA PENGUJI TESIS
Ketua : Dr. Mimpin Ginting, MS
Anggota : 1. Prof. Basuki Wirjosentono MS, Ph.D 2. Prof. Dr. Jamaran Kaban, MSc 3. Dr. Hamonangan, MSc
4. Dr. Donald Siahaan
Universitas Sumatera Utara
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 13 Maret 1967 dan telah dikarunai tiga orang anak. Penulis menyelesaikan pendidikan dasar di SD Srikandi Jakarta tahun 1979, pendidikan menengah pertama di SMPN 44 Jakarta tahun 1982 serta pendidikan menengah atas di SMAN 21 Jakarta tahun 1985. Selanjutnya pada tahun yang sama penulis diterima di jurusan kimia Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas Padjadjaran
Bandung, melalui seleksi mahasiswa baru (SIPENMARU), dan menyelesikan studi pada tahun 1991. Setelah lulus S1 sempat bekerja di beberapa instansi swasta, diantaranya sebagai dosen di Politeknik Gajah Tunggal selama lima tahun, sebagai manajer training di Lembaga Swadaya Masyarakat selama 7 tahun dan sebagai staf pengajar SMA selama 3 tahun. Pada tahun 2009 (semester genap) penulis melanjutkan pendidikan S2 pada Program Magister ilmu kimia pada Fakultas Matematika Dan Ilmu Pengetahuan Alam Universitas Sumatera Utara Sumatra Utara dan lulus pada bulan Mei tahun 2012.
i
KATA PENGANTAR
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas segala rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan penelitian dan penulisan tesis ini. Tesis ini disusun sebagai salah satu syarat untuk memperoleh gelar Magister Sains dalam program studi ilmu kimia pada Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. Penulis mengucapkan terimakasih dan penghargaan setinggi-tingginya kepada:
Bapak Dr. Mimpin Ginting, MS selaku Pembimbing Utama dan Bapak Dr.
Donald Siahaan selaku Anggota Komisi Pembimbing yang telah mengorbankan waktu dan tenaga untuk memberikan pengetahuan dan bimbingan yang sangat bermanfaat bagi penyusunan tesis ini.
Prof. Basuki Wirjosentono, MS, Ph.D dan Prof. Dr. Jamaran Kaban, MSc serta Dr. Hamonangan, MSc selaku penguji yang banyak memberikan masukan dan saran untuk penyusunan tesis ini.
Kepada Bapak Direktur Pusat Penelitian Kelapa Sawit (PPKS), Dr.
Witjaksana Darmosarkoro yang telah memberikan kesempatan dan segala fasilitas untuk melakukan penelitian yang menunjang penyusunan tesis.
Kepala Laboratorium Pengolahan Hasil dan Mutu dan para kelompok penelitinya serta Bapak Hasrul Hasibuan, MS dan Ibu Frisda, MS yang telah memberikan perhatian dan bantuannya selama melakukan penelitian.
Secara khusus dan terimakasih yang sedalam-dalamnya tak lupa penulis haturkan kepada suami tercinta Ir. Tumpal P. Saragi MSc dan ananda tersayang
Universitas Sumatera Utara
Andri, Aldri dan Lina atas kasih sayang, motivasi, pengorbanan, kesabaran dan hiburannya dalam menemani penulis menyelesaikan pendidikan.
Akhirnya kepada semua pihak yang telah membantu dalam melaksanakan pendidikan dan penelitian ini penulis menyampaikan terimakasih yang tak terhingga, semoga Allah SWT memberikan balasan yang setimpal.
Medan, 4 Mei 2012
Sri Kuncorowati NIM. 097006036
iii
OPTIMASI SINTESIS MONOGLISERIDA DARI MINYAK INTI SAWIT MENGGUNAKAN KATALIS NATRIUM HIDROKSIDA DAN PELARUT
TER-BUTANOL
ABSTRAK
Monogliserida merupakan salah satu produk yang dihasilkan dari minyak inti sawit yang berfungsi sebagai emulsifier. Industri sabun, deterjen, kosmetik dan pangan sangat membutuhkan monogliserida bagi pengolahan produksinya, namun di Indonesia ketersediannya masih kurang memadai sehingga harus diimpor. Kondisi ini menunjukkan bahwa peluang investasi dan produksi MG di dalam negeri sangat baik.
Penelitian bertujuan untuk melakukan sintesis monogliserida melalui gliserolisis minyak inti sawit yaitu Refined Bleached Deodorized Palm Kernel Oil (RBDPKO) menggunakan katalis NaOH dalam pelarut ter-butanol dan untuk mengetahui kondisi optimum reaksi seperti: rasio mol RBDPKO/gliserol, konsentrasi katalis serta suhu reaksi.
Penelitian berupa eksperimen laboratorium yang dibagi menjadi tiga tahap: 1).
Karaktrerisasi bahan baku yakni menentukan kadar asam lemak bebas dan kadar air dari bahan baku yang digunakan 2). Penentuan titik tengah yang digunakan sebagai titik nol dalam percobaan 3). Menentukan kondisi optimum reaksi dengan metode respon permukaan dimana variabel bebasnya diambil dari hasil percobaan pada penentuan titik tengah yakni: rasio mol gliserol/RBDPKO titik tertinggi, titik nol dan titik terendahnya masing-masing (10:1, 15:1 dan 20:1), konsentrasi katalis (1%, 1,5% dan 2% b/bRBDPKO) serta suhu (80o, 90o dan 95o
Hasil analisis karakteristik bahan baku didapatkan kadar asam lemak bebas 0,18%
dan kadar air 0,041%. Dari pengolahan data analisis hasil giserolisis menggunakan parangkat lunak minitab 14 didapatkan kondisi optimum reaksi pada rasio gliserol/RBDPKO (7:1-10:1), konsentrasi katalis (1-2)% serta suhu pada (82-90)
C). Sedangkan untuk variabel tetap adalah total campuran reaksi 200 gram, kecepatan pengadukan 700 rpm, waktu pengadukan 1 jam dan jumlah pelarut 20 ml/10 gram RBDPKO. Analisis dilakukan dengan metode kromatografi lapis tipis dan kromatografi gas.
oC.
Kata kunci: Gliserolisis, minyak inti sawit, monogliserida, natrium hidroksida, ter- butanol.
Universitas Sumatera Utara
OPTIMIZATION OF THE SYNTHESIS OF MONOGLYCERIDES FROM PALM KERNEL OIL USING SODIUM HYDROXIDE AS CATALYST
AND SOLVENT ter-BUTANOL
ABSTRACT
Monoglyceride is one of the products produced from palm kernel oil that functions as emulsifier. In Manufacturing of soap, detergents, cosmetics and food,the monoglyceride is essentialfor their processing production, but in Indonesia the availability is still inadequate so it must be imported. This condition indicates that the investment opportunities and MG production in the country is very prospective.
The research aims to conduct the monoglyceride synthesis through glycerolysis of
palm kernel oil namelyRefinedBleachedDeodorizedPalmKernelOil(RBDPKO) usingNaOHcatalys
tin asolvent
Research inexperimental laboratory experiments was divided into three phases: 1).
Characterization of the raw materials that determine the levels of free fatty acids and water content of the raw material used 2). Determination of the midpoint is used as the zero point in the experiment 3). Determine the optimum reaction conditions by response surface method in which the independent variables drawn from the results of experiments on the determination of the midpoint of which were: mole ratio of glycerol / RBDPKO highest point, the zero point and lowest point of each (10:1, 15:1 and 20:1) , the concentration of catalyst (1%, 1.5% and 2% w / bRBDPKO) and temperature (80
tert-butanol solvent and to determine the optimum reaction conditions such as: the mole ratio RBDPKO / glycerol, the catalyst concentration as well as the reaction temperature
o, 90o and 95o
From the characteristics of the raw materials analysis obtained free fatty acid contents 0.18% and the water contents0.041%. From the result of data software using Minitab 14, optimum reaction conditions obtained in the ratio of glycerol / RBDPKO (7:1-10:1), catalyst concentration (1-2)% and the temperature on the (82- 90)
C). As for the fixed variable was the total reaction mixture of 200 grams, the stirring speed of 700 rpm, stirring time of 1 hour and the amount of solvent is 20 ml/10 grams RBDPO. Analyses were performed through the method of thin layer chromatography and gas chromatography.
oC.
Keywords : Glycerolysis, monoglyceride, sodium hydroxide, palm kernel oil, tert-butanol.
v
DAFTAR ISI
KATA PENGANTAR i
ABSTRAK iii
ABSTRACT iv
DAFTAR ISI v
DAFTAR GAMBAR DAFTAR TABEL DAFTAR LAMPIRAN
BAB I. PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Perumusan Masalah 3
1.3 Tujuan Penelitian 3
1.4. Ruang Lingkup Penelitian 3
1.5 Manfaat Penelitian 3
BAB II. TINJAUAN PUSTAKA 4
2.1. Minyak Inti sawit 4
2.2. Monogliserida 7
2.2.1. Kegunaan Monogliserida 7
2.2.2. Sintesis Monogliserida 8
2.3. Transesterifikasi 9
2.3.1. Pengaruh Asam Lemak Dan Kadar Air 10
2.3.2. Macam Dan Konsentrasi Katalis 12
2.3.3. Rasio Molar Alkohol Terhadap Minyak dan Jenis Alkohol 13
2.3.4. Suhu Reaksi 13
2.4. ter-Butanol 13
2.5. Gliserol 14
2.6. Kromatografi 15
Universitas Sumatera Utara
2.6.1. Kromatografi Lapis Tipis 16
2.6.2. Kromatografi Gas 17
BAB III. METODOLOGI PENELITIAN 19
3.1. Tempat dan Waktu Penelitian 19
3.2. Alat dan Bahan 19
3.2.1. Bahan yang digunakan 19
3.2.2 Peralatan 19
3.3. Metode Penelitian 21
3.3.1. Karakterisasi Bahan Baku 21
3.3.2. Penentuan Titik Tengah 22
3.3.3. Penetapan Kondisi Optimum 22
3.3.4. Prosedur 25
3.3.4.1. Gliserolisis 25
3.3.4.2. Prosedur Analisis Gliserida dengan KLT 26 3.3.4.3. Prosedur Analisis Gliserida dengan KG 27
3.4. Analisis Kadar Monogliserida 27
3.4.1. Analisis Kadar Monogliserida Dengan KG 27 3.4.2 Analisis Kadar Monogliserida Dengan KLT 30
BAB IV. HASIL DAN PEMBAHASAN 32
4.1. Karakteristik Bahan Baku 32
4.2. Penentuan Titik Tengah 34
4.3. Penetapan Kondisi Optimum 36
4.3.1. Pengaruh Variabel Bebas Terhadap Kadar MG 40 4.3.2. Pengaruh Rasio Gliserol/RBDPKO Terhadap Kadar MG 41 4.3.3. Pengaruh Katalis Terhadap Kadar MG 44 4.3.4. Pengaruh Suhu Terhadap Kadar MG 45
BAB V. KESIMPULAN DAN SARAN 47
5.1. Kesimpulan 47
5.2. Saran 47
DAFTAR PUSTAKA 48
LAMPIRAN
vii
Universitas Sumatera Utara
DAFTAR GAMBAR
Nomor Judul Halaman
2.1. Buah Kelapa Sawit 4
2.2. Reaksi Penyabunan 6
2.3. Struktur Monogliserida 8
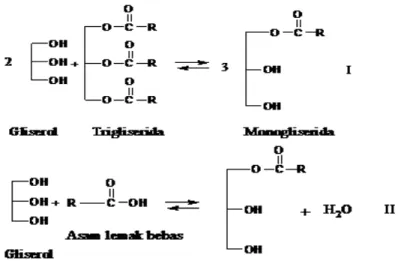
2.4. Reaksi Untuk Memproduksi Monogliserida Secara Industri Kimia 8
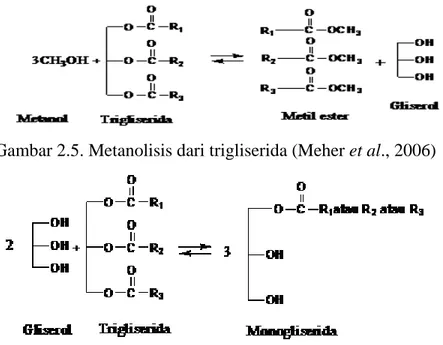
2.5. Metanolisis dari Trigliserida 10
2.6. Gliserolisis dari Trigliserida 10
2.7. Mekanisme Transesterifikasi dengan Katalis Basa 12
2.8. Struktur ter-Butanol 14
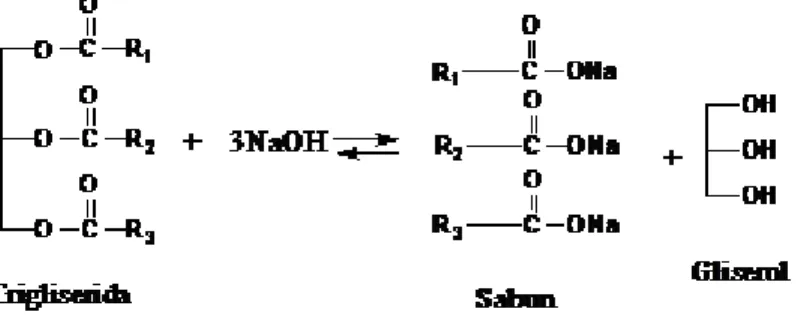
2.9. Reaksi Saponifikasi Lemak 15
2.10. Reaksi Transesterifikasi Trigliserida 15
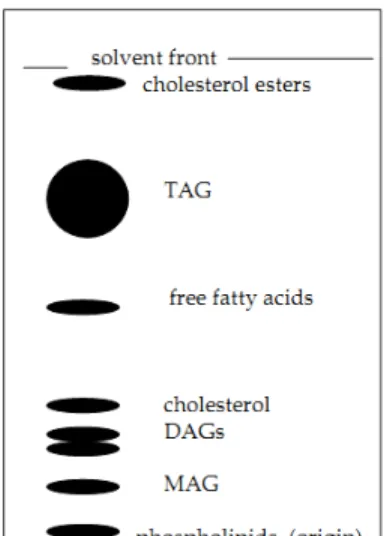
2.11. Hasil KLT Ekstrak Lipid 17
2.12. Kromatogram Standar Internal Kromatografi Gas 18 2.13. Kromatogram Asam Lemak Metil Ester Hasil Transesetrifikasi 18
Minyak Nabati
3.1. Peralatan Penelitian 20
3.2. Diagram Alir Gliserolisis Pada Sintesis Monogliserida 25 3.3. Kromatogram Standar Untuk Mono-, Di- dan Trigliserida 28
3.4. Reaksi Asam Laurat dan Gliserol 28
3.5. Kromatogram dari Hasil Reaksi Asam Laurat dan Gliserol 29
3.6. Kromatogram Hasil Gliserolisis Sampel 1 29
3.7. Contoh Spot dari KLT Hasil Gliserolisis dan Hasil Sintesis 30 Monolaurin (Pembanding)
4.1. Reaksi Penyabunan Antara Katalis dengan Asam Lemak Bebas 32
4.2. Reaksi Hidrolisis Trigliserida 34
4.3. Tahapan Reaksi Gliserolisis 42
4.4. Kontur Kadar MG Terhadap Rasio Gliserol/RBDPKO dan Katalis 43
ix
4.5. Kontur Kadar MG Terhadap Rasio Gliserol/RBDPKO dan Suhu 43
4.6. Kontur Kadar MG Terhadap Katalis dan Suhu 44
4.7. Reaksi Gliserol dengan Katalis NaOH 45
Universitas Sumatera Utara
DAFTAR TABEL
Nomor Judul Halaman
2.1. Komposisi asam lemak minyak inti sawit dan minyak sawit 5 3.1. Tingkat Kode Untuk Variabel Bebas yang Digunakan Dalam 23
Percobaan Gliserolisis RBDPKO dengan Gliserol
3.2. Matriks CCD 3 Variabel Gliserolisis RBDPKO dengan Katalis NaOH 24 4.1. Komposisi asam bebas, kadar ALB dan kadar air bahan baku RBDPKO 33 4.2. Hasil Gliserolisis Penentuan Titik Tengah Untuk Rasio Gliserol/ 35
RBDPKO
4.3. Hasil Gliserolisis Penentuan Titik Tengah Untuk Konsentrasi Katalis 35 4.4. Hasil Gliserolisis Penentuan Titik Tengah Untuk Suhu 36 4.5. Kadar Monogliserida Hasil Analisa dengan Metode KG Pada Beragam 37
Kondisi Proses
4.6. ANOVA Untuk Kadar MG Hasil Analisis KG 38
4.7. Kadar Monogliserida Hasil Analisis dengan Metode KLT 39
4.8. ANOVA Untuk Kadar MG Hasil Analisis KLT 40
4.9. Matriks Interaksi Variabel Bebas Terhadap Kadar MG 41
xi
DAFTAR LAMPIRAN
Nomor Judul Halaman
1. Kromatogram Komposisi Asam Lemak dari RBDPKO L-1
2. Penimbangan Bahan Baku L-2
3. Kadar MG, DG dan TG Penentuan Titik Tengah Untuk L-3 Rasio Gliserol/RBDPKO
4. Kadar MG, DG dan TG Penentuan Titik Tengah Untuk Konsentrasi Katalis L-4 5. Kadar MG, DG dan TG Penentuan Titik Tengah Untuk Suhu L-5
6. Kadar MG, DG dan TG Hasil Analisis dengan KLT L-6
7. Hasil KLT Pada Penentuan Campuran Pengelusi yang Digunakan Dalam L-7 Analisis Monogliserida dengan KLT
8. Contoh Spot-spot pada analisis KLT sampel no: 1 L-8
9. Kadar MG, DG dan TG Hasil Analisis KG L-9
10. Contoh Kromatogram Analisis KG L-10
11. Kromatogram Hasil Reaksi Asam Laurat dengan Gliserol L-11 12. Tabel Analisa Disain Metodologi Survey Permukaan L-12
Universitas Sumatera Utara
BAB I
PENDAHULUAN
1.1. Latar Belakang
Perkebunan sawit Indonesia pada 2011 mencapai 8,04 juta hektar dengan produksi crude palm oil (CPO) sebanyak 22 juta ton. Dari produksi cpo tersebut, sekitar 70% diekspor sehingga menghasilkan devisa sebesar 16,4 miliar dolar AS (Ditjenbun, 2011). Nilai ekspor yang diperoleh dari komoditas sawit tersebut memang cukup besar, namun nilai itu masih dapat ditingkatkan lagi jika yang diekspor adalah turunannya.
Salah satu produk turunan minyak sawit adalah monogliserida (MG), yang berfungsi sebagai emulsifier, yaitu zat penstabil emulsi pada pembuatan sabun, deterjen dan kosmetik, serta pengolahan pangan. Industri sabun, deterjen, kosmetik dan pangan sangat membutuhkan MG untuk pengolahan produksinya, namun di Indonesia ketersediannya masih kurang memadai sehingga harus diimpor. Kondisi ini menunjukkan bahwa peluang investasi dan produksi MG di dalam negeri sangat baik.
Minyak inti sawit dapat dimanfaatkan sebagai bahan baku dalam sintesis monogliserida, karena asam lemak dari minyak inti sawit didominasi oleh asam laurat (C12:0) dan asam miristat (C14:0
Monogliserida dapat diproduksi dengan dua cara. Pertama, esterifikasi langsung dari gliserol dengan asam lemak, dimana gliserol bereaksi dengan asam lemak dalam kondisi tertentu (Pariente and Alvarez, 2003 dan Bellot et al., 2001).
Kedua interesterifikasi trigliserida dengan gliserol, dimana trigliserida bereaksi dengan gliserol dengan adanya katalis menghasilkan mono-, di- dan trigliserida.
(Dossat et al., 2002 dan Bancquart et al., 2001).
), masing-masing 48% dan 16%, sehingga pembentukan monogliserida lebih stabil (Gurr, 1992). Pemanfaatan minyak inti sawit untuk pembuatan MG ini merupakan salah satu bentuk diversifikasi dan peningkatan nilai ekonomi untuk produk-produk yang berbasis kelapa sawit.
2
Monogliserida yang dihasilkan dalam skala industri diproduksi dengan cara gliserolisis, yakni reaksi antara trigliserida dengan gliserol menghasilkan mono-, di- dan trigliserida (Campbel et al., 1996). Reaksi gliserolisis akan berjalan lambat bila tanpa katalis dan katalis yang biasa digunakan adalah katalis asam atau basa. Reaksi dengan katalis basa berjalan lebih cepat dan katalis yang biasa digunakan adalah natrium hidroksida, kalium hidroksida dan natrium metoksida. Reaksi menggunakan katalis senyawa alkali ini membutuhkan suhu yang tinggi (220-250oC) sehingga menyebabkan produk berwarna gelap dan bau tidak sedap (Noereddini and Medikonduru, 1997). Selain katalis tersebut, reaksi gliserolisis dapat dilakukan dengan katalis enzim lipase. Suhu reaksi dengan katalis ini hanya sekitar 30o
Untuk menurunkan suhu pada gliserolisis dengan katalis senyawa alkali, pelarut yang dipakai untuk meningkatkan kelarutan minyak dalam gliserol adalah alkohol misalnya tert-butanol. Tert-butanol merupakan media reaksi paling baik karena pelarut ini tidak diesterifikasi oleh asam lemak, non toksik, relatif tidak berwarna dan mempunyai titik didih rendah sehingga mudah dihilangkan dari campuran reaksi (Choo et al, 2006).
C, namun katalis enzim lipase harganya mahal dan waktu reaksinya lama (Kaewthong and Kittikun, 2005).
Dengan pertimbangan tersebut, pengembangan dan penelitian lebih lanjut untuk produksi monogliserida perlu dilakukan. Penerapan teknik gliserolisis Refined Bleached Deodorized Palm Kernel Oil (RBDPKO) menggunakan katalis natrium hidroksida (NaOH) dan pelarut ter-butanol ini diharapkan dapat menghasilkan MG dengan kualitas yang lebih baik.
Universitas Sumatera Utara
3
1.2. Perumusan Masalah
Bagaimana perbandingan mol RBDPKO dan gliserol, konsentrasi katalis dan suhu operasi dapat mempengaruhi reaksi gliserolisis minyak inti sawit menggunakan katalis NaOH dalam pelarut ter-butanol.
1.3. Tujuan Penelitian
Mengetahui kondisi optimum reaksi sintesis monogliserida melalui gliserolisis RBDPKO menggunakan katalis NaOH dan pelarut ter-butanol seperti:
rasio RBDPKO/gliserol, konsentrasi katalis serta suhu reaksi.
1.4. Ruang Lingkup Penelitian
1. Gliserolisis dilakukan dengan metode batch dimana kondisinya seperti pada rancangan percobaan.
2. Analisis MG dilakukan dengan kromatografi lapis tipis (KLT) dan kromatografi gas (KG).
1.5. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan tambahan informasi terhadap pengembangan industri olekimia sebagai bahan dasar pembuatan emulsifier turunan minyak sawit melalui reaksi gliserolisis. Selain itu diharapkan dapat memperkaya jenis emulsier yang sangat bermanfaat bagi industri sabun, deterjen, kosmetik dan pangaan.
4
BAB II
TINJAUAN PUSTAKA
2.1.Minyak Inti Sawit
Minyak inti sawit adalah minyak nabati yang berasal dari inti kelapa sawit Elaeis guineensis dan dapat dimakan. Inti sawit mengandung minyak sekitar 50%
yang disusun oleh asam lemak jenuh terutama asam laurat. Ia bersifat padat pada suhu ruang di daerah beriklim sedang, dan hampir tak berwarna yang bervariasi dari putih menjadi agak kuning (Ekwenye and Ijeomah, 2005).
Minyak inti sawit mempunyai komposisi asam lemak yang berbeda dengan minyak sawit (Tabel 2.1), walaupun keduanya berasal dari buah kelapa sawit. Minyak sawit berasal dari mesokarp sementara minyak inti sawit berasal dari inti atau biji buah kelapa sawit (Gambar 2.1).
Gambar 2.1. Buah kelapa sawit
Asam lemak dari minyak inti sawit didominasi oleh asam laurat (C12:0) dan asam miristat (C14:0), masing-masing 46-52% dan 14-17%, sehingga minyak inti sawit dapat dimanfaatkan sebagai bahan baku dalam sintesis MG seperti monolaurat
Universitas Sumatera Utara
5
dan monomiristat. Pembentukan MG dengan bahan baku minyak inti sawit ini akan lebih stabil karena kandungan asam lemak jenuh tersebut (Gurr, 1992) .
Tabel 2.1. Komposisi asam lemak minyak inti dan kelapa sawit
Asam Lemak Minyak inti
sawit (%)
Minyak kelapa sawit (%)
Asam Laurat C12:0 46-52
Asam MiristatC14:0 14-17 1,1-2,5
Asam Palmitat C16:0 6,5-9 40-46
Asam Kaproat C10:0 3-7
Asam Kaprilat C8:0 3-4
Asam Stearat jenuh C18:0 1-2,5 3,6-4,7
Asam Oleat C18:1 13-19 39-45
Asam Linoleat C18:2 0,5-2 7-11
Sumber: Ketaren (2008)
Refined Bleached Deodorized Palm Kernel Oil (RBDPKO) merupakan produk minyak inti sawit yang dibuat menggunakan proses penyulingan untuk menghilangkan asam lemak bebas serta penjernihan untuk menghilangkan warna dan penghilangan bau. Secara garis besar proses pengolahan minyak inti sawit kasar (CPKO) menjadi minyak RBDPKO, terdiri dari dua tahap yaitu tahap pemurnian (refinery) dan pemisahan (fractionation). Tahap pemurnian terdiri dari penghilangan gum (degumming),pemucatan (bleaching) dan penghilangan bau (deodorization).
Tahap pemisahan terdiri dari proses pengkristalan (crystalization) dan pemisahan fraksiCPKO (Zin, 2006). Hasil dari proses pemisahan itu disebut DPO (Degummed Palm Oil). DPO yang dihasilkan dari proses degumming akan disaring. Hasil dari penyaringan tersebut adalah DBPO (Degummed Bleached Palm Oil) yang selanjutnya akan diproses untuk tahap deodorizing.
Ada dua jenis teknik pemurnian yang dapat dilakukan untuk minyak sawit: (i)
6
(i). Pemurnian Kimia (basa)
Pemurniaan kimia disebut juga pemurnian basa merupakan teknik konvensional yang digunakan untuk memurnikan minyak sawit mentah. Biasanya melibatkan 3 tahap proses pemurnian (Djikstra, 2004) yakni :
• Penghilangan getah dan penetralan
Dalam tahap proses ini, bagian fosfatida dari minyak dihilangkan dengan menambahkan reagen di bawah kondisi tertentu. Reagen yang ditambahkan biasanya adalah asam fosfat atau sitrat. Caranya dengan menambahkan sejumlah reagen tertentu ke dalam minyak untuk waktu dan parameter tertentu, sehingga fosfotida terpisah dari minyak, kemudian bagian fosfatidanya dihilangkan dengan pengendapan. Setelah itu minyak dinetralisasi dengan basa untuk menghilangkan asam lemak bebas sehingga terbentuk sabun. Kemudian sabun dihilangkan dari minyak dengan metode pemisahan berdasarkan gaya berat. Untuk memisahkan sisa alkali minyak dicuci dengan air panas. Reaksi kimia yang terlibat dalam proses ini adalah sebagai berikut:
R-COOH + NaOH R-COONa + H2
Gambar 2.2. Reaksi penyabunan (Zin, 2006) O
• Pemucatan dan Penyaringan
Pada tahap pemucatan ini, minyak dimasukkan ke dalam labu silinder dengan agitator yang disebut Bleacher, kemudian dipanaskan di atas 90oC dengan uap dan dibiarkan dalam kondisi vakum. Selanjutnya kelembaban dari minyak diuapkan sehingga minyak menjadi kering. Minyak yang telah kering kemudian ditambahkan reagen pemutih dan karbon. Reagen ini akan menyerap sebagian besar warna sisa minyak setelah netralisasi. Campuran minyak dan reagen pemutih selanjutnya disaring, sehingga menghasilkan minyak yang jernih. Kemudian minyak didehidrasi pada kondisi vakum untuk menghindari kerusakan yang disebabkan oksigen.
Universitas Sumatera Utara
7
• Penghilangan bau
Setelah pemutihan minyak menjadi jernih, namun masih mempunyai bau yang kurang enak baik karena bau aslinya ataupun bau karena bahan-bahan kimia yang ditambahkan selama netralisasi. Minyak kemudian dimasukkan ke dalam tangki Deodoriser dan dibiarkan pada kondisi vakum tinggi dan dipanaskan pada suhu 200o
(ii). Pemurnian fisika
C, dengan uap tekanan tinggi dan uap terbuka dilewatkan melalui minyak.
Bahan-bahan yang mudah menguap diuapkan dengan uap langsung. Kemudian minyak didinginkan dan dijernihkan melalui penyaring tekan untuk mendapatkan minyak yang berkilau. Tujuan deodorisasi ini adalah untuk membuat minyak bercampur dan rasanya hambar, maka bilangan peroksida yang dihasilkan dari proses ini harus seminimal mungkin.
Pada pemurnian fisika asam lemak bebas dihilangkan dengan distilasi pada suhu yang lebih tinggi dan tekanan rendah yang menggantikan penggunaan basa seperti dalam penyulingan kimia. Penyulingan fisika dikenal juga sebagai penghilangan asam (penghilangan bau) dengan destilasi uap dimana asam lemak bebas (ALB) dan komponen yang mudah menguap lain didestilasi dari minyak menggunakan reagen pengupas. Sebelum dilakukan penyulingan fisika dilakukan terlebih dahulu tahapan pendahuluan yakni: proses penghilangan getah, pemutihan dan penghilangan bau.
2.2. Monogliserida
2.2.1. Kegunaan monogliserida
Monogliserida (MG) adalah monoester asam lemak dari gliserol (Gambar 2.3). Monogliserida merupakan lemak yang terdiri dari suatu kepala lipofilik dan ekor hidrofilik, yang memberikan sifat detergen. Sifat inilah yang dapat mengurangi tegangan antar muka dari sistem minyak-air, sehingga monogliserida dapat digunakan sebagai zat pengemulsi dan penstabil dalam industri makanan (Birkhahn et al. 1997).
Selain sebagai pengemulsi dalam makanan, monogliserida juga digunakan dalam
8
industri farmasi dan kosmetik, karena sifat fisikokimianya, khususnya keseimbangan hidrofilik/lipofilik (HLB) (Jungermann, 1991).
Gambar 2.3. Struktur Monogliserida (Jungermann, 1991)
2.2.2. Sintesis Monogliserida
Pada skala industri, ada dua proses utama untuk produksi monogliserida.
Pertama dengan gliserolisis seperti transesterifikasi trigliserida (lemak atau minyak) dengan gliserol pada suhu tinggi (493-523)oK menggunakan katalis basa kuat (Gambar 2.4). Katalis basa yang biasa digunakan adalah KOH dan Ca(OH)
2
(Sonntag, 1992). Reaksi dengan menggunakan katalis ini memerlukan penetralan, biasanya dengan asam fosfat dan garam yang terbentuk perlu untuk dihilangkan.
Gambar 2.4. Reaksi untuk memproduksi monogliserida secara industri kimia: (I) Transesterifikasi: gliserolisis dari trigliserida dengan gliserol; (II) Esterifikasi langsung: gliserolisis dari asam lemak dengan gliserol (Bossaert et al, 1999).
Universitas Sumatera Utara
9
Cara yang kedua adalah esterifikasi gliserol dengan asam lemak pada suhu tinggi di atas 523o
Gugus hidroksil dalam gliserol reaktivitasnya tidak berbeda. Esterifikasi langsung atau transesterifikasi dari gliserol memberikan suatu campuran mono-, di- dan tri-gliserida, dan gliserol tidak larut, yang biasanya mengandung 40- 60% monogliserida dan digliserida 35-45%. Oleh karena itu, penting untuk meningkatkan selektivitas monogliserida serta meningkatkan konversi bahan baku dengan mengoptimalkan kondisi-kondisi reaksi dan merancang katalis padat yang sesuai (Meher et al., 2006).
K. Agar suhu reaksi lebih rendah dibutuhkan katalis asam seperti asam sulfat, asam fosfat dan asam sulfonat organik. Karena suhu yang digunakan dalam proses tinggi maka monogliserida yang dihasilkan mengalami kerusakan warna dan rasa (Heykants et al, 1997). Oleh karena itu distilasi diperlukan untuk memurnikan produk.
Choo et al., (2006) telah melaporkan sintesis monogliserida dengan gliserolisis minyak stearin yang telah dihidrogenasi menggunakan katalis NaOH dan pelarut ter-butanol. Percobaan yang dilakukan pada perbandingan berat minyak stearin/gliserol 1:1, suhu 90oC, waktu 1 jam, konsentrasi katalis 1% dan perbandingan berat minyak/pelarut 1:2 menghasilkan monogliserida 84% sebelum pemurnian.
2.3. Transesterifikasi
Transesterifikasi melalui alkoholisis adalah perubahan oleh alkohol menjadi ester. Jika dalam transesterifikasi digunakan metanol disebut sebagai metanolisis dan jika yang digunakan gliserol maka disebut gliserolisis, seperti dalam Gambar 2.5 dan 2.6.
10
Gambar 2.5. Metanolisis dari trigliserida (Meher et al., 2006)
Gambar 2.6. Gliserolisis dari trigliserida (Muniyappa et al.,1996)
Proses transesterifikasi dipengaruhi oleh beberapa faktor antara lain: kadar asam lemak, jenis dan konsentrasi katalis, rasio minyak/gliserol dan suhu reaksi.
2.3.1. Pengaruh Asam Lemak Bebas Dan Kadar Air
Kandungan asam lemak bebas (ALB) dan kadar air merupakan parameter kunci dalam menentukan kelangsungan transesterifikasi minyak nabati. Agar reaksi dengan menggunakan katalis basa dapat sempurna, kandungan asam lemak bebas harus kurang dari 1 % (Berrios et al., 2010). Kandungan asam lemak yang lebih tinggi akan menurunkan efisiensi konversi dan menyebabkan pembentukan sabun.
Ma et al (1999) mempelajari transeterifikasi asam lemak daging sapi dengan katalis NaOH tanpa penambahan ALB dan air, menghasilkan ester lemak sapi paling tinggi. Ketika 0,6% ALB ditambahkan menghasilkan ester paling rendah yakni kurang 5 % dengan kandungan air yang bertambah. Produk yang dihasilkan berbentuk padat pada suhu kamar sama dengan asam lemak daging sapi asli. Jika 0,9% air ditambahkan tanpa penambahan ALB menghasilkan 17 % ester lemak sapi.
Universitas Sumatera Utara
11
Bahan awal yang digunakan untuk alkoholisis dengan katalis basa harus memenuhi spesifikasi tertentu. Trigliserida harus memiliki kadar asam yang rendah dan semua bahan harus anhidrat. Penambahan katalis NaOH berlebih mengkompensasi keasaman yang lebih tinggi, tetapi sabun yang dihasilkan menyebabkan peningkatan viskositas atau pembentukan gel yang mengganggu reaksi dan pemisahan gliserol. Bila kondisi reaksi tidak sesuai dengan persyaratan tersebut, ester yang dihasilkan berkurang. Metoksida dan hidroksida dari natrium harus dijaga dalam keadaan anhidrat. Kontak berkepanjangan dengan udara akan mengurangi efektivitas katalis ini melalui interaksi dengan air dan karbon dioksida.
Tahapan reaksinya seperti pada Gambar 2.7.
Tahap pendahuluan:
OH- + ROH RO- + H2O
Tahap pertama:
Tahap kedua:
Tahap ketiga:
12
Dimana:
R’ = Rantai karbon dari asam lemak R = Gugus alkil dari alkohol
Gambar 2.7. Mekanisme transesterifikasi dengan katalis basa (Meher et al., 2006)
2.3.2. Jenis Dan Konsentrasi Katalis
Katalis yang digunakan untuk reaksi transesterifikasi trigliserida (TG) diklasifikasikan sebagai katalis basa, asam, enzim dan heterogen. Diantara keempat katalis itu katalis basa seperti natrium hidroksida, natrium metoksida, kalium hidroksida, kalium metoksida lebih efektif. Bila TG yang digunakan mempunyai kandungan asam lemak dan air yang tinggi lebih baik digunakan katalis asam. Katalis asamnya dapat asam sulfat, asam fosfat, asam klorida atau asam sulfonat organik.
Metanolisis dari lemak daging sapi yang telah dilakukan menggunakan katalis natrium hidroksida (NaOH) dan natrium metoksida (NaOMe) ditemukan bahwa NaOH lebih baik daripada NaOMe, dimana NaOH mempunyai aktivitas maksimum 0,3% (persen berat minyak), sementara NaOMe 0,5%. Disamping itu NaOMe dapat membentuk beberapa hasil samping terutama garam-garam natrium (Meher et al., 2006).
Dalam proses metanolisis dengan katalis basa yang sering digunakan NaOH atau KOH, dengan konsentrasi dari 0,4 - 2% (persen berat minyak). Proses ini, baik untuk minyak yang sudah difraksinasi maupun yang masih mentah, menghasilkan konversi yang baik dengan katalis NaOH atau KOH 1%. Metanolisis dari minyak kedele dengan katalis KOH 1% telah memberikan nilai dan viskositas ester terbaik.
Universitas Sumatera Utara
13
2.3.3. Rasio Molar Alkohol Terhadap Minyak Dan Jenis Alkohol
Secara teori, rasio molar gliserol terhadap trigliserida membutuhkan 2 mol gliserol untuk 1 mol trigliserida untuk menghasilkan 3 mol monogliserida (Muniyappa et al., 1996). Kelebihan gliserol digunakan untuk memastikan bahwa trigliserida telah berubah menjadi monogliserida dengan sempurna. Rasio gliserol/trigliserida yang lebih tinggi dapat menghasilkan monogliserida lebih besar dalam waktu yang singkat. Hasil monogliserida meningkat bila rasio gliserol/trigliserida dinaikkan melebihi 3 dan mencapai maksimum. Meningkatnya gliserol lebih lanjut akan melebihi rasio optimal tidak akan meningkatkan hasil tetapi akan meningkatkan biaya perolehan kembali.
2.3.3. Suhu Reaksi
Suhu mempengaruhi reaksi dan hasil pada sintesa monogliserida. Suhu reaksi yang lebih tinggi dapat menurunkan viskositas minyak dan mengakibatkan peningkatan laju reaksi, sehingga mempersingkat waktu reaksi. Namun bila suhu reaksi meningkat melebihi tingkat optimal, hasil monogliserida yang terbentuk menurun karena suhu reaksi yang lebih tinggi mempercepat reaksi saponifikasi dari trigliserida. Suhu reaksi harus lebih kecil dari titik didih gliserol untuk memastikan bahwa gliserol tidak akan keluar melalui penguapan. Tergantung dari minyak yang digunakan, suhu optimal berkisar antara 280o – 290oC (Meher et al., 2006).
2.4. Ter-Butanol
Ter-Butanol atau 2-metil-2-propanol (Gambar 2.8), adalah alkohol tersier sederhana yang merupakan salah satu dari keempat isomer butanol. tert-Butanol merupakan cairan bening dengan bau seperti kapur barus, sangat mudah larut dalam air dan larut dalam etanol dan dietil eter. Keunikan dari isomer butanol ini adalah kecenderungannya untuk menjadi padat pada suhu kamar, dengan titik leleh sedikit di atas 25° C (Wikipedia.org, 13 Peb 2012).
14
Secara komersial tert-butanol dibuat dari isobutana sebagai hasil samping dari sintesis. ter-Butanol dapat juga dibuat dari hidrasi katalitik iso butilena. Penggunaan tert-butanol adalah sebagai pelarut, denaturan untuk etanol, sebagai bahan dalam penghilang cat, pendorong oktan untuk bensin, intermediate dalam sintesis komoditi bahan kimia lain seperti metil ter-butil eter, aroma dan parfum.
Gambar 2.8. Struktur ter-Butanol (Johnson et al., 1950)
Sebagai alkohol tersier, ter-butanol lebih stabil terhadap oksidasi dan kurang reaktif dibandingkan dengan isomer butanol lainnya. tert-Butanol merupakan pelarut yang sangat baik untuk reaksi esterifikasi, karena tidak ikut dalam reaksi. ter-Butanol juga tidak beracun, tidak berbau dan mempunyai titik didih rendah, sehingga membuatnya mudah untuk dihilangkan dalam campuran reaksi. ter-Butanol yang sudah didehidrasi pada kondisi asam sangat baik digunakan dalam reaksi gliserolisis yang menggunakan katalis basa (Dudley, 1957).
2.5. Gliserol
Gliserol adalah senyawa poliol sederhana berupa cairan kental yang tidak berbau dan tidak berwarna. Gliserol mempunyai rasa manis dan sifat racun rendah dan digunakan dalam industri farmasi. Gliserol mempunyai tiga gugus hidroksil yang berperan dalam kelarutan dalam air dan sifat higroskopiknya. (Wikipedia.org, 13 Peb 2012).
Gliserol menjadi back bone trigliserida yang terutama dihasilkan oleh saponifikasi lemak sebagai produk samping dari pembuatan sabun. Reaksi saponifikasi ditunjukkan pada Gambar 2.9.
Universitas Sumatera Utara
15
Gambar 2.9. Reaksi saponifikasi lemak (Schumann and Siekman, 2005)
Gliserol juga merupakan produk sampingan dari produksi biodiesel melalui transesterifikasi, membentuk gliserol mentah yang berwarna gelap dan kental seperti sirup. Reaksi pembentukan gliserol melalui transesterifikasi seperti pada Gambar 2.10. Gliserol mentah dapat direaksikan dengan trigliserida dengan bantuan katalis basa NaOH sehingga membentuk monogliserida seperti ditunjukkan pada Gambar 2.4 (I).
Gambar 2.10. Reaksi transesterifikasi trigliserida: 1). Trigliserida 2). Alkohol 3) Ester 4).Gliserol (Riemenschneider and Bolt, 2005)
2.6. Kromatografi
Kromatografi adalah suatu metode pemisahan berdasarkan perbedaan perpindahan komponen-komponen senyawa diantara dua fase yaitu fase diam dan fase gerak. Fase diam dapat berupa cair atau padat, sementara fase gerak dapat berupa gas atau cair (Stahl, 1958). Jika fase diam berupa padat maka cara tersebut dikenal
16
sebagai kromatografi serapan, jika zat cair dikenal sebagai kromatografi partisi.
Berdasarkan fase geraknya kromatografi dibagi menjadi empat sistem :
• Fase bergerak cair – fase diam padat, seperti kromatografi lapis tipis dan kromatografi penukar ion
2. Fase bergerak gas – fase diam padat, seperti kromatografi gas padat
3. Fase bergerak cair – fase diam cair, seperti kromatografi cair kinerja tinggi
4.Fase bergerak gas – fase tetap cair, seperti kromatografi gas cair dan kromatografi kolom kapiler.
2.6.1. Kromatografi Lapis Tipis
Kromatografi lapis tipis (KLT) termasuk kromatografi serapan dimana sebagai fase diam berupa zat padat yang disebut adsorben (penyerap) dan fase gerak adalah zat cair yang disebut larutan pengembang. Sejumlah kecil ekstrak lipid atau minyak «200 mg dapat dipisahkan oleh KLT silika gel dengan menggunakan pengembang yang sesuai. Visualisasi dari bercak KLT biasanya dilakukan dengan lampu UV pada plat silika gel yang diresapi dengan indikator flouresens atau dengan menyemprotkan plat dengan 50% asam sulfat dalam etanol (atau 80 % kalium dikromat dalam asam sulfat) (Abidi, 2001).
Pemisahan lipid dari ekstraknya dengan KLT dilakukan dengan menggunakan plat silica gel H. Pertama plat KLT diberi garis untuk sampel dan standard, garis diberi jarak beberapa inci dari dasar plat untuk memastikan sampel tidak terbenam dalam larutan pengembang, untuk itu digunakan silet, dibuat goresan vertikal antara garis jalur. Plat diaktifkan dengan memasukkannya dalam oven 100oC selama satu jam. Larutan pengembang adalah campuran heksan:dietil eter:asam asetat (80:20:2).
Setelah KLT selesai dijalankan, bercak disemprot dengan flouresens dan divisualisasi di bawah lampu UV dan difoto. Bercak yang nampak kemudian dilingkari dengan pensil, Lipid netral akan terpisah seperti Gambar 2.11 (Christie, 2003).
Universitas Sumatera Utara
17
Gambar 2.11. Hasil KLT ekstrak lipid (Christie, 2003).
2.6.2. Kromatografi Gas
Analisis kromatografi gas (KG) telah dikembangkan untuk menentukan komponen-komponen campuran yang mengandung turunan ester asam lemak bebas, gliserol, mono-, di-, dan trigliserida dari reaksi transesterifikasi minyak sayur.
Analisis KG telah dilakukan menggunakan kolom kapiler yang DB-5HT suhu tinggi dan menggunakan 1,2,3-trikaproilgliserol (trikaprin) sebagai standar internal.
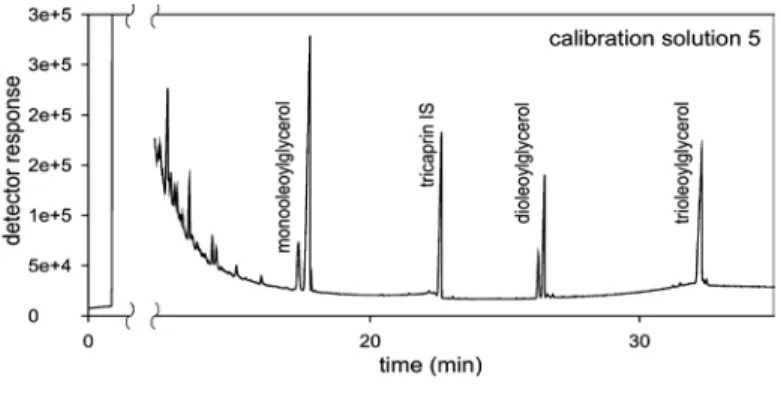
Sebelum analisa, komponen telah mengalami derivatisasi oleh N-metil-N-trimetil silil trifluoro asetamida (MSTFA). Sebagai gas pembawa adalah gas helium bertekanan 50 kPa. Program suhu yaitu 50o C dan ditahan 1 menit, diprogram pada 15◦C / menit sampai 180o C, diprogram di 7◦C / menit sampai 230◦ C, diprogram pada 10◦ C / menit hingga 390◦C, suhu final ditahan selama 5 menit. Injektor dan detektor suhu adalah 380◦C. Jumlah sampel disuntikkan pada kolom adalah 2 uL (Wawrzyniak et al., 2005). Senyawa yang dianalisa diidentifikasi berdasarkan waktu retensi relatif dari standar internal (Gambar 2.12).
18
Gambar 2.12. Kromatogram standar internal kromatografi gas (Wawrzyniak et al., 2005)
Pita kromatografik yang diperuntukkan asam lemak cukup intens dan karakteristik dan dapat diamati dalam kromatogram minyak diesel yang dicampur dengan asam lemak metil ester untuk tingkat yang berbeda. Gambar 2.13 menyajikan sebuah kromatogram asam lemak metil ester yang diperoleh dari transesterifikasi minyak nabati.
Gambar 2.13. Kromatogram asam lemak metil ester hasil transesterifikasi minyak nabati (Wawrzyniak et al, 2005)
Universitas Sumatera Utara
BAB III METODOLOGI
3.1. Tempat dan Waktu Penelitian
Penelitian ini adalah eksperimen laboratorium dilakukan di Laboratorium Pangan dan Mutu Pusat Penelitian Kelapa Sawit (PPKS), Jl. Brigjen Katamso No. 51 Medan-Sumatera Utara. Waktu penelitian adalah 11 bulan yang terdiri dari studi pustaka, penyusunan proposal, penelitian pendahuluan, penelitian utama dan penyusunan thesis.
3.2. Alat dan Bahan
3.2.1. Bahan yang Digunakan
Refined Bleached Deodorized PalmkernelOil (RBDPKO) dari pabrik Refined minyak sawit lokal di Medan sebagai bahan baku utama yang sebelumnya dianalisa kadar asam lemak bebasnya. Gliserol, natrium hidroksida, ter-butanol (sebagai bahan untuk gliserolisis), n-Hexan, dietil eter, petroleum eter, asam asetat glasial, kloroform, silika gel 60 G (sebagai bahan untuk KLT), N,N bis (trimetilsilil) trifluoro asetamida (BSTFA), piridin, trimetilklorsilan (TMCS), n-heptan, trikaprin (sebagai bahan untuk kromatografi gas) bahan-bahan tersebut semuanya pro analis dan gas nitrogen sebagai gas pembawa pada kromatografi gas.
3.2.2. Peralatan
Alat-alat yang digunakan pada penelitian ini adalah : termometer, reaktor gliserolisis, plat KLT dan gelas Chamber, lampu UV, kromatografi gas (Shimadzu) dengan detektor ionisasi nyala, neraca analitis, oven (Gambar 3.1), statip serta peralatan gelas seperti: corong pisah, gelas Erlenmeyer, gelas ukur, gelas Beaker, corong gelas, pipet ukur, pipet tetes, gelas arloji.
20
(1) (2) (3)
(4) (5) (6)
Gambar 3.1. Peralatan penelitian :(1) Reaktor gliserolisis (2) Plat KLT dan gelas Chamber (3) Lampu UV (4) Unit kromatografi gas (5) Timbangan analitis (6) Oven
Universitas Sumatera Utara
21
3.3. Metode Penelitian
3.3.1. Karakterisasi Bahan Baku
Karakterisasi RBDPKO dilakukan untuk mengetahui keadaan awal bahan baku meliputi: komposisi asam lemak bebas menggunakan kromatografi gas serta kadar air dan kandungan asam lemak bebas (ALB), dengan prosedur sebagai berikut:
1. Asam lemak bebas (ALB) (AOCS, 1995):
Sampel dipanaskan sampai mencair namun pemanasan tidak boleh melebihi 10o
N
C di atas titik leleh. Kemudian sampel ditimbang ± 5 gram dalam gelas Erlenmeyer dan ditambahkan 50 ml alkohol netral (95%) serta indikator fenoftalein.
Setelah itu sampel tadi dipanaskan dan dititrasi dengan KOH 0,1 N sampai larutan berwarna merah rose. Volume KOH yang dipakai kemudian dicatat dan dihitung dengan menggunakan rumus:
KOH x 200 x V titran
% ALB = Berat sampel x 1000 x 100 %
• Kadar air (AOCS, 1995) :
Sampel diaduk kemudian ditimbang sebanyak ± 5 gram dalam cawan.
Kemudian sampel yang telah ditimbang tadi dimasukkan ke dalam oven dan dikeringkan pada suhu 105oC ± 1o
Bobot yang hilang (g)
C selama 30 menit. Setelah itu sampel diangkat dari oven dan didinginkan dalam desikator sampai suhu kamar dan ditimbang.
Pekerjaan tersebut diulang lagi sampai kehilangan bobot selama pemanasan sampel tidak lebih dari 0,05%. Kadar air dihitung dengan menggunakan rumus:
Kadar air (%) = X 100 % Bobot sampel (g)
Dimana bobot yang hilang adalah : bobot sampel sebelum pemanasan - bobot sampel setelah pemanasan
22
3.3.2. Penentuan Titik Tengah
Penentuan titik tengah dilakukan untuk mencari titik tengah (titik nol) pada rancangan percobaan menggunakan metode permukaan respon yaitu dengan menentukan kondisi yang menghasilkan kadar monogliserida paling banyak. Kondisi percobaan meliputi variabel bebas yakni: rasio molar gliserol/RBDPKO, konsentrasi katalis dan suhu, sedangkan variabel tetapnya adalah total campuran reaksi 200 gram, kecepatan pengadukan 700 rpm, waktu pengadukan 1 jam dan jumlah pelarut 20 ml/10 gram RBDPKO, prosedurnya sebagai berikut :
• Menentukan titik tengah perbandingan molar RBDPKO/gliserol dilakukan dengan menguji empat nilai perbandingan molar RBDPKO/gliserol yaitu 1:8, 1:10, 1:15 dan 1:20. Pada percobaan ini suhu yang digunakan 90o
• Menentukan titik tengah konsentrasi katalis dilakukan dengan menguji empat nilai konsentrasi katalis yakni (0,5; 1; 1,5dan 2)% b/b. Suhu 90
C, konsentrasi katalis 1% dan waktu 1 jam.
o
• Menentukan titik tengah suhu dilakukan dengan menguji empat nilai suhu yakni 80
C dan waktu 1 jam, sementara perbandingan molar RBDPKO/gliserol yang digunakan adalah perbandingan yang menghasilkan nilai tertinggi yang dihasilkan dari percobaan pertama.
o, 85o, 90o, 95o C. Kondisi prosesnya adalah waktu 1 jam dan perbandingan molar RBDPKO/gliserol dan katalis yang digunakan sesuai dengan nilai tertinggi dari percobaan sebelumnya.
3.3.3. Penetapan Kondisi Optimum
Rancangan percobaan yang digunakan pada tahap ini mengikuti rancangan Central Composite Design (CCD) dengan metode permukaan respon yang terdiri dari tiga variabel yaitu perbandingan mol RBDPKO/gliserol, konsentrasi katalis waktu dan suhu reaksi gliserolisis. Interval variabel berupa perlakuan dan kode perlakuan dapat dilihat pada Tabel 3.1.
Universitas Sumatera Utara
23
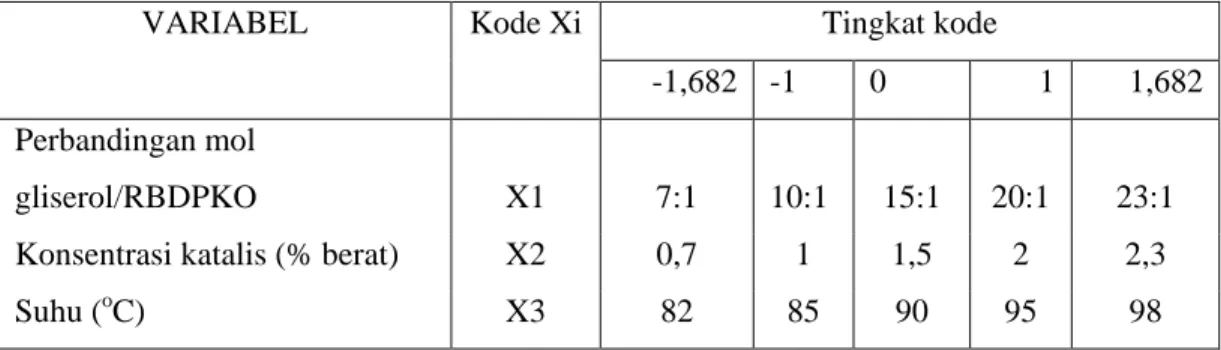
Tabel 3.1. Tingkat kode untuk variabel bebas yang digunakan dalam percobaan gliserolisis RBDPKO dengan gliserol
VARIABEL Kode Xi Tingkat kode
-1,682 -1 0 1 1,682
Perbandingan mol
gliserol/RBDPKO X1 7:1 10:1 15:1 20:1 23:1
Konsentrasi katalis (% berat) X2 0,7 1 1,5 2 2,3
Suhu (oC) X3 82 85 90 95 98
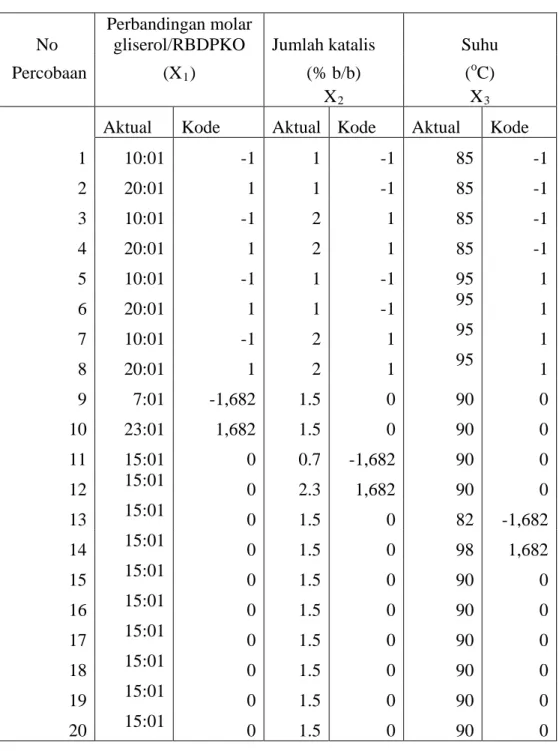
Dua puluh set percobaan terdiri dari 8 run pertama (1-8) dengan tingkat kode (±1) untuk masing-masing faktor (factorial point). Kemudian 6 run yang disebut star point dengan tingkat terkode (±α) sebagai significant curvature effect (run 9-14), terakhir 6 run tambahan (run 15-20) merupakan titik tengah (yang diambil dari uji pendahuluan) sebagai perkiraan daerah lekukan kurva dengan kode 0 untuk masing- masing faktor. Jarak titik bintang dan titik tengah adalah α = 2 n/4, dimana untuk 3 faktor α = 1,682. Matriks CCD pada percobaan ini disusun dalam Tabel 3.2, untuk menentukan matriks CCD digunakan rumus :
α = Xi – (level tinggi + level rendah)/2 (level tinggi - level reandah)/2
Pers (3.1)
24
Tabel 3.2. Matriks CCD 3 variabel gliserolisis RBDPKO dengan katalis NaOH
No
Perbandingan molar
gliserol/RBDPKO Jumlah katalis Suhu
Percobaan (X1) (% b/b) (oC)
X2 X3
Aktual Kode Aktual Kode Aktual Kode
1 10:01 -1 1 -1 85 -1
2 20:01 1 1 -1 85 -1
3 10:01 -1 2 1 85 -1
4 20:01 1 2 1 85 -1
5 10:01 -1 1 -1 95 1
6 20:01 1 1 -1 95
1
7 10:01 -1 2 1 95
1
8 20:01 1 2 1 95
1
9 7:01 -1,682 1.5 0 90 0
10 23:01 1,682 1.5 0 90 0
11 15:01 0 0.7 -1,682 90 0
12 15:01
0 2.3 1,682 90 0
13 15:01
0 1.5 0 82 -1,682
14 15:01
0 1.5 0 98 1,682
15 15:01
0 1.5 0 90 0
16 15:01
0 1.5 0 90 0
17 15:01
0 1.5 0 90 0
18 15:01
0 1.5 0 90 0
19 15:01
0 1.5 0 90 0
20 15:01
0 1.5 0 90 0
Universitas Sumatera Utara
25
3.3.4. Prosedur 3.3.4.1. Gliserolisis
Gliserolisis dilakukan dengan melarutkan NaOH 1% berat (berdasarkan berat minyak) dengan gliserol, kemudian campuran direflux pada 100oC sambil diaduk menggunakan pengaduk magnetik. Setelah suhu tercapai ditambahkan RBDPKO (perbandingan RBDPKO/gliserol = 1:10 mol/mol) dan ter-butanol (1:2 wRBDPKO/vter-
butanol
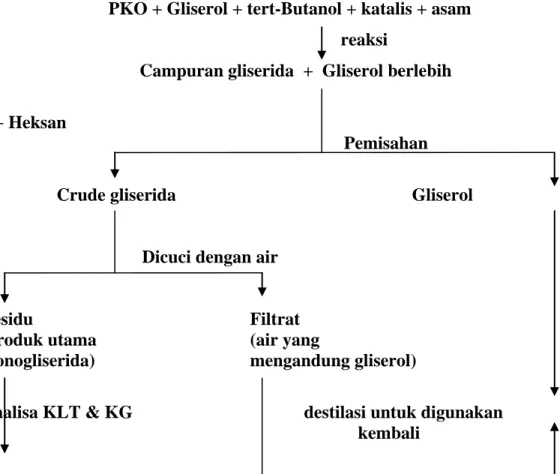
PKO + Gliserol + tert-Butanol + katalis + asam
) dan reaksi dilakukan sesuai suhu yang diinginkan selama 1 jam. Reaksi dihentikan dengan penambahan sedikit asam asetat. Lapisan atas yang mengandung campuran gliserida dipisahkan dan dicuci dengan aquades sebanyak tiga kali untuk menghilangkan gliserol dan asam asetat. Diagram alir gliserolisis ini seperti pada Gambar 3.2.
reaksi
Campuran gliserida + Gliserol berlebih
+ Heksan
Pemisahan
Crude gliserida Gliserol
Dicuci dengan air
Residu Filtrat
(produk utama (air yang
monogliserida) mengandung gliserol)
Analisa KLT & KG destilasi untuk digunakan
kembali
MG, DG, TG
Gambar 3.2. Diagram alir gliserolisis pada sintesa monogliserida
26
3.3.4.2. Prosedur Analisis Gliserida denganKromatografi Lapis Tipis (KLT) (Anggirasti, 2008)
Sebanyak ± 0,05 g hasil gliserolisis dilarutkan dalam 1 ml kloroform, kemudian 1 μl larutan diaplikasikan pada plat KLTdalam bentuk spot bulat (ditotol) dengan jarak antar spot 2 cm. Plat KLTkemudian dielusi menggunakan campuran pelarut heksan : dietil eter : asam asetat glasial (80:20:2 v/v/v) yang telah dijenuhkan dalam chamber glass. Setelah elusi mencapai tanda batas atas, platdikeluarkan dari chamber kemudian didiamkan beberapa menit sampai uap dari pelarut hilang.
Identifikasi kemudian dilakukan dengan menyemprotkan larutan 2’,7’- dichlorofluorescein pada plat KLT tadi sehingga fraksi-fraksi hasil pemisahan produk dapat dilihat di bawah sinar UV dengan panjang gelombang 366 nm. Spot-spot yang terbentuk kemudian diberi tanda dengan menggunakan pensil untuk memperjelas area fraksi-fraksi yang telah terpisah.
Pengukuran kadar MG dilakukan secara semi kuantitatif dengan membandingkan luas area fraksi MG dengan total fraksi yang terbentuk dari pengelusian hasil gliserolisis tersebut. Caranya adalah dengan menggambar ulang spot yang terbentuk tadi di atas kertas kalkir, kemudian kertas-kertas ini digunting sesuai dengan spot tersebut, sehingga masing-masing guntingan ini bisa ditimbang.
Hasil timbangan menunjukkan kadar masing-masing fraksi. Perhitungan kadar masing-masing fraksi itu adalah sebagai berikut.
Kadar MG (%) = Bobot kertas fraksi MG (g) Bobot total frakksi (g)
x 100 % pers (3.2)
Kadar DG (%) = Bobot kertas fraksi DG (g) Bobot total frakksi (g)
x 100 % pers (3.3)
Kadar TG (%) = Bobot kertas fraksi TG (g) Bobot total frakksi (g)
x 100 % pers (3.4)
Universitas Sumatera Utara
27
3.3.4.3. Prosedur Analisis Gliserida Dengan Kromatografi Gas (KG) (AOCS, 1995)
Sampel (produk utama monogliserida) ditimbang 0,001-0,005 gram dan dimasukkan dalam tabung reaksi bertutup.Kemudian ditambahkan 0, 2 ml reagen N- N-bis(trimetilsilil) trifluroasetamida (BSTFA), 0,1 ml Trimetilklorsilan (TMCS) dan 0,1 ml larutan standar internal kemudian tabung ditutup dan divortex sampai homogen.Setelah itu campuran dipanaskan pada suhu 70oC selama 20 menit dan disuntikkan ke dalam kromatografi gas (KG) model Shimadzu dilengkapi dengan detektor ionisasi nyala. Kolom yang digunakan adalah kolom kapiler DB-5HT (5%- phenyl)-methyl polysiloxane (6 m x 0,32 mm). Suhu detektor dan injektor 350oC dan digunakan model split injektor dengan split injector 200:1. Suhu oven diprogram dari 160 sampai 350oC pada 30oC/min dan ditahan pada 350oC selama 25 menit. Nitrogen digunakan sebagai gas pembawa dengan kecepatan alir 200 ml/menit. Waktu proses 30 menit dan sampel diInjeksikan 1 µL secara manual.
3.4. Analisa Kadar Monogliserida 3.4.1. Analisa DenganKromatografi Gas
Identifikasi puncak-puncak gliserida dilakukan dengan membandingkannya dengan kromatogram standar (Gambar 3.3). Pada Gambar itu
ditunjukkan bahwa puncak terdapat pada waktu pemisahan 6,5 - 8 menit, puncak monogliserida (10,5 – 18 menit) diikuti dengan standar internal tricaprin (18,8 menit), setelah itu digliserida (20 – 21,5 menit) dan trigliserida (22 – 24 menit).
28
Gambar 3.3. Kromatogram standar untuk mono-, di- dan trigliserida
Karena standar hanya mengandung satu komponen dari masing-masing senyawa mono-, di- dan trigliserida, identifikasi semua komponen dilakukan juga dengan membandingkannya dengan kromatogram hasil reaksi asam laurat dengan gliserol yang menghasikan monolaurat sebagai hasil utama (Gambar 3.5), dimana reaksinya seperti ditunjukkan Gambar 3.4, berikut ini.
Gambar 3.4. Reaksi asam laurat dan gliserol
Universitas Sumatera Utara
29
Gambar 3.5. Kromatogram dari hasil reaksi asam laurat dengan gliserol
Pada Gambar 3.5. terlihat bahwa puncak monogliserida (monolaurat) terdapat pada waktu retensi 7,3 menit. Kedua kromatogram pada Gambar 3.4 dan 3.5 digunakan sebagai acuan dalam mengidentifikasi senyawa monogliserida, yakni dengan membandingkannya dengan kromatogram sampel yang dianalisa. Gambar 3.6 merupakan contoh kromatogram dari hasil gliserolisis sampel 1.
Gambar 3.6. Kromatogram hasil gliserolisis sampel 1
30
3.4.2. Analisa Kadar Monogliserida dengan Kromatografi Lapis Tipis
Sebelum dilakukan pemisahan fraksi gliserida ditentukan terlebih dahulu larutan pengelusinya, agar didapatkan pemisahan yang benar-benar baik. Larutan pengelusi yang diujikan didasarkan pada penelitian yang sudah pernah dlakukan antara lain : Campuran heksan : dietil eter : asam asetat (80:20:2) (Sihotang, 2006).
dan petroleum eter : dietil eter : asam asetat (70:30:0,2) (Anggirasti, 2008).
Campuran pengelusi yang digunakan merupakan variasi dari keduanya yakni 1. petroleum eter : dietil eter : asam asetat (70:30:0,2) 2. petroleum eter : dietil eter :
asam asetat (80:20:0,2) 3. petroleum eter : dietil eter : asam asetat (90:10:0,2) 4. heksan : dietil eter : asam asetat (80:20:2) 5. heksan : dietil eter : asam asetat
(90:10:2) 6. heksan : dietil eter : asam asetat (70:30:2). Pengukuran kadar dari fraksi gliserida dilakukan dengan membandingkan luas area fraksi masing-masing gliserida tersebut dengan total fraksi gliserida yang terbentuk dari pengelusian. Setelah spot yang terbentuk dari pengelusian tadi digambar diatas kertas kalkir, kemudian gambarnya digunting dan masing-masing guntingan ditimbang. Hasil timbangannya dihitung menggunakan persamaan 3.2-3.4.
Untuk menentukan fraksi mono-, di- dan trigliserida dibandingkan dengan larutan standar, dan karena larutan standar di laboratorium tidak tersedia maka sebagai pembanding dilakukan sintesa monolaurin dengan mereaksikan asam laurat dengan gliserol sehingga didapatkan mono-, di- dan trigliserida sebagai pembanding (Gambar 3.7).
Universitas Sumatera Utara
31
Fraksi TG
Fraksi DG
Fraksi MG
Hasil gliserolisis pembanding
Gambar 3.7. Contoh spot dari KLT hasil gliserolisis dan hasil sintesis monolaurin (pembanding)
32
BAB IV
HASIL DAN PEMBAHASAN
4.1. Karakteristik Bahan Baku
Analisa bahan baku Refined Bleached Deodorized PalmkernelOil (RBDPKO) meliputi komposisi asam lemak bebas (ALB), kadar ALB dan kadar air, seperti disajikan pada Tabel 4.1.
Tabel 4.1. Komposisi asam lemak, kadar ALB dan kadar air bahan baku RBDPKO
NO PARAMETER
% berat 1 Asam laurat (C12:0) 51,78 2 Asam miristat (C14:0) 15,54 3 Asam oleat (C18:1) 13,99 4 Asam palmitat (C16:0) 7,74 5 Asam Oktanoat (C8:0) 3,43 6 Asam Kaprat (C10:0) 3,36 7 Asam linoleat (C18:2) 2,16 8 Asam stearat (C18:0) 1,85 9 Kadar asam lemak bebas 0,18
10 Kadar air 0,041
Kadar ALB yang terdapat dalam bahan baku sangat berpengaruh dalam proses transesterifikasi yang menggunakan katalis basa. Kadar ALB yang diperbolehkan untuk reaksi tersebut adalah harus lebih rendah dari 1% (Berrios at al, 2007). Kadar asam yang lebih tinggi akan mengakibatkan reaksi transesterifikasi terganggu akibat terjadinya reaksi penyabunan antara katalis (natrium hidroksida) dengan ALB
Universitas Sumatera Utara
33
membentuk sabun dan air (Gambar 4.1). Saponifikasi menghalangi pemisahan ester dari gliserol dan mengurangi hasil dan tingkat pembentukan monogliserida.
Gambar 4.1. Reaksi penyabunan antara katalis dengan asam lemak bebas
Dari persamaan reaksi di atas dapat dinyatakan bahwa dari 1 mol ALB dan 1 mol NaOH yang direaksikan menghasilkan 1 mol sabun dan 1 mol air. Jika digunakan 1% ALB atau sama dengan 1 mg ALB dalam 10 g trigliserida (TG) atau sama dengan 0,05 mol, perhitungannya sebagai berikut :
Mol ALB = g ALB/BM ALB (BM ALB dianggap BM asam laurat karena kadar asam laurat paling banyak terkandung dalam RBDPKO yakni 46-52 %).
Mol ALB = 10-3 g/200 g mol-1
Jika NaOH yang digunakan sama maka akan terbentuk 0,05 mol sabun atau sama dengan 0,05 mol x 222 g mol
= 0,05 mol
-1
Sabun yang dihasilkan = 18 x 10
= 11,1 gram. ALB bahan baku yang digunakan 0,18%
berarti akan menghasikan 0,20 gram sabun yakni :
-5 g/200 g mol-1
Kadar air yang diperbolehkan harus kurang atau sama dengan 0,3 % (Freedman et.al, 1984). Karena air yang terkandung dalam sampel akan menghambat reaksi transesterifikasi dan dapat menyebabkan terhidrolisanya trigliserida (TG) menjadi digliserida (DG) dan ALB seperti yang ditunjukkan dalam Gambar 4.2. Pada karakterisasi bahan baku kandungan kadar air adalah 0,041 %, kadar tersebut lebih kecil dari kadar air maksimum yang dianjurkan.
x 222 g mol -1 = 0,20 gram
34
Gambar 4.2. Reaksi hidrolisis trigliserida
4.2. Penentuan Titik Tengah
Penentuan titik tengah dilakukan untuk menentukan nilai dari level-level percobaan dengan metode permukaan respon , sehingga dapat ditetapkan nilai-nilai pada level rendah (-1), tinggi (1) dan tengah (0). Nilai pada uji pendahuluan ini didasarkan pada publikasi penerapan paten dari Choo et al (2006). Penelitian dilakukan dengan mereaksikan minyak stearin menggunakan katalis NaOH sebanyak 1 % berat (berdasarkan berat minyak). Suhu yang digunakan adalah 90o
Hasil percobaan penentuan titik tengah (Tabel 4.2-4.4), yang analisisnya menggunakan KLT, menunjukkan bahwa kadar MG paling tinggi terdapat pada kondisi: perbandingan molar gliserol/RBDPKO 15:1, konsentrasi katalis 1.5% dan suhu 90
C dan minyak/gliserol yang digunakan 1/1 (perbandingan berat bahan) atau 1/8 (perbandingan molar), dengan waktu reaksi selama 1 jam dan perbandingan minyak dan pelarut ter-butanol yang digunakan 1:2 (berat/volum).
oC yakni dengan kadar MG sebesar 58,15 %. Hasil pada Tabel itu menjadi acuan pada optimasi gliserolisis menggunakan rancangan komposisi tengah (central composite design) dengan metodologi permukaan respon 3 variabel, dimana nilainya digunakan sebagai titik tengah yakni perbandingan molar gliserol/RBDPKO 15:1, konsentrasi katalis 1.5 % dan suhu 90o C. Sebagai batas atas dan batas bawah diambil sekitar nilai tersebut yakni 1:20 untuk batas atas dan 1:10 untuk batas bawahnya.
Demikian juga untuk suhu yakni batas atas 95o dan batas bawah 85o C. Untuk
Universitas Sumatera Utara
35
konsentrasi katalis batas atas 2 % dan batas bawah 1 %. Nilai α yang merupakan batas antara titik tengah dan titik bintang dihitung berdasarkan Persamaan 3.1, untuk rancangannya dapat dilihat pada Tabel 3.1 dan 3.2.
Tabel 4.2. Hasil gliserolisis penentuan titik tengah untuk rasio gliserol/RBDPKO
NO Rasio MG DG TG
Gliserol/RBDPKO (%) (%) (%)
1 8:1 32,12 8,33 59,55
2 10:1 48,39 13,2 38,42
3 15:1 53,36 12,34 34,3
4 20:1 31,16 19,96 48,88
Katalis : 1 % (persen berat berdasarkan berat minyak )
Suhu : 90o
Minyak/pelarut(t-butanol) : 1/2 (berat/volum) C
Tabel 4.3. Hasil gliserolisis penentuan titik tengah untuk konsentrasi katalis
NO Konsentrasi katalis (%) MG DG TG
(%) (%) (%)
1 0,5 29,5 46,23 24,27
2 1 53,36 12,34 34,3
3 1,5 58,17 9,02 32,14
4 2 48,72 22,72 28,56
Rasio gliserol/RBDPKO : 15:1
Suhu : 90o
Minyak/pelarut(t-butanol) : 1/2 (berat/volum) C
36
Tabel 4.4. Hasil gliserolisis penentuan titik tengahuntuk suhu
NO Suhu oC MG DG TG
(%) (%) (%)
1 80 28,28 33,68 38,05
2 85 29,17 8,33 62,5
3 90 58,17 9,02 32,14
4 95 41,04 16,61 42,35
Rasio gliserol/RBDPKO : 15:1
Katalis : 1,5 %
Minyak/pelarut(t-butanol) : 1/2 (berat/volum)
4.3. Penetapan Kondisi Optimum
Hasil gliserolisis RBDPKO dari penelitian ini ditampilkan dalam Tabel 4.5 dan 4.7. Data-data yang diperoleh, selanjutnya diolah dengan perangkat lunak minitab 14. Hasil analisis varian (ANOVA) untuk model pada pengukuran dengan metode kromatografi gas (KG) yang ditampilkan pada Tabel 4.6 menunjukkan bahwa model linear (p = 0,000) signifikan karena nilai p kurang dari α = 0,05. Sebaliknya model kuadratik dan non linear tidak signifikan. maka model yang tepat adalah model linear. Tabel juga menunjukkan nilai p hasil uji lack of fit bernilai 0,299. Jika digunakan α sebesar 5%, maka tidak ada lack of fit, hal ini berarti model sesuai dengan data.
Universitas Sumatera Utara
37
Tabel 4.5. Kadar monogliserida hasil analisa dengan metode KG pada beragam kondisi proses
No.
Percobaan X1 X2 X3 Y
1 10:1 1 85 66,44
2 20:1 1 85 17,25
3 10:1 2 85 78,79
4 20:1 2 85 21,69
5 10:1 1 95 51,20
6 20:1 1 95
26,13
7 10:1 2 95
74,03
8 20:1 2 95
35,40
9 7:1 1.5 90 74,58
10 23:1 1.5 90 22,61
11 15:1 0.7 90 23,47
12 15:1
2.3 90 75,87
13 15:1
1.5 82 75,9
14 15:1
1.5 98 52,53
15 15:1
1.5 90 56,27
16 15:1
1.5 90 55,33
17 15:1
1.5 90 47,24
18 15:1
1.5 90 36,23
19 15:1
1.5 90 42,00
20 15:1
1.5 90 62,00
Dimana:
X1 = Rasio gliserol/RBDPKO X2
X
= Katalis (% berat minyak)
3 = Suhu (oC) Y = Kadar monogliserida (%)