i
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Ilmu Farmasi
Oleh:
Adhitya Eka Prasetya NIM : 068114021
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
Kupersembahkan karya ini untuk:
Bapak, Ibu, dan Adik yang selalu menyayangi dan memberiku
semangat
Sahabat-sahabatku yang selalu setia menemaniku saat duka
maupun suka
v Nama : Adhitya Eka Prasetya Nomor Mahasiswa : 068114021
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
Penetapan Kadar Aspartam dalam Minuman Serbuk Beraroma Merek “X”
secara Kromatografi Cair Kinerja Tinggi Fase Terbalik
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, me-ngalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 19 Juli 2010
Yang menyatakan
vi
KATA PENGANTAR
Puji syukur kepada Yesus Kristus, atas berkat dan perlindungan-Nya, sehingga penulis dapat menyelesaikan skripsi yang berjudul “Penetapan Kadar Aspartam dalam Minuman Serbuk Beraroma Merek “X” secara Kromatografi Cair Kinerja Tinggi Fase Terbalik”. Skripsi ini disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S. Farm.) di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta. Pada kesempatan ini, penulis ingin mengucapkan terima kasih kepada:
1. Rita Suhadi, M.Si., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma ( USD ) Yogyakarta.
2. Prof. Dr. Sudibyo Martono, M.S., Apt. selaku dosen pembimbing yang telah memberikan motivasi dan diskusi.
3. Christine Patramurti, M.Si., Apt. selaku dosen penguji yang telah memberikan diskusi, kritik, dan saran.
4. Jeffry Julianus, M.Si. selaku dosen penguji yang telah memberikan diskusi, kritik, dan saran.
5. Kedua orang tuaku dan adikku, yang telah membantu dalam doa dan mengasihiku selalu.
vii
8. Yola, terima kasih telah bersedia menjadi partner skripsiku.
9. Bapak Tarsisius Suhardiyono beserta keluarga, atas tumpangannya selama 4 tahun.
10. Teman-teman seperjuangan Boim, Roby, Aya, Tony, Nica, Utz, Nduti atas persahabatan dan keceriaannya.
11. Teman-teman kelas A angkatan 2006 dan teman-teman kelompok A angkatan 2006 atas persahabatan dan kekompakannya.
12. Teman-teman Tasura 52 (Surya, Aden, Felix, Roy, dkk) atas persahabatan dan kebersamaannya.
13. Semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah banyak membantu penulis. Dalam hal ini, penulis mohon maaf.
Penulis menyadari bahwa masih banyak kekurangan dalam penyusunan skripsi ini, penulis memohon kritik dan saran yang sifatnya membangun. Penulis memiliki harapan yang sangat besar, semoga laporan ini dapat bermanfaat bagi pembaca.
Yogyakarta, Juli 2010
viii
INTISARI
Aspartam merupakan bahan tambahan makanan yang berfungsi sebagai pemanis buatan. Produk minuman serbuk beraroma menggunakan aspartam sebagai pemanis buatan karena tingkat kemanisannya yang tinggi dan harganya yang relatif murah. Produk minuman serbuk beraroma termasuk dalam kategori minuman ringan. Peraturan Kepala POM No. HK 00.05.5.1.4547/2004 batas maksimum penggunaan aspartam adalah 50 mg/kg berat badan per hari. Penelitian ini dilakukan untuk menetapkan kadar aspartam dalam minuman serbuk beraroma dengan metode kromatografi cair kinerja tinggi dan untuk mengetahui kadar aspartam dalam minuman serbuk beraroma merek “X” sesuai dengan yang tertera di kemasan.
Penelitian ini merupakan jenis penelitian non eksperimental deskriptif. Aspartam dianalisis menggunakan metode Kromatografi Cair Kinerja Tinggi fase terbalik dengan fase diam kolomKromasil100-5 C18(panjang kolom 25 cm dan
internal diameter 4,6 mm), ukuran partikel 5 µm; fase gerak campuran bufer fosfat pH 4 : asetonitril (80:20), kecepatan alir 1,4 ml/menit, dan detektor UV 214 nm yang telah tervalidasi.
Berdasarkan analisis hasil yang dilakukan, diperoleh bahwa rata-rata kadar aspartam dalam minuman serbuk beraroma merek “X” 22,63 mg/sachet. Dengan demikian dapat disimpulkan kadar aspartam dalam minuman serbuk beraroma merek “X” tidak sesuai dengan kadar yang tertera di kemasan.
ix
level of sweetness and it cheap relatively price. Flavor powder drink products include in category of softdrink. The Requirement of National Agency Drug and Food Control number: HK.00.05.5.1.4547/2004, about artificial sweeteners mentioned that maximum limit of aspartame in softdrink is 50 mg/kg. This research was done to determine the concentration of aspartame in flavor powder drink and to know whether the concentration listed on the packaging line.
This research was a non experimental descriptive research, used reverse-phase High Performance Liquid Chromatography (HPLC) method with stationary phase Kromasil 100-5 C18column(column length 25 cm and internal diameter 4,6
mm), partikel size 5 µm; mixture buffer phospat pH 4 : acetonitril (80:20) as mobile phase, flow rate 1,4 mL/minute, and detector UV 214 nm which have been validated.
Based on the result analysis, it is found that the average of concentration of aspartame in flavor powder drink merk “X” is 22.63 mg/sachet. In conclusion, the concentration of aspartame in flavor powder drink merk “X” not in accordance with levels indicated on the packaging.
x
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 19 Juli 2010 Penulis
xi
HALAMAN JUDUL ……… HALAMAN PERSETUJUAN PEMBIMBING ………. HALAMAN PENGESAHAN ………. HALAMAN PERSEMBAHAN ……….. HALAMAN LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ……… KATA PENGANTAR ……… INTISARI ………
ABSTRACT………
PERNYATAAN KEASLIAN KARYA ………...…….. DAFTAR ISI ……… DAFTAR TABEL ………...……….. DAFTAR GAMBAR ………...……… DAFTAR LAMPIRAN ……… BAB I PENGANTAR
A. Latar Belakang Penelitian ...……….. B. Permasalahan ………... C. Keaslian Penelitian ……….. D. Manfaat Penelitian ……….. E. Tujuan Penelitian ………..
xii BAB II PENELAAHAN PUSTAKA
A. Serbuk Minuman Beraroma ..……… B. Zat Aditif …. .……...………. C. Aspartam ………..………. 1. Pengertian Aspartam ... 2. Penggunaan Aspartam ………...………... 3. Kajian Keamanan …….……… 4. Metode Analisis Aspartam ………. D. Kromatografi Cair Kinerja Tinggi .……….……….. 1. Definisi Kromatografi Cair Kinerja Tinggi ……… 2. Kromatografi Partisi Fase Terbalik ……… 3. Detektor ………. 4. Analisis Kualitatif dan Analisis Kuantitatif ……….. E. Kesahihan Metode Analisis …... F. Landasan Teori ...…... G. Hipotesis ……… BAB III METODE PENELITIAN
A. Jenis dan Rancangan Penelitian ……… B. Variabel Penelitian dan Definisi Operasional ……… C. Alat Penelitian ………...……… D. Bahan Penelitian ……… E. Tata Cara Penelitian ……….
1. Pemilihan Sampel …...……….
xiii
5. Pembuatan larutan sampel ... 6. Penetapan kadar asparam ……….. F. Analisis Hasil ……… BAB IV HASIL DAN PEMBAHASAN
A. Pemilihan Sampel ... B. Pembuatan Kurva Baku Aspartam ...……… C. Penyiapan Sampel …...……….. D. PenentuanRecovery, Kesalahan Acak, dan Kesalahan Sistemik ……….. E. Penetapan Kadar Aspartam ……… BAB V KESIMPULAN DAN SARAN
xiv
DAFTAR TABEL
Tabel I. Kadar AspartamvsAUC ... Tabel II. Data perhitunganrecoverydan kesalahan sistemik ... Tabel III. Hasil penetapan kadar aspartam dalam sampel ...
xv
Gambar 2. Degradasi aspartam ... Gambar 3. Sistematik Instrumen KCKT ... Gambar 4. Hubungan korelasi antara kadar aspartam dan nilai AUC
replikasi II ... Gambar 5. Kromatogram Sampel ... Gambar 6. Kromatogram Baku ...
11 13
xvi
DAFTAR LAMPIRAN
Lampiran 1. Penimbangan Sampel (Minuman Serbuk Beraroma) ... Lampiran 2. Contoh perhitungan kadar aspartam dalam sampel …... Lampiran 3. Hasil penetapan kadar aspartam dalam sampel ………. Lampiran 4. Perhitungan nilairecovery, kesalahan acak, dan kesalahan
sistemik aspartam ……... Lampiran 5. Kromatogram Sampel... Lampiran 6. Lembar Spesifikasi Kolom ... Lampiran 7. Sertifikat analisis aspartam ……….. Lampiran 8. Komposisi minuman serbuk beraroma merek “X”...
42 44 45
A. Latar Belakang Penelitian
Dewasa ini, penggunaan bahan tambahan sangat banyak digunakan dalam berbagai jenis makanan dan minuman. Salah satunya adalah zat pemanis buatan yang biasanya terbuat dari bahan kimia. Pemanis buatan digunakan oleh banyak produsen makanan atau minuman ringan karena rasanya yang jauh lebih manis dan rendah kalori. Pemanis buatan yang belakangan ini sering digunakan salah satunya adalah aspartam.
Aspartam adalah pemanis buatan dari golongan gula non-sakarida yang banyak dipakai untuk produk-produk diet atau produk rendah kalori. Aspartam dibuat dengan menggabungkan 2 buah asam amino, yaitu fenilalanin dan asam aspartat dengan derajat kemanisan sekitar 160 sampai 200 kali gula pasir dan hampir tidak mengandung kalori. Saat ini aspartam dijual dalam berbagai bentuk, seperti cair, butiran, enkapsulasi dan juga tepung.
Belakangan ini pemanis buatan menimbulkan kontroversi akibat efek sampingnya. Di dalam tubuh aspartam terurai menjadi fenilalanin dan asam aspartat. Fenilalanin sebenarnya termasuk asam amino esensial yang diperlukan oleh tubuh dan tidak akan menjadi masalah bagi mereka yang kondisi tubuhnya sehat tanpa gangguan. Bagi mereka yang menderita fenilketonurea akan terjadi penumpukan fenilalanin dalam darah yang dapat mengakibatkan keterbelakangan mental. Selain itu, menurut penelitian di University of Liverpool Inggris yang
2
diterbitkan dalam Journal Toxicological Sciences menyimpulkan bahwa penggunaan pemanis aspartam dapat menimbulkan interaksi yang menyebabkan gangguan terhadap perkembangan sistim saraf anak-anak.
Pemakaian aspartam sebagai pemanis buatan masih diijinkan namun dengan batas-batas pemakaian yang dianjurkan agar penggunaannya aman. Di Indonesia, berdasarkan Peraturan Kepala POM No. HK 00.05.5.1.4547/2004 pasal 6 ayat 3, produk pangan yang mengandung aspartam wajib mencantumkan peringatan yang tertulis jelas pada kemasan produk bagi pasien fenilketonuria. Berdasarkan Peraturan Kepala POM No. HK 00.05.5.1.4547/ 2004 batas maksimum penggunaan aspartam adalah 50 mg/kg berat badan per hari (Anonim, 2004).
Analisis aspartam dalam minuman serbuk beraroma pada penelitian ini
menggunakan metode Kromatografi Cair Kinerja Tinggi (KCKT), karena analisis
dengan KCKT memiliki daya pisah baik, peka, penyiapan sampel mudah, dan
dapat dihubungkan dengan detektor yang sesuai (Johnson dan Stevenson, 1978). Beberapa pustaka menunjukkan bahwa metode KCKT fase terbalik merupakan
ringan bersoda menggunakan metode KCKT dengan detektor UV dan fase gerak asetonitril : bufer asetat (5 : 95).
Penelitian ini penting dilakukan karenapenelitian ini menunjukkan apakah kadar aspartam dalam minuman serbuk beraroma sesuai dengan yang tertera pada
kemasan minuman serbuk beraroma yaitu sebanyak 35 mg/sachet. Hal ini perlu
dilakukan karena apabila konsumsi pemanis buatan berlebihan dapat
membahayakan kesehatan (Soerjodibroto, 2002). Selain itu, belum adanya
penelitian tentang penetapan kadar aspartam dalam minuman serbuk beraroma
juga mendasari penulis untuk melakukan penelitian ini.
Pada penelitian ini akan diuji apakah metode KCKT fase terbalik yang telah memiliki validitas yang baik dapat digunakan untuk penetapan kadar aspartam dalam minuman serbuk beraroma. Penelitian yang dilakukan penulis merupakan upaya bersama dan kesinambungan dari penelitian Yolanda (2010).
B. Permasalahan
Berdasarkan latar belakang tersebut muncul permasalahan sebagai berikut:
1. Apakah metode KCKT fase terbalik yang telah tervalidasi dapat digunakan untuk penetapan kadar aspartam dalam minuman serbuk beraroma?
4
C. Keaslian penelitian
Sejauh penelusuran pustaka yang telah dilakukan, penelitian tentang penetapan kadar aspartam dalam minuman serbuk beraroma dengan metode kromatografi cair kinerja tinggi belum pernah dilakukan. Adapun penelitian yang sudah pernah dilakukan yaitu oleh Hayun dkk.(2004) tentang Penetapan kadar sakarin, asam benzoat, asam sorbat, kofeina, dan aspartam di dalam beberapa minuman ringan bersoda secara kromatografi cair kinerja tinggi dan Michael dkk. (1985) tentang determinasi aspartam, kafein, sakarin, dan asam benzoat dalam minuman dengan kromatografi cair kinerja tinggi.
D. Manfaat penelitian
1. Manfaat teoritis
a. Penelitian ini diharapkan dapat bermanfaat sebagai sumber informasi tentang berapakah kadar aspartam dalam minuman serbuk beraroma.
b. Penelitian ini diharapkan dapat bermanfaat sebagai sumber informasi tentang apakah kadar aspartam dalam minuman serbuk beraroma sesuai dengan kadar aspartam yang tertera pada kemasan minuman serbuk beraroma.
2. Manfaat metodologis
E. Tujuan Penelitian
1. Untuk menetapkan kadar aspartam dalam minuman serbuk beraroma dengan metode kromatografi cair kinerja tinggi yang telah tervalidasi.
BAB II
PENELAAHAN PUSTAKA
A. Serbuk Minuman Beraroma
Serbuk minuman beraroma adalah produk yang merupakan campuran tepung gula pasir dengan aroma dan bahan tambahan makanan lainnya yang diijinkan (Anonim, 1995 b). Minuman beraroma adalah produk yang diperoleh dengan mencampur air minum dan bahan penyedap rasa dan aroma, dengan atau tanpa penambahan gula, glukosa, atau bagian buah yang dapat dimakan, sari buah, karbon dioksida, dan bahan tambahan makanan yang diijinkan.
Serbuk minuman beraroma termasuk dalam kategori minuman ringan. Menurut Keputusan Badan Pengawasan Obat dan Makanan nomor: 02240/B/SK/VII/91, minuman ringan adalah produk yang diperoleh tanpa melalui proses fermentasi dengan atau tanpa penambahan CO2; dapat langsung diminum
atau diminum setelah diencerkan; tidak termasuk susu dan “milk shake”, sari buah, teh, kopi, coklat dan hasil olahannya, minuman beralkohol; dan tidak boleh ditambahkan alkohol (Anonim, 1991).
B. Zat Aditif
Zat aditif adalah zat atau campuran zat yang ditambahkan pada makanan dalam proses pembuatan, penggunaan, pengemasan, dan penyimpanan untuk tujuan peningkatan mutu. Pemakaiannya diijinkan selama:
1. Benar-benar dibutuhkan dalam makanan
2. Dapat meningkatkan gizi, mutu, kestabilan makanan
3. Dapat menjadikan makanan lebih menarik namun tanpa memberi efek samping pada penggunaan secara normal (Sudarmadji dkk., 1996).
Pada dasarnya, bahan tambahan dapat dibagi menjadi 2 bagian besar:
1. Aditif sengaja, yaitu bahan tambahan yang sengaja diberikan dengan maksud dan tujuan tertentu, seperti untuk meningkatkan konsistensi, nilai gizi, cita rasa, mengendalikan keasaman atau kebasaan, serta memantapkan bentuk dan rupa.
2. Aditif tidak sengaja, yaitu bahan tambahan yang terdapat dalam makanan dalam jumlah yang sangat kecil yang diakibatkan dari proses pengolahan (Winarno, 1992).
Salah satu bahan yang sering ditambahkan ke dalam bahan pangan adalah pemanis. Bahan pemanis dapat digolongkan menjadi 2 macam, yaitu:
1. Pemanis alami adalah bahan pemanis yang biasanya telah terdapat secara alami. Contoh : sukrosa, fruktosa, glukosa, sorbitol, steviosida, glisithizin dan pilodulsin.
2. Pemanis sintetik, adalah bahan pemanis yang biasanya dihasilkan dari hasil rekayasa manusia atau bahan pemanis yang tidak terdapat secara alami. Contohnya: siklamat, Na-sakarin, aspartam (Lutony, 1993).
8
Meski banyak ditemukan zat pemanis sintetik tetapi hanya beberapa saja yang dipakai dalam bahan makanan karena diperkirakan bersifat karsinogen. Zat pemanis sintetik yang banyak digunakan dalam makanan dan minuman adalah garam Ca atau Na-sakarin (Winarno, 1992).
Aneka produk yang selalu diberi tambahan pemanis adalah selai, jeli,
marmalade, sari buah, buah dan sayur dalam kaleng, susu kental manis, chutney, manisan buah-buahan, kembang gula, cordial (sirup buah-buahan), abon dan
corned beef. Disebutkan bahwa pemanis buatan hanya digunakan untuk perusahaan makanan dan minuman berkalori rendah dan harus dicantumkan jenis dan dosis bahan pemanis yang digunakan. Disertakan tulisan yang menerangkan bahwa makanan atau minuman tersebut hanya untuk penderita diabetes atau berkalori rendah (Lutony, 1993).
Dengan fungsi bahan pemanis yang dapat memperbaiki flavor bahan makanan, maka rasa manis yang timbul dapat meningkatkan kelezatan makanan tersebut. Selain itu, kadang dengan penambahan bahan pemanis juga dapat memperbaiki tekstur bahan makanan misalnya dengan kenaikkan viskositas, menambah bobot rasa (body) sehingga meningkatkan mutu sifat kunyah (mouth fullness) bahan makanan (Sudarmadji, 1982).
Pemanis buatan digunakan untuk memberi rasa manis pada makanan. Pemanis buatan ini tidak menghasilkan energi, oleh karena itu pemanis buatan banyak digunakan oleh mereka yang membatasi konsumsi gula atau penderita
pedagang dalam produk-produknya. Pemanis buatan yang banyak digunakan adalah sakarin, siklamat dan aspartam (Almatsier, 2002).
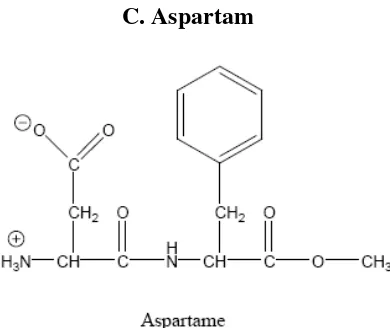
C. Aspartam
Gambar 1. Struktur kimia Aspartam
1. Pengertian Aspartam
Aspartam (gambar 1) adalah senyawa metil ester dipeptida, yaitu L-aspartil-L-alanin-metilester dengan rumus C14H18N2O5 memiliki kemanisan
100-200 kali sukrosa. Aspartam mengandung tak kurang dari 98,0% dan tidak lebih dari 102,0% C14H18N2O5.Kelarutan aspartam dalam air tergantung pada pH dan
suhu. Kelarutan maksimum tercapai pada pH 2,2 (20 mg/mL pada 250C) (Anonim, 1995 a).
10
sehingga tidak baik digunakan dalam bahan pangan yang diolah melalui pemanasan.
2. Penggunaan Aspartam
Mengacu pada asam amino pembentuk aspartam, maka aspartam bukanlah termasuk suatu bahan pemanis nonkalori karena seperti protein, aspartam dimetabolisme menjadi asam amino-asam amino penyusunnya dan memiliki nilai energi 4 kkal/g. Tetapi, karena dalam penggunaannya 100g sukrosa dapat diganti dengan 1g aspartam maka dapat dikatakan bahwa aspartam merupakan bahan pemanis nonkalori (Marie dan Piggott, 1991).
Aspartam merupakan nama pemanis buatan yang dikenal di kalangan orang-orang yang sering menggunakan pemanis yang rendah kalori. Selain pada pemanis tersebut, aspartam juga sering ditemukan dalam minuman-minuman ringan, permen karet bebas gula, dan ada pula yang terdapat dalam multivitamin. Aspartam sering digunakan karena tingkat kemanisannya yang tinggi, tetapi rendah kalori dan aman bagi orang-orang penderita diabetes (Tambunan, 2008).
3. Kajian Keamanan
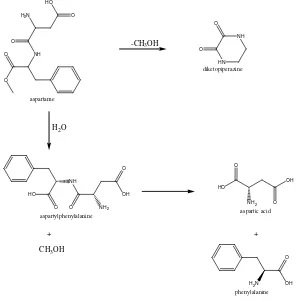
O
Gambar 2. Degradasi aspartam (Anonim, 1988)
Bagi penderita penyakit keturunan yang berhubungan dengan kelemahan mental (fenilketonurea/ PKU) dilarang untuk mengonsumsi aspartam karena adanya fenilalanin dalam tubuh penderita PKU diduga dapat menyebabkan kerusakan otak dan pada akhirnya akan mengakibatkan cacat mental.
12
Penggunaan aspartam bagi orang yang menderita penyakit turunan yang dikenal sebagai fenilketonurea perlu mendapat perhatian khusus. Orang yang menderita penyakit tersebut tidak mampu memetabolisme fenilalanin. Berlebihnya jumlah fenilalanin dalam tubuh penderita dapat menyebabkan kerusakan otak yang dapat mengakibatkan cacat mental, karena adanya penumpukan fenilalanin di otak (Marie dan Piggott, 1991).
Di Indonesia, berdasarkan Peraturan Kepala POM No. HK 00.05.5.1.4547/2004 pasal 6 ayat 3, produk pangan yang mengandung aspartam wajib mencantumkan peringatan yang tertulis jelas pada kemasan produk bagi pasien fenilketonurea. Berdasarkan Peraturan Kepala POM No. HK 00.05.5.1.4547/ 2004 batas maksimum penggunaan aspartam adalah 50 mg/kg berat badan per hari.
4. Metode Analisis Aspartam
Aspartam dapat ditentukan secara kualitatif dengan kromatografi lapis tipis (KLT) didasarkan pada pemisahan dengan KLT karena perbedaan afinitas aspartam terhadap fase diam dan fase geraknya. Fase diam untuk penetapan kadar aspartam ini adalah silika gel 60 GF 254, sedangkan fase geraknya adalah sistem pengembang n-butanol:asam asetat glasial: air (2:1:1). Untuk menampakkan noda digunakan larutan ninhidrin 0,2% dalam air dan larutan brom 1% dalam CCl4.
Penentuan Aspartam secara kualitatif dapat dilakukan secara titrasi menggunakan larutan Li/Na metoksida (0,01N), N-N-dimetil formamida dan indikator timol biru (Mahindru, 2000). Penetapan kadar aspartam dalam minuman dan makanan yang paling umum digunakan saat ini adalah dengan metode KCKT fase terbalik menggunakan fase diam C18 dan dua jenis fase gerak yang dapat
dipilih yaitu metanol:bufer asetat atau asetonitril:bufer fosfat (Nollet, 2000).
D. Kromatografi Cair Kinerja Tinggi
1. Definisi Kromatografi Cair Kinerja Tinggi
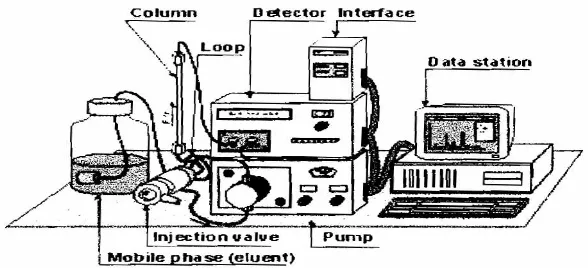
Kromatografi adalah istilah umum untuk berbagai cara penetapan pemisahan berdasarkan partisi zat cair antara fase yang bergerak dapat berupa gas atau zat cair, dan fase diam dapat berupa zat cair atau zat padat (Johnson dan Stevenson, 1978). Metode KCKT adalah metode kromatografi yang fase geraknya dialirkan cepat dengan bantuan tekanan dari pompa dan hasilnya dideteksi dengan detektor (Gritter dkk., 1985). Skematis instrumen KCKT dapat dilihat pada Gambar 3.
14
2. Kromatografi Partisi Fase Terbalik
Menurut Gritter dkk. (1991), konsep pengembangan kromatografi cair partisi yaitu perlakuan sampel dalam kondisi cair-cair tergantung pada kelarutannya di dalam kedua cairan yang terlibat. Jika solut ditambahkan ke dalam kondisi yang terdiri atas dua pelarut yang tidak bercampur dan keseluruhan kondisi dibiarkan seimbang, solut akan tersebar antara kedua fase itu menurut persamaan:
Cm Cs
K
K adalah koefesien distribusi, Cs adalah konsentrasi solut dalam fase diam dan
Cm adalah konsentrasi solut dalam fase gerak (Skoog dkk., 1994). Hal-hal yang harus diperhatikan dalam pemilihan metode kromatografi partisi fase balik adalah: 1. Kolom
Kolom yang digunakan pada jenis kromatografi ini adalah kemasan fase terikat. Fase diam yang biasa digunakan pada kromatografi partisi fase balik adalah oktadesilsilan (ODS). Selain ODS, dikenal pula silika dengan substitusi oktil (C8) (Munson, 1984).
2. Fase gerak
3. Detektor
Detektor yang baik hendaknya memiliki kepekaan tinggi, rentang respon liniernya lebar, tidak dipengaruhi perubahan suhu dan aliran, memberikan hasil dengan keterulangan yang baik. Secara umum, detektor dibagi menjadi 2 kategori, yaitu:
a. Bulk property detectors
Detektor jenis ini merupakan detektor yang mengukur perubahan sifat fisik fase gerak dan solut. Detektor tipe ini cenderung relatif tidak sensitif dan menghendaki suhu yang terkendali. Contoh detektor jenis ini yaitu detektor indeks bias.
b. Solute property detectors
Detektor jenis merupakan detektor yang hanya mengukur sifat fisik solut. Detektor tipe ini 1000 kali lebih sensitif dan mampu mengukur solut sampai satuan nanogram atau lebih kecil lagi. Contoh detektor jenis ini yaitu detektor fluoresensi, detektor penyerapan (UV-Vis), dan detektor elektrokimia (Munson, 1984).
4. Analisis Kualitatif dan Analisis Kuantitatif
16
Resolusi (Rs) didefinisikan sebagai jarak antara dua puncak dibagi dengan rata-rata lebar dasar puncak. Resolusi dikatakan baik apabila nilai Rs ≥ 1,5 yang berarti pemisahan telah mencapai 99,7% (Sastrohamidjojo, 2002). Resolusi juga dipengaruhi oleh beberapa faktor yang dapat terlihat pada persamaan berikut
Rs =
Untuk memperbaiki daya pisah maka faktor-faktor tersebut perlu dioptimasi. Cara optimasi efisiensi kolom (a) dapat dilakukan dengan menambah jumlah lempeng teoritis (N), yaitu dengan menambah panjang kolom (N=L/H) sehingga diperoleh puncak yang kecil dan resolusi yang baik. Optimasi faktor selektivitas (b) dapat dilakukan dengan mengganti pelarut atau mengubah komposisi pelarut yang digunakan sehingga efisiensi pelarut bertambah dan resolusi juga meningkat. Optimasi faktor kapasitas (c) dapat dilakukan dengan memvariasi kekuatan pelarut sehingga fase gerak dapat memberikan nilaik’suatu komponen sampel menjadi lebih besar atau lebih kecil. Dengan meningkatkan nilaik’maka akan memperbaiki resolusi (Noegrohati, 1994).
E. Kesahihan Metode Analisis Instr
Parameter-parameter yang digunakan sebagai pedoman dalam kesahihan metode analisis antara lain:
1. Akurasi
Akurasi adalah suatu ukuran kedekatan nilai hasil percobaan dengan nilai yang sesungguhnya. Akurasi suatu metode biasanya dinyatakan dengan persen
recovery(Anonim, 2005). Akurasi untuk bahan obat dengan kadar kecil biasanya disepakati 90-110%, akurasi untuk kadar obat yang lebih besar biasanya disepakati 95-105%, akurasi untuk bahan baku biasanya disepakati 98-102% sedangkan untuk bioanalisis rentang akurasi 80-120% masih bisa diterima (Mulja dan Hanwar, 2003).
2. Presisi
Presisi adalah suatu ukuran kedekatan nilai data satu dengan data lainnya dalam suatu pengukuran pada kondisi analisis yang sama. Presisi sering kali diukur sebagai persen Relative Standard Deviation (RSD) atau Coefficient of Variation (CV) untuk sejumlah sampel yang berbeda bermakna secara statistik. Kriteria presisi diberikan jika metode memberikan nilai CV < 2,8% untuk kadar analit 1-10% (Harmita, 2004).
3. Linieritas
18
4. Sensitivitas
Sensitivitas merupakan kemampuan suatu metode untuk mengukur dengan akurat respon analit diantara seluruh komponen sampel yang mungkin ada dalam matriks sampel (Mulja dan Hanwar, 2003).
5. Spesifisitas
Spesifisitas merupakan karakteristik terpenting dari suatu metode dan harus ditetapkan sebagai salah satu variabel yang utama. Spesifisitas merupakan kemampuan suatu metode untuk mengukur dengan akurat respon analit di antara seluruh komponen sampel potensial yang mungkin ada dalam matriks sampel (Mulja dan Hanwar, 2003).
6.Limit of Detection(LOD)
LOD adalah konsentrasi analit terendah dalam sampel yang masih dapat diukur pada kondisi percobaan tertentu tetapi tidak perlu secara kuantitatif. Penentuan LOD pada metode instrumental dapat didasarkan pada signal to noise ratio yaitu dengan cara membandingkan hasil pengukuran analit yang telah diketahui konsentrasinya terhadap respon blangko. Konsentrasi analit yang mampu memberikan respon 2-3 kali respon blangko inilah yang kemudian ditetapkan sebagai LOD. Penentuan LOD dapat pula didasarkan pada standar deviasi yang diperoleh dari pengukuran sejumlah blangko yang kemudian dikalikan dengan faktor sebesar 2 atau 3 (Anonim, 1995 c).
7.Limit of Quantitation(LOQ)
tertentu dari suatu metode. LOQ merupakan parameter uji kuantitatif untuk senyawa berkadar rendah dalam sampel yang mengandung bahan-bahan lainnya seperti bahan pengotor dalam serbuk obat dan hasil degradasi dari suatu produk obat jadi. Penentuan LOQ pada metode instrumental biasanya didasarkan pada standar deviasi yang diperoleh dari pengukuran sejumlah blangko yang kemudian dikalikan dengan suatu faktor sebesar 10 (Anonim, 1995 c).
8.Range
Range adalah interval antara konsentrasi terendah sampai konsentrasi tertinggi dari analit yang dapat diukur secara kuantitatif menggunakan metode analisis tertentu dan menghasilkan akurasi serta presisi yang memadai. Biasanya
range mempunyai satuan yang sama dengan satuan yang digunakan pada hasil analisis (Anonim, 1995 c).
F. Landasan Teori
KCKT merupakan kromatografi yang fase geraknya dialirkan dengan bantuan tekanan dari pompa dan hasilnya dideteksi dengan detektor. Metode KCKT dapat digunakan untuk analisis senyawa multi komponen karena KCKT merupakan metode pemisahan sekaligus mengidentifikasi senyawa dalam sampel yang berupa campuran.
20
Yolanda (2010) dan penetapan kadar oleh penulis mengacu pada jurnal-jurnal yang ada, yang kemudian kadar aspartam yang didapat dari hasil penelitian dibandingkan dengan kadar aspartam yang tertera dalam kemasan minuman serbuk merek “X”. Batas maksimum aspartam yang diijinkan dalam minuman ringan adalah 50 mg/kg berat badan per hari.
G. Hipotesis
Berdasarkan landasan teori di atas, dapat disusun suatu hipotesis sebagai berikut:
1. Metode KCKT fase terbalik yang telah tervalidasi dapat digunakan untuk penetapan kadar aspartam dalam minuman serbuk beraroma.
A. Jenis dan Rancangan Penelitian
Penelitian ini tergolong dalam penelitian non-eksperimental analitik.
B. Variabel dan Definisi Operasional
1. Variabel penelitian
a. Variabel bebas
Variabel bebas yaitu variabel yang direncanakan untuk diberi pengaruh terhadap variabel tergantung. Variabel bebas dalam penelitian ini adalah sediaan minuman serbuk beraroma merek “X”.
b. Variabel tergantung
Variabel tergantung yaitu titik pusat permasalahan yang merupakan kriteria penelitian ini. Variabel tergantung dalam penelitian ini adalah validitas parameter yang berupa: kesesuaian sistem penetapan kadar aspartam dalam minuman serbuk beraroma pada KCKT dan kadar aspartam dalam minuman serbuk beraroma.
c. Variabel terkendali
Variabel terkendali yaitu variabel yang diketahui atau secara teoritis mempunyai pengaruh terhadap variabel tergantung, tetapi dapat dikendalikan. Variabel terkendali dalam penelitian ini adalah:
22
1) Alat yang digunakan yaitu HPLC, dikendalikan dengan cara mengukur validitas metode yang digunakan [ % perolehan kembali (recovery), kesalahan sistemik dan kesalahan acak ].
2) Pengotor-pengotor sistem KCKT yang bisa berasal dari alat dan pelarut.
2. Definisi operasional dalam penelitian ini adalah:
a. Aspartam yang ditetapkan kadarnya adalah aspartam yang terdapat dalam minuman serbuk beraroma merek “X”.
b. Minuman serbuk beraroma yang dianalisis adalah minuman serbuk merek “X” yang mencantumkan adanya kandungan aspartam pada kemasannya. Tercantumkan dalam kemasan bahwa kadar aspartam adalah 0,035 g/sachet. Sampel yang dipilih memiliki nomor produksi yang sama.
c. Sistem Kromatografi Cair Kinerja Tinggi (KCKT) fase terbalik yang digunakan adalah seperangkat alat KCKT dengan fase diam kolom
reversed phase Kromasil 100-5 C18250 x 4,6 mm ukuran partikel 5 µm
dan fase gerak campuran bufer fosfat pH 4 dan asetonitril, dengan perbandingan 80:20.
d. Kadar aspartam dalam minuman serbuk dalam satuan mg/sachet.
C. Alat-alat penelitian
Alat - alat yang digunakan dalam penelitian ini adalah seperangkat KCKT yang terdiri dari pompa merek Shimadzu LC-10 AD, detektor UV Vis merek
ShimadzuSPD 10 AV, CBM 101 merek Shimadzu, seperangkat komputer merek
model 77251, kolom C-18 merek Kromasil 4,6 mm x 25 cm , syringe merek
Hamilton Part, alat degassing ultrasonik merek Retsch tipe T640, penyaring
Whatmann anorganik dan organik, membran filter merek Whatmann, neraca analitik merek Scaltec SBC 22, vakum merek Gast model DOA-P104-BN,
Millipore ukuran pori 0,45 µm, seperangkat alat gelas yang lazim digunakan di laboratorium analisis.
D. Bahan-bahan penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah aspartam (NutraSweet Company), kalium dihidrogen fosfat, asetonitril, dan metanol (E. Merck), aquabidestilata (Ikapharmindo Putramas), dan sampel minuman serbuk beraroma merek “X” 35 mg/sachet.
E. Tata Cara Penelitian
1. Pemilihan sampel
Sampel yang dipilih adalah minuman serbuk beraroma yang mencantumkan kandungan aspartam pada kemasannya. Sampel yang digunakan sebanyak 20 kemasan dengan nomor kode produksi yang sama dilakukan 7 kali replikasi dan dibuat duplo di setiap replikasi, yaitu dilakukan pemipetan sampel sebanyak 2 kali.
2. Pembuatan larutan baku aspartam
24
3. Pembuatan fase gerak
Fase gerak yang digunakan dalam penelitian ialah menggunakan campuran bufer fosfat pH 4 dan asetonitril dengan perbandingan 80:20. Bufer fosfat dibuat dengan melarutkan 0,85 g KH2PO4 dalam akuabides hingga volume 500,0 mL
kemudian ditambahkan beberapa tetes asam fosfat sampai pH 4. Fase gerak dibuat sesuai dengan volume yang dibutuhkan, kemudian dicampur dan disaring dengan menggunakan kertas saring anorganik Whatmann 0,45 µm diameter 47 mm dengan bantuan pompa vakum Gastdan glass filter Whatmannkapasitas 300 mL. Fase gerak kemudian didegassingdengan alat ultrasonic Retsch selama 15 menit.
4. Pembuatan seri larutan baku aspartam
Larutan baku induk aspartam dari langkah 2 di atas dipipet 1,0; 1,5; 2,0; 2,5; dan 3,0 mL kemudian dimasukkan ke dalam labu ukur 10,0 mL dan diencerkan dengan fase gerak bufer fosfat : asetonitril (80:20) sampai tanda sehingga didapatkan konsentrasi seri aspartam 2; 3; 4; 5; dan 6 mg/100mL. Kemudian disaring dengan Millipore dan didegassing selama 15 menit dan diinjeksikan ke sistem KCKT dengan kecepatan alir 1,4 mL dan komposisi fase gerak bufer fosfat pH 4 : asetonitril (80:20). AUC (Area Under Curve) untuk tiap
peak yang muncul diamati dari kromatogram yang didapat. Lalu, ditentukan persamaan regresi linear antara kadar tiap analit terhadap AUC.
5. Pembuatan larutan sampel
gerak hingga 10,0 mL. Pipet 2,0 mL masukkan ke dalam labu ukur 10,0 mL dan encerkan dengan fase gerak hingga tanda. Larutan tersebut disaring dengan
Millipore dan didegassing selama 15 menit. Replikasi dilakukan 7 kali dan dilakukan duplo untuk setiap replikasi.
6. Penetapan kadar aspartam
Larutan sampel diinjeksikan dalam injector port dengan menggunakan KCKT syringe Microliter tipe 710 dengan fase diam kolom Kromasil 100-5 C18
250 x 4,6 mm, fase gerak dengan komposisi bufer fosfat pH 4 : asetonitril (80:20), serta kecepatan alir fase gerak 1,4 mL/menit. Injeksikan 40 µL dan detektor diatur pada λ 214 nm. Amati kromatogram yang dihasilkan. Dengan memasukkan nilai AUC sampel dalam persamaan kurva baku aspartam, maka akan didapatkan kadar aspartam dalam sampel. Data disajikan dengan satuan mg/sachet. Lakukan pengulangan penimbangan 7 kali dan lakukan duplo pada masing-masing pengulangan.
F. Analisis Hasil
1. Jenis statistika dan uji statistik yang dipakai
a. Jenis statistika. Penelitian ini menggunakan jenis statistika deskriptif. b. Uji statistik. Uji-uji statistik yang akan dipakai : Regresi Linear.
26
2. Analisis yang dilakukan dalam penelitian ini
A. Pemilihan Sampel
Penilitian ini bersifat deskriptif sehingga untuk populasi besar diambil sampel sebanyak 10% dan untuk populasi kecil 20% (Sevilla dkk., 1993). Hasil pendataan menunjukkan bahwa jumlah minuman serbuk beraroma yang beredar di Yogyakarta sebanyak 5 merek. Jumlah ini termasuk dalam populasi kecil, maka untuk penelitian ini diambil 20% dari merek minuman serbuk beraroma yang ada secara acak yaitu 1 merek.
Berdasarkan hasil tersebut, maka pengambilan sampel tersebut diwakili oleh 20 kemasan dengan kode nomor produksi yang sama. Pemilihan kode nomor produksi yang sama bertujuan untuk mendapatkan kriteria homogenitas karena diasumsikan bahwa sampel dengan kode nomor produksi sama bersifat homogen.
Kriteria lainnya yang harus dipenuhi dalam pemilihan sampel adalah representatif, yakni sampel yang dianalisis benar-benar mencerminkan populasi yang diwakilinya, dan 20 kemasan diharapkan telah memenuhi persyaratan tersebut. Replikasi dilakukan 7 kali, dan dilakukan duplo pada setiap replikasi, yakni pemipetan 2 kali untuk setiap replikasi. Replikasi 7 kali ditujukan untuk mengetahui reprodusibilitasnya.
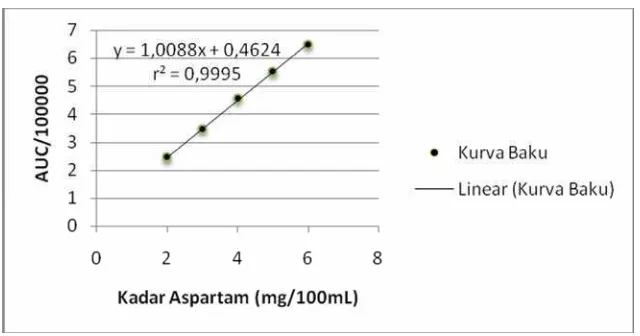
B. Pembuatan Kurva Baku Aspartam
Pembuatan kurva baku bertujuan untuk memperoleh persamaan regresi linear yang selanjutnya digunakan untuk menghitung kadar aspartam dalam
28
sampel. Linieritas suatu kurva baku menunjukkan bahwa kenaikan respon yang terjadi dikarenakan deteksi instrumen sebanding dengan kenaikan konsentrasi baku yang digunakan. Parameter linieritas suatu kurva ditentukan dengan nilai koefisien korelasi (r) lebih besar dari 0,999 (Snyder dkk., 1997).
Lima seri konsentrasi yang dibuat untuk pembuatan kurva baku yakni 2, 3, 4, 5, dan 6 mg/100mL, diinjeksikan ke instrumen KCKT dan dibaca oleh detektor
pada λ 214 nm. Dilakukan tiga kali replikasi untuk setiap seri konsentrasi dengan
tujuan untuk mendapatkan nilai (r) yang terbaik, yakni nilai (r) yang lebih besar dari 0,999.
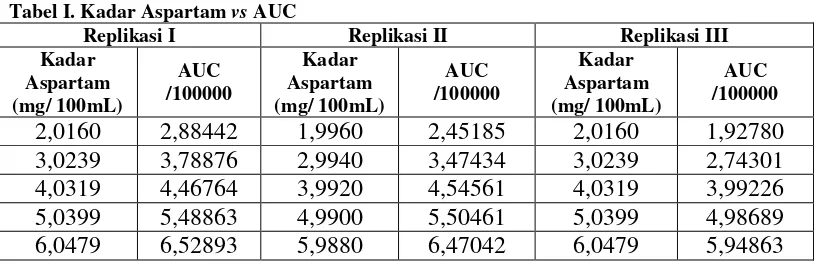
Persamaan regresi linear yang didapatkan merupakan hubungan antara konsentrasi aspartam vs AUC (Area Under Curve) yang dihasilkan dari penginjeksian pada sistem KCKT. Kadar aspartam dalam sampel dihitung dengan memasukkan AUC sampel ke dalam persamaan kurva baku yang didapatkan. Hasilnya dapat terlihat di Tabel I.
Tabel I. Kadar AspartamvsAUC
Replikasi I Replikasi II Replikasi III Kadar
2,0160 2,88442 1,9960 2,45185 2,0160 1,92780
3,0239 3,78876 2,9940 3,47434 3,0239 2,74301
4,0319 4,46764 3,9920 4,54561 4,0319 3,99226
5,0399 5,48863 4,9900 5,50461 5,0399 4,98689
6,0479 6,52893 5,9880 6,47042 6,0479 5,94863
Persamaan kurva baku yang diperoleh dari ketiga replikasi tersebut : I. y = 0,8918x + 1,0361 ; r = 0,997 ; r2= 0,994
Ketiga persamaan kurva baku diatas telah memiliki nilai linieritas yang baik. Dari ketiga persamaan kurva baku yang diperoleh dipilih persamaan kurva baku yang paling linier. Linieritas menyatakan hubungan korelasi antara kadar aspartam dengan AUC yang dihasilkan. Linieritas dinyatakan sebagai koefisien korelasi (r). Secara statistik, nilai r dapat dikatakan baik apabila sudah lebih besar daripada rtabel dengan taraf kepercayaan dan derajat bebas tertentu. Dengan taraf
kepercayaan 99% dan derajat bebas 3, maka rtabel adalah sebesar 0,959. Ketiga
persamaan kurva baku di atas sudah memberikan hubungan korelasi yang baik antara kadar dan serapan sebab r-nya lebih besar daripada rtabel. Persamaan kurva
30
Gambar 3. Hubungan korelasi antara kadar aspartam dan nilai AUC Replikasi II
C. Penyiapan Sampel
Sebelum penyiapan sampel, masing-masing sampel dalam tiap kemasan dihomogenkan terlebih dahulu. Proses homogenisasi dilakukan dengan menggunakan metodeassay, yakni mencampurkan semua sampel menjadi satu ke dalam suatu wadah tertentu. Penyiapan sampel ini bertujuan untuk mendapatkan larutan sampel yang bebas endapan dan jernih atau bening.
mengurangi umur normal kolom (Snyder dkk., 1997). Filtrat yang didapatkan selanjutnya didegassing selama 15 menit untuk menghilangkan gelembung yang terdapat dalam larutan, karena adanya gelembung dikhawatirkan dapat mengganggu pengukuran. Setelah larutan sampel selesai disaring dan didegassing, sampel diinjeksikan ke sistem KCKT dan dianalisis dengan metode KCKT.
D. PenentuanRecovery, Kesalahan Acak, dan Kesalahan Sistematik
Validitas metode merupakan ukuran kesahihan suatu metode yang digunakan. Validitas yang diuji pada penelitian ini meliputi akurasi dan presisi. Akurasi menggambarkan apakah suatu metode menghasilkan nilai pengukuran yang sama atau mendekati nilai sebenarnya, sedangkan presisi menunjukkan apakah metode yang digunakan memiliki ketelitian sehingga pada pengulangan pengukuran akan memberikan nilai yang sama.
Recovery merupakan parameter untuk akurasi suatu metode analisis.
Recovery dan kesalahan sistematik pada metode KCKT fase terbalik ini ditentukan dari kadar terukur aspartam dibandingkan dengan kadar aspartam yang diketahui (teoritis).
32
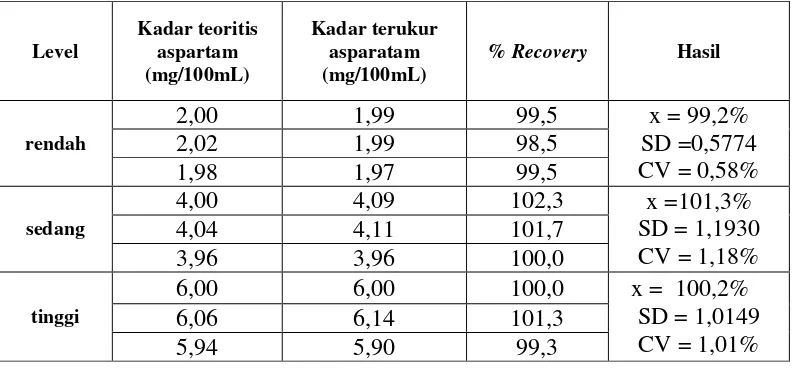
Tabel II. Data perhitunganrecoverydan kesalahan acak
Persamaan recovery suatu metode analisis adalah 98 - 102 % (Harmita, 2004), dari tabel II terlihat bahwa dari ke-3 seri kadar aspartam dengan replikasi tiga kali memberikanrecovery 99,2 - 101,3% yang masuk dalam rangerecovery
yang baik. Hal ini berarti bahwa metode KCKT memiliki akurasi yang baik untuk menetapkan kadar aspartam dalam minuman serbuk beraroma merek “X”.
E. Penetapan Kadar Aspartam
Penetapan kadar aspartam dalam minuman serbuk beraroma yang dilakukan menggunakan dua puluh kemasan dengan merek “X”. Penetapan kadar dilakukan secara duplo. Kondisi yang digunakan untuk menetapkan kadar aspartam dalam minuman serbuk beraroma adalah kondisi yang didapat dari hasil validasi metode penetapan kadar aspartam dengan metode KCKT yang dilakukan oleh Yolanda (2010).
Pada sediaan minuman serbuk beraroma terdapat pula bahan-bahan lain yang mungkin dapat mengganggu penetapan kadar aspartam. Oleh karena itu, metode KCKT harus dapat memisahkan aspatam dari bahan-bahan lain yang ada dalam minuman serbuk beraroma tersebut.
34
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5
µm
Fase gerak: bufer fosfat pH 4 : asetonitril (80:20) Kecepatan alir: 1,4 mL/menit
Injeksi: sampel 40 µL Detektor: UV 214 nm
Gambar 5. Kromatogram Sampel Minuman Serbuk Beraroma Merek “X”
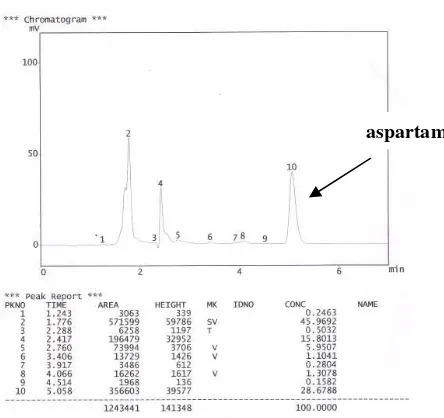
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5
µm
Fase gerak: bufer fosfat pH 4 : asetonitril (80:20) Kecepatan alir: 1,4 mL/menit
Injeksi: sampel 40 µL Detektor: UV 214 nm
aspartam
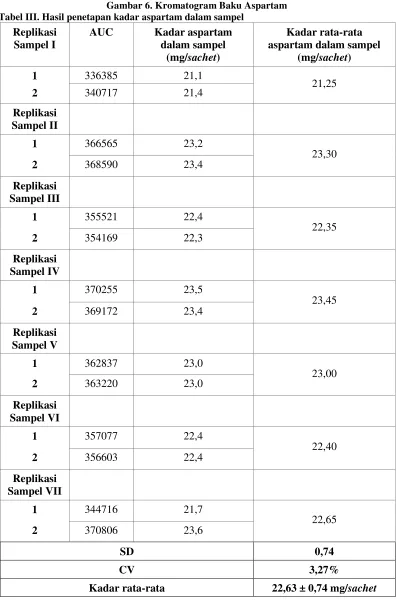
Gambar 6. Kromatogram Baku Aspartam Tabel III. Hasil penetapan kadar aspartam dalam sampel
Replikasi
2 340717 21,4 21,25
Replikasi
2 363220 23,0 23,00
Replikasi
36
Precision yang dimaksudkan dalam penelitian ini adalah repeatability, yaitu suatu ukuran kedekatan nilai data yang satu dengan yang lain dalam satu pengukuran pada kondisi analisi yang sama. Precision dinyatakan dengan
Coefficient of Variation (CV). Tabel III dari penelitian ini menunjukkan bahwa harga CV yang diperoleh pada penetapan kadar aspartam dalam minuman serbuk merek “X” adalah 3,27%. Nilai CV tersebut masih berada pada batasan CV yang memenuhi syarat untuk kadar analit > 0,1% yaitu 3,7% (Yuwono, M. dan Indrayanto, G., 2005), sehingga dapat dinyatakan bahwa metode KCKT memiliki presisi yang baik pada penetapan kadar aspartam dalam minuman serbuk beraroma merek “X”.
Tabel III dari penelitian ini juga menunjukkan bahwa kadar rata-rata aspartam dalam minuman serbuk beraroma merek “X” pada 7 replikasi yaitu 22,63 ± 0,74 mg/sachet. Hal ini berarti bahwa kadar aspartam yang diperoleh di laboratorium berbeda dengan kadar aspartam yang tertera pada kemasan yaitu 35 mg/sachet. Perbedaan kadar ini disebabkan karena terjadinya perbedaan bobot sampel. Pada saat penimbangan sampel yang dilakukan didapatkan bobot sampel rata-rata tiap kemasan sebesar 10,05 g. Sedangkan bobot sampel yang tertera pada kemasan adalah 12 g. Selain itu, perbedaan kadar tersebut bisa disebabkan masih adanya pengotor yang terdapat dalam sampel yang dapat menggangu pengukuran. Perbedaan kadar ini tidak menjadi masalah karena kadar yang didapat masih dibawah batas penggunaan maksimum yang ditetapkan pada peraturan POM.
38
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Penetapan kadar aspartam dalam minuman serbuk beraroma merek ”X” dengan metode KCKT fase terbalik menghasilkan nilai recovery98-102% dancoefficient of variation (CV) < 2,8%. Dengan demikian dapat disimpulkan bahwa metode KCKT fase terbalik memiliki validitas yang baik untuk penetapan kadar aspartam dalam minuman serbuk beraroma merek ”X”.
2. Kadar aspartam dalam minuman serbuk beraroma merek ”X” hasil penelitian laboratorium adalah sebesar 22,63 ± 0,74 mg/sachet. Dengan demikian, dapat disimpulkan bahwa kadar aspartam dalam minuman serbuk beraroma merek ”X” tidak sesuai dengan kadar aspartam yang tertera pada kemasan minuman serbuk beraroma.
B. Saran
DAFTAR PUSTAKA
Almatsier, S, 2002, Prinsip Dasar Ilmu Gizi, PT Gramedia Pustaka Utama, Jakarta.
Anonim, 1991, Keputusan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia No. 02240/B/SK/VII/91 Tentang Persyaratan Mutu Serta Label dan Periklanan Makanan, Badan Pengawas Obat dan Makanan, Jakarta. Anonim, 1995 a, Farmakope Indonesia, edisi IV, 1066, Departemen Kesehatan
Republik Indonesia, Jakarta.
Anonim, 1995 b, Standar Nasional Indonesia 01-3722-1995 Tentang Serbuk Minuman Rasa Jeruk,Jilid V, Dewan Stadarisasi Nasional, Jakarta.
Anonim, 1995 c,The United State Pharmacopoeia 23,Jilid 2, 1982-1984, Unites States Pharmacopoeia Convention, Inc., Rockville.
Anonim, 2004, Keputusan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia No. HK. 00. 05. 5. 1. 4547 tanggal 21 Oktober 2004 Tentang Persyaratan Penggunaan Bahan Tambahan Pangan Pemanis Buatan dalam Produk Pangan, 2, Badan Pengawas Obat dan Makanan, Jakarta.
Anonim, 2005, The United States Pharmacopeia 28th edition, 2748-2751, United States Pharmacopeial Convention, Inc., Rockville.
Gritter, R.J., Bobbitt, J.M., and Schwarting, A.E., 1991, Pengantar Kromatografi, diterjemahkan oleh Kosasih Padmawinata, Edisi II, 205-219, ITB, Bandung. Harmita, 2004, Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya, Majalah Ilmu Kefarmasian, Vol. I, No.3, Desember 2004,
117–135, Departemen Farmasi FMIPA UI, Depok.
Hayun, Yahdiana, H. dan Aziza, C.N., 2004, Penetapan kadar sakarin, asam benzoat, asam sorbat, kofeina, dan aspartam di dalam beberapa minuman ringan bersoda secara kromatografi cair kinerja tinggi, Majalah Ilmu Kefarmasian, Vol. I, No.3, Desember 2004, 148-159, Departemen Farmasi FMIPA UI, Depok.
Johnson, E.L. and Stevenson, R., 1978, Basic Liquid Chromatography,
diterjemahkan oleh Kosasih Padmawinata, 6-9, ITB, Bandung.
Kazakevich, Y. and Mc.Nair, H., 1996, Basic Liquid Chromatography, Textbook on HPLC, http://hplc.chem.shu.edu/NEW/HPLC_Book/, diakses pada tanggal 4 Januari 2010
40
Mahindru, S. N, 2000,Food Additives Characteristic, Detection, and Estimation, 69-72, Tata McGraw-Hill Publishing Company Limited, New Delhi.
Marie, S. dan Piggott, J, R., 1991,In Handbook of Sweeteners, 116-185, Blackie, Glasgow.
Michael et al., 1985, Determination of Aspartame, Caffeine, Saccharin, and Benzoic Acid in Beverages by High Performance Liquid Chromatography, Boston University.
Mulja, M. dan Hanwar, D., 2003, Prinsip-Prinsip Cara Berlaboratorium yang Baik (Good Laboratory Practice), Majalah Farmasi Indonesia Airlangga, Vol.III, No.2, 71-76, Universitas Airlangga Press, Surabaya.
Mulja, M. dan Suharman, 1995, Analisis Instrumental, 6-11, Universitas Airlangga Press, Surabaya.
Munson, J.W., 1984, Pharmaceutical Analysis Modern Methods, diterjemahkan oleh Harjana, Parwa.B,15,33-34, Universitas Airlangga Press, Surabaya. McNair, H, M. dan Boneli, E, J., 1988, Dasar Kromatografi Gas, diterjemahkan
oleh Kosasih Padmawinata, 19, ITB, Bandung.
Noegrohati, S., 1994,Pengantar Kromatografi, 16-17, UGM, Yogyakarta.
Nollet, L, 1996, Handbook of food analysis, vol 2, 1745-1746,1835-1844,1853-1857, Marcell Dekker Inc, New York.
Nollet, Leo, M.L., 2000, Food Analysis by HPLC, 533-538, Marcell Dekker Inc, New York.
Sakidja, M.S., 1989, Kimia Pangan, 103-108, Departemen Pendidikan dan Kebudayaan Direktorat Jendral Pendidikan Tinggi Pengembangan Lembaga Pendidikan Tenaga Kependidikan, Jakarta.
Sastrohamidjojo, H., 2002, Kromatografi, edisi kedua, 71, Liberty Yogyakarta, Yogyakarta.
Sevilla, L.G., Ochave, J.A., Punsalon, T.G., Regala, B.P., and Uriarte, G.G, 1993, Pengantar Metode Penelitian, diterjemahkan oleh Tuwu, A., Edisi I, 163, UI Press, Jakarta.
Skoog, D.A., West, D.M., and Holler, F.J., 1994, Analytical Chemistry: An Introduction, 6
th
Ed., 490,494, Harcourt Brace College, Philadelphia.
Snyder, L.R., Kirkland, J.J., and Glajch, J.L., 1997, Practical HPLC Method Development, 2
nd
Soerjodibroto, Waluyo, 2002, Menyimak kandungan soft drink,
http://www.kompas.com/health/news/0202/26051556.html, diakses tanggal 6 Januari 2010.
Sudarmadji, S, 1982, Bahan – Bahan Pemanis, Agritec, Yogyakarta.
Sudarmaji, S., Haryono, B., dan Suhardi, 1996, Analisa untuk Bahan Makanan dan Pertanian, 14-19, Penerbit Liberty, Yogyakarta.
Tambunan, K.C, 2008, Aspartam Racun Manis yang Mematikan,
http://www.wikimu.com/News/DisplayNews.aspx?id=6205&post=1, diakses tanggal 6 Maret 2010.
Winarno, F.G, 1992, Kimia Pangan dan Gizi, PT Gramedia Pustaka Utama. Jakarta.
Lampiran 1. Penimbangan Sampel (Minuman Serbuk Beraroma)
Penimbangan sampel menggunakan teknik weighing by difference:
Sampel I
Kertas : 0,1299 g
Kertas + zat : 0,8163 g Kertas + sisa : 0,1299 g
Zat : 0,6864 g
Sampel II
Kertas : 0,1299 g
Kertas + zat : 0,8175 g Kertas + sisa : 0,1304 g
Zat : 0,6871 g
Sampel III
Kertas : 0,1341 g
Kertas + zat : 0,8219 g Kertas + sisa : 0,1341 g
Zat : 0,6878 g
Sampel IV
Kertas : 0,1300 g
Kertas + zat : 0,8168 g Kertas + sisa : 0,1303 g
Zat : 0,6863 g
Sampel V
Kertas : 0,1324 g
Kertas + zat : 0,8198 g Kertas + sisa : 0,1328 g
43
Sampel VI
Kertas : 0,1357 g
Kertas + zat : 0,8281 g Kertas + sisa : 0,1362 g
Zat : 0,6919 g
Sampel VII
Kertas : 0,1312 g
Kertas + zat : 0,8175 g Kertas + sisa : 0,1315 g
Lampiran 2. Contoh perhitungan kadar aspartam dalam sampel
Perhitungan kadar aspartam
Timbang 0,686 g sampel/ 10,0 mL fase gerak
Pipet 2,0 mL/ 10,0 mL fase gerak
Saring denganMillipore, didegassingselama 15 menit
injek ke sistem KCKT 40 µL Luas area
Aspartam
y = 1,0088x + 0,4624
Sampel I, Replikasi 1
y = 1,0088x + 0,4624 336385 = 1,0088x + 0,4624 x = 2,8762 mg/ 100mL
= 0,2876 mg/10mL = 0,2876 mg/2mL = 0,2876 x mg/10mL = 1,438 mg/10mL
Kadar aspartam dalam sampel = xbobot sampel rata-rata
= x 10,05 g/sachet
= 0,0211 g/sachet
= 21,1 g/sachet
45
Lampiran 3. Hasil penetapan kadar aspartam dalam sampel
Replikasi Sampel I
AUC Kadar aspartam dalam sampel (mg/sachet)
Kadar rata-rata aspartam dalam sampel
(mg/sachet)
1 336385 21,1
2 340717 21,4 21,25
Replikasi
2 363220 23,0 23,00
Replikasi
Lampiran 4. Perhitungan nilairecovery, kesalahan acak, dan kesalahan
sistemik aspartam
1. Recovery
Diketahui : Kadar teoritis = 2,00 mg/ 100mL Kadar terukur = 1,99 mg/ 100mL
Recovery= .100%
Kesalahan sistemik = 100% – %recovery
= 100% – 99,5% = 0,5 %
3. Kesalahan acak
47
Lampiran 5. Kromatogram Sampel
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
49
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
51
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
53
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
55
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
57
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
59
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
Instrumen: VarianShimadzuLC-10 AD
Fase diam:Kromasil100-5 C18250 x 4,6 mm ukuran partikel 5 µm
Fase gerak: 12,5 mM KH2PO4pH 4 : asetonitril (80:20)
61
63
65
Lampiran 8. Komposisi sampel minuman serbuk merek “X”
BIOGRAFI PENULIS