BAB 2
TINJAUAN PUSTAKA
2.1. Talas (Colocasia esculenta)
Talas (Colocasia esculenta) merupakan tanaman pangan yang termasuk jenis herba menahun. Talas memiliki berbagai nama umum di seluruh dunia, yaitu Taro, Old cocoyam, Abalong, Taioba, Arvi, Keladi, Satoimo, Tayoba, dan Yu-Tao serta Sukat dalam bahasa Karo. Tanaman ini diklasifikasikan sebagai tumbuhan berbiji (Spermatophyta) dengan biji tertutup (Angiospermae) dan berkeping satu (Monocotyledonae). Taksonomi tumbuhan talas secara lengkap adalah sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Monocotyledone Ordo : Arales
Famili : Araceae Genus : Colocasia
Penelitian tentang pati talas maupun tepung talas di Indonesia masih terbatas, misalnya Widowati, dkk (1997) tentang pengaruh NaCl dan konsentrasi NaCO3 pada ekstraksi serta
karakterisasi beberapa varietas talas (Colocasia esculenta L. Schott). Kadar pati pada talas adalah sekitar 80% dengan kadar amilopektin dan amilosa adalah masing-masing 74,45% dan 5,55%. (Rahmawaty, et al.,2012). Kandungan kimia dari talas dapat dilihat pada Tabel 2.1.
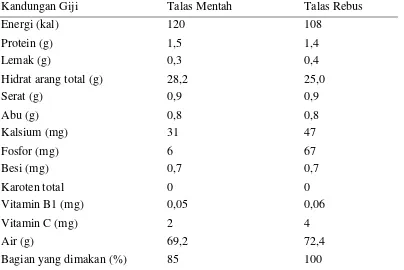
Tabel 2.1 Kandungan Talas
Kandungan Giji Talas Mentah Talas Rebus
Energi (kal) 120 108
Protein (g) 1,5 1,4
Lemak (g) 0,3 0,4
Hidrat arang total (g) 28,2 25,0
Serat (g) 0,9 0,9
Abu (g) 0,8 0,8
Kalsium (mg) 31 47
Fosfor (mg) 6 67
Besi (mg) 0,7 0,7
Karoten total 0 0
Vitamin B1 (mg) 0,05 0,06
Vitamin C (mg) 2 4
Air (g) 69,2 72,4
Bagian yang dimakan (%) 85 100
Sumber: Slamet D.S. dan Ig. Tarkotjo (1980), Majalah Gii dan Makanan.Jilid 4.Hal 26. Pusat Penelitian dan Pengembangan Kesehatan Depkes RI
Talas merupakan tanaman sekulen yaitu tanaman yang umbinya banyak mengandung air.Umbi tersebut terdiri dari umbi primer dan umbi sekunder.Kedua umbi tersebut berada dibawah permukaan tanah. Hal yang membedakannya adalah umbi primer merupakan umbi induk yang memiliki bentuk silinder dengan panjang 30 cm dan diameter 15 cm, sedangkan umbi sekunder merupakan umbi yang tumbuh di sekitar umbi primer dengan ukuran lebih kecil. Umbi sekunder ini digunakan oleh talas untuk melakukan perkembangbiakannya secara vegetative (Koswara, 2010).
Umbi talas memiliki berbagai macam bentuk yang sangat tergantung dengan lingkungan tempat tumbuh serta varietasnya. Minantyorini dan Hanari(2002) melakukan identifikasi dan melakukan klasifikasi terhadap plasma nutfah berbagai jenis talas. Hasilnya dapat dilihat pada Gambar 2.1 yang menunjukkan berbagai macam bentuk dari umbi talas, mulai dari yang kerucut (1), membulat (2), silindris (3), elips (4), halter (5), memanjang (6), datar dan bermuka banyak (7), dan tandan (8). Umumnya talas yang tersebar di Indonesia memiliki bentuk kerucut, silindris, atau elips, dengan sebagian kecil daerah memproduksi talas dengan bentuk umbi membulat, halter, memanjang, dan tandan. Untuk bentuk umbi datar dan bermuka banyak, hingga kini belum ada ditemui di Indonesia.
2.2. Asam Sitrat
Asam sitrat merupakan asam organik lemah yang ditemukan pada daun dan buah tumbuhan genus Citrus (jeruk-jerukan). Rumus molekul asam sitrat adalah C6H8O7 dengan nama IUPAC
asam 2-hidroksi-1,2,3-propamatrikarboksilat. Titik lebur dari asam sitrat yaitu 1530C (426 K).Senyawa ini merupakan bahan pengawet yang baik dan alami, selain digunakan sebagai penambah rasa masam pada makanan dan minuman ringan.Dalam biokimia, asam sitrat dikenal sebagai senyawa antara dalam siklus asam sitrat yang terjadi di dalam mitokondria, yang penting dalam metabolism makhluk hidup.Zat ini juga dapat digunakan sebagi zat pembersih yang ramah lingkungan dan sebagai antioksidan.
Keasaman asam sitrat didapatkan dari tiga gugus karboksil COOH yang dapat melepas proton dalam larutan.Jika hal ini terjadi, ion yang dihasilkan adalah ion sitrat.Sitrat sangat baik digunakan dalam larutan penyangga untuk mengendalikan pH larutan.Ion sitrat dapat beraksi dengan banyak ion logam membentuk garam sitrat.Selain itu, sitrat dapat mengikat ion-ion logam dengan pengkelatan, sehingga digunakan sebagai pengawet dan penghilang kesadahan air.
Pada temperatur kamar, asam sitrat berbentuk serbuk kristal berwarna putih. Serbuk kristal tersebut dapat berupa bentuk anhidrus (bebas air), atau bentuk monohidrat yang mengandung satu molekul air untuk setiap molekul asam sitrat. Bentuk anhidrus asam sitrat mengkristal dalam air panas, sedangkan bentuk monohidrat didapatkan dari kristalisasi asam sitrat dalam air dingin. Bentuk monohidrat tersebut dapat diubah menjadi bentuk anhidrus melalui pemanasan di atas 740C.
Secara kimia, asam sitrat bersifat seperti asam karboksilat lainnya. Jika dipanaskan diatas 1750C, asam sitrat terurai dengan melepaskan karbon dioksida dan air (id.wikipedia.org). Struktur asam sitrat dapat dilihat pada Gambar 2.2.
H2C
C
COOH
HO COOH
H2C COOH
2.3. Pati
Pati merupakan sumber pangan dan mengandung karbohidrat yang terdapat pada tumbuh-tumbuhan. Pati memiliki rumus umum (C6H10O5)n, dimana n lebih dari 1000 (Egan,1981). Pati
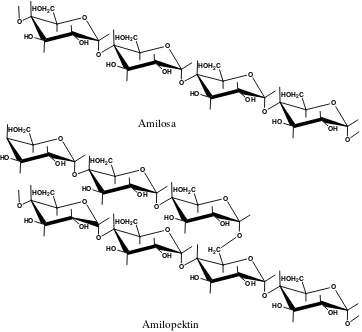
terdiri atas dua macam polisakarida yang kedua-duanya adalah polimer dari glukosa, yaitu amilosa (kira-kira 20-28 %) dan amilopektin (kira-kira 80-72%). Amilosa terdiri atas 250-300 unit D-glukosa yang terikat dengan ikatanα 1,4-glikosidik. Amilopektin juga terdiri atas molekul D-glukosa yang mempunyai ikatan disamping 1,4-glikosidik, juga percabangannya pada ikatan 1,6-glikosidik. Molekul amilopektin lebih besar daripada molekul amilosa karena terdiri atas lebih dari 1000 unit glukosa. Butir-butir pati tidak larut dalam air dingin tetapi apabila air dipanaskan, akan membentuk gel (gelatinisasi). Larutan patiapabila diberi larutan iodium akan berwarna biru. Amilopektin dengan iodium akan memberikan warna ungu atau merah lembayung (Poedjiadi,1994).
O
Gambar 2.3. Struktur Dari Amilosa dan Amilopektin ( Miller, 1980)
Glikogen adalah polisakarida yang digunakan sebagai tempat penyimpanan glukosa dalam sistem hewan (terutama dalam hati dan otot). Dari segi struktur, glikogen mirip amilopektin. Glikogen mengandung rantai glukosa yang terikat-1,4’- dengan percabangan-percabangan (1,6’-). Beda antara glikogen dan amilopektin adalah bahwa glikogen lebih bercabang daripada amilopektin (Fessenden,1982).
Pati yang telah mengalami gelatinasi dapat dikeringkan, tetapi molekul molekul tersebut tidak dapat kembali lagi ke sifat-sifatnya sebelum gelatinasi. Bahan yang telah kering tersebut masih mampu menyerap air dalam jumlah yang besar.Suhu gelatinasi tergantung juga pada konsentrasi pati.Makin kental larutan, suhu tersebut makin lambat tercapai, sampai suhu tertentu kekentalan tidak bertambah, bahkan kadang-kadang turun.Suhu gelatinasi berbeda-beda bagi tiap jenis pati dan merupakan suatu kisaran. Dengan viskosimeter suhu gelatinasi dapat ditentukan, misalnya pada jagung 62-70 0C, beras 68-78 0C, gandum 54,5- 64 0C (Winarno, 1980).
Selulosa merupakan polisakarida pembangun yang paling penting. Bahan ini menyusun dinding sel tumbuhan, terutama kayu. Kapas terdiri dari 80% selulosa murni. Seperti halnya amilosa, selulosa adalah polimer linear yang terdiri dari unit D-glukosa. Semua unit D-glukosa ini, berkisar dari 300 sampai 15000, dihubungkan oleh ikatan ß-(1,4), bukan alfa. Betapa besarnya perbedaan dari selisih yang kecil ini. Pertama, bentuk molekul selosa dan amilosa berbeda karena ikatan -(1,4) pada amilosa cenderung membentuk struktur spiral yang longgar, sedangkan ikatan ß-(1,4) pada selulosa cenderung membentuk rantai lurus.
2.4. Modifikasi Pati
Pati termodifikasi atau lebih dikenal dengan turunan pati dapat diproduksi dengan beberapa metode yaitu, metode fisikawi, kimiawi dan enzimatis yang pada dasarnya untuk mengubah sifat alami dari pati. Pati termodifikasi berguna di berbagai bidang, misalnya di bidang produksi makanan, yaitu sebagi agen pengisi, stabilizer dan emulsifier; di bidang farmasi, yaitu sebagai desintegrants dan carrier; dan aditif pengikat pada pelapis kertas (Gotlieb, et al. 2005).
Pati adalah sebuah senyawa alamiah, biodegradable murah dan mudah diperoleh.Tersebar luas dalam batang, akar, dan buah dari tumbuhan berdaun hijau. Terdapat unit glukosa (C6H10O5)n dengan n diantara 300 sampai 1000. Pati terbentuk dari 2 campuran dari 2 polimer
yang disebut dengan amilosa dan amilopektin. Amilosa adalah sebuah polimer linier dengan berat molekul kurang dari 0,5 juta Dalton (derajat polimerisasi dari 15 x 102 – 6 x 103)
bergantung pada sumber botaninya. Makromolekul amilosa merupakan dari α-D-glukopiranosa
yang tergantung d ari ik atan α-1,4 asetal. Makromolekul amilopektin lebih besar dan banyak bercabang dengan berat molekul sekitar 50-100 juta Dalton dan derajat polimerisasi sekitar 3 x 105 – 3 x 106 (Neelam, et al. 2012). Beberapa metode dalam modifikasi pati yaitu:
2.4.1. Metode Fisika
2.4.2. Metode Kimia
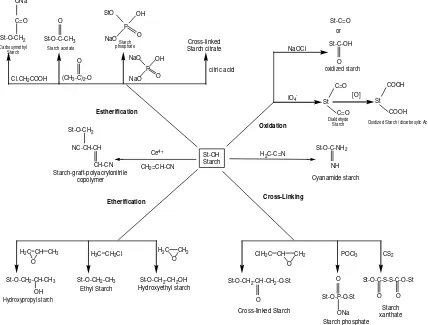
Metode kimia melibatkan gugus fungsi awal pada molekul pati, menghasilkan perubahan secara nyata sifat fisiko-kimianya. Contoh dari teknik ini yaitu, eterifikasi, esterifikasi, ikat silang, penambahan asam, oksidasi dan dwi modifikasi (Neelam, et al. 2012). Beberapa modifikasi secara kimia menggunakan berbagai pereaksi seperti pada gambar 2.4.
2.4.3. Metode Enzimatis
Metode ini meliputi tentang suspensi pati menjadi sejumlah dari enzim-enzim utam termasuk hidrolisis enzim yang cenderung untuk menghasilkan turunan fungsional yang besar.Beberapa enzim yang telah diteliti yaitu, amilomaltase, siklomaltodekstrinase, siklomaltodekstrin dan glukanosiltransferase (Neelam, et al. 2012).
St-OH
Starch Oxidized Starch (dicarboxylic Acid) Carboxymethyl
Starch Starch acetate
Starch
phosphate Starch citrateCross-linked
citric acid
Starch-graft-polyacrylonitrile
copolymer Cyanamide starch
Hydroxypropyl starch
Ethyl Starch Hydroxyethyl starch
Cross-linked Starch
2.4.4. Metode Modifikasi Genetika
Teknik – teknik pada metode ini meliputi teknologi transgenik bahwa target enzim yang terlibat dalam biosintesis pati demikian hakikat dari keuntungan dari bahaya kimia lingkungan paska panen dan modifikasi enzimatis. Beberapa metode yang telah diteliti yaitu pati bebas amilosa, pati tinggi amilosa dan altered amilopektin structure (Neelam, et al. 2012).
2.5. Pati Sitrat
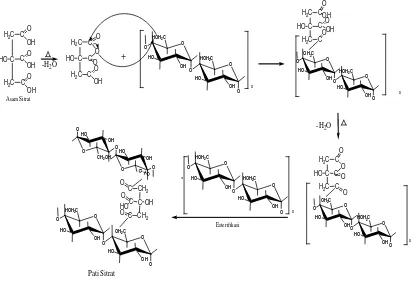
Pati sitrat dapat disintesis dengan cara esterifikasi gugus karboksil bebas dari monomer anhidroglukosa dari pati dengan asam sitrat. Asam sitrat memiliki 3 gugus karboksilat yang dapat menghubungkan gugus karboksil dari asam sitrat dengan gugus hidroksil dari pati dengan hasil samping H2O dan membentuk reaksi ikat silang dengan asam sitrat sebagai agen pengikat
silang. Interaksi antara asam sitrat dengan pati dapat meningkatkan pertahanan terhadap air dengan cara mengurangi gugus hidroksil dari pati (Borredon, et al., 1997). Gugus karboksilat dari asam sitrat dapat membentuk ikatan kuat dengan gugus hidroksil dari pati, sehingga mencegah rekristalisasi dan retrogradasi.Asam sitrat tidak beracun sehingga tidak berbahaya bila masuk dalam tubuh (metabolism asam sitrat atau siklus Krebs) (Yang, et al., 2004).
H2C 2.5 Skema Reaksi dari Asam Sitrat dengan Pati (Chowdary, 2011)
2.6. Esterifikasi
Esterifikasi adalah suatu reaksi ionik yang merupakan gabungan dari reaksi adisi dan reaksi penataan ulang dieliminasi (Davidek, 1990).Esterifikasi juga dapat didefenisikan sebagai reaksi antara asam karboksilat dan alkohol (Gandhi,1997).Esterifikasi dapat dilakukan dengan menggunakan katalis enzim (lipase) dan asam anorganik (asam sulfat dan asam klorida), dengan berbagai variasi alkohol biasanya metanol, etanol, 1-propanol, 1-butanol, amyl alkohol, dan lain-lain (Ozgulsun, 2008). Asam anorganik yang digunakan sebagai katalis akanmenyebabkan asam karboksilat mengalami konjugasi sehingga asam konjugat dari asam karboksilat tersebutlah yang akan berperan sebagai substrat.
secara berlebih.Pertambahan hasil juga dipengaruhi oleh dehidrasi yang artinya menarik air terbentuk sebagai hasil samping reaksi. Air dapat dipisahkan dengan cara menambahkan pelarut yang bersifat non polar seperti misalnya benzene dan kloroform sehingga air yang terbentuk akan segera terikat pada pelarut yang digunakan atau dengan menambahkan molecular sieves (Yan, 2001).
Esterifikasi asam karboksilat dengan asam alkohol merupakan reaksi reversible.Bila asam karboksilat diesterkan, digunakan alkohol berlebih.Untuk membuat reaksi kebalikannya, yakni hidrolisis berkataliskan asam dari ester menjadi asam karboksilat digunakan air secara berlebihan. Kelebihan air akan menggeser kesetimbangan ke arah sisi asam karboksilat (Fessenden, 1982). Salah satu reaksi esterifikasi dapat dilihat pada Gambar 2.6.
RCOH R'OH RCOR' H2O
O O
+
H+, Kalor
+
Suatu Asam
Karboksilat Suatu alkohol
Suatu Ester
Gambar 2.6.Reaksi esterifikasi secara umum (Fessenden, 1982)
2.7. Modifikasi Pati Ikat Silang (Cross-lingking)
Seperti pada umumnya pati yang dipakai dalam industri ditentukan oleh sifat rheologi dari pasta pati yang dihasilkan dari pati tersebut seperti viskositas, kekuatan gel, kejernihan, dan kestabilan rheologi.Pada pemanasan suspensi pati maka ikatan primer yang menyusun molekul dalam suatu struktur yang kompak akan pecah karena terjadinya hidrasi granula mengisap air dan mengembang, sebagian granula akan mengembang pada suhu yang sangat terbatas, pengembangan terjadi pada dua tingkat yaitu setelah gelatinasi dan pendinginan (Koswara, 2009).
Maxwell (1976) mencoba mengembangkan reaksi cross-lingking untuk menghambat pengembangan pati dengan tujuan stabilitas viskositas pengembangan pati dengan tujuan untuk stabilitas viskositas pasta pati. “Cross-linking” dipakai apabila dibutuhkan pati dengan viskositas tinggi atau pati dengan ketahanan geser yang baik seperti dalam pembuatan pasta dengan pemasakan kontinu dan pemasakan cepat pada injeksi uap.
Berjenis cross-link agent telah banyak digunaka seperti epiklorhidrin, tri-meta fosfat diman keduanya sering dipakai untuk pembuatan makanan dan juga industri pati. Cross-link agent lain yang biasa dipakai dalam industri adalah aldehid, dialdehid, vynil sulfon, di-epoksida, dan lain-lain.Beberapa resin formaldehida urea juga dipakai untuk cross-linking agent untuk beberapa aplikasi. Bila pati ikatan silang dibuat pada air dingin misalnya dengan drum-drying maka kurang terjadi kerusakan granula dan dapat dipergunakan cross-linking yang tidak aktif seperti senyawa alifatik dengan dua atau tiga gugus fungsionil misalnya di-halida. Secara umum beberapa molekul dapat bereaksi dengan dua atau lebih gugus hidroksil disebut cross-linking agent molekul ini dapat dipilih sesuai dengan bentuk produk akhir yang diinginkan.Derajat pengembangan pati cross-linking menunjukkan ciri yang linier tergantung pada perbandingan molar. Proses cross-linking akan efisien bila epiklorohidrina diberikan pada fase uap untuk membentuk film tipis pada pasta atau pati kering. Proses ini dilakukan oleh hofseiter untuk tekstil (Whistler, 1984).
sodium trimetafosfat, sodium tripolifosfat, epiklorohidrin, dan 1,2,3,4-diepoksibutana digunakan untuk memperbaiki sifat mekanin dan stabilitas air dari produk pati (Hirsc et al, 2002).
2.8. Swelling Power
Swelling power dipengaruhi oleh kemampuan molekul pati untuk mengikat air melalui pembentukan ikatan hydrogen.Setelah gelatinisasi iktatan hidrogen antara molekul pati terputus dan digantikan oleh ikatan hidrogen dengan air.Sehingga pati dalam tergelatinisasi dan granula-granula pati yang mengembang secara maksimal. Proses mengembangnya granula-granula pati ini disebabkan banyaknya air yang terserap kedalam tiap granula pati dan granula pati yang mengembang tersebut mengakibatkan swelling power menjadi meningkat (Herawati, 2010).