BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan 2.1.1 Habitat
Tumbuhan jintan hitam (Nigella sativa L.) merupakan salah satu
spesies dari genus Nigella yang memiliki kurang lebih 14 spesies tanaman
yang termasuk dalam famili Ranunculaceae (Widyaningrum, 2012). Jintan
hitam juga dikenal dengan nama daerah jinten hitam pahit, sedangkan nama
asingnya black cumin (Inggris), habbatussauda (Arab), kalonji (India)
(Mahendra, 2008).
2.1.2 Morfologi
Tanaman jintan hitam merupakan tanaman semak belukar dengan
ketinggian 50 cm. Tanaman ini memiliki batang tegak dan berusuk, daunnya
berbentuk lanset dan bergaris dengan panjang 1,5 sampai 2 mm. Ujungnya
runcing serta memiliki tiga tulang daun yang berbulu (Rahmi, 2011). Bunga
jintan hitam memiliki lima buah kelopak bunga yang berbentuk bulat telur,
pangkalnya mengecil membentuk sudut yang pendek (Widyaningrum, 2012),
ujungnya agak runcing sampai agak tumpul serta memiliki benang sari yang
tergolong banyak (Depkes, 1979).
Buah jintan hitam berbentuk bulat panjang dan berwarna coklat
kehitaman, biji kecil bersudut tiga sampai empat tidak beraturan, panjangnya
hitam kecoklatan, hitam kelabu sampai hitam, kasar dan berkerut
(Widyaningrum, 2012; Depkes, 1979).
2.1.3 Sistematika tumbuhan
Menurut Widyaningrum (2012) tanaman jintan hitam (Nigella sativa
L.) diklasifikasikan sebagai berikut:
Kingdom : Plantae
Divisio : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Ranunculales
Famili : Ranunculaceae
Genus : Nigella
Spesies : Nigella sativa L.
2.1.3 Kandungan kimia
Kandungan kimia biji Nigella sativa L. adalah saponin, polifenol
(Hutapea, 1994), alkaloida, steroida dan flavonoida (Liu, et al., 2011).
Kandungan kimia lainnya adalah protein, karbohidrat dan asam lemak esensial.
Disamping itu terdiri dari asam linoleat, asam oleat, kalsium, kalium, besi,
seng, magnesium, selenium, natrium, vitamin A, vitamin B1, vitamin B2,
niasin, vitamin C . Argin (untuk pertumbuhan bayi), 15 asam amino termasuk
delapan dari sembilan asam amino utama dan serat (Mahendra, 2008), karoten
yang akan diubah oleh hati menjadi vitamin A yang dikenal berfungsi sebagai
2.2 Uraian Kimia 2.2.1 Alkaloida
Alkaloida adalah suatu golongan senyawa organik yang terbanyak
ditemukan dialam. Hampir seluruh senyawa alkaloida berasal dari
tumbuh-tumbuhan yang tersebar luas dalam berbagai jenis tumbuh-tumbuhan. Semua alkaloida
mengandung paling sedikit satu atom nitrogen yang biasanya bersifat basa dan
pada sebagian besar alkaloid atom nitrogen ini merupakan bagian dari cincin
heterosiklik (Lenny, 2006). Menurut Harborne, alkaloida adalah senyawa
bersifat basa yang mengandung satu atau lebih atom nitrogen yang terletak
dalam sistem siklik. Disamping itu alkaloida dapat didefinisikan sebagai suatu
senyawa yang mengandung nitrogen, bersifat basa, terdapat pada tanaman
dalam jumlah yang relatif kecil dan mempunyai aktivitas farmakologi.
Pengertian ini terlalu luas, karena tidak semua senyawa yang mengandung
nitrogen merupakan alkaloida. Protein, klorofil, asam amino misalnya
bukanlah alkaloida walaupun mengandung nitrogen. Hegnauer memberikan
batasan bahwa alkaloida adalah senyawa bersifat toksik yang bekerja terhadap
sistem syaraf pusat, bersifat basa, mengandung nitrogen heterosiklik, disintesa
dalam tumbuhan dari asam amino atau turunannya dan umumnya tersebar pada
tumbuh-tumbuhan (Farnsworth, 1966).
Klasifikassi alkaloida menurut Hegnauer (Farnsworth, 1966) adalah
1. Alkaloida Sejati
Alkaloida ini dibentuk atau berasal dari asam amino yang umumnya
mempunyai unsur nitrogen yang terikat pada cincin heterosiklik dan
kebanyakan bersifat basa seperti vinkristina dan reserpina, kecuali
kolkisina yang tidak mempunyai cincin heterosiklik dan tidak bersifat basa.
N
Gambar 2.1 Struktur alkaloida vinkristina
N
O
Gambar 2.3 Struktur alkaloida kolkisina
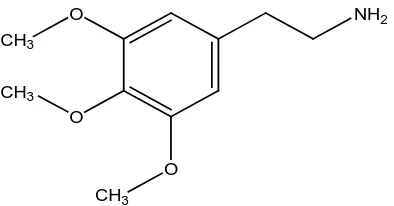
2. Protoalkaloida
Alkaloida ini dibentuk dari asam amino, tetapi unsur nitrogennya tidak
terikat pada cincin heterosiklik dan bersifat basa. Contohnya meskalina dan
3. Pseudoalkaloida
Alkaloid ini merupakan alkaloida bukan turunan asam amino, pada
umumnya mempunyai unsur nitrogen yang terikat pada cincin heterosiklik
dan biasanya bersifat basa. Alkaloida yang penting dari golongan ini adalah
alkaloida golongan purina seperti kafeina.
N
N
N H N
Gambar 2.6 Struktur alkaloida golongan purin
N
N N
N O
O
Gambar 2.7 Struktur alkaloida kafeina
Menurut Evans (2009), pembagian alkaloida berdasarkan letak atom
nitrogen adalah:
A. Non heterosiklik atau atipikal alkaloida, disebut juga protoalkaloida
atau amin biologis misalnya efedrina yang terdapat dalam Ephedra
distachya.
B. Heterosiklik atau tipikal alkaloida yang dibagi kedalam 12 grup
berdasarkan struktur cincinnya, yaitu:
1. Alkaloida golongan pirol dan pirolidina, contohnya higrina pada
H N
Gambar 2.8 Struktur alkaloida golongan pirol
H N
Gambar 2.9 Struktur alkaloida golongan pirolidin
N
CH3
H2
C C CH3
O
Gambar 2.10 Struktur alkaloida higrina
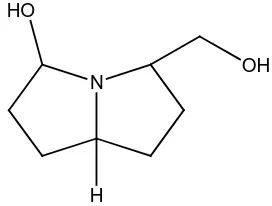
2. Alkaloida golongan pirolizidina, contohnya retronesina pada
Crotalaria retusa.
N
Gambar 2.11 Struktur alkaloida golongan pirolizidina
N HO
OH
H
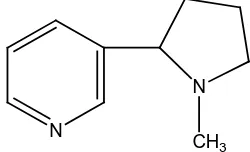
3. Alkaloida golongan piridina dan piperidina, contohnya nikotin
pada tumbuhan Nicotiana tabaccum dan koniin pada tumbuhan
Conium maculatum. N
Gambar 2.13 Struktur alkaloida golongan piridina
N
N
CH3
Gambar 2.14 Struktur alkaloida nikotina
H N
Gambar 2.15 Struktur alkaloida golongan piperidina
N
H CH2
H2 C
CH3
Gambar 2.16 Struktur alkaloida koniin
4. Alkaloida golongan tropan, contohnya atropin pada tumbuhan
Gambar 2.17 Struktur alkaloida tropan
CH3 N OCCH H3C
HO
O
Gambar 2.18 Struktur alkaloida atropin
5. Alkaloida isokuinolina, contohnya papaverina pada tumbuhan
Papaver somniferum.
N
Gambar 2.19 Struktur alkaloida golongan isokuinolina
N H3CO
H3CO
OCH3
OCH3
6. Alkaloida golongan kuinolizidina, contohnya sitisina pada
tumbuhan Cytisus scoparius.
N
Gambar 2.21 Struktur alkaloida golongan kuinolizidina
N H
H NH
O
Gambar 2.22 Struktur alkaloida sitisina
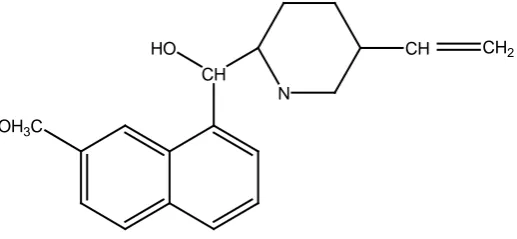
7. Alkaloida golongan kuinolina, contohnya kuinina pada tumbuhan
Cinchona ledgeriana.
N
Gambar 2.23 Struktur alkaloida golongan kuinolina
CH HO
N
CH
OH3C
CH2
8. Alkaloida golongan indol, contohnya reserpina pada tumbuhan
Rauwolfia serpentina.
H N
Gambar 2.25 Struktur alkaloida golongan indol
N H
N
O H3CO
OCH3
OCH3
OCH3 H
COOCH3 H
H
OCH3 O
Gambar 2.26 Struktur alkaloida reserpina
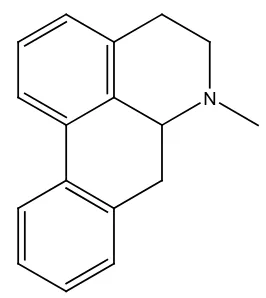
9. Alkaloida golongan aporfina, contohnya morfina pada tumbuhan
Papaver somniferum.
N
10.Alkaloida golongan imidazol, contohnya pilokarpina pada
tumbuhan Pilocarpus jaborandi.
H N
N
Gambar 2.28 Struktur alkaloida golongan imidazol
N
Gambar 2.29 Struktur alkaloida pilokarpina
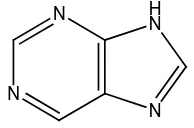
11.Alkaloida golongan purina, contohnya kafeina pada tumbuhan
Coffea arabica.
N
N
N H N
Gambar 2.30 Struktur alkaloida golongan purina
N
N N
N O
O
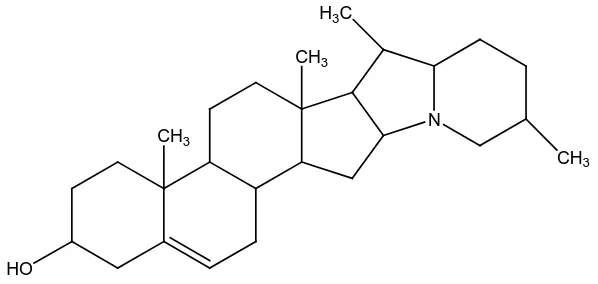
12.Alkaloida golongan steroida, contohnya solanidina pada tumbuhan
Solanum tuberosum.
Gambar 2.32 Struktur alkaloida golongan steroida
N
HO
CH3
CH3 H3C
CH3
Gambar 2.33 Struktur alkaloida solanidina
Fungsi alkaloida dalam tumbuhan belum diketahui secara pasti,
kemungkinan berfungsi sebagai penarik atau penghalau serangga, ataupun
dapat bersifat sebagai zat pengatur tumbuh. Namun dari hasil pengamatan
ternyata sebagian besar tumbuhan dapat melangsungkan kehidupan tanpa
melibatkan alkaloida. Hal ini menunjukkan bahwa alkaloida dalam tumbuhan
tidak begitu penting peranannya dan belum dapat dimengerti jelas (Harborne,
Alkaloida yang telah diisolasi berbentuk kristal dengan titik lebur
tertentu. Beberapa diantaranya berbentuk amorf dan sebagian kecil berbentuk
cair seperti nikotina dan koniina. Kebanyakan alkaloida tidak berwarna, tetapi
alkaloida yang berstruktur kompleks dan mempunyai ikatan rangkap
terkonjugasi kebanyakan berwarna, misalnya: berberina berwarna kuning,
betanina berwarna merah. Alkaloida dalam bentuk basa bebas umumnya larut
dalam pelarut organik (Cordell, 1981).
Sifat alkaloida yang paling umum adalah basa lemah, kebasaan dari
alkaloida ini bergantung pada ketersediaan pasangan elektron sunyi dari
nitrogen (Cordell, 1981). Bila gugus fungsi yang berdekatan dengan nitrogen
bersifat sebagai penolak elektron, seperti gugus alkali, maka ketersediaan
elektron disekitar nitrogen akan bertambah, mengakibatkan alkaloida bersifat
lebih basa. Sebaliknya bila gugus fungsi yang melekat pada nitrogen bersifat
sebagai penarik elektron, seperti gugus karbonil maka ketersediaan elektron
disekitar nitrogen akan berkurang, mengakibatkan alkaloida bersifat netral
bahkan sedikit bersifat asam (Lenny, 2006).
Sifat kebasaan alkaloida sangat berpengaruh terhadap kestabilannya.
Alkaloida dapat terurai oleh pengaruh oksigen, panas dan cahaya. Penguraian
alkaloida selama atau setelah isolasi dapat menjadi masalah yang serius jika
disimpan dalam waktu lama. Pembentukan garam dengan asam organik seperti
tartrat, sitrat atau asam anorganik seperti asam klorida, asam sulfat dapat
2.2.2 Glikosida
Glikosida adalah senyawa organik yang bila dihidrolisis menghasilkan
satu atau lebih gula yang disebut glikon dan bagian bukan gula yang disebut
aglikon. Gula yang paling sering dijumpai dalam glikosida adalah glukosa.
Glikosida dihidrolisis dengan cara pendidihan dalam asam encer. Secara kimia
dan fisiologi, glikosida alam cendrung dibedakan berdasarkan bagian
aglikonnya (Robinson, 1995).
Berdasarkan hubungan ikatan antara glikon dan aglikonnya, glikosida
dapat dibagi menjadi empat (Farnsworth, 1966) yaitu:
1. O-glikosida, jika ikatan antara glikon dengan aglikon dihubungkan oleh
atom O, contohnya: salisin
CH2OH
O
C6H11O5
Gambar 2.34 Struktur salisin
2. S-glikosida, jika ikatan antara glikon dengan aglikon dihubungkan oleh
atom S, contohnya: sinigrin
CHCH2C
CH
2NOSO
3K
C
6H
11O
5S
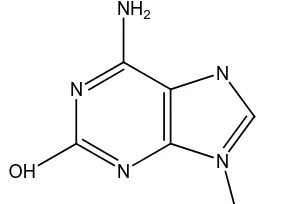
3. N-glikosida, jika ikatan antara glikon dengan aglikon dihubungkan oleh
atom N, contohnya: krotonosida
N N
N N NH2
OH
C5H9O4
Gambar 2.36 Struktur kronotosida
4. C-glikosida, jika ikatan antara glikon dengan aglikon dihubungkan oleh
atom C, contohnya: barbaloin
OH
H C6H11O5
CH2OH
OH O
Gambar 2.37 Struktur barbaloin
2.2.3 Saponin
Saponin merupakan senyawa aktif permukaan yang kuat, dapat
menimbulkan busa jika dikocok dalam air, pada konsentrasi rendah sering
menyebabkan hemolisis sel darah merah (Robinson, 1995). Uji saponin yang
sederhana ialah dengan mengocok ekstrak alkohol air dari tumbuhan dalam
tabung reaksi, maka akan terbentuk busa yang bertahan lama pada permukaan
berdasarkan kemampuannya menghemolisis sel darah dan memberikan reaksi
warna yang karakteristik pada uji Liebermann-Burchard (Farnsworth, 1966).
Berdasarkan bagian glikonnya dikenal dua jenis saponin, yaitu saponin
steroida dan saponin triterpenoida (Farnsworth, 1966).
O O
HO
CH3
CH3
H3C
CH3
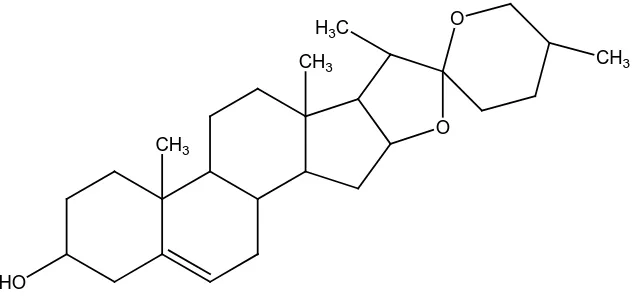
Gambar 2.38 Struktur sapogenin steroida
HO
COOH
Gambar 2.39 Struktur sapogenin triterpenoida
2.2.4 Triterpenoida/steroida
Triterpenoida adalah senyawa yang kerangka karbonnya berasal dari
enam satuan isopren dan secara biosintesis dibuat dari senyawa
Gambar 2.40 Struktur skualena
Steroida merupakan triterpen yang mempunyai inti siklopentano
perhidrofenantren (Harborne, 1987). Inti steroida dasar sama dengan inti
kolesterol, tetapi pada posisi 10 dan 13 terdapat gugus metal yang terikat pada
sistem cincin. Pada umumnya steroida tumbuhan berupa alkohol dengan gugus
hidroksil pada C3 sehingga steroida sering juga disebut sterol (Robinson,
1995).
2.2.5 Flavonoida
Flavonoida merupakan salah satu metabolit sekunder. Keberadaannya
dalam daun kemungkinan dipengaruhi oleh adanya proses fotosintesis sehingga
daun muda belum terlalu banyak mengandung flavonoida (Markham, 1988).
Senyawa flavonoida mempunyai struktur C6-C3-C6. Tiap bagian C6
merupakan cincin benzena yang dihubungkan oleh atom C3 yang merupakan
rantai alifatik (Sastrohamidjojo, 1996; Markham, 1988).
Flavonoida umumnya terdapat dalam tumbuhan terikat pada gula
sebagai glikosida. Flavonoida terdapat dalam bentuk bebas maupun terikat
sebagai glikosida. Glikosidanya larut dalam air dan etanol tapi tidak larut
dalam pelarut organik, sedangkan geninnya (aglikon) tidak larut dalam air
tetapi larut dalam pelarut-pelarut organik.
Klasifikasi flavonoida dalam tumbuhan berdasarkan sifat kelarutannya
dan reaksi-reaksi warnanya, kemudian dilanjutkan dengan kromatografi kertas
satu dimensi dari ekstrak terhidrolisis dan dua dimensi dari ekstrak alkohol
langsung. Kerangka dan skema pemberian nomor dan tipe-tipe flavonoiida
adalah sebagai berikut:
O
O
OH
Gambar 2.43 Struktur flavonoida golongan flavonol
O
O
Gambar 2.44 Struktur flavonoida golongan isoflavon
O
O
Gambar 2.45 Struktur flavonoida golongan flavonon
O
O
OH
O
O
CH
Gambar 2.47 Struktur flavonoida golongan auron
O
Gambar 2.48 Struktur flavonoida golongan khalkon
O
OH OH
OH
OH HO
Gambar 2.49 Struktur flavonoida golongan katekin
O
HO OH
OH
O+
OH
Gambar 2.51 Struktur flavonoida golongan antosianidin
2.2.6 Tanin
Tanin terdapat luas pada tumbuhan berpembuluh, dalam Angiospermae
terdapat khusus di jaringan kayu. Tanin dapat bereaksi dengan protein
membentuk kopolimer mantap yang tidak larut dalam air. Dalam industri, tanin
adalah senyawa yang berasal dari tumbuhan, yang mampu mengubah kulit
hewan yang mentah menjadi kulit siap pakai karena kemampuannya
menyambung silang protein (Harbone, 1987).
Secara kimia terdapat dua jenis utama tanin (Harborne, 1987) yaitu :
1. Tanin terkondensasi
Tanin terkondensasi terbentuk dengan cara kondensasi katekin tunggal
(galokatekin) yang membentuk senyawa dimer dan oligomer yang lebih
tinggi. Ikatan karbon-karbon menghubungkan satu satuan flavon dengan
satuan berikutnya melalui ikatan 4-8 atau 6-8. Kebanyakan flavolan
mempunyai 2-20 satuan flavon. Tanin terkondensasi disebut juga dengan
proantosianidin karena bila direaksikan dengan asam panas, beberapa ikatan
karbon-karbon penghubung satuan terputus dan dibebaskanlah monomer
antosianidin.
2. Tanin terhidrolisis
a. Depsida galoil glukosa
Pada senyawa ini, inti yang berupa glukosa dikelilingi oleh lima gugus
ester galoil atau lebih.
b. Dimer asam galat
Inti molekul berupa senyawa dimer asam galat, yaitu asam
heksahidroksidifenat yang berikatan dengan glukosa. Tanin terhidrolisis
disebut juga elagitanin yang pada hidrolisis menghasilkan asam galat.
2.3 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak larut dengan pelarut cair. Senyawa
aktif yang terdapat dalam berbagai simplisia dapat digolongkann ke dalam
golongan minyak atsiri, alkaloida, flavonoida dan lain-lain. Dengan
diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah
pemilihan pelarut dan cara ekstraksi yang tepat (Depkes, 2000).
Metode ekstraksi dengan menggunakan pelarut ada beberapa cara, yaitu
(Depkes, 2000):
1. Cara dingin
a. Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan
menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan
adanya perbedaan konsentrasi antara larutan zat aktif di dalam dan diluar
sel maka larutan terpekat didesak keluar. Proses ini berulang sehingga
terjadi keseimbangan konsentrasi antara larutan di dalam dan di luar sel.
Maserasi digunakan untuk penyarian simplisia yang mengandung
zat aktif yang mudah larut dalam cairan penyari. Cairan penyari yang
digunakan dapat berupa air, etanol, metanol, etanol-air atau pelarut lainnya.
Maserasi berarti dilakukan pengulangan penambahan pelarut setelah
dilakukan penyaringan maserat pertama, dan seterusnya. Keuntungan cara
penyarian dengan maserasi adalah cara pengerjaan dan peralatan yang
digunakan sederhana dan mudah diusahakan.
b. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna pada suhu kamar. Proses perkolasi terdiri tahapan pengembangan
bahan, tahap maserasi antara, tahap perkolasi sebenarnya, terus menerus
sampai diperoleh ekstrak (perkolat) yang jumlahnya 1-5 kali bahan.
2. Cara panas
a. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur yang
mencapai titik didihnya, selama waktu tertentu dan jumlah pelarut yang
relatif konstan dengan adanya pendingin balik.
b. Sokletasi
Sokletasi adalah ekstraksi dengan menggunakan pelarut yang selalu
ekstraksi berulang-ulang dan jumlah pelarut yang relatif konstan dengan
adanya pendingin balik.
c. Digesti
Digesti adalah maserasi dengan pengadukan yang berulang-ulang
pada temperatur yang lebih tinggi dari temperatur ruangan, yaitu secara
umum dilakukan pada temperatur 40-50°C.
d. Infundasi
Infundasi adalah ekstraksi dengan pelarut air, dilakukan pada suhu
96-98°C selama 15 - 20 menit.
e. Dekoktasi
Dekoktasi adalah infus pada waktu yang lebih lama dan temperatur
sampai titik didih air.
2.4 Kromatografi
Kromatografi adalah suatu metode pemisahan berdasarkan proses
migrasi dari komponen-komponen senyawa diantara dua fase, yaitu fase diam
dan fase gerak. Fase gerak membawa zat terlarut melalui media sehingga
terpisah dari zat terlarut lainnya yang terelusi lebih awal atau lebih akhir.
Umumnya zat terlarut dibawa melewati media pemisah oleh aliran suatu
pelarut berbentuk cairan atau gas yang disebut eluen. Fase diam dapat
bertindak melarutkan zat terlarut sehingga terjadi partisi antara fase diam dan
Cara-cara kromatografi dapat digolongkan sesuai dengan sifat-sifat dari
fase diam, yang dapat berupa zat padat atau zat cair. Jika fase diam berupa zat
padat disebut kromatografi serapan; jika berupa zat cair disebut kromatografi
partisi. Karena fase gerak dapat berupa zat cair atau gas maka terdapat empat
macam sistem kromatografi, yaitu:
1. Fase gerak cair-fase diam padat (kromatografi serapan):
− kromatografi lapis tipis
− kromatografi kolom
2. Fase gerak gas-fase diam padat:
− kromatografi gas padat
3. Fase gerak cair-fase diam cair (kromatografi partisi):
− kromatografi kertas
4. Fase gerak gas –fase diam cair:
− kromatografi gas-cair
Pemisahan dengan kromatografi tergantung pada kenyataan bahwa
senyawa-senyawa yang dipisahkan terdistribusi diantara fase gerak dan fase
diam dalam perbandingan yang sangat berbeda-beda dari satu senyawa
terhadap senyawa yang lain (Sastrohamidjojo, 1991).
2.4.1 Kromatografi lapis tipis
Kromatografi lapis tipis termasuk kromatografi adsorpsi (serapan),
dimana sebagai fase diam digunakan zat padat yang disebut adsorben
(penyerap) dan fase gerak adalah zat cair yang disebut dengan larutan
Kromatografi lapis tipis dapat dipakai untuk dua tujuan (Gritter, dkk.,
1991) yaitu:
1. Sebagai metode untuk mencapai hasil kualitatif (analitik) dan kuantitatif
(preparatif).
2. Untuk mencari sistem pelarut yang akan dipakai dalam kromatografi kolom.
Pada kromatografi lapis tipis, fase diam berupa lapisan tipis yang terdiri
atas bahan padat yang dilapiskan pada permukaan penyangga datar yang
terbuat dari kaca atau logam. Lapisan melekat pada permukaan dengan bantuan
bahan pengikat. Beberapa contoh fase diam yang digunakan untuk pemisahan
dalam kromatografi lapis tipis yaitu silika gel, alumina, kieselguhr dan selulosa
(Gritter, dkk., 1991).
Pada kromatografi lapis tipis lapisan fase diam harus sesedikit mungkin
mengandung air, karena air akan menempati semua titik penyerapan sehingga
tidak akan ada senyawa yang melekat. Oleh karena itu, sebelum digunakan plat
kromatografi lapis tipis perlu diaktifkan dengan pemanasan pada 1100C selama
30 menit (Gritter, dkk., 1991; Stahl, 1985)
Fase gerak terdiri dari satu atau beberapa pelarut dan bila diperlukan
dapat menggunakan sistem pelarut multi komponen, berupa suatu campuran
sesederhana mungkin yang terdiri atas maksimum tiga komponen. Pada
pemisahan senyawa organik selalu menggunakan pelarut campuran, tujuannya
untuk memperoleh polaritasnya yang tepat sehingga diperoleh pemisahan
masing-Rf = jarak titik pusat bercak dari titik awal
jarak garis depan fase gerak dari titik awal
masing pelarut sehingga dengan demikian akan diperoleh sistem pengembang
yang cocok (Stahl, 1985).
Jarak pengembangan senyawa pada kromatogram biasanya dinyatakan
dengan harga Rf (Stahl, 1985).
Jarak yang ditempuh oleh tiap bercak dari titik penotolan diukur dari
pusat bercak. Harga Rf berada antara 0,00 – 1,00. Harga Rf ini sangat berguna
untuk mengindentifikasi suatu senyawa (Eaton, 1989).
Faktor-faktor yang mempengaruhi harga Rf adalah sebagai berikut
(Sastrohamidjojo, 1991):
1. Struktur kimia senyawa yang dipisahkan
2. Sifat penyerap
3. Tebal dan kerataan lapisan penyerap
4. Pelarut dan derajat kemurniannya
5. Derajat kejenuhan uap pengembang dalam bejana
6. Teknik percobaan
7. Jumlah cuplikan yang digunakan
8. Suhu
2.4.2 KLT Preparatif
Salah satu metode pemisahan senyawa bahan alam yang memakai
peralatan yang paling dasar ialah kromatografi lapis tipis preparatif. KLT
pemakaian hanya dalam jumlah milligram. Ukuran pelat yang biasa digunakan
yaitu 20 x 20 cm atau 20 x 40 cm. Penjerap yang paling umum ialah silika gel
dan dipakai untuk pemisahan senyawa lipofil maupun campuran senyawa
hidrofil. Cuplikan sampel dilarutkan dalam sedikit pelarut sebelum ditotolkan
pada pelat KLTP dimana konsentrasinya sekitar 5-10%. Penotolan dapat
dilakukan dengan tangan (pipet) ataupun dengan penotol otomatis
(Hostettmann, 1995).
Pilihan pelarut ditentukan berdasarkan pemeriksaan pendahuluan
memakai KLT analitik. Karena ukuran partikel penjerap kira-kira sama, pelarut
yang dipakai pada KLT analitik dapat dipakai langsung pada KLTP.
Kebanyakan penjerap KLTP mengandung indikator fluoresensi yang
membantu mendeteksi kedudukan pita yang terpisah sepanjang senyawa yang
dipisahkan menyerap sinar UV. Untuk senyawa yang tidak menyerap sinar UV,
ada beberapa pilihan :
a. Menyemprot dengan air (misalnya saponin)
b. Menutup pelat dengan sepotong kaca kemudian menyemprot salah satu sisi
dengan pereaksi semprot
c. Menambahkan senyawa pembanding (Hostettmann, 1995).
2.5 Spektrofotometri Sinar Ultraviolet
Spektrofotometer UV pada umumnya digunakan untuk:
2. Menjelaskan informasi dari struktur berdasarkan panjang gelombang
maksimum suatu senyawa.
3. Mampu menganalisis senyawa organic secara kuantitatif dengan
menggunakan hokum Lambert-Beer (Dachriyanus, 2004).
Serapan molekul di dalam daerah ultraviolet bergantung pada struktur
elektronik dari molekul. Apabila suatu molekul menyerap radiasi ultraviolet, di
dalam molekul tersebut terjadi perpindahan tingkat energi elektron-elektron
ikatan pada orbital molekul paling luar dari tingkat energi yang lebih rendah ke
tingkat energi yang paling tinggi (Noerdin, 1985).
Spektrum ultraviolet dari suatu senyawa biasanya diperoleh dengan
melewatkan cahaya dengan panjang gelombang tertentu (cahaya monokromati)
melalui larutan encer senyawa tersebut. Sistem (gugus atom) yang
menyebabkan terjadinya absorpsi cahaya disebut kromofor. Kromofor yang
menyebabkan terjadinya transisi σ→σ* ialah senyawa yang mempunyai
elektron pada orbital molekul σ, yaitu molekul organik jenuh yang tidak
mempunyai atom dengan pasangan elektron sunyi. Senyawa yang mempunyai
transisi σ→σ* mengabsorpsi cahaya pada panjang gelombang sekitar 150 nm
(Creswell, et al., 1982).
Kromofor yang menyebabkan terjadinya transisi n→σ* ialah senyawa
yang hanya mempunyai orbital molekul n dan σ, yaitu molekul organik jenuh
yang mempunyai satu atau lebih atom dengan pasangan elektron sunyi.
Kromofor yang menyebabkan terjadinya transisi π→π* ialah senyawa yang
transisi n→σ* dan π→π* mengabsorpsi cahaya pada panjang gelombang
sekitar 20 nm (Creswell, et al., 1982).
Kromofor yang menyebabkan transisi n→π* ialah senyawa yang
mempunyai orbital molekul n maupun π yaitu senyawa yang mengandung atom
yang mempunyai pasangan elektron sunyi dan orbital π. Senyawa yang
mempunyai transisi n→π* mengabsorpsi cahaya yang panjang gelombang 200
-400 nm (Creswell, et al., 1982).
Istilah-istilah yang sering digunakan di dalam membicarakan spektra
elektronik yaitu:
Kromofor : Suatu gugus kovalen tidak jenuh yang bertanggung jawab untuk
serapan elektronik.
Auksokrom : Suatu gugus jenuh dengan elektron tidak terikat dimana bila
menempel kepada suatu kromofor dapat mengubah panjang gelombang dan
intensitas serapan.
Pergeseran batokromik : Pergeseran serapan ke panjang gelombang yang lebih
panjang karena sisipan atau pengaruh pelarut (geseran merah).
Pergeseran hipsokromik : Pergeseran serapan ke panjang gelombang yang
lebih pendek disebabkan substitusi atau pengaruh pelarut (geseran biru).
Efek hiperkromik : Kenaikan dalam intensitas serapan.
Efek hipokromik : Penurunan dalam intensitas serapan (Silverstein, 1986).
1. Menentukan gugus fungsi suatu senyawa organik
2. Mengetahui informasi struktur suatu senyawa organik dengan
membandingkan daerah sidik jarinya.
Pengukuran pada spektrum inframerah dilakukan pada daerah cahaya
inframerah tengah (mid-infrared) yaitu pada panjang gelombang 2,5-50 μm
atau bilangan gelombang 4000-200 cmˉ1. Energi yang dihasilkan oleh radiasi
ini akan menyebabkan vibrasi atau getaran pada molekul. Pita absorbsi
inframerah sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus
fungsi. Metoda ini sangat berguna untuk mengidentifikasi senyawa organik dan
organometalik.
Jika suatu frekuensi tertentu dari radiasi inframerah dilewatkan pada
sampel suatu senyawa organik maka akan terjadi penyerapan frekuensi oleh
senyawa tersebut. Detektor yang ditempatkan pada sisi lain dar senyawa akan
mendeteksi frekuensi yang dilewatkan pada sampel yang tidak diserap oleh
senyawa. Banyaknya frekkuensi yang melewati senyawa (yang tidak diserap)
akan diukur sebagai persen transmitan (Dachriyanus, 2004).
Daerah inframerah terletak antara spektrum elektromagnetik cahaya
tampak dan spektrum radio, yakni antara 4000-400 cm-1. Penggunaan
spektrofotometri inframerah yang dimaksudkan untuk analisa lebih banyak
ditujukan untuk identifikasi suatu senyawa melalui gugus fungsinya. Spektrum
inframerah senyawa organik bersifat khas, artinya senyawa yang berbeda akan
Penafsiran spektrum inframerah dari suatu senyawa yang belum
diketahui haruslah ditujukan pada penentuan ada atau tidaknya beberapa gugus
fungsional utama seperti C=O, O-H, N-H, C-O, C=C, C≡C, C=N, C≡N, dan
NO2. Langkah-langkah yang umum dilakukan untuk memeriksa pita-pita yang
penting pada hasil spektrum inframerah (Pavia, et al., 1988):
1. Gugus karbonil
Gugus C=O memberikan puncak yang kuat pada daerah 1820-1660 cm-1.
2. Bila gugus C=O ada, periksalah gugus-gugus berikut (jika C=O tidak ada
langsung ke nomor 3).
Asam : periksalah gugus O-H, merupakan serapan melebar di
daerah 3300-2500 cm-1
Amida : periksalah gugus N-H, merupakan serapan medium
didaerah 3500 cm-1, kadang-kadang dengan puncak
rangkap.
Ester : periksalah gugus C-O, merupakan serapan medium
didaerah 1300-1000 cm-1.
Anhidrida : mempunyai dua serapan C=O di daerah 1810 dan 1760
cm-1.
Aldehida : periksalah gugus C-H, merupakan dua serapan lemah
didaerah 2850 dan 2750 cm-1 yaitu disebelah kanan
serapan C-H.
Alkohol atau fenol : periksalah gugus O-H, merupakan serapan melebar
di daerah 3600-3300 cm-1 yang diikuti adanya
serapan C-O di daerah 1300-1000 cm-1.
Amina : periksalah gugus N-H, yaitu serapan medium di
daerah 3500 cm-1.
Eter : periksalah gugus C-O (dan tidak adanya O-H), yaitu
serapan medium di daerah 1300-1000 cm-1.
4. Ikatan rangkap dua atau cincin aromatik
− Serapan lemah C=C di daerah 1650 cm-1.
− Serapan medium sampai kuat pada daerah 1650-1450 cm-1sering
menunjukkan adanya cincin aromatik.
− Buktikan kemungkinan di atas dengan memperhatikan serapan pada
daerah C-H aromatik di sebelah kiri 3000 cm-1, sedangkan C-H alifatis
terjadi di sebelah kanan daerah tersebut.
5. Ikatan rangkap tiga
− Serapan medium dan tajam dari C≡N di daerah 2250 cm-1.
− Serapan medium dan tajam dari C≡C di daerah 2150 cm-1.
6. Gugus nitro
− Dua serapan yang kuat di daerah 1600-1500 cm-1 dan 1390-1300 cm-1.
7. Hidrokarbon
− Apabila keenam serapan di atas tidak ada.
− Serapan yang sangat sederhana di daerah 1450 cm-1 (CH2) dan 1375